Die absolute Konfiguration und ihre Zuordnung C H
|
|
|
- Irma Althaus
- vor 7 Jahren
- Abrufe
Transkript
1 Die absolute Konfiguration und ihre Zuordnung estimmung der Konfiguration nach der R,S-omenklatur von ahn-ingold-prelog (IP-omenklatur) - einer omenklatur-konvention, deren Resultat keie absolute physikalische edeutung hat Prinzip: 1) rdnen der Substituenten am hiralitätszentrum nach fallenden Prioritäten = Sequenzregeln 2) estimmung des hiralitätssinnes gemäss folgender Vorschrift vgl. auch Kaufmann, ädener, 10. ufl., S Sequenzregeln: eachte: eispiele: 1) Priorität nach fallender rdnungszahl 2) Priorität nach fallender Massenzahl 3) Doppelbindungen zählen wie 2 Einfachbindungen, Dreifachbindungen wie 3 Einfachbindungen 4) Priorität Z > E 5) Priorität R-iralität > S-hiralität - wenn Sequenz in 1. Ligandensphäre nicht unterscheidbar ist, dann entscheidet die 2. Ligandensphäre - wenn Sequenz in 2. Ligandensphäre nicht unterscheidbar ist, dann entscheidet die 3. Ligandenshpäre etc. () () 3 2 S-lanin R-arvon () (L-lanin) (im Pfefferminzöl)
2 a b Fischer-Projektion: d c d c b a Konvention zur Wiedergabe der hiralität in zweidimensionalen Projektionsformeln a oder b c oder a b etc. d c d Konvention: vgl. auch Kaufmann, ädener, 10. ufl., S. 248 (-)-Milchsäure: (+)-Milchsäure: 3 3 D- Vorliegen eines asymmetrischen Kohlenstoffzentrums, hiralitätszentrums (ist gegeben, wenn -tom von vier (konstitutionell) verschiedenen Resten umgeben ist; dies wird häufig durch einen * hervorgehoben) die zwei stereoisomeren Formen von Milchsäure, nämlich (-)-Milchsäure und (+)-Milchsäure, unterscheiden sich durch ihre absolute Konfiguration (am -2) L- (- rechts) (- links) D- und L- stehen in keinem Zusammenhang mit der Richtung der optischen Drehung, sondern beziehen sich lediglich auf die Fischer- Projektionsformeln (+)-Weinsäure (+)-Glucose
3 Moleküle mit mehreren asymmetrischen -tomen: allgemein: 1 asymmetrisches -tom = 2 Stereoisomere 2 asymmetrische (konstitutionell e) -tome = 4 Stereoisomere n asymmetrische (konstitutionell e) -tome = 2 n Stereoisomere Diastereomerie: eispiel für eine Verbindung mit zwei konstitutionell en hiralitätszentren:,2 n - Regel (2R,3R) D-Erythrose L-Erythrose (2S,3S) (2S,3R) D-Threose L-Threose (2R,3S)
4 Diastereomerie: eispiel für eine Verbindung mit zwei konstitutionell GLEIE hiralitätszentren: (+)-2R,3R Weinsäure (-)-2S,3S Weinsäure Smp. 170 [α] T ( 2., 0.2 g/ml) = + 12 D Smp. 170 [α]t ( 2., 0.2 g/ml) = - 12 D Mesoweinsäure R,S-Weinsäure Smp. 140 optisch inaktiv eachte: (1:1)-Gemisch aus (+)-Weinsäure und (-) Weinsäure: (±)-Weinsäure, = Traubensäure, racemische Weinsäure Smp. 206 [α] T ( 2., 0.2 g/ml) = 0 D
5 eispiele zur biologischen, pharmakologischen edeutung von Enantiomeren: S S 2 2 Limonen Penicillamin arbiturat Ethambutol Thalidomid, ontergan Propanolol 2 2 Thyroxin
6 Spiegelbildsymmetrie ohne asymmetrisches : z..: tropisomerie: llene mit obigen Substitutionsmuster sind optisch aktiv iphenylsysteme mit grossen Resten weisen keine freie Drehbarkeit auf; die beiden möglichen Konformere sind nicht identisch, sondern verhalten sich wie ild und Spiegelbild (chromatographisch trennbar) usnahme von 2 n -Regel bei cyclischen Sytemen: z.. D-(+)-ampher (aus dem olz des apanbaumes) möglich, da die beiden * konstitutionell voneinander abhängig sind! durch die Verbundenheit im Molekül ist die relative Konfiguration der beiden * fixiert; d.h. bei L-(-)-ampher gegebener absoluter Konfiguration eines der beiden * ist die (im Mutterkrautöl) absoluter Konfiguration des anderen ebenfalls festgelegt. Konfiguration = räumliche nordnung der tome in einem Molekül bzw. Molekülteil relative Konfiguration = räumliche Relativanordnung der tome im Molekül; Konfiguration ohne Spezifikation des hiralitätssinnes absolute Konfiguration = räumliche nordnung der tome im Molekül; Konfiguration mit Spezifikation des hiralitätssinnes
7 Übersicht: 2 Verbindungen identische Verbindungen
Stereoisomerie. C 2 H 4 O 2 Schmelzpunkt 17 Grad Celcius
 3. Stereochemie Stereoisomerie Definition Isomerie: Als Isomere bezeichnet man Moleküle mit gleicher Summenformel, die sich jedoch in der Sequenz der Atome (Konstitutionsisomere) oder deren räumlichen
3. Stereochemie Stereoisomerie Definition Isomerie: Als Isomere bezeichnet man Moleküle mit gleicher Summenformel, die sich jedoch in der Sequenz der Atome (Konstitutionsisomere) oder deren räumlichen
weiteres Beispiel für Stereoisomere: Enantiomere Spiegelebene
 Stereoisomere - Isomerie I: Konstitutionsisomere (siehe oben) - Isomerie II: Konformationsisomere (Konformere, siehe oben) - Isomerie III: Stereoisomere; Stereoisomere weisen eine identische Konstitution
Stereoisomere - Isomerie I: Konstitutionsisomere (siehe oben) - Isomerie II: Konformationsisomere (Konformere, siehe oben) - Isomerie III: Stereoisomere; Stereoisomere weisen eine identische Konstitution
Tetraeder mit gleichen und verschiedenen Ecken (1, 2, 3, 4)
 Prof. Dr..-U. Reißig rganische hemie 7. Tetraeder mit gleichen und verschiedenen Ecken (,,, ) Diese drei Tetraeder sind mit ihrem Spiegelbild deckbar, d. h. es ist achiral. gleiche Ecken "chemisches Beispiel"
Prof. Dr..-U. Reißig rganische hemie 7. Tetraeder mit gleichen und verschiedenen Ecken (,,, ) Diese drei Tetraeder sind mit ihrem Spiegelbild deckbar, d. h. es ist achiral. gleiche Ecken "chemisches Beispiel"
Konfigurationsisomerie
 Konfigurationsisomerie Enatiomerie, Diastereomerie (σ undπ). Prof.Dr. Ivo C. Ivanov 1 Optische Aktivität Zur Bestimmung des Drehwertes bedient man sich eines Polarimeters, dessen Aufbau nachfolgend schematisch
Konfigurationsisomerie Enatiomerie, Diastereomerie (σ undπ). Prof.Dr. Ivo C. Ivanov 1 Optische Aktivität Zur Bestimmung des Drehwertes bedient man sich eines Polarimeters, dessen Aufbau nachfolgend schematisch
4. Stereochemie. Das wichtigste Kriterium für Chiralität ist, dass sich Objekt und Spiegelbild nicht zur Deckung bringen lassen.
 4. Stereochemie Auch die cis-trans-isomerie zählt zur Stereoisomerie: 4.1 Chirale Moleküle Chirale Moleküle besitzen ein asymmetrisches C- Atom = Chiralitätszentrum. Das wichtigste Kriterium für Chiralität
4. Stereochemie Auch die cis-trans-isomerie zählt zur Stereoisomerie: 4.1 Chirale Moleküle Chirale Moleküle besitzen ein asymmetrisches C- Atom = Chiralitätszentrum. Das wichtigste Kriterium für Chiralität
Prof. Dr. Stephen Hashmi, Sommersemester Organische Chemie für Technische Biologen, Organische Chemie für Lehramtskandidaten, Teil 5
 Prof. Dr. ashmi, Sommersemester 2005 45 Mechanismus der 1,2-Isomerisierung: Start: [o III ] Kette: reversible omolyse nur 65 kj/mol Metall--Bindung Organometall-Verbindung X + [o II ] + -Abstraktion das
Prof. Dr. ashmi, Sommersemester 2005 45 Mechanismus der 1,2-Isomerisierung: Start: [o III ] Kette: reversible omolyse nur 65 kj/mol Metall--Bindung Organometall-Verbindung X + [o II ] + -Abstraktion das
Spezielle Methoden der pharmazeutischen Chemie 2
 Spezielle thoden der pharmazeutischen Chemie 2 Asymmetrische Synthese (für Diplomanden und Dissertanten im Fach Pharmazeutischen Chemie/Synthese) Kapiteleinteilung: 1. Symmetrie, Asymmetrie, Chiralität
Spezielle thoden der pharmazeutischen Chemie 2 Asymmetrische Synthese (für Diplomanden und Dissertanten im Fach Pharmazeutischen Chemie/Synthese) Kapiteleinteilung: 1. Symmetrie, Asymmetrie, Chiralität
- Punktsymmetriegruppe Gesamtheit aller Symmetrieelemente: Gruppentheorie
 195 14. Stereochemie Bereits am Anfang der Vorlesung einige Grundbegriffe: Konformation, Enantio- und Diastereomerie Jetzt nochmals systematisch und genauer a) Symmetrie und hiralität α) Symmetrieelemente
195 14. Stereochemie Bereits am Anfang der Vorlesung einige Grundbegriffe: Konformation, Enantio- und Diastereomerie Jetzt nochmals systematisch und genauer a) Symmetrie und hiralität α) Symmetrieelemente
Stereochemie. mit Vitamin C. Süßstoff Aspartam (QWKlOWÃHLQHÃ3KHQ\ODODQLQTXHOOH. L(+)-Milchsäure. Zuckeraustauschstoff Sorbit
 Stereochemie mit Vitamin Süßstoff Aspartam (QWKlWÃLQÃ3KQ\DDQLQTX L(+)-Milchsäure Zuckeraustauschstoff Sorbit hemie für Mediziner Isomerie organischer Verbindungen Isomere Konstitutionsisomere Stereoisomere
Stereochemie mit Vitamin Süßstoff Aspartam (QWKlWÃLQÃ3KQ\DDQLQTX L(+)-Milchsäure Zuckeraustauschstoff Sorbit hemie für Mediziner Isomerie organischer Verbindungen Isomere Konstitutionsisomere Stereoisomere
7. Stereochemie. Isomere. Alkene. Cycloalkane
 7. Stereochemie 56 In den vorhergehenden Kapiteln haben wir zwei Arten von Isomerie kennengelernt (z.b. Seiten 12, 20 und 23), die Konstitutionsisomerie, und die Stereoisomerie : Isomere Konstitutionsisomerie
7. Stereochemie 56 In den vorhergehenden Kapiteln haben wir zwei Arten von Isomerie kennengelernt (z.b. Seiten 12, 20 und 23), die Konstitutionsisomerie, und die Stereoisomerie : Isomere Konstitutionsisomerie
Moleküle mit mehr als einem Chiralitätselement
 Moleküle mit mehr als einem hiralitätselement Natürlich kommt es häufig vor, dass Moleküle mehr als ein hiralitätselement enthalten. ierbei ist eine neue Art der Isomerie zu finden. Im Folgenden sind zunächst
Moleküle mit mehr als einem hiralitätselement Natürlich kommt es häufig vor, dass Moleküle mehr als ein hiralitätselement enthalten. ierbei ist eine neue Art der Isomerie zu finden. Im Folgenden sind zunächst
Grundlagen zum Verständnis chemischer Reaktionen = Handwerkszeug
 Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
Isomerie. Ethanol. Stereoisomere: gleiche Summenformel, gleiche Verknüpfung der Atome, aber in unterschiedlicher Raumrichtung. trans- oder E-2-Buten
 Isomerie Folie271 Konstitutions- zw. Strukturisomere: gleiche Summenformel, unterschiedliche Verknüpfung der Atome: Beispiele: 2 6 : 3 3 3 2 Dimethylether Ethanol 4 10 : 3 2 2 3 3 3 n-butan 3 Isoutan Stereoisomere:
Isomerie Folie271 Konstitutions- zw. Strukturisomere: gleiche Summenformel, unterschiedliche Verknüpfung der Atome: Beispiele: 2 6 : 3 3 3 2 Dimethylether Ethanol 4 10 : 3 2 2 3 3 3 n-butan 3 Isoutan Stereoisomere:
Weiterführende Fragen und Knobeleien zur Vorlesung Organische Chemie für chemieinteressierte Studierende mit Chemie als Nebenfach.
 Weiterführende Fragen und Knobeleien zur Vorlesung rganische Chemie für chemieinteressierte Studierende mit Chemie als Nebenfach Teil II Mit diesem Blatt will ich Sie anregen, weiter über das Thema Chiralität
Weiterführende Fragen und Knobeleien zur Vorlesung rganische Chemie für chemieinteressierte Studierende mit Chemie als Nebenfach Teil II Mit diesem Blatt will ich Sie anregen, weiter über das Thema Chiralität
4. Stereoisomerie! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind!
 4. Stereoisomerie! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind! http://de.wikipedia.org/wiki/datei:isomerism ball de.svg OC I Lehramt F. H. Schacher 1 Stereoisomerie andere
4. Stereoisomerie! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind! http://de.wikipedia.org/wiki/datei:isomerism ball de.svg OC I Lehramt F. H. Schacher 1 Stereoisomerie andere
4. Stereoisomerie. ! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind! Organische Chemie I LA / J. C.
 4. Stereoisomerie! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind! http://de.wikipedia.org/wiki/datei:isomerism-ball-de.svg Organische Chemie I LA / J. C. Brendel 1 Stereoisomerie
4. Stereoisomerie! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind! http://de.wikipedia.org/wiki/datei:isomerism-ball-de.svg Organische Chemie I LA / J. C. Brendel 1 Stereoisomerie
Prochiralität H 3 C O
 Prochiralität Es gibt Verbindungen, die selber nicht chiral sind, aber eine Vorform der hiralität enthalten. Solche Verbindungen (oder Strukturelemente einer komplexeren Verbindung) enthalten eine Spiegelebene,
Prochiralität Es gibt Verbindungen, die selber nicht chiral sind, aber eine Vorform der hiralität enthalten. Solche Verbindungen (oder Strukturelemente einer komplexeren Verbindung) enthalten eine Spiegelebene,
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Übung 9: Aufbau und Struktur organischer Verbindungen Übung für Medizinische Biologen - Jun.-Prof. Dr. Michael Giese.
 Zusammenfassung Aufbau und Struktur organischer Verbindungen Kohlenstoff besitzt eine Sonderstellung unter den Elementen ybridisierungsmodell beschreibt die Bindungsverhältnisse in Kohlenstoffverbindungen
Zusammenfassung Aufbau und Struktur organischer Verbindungen Kohlenstoff besitzt eine Sonderstellung unter den Elementen ybridisierungsmodell beschreibt die Bindungsverhältnisse in Kohlenstoffverbindungen
Chemie für Biologen, 2017
 Chemie für Biologen, 2017 Übung 10 Stereochemie (Thema 11.1 11.4) Aufgabe 1: a) Zeichnen Sie den Isomeren-Stammbaum auf. b) Erklären Sie folgende Isomerie-Arten: i) Konstitutionsisomere Konstitutionsisomere
Chemie für Biologen, 2017 Übung 10 Stereochemie (Thema 11.1 11.4) Aufgabe 1: a) Zeichnen Sie den Isomeren-Stammbaum auf. b) Erklären Sie folgende Isomerie-Arten: i) Konstitutionsisomere Konstitutionsisomere
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 0-2, S04 T0 A02 Paul Rademacher Institut für rganische hemie der Universität Duisburg-Essen (Teil 2: 2.0.2005) MILESS: hemie für Biologen 28 Konstitutionsisomere:
hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 0-2, S04 T0 A02 Paul Rademacher Institut für rganische hemie der Universität Duisburg-Essen (Teil 2: 2.0.2005) MILESS: hemie für Biologen 28 Konstitutionsisomere:
Isomerie I. Konstitutionsisomerie. Identifizieren Sie alle Konstitutionsisomere. a b c. a b c d
 Isomerie I Konstitutionsisomerie Identifizieren Sie alle Konstitutionsisomere. 1. a) Br b) a b c) a b c 2. a b I a b c d e f 3. a b c d e f g R,S-omenklatur Bestimmen der absoluten Konfiguration am Chiralitätszentrum:
Isomerie I Konstitutionsisomerie Identifizieren Sie alle Konstitutionsisomere. 1. a) Br b) a b c) a b c 2. a b I a b c d e f 3. a b c d e f g R,S-omenklatur Bestimmen der absoluten Konfiguration am Chiralitätszentrum:
Vokabular zur Stereochemie
 Vokabular zur tereochemie Zwei Moleküle mit gleicher ummenformel sind: deckungsgleich = identisch Isomere Konstitutionsisomere tereoisomere Enantiomere Diastereomere Konstitutionsisomere: Moleküle mit
Vokabular zur tereochemie Zwei Moleküle mit gleicher ummenformel sind: deckungsgleich = identisch Isomere Konstitutionsisomere tereoisomere Enantiomere Diastereomere Konstitutionsisomere: Moleküle mit
Organische Chemie für Studierende mit Nebenfach Chemie Andreas Rammo
 Organische Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Arene Arene sind cyclisch konjugierte
Organische Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Arene Arene sind cyclisch konjugierte
Gruppenunterricht zum Thema Stereoisomerie
 Gruppenunterricht zum Thema Stereoisomerie Unterlagen Fach: Institution: Adressaten: Kurs: Gruppenarbeitsform: Dauer: Autor: Betreuer: Erprobungsstatus: Chemie Gymnasium Maturanden im letzten Jahr des
Gruppenunterricht zum Thema Stereoisomerie Unterlagen Fach: Institution: Adressaten: Kurs: Gruppenarbeitsform: Dauer: Autor: Betreuer: Erprobungsstatus: Chemie Gymnasium Maturanden im letzten Jahr des
8. Stereochemie organischer Moleküle 8.1
 8. Stereochemie organischer Moleküle 8.1 Stereochemie organischer Moleküle Zur Darstellung der Struktur organischer Moleküle werden oft Formeln verwendet, welche den räumlichen Bau nicht zum Ausdruck bringen.
8. Stereochemie organischer Moleküle 8.1 Stereochemie organischer Moleküle Zur Darstellung der Struktur organischer Moleküle werden oft Formeln verwendet, welche den räumlichen Bau nicht zum Ausdruck bringen.
Kohlenwasserstoffe. sp 3 -Orbitale. Alkane. Alkene. sp 2 - Orbitale p z - Orbital. sp -Orbitale p y, p z - Orbitale. Alkine
 Kohlenwasserstoffe sp 3 -Orbitale Alkane sp 2 - Orbitale p z - Orbital Alkene sp -Orbitale p y, p z - Orbitale Alkine Offenkettige Alkane 4 4 than "Erdgas" 2 6 3 3 Ethan 3 8 3 2 3 Propan Bei Raumtemperatur
Kohlenwasserstoffe sp 3 -Orbitale Alkane sp 2 - Orbitale p z - Orbital Alkene sp -Orbitale p y, p z - Orbitale Alkine Offenkettige Alkane 4 4 than "Erdgas" 2 6 3 3 Ethan 3 8 3 2 3 Propan Bei Raumtemperatur
Chiralitätszentrum X X
 hiralitätszentrum Die weitaus meisten chiralen Verbindungen ist deswegen chiral, weil sie sog. asymmetrische Kohlenstoffatome enthalten. Dies sind tetraedrisch konfigurierte -Atome mit vier verschiedenen
hiralitätszentrum Die weitaus meisten chiralen Verbindungen ist deswegen chiral, weil sie sog. asymmetrische Kohlenstoffatome enthalten. Dies sind tetraedrisch konfigurierte -Atome mit vier verschiedenen
Essigsäure und Co Stationenlernen Carbonsäuren
 8. arbonsäuren 8.1 Essigsäure und o Stationenlernen arbonsäuren arbonsäuren Der erste Vertreter der arbonsäuren, den wir im Unterricht hergestellt haben ist die Benzoesäure. Strukturell einfachere Vertreter
8. arbonsäuren 8.1 Essigsäure und o Stationenlernen arbonsäuren arbonsäuren Der erste Vertreter der arbonsäuren, den wir im Unterricht hergestellt haben ist die Benzoesäure. Strukturell einfachere Vertreter
ein Zweig der chemischen Wissenschaft, der sich mit der dreidimensionalen Struktur der Moleküle beschäftigt
 Stereochemie Stereochemie: ein Zweig der chemischen Wissenschaft, der sich mit der dreidimensionalen Struktur der Moleküle beschäftigt Stereoisomerie: unterschiedliche räumliche Anordnungen der Atome oder
Stereochemie Stereochemie: ein Zweig der chemischen Wissenschaft, der sich mit der dreidimensionalen Struktur der Moleküle beschäftigt Stereoisomerie: unterschiedliche räumliche Anordnungen der Atome oder
Hydroxycarbonsäuren. Systematischer Name (Trivialname) Struktur O HO CH 2. Hydroxyethansäure (Glykolsäure) CO 2 C OH
 Prof. Dr..-U. Reißig rganische hemie I 12.01 ydroxycarbonsäuren Systematischer Name (Trivialname) Struktur ydroxyethansäure (Glykolsäure) 2 2 2-ydroxypropansäure (Milchsäure) (S)-(+) 2 (R)-( ) 2 3-ydroxybutansäure
Prof. Dr..-U. Reißig rganische hemie I 12.01 ydroxycarbonsäuren Systematischer Name (Trivialname) Struktur ydroxyethansäure (Glykolsäure) 2 2 2-ydroxypropansäure (Milchsäure) (S)-(+) 2 (R)-( ) 2 3-ydroxybutansäure
Isomerie organischer Verbindungen
 15 Isomerie organischer Verbindungen Organische Verbindungen können, bei gleicher Summenformel, sehr unterschiedliche Strukturen besitzen. Moleküle mit gleicher Summenformel aber unterschiedlicher Struktur
15 Isomerie organischer Verbindungen Organische Verbindungen können, bei gleicher Summenformel, sehr unterschiedliche Strukturen besitzen. Moleküle mit gleicher Summenformel aber unterschiedlicher Struktur
Optische Aktivität und Spiegelbildisomerie
 Optische Aktivität und Spiegelbildisomerie Die optische Aktivität gibt Aufschluß über die chemische Struktur Zusammenfassung Dieses Script ist eine Einführung in die Spiegelbildisomerie von Molekülen.
Optische Aktivität und Spiegelbildisomerie Die optische Aktivität gibt Aufschluß über die chemische Struktur Zusammenfassung Dieses Script ist eine Einführung in die Spiegelbildisomerie von Molekülen.
L.9 Organische Chemie I
 L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
Chiralität in der Natur und synthetisch
 Chiralität in der Natur und synthetisch Universität Ulm Demonstrationskurs 09/10 Christine Ohmayer Folie 1 Beispiel Carvon Summenformel von Carvon : C 12 H 10 O Eigenschaften: farblose Flüssigkeit Geruch:
Chiralität in der Natur und synthetisch Universität Ulm Demonstrationskurs 09/10 Christine Ohmayer Folie 1 Beispiel Carvon Summenformel von Carvon : C 12 H 10 O Eigenschaften: farblose Flüssigkeit Geruch:
Stereochemie. Grundbegriffe. Bearbeitet von K.-H Hellwich
 Stereochemie Grundbegriffe Bearbeitet von K.-H Hellwich Neuausgabe 2007. Taschenbuch. xii, 120 S. Paperback ISBN 978 3 540 71707 2 Format (B x L): 14 x 21,6 cm Gewicht: 181 g Weitere Fachgebiete > Chemie,
Stereochemie Grundbegriffe Bearbeitet von K.-H Hellwich Neuausgabe 2007. Taschenbuch. xii, 120 S. Paperback ISBN 978 3 540 71707 2 Format (B x L): 14 x 21,6 cm Gewicht: 181 g Weitere Fachgebiete > Chemie,
Lebewesen enthalten weitaus mehr Molekülarten und beherbergen weitaus mehr chemische Reaktionsarten als die ganze anorganische Welt.
 Lebewesen enthalten weitaus mehr Molekülarten und beherbergen weitaus mehr chemische Reaktionsarten als die ganze anorganische Welt. Die aus Biomolekülen aufgebauten biologischen Strukturen sind äußerst
Lebewesen enthalten weitaus mehr Molekülarten und beherbergen weitaus mehr chemische Reaktionsarten als die ganze anorganische Welt. Die aus Biomolekülen aufgebauten biologischen Strukturen sind äußerst
Monosaccharide: Einfache Zucker, z. B. Glucose, Fructose, Ribose
 Vorlesung 6 Kohlenhydrate Ursprünglich (Karl Schmidt, 18) bezeichnete man als Kohlenhydrate Verbindungen der Summenformel n ( ) n. Diese Definition ist nicht mehr streng gültig. Monosaccharide: Einfache
Vorlesung 6 Kohlenhydrate Ursprünglich (Karl Schmidt, 18) bezeichnete man als Kohlenhydrate Verbindungen der Summenformel n ( ) n. Diese Definition ist nicht mehr streng gültig. Monosaccharide: Einfache
Bestimmen Sie für die folgenden Verbindungen den korrekten Namen nach IUPAC inklusive die korrekte Stereochemie nach CIP-Nomenklatur.
 Aufgabe: Nomenklatur estimmen Sie für die folgenden Verbindungen den korrekten Namen nach IUPA inklusive die korrekte Stereochemie nach IP-Nomenklatur. P 2 r Wieviele Stereoisomere sind denkbar S Wieviele
Aufgabe: Nomenklatur estimmen Sie für die folgenden Verbindungen den korrekten Namen nach IUPA inklusive die korrekte Stereochemie nach IP-Nomenklatur. P 2 r Wieviele Stereoisomere sind denkbar S Wieviele
Fragen aus dem ersten Abschnitt der pharmazeutischen Prüfung
 Agenda Losartan - Synthese Fragen aus dem ersten Abschnitt der pharmazeutischen Prüfung Peptidsynthesen, Nylon, Zucker Biphenylsynthese - Ullmann-Verfahren Das Ullmann-Verfahren stellt eine Biphenyl-Synthese
Agenda Losartan - Synthese Fragen aus dem ersten Abschnitt der pharmazeutischen Prüfung Peptidsynthesen, Nylon, Zucker Biphenylsynthese - Ullmann-Verfahren Das Ullmann-Verfahren stellt eine Biphenyl-Synthese
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1. Grundwissen 10.Klasse NTG 2 Grundwissen 10.Klasse NTG 2
 Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Kohlenhydrate und ihre Funktionen
 Kohlenhydrate und ihre Funktionen Gliederung Monosaccharide Aufbau Nomenklatur Stereoisomerie/Konfiguration Zyklisierung O-glykosidische Bindung N-glykosidische Bindung Disaccharide Kohlenhydrate im Überblick
Kohlenhydrate und ihre Funktionen Gliederung Monosaccharide Aufbau Nomenklatur Stereoisomerie/Konfiguration Zyklisierung O-glykosidische Bindung N-glykosidische Bindung Disaccharide Kohlenhydrate im Überblick
Energie. 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital
 sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
Kohlenhydrate. Monosaccharide
 Kohlenhydrate Monosaccharide Konstitution = Verkettung der Atome; Konstitutionsisomere oder Strukturisomere: gleiche Summenformel, aber unterschiedliche Struktur; z.b. Propanol und Isopropanol. Aldosen
Kohlenhydrate Monosaccharide Konstitution = Verkettung der Atome; Konstitutionsisomere oder Strukturisomere: gleiche Summenformel, aber unterschiedliche Struktur; z.b. Propanol und Isopropanol. Aldosen
NMR-Methoden zur chiralen Erkennung
 Spektroskopie in der rganischen hemie NMR-Methoden zur chiralen Erkennung Mit Ausnahme der D-Spektroskopie (D = irculardichroismus) sind alle spektroskopischen Methoden auch die NMR achiral, d.h. sie können
Spektroskopie in der rganischen hemie NMR-Methoden zur chiralen Erkennung Mit Ausnahme der D-Spektroskopie (D = irculardichroismus) sind alle spektroskopischen Methoden auch die NMR achiral, d.h. sie können
Abschlussklausur zur Grundvorlesung Organische Chemie im SS 2007 Nachholtermin -
 Prof. Dr. H.-A. Wagenknecht Institut für rganische Chemie Universität Regensburg Abschlussklausur zur Grundvorlesung rganische Chemie im SS 2007 Nachholtermin - am Freitag, dem 12. ktober 2007... Vorname:...
Prof. Dr. H.-A. Wagenknecht Institut für rganische Chemie Universität Regensburg Abschlussklausur zur Grundvorlesung rganische Chemie im SS 2007 Nachholtermin - am Freitag, dem 12. ktober 2007... Vorname:...
Übungen zur VL Chemie für Biologen und Humanbiologen Lösung Übung 9
 Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Wissenschaftliche Fachliteratur und Lehrbücher
 Wissenschaftliche Fachliteratur und Lehrbücher Lehrbuch «rganische hemie» Satz, Umbruch, Druckvorbereitung Stereochemie Anordnung von Atomen im Raum und die Stereochemie von Additionsreaktionen 5.1 is/trans-isomere.....................................
Wissenschaftliche Fachliteratur und Lehrbücher Lehrbuch «rganische hemie» Satz, Umbruch, Druckvorbereitung Stereochemie Anordnung von Atomen im Raum und die Stereochemie von Additionsreaktionen 5.1 is/trans-isomere.....................................
Skript zur Vorlesung Organische Chemie (Prof. M. Albrecht) an der RWTH Aachen
 Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Gruppenunterricht zum Thema Stereoisomerie
 Gruppenunterricht zum Thema Stereoisomerie Anleitung Fach: Institution: Adressaten: Kurs: Gruppenarbeitsform: Dauer: Autor: Betreuer: Erprobungsstatus: Chemie Gymnasium Maturanden im letzten Jahr des Chemieunterrichtes
Gruppenunterricht zum Thema Stereoisomerie Anleitung Fach: Institution: Adressaten: Kurs: Gruppenarbeitsform: Dauer: Autor: Betreuer: Erprobungsstatus: Chemie Gymnasium Maturanden im letzten Jahr des Chemieunterrichtes
Organische Chemie für MST 6. Lienkamp/ Prucker/ Rühe
 Organische Chemie für MST 6 Lienkamp/ Prucker/ Rühe Valenzisomere Inhalt 6 Isomerie Konstitutionsisomere Tautomere/ Protonenisomere (= Strukturisomere) Skelett-Isomere Isomerie Isomere = Substanzen mit
Organische Chemie für MST 6 Lienkamp/ Prucker/ Rühe Valenzisomere Inhalt 6 Isomerie Konstitutionsisomere Tautomere/ Protonenisomere (= Strukturisomere) Skelett-Isomere Isomerie Isomere = Substanzen mit
im Molekül eine Dreifachbindung (eine σ-bindung,
 1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
Die kleinsten Zuckermoleküle. Zucker zeigen gemeinsame funktionelle Gruppen
 Ein Kapitel Zuckerchemie Die Strukturen der Zucker Das Geheimnis aller Zucker ist: Stoffe mit mindestens 2 Hydroxygruppen (-OH) schmecken süß. Glykol (=Ethandiol) oder Glycerin (=Propantriol) schmecken
Ein Kapitel Zuckerchemie Die Strukturen der Zucker Das Geheimnis aller Zucker ist: Stoffe mit mindestens 2 Hydroxygruppen (-OH) schmecken süß. Glykol (=Ethandiol) oder Glycerin (=Propantriol) schmecken
viele zeitgenössische Kraftsportler hingegen versuchen, sich Muskelmasse mit Hilfe sogenannter Protein-Drinks zuzulegen.
 Quelle: comedix.de Die Freunde von Asterix-Comics wissen aus Band XII ( Asterix bei den Olympischen Spielen ), daß die als sehr sportlich geltenden Spartaner sich bevorzugt von Olivenkernen und fettem
Quelle: comedix.de Die Freunde von Asterix-Comics wissen aus Band XII ( Asterix bei den Olympischen Spielen ), daß die als sehr sportlich geltenden Spartaner sich bevorzugt von Olivenkernen und fettem
ISBN (Print); (PDF)
 Bibliografische Information der Deutschen Bibliothek Die Deutsche Bibliothek verzeichnet diese Publikation in der Deutschen Nationalbibliografie; detaillierte bibliografische Daten sind im Internet über
Bibliografische Information der Deutschen Bibliothek Die Deutsche Bibliothek verzeichnet diese Publikation in der Deutschen Nationalbibliografie; detaillierte bibliografische Daten sind im Internet über
Molekülsymmetrie und Kristallographie. Chiralität
 hiralität Die hiralität ist eines der wichtigsten Grundprinzipien der Natur überhaupt. Sie bezeichnet die Tatsache, dass es Gegenstände gibt, die sich zueinander wie Bild und Spiegelbild verhalten, sich
hiralität Die hiralität ist eines der wichtigsten Grundprinzipien der Natur überhaupt. Sie bezeichnet die Tatsache, dass es Gegenstände gibt, die sich zueinander wie Bild und Spiegelbild verhalten, sich
Modul: BS Chemie II Organische Chemie Klausur zum Organisch-Chemischen Grundpraktikum für. Studierende der Biologie
 Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Department für Chemie Prof. Dr. A. G. Griesbeck Greinstr. 4 50939 Köln Modul: BS Chemie II rganische Chemie Klausur zum
Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Department für Chemie Prof. Dr. A. G. Griesbeck Greinstr. 4 50939 Köln Modul: BS Chemie II rganische Chemie Klausur zum
Kohlenhydrate. spielen in der Natur eine sehr wichtige Rolle. dienen als Energiespeicher: Stärke, Glykogen
 Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
F r e i t a g, 3. J u n i
 F r e i t a g, 3. J u n i 2 0 1 1 L i n u x w i r d 2 0 J a h r e a l t H o l l a, i c h d a c h t e d i e L i n u x - L e u t e s i n d e i n w e n i g v e r n ü n f t i g, a b e r j e t z t g i b t e
F r e i t a g, 3. J u n i 2 0 1 1 L i n u x w i r d 2 0 J a h r e a l t H o l l a, i c h d a c h t e d i e L i n u x - L e u t e s i n d e i n w e n i g v e r n ü n f t i g, a b e r j e t z t g i b t e
S o n n t a g, 2 6. N o v e m b e r
 S o n n t a g, 2 6. N o v e m b e r 2 0 1 7 A u s f l u g n a c h N e v a d a u n d A r i z o n a D e r g r o ß e S o h n u n d i c h g i n g e n a u f e i n e F a h r t i n R i c h t u n g N e v a d a
S o n n t a g, 2 6. N o v e m b e r 2 0 1 7 A u s f l u g n a c h N e v a d a u n d A r i z o n a D e r g r o ß e S o h n u n d i c h g i n g e n a u f e i n e F a h r t i n R i c h t u n g N e v a d a
R a i n e r N i e u w e n h u i z e n K a p e l l e n s t r G r e v e n T e l / F a x / e
 R a i n e r N i e u w e n h u i z e n K a p e l l e n s t r. 5 4 8 6 2 8 G r e v e n T e l. 0 2 5 7 1 / 9 5 2 6 1 0 F a x. 0 2 5 7 1 / 9 5 2 6 1 2 e - m a i l r a i n e r. n i e u w e n h u i z e n @ c
R a i n e r N i e u w e n h u i z e n K a p e l l e n s t r. 5 4 8 6 2 8 G r e v e n T e l. 0 2 5 7 1 / 9 5 2 6 1 0 F a x. 0 2 5 7 1 / 9 5 2 6 1 2 e - m a i l r a i n e r. n i e u w e n h u i z e n @ c
L 3. L a 3. P a. L a m 3. P a l. L a m a 3. P a l m. P a l m e. P o 4. P o p 4. L a. P o p o 4. L a m. Agnes Klawatsch
 1 L 3 P 1 L a 3 P a 1 L a m 3 P a l 1 L a m a 3 P a l m 2 P 3 P a l m e 2 P o 4 L 2 P o p 4 L a 2 P o p o 4 L a m 4 L a m p 6 N a 4 L a m p e 6 N a m 5 5 A A m 6 6 N a m e N a m e n 5 A m p 7 M 5 A m p
1 L 3 P 1 L a 3 P a 1 L a m 3 P a l 1 L a m a 3 P a l m 2 P 3 P a l m e 2 P o 4 L 2 P o p 4 L a 2 P o p o 4 L a m 4 L a m p 6 N a 4 L a m p e 6 N a m 5 5 A A m 6 6 N a m e N a m e n 5 A m p 7 M 5 A m p
S o n n t a g, 5. A u g u s t
 S o n n t a g, 5. A u g u s t 2 0 1 8 R ü c k b l i c k, A b s c h i e d, v i e l p a s s i e r t u n d k e i n e Z e i t D r e i M o n a t e s i n d v e r g a n g e n, v o l l g e s t o p f t m i t s
S o n n t a g, 5. A u g u s t 2 0 1 8 R ü c k b l i c k, A b s c h i e d, v i e l p a s s i e r t u n d k e i n e Z e i t D r e i M o n a t e s i n d v e r g a n g e n, v o l l g e s t o p f t m i t s
Das Tetraeder-Bällchen/Oktaeder-Bällchen
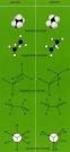
 H-Atome: klein, weiß Edelgas-Atome: He, Ne, Ar, Kr, Xe, Rn: verschiedene Lila-Töne Metalle: Natrium, Calcium: eher Dunkelblau-Töne Nichtmetalle: C N O F P S Cl grau (kopiert) hellblau rot hellgelb orange
H-Atome: klein, weiß Edelgas-Atome: He, Ne, Ar, Kr, Xe, Rn: verschiedene Lila-Töne Metalle: Natrium, Calcium: eher Dunkelblau-Töne Nichtmetalle: C N O F P S Cl grau (kopiert) hellblau rot hellgelb orange
Prof. Dr. Thomas Heinze Institut für Organische Chemie und Makromolekulare Chemie Humboldtstraße Jena
 Vorlesung/Seminare Organische Chemie für Materialwissenschaften Prof. Dr. Thomas Heinze Institut für Organische Chemie und Makromolekulare Chemie Humboldtstraße 10 07743 Jena 03641/9 48270 03641/9 48271
Vorlesung/Seminare Organische Chemie für Materialwissenschaften Prof. Dr. Thomas Heinze Institut für Organische Chemie und Makromolekulare Chemie Humboldtstraße 10 07743 Jena 03641/9 48270 03641/9 48271
Stoffklassen in der Organischen Chemie. Nomenklaturfragen. Isomerie und sterischer Bau
 Stoffklassen in der Organischen Chemie Nomenklaturfragen Isomerie und sterischer Bau 1 Stoffklassen in der organischen Chemie Kohlenwasserstoffe Kohlenwasserstoffe mit Substituenten Y (eteroatom oder funktionelle
Stoffklassen in der Organischen Chemie Nomenklaturfragen Isomerie und sterischer Bau 1 Stoffklassen in der organischen Chemie Kohlenwasserstoffe Kohlenwasserstoffe mit Substituenten Y (eteroatom oder funktionelle
Klausur zur Vorlesung Allgemeine Chemie II
 Klausur zur Vorlesung Allgemeine Chemie II (rganische Chemie, Prof. Lindhorst, WS 2007/08) für Studierende der Medizin und Zahnmedizin am 12. 01. 2009 ame: Studienfach: Matrikelnummer: Ich versichere,
Klausur zur Vorlesung Allgemeine Chemie II (rganische Chemie, Prof. Lindhorst, WS 2007/08) für Studierende der Medizin und Zahnmedizin am 12. 01. 2009 ame: Studienfach: Matrikelnummer: Ich versichere,
Zur Erreichung der Maximalnote sind von den gestellten Aufgaben 8 richtig zu lösen.
 SCRIFTLICE PRÜFUG CE 172 RGAISCE CEMIE FÜR DIE BILGIE Dienstag, 17. Juni 2014, 14:00 16:00 örsaal 30/45/60 Universität Zürich-Irchel Zur Erreichung der Maximalnote sind von den gestellten Aufgaben 8 richtig
SCRIFTLICE PRÜFUG CE 172 RGAISCE CEMIE FÜR DIE BILGIE Dienstag, 17. Juni 2014, 14:00 16:00 örsaal 30/45/60 Universität Zürich-Irchel Zur Erreichung der Maximalnote sind von den gestellten Aufgaben 8 richtig
Stereochemie. spezielle Sicht auf die Chemie, keine eigentliche Teildisziplin. abgeleitet von stereo = griech. für körperliche, räumlich
 Stereochemie Die Stereochemie befasst sich mit der Untersuchung von Eigenschaften und Reaktionen chemischer Verbindungen auf Grundlage und unter besonderer Berücksichtigung der räumlichen Struktur. spezielle
Stereochemie Die Stereochemie befasst sich mit der Untersuchung von Eigenschaften und Reaktionen chemischer Verbindungen auf Grundlage und unter besonderer Berücksichtigung der räumlichen Struktur. spezielle
4. Isomerie von Komplexverbindungen
 4. Isomerie von Komplexverbindungen 4. Isomerie bei Koordinationsverbindungen Grundsätzlich unterscheidet man Konstitutionsisomerie Strukturisomerie) und Stereoisomerie (Konfigutationsisomerie). Konstitutionsisomerie:
4. Isomerie von Komplexverbindungen 4. Isomerie bei Koordinationsverbindungen Grundsätzlich unterscheidet man Konstitutionsisomerie Strukturisomerie) und Stereoisomerie (Konfigutationsisomerie). Konstitutionsisomerie:
7 HT-NMR-Experimente und CD-Messungen
 71 7 HT-M-Experimente und CD-Messungen 7.1 otamerengleichgewichte der -geschützten Verbindungen in der M-Spektroskopie Alle synthetisierten -geschützten Verbindungen zeigen sowohl im 1 H-M- als auch im
71 7 HT-M-Experimente und CD-Messungen 7.1 otamerengleichgewichte der -geschützten Verbindungen in der M-Spektroskopie Alle synthetisierten -geschützten Verbindungen zeigen sowohl im 1 H-M- als auch im
Organische Chemie im Überblick
 Evelyne Chelain Nadeqe Lubin-Germain Jacques Uziel Organische Chemie im Überblick Grundwissen in Lerneinheiten Aus dem Französischen übersetzt von Karin Beifuss ~ Springer Spektrum Inhaltsverzeichnis 1
Evelyne Chelain Nadeqe Lubin-Germain Jacques Uziel Organische Chemie im Überblick Grundwissen in Lerneinheiten Aus dem Französischen übersetzt von Karin Beifuss ~ Springer Spektrum Inhaltsverzeichnis 1
Die Verwendung von Rot- und Bleistift sowie Tipp-Ex ist untersagt!!!
 Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Department für Chemie Prof. Dr..-G. Schmalz Prof. Dr. A. G. Griesbeck M.Sc. P. Thomopoulou Greinstr. 4 50939 Köln Modul:
Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Department für Chemie Prof. Dr..-G. Schmalz Prof. Dr. A. G. Griesbeck M.Sc. P. Thomopoulou Greinstr. 4 50939 Köln Modul:
Vorwort zur ersten Auflage
 Vorwort zur ersten Auflage Die Stereochemie ist heute eines der wichtigsten Teilgebiete der Chemie und wegen der Chiralität der Grundbausteine jeglichen Lebens auch jeder anderen Wissenschaft, in der Chemie
Vorwort zur ersten Auflage Die Stereochemie ist heute eines der wichtigsten Teilgebiete der Chemie und wegen der Chiralität der Grundbausteine jeglichen Lebens auch jeder anderen Wissenschaft, in der Chemie
Molekülsymmetrie und Kristallographie
 Optische Aktivität Wie schon im Skriptum 5 erwähnt ist es nicht einfach, aus experimentellen Daten auf die Absolutkonfiguration einer chiralen Verbindung zu schließen. In den meisten Fällen verwendet man
Optische Aktivität Wie schon im Skriptum 5 erwähnt ist es nicht einfach, aus experimentellen Daten auf die Absolutkonfiguration einer chiralen Verbindung zu schließen. In den meisten Fällen verwendet man
3. Mit der Chiralität verwandte geometrische Moleküleigenschaften
 . Mit der hiralität verwandte geometrische Moleküleigenschaften In diesem Kapitel werden drei mit dem Konzept der hiralität verwandte Phänomene behandelt. In beiden Fällen handelt es sich um achirale Verbindungen,
. Mit der hiralität verwandte geometrische Moleküleigenschaften In diesem Kapitel werden drei mit dem Konzept der hiralität verwandte Phänomene behandelt. In beiden Fällen handelt es sich um achirale Verbindungen,
Prof. Dr. Th. K. Lindhorst, SS 2003, Übungsklausur. Übungsklausur. zur Vorlesung Allgemeine Chemie II, SS 2003 Experimentalvorlesung, OC I
 Übungsklausur zur Vorlesung Allgemeine Chemie II, SS 2003 Experimentalvorlesung, C I Diese Auswahl von Aufgaben wurde auf Anfrage zusammengestellt; die Klausur könnte also beispielsweise wie folgt lauten
Übungsklausur zur Vorlesung Allgemeine Chemie II, SS 2003 Experimentalvorlesung, C I Diese Auswahl von Aufgaben wurde auf Anfrage zusammengestellt; die Klausur könnte also beispielsweise wie folgt lauten
2. Übungsblatt. Organische Chemie für Studierende mit Nebenfach Chemie
 Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Modul: BS Chemie II Organische Chemie Nachklausur zum Organisch-Chemischen Grundpraktikum für. Studierende der Biologie
 Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Institut für rganische Chemie Prof. Dr. A. G. Griesbeck Greinstr. 4 50939 Köln Modul: BS Chemie II rganische Chemie Nachklausur
Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Institut für rganische Chemie Prof. Dr. A. G. Griesbeck Greinstr. 4 50939 Köln Modul: BS Chemie II rganische Chemie Nachklausur
0.1 Kohlen(stoff)hydrate
 1 03.04.2006 0.1 Kohlen(stoff)hydrate [Schlussfolgerungen der Versuche: Trauben- und Rohrzucker enthalten 2 O. Bei Versetzung mit Schwefelsäure entsteht elementarer Kohlenstoff. Trauben- und Rohrzucker
1 03.04.2006 0.1 Kohlen(stoff)hydrate [Schlussfolgerungen der Versuche: Trauben- und Rohrzucker enthalten 2 O. Bei Versetzung mit Schwefelsäure entsteht elementarer Kohlenstoff. Trauben- und Rohrzucker
Beispielklausur Allgemeine Chemie II (Organische Chemie)
 Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
Die hierarchische Organisation biologischer Strukturen
 Das Lehrbuch Die hierarchische Organisation biologischer Strukturen Die drei Etappen der Evolution von Leben Was ist Biochemie? Untersuchung des Lebens auf molekularer Ebene Leben, wie wir es kennen, ist
Das Lehrbuch Die hierarchische Organisation biologischer Strukturen Die drei Etappen der Evolution von Leben Was ist Biochemie? Untersuchung des Lebens auf molekularer Ebene Leben, wie wir es kennen, ist
Thema: Komplexverbindungen, die koordinative Bindung. Koordinationszahl, 18-Elektronen-Schale, ein- mehrzähnige Liganden, EDTA,
 Wiederholung der letzten Vorlesungsstunde: Thema: Komplexverbindungen, die koordinative Bindung Koordinationschemie nach A. Werner, Zentralteilchen, Liganden, Koordinationszahl, 18-Elektronen-Schale, ein-
Wiederholung der letzten Vorlesungsstunde: Thema: Komplexverbindungen, die koordinative Bindung Koordinationschemie nach A. Werner, Zentralteilchen, Liganden, Koordinationszahl, 18-Elektronen-Schale, ein-
Chemie der Kohlenhydrate
 Chemie der Kohlenhydrate Grundlegendes Der Begriff Kohlenhydrate: Wurde ursprünglich aus der Formel für Glukose abgeleitet. C 6 H 12 O 6 = C 6 (H 2 O) 6 Bzw. allgemein: C n (H 2 O) m Diese missleitende
Chemie der Kohlenhydrate Grundlegendes Der Begriff Kohlenhydrate: Wurde ursprünglich aus der Formel für Glukose abgeleitet. C 6 H 12 O 6 = C 6 (H 2 O) 6 Bzw. allgemein: C n (H 2 O) m Diese missleitende
Organische Chemie. Einstieg. Chemie-Formeldarstellungen. Formeldarstellungen der Chemie: Bei Ionenverbindungen: Verhältnisformeln. , AlF 3. etc.
 Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
2.Präparat: 1,2 Dibrom -1-phenylethan
 Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Chiralität und Leben
 Chiralität und Leben Symmetrie: Ebenmaß Geometrie: Bestimmte Operationen bilden Objekt auf sich selbst ab (dabei bleibt es quasi unverändert) Rotationssymmetrie Achsensymmetrie - Spiegelsymmetrie Punktsymmetrie
Chiralität und Leben Symmetrie: Ebenmaß Geometrie: Bestimmte Operationen bilden Objekt auf sich selbst ab (dabei bleibt es quasi unverändert) Rotationssymmetrie Achsensymmetrie - Spiegelsymmetrie Punktsymmetrie
3. AUFBAU ORGANISCHER VERBINDUNGEN - ISOMERIEN
 3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
4 Naturstoffe. 1 Elemente Chemie Kursstufe Baden-Württemberg Ernst Klett Verlag GmbH, Stuttgart Lösungen zu den Durchblick-Seiten
 Lösungen zu den Durchblick-Seiten 4.32 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 2 O O + O O O 2 5 O a-ethylglucosid 2 O O O 2 5 O O O b-ethylglucosid A2 O O O L-Erythrose Enantiomere O O
Lösungen zu den Durchblick-Seiten 4.32 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 2 O O + O O O 2 5 O a-ethylglucosid 2 O O O 2 5 O O O b-ethylglucosid A2 O O O L-Erythrose Enantiomere O O
b) Zeichnen Sie die beiden möglichen Isomere der Aldol-Kondensation und bezeichnen Sie die Stereochemie der Produkte.
 1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Zeichnen Sie die beiden
1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Zeichnen Sie die beiden
Inhaltsverzeichnis zu Kapitel 5. Halogenalkane
 Inhaltsverzeichnis zu Kapitel 5. alogenalkane 5. alogenalkane 5.1 omenklatur 62 5.2 Stereoisomere 62 5.3 Darstellung von alogenalkanen 65 5.3.1 Radikalische Substitution 65 5.3.2 Elektrophile Addition
Inhaltsverzeichnis zu Kapitel 5. alogenalkane 5. alogenalkane 5.1 omenklatur 62 5.2 Stereoisomere 62 5.3 Darstellung von alogenalkanen 65 5.3.1 Radikalische Substitution 65 5.3.2 Elektrophile Addition
1. Die folgenden Alkene liefern bei der elektrophilen Addition von Brom unterschiedliche kationische Zwischenstufen.
 Professor Lindhorst rganische Chemie 1: rganisch-chemische Reaktionsmechanismen chem303 WS 2008/09 ÜUNG 4 Addition an CC-hrfachbindungen - LÖSUNGEN - 1. Die folgenden Alkene liefern bei der elektrophilen
Professor Lindhorst rganische Chemie 1: rganisch-chemische Reaktionsmechanismen chem303 WS 2008/09 ÜUNG 4 Addition an CC-hrfachbindungen - LÖSUNGEN - 1. Die folgenden Alkene liefern bei der elektrophilen
Arbeitsheft Isomerie Inhalt Jakob 1 Inhaltsverzeichnis: Seite: Vorkenntnisse: 1 Grundlagen. Atombindung, Nichtmetalle, Valenzelektronen, Bindende und
 Arbeitsheft Isomerie Inhalt Jakob 1 Inhaltsverzeichnis: Seite: Vorkenntnisse: 1 Grundlagen Atombindung, Nichtmetalle, Valenzelektronen, Bindende und 1.1 Verkürzte Schreibweisen 2 Freie Elektronenpaare,
Arbeitsheft Isomerie Inhalt Jakob 1 Inhaltsverzeichnis: Seite: Vorkenntnisse: 1 Grundlagen Atombindung, Nichtmetalle, Valenzelektronen, Bindende und 1.1 Verkürzte Schreibweisen 2 Freie Elektronenpaare,
Nachweis und Trennung von Stereoisomeren
 Nachweis und Trennung von Stereoisomeren Analyse von Stereoisomeren Problem: Unbekannte Verbindung Aufklärung der Struktur Diastereomere: Enantiomere: unterschiedliche physikalische und chemische Eigenschaften
Nachweis und Trennung von Stereoisomeren Analyse von Stereoisomeren Problem: Unbekannte Verbindung Aufklärung der Struktur Diastereomere: Enantiomere: unterschiedliche physikalische und chemische Eigenschaften
OC 3 - Stereochemie. Allgemeine Hintergründe
 OC 3 - Stereochemie Allgemeine Hintergründe Einführung Folie Nr. 2 3-dimensionale Anordnung (relativ/absolut) in der realen Welt sind extrem wichtig Bild rechts: http://de.wikipedia.org/wiki/pfefferminz,
OC 3 - Stereochemie Allgemeine Hintergründe Einführung Folie Nr. 2 3-dimensionale Anordnung (relativ/absolut) in der realen Welt sind extrem wichtig Bild rechts: http://de.wikipedia.org/wiki/pfefferminz,
ChemPad3 eine Anleitung
 ChemPad3 eine Anleitung übersetzt und adaptiert von Bernhard Sieve, IDN, Leibniz Universität Hannover Herzlich Willkommen zu ChemPad! ChemPad ist ein kleines kostenfreies Programm für Lehrkräfte, Schüler
ChemPad3 eine Anleitung übersetzt und adaptiert von Bernhard Sieve, IDN, Leibniz Universität Hannover Herzlich Willkommen zu ChemPad! ChemPad ist ein kleines kostenfreies Programm für Lehrkräfte, Schüler
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Wiederholungs-Klausur zur Vorlesung OC1 "Organischen Chemie 1" SS 2013 am
 Wiederholungs-Klausur zur Vorlesung OC1 "Organischen Chemie 1" SS 2013 am 11.10.2013 A Name...MUSTERLÖSUNG... Vorname... Matrikel-Nr... Studiengang... Viel Erfolg! Bitte schreiben Sie Ihren Namen in BLOCKSCHRIFT
Wiederholungs-Klausur zur Vorlesung OC1 "Organischen Chemie 1" SS 2013 am 11.10.2013 A Name...MUSTERLÖSUNG... Vorname... Matrikel-Nr... Studiengang... Viel Erfolg! Bitte schreiben Sie Ihren Namen in BLOCKSCHRIFT
