Michaelis-Menten-Kinetik
|
|
|
- Emil Vogel
- vor 9 Jahren
- Abrufe
Transkript
1 Michaelis-Menten-Kinetik Peter Bützer Inhalt 1 Einführung Modell Modellannahmen Drei Fälle Simulationsdiagramm (Typ ), Systemdynamik Dokumentation (Gleichungen, Parameter) Zeitdiagramm Interpretation Simulationsdiagramm (Typ 1,,4) Modellannahmen Dokumentation (Gleichungen, Parameter) Zeitdiagramm Andere Darstellung des Modells Dokumentation (Gleichungen, Parameter) Einführung Die Basis für die Enzymkinetik hat der französische Physiko-Chemier Victor Henri ( ) mit seinen Arbeiten gelegt. Darauf aufbauend haben der deutsche Mediziner und Bakteriologe Leonor Michaelis ( ) und die kanadische Medizinerin Maud Leonora Menten ( ) 191 mit ihrem Modell den Grundstein für die Enzymkinetik gelegt. Enzyme sind Proteine, die in der belebten Natur nicht nur als Biokatalysatoren sondern ebenso beudeutsam als Regler wirksam sind. Sie werden heute in vielen Gebieten z.b. in der Analytik, der Medizin, der Lebensmittelchemie, bei Waschmitteln und der Technik eingesetzt. Abbildung 1: Molekülmodell des Enzyms Catalase Prof. Dr. Peter Bützer, Pädagogische Hochschule, St.Gallen
2 2 2 Modell Das Modell eines Enzyms dargestellt als chemisches Reaktionsgleichungs-System: E + S ES v Das Enzym E reagiert mit dem Substrat S in einer Gleichgewichtsreaktion zum Enzym- Substrat-Komplex ES. Dieser Komplex zerfällt in einer bestimmten Geschwindigkeit v zum Produkt, welche umso grösser ist, je grösser die Konzentration ES. [E]: Enzym-Konzentration (mol/l) [: Substratkonzentration (mol/l) [E: Enzym-Substrat-Komplex-Konzentration: (mol/l)) Km: Dissoziationskonstante (mol/l) Michaelis-Menten-Konstante v: Geschwindigkeit (mol/l/s) : Gleichgewicht : Irreversible Reaktion v = k 1 *[E]*[; Geschwindigkeit der Hinreaktion (Gleichgewicht) v = k 2 *[E; Geschwindigkeit der Rückreaktion (Gleichgewicht) Km= k 2 /k 1 v = k *[E ; Geschwindigkeit der Produktbildung 2.1 Modellannahmen [ E] [ 1. Gleichgewicht: Km ; als Dissoziationsgleichgewicht dargestellt [ ES ] 2. Geschwindigkeit: v = k [E; Je mehr Substrat an den Enzymen gebunden ist, desto rascher ist der Umsatz.. Maximale Geschwindigkeit: v max = k [E tot ]; alle vorhandenen Enzyme arbeiten gleichzeitig. 4. Massenbilanz: [E tot ] = [E] + [E Aus diesen 4 Gleichungen erhält man durch geeignete Umformung die Gleichung von Michaelis-Menten: vmax v vmax v [ E] [ Etot ] [ ES ] k k k vmax v [ [ E] [ k ( vmax v) [ Km v v v k k v Km v v Km v [ v v ( Km [ ) v v v max max [ v [ max [ Km [ max [ [ Das auch ist die analoge Darstellung zur Monod-Kinetik!
3 2.2 Drei Fälle 1. [ << Km: v v max [/Km = k [; Die Geschwindigkeit ist ungefähr proportional der Substratkonzentration 2. [ Km: Die Gleichung kann nicht vereinfacht werden. [ >> Km: v v max ; Die Geschwindigkeit ist immer maximal (wie beim Alkoholabbau beim Menschen über 0.02 Promille) 2. Simulationsdiagramm 1 (Typ ) 2, Systemdynamik Km vm Substrat v Produkt Abbildung 2: Einfachstes Simulationsdiagramm Konstantes Volumen, daher ist Verwendung von Konzentrationen zulässig (es wird eigentlich mit der extensiven Grösse der Masse [mg] gerechnet). 2.4 Dokumentation (Gleichungen, Parameter) (01) FINAL TIME = 1000 Units: Hour The final time for the simulation. (02) INITIAL TIME = 0 Units: Hour The initial time for the simulation. (0) Km= 55 Units: mg/l [1,10000,1000] Km: Michaelis-Menten-Konstante (04) Produkt= INTEG (v, 0) Units: mg/l [0,?] Produktkonzentration (05) SAVEPER = 10 Units: Hour [0,?] The frequency with which output is stored. (06) Substrat= INTEG (-v, 1000) Units: mg/l [0,?] Substratkonzentration (07) TIME STEP = 0.1 Units: Hour [0,?] 1 Software: Programm Vensim PLE, Ventana Systems, Inc. 2 Bützer Peter, Roth Markus, Die Zeit im Griff, Systemdynamik in Chemie und Biochemie, verlag pestalozzianum, Zürich 2006, S. 50ff
4 4 The time step for the simulation. (08) v= vm*substrat/(km+substrat) Units: mg/l/hour [0,?] Reaktionsgeschwindigkeit; das ist die übliche Formel der Michaelis-Menten-Kinetik (09) vm= 2.9 Units: mg/l/hour [0,?] vm: Maximale Reaktions-Geschwindigkeit 2.5 Zeitdiagramm 4 Umsatz Substrat v : Current mg/(l*hour) Abbildung : Zeitdiagramm der Gleichgewichtseinstellung 2.6 Interpretation Die Simulation ist sehr einfach! Für kleine Substratkonzentrationen ([ << Km) ist die Reaktionsgeschwindigkeit ungefähr proportional der Substratkonzentration. Bei ganz grossen Substratkonzentrationen ([ >> Km) bleibt die Reaktionsgeschwindigkeit ungefähr konstant bei v max.
5 5 Simulation der Produktkonzentration Modell: k E S k ES k 1 2 P E [E] : Enzym-Konzentration (mol/l) [ : Substratkonzentration (mol/l) [E : Enzym-Substrat-Komplex-Konzentration: (mol/l)) [P] : Produktkonzentration (mol/l) : Gleichgewicht : Irreversible Reaktion k 1,k 2 : Reaktions-Geschwindigkeitskonstanten (mol/l/s) des Gleichgewichts k : Reaktions-Geschwindigkeitskonstante (1/s) Km= k 2 /k 1 : Gleichgewichts-Dissoziationskonstante (mol/l) Michaelis-Menten- Konstante Wichtig: Die beiden Gleichgewichtskonstanten k 1 und k 2 haben unterschiedliche Einheiten und sind daher nicht direkt vergleichbar! 2.7 Simulationsdiagramm (Typ 1,,4) 2 k1 k2 k S RG2 ES P RG RG1 Ef RGe2 RGe1 Eg Abbildung 4: Simulationsdiagramm mit getrennten Substrat-Produkt- und Enzym-Umsetzungen 2.8 Modellannahmen Konstantes Volumen, daher Verwendung von Konzentrationen Ef : Freies Enzym (mol/l) Eg: Gebundenes Enzym (mol/l) 2.9 Dokumentation (Gleichungen, Parameter) (01) Ef= INTEG ( +RGe2-RGe1, 0.01) Freies Enzym, das mit S reagieren kann (02) Eg= INTEG ( RGe1-RGe2, 0)
6 6 Gebundenes Enzym (0) ES= INTEG ( RG1-RG2-RG, 0) Enzym-Substrat-Komplex (04) FINAL TIME = 00 Units: Second The final time for the simulation. (05) INITIAL TIME = 0 Units: Second The initial time for the simulation. (06) k1= 0.5 Units: l/(second*mmol) [0,5] (07) k2= Units: 1/Second [0,?] (08) k= Units: 1/Second [0,] (09) Km= k2/k1 Michaelis-Menten-Konstante; Dissoziationskonstante (10) P= INTEG (RG, 0) (11) RG1= k1*ef*s Units: mmol/(l*second) [0,?] (12) RG2= k2*es (1) RG= k*es (14) RGe1= k1*s*ef (15) RGe2= (k2+k)*eg ES zerfällt zurück zu S (Gleichgewicht) und zu (S+P); die erste Reaktion hat k2, die zweite k. Da beide Reaktionen gleichzeitig ablaufen, zerfällt ES (also auch das gebundene Eg) mit (k2+k)*eg (16) S= INTEG (+RG2-RG1, 1) (17) SAVEPER = TIME STEP Units: Second [0,?] The frequency with which output is stored. (18) TIME STEP = 0.1 Units: Second [0,?] The time step for the simulation.
7 Zeitdiagramm 0.8 P Time (Second) P : Current mmol/l Abbildung 5: Zeitdiagramm bei relativ grossen Enzymmengen 2.11 Andere Darstellung des Modells k1 Km k2 k S ES P RG1 RG Ef Eg RGe1 Abbildung 6: Michaelis-Menten-Kinetik mit Berechnung von Km 2.12 Dokumentation (Gleichungen, Parameter) (01) Ef= INTEG ( -RGe1, 0.01) Freies Enzym, das mit S reagieren kann (02) Eg= INTEG ( RGe1, 0) Gebundenes Enzym (0) ES= INTEG ( RG1-RG, 0) Enzym-Substrat-Komplex
8 8 (04) FINAL TIME = 00 Units: Second The final time for the simulation. (05) INITIAL TIME = 0 Units: Second The initial time for the simulation. (06) k1= 0.5 Units: l/(second*mmol) [0,5] (07) k2= k1*km Units: 1/Second [0,?] (08) k= Units: 1/Second [0,] (09) Km= 0.02 Michaelis-Menten-Konstante; Dissoziationskonstante (10) P= INTEG (RG, 0) (11) RG1= k1*ef*s-k2*es Units: mmol/(l*second) [0,?] (12) RG= k*es (1) RGe1= k1*s*ef-(k2+k)*eg ES zerfällt zurück zu S (Gleichgewicht) und zu (S+P); die erste Reaktion hat k2, die zweite k. Da beide Reaktionen gleichzeitig ablaufen, zerfällt ES (also auch das gebundene Eg) mit (k2+k)*eg (14) S= INTEG (-RG1, 1) (15) SAVEPER = TIME STEP Units: Second [0,?] The frequency with which output is stored. (16) TIME STEP = 0.1 Units: Second [0,?] The time step for the simulation.
Monod-Kinetik. Peter Bützer
 Monod-Kinetik Peter Bützer Inhalt 1 Einleitung... 1 1.1 Modell... 1 1.2 Modellannahmen... 2 1. Gleichung... 2 1.4 Drei Fälle... 2 Simulation, Systemdynamik... 2.1 Simulationsdiagramm (Typ 1)... 2.2 Dokumentation
Monod-Kinetik Peter Bützer Inhalt 1 Einleitung... 1 1.1 Modell... 1 1.2 Modellannahmen... 2 1. Gleichung... 2 1.4 Drei Fälle... 2 Simulation, Systemdynamik... 2.1 Simulationsdiagramm (Typ 1)... 2.2 Dokumentation
Ethanolbildung in Bananen
 Ethanolbildung in Bananen Peter Bützer Inhalt 1 Einführung... 1 2 Modell... 2 2.1 Annahmen:... 2 2.2 Simulation(Typ 1)... 2 2.3 Dokumentation (Gleichungen, Parameter)... 3 2.4 Vergleich der Simulation
Ethanolbildung in Bananen Peter Bützer Inhalt 1 Einführung... 1 2 Modell... 2 2.1 Annahmen:... 2 2.2 Simulation(Typ 1)... 2 2.3 Dokumentation (Gleichungen, Parameter)... 3 2.4 Vergleich der Simulation
Titration einer Säure mit einer Base
 Titration einer Säure mit einer Base Peter Bützer Inhalt 1 Einleitung... 1 2 Modellannahmen (Systemdynamik)... 2 3 Simulationsdiagramm (Typ 1)... 2 4 Dokumentation (Gleichungen, Parameter)... 3 5 Simulation...
Titration einer Säure mit einer Base Peter Bützer Inhalt 1 Einleitung... 1 2 Modellannahmen (Systemdynamik)... 2 3 Simulationsdiagramm (Typ 1)... 2 4 Dokumentation (Gleichungen, Parameter)... 3 5 Simulation...
Hefewachstum. Peter Bützer
 Hefewachstum Peter Bützer Inhalt 1 Hefe... 1 2 Das System als Black Box... 2 3 Messung des... 2 4 Modell... 3 5 Simulation (Typ 9)... 3 5.1 Simulationsdiagramm... 4 5.2 Messung... 4 5.3 Dokumentation (Gleichungen,
Hefewachstum Peter Bützer Inhalt 1 Hefe... 1 2 Das System als Black Box... 2 3 Messung des... 2 4 Modell... 3 5 Simulation (Typ 9)... 3 5.1 Simulationsdiagramm... 4 5.2 Messung... 4 5.3 Dokumentation (Gleichungen,
Gipshärtung Energiefreisetzung, Systemdynamik
 Gipshärtung Energiefreisetzung, Systemdynamik Inhalt 1 Reaktion... 1 2 Experiment... 2 3 Simulation... 3 3.1 Simulationsdiagramm... 3 3.2 Dokumentation (Gleichungen, Parameter)... 3 3.3 Zeitdiagramm...
Gipshärtung Energiefreisetzung, Systemdynamik Inhalt 1 Reaktion... 1 2 Experiment... 2 3 Simulation... 3 3.1 Simulationsdiagramm... 3 3.2 Dokumentation (Gleichungen, Parameter)... 3 3.3 Zeitdiagramm...
Kohlenmonoxid aus Ethanal, CH 3 -CHO
 Kohlenmonoxid aus Ethanal, CH 3 -CHO Peter Bützer Chemiker haben viele nette Reaktionen! Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung... 2 2.1 Beobachtungen/Messungen, Datenbasis... 2 2.2 Reaktionsgleichungen/Berechnungen...
Kohlenmonoxid aus Ethanal, CH 3 -CHO Peter Bützer Chemiker haben viele nette Reaktionen! Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung... 2 2.1 Beobachtungen/Messungen, Datenbasis... 2 2.2 Reaktionsgleichungen/Berechnungen...
Kohlendioxidfreisetzung aus Champagner. 1 Einleitung/Theorie. Peter Bützer. Inhalt
 Kohlendioxidfreisetzung aus Champagner Inhalt 1 Einleitung/Theorie... 1 2 Experiment... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen... 2 2.4 Reaktionsgleichungen/Berechnungen...
Kohlendioxidfreisetzung aus Champagner Inhalt 1 Einleitung/Theorie... 1 2 Experiment... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen... 2 2.4 Reaktionsgleichungen/Berechnungen...
Daisyworld. Peter Bützer. 1 Eine kurze Theorie. Inhalt
 Daisyworld Peter Bützer Inhalt 1 Eine kurze Theorie... 1 2 Aufgabe... 2 3 Simulation, Lösung (Typ 3), Systemdynamik... 3 3.1 Annahmen... 3 3.2 Simulationsdiagramm... 3 3.3 Zeitdiagramm... 4 3.4 Dokumentation
Daisyworld Peter Bützer Inhalt 1 Eine kurze Theorie... 1 2 Aufgabe... 2 3 Simulation, Lösung (Typ 3), Systemdynamik... 3 3.1 Annahmen... 3 3.2 Simulationsdiagramm... 3 3.3 Zeitdiagramm... 4 3.4 Dokumentation
Atmung, Dissimilation
 Atmung, Dissimilation Peter Bützer Abbildung 1: Atmung Inhalt 1 Physiologisches... 1 2 Atmung, eine Reaktion 0. Ordnung... 2 3 Simulation... 2 4 Interpretation... 4 5 Mikroökologie im Zimmer... 4 6 Interpretation...
Atmung, Dissimilation Peter Bützer Abbildung 1: Atmung Inhalt 1 Physiologisches... 1 2 Atmung, eine Reaktion 0. Ordnung... 2 3 Simulation... 2 4 Interpretation... 4 5 Mikroökologie im Zimmer... 4 6 Interpretation...
Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse
 Wasserelektrolyse Peter Bützer Inhalt Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse 1 Einleitung/Theorie... 1 2 Datenbasis... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen...
Wasserelektrolyse Peter Bützer Inhalt Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse 1 Einleitung/Theorie... 1 2 Datenbasis... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen...
Phototrope Gläser. Dr. Peter Bützer. Inhalt
 1 Phototrope Gläser Inhalt 1 Einleitung/Theorie... 2 2 Experiment... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen... 3 2.4 Reaktionsgleichungen/Berechnungen... 3 3 Simulation,
1 Phototrope Gläser Inhalt 1 Einleitung/Theorie... 2 2 Experiment... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen... 3 2.4 Reaktionsgleichungen/Berechnungen... 3 3 Simulation,
Säureangriff auf die Zähne
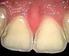 Säureangriff auf die Zähne Eine erfolgreiche Reduktion ist vielleicht die erfolgreichste Form aller wissenschaftlichen Erklärungen, die man sich vorstellen kann. 1 Karl R. Popper, (1902-199) britischer
Säureangriff auf die Zähne Eine erfolgreiche Reduktion ist vielleicht die erfolgreichste Form aller wissenschaftlichen Erklärungen, die man sich vorstellen kann. 1 Karl R. Popper, (1902-199) britischer
Zink, ein wichtiges Spurenelement
 Zink, ein wichtiges Spurenelement Peter Bützer Inhalt 1 Einleitung... 1 2 Aufgaben... 2 3 Lösungen... 3 3.1 Simulationsdiagramm (Typ 1)... 3 3.2 Dokumentation (Gleichungen, Parameter)... 3 3.3 Zeitdiagramm...
Zink, ein wichtiges Spurenelement Peter Bützer Inhalt 1 Einleitung... 1 2 Aufgaben... 2 3 Lösungen... 3 3.1 Simulationsdiagramm (Typ 1)... 3 3.2 Dokumentation (Gleichungen, Parameter)... 3 3.3 Zeitdiagramm...
Sauerstoffbindung im Blut
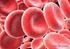 Sauerstoffbindung im Blut Die Fähigkeit uns zu wundern, ist das Einzige, was wir brauchen, um gute Philosophen zu werden. Gaarder Jostein, Sofies Welt 1 Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung...
Sauerstoffbindung im Blut Die Fähigkeit uns zu wundern, ist das Einzige, was wir brauchen, um gute Philosophen zu werden. Gaarder Jostein, Sofies Welt 1 Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung...
Indigokarmin, Indigotin - Metabolismus
 Indigokarmin, Indigotin - Metabolismus Inhalt 1.1 Chemische Charakterisierung,... 1 1.2 Verwendung und physiologische Eigenschaften... 3 1.3 Simulation des Metabolismus (Simulations-Typ 4), Systemdynamik...
Indigokarmin, Indigotin - Metabolismus Inhalt 1.1 Chemische Charakterisierung,... 1 1.2 Verwendung und physiologische Eigenschaften... 3 1.3 Simulation des Metabolismus (Simulations-Typ 4), Systemdynamik...
Gegenstand der letzten Vorlesung
 Gegenstand der letzten Vorlesung Reaktionsgeschwindigkeit Reaktionsordnung Molekularität Reaktion 0., 1.,. Ordnung Reaktion pseudo-erster Ordnung Aktivierungsenergie Temperaturabhängigkeit der Geschwindigkeitskonstanten
Gegenstand der letzten Vorlesung Reaktionsgeschwindigkeit Reaktionsordnung Molekularität Reaktion 0., 1.,. Ordnung Reaktion pseudo-erster Ordnung Aktivierungsenergie Temperaturabhängigkeit der Geschwindigkeitskonstanten
Urease. Peter Bützer. 1 Das Enzym Urease. Inhalt
 Urease Inhalt 1 Das Enzym Urease... 1 2 Das Substrat arnstoff... 2 3 Die chemische Reaktion... 2 4 Folgerung... 4 5 Messung... 4 6 Aufgabenstellung... 5 6.1 Simulation... 5 6.1.1 Annahmen... 5 6.1.2 Simulationsdiagramm
Urease Inhalt 1 Das Enzym Urease... 1 2 Das Substrat arnstoff... 2 3 Die chemische Reaktion... 2 4 Folgerung... 4 5 Messung... 4 6 Aufgabenstellung... 5 6.1 Simulation... 5 6.1.1 Annahmen... 5 6.1.2 Simulationsdiagramm
Systemdynamik: Iodwasserstoff-Gleichgewicht
 1 Systemdynamik: Iodwasserstoff-Gleichgewicht Inhalt 1 Einleitung... 1 2 Reaktionsgleichung, Substanzdaten... 2 3 Simulation... 3 3.1 Simulationsdiagramm (Reaktions Typ 3)... 3 3.2 Zeitdiagramme... 3 3.3
1 Systemdynamik: Iodwasserstoff-Gleichgewicht Inhalt 1 Einleitung... 1 2 Reaktionsgleichung, Substanzdaten... 2 3 Simulation... 3 3.1 Simulationsdiagramm (Reaktions Typ 3)... 3 3.2 Zeitdiagramme... 3 3.3
Probleme sind Gelegenheiten zu zeigen, was man kann. Duke Ellington, amerikanischer Jazz-Musiker (1899-1974)
 1 H 2 -Atemtest (Lactose-Toleranztest) Inhalt Probleme sind Gelegenheiten zu zeigen, was man kann. Duke Ellington, amerikanischer Jazz-Musiker (1899-1974) 1 Lactose-Intoleranz: Einführung... 1 2 Wasserstoff...
1 H 2 -Atemtest (Lactose-Toleranztest) Inhalt Probleme sind Gelegenheiten zu zeigen, was man kann. Duke Ellington, amerikanischer Jazz-Musiker (1899-1974) 1 Lactose-Intoleranz: Einführung... 1 2 Wasserstoff...
Biostatistik, Winter 2018/19
 1/37 Biostatistik, Winter 2018/19 Differentialgleichungen 2. Ordnung Prof. Dr. Achim Klenke http://www.aklenke.de 5. Vorlesung: 16.11.2018 2/37 Inhalt 1 Differentialgleichungen 1. Ordnung Michaelis-Menten
1/37 Biostatistik, Winter 2018/19 Differentialgleichungen 2. Ordnung Prof. Dr. Achim Klenke http://www.aklenke.de 5. Vorlesung: 16.11.2018 2/37 Inhalt 1 Differentialgleichungen 1. Ordnung Michaelis-Menten
(a) Lösen Sie die Differentialgleichung unter Verwendung der Mathematica-Funktion DSolve.
 Institut für Physikalische Chemie Methodenkurs Anwendungen von Mathematica und Matlab in der Physikalischen Chemie im WS 205/206 Prof Dr Stefan Weber, Dr Till Biskup Aufgabenblatt zum Teil (Mathematica)
Institut für Physikalische Chemie Methodenkurs Anwendungen von Mathematica und Matlab in der Physikalischen Chemie im WS 205/206 Prof Dr Stefan Weber, Dr Till Biskup Aufgabenblatt zum Teil (Mathematica)
Nutzung von Origin in der Enzym-Kinetik
 Nutzung von Origin in der Enzym-Kinetik Ausgangssituation Die Geschwindigkeit einer enzymatischen Reaktionen bei vorgegebener Enzymkonzentration aber verschiedener Substratkonzentration berechnen und grafisch
Nutzung von Origin in der Enzym-Kinetik Ausgangssituation Die Geschwindigkeit einer enzymatischen Reaktionen bei vorgegebener Enzymkonzentration aber verschiedener Substratkonzentration berechnen und grafisch
Zementhärtung. Peter Bützer
 Zementhärtung Peter Bützer Vollkommenheit entsteht offensichtlich nicht dann, wenn man nichts mehr hinzuzufügen hat, sondern, wenn man nichts mehr wegnehmen kann. Antoine de Saint-Exupéry, französischer
Zementhärtung Peter Bützer Vollkommenheit entsteht offensichtlich nicht dann, wenn man nichts mehr hinzuzufügen hat, sondern, wenn man nichts mehr wegnehmen kann. Antoine de Saint-Exupéry, französischer
Stoffwechsel bei Mehlkäferlarven
 Stoffwechsel bei Mehlkäferlarven Franziskus Graber, Peter Bützer 1 Inhalt 1 Einleitung... 1 2 Warum gerade der Mehlwurm als Versuchstier?... 2 3 Das Experiment... 2 3.1 Einige Bilder von Mehlkäferlarven...
Stoffwechsel bei Mehlkäferlarven Franziskus Graber, Peter Bützer 1 Inhalt 1 Einleitung... 1 2 Warum gerade der Mehlwurm als Versuchstier?... 2 3 Das Experiment... 2 3.1 Einige Bilder von Mehlkäferlarven...
2 NO 2 N 2 O 4, ein einfaches Gleichgewicht
 2 NO 2 N 2 O 4, ein einfaches Gleichgewicht Peter Bützer Inhalt 1 Einführung... 1 2 Grundlagen zur Reaktion... 1 3 Simulation (Typ 3), Systemdynamik... 4 3.1 Das einfache Gleichgewicht... 4 3.2 Das Prinzip
2 NO 2 N 2 O 4, ein einfaches Gleichgewicht Peter Bützer Inhalt 1 Einführung... 1 2 Grundlagen zur Reaktion... 1 3 Simulation (Typ 3), Systemdynamik... 4 3.1 Das einfache Gleichgewicht... 4 3.2 Das Prinzip
Kläranlage, biologischer Teil (Abwasserreinigungsanlage, ARA)
 Kläranlage, biologischer Teil (Abwasserreinigungsanlage, ARA) Peter Bützer Inhalt 1 Abwasser?... 1 2 Einleitung... 2 3 Aufgabe... 2 3.1 Substanzdaten... 2 3.2 Daten für das Kläranlagemodell... 3 3.3 Anlage...
Kläranlage, biologischer Teil (Abwasserreinigungsanlage, ARA) Peter Bützer Inhalt 1 Abwasser?... 1 2 Einleitung... 2 3 Aufgabe... 2 3.1 Substanzdaten... 2 3.2 Daten für das Kläranlagemodell... 3 3.3 Anlage...
Katalyse. höhere Reaktionsgeschwindigkeit bei derselben Temperatur! Achtung: Gleichgewicht der chemischen Reaktion wird nicht verschoben
 Katalyse Ein Katalysator setzt Aktivierungsenergie einer Reaktion herab, indem er einen anderen Reaktionsweg ermöglicht, so dass der geschwindigkeitsbestimmende Schritt der nicht-katalysierten Reaktion
Katalyse Ein Katalysator setzt Aktivierungsenergie einer Reaktion herab, indem er einen anderen Reaktionsweg ermöglicht, so dass der geschwindigkeitsbestimmende Schritt der nicht-katalysierten Reaktion
Praktikum. Enzymkinetik am Beispiel der Protease Trypsin
 Praktikum Methoden der molekularen Biowissenschaften Teil 1: Biochemie Enzymkinetik am Beispiel der Protease Trypsin Prof. Walter Nickel Biochemie-Zentrum der Universität Heidelberg Thermodynamische Eigenschaften
Praktikum Methoden der molekularen Biowissenschaften Teil 1: Biochemie Enzymkinetik am Beispiel der Protease Trypsin Prof. Walter Nickel Biochemie-Zentrum der Universität Heidelberg Thermodynamische Eigenschaften
1.1. Grundlage aller enzymkinetischen Untersuchungen ist die Michaelis-Menten- Gleichung: V 0 = V max x [S] K m + [S]
![1.1. Grundlage aller enzymkinetischen Untersuchungen ist die Michaelis-Menten- Gleichung: V 0 = V max x [S] K m + [S] 1.1. Grundlage aller enzymkinetischen Untersuchungen ist die Michaelis-Menten- Gleichung: V 0 = V max x [S] K m + [S]](/thumbs/58/42178387.jpg) 1.1 ABSHNITT 1: ENZYME Einführung Enzyme sind informationelle Makromoleküle und als solche Instrumente gezielter Prozeßsteuerung. Sie haben eine katalytische und eine kognitive Funktion. Die katalytische
1.1 ABSHNITT 1: ENZYME Einführung Enzyme sind informationelle Makromoleküle und als solche Instrumente gezielter Prozeßsteuerung. Sie haben eine katalytische und eine kognitive Funktion. Die katalytische
1 Michaelis-Menten-Kinetik
 Physikalische Chemie II Lösung 2 9. Dezember 206 Michaelis-Menten-Kinetik. Das Geschwindigkeitsgesetz für die zeitliche Änderung der ES-Konzentration ist durch folgendes Geschwindigkeitsgesetz beschrieben:
Physikalische Chemie II Lösung 2 9. Dezember 206 Michaelis-Menten-Kinetik. Das Geschwindigkeitsgesetz für die zeitliche Änderung der ES-Konzentration ist durch folgendes Geschwindigkeitsgesetz beschrieben:
Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease.
 A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
Den Magnesiumbedarf des Menschen abschätzen
 Den Magnesiumbedarf des Menschen abschätzen Peter Bützer Inhalt Die Zeit ist vorbeigegangen und niemand weiss wohin. 1 Einleitung... 1 2 Aufgabe... 2 3 Simulation, Systemdynamik... 3 3.1 Simulationsmodell
Den Magnesiumbedarf des Menschen abschätzen Peter Bützer Inhalt Die Zeit ist vorbeigegangen und niemand weiss wohin. 1 Einleitung... 1 2 Aufgabe... 2 3 Simulation, Systemdynamik... 3 3.1 Simulationsmodell
K3: Bestimmung der Michaelis-Menten-Kinetik von Urease
 K3: Bestimmung der Michaelis-Menten-Kinetik von Urease Einleitung: In diesem Versuch soll die Umsetzung von Harnstoff durch das Enzym Urease beobachtet werden. Fast alle Enzyme sind Proteine, manche bestehen
K3: Bestimmung der Michaelis-Menten-Kinetik von Urease Einleitung: In diesem Versuch soll die Umsetzung von Harnstoff durch das Enzym Urease beobachtet werden. Fast alle Enzyme sind Proteine, manche bestehen
[A] = c(a) in den Einheiten mol/l (1) Eine tiefgestellte Null wie bei [A] 0 zeigt an, dass es sich um eine Anfangskonzentration
![[A] = c(a) in den Einheiten mol/l (1) Eine tiefgestellte Null wie bei [A] 0 zeigt an, dass es sich um eine Anfangskonzentration [A] = c(a) in den Einheiten mol/l (1) Eine tiefgestellte Null wie bei [A] 0 zeigt an, dass es sich um eine Anfangskonzentration](/thumbs/66/55829074.jpg) 1 Ableitung des Massenwirkungsgesetzes Mit dem Umfüllexperiment haben wir herausgefunden, dass die Stoffmengen oder die Stoffmengenkonzentrationen im Gleichgewicht auf einen Grenzwert zulaufen. Außerdem
1 Ableitung des Massenwirkungsgesetzes Mit dem Umfüllexperiment haben wir herausgefunden, dass die Stoffmengen oder die Stoffmengenkonzentrationen im Gleichgewicht auf einen Grenzwert zulaufen. Außerdem
Aufnahme- und Enzymkinetik
 Aufnahme- und Enzymkinetik Kinetik = Verlauf einer Reaktion unter verschiedenen Bedingungen Alle enzym-katalysierten Reaktionen unterliegen Geschwindigkeitsgesetzen Carrier = Enzyme Enzyme sind Biokatalysatoren
Aufnahme- und Enzymkinetik Kinetik = Verlauf einer Reaktion unter verschiedenen Bedingungen Alle enzym-katalysierten Reaktionen unterliegen Geschwindigkeitsgesetzen Carrier = Enzyme Enzyme sind Biokatalysatoren
Modul 1 Dynamik multidsziplinär
 Dynamik multidisziplinär Diese Lerneinheit befasst sich mit den Grundlagen der Kinetik am Beispiel des enzymatischen Abbaus von Alkohol Zum Verständnis für die Abbaukinetik pseudo-nullter Ordnung! Zur
Dynamik multidisziplinär Diese Lerneinheit befasst sich mit den Grundlagen der Kinetik am Beispiel des enzymatischen Abbaus von Alkohol Zum Verständnis für die Abbaukinetik pseudo-nullter Ordnung! Zur
GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN
 45 GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN A. BIOCHEMISCHE GRUNDLAGEN Die katalytischen Eigenschaften eines Enzyms können durch verschiedene Faktoren beeinflusst werden. Dazu
45 GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN A. BIOCHEMISCHE GRUNDLAGEN Die katalytischen Eigenschaften eines Enzyms können durch verschiedene Faktoren beeinflusst werden. Dazu
4.1. Eigenschaften von Enzymen
 4. Enzyme 106 107 4.1. Eigenschaften von Enzymen Enzyme sind Proteine, die chemische Reaktionen beschleunigen (Biokatalysatoren) Herausragende Merkmale verglichen mit anderen Katalysatoren: drastische
4. Enzyme 106 107 4.1. Eigenschaften von Enzymen Enzyme sind Proteine, die chemische Reaktionen beschleunigen (Biokatalysatoren) Herausragende Merkmale verglichen mit anderen Katalysatoren: drastische
Vertiefendes Seminar zur Vorlesung Biochemie I. Bearbeitung Übungsblatt 6
 Vertiefendes Seminar zur Vorlesung Biochemie I 04.12.2015 Bearbeitung Übungsblatt 6 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
Vertiefendes Seminar zur Vorlesung Biochemie I 04.12.2015 Bearbeitung Übungsblatt 6 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail. Mag. Gerald Trutschl
 Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail Mag. Gerald Trutschl 1 Inhalt 1. Enzym Reaktion im Detail 2. Thermodynamische Reaktion 3. Katalysemechanismen 4. Michaelis-Menten-Konstante
Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail Mag. Gerald Trutschl 1 Inhalt 1. Enzym Reaktion im Detail 2. Thermodynamische Reaktion 3. Katalysemechanismen 4. Michaelis-Menten-Konstante
Mefenaminsäure 2-(2,3-Dimethylanilino)benzoesäure,
 Mefenaminsäure 2-(2,3-Dimethylanilino)benzoesäure, Peter Bützer Inhalt 1 Chemische Charakterisierung... 1 2 Markennamen... 2 3 Galenische Form, Wirkstoffmenge pro Dosis... 2 4 Wirkung... 2 5 Indikationen/Anwendungen...
Mefenaminsäure 2-(2,3-Dimethylanilino)benzoesäure, Peter Bützer Inhalt 1 Chemische Charakterisierung... 1 2 Markennamen... 2 3 Galenische Form, Wirkstoffmenge pro Dosis... 2 4 Wirkung... 2 5 Indikationen/Anwendungen...
Herleitung des Massenwirkungsgesetzes für das chemische Gleichgewicht zwischen Iod, Wasserstoff und Iodwasserstoff
 Lernaufgabe zum Thema Herleitung des Massenwirkungsgesetzes für das chemische Gleichgewicht zwischen Iod, Wasserstoff und Iodwasserstoff Unterrichtsfach Schultyp Zielgruppe Chemie Gymnasium, alle Typen
Lernaufgabe zum Thema Herleitung des Massenwirkungsgesetzes für das chemische Gleichgewicht zwischen Iod, Wasserstoff und Iodwasserstoff Unterrichtsfach Schultyp Zielgruppe Chemie Gymnasium, alle Typen
GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN
 53 GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN BIOCHEMISCHE GRUNDLAGEN Die katalytischen Eigenschaften eines Enzyms können durch verschiedene Faktoren beeinflusst werden. Dazu gehören
53 GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN BIOCHEMISCHE GRUNDLAGEN Die katalytischen Eigenschaften eines Enzyms können durch verschiedene Faktoren beeinflusst werden. Dazu gehören
Glykämischer Index. Peter Bützer
 Glykämischer Index Peter Bützer Inhalt 1 Einleitung/Theorie... 1 2 Datenbasis... 3 2.1 Aufgabenstellung... 3 2.2 Durchführung... 3 2.3 Beobachtungen/Messungen... 3 2.4 Reaktionsgleichungen/Berechnungen...
Glykämischer Index Peter Bützer Inhalt 1 Einleitung/Theorie... 1 2 Datenbasis... 3 2.1 Aufgabenstellung... 3 2.2 Durchführung... 3 2.3 Beobachtungen/Messungen... 3 2.4 Reaktionsgleichungen/Berechnungen...
K3: Bestimmung der Michaelis-Menten-Kinetik von Urease
 K3: Bestimmung der Michaelis-Menten-Kinetik von Urease Einleitung: In diesem Versuch soll die Umsetzung von Harnstoff durch das Enzym Urease beobachtet werden. Fast alle Enzyme sind Proteine, manche bestehen
K3: Bestimmung der Michaelis-Menten-Kinetik von Urease Einleitung: In diesem Versuch soll die Umsetzung von Harnstoff durch das Enzym Urease beobachtet werden. Fast alle Enzyme sind Proteine, manche bestehen
Die Geschwindigkeit zum Gleichgewicht
 2F 3F 6F 7F 8F Inhalt Die Geschwindigkeit zum Gleichgewicht Peter Bützer 0H1 1H2 2H3 8H4 15H5 Einleitung... 17H1 Reaktionsgleichung, Substanzdaten... 18H2 Simulation... 19H3 3H3.1 Simulationsdiagramm (Reaktions-Typ
2F 3F 6F 7F 8F Inhalt Die Geschwindigkeit zum Gleichgewicht Peter Bützer 0H1 1H2 2H3 8H4 15H5 Einleitung... 17H1 Reaktionsgleichung, Substanzdaten... 18H2 Simulation... 19H3 3H3.1 Simulationsdiagramm (Reaktions-Typ
7 ENZYMKINETIK 7.5 Pre-steady State Kinetik bei schnellen Reaktionen. (t 1 e (k 1[S] 0 +k 2 +k 1. k 1 [S] 0 + k 2 + k 1. t/ms
![7 ENZYMKINETIK 7.5 Pre-steady State Kinetik bei schnellen Reaktionen. (t 1 e (k 1[S] 0 +k 2 +k 1. k 1 [S] 0 + k 2 + k 1. t/ms 7 ENZYMKINETIK 7.5 Pre-steady State Kinetik bei schnellen Reaktionen. (t 1 e (k 1[S] 0 +k 2 +k 1. k 1 [S] 0 + k 2 + k 1. t/ms](/thumbs/97/132715863.jpg) v0(t) [P](t) " & $ " & $ " [P] = v max τ k 2 [S] 0 [E] 0 [S] 0 +(k + k 2 )/k " & " % " $ " # v max " $ & (t e (k [S] 0 +k 2 +k ) )t & # ' ' # " $ & k [S] 0 + k 2 + k t/ms t/ms Bild 5: Allmähliche Annäherung
v0(t) [P](t) " & $ " & $ " [P] = v max τ k 2 [S] 0 [E] 0 [S] 0 +(k + k 2 )/k " & " % " $ " # v max " $ & (t e (k [S] 0 +k 2 +k ) )t & # ' ' # " $ & k [S] 0 + k 2 + k t/ms t/ms Bild 5: Allmähliche Annäherung
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo
 Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: [email protected] innere Energie U Energieumsatz bei
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: [email protected] innere Energie U Energieumsatz bei
Michaelis-Menten-Gleichung
 Physikalisch-Chemische Praktika Michaelis-Menten-Gleichung Versuch K4 1 Aufgabe Experimentelle Bestimmung der Kinetik der Zersetzung von Harnsto durch Urease. 2 Grundlagen Im Bereich der Biochemie spielen
Physikalisch-Chemische Praktika Michaelis-Menten-Gleichung Versuch K4 1 Aufgabe Experimentelle Bestimmung der Kinetik der Zersetzung von Harnsto durch Urease. 2 Grundlagen Im Bereich der Biochemie spielen
Richtung von spontanem Prozeßablauf und Veränderung der G in Abhängigkeit vom Vorzeichen der Enthalpie und der Entropie
 Richtung von spontanem Prozeßablauf und Veränderung der G in Abhängigkeit vom Vorzeichen der Enthalpie und der Entropie H S G= H-T S Prozeß 1. (-) (+) (-) immer exergonisch, erfolgt spontan bei allen Temperaturen
Richtung von spontanem Prozeßablauf und Veränderung der G in Abhängigkeit vom Vorzeichen der Enthalpie und der Entropie H S G= H-T S Prozeß 1. (-) (+) (-) immer exergonisch, erfolgt spontan bei allen Temperaturen
(a) Lösen Sie die Differentialgleichung unter Verwendung der Mathematica-Funktion DSolve.
 Institut für Physikalische Chemie Methodenkurs Anwendungen von Mathematica und Matlab in der Physikalischen Chemie im WS 06/07 Prof Dr Stefan Weber, Dr Till Biskup Aufgabenblatt zum Mathematica-Teil vom
Institut für Physikalische Chemie Methodenkurs Anwendungen von Mathematica und Matlab in der Physikalischen Chemie im WS 06/07 Prof Dr Stefan Weber, Dr Till Biskup Aufgabenblatt zum Mathematica-Teil vom
Chemisches Gleichgewicht in homogenen Systemen I Seminarvortrag SoSe 08
 Chemisches Gleichgewicht in homogenen Systemen I Seminarvortrag SoSe 08 Sebastian Meiss 14. Mai 2008 1 Historischer Einstieg Erstmals wurde das Massenwirkungsgesetz 1867 von dem norwegischen Mathematiker
Chemisches Gleichgewicht in homogenen Systemen I Seminarvortrag SoSe 08 Sebastian Meiss 14. Mai 2008 1 Historischer Einstieg Erstmals wurde das Massenwirkungsgesetz 1867 von dem norwegischen Mathematiker
Reaktionskinetik. Geschwindigkeitsgesetze
 Reaktionskinetik Geschwindigkeitsgesetze Lernziele: Thermodynamische Beschreibung chemischer Reaktionen Berechnen und Beschreiben von Reaktionsordnungen Kinetische Beschreibung von Reaktionsmechanismen
Reaktionskinetik Geschwindigkeitsgesetze Lernziele: Thermodynamische Beschreibung chemischer Reaktionen Berechnen und Beschreiben von Reaktionsordnungen Kinetische Beschreibung von Reaktionsmechanismen
Grundlagen der Chemie Chemisches Gleichgewicht
 Chemisches Gleichgewicht Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Das Massenwirkungsgesetz Wenn Substanzen
Chemisches Gleichgewicht Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Das Massenwirkungsgesetz Wenn Substanzen
Enzymkinetik: Kinetik der alkalischen Phosphatase mit dem Substrat p-nitrophenylphosphat
 Biophysikalisches Praktikum Institut für Biophysik Johann Wolfgang Goethe-Universität Frankfurt am Main Enzymkinetik: Kinetik der alkalischen Phosphatase mit dem Substrat p-nitrophenylphosphat (letzte
Biophysikalisches Praktikum Institut für Biophysik Johann Wolfgang Goethe-Universität Frankfurt am Main Enzymkinetik: Kinetik der alkalischen Phosphatase mit dem Substrat p-nitrophenylphosphat (letzte
ENZYME. Teil 1: Grundlagen und Substratbestimmungen
 ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
6. Fragentyp A Wie berechnet man die ph-werte wässriger Lösungen starker Basen? A) ph = pks - log [HA] / 2 B) ph = 14 + log [OH-] C) ph = 7+ 1/2 pkb +
![6. Fragentyp A Wie berechnet man die ph-werte wässriger Lösungen starker Basen? A) ph = pks - log [HA] / 2 B) ph = 14 + log [OH-] C) ph = 7+ 1/2 pkb + 6. Fragentyp A Wie berechnet man die ph-werte wässriger Lösungen starker Basen? A) ph = pks - log [HA] / 2 B) ph = 14 + log [OH-] C) ph = 7+ 1/2 pkb +](/thumbs/77/74984433.jpg) 1. Fragentyp D Welche der folgenden Einheiten für den molaren Extinktionskoeffizienten ist/sind korrekt? 1) liter I mol x cm 2) liter I mol 3) cm2 / mmol 4) cm2 / mmol x m1 2. Wie lautet die Henderson-Hasselbalch-Gleichung?
1. Fragentyp D Welche der folgenden Einheiten für den molaren Extinktionskoeffizienten ist/sind korrekt? 1) liter I mol x cm 2) liter I mol 3) cm2 / mmol 4) cm2 / mmol x m1 2. Wie lautet die Henderson-Hasselbalch-Gleichung?
Biochemische UE Alkaline Phosphatase.
 Biochemische UE Alkaline Phosphatase [email protected] Alkaline Phosphatase: Katalysiert die Hydrolyse von Phosphorsäure-Estern: O - O - Ser-102 R O P==O O - H 2 O R OH + HO P==O O - ph-optimum im
Biochemische UE Alkaline Phosphatase [email protected] Alkaline Phosphatase: Katalysiert die Hydrolyse von Phosphorsäure-Estern: O - O - Ser-102 R O P==O O - H 2 O R OH + HO P==O O - ph-optimum im
Versuch 4. Enzymkinetik
 Versuch 4 Enzymkinetik Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann [email protected] X X X Dr. Postina Wird benotet?: Aufgabenstellung Ermittlung der maximalen Reaktionsgeschwindigkeit
Versuch 4 Enzymkinetik Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann [email protected] X X X Dr. Postina Wird benotet?: Aufgabenstellung Ermittlung der maximalen Reaktionsgeschwindigkeit
Harnstoffspaltung durch Urease. Messzylinder, 50 ml Stativ Muffe Greifklemme, klein Magnetrührer Rührfisch
 Prinzip Bei der Spaltung von Harnstoff entstehen Kohlenstoffdioxid und Ammoniak, wobei insbesondere letzteres mit Wasser leicht zu Ammonium- und Hydroxidionen reagiert. Daher bietet sich eine Verfolgung
Prinzip Bei der Spaltung von Harnstoff entstehen Kohlenstoffdioxid und Ammoniak, wobei insbesondere letzteres mit Wasser leicht zu Ammonium- und Hydroxidionen reagiert. Daher bietet sich eine Verfolgung
9 ENZYMKINETIK 9.5 Pre-steady State Kinetik bei schnellen Reaktionen. 9.5 Pre-steady State Kinetik bei schnellen Reaktionen
 9.5 Pre-steady State Kinetik bei schnellen Reaktionen Die bisherige Diskussion der enzymkatalytischen Mechanismen hat sich auf stationäre Zustände beschränkt. Dies wurde dazu benutzt, die Parameter v max,k
9.5 Pre-steady State Kinetik bei schnellen Reaktionen Die bisherige Diskussion der enzymkatalytischen Mechanismen hat sich auf stationäre Zustände beschränkt. Dies wurde dazu benutzt, die Parameter v max,k
Vorlesung Allgemeine Chemie Teil Physikalische Chemie WS 2009/10
 Vorlesung Allgemeine Chemie Teil Physikalische Chemie WS 2009/10 Dr. Lars Birlenbach Physikalische Chemie, Universität Siegen Raum AR-F0102 Tel.: 0271 740 2817 email: [email protected] Lars
Vorlesung Allgemeine Chemie Teil Physikalische Chemie WS 2009/10 Dr. Lars Birlenbach Physikalische Chemie, Universität Siegen Raum AR-F0102 Tel.: 0271 740 2817 email: [email protected] Lars
endotherme Reaktionen
 Exotherme/endotherme endotherme Reaktionen Edukte - H Produkte Exotherme Reaktion Edukte Produkte + H Endotherme Reaktion 101 Das Massenwirkungsgesetz Das Massenwirkungsgesetz Gleichgewicht chemischer
Exotherme/endotherme endotherme Reaktionen Edukte - H Produkte Exotherme Reaktion Edukte Produkte + H Endotherme Reaktion 101 Das Massenwirkungsgesetz Das Massenwirkungsgesetz Gleichgewicht chemischer
= Durchschnittliche Bildungs- Geschwindigkeit [mol/s] = Durchschnittliche Verbrauchs- Geschwindigkeit [mol/s]
![= Durchschnittliche Bildungs- Geschwindigkeit [mol/s] = Durchschnittliche Verbrauchs- Geschwindigkeit [mol/s] = Durchschnittliche Bildungs- Geschwindigkeit [mol/s] = Durchschnittliche Verbrauchs- Geschwindigkeit [mol/s]](/thumbs/94/122358469.jpg) Ache2 Kapitel 14: Chemische Kinetik (Geschwindigkeit) Reaktionsgeschwindigkeit Beeinflussung: 1. Aggregatszustände der Reaktanten: Je öfters Moleküle zusammenstossen, desto schneller reagieren sie. (Oberflächenvergrösserung
Ache2 Kapitel 14: Chemische Kinetik (Geschwindigkeit) Reaktionsgeschwindigkeit Beeinflussung: 1. Aggregatszustände der Reaktanten: Je öfters Moleküle zusammenstossen, desto schneller reagieren sie. (Oberflächenvergrösserung
Enzyme. Prof. Dr. Albert Duschl
 Enzyme Prof. Dr. Albert Duschl Katalyse Reaktionen laufen normalerweise nicht spontan ab, auch wenn insgesamt dabei Energie gewonnen werden sollte. Es muß zunächst eine Aktivierungsenergie aufgebracht
Enzyme Prof. Dr. Albert Duschl Katalyse Reaktionen laufen normalerweise nicht spontan ab, auch wenn insgesamt dabei Energie gewonnen werden sollte. Es muß zunächst eine Aktivierungsenergie aufgebracht
Gefährdung durch Polonium-210 ( Po)
 Gefährdung durch Polonium-210 ( 210 84Po) Peter Bützer Inhalt 1 Wie lässt sich die Gefährdung durch Polonium-210 abschätzen?... 2 2 Grundbegriffe... 2 3 Ein kurzer Steckbrief zu Polonium... 2 4 Gewinnung...
Gefährdung durch Polonium-210 ( 210 84Po) Peter Bützer Inhalt 1 Wie lässt sich die Gefährdung durch Polonium-210 abschätzen?... 2 2 Grundbegriffe... 2 3 Ein kurzer Steckbrief zu Polonium... 2 4 Gewinnung...
Enzym-Kinetik (Abb. 1) Das Thema der heutigen Vorlesung ist die Kinetik isolierter und gereinigter Enzyme zum Verständnis ihrer Reaktionsmechanismen.
 1 Enzym-Kinetik (Abb. 1) Das Thema der heutigen Vorlesung ist die Kinetik isolierter und gereinigter Enzyme zum Verständnis ihrer Reaktionsmechanismen. Wie ich schon erwähnte, ist die Geschwindigkeit (V)
1 Enzym-Kinetik (Abb. 1) Das Thema der heutigen Vorlesung ist die Kinetik isolierter und gereinigter Enzyme zum Verständnis ihrer Reaktionsmechanismen. Wie ich schon erwähnte, ist die Geschwindigkeit (V)
Das Chemische Gleichgewicht
 Das Chemische Gleichgewicht Geschwindigkeit der Hinreaktion: v hin = k hin c(a 2 ) c(x 2 ) Geschwindigkeit der Rückreaktion: v rück = k rück c 2 (AX) Gleichgewicht: v hin = v rück k hin c(a 2 ) c(x 2 )
Das Chemische Gleichgewicht Geschwindigkeit der Hinreaktion: v hin = k hin c(a 2 ) c(x 2 ) Geschwindigkeit der Rückreaktion: v rück = k rück c 2 (AX) Gleichgewicht: v hin = v rück k hin c(a 2 ) c(x 2 )
Aufgabengruppe BMS Chemie
 Aufgabengruppe BMS Chemie Zeitvorgabe: Bitte lösen Sie die folgenden 24 Aufgaben innerhalb von 18 Minuten! 1) Welche Aussagen treffen auf Proteine zu? I. Die Primärstruktur gibt die Aminosäurenabfolge
Aufgabengruppe BMS Chemie Zeitvorgabe: Bitte lösen Sie die folgenden 24 Aufgaben innerhalb von 18 Minuten! 1) Welche Aussagen treffen auf Proteine zu? I. Die Primärstruktur gibt die Aminosäurenabfolge
Versuch: Enzyme (LDH)
 Versuch: Enzyme (LDH) 25.11.02 Seiten im Campell, Tierphysbuch (Penzlin) und Eckert Zusammenfassung Campbell S. 105-113 Zusammenfassung Eckert S. 77 89 Zusammenfassung Penzlin S. 50 ff. Allgemein: Temperatur
Versuch: Enzyme (LDH) 25.11.02 Seiten im Campell, Tierphysbuch (Penzlin) und Eckert Zusammenfassung Campbell S. 105-113 Zusammenfassung Eckert S. 77 89 Zusammenfassung Penzlin S. 50 ff. Allgemein: Temperatur
Grundlagen der Zellulären Biochemie
 Grundlagen der Zellulären Biochemie Enzyme Vorlesung zum Modul BCB P07 im Bachelor-Studiengang Biochemie Hannover Prof. J. Alves, Institut für Biophysikalische Chemie, MHH Enzyme Der Name Enzym wurde 1878
Grundlagen der Zellulären Biochemie Enzyme Vorlesung zum Modul BCB P07 im Bachelor-Studiengang Biochemie Hannover Prof. J. Alves, Institut für Biophysikalische Chemie, MHH Enzyme Der Name Enzym wurde 1878
Enzyme SPF BCH am
 Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Grundlagen der Kinetik
 Kapitel 1 Grundlagen der Kinetik In diesem Kapitel werden die folgenden Themen kurz wiederholt: Die differenziellen und integralen Geschwindigkeitsgesetze von irreversiblen Reaktionen., 1., und. Ordnung
Kapitel 1 Grundlagen der Kinetik In diesem Kapitel werden die folgenden Themen kurz wiederholt: Die differenziellen und integralen Geschwindigkeitsgesetze von irreversiblen Reaktionen., 1., und. Ordnung
Praktikum Biochemie Einführung in die Molekularbiologie. Bettina Siebers
 Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli Reinigung Protein Aktivitätstest Platte in 9 Teile
Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli Reinigung Protein Aktivitätstest Platte in 9 Teile
Fragen zum Versuch 11a Kinetik Rohrzuckerinversion:
 Fragen zum Versuch 11a Kinetik Rohrzuckerinversion: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen
Fragen zum Versuch 11a Kinetik Rohrzuckerinversion: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen
Inhaltsverzeichnis Hinweise zur Benutzung Einführung in die Arbeits- und Denkweise Basis der Thermodynamik
 Inhaltsverzeichnis 1 Hinweise zur Benutzung... 1 1.1 Ausrichtung...... 1 1.2 Lernhilfen und -kontrollen...... 4 2 Einführung in die Arbeits- und Denkweise... 9 2.1 Zielsetzung...... 9 2.2 Wichtige physikalische
Inhaltsverzeichnis 1 Hinweise zur Benutzung... 1 1.1 Ausrichtung...... 1 1.2 Lernhilfen und -kontrollen...... 4 2 Einführung in die Arbeits- und Denkweise... 9 2.1 Zielsetzung...... 9 2.2 Wichtige physikalische
Eine Runaway-Reaktion
 Eine Runaway-Reaktion Peter Bützer, Markus Roth Inhalt 0H1 1H2 2H3 3H4 8H5 15H6 17H7 18H8 19H9 20H10 Dynamik in der Chemie... 21H1 Schritte der Systemdynamik... 22H2 Ein Katalysator... 23H3 Das Experiment...
Eine Runaway-Reaktion Peter Bützer, Markus Roth Inhalt 0H1 1H2 2H3 3H4 8H5 15H6 17H7 18H8 19H9 20H10 Dynamik in der Chemie... 21H1 Schritte der Systemdynamik... 22H2 Ein Katalysator... 23H3 Das Experiment...
Dynamik der Ammoniaksynthese
 Dynamik der Ammoniaksynthese Peter Bützer Die intellektuelle Verantwortlichkeit besteht darin, eine Sache so klar und deutlich hinzustellen, dass man dem Betreffenden, wenn er etwas Falsches oder Unklares
Dynamik der Ammoniaksynthese Peter Bützer Die intellektuelle Verantwortlichkeit besteht darin, eine Sache so klar und deutlich hinzustellen, dass man dem Betreffenden, wenn er etwas Falsches oder Unklares
Lösung 7. Allgemeine Chemie I Herbstsemester Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf.
 Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
1) Ein offenes System zeichnet sich immer durch eine konstante Temperatur aus. zeichnet sich immer durch eine konstante Masse aus.
 1) Ein offenes System zeichnet sich immer durch eine konstante Temperatur aus. zeichnet sich immer durch eine konstante Masse aus. kann mit der Umgebung Energie austauschen. kann mit der Umgebung Entropie
1) Ein offenes System zeichnet sich immer durch eine konstante Temperatur aus. zeichnet sich immer durch eine konstante Masse aus. kann mit der Umgebung Energie austauschen. kann mit der Umgebung Entropie
Film der Einheit Gleichgewichte
 Film der Einheit Gleichgewichte Gleichgewichte in verschiedenen Disziplinen Richtung und Vollständigkeit einer Reaktion Chemisches Gleichgewicht Was ist das? Chemisches Gleichgewicht als dynamischer Prozess
Film der Einheit Gleichgewichte Gleichgewichte in verschiedenen Disziplinen Richtung und Vollständigkeit einer Reaktion Chemisches Gleichgewicht Was ist das? Chemisches Gleichgewicht als dynamischer Prozess
Autokatalysator (Abgaskatalysator, Fahrzeugkatalysator, Systemdynamik)
 Autokatalysator (Abgaskatalysator, Fahrzeugkatalysator, Systemdynamik) Peter Bützer Abstract Die chemischen Grundlagen der Verbrennung sind die Grundlage für die Funktion des Abgaskatalysators. Über die
Autokatalysator (Abgaskatalysator, Fahrzeugkatalysator, Systemdynamik) Peter Bützer Abstract Die chemischen Grundlagen der Verbrennung sind die Grundlage für die Funktion des Abgaskatalysators. Über die
Enzymkinetik in der Schule Michaelis-Menten-Kinetik von Urease. Das Enzym Urease. Sara Müller 1, 2, Marianne Kromke 2, Helmut Vogt 2, Daniela Moll 3
 Enzymkinetik in der Schule Michaelis-Menten-Kinetik von Urease Sara Müller 1, 2, Marianne Kromke 2, Helmut Vogt 2, Daniela Moll 3 1 Science Bridge, Universität Kassel 2 Abt. Didaktik der Biologie, Universität
Enzymkinetik in der Schule Michaelis-Menten-Kinetik von Urease Sara Müller 1, 2, Marianne Kromke 2, Helmut Vogt 2, Daniela Moll 3 1 Science Bridge, Universität Kassel 2 Abt. Didaktik der Biologie, Universität
Enzyme: Grundlegende Konzepte und Kinetik
 Enzyme: Grundlegende Konzepte und Kinetik Enzyme sind Katalysatoren biologischer Systeme Wichtigste Eigenschaften: katalytische Stärke und Spezifität Nahezu alle bekannten Enzyme sind Proteine, es gibt
Enzyme: Grundlegende Konzepte und Kinetik Enzyme sind Katalysatoren biologischer Systeme Wichtigste Eigenschaften: katalytische Stärke und Spezifität Nahezu alle bekannten Enzyme sind Proteine, es gibt
Enzymatische Hydrolyse von Harnstoff
 Übungen in physikalischer Chemie für B.Sc.-Studierende Versuch Nr.: W11 Version 217 (18817) Kurzbezeichnung: Enzymkinetik Enzymatische Hydrolyse on Harnstoff Aufgabenstellung Die enzymkatalysierte Hydrolyse
Übungen in physikalischer Chemie für B.Sc.-Studierende Versuch Nr.: W11 Version 217 (18817) Kurzbezeichnung: Enzymkinetik Enzymatische Hydrolyse on Harnstoff Aufgabenstellung Die enzymkatalysierte Hydrolyse
Chemie Protokoll. Versuch 2 3 (RKV) Reaktionskinetik Esterverseifung. Stuttgart, Sommersemester 2012
 Chemie Protokoll Versuch 2 3 (RKV) Reaktionskinetik Esterverseifung Stuttgart, Sommersemester 202 Gruppe 0 Jan Schnabel Maximilian Möckel Henri Menke Assistent: Durmus 20. Mai 202 Inhaltsverzeichnis Theorie
Chemie Protokoll Versuch 2 3 (RKV) Reaktionskinetik Esterverseifung Stuttgart, Sommersemester 202 Gruppe 0 Jan Schnabel Maximilian Möckel Henri Menke Assistent: Durmus 20. Mai 202 Inhaltsverzeichnis Theorie
Benutzen Sie, falls erforderlich, die folgenden Werte für die Naturkonstanten. Naturkonstante Zahlenwert Einheit
 Benutzen Sie, falls erforderlich, die folgenden Werte für die Naturkonstanten. Naturkonstante Zahlenwert Einheit Allgemeine Gaskonstante R 8,3145 J mol -1 K -1 Elementarladung e 1,6022 10-19 C Faradaykonstante
Benutzen Sie, falls erforderlich, die folgenden Werte für die Naturkonstanten. Naturkonstante Zahlenwert Einheit Allgemeine Gaskonstante R 8,3145 J mol -1 K -1 Elementarladung e 1,6022 10-19 C Faradaykonstante
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
Vom Molekül zur Zelle Block 3 Seminar / Praktikum 2
 Vom Molekül zur Zelle Block 3 Seminar / Praktikum 2 Diese Präsentation befindet sich auf der Lehr-Inhalts Seite des Inst f. unter www.meduniwien.ac.at/hp/medizinische-genetik/lehre Helmut Dolznig Inst.
Vom Molekül zur Zelle Block 3 Seminar / Praktikum 2 Diese Präsentation befindet sich auf der Lehr-Inhalts Seite des Inst f. unter www.meduniwien.ac.at/hp/medizinische-genetik/lehre Helmut Dolznig Inst.
V 23 Dilatometrische Bestimmung reaktionskinetischer Größen
 Grundpraktikum Physikalische Chemie V 23 Dilatometrische Bestimmung reaktionskinetischer Größen Überarbeitetes Versuchsskript, L. Kibler, 19.11.2007 1 1. Vorkenntnisse Vor Durchführung des Versuches sollten
Grundpraktikum Physikalische Chemie V 23 Dilatometrische Bestimmung reaktionskinetischer Größen Überarbeitetes Versuchsskript, L. Kibler, 19.11.2007 1 1. Vorkenntnisse Vor Durchführung des Versuches sollten
3.4 Energieumsatz bei Reaktionen
 3.4 Energieumsatz bei Reaktionen Versuch: Verbrennen eines Stückes Holz Beobachtung: Energie wird freigesetzt in Form von Wärme. Jede Reaktion ist mit einem Energieumsatz gekoppelt. Reaktionen, bei denen
3.4 Energieumsatz bei Reaktionen Versuch: Verbrennen eines Stückes Holz Beobachtung: Energie wird freigesetzt in Form von Wärme. Jede Reaktion ist mit einem Energieumsatz gekoppelt. Reaktionen, bei denen
K4 Argumentation B3 Werte und Normen
 Thema/Kontext: Auf die Geschwindigkeit kommt es an Inhaltsfeld: Reaktionsgeschwindigkeit und Gleichgewichtsreaktionen Inhaltliche Schwerpunkte: Schwerpunkte übergeordneter Kompetenzerwartungen: Reaktionsgeschwindigkeit
Thema/Kontext: Auf die Geschwindigkeit kommt es an Inhaltsfeld: Reaktionsgeschwindigkeit und Gleichgewichtsreaktionen Inhaltliche Schwerpunkte: Schwerpunkte übergeordneter Kompetenzerwartungen: Reaktionsgeschwindigkeit
Das chemische Gleichgewicht
 Das chemische Gleichgewicht Modell: Geschlossenes Gefäß mit Flüssigkeit, die verdampft ( T=const ) Moleküle treten über in die Dampfphase H 2 O (l) H 2 O (g) H 2 O (g) Dampfdruck p H 2 O (l) T = const.
Das chemische Gleichgewicht Modell: Geschlossenes Gefäß mit Flüssigkeit, die verdampft ( T=const ) Moleküle treten über in die Dampfphase H 2 O (l) H 2 O (g) H 2 O (g) Dampfdruck p H 2 O (l) T = const.
Fragen zum Versuch Kinetik:
 Fragen zum Versuch Kinetik: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen von Rohrzucker im Wasser
Fragen zum Versuch Kinetik: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen von Rohrzucker im Wasser
