9 Herkunft des ATP. 9.2 Der Citratzyklus
|
|
|
- Werner Dittmar
- vor 7 Jahren
- Abrufe
Transkript
1 Der Citratzyklus Im Rahmen des Citratzyklus wird Acetyl-CoA zu zwei Molekülen CO 2 umgewandelt, wobei zusätzlich noch Energie in Form von ATP und GTP sowie Reduktionsäquivalente in Form von NADH/H + und FADH 2 entstehen. Der Citratzyklus findet vollständig in den Mitochondrien statt und kann daher in allen unseren Zellen bis auf den Erythrozyten ablaufen.
2 9.2 Der Citratzyklus 201 Diesem einzigartigen Stoffwechselweg hat man im Laufe der Zeit viele Attribute verpasst. Die einen bezeichnen den Citratzyklus als das Zentrum, die anderen als die Drehscheibe des gesamten Stoffwechsels in einem Organismus. Beides trifft den Nagel auf den Kopf, denn der Citratzyklus verbindet tatsächlich so ziemlich alle Abbau- und auch viele Biosynthesewege von Kohlenhydraten, Aminosäuren, Lipiden und anderen biochemischen Stoffklassen. (Trotzdem wurde die Erstpublikation des Citratzyklus von der renommierten Zeitschrift Nature abgelehnt...) Die Abbauprodukte der drei Hauptnährstoffe (v. a. Acetyl- CoA) werden durch den Citratzyklus vollständig verstoffwechselt und danach einer gemeinsamen Endstrecke, der Atmungskette ( S. 214), zugeführt. Daraus erklärt sich auch die Lokalisation des Citratzyklus im Mitochondrium, in dessen Matrix sich alle dazu benötigten Enzyme befinden. Der Citratzyklus liegt also in nächster Nähe zu den Komplexen der Atmungskette, wodurch beide Prozesse optimal aneinander gekoppelt sind. Ein Enzym des Citratzyklus wird (als Komplex II) sogar direkt der Atmungskette zugerechnet. Seinen Namen hat er übrigens vom Einstiegsmolekül Citrat, einer Tricarbonsäure, die aus der Reaktion von Acetyl-CoA mit Oxalacetat entsteht. Der Citratzyklus wurde schon 1937 von Hans Krebs ( ) postuliert, weshalb er gelegentlich auch Krebs-Zyklus genannt wird. (Die Nationalsozialisten haben Krebs übrigens gezwungen, das Land zu verlassen, weshalb er zum Zeitpunkt der Entdeckung in England lebte. Daher wird der Citratzyklus im anglo-amerikanischen Sprachraum als Krebs cycle bezeichnet.) Zunächst war man sich nicht ganz sicher, ob Citrat oder nicht doch eine andere Tricarbonsäure, z. B. das Isocitrat, das Einstiegsmolekül darstellten. Daher hält sich auch heute noch gelegentlich der anfängliche Name Tricarbonsäure- Zyklus. Worum geht es beim Citratzyklus? Die entscheidende Aufgabe des Citratzyklus besteht darin, Acetyl-CoA in einem Kreisprozess zu CO 2, NADH/H +, FADH 2 und GTP abzubauen. Die Reduktionsäquivalente NADH/H + und FADH 2 liefern dann in der Atmungskette das, wofür die Zelle den ganzen Aufwand eigentlich betreibt, nämlich Energie in Form von ATP. CO 2 ist ein Abfallprodukt und wird abgeatmet. Um den Acetyl-Rest nur einfach abzubauen, scheint der Citratzyklus reichlich kompliziert geraten. Und in der Tat steckt da noch mehr dahinter: Der Citratzyklus bietet nämlich auch zahlreiche Ein- und Ausgangsmöglichkeiten für Biosynthesewege. Wir beginnen hier mit dem einfachen Abbau des Acetyl- CoAund lüften dann erst später die tieferen Geheimnisse dieser Drehscheibe des Stoffwechsels. Katabole Funktionen des Citratzyklus Chemisch betrachtet sind vier der acht Reaktionen des Citratzyklus Oxidationen, bei denen die Elektronen (zusammen mit Protonen) an NAD + oder FAD weitergegeben werden. Bei diesen handelt es sich um spezialisierte Elektronentransporter, die die Elektronen zur Atmungskette transportieren. Der Citratzyklus ist ein Kreisprozess, da das Eingangsmolekül Oxalacetat nach den acht Reaktionen wieder unversehrt vorliegt. Beim Durchlauf eines Acetyl-Restes entstehen dabei zwei Moleküle CO 2, acht Wasserstoffatome, die an die Elektronentransporter weitergegeben werden, und ein GTP. Anabole Funktionen des Citratzyklus Zwischenstufen des Citratzyklus dienen häufig als Biosynthesevorstufen für die folgenden Moleküle: Glukose Aminosäuren Häm Fettsäuren Nach Verbrauch der Zwischenstufen ist es erforderlich, diese wieder nachzuliefern, da der Zyklus sonst unterbrochen und kein Oxalacetat regeneriert würde. Diese auffüllenden Reaktionen werden nach dem griechischen Wort dafür als anaplerotische Reaktionen bezeichnet Reaktionen des Citratzyklus Man kann die Reaktionen des Citratzyklus in zwei große Abschnitte untergliedern: 1. Im ersten Abschnitt erfolgt die Reaktion vom Citrat zum Succinat, was dem Abbau des Acetyl-Restes zu zwei Molekülen CO 2 entspricht. 2. Im zweiten Abschnitt wird das Succinat wieder zu Oxalacetat regeneriert, um eine neue Runde starten zu können. Beide Abschnitte liefern Energie, sowohl als GTP (direkt verwertbar) als auch in Form von NADH/H + und FADH 2,wo die Energie zunächst gespeichert wird. Da Acetyl-CoA keine vier (wie sie für zwei CO 2 benötigt werden...), sondern nur ein Sauerstoffatom enthält, müssen die restlichen drei aus anderen Quellen stammen. Zwei von ihnen entstammen Wasser, das im Rahmen des Zyklus addiert wird, eines der Reaktion von Succinyl-CoAzum Succinat, bei der durch Bildung von GTP aus GDP und anorganischem Phosphat stöchiometrisch ebenfalls Wasser hinzugefügt wird.
3 202 Das Coenzym Ahat seine Aufgabe mit der Abgabe des Acetyl-Restes erfüllt und kann sich neuen Aufgaben zuwenden. Bildung von Isocitrat Zerlegung des Acetyl-CoA in zwei CO 2 und zwei H Bei der Reaktion vom Isocitrat (C 6 ) zum α-ketoglutarat (C 5 ) wird das erste CO 2 abgespalten. Bei der sich anschließenden Reaktion zum Succinyl-CoA(C 4 ) das zweite. Angemerkt sei noch, dass das CO 2 nicht direkt vom Acetyl-CoA stammt. Um genau diese C-Atome abzubauen, sind mehrere Umläufe erforderlich. Ziel des Citratzyklus ist es, Moleküle zu oxidieren, um Energie zu erzeugen. Am Citrat kann man jedoch die OH-Gruppe nicht mehr oxidieren, da es sich um einen tertiären Alkohol handelt ( S. 8). Aber die Zelle weiß sich natürlich zu helfen und lagert die Hydroxyl-Gruppe einfach um. Dadurch entsteht ein sekundärer Alkohol (das Isocitrat), der oxidiert werden kann. Auf molekularer Ebene wird dabei zunächst Wasser vom Citrat abgespalten, um es an anderer Stelle wieder anzulagern. Das dabei entstehende Zwischenprodukt nennt sich cis- Aconitat und das zuständige Enzym daher Aconitase (formaler auch Aconitat-Hydratase). Es katalysiert zunächst eine Dehydratisierung und gleich anschließend eine Hydratisierung. Diese Reaktion ist reversibel, läuft aber gerichtet ab, da das entstehende Isocitrat schnell weiterreagiert. Oxidation von Isocitrat zu α-ketoglutarat Jetzt kommen wir zur ersten Reaktion, die richtig Energie abwirft. Die Isocitrat-Dehydrogenase katalysiert die oxidative Decarboxylierung von Isocitrat zu α-ketoglutarat, wobei das erste Molekül CO 2 und das erste NADH/H + entstehen. Bildung des Einstiegsmoleküls Citrat Bei der ersten Reaktion des Citratzyklus handelt es sich um eine Kondensation, bei der der Acetyl-Rest des Acetyl-CoA an das Trägermolekül Oxalacetat addiert wird. Diese durch die Citrat-Synthase katalysierte Reaktion ist stark exergon ( G 0I = -38 kj/mol), was wichtig ist, da nur wenig Oxalacetat vorhanden ist, und die Reaktion dennoch ablaufen soll. Oxidation von α-ketoglutarat zu Succinyl-CoA Die Reaktion von α-ketoglutarat zu Succinyl-CoAist wieder eine oxidative Decarboxylierung und entspricht im Prinzip der vorangegangenen Reaktion. Bei beiden Reaktionen werden α-ketosäuren unter CO 2 -Abspaltung oxidiert. Die Energie aus der Oxidation wird dieses Mal jedoch zusätzlich noch benutzt, um die Thioesterbindung von Succinyl- CoAzu bilden. Dadurch wird die Energie also kurze Zeit in einer energiereichen Bindung gespeichert. Elektronenak-
4 9.2 Der Citratzyklus 203 zeptor ist erneut NAD +, das zu NADH/H + wird ( G 0 = -37 kj/ mol). Regeneration des Oxalacetat Die folgenden drei Reaktionen dienen dem Wiedereinbau eines Sauerstoffatoms in das Molekül. Die Reaktionsfolge entspricht dabei den ersten drei Schritten der β-oxidation, bei denen ebenfalls ein Sauerstoffatom neu in ein Molekül eingefügt wird ( S. 124). Dieses O-Atom hatte man sich weiter vorne nur geliehen, um ein ganzes Molekül CO 2 abzuspalten. Der α-ketoglutarat-dehydrogenase-komplex gleicht strukturell der Pyruvat-Dehydrogenase (PDH, S. 86), sie katalysieren auch eine ähnliche Art von Reaktion. Auch die α-ketoglutarat-dehydrogenase besteht aus drei Enzymen, wobei das erste Enzym eine andere Aminosäuresequenz als die PDH aufweist, was zur Substratspezifität der beiden Enzyme führt. Die anderen beiden Enzyme sind sich allerdings sehr ähnlich. Beide enthalten kovalent gebundene Lipoyleinheiten, ferner auch enzymgebundenes TPP, gebundenes Lipoat sowie FAD, NAD + und CoA. Reaktion von Succinyl-CoA zu Succinat Wie beim Acetyl-CoA bringt die Hydrolyse der Thioesterbindung von Succinyl-CoAeine Menge Energie ( G 0 = -36 kj/mol), die für die Herstellung einer Phosphorsäureanhydridbindung im GTP genutzt wird. Dies ist rechnerisch mit der Biosynthese eines ATP gleichzusetzen, da beide Nukleotide durch die Nukleosiddiphosphat-Kinase leicht und ohne Energieverlust ineinander umzuwandeln sind. Oxidation von Succinat zu Fumarat Bei dieser ersten Reaktion der Regeneration von Oxalacetat nimmt die Succinat-Dehydrogenase die Dehydrierung von Succinat zu Fumarat vor. Dabei wird nicht genug Energie frei, um ein NAD + zu reduzieren, so dass die Zelle auf FAD ausweicht, das schon mit niedrigeren Oxidationsenergien zu FADH 2 reduziert werden kann ( S. 211). Bei dieser Reaktion handelt es sich um eine Substratkettenphosphorylierung, wie wir sie ja schon bei der Glykolyse kennen gelernt haben ( S. 81). Man nennt das so, um den Unterschied zur oxidativen Phosphorylierung in der Atmungskette ( S. 214) zu verdeutlichen. Das Enzym, das diese reversible Reaktion katalysiert, hat den Namen Succinyl-CoA-Synthetase oder häufig auch Succinat-Thiokinase. Die Succinat-Dehydrogenase ist das einzige Enzym des Citratzyklus, das nicht in der Mitochondrien-Matrix herumschwimmt, sondern fest an die innere Mitochondrienmembran gebunden ist. Da das FAD im Enzym kovalent gebunden vorliegt, handelt es sich bei der Succinat-Dehydrogenase um ein Flavoprotein. Sie enthält zusätzlich noch Eisen-Schwefel-Zentren und wird auch als Komplex II der Atmungskette bezeichnet. Die aufgenommenen Elektronen gehen dabei vom Succinat auf das FAD über, das zum FADH 2 reduziert wird. FADH 2 überträgt sie auf die Fe-S-Zentren, die sie dann an einen Sammelpunkt in der Atmungskette, dem Ubichinon, weitergeben. Die Succinat-Dehydrogenase reagiert dabei direkt mit dem Ubichinon, das Elektronen von verschiedenen Enzymen aufnehmen kann.
5 204 Neben dieser mitochondrialen Malat-Dehydrogenase gibt es noch eine zytosolische, die vor allem für den Malat- Shuttle eine wichtige Rolle spielt ( S. 213) Anabole Funktionen was der Citratzyklus noch alles kann Der Citratzyklus ist sicher nicht der einfachste Weg vom Acetat zum CO 2. Aufgrund seiner zusätzlichen wichtigen Rolle für einige Biosynthesen hat er sich aber wohl in der Evolution als der günstigste für die gesamte Zelle herausgestellt. Wegen der zusätzlich zum katabolen Acetat-Abbau existierenden anabolen Funktion bezeichnet man den Citratzyklus auch als amphibolen Stoffwechselweg. Hydratisierung von Fumarat zu Malat Das Enzym Fumarase (oder formaler Fumarat-Hydratase) lagert an Fumarat reversibel Wasser an, wodurch es zum Malat wird. Biosynthese der Aminosäuren Verschiedene Zwischenprodukte des Citratzyklus dienen der Biosynthese von Aminosäuren. Es handelt sich hier um die entsprechenden α-ketosäuren. A us α-ketoglutarat kann z. B. durch eine Transaminierung Glutamat entstehen eine der häufigsten Transaminierungsreaktionen in unseren Zellen. Aus Oxalacetat entsteht entsprechend Aspartat, vor allem durch den Einsatz der Aspartat-Aminotransferase (AST). Die Biosynthese der Aminosäuren erfolgt dabei sowohl im Zytosol als auch in den Mitochondrien je nach Aminosäure und eingeschlagenem Biosyntheseweg. Oxidation von Malat zu Oxalacetat Durch eine Dehydrierung mit der NAD + -abhängigen Malat- Dehydrogenase wird aus Malat Oxalacetat. Die dabei frei werdenden Elektronen werden zusammen mit einem Proton auf den Elektronentransporter NAD + übertragen, das zum NADH/H + wird. Das Gleichgewicht der Reaktion liegt weit auf der Seite des Malat. Da Oxalacetat jedoch weiter reagiert, läuft die Reaktion trotz eines G 0 von + 28 kj/mol ab. Glukose-Biosynthese Für die Herstellung von Glukose (Glukoneogenese) eignet sich Oxalacetat sehr gut. Die Zelle zieht es im Bedarfsfall aus dem Citratzyklus ab. Das Enzym, das den ersten Schritt katalysiert, ist die Phosphoenolpyruvat-Carboxykinase (PEP-CK), die in erster Linie zytosolisch vorkommt (ist logisch, denn da brauchen wir ja auch die Glukose, die an-
6 9.2 Der Citratzyklus 205 schließend ans Blut abgegeben werden soll). Oxalacetat wird dazu mithilfe des Malat-Shuttles aus den Mitochondrien geschafft ( S. 224). Im Zytosol wird es dann von der PEP-CK decarboxyliert und gleichzeitig phosphoryliert, wodurch Phosphoenolphosphat entsteht. Daneben benötigt man Succinyl-CoAnoch, um Ketonkörper abzubauen. Diese müssen nämlich zunächst mit Succinyl- CoAaktiviert werden, bevor man sie oxidieren kann ( S. 143). Die Decarboxylierung von Oxalacetat liefert zusammen mit der Hydrolyse eines GTP genug Energie, um eine energiereiche Enolphosphat-Bindung in das Molekül einzubauen. Diese Reaktion läuft natürlich vor allem in der Leber und den Nieren ab, da das die einzigen Organe sind, die ordentlich Glukoneogenese betreiben können (daneben noch ein kleines bisschen der Darm). Häm-Biosynthese und Ketonkörperabbau Succinyl-CoAist Ausgangsstoff für die Häm-Biosynthese ( S. 496). Häm benötigt der Körper, um es in Hämoglobin (Hb) oder Cytochrome einzubauen, die aufgrund ihres Zentralatoms Eisen in der Lage sind, Sauerstoff (im Hb) oder Elektronen (in den Cytochromen) zu transportieren. In der ersten und geschwindigkeitsbestimmenden Reaktion reagiert Succinyl-CoAin den Mitochondrien mit der einfachsten Aminosäure Glycin zu δ-aminolävulinsäure (δ-als). Fettsäure- und Cholesterin-Biosynthese Während der Abbau von Fettsäuren, die β-oxidation, in den Mitochondrien der Zellen stattfindet, läuft die Biosynthese neuer Fettsäuren, wie die meisten Biosynthesen, im Zytosol ab. Diese Trennung des Ab- und Aufbaus gleichartiger Stoffe ist ja eines der Grundprinzipien des Stoffwechsels. Für die Zwischenprodukte des Citratzyklus sind daher Transportsysteme notwendig, die sie aus den Mitochondrien ins Zytosol bringen. Für die Fettsäure-Biosynthese benötigt die Zelle Acetyl- CoA, das allerdings nur im Mitochondrium entsteht und dieses auch nicht so ohne weiteres verlassen kann. Der Trick des Acetyl-CoA, doch ins Zytosol zu gelangen, liegt darin, sich mit Oxalacetat zu Citrat zu verbinden, das die Mitochondrienmembran (über einen Tricarbonsäuren-Transporter, S. 225) durchdringen kann. Im Zytosol erfolgt dann durch die ATP-abhängige Citrat-Lyase die Aufspaltung zurück in Acetyl-CoA und Oxalacetat. (Oxalacetat kann zu Malat reduziert werden und so über den Malat-Aspartat- Shuttle wieder ins Mitochondrium gelangen, S. 224.) Auch für die im Zytosol beginnende Cholesterin-Biosynthese ( S. 146) wird Acetyl-CoA benötigt. Das Enzym Aminolävulinsäure-Synthase benötigt dazu das Coenzym Pyridoxalphosphat (PALP, S. 177), das aus Vitamin B 6 entsteht. Genau an dieser Stelle wirkt sich dann auch ein Vitamin-B 6 -Mangel aus, da die entscheidende Reaktion für die Häm-Biosynthese nicht stattfindet. Langfristig führt das zu einer Anämie ( S. 510).
7 Anaplerotische Reaktionen wie der Citratzyklus wieder aufgefüllt wird Da aus dem Citratzyklus auch Stoffe abgezogen werden, um sie für Biosynthesen zu verwenden, muss man diese hin und wieder nachfüllen, damit der Zyklus nicht stehen bleibt. Diese Auffüll-Aktionen nennt man anaplerotische Reaktionen. Sie sind unbedingt erforderlich, da die Konzentrationen der Zwischenprodukte des Citratzyklus recht gering sind. Entnahme und Nachschub unterliegen dabei einem dynamischen Gleichgewicht, was dazu führt, dass die Konzentrationen der Zwischenprodukte immer annähernd gleich bleiben. Drei anaplerotische Reaktionen spielen eine besonders große Rolle für unsere Zellen und werden daher hier erläutert. Pyruvat-Carboxylase Dieses Enzym katalysiert die wichtigste anaplerotische Reaktion, bei der Pyruvat biotinabhängig zu Oxalacetat carboxyliert wird. Das Vitamin Biotin ( S.130) fungiert dabei als Coenzym der Pyruvat-Carboxylase. Malat-Enzym Das zytosolische Malat-Enzym katalysiert die Reaktion von Malat zum Pyruvat. Es stellt damit eine weitere Möglichkeit dar, zytosolisches Malat wieder in das Mitochondrium zu schaffen. Wie schon erwähnt, kann Citrat vom Mitochondrium in das Zytosol transportiert werden, um dort in Acetyl-CoA und Oxalacetat zerlegt zu werden. Acetyl-CoA kann dann als Ausgangsstoff für die Fettsäure-Biosynthese ( S. 128) dienen, das Oxalacetat muss wieder in das Mitochondrium gebracht werden. Dazu wird es zunächst durch die Malat-Dehydrogenase zu Malat reduziert (ein Vorgang, der reversibel ist). Malat kann dann entweder selbst durch den Malat-Shuttle ( S. 224) in das Mitochondrium gelangen, oder aber es wird durch das Malat-Enzym zu Pyruvat umgewandelt. Die Funktion dieser Reaktion ist es, bei Bedarf Oxalacetat in größeren Mengen zur Verfügung zu stellen, damit der Citratzyklus schneller läuft. Staut sich Pyruvat vor dem Citratzyklus an, da dieser nicht mehr hinterher kommt, wird einiges von diesem Pyruvat intramitochondrial zu Oxalacetat carboxyliert. Damit kann wieder mehr Acetyl-CoA zu Citrat reagieren und der Stau ist beseitigt. Glukoneogenese. Die Pyruvat-Carboxylase-Reaktion läuft besonders in Leber und Niere ab, den beiden Organen, die Glukoneogenese für den restlichen Organismus betreiben. Die Glukoneogenese verbraucht nämlich Oxalacetat, was über die Pyruvat-Carboxylase wieder nachgeliefert wird. Glutamat-Dehydrogenase Die Glutamat-Dehydrogenase (in der Klinik kurz GLDH) katalysiert die Desaminierung von Glutamat zu α-ketoglutarat, das in den Citratzyklus eingeschleust werden kann. Die GLDH kommt in allen Organen vor, vor allem aber in den Mitochondrien der Leber. Kann man sie im Blut nachweisen, spricht das für eine starke Schädigung der Leber, da die mitochondrialen Enzyme erst freigesetzt werden, wenn selbst die Mitochondrien der Zelle kaputt sind. Die Normalwerte der GLDH liegen bei unter 3 U/l im Blut ( S. 558). Wie zu erkennen ist, wird bei dieser Reaktion auch noch NADPH/H + gebildet, das die Zelle für die Fettsäure-Biosynthese gut gebrauchen kann. Pyruvat kann dann über den Pyruvat/H + -Symporter wieder in das Mitochondrium gelangen und verschiedene Reaktionen eingehen beispielsweise die Decarboxylierung zum Acetyl-CoA, womit der Kreis dann geschlossen wäre.
8 9.2 Der Citratzyklus 207 Der Zusammenhang mit dem Harnstoffzyklus Fumarat wird nicht nur im Rahmen des Citratzyklus aus Succinat gebildet, sondern entsteht auch im Harnstoffzyklus als Abfallprodukt aus Argininosuccinat und fließt von dort in den Citratzyklus ein. Nach dem Umbau zu Oxalacetat kann es wieder zu Aspartat (mittels AST) transaminiert werden, das mit Citrullin erneut zu Argininosuccinat reagiert. Pyruvat-Carboxylase. Ein erhöhtes Angebot an Acetyl-CoA stimuliert die Pyruvat-Carboxylase. Dadurch wird vermehrt Pyruvat zu Oxalacetat umgebaut (anaplerotische Reaktion) und der Citratzyklus beschleunigt. Allerdings ist zu beachten, dass die Reaktionen von Fumarat zu Oxalacetat im Zytosol stattfinden und so allenfalls indirekt dem Citratzyklus zugerechnet werden können Zwischenbilanz Bevor wir weiter zur Atmungskette gehen, ziehen wir eine Zwischenbilanz und schauen, was bisher an Energie in die Regulation des Citratzyklus Die Durchsatzgeschwindigkeit des Citratzyklus hängt vom energetischen Zustand der Zelle ab. ATP, Citrat und reduzierte Coenzyme (NADH/H + u. a.) weisen darauf hin, dass es der Zelle energetisch gut geht, worauf der Citratzyklus gehemmt wird. Drei Enzyme des Citratzyklus katalysieren besonders exergone Reaktionen. Hier besteht daher die Möglichkeit einer wirkungsvollen Regulation. Es handelt sich dabei um die Citrat-Synthase, die den ersten Schritt im Citratzyklus katalysiert, und um die beiden oxidativen Phosphorylierungen, die durch die Isocitrat-Dehydrogenase und die Succinat- Dehydrogenase katalysiert werden. Die Regulation des Citratzyklus betrifft vor allem den Stoffwechsel einer Zelle und nur indirekt den Gesamtorganismus. Daher erfolgt die Regulation nur allosterisch. Hormone greifen an dieser Stelle nicht in den Zellstoffwechsel ein. Steuerung über die Pyruvat-Dehydrogenase. In erster Linie entscheidend für die Aktivität des Citratzyklus ist jedoch der Nachschub an Acetyl-CoA durch die Pyruvat-Dehydrogenase (PDH), deren Aktivitätszustand durch gezielte Phosphorylierung und Dephosphorylierung verändert werden kann. Die PDH ist im dephosphorylierten Zustand aktiv, phosphoryliert hingegen inaktiv ( S. 87).
9 208 Speicherformen ATP, NADH/H + oder FADH 2 umgewandelt wurde. Als Beispiel dient die Glukose, mit der sich die Energieausbeute sehr anschaulich zeigen lässt. Wir haben jetzt am Ende des Citratzyklus die Glukose immerhin schon in sechs Moleküle CO 2 und jede Menge Elektronen zerlegt. Um diese Elektronen nicht völlig ihrem Schicksal zu überlassen, haben sich spezialisierte Elektronen-Transporter gefunden, die ihnen den Weg zur Atmungskette weisen. Wie viel Energie kann man damit nun erzeugen? ATP. Pro Molekül Glukose haben wir aus der Glykolyse direkt zwei ATP gewonnen und aus dem Citratzyklus (zwei Durchläufe...) noch einmal direkt zwei ATP (als energetisch gleichwertiges GTP). Das ist natürlich nicht so üppig. Wichtiger sind die nicht nur zahl-, sondern auch energiereichen Elektronen, die zusammen mit Protonen an NADH/H + und FADH 2 gebunden sind. Elektronen. In der Glykolyse haben wir pro Molekül Glukose zwei Moleküle NADH/H + gewonnen. Durch die anschließende Pyruvat-Dehydrogenase-Reaktion entstehen noch einmal zwei. Zwei Durchläufe des Citratzyklus produzieren sechs Moleküle NADH/H + und zwei Moleküle FADH 2, die alle jeweils zwei Elektronen an die Atmungskette abgeben können. Macht also insgesamt 24 Elektronen. Ausbeute in der Atmungskette. Wenn wir jetzt schon einmal vorausschicken, dass in der Atmungskette im Mittel pro NADH/H + etwa 2,5 und pro FADH 2 etwa 1,5 Moleküle ATP entstehen, ergibt das zusammen 32 ATP. Während anaerob in der Glykolyse also nur zwei ATP entstehen, werden es im aeroben Zustand immerhin 32 ATP. Es war also durchaus eine schlaue Idee der ersten Eukaryonten, sich Mitochondrien als Haustiere zu halten. 9.3 Die Reduktionsäquivalente NADH und seine Kollegen Die verschiedenen Elektronen-Transporter (NADH, FADH und NADPH) sind uns nun schon einige Male im Stoffwechsel begegnet. Hier beschäftigen wir uns mit allen Dreien zusammen und zeigen deren Gemeinsamkeiten und Unterschiede auf. Allen Reduktionsäquivalenten gemeinsam ist, dass sie Redox-Coenzyme sind. Sie beteiligen sich an den Elektronen- Verschiebungen bei Redoxreaktionen und besitzen ein Vitamin als Grundgerüst. Wir verwenden NADH und FADH als Abkürzungen für die Form, bei der nicht zwischen oxidierter (NAD + bzw. FAD) und reduzierter (NADH/H + und FADH 2 ) Form unterschieden wird. Bei Redoxreaktionen werden die Elektronen meist zusammen mit Protonen übertragen. Allgemein spricht man daher von Reduktionsäquivalenten. Sauerstoff ist nur selten beteiligt. Oxidoreduktasen katalysieren sowohl Oxidationen als auch Reduktionen ( S. 63) und benötigen für ihre Arbeit Coenzyme. Entweder fallen bei der Oxidation eines Stoffes (z. B. Alkohol zu Aldehyd) Elektronen an, die von jemandem aufgenommen werden müssen. Oder es werden für reduktive Reaktionen (z. B. Aldehyd zu Alkohol) Elektronen benötigt, die jemand spenden muss. Diese Jemande sind spezialisierte Elektronen-Transporter, die reversibel Elektronen aufnehmen und (meist an anderer Stelle) wieder abgeben können. Die Coenzyme der Oxidoreduktasen sind also Elektronen- Transporter. Sie lassen sich noch einmal in lösliche Coenzyme und kovalent an die Enzyme gebundene prosthetische Gruppen unterteilen. NADH und NADPH sind lösliche Coenzyme, die sich reversibel an Oxidoreduktasen (meist Dehydrogenasen) anlagern. FADH ist meist kovalent an Oxidoreduktasen gebunden und wird dann als prosthetische Gruppe bezeichnet. Katabolismus und Anabolismus. Man kann die Coenzyme auch nach ihrer Rolle im Stoffwechsel einteilen: NADH und FADH sind meist an katabolen Oxidationen beteiligt, bei denen sie die frei werdenden Elektronen aufnehmen. Beide liegen daher im Zytosol eher in ihren oxidierten Formen vor (NAD + und FAD) bereit, reduziert zu werden. NADPH befindet sich im Zytosol, wo es in seiner reduzierten Form (NADPH/H + ) vor allem Biosynthesen als Spender energiereicher Elektronen dient. Vorteil dieser funktionellen Spezialisierung der Coenzyme ist, dass im Zytosol einer Zelle zwei verschiedene Elektronen-Transporter mit ganz unterschiedlichen Aufgaben gleichzeitig nebeneinander vorliegen können. Zurzeit sind übrigens mehr als 200 Enzyme bekannt, die entweder NADH oder NADPH als Coenzym verwenden. Nur sehr wenige Enzyme können mit beiden Coenzymen arbeiten. Zu diesen bemerkenswerten Ausnahmen gehört die mitochondriale Glutamat-Dehydrogenase ( S. 558).
10.2 Der Citratzyklus 203
 10.2 Der Citratzyklus 203 Ketonkörper-Biosynthese. Bei den Ketonkörpern handelt es sich um die verschiffbare Form von Acetyl-CoA. Staut sich viel Acetyl-CoA in der Leber an im Hungerzustand, dann werden
10.2 Der Citratzyklus 203 Ketonkörper-Biosynthese. Bei den Ketonkörpern handelt es sich um die verschiffbare Form von Acetyl-CoA. Staut sich viel Acetyl-CoA in der Leber an im Hungerzustand, dann werden
- der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen
 Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Der Energiestoffwechsel eukaryotischer Zellen
 Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus)
 Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
schnell und portofrei erhältlich bei
 Kurzlehrbuch Biochemie Kurzlehrbuch Biochemie Bearbeitet von Melanie Königshoff, Timo Brandenburger 2. überarb. Aufl. 2007. Taschenbuch. 46 S. Paperback ISBN 978 3 13 136412 8 Format (B x L): 24 x 17 cm
Kurzlehrbuch Biochemie Kurzlehrbuch Biochemie Bearbeitet von Melanie Königshoff, Timo Brandenburger 2. überarb. Aufl. 2007. Taschenbuch. 46 S. Paperback ISBN 978 3 13 136412 8 Format (B x L): 24 x 17 cm
Regulation der Glykolyse: Phosphofructokinase
 Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus. Citratzyklus
 Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Kataboler und Anaboler Stoffwechsel
 Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Grundzüge des Energiestoffwechsels I
 Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Grundlagen der Physiologie
 Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
Was bisher geschah 1
 Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Stoffwechsel. Metabolismus (3)
 Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
KOHLENHYDRATE PYRUVAT-DEHYDROGENASE
 PYRUVAT-DEHYDROGENASE PYRUVAT-DEHYDROGENASE: Um ein Optimum Beute garantieren zu können, Wird das entstandene Pyruvat (bei der aeroben) Glykolyse, durch die PDH in Acetyl-CoA umgewandelt, um dann, Teil
PYRUVAT-DEHYDROGENASE PYRUVAT-DEHYDROGENASE: Um ein Optimum Beute garantieren zu können, Wird das entstandene Pyruvat (bei der aeroben) Glykolyse, durch die PDH in Acetyl-CoA umgewandelt, um dann, Teil
Einige Vorwörter. Liebe Leser! Liebe Leser!
 Liebe Leser! V Einige Vorwörter Liebe Leser! Die Biochemie ist eines der wichtigsten Fächer der Vorklinik, obwohl es gemeinhin leider als lästiges und kompliziertes Fach gilt. Dabei kann Biochemie sogar
Liebe Leser! V Einige Vorwörter Liebe Leser! Die Biochemie ist eines der wichtigsten Fächer der Vorklinik, obwohl es gemeinhin leider als lästiges und kompliziertes Fach gilt. Dabei kann Biochemie sogar
Mechanismen der ATP Synthese in Mitochondrien
 Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Kraftwerk Körper Energiegewinnung in unseren Zellen
 Was passiert eigentlich, wenn wir etwas essen und dann loslaufen müssen? Wie können unsere Zellen die Stoffen aus der Nahrung zur Energiegewinnung nutzen? Die Antwort auf diese Fragen gibt s in diesem
Was passiert eigentlich, wenn wir etwas essen und dann loslaufen müssen? Wie können unsere Zellen die Stoffen aus der Nahrung zur Energiegewinnung nutzen? Die Antwort auf diese Fragen gibt s in diesem
Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O O 2 6 CO H 2 O G kj
 Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O G 0-2872 kj Hydrolyse der Stärke Ausgangssubstrate: Glucose, Fructose Stärkehydrolyse: Amylasen Endo- ( -Amylase) und
Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O G 0-2872 kj Hydrolyse der Stärke Ausgangssubstrate: Glucose, Fructose Stärkehydrolyse: Amylasen Endo- ( -Amylase) und
Atmung Übersicht. Atmung der Mitochondrien
 Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
Reaktionen der Zellatmung (1)
 ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
Ueberblick des Zuckerabbaus: Pyruvat!
 Ueberblick des Zuckerabbaus: Pyruvat + 2 ATP Oxidativer Abbau Fermentation (Muskel) Alkohol-Gärung (Hefe) Alkoholische Gärung: In Hefe wird unter aneroben Bedingungen NAD + durch Umwandlung von Pyruvat
Ueberblick des Zuckerabbaus: Pyruvat + 2 ATP Oxidativer Abbau Fermentation (Muskel) Alkohol-Gärung (Hefe) Alkoholische Gärung: In Hefe wird unter aneroben Bedingungen NAD + durch Umwandlung von Pyruvat
Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat
 Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
Der Stoffwechsel. Wir zeigen dir wie er funktioniert.
 Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Guter Stoffwechsel, schlechter Stoffwechsel, der Stoffwechsel schläft, den Stoffwechsel ankurbeln,
Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Guter Stoffwechsel, schlechter Stoffwechsel, der Stoffwechsel schläft, den Stoffwechsel ankurbeln,
Biochemie II - Tutorium
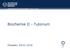 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
1. Biochemie-Klausur Zahnmediziner, WS 03/04
 1. Biochemie-Klausur Zahnmediziner, WS 03/04 1. Welche Aussage zur ß-Oxidation von Fettsäuren in Peroxisomen ist falsch? A) Die Aufnahme langkettiger Fettsäuren in die Peroxisomen erfolgt Carnitin-unabhängig!
1. Biochemie-Klausur Zahnmediziner, WS 03/04 1. Welche Aussage zur ß-Oxidation von Fettsäuren in Peroxisomen ist falsch? A) Die Aufnahme langkettiger Fettsäuren in die Peroxisomen erfolgt Carnitin-unabhängig!
Das Sinnloseste: der Zitronensäurezyklus
 Vortrag zum Thema Das Sinnloseste: der Zitronensäurezyklus von Daniel Metzsch 1 Inhalte 1. Zuerst ein paar Strukturformeln 2. Einordnung in den Metabolismus 3. Überblick über den Zitronensäurezyklus 4.
Vortrag zum Thema Das Sinnloseste: der Zitronensäurezyklus von Daniel Metzsch 1 Inhalte 1. Zuerst ein paar Strukturformeln 2. Einordnung in den Metabolismus 3. Überblick über den Zitronensäurezyklus 4.
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
3.4 Citratcyclus Fehlertext
 3.4 Citratcyclus Fehlertext. Lesen Sie den nebenstehenden Text 23 Fehler, indem Sie die Fehler unterstreichen, Der Citratcyclus wird als die Drehscheibe des gesamten Stoff - wechsels im Organismus bezeichnet.
3.4 Citratcyclus Fehlertext. Lesen Sie den nebenstehenden Text 23 Fehler, indem Sie die Fehler unterstreichen, Der Citratcyclus wird als die Drehscheibe des gesamten Stoff - wechsels im Organismus bezeichnet.
Atmungskette inklusive Komplex II
 Atmungskette inklusive Komplex II Energiegewinnung durch oxidative Phosphorylierung GW2014 Das Prinzip der Oxidativen Phosphorylierung 14_01_01_harness_energy.jpg Chemiosmotische Kopplung 2016 1 1) 2)
Atmungskette inklusive Komplex II Energiegewinnung durch oxidative Phosphorylierung GW2014 Das Prinzip der Oxidativen Phosphorylierung 14_01_01_harness_energy.jpg Chemiosmotische Kopplung 2016 1 1) 2)
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Präsentation STOFFWECHSEL STOFFWECHSEL. Fettstoffwechsel im Sport. Biologische Oxidation Zitratzyklus und Atmungskette
 STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
LIPIDE. Periphere Gruppe mit Cysteinylrest. FS-Synthase. Zentrale Gruppe Phosphopanthetinarm kovalente Bindung
 Periphere Gruppe mit Cysteinylrest FS-Synthase Zentrale Gruppe Phosphopanthetinarm kovalente Bindung Die FS-Biosynthse aus Acetyl-CoA und Malonyl-CoA, wird komplett an dem dimeren Multienzymkomplex FETTSÄURESYNTHETASE
Periphere Gruppe mit Cysteinylrest FS-Synthase Zentrale Gruppe Phosphopanthetinarm kovalente Bindung Die FS-Biosynthse aus Acetyl-CoA und Malonyl-CoA, wird komplett an dem dimeren Multienzymkomplex FETTSÄURESYNTHETASE
BIOCHEMIE. Prof. Manfred SUSSITZ. über(be)arbeitet und zusammengestellt nach Internetvorlagen:
 BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 23.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 23.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Anaerobe NADH-Regeneration: Gärung
 Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Alkoholische Gärung H 3
Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Alkoholische Gärung H 3
Versuch 6. Leitenzyme
 Versuch 6 Leitenzyme Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X Dr. Kojro Einleitung Ziel dieses Versuches ist der Nachweis von bestimmten
Versuch 6 Leitenzyme Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X Dr. Kojro Einleitung Ziel dieses Versuches ist der Nachweis von bestimmten
Stoffwechsel. Die Chemie des Lebens ist in Stoffwechselwegen organisiert
 Die Chemie des Lebens ist in Stoffwechselwegen organisiert Der Stoffwechsel ist die Summe aller chemischen Reaktionen, die in den Zellen eines Organismus auftreten. Unter Mithilfe von Enzymen verläuft
Die Chemie des Lebens ist in Stoffwechselwegen organisiert Der Stoffwechsel ist die Summe aller chemischen Reaktionen, die in den Zellen eines Organismus auftreten. Unter Mithilfe von Enzymen verläuft
Kapitel 5: 1. Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D.
 Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
Gluconeognese Neusynthese von Glucose aus Pyruvat
 Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Schritt für Schritt Simulation Die Atmungskette
 KENNZEICHEN: KURS - SCHULE - - Schritt für Schritt Simulation Die Atmungskette Inhalt Übersicht über das Mitochondrium und die Mitochondrienmembran S.2 Zeichenerklärung S.3 Stichwortverzeichnis S.4 Leitfaden
KENNZEICHEN: KURS - SCHULE - - Schritt für Schritt Simulation Die Atmungskette Inhalt Übersicht über das Mitochondrium und die Mitochondrienmembran S.2 Zeichenerklärung S.3 Stichwortverzeichnis S.4 Leitfaden
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase
 Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Oxidative Phosphorylierung
 BICEMIE DER ERÄRUG II Grundzüge des Metabolismus xidative Phosphorylierung 24.04.2012 xidative Phosphorylierung xidative Phosphorylierung -Die Elektronen in AD und in FAD 2 (hohes Übertragungspotential)
BICEMIE DER ERÄRUG II Grundzüge des Metabolismus xidative Phosphorylierung 24.04.2012 xidative Phosphorylierung xidative Phosphorylierung -Die Elektronen in AD und in FAD 2 (hohes Übertragungspotential)
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Z11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
Grundzüge des Energiestoffwechsels I
 Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Reduction / Oxidation
 Reduction / Oxidation Pyruvat C6H12O 6 Glucose Glycogen Glucose-6-P Glycolyse 2 e - 2 Pyruvat 2 e - 2 Acetyl-CoA 2 CO 2 ATP ADP ATP ADP Citrat-Zyklus oder Tricarbonsäure 4 CO 2 8 e - Zyklus 6 O2 6 H 2
Reduction / Oxidation Pyruvat C6H12O 6 Glucose Glycogen Glucose-6-P Glycolyse 2 e - 2 Pyruvat 2 e - 2 Acetyl-CoA 2 CO 2 ATP ADP ATP ADP Citrat-Zyklus oder Tricarbonsäure 4 CO 2 8 e - Zyklus 6 O2 6 H 2
Z 11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
Klausur zur Vorlesung Biochemie I im WS 2001/02
 (insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
(insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
Bioenergetik. Technische Universität Ilmenau, FG Nanotechnologie. Zentrum für Mikro- und Nanotechnologien
 Bioenergetik Quellen: 1. Physiologie des Menschen (mit Pathophysiologie) R.F. Schmidt, F. Lang, G. Thews, 29. Auflage Springer Medizin Verlag Heidelberg (2005), ISBN 3-540-21882-3. 2. www.cg.bnv bamberg.de/t3/fileadmin/images/fachbereiche/biologie/dateien/kh-abbau.ppt
Bioenergetik Quellen: 1. Physiologie des Menschen (mit Pathophysiologie) R.F. Schmidt, F. Lang, G. Thews, 29. Auflage Springer Medizin Verlag Heidelberg (2005), ISBN 3-540-21882-3. 2. www.cg.bnv bamberg.de/t3/fileadmin/images/fachbereiche/biologie/dateien/kh-abbau.ppt
➃ ➄ ➅ ➄ ➃ ➆ ➇ ➈ ➉ ➃ ➄. 2.2 Dünndarm. 2.1 Verdauungstrakt
 2. Verdauungstrakt. Malen Sie die verschiedenen Verdauungsorgane mit unterschiedlichen Farben an. 2. Schreiben Sie die Bezeichnungen der Verdauungsorgane und der Verdauungssäfte mit Mengenangabe in den
2. Verdauungstrakt. Malen Sie die verschiedenen Verdauungsorgane mit unterschiedlichen Farben an. 2. Schreiben Sie die Bezeichnungen der Verdauungsorgane und der Verdauungssäfte mit Mengenangabe in den
Seiten im Campbell und Tierphsbuch. Citratsäurezyklus: T. S. 53 / Cam. S. 180 f, , , 190
 Versuch: Atmung Seiten im Campbell und Tierphsbuch Zusammenfassung Campbell S. 915 bis 925 RQ Tierphys S. 259 Was sind Tracheen? T. S. 255 / Cam S. 746 f., 917 ff., 1349 Lunge : T. S. 243 ff. / Cam S.
Versuch: Atmung Seiten im Campbell und Tierphsbuch Zusammenfassung Campbell S. 915 bis 925 RQ Tierphys S. 259 Was sind Tracheen? T. S. 255 / Cam S. 746 f., 917 ff., 1349 Lunge : T. S. 243 ff. / Cam S.
Um diesen Prozess zu verstehen, müssen wir die Wege der Glukose genauer betrachten.
 Glukose hilft uns, auch bei intensiven Belastungen zu überleben. Wieso? Um diesen Prozess zu verstehen, müssen wir die Wege der Glukose genauer betrachten. In diesem Artikel geht es nicht nur um den Abbau
Glukose hilft uns, auch bei intensiven Belastungen zu überleben. Wieso? Um diesen Prozess zu verstehen, müssen wir die Wege der Glukose genauer betrachten. In diesem Artikel geht es nicht nur um den Abbau
12. Oxidative Phosphorylierung
 12. Oxidative Phosphorylierung 303 Zweck: Gewinnung von ATP Regeneration von NAD + und FAD Gesamtreaktionen: 3 ADP + 3 P i 3 ATP NADH + 0,5 O 2 + H + NAD + + H-O-H 2 ADP + 2 P i 2 ATP FADH 2 + 0,5 O 2
12. Oxidative Phosphorylierung 303 Zweck: Gewinnung von ATP Regeneration von NAD + und FAD Gesamtreaktionen: 3 ADP + 3 P i 3 ATP NADH + 0,5 O 2 + H + NAD + + H-O-H 2 ADP + 2 P i 2 ATP FADH 2 + 0,5 O 2
Asmaa Mebrad Caroline Mühlmann Gluconeogenese
 Gluconeogenese Asmaa Mebrad Caroline Mühlmann 06.12.2004 Definition: wichtiger Stoffwechselweg, bei dem Glucose aus Nicht-Kohlenhydrat-Vorstufen synthetisiert wird Ablauf bei längeren Hungerperioden dient
Gluconeogenese Asmaa Mebrad Caroline Mühlmann 06.12.2004 Definition: wichtiger Stoffwechselweg, bei dem Glucose aus Nicht-Kohlenhydrat-Vorstufen synthetisiert wird Ablauf bei längeren Hungerperioden dient
Energie aus Aminosäuren - Wundermittel Protein?
 Jeder von uns kennt die Versprechen der Eiweißshakes: Mehr Proteine machen dich schlank, jung und wunderschön. Aber was haben Proteine an sich, das diese Versprechen rechtfertigt? Dies ist der vierte Teil
Jeder von uns kennt die Versprechen der Eiweißshakes: Mehr Proteine machen dich schlank, jung und wunderschön. Aber was haben Proteine an sich, das diese Versprechen rechtfertigt? Dies ist der vierte Teil
Der Stoffwechsel: Konzepte und Grundmuster
 Der Stoffwechsel: Konzepte und Grundmuster 1 Lebende Organismen Was unterscheidet lebende Organismen von toter Materie? Lebende Organismen haben einen hohen Gehalt an chemischer Komplexität und Organisation
Der Stoffwechsel: Konzepte und Grundmuster 1 Lebende Organismen Was unterscheidet lebende Organismen von toter Materie? Lebende Organismen haben einen hohen Gehalt an chemischer Komplexität und Organisation
KOHLENHYDRATE. Die Glykolyse
 Die Glykolyse Hexokinase Glucose Kostet 1ATP Mg 2+ Glucose-6-P Die Glucokinase kann durch Insulin induziert werden in : 1) Den Fettzellen 2) Den ß-Zellen des Pankreas 3) Der Nierenrinde 4) Der Leber Die
Die Glykolyse Hexokinase Glucose Kostet 1ATP Mg 2+ Glucose-6-P Die Glucokinase kann durch Insulin induziert werden in : 1) Den Fettzellen 2) Den ß-Zellen des Pankreas 3) Der Nierenrinde 4) Der Leber Die
Musterlösung. Frage Summe Note Punkte 1, ,5 1,0
 Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Pentosephosphat-Weg: alternativer Abbau von Glucose. Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet.
 Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
9. Abbau der Glukose zum Pyruvat
 9. Abbau der Glukose zum Pyruvat 236 9.1. Übersicht: Abbau von Glucose Pentosephosphate Pathway (PPP) NADP + NADPH Glucose Glycolysis Oxidative Phosphorylation PDH Complex Citric Acid Citric Acid Cycle
9. Abbau der Glukose zum Pyruvat 236 9.1. Übersicht: Abbau von Glucose Pentosephosphate Pathway (PPP) NADP + NADPH Glucose Glycolysis Oxidative Phosphorylation PDH Complex Citric Acid Citric Acid Cycle
Einführung in die Biochemie Glykolyse
 Glykolyse Der Abbau der Glukose beginnt beim aeroben und beim anaeroben Abbau nach dem gleichen rinzip, der Glykolyse. Dabei wird Brenztraubensäure (2-Ketopropansäure) gebildet. Die Glykolyse ist die erste
Glykolyse Der Abbau der Glukose beginnt beim aeroben und beim anaeroben Abbau nach dem gleichen rinzip, der Glykolyse. Dabei wird Brenztraubensäure (2-Ketopropansäure) gebildet. Die Glykolyse ist die erste
❶ ❷ ❸ ❹ 1) ATP: 2) Energiegewinnungswege:
 1) ATP: ist der Energielieferant des Körpers. Die Spaltung von ATP (Adenosintriphosphat) zu ADP (Adenosindiphosphat) + P gibt Energie frei, welche der Körper nutzen kann (z.b. Muskel für Kontraktion, vgl.
1) ATP: ist der Energielieferant des Körpers. Die Spaltung von ATP (Adenosintriphosphat) zu ADP (Adenosindiphosphat) + P gibt Energie frei, welche der Körper nutzen kann (z.b. Muskel für Kontraktion, vgl.
Redoxprozesse. Warum ist Sauerstoff für uns lebensnotwendig?
 Redoxprozesse Diese Lerneinheit befasst sich mit der Knallgasexplosion und Atmungskette - eine biologische Betrachtung von Redoxreaktionen mit den folgenden Lehrzielen: Warum ist Sauerstoff für uns lebensnotwendig?
Redoxprozesse Diese Lerneinheit befasst sich mit der Knallgasexplosion und Atmungskette - eine biologische Betrachtung von Redoxreaktionen mit den folgenden Lehrzielen: Warum ist Sauerstoff für uns lebensnotwendig?
Abschlussklausur zur Vorlesung Biomoleküle II WS 2004/05
 16.02.2005 Abschlussklausur zur Vorlesung Biomoleküle II WS 2004/05 Name: Studienfach: Matrikelnummer: Fachsemester: Hinweise: 1. Bitte tragen Sie Ihren Namen, Matrikelnummer, Studienfach und Semesterzahl
16.02.2005 Abschlussklausur zur Vorlesung Biomoleküle II WS 2004/05 Name: Studienfach: Matrikelnummer: Fachsemester: Hinweise: 1. Bitte tragen Sie Ihren Namen, Matrikelnummer, Studienfach und Semesterzahl
Versuchsprotokoll: Leitenzyme
 Versuchsprotokoll: Leitenzyme Aufschluss von Lebergewebe / Fraktionierte Zentrifugation / Aufschluss von Mitochondrien / Nachweis von Leitenzymen im Cytosol und 1.1. Einleitung Für die Trennung der Organellen
Versuchsprotokoll: Leitenzyme Aufschluss von Lebergewebe / Fraktionierte Zentrifugation / Aufschluss von Mitochondrien / Nachweis von Leitenzymen im Cytosol und 1.1. Einleitung Für die Trennung der Organellen
Der Fettsäurestoffwechsel. Basierend auf Stryer Kapitel 22
 Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
BIOCHEMIE des Stoffwechsels ( )
 BIOCHEMIE des Stoffwechsels (772.113) 7. Einheit Citrat- und Glyoxylat-Cyclus Citrat-Cyclus Allgemeines Reaktionsfolge Thermodynamik und Regulation Amphibole Natur des Citrat-Cyclus Anaplerotische Reaktionen
BIOCHEMIE des Stoffwechsels (772.113) 7. Einheit Citrat- und Glyoxylat-Cyclus Citrat-Cyclus Allgemeines Reaktionsfolge Thermodynamik und Regulation Amphibole Natur des Citrat-Cyclus Anaplerotische Reaktionen
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8,
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8,
Was ist denn NAD / NADP??
 Exkurs Oxidative Desaminierung: Was ist denn NAD / NADP?? Exkurs Oxidative Desaminierung: NAD / NADP gehört zum Vitamin B2- Komplex Nikotinsäureamid = Nikotinamid= Vit B3 Exkurs Oxidative Desaminierung:
Exkurs Oxidative Desaminierung: Was ist denn NAD / NADP?? Exkurs Oxidative Desaminierung: NAD / NADP gehört zum Vitamin B2- Komplex Nikotinsäureamid = Nikotinamid= Vit B3 Exkurs Oxidative Desaminierung:
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Biologie für Mediziner
 Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Klausurbogen im Studiengang B.Sc. Biologie Modul BSc-Bio-7, Teilklausur Biochemie vom
 Johann Wolfgang Goethe-Universität Frankfurt am Main Deckblatt Fachbereich Biowissenschaften Klausurbogen im Studiengang B.Sc. Biologie Modul BSc-Bio-7, Teilklausur Biochemie vom 08.12.2008 Name: Vorname:
Johann Wolfgang Goethe-Universität Frankfurt am Main Deckblatt Fachbereich Biowissenschaften Klausurbogen im Studiengang B.Sc. Biologie Modul BSc-Bio-7, Teilklausur Biochemie vom 08.12.2008 Name: Vorname:
Klausur zur Vorlesung Biochemie I im WS 1993/1994. am 18. Februar Nachklausur zur Vorlesung Biochemie I im WS 1993/1994. am 30. Mai 1994.
 Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lehrerhandreichungen zu: "Zellatmung" Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lehrerhandreichungen zu: "Zellatmung" Das komplette Material finden Sie hier: School-Scout.de Schlagwörter ADP; Atmungskette; ATP;
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lehrerhandreichungen zu: "Zellatmung" Das komplette Material finden Sie hier: School-Scout.de Schlagwörter ADP; Atmungskette; ATP;
Schrittweise Oxidation und Decarboxylierung von Glucose-6-phosphat zu Ribulose-5- phosphat
 1. Der plastidäre oxidative Pentosephosphatweg Abbau von Hexose unter NADPH+H + -Synthese Schlüsselenzym=Glucose-6-phosphat-Dehydrogenase Glucose-6-phosphat-Dehydrogenase wird durch Thioredoxin im reduzierten
1. Der plastidäre oxidative Pentosephosphatweg Abbau von Hexose unter NADPH+H + -Synthese Schlüsselenzym=Glucose-6-phosphat-Dehydrogenase Glucose-6-phosphat-Dehydrogenase wird durch Thioredoxin im reduzierten
Pharmazeutische Biologie Grundlagen der Biochemie
 harmazeutische Biologie Grundlagen der Biochemie A Enzyme E1 E2 E3 E4 Biosynthese A B D E B E7 E2 E6 E1 E3 E5 E4 E1 E2 E5 E4 rof. Dr. Theo Dingermann Institut für harmazeutische Biologie Goethe-Universität
harmazeutische Biologie Grundlagen der Biochemie A Enzyme E1 E2 E3 E4 Biosynthese A B D E B E7 E2 E6 E1 E3 E5 E4 E1 E2 E5 E4 rof. Dr. Theo Dingermann Institut für harmazeutische Biologie Goethe-Universität
Kohlenstoffdioxid wird in lichtabhängigen Reaktion freigesetzt Sauerstoff wird wie in der Atmung verbraucht. Lichtatmung
 1. Kompartimentierung bei der Photorespiration Kohlenstoffdioxid wird in lichtabhängigen Reaktion freigesetzt Sauerstoff wird wie in der Atmung verbraucht. Lichtatmung Kosten: o Energie, da ATP verbraucht
1. Kompartimentierung bei der Photorespiration Kohlenstoffdioxid wird in lichtabhängigen Reaktion freigesetzt Sauerstoff wird wie in der Atmung verbraucht. Lichtatmung Kosten: o Energie, da ATP verbraucht
Die Atmungskette. 1. Einleitung und Funktion. Inhalt:
 Die Atmungskette Inhalt: 1. Einleitung und Funktion 2. Die einzelnen Komplexe der Atmungskette 3. Zusammengefasst: Die Vorgänge in der Atmungskette 4. Transporte durch die Mitochondrienmembran 5. Die Regulation
Die Atmungskette Inhalt: 1. Einleitung und Funktion 2. Die einzelnen Komplexe der Atmungskette 3. Zusammengefasst: Die Vorgänge in der Atmungskette 4. Transporte durch die Mitochondrienmembran 5. Die Regulation
Pentosephosphatzyklus. Synonym: Hexosemonophosphatweg
 Pentosephosphatzyklus Synonym: Hexosemonophosphatweg Gliederung Funktion & Lokalisation Grundgerüst des Ablaufs Anpassung an Stoffwechselsituation Regelung Beispielreaktion Funktion & Lokalisation Gewinnung
Pentosephosphatzyklus Synonym: Hexosemonophosphatweg Gliederung Funktion & Lokalisation Grundgerüst des Ablaufs Anpassung an Stoffwechselsituation Regelung Beispielreaktion Funktion & Lokalisation Gewinnung
Aminosäuren & Ketosäuren BIOGENE AMINE
 BIOGENE AMINE Von Mohammed Jaber BIOGENE AMINE: Biogene Amine sind AS ohne COOH-Gruppe! Und warum sind sie so wichtig? Von Mohammed Jaber und Proteine BIOGENE AMINE: Durch die Abspaltung der COOH- Gruppe
BIOGENE AMINE Von Mohammed Jaber BIOGENE AMINE: Biogene Amine sind AS ohne COOH-Gruppe! Und warum sind sie so wichtig? Von Mohammed Jaber und Proteine BIOGENE AMINE: Durch die Abspaltung der COOH- Gruppe
Stoffwechsel der essentiellen Aminosäuren
 Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Mitochondriale Elektronentransportkette (Atmungskette)
 Mitochondriale Elektronentransportkette (Atmungskette) Mitochondriale Elektronentransportkette (Atmungskette) Komplex I und II übetragen Elektronen auf Coenzym Q (Ubichinon) Gekoppelte Elektronen-Protonen
Mitochondriale Elektronentransportkette (Atmungskette) Mitochondriale Elektronentransportkette (Atmungskette) Komplex I und II übetragen Elektronen auf Coenzym Q (Ubichinon) Gekoppelte Elektronen-Protonen
Praktikumsreferat Biochemie
 Praktikumsreferat Biochemie Thema: Glycolyse und Gluconeogenese 1. Glycolyse im Überblick Die Glycolyse (gr.: glykys = süß, lysis = auflösen) beschreibt den Abbau von Glucose zu Pyruvat (aerobe Glycolyse
Praktikumsreferat Biochemie Thema: Glycolyse und Gluconeogenese 1. Glycolyse im Überblick Die Glycolyse (gr.: glykys = süß, lysis = auflösen) beschreibt den Abbau von Glucose zu Pyruvat (aerobe Glycolyse
7 Oxidativer Abbau von Pyruvat: Die Reaktionen der Pyruvat-Dehydrogenase und des Citratzyklus
 A 7.1 inführung 103 7 xidativer Abbau von Pyruvat: Die Reaktionen der Pyruvat-Dehydrogenase und des itratzyklus 7.1 inführung Die Abbauwege aller Kohlenhydrate vereinigen sich letztlich in der Glykolyse
A 7.1 inführung 103 7 xidativer Abbau von Pyruvat: Die Reaktionen der Pyruvat-Dehydrogenase und des itratzyklus 7.1 inführung Die Abbauwege aller Kohlenhydrate vereinigen sich letztlich in der Glykolyse
Biochemie II. im Wintersemester 2009/2010. Joachim Wegener. Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg
 Biochemie II im Wintersemester 2009/2010 Joachim Wegener Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg 18.10.2010 1/14 Biochemie II im WS 2010 / 2011 All Dozenten auf einen
Biochemie II im Wintersemester 2009/2010 Joachim Wegener Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg 18.10.2010 1/14 Biochemie II im WS 2010 / 2011 All Dozenten auf einen
Versuch 5. Isocitrat-Dehydrogenase
 Versuch 5 Isocitrat-Dehydrogenase Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X PD Dr. Gimpl Einleitung Ziel des Versuches ist es, die Abhängigkeit
Versuch 5 Isocitrat-Dehydrogenase Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X PD Dr. Gimpl Einleitung Ziel des Versuches ist es, die Abhängigkeit
Primärstoffwechsel. Prof. Dr. Albert Duschl
 Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Zellulärer Abbau von Proteinen in Aminosäuren:! Proteine werden in Zellen durch Proteasom-Komplexe in! einzelne Aminosäuren abgebaut.!
 Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Atmung Respiration 1
 Atmung Respiration 1 Atmung Die oxidative Phosphorylierung ist der letzte Schritt einer Serie von Energieumwandlungen, die insgesamt als Zellatmung oder einfach Atmung (Respiration) bezeichnet werden 2
Atmung Respiration 1 Atmung Die oxidative Phosphorylierung ist der letzte Schritt einer Serie von Energieumwandlungen, die insgesamt als Zellatmung oder einfach Atmung (Respiration) bezeichnet werden 2
Importance of Glucose
 Importance of Glucose C6H12O6 Glucose 2 C3 Glycogen Glucose-6-P Glycolyse 2 Pyruvat 2 C2 2 Acetyl-CoA 2 CO2 2 (C4 + C2) Citrat-Zyklus oder Tricarbonsäure 4 CO2 Zyklus 6 H O 2 6 O2 Atmungskette Als Produkt
Importance of Glucose C6H12O6 Glucose 2 C3 Glycogen Glucose-6-P Glycolyse 2 Pyruvat 2 C2 2 Acetyl-CoA 2 CO2 2 (C4 + C2) Citrat-Zyklus oder Tricarbonsäure 4 CO2 Zyklus 6 H O 2 6 O2 Atmungskette Als Produkt
Wiederholung. Fettsäuresynthese: Multienzymkomplex Sekundäre Pflanzenstoffe
 Wiederholung Ökologie der C 4 -Pflanzen CAM-Zyklus: primäre CO 2 -Fixierung in der Nacht, Übertragung an Ribulose-1,5-bisphosphat am Tag: zeitliche Kompartimentierung Photorespiration, Lichtatmung Photosynthese
Wiederholung Ökologie der C 4 -Pflanzen CAM-Zyklus: primäre CO 2 -Fixierung in der Nacht, Übertragung an Ribulose-1,5-bisphosphat am Tag: zeitliche Kompartimentierung Photorespiration, Lichtatmung Photosynthese
I. Zellatmung. =Abbau von Kohlenhydraten unter Sauerstoffverbrauch (aerob) KH + O 2 --> CO 2 + H 2 O + Energie
 KATABOLISMUS Abbau komplexer organischer Moleküle (reich an Energie) zu einfacheren (mit weniger Energie). Ein Teil der Energie wird genutzt um Arbeit zu verrichten (Zelle erhalten, Wachstum) I. Zellatmung
KATABOLISMUS Abbau komplexer organischer Moleküle (reich an Energie) zu einfacheren (mit weniger Energie). Ein Teil der Energie wird genutzt um Arbeit zu verrichten (Zelle erhalten, Wachstum) I. Zellatmung
Reduction / Oxidation
 H :! H.. C.. H :! H H :! H.. C.. OH :! H H :! H 3 C.. C.. OH :! H O ::! H 3 C.. C.. H O ::! H 3 C.. C.. O -! O=C=O Oxidationszahl Methan -4 Methanol -2 Ethanol -1 Acetaldehyd +1 Acetat +3 Kohlendioxyd
H :! H.. C.. H :! H H :! H.. C.. OH :! H H :! H 3 C.. C.. OH :! H O ::! H 3 C.. C.. H O ::! H 3 C.. C.. O -! O=C=O Oxidationszahl Methan -4 Methanol -2 Ethanol -1 Acetaldehyd +1 Acetat +3 Kohlendioxyd
Bioenergetik. Prof. Dr. Albert Duschl
 Bioenergetik Prof. Dr. Albert Duschl Gesetze der Thermodynamik 1. Gesetz: Die Summe der Energie im Universum ist gleich. 2. Gesetz: Die Entropie nimmt zu. Geordnete Strukturen, wie Lebewesen, verletzen
Bioenergetik Prof. Dr. Albert Duschl Gesetze der Thermodynamik 1. Gesetz: Die Summe der Energie im Universum ist gleich. 2. Gesetz: Die Entropie nimmt zu. Geordnete Strukturen, wie Lebewesen, verletzen
5. Biochemie- Seminar
 5. Biochemie- Seminar 5. Biochemie- Seminar Kohlenhydrate II und biologische Oxidation Verweise mit [L] beziehen sich auf Biochemie und Pathobiochemie von Löffler, Petrides, Heinrich; 8. Auflage. Glycogenbiosynthese
5. Biochemie- Seminar 5. Biochemie- Seminar Kohlenhydrate II und biologische Oxidation Verweise mit [L] beziehen sich auf Biochemie und Pathobiochemie von Löffler, Petrides, Heinrich; 8. Auflage. Glycogenbiosynthese
SIP1A Refresher Biochemie
 SIP1A Refresher Biochemie WS 2016/17 AKH Hs. 1, 2.2.2017, 17:00 19:00 N. Erwin Ivessa Department für Medizinische Biochemie n-erwin.ivessa@meduniwien.ac.at INHALT 38 Stunden Biochemie SIP1A Relevantes
SIP1A Refresher Biochemie WS 2016/17 AKH Hs. 1, 2.2.2017, 17:00 19:00 N. Erwin Ivessa Department für Medizinische Biochemie n-erwin.ivessa@meduniwien.ac.at INHALT 38 Stunden Biochemie SIP1A Relevantes
