Isocyanatfreie Polyurethane auf Basis von nachwachsenden Rohstoffen und Kohlenstoffdioxid
|
|
|
- Anna Kohl
- vor 7 Jahren
- Abrufe
Transkript
1 Isocyanatfreie Polyurethane auf Basis von nachwachsenden Rohstoffen und Kohlenstoffdioxid INAUGURALDISSERTATION Zur Erlangung der Doktorwürde der Fakultät für Chemie und Pharmazie der Albert-Ludwigs-Universität Freiburg im Breisgau Vorgelegt von Moritz Bähr aus Freiburg im Breisgau Freiburg im Breisgau, Januar 2013
2
3 Vorsitzender des Promotionsausschusses: Referent: Korreferent: Prof. Dr. Thorsten Koslowski Prof. Dr. Rolf Mülhaupt Prof. Dr. Dr. Christian Friedrich Datum der Promotion:
4 Danksagung Die vorliegende Arbeit entstand in der Zeit von März 2009 bis Oktober 2012 am Institut für Makromolekulare Chemie der Albert-Ludwigs-Universität Freiburg. Zurückblickend auf mein Chemiestudium gilt es vielen Mitmenschen, die mich in dieser schönen, aber auch sehr kraftraubenden Zeit begleitet haben, zu danken. Zu allererst möchte ich mich bei Prof. Dr. Rolf Mülhaupt für die Bereitstellung des interessanten Themas bedanken. Weiterhin möchte ich mich bei ihm für sein stetes Interesse an den Arbeitsergebnissen, den zum selbstständigen Arbeiten gewährten Freiraum, sowie den hervorragenden Arbeitsbedingungen sehr bedanken. Herrn Prof. Dr. Dr. Friedrich danke ich für die freundliche Übernahme des Korreferats. Ein besonderes Dankeschön gilt meiner Frau die mich mit all Ihrer Kraft und Geduld unterstützt hat. Alessandro Bitto danke ich, da er während unserer Zusammenarbeit immer ein offenes Ohr für meine Fragen und Probleme hatte. Danken möchte ich allen Arbeitskreismitgliedern, im speziellen Benjamin Ritter, Hannes Blattmann, Maria Fleischer und Benjamin Kerscher für die Hilfe gut Zusammenarbeit und für die Korrrektur meiner Arbeit. Weiterhin danke ich Marco Angarano, Andreas Schüssele, Katharina Oelker, Benjamin Schöpf, Axel Pfahler, Damien Fourcade, Oliver Karstensen, und Folke Tölle für Ihrer Hilfsbereitschaft und dem regen Erfahrungsaustausch bei der Arbeit. Ein herzliches Dankeschön gilt Alexander Rossel, Erik Hügele und Harald Bartholomä für die technische Unterstützung in Wort und Tat. Frau Frederike Jones und Frau Carmen Hermann gilt mein Dank für die schnelle und unbürokratische Unterstützung bei allen anfallenden Formalitäten. Ein sehr großer Dank gilt meiner Familie, die wie kein anderer an meinem Studium, aber vor allem an meinem Leben teilgenmommen hat. Bei meinen Eltern Ludolf Bähr und Ursula Becker, die mir dieses Studium erst ermöglichten, möchte ich mich besonders bedanken. Meinen Onkels danke ich für die Zustimmung bei meiner Entscheidung dieses Studium zu beginnen, und für all das gute Zusprechen, der seelischen Unterstützung und dem stetigen Interesse an mir. a
5 Als Hirte erlaube mir zu dienen mein Vatter dir, deine Macht reiste uns durch deine Hand, diese verbindet uns wie ein heiliges Band! Wir waten durch ein Meer von Blut, gib uns dafür Kraft und Mut: Et nomine Patris, et filii et spiritus sancti, Amen Der blutige Pfad Gottes b
6 Abkürzungen Atm. Athmosphäre APS (3-Aminopropyl)-trimethoxysilan BD Bruchdehnung BDA Diaminobutan bzw. beziehungsweise c Konzentration C Grad Celsius CH 2 Cl 2 Dichlormethan CFK Carbon-faserverstärkter Kunststoff CSBO Carbonated soybean oil CL Limonendicarbonat CLSO Carbonated linseed oil CLSO-ZSA Carbonatisiertes Leinsamenöl-Zitronensäure-Amid CO 2 Kohlenstoffdioxid dest. H 2 O destilliertes Wasser DMA Dynamisch-Mechanische Analyse d.h. das heißt DADO Diaminododecan DSC Differential Scanning Calometrie EDA Ethylendiamin EE Essigsäureethylester E-Modul Elastizitätsmodul ESBO Epoxidiertes Sojabohnenöl ESEM Atmosphärenrasterelektronenmikroskop EL Epoxidiertes Limonen ELSO Epoxidiertes Leinsamenöl ELSO-ZSA Epoxidiertes Leinsamenöl-Zitronensäure-Amid FG Lupasol FG g Gramm g/mol Gramm pro Mol Gew.-% Gewichtsprozent gjdt globale Jahresdurchschnittstemperatur GPC Gel Permeations Chromatographie G20 Lupasol G20 h Stunde HMDA Hexamethylendiamin ISO Internationale Organisation für Normung IPDA Isophorondiamin IR Infrarotspektroskopie L Liter LSO Leinsamenöl LSO-Amide Leinsamenöl-Amide LSO-ZSA Leinsamenöl-Zitronensäure-Amid c
7 m Masse MCPBA meta-chlorperbenzoesäure m x x-ter Massenverlust min Minute Mio Millionen ml Milliliter mm Millimeter MPa Megapascal M W gewichtsgemitteltes Molekulargewicht NIPU Non Isocyanat Polyurethan n.b. nicht bestimmt nm Nanometer NMR Nuclear Magnetic Resonance Spektroskopie p Druck PAG Primäre Aminogruppen PR Lupasol PR RG Reaktive Gruppen s Sekunde s. siehe SiO 2 Siliziumdioxid Smp. Schmelzpunkt /-bereich T Tonnen TBAB tetra-butylammoniumbromid TGA Thermogravimetrische Analyse THMDA Trimethylhexamethylendiamin T G Glasübergangstemperatur TGA Thermo-Gravimetrische Analyse T Z Zersetzungstemperatur u.a. unter anderem usw. und so weiter z.b. zum Beispiel ZS Zitronensäure ZSA Zitronsäure-Amide ε Dehnung ε-bruch Bruchdehnung d
8 Veröffentlichungen / Patente / Berichte / Vorträge Veröffentlichungen / Patente Isocyanatfreie Polyurethane Isocyanatfreie Polyurethane erhältlich durch Umsetzung von im wesentlichen glycerinestergruppen-freien Carbonatgruppen enthaltenden Monomeren mit Aminogruppen enthaltenden Monomeren. Moritz Bähr, Rolf Mülhaupt, DE A1. Linseed and soybean oil-based polyurethanes prepared via the non-isocyanate route and catalytic carbon dioxide conversion. Moritz Bähr, Rolf Mülhaupt, Green Chemistry, 2012, 14, Cyclic limonene dicarbonate as a new monomer for non-isocyanate oligo- and polyurethanes (NIPU) based upon terpenes. Moritz Bähr, Alexandro Bitto, Rolf Mülhaupt, Green Chemistry, 2012, 14, Linseedoil amide based NIPUs. Moritz Bähr, Rolf Mülhaupt, Manuskript liegt vor, Poster New non isocyanate polyurethanes upon catalytic carbon dioxide conversion of epoxidized plant oils and limonene Moritz Bähr, Rolf Mülhaupt, 5 th Workshop on Fats and Oils as Renewable Feedstock for the Chemical Industry 2012, Karlsruhe. New Non-Isocyanate Polyurethanes with improved stability from renewable resources and carbon dioxide, Moritz Bähr, Maria Fleischer, Rolf Mülhaupt, Macromoleculares Kolloqium 2012, Freiburg. Isocyanat Free Polyurethanes from Renewable Raw Materials, Moritz Bähr, Maria Fleischer, Rolf Mülhaupt,1st Humbold adward winners Forum 2011, Bonn. Isocyanatfreie Polyurethanchemie auf Basis von CO 2 und Nachwachsenden Rohstoffen, Moritz Bähr, Maria Fleischer, Rolf Mülhaupt, Tag der Forschung der Fakultät für Chemie, Pharmazie und Geowissenschaften 2010, Freiburg. e
9 Veröffentlichungen / Patente / Berichte / Vorträge Berichte Kunststoffe aus Kohlenstoffdioxid und nachwachsenden Rohstoffen: Isocyanatfreie Polyurethanchemie, Moritz Bähr, Maria Fleischer, Alexandro Bitto, Rolf Mülhaupt, FMF-Jahresbericht Kunststoffe aus Kohlenstoffdioxid und nachwachsenden Rohstoffen: Isocyanatfreie Polyurethanchemie, Moritz Bähr, Maria Fleischer, Alexandro Bitto, Rolf Mülhaupt, FMF-Jahresbericht Abschlussbericht Kunststoffe und polymere Compounds auf Basis von Kohlenstoffdioxid, Moritz Bähr, Alexandro Bitto, Maria Fleischer, Benjamin Ritter, Rolf Mülhaupt, Vorträge (Auswahl) Moritz Bähr, Alexandro Bitto, Rolf Mülhaupt: 1-7. VW-Projekttreffen Polymere und Compounds auf der Basis von Kohlenstoffdioxid, Freiburg: Moritz Bähr, Rolf Mülhaupt: Kunststoffe aus Kohlenstoffdioxid und nachwachsenden Rohstoffen: Isocyanatfreie Polyurethanchemie, 19te interne FMF-Kolloquium, Schluchsee: Moritz Bähr, Rolf Mülhaupt: 1. Evonik Projekttreffen Polymere auf Basis von Kohlenstoffdioxid und nachwachsenden Rohstoffen: Isocyanatfreie Polyurethanchemie, Freiburg: Moritz Bähr, Rolf Mülhaupt: Kunststoffe aus Kohlenstoffdioxid und nachwachsenden Rohstoffen: Isocyanatfreie Polyurethanchemie, 20te interne FMF-Kolloquium, Schluchsee, Kooperationen Volkswagen AG, Kunststoffe und polymere Compounds auf Basis von Kohlenstoffdioxid. f
10 Inhaltsverzeichnis Inhaltsverzeichnis 1 Einleitung Klimaerwärmung und CO Klimaerwärmung Eigenschaften von CO CO 2 Fixierung Nachwachsende Rohstoffe Pflanzenöle Terpene Polymere aus CO 2 und Epoxiden Polycarbonate aus CO 2 und Epoxiden Cyclische Carbonate aus CO 2 und Epoxiden Epoxidierungsmethoden für Pflanzenöle Prinzipien der Green Chemistry Aufgabenstellung Polymere auf Basis von Kohlenstoffdioxid NIPUs auf Basis von carbonatisierten Pflanzenölen Optimierung der Carbonatisierung von Pflanzenölen NIPUs aus cyclischen Carbonaten ohne Glycerinestergruppen NIPU Composite Herstellung und Epoxidierung von Leinsamenöl-Amiden Aminolyse von Leinsamenöl Epoxidierung von Leinsamenöl-Amiden Epoxidierungsmethoden Cyclische Carbonate aus epoxidierten, nachwachsenden Rohstoffen Synthese cyclischer Carbonate mittels homogener Katalyse Cyclische Carbonate auf Basis nachwachsender Rohstoffe Herstellung von Pflanzenölcarbonaten Leinsamenöl-Amid-Carbonate Limonendicarbonat Polybutadiencarbonat Synthese cyclischer Carbonate mittels heterogener Katalyse g
11 Inhaltsverzeichnis Herstellung von Leinsamenölcarbonat und Limonendicarbonat mittels... Festphasenkatalysatoren Isocyanatfreie Polyurethane auf Basis nachwachsender Rohstoffe NIPUs auf Basis von Pflanzenölcarbonaten NIPUs basierend auf Pflanzenölcarbonaten und linearen Diaminen NIPUs basierend auf Pflanzenölcarbonate und sterisch anspruchsvollen Diaminen NIPUs basierend auf Leinsamenölcarbonat und Diamin-Mischungen NIPUs aus Sojabohnenölcarbonat und Lupasol FG Pflanzenölbasierte NIPU-Boehmit Composite NIPUs aus (3-Aminopropyl)-trimethoxysilan und Pflanzenölcarbonaten Funktionalisierung von DisperalS mit (3-Aminopropyl)-trimethoxysilan Herstellung von NIPU-DisperalS-Composite Pflanzenölbasierte NIPU-CFK-Laminate Herstellung von Pflanzenölbasierten CFK-NIPUs NIPUs auf Basis von Leinsamenöl-Amid Carbonaten Herstellung von Leinsamenöl-Amid Carbonat basierten NIPUs NIPUs basierend auf Limonendicarbonat Bestimmung der Reaktionsgeschwindigkeit von CL mit Aminen NIPU Gießharze auf Basis von Limonendicarbonat Lineare NIPU-Präpolymere auf Basis von Limonendicarbonat und Diaminen Zusammenfassende Diskussion und Ausblick Einleitung Epoxidierte Leinsamenöl-Amide Herstellung von Leinsamenöl-Amiden Epoxidierung der Leinsamenölamide Cyclische Carbonate aus epoxidierten nachwachsenden Rohstoffen Synthese cyclischer Carbonate mittels homogener Katalyse Synthese cyclischer Carbonate mittels heterogener Katalyse Übersicht über die hergestellten cyclischen Carbonate Isocyanatfreie Polyurethane auf Basis nachwachsender Rohstoffe NIPUs auf Basis von Pflanzenölcarbonaten Bestimmung der Gel- und Topfzeiten für NIPUs aus Pflanzenölcarbonaten NIPUs basierend auf Pflanzenölcarbonaten und linearen Diaminen NIPUs basierend auf Pflanzenölcarbonate und sterisch anspruchsvollen Diaminen h
12 Inhaltsverzeichnis NIPUs basierend auf Leinsamenölcarbonat und Diamin-Mischungen Pflanzenölcarbonat basierte Composite Pflanzenölcarbonat basierte NIPU-DisperalS Composite NIPUs auf Basis von Leinsamenöl-Amid Carbonaten NIPUs basierend auf Limonendicarbonat NIPU-Gießharze auf Basis von Limonendicarbonat Lineare NIPU-Präpolymere auf Basis von Limonendicarbonat und Diaminen Ausblick Cyclische Carbonate auf Basis nachwachsender Rohstoffe Isocyanatfreie Polyurethane auf Basis nachwachsender Rohstoffe NIPU-Composite auf Basis nachwachsender Rohstoffe Experimenteller Teil Verwendete Chemikalien Aminolyse von Leinsamenöl und Zitronensäuretriethylester mit verschiedenen Diaminen Epoxidierung von Leinsamenöl-Amiden Epoxidierung mit MCPBA Peressigsäure-Verfahren In Situ-Verfahren Herstellung von cyclischen Carbonaten mit TBAB als Katalysator Herstellung von cyclischen Carbonaten mit Festphasenkatalysatoren Aktivierung von Aerosil Synthese von SiO 2 -(3-Iodopropyl)trimethoxysilan Synthese von SiO 2 -C 3 H 6 I-4-Pyrrolidinopyridin (SiO 2 -I) Synthese von SiO 2 -C 3 H 6 I-1-Butylimidazol (SiO 2 -ImI) Synthese von SiO 2 -C 3 H 6 I-Tributylphosphin (SiO 2 -PI) Synthese von cyclischen Carbonaten mittels Festphasen Katalysatoren Herstellung von NIPUs Bestimmung der Topf und Gelzeiten NIPUs basierend auf Pflanzenölcarbonaten und Diaminen NIPUs basierend auf Pflanzenölcarbonaten und Aminhärter Mischungen NIPUs basierend auf Leinsamenöl-Amid Carbonaten NIPUs-Gießharze basierend auf Limonendicarbonbat und polyfunktionellen Aminhärtern NIPUs-Präpolymere auf Basis von Limonendicarbonat und Diaminen i
13 Inhaltsverzeichnis 7.7 Pflanzenölbasierte NIPU-Boehmit Composite NIPUs aus (3-Aminopropyl)-trimethoxysilan und Pflanzenölcarbonaten Funktionalisierung von DisperalS mit (3-Aminopropyl)-trimethoxysilan Herstellung von NIPU-DisperalS-Composite Pflanzenölbasierte NIPU-CFK-Laminate Analytik Magnetische-Kernresonanz-Spektroskopie (NMR) Infrarot-Spektroskopie (IR) Thermogravimetrische Analyse (TGA) Dynamisch mechanische Analyse (DMA) Quellungsversuche Konduktometrische Titration Kegelplattenviskosimeter Atmosphärenrasterelektronenmikroskop (ESEM) Zug-/Dehnungs-Versuch Gelpermeationschromatographie (GPC) Topfzeit- und Gelpunktsbestimmung Probenverzeichnis Literaturverzeichnis Kurzzusammenfassung Lebenslauf j
14 1 Einleitung 1 Einleitung Im Jahr 2010 wurden 265 Mio. t Kunststoff weltweit erzeugt. 1 Die chemischen Rohstoffe dafür wurden zu 90% aus Erdöl und Erdgas gewonnen. 2 Obwohl dies nur 4% des weltweiten Erdölverbrauchs entspricht ist es in Zeiten immer knapper werdender fossiler Rohstoffe wichtig Alternativen zu der konventionellen Kunststofferzeugung zur Verfügung zu haben. So wurden Mio. t Erdöl gefördert, bei einem gleichbleibenden Verbrauch wird ein Ende der Erdölreserven zwischen den Jahren erwartet. Allerdings wird bereits ab die maximal jährliche Fördermenge von 3928 Mio. t erwartet. 3 Ab diesem Zeitpunkt kann man nicht mehr durch höhere Fördermengen auf Wirtschaftskrisen oder durch eine von Kriegen verursachte Ölknappheit reagieren. Die Folgen werden drastische Preissteigerungen des Rohölpreises sein. Ein weiterer Aspekt ist die anthropogene Klimaerwärmung durch die vermehrte Freisetzung von Treibhausgasen seit der industriellen Revolution. Im Bereich der Polymerchemie ist es auf vielfältige Weise möglich auf diese Entwicklungen zu reagieren. Beispielweise können durch die Verwendung von nachwachsenden Rohstoffen und die chemisch Fixierung des Treibhausgases Kohlenstoffdioxid klimaneutrale Materialien hergestellt werden. 1.1 Klimaerwärmung und CO Klimaerwärmung Als Klimawandel wird der in den letzten Jahrzehnten fortwährende Anstieg der globale Jahresdurchschnittstemperatur (gjdt) bezeichnet. In der Erdgeschichte schwankte die gjdt zwar schon immer, aber in den letzten Jahrzehnten nahm die Erwärmung in der erdnahen Atmosphäre und in den Meeren deutlich zu. Wie Abbildung 1.1 gezeigt ist die gjdt in den letzten 30 Jahren um 0.6 C angestiegen. 4 1
15 Abweichungen [ C] 1 Einleitung 0,75 Abweichungen der globalen Durchschnittstemperatur 0,50 0,25 0,00 Jahres Mittel 5-Jahres Mittel -0,25-0, Jahr Abbildung 1.1: Abweichung der globalen Durchschnittstemperatur vom Referenzzeitraum Der Anstieg um 0.6 C der gjdt mag auf den ersten Blick nicht viel sein, aber bereits ein Anstieg von nur 2 C würde verheerende Auswirkungen auf unsere Umwelt haben: Abschmelzen der Polkappen, Anstieg des Meeresspiegel, Klimaveränderungen wie z.b. langanhaltende Trockenzeiten in Südeuropa und Afrika und vermehrtes Auftreten von extremen Wetterphänomen wie z.b. Tornados, Hurrikane, Taifune, El Niño usw. 5 Als Ursache dieser Temperaturerhöhung gilt die erhöhte Konzentration von Treibhausgasen. 6 Diese Treibhausgase - Wasserdampf, Kohlenstoffdioxid, Methan und Lachgas - sind ein natürlicher Bestandteil unserer Atmosphäre. 7 Sie lassen das kurzwellige Sonnenlicht zur Erdoberfläche durch, absorbieren aber die langwellige Infrarotstrahlung, die von der Erdoberfläche abgestrahlt wird. Dadurch erwärmen sie sich selbst und die Atmosphäre (Kirchhoffsches Strahlungsgesetz). In ihrer ursprünglichen Konzentration bilden sie den natürlichen Treibhauseffekt mit einem globalen Temperaturbereich, der die Grundlage für Leben auf der Erde ist. 8 Als Folge der weltweiten Industrialisierung hat jedoch der Ausstoß an Treibhausgasen sehr stark zugenommen. Es wird geschätzt, dass gegenwärtig ca. 7.2 Gt Kohlenstoff (hauptsächlich CO 2 ) pro Jahr die atmosphärische Zusammensetzung verändert haben. 9 Die erhöhten Methan- und Lachgas-Konzentrationen sind auf die verstärkte Viehzucht zurückzuführen, während durch das Verbrennen von fossilen Rohstoffen wie Kohle, Erdöl und Erdgas vor allem der CO 2 -Gehalt erhöht wurde. 10 Eiskernbohrungen in der Antarktis belegen, dass heute (2011) mit 390 ppm die höchste CO 2 - Konzentration in der Atmosphäre seit Jahren vorhanden ist. 11 In Bezug zu 2
16 Kohlenstoffdioxid Methan Lachgas Halogenierte Kohlenwasserstoffe Ozon in Troposphäre Solarstrahlung Aerosole Albedo Effekte Nettoeffekt anthropogen Strahlungsantrieb (W/m 2 ) 1 Einleitung Kohlenstoffdioxid ist zu beachten, dass im molaren Vergleich zu Methan oder Lachgas, CO 2 weniger effektiv Infrarotstrahlung aufnimmt und abgibt. Aber da CO 2 in überproportinal größeren Mengen vorhanden ist, trägt es hauptsächlich zum Klimawandel bei. Als Kenngröße ist hier der Strahlungsantrieb zu nennen. Er beschreibt eine externe Störung der Strahlungsbilanz des Klimasystems der Erde durch Treibhausgase oder durch die Bestrahlungsstärke der Sonne. 12 (s. Abbildung 1.2). 2,0 Treibhausgase 1,5 1,0 0,5 0,0-0,5-1,0 Abbildung 1.2: Komponenten des Strahlungsantriebs. 12 Die Treibhausgase haben einen positiven Strahlungsantrieb und verstärken somit den Treibhauseffekt. Aerosole sowie der Albedo Effekt weisen einen negativen Strahlungsantrieb auf, was zu einer Abkühlung der Atmosphäre führt. Deutlich bemerkbar macht sich dieser Effekt nach Vulkanausbrüchen, wo es zu einer deutlichen Absenkung der gjdt kommen kann. In der Summe der von Menschen verursachten (anthropogenen) Effekte bleibt ein positiver Strahlungsantrieb, der zu einer Erwärmung der Atmosphäre führt. Der anthropogene Nettoeffekt ist genauso groß wie der von CO 2 verursachte Strahlungsantrieb. Zusätzlich zu seiner klimaschädlichen Wirkung ist CO 2 auch schädlich für die Weltmeere, da es sich in Wasser löst und Kohlensäure bildet. Dies 3
17 1 Einleitung führt zu einem erhöhten ph-wert, was viele auf Kalk angewiesene Lebewesen (Korallen, Muscheln usw.) absterben lässt. 13 Aufgrund seines maßgeblichen Anteils am Strahlungsantrieb und der Versauerung der Meere ist es von großem Interesse, die Entstehung von Kohlenstoffdioxid zu vermeiden oder es unschädlich zu machen. CO 2 kann auf verschiedenen Wegen gebunden werden. Beispielweise ist es möglich, CO 2 mittels CCS-Verfahren in unterirdischen Speichern zu entsorgen oder es als Rohstoff zu nutzen Eigenschaften von CO 2 Kohlenstoffdioxid ist ein farbloses, nicht brennbares und geruchloses Gas. 14 Es kommt in unsere 15, 16 Atmosphäre in einer Konzentration von 390 ppm vor, dies entspricht 3000 Gt. Hinzu kommen jedes Jahr ca. 36 Gt anthropogenes, d.h. vom Menschen verursachtes CO Abbildung 1.3 sieht man das Phasendiagramm von CO 2. In 5.2 bar Abbildung 1.3: Phasendiagramm von CO 2 (nicht Maßstabsgerecht). 4
18 1 Einleitung CO 2 besitzt einen Tripelpunkt bei 5.11 bar und K und hat seinen kritischen Punkt bei 73.8 bar und 31 C. Überkritisches CO 2 wird aufgrund seiner sehr guten Lösungseigenschaften als Extraktionsmittel für Koffein aus Kaffee oder andere Naturstoffe verwendet. 18 CO 2 absorbiert Licht im infraroten Bereich, so dass es die Wärmeabstrahlung der Erde in den Weltraum verhindert und somit zum Treibhauseffekt beiträgt. Kohlenstoffdioxid besitzt eine sehr hohe Standardbildungsenthalpie von -393 kj/mol 19 und ist daher eine sehr beständige Verbindung. Es zerfällt erst bei 1205 C in Kohlenstoffmonoxid und Sauerstoff. 14 Deshalb kann es als Schutzgas bei chemischen Prozessen oder in Feuerlöschern eingesetzt werden. CO 2 ist in Wasser relativ gut löslich und reagiert zu einem geringen Anteil (0.2%) zu Kohlensäure. Dies wurde im Jahr 1780 von Johann Jakop Schweppe ausgenutzt um Erfrischungsgetränke haltbarer zu machen. 20 Weiterhin kommt CO 2 als Treibgas, Kühlmittel 21 oder als Flüssigkeit zum Transport von Kohle in Pipelines zur Anwendung. Großtechnisch ist es ein Bestandteil bei der Synthese von Harnstoff, Methanol, cyclischen Carbonaten, Salizylsäure und Soda Weitere relevante Umsetzungen mit CO 2 werden mit Wasserstoff, Alkoholen, Acetalen, Epoxiden, Aminen, C-C- Mehrfachbindungen und Oxetanen bei Anwesenheit von Katalysatoren durchgeführt CO 2 Fixierung Wie bereits in Kapitel beschrieben, ist CO 2 ein Treibhausgas. Aus diesem Grund besteht großer Bedarf an Möglichkeiten, CO 2 aus der Atmosphäre zu entfernen und sicher zu speichern. Dies kann auf drei verschiedenen Wegen bewerkstelligt werden: 1) Eine Möglichkeit ist die physikalische Speicherung von CO 2 unter der Erdoberfläche, das sogenannte CCS-Verfahren (Carbon dioxide Capture and Storage). 12 Dabei wird das bei Großanlagen (Braunkohlekraftwerke, Zementwerke) anfallende CO 2 von den restlichen Abgasen getrennt, verflüssigt und in unterirdischen Kavernen gelagert. 28 Allerdings wirft dieses Verfahren noch viele ungelöste Fragen und Probleme auf. Beispielsweise ist zusätzliche Energie notwendig um das CO 2 zu verflüssigen und unter die Erde zu pumpen. Weiterhin gibt es keine Langzeitversuche, zur Klärung der Gefahren während einer langen Lagerung. Risse in den Gesteinsschichten können durch Erdbewegungen oder chemische Reaktionen des CO 2 entstehen. Dies würde zu einem unkontrollierten Freisetzen von großen Mengen an CO 2 führen. 29 5
19 1 Einleitung 2) Als zweites kann die Syntheseleistung der Natur ausgenutzt werden, wobei durch Photosynthese CO 2 in Biomasse überführt wird. Durch Biokonversion mit Hilfe von Mikroorganismen lässt sich die Biomasse in verschiedene Substanzen umgewandeln. 30 3) Die dritte Möglichkeit besteht darin, CO 2 chemisch zu fixieren. Da CO 2 eine thermodynamisch sehr stabile Verbindung ist (Standardbildungsenthalpie = -393 kj/mol), geht es chemische Reaktionen nur ein, wenn viel Energie in eine Reaktion investiert wird, 30, 31 der Reaktionspartner hochenergetisch ist oder wenn Katalysatoren verwendet werden. Durch die Kombination der Wege 2 und 3, also die chemische Fixierung von CO 2 in Substanzen auf Basis nachwachsender Rohstoffe, kann eine optimale Ausnutzung der Ressourcen erreicht werden. In Abbildung 1.4 ist ein Überblick über die Chemie der Kohlenstoffdioxid-Nutzung wiedergegeben. Polycarbonate Cyclische Carbonate Alkylcarbonate Chemische Fixierung PLA PHB Biopolymere Biotechnologie CO 2 Photosynthese Monomere Furfurylalkohol Polyole Methanol Biosprit Ethanol Synthesegas CO/H 2 Kohlenhydrate (Cellulose, Zucker, Stärke) Öle, Fette, Terpene Biomasse Biokonversion Mikroorganismen, Enzyme 24, 29, 30, 32, 33 Abbildung 1.4: Chemie der Kohlenstoffdioxid-Nutzung. 6
20 1 Einleitung Weltweit entstehen rund 140 Mrd. t Biomasse pro Jahr, davon werden 6 Mrd. t pro Jahr genutzt. 34 Im Vergleich dazu belaufen sich 2008 die geförderten Mengen fossiler Energieträger sich auf 3.4 Mrd. t Kohle, 3.9 Mrd. t Erdöl 1.8 Mrd. t Erdgas. 35 Die Produkte der Photosynthese werden in vielfältiger Weise als nachwachsende Rohstoffe genutzt. In Deutschland wurden 2011 bereits 19% der Anbaufläche ( ha) für die Herstellung von nachwachsenden Rohstoffen genutzt. Die deutsche Industrie hat 2008 insgesamt 3.6 Mio. t nachwachsende Rohstoffe (ohne Holz) verarbeitet. 36 Aus der Biomasse können durch einfache Extraktionen Kohlenhydrate wie Cellulose, Zucker und Stärke gewonnen werden, darüber hinaus in großem Maßstab auch Pflanzenöle, Fette und Terpene. Mit Hilfe von Mikroorganismen und Enzymen ist es möglich, aus der Biomasse eine Vielzahl von Monomeren, Lösungsmitteln sowie Treibstoffen herzustellen. Als Monomere werden beispielweise großtechnisch Lactid, 37 Furfurylderivate, Polyole usw. gewonnen. Ebenfalls unter Einsatz von Mikroorganismen ist die Herstellung von Polyhdroxybuttersäure (PHB) aus Glucose oder Stärke industriell möglich. 42 Die Vergärung von Biomasse zu Bio-Ethanol und Bio-Methanol erlaubt auch die Herstellung von Treibstoff. Dies stellt allerdings eine extrem ineffiziente Nutzung der verfügbaren landwirtschaftlichen Fläche dar. 43 Aus Biomasse lässt sich auch Synthesegas herstellen, was wiederum für die Produktion von Ethanol, Butanol, Aceton, usw. verwendet werden kann. 44 Die chemische Fixierung bietet die Möglichkeit CO 2 als C 1 -Baustein einzusetzen. Allerdings muss aufgrund seiner thermischen Stabilität für die Reaktion viel Energie zur Verfügung gestellt werden oder es ist der Einsatz von maßgeschneiderten Katalysatoren erforderlich. So kann mit Hilfe von Kupfer- und Zinkoxid-Katalysatoren mit hoher Selektivität Methanol hergestellt werden. 45, 46 Mit Methanol und CO 2 ist die Herstellung von Dimethylcarbonat möglich, das als Phosgenersatz und Alkylierungsmittel eingesetzt wird. 24, 47, 48 Mit Hilfe von Epoxiden werden seit 1950 im großen Maßstab cyclische Carbonate aus CO 2 gewonnen. 49 Diese sind polar, aprotisch, ungiftig, besitzen einen hohen Dampfdruck und Siedepunkt und sind thermisch sehr stabil, was sie zu interessanten Lösungsmitteln in Lithium-Ionen-Batterien macht. 47, 50, 51 Mittels Epoxiden und CO 2 ist es unter Verwendung von Metall-Katalysatoren aber auch möglich Polycarbonate 32, 49, herzustellen. 7
21 1 Einleitung 1.2 Nachwachsende Rohstoffe Im Jahr 2008 wurden in Deutschland rund 3.6 Mio. t nachwachsende Rohstoffe (NaWaRo) industriell stofflich genutzt. Im Einzelnen betrachtet wurden ca. 1.4 Mio. t Öle und Fette, ca. 1.5 Mio. t Kohlenhydrate und ca. 0.7 Mio. t sonstige NaWaRos verarbeitet. 55 Durch die Verarbeitung von nachwachsenden Rohstoffen zu langlebigen Produkten kann CO 2 auf Dauer gebunden werden. Naturfaserverstärkte Werkstoffe sind eine wichtige Anwendung von NaWaRos. Dabei werden Fasern wie z.b. Baumwoll-, Flachs-, Hanffasern und Fasern von exotischen Nutzpflanzen (Jute, Abaca, Kenaf, Kokos, Sisal) mit verschiedenen Kunststoffen zu Bauteilen verarbeitet. Die naturfaser verstärkten Kunststoffe (NFK) weisen hohe Steifigkeiten und Festigkeiten auf. Im Vergleich zu Glasfaser-verstärkten Kunststoffen (GFK) besitzen sie eine geringe Dichte und sind im Vergleich zu Carbonfaser-verstärkten Kunstoffen (CFK) wesentlich günstiger. Diese Eigenschaften machen NFK zu idealen Werkstoffen für die Automobilindustrie, für die sie auch in den 1980er entwickelt wurden. 34 Durch Modifizierung von natürlichen Biopolymere z.b. Stärke, Cellulose, Chitosan, Casein, Gluten, Kollagen, Naturkautschuk können biobasierte Kunststoffe, d. h. Kunststoffe auf Basis nachwachsender Rohstoffe, hergestellt werden. Aufgrund der hohen Produktionskosten im Vergleich zu erdölbasierten Kunststoffen werden biobasierte Kunststoffe nur in geringen Mengen produziert. 55 Der größte Teil der genutzten NaWaRos sind Öle und Fette. Hauptsächlich werden sie zu Tensiden für Waschmittel verarbeitet. Allein in Deutschland wurden t Tenside hergestellt und rund t verbraucht, der Rest ging in den Export. Weiterhin werden Öle als Schmierstoffe, bei der Herstellung von Polymeren, als Polymeradditive, für Lacke/Farben sowie als Lösungsmittel verwendet. 56 Einen festen Bestandteil stellen NaWaRo auch als Lieferanten für Fein- und Spezialchemikalien dar. So bilden pflanzliche Inhaltsstoffe weiterhin die Grundlage für viele Medikamente (Sonnenhut, Baldrian, Herbstzeitlose), Farbstoffe (Saflor, Färberknöterich, Färberwau) und Duftstoffe (Rosen, Orangen). 57 8
22 1 Einleitung Pflanzenöle Wie bereits erwähnt, nehmen Fette und Öle einen enormen Anteil an den industriell genutzten NaWaRos ein. Wobei Seifen und Tenside mengenmäßig den größte Anteil ausmachen. 58, 59 Die Pflanzenöle werden hauptsächlich aus sognannten Ölpflanzen gewonnen. Dabei befindet sich das Öl in den Früchten oder in den Samen. Üblicherweise besteht ein Pflanzenöl aus einem Triglycerid mit verschiedenen Fettsäuren. Die Fettsäuren unterscheiden sich durch die Anzahl der Kohlenstoffatome (C) und die Anzahl der Doppelbindungen (DB). In Abbildung 1.5 ist exemplarisch ein Triglycerid abgebildet und Tabelle 1.1 gibt die Zusammensetzungen der industriell am häufigsten verwendeten Pflanzenöle wieder. Durch Züchtung kann die Fettsäurezusammensetzung in den Pflanzen je nach Bedarf verändert werden. So besitzt europäisches Leinsamenöl einen deutlich höheren Anteil an der dreifach ungesättigten Linolensäure wie das nordamerikanische Leinsamenöl Je nach Anteil an ungesättigten Fettsäuren unterscheidet man zwischen nichttrocknenden (Olivenöl), halbtrocknenden (Soja- oder Rapsöl) und trocknenden Pflanzenölen (Leinsamenöl). Wobei sich Trocknung auf die oxidative Polymerisation von ungesättigten Fettsäuren bezieht. Ausgelöst wird dies durch den Sauerstoff in der Luft. Dieses Verharzen des Öls wurde für die Herstellung von Linoleum als Fußbodenbelag und für Ölfarben genutzt. 63 Für Schmierstoffe und für Hochtemperaturanwendungen kommen vor allem gesättigte Pflanzenöle infrage, da sie oxidationsunempfindlich sind und einen hohen Rauchpunkt aufweisen. 56 Für die Oleochemie sind ungesättigte Pflanzenöle am besten geeignet, da über die Doppelbindungen eine Vielzahl von chemischen Modifikationen möglich ist. Als Beispiele sind hier Hydrierung, Epoxidierung, Metathese-Reaktionen, EN-Reaktionen, Hydroformulierungen zu nennen. 56, 58, Diese Reaktionen erlauben unter anderem auch die Herstellung zahlreicher unterschiedlichster Monomere für die Kunststoffindustrie. Etabliert ist die Herstellung von Polyolen aus epoxidierten Pflanzenölen, welche mit Isocyanaten zu Polyurethanen umgesetzt werden können Besonders interessant ist Ricinolsäure, da sie die Grundlage für die Herstellung von 11-Aminoundecansäure für PA11 (Rilsan ), sowie Sebacinsäure darstellt. Sebacinsäure kann wiederrum zu Polyester, Polyamide, Schmiermitteln und Weichmachern verarbeitet werden. 72 9
23 1 Einleitung Abbildung 1.5: Triglycerid mit verschiedenen Fettsäuren (C:DB = 18:1, 18:2, 18:3). Tabelle 1.1: Fettsäuren-Zusammensetzung von verschiedenen Pflanzenölen. 60 Palmenöl Olivenöl Rübsamenöl Rapsöl Baumwollsamenöl Maisöl Sojabohnenöl Leinsamenöl Fettsäure C : DB Myristin- 14 : Myristolein- 14 : Palmitin- 16 : Palmitolein- 16 : Margarin- 17 : Margarolein- 17 : Stearin- 18 : Öl- 18 : Linol- 18 : [Gew.-%] Linolen- 18 : a b Arachin- 20 : Gadolein- 20 : Eicosadienoin- 20 : Behen- 22 : Eruca- 22 : Lignorcerin- 24 : Durchschnitt DB/Triglycerid a = maximaler Gehalt in Amerikanischen Leinsamenöl, b = = maximaler Gehalt in Europäischen Leinsamenöl, C = Kohlenstoffatome; DB = Doppelbindungen. 10
24 1 Einleitung Terpene Geschichtlich lässt sich der Begriff Terpen aus dem Wort Terpentin ableiten. Terpentin (Balsamum Terebinthinae) ist das zähflüssige Kiefernharz, das durch Verletzungen der Baumrinde entsteht. Terpentin enthält verschiedene Harzsäuren und Kohlenwasserstoffe, welche als Terpene bezeichnet wurden. Heute sind Terpene der Sammelbegriff für Naturstoffe, die aus Isoprenuntereinheiten aufgebaut sind. In Blüten, Blättern, Stängeln, Nadeln, Wurzeln, Samen, Früchten und in Harzen von ca Pflanzen befinden sich etherische Öle Diese komplexen Gemische enthalten überwiegend Terpene. Gewonnen bzw. angereichert werden sie durch Wasserdampfdestillation, Extraktion oder wie bei Myrrhe und Naturkautschuk durch Anritzen der Rinde. Da viele etherischen Öle einen ausgeprägten Geruch bzw. Geschmack besitzen, werden sie in der Parfümerie oder als Geschmacks- und Duftveredler von Nahrungsmitteln, Reinigungsmitteln und Lösungsmitteln verwendet. Beispiele hierfür sind zum einen das Rosenblütenöl, welches als Duftstoff für Parfüm Verwendung findet. Zum anderen ist Limonen als Orangengenaroma häufig in Putzmitteln anzutreffen. Viele Pflanzen erzeugen flüchtige, aromatische Terpene, um Insekten für die Bestäubung anzulocken oder toxische Terpene um Fressfeinde abzuwehren. Zudem sind zahlreiche Terpene auch als Hormone (Steroide) und Vitamine (A, E, K) im Stoffwechsel von Lebewesen zu finden. 75 Die Biosynthese der Terpene wurde als erstes von F. Lynen und K. Bloch verstanden, die dafür 1964 mit dem Nobelpreis geehrt wurden. Die biogenetische Vorstufe der Terpene ist das Acetyl- Coenzym A (Acetyl-CoA), eine biologische Version einer aktivierten Essigsäure. Durch eine Claisen-Kondensation zweier Acetyl-CoA entsteht Acetoacetyl-CoA, durch weitere Reaktionen entsteht schließlich die Mevalonsäure. 73 Mevalonsäure ist der Grundbaustein für alle Terpene. Von ihr ausgehend, entsteht durch eine zweifache Phosphorylierung, Decarboxylierung und Wasserabspaltung Isopentenylpyrophosphat (IPP), auch aktives Isopren genannt. IPP wird durch eine Isomerase in das stabilere 3,3-Dimethylallylpyrophosphat (DMAPP) umgelagert. Die Weiterreaktion verschiedener Pyrophosphate führt schließlich zu den Terpenen (s. Abbildung 1.6)
25 1 Einleitung Acetyl-CoAS Acetoacetyl-CoAS Mevalonsäure - HSCoAS - CO 2, - H 2 O DMAPP IPP Terpenylpyrophosphat Abbildung 1.6: Vereinfachte Darstellung der Biosynthese von Terpenen mit Acetyl-Coenzym A (Acetyl-CoAS). Terpene und Terpenoide sind eine sehr umfangreiche Klasse von Naturstoffen. Ihre Eigenschaften reichen von flüchtig, niedermolekular bis hin zu hochmolekularen, polymeren Verbindungen. Sie lassen sich einteilen in acyclische, mono-, bi- und tri- sowie tetracyclische und kondensierte Stoffe. Weiterhin können sie eine Vielzahl von funktionellen Gruppen aufweisen; so gibt es Terpene die als Alkohole, Ketone, Aldehyde, Epoxide, heterocyclische Verbindungen, Ether, Carbonsäuren und Ester bezeichnet werden. 75 Eine einheitliche Bezeichnung der Terpene ist durch die Anzahl der C5-Isopreneinheiten möglich. So weisen Monoterpene (C10) zwei Isopreneinheiten, Sesquiterpene (C15) drei Isopreneinheiten, Diterpene (C20) vier Isopreneinheiten auf. Dieser als biogenetische Isoprenregel bekannte Aufbau der Isoprenoide wurde ursprünglich von O. Wallach [1887, Chemienobelpreis 1910] aufgestellt und später von L. Ruzicka [1922, Chemienobelpreis 1939] formuliert. 75 In Abbildung 1.7 ist ein Überblick über verschiedene Terpene wiedergeben. 12
26 1 Einleitung n = 2 Monoterpene C 10 Sesquiterpene C 15 Biogenetische Isoprenregel nach L. Ruzicka Isopren = C 5 n n = 3 n = 4 n = 5 n = 6 n = 8 Diterpene C 20 Sesterpene C 25 Triterpene C 30 Tetraterpene C 40 n 10 Polyterpene C 50 Acyclische, Monocyclische, Bicyclische, Triczyclische uva. Zizamin B (Insekten, Pilze) Steroide Carotinoide β-carotin cis- trans- Limonen Orangenschale b-curcumen (Ingwer) Vitamin A1 Naturkutschuk elastisch M g/mol Guttapercha nicht elastisch M g/mol Abbildung 1.7: Übersicht und Aufbau der Terpene. Besonders interessant ist das Monoterpen Limonen (s. Abbildung 1.7). Es kommt in der Natur als (R)-(+)-Limonen und (S)-(-)-Limonen vor. (R)-(+)-Limonen ist der Hauptbestandteil von etherischen Ölen in der Schale von Zitrusfrüchten und fällt somit in großen Mengen als Abfallprodukt bei der Orangensaftherstellung an. Pro Jahr fallen so ca Megatonnen aus der Orangensaftindustrie an. 76 (S)-(-)-Limonen ist ein Bestandteil von Edeltannen-, Fichtennadel-, Muskatnuss- und Pfefferminzöl. Weiterhin wird Limonen durch die säurekatalysierte Isomerisierung aus den bicyclischen Monoterpenen -, und -Pinen hergestellt. 74 -, und - Pinene wiederum sind die Hauptbestandteile von Terpentin. Somit tritt Limonen als nachwachsender Rohstoff nicht in Konkurrenz zur Lebensmittelindustrie. Industriell genutzt wird Limonen als Duft- und Aromastoff, 74 Lösungsmittel, 76 natürliches Insektizid 77, und Reaktivverdünner für Klebstoffe
27 1 Einleitung 1.3 Polymere aus CO 2 und Epoxiden Da Kohlenstoffdioxid ein ungiftiges, farbloses, nicht brennbares, geruchloses Gas ist und in großen Mengen als Verbrennungsprodukt anfällt, ist es ideal als Rohstoff geeignet. Allerdings ist CO 2 eine besonders stabile Verbindung, weshalb es Reaktionen nur mit energiereichen Reaktionspartnern, unter extremen Bedingungen (hohe Temperatur, hoher Druck) oder mit Hilfe von Katalysatoren eingeht. Eine schon seit langem bekannte Möglichkeit Kohlenstoffdioxid chemisch zu fixieren ist die katalytische Reaktion von Epoxiden mit CO 2. Die Epoxide sind aufgrund ihrer Ringspannung (115 kj / mol) sehr reaktiv und können mit Hilfe von Katalysatoren mit CO 2 reagieren. Durch die Wahl des Katalysators entstehen entweder cyclische Carbonate oder Polycarbonate. 31 Für die Herstellung von Polymeren durch chemische Fixierung von CO 2 gibt es daher 2 Möglichkeiten: 1. CO 2 wird direkt als Monomer Verwendet. 2. Man verwendet cyclische Carbonate als Monomer. Im Folgenden werden die Herstellung von Polycarbonaten und cyclischen Carbonaten getrennt voneinander besprochen. Weiterhin wird gezeigt, wie mit Aminen aus cyclischen Carbonaten Polyurethane hergestellt werden können Polycarbonate aus CO 2 und Epoxiden Polycarbonate sind industriell wichtige Materialien, da sie durch ihre Eigenschaften wie Festigkeit, Leichtigkeit, Strapazierfähigkeit, biologische Abbaubarkeit, Hitzebeständigkeit, einfache Verarbeitbarkeit, hohe Transparenz und gute elektrische Isolation in vielen Bereichen Verwendung finden. Beispielweise werden aus ihnen CD s, Brillengläser, Schutzscheiben, Flugzeugfenster, Autoscheinwerfer usw. hergestellt. Daher ist die übergangsmetallkatalysierte Synthese von Polycarbonaten aus Kohlenstoffdioxid und Epoxiden einer der attraktivsten Prozesse für die Polymerindustrie. Im Jahr 1969 veröffentlichte die Gruppe um S. Inoue die Copolymerisation von Propylenoxid mit CO 2 unter atmosphärischem Umgebungsdruck. Als Katalysatoren verwendeten sie Triethylaluminium- und Diethylzinkverbindungen. 52, 79 Allerdings entstand bei der Reaktion neben dem Polypropylencarbonat in großen Mengen das cyclische Carbonat Propylencarbonat (s. Abbildung 1.8). 14
28 1 Einleitung CO 2 Einbau CO 2 Polymerisation PO Einbau Backbiting Abbildung 1.8: Vereinfachter 2-Komponenten-Mechanismus der Bildung von Polycarbonat, cyclischem Carbonat aus Epoxiden und CO L n = n Liganden, M = Metall, P = Polymer. Als Mechanismus für diese Polymerisation wird eine Insertion des CO 2 zwischen die Metall- Ligand-Bindung angenommen. Eine vollständige Aufklärung steht noch aus. Der Grund für die Entstehung von cyclischen Carbonaten als Nebenprodukt liegt in der energetisch günstigeren Position der cyclischen Carbonate gegenüber dem Polycarbonat und dem Backbiting Mechanismus (s. Abbildung 1.8). 31 Erst die Verwendung von Single-site-Katalysatoren änderte dies. Als erstes wurde ein Aluminiumporphyrin-Katalysator entwickelt, der als erster klassischer Homogenkatalysator für diese Reaktion gilt. 81 Im Laufe der Jahre wurde gefunden, dass sich folgende Metalle am besten als Katalysatoren für die Copolymerisation von CO 2 und Epoxiden 82, 83 eigenen: Al, Cr, Co, Mg, Li, Zn, Cu, Lathanoide und Cd. Die Weiterentwicklung der Liganden und die bis dahin effektivsten Systeme wurden in verschiedenen Übersichtsartikeln beschrieben. 24, 31, 49, 80, Zu den bisher aktivsten Katalysatoren zählen die Zinkphenoxide die von Darensbourg et al. 89, 90 entwickelt wurden, die -Diketiminatokomplexe die von Coats et al. 91, 92 sowie die Salen-Katalysatoren die von diesen beiden und anderen eingeführt wurden Eine weitere Steigerung der Polymerisationsaktivität um mehrere Größenordnungen erreichte die Verankerung von Co-Katalysatoren an den etablierten Salen-Komplexen Durch die Zugabe eines weiteren Monomers können durch Terpolymerisation noch weitere Polycarbonate hergestellt werden, beispielsweise Poly(ester-co-carbonate) durch die Zugabe von organischen Säureanhydriden. 104, 105 Weiterhin lassen sich mit Hilfe von Doppelmetallcyanid-Katalysatoren
29 1 Einleitung Epoxide, Alkohole und CO 2 zu Polyetherpolycarbonat-polyolen umsetzen. Diese sind für die Polyurethanchemie als Polyol Komponenten von großem Interesse (s. Abbildung 1.9). 106 Durch die Verwendung eines mehrfunktionellen Alkohols kann die Funktionalität des Polyetherpolycarbonat-polyols eingestellt werden. Die Firma Bayer entwickelt zur Zeit unter dem 107, 108 Namen Dream Productions eine Produktlinie auf dieser Basis. + + CO 2 Kat. Abbildung 1.9: Herstellung von Polyetherpolycarbonat-polyol aus einem Alkoholstarter, Epoxid und CO Cyclische Carbonate aus CO 2 und Epoxiden Niedermolekulare, cyclische Carbonate wie Ethylencarbonat, Propylencarbonat, Glycerincarbonat und Butylencarbonat sind ungiftig, polar, biologisch abbaubar, besitzen hohe Siedepunkte und einen niedrigen Dampfdruck. 47, 50, Eingesetzt werden sie deshalb vor allem als grüne Lösungsmittel. Anwendung finden sie auch als Reaktivverdünner, Weichmacher und sind Rohstoff für verschiedene Ausgangsstoffe. Verbindungen mit mehr als zwei cyclischen Carbonaten pro Molekül werden unter anderem als Monomere für die isocyanatfreie Polyurethanchemie verwendet. (s. Kapitel ). Bekannt sind lineare und cyclische Carbonate bereits seit Damals wurden verschiedene Alkohole mit Phosgen zu Alkylcarbonaten umgesetzt. 112 Allerdings sind die Hauptprodukte lineare Carbonate; cyclische Carbonate treten nur in geringen Mengen auf. Erst 1943 wurde durch die Umsetzung von Ethylenoxid (R = H) mit CO 2 unter hohen Druck (150 bar) und bei C eine gezielte Synthese cyclischer Carbonate möglich (s. Abbildung 1.10). 113 p(co 2 ); T Kat. Abbildung 1.10: Herstellung von cyclischen Carbonaten aus Epoxiden. Als Katalysatoren kamen zunächst NaOH auf Aktivkohle zum Einsatz, später dann Ammoniumcarbonate, Ammoniumhydroxide 114 dann Magnesium- und Calciumhalogenide. 115 Ab 1956 setzten sich die auch heute noch verwendeten Alkylammonium-, Alkylphosphonium- 16
30 1 Einleitung Halogenide durch. 116 Gleichzeitig wurden auch andere cyclische Carbonate wie Propylencarbonat hergestellt In Abbildung 1.11 ist der Bildungsmechanismus der cyclischen Carbonaten, bei der Verwendung von Metallsalzen als Katalysator, aus Epoxiden mit CO 2 abgebildet. Abbildung 1.11: Bildungsmechanismus der cyclischen Carbonate unter Verwendung von Metallsalzen als Katalysator. 49 M + = Metallion oder Lewissäure, A = Anion oder Nucleophil. Bei der Verwendung von Alkali-, Erdalkalisalzen bzw. Lewissäuren als Katalysator koordiniert das Metallatom an das Epoxid. Dadurch wir die Epoxidbindung geschwächt, so dass das Gegenion nucleophil angreifen kann. Das entstehende Oxoniumion ist reaktiv genug, um ein CO 2 -Molekül anzugreifen. Das entstehende Carbonat kann nun das Gegenion durch einen Ringschluss verdrängen und das cyclische Carbonat bilden. Der Mechanismus für die Alkyammonium- und Alkylphosphoniumhalogenide unterscheidet sich nur geringfügig. Die Oniumionen koordinieren nicht zum Sauerstoffatom des Epoxids, dafür sind die Halogenidgegenionen nucleophiler und gleichen so die fehlende Aktivierung durch die Lewissäure aus. 49 Das Problem bei diesen Katalysatoren sind allerdings die drastischen Bedingungen, bei denen die Epoxide mit CO 2 umgesetzt werden müssen. Dafür sind Temperaturen von über 120 C und hohe CO 2 -Drücke über 10 bar erforderlich, um gute Aktivitäten zu erhalten. 120 Eine erste deutliche Verbesserung konnte durch die Zugabe von Kronenether erreicht werden. Rockiki et al. fanden dabei heraus, dass Nucleophile der Anionen durch den Kronen-Ether gesteigert werden konnten. 121 Allerdings führt die Kombination von Lewissäure und Oniumhalogeniden zu einer 17
31 1 Einleitung noch deutlicheren Steigerung der Aktivität. So zeigen Kombinationen von Zinkhalogeniden mit Ph 4 PI, 122 Zinnhalogenide mit DMAP 123 sowie ein NiCl 2 /PPh 3 -Katalysatorsystem mit tetra-butylammoniumbromid als Cokatalysator 124, 125 die höchsten Aktivitäten. Ebenfalls sehr gut geeignet sind maßgeschneiderte Salen-Katalysatoren, wie sie auch schon für die Polycarbonatsynthese verwendet wurden. Mit Cr-, Co-, Al-Salen-Katalysatoren wurden bei Raumtemperatur und 6 bar bei der Synthese von Propylencarbonat aus Propylenoxid vollständige Umsätze erreicht. Außerdem ist es mit ihnen möglich enantiomerenreine, cyclische Carbonate herzustellen. 126 Im Gegensatz zu den ionischen Katalysatoren wird bei den Salen-Katalysatoren wie bei der Copolymeristion von Epoxiden mit CO 2 ein Insertionsmechanismus diskutiert. Ein Nachteil dieser homogenen Katalysatoren ist, dass sie aus dem Produkt aufwendig abgetrennt werden müssen. Vor allem die Metall-Salen und Zinnhaltigen Katalysatoren sind giftig und dürfen nicht im Produkt enthalten sein. Aus diesem Grund wurden von verschiedenen Gruppen die katalytisch-aktiven Substanzen auf Feststoffoberflächen geträgert Dabei zeigte es sich, dass die Anwesenheit von Hydroxygruppen auf der Oberfläche die Reaktionsgeschwindigkeit deutlich erhöht. 137 In Abbildung 1.12 ist ein möglicher Mechanismus wiedergegeben. Abbildung 1.12: Festphasen unterstützter Bildungsmechanismus von cyclischen Carbonaten. K + = Kation, A - = Anion. 18
32 1 Einleitung Analog zu dem Bildungsmechanismus der cyclischen Carbonate in Anwesenheit von Lewissäuren (Abbildung 1.11) koordiniert auch hier im ersten Schritt das Epoxid zur Lewissäure. Dadurch wird die C-O-C Bindung geschwächt und das Nucleophil kann leichter angreifen. Im nächsten Schritt wird diskutiert ob das CO 2 -Molekül zunächst auf der Oberfläche durch die Hydroxygruppen gebunden und analog zum Epoxid aktiviert wird. Die Aktivierung und die Koordination in die Nähe des Alkoholats würden eine schnellere Reaktion zum Carbonat zur 127, 128, Folge haben. Als Feststoffe eigenen sich vor allem Siliziumoxidverbindungen mit großer Oberfläche. Die Gruppe um Motakura verwendete beispielweise ein Aerosil 300, ein SiO 2 mit einer spezifischen Oberfläche von 300 m 2 /g. Durch Funktionalisierung der Hydroxygruppen mit 3-Iodopropyltrimethoxysilan und anschließender Umsetzung mit tertiären Aminen konnten sie verschiedene Ammoniumhalogenide herstellen. Bei CO 2 -Umgebungsdruck und 100 C erreichten sie mit Propylenoxid, Styroloxid, Epichlorhydrin und verschiedenen anderen endständigen Epoxiden nach 20.5 h nahezu vollständige Umsätze. 127 Im Vergleich zu den homogenen Analoga wurde bei den geträgerten Katalysatoren eine deutlich höhere Aktivität gemessen. Die bisher besprochenen Umsetzungen von Epoxiden mit CO 2 zu cyclischen Carbonaten bezogen sich alle auf Ethylenoxid und endständige Epoxide an kleine Moleküle wie Propylenoxid und Styroloxid. Bei einigen Veröffentlichungen wurde auch die Umsetzung des sterisch anspruchsvolleren Cyclohexenoxid mit CO 2 untersucht. Dabei stellte sich für alle Katalysatorenarten heraus, dass Cyclohexenoxid wesentlich weniger reaktiv ist als Ethylenoxid 129, 133, und endständigen Epoxide. Für die Herstellung von linearen und vernetzten Systemen ist es notwendig, Monomere mit 2 cyclischen Carbonaten pro Molekül zu besitzen. Bei Verbindungen mit endständigen Epoxiden wie Poly(glycidylmethacrylat) wurden dabei keine Reaktivitätsunterschiede festgestellt Herstellung von cyclischen Carbonaten auf Basis von nachwachsenden Rohstoffen Vor allem die Herstellung von Sojabohnenölcarbonat aus epoxidiertem Sojabohnenöl wurde von einigen Gruppen untersucht. 144 Dabei muss beachtet werden, dass epoxidierte Pflanzenölen keine endständigen Epoxide tragen. Javni et al. verwendeten tetra-butylammoniumbromid (TBAB) als Katalysator und stellten bei 56.5 MPa CO 2 -Druck und 140 C eine nahezu vollständige 19
33 1 Einleitung Konversion der Epoxide nach 24 h fest. Weiterhin konstatierten sie, dass bei CO 2 -Umgebungsdruck und 140 C selbst nach 140 h kein vollständiger Umsatz zu erreichen ist. 145 Die Verwendung von überkritischem CO 2 sowie die Verwendung von SnCl 4 als Co- Katalysator führte zu keiner signifikanten Verkürzung der Reaktionszeit. 146, 147 Von Boyer et al. wurden zudem auf Basis von Fettsäureestern und Metathesereaktionen endständige Doppelbindungen erzeugt, epoxidiert und zu endständigen cyclischen Carbonaten umgesetzt. Sie konnten mit TBAB als Katalysator bei 10 bar CO 2 -Druck, 120 C nach 100 min einen vollständigen Umsatz der Epoxide nachweisen Reaktionsmöglichkeiten von fünf gliedrigen, cyclischen Carbonaten Cyclische Carbonate können mit Nucleophilen auf zwei Arten reagieren. Harte Nucleophile wie aliphatische Amine und Alkohole reagieren mit dem Carbonyl Sauerstoff und öffnen den Ring. Weiche Nucleophile wie Anilin, Phenol und Carboxylate greifen an den Alkylen-Kohlenstoffatomen an. Beachten muss man allerdings, dass abhängig vom harten Nucleophil ab 90 C ebenfalls eine Alkylierung auftreten kann. Ab 150 C finden dann 50, 149 ausschließlich die Alkylierungsreaktionen statt (s. Abbildung 1.13). Alkylierung Ringöffnung - CO 2 Weiches Nu z.b. Aromatische Amine Phenole Carboxylate Hartes Nu 90 C Aliphatische Amine, Alkohole - CO 2 Nu C Abbildung 1.13: Reaktionsmöglichkeiten von cyclischen Carbonaten mit Nucleophilen. Aufgrund dieser beiden Reaktionsmöglichkeiten ergibt sich für die Reaktion von Nuclophilen mit cyclischen Carbonaten eine große Vielfalt an Reaktionsprodukten. In Abbildung 1.14 ist eine Auswahl an Reaktionsmöglichkeiten für Alkohole und Amine wiedergegeben. 20
34 1 Einleitung H + kationische bzw. anionische Polymerisation - H 2 O H 2 O Abbildung 1.14: Übersicht über die Reaktionsprodukte bei der Reaktion von cyclischen Carbonaten mit Alkoholen und Aminen. 50 R 1 = Alkyl- oder H, R 2 = Alkyl oder H, R 3 = Alkyl, R 4 = Alkyl, R 5 = Aryl oder Alkyl wenn T > 140 C, R 6 = H oder Alkyl, R 7 = Alkyl. Cyclische Carbonate können mit aliphatischen Alkoholen umgeestert werden. Dies kann ausgenutzt werden um größere cyclische Carbonate (Ringgröße > 6 Atome) und lineare Carbonate wie Dimethylcarbonat herzustellen. 153 Mit Diolen und Ethylen- bzw. Propylencarbonat ist auf diese Weise die Herstellung von Polycarbonaten möglich. 46, 111, Mit aromatischen Alkoholen, Aminen, Thiolen oder mit aliphatischen Alkoholen oberhalb 140 C findet unter CO 2 -Freisetzung eine Alkylierung des Alkohols statt. 48, 50, 157, 158 Ethylen- oder Propylencarbonat werden so als Kettenverlängerer für aromatische Alkohole verwendet, da PC und EC im Gegensatz zu Ethylenoxid und Propylenoxid nur einmal mit den phenolischen Hydroxygruppen reagieren und dabei kein unkontrolliertes Kettenwachstum zu beobachten ist. 159 Carboxylate reagieren mit cyclischen Carbonaten unter CO 2 -Abspaltung zu Estern. Die dabei entstehende 21
35 1 Einleitung 160, 161 Hydroxygruppe kann für weitere Funktionalisierungen genutzt werden. Mit primären Aminen reagieren cyclische Carbonate bis 90 C ausschließlich unter Ringöffnung zu Urethanen. Weil dabei in β-position eine Hydroxygruppe entsteht spricht man hier von 162, 163 β-hydroxy-urethanen. Bei höheren Temperaturen findet unter CO 2 -Freisetzung eine Alkylierung der Amine statt. 48 Die β-hydroxy-urethane können bei höheren Temperaturen >200 C mit primären Aminen zu Harnstoffen weiterreagieren. 164 Ab Temperaturen von 150 C können β-hydroxy-urethane (wenn R 6 = H) unter Wasserfreisetzung zu Oxazolidonen und mit einem weiteren Äquivalent primärer Amine schließlich über 165, 166 Hydroxy-Harnstoff (nicht abgebildet) zu Imidazolidinonen reagieren. Die anionische bzw. kationische Ringöffnende Polymerisation von 5-gliedrigen, cyclischen Carbonaten führt neben Polycarbonat auch zu Polyethergruppen im Polymer. Erklärbar ist dies durch die geringe Ringspannung und die positive Entropie durch die Polymerisation. Dadurch wird die Reaktionsenthalpie mit zunehmender Kettenlänge positiv. Hinzu kommt eine niedrige Ceiling-Temperatur, die beispielsweise bei Ethylencarbonat nur 25 C beträgt. Trotzdem ist es möglich cyclische Carbonate bei Temperaturen >100 C zu polymerisieren, da es während der Polymerisation zu einer Alkylierung unter CO 2 -Freisetzung kommt. Die Bildung des Polyethers ist dadurch thermodynamisch und entropisch begünstigt, so dass hohe Molekulargewichte erreicht werden können Isocyanatfreie Polyurethane 1937 entdeckte Otto Bayer, dass die Polyaddtionsreaktion von Isocyanaten mit Polyolen zur Bildung von Polyurethanen führt (s. Abbildung 1.15). 171, 172 Die Einführung von Polyesterpolyolen und Polyetherpolyolen als Vernetzer und die Entwicklung von Treibmitteln erweiterte in den 50er Jahren das Anwendungsspektrum und führte somit zu einer erhöhten Nachfrage an Polyurethanen. Die Hauptanwendungsgebiete von Polyurethanen sind Dämm- und Fugenmaterial, Polsterschaumstoffe, Lacke, Beschichtungen, Klebstoffe wurden weltweit mehr als 12 Mio. t Polyurethane verbraucht. 173 Trotz der vielseitigen Anwendbarkeit und leichten Herstellbarkeit hat diese Art der Herstellung von Polyurethanen mehrere Nachteile. Dies sind zum einen die toxische Syntheseroute, ihre Giftigkeit und die Wasserempfindlichkeit der Isocyanate. Isocyanate werden großtechnisch durch die Umsetzung von primären Aminen mit Phosgen hergestellt. Phosgen ist ein sehr giftiges Gas und wurde unter anderem im Ersten 22
36 1 Einleitung Weltkrieg als Giftgas eingesetzt, 174 daher darf es nur unter speziellen Sicherheitsvorkehrungen industriell genutzt werden. Die Isocyanate sind ebenfalls giftig und reagieren mir Wasser zu Carbamidsäuren, die unter CO 2 -Abgabe zu Aminen zerfallen. Dies macht eine trockene Lagerung notwendig. Zudem müssen die Reaktionspartner (Polyole, Füllstoffe, Additive) ebenfalls wasserfrei sein, da es sonst durch die CO 2 -Freisetzung zu einer ungewollten Blasenbildung kommt. Weiterhin ist bekannt, dass es bei der Bildung von Polyurethanen aus Polyolen und Isocyanaten auch zu einer Ausbildung von thermischinstabilen Allophanat-Einheiten kommen kann. Amin Phosgen Isocyanat Polyol - HCl + + Allophanat Polyurethan Abbildung 1.15: Herstellung von Isocyanaten und Weiterreaktion mit Polyolen zu Polyurethanen. Mögliche Nebenreaktion der Urethane mit Isocyanaten zu Allophanaten. Alternativ können auch, wie bereits in Kapitel vorgestellt, cyclische Carbonate mit Aminen zu Hydroxy-Urethanen umgesetzt werden. Die Hydroxy-Urethane von Figosky NIPUs für Non-Isocyanat-Polyurethane genannt, haben viele Vorteile gegenüber den Isocyanat basierten Systemen. Die Ausgangstoffe sind wasserunempfindlich und weniger giftig wie die Isocyanate, weiterhin finden bei der Härtung keine Nebenreaktionen statt. Aufgrund ihrer Hydroxygruppen in -Stellung zur Urethaneinheit sind sie in der Lage Wasserstoffbrückenbindungen innerhalb der Matrix auszubilden (s. Abbildung 1.16). 175 führt im Vergleich zu Polyurethanen zu einer höheren mechanischen Belastbarkeit und zu einer wesentlich besseren Resistenz gegenüber organischen Lösungsmitteln Dies Darüber hinaus erreichen NIPUs aufgrund des Fehlens von Allophanateinheiten Zersetzungstemperaturen bis zu 388 C. 177, 178 Diese Eigenschaften machen NIPUs für viele Anwendungen interessant. Im Besonderen werden sie als chemikalienbeständige Beschichtungen, Lacke und Schäume 179, 180 verwendet.
37 1 Einleitung + Abbildung 1.16: Ausbildung von Wasserstoffbrückenbindungen innerhalb der NIPU-Matrix. Von verschiedenen Gruppen wurde die Geschwindigkeit der Reaktion von cyclischen Carbonaten und Aminen untersucht. Die Gruppe um H. Tomita fand beispielsweise heraus, dass 5-gliedrige Carbonate im Vergleich zu 6-gliedrigen und 7-gliedrigen Carbonaten wesentlich langsamer reagieren. Dies liegt an der um 2.86 kcal/mol bei 6-gliedrigen und der um 5.64 kcal/mol höheren Ringspannung bei 7-gliedrigen 181 cyclischen Carbonaten. Ebenfalls konnten sie zeigen, das seine elektronenziehende Gruppe in -Methylenposition zu einem 5-gliedrigen cyclischen Carbonat einen beschleunigenden Effekt auf die NIPU-Bildung hat. 182 Weiterhin wurde festgestellt, dass der Aufbau und die Art des Amin-Härters einen deutlichen Einfluss auf die Reaktionsgeschwindigkeit hat. So nimmt die Reaktivität der aliphatischen Amine mit Substituenten in -Position weniger ab als in -Position zur Aminfunktion. 183 Auch wurde von verschiedenen Arbeitsgruppen gezeigt, dass primäre Amine mit 5-gliedrigen cyclischen Carbonaten deutliche schneller reagieren als sekundäre Amine Zusätzlich konnten Ochiai et al. zeigen, dass in Anwesenheit von primären und sekundären Aminogruppen die cyclischen Carbonate ausschließlich mit den primären Aminen reagieren. 184 Erklärbar ist dies mit dem Bildungsmechanismus der NIPUs (s. Abbildung 1.17) H + Abbildung 1.17: Bildungsmechanismus von isocyanatfreien Polyurethanen aus cyclischen Carbonaten und 188, 189 Aminen. 24
38 1 Einleitung Die Bildung von NIPUs ist eine 3-stufige Reaktion, die aus mehreren Gleichgewichten besteht. In der ersten Stufe wird das cyclische Carbonat vom Amin nucleophil angegriffen. Dabei entsteht eine Tetraederzwischenstufe. Die Lage des Gleichgewichts der Bildung der Tetraeder- Zwischenstufe ist abhängig von der Geometrie und der Art des Amins. Sterische Hinderungen ( -, -Substituent oder sekundäres Amin) verschieben das Gleichgewicht auf Eduktseite. Im nächsten Schritt wird durch ein weiteres Amin die Tetraederzwischenstufe deprotoniert und 188, 189 reagiert schließlich nach der Reprotonierung zum Hydroxy-Urethan weiter. Die bisher hergestellten NIPUs können in lineare und vernetzte Systeme unterschieden werden. Bei der Herstellung von linearen NIPUs eignen sich am besten bis-cyclo-carbonate und lineare Diamine. Als Lösungsmittel werden in aller Regel hochsiedende, aprotische Substanzen wie DMF, DMSO, DMAc oder auch Toluol verwendet. 190 In aller Regel werden bei NIPUs aus 5-gliedrigen, cyclischen Carbonaten nicht so hohe Molmassen erreicht wie mit Isocyanaten und Polyolen. Dies liegt vor allem an der größeren Reaktivität von Isocyanaten. Es wurde festgestellt, dass die Molmasse der NIPUs sehr von der Struktur des verwendeten Diamins abhängt. Die bisher höchsten erreichbaren Molmassen zwischen g/mol wurden dabei mit den linearen Diaminen Hexamethylendiamin bzw. Diaminododecan und verschiedenen auf Bisglycidylethern basierenden cyclischen Carbonaten erreicht. 191 Aufgrund der niedrigen Molmasse und den steuerbaren funktionellen Gruppen werden lineare NIPUs als Vernetzer oder Präpolymere für Beschichtungen oder Lacke verwendet. 192, 193 Die verschiedenen funktionellen Gruppen Amine, cyclische Carbonate und Hydroxygruppen können für weitere Reaktionen genutzt werden Seit langem ist auch die Verwendung von cyclischen Carbonaten als Reaktivverdünner und Schlagzähmodifikatoren in der Epoxidchemie bekannt. Da primäre Amine nur mit cyclischen Carbonaten und sekundäre Amine mit Epoxiden reagieren, eigenen sich Ethylenimine (Triethylenetetraamin (TETA) und Diethylenetriamine (DETA)) als Härter für solche Systeme. 197 Dabei können durch ein Temperaturprogramm gesteuert, zuerst die cyclischen Carbonate und anschließend, bei höheren Temperaturen, die Epoxide mit den Aminen umgesetzt werden Weiterhin ist es auch möglich aus Verbindungen, die mehr als zwei cyclische Carbonate pro 175, 176, 180, 201, 202 Molekül besitzen und polyfunktionellen Aminen NIPU-Netzwerke herzustellen. Unterschiedliche Synthesestrategien erlauben die Herstellung von Verbindungen mit polyfunktionellen cyclischen Carbonaten. 25
39 1 Einleitung 1) Vinylethylen Carbonate (VEC), Propylencarbonatacrylat (PAC) und Propylencarbonaten methacrylat (PCMA) können mit sich selbst oder mit anderen Vinylester Copolymersiert werden ) Aus polyfunktionellen Alkoholen (z.b. Trimethylolpropantricarbonat) lassen sich mit Epichlorhydrin Gylcidylether herstellen und anschließend mit CO 2 zu polyfunktionelle, cyclischen Carbonaten umsetzen (Trimethylolpropantricarbonat TMP-TC). 50 3) Mehrfachungesättigte Verbindungen können epoxidiert und anschließend mit CO 2 zu 144, 203 polyfunktionellen, cyclischen Carbonaten umgesetzt werden. VEC PAC PCMA TMP-TC Abbildung 1.18: Polymerisierbare cyclische Carbonate Vinylethylencarbonat (VEC), Propylencarbonatacrylat (PAC), Propylencarbonatmethacrylat (PCMA) und Trimethylolpropantricarbonat (TMP-TC). Figovsky et al. fanden allerdings heraus, dass bei einem unvollständiger Umsatz der Epoxide zu cyclischen Carbonaten bessere mechanische Eigenschaften und eine bessere Verabeitbarkeit zu erreichen sind. Mit seinen Hybrid-NIPUs (HNIPU) kann die unterschiedliche Reaktivität von Epoxiden und cyclischen Carbonaten mit Aminen ausgenutzt werden. So ist es beispielsweise möglich mit aromatischen Aminen die Epoxide zu härten und anschließend mit aliphatischen primären Aminen die cyclischen Carbonate umzusetzen. Außerdem ist mit Aminen, die primäre und sekundäre Aminogruppen tragen (TETA, DETA) eine temperaturgesteurte, getrennte Härtung von cyclischen Carbonaten und Epoxiden möglich. 204 Aufgrund ihrer Chemikalienbeständigkeit, Temperaturbeständigkeit und Unempfindlichkeit gegenüber Feuchtigkeit sind NIPUs hervorragend als Beschichtungen, Farben und Lacke für anspruchsvolle Umwelbedingungen geeignet. 26
40 1 Einleitung Isocyanatfreie Polyurethane auf Basis nachwachsender Rohstoffe Durch die Kombination von nachwachsenden Rohstoffen in Verbindung mit der chemischen Fixierung von CO 2 ist es möglich Kunststoffe mit einer optimalen Ökobilanz zu schaffen. Zudem gelingt es mit der isocyanatfreien Polyurethanchemie Kunststoffe ohne toxische Reaktionspartner herzustellen. Im Jahr 2004 ist es der Gruppe um G.L. Wilkes gelungen aus Sojabohnenölcarbonat 144, 205 (CSBO) isocyanatfreie Polyurethan-Gießharze herzustellen (s. Abbildung 1.19). Sie härteten das CSBO mit Ethylendiamin, Hexamethylendiamin und Tris(2-aminoethyl)amin. Allerdings verwendeten sie CSBO mit einem geringen Carbonatgehalt. Die daraus hergestellten NIPUs wiesen nur geringe Zugfestigkeiten (max. 1.5 MPa) auf. Erst ein vollständiger Umsatz der Epoxide zu cyclischen Carbonaten durch Javni et al. führte zu NIPUs mit Zugfestigkeiten von 145, 146, 197 maximal 6 MPa bei einer Bruchdehnung von 90%. Abbildung 1.19: Herstellung von NIPU-Gießharzen aus Sojabohnenölcarbonat und Diamin. 144 Lineare NIPUs wurden von Boyer et al. hergestellt. Sie setzten Fettsäureesternbiscarbonate mit Ethylendiamin und Isophorondiamin (IPDA) zu linearen NIPUs um. Dabei wurde mit IPDA ein maximales Molekulargewicht bis g/mol erreicht. 27
Weniger CO 2 dem Klima zuliebe Lehrerinformation
 Lehrerinformation 1/8 Arbeitsauftrag Der CO 2- Kreislauf wird behandelt und die Beeinflussung des Menschen erarbeitet. Die Schülerberichte (Aufgabe 3) dienen als Grundlage zur Diskussion im Plenum. Ziel
Lehrerinformation 1/8 Arbeitsauftrag Der CO 2- Kreislauf wird behandelt und die Beeinflussung des Menschen erarbeitet. Die Schülerberichte (Aufgabe 3) dienen als Grundlage zur Diskussion im Plenum. Ziel
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt: Organische Chemie II. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Erneuerbare statt fossile Rohstoffe
 Erneuerbare statt fossile Rohstoffe Zollikofen 5. Februar 2016 Christian Suter, suterscience GmbH christian.suter@suterscience.com Es werden Ergebnisse der SATW-Studie Erneuerbare statt fossile Rohstoffe
Erneuerbare statt fossile Rohstoffe Zollikofen 5. Februar 2016 Christian Suter, suterscience GmbH christian.suter@suterscience.com Es werden Ergebnisse der SATW-Studie Erneuerbare statt fossile Rohstoffe
Stoffplan GLF Chemie 4Mb
 Organische Chemie Stoffplan GLF Chemie 4Mb Theorie: Organische Chemie: -Kohlenwasserstoffe -Aromatische Kohlenwasserstoffe: z.b. Benzol -Organische Sauerstoffverbindungen: z.b. Ethanol -Von der Organik
Organische Chemie Stoffplan GLF Chemie 4Mb Theorie: Organische Chemie: -Kohlenwasserstoffe -Aromatische Kohlenwasserstoffe: z.b. Benzol -Organische Sauerstoffverbindungen: z.b. Ethanol -Von der Organik
BIOFOLIEN BIOMATERIALIEN TRENDS. Jan SWITTEN 2014
 BIOFOLIEN BIOMATERIALIEN TRENDS Jan SWITTEN 2014 1 Was sind Biokunststoffe Definition European Bioplastics Kunststoffe entstanden aus nachwachsenden Rohstoffen oder Abbaubare oder kompostierbare Kunststoffe
BIOFOLIEN BIOMATERIALIEN TRENDS Jan SWITTEN 2014 1 Was sind Biokunststoffe Definition European Bioplastics Kunststoffe entstanden aus nachwachsenden Rohstoffen oder Abbaubare oder kompostierbare Kunststoffe
Leseprobe. Georg Abts. Kunststoff-Wissen für Einsteiger ISBN: Weitere Informationen oder Bestellungen unter
 Leseprobe Georg Abts Kunststoff-Wissen für Einsteiger ISBN: 978-3-446-42009-0 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-42009-0 sowie im Buchhandel. Carl Hanser Verlag,
Leseprobe Georg Abts Kunststoff-Wissen für Einsteiger ISBN: 978-3-446-42009-0 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-42009-0 sowie im Buchhandel. Carl Hanser Verlag,
Einführung in die CO 2 -Nutzung
 Einführung in die CO 2 -Nutzung Niklas von der Assen Arbeitsgruppe Energiesystemtechnik Lehrstuhl für Technische Thermodynamik RWTH Aachen University, Nachbarschaftsforum Niederaußem Lehrstuhl für Technische
Einführung in die CO 2 -Nutzung Niklas von der Assen Arbeitsgruppe Energiesystemtechnik Lehrstuhl für Technische Thermodynamik RWTH Aachen University, Nachbarschaftsforum Niederaußem Lehrstuhl für Technische
FRAUNHOFER-INSTITUT FÜR. Produkte aus nachwachsenden Rohstoffen
 FRAUNHOFER-INSTITUT FÜR Chemische Technologie ICT Produkte aus nachwachsenden Rohstoffen Produkte aus nachwachsenden Rohstoffen Vor dem Hintergrund einer rasant wachsenden Weltbevölkerung und knapper werdender
FRAUNHOFER-INSTITUT FÜR Chemische Technologie ICT Produkte aus nachwachsenden Rohstoffen Produkte aus nachwachsenden Rohstoffen Vor dem Hintergrund einer rasant wachsenden Weltbevölkerung und knapper werdender
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Kernlehrpläne ab Schuljahr 2014/15 Schuleigener Lehrplan / FMG / Sekundarstufe II CHEMIE
 CHEMIE QUALIFIKATIONSSPHASE 2 GRUNDKURS Konkretisierung der Unterrichtsvorhaben Unterrichtsvorhaben I: Vom fossilen Rohstoff zum Anwendungsprodukt Sequenzierung inhaltlicher Aspekte Organische Reaktionsabläufe
CHEMIE QUALIFIKATIONSSPHASE 2 GRUNDKURS Konkretisierung der Unterrichtsvorhaben Unterrichtsvorhaben I: Vom fossilen Rohstoff zum Anwendungsprodukt Sequenzierung inhaltlicher Aspekte Organische Reaktionsabläufe
Wald, Holz und Kohlenstoff
 Wald, Holz und Kohlenstoff Dr. Uwe Paar Landesbetrieb HESSEN-FORST Nordwestdeutsche Forstliche Versuchsanstalt Gliederung Bedeutung des Waldes Leistungen nachhaltiger Forstwirtschaft Wie entsteht Holz?
Wald, Holz und Kohlenstoff Dr. Uwe Paar Landesbetrieb HESSEN-FORST Nordwestdeutsche Forstliche Versuchsanstalt Gliederung Bedeutung des Waldes Leistungen nachhaltiger Forstwirtschaft Wie entsteht Holz?
Stoffliche Nutzung nachwachsender Rohstoffe
 Oliver Türk Stoffliche Nutzung nachwachsender Rohstoffe Grundlagen - Werkstoffe - Anwendungen Mit 337 Abbildungen und 128 Tabellen Springer Vieweg Inhaltsverzeichnis Vorwort VII Danksagung IX Abkürzungsverzeichnis
Oliver Türk Stoffliche Nutzung nachwachsender Rohstoffe Grundlagen - Werkstoffe - Anwendungen Mit 337 Abbildungen und 128 Tabellen Springer Vieweg Inhaltsverzeichnis Vorwort VII Danksagung IX Abkürzungsverzeichnis
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 17.11.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 17.11.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Die NawaRo-Entdecker - Nachwachsende Rohstoffe vom Acker und aus dem Wald
 Kompetenzzentrum HessenRohstoffe (HeRo) e.v. Am Sande 20 l 37213 Witzenhausen Station: Die NawaRo-Entdecker - Nachwachsende Rohstoffe vom Acker und aus dem Wald Kontakt: Anja Neubauer (Ansprechpartnerin,
Kompetenzzentrum HessenRohstoffe (HeRo) e.v. Am Sande 20 l 37213 Witzenhausen Station: Die NawaRo-Entdecker - Nachwachsende Rohstoffe vom Acker und aus dem Wald Kontakt: Anja Neubauer (Ansprechpartnerin,
Beispielaufgaben IChO 2. Runde 2019 Säurederivate. H2, Pd/C
 Beispielaufgaben Ih 2. Runde 2019 Säurederivate Beispiel 1 ligocarbonsäuren Gegeben sei folgendes Reaktionsschema: A H2, Pd/ H 2, Lindlar Na/NH 3(l) B D Base E A hat eine molare Masse von 118,09 g mol
Beispielaufgaben Ih 2. Runde 2019 Säurederivate Beispiel 1 ligocarbonsäuren Gegeben sei folgendes Reaktionsschema: A H2, Pd/ H 2, Lindlar Na/NH 3(l) B D Base E A hat eine molare Masse von 118,09 g mol
Kernlehrpläne ab Schuljahr 2014/15 Schuleigener Lehrplan / FMG / Sekundarstufe II CHEMIE
 CHEMIE QUALIFIKATIONSSPHASE 2 LEISTUNGSKURS Konkretisierung der Unterrichtsvorhaben Unterrichtsvorhaben I: Vom fossilen Rohstoff zum Anwendungsprodukt Organische Reaktionsabläufe Oxidationsreihe der Alkohole
CHEMIE QUALIFIKATIONSSPHASE 2 LEISTUNGSKURS Konkretisierung der Unterrichtsvorhaben Unterrichtsvorhaben I: Vom fossilen Rohstoff zum Anwendungsprodukt Organische Reaktionsabläufe Oxidationsreihe der Alkohole
Stundenübersicht über das IHF Organische Produkte Werkstoffe und Farbstoffe
 Stundenübersicht über das IHF Organische Produkte Werkstoffe und Farbstoffe Unterrichtsvorhaben I Inhaltlicher Schwerpunkt Organische Verbindungen und Reaktionswege Kontext Vom fossilen Rohstoff zum Anwendungsprodukt
Stundenübersicht über das IHF Organische Produkte Werkstoffe und Farbstoffe Unterrichtsvorhaben I Inhaltlicher Schwerpunkt Organische Verbindungen und Reaktionswege Kontext Vom fossilen Rohstoff zum Anwendungsprodukt
Elemente des Periodensystems. Natürliche Häufigkeit der Elemente
 Elemente des Periodensystems Natürliche Häufigkeit der Elemente 1 Der Wasserstoff Vorkommen Eigenschaften Gewinnung Verwendung Verbindungen 2 Vorkommen Interstellare Wasserstoffwolken Orion-Nebel und auf
Elemente des Periodensystems Natürliche Häufigkeit der Elemente 1 Der Wasserstoff Vorkommen Eigenschaften Gewinnung Verwendung Verbindungen 2 Vorkommen Interstellare Wasserstoffwolken Orion-Nebel und auf
Chemie für Biologen, Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema ) iii) Carbonsäure iv) Dicarbonsäure
 Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Aldehyde und Ketone Carbonylverbindungen
 Aldehyde und Ketone Carbonylverbindungen Prof. Dr. Ivo C. Ivanov 1 Prof. Dr. Ivo C. Ivanov 2 Die Siedepunkte liegen höher als bei den jeweils zugrundeliegenden Alkanen, eine Folge des polaren Charakters
Aldehyde und Ketone Carbonylverbindungen Prof. Dr. Ivo C. Ivanov 1 Prof. Dr. Ivo C. Ivanov 2 Die Siedepunkte liegen höher als bei den jeweils zugrundeliegenden Alkanen, eine Folge des polaren Charakters
O H H 3 C. Methanol. Molekulargewicht Siedepunkt Löslichkeit in Wasser H 3 C-OH. unbegrenzt H 3 C-Cl. 7.4 g/l H 3 C-CH 3 -24/C -88/C
 Struktur und Eigenschaften 3 C 3 C C 3 105 109 112 Wasser Methanol Dimethylether Vektoraddition der einzelnen Dipolmomente eines Moleküls zum Gesamtdipolmoment Anmerkung zu aktuellen Ereignissen: itrofen
Struktur und Eigenschaften 3 C 3 C C 3 105 109 112 Wasser Methanol Dimethylether Vektoraddition der einzelnen Dipolmomente eines Moleküls zum Gesamtdipolmoment Anmerkung zu aktuellen Ereignissen: itrofen
Stoffliche Nutzung von Biomasse in der chemischen Industrie Perspektiven für Biomethan
 3. Dezember 2015 Stoffliche Nutzung von Biomasse in der chemischen Industrie Perspektiven für Biomethan Dr. Jörg Rothermel, DENA Biogaspartner, Berlin, 3. Dezember 2015 Agenda Rohstoffe in der Chemie Biomasse
3. Dezember 2015 Stoffliche Nutzung von Biomasse in der chemischen Industrie Perspektiven für Biomethan Dr. Jörg Rothermel, DENA Biogaspartner, Berlin, 3. Dezember 2015 Agenda Rohstoffe in der Chemie Biomasse
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
A) Bei zweiprotonigen Säuren wird zur vollständigen Neutralisation exakt ein
 1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist richtig? A) Bei zweiprotonigen Säuren wird zur vollständigen Neutralisation exakt ein Äquivalent an Natronlauge
1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist richtig? A) Bei zweiprotonigen Säuren wird zur vollständigen Neutralisation exakt ein Äquivalent an Natronlauge
Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler
 Prof. Dr. J. Christoffers Institut für Organische Chemie Universität Stuttgart 29.04.2003 Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 1. Einführung 2.
Prof. Dr. J. Christoffers Institut für Organische Chemie Universität Stuttgart 29.04.2003 Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 1. Einführung 2.
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Natürlicher Klimawandel
 Klimasystem Das { } der Erde besteht aus verschiedenen Untersystemen, wobei die fünf wichtigsten die Atmosphäre (Luft), die Hydrosphäre (Wasser), die Kryosphäre (Eis), die Biosphäre (Leben) und die Pedosphäre
Klimasystem Das { } der Erde besteht aus verschiedenen Untersystemen, wobei die fünf wichtigsten die Atmosphäre (Luft), die Hydrosphäre (Wasser), die Kryosphäre (Eis), die Biosphäre (Leben) und die Pedosphäre
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 03.02.2016 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 03.02.2016 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 13.02.2017 Die Klausur besteht aus 10 Seiten. Bitte zu den folgenden Aufgaben die jeweils richtige Antwort (A, B, C, D) bzw. den berechneten Wert (ohne Maßeinheit)
Chemisches Praktikum für Biologen Klausur am 13.02.2017 Die Klausur besteht aus 10 Seiten. Bitte zu den folgenden Aufgaben die jeweils richtige Antwort (A, B, C, D) bzw. den berechneten Wert (ohne Maßeinheit)
41. Welches der folgenden Elemente zeigt die geringste Tendenz, Ionen zu bilden?
 41. Welches der folgenden Elemente zeigt die geringste Tendenz, Ionen zu bilden? A) Ca B) C C) F D) Na 42. Steinsalz löst sich in Wasser, A) weil beide Ionen Hydrathüllen bilden können B) es eine Säure
41. Welches der folgenden Elemente zeigt die geringste Tendenz, Ionen zu bilden? A) Ca B) C C) F D) Na 42. Steinsalz löst sich in Wasser, A) weil beide Ionen Hydrathüllen bilden können B) es eine Säure
Elektrophile Additionen von HX an die CC-Doppelbindung (Vollhardt, 3. Aufl., S , 4. Aufl., S ; Hart, S ; Buddrus, S.
 Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
Station 1 Was ist Palmöl?
 Station 1 Was ist Palmöl? Ein Mitglied der Gruppe liest den Text vor, und danach betrachten Sie gemeinsam die Abbildungen und Grafiken. Text Testen Sie nun Ihr Wissen zum Thema Palmöl im Spiel. Würfel,
Station 1 Was ist Palmöl? Ein Mitglied der Gruppe liest den Text vor, und danach betrachten Sie gemeinsam die Abbildungen und Grafiken. Text Testen Sie nun Ihr Wissen zum Thema Palmöl im Spiel. Würfel,
Organostickstoff- Verbindungen
 rganostickstoff- Verbindungen [1] Chiralität von Aminen [2] -Enantiomere Isomerisieren sehr schnell -E A 20-30 KJ/mol [2] Alkylierung von Ammoniak [2] [2] [2] -geringe Selektivität aufgrund von Mehrfachalkylierung
rganostickstoff- Verbindungen [1] Chiralität von Aminen [2] -Enantiomere Isomerisieren sehr schnell -E A 20-30 KJ/mol [2] Alkylierung von Ammoniak [2] [2] [2] -geringe Selektivität aufgrund von Mehrfachalkylierung
im Molekül eine Dreifachbindung (eine σ-bindung,
 1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
Welt der Chemie Feuerwerk 178 Selbst untersucht Eigenschaften von Alkali- und Erdalkalimetallen 179 Natrium 180
 Inhalt Alkali- und Erdalkalimetalle 177 Welt der Chemie Feuerwerk 178 Selbst untersucht Eigenschaften von Alkali- und Erdalkalimetallen 179 Natrium 180 Die Elemente der I. Hauptgruppe 182 Magnesium und
Inhalt Alkali- und Erdalkalimetalle 177 Welt der Chemie Feuerwerk 178 Selbst untersucht Eigenschaften von Alkali- und Erdalkalimetallen 179 Natrium 180 Die Elemente der I. Hauptgruppe 182 Magnesium und
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)
 Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)... interpretieren den zeitlichen Ablauf chemischer Reaktionen in Abhängigkeit von verschiedenen Parametern (u.a. Oberfläche, Konzentration, Temperatur)
Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)... interpretieren den zeitlichen Ablauf chemischer Reaktionen in Abhängigkeit von verschiedenen Parametern (u.a. Oberfläche, Konzentration, Temperatur)
Der Treibhauseffekt. Tabelle 1: Übersicht der wichtigsten Charakteristika der "Treibhausgase"
 Der Treibhauseffekt Ein wichtiger Begriff, der immer wieder im Zusammenhang mit den Klimaänderungen auftaucht, ist der Treibhauseffekt. Durch diesen Vorgang wird die Erdatmosphäre ähnlich wie die Luft
Der Treibhauseffekt Ein wichtiger Begriff, der immer wieder im Zusammenhang mit den Klimaänderungen auftaucht, ist der Treibhauseffekt. Durch diesen Vorgang wird die Erdatmosphäre ähnlich wie die Luft
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
V1 Wunderwasser (Hydrophobierung eines Gasbetonsteins)
 V1 Wunderwasser (Hydrophobierung eines Gasbetonsteins) Thema: Animation Kontexte / Anwendungen Hydrophobierung Dipol-Wechselwirkungen > Lerntools > Hydrophobierung (Wechselwirkungen, Wasser als Dipol,
V1 Wunderwasser (Hydrophobierung eines Gasbetonsteins) Thema: Animation Kontexte / Anwendungen Hydrophobierung Dipol-Wechselwirkungen > Lerntools > Hydrophobierung (Wechselwirkungen, Wasser als Dipol,
SUCHE NACH DER PERFEKTEN LÖSUNG
 aquatak SUCHE NACH DER PERFEKTEN LÖSUNG Die Säntis Analytical AG bietet seit 1999 im Bereich der Verbrauchsmaterialien für die Analytik, von der Idee, über die Entwicklung bis zur serienreifen Produktion,
aquatak SUCHE NACH DER PERFEKTEN LÖSUNG Die Säntis Analytical AG bietet seit 1999 im Bereich der Verbrauchsmaterialien für die Analytik, von der Idee, über die Entwicklung bis zur serienreifen Produktion,
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Das Energiebilanzmodell MSCM
 Das Energiebilanzmodell MSCM Ein Energiebilanzmodell, wie das MSCM eines ist, betrachtet die Energieflüsse im Erdsystem. Daraus berechnet es die Differenz der von der Sonne eingestrahlten Energie und der
Das Energiebilanzmodell MSCM Ein Energiebilanzmodell, wie das MSCM eines ist, betrachtet die Energieflüsse im Erdsystem. Daraus berechnet es die Differenz der von der Sonne eingestrahlten Energie und der
Katalyse. Martin Babilon 14/07/2011. Katalyse. Martin Babilon Universität Paderborn. 14 Juli Montag, 18. Juli 2011
 Katalyse Universität Paderborn 14 Juli 2011 1 Übersicht Motivation & Einleitung Katalyse-Zyklus homogene Katalyse heterogene Katalyse 2 Motivation 3 Geschichte der Katalyse 6000 v. Christus: Alkoholvergärung
Katalyse Universität Paderborn 14 Juli 2011 1 Übersicht Motivation & Einleitung Katalyse-Zyklus homogene Katalyse heterogene Katalyse 2 Motivation 3 Geschichte der Katalyse 6000 v. Christus: Alkoholvergärung
Biogas Lehrerinformation
 Lehrerinformation 1/5 Arbeitsauftrag Die Sch betrachten den -Prozess und erkennen die Gemeinsamkeiten. Ziel Die Sch erklären den Prozess zur Gewinnung von Material Lösungen Sozialform EA Zeit 20 Zusätzliche
Lehrerinformation 1/5 Arbeitsauftrag Die Sch betrachten den -Prozess und erkennen die Gemeinsamkeiten. Ziel Die Sch erklären den Prozess zur Gewinnung von Material Lösungen Sozialform EA Zeit 20 Zusätzliche
Je nach der Zusammensetzung vom Bioabfall werden zwischen 105 bis 130 m 3 Biogas pro Tonne gewonnen.
 Lehrerinformation 1/5 Arbeitsauftrag Die Sch betrachten den -Prozess und erkennen die Gemeinsamkeiten. Ziel Die Sch erklären den Prozess zur Gewinnung von. Material Lösungen Sozialform EA Zeit 20 Zusätzliche
Lehrerinformation 1/5 Arbeitsauftrag Die Sch betrachten den -Prozess und erkennen die Gemeinsamkeiten. Ziel Die Sch erklären den Prozess zur Gewinnung von. Material Lösungen Sozialform EA Zeit 20 Zusätzliche
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Die Welt der Kohlenstoffverbindungen - Eine Einführung (PDF- Datei)
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die Welt der Kohlenstoffverbindungen - Eine Einführung (PDF- Datei) Das komplette Material finden Sie hier: School-Scout.de VII/A
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die Welt der Kohlenstoffverbindungen - Eine Einführung (PDF- Datei) Das komplette Material finden Sie hier: School-Scout.de VII/A
Uni Konstanz - Kristallinität als Schlüsselfunktion
 Powered by Seiten-Adresse: https://www.gesundheitsindustriebw.de/de/fachbeitrag/aktuell/uni-konstanz-kristallinitaetals-schluesselfunktion/ Uni Konstanz - Kristallinität als Schlüsselfunktion Nachwachsende
Powered by Seiten-Adresse: https://www.gesundheitsindustriebw.de/de/fachbeitrag/aktuell/uni-konstanz-kristallinitaetals-schluesselfunktion/ Uni Konstanz - Kristallinität als Schlüsselfunktion Nachwachsende
Grundlagen der Chemie Lösungen Prof. Annie Powell
 Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Welcher Indikator ist für die Titration von Essigsäure (pks =4.76) mit Natronlauge am besten geeignet?
 1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist falsch? A) Säuren erhöhen durch Abgabe eines Protons an Wasser die H3O + -Konzentration einer Lösung. B)
1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist falsch? A) Säuren erhöhen durch Abgabe eines Protons an Wasser die H3O + -Konzentration einer Lösung. B)
Nutzung von CO 2 in fossilen Energieumwandlungskreisläufen 13. Brandenburger Energietag. K. Büker Cottbus, 15. September 2011
 Nutzung von CO 2 in fossilen Energieumwandlungskreisläufen 13. Brandenburger Energietag K. Büker Cottbus, 15. September 2011 2 Mehr als 2.000 von Uhde gebaute Anlagen auf allen Kontinenten. Düngemittel
Nutzung von CO 2 in fossilen Energieumwandlungskreisläufen 13. Brandenburger Energietag K. Büker Cottbus, 15. September 2011 2 Mehr als 2.000 von Uhde gebaute Anlagen auf allen Kontinenten. Düngemittel
Übungsaufgaben Chemie Nr. 3
 Übungsaufgaben Chemie Nr. 3 22) Wie hoch ist die Molarität der jeweiligen Lösungen, wenn die angegebene Substanzmenge in Wasser gelöst und auf 200 ml aufgefüllt wurde? a) 58.44g NaCl (Kochsalz) b) 100
Übungsaufgaben Chemie Nr. 3 22) Wie hoch ist die Molarität der jeweiligen Lösungen, wenn die angegebene Substanzmenge in Wasser gelöst und auf 200 ml aufgefüllt wurde? a) 58.44g NaCl (Kochsalz) b) 100
Kohlendioxid als Ressource
 Kohlendioxid als Ressource Vom Abfall zum Rohstoff Plus-Forschung macht mehr aus Treibhausgas Neue Wege zu einer nachhaltigen Rohstoffversorgung Die Chemische Industrie ist der Zulieferer für eine große
Kohlendioxid als Ressource Vom Abfall zum Rohstoff Plus-Forschung macht mehr aus Treibhausgas Neue Wege zu einer nachhaltigen Rohstoffversorgung Die Chemische Industrie ist der Zulieferer für eine große
Fraunhofer IGB. Chemische Energiespeicher Katalyse und Prozess. Projektgruppe BioCat Straubing Sommersymposium am 27. Juni Dr.
 Fraunhofer IGB Projektgruppe BioCat Straubing Sommersymposium am 27. Juni 2013 Chemische Energiespeicher Katalyse und Prozess Dr. Tobias Gärtner AGENDA 1. Fraunhofer IGB 2. Kompetenzzentrum für nachwachsende
Fraunhofer IGB Projektgruppe BioCat Straubing Sommersymposium am 27. Juni 2013 Chemische Energiespeicher Katalyse und Prozess Dr. Tobias Gärtner AGENDA 1. Fraunhofer IGB 2. Kompetenzzentrum für nachwachsende
Biopolymere - Biowerkstoffe. Biobasierte Polyamide: Bewährte Werkstoffe in einem neuen Licht
 Biopolymere - Biowerkstoffe Biobasierte Polyamide: Bewährte Werkstoffe in einem neuen Licht Dr. Georg Stöppelmann, Research & Development EMS-Chemie AG + 41 81 632 6558 georg.stoeppelmann@emsgrivory.com
Biopolymere - Biowerkstoffe Biobasierte Polyamide: Bewährte Werkstoffe in einem neuen Licht Dr. Georg Stöppelmann, Research & Development EMS-Chemie AG + 41 81 632 6558 georg.stoeppelmann@emsgrivory.com
B E I S P I E L A R B E I T / Aufgaben. Kultusministerium
 B E I S P I E L A R B E I T / Aufgaben Kultusministerium Name, Vorname: Klasse: Schule: Seite 1 von 6 B E I S P I E L A R B E I T / Aufgaben Aufgabe 1: Stoffe und ihre Eigenschaften a) Die Naturwissenschaft
B E I S P I E L A R B E I T / Aufgaben Kultusministerium Name, Vorname: Klasse: Schule: Seite 1 von 6 B E I S P I E L A R B E I T / Aufgaben Aufgabe 1: Stoffe und ihre Eigenschaften a) Die Naturwissenschaft
CO 2 -Abscheidung im Kraftwerksbetrieb
 im Kraftwerksbetrieb im Kraftwerksbetrieb Seite 1/26 Inhalt Einführungsvideo Kohlenstoffdioxid Braunkohlekraftwerk - CO 2 -Verwertung im Kraftwerksbetrieb Seite 2/26 im Kraftwerksbetrieb Seite 3/26 Natürliches
im Kraftwerksbetrieb im Kraftwerksbetrieb Seite 1/26 Inhalt Einführungsvideo Kohlenstoffdioxid Braunkohlekraftwerk - CO 2 -Verwertung im Kraftwerksbetrieb Seite 2/26 im Kraftwerksbetrieb Seite 3/26 Natürliches
FDM-Materialien. Kontaktieren Sie uns, wenn Sie ein anderes Filament benötigen. z.b.: Farbe, Material oder Shore Härte.
 Kontakt: SteRo3D Rapid Prototyping Stephan Roth Duttentalstraße 18 78532 Tuttlingen Telefon: +49 176 5781 6449 E-Mail: info@stero3d.de Homepage: www.stero3d.de Kontaktieren Sie uns, wenn Sie ein anderes
Kontakt: SteRo3D Rapid Prototyping Stephan Roth Duttentalstraße 18 78532 Tuttlingen Telefon: +49 176 5781 6449 E-Mail: info@stero3d.de Homepage: www.stero3d.de Kontaktieren Sie uns, wenn Sie ein anderes
STOFFE U N D STOFFTRENNUNG
 Inhalt WAS IST CHEMIE? 10 STOFFE U N D STOFFTRENNUNG 22 Chemie erlebt Chem ie-chancen und Gefahren...12 Umgang mit Chemikalien... 14 Chemie erlebt Chemie is t... 16 Methode Regeln beim Experimentieren...17
Inhalt WAS IST CHEMIE? 10 STOFFE U N D STOFFTRENNUNG 22 Chemie erlebt Chem ie-chancen und Gefahren...12 Umgang mit Chemikalien... 14 Chemie erlebt Chemie is t... 16 Methode Regeln beim Experimentieren...17
Aufgabe 1.1 Welche der folgenden Aussagen in Bezug auf nachfolgende Reaktionsgleichung ist falsch? HCl + NH3 NH4 + + Cl -
 1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen in Bezug auf nachfolgende Reaktionsgleichung ist falsch? HCl + NH3 NH4 + + Cl - A) Salzsäure ist eine stärkere
1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen in Bezug auf nachfolgende Reaktionsgleichung ist falsch? HCl + NH3 NH4 + + Cl - A) Salzsäure ist eine stärkere
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine
 4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
Unterrichtsstunde zum Thema Kunststoffe. von Stefan Döge
 Unterrichtsstunde zum Thema Kunststoffe von Stefan Döge Inhalt 1. Begriff Kunststoff und Einteilung 2. Kunststoffarten 3. Reaktionsarten 4. Taktizität, Copolymere 5. Verarbeitung 6. Wiederverwertung 7.
Unterrichtsstunde zum Thema Kunststoffe von Stefan Döge Inhalt 1. Begriff Kunststoff und Einteilung 2. Kunststoffarten 3. Reaktionsarten 4. Taktizität, Copolymere 5. Verarbeitung 6. Wiederverwertung 7.
Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer. Brennstoffe. Wir Unterscheiden grundsätzlich Brennstoffe in:
 Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer Wir Unterscheiden grundsätzlich in: Feste Flüssige Gasförmige Biomasse Feste Torf Holz Kohle Brikett Koks Anthrazit Holz: Anwendung: Kachelofen,
Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer Wir Unterscheiden grundsätzlich in: Feste Flüssige Gasförmige Biomasse Feste Torf Holz Kohle Brikett Koks Anthrazit Holz: Anwendung: Kachelofen,
4. Chemische Reaktionen und Energieumsatz, Thermochemie
 Chemie RG mit LS, Themenbereiche, Seite 1 von 4 Chemie im Realgymnasium mit LS, 6-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
Chemie RG mit LS, Themenbereiche, Seite 1 von 4 Chemie im Realgymnasium mit LS, 6-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
schulinterne Kurzübersicht der Unterrichtsvorhaben 1
 schulinterne Kurzübersicht der Unterrichtsvorhaben 1 Fach: Chemie Jahrgangsstufe(n): Einführungsphase erstes und zweites Halbjahr Inhaltsfeld: Kohlenstoffverbindungen und Gleichgewichtsreaktionen Fachlicher
schulinterne Kurzübersicht der Unterrichtsvorhaben 1 Fach: Chemie Jahrgangsstufe(n): Einführungsphase erstes und zweites Halbjahr Inhaltsfeld: Kohlenstoffverbindungen und Gleichgewichtsreaktionen Fachlicher
Technik. Geschrieben 29. Apr :18 Uhr
 Technik Kerosin aus CO2, Wasser und Solarenergie hergestellt :: Technik :: Technik Technik: Kerosin aus CO2, Wasser und Solarenergie hergestellt Geschrieben 29. Apr 2014-13:18 Uhr Eine internationale Forschergruppe
Technik Kerosin aus CO2, Wasser und Solarenergie hergestellt :: Technik :: Technik Technik: Kerosin aus CO2, Wasser und Solarenergie hergestellt Geschrieben 29. Apr 2014-13:18 Uhr Eine internationale Forschergruppe
Klausur zur Vorlesung "Grundzüge der Chemie" für Studierende des Maschinenbaus BITTE AUSFÜLLEN BITTE HALTEN SIE IHREN STUDENTAUSWEIS BEREIT
 1 PUNKTZAL NTE Klausur zur Vorlesung "Grundzüge der hemie" für Studierende des Maschinenbaus Termin: 17. Juni 2003 rt: Z 10 Zeit: 9.30-11.30 Uhr Dauer: 120 Minuten BITTE AUSFÜLLEN BITTE ALTEN SIE IREN
1 PUNKTZAL NTE Klausur zur Vorlesung "Grundzüge der hemie" für Studierende des Maschinenbaus Termin: 17. Juni 2003 rt: Z 10 Zeit: 9.30-11.30 Uhr Dauer: 120 Minuten BITTE AUSFÜLLEN BITTE ALTEN SIE IREN
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Einflüsse auf die adsorptive Entschwefelung flüssiger Kohlenwasserstoffe für moderne Brennstoffzellensysteme
 Einflüsse auf die adsorptive Entschwefelung flüssiger Kohlenwasserstoffe für moderne Brennstoffzellensysteme Von der Fakultät für Georessourcen und Materialtechnik der Rheinisch Westfälischen Technischen
Einflüsse auf die adsorptive Entschwefelung flüssiger Kohlenwasserstoffe für moderne Brennstoffzellensysteme Von der Fakultät für Georessourcen und Materialtechnik der Rheinisch Westfälischen Technischen
Das Haber-Bosch-Verfahren
 Das Haber-Bosch-Verfahren 3 + 2 NH 3 H = - 92 kj/mol Ammoniak, NH 3 - Eigenschaften - farbloses Gas - charakteristischer, stechender, zu Tränen reizender Geruch, - Sdp.: - 33 C - gutes Lösungsmittel für
Das Haber-Bosch-Verfahren 3 + 2 NH 3 H = - 92 kj/mol Ammoniak, NH 3 - Eigenschaften - farbloses Gas - charakteristischer, stechender, zu Tränen reizender Geruch, - Sdp.: - 33 C - gutes Lösungsmittel für
Ammoniaksynthese. Erstellt von Daniel Flanz und Paul Fehren
 Ammoniaksynthese Erstellt von Daniel Flanz und Paul Fehren Inhaltsverzeichnis Geschichte der Ammoniaksynthese Eigenschaften von Ammoniak Herstellungsverfahren Haber-Bosch-Verfahren Alternativen Schwachpunkte
Ammoniaksynthese Erstellt von Daniel Flanz und Paul Fehren Inhaltsverzeichnis Geschichte der Ammoniaksynthese Eigenschaften von Ammoniak Herstellungsverfahren Haber-Bosch-Verfahren Alternativen Schwachpunkte
Möglichkeiten und Technologien für die stoffliche Nutzung agrarischer Reststoffe
 Möglichkeiten und Technologien für die stoffliche Nutzung agrarischer Reststoffe Dr. Henning Storz, Jörn Oetken Thünen-Institut für Agrartechnologie Braunschweig Seite Innovationsforum 1 Storz, SpreuStroh
Möglichkeiten und Technologien für die stoffliche Nutzung agrarischer Reststoffe Dr. Henning Storz, Jörn Oetken Thünen-Institut für Agrartechnologie Braunschweig Seite Innovationsforum 1 Storz, SpreuStroh
Schriftliche Abschlussprüfung Chemie
 Sächsisches Staatsministerium für Kultus Schuljahr 1999/ Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Sächsisches Staatsministerium für Kultus Schuljahr 1999/ Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Aktuelle Beispiele aus der Forschung
 Vorlesung: Allgemeine Chemie Organische Chemie 05.12.; 08.12.; Prof. Dr. C. Meier Eine Einführung in die Organische Chemie Themen: Elektronenstruktur, kovalente Bindung, Säure-Basen-Eigenschaften in Abhängigkeit
Vorlesung: Allgemeine Chemie Organische Chemie 05.12.; 08.12.; Prof. Dr. C. Meier Eine Einführung in die Organische Chemie Themen: Elektronenstruktur, kovalente Bindung, Säure-Basen-Eigenschaften in Abhängigkeit
Biomasse/Biomüll. Biogas/Biogasanlage. Blockheizkraftwerk. Müllheizkraftwerk. Pelletheizung
 Biomasse/Biomüll Biogas/Biogasanlage Blockheizkraftwerk Müllheizkraftwerk Pelletheizung Christoph Hennemann 10 a 09.03.2010 Biomasse: Als Biomasse wird die gesamte organische Substanz bezeichnet. Basis
Biomasse/Biomüll Biogas/Biogasanlage Blockheizkraftwerk Müllheizkraftwerk Pelletheizung Christoph Hennemann 10 a 09.03.2010 Biomasse: Als Biomasse wird die gesamte organische Substanz bezeichnet. Basis
Planungsblatt Physik für die 3B
 Planungsblatt Physik für die 3B Woche 20 (von 15.01 bis 19.01) Hausaufgaben 1 Bis Montag 22.01: Lerne die Notizen von Woche 20! Kernbegriffe dieser Woche: Energie, Leistung, Wärme, Wärmeleitung, Konvektion,
Planungsblatt Physik für die 3B Woche 20 (von 15.01 bis 19.01) Hausaufgaben 1 Bis Montag 22.01: Lerne die Notizen von Woche 20! Kernbegriffe dieser Woche: Energie, Leistung, Wärme, Wärmeleitung, Konvektion,
ALDEHYDE & KETONE. Referat über die Carbonylverbindungen: Aldehyde und Ketone Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium
 ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
Brandklassen Lehrerinformation
 Lehrerinformation 1/5 Arbeitsauftrag Ziel SuS lesen Text zu Brandarten und ergänzen mit eigenen Ideen Feuerkomponenten studieren Feuer-Bild malen Löschmittel zu Brennstoffen zuordnen Abgleichen der eigenen
Lehrerinformation 1/5 Arbeitsauftrag Ziel SuS lesen Text zu Brandarten und ergänzen mit eigenen Ideen Feuerkomponenten studieren Feuer-Bild malen Löschmittel zu Brennstoffen zuordnen Abgleichen der eigenen
4. Reaktionsgeschwindigkeit und chemisches Gleichgewicht
 Chemie RG mit DG, Themenbereiche, Seite 1 von 4 Chemie im Realgymnasium mit DG, 5-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
Chemie RG mit DG, Themenbereiche, Seite 1 von 4 Chemie im Realgymnasium mit DG, 5-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
Stoffklasse: LIPIDE Funktionen in der Zelle
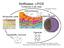 Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on
 Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on Dietikon, 24. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on Dietikon, 24. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung bildet mit einem primären Amin ein Imin.
Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung bildet mit einem primären Amin ein Imin.
Station 1.1: Dampfreformierung
 Station 1.1: Dampfreformierung Kosten: 8 Energie pro Methan, 1 Wasser pro Methan Ausgangsstoff: Kohlenwasserstoffverbindung(meist Erdgase), Wasser(dampf), Wärme Funktion: prinzipiell eine Verbrennung des
Station 1.1: Dampfreformierung Kosten: 8 Energie pro Methan, 1 Wasser pro Methan Ausgangsstoff: Kohlenwasserstoffverbindung(meist Erdgase), Wasser(dampf), Wärme Funktion: prinzipiell eine Verbrennung des
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
5.8. Polyaddition (2) - Polyurethanbildung. Aufgabe. Wie wird Polyurethan-Schaum hergestellt?
 Naturwissenschaften - Chemie - Polymerchemie - 5 Mechanismus der Kunststoffbildung (P7181700) 5.8. Polyaddition (2) - Polyurethanbildung Experiment von: Seb Gedruckt: 02.04.2014 14:07:34 intertess (Version
Naturwissenschaften - Chemie - Polymerchemie - 5 Mechanismus der Kunststoffbildung (P7181700) 5.8. Polyaddition (2) - Polyurethanbildung Experiment von: Seb Gedruckt: 02.04.2014 14:07:34 intertess (Version
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Intensivkurs Biologie
 Intensivkurs 2016 - Biologie 1. Makromoleküle Lektüre im Cornelsen, Biologie Oberstufe : Chemische Grundlagen: Lipide (S. 40), Proteine (S. 41-42), Kohlenhydrate (S. 92-93) 1.1. Kohlenstoff-Verbindungen
Intensivkurs 2016 - Biologie 1. Makromoleküle Lektüre im Cornelsen, Biologie Oberstufe : Chemische Grundlagen: Lipide (S. 40), Proteine (S. 41-42), Kohlenhydrate (S. 92-93) 1.1. Kohlenstoff-Verbindungen
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 31.10.2016 Die Klausur besteht aus 9 Seiten. Bitte zu den folgenden Aufgaben die jeweils richtige Antwort (A, B, C, D) bzw. den berechneten Wert (ohne Maßeinheit)
Chemisches Praktikum für Biologen Klausur am 31.10.2016 Die Klausur besteht aus 9 Seiten. Bitte zu den folgenden Aufgaben die jeweils richtige Antwort (A, B, C, D) bzw. den berechneten Wert (ohne Maßeinheit)
Chemie Alkohole, Aldehyde & Ketone, Carbonsäuren
 Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lehrerhandreichungen zu: "Der Kohlenstoffkreislauf"
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lehrerhandreichungen zu: "Der Kohlenstoffkreislauf" Das komplette Material finden Sie hier: School-Scout.de Schlagwörter Assimilation;
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lehrerhandreichungen zu: "Der Kohlenstoffkreislauf" Das komplette Material finden Sie hier: School-Scout.de Schlagwörter Assimilation;
Grundlagen der Organischen Chemie
 Grundlagen der Organischen Chemie Vorlesung im WS 2010/2011 1. Einführung 1 1.1 Die wunderbare Welt der Organischen Chemie 1.2 Kohlenstoff ein ganz besonderes Element 4 2. Die kovalente Bindung 5 2.1 Atomorbitale
Grundlagen der Organischen Chemie Vorlesung im WS 2010/2011 1. Einführung 1 1.1 Die wunderbare Welt der Organischen Chemie 1.2 Kohlenstoff ein ganz besonderes Element 4 2. Die kovalente Bindung 5 2.1 Atomorbitale
Aufgabengruppe BMS Chemie
 Aufgabengruppe BMS Chemie Zeitvorgabe: Bitte lösen Sie die folgenden 24 Aufgaben innerhalb von 18 Minuten! 1) Welche Aussagen treffen auf Proteine zu? I. Die Primärstruktur gibt die Aminosäurenabfolge
Aufgabengruppe BMS Chemie Zeitvorgabe: Bitte lösen Sie die folgenden 24 Aufgaben innerhalb von 18 Minuten! 1) Welche Aussagen treffen auf Proteine zu? I. Die Primärstruktur gibt die Aminosäurenabfolge
Polymer- Carbon Nanotube- Komposite. Lysander Jankowsky (136309)
 Polymer- Carbon Nanotube- Komposite Lysander Jankowsky (136309) Lysander.jankowsky@uni-jena.de Gliederung Was sind Carbon Nanotubes (CNTs) Herstellung von CNTs Funktionalisierung von CNTs - Defekt- Funktionalität
Polymer- Carbon Nanotube- Komposite Lysander Jankowsky (136309) Lysander.jankowsky@uni-jena.de Gliederung Was sind Carbon Nanotubes (CNTs) Herstellung von CNTs Funktionalisierung von CNTs - Defekt- Funktionalität
Fettchemie Hauptbestandteile der Fette und Öle Fettbegleitstoffe... 14
 Einleitung... 4 Markt und Verbrauch... 6 Verbrauchszahlen... 6 Haupterzeugerländer... 6 Fettchemie... 12 Hauptbestandteile der Fette und Öle... 12 Fettbegleitstoffe... 14 Speisefette in der Ernährung...
Einleitung... 4 Markt und Verbrauch... 6 Verbrauchszahlen... 6 Haupterzeugerländer... 6 Fettchemie... 12 Hauptbestandteile der Fette und Öle... 12 Fettbegleitstoffe... 14 Speisefette in der Ernährung...
0 Einleitung 0.1 Vorbemerkungen
 0 Einleitung 0.1 Vorbemerkungen Professur Radiochemie Sommersemester 2010 Vorlesung: Umweltchemie Gliederung: 0 Einleitung 0.1 Vorbemerkungen 0.2 Definition Umweltchemie 1 Entstehung der Umwelt 1.1 Bildung
0 Einleitung 0.1 Vorbemerkungen Professur Radiochemie Sommersemester 2010 Vorlesung: Umweltchemie Gliederung: 0 Einleitung 0.1 Vorbemerkungen 0.2 Definition Umweltchemie 1 Entstehung der Umwelt 1.1 Bildung
c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
 Carbonsäuren schriftliche Ausarbeitungen zu folgenden Themen: a) Eigenschaften von organischen Säuren b) Begriff der homologen Reihe der Carbonsäuren c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
Carbonsäuren schriftliche Ausarbeitungen zu folgenden Themen: a) Eigenschaften von organischen Säuren b) Begriff der homologen Reihe der Carbonsäuren c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
Kapitel 02: Erdgas und Erdöl
 Kapitel 02: Erdgas und Erdöl 1 Kapitel 02: Erdgas und Erdöl Kapitel 02: Erdgas und Erdöl 2 Inhalt Kapitel 02: Erdgas und Erdöl...1 Inhalt... 2 Einige Produkte aus Erdöl...3 Erdöl ist nicht gleich Erdöl...3
Kapitel 02: Erdgas und Erdöl 1 Kapitel 02: Erdgas und Erdöl Kapitel 02: Erdgas und Erdöl 2 Inhalt Kapitel 02: Erdgas und Erdöl...1 Inhalt... 2 Einige Produkte aus Erdöl...3 Erdöl ist nicht gleich Erdöl...3
Homologe Reihe der unverzweigten Alkane C n H (2n+2)
 Organische hemie I 3.01 Homologe Reihe der unverzweigten Alkane n H (2n+2) (Paraffine) (veraltet: normale Alkane = n-alkane) Name Konstitution Siedepunkt ausführliche Schreibweise Stenographie [ ] Methan
Organische hemie I 3.01 Homologe Reihe der unverzweigten Alkane n H (2n+2) (Paraffine) (veraltet: normale Alkane = n-alkane) Name Konstitution Siedepunkt ausführliche Schreibweise Stenographie [ ] Methan
Chemie 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter Wasser (= 1000g)?
 Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
