Grundlagen der Stoffwechselphysiologie
|
|
|
- Matthias Schuler
- vor 7 Jahren
- Abrufe
Transkript
1 1 Grundlagen der Stoffwechselphysiologie -Fragenkatalog- Bitte beachten: Die endgültige Formulierung der Fragen in der Klausur kann von den Formulierungen im Fragenkatalog abweichen Bei manchen Fragen kann es Überschneidungen geben das ist gewollt! In der Klausur können hier gestellte Einzelfragen zusammengefasst werden oder es können nur Teile einer Frage gestellt werden
2 2 Wasser und ph-homöostase 1. Kolligative Eigenschaften wässriger Lösungen: a) Was sind kolligative Eigenschaften von (verdünnten) wässrigen Lösungen? b) Nennen Sie zwei Beispiele für kolligative Eigenschaften. 2. Welche Eigenschaft des Lösungsmittels Wasser ist für das Dissoziationsverhalten von Säuren und Basen maßgeblich? 3. Was versteht man unter dem Begriff ph-homöostase? 4. Woraus besteht ein einfaches Puffersystem? 5. Nennen Sie drei Hauptmechanismen, über die die ph-homöostase im Blut erfolgt 6. Nennen Sie wichtige physiologische Puffersysteme und ihren Wirkungsort Puffersystem Wirkungsort 7. Puffersysteme im Blut: Nennen Sie die beiden Hauptpuffersysteme im Blut und ihren Anteil an der Gesamtpufferkapazität Hauptfraktion Anteil an der Pufferkapazität (%) 8. Aus welcher Gleichung geht hervor, dass zunächst das Verhältnis von konjugierter Base zur Säure den ph-wert einer gepufferten Lösung bestimmt? (Gleichung + Formel) 9. Aus welchen Nahrungsbestandteilen entstehen netto Protonen (H + )? 10. Aus welchen Nahrungsbestandteilen entstehen netto Hydroxylionen (OH - )? 11.Renale Mechanismen, die an der ph-homöostase beteiligt sind: a) Über welche Reaktion können Protonen (H + ) in den Tubuluszellen gebildet werden? (incl. Gleichung) b) Über welchen Mechanismus werden die Protonen (H + ) in das Tubuluslumen sezerniert? c) In welcher Form werden die Protonen (H + ) im Urin überwiegend ausgeschieden?
3 3 Biokatalyse 12. a) Zu welcher Stoffklasse gehören die meisten Enzyme b) Welche Funktion haben Enzyme? 13. a) Nennen Sie drei Beispiele für Coenzyme bzw. Cosubstrate, die Wasserstoff (Elektronen) übertragen b) Nennen Sie 3 Beispiele für Coenzyme, die andere Gruppen (nennen) übertragen Coenzym übertragene Gruppe 14. a) Welcher Parameter beschreibt die Affinität zwischen Enzym und Substrat? b) Wie ist dieser Parameter definiert? c) Wie sieht die Beziehung zwischen diesem Parameter und der Affinität aus? 15. Wie heißen Substanzen, welche die Enzymaktivität beeinflussen (a) und wie können sich diese Substanzen auf die Enzymaktivität auswirken? 16. Welche Grundtypen der Hemmung von Enzymen gibt es? 17. Kompetitive Hemmung eines Enzyms: a) beschreiben Sie das Prinzip b) Wie muss die Bindung des Inhibitors im aktiven Zentrum sein? c) Wie wirkt sich ein kompetitiver Inhibitor auf K m und V max aus? 18. Nicht-kompetitive Hemmung eines Enzyms: a) beschreiben Sie das Prinzip b) Wie ist die Bindung des Inhibitors? c) Wie wirkt sich ein nicht-kompetitiver Inhibitor auf K m und V max aus?
4 4 Nucleinsäurenstoffwechsel 19. Was versteht man unter a) Replikation b) Transkription c) Translation 20. Wie werden die für ein Polypeptid (Protein) codierenden (a) bzw. nicht codierenden Abschnitte auf der DNA (mrna) genannt 21. Bei der Replikation der DNA werden sogenannte Primer gebildet. a) Was ist ein Primer? b) Gibt es Unterschiede bezüglich der Synthese von Primern am Führungs- bzw. Folgestrang? 22. Beschreiben Sie die Bildung einer reifen mrna aus einer primären oder prä-mrna (Processing) 23. a) An welchen makromolekularen Komplexen findet die Proteinbiosynthese statt? b) Wie sind diese Komplexe aufgebaut? 24. Was ist Voraussetzung für die Paarung der kleinen und großen Ribosomenuntereinheit bei der Translation 25. Nennen Sie die energieverbrauchenden Teilschritte bei der Knüpfung einer neuen Peptidbindung im Rahmen der Translation (Elongationsphase) und geben Sie den jeweiligen Energiebedarf (in ATP-Äquivalenten)an: Schritt, der Energie benötigt wieviel Energie 26. Wie werden die die DNA-Stränge genannt, an denen die Synthese des Tochterstrangs kontinuierlich bzw. diskontinuierlich abläuft? 27. An welchem Ende der DNA- oder RNA-Einzelstrangs erfolgt die Anknüpfung neuer Nucleotide?
5 5 BIOENERGETIK 28. a) Was versteht man unter dem Begriff Atmungskette? b) Welche Substrate werden in der Atmungskette umgesetzt? c) Welchen Reaktionstyp katalysieren die Komplexe I-IV in der Atmungskette? 29. Nennen Sie die Funktion der 4 Redox- Komplexe der Atmungskette Komplex Funktion 30. a) Durch welchen elektrochemischen Gradienten wird die Bildung von ATP getrieben? b) An welcher Membran wird dieser Gradient aufgebaut? c) Durch welches Enzymsystem erfolgt letztlich die Synthese von ATP? d) Was sind die notwendigen Ausgangssubstrate für die Bildung von ATP? Kohlenhydrate 31. Nennen Sie 3 prinzipielle Funktionen von Kohlenhydraten für den Organismus 32. Nennen Sie 3 Beispiele für physiologisch wichtige Hexosen und ihre Bedeutung im Organismus Hexose Bedeutung 33. Nennen Sie 2 Beispiele für physiologisch wichtige Pentosen und ihre Bedeutung im Organismus Pentose Bedeutung 34. Nennen Sie 4 Monosaccharide, die als Zwischenprodukte (phosphoryliert) im Stoffwechsel vorkommen und den dazugehörigen Stoffwechselwe Monosaccharid/Zahl der C-Atome Stoffwechselweg
6 6 35. Nennen Sie 3 physiologisch wichtige Derivate von Monosacchariden (keine Zwischenprodukte aus Stoffwechselwegen) 36. Charakterisieren Sie 2 Funktionen von Glucuronsäure im Organismus 37. Aminozucker: Nennen Sie ein Beispiel (a), den prinzipiellen Aufbau (b) sowie ein Beispiel für Moleküle, die Aminozucker als Bestandteil aufweisen (c) 38. Nennen Sie 3 Beispiele für Glycoproteine 39. Welche Monosaccharide kommen in Glycoproteinen vor? (3 Beispiele) 40. Welche Oligosaccharide /Polysaccharide (nicht Disaccharide) aus der Nahrung können durch die Verdauungsenzyme des Menschen/des Tieres verdaut werden? Name Bausteine Art der glycosidischen Bindung; zwischen welchen C-Atomen der beteiligten Monosaccharide? Lipide 41. In welche beiden Haupklassen lassen sich Lipide einteilen? 42. Charakterisieren Sie den Aufbau von verseifbaren Lipiden a) Prinzipieller Aufbau b) Alkoholkomponenten (3 Beispiele) 43. Nennen Sie 4 Funktionen von Triacylglycerinen 44. Welche Lipide sind Bestandteile menschlicher/tierischer Biomembranen?
7 7 45. Charakterisieren Sie physiologisch wichtige bzw. häufig vorkommende langkettige Fettsäuren: Name Gesättigte Fettsäuren (2 Beispiele) Kettenlänge Monoensäuren ( 1 Beispiel) Polyensäuren (4 Beispiele) 46. Welche bei Mensch und Tier wichtigen Fettsäuren gehören zur Gruppe der n-3-fettsäuren, welche zur Gruppe der n-6-fettsäuren (Name, Kettenlänge, Zahl der Doppelbindungen) Name Kettenlänge (C-Atome) Doppelbindungen n-6-fettsäuren (3 Beispiele) n- 3-Fettsäuren (3 Beispiele) 47. a) Welche Fettsäuren sind essentiell? b) Nennen Sie prinzipielle Funktionen der essentiellen Fettsäuren: 48. Nennen Sie die 3 Untergruppen der Eicosanoide und ordnen Sie ihnen jeweils eine Funktion zu: Untergruppe beteiligt an 49. Welche Enzyme (Gruppennamen) sind an der Bildung von Eicosapentaensäure und Arachidonsäure aus den ursprünglichen Fettsäuren beteiligt?
8 8 50. Welches Enzym ist an der Bildung von Prostaglandinen, Thromoboxanen bzw. Leukotrienen beteiligt? Substrat an der Synthese beteiligtes Enzym Prostaglandine Thromboxane Leukotriene 51. a) Nennen Sie die Hauptfunktion von Phosphoglyceriden b) Beschreiben Sie den Aufbau von Phosphoglyceriden 52. Welche Alkohole (4 Beispiele) kommen in Phosphoglyceriden vor? 53. Nennen Sie vier Phosphoglyceride 54. Nennen Sie drei Grundfunktionen von Cholesterin im Organismus Nucleoside, Nucleotide und Polynucleotide 55. Nennen Sie die prinzipiellen Bestandteile eines (a) Nucleosides und (b) eines Nucleotides 56. Nennen Sie die im Organismus vorkommenden Purinbasen (a) und Pyrimidinbasen (b) 57. Welche Monosaccharide kommen in Nucleosiden/Nucleotiden vor? 58. Nennen Sie biologisch wichtige Mononucleoside (a) und Mononucleotide (b) einschließlich ihrer Funktion(en) (nicht Aufbau von Nucleinsäuren) a) Nucleosid (1 Beispiel) b) Nucleotide (4 Beispiele)
9 9 59. Nennen Sie die molekularen Bestandteile von Ribonucleinsäuren (RNA) und Desoxyribonucleinsäuren (DNA) RNA DNA Pentose Purinbasen Pyrimidinbasen 60. Zwischen welchen Basen der DNA bilden sich Wasserstoffbrücken aus? Nennen Sie die Zahl der Wasserstoffbrücken Basen Zahl der Wasserstoffbrücken 61. Nennen Sie vier Unterschiede zwischen DNA und RNA 62. Nennen Sie die RNA-Klassen und ihre Funktion RNA-Klasse Funktion Aminosäuren- Peptide - Proteine 63. Nennen Sie Beispiele für Aminosäuren a) mit einer hydrophoben Seitenkette ( 5 Beispiele) b) einer hydrophilen Seitenkette ( 3 Beispiele) c) mit einer ambiphilen Seitenkette ( 4 Beispiele) 64. Welche Aminosäuren enthalten Schwefel? 65. Nennen Sie vier prinzipielle Funktionen von Aminosäuren
10 Nennen Sie drei nicht-proteinogene Aminosäuren sowie Proteine, in denen Sie vorkommen Nicht-proteinogene AS Vorkommen/Funktion 67. Nennen Sie zwei Beispiele für nicht-proteinogene Aminosäuren als Zwischenprodukte von Stoffwechselwegen Nicht-proteinogene AS Vorkommen / Funktion 68. Nennen Sie zwei Beispiele für nicht-proteinogene Aminosäuren als Vorstufe für andere niedermolekulare Verbindungen Nicht-proteinogene AS Vorkommen / Funktion 69. (a) Wie sind essentielle Aminosäuren definiert und (b) nennen Sie die essentiellen Aminosäuren 70. Nennen Sie prinzipielle Funktionen von Proteinen/Polypeptiden im Organismus (vier Beispiele, wenn möglich genauer spezifizieren) 71. Bennen und beschreiben Sie die Hierarchiestufen der Proteinkonformation Struktur Beschreibung 72. a) Was bewirkt die Sekundärstruktur in einem Protein? b) Nennen Sie die verschiedenen Formen der Sekundärstruktur eines Proteins 73. a) Was bewirkt die Tertiärstruktur in einem Protein? b) Nennen Sie die beiden Grundformen von Proteinen mit unterschiedlicher Tertiärstruktur c) durch welche Bindungskräfte kann die Tertiärstruktur stabilisiert werden?
11 11 Intermediärstoffwechsel 74. Schlüsselmoleküle im Intermediärstoffwechsel: a) Zu welchen Molekülen kann Pyruvat umgesetzt werden? b) Zu welchen Stoffwechselwegen hat Pyruvat eine Beziehung? 75. Nennen Sie die Vorteile von Stoffwechselzyklen 76. Nennen Sie Faktoren/Mechanismen, durch welche die Aktivität von Schlüsselenzymen beeinflusst werden kann (nicht Temperatur) 77. Was versteht man unter dem Begriff Enzymatische Interkonvertierung Citratcyclus 78. Nennen Sie die beiden prinzipiellen Funktionen des Citratcyclus 79. Nennen Sie zwei α-ketocarbonsäuren, die im Citratcyclus vorkommen 80. Nennen Sie die einzelnen Schritte des Citratcyclus Umsetzungsgleichungen verantwortliches Enzym
12 Aus welchen Stoffwechselwegen (Quellen) stammt das Acetyl-CoA, das in den Citratcyclus eingeschleust wird? 82. a) Wieviele Dehydrierungsreaktionen gibt es im Citratcyclus? b) Bei welchen Reaktionsschritten finden Dehydrierungen statt? c) Wieviele Decarboxylierungsreaktionen gibt es im Citratcyclus? d) Bei welchen Reaktionsschritten finden Decarboxylierungen statt (X Y)? e) Wieviel Mol NADH werden bei der vollständigen Oxidation 1 Mols Acetyl-CoA gebildet? f) Wieviel Mol FADH 2 werden bei der vollständigen Oxidation 1 Mols Acetyl-CoA gebildet? g) Wieviel Mol ATP werden bei der vollständigen Oxidation 1 Mols Acetyl-CoA gebildet? 83. Welchem Zweck dienen anaplerotische Reaktionen des Citratcyclus? 84. Nennen Sie die wichtigste anaplerotische Reaktion des Citratcyclus (komplette Reaktionsgleichung) sowie das dazugehörige Enzym Reaktionsgleichung Enzym Kohlenhydratstoffwechsel 85. a) In welche Form wird Glucose nach der Aufnahme in Zellen umgewandelt? b) Welche Enzyme katalysieren die Bildung der genannten Form? 86. Nennen Sie die Abfolge der Metabolite bei der Glykolyse (Milchsäuregärung) 87. a) Wie viel Mol ATP liefert der Abbau von einem Mol Glucose in der Glykolyse unter anaeroben Bedingungen? b) Wie wird die Bildung von ATP in der Glykolyse bezeichnet? c) Nennen Sie die Teilreaktionen, bei denen ATP gebildet wird und die Enzyme, die diese Teilschritte katalysieren. Teilschritt (X Y) Enzym
13 Nennen Sie die drei irreversiblen Reaktionsschritte der Glykolyse und die dazugehörigen Enzyme Reaktionsschritt Enzym 89. Wie werden die irreversiblen Schritte der Glykolyse im Rahmen der Gluconeogenese umgangen? (Reaktionen, Enzyme) Umgehungsreaktion (X Y) katalysiert durch Enzym 90. a) Was versteht man unter Gluconeogenese? b) Welchen Zweck hat die Gluconeogenese? c) In welchen Organen findet Gluconeogenese statt? d) Welche Gewebe sind auf Glucose als Energiequelle angewiesen? 91. a) Nennen Sie die wichtigsten Präkursoren (= Ausgangsprodukte) für die Gluconeogenese in der Reihenfolge der quantitativen Bedeutung beim Menschen b) Welches zusätzliche Ausgangsprodukt spielt für die Gluconeogenese beim Wiederkäuer eine wichtige Rolle? 92. a) Welche Funktionen erfüllt der erste Teil Hexosemonophosphatwegs/ Pentosephosphatcylcus und b) der zweite Teil des? b) Welche Funktionen erfüllt der zweite Teil Hexosemonophosphatwegs/ Pentosephosphatcylcus? 93. Wie heißt das Enzym, das Glucose-6-phosphat in 6-Phosphogluconolacton umwandelt und in welchem Stoffwechselweg ist es lokalisiert? 94. Nennen Sie das Schlüsselenzym des Hexosemonophosphatwegs 95. a) Nennen Sie das Schlüsselenzym der Glycogensynthese b) In welchen Organen wird besonders viel Glycogen gespeichert? c) Welches dieser Organe trägt zur Erhöhung der Blutglucose bei? 96. a) Welches Enzym ist das Schlüsselenzym des Glycogenabbaus? b) Welche Bindungen spaltet dieses Enzym? c) Welches monomere Produkt entsteht cabei?
14 14 Fettstoffwechsel 97. Welche Enzyme katalysieren den intrazellulären Abbau von Triacylglycerinen und welche Produkte entstehen dabei? Enzym Produkt 98. Beschreiben Sie die Schritte bei der Aktivierung von freien Fettsäuren (mit Nennung des Enzyms) und nennen Sie das ensprechende Zellkompartiment, in dem der Aktivierungsschritt stattfindet? Schritt (Reaktionsgleichung) Enzym Zellkompartiment 99. a) Beschreiben Sie die Schritte des Abbaus von freien Fettsäuren in der ß-Oxidation. (Von welchen Enzymen werden diese Schritte katalysiert? In welchem Zellkompartiment finden diese Schritte statt? b) Sind diese Schritte reversibel? Schritt(Reaktionsgleichung) Enzym Zellkompartiment 100. Welche Funktion hat Carnitin im Fettsäurenstoffwechsel 101. Beschreiben Sie die Teilreaktionen (Reaktionsgleichungen) des Transfer aktivierter langkettiger Fettsäuren aus dem Cytosol in die Mitochondrienmatrix und nennen Sie das jeweilige Enzym und den Ort der Reaktion Reaktion Enzym Ort 102. a) In welchem Zellkompartiment findet die Fettsäurebiosynthese statt? b) Nennen Sie das Schlüsselenzym der Fettsäurebiosynthese und beschreiben Sie die durch dieses Enzym katalysierte Reaktion in Form einer Gleichung An welcher Gruppe der Fettsäuresynthase finden die Kondensierungsreaktionen im Rahmen der Fettsäuresynthese statt? 104. Wie wird Acetyl-CoA für die Fettsäuresynthese aus den Mitochondrien ins Cytosol transportiert? Nennen Sie die Reaktionsschritte in Form von Gleichungen.
15 Welche einfach ungesättigten Fettsäuren kann der Mensch bzw. das Tier selbst synthetisieren? Nennen Sie auch die Position der Doppelbindung und die entsprechenden Vorstufen Ungesättigte Fettsäure Position Doppelbindung Vorstufe 106. Ergänzen Sie die nachfolgende Tabelle zur Fettsäuresynthese/zum Fettsäureabbau Ort Coenzyme Anzahl Enzyme Konfiguration der auftretende Isomere Fettsäuresynthese Fettsäureabbau 107. Nennen Sie die Verbindungen, die als Ketonkörper bezeichnet werden. Handelt es sich dabei in jedem Fall um Ketone? Verbindung Keton?(ja/nein) 108. Beschreiben Sie die einzelnen Schritte der Ketonkörperbiosynthese in Form von Gleichungen. Von welchen Enzymen werden diese Reaktionen katalysiert? Reaktion (X Y) Enzym 109. Unter welchen Bedingungen kommt es vermehrt zur Bildung von Ketonkörpern? a) biochemischer Aspekt b) physiologische Situation (2 Beispiele) 110. a) In welchen Organen werden Ketonkörper gebildet? b) In welchen Organen werden Ketonkörper verwertet? 111. Beschreiben Sie die Teilreaktionen bei der Verwertung von β-hydroxybutyrat und nennen Sie die daran beteiligten Enzyme (Zusatzpunkte für Enzyme!). Reaktion (X Y) Enzym
16 a) Aus welcher Ausgangsverbindung wird Cholesterin synthetisiert? b) Nennen Sie das Schlüsselenzym der Cholesterinbiosynthese c) Nennen Sie die vier Stufen der Cholesterinbiosynthese d) Nennen Sie 3 physiologisch wichtige Funktionen von Cholesterin 113. Nennen Sie vier typische Lipide im Blutplasma und wie werden die genannten Lipide im Blutplasma transportiert? Lipid Transport 114. Nennen Sie die vier Hauptklassen der Lipoproteine im Blutplasma nach der Reihenfolge ihrer Dichte (zunehmend) 115. Mit dem Anstieg welcher Komponente von Lipoproteinen nimmt deren Dichte ab? 116. Was bedeutet die Abkürzung LCAT? 117. Welche physiologisch wichtigen Fettsäuren gehören zur Gruppe der n-3-fettsäuren, welche zur Gruppe der n-6-fettsäuren (Name, Kettenlänge, Zahl der Doppelbindungen) Name n-3/n-6 Kettenlänge Anzahl Doppelbindungen 118. Welche Enzyme (Gruppennamen) sind an der Bildung von Eicosapentaensäure und Arachidonsäure aus den entsprechenden Vorstufen beteiligt? 119. Welche Verbindungen (Gruppenbezeichnung) zählen zu den Eicosanoiden? Welche Enzyme sind an der Bildung der verschiedenen Eiosanoide beteiligt? Eicosanoid (Gruppe) Enzym
17 17 Aminosäurenstoffwechsel 120. Welchen prinzipiellen Reaktionen unterliegen Aminosäuren? 121. a) Nennen Sie die häufigste Reaktion der Aminogruppe b) Beschreiben Sie das Reaktionsprinzip der genannten Reaktion in Form einer Reaktionsgleichung c) Welches Co-Enzym/Co-Substrat spielt bei den meisten Reaktionen im Aminosäuren-stoffwechsel eine Rolle? 122. Nennen Sie drei Beispiele für Aminosäuren und ihre korrespondierenden α- Ketocarbonsäuren Aminosäure korr. α- Ketocarbonsäure 123. a) Nennen Sie eine Aminosäure, die oxidativ decarboxyliert wird b) Beschreiben Sie die oxidative Decarboxylierung der genannten Aminosäure in Form einer Reaktionsgleichung. Welches Enzym katalysiert diese Reaktion? Gleichung (X Y) Enzym 124. a) Über welche Reaktion entstehen biogene Amine? b) Welche Enzyme katalysieren diese Reaktion? 125. Nennen Sie drei Beispiele für biogene Amine und ihre Aminosäurevorstufen Biogenes Amin gebildet aus 126. In welcher Form wird der Stickstoff aus der Aminogruppe der Aminsäuren ausgeschieden? 127. Welche Rolle spielt der Aspartatcyclus im Rahmen der Harnstoffbiosynthese? 128. a) Wie liegt Ammoniak im Blut vor? b) Warum sind erhöhte Ammoniak -Konzentrationen im Blut kritisch? c) in welchem Blutgefäß kommen physiologischerweise hohe NH 4 + -Konzentrationen vor?
18 In welcher fixierten Form wird Ammoniak vorwiegend im Blut transportiert? 130. Wie heißt das (mikrobielle) Enzym, das Harnstoff spaltet? 131. a) In welchem Organ findet die Biosynthese von Harnstoff statt? b) Wo wird Harnstoff ausgeschieden? 132. a) Nennen Sie die 5 Teilreaktionen (in Form von Gleichungen) der Harnstoffbiosynthese sowie die beteiligten Enzyme. Teilreaktion (X Y) Enzym b) In welchen Zellkompartimenten finden die einzelnen Teilreaktion der Harnstoffbiosynthese statt? c) Wieviel Energieäquivalente (als Mol ATP) werden für die Biosynthese von einem Mol Harnstoff verbraucht? 133. Nennen Sie die Funktionen von Glutamat als Drehscheibe des NH 3 -Stoffwechsels (Beispiele: Zusatzpunkte) 134. In welchem Zusammenhang steht die Bildung von Harnsäure mit der Aufnahme bzw. dem Abbau von Aminosäuren? 135. Welche Verbindungen werden im Stoffwechsel zu Harnsäure abgebaut?
Klausur zur Vorlesung Biochemie I im WS 2001/02
 (insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
(insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
Z11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
1 Vom Organismus zum Molekül... 3
 I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
Z 11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
Kataboler und Anaboler Stoffwechsel
 Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Inhaltsverzeichnis. I Stoffwechsel. 1 Vom Organismus zum Molekül Aminosäuren Peptide und Proteine Enzyme...
 XI I Stoffwechsel 1 Vom Organismus zum Molekül...................... 2 1.1 Aufbau des Organismus.............................. 2 1.2 Chemische Grundlagen des Stoffwechsels.................. 6 1.3 Informationsübertragung
XI I Stoffwechsel 1 Vom Organismus zum Molekül...................... 2 1.1 Aufbau des Organismus.............................. 2 1.2 Chemische Grundlagen des Stoffwechsels.................. 6 1.3 Informationsübertragung
- der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen
 Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Klausur zur Vorlesung Biochemie I im WS 1993/1994. am 18. Februar Nachklausur zur Vorlesung Biochemie I im WS 1993/1994. am 30. Mai 1994.
 Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Inhaltsverzeichnis. a. Chemie der Aminosäuren und Peptide
 Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Übungsfragen zur Vorlesung Einführung in die Biologie, Zell- und Molekularbiologie Teil Biochemie PD Dr. Udo Rau. (Biomoleküle allgemein)
 Übungsfragen zur Vorlesung Einführung in die Biologie, Zell- und Molekularbiologie Teil Biochemie PD Dr. Udo Rau (Biomoleküle allgemein) 1) Aus welchen Elementen besteht die Zelle zu 99%? 2) Warum ist
Übungsfragen zur Vorlesung Einführung in die Biologie, Zell- und Molekularbiologie Teil Biochemie PD Dr. Udo Rau (Biomoleküle allgemein) 1) Aus welchen Elementen besteht die Zelle zu 99%? 2) Warum ist
Seminar Biochemie. Lipide und Lipidstoffwechsel. Dr. Christian Hübbers
 Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, Triglyceride, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese,
Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, Triglyceride, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese,
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
-Klausur Biochemie Name:
 -Klausur Biochemie -03.02.5 Name: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
-Klausur Biochemie -03.02.5 Name: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
Stoffwechsel. Metabolismus (3)
 Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Seminar Biochemie. Lipide und Lipidstoffwechsel. Dr. Christian Hübbers
 Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, TG, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese, MalonylCoA,
Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, TG, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese, MalonylCoA,
Organische Chemie der biologischen Stoffwechselwege
 Organische Chemie der biologischen Stoffwechselwege John McMurry / Tadhg Begley aus dem Amerikanischen übersetzt von Karin Beifuss ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum k_/l AKADEMISCHER VERLAG
Organische Chemie der biologischen Stoffwechselwege John McMurry / Tadhg Begley aus dem Amerikanischen übersetzt von Karin Beifuss ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum k_/l AKADEMISCHER VERLAG
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine
 4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
Musterlösung. Frage Summe Note Punkte 1, ,5 1,0
 Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O O 2 6 CO H 2 O G kj
 Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O G 0-2872 kj Hydrolyse der Stärke Ausgangssubstrate: Glucose, Fructose Stärkehydrolyse: Amylasen Endo- ( -Amylase) und
Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O G 0-2872 kj Hydrolyse der Stärke Ausgangssubstrate: Glucose, Fructose Stärkehydrolyse: Amylasen Endo- ( -Amylase) und
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Der Energiestoffwechsel eukaryotischer Zellen
 Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Kohlenhydrate Aminosäuren Peptide
 Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Kohlenhydrate. Prof. Dr. Albert Duschl
 Kohlenhydrate Prof. Dr. Albert Duschl Kohlenhydrate in der Nahrung Kohlenhydrate sind in zwei Formen in unserer Nahrung vorhanden: Als komplexe Zucker, wie Stärke in Getreideprodukten, und als einfache
Kohlenhydrate Prof. Dr. Albert Duschl Kohlenhydrate in der Nahrung Kohlenhydrate sind in zwei Formen in unserer Nahrung vorhanden: Als komplexe Zucker, wie Stärke in Getreideprodukten, und als einfache
Intensivkurs Biologie
 Intensivkurs 2016 - Biologie 1. Makromoleküle Lektüre im Cornelsen, Biologie Oberstufe : Chemische Grundlagen: Lipide (S. 40), Proteine (S. 41-42), Kohlenhydrate (S. 92-93) 1.1. Kohlenstoff-Verbindungen
Intensivkurs 2016 - Biologie 1. Makromoleküle Lektüre im Cornelsen, Biologie Oberstufe : Chemische Grundlagen: Lipide (S. 40), Proteine (S. 41-42), Kohlenhydrate (S. 92-93) 1.1. Kohlenstoff-Verbindungen
Primärstoffwechsel. Prof. Dr. Albert Duschl
 Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Biochemie. Kurzes Lehrbuch der. für Mediziner und Naturwissenschaftler. Von Peter Karlson. 12., völlig neubearbeitete Auflage
 Kurzes Lehrbuch der Biochemie für Mediziner und Naturwissenschaftler Von Peter Karlson 12., völlig neubearbeitete Auflage 177 Abbildungen 323 Formelbilder und Schemata 37 Tabellen 2008 AGI-Information
Kurzes Lehrbuch der Biochemie für Mediziner und Naturwissenschaftler Von Peter Karlson 12., völlig neubearbeitete Auflage 177 Abbildungen 323 Formelbilder und Schemata 37 Tabellen 2008 AGI-Information
Stoffwechsel der essentiellen Aminosäuren
 Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
-Klausur Biochemie Name: Matrikelnr.: 1. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist.
 4.07.205 Name: Matrikelnr.:. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist. 2. Was bedeutet es, wenn eine schwache Säure einen pks von 5 hat? 3. Nennen Sie
4.07.205 Name: Matrikelnr.:. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist. 2. Was bedeutet es, wenn eine schwache Säure einen pks von 5 hat? 3. Nennen Sie
Zellulärer Abbau von Proteinen in Aminosäuren:! Proteine werden in Zellen durch Proteasom-Komplexe in! einzelne Aminosäuren abgebaut.!
 Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Abschlussklausur zur Vorlesung Biomoleküle II WS 2004/05
 16.02.2005 Abschlussklausur zur Vorlesung Biomoleküle II WS 2004/05 Name: Studienfach: Matrikelnummer: Fachsemester: Hinweise: 1. Bitte tragen Sie Ihren Namen, Matrikelnummer, Studienfach und Semesterzahl
16.02.2005 Abschlussklausur zur Vorlesung Biomoleküle II WS 2004/05 Name: Studienfach: Matrikelnummer: Fachsemester: Hinweise: 1. Bitte tragen Sie Ihren Namen, Matrikelnummer, Studienfach und Semesterzahl
Biochemie II - Tutorium
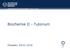 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Kapitel 5: 1. Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D.
 Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
Grundlagen der Physiologie
 Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
- Biochemieklausur Name: Matrikelnr.:
 07.02.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
07.02.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Was bisher geschah 1
 Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus)
 Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Punkte 1. a) Erklären Sie wieso das Wassermolekül ein Dipol ist (gerne mit Zeichnung).
 -Klausur Biochemie - 20.07.6 Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
-Klausur Biochemie - 20.07.6 Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Kohlenhydrate C n. O) n (H 2. z.b. C 6 O 6 O) 6 H 12 : C 6. Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Monosaccharide
 Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Beispiele für Prüfungsfragen zu den Einheiten. 2, 3, 5, 9-12, 15, 16, und 21 (Hartig)
 Beispiele für Prüfungsfragen zu den Einheiten 2, 3, 5, 9-12, 15, 16, und 21 (Hartig) Untenstehendes Molekül ist ein Peptidhormon. Wieviele Peptidbindungen besitzt dieses Molekül (zeichnen Sie diese ein)?
Beispiele für Prüfungsfragen zu den Einheiten 2, 3, 5, 9-12, 15, 16, und 21 (Hartig) Untenstehendes Molekül ist ein Peptidhormon. Wieviele Peptidbindungen besitzt dieses Molekül (zeichnen Sie diese ein)?
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8,
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8,
Aminosäuren 1. Aufbau der Aminosäuren
 Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
BIOCHEMIE. Teil 2: Aminosäuren, Proteine, Enzyme. Urheberrechtlich geschütztes Material. Lernkarteikarten Veterinärmedizin - BIOCHEMIE
 Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
9. Abbau der Glukose zum Pyruvat
 9. Abbau der Glukose zum Pyruvat 236 9.1. Übersicht: Abbau von Glucose Pentosephosphate Pathway (PPP) NADP + NADPH Glucose Glycolysis Oxidative Phosphorylation PDH Complex Citric Acid Citric Acid Cycle
9. Abbau der Glukose zum Pyruvat 236 9.1. Übersicht: Abbau von Glucose Pentosephosphate Pathway (PPP) NADP + NADPH Glucose Glycolysis Oxidative Phosphorylation PDH Complex Citric Acid Citric Acid Cycle
Inhaltsverzeichnis. Organische Chemie und Biochemie 1. Proteine und Peptide 23. Enzyme 47. Coenzyme 71
 Inhaltsverzeichnis Organische Chemie und Biochemie 1 1. Die chemische Bindung 1 2. Das Wasser 2 3. Der Kohlenwasserstoff als Grandkörper 4 4. Die funktionellen Gruppen 6 5. Biochemisch wichtige Reaktionen
Inhaltsverzeichnis Organische Chemie und Biochemie 1 1. Die chemische Bindung 1 2. Das Wasser 2 3. Der Kohlenwasserstoff als Grandkörper 4 4. Die funktionellen Gruppen 6 5. Biochemisch wichtige Reaktionen
Reaktionen der Zellatmung (1)
 ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
Kohlenhydrate. spielen in der Natur eine sehr wichtige Rolle. dienen als Energiespeicher: Stärke, Glykogen
 Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
BIOCHEMIE. Prof. Manfred SUSSITZ. über(be)arbeitet und zusammengestellt nach Internetvorlagen:
 BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
Auswahlverfahren Medizin Prüfungsgebiet Chemie. 6.Termin Organische Chemie Naturstoffe
 Auswahlverfahren Medizin Prüfungsgebiet Chemie 6.Termin Organische Chemie Naturstoffe Kursleiter Mag. Wolfgang Mittergradnegger IFS Kurs 2009 Organische Chemie Naturstoffe Fette Kohlenhydrate Proteine
Auswahlverfahren Medizin Prüfungsgebiet Chemie 6.Termin Organische Chemie Naturstoffe Kursleiter Mag. Wolfgang Mittergradnegger IFS Kurs 2009 Organische Chemie Naturstoffe Fette Kohlenhydrate Proteine
Enzyme SPF BCH am
 Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
- Biochemieklausur Name: Matrikelnr.:
 08.07.20 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
08.07.20 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Inhaltsverzeichnis. Proteins 37. Organisch Gftersi zr.ü??-3shq^is 1
 Inhaltsverzeichnis Organisch Gftersi zr.ü??-3shq^is 1 1. Die chemische Bindung 1 2. Das Wasser 2 3. Der Kohlenwasserstoff als Grundkörper 3 4. Die funktionellen Gruppen 6 5. Biochemisch wichtige Reaktionen
Inhaltsverzeichnis Organisch Gftersi zr.ü??-3shq^is 1 1. Die chemische Bindung 1 2. Das Wasser 2 3. Der Kohlenwasserstoff als Grundkörper 3 4. Die funktionellen Gruppen 6 5. Biochemisch wichtige Reaktionen
-Klausur Biochemie Name:
 -Klausur Biochemie -0.02.6 Name: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
-Klausur Biochemie -0.02.6 Name: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
8. Tutorium AMB/OBOE
 8. Tutorium AMB/OBOE 15.12.05 4.13 Welches Begriffspaar vervollständigt folgenden Satz über funktionelle Gruppen in der organischen Chemie. Carboxyl verhält sich zu wie zu Base. a) Säure... Carboxyl b)
8. Tutorium AMB/OBOE 15.12.05 4.13 Welches Begriffspaar vervollständigt folgenden Satz über funktionelle Gruppen in der organischen Chemie. Carboxyl verhält sich zu wie zu Base. a) Säure... Carboxyl b)
Basiswissen Ernährungslehre
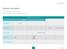 Basiswissen Ernährungslehre Hauptnährstoffgruppen und bioaktive Substanzen Ergänze folgende Übersicht zu den natürlichen Bestandteilen der Nahrung Natürliche Bestandteile der Nahrung Nährstoffe Funktionsgruppen
Basiswissen Ernährungslehre Hauptnährstoffgruppen und bioaktive Substanzen Ergänze folgende Übersicht zu den natürlichen Bestandteilen der Nahrung Natürliche Bestandteile der Nahrung Nährstoffe Funktionsgruppen
Fragen zur Vorlesung Grundlagen der Biologie (I) Teil 1: Biomoleküle (B. Moerschbacher)
 Fragen zur Vorlesung Grundlagen der Biologie (I) Teil 1: Biomoleküle (B. Moerschbacher) Wieviele Elektronen, Protonen und Neutronen besitzt ein Kohlenstoffatom? Wie unterscheiden sich die Kohlenstoffisotope
Fragen zur Vorlesung Grundlagen der Biologie (I) Teil 1: Biomoleküle (B. Moerschbacher) Wieviele Elektronen, Protonen und Neutronen besitzt ein Kohlenstoffatom? Wie unterscheiden sich die Kohlenstoffisotope
Stoffwechselphysiologie. Zusammenfassung für das mündliche Abitur
 Naturwissenschaft Sarah Fuhrken Stoffwechselphysiologie. Zusammenfassung für das mündliche Abitur Zusammenfassung Stoffwechselphysiologie Lernzettel Biologie, 1. Semester Brown sche Molekularbewegung:
Naturwissenschaft Sarah Fuhrken Stoffwechselphysiologie. Zusammenfassung für das mündliche Abitur Zusammenfassung Stoffwechselphysiologie Lernzettel Biologie, 1. Semester Brown sche Molekularbewegung:
Schrittweise Oxidation und Decarboxylierung von Glucose-6-phosphat zu Ribulose-5- phosphat
 1. Der plastidäre oxidative Pentosephosphatweg Abbau von Hexose unter NADPH+H + -Synthese Schlüsselenzym=Glucose-6-phosphat-Dehydrogenase Glucose-6-phosphat-Dehydrogenase wird durch Thioredoxin im reduzierten
1. Der plastidäre oxidative Pentosephosphatweg Abbau von Hexose unter NADPH+H + -Synthese Schlüsselenzym=Glucose-6-phosphat-Dehydrogenase Glucose-6-phosphat-Dehydrogenase wird durch Thioredoxin im reduzierten
1) Zu jedem der 11 Kapitel gibt es 10 Fragen in diesem Fragenkatalog.
 FRAGENKATALOG 1 1) Zu jedem der 11 Kapitel gibt es 10 Fragen in diesem Fragenkatalog. 3) Bei der schriftlichen Prüfung kommt je eine Frage aus 10 der 11 Kapitel (10 Hauptfragen), plus eine Zusatzaufgabe.
FRAGENKATALOG 1 1) Zu jedem der 11 Kapitel gibt es 10 Fragen in diesem Fragenkatalog. 3) Bei der schriftlichen Prüfung kommt je eine Frage aus 10 der 11 Kapitel (10 Hauptfragen), plus eine Zusatzaufgabe.
1) Erklären sie die Begriffe Primär Sekundär und Tertiärstruktur von Proteinen. Nennen Sie drei typische Sekundärstrukturelemente (6P)
 1. Klausur zum Modul 5.3 Biochemie WS 09/10 12.2.2010 1) Erklären sie die Begriffe Primär Sekundär und Tertiärstruktur von Proteinen. Nennen Sie drei typische Sekundärstrukturelemente (6P) 2) Welche Funktion
1. Klausur zum Modul 5.3 Biochemie WS 09/10 12.2.2010 1) Erklären sie die Begriffe Primär Sekundär und Tertiärstruktur von Proteinen. Nennen Sie drei typische Sekundärstrukturelemente (6P) 2) Welche Funktion
Gluconeognese Neusynthese von Glucose aus Pyruvat
 Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
PROTEINBIOSYNTHESE "Das zentrale Dogma der Molekularbiologie"
 PROTEINBIOSYNTHESE "Das zentrale Dogma der Molekularbiologie" Die für die Synthese von Eiweißstoffen notwendigen Schritte sind: (1) Replikation der DNA: Vor jeder Zellteilung wird die gesamte zelluläre
PROTEINBIOSYNTHESE "Das zentrale Dogma der Molekularbiologie" Die für die Synthese von Eiweißstoffen notwendigen Schritte sind: (1) Replikation der DNA: Vor jeder Zellteilung wird die gesamte zelluläre
Citratzyklus. Citratzyklus
 Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Proteinogene Aminosäuren. Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren
 Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Lipide. Dr. med. Tamás Pándics. Biochemie I. SEMMELWEIS UNIVERSITÄT Institut für Medizinische Biochemie
 Lipide Biochemie I Dr. med. Tamás Pándics SEMMELWEIS UNIVERSITÄT Institut für Medizinische Biochemie Lipide Definition: hydrophobe Biomoleküle Heterogene Gruppe mit abwechslungsreichen Funktionen: Bestandteile
Lipide Biochemie I Dr. med. Tamás Pándics SEMMELWEIS UNIVERSITÄT Institut für Medizinische Biochemie Lipide Definition: hydrophobe Biomoleküle Heterogene Gruppe mit abwechslungsreichen Funktionen: Bestandteile
Einführung in die Biochemie Glykolyse
 Glykolyse Der Abbau der Glukose beginnt beim aeroben und beim anaeroben Abbau nach dem gleichen rinzip, der Glykolyse. Dabei wird Brenztraubensäure (2-Ketopropansäure) gebildet. Die Glykolyse ist die erste
Glykolyse Der Abbau der Glukose beginnt beim aeroben und beim anaeroben Abbau nach dem gleichen rinzip, der Glykolyse. Dabei wird Brenztraubensäure (2-Ketopropansäure) gebildet. Die Glykolyse ist die erste
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
-Klausur Biochemie Name: Matrikelnr.:
 25.07.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
25.07.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Der Stoffwechsel. Wir zeigen dir wie er funktioniert.
 Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Guter Stoffwechsel, schlechter Stoffwechsel, der Stoffwechsel schläft, den Stoffwechsel ankurbeln,
Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Guter Stoffwechsel, schlechter Stoffwechsel, der Stoffwechsel schläft, den Stoffwechsel ankurbeln,
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne
 Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Regulation der Glykolyse: Phosphofructokinase
 Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne
 Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Pentosephosphatzyklus. Synonym: Hexosemonophosphatweg
 Pentosephosphatzyklus Synonym: Hexosemonophosphatweg Gliederung Funktion & Lokalisation Grundgerüst des Ablaufs Anpassung an Stoffwechselsituation Regelung Beispielreaktion Funktion & Lokalisation Gewinnung
Pentosephosphatzyklus Synonym: Hexosemonophosphatweg Gliederung Funktion & Lokalisation Grundgerüst des Ablaufs Anpassung an Stoffwechselsituation Regelung Beispielreaktion Funktion & Lokalisation Gewinnung
Der Fettsäurestoffwechsel. Basierend auf Stryer Kapitel 22
 Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
«Ausdauertraining» Naturwissenschaftliche Aspekte
 EHSM / Trainerbildung Jost Hegner Was verstehen wir unter «Leistung» im pädagogischen Sinne? unter «Leistung» im physikalischen Sinne: Power (in Joule/s; Watt)? unter «Leistung» im physiologischen Sinne:
EHSM / Trainerbildung Jost Hegner Was verstehen wir unter «Leistung» im pädagogischen Sinne? unter «Leistung» im physikalischen Sinne: Power (in Joule/s; Watt)? unter «Leistung» im physiologischen Sinne:
schnell und portofrei erhältlich bei
 Kurzlehrbuch Biochemie Kurzlehrbuch Biochemie Bearbeitet von Melanie Königshoff, Timo Brandenburger 2. überarb. Aufl. 2007. Taschenbuch. 46 S. Paperback ISBN 978 3 13 136412 8 Format (B x L): 24 x 17 cm
Kurzlehrbuch Biochemie Kurzlehrbuch Biochemie Bearbeitet von Melanie Königshoff, Timo Brandenburger 2. überarb. Aufl. 2007. Taschenbuch. 46 S. Paperback ISBN 978 3 13 136412 8 Format (B x L): 24 x 17 cm
LIPIDE. Periphere Gruppe mit Cysteinylrest. FS-Synthase. Zentrale Gruppe Phosphopanthetinarm kovalente Bindung
 Periphere Gruppe mit Cysteinylrest FS-Synthase Zentrale Gruppe Phosphopanthetinarm kovalente Bindung Die FS-Biosynthse aus Acetyl-CoA und Malonyl-CoA, wird komplett an dem dimeren Multienzymkomplex FETTSÄURESYNTHETASE
Periphere Gruppe mit Cysteinylrest FS-Synthase Zentrale Gruppe Phosphopanthetinarm kovalente Bindung Die FS-Biosynthse aus Acetyl-CoA und Malonyl-CoA, wird komplett an dem dimeren Multienzymkomplex FETTSÄURESYNTHETASE
STRUKTUR UND FUNKTION DER PFLANZE :00
 NAME: e-mail: Matr.Nr.: Studienkennz.: STRUKTUR UND FUNKTION DER PFLANZE 16.05.2007 14:00 1. Die Organellen, in den Photosynthese stattfindet, bezeichnet man als. Die Grundsubstanz nennt man...., die Membransysteme.....
NAME: e-mail: Matr.Nr.: Studienkennz.: STRUKTUR UND FUNKTION DER PFLANZE 16.05.2007 14:00 1. Die Organellen, in den Photosynthese stattfindet, bezeichnet man als. Die Grundsubstanz nennt man...., die Membransysteme.....
In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit
 In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit in der Nucleotidsequenz der DNA verschlüsselt (codiert)
In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit in der Nucleotidsequenz der DNA verschlüsselt (codiert)
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
1. Biochemie-Klausur Zahnmediziner, WS 03/04
 1. Biochemie-Klausur Zahnmediziner, WS 03/04 1. Welche Aussage zur ß-Oxidation von Fettsäuren in Peroxisomen ist falsch? A) Die Aufnahme langkettiger Fettsäuren in die Peroxisomen erfolgt Carnitin-unabhängig!
1. Biochemie-Klausur Zahnmediziner, WS 03/04 1. Welche Aussage zur ß-Oxidation von Fettsäuren in Peroxisomen ist falsch? A) Die Aufnahme langkettiger Fettsäuren in die Peroxisomen erfolgt Carnitin-unabhängig!
Taschenatlas Biochemie des Menschen
 Taschenatlas Biochemie des Menschen Bearbeitet von Jan Koolman, Klaus-Heinrich Röhm 4., vollständig überarbeitete und erweiterte Auflage 2009. Buch. XII, 529 S. Kartoniert ISBN 978 3 13 759404 8 Format
Taschenatlas Biochemie des Menschen Bearbeitet von Jan Koolman, Klaus-Heinrich Röhm 4., vollständig überarbeitete und erweiterte Auflage 2009. Buch. XII, 529 S. Kartoniert ISBN 978 3 13 759404 8 Format
Stoffklasse: LIPIDE Funktionen in der Zelle
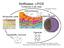 Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
Übungsfragen Biochemie 1. Erklären Sie die Begriffe
 Übungsfragen Biochemie 1 Erklären Sie die Begriffe Adsorption Diffusion Dialyse Enantiomere Diastereomere Verseifung Fett Lipid essentielle Fettsäure essentielle Aminosäure Kohlenhydrat Disaccharid Peptid
Übungsfragen Biochemie 1 Erklären Sie die Begriffe Adsorption Diffusion Dialyse Enantiomere Diastereomere Verseifung Fett Lipid essentielle Fettsäure essentielle Aminosäure Kohlenhydrat Disaccharid Peptid
Folsäure. Struktur = Pteroylglutamat; PteGLU n
 Folsäure Struktur = Pteroylglutamat; PteGLU n Biochemische Wirkungsweise Übertragung von C1-Einheiten; Wirksame Form ist das Tetrahydrofolat (H 4 -Folat), das durch Serin in das N 5,N 10 -Methylentetrahydrofolat
Folsäure Struktur = Pteroylglutamat; PteGLU n Biochemische Wirkungsweise Übertragung von C1-Einheiten; Wirksame Form ist das Tetrahydrofolat (H 4 -Folat), das durch Serin in das N 5,N 10 -Methylentetrahydrofolat
Mechanismen der ATP Synthese in Mitochondrien
 Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Hast du dich schon mal gefragt, wie aus dem Essen in deinem Mund eigentlich Energie wird und wie du das am effizientesten für dich nutzen kannst?
 Hast du dich schon mal gefragt, wie aus dem Essen in deinem Mund eigentlich Energie wird und wie du das am effizientesten für dich nutzen kannst? Dann ist diese Grundlagenreihe zum Stoffwechsel und Energiegewinnung
Hast du dich schon mal gefragt, wie aus dem Essen in deinem Mund eigentlich Energie wird und wie du das am effizientesten für dich nutzen kannst? Dann ist diese Grundlagenreihe zum Stoffwechsel und Energiegewinnung
Wiederholungsklausur zur Vorlesung Biochemie IV im SS 2000
 Wiederholungsklausur zur Vorlesung Biochemie IV im SS 2000 am 15.11.2000 von 13.45 15.15 Uhr (insgesamt 100 Punkte, mindestens 50 erforderlich) Bitte Name, Matrikelnummer und Studienfach 1. Wie erfolgt
Wiederholungsklausur zur Vorlesung Biochemie IV im SS 2000 am 15.11.2000 von 13.45 15.15 Uhr (insgesamt 100 Punkte, mindestens 50 erforderlich) Bitte Name, Matrikelnummer und Studienfach 1. Wie erfolgt
I. Zellatmung. =Abbau von Kohlenhydraten unter Sauerstoffverbrauch (aerob) KH + O 2 --> CO 2 + H 2 O + Energie
 KATABOLISMUS Abbau komplexer organischer Moleküle (reich an Energie) zu einfacheren (mit weniger Energie). Ein Teil der Energie wird genutzt um Arbeit zu verrichten (Zelle erhalten, Wachstum) I. Zellatmung
KATABOLISMUS Abbau komplexer organischer Moleküle (reich an Energie) zu einfacheren (mit weniger Energie). Ein Teil der Energie wird genutzt um Arbeit zu verrichten (Zelle erhalten, Wachstum) I. Zellatmung
SPEYER-KOLLEG AUGUST 2003 FACHKONFERENZ CHEMIE / BIOLOGIE
 STOFFPLAN CHEMIE GRUNDKURS 1. Halbjahr (K 1) 1. ATOMMODELL Kern- / Hülle-Modell (nach Bohr / Sommerfeld vereinfacht) Ergebnisse des "Wellenmechanischen Atommodells" Quantenzahlen, "Orbitale"(s-, p-, d-)
STOFFPLAN CHEMIE GRUNDKURS 1. Halbjahr (K 1) 1. ATOMMODELL Kern- / Hülle-Modell (nach Bohr / Sommerfeld vereinfacht) Ergebnisse des "Wellenmechanischen Atommodells" Quantenzahlen, "Orbitale"(s-, p-, d-)
Einführung in die Biochemie Wirkungsweise von Enzymen
 Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion. Mag. Gerald Trutschl
 Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Inhaltsverzeichnis. Einleitung...1
 Inhaltsverzeichnis Einleitung...1 1 Terpene...5 1.1 Monoterpene...6 1.2 Sesquiterpene...19 1.3 Diterpene...26 1.4 Sesterterpene...33 1.5 Triterpene...33 1.6 Tetraterpene...39 1.7 Polyisoprene...42 1.8
Inhaltsverzeichnis Einleitung...1 1 Terpene...5 1.1 Monoterpene...6 1.2 Sesquiterpene...19 1.3 Diterpene...26 1.4 Sesterterpene...33 1.5 Triterpene...33 1.6 Tetraterpene...39 1.7 Polyisoprene...42 1.8
Grundlagen der Molekularen Biophysik WS 2011/12 (Bachelor) Dozent: Prof Dr. Ulrike Alexiev (R , Tel /Sekretariat Frau Endrias Tel.
 Grundlagen der Molekularen Biophysik WS 2011/12 (Bachelor) Dozent: Prof Dr. Ulrike Alexiev (R.1.2.34, Tel. 55157/Sekretariat Frau Endrias Tel. 53337) Tutoren: Dr. Kristina Kirchberg, Alex Boreham 6-stündig
Grundlagen der Molekularen Biophysik WS 2011/12 (Bachelor) Dozent: Prof Dr. Ulrike Alexiev (R.1.2.34, Tel. 55157/Sekretariat Frau Endrias Tel. 53337) Tutoren: Dr. Kristina Kirchberg, Alex Boreham 6-stündig
