GEBRAUCHSANLEITUNG EMBLEM S-ICD. Subkutane Elektrode REF 3401
|
|
|
- Georg Dresdner
- vor 5 Jahren
- Abrufe
Transkript
1 GEBRAUCHSANLEITUNG EMBLEM S-ICD Subkutane Elektrode REF 3401
2
3 Inhaltsverzeichnis GEBRAUCHSANWEISUNG...1 Beschreibung...1 Weitere Informationen...1 Informationen zur bedingten MRT-Tauglichkeit des Systems...1 Indikationen...2 Kontraindikationen...3 Warnhinweise...3 Vorsichtsmaßnahmen...5 Potentielle Nebenwirkungen...7 Garantie...9 INFORMATIONEN VOR DER IMPLANTATION...9 Vorbereitung der Implantation...9 Verpackungsinhalt...9 Zubehör...9 IMPLANTATION Überblick NACH DER IMPLANTATION Nachsorgeverfahren nach der Implantation Explantation SPEZIFIKATION Subkutane EMBLEM S-ICD-Elektrode Spezifikationen Definition der Symbole auf dem Verpackungsetikett... 16
4 [1] Nahtloch, [2] distale Wahrnehmungselektrode, [3] Defibrillationswendel, [4] proximale Wahrnehmungselektrode, [5] Terminalelektrodenstecker für proximale Wahrnehmungselektrode, [6] SQ-1 S-ICD-Stecker (vom Standard abweichend), [7] Terminalelektrodenstecker für Defibrillationswendel, [8] Anschlussstift (Elektrodenstecker für distale Wahrnehmungselektrode) Dieses Produkt ist u. U. durch eines oder mehrere Patente geschützt. Patentinformationen erhalten Sie unter Folgende Marken sind Marken der Boston Scientific Corporation oder ihrer Tochtergesellschaften: EMBLEM,IMAGEREADY.
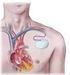
5 GEBRAUCHSANWEISUNG Beschreibung Die subkutane Elektrode EMBLEM S-ICD (die subkutane Elektrode ) ist eine Komponente des S-ICD Systems von Boston Scientific, die Patienten verschrieben wird, wenn die Behandlung von Herzrhythmusstörungen angezeigt ist. Das S-ICD System erkennt kardiale Aktivitäten und verabreicht eine Defibrillationstherapie. Die subkutane Elektrode wird so implantiert, dass der distale Teil parallel zum linken Sternumrand liegt und das proximale Ende über einen SQ-1 S-ICD-Stecker mit einem EMBLEM S-ICD System-Aggregat verbunden wird 1. Die subkutane Elektrode ist auch mit dem Aggregat Cameron Health Modell 1010 SQ-RX kompatibel. Die subkutane Elektrode umfasst eine Hochspannungs-Schockelektroden-Coil zur Bereitstellung der Defibrillationsenergie. Die Schockelektrode besteht aus Multifilaren aus Metalldraht, geformt in eine Defibrillationswendel von 8 cm Länge. Die Defibrillation erfolgt zwischen der Coil an der subkutanen Elektrode und dem elektrisch leitenden Aggregat-Gehäuse. Die subkutane Elektrode umfasst auch proximale und distale Detektions- Ringelektroden. Diese Wahrnehmungselektroden verwenden metallische Schläuche, die mechanisch am subkutanen Elektrodenkörper angebracht sind. Die Detektion erfolgt zwischen den beiden elektrisch leitenden Ringen an der subkutanen Elektrode oder zwischen einem der Ringe an der subkutanen Elektrode und dem elektrisch leitenden Aggregat-Gehäuse. Weitere Informationen Die Anweisungen in dieser Gebrauchsanweisung sollten in Verbindung mit anderen Referenzen verwendet werden, dazu gehören auch die entsprechenden Gebrauchsanweisungen des S-ICD-Aggregats und die Gebrauchsanweisung der Elektroden-Einführhilfe. Informationen zu MRT-Scans finden Sie im technischen MRT-Leitfaden zum ImageReady S-ICD System des Typs MRT tauglich (im Folgenden als Technischer Leitfaden MRT bezeichnet). ZIELGRUPPE Diese Dokumentation ist für Fachleute vorgesehen, die in der Implantation von Geräten und/oder in der Durchführung von Gerätenachsorgen geschult wurden oder darin erfahren sind. Informationen zur bedingten MRT-Tauglichkeit des Systems Eine subkutane Elektrode von Boston Scientific/Cameron Health kann als Teil des ImageReady S-ICD Systems verwendet werden, wenn eine Verbindung zu einem MRT-tauglichen S-ICD-Aggregat besteht. Patienten mit einem MRT- 1. SQ-1 ist ein vom Standard abweichender Stecker, den es nur beim S-ICD System gibt 1
6 tauglichen S-ICD System können einem MRT-Scan unterzogen werden, wenn alle Nutzungsbedingungen des Technischen Leitfadens MRT erfüllt sind. Zu den Komponenten, die den bedingt MRT-tauglichen Status benötigen, gehören bestimmte S-ICD-Aggregat-Modelle, Elektroden und Zubehör von Boston Scientific sowie das Programmiergerät und die Softwareanwendung zur Programmierung. Die Modellnummern des MRT-tauglichen S-ICD Aggregats und der Komponenten sowie eine vollständige Beschreibung des ImageReady S-ICD Systems finden Sie im Technischen Leitfaden MRT. Eine umfassende Liste von Warnhinweisen, Vorsichtsmaßnahmen und Nutzungsbedingungen für MRT-Scans von Patienten mit einem implantierten ImageReady-S-ICD System finden Sie im Technischen Leitfaden MRT. MRT-Nutzungsbedingungen bei implantierten Elektroden Die folgende Untergruppe der MRT-Nutzungsbedingungen gilt für die Implantation und dient als Leitfaden, um sicherzustellen, dass ein vollständiges ImageReady S-ICD System implantiert wird. Eine vollständige Liste der Vorsichtsmaßnahmen, Nutzungsbedingungen und potenziellen Nebenwirkungen, die bei erfüllten bzw. nicht erfüllten Nutzungsbedingungen gelten, sind im Technischen Leitfaden MRT enthalten. Alle Punkte der vollständigen Liste der Nutzungsbedingungen müssen erfüllt sein, damit ein MRT-Scan als MRT-tauglich gelten kann. Dem Patienten wurde ein ImageReady S-ICD System implantiert Es sind keine anderen aktiven oder aufgegebenen implantierten Geräte, Komponenten oder Zubehörteile vorhanden, darunter beispielsweise Elektrodenadapter, Verlängerungen, Elektroden oder Aggregate Der Patient ist nach Beurteilung klinisch in der Lage, über die gesamte Dauer, in der sich das Aggregat im MRT-Schutz-Modus befindet, ohne Tachykardie-Schutz auszukommen Implantation und/oder Neueinsetzen der Elektroden oder Nachoperation des ImageReady S-ICD Systems liegt mindestens sechs (6) Wochen zurück Keine Anzeichen für Elektrodenbruch oder Schädigung der Integrität des Aggregat-Elektroden-Systems HINWEIS: Aufgrund anderer implantierter Geräte oder Patientenzustände kann ein Patient für einen MRT-Scan ungeeignet sein, unabhängig vom Status des ImageReady S-ICD Systems. Indikationen Das S-ICD System wurde entwickelt, um eine Defibrillationstherapie zur Behandlung von lebensbedrohlichen ventrikulären Tachyarrhythmien bei Patienten durchzuführen, die keine symptomatische Bradykardie, unablässige ventrikuläre Tachykardie oder spontane, häufig wiederkehrende ventrikuläre Tachykardie haben, die zuverlässig mit Antitachykardiestimulation beendet wird. 2
7 Kontraindikationen Unipolare Stimulation und impedanzbasierte Funktionen sind für die Verwendung mit dem S-ICD System kontraindiziert. WARNHINWEISE HINWEIS: Lesen und befolgen Sie vor der Verwendung des S-ICD Systems alle Warnhinweise und Vorsichtsmaßnahmen, die in der entsprechenden Gebrauchsanweisung für das EMBLEM S-ICD-Aggregat angegeben sind. Allgemein Kenntnis der Produktliteratur. Lesen Sie dieses Handbuch aufmerksam durch, bevor Sie das S-ICD System verwenden, um Schäden am Aggregat und/oder der subkutanen Elektrode zu vermeiden. Solche Schäden können zu Verletzungen oder zum Tod des Patienten führen. Nur für den Gebrauch bei einem einzigen Patienten. Nicht zur Wiederverwendung, Wiederaufbereitung oder Resterilisierung. Die Wiederverwendung, Wiederaufbereitung oder Resterilisierung kann die strukturelle Integrität des Geräts beeinträchtigen und/oder zu Funktionsstörungen des Geräts führen, was wiederum Verletzung, Krankheit oder Tod des Patienten zur Folge haben kann. Wiederverwendung, Aufbereitung oder Resterilisation können außerdem ein Kontaminationsrisiko für das Gerät darstellen und/oder Infektionen beim Patienten oder Kreuzinfektionen verursachen, u. a. die Übertragung von Infektionserkrankungen von einem Patienten auf einen anderen. Die Kontaminierung des Geräts kann zu Verletzung, Erkrankung oder Tod von Patienten führen. Kompatibilität der Komponente. Alle implantierbaren Komponenten von Boston Scientific S-ICD wurden nur für die Verwendung mit dem Boston Scientific oder Cameron Health S-ICD System entwickelt. Die Verbindung einer S-ICD System-Komponente mit einer nichtkompatiblen Komponente wurde nicht getestet und kann dazu führen, dass die lebensrettende Defibrillationstherapie fehlschlägt. Backup mit externem Defibrillator. Halten Sie während der Implantation und der Nachsorgetests immer externe Defibrillationssysteme sowie in HLW geschultes medizinisches Personal bereit. Falls eine induzierte ventrikuläre Tachyarrhythmie nicht rechtzeitig terminiert wird, kann dies zum Tod des Patienten führen. Handhabung Richtige Handhabung. Handhaben Sie die Komponenten des S-ICD Systems immer vorsichtig, und achten Sie dabei auf Sterilität. Falls diese Richtlinien nicht eingehalten werden, kann dies zu Verletzung, Erkrankung oder Tod von Patienten führen. Achten Sie darauf, dass Sie die Komponenten nicht beschädigen. Achten Sie darauf, dass Sie die Komponenten des S-ICD Systems nicht verändern, einschneiden, zerdrücken, überdehnen oder auf andere Weise beschädigen. Eine Beschädigung des S-ICD Systems kann zu einer 3
8 unangebrachten Schockabgabe oder fehlgeschlagenen Therapie für den Patienten führen. Handhabung der subkutanen Elektrode. Handhaben Sie den Stecker der subkutanen Elektrode vorsichtig. Vermeiden Sie jeglichen Kontakt des Steckers mit chirurgischen Instrumenten wie Pinzetten, Gefäßklemmen oder Klemmwerkzeugen. Der Stecker könnte beschädigt werden. Schäden am Stecker können zu einer Beeinträchtigung der Dichtungseigenschaften und somit zu einer gestörten Detektion, einem Therapieverlust oder der Abgabe einer unangemessenen Therapie führen. Implantation Armpositionierung. Es muss auf die Platzierung des Arms auf Seite des Geräteimplantats geachtet werden, um eine Verletzung des Nervus ulnaris und des Plexus brachialis zu vermeiden, wenn sich der Patient während der Geräteimplantation und vor VF-Induktion oder Schockabgabe, in supiner Lage befindet. Während der Implantationsphase des Verfahrens muss der Arm abduziert werden (Winkel höchstens 60 ), wobei sich die Hand in supiner Lage (Handfläche nach oben) befindet. Es ist übliche Praxis, den Arm an einem Armbrett zu befestigen, um die Position während der Geräteimplantation zu erhalten. Fixieren Sie den Arm bei Defibrillationstests nicht zu eng. Eine Höherlegung des Torsos durch Stützen kann die Schultergelenke ebenfalls belasten und sollte während Defibrillationstests vermieden werden. Systemmigration. Verwenden Sie geeignete Verankerungstechniken, wie im Implantationsverfahren beschrieben, um eine Dislokation und/oder Verschiebung des S-ICD Systems zu vermeiden. Die Dislokation und/oder Verschiebung des S-ICD Systems kann zu einer unangebrachten Schockabgabe oder fehlgeschlagenen Therapie für den Patienten führen. Die Implantation muss außerhalb der Zone III des MRT-Standorts erfolgen. Die Implantation des Systems darf nicht in Bereichen durchgeführt werden, die in den Richtlinien des American College of Radiology für sichere MRT-Praktiken (Guidance Document for Safe MR Practices) 2 als Zone III (oder höher) definiert werden. Einige Zubehörteile, die mit dem Aggregat und den Elektroden verwendet werden, wie z. B. Drehmoment-Schraubendreher und Werkzeuge zur Implantation der Elektroden, sind nicht bedingt MRT-tauglich und dürfen nicht im MRT- Untersuchungsraum, Kontrollraum oder in Zone III oder IV des MRT- Standorts verwendet werden. Nach der Implantation Diathermie. Führen Sie keine Diathermiebehandlung an Patienten mit einem implantierten S-ICD System durch. Die Interaktion der Diathermie- Therapie mit einem implantierten S-ICD-Aggregat oder -Elektrode kann Aggregat beschädigen und den Patienten verletzen. Einfluss der Magnetresonanztomographie (MRT). Werden nicht alle MRT-Nutzungsbedingungen (wie im Technischen Leitfaden MRT beschrieben) eingehalten, erfüllt die MRT-Untersuchung eines Patienten 2. Kanal E, et al., American Journal of Roentgenology 188: ,
9 nicht die MRT-Nutzungsanforderungen für das implantierte System und kann signifikante Verletzungen oder den Tod des Patienten und/oder die Beschädigung des implantierten Systems zur Folge haben. Potentielle Nebenwirkungen, die eintreten können, wenn die Nutzungsbedingungen eingehalten bzw. nicht eingehalten werden, sowie eine vollständige Liste der Warnhinweise und Vorsichtsmaßnahmen in Bezug auf die MRT-Tauglichkeit sind im Technischen Leitfaden MRT aufgeführt. VORSICHTSMASSNAHMEN Klinische Überlegungen Verwendung in der Pädiatrie. Die Verwendung des S-ICD Systems in der Pädiatrie wurde noch nicht untersucht. Verfügbare Therapien. Das S-ICD System bietet keine Langzeit- Bradykardiestimulation, Cardiale Resynchronisationstherapie (CRT) oder Antitachykardiestimulation (ATP). Sterilisation und Lagerung Falls die Verpackung beschädigt ist. Die Blisterschalen und der Inhalt werden vor dem letzten Verpacken mit Ethylenoxidgas sterilisiert. Wenn Sie das Aggregat und/oder die subkutane Elektrode erhalten, ist es/sie steril, wenn die Verpackung intakt ist. Wenn die Verpackung nass, durchlöchert, geöffnet oder anderweitig beschädigt ist, schicken Sie das Aggregat und/oder die subkutane Elektrode an Boston Scientific zurück. Verwendbar bis -Datum. Das Aggregat und/oder die subkutane Elektrode muss bis zum auf der Verpackung angegebenen VERWENDBAR BIS-Datum implantiert werden, da dieses Datum eine gesicherte Haltbarkeitsdauer angibt. Wenn das Datum beispielsweise 1. Januar lautet, darf das Produkt ab dem 2. Januar nicht mehr implantiert werden. Lagerungstemperatur. Der empfohlene Lagerungstemperaturbereich liegt zwischen -18 C und +55 C (0 F bis +131 F). Implantation Herstellen des subkutanen Tunnels. Verwenden Sie bei der Implantation und Positionierung der subkutanen Elektrode nur Werkzeug und Zubehör von Boston Scientific, das zur Implantation der subkutanen Elektrode ausgelegt ist, um die subkutanen Tunnel herzustellen. Vermeiden Sie die Tunnelierung in der Nähe anderer subkutan implantierter medizinischer Geräte oder Komponenten, zum Beispiel einer implantierbaren Insulinpumpe, Arzneimittelpumpe, Sternumdrähten aus vorherigen Sternotomien oder einem Herzunterstützungssystem. Länge des oberen Tunnels. Stellen Sie sicher, dass der obere Tunnel lang genug für den Abschnitt der Elektrode von der distalen Spitze bis zur Nahtmanschette ist, sodass der Defibrillationswendel nicht geknickt oder gekrümmt wird. Ein Knick oder eine Krümmung des Defibrillationswendels im oberen Tunnel kann zu einer beeinträchtigten Detektion und/oder 5
10 Therapieabgabe führen. Nach Einführen der Elektrode in den oberen Tunnel können Sie mittels Röntgen oder Durchleuchtung bestätigen, dass kein Knick bzw. keine Krümmung vorliegt. Nahtposition. Vernähen Sie nur die Bereiche, die in den Anweisungen zur Implantation angegeben sind. Vernähen Sie keinesfalls direkt über dem subkutanen Elektrodenkörper. Es darf nicht direkt über dem subkutanen Elektrodenkörper genäht werden, da dies zu strukturellen Beschädigungen führen kann. Verwenden Sie die Nahtmanschette, um eine Bewegung der subkutanen Elektrode zu vermeiden. Die subkutane Elektrode nicht am Übergang zum Elektrodenanschlussblock knicken. Führen Sie den Anschlussstecker der subkutanen Elektrode gerade in den Anschluss des Aggregats ein. Die subkutane Elektrode nicht am Übergang zum Anschlussblock der subkutanen Elektrode knicken. Falsches Einführen kann die Isolation oder den Stecker beschädigen. Sternum-Drähte. Wenn Sie das S-ICD System bei einem Patienten mit Sternum-Drähten implantieren, stellen Sie sicher, dass die Sternum- Drähte nicht mit den distalen und proximalen Detektions-Elektroden in Kontakt geraten (zum Beispiel durch Verwendung von Fluoroskopie). Wenn zwischen einer Detektions-Elektrode und einem Sternum-Draht ein Metall mit Metall in Kontakt gerät, kann die Detektion beeinträchtigt werden. Falls erforderlich, sollten Sie einen neuen Tunnel für die Elektrode herstellen, um eine ausreichende Trennung zwischen den Detektions- Elektroden und Sternum-Drähten sicherzustellen. Krankenhaus und medizinische Einrichtungen Externe Defibrillation. Eine externe Defibrillation oder Kardioversion kann das Aggregat oder die subkutane Elektrode beschädigen. Um eine Beschädigung der implantierten Systemkomponenten zu vermeiden, berücksichtigen Sie folgende Punkte: Platzieren Sie keine Defibrillationselektroden (oder Paddles) direkt über dem Aggregat oder der subkutanen Elektrode. Platzieren Sie die Defibrillationselektroden (oder Paddles) so weit von den implantierten Systemkomponenten entfernt wie möglich. Stellen Sie die Energie des externen Defibrillators auf einen möglichst geringen, klinisch akzeptablen Wert ein. Überprüfen Sie nach einer externen Kardioversions- oder Defibrillationsepisode die Funktion des Aggregats (empfohlene Nachsorgemaßnahmen für die Zeit nach der Therapie finden Sie in der Gebrauchsanleitung für das entsprechende S-ICD-Aggregat). Herz-Lungen-Wiederbelebung. Die Herz-Lungen-Wiederbelebung (HLW) kann die Detektion vorübergehend beeinträchtigen und die Therapie verzögern. Elektrokauterisation und Radiofrequenz (RF)-Ablation. Elektrokauterisation und Radiofrequenzablation kann ventrikuläre Arrhythmien und/oder Kammerflimmern induzieren und zu 6
11 unangebrachten Schockabgaben und Inhibierung der Post-Schock- Stimulation führen. Seien Sie zudem vorsichtig, wenn Sie bei Patienten mit implantierten Geräten ein anderes Ablationsverfahren am Herzen anwenden. Wenn Elektrokauterisation oder RF-Ablation medizinisch notwendig sind, führen Sie folgende Maßnahmen durch, um die Risiken für den Patienten und das Gerät so weit wie möglich zu reduzieren: Halten Sie einen externen Defibrillator bereit. Programmieren Sie das Aggregat in den Modus Therapie Off. Vermeiden Sie den direkten Kontakt zwischen den Elektrokautergeräten bzw. Ablationskathetern und dem Aggregat und der subkutanen Elektrode. Achten Sie darauf, dass der Strompfad so weit wie möglich vom Aggregat und der subkutanen Elektrode entfernt verläuft. Wenn eine RF-Ablation und/oder Elektrokauterisation im Gewebe in der Nähe des Aggregats oder der subkutanen Elektrode durchgeführt wird, überprüfen Sie die Funktion des Aggregats (empfohlene Nachsorgemaßnahmen für die Zeit nach der Therapie finden Sie in der Gebrauchsanweisung für das entsprechende S-ICD-Aggregat). Verwenden Sie bei der Elektrokauterisation soweit möglich ein bipolares Elektrokautersystem, und arbeiten Sie mit kurzen, intermittierenden und unregelmäßigen Bursts mit geringstmöglichen Stromstärken. Setzen Sie das Aggregat nach Beenden des Verfahrens wieder in den Modus Therapie On. Explantation und Entsorgung Vorgehensweise beim Explantieren. Reinigen und desinfizieren Sie implantierte Komponenten nach Standardverfahren zur Handhabung kontaminierter Geräte. Potentielle Nebenwirkungen Potentielle Nebenwirkungen nach der Implantation des S-ICD Systems umfassen die folgenden, sind jedoch nicht auf diese begrenzt: Beschleunigung/Induktion atrialer oder ventrikulärer Arrhythmie Nebenwirkungen bei den Induktionstests Allergische Reaktion/Nebenwirkung auf das System oder Medikation Blutung Bruch des Leiters Bildung von Zysten Tod Verzögerte Therapieabgabe Beschwerden oder verzögerte Heilung der Inzision Deformierung und/oder Bruch der Elektrode 7
12 Fehlende Isolierung der Elektrode Erosion/Extrusion Unfähigkeit zur Therapieabgabe Fieber Hämatom/Serom Hämatothorax Fehlerhafte Verbindung der Elektrodenpole mit dem Gerät Ausfall der Kommunikation mit dem Gerät Inhibition der Defibrillation oder Stimulation Fehlerhafte Post-Schock-Stimulation Ungeeignete Schockabgabe Infektion Verletzungen oder Schmerzen der oberen Gliedmaßen, einschließlich Schlüsselbein, Schulter und Arm Keloidbildung Verschiebung oder Dislokation des Systems Muskel-/Nervenstimulation Nervenschäden Pneumothorax Beschwerden nach dem Schock/der Stimulation Vorzeitige Erschöpfung der Batterie Nicht vorhersehbares Versagen von Komponenten Schlaganfall Subkutanes Emphysem Chirurgische Neueinsetzung oder Ersatz des Systems Synkope Geweberötungen, Reizung, Taubheit oder Nekrose Eine Liste potentieller Nebenwirkungen in Verbindung mit MRT-Scans ist im Technischen Leitfaden für die MRT-Anwendung enthalten. Wenn Nebenwirkungen auftreten, sind möglicherweise invasive Korrekturmaßnahmen und/oder eine Modifikation bzw. Entfernung des S-ICD Systems erforderlich. Patienten, die ein S-ICD System erhalten, entwickeln unter Umständen die folgenden psychische Störungen, sind jedoch nicht auf diese begrenzt: Depression/Unruhe Furcht vor Fehlfunktion des Geräts Angst vor Schocks Phantomschocks 8
13 Garantie Eine Erklärung zur beschränkten Garantie für die subkutane Elektrode ist unter verfügbar. Ein Exemplar kann bei Boston Scientific angefordert werden. Weitere Informationen befinden sich auf der Rückseite. INFORMATIONEN VOR DER IMPLANTATION Vorbereitung der Implantation Bedenken Sie vor der Implantation folgende Punkte: Das S-ICD System ist für die Positionierung durch anatomische Referenzpunkte konzipiert. Es wird jedoch empfohlen, anhand einer Röntgenaufnahme der Brust vor der Implantation sicherzustellen, dass der Patient keine auffällige atypische Anatomie aufweist (z. B. Dextrokardie). Ziehen Sie in Erwägung, die angestrebte Position der implantierten Systemkomponenten und/oder Inzisionen vor dem Verfahren zu markieren. Orientieren Sie sich dabei an anatomischen Referenzpunkten oder verwenden Sie die Durchleuchtung. Falls Abweichungen von den Implantationsanweisungen erforderlich sind, um das Verfahren auf Körpergröße und -bau abzustimmen, sollte vor der Implantation ein Röntgenthorax erstellt und zu Rate gezogen werden. WARNUNG: Es muss auf die Platzierung des Arms auf Seite des Geräteimplantats geachtet werden, um eine Verletzung des Nervus ulnaris und des Plexus brachialis zu vermeiden, wenn sich der Patient während der Geräteimplantation und vor VF-Induktion oder Schockabgabe, in supiner Lage befindet. Während der Implantationsphase des Verfahrens muss der Arm abduziert werden (Winkel höchstens 60 ), wobei sich die Hand in supiner Lage (Handfläche nach oben) befindet. Es ist übliche Praxis, den Arm an einem Armbrett zu befestigen, um die Position während der Geräteimplantation zu erhalten. Fixieren Sie den Arm bei Defibrillationstests nicht zu eng. Eine Höherlegung des Torsos durch Stützen kann die Schultergelenke ebenfalls belasten und sollte während Defibrillationstests vermieden werden. Verpackungsinhalt Lagern Sie sie in einem sauberen, trockenen Bereich. Die folgenden vorsterilisierten Teile sind der subkutanen Elektrode beigepackt: Zwei Silikon-Nahtmanschetten Des Weiteren ist Produktliteratur im Lieferumfang enthalten. Zubehör Zusätzlich zu dem der Elektrode beigepackten Zubehör ist separat verpacktes Elektrodenzubehör erhältlich. Im Folgenden finden Sie eine Liste des Zubehörs, das für die Implantation der Elektrode verwendet werden kann, aber nicht im Lieferumfang der Elektrode enthalten sind: EMBLEM S-ICD Elektroden-Einführsystem (Modell 4712) EMBLEM S-ICD Einführhilfe für subkutane Elektroden (Modell 4711) 9
14 Geschlitzte Nahtmanschette; zusätzliche geschlitzte Nahtmanschetten, die mit der Elektrode kompatibel sind, sind als Zubehör erhältlich (Modell 4760) Hinweis: Die Elektrodenkappe (Modell 7007) kann ebenfalls verwendet werden. IMPLANTATION Überblick HINWEIS: Anweisungen zur Implantation der subkutanen Elektrode befinden sich in der Gebrauchsanweisung für die jeweils verwendeten Einführhilfen (siehe "Zubehör" auf Seite 9). Wird die Elektrode beispielsweise mit dem EMBLEM S-ICD Elektroden-Einführsystem (Modell 4712) implantiert, können Sie die Anweisungen zur Implantation der Gebrauchsanleitung des EMBLEM S-ICD Elektroden-Einführsystems entnehmen. Dieser Abschnitt enthält einen Überblick über die Informationen, die zur Implantation des S-ICD Systems einschließlich der subkutanen Elektrode erforderlich sind. WARNUNG: Alle implantierbaren Komponenten von Boston Scientific S-ICD wurden nur für die Verwendung mit dem Boston Scientific oder Cameron Health S-ICD System entwickelt. Die Verbindung einer S-ICD System- Komponente mit einer nichtkompatiblen Komponente wurde nicht getestet und kann dazu führen, dass die lebensrettende Defibrillationstherapie fehlschlägt. WARNUNG: Die Implantation des Systems darf nicht in Bereichen durchgeführt werden, die in den Richtlinien des American College of Radiology für sichere MRT-Praktiken (Guidance Document for Safe MR Practices) 3 als Zone III (oder höher) definiert werden. Einige Zubehörteile, die mit dem Aggregat und den Elektroden verwendet werden, wie z. B. Drehmoment- Schraubendreher und Werkzeuge zur Implantation der Elektroden, sind nicht bedingt MRT-tauglich und dürfen nicht im MRT-Untersuchungsraum, Kontrollraum oder in Zone III oder IV des MRT-Standorts verwendet werden. HINWEIS: Wenn der Elektrodenstecker zum Zeitpunkt der Elektrodenimplantation nicht an ein Aggregat angeschlossen wird, müssen Sie eine Kappe auf den Elektrodenstecker aufsetzen, bevor Sie den Einschnitt für die Tasche schließen. Die Elektrodenkappe ist speziell für diesen Zweck vorgesehen. Sichern Sie die Elektrodenkappe mit einer Naht, um sie in Position zu halten. HINWEIS: Die Verwendung einer Boston Scientific-/Cameron Health- Elektrode ist erforderlich, damit ein implantiertes System als bedingt MRTtauglich betrachtet werden kann. Im Technischen Leitfaden MRT sind die Modellnummern der Systemkomponenten enthalten, die benötigt werden, um die Nutzungsbedingungen zu erfüllen. 3. Kanal E, et al., American Journal of Roentgenology 188: ,
15 Das Aggregat und die subkutane Elektrode werden in der Regel subkutan im linken thorakalen Bereich implantiert. Die Einführhilfen werden verwendet, um die subkutanen Tunnel anzulegen, in die die Elektrode eingeführt wird. Der Defibrillationswendel muss immer parallel zum Sternum und in der Nähe bzw. mit Kontakt zur tiefen Faszie, unter dem Fettgewebe und ca. 1 2 cm von der Mittellinie des Sternums entfernt positioniert werden (Abbildung 1 Platzierung des S-ICD Systems auf Seite 11 und Abbildung 2 Subkutane Hautschichten auf Seite 12). Abbildung 1. Platzierung des S-ICD Systems 11
16 [1] Haut, [2] Hypodermis, [3] Fettschicht, [4] tiefe Faszie, [5] subfasziales Gewebe (Muskel oder Knochen), [6] Korrekte Stelle für subkutane Tunnel und die S-ICD subkutane Elektrode Abbildung 2. Subkutane Hautschichten Das Positionieren des Aggregats und der Elektrode kann durch verschiedenen Techniken erreicht werden. Für die optimale Positionierung der subkutanen Elektrode an der faszialen Fläche sollten bei der Auswahl der Implantationstechnik die Präferenz des Arztes und die Patientenbeurteilung berücksichtigt werden. Die Elektrode und das Gerät sollten vorsichtig direkt auf der Faszie ohne darunterliegendem Fettgewebe positioniert werden. Hohe Schock-Impedanz der Elektrode kann mit Fettgewebe unter der Coil-Elektrode assoziiert werden, was ein Repositionieren der Elektrode auf die Faszie erforderlich machen kann. Zur Maximierung der Herzmasse zwischen dem Aggregat und der Elektrode unter gleichzeitiger Beibehaltung der Detektionsparameter wird transthorakale Defibrillation durch die Positionierung einer anterioren Elektrode und einem Gerät an der mittleren oder der posterioren Achselhöhlenlinie erreicht. Falls entweder während eines Defibrillationstests oder später während (einer) spontanen ambulanten Episode(n) die Konvertierung von VT/VF ohne ausreichende Sicherheitsmarge fehlschlägt, sollte der Arzt die Position der Elektrode und des Geräts mithilfe von anatomischen Referenzpunkten oder einer Fluoroskopie überprüfen. Eine weiter posterior gelegene Lage des Geräts kann die Defibrillationsschwelle herabsetzen. Je nach Körperbau und Anatomie des Patienten kann der Arzt eine andere Position des Geräts zwischen dem M. serratus anterior und dem M. latissimus dorsi wählen. Die Fixierung des Geräts an die Muskulatur ist notwendig, um die 12
17 Position zu sichern, Leistung zu gewährleisten und Wundkomplikationen zu minimieren. Ein guter Kontakt zwischen Gewebe und der Elektrode und dem Aggregat wichtig, um die Detektion und die Therapieabgabe zu optimieren. Verwenden Sie chirurgische Standardtechniken, um einen guten Gewebekontakt herzustellen. Hierfür können Sie bspw. das Gewebe feucht halten und kontinuierlich mit steriler Kochsalzlösung spülen. Entfernen Sie außerdem restliche Luft über die Inzisionen, bevor und während Sie die Hautinzision schließen. Vermeiden Sie dabei Lufteinschlüsse im subkutanen Gewebe. Der Gebrauchsanweisung der zur Implantation der subkutanen Elektrode verwendeten Einführhilfe können Sie Anweisungen zur Implantation entnehmen, einschließlich Herstellung der subkutanen Tunnel, Einführen der Elektrode, Verankern der Elektrode und Prüfen der Elektroden-Position vor dem Verschließen. NACH DER IMPLANTATION Nachsorgeverfahren nach der Implantation Es wird empfohlen, die Gerätefunktionen regelmäßig von geschultem Personal in Form von Nachsorgeuntersuchungen überprüfen zu lassen, um die Geräteleistung und den entsprechenden aktuellen Gesundheitsstatus des Patienten während der Funktionsdauer des Geräts zu überprüfen. Weitere Informationen finden Sie in den Handbüchern zum entsprechenden Aggregat. WARNUNG: Halten Sie während der Implantation und der Nachsorgetests immer externe Defibrillationssysteme sowie in HLW geschultes medizinisches Personal bereit. Falls eine induzierte ventrikuläre Tachyarrhythmie nicht rechtzeitig terminiert wird, kann dies zum Tod des Patienten führen. Während einer Nachsorge wird empfohlen, die Position der subkutanen Elektrode regelmäßig durch Abtasten und/oder Röntgen zu überprüfen. Wenn die Gerätekommunikation mit dem Programmiergerät hergestellt wurde, benachrichtigt das Programmiergerät den Arzt automatisch, wenn ungewöhnliche Zustände auftreten. Weitere Informationen sind der Gebrauchsanleitung des EMBLEM S-ICD-Programmiergeräts zu entnehmen. Behandlung und Nachsorge des Patienten liegen im Ermessen des behandelnden Arztes. Es wird jedoch empfohlen, die entsprechenden Untersuchungen einen Monat nach der Implantation und mindestens alle 3 Monate durchzuführen, um den Zustand des Patienten zu überwachen und die Funktion des Gerätes zu beurteilen. Explantation HINWEIS: Senden Sie alle explantierten Aggregate und subkutanen Elektroden an Boston Scientific zurück. Die Untersuchung der explantierten Aggregate und subkutanen Elektroden kann Informationen für eine weitere Verbesserung der Systemzuverlässigkeit und die Anrechnung von Garantieleistungen ergeben. 13
18 WARNUNG: Nicht zur Wiederverwendung, Wiederaufbereitung oder Resterilisierung. Die Wiederverwendung, Wiederaufbereitung oder Resterilisierung kann die strukturelle Integrität des Geräts beeinträchtigen und/ oder zu Funktionsstörungen des Geräts führen, was wiederum Verletzung, Krankheit oder Tod des Patienten zur Folge haben kann. Wiederverwendung, Aufbereitung oder Resterilisation können außerdem ein Kontaminationsrisiko für das Gerät darstellen und/oder Infektionen beim Patienten oder Kreuzinfektionen verursachen, u. a. die Übertragung von Infektionserkrankungen von einem Patienten auf einen anderen. Die Kontaminierung des Geräts kann zu Verletzung, Erkrankung oder Tod von Patienten führen. Nehmen Sie in folgenden Fällen Kontakt mit Boston Scientific auf: Wenn ein Produkt außer Betrieb genommen wird. Beim Tod eines Patienten (ungeachtet der Todesursache). Stellen Sie in diesem Fall den Autopsiebericht bereit, falls ein solcher vorliegt. Bei anderen Beobachtungen oder Gründen von Komplikationen. HINWEIS: Die Entsorgung explantierter Aggregate und/oder subkutanen Elektroden unterliegt den einschlägigen Gesetzen und Vorschriften. Wenden Sie sich bitte an Boston Scientific (die Kontaktdaten finden Sie auf der Rückseite dieser Gebrauchsanleitung), um die Rücksendung des Produkts zu organisieren. VORSICHT: Reinigen und desinfizieren Sie implantierte Komponenten nach Standardverfahren zur Handhabung kontaminierter Geräte. Beachten Sie bei der Explantation und Rücksendung des Aggregats und/oder der subkutanen Elektrode folgende Punkte: Fragen Sie das Aggregat ab, und drucken Sie alle Berichte aus. Deaktivieren Sie das Aggregat vor der Explantation. Trennen Sie die subkutane Elektrode vom Aggregat. Wenn die subkutane Elektrode nicht explantiert wird und der Stecker nicht an ein Aggregat angeschlossen wird, müssen Sie eine Kappe auf den Elektrodenstecker aufsetzen, bevor Sie den Einschnitt für die Tasche schließen. Die Elektrodenkappe ist speziell für diesen Zweck vorgesehen. Sichern Sie die Elektrodenkappe mit einer Naht, um sie in Position zu halten. Wenn eine subkutane Elektrode explantiert wird, versuchen Sie, sie intakt zu explantieren, und senden Sie sie ungeachtet ihres Zustands ein. Entfernen Sie die subkutane Elektrode nicht mit Gefäßklemmen oder anderen Klemmwerkzeugen, die die Elektrode beschädigen könnten. Verwenden Sie Werkzeuge nur, wenn die subkutane Elektrode mit der Hand nicht entfernt werden kann. Aggregat und die subkutane Elektrode mit einem Desinfektionsmittel abwaschen (aber nicht eintauchen), um Körperflüssigkeiten und Verschmutzungen zu entfernen. Achten Sie darauf, dass keine Flüssigkeiten in die Anschlussbuchse des Aggregats gelangen. 14
19 Verwenden Sie ein Rücksende-Kit (Returned Product Kit) von Boston Scientific, um das Aggregat und/oder die subkutane Elektrode ordnungsgemäß zu verpacken, und senden Sie es an Boston Scientific zurück. SPEZIFIKATION Subkutane EMBLEM S-ICD-Elektrode Spezifikationen Tabelle 1. Elektrodenspezifikationen Komponente Stecker Länge Größe distale Spitze Wendelgröße Spezifikation SQ-1 S-ICD-Stecker (vom Standard abweichend) 45 cm 3,84 mm 9 Fr Größe Elektrodenschaft 7 Fr Oberfläche der distalen Detektionsfläche 36 mm 2 Oberfläche der proximalen Detektionsfläche Detektionsposition 46 mm 2 Defibrillationsfläche 750 mm 2 Distale Elektrode an der Spitze Proximale Elektrode: 120 mm von der Spitze entfernt Defibrillationsposition Isolierungsmaterial Material der Elektrode, Detektionsleiter und Stecker-Pins Material der Nahtmanschette Lagerungstemperaturbereich Maximaler Außendurchmesser an den SQ- 1-S-ICD-Steckerdichtungen Durchmesser Defibrillationswendel Schockimpedanz der Elektrode 20 mm von der Spitze entfernt Polycarbonat-Polyurethan MP35N Silikon -18 C bis +55 C (0 F bis +131 F) 4,0 mm 3,0 mm Ω a Maximaler Elektrodenleiter-Widerstand 15
20 Tabelle 1. Elektrodenspezifikationen (Fortsetzung) Vom Anschluss des Hochspannungs- Elektrodensteckerring zur Defibrillationswendel Vom Niederspannungs-Anschlussstift zum distalen Wahrnehmungselektrodenring Vom Anschluss der distalen Niederspannungs-Detektionselektrode zum proximalen Wahrnehmungselektrodenring 1 Ω 50 Ω 50 Ω a. Post-Schock-Stimulation verwendet denselben Vektor wie die Stimulation Definition der Symbole auf dem Verpackungsetikett Folgende Symbole können auf der Verpackung und dem Etikett benutzt werden. Tabelle 2. Symbole auf der Verpackung Symbol Beschreibung Mit Ethylenoxidgas sterilisiert Herstellungsdatum Autorisierter Repräsentant in der Europäischen Gemeinschaft Verwendbar bis Seriennummer Chargenbezeichnung Bestellnummer Temperaturbegrenzung Hier öffnen 16
21 Tabelle 2. Symbol Symbole auf der Verpackung (Fortsetzung) Beschreibung Gebrauchsanweisung auf der folgenden Website beachten: Nicht resterilisieren Nicht zur Wiederverwendung Nicht verwenden, wenn die Verpackung beschädigt ist Hersteller MRT-tauglich SQ-1 S-ICD-Stecker (vom Standard abweichend) CE-Konformitätszeichen mit Angabe der Zertifizierungsstelle, die den Gebrauch des Kennzeichens zulässt. Adresse des australischen Verantwortlichen 17
22
23
24 Boston Scientific Corporation 4100 Hamline Avenue North St. Paul, MN USA Guidant Europe NV/SA; Boston Scientific Green Square, Lambroekstraat 5D 1831 Diegem, Belgium Boston Scientific (Australia) Pty Ltd PO Box 332 Botany NSW 1455 Australia Free Phone Free Fax CARDIAC ( ) Boston Scientific Corporation or its affiliates. All rights reserved DE Europe Authorized 2015 * *
EMBLEM S-ICD. rsion überholt. Nicht verwenden. Version obsolète. Ne pas utiliser. ated version. Do not use.
 GEBRAUCHSANLEITUNG EMBLEM S-ICD Subkutane Elektrode REF 3401 Folgende Marken sind Marken der Boston Scientific Corporation oder ihrer Tochtergesellschaften: EMBLEM und IMAGEREADY. Dieses Produkt ist möglicherweise
GEBRAUCHSANLEITUNG EMBLEM S-ICD Subkutane Elektrode REF 3401 Folgende Marken sind Marken der Boston Scientific Corporation oder ihrer Tochtergesellschaften: EMBLEM und IMAGEREADY. Dieses Produkt ist möglicherweise
GEBRAUCHSANLEITUNG EMBLEM S-ICD. Elektroden-Einführsystem REF 4712
 GEBRAUCHSANLEITUNG EMBLEM S-ICD Elektroden-Einführsystem REF 4712 Inhaltsverzeichnis Beschreibung...1 Informationen zu den Marken...1 Weitere Informationen...1 Indikationen...1 Kontraindikationen...2
GEBRAUCHSANLEITUNG EMBLEM S-ICD Elektroden-Einführsystem REF 4712 Inhaltsverzeichnis Beschreibung...1 Informationen zu den Marken...1 Weitere Informationen...1 Indikationen...1 Kontraindikationen...2
LATITUDE -PROGRAMMIERSYSTEM, MODELL 3300
 LATITUDE -PROGRAMMIERSYSTEM, MODELL 3300 ERGÄNZUNG ZU HANDBÜCHERN FÜR AGGREGATE * * Technische Handbücher und Referenzhandbücher für Ärzte Diese Ergänzung bietet einen umfassenden Überblick über die zentralen
LATITUDE -PROGRAMMIERSYSTEM, MODELL 3300 ERGÄNZUNG ZU HANDBÜCHERN FÜR AGGREGATE * * Technische Handbücher und Referenzhandbücher für Ärzte Diese Ergänzung bietet einen umfassenden Überblick über die zentralen
Version überholt. Nicht verwenden. Version obsolète. Ne pas utiliser. Versione obsoleta. Non utilizzare. Verouderde versie. Niet gebruiken.
 *359386-002* 359386-002 DE 2014-10 Aktualisierung der Kennzeichnung Diese Aktualisierung enthält Informationen zur LVAT-Funktion von PaceSafe TM und den LV VectorGuide TM für AUTOGEN TM X4-, DYNAGEN TM
*359386-002* 359386-002 DE 2014-10 Aktualisierung der Kennzeichnung Diese Aktualisierung enthält Informationen zur LVAT-Funktion von PaceSafe TM und den LV VectorGuide TM für AUTOGEN TM X4-, DYNAGEN TM
LATITUDE -PROGRAMMIERSYSTEM, MODELL 3300
 LATITUDE -PROGRAMMIERSYSTEM, MODELL 3300 ERGÄNZUNG ZU HANDBÜCHERN FÜR AGGREGATE * * Technische Handbücher und Referenzhandbücher für Ärzte Diese Ergänzung bietet einen umfassenden Überblick über die zentralen
LATITUDE -PROGRAMMIERSYSTEM, MODELL 3300 ERGÄNZUNG ZU HANDBÜCHERN FÜR AGGREGATE * * Technische Handbücher und Referenzhandbücher für Ärzte Diese Ergänzung bietet einen umfassenden Überblick über die zentralen
EMBLEM S-ICD, EMBLEM MRIS-ICD
 GEBRAUCHSANLEITUNG EMBLEM S-ICD, EMBLEM MRIS-ICD SUBKUTANER IMPLANTIERBARER KARDIOVERTER/DEFIBRILLATOR REF A209, A219 Inhaltsverzeichnis Beschreibung...1 Über diese Gebrauchsanweisung...1 Weitere Informationen...2
GEBRAUCHSANLEITUNG EMBLEM S-ICD, EMBLEM MRIS-ICD SUBKUTANER IMPLANTIERBARER KARDIOVERTER/DEFIBRILLATOR REF A209, A219 Inhaltsverzeichnis Beschreibung...1 Über diese Gebrauchsanweisung...1 Weitere Informationen...2
IMAGEREADY MR CONDITIONAL S-ICD SYSTEM
 TECHNISCHER LEITFADEN MRT IMAGEREADY MR CONDITIONAL S-ICD SYSTEM REF A209- und A219-Impulsgeneratoren und alle Modelle der subkutanen Elektroden von Boston Scientific/Cameron Health ÜBER DIESE GEBRAUCHSANWEISUNG
TECHNISCHER LEITFADEN MRT IMAGEREADY MR CONDITIONAL S-ICD SYSTEM REF A209- und A219-Impulsgeneratoren und alle Modelle der subkutanen Elektroden von Boston Scientific/Cameron Health ÜBER DIESE GEBRAUCHSANWEISUNG
A Closer Look. Programmieren eines CRT-Geräts wenn keine linksventrikuläre -Elektrode verwendet wird ZUSAMMENFASSUNG. Geräteprogrammierung
 A Closer Look ZUSAMMENFASSUNG Dieser Artikel fasst die Schritte zur Geräteprogrammierung zusammen, für den Fall, dass eine linksventrikuläre (LV-) Elektrode zwar implantiert jedoch nicht verwendet wird
A Closer Look ZUSAMMENFASSUNG Dieser Artikel fasst die Schritte zur Geräteprogrammierung zusammen, für den Fall, dass eine linksventrikuläre (LV-) Elektrode zwar implantiert jedoch nicht verwendet wird
Implantierbare Elektrode
 355403-223 MR Conditional FINELINE II STEROX.book Page 1 Tuesday, April 7, 2015 9:49 PM GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE FINELINE II STEROX Implantierbare Elektrode 4456/4457/4458/4459/4479/4480
355403-223 MR Conditional FINELINE II STEROX.book Page 1 Tuesday, April 7, 2015 9:49 PM GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE FINELINE II STEROX Implantierbare Elektrode 4456/4457/4458/4459/4479/4480
Programmiergerät EMBLEM S-ICD
 . 3200 GEBRAUCHSANLEITUNG DES PROGRAMMIERGERÄTS Programmiergerät EMBLEM S-ICD LISTE DER ABKÜRZUNGEN AC Alternating current (Wechselstrom) LCD Liquid crystal display (Flüssigkristallanzeige) AF Vorhofflimmern
. 3200 GEBRAUCHSANLEITUNG DES PROGRAMMIERGERÄTS Programmiergerät EMBLEM S-ICD LISTE DER ABKÜRZUNGEN AC Alternating current (Wechselstrom) LCD Liquid crystal display (Flüssigkristallanzeige) AF Vorhofflimmern
TECHNISCHER LEITFADEN MRT IMAGEREADY MR CONDITIONAL PACING SYSTEM REF J065, J066, J067, J175, J176, J177, J275, J276, J277, J279, L110, L111, L131,
 TECHNISCHER LEITFADEN MRT IMAGEREADY MR CONDITIONAL PACING SYSTEM REF J065, J066, J067, J175, J176, J177, J275, J276, J277, J279, L110, L111, L131, L210, L211, L231, L310, L311, L331, 4456, 4457, 4458,
TECHNISCHER LEITFADEN MRT IMAGEREADY MR CONDITIONAL PACING SYSTEM REF J065, J066, J067, J175, J176, J177, J275, J276, J277, J279, L110, L111, L131, L210, L211, L231, L310, L311, L331, 4456, 4457, 4458,
IMAGEREADY MR CONDITIONAL PACING SYSTEM
 TECHNISCHER LEITFADEN FÜR DIE MRT-ANWENDUNG IMAGEREADY MR CONDITIONAL PACING SYSTEM REF J065, J066, J067, J175, J176, J177, J275, J276, J277, J279, L110, L111, L131, L210, L211, L231, L310, L311, L331,
TECHNISCHER LEITFADEN FÜR DIE MRT-ANWENDUNG IMAGEREADY MR CONDITIONAL PACING SYSTEM REF J065, J066, J067, J175, J176, J177, J275, J276, J277, J279, L110, L111, L131, L210, L211, L231, L310, L311, L331,
REVEAL LINQ LNQ11. Insertable Cardiac Monitor Informationen zu MRT-Untersuchungen. MRT-Gebrauchsanweisung
 REVEAL LINQ LNQ11 Insertable Cardiac Monitor Informationen zu MRT-Untersuchungen MRT-Gebrauchsanweisung 0123 2013 Die folgende Liste beinhaltet Marken oder eingetragene Marken von Medtronic in den USA
REVEAL LINQ LNQ11 Insertable Cardiac Monitor Informationen zu MRT-Untersuchungen MRT-Gebrauchsanweisung 0123 2013 Die folgende Liste beinhaltet Marken oder eingetragene Marken von Medtronic in den USA
Implantation eines ICD- oder CRT-Systems
 Implantation eines ICD- oder CRT-Systems Patient: Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen ist die Implantation eines ICD- (implantierbarer Kadioverter- Defibrillator) oder CRT-(cardiale
Implantation eines ICD- oder CRT-Systems Patient: Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen ist die Implantation eines ICD- (implantierbarer Kadioverter- Defibrillator) oder CRT-(cardiale
System zur Stimulation des unteren Ösophagussphinkters. MRT Leitlinien mit EndoStim LES-Stimulator Modell 1002
 System zur Stimulation des unteren Ösophagussphinkters MRT Leitlinien mit EndoStim LES-Stimulator Modell 1002 EndoStim ist eine eingetragene Handelsmarke von EndoStim B.V. Vor der Verwendung des Geräts
System zur Stimulation des unteren Ösophagussphinkters MRT Leitlinien mit EndoStim LES-Stimulator Modell 1002 EndoStim ist eine eingetragene Handelsmarke von EndoStim B.V. Vor der Verwendung des Geräts
Gebrauchsanweisung Ösophagus-Stent Danis Seal (Danis Seal) Nicht-aktive implantierbare Vorrichtung
 Hergestellt von: ELLA CS, s.r.o. Milady Horakove 504 500 06 Hradec Kralove 6 Tschechische Republik Telefon: +420 49 527 91 11 Fax: +420 49 526 56 55 E-Mail: volenec@ellacs.eu Lieferumfang: Gebrauchsanweisung
Hergestellt von: ELLA CS, s.r.o. Milady Horakove 504 500 06 Hradec Kralove 6 Tschechische Republik Telefon: +420 49 527 91 11 Fax: +420 49 526 56 55 E-Mail: volenec@ellacs.eu Lieferumfang: Gebrauchsanweisung
A Closer Look. Boston Scientific ICD und CRT-D Indikatoren für den Austausch von Geräten ZUSAMMENFASSUNG
 A Closer Look ZUSAMMENFASSUNG Bei ICD- und CRT-D-Systemen der Modelle PUNCTUA TM, ENERGEN TM, INCEPTA TM, COGNIS und TELIGEN von Boston Scientific wird der Batteriestatus anhand der, der Ladezeit und der
A Closer Look ZUSAMMENFASSUNG Bei ICD- und CRT-D-Systemen der Modelle PUNCTUA TM, ENERGEN TM, INCEPTA TM, COGNIS und TELIGEN von Boston Scientific wird der Batteriestatus anhand der, der Ladezeit und der
Version überholt. Nicht verwenden. Version obsolète. Ne pas utiliser. Versione obsoleta. Non utilizzare. Verouderde versie. Niet gebruiken.
 TECHNISCHER LEITFADEN MRT IMAGEREADY MR CONDITIONAL PACING SYSTEM REF J065, J066, J067, J175, J176, J177, J275, J276, J277, J279, L110, L111, L131, L210, L211, L231, L310, L311, L331, 4456, 4457, 4458,
TECHNISCHER LEITFADEN MRT IMAGEREADY MR CONDITIONAL PACING SYSTEM REF J065, J066, J067, J175, J176, J177, J275, J276, J277, J279, L110, L111, L131, L210, L211, L231, L310, L311, L331, 4456, 4457, 4458,
HiRes 90K und HiRes 90K ADVANTAGE Cochlea-Implantate
 Magnetresonanztomografie (MRT) für HiRes 90K und HiRes 90K ADVANTAGE Cochlea-Implantate Deutsch Advanced Bionics Inhalt MRT bei Personen mit HiRes 90K oder HiRes 90K Advantage Implantat...2 Warnhinweis...2
Magnetresonanztomografie (MRT) für HiRes 90K und HiRes 90K ADVANTAGE Cochlea-Implantate Deutsch Advanced Bionics Inhalt MRT bei Personen mit HiRes 90K oder HiRes 90K Advantage Implantat...2 Warnhinweis...2
DRINGENDER SICHERHEITSHINWEIS
 DRINGENDER SICHERHEITSHINWEIS Fehlaktivierung der Sicherung des internen Akkus der Astral kann zu einem Stromausfall führen BRIEF FÜR PATIENTEN/PFLEGEPERSONEN Referenz: FSN1706001 Datum: 27. Juni 2017
DRINGENDER SICHERHEITSHINWEIS Fehlaktivierung der Sicherung des internen Akkus der Astral kann zu einem Stromausfall führen BRIEF FÜR PATIENTEN/PFLEGEPERSONEN Referenz: FSN1706001 Datum: 27. Juni 2017
Gebrauchsanweisung Art.-Nr V04. Vaginalelektrode. Für den ausschliesslich persönlichen Gebrauch durch. Frau...
 DE Gebrauchsanweisung Art.-Nr.100810-V04 Vaginalelektrode Für den ausschliesslich persönlichen Gebrauch durch Frau... schwa-medico Gebrauchsanweisung - Vaginalelektrode Zweckbestimmung Diese Elektrode
DE Gebrauchsanweisung Art.-Nr.100810-V04 Vaginalelektrode Für den ausschliesslich persönlichen Gebrauch durch Frau... schwa-medico Gebrauchsanweisung - Vaginalelektrode Zweckbestimmung Diese Elektrode
Bedienungsanleitung. Tauchpumpe Speedpump FLAT TPX 3200
 Bedienungsanleitung Tauchpumpe Speedpump FLAT TPX 3200 Art. Nr. 00-41050 2012_V3 Seite 1 von 6 Grundsätzliche Sicherheitsvorkehrungen sind stets einzuhalten. Fehler durch Nichtbeachtung der folgenden Anweisungen
Bedienungsanleitung Tauchpumpe Speedpump FLAT TPX 3200 Art. Nr. 00-41050 2012_V3 Seite 1 von 6 Grundsätzliche Sicherheitsvorkehrungen sind stets einzuhalten. Fehler durch Nichtbeachtung der folgenden Anweisungen
SingStar -Mikrofon-Set Bedienungsanleitung. SCEH Sony Computer Entertainment Europe
 SingStar -Mikrofon-Set Bedienungsanleitung SCEH-0001 7010521 2010 Sony Computer Entertainment Europe Vielen Dank, dass Sie das SingStar -Mikrofon-Set erworben haben. Bevor Sie dieses Produkt verwenden,
SingStar -Mikrofon-Set Bedienungsanleitung SCEH-0001 7010521 2010 Sony Computer Entertainment Europe Vielen Dank, dass Sie das SingStar -Mikrofon-Set erworben haben. Bevor Sie dieses Produkt verwenden,
Medizinisches Fach- und Pflegepersonal in medizinischen Einrichtungen, Homecare Provider und Fachhändler von Astral Beatmungsgeräten.
 .. o. Astral - Akku-Austausch-Aktion S/CHER/-/E/TSf-1/NWE/S Referenz: FSN1608001 Datum: 12. August 2016 Verteilung: Medizinisches Fach- und Pflegepersonal in medizinischen Einrichtungen, Homecare Provider
.. o. Astral - Akku-Austausch-Aktion S/CHER/-/E/TSf-1/NWE/S Referenz: FSN1608001 Datum: 12. August 2016 Verteilung: Medizinisches Fach- und Pflegepersonal in medizinischen Einrichtungen, Homecare Provider
Dringender Sicherheitshinweis
 30 Juni 2017 Dringender Sicherheitshinweis zum ICD-Programmiergerät, Modell 3200, NACHTRAG Ref. 100000038388-FA Revision C -, Sehr geehrte Damen und Herren, Anfang des Jahres hat Boston Scientific Ärzte
30 Juni 2017 Dringender Sicherheitshinweis zum ICD-Programmiergerät, Modell 3200, NACHTRAG Ref. 100000038388-FA Revision C -, Sehr geehrte Damen und Herren, Anfang des Jahres hat Boston Scientific Ärzte
Bedienungsanleitung. MICROPERC -Set steril, zur Einmalverwendung PD-PN-1008
 Bedienungsanleitung MICROPERC -Set steril, zur Einmalverwendung PD-PN-1008 PMT GmbH Im Gewerbegebiet 11 D 66709 Weiskirchen Telefon: +49 (0)6876 9100-0 PD_IFU_MICROPERC-Set-D_A 1 1 Sicherheit 1.1 Vorgesehener
Bedienungsanleitung MICROPERC -Set steril, zur Einmalverwendung PD-PN-1008 PMT GmbH Im Gewerbegebiet 11 D 66709 Weiskirchen Telefon: +49 (0)6876 9100-0 PD_IFU_MICROPERC-Set-D_A 1 1 Sicherheit 1.1 Vorgesehener
Interne GSM-Antenne V Nachtrag zur Installation
 Interne GSM-Antenne 970.195 V1 2015.04 de Nachtrag zur Installation Interne GSM-Antenne Sicherheitshinweise de 3 1 Sicherheitshinweise VORSICHT! Lesen Sie diese Sicherheitshinweise vor der Installation
Interne GSM-Antenne 970.195 V1 2015.04 de Nachtrag zur Installation Interne GSM-Antenne Sicherheitshinweise de 3 1 Sicherheitshinweise VORSICHT! Lesen Sie diese Sicherheitshinweise vor der Installation
TIELLE NICHTHAFTEND. Nichthaftender Hydropolymerverband. Technologie
 TIELLE NICHTHAFTEND Nichthaftender Hydropolymerverband Mit Technologie DE Produktbeschreibung Der nichthaftende TIELLE Hydropolymerverband absorbiert Exsudat, hält bei wenig bis stark exsudierenden Wunden
TIELLE NICHTHAFTEND Nichthaftender Hydropolymerverband Mit Technologie DE Produktbeschreibung Der nichthaftende TIELLE Hydropolymerverband absorbiert Exsudat, hält bei wenig bis stark exsudierenden Wunden
Technische Information Neuromodulation
 Technische Information Neuromodulation MRT bei Patienten mit implantiertem Medtronic Neurostimulationssystem zur Sakralnervenmodulation (Interstim -Therapie) Sehr geehrte Damen und Herren, Sie hatten uns
Technische Information Neuromodulation MRT bei Patienten mit implantiertem Medtronic Neurostimulationssystem zur Sakralnervenmodulation (Interstim -Therapie) Sehr geehrte Damen und Herren, Sie hatten uns
GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE ENDOTAK RELIANCE S
 GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE ENDOTAK RELIANCE Stimulations-/Detektions- und Defibrillations-Elektrode Integrierte bipolare DF4-LLHH- und DF4-LLHO-Stecker Aus-/eindrehbare Fixierung ENDOTAK
GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE ENDOTAK RELIANCE Stimulations-/Detektions- und Defibrillations-Elektrode Integrierte bipolare DF4-LLHH- und DF4-LLHO-Stecker Aus-/eindrehbare Fixierung ENDOTAK
Dringender Sicherheitshinweis
 SOLD_TO_NAME Physician_name - Departement SOLD_TO_STREET SOLD_TO_POSTAL_CODE SOLD_TO_CITY SOLD_TO_COUNTRY Januar 2017 Boston Scientific FSN über Programmiergeräte des Modells 3200 S-ICD Sehr geehrter Kollege,
SOLD_TO_NAME Physician_name - Departement SOLD_TO_STREET SOLD_TO_POSTAL_CODE SOLD_TO_CITY SOLD_TO_COUNTRY Januar 2017 Boston Scientific FSN über Programmiergeräte des Modells 3200 S-ICD Sehr geehrter Kollege,
Ergänzung: Bedienerhandbuch für das
 Ergänzung: Bedienerhandbuch für das AutoPulse Reanimationssystem Modell 100 mit Defibrillatorschnittstelle 3.5 Regelmäßige EKG-Überwachung (Elektrokardiogramm) und/oder Defibrillation Wenn das AutoPulse
Ergänzung: Bedienerhandbuch für das AutoPulse Reanimationssystem Modell 100 mit Defibrillatorschnittstelle 3.5 Regelmäßige EKG-Überwachung (Elektrokardiogramm) und/oder Defibrillation Wenn das AutoPulse
M25 megaphon. bedienungsanleitung
 M25 megaphon bedienungsanleitung Musikhaus Thomann e.k. Treppendorf 30 96138 Burgebrach Deutschland Telefon: +49 (0) 9546 9223-0 E-Mail: info@thomann.de Internet: www.thomann.de 25.10.2012 Inhaltsverzeichnis
M25 megaphon bedienungsanleitung Musikhaus Thomann e.k. Treppendorf 30 96138 Burgebrach Deutschland Telefon: +49 (0) 9546 9223-0 E-Mail: info@thomann.de Internet: www.thomann.de 25.10.2012 Inhaltsverzeichnis
Lyric3 Programmierstift. Gebrauchsanweisung für Hörgeräteakustiker
 Lyric3 Programmierstift Gebrauchsanweisung für Hörgeräteakustiker Willkommen Dies ist der neue Lyric3 Programmierstift von Phonak. Der Lyric3 Programmierstift wurde speziell für Sie als Hörgeräteakustiker
Lyric3 Programmierstift Gebrauchsanweisung für Hörgeräteakustiker Willkommen Dies ist der neue Lyric3 Programmierstift von Phonak. Der Lyric3 Programmierstift wurde speziell für Sie als Hörgeräteakustiker
Pflege der Schraubeneintrittsstelle bei Versorgung mit Fixateur Externe
 PAT I E N T E N I N F O R M AT I O N Pflege der Schraubeneintrittsstelle bei Versorgung mit Fixateur Externe EXTERNE FIXATION Was ist externe Fixation? Bei der Behandlung eines Knochens, um eine Fraktur
PAT I E N T E N I N F O R M AT I O N Pflege der Schraubeneintrittsstelle bei Versorgung mit Fixateur Externe EXTERNE FIXATION Was ist externe Fixation? Bei der Behandlung eines Knochens, um eine Fraktur
 Ortho-Collar www.teufel-international.com Gebrauchsanweisung Inhalt Beschreibung Beschreibung 2 Indikation 2 Kontraindikation 2 Funktion 2 Abrechnungsposition 2 Sicherheit 3 REF/Größen 3 Anwendung/Anpassung
Ortho-Collar www.teufel-international.com Gebrauchsanweisung Inhalt Beschreibung Beschreibung 2 Indikation 2 Kontraindikation 2 Funktion 2 Abrechnungsposition 2 Sicherheit 3 REF/Größen 3 Anwendung/Anpassung
INDIKATIONEN Der TITAN-PORT APH ermöglicht einen wiederholten Gefäßzugang zur Apherese.
 INDIKATIONEN Der TITAN-PORT APH ermöglicht einen wiederholten Gefäßzugang zur Apherese. Der Vorteil liegt in der Anwendung eines geschlossenen Systems mit geringerer Infektionsrate und längerer Verweildauermöglichkeit.
INDIKATIONEN Der TITAN-PORT APH ermöglicht einen wiederholten Gefäßzugang zur Apherese. Der Vorteil liegt in der Anwendung eines geschlossenen Systems mit geringerer Infektionsrate und längerer Verweildauermöglichkeit.
WITH SAFETAC TECHNOLOGY
 zur Verfügung gestellt von Gebrauchs.info Ag WITH SAFETAC TECHNOLOGY 0086 Canada 1-800-494-5134 EP 855 921 USP 6,051,747 EP 865 781 USP 6,040,492 Mölnlycke Health Care AB (Publ), Box 13080, SE-402 52 Göteborg,
zur Verfügung gestellt von Gebrauchs.info Ag WITH SAFETAC TECHNOLOGY 0086 Canada 1-800-494-5134 EP 855 921 USP 6,051,747 EP 865 781 USP 6,040,492 Mölnlycke Health Care AB (Publ), Box 13080, SE-402 52 Göteborg,
SIMATIC. Produktinformation zum Fast Connect-Stecker. Einleitung. Peripheriebaugruppen und Kompakt-CPUs mit Fast. Connect verdrahten
 SIMATIC Einleitung 1 Peripheriebaugruppen und Kompakt-CPUs mit Fast 2 Connect verdrahten SIMATIC Produktinformation zum Fast Connect-Stecker Produktinformation 07/2007 A5E01103145-01 Sicherheitshinweise
SIMATIC Einleitung 1 Peripheriebaugruppen und Kompakt-CPUs mit Fast 2 Connect verdrahten SIMATIC Produktinformation zum Fast Connect-Stecker Produktinformation 07/2007 A5E01103145-01 Sicherheitshinweise
Gebrauchsanweisung Art.-Nr V04. Analelektrode. Für den ausschliesslich persönlichen Gebrauch durch. Frau/Herr...
 DE Gebrauchsanweisung Art.-Nr.100811-V04 Analelektrode Für den ausschliesslich persönlichen Gebrauch durch Frau/Herr... schwa-medico Gebrauchsanweisung - Analelektrode Zweckbestimmung Diese Analelektrode
DE Gebrauchsanweisung Art.-Nr.100811-V04 Analelektrode Für den ausschliesslich persönlichen Gebrauch durch Frau/Herr... schwa-medico Gebrauchsanweisung - Analelektrode Zweckbestimmung Diese Analelektrode
HDMI Kabeltester Bedienungsanleitung
 HDMI Kabeltester Bedienungsanleitung CNT 7 L CNT7L_Manual-de_99.indd 1 30.09.2013 11:24:47 ! Achtung! Lesen Sie die Bedienungsanleitung vollständig und sorgfältig durch. Es ist Bestandteil des Produktes
HDMI Kabeltester Bedienungsanleitung CNT 7 L CNT7L_Manual-de_99.indd 1 30.09.2013 11:24:47 ! Achtung! Lesen Sie die Bedienungsanleitung vollständig und sorgfältig durch. Es ist Bestandteil des Produktes
GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE RELIANCE 4 FRONT
 GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE RELIANCE 4 FRONT Stimulations-/Detektions- und Defibrillations-Elektrode Integrierte bipolare DF4-LLHH- und DF4-LLHO-Stecker Aus-/eindrehbare Fixierung Single-Schock-Coil
GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE RELIANCE 4 FRONT Stimulations-/Detektions- und Defibrillations-Elektrode Integrierte bipolare DF4-LLHH- und DF4-LLHO-Stecker Aus-/eindrehbare Fixierung Single-Schock-Coil
ARTIC2SP/4SP. Installation und Betrieb ALLGEMEINE INFORMATIONEN WERKZEUGE TECHNISCHE DATEN ABMESSUNGEN INSTALLATIONS-ARTEN VERPACKUNG
 ALLGEMEINE INFORMATIONEN WERKZEUGE TECHNISCHE DATEN ABMESSUNGEN INSTALLATIONS-ARTEN VERPACKUNG MONTAGE UND INSTALLATION DES MECHANISMUS/MOTOREN 3 JUSTIERUNG /ENDE EINSCHLAG 5 NOTENTRIEGELUNG 6 ARTICSP/4SP
ALLGEMEINE INFORMATIONEN WERKZEUGE TECHNISCHE DATEN ABMESSUNGEN INSTALLATIONS-ARTEN VERPACKUNG MONTAGE UND INSTALLATION DES MECHANISMUS/MOTOREN 3 JUSTIERUNG /ENDE EINSCHLAG 5 NOTENTRIEGELUNG 6 ARTICSP/4SP
INFORMATIONEN ZUR HF10 -THERAPIE
 INFORMATIONEN ZUR HF10 -THERAPIE Wenn sie vor GLÜCK sprachlos ist, sprechen die Resultate Bände. 79 % von Patienten mit schweren Rücken- oder Beinschmerzen erfuhren beträchtliche Linderung dank der HF10-Therapie.
INFORMATIONEN ZUR HF10 -THERAPIE Wenn sie vor GLÜCK sprachlos ist, sprechen die Resultate Bände. 79 % von Patienten mit schweren Rücken- oder Beinschmerzen erfuhren beträchtliche Linderung dank der HF10-Therapie.
INGEVITY MRI GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE. Stimulations-/Detektions-Elektrode Bipolarer IS-1 Stecker Aus-/eindrehbare Fixierung
 GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE INGEVITY MRI Stimulations-/Detektions-Elektrode Bipolarer IS-1 Stecker Aus-/eindrehbare Fixierung Gerade REF 7740,7741,7742 Inhaltsverzeichnis GEBRAUCHSANWEISUNG...1
GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE INGEVITY MRI Stimulations-/Detektions-Elektrode Bipolarer IS-1 Stecker Aus-/eindrehbare Fixierung Gerade REF 7740,7741,7742 Inhaltsverzeichnis GEBRAUCHSANWEISUNG...1
Klarfit Klimmzugstange
 Klarfit Klimmzugstange 10004638 Sehr geehrter Kunde, zunächst möchten wir Ihnen zum Erwerb Ihres Gerätes gratulieren. Bitte lesen Sie die folgenden Anschluss- und Anwendungshinweise sorgfältig durch und
Klarfit Klimmzugstange 10004638 Sehr geehrter Kunde, zunächst möchten wir Ihnen zum Erwerb Ihres Gerätes gratulieren. Bitte lesen Sie die folgenden Anschluss- und Anwendungshinweise sorgfältig durch und
Gebrauchsanweisung. für den Mann. VaPro / VaPro F-Style VaPro Plus / VaPro Plus F-Style. Kontinenzversorgung People First
 VaPro / VaPro F-Style VaPro Plus / VaPro Plus F-Style Einmalkatheter zur Intermittierenden Katheterisierung Gebrauchsanweisung für den Mann Kontinenzversorgung People First VaPro / VaPro F-Style Berührungsfreier
VaPro / VaPro F-Style VaPro Plus / VaPro Plus F-Style Einmalkatheter zur Intermittierenden Katheterisierung Gebrauchsanweisung für den Mann Kontinenzversorgung People First VaPro / VaPro F-Style Berührungsfreier
Verordnung über Medizinprodukte - MPV (Medizinprodukte-Verordnung)
 Verordnung über Medizinprodukte - MPV (Medizinprodukte-Verordnung) Vom 20. Dezember 2001,Bundesgesetzblatt I Nr. 72, S. 3854 22. Dezember 2001, geändert durch Bundesgesetzblatt I S. 4456 vom 4. Dezember
Verordnung über Medizinprodukte - MPV (Medizinprodukte-Verordnung) Vom 20. Dezember 2001,Bundesgesetzblatt I Nr. 72, S. 3854 22. Dezember 2001, geändert durch Bundesgesetzblatt I S. 4456 vom 4. Dezember
TOP BENDER 050-EDT - Bedienungsanleitung -
 TOP BENDER 050-EDT - Bedienungsanleitung - Seite 1 Sicherheitsrichtlinien Dieses Handbuch enthält Hinweise, die Ihrer persönlichen Sicherheit sowie dem Schutz der Produkte und der damit verbundenen Anlage
TOP BENDER 050-EDT - Bedienungsanleitung - Seite 1 Sicherheitsrichtlinien Dieses Handbuch enthält Hinweise, die Ihrer persönlichen Sicherheit sowie dem Schutz der Produkte und der damit verbundenen Anlage
Leistung und Auswahl. TRUEtome. Optimierte Führungsdraht-Sondierung zur Behandlung pankreatikobiliärer Erkrankungen. Sondierungspapillotom
 Leistung und Auswahl Optimierte Führungsdraht-Sondierung zur Behandlung pankreatikobiliärer Erkrankungen TRUEtome Mit dem TRUEtome können endoskopische retrograde Cholangiopankreatographieverfahren (ERCP)
Leistung und Auswahl Optimierte Führungsdraht-Sondierung zur Behandlung pankreatikobiliärer Erkrankungen TRUEtome Mit dem TRUEtome können endoskopische retrograde Cholangiopankreatographieverfahren (ERCP)
Aufzeichnen und Senden von Episoden
 Patienten-Handbuch Aufzeichnen und Senden von Episoden mit Ihrem implantierbaren Arrhythmie-Monitor SJM Confirm Der Patientenaktivator ist Bestandteil des implantierbaren Arrhythmie-Monitors (Implantable
Patienten-Handbuch Aufzeichnen und Senden von Episoden mit Ihrem implantierbaren Arrhythmie-Monitor SJM Confirm Der Patientenaktivator ist Bestandteil des implantierbaren Arrhythmie-Monitors (Implantable
KURZLEITFADEN: LADEGERÄT
 KURZLEITFADEN: LADEGERÄT 1. Ladespule 2. Batteriestandsanzeige für das Ladegerät 3. Anzeige Antennenstärke 4. Taste Stimulation aus VORBEREITEN DES LADEVORGANGS 1. Platzieren Sie die Mitte der kreisförmigen
KURZLEITFADEN: LADEGERÄT 1. Ladespule 2. Batteriestandsanzeige für das Ladegerät 3. Anzeige Antennenstärke 4. Taste Stimulation aus VORBEREITEN DES LADEVORGANGS 1. Platzieren Sie die Mitte der kreisförmigen
MRT-RICHTLINIEN FÜR DIE INSPIRE-THERAPIE
 MRT-RICHTLINIEN FÜR DIE INSPIRE-THERAPIE Ärzte-Handbuch ONLY Folgendes ist eine Marke von Inspire Medical Systems, Inc.: Inspire Dieses Produkt und/oder die Verwendung dieses Produkts für eine Methode
MRT-RICHTLINIEN FÜR DIE INSPIRE-THERAPIE Ärzte-Handbuch ONLY Folgendes ist eine Marke von Inspire Medical Systems, Inc.: Inspire Dieses Produkt und/oder die Verwendung dieses Produkts für eine Methode
Umlenkrolle Modell RP-701. Gebrauchsanweisung HINWEIS ZUR INSTALLATION. Bitte vor Nutzung immer erst die Gebrauchsanweisung durchlesen
 Umlenkrolle Modell RP-701 Gebrauchsanweisung HINWEIS ZUR INSTALLATION Bitte vor Nutzung immer erst die Gebrauchsanweisung durchlesen DIE GEBRAUCHSANWEISUNG ENTHÄLT INFORMATIONEN ZUR ORDNUNGSGEMÄSSEN NUTZUNG
Umlenkrolle Modell RP-701 Gebrauchsanweisung HINWEIS ZUR INSTALLATION Bitte vor Nutzung immer erst die Gebrauchsanweisung durchlesen DIE GEBRAUCHSANWEISUNG ENTHÄLT INFORMATIONEN ZUR ORDNUNGSGEMÄSSEN NUTZUNG
UNI-DEX WIDEX A/S. Nymoellevej 6, 3540 Lynge, Denmark Manual no.: #01. É[5qr0w6 ;;ll;g]
![UNI-DEX WIDEX A/S. Nymoellevej 6, 3540 Lynge, Denmark Manual no.: #01. É[5qr0w6 ;;ll;g] UNI-DEX WIDEX A/S. Nymoellevej 6, 3540 Lynge, Denmark Manual no.: #01. É[5qr0w6 ;;ll;g]](/thumbs/60/44352928.jpg) UNI-DEX WIDEX A/S Nymoellevej 6, 3540 Lynge, Denmark www.widex.com Manual no.: 9 514 0259 099 #01 É[5qr0w6 ;;ll;g] 1 4 1.3 1.4 1.6 1.5 1.7 1.2 1.1 4.1 4.2 2 2.2 (1) (2) 2.1 5 3 3.2 5.2 5.1 3.3 3.1 5.3
UNI-DEX WIDEX A/S Nymoellevej 6, 3540 Lynge, Denmark www.widex.com Manual no.: 9 514 0259 099 #01 É[5qr0w6 ;;ll;g] 1 4 1.3 1.4 1.6 1.5 1.7 1.2 1.1 4.1 4.2 2 2.2 (1) (2) 2.1 5 3 3.2 5.2 5.1 3.3 3.1 5.3
Unterstützt die Sondierung und erleichtert die Passage von Stenosen
 NaviPro Hydrophiler Führungsdraht Unterstützt die Sondierung und erleichtert die Passage von Stenosen Optimierte Führungsdraht-Sondierung zur Behandlung pankreatikobiliärer Erkrankungen Allgemeine Informationen
NaviPro Hydrophiler Führungsdraht Unterstützt die Sondierung und erleichtert die Passage von Stenosen Optimierte Führungsdraht-Sondierung zur Behandlung pankreatikobiliärer Erkrankungen Allgemeine Informationen
TTS ist stolz darauf, Teil von
 Garantie & Support Dieses Produkt wird mit einem Jahr Garantie für Probleme versehen, die während der normalen Nutzung auftreten. Falsche Handhabung Power Pods oder das Öffnen des Gerätes macht diese Garantie
Garantie & Support Dieses Produkt wird mit einem Jahr Garantie für Probleme versehen, die während der normalen Nutzung auftreten. Falsche Handhabung Power Pods oder das Öffnen des Gerätes macht diese Garantie
Arbeitsspeicher. Hinweis: Online-Anweisungen finden Sie unter der Adresse
 Deutsch Arbeitsspeicher Austausch Anleitung Bitte folgen Sie diesen Anweisungen gewissenhaft. Geschieht dies nicht, können die Geräte beschädigt werden, und Ihr Garantieanspruch kann verlorengehen. Hinweis:
Deutsch Arbeitsspeicher Austausch Anleitung Bitte folgen Sie diesen Anweisungen gewissenhaft. Geschieht dies nicht, können die Geräte beschädigt werden, und Ihr Garantieanspruch kann verlorengehen. Hinweis:
Patientendaten-Management
 GEBRAUCHSANWEISUNG Patientendaten-Management Anwendungsmodell 3931 zur Verwendung mit dem LATITUDE -Programmiersystem, Modell 3300. INHALTSVERZEICHNIS GEBRAUCHSANWEISUNG... 1 Informationen zu Marken...
GEBRAUCHSANWEISUNG Patientendaten-Management Anwendungsmodell 3931 zur Verwendung mit dem LATITUDE -Programmiersystem, Modell 3300. INHALTSVERZEICHNIS GEBRAUCHSANWEISUNG... 1 Informationen zu Marken...
DRINGENDE SICHERHEITSINFORMATION
 Empfänger Anschrift München, 14.12.2018 DRINGENDE SICHERHEITSINFORMATION Marktfreigabe einer neuen Softwareversion zur Unterstützung der Therapien bei implantierten Platinium Geräten im Falle des Auftretens
Empfänger Anschrift München, 14.12.2018 DRINGENDE SICHERHEITSINFORMATION Marktfreigabe einer neuen Softwareversion zur Unterstützung der Therapien bei implantierten Platinium Geräten im Falle des Auftretens
AS Medizintechnik GmbH Sattlerstraße Tuttlingen Germany
 1 Sicherheit und Verantwortung 1.1 Bestimmungsgemäßer Gebrauch Zweckbestimmung er Schaft ist ein wiederverwendbares invasives Produkt zur kurzzeitigen Anwendung und dient dem Einbringen von Optiken, Instrumenten
1 Sicherheit und Verantwortung 1.1 Bestimmungsgemäßer Gebrauch Zweckbestimmung er Schaft ist ein wiederverwendbares invasives Produkt zur kurzzeitigen Anwendung und dient dem Einbringen von Optiken, Instrumenten
Subkutaner ICD S-ICD Schutz, ohne das Herz zu berühren Eine Information für Patienten
 Subkutaner ICD S-ICD Schutz, ohne das Herz zu berühren Eine Information für Patienten Eine Information für Patienten WICHTIG Bitte beachten: Die von Boston Scientific Corporation (BSC) bereitgestellten
Subkutaner ICD S-ICD Schutz, ohne das Herz zu berühren Eine Information für Patienten Eine Information für Patienten WICHTIG Bitte beachten: Die von Boston Scientific Corporation (BSC) bereitgestellten
GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE RELIANCE 4 FRONT
 GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE RELIANCE 4 FRONT Stimulations-/Detektions- und Defibrillations-Elektrode Integrierte bipolare DF4-LLHH- und DF4-LLHO-Stecker Ankerfixierung Single-Schock-Coil
GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE RELIANCE 4 FRONT Stimulations-/Detektions- und Defibrillations-Elektrode Integrierte bipolare DF4-LLHH- und DF4-LLHO-Stecker Ankerfixierung Single-Schock-Coil
FAQ/Häufige Fragen ALLGEMEINE FRAGEN ZUR OPTUNE-THERAPIE
 FAQ/Häufige Fragen ALLGEMEINE FRAGEN ZUR OPTUNE-THERAPIE WO ERHALTE ICH OPTUNE? IST OPTUNE FÜR MICH GEEIGNET? MUSS ICH FÜR DIE OPTUNE-THERAPIE IN EIN KRANKENHAUS? WERDE ICH WEITERHIN VON MEINEN MEDIZINISCHEN
FAQ/Häufige Fragen ALLGEMEINE FRAGEN ZUR OPTUNE-THERAPIE WO ERHALTE ICH OPTUNE? IST OPTUNE FÜR MICH GEEIGNET? MUSS ICH FÜR DIE OPTUNE-THERAPIE IN EIN KRANKENHAUS? WERDE ICH WEITERHIN VON MEINEN MEDIZINISCHEN
DIE STECKER 1 - ALLGEMEINE HINWEISE WICHTIG! ACHTUNG VERSION MIT STANDARD-LAGERSCHALEN VERSION MIT OS-FIT LAGERSCHALEN. Rev.
 DIE STECKER - ALLGEMEINE HINWEISE WICHTIG! Beim Zusammenbau der elektrischen Stecker muss darauf geachtet werden, dass keine Flüssigkeiten oder Verunreinigungen an diese gelangen. Um bei der Montage des
DIE STECKER - ALLGEMEINE HINWEISE WICHTIG! Beim Zusammenbau der elektrischen Stecker muss darauf geachtet werden, dass keine Flüssigkeiten oder Verunreinigungen an diese gelangen. Um bei der Montage des
Pin-Pflege bei Versorgung mit Fixateur Externe
 PATIENTEN INFORMATION Pin-Pflege bei Versorgung mit Fixateur Externe INHALTSVERZEICHNIS WAS IST EXTERNE FIXATION? 1 WARUM IST DIE PIN-EINTRITTSSTELLE SO WICHTIG? 1 PFLEGE UND REINIGUNG 2 WAS IST ERFORDERLICH?
PATIENTEN INFORMATION Pin-Pflege bei Versorgung mit Fixateur Externe INHALTSVERZEICHNIS WAS IST EXTERNE FIXATION? 1 WARUM IST DIE PIN-EINTRITTSSTELLE SO WICHTIG? 1 PFLEGE UND REINIGUNG 2 WAS IST ERFORDERLICH?
Kanülierungsschulung
 Kanülierungsschulung Beachten Sie alle Kontraindikationen, Warn- und Vorsichtshinweise, möglichen unerwünschten Ereignisse sowie alle anderen Hinweise in der Gebrauchsanweisung. 00274 DE Rev F 12Sep2014
Kanülierungsschulung Beachten Sie alle Kontraindikationen, Warn- und Vorsichtshinweise, möglichen unerwünschten Ereignisse sowie alle anderen Hinweise in der Gebrauchsanweisung. 00274 DE Rev F 12Sep2014
UT-CG010EPS R Set Magnete und Kabeldurchführungen SR-RE EPS. UT-CG010ATEPS R Set Magnete und Kabeldurchführungen ATH EPS
 MONTAGE 1 - RUNDE POWER UNIT (LÖSUNG 2) 1.1 - ANBRINGUNG IM INNEREN DES SATTELROHRS MIT KABELN NACH OBEN (MIT MEHR PLATZBEDARF NACH UNTEN) Empfohlen bei kleineren Rahmen, bei denen die Power Unit an der
MONTAGE 1 - RUNDE POWER UNIT (LÖSUNG 2) 1.1 - ANBRINGUNG IM INNEREN DES SATTELROHRS MIT KABELN NACH OBEN (MIT MEHR PLATZBEDARF NACH UNTEN) Empfohlen bei kleineren Rahmen, bei denen die Power Unit an der
GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE ENDOTAK RELIANCE SG
 GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE ENDOTAK RELIANCE Stimulations-/Detektions- und Defibrillations-Elektrode Integrierte bipolare DF4-LLHH- und DF4-LLHO-Stecker Ankerfixierung ENDOTAK RELIANCE
GEBRAUCHSANWEISUNG FÜR DEN ARZT ZUR ELEKTRODE ENDOTAK RELIANCE Stimulations-/Detektions- und Defibrillations-Elektrode Integrierte bipolare DF4-LLHH- und DF4-LLHO-Stecker Ankerfixierung ENDOTAK RELIANCE
Handbuch Reparatur. Scheuten Module Reparatur-Kit (Solexus Anschlussdose) Patent pending, all rights reserved
 Handbuch Reparatur Scheuten Module Reparatur-Kit (Solexus Anschlussdose) Patent pending, all rights reserved De Steeg 3 6333 AT Schimmert Niederlande T +31 (0) 45 404 04 14 www.junctionboxrepair.com Seite
Handbuch Reparatur Scheuten Module Reparatur-Kit (Solexus Anschlussdose) Patent pending, all rights reserved De Steeg 3 6333 AT Schimmert Niederlande T +31 (0) 45 404 04 14 www.junctionboxrepair.com Seite
Aufbereitung der Zusatzinstrumente in der flexiblen Endoskopie. DGKS Irene Reinthaler Fa. MicroMed GmbH
 Aufbereitung der Zusatzinstrumente in der flexiblen Endoskopie DGKS Irene Reinthaler Fa. MicroMed GmbH Endotherapieprodukte sind alle Instrumente, die sich durch den Arbeitskanal von flexiblen Endoskopen
Aufbereitung der Zusatzinstrumente in der flexiblen Endoskopie DGKS Irene Reinthaler Fa. MicroMed GmbH Endotherapieprodukte sind alle Instrumente, die sich durch den Arbeitskanal von flexiblen Endoskopen
1 Patienteninformation
 Patienteninformation 1 2 3 4 Verbesserung der Bewegungsfähigkeit Das Gerät GONDOLA wurde entwickelt, um eine AMPS- Behandlung (Automatisierte Mechanische Periphere Stimulation) zu bieten. Die AMPS-Behandlung
Patienteninformation 1 2 3 4 Verbesserung der Bewegungsfähigkeit Das Gerät GONDOLA wurde entwickelt, um eine AMPS- Behandlung (Automatisierte Mechanische Periphere Stimulation) zu bieten. Die AMPS-Behandlung
Selbstlernmodul: Einsatz des PleuraFlow Systems auf der Intensivstation
 Clearing the Pathway to Recovery Selbstlernmodul: Einsatz des PleuraFlow Systems auf der Intensivstation Anschließen, Austauschen oder Entfernen eines PleuraFlow Systems auf der Intensivstation Haftungsausschluss:
Clearing the Pathway to Recovery Selbstlernmodul: Einsatz des PleuraFlow Systems auf der Intensivstation Anschließen, Austauschen oder Entfernen eines PleuraFlow Systems auf der Intensivstation Haftungsausschluss:
Injektor zur Implantation von hydrophilen preloaded 1stQ Intraokularlinsen
 Gebrauchsanweisung 1st Inject P2.2 Instrument Injektor zur Implantation von hydrophilen preloaded 1stQ Intraokularlinsen Gebrauchsanweisungen werden auf unserer Webseite bereitgestellt: www.1stq.de Inhalt:
Gebrauchsanweisung 1st Inject P2.2 Instrument Injektor zur Implantation von hydrophilen preloaded 1stQ Intraokularlinsen Gebrauchsanweisungen werden auf unserer Webseite bereitgestellt: www.1stq.de Inhalt:
G112 gitarren box. bedienungsanleitung
 G112 gitarren box bedienungsanleitung Musikhaus Thomann Thomann GmbH Hans-Thomann-Straße 1 96138 Burgebrach Deutschland Telefon: +49 (0) 9546 9223-0 E-Mail: info@thomann.de Internet: www.thomann.de 06.03.2017,
G112 gitarren box bedienungsanleitung Musikhaus Thomann Thomann GmbH Hans-Thomann-Straße 1 96138 Burgebrach Deutschland Telefon: +49 (0) 9546 9223-0 E-Mail: info@thomann.de Internet: www.thomann.de 06.03.2017,
Externe GSM-Antenne V Nachtrag zur Installation
 Externe GSM-Antenne 970.191 V1 2015.04 de Nachtrag zur Installation Externe GSM-Antenne Sicherheitshinweise de 3 1 Sicherheitshinweise VORSICHT! Lesen Sie diese Sicherheitshinweise vor der Installation
Externe GSM-Antenne 970.191 V1 2015.04 de Nachtrag zur Installation Externe GSM-Antenne Sicherheitshinweise de 3 1 Sicherheitshinweise VORSICHT! Lesen Sie diese Sicherheitshinweise vor der Installation
RESONATE HF ICD, RESONATE EL ICD, PERCIVA HFICD, PERCIVA ICD, CHARISMA ELICD, VIGILANT ELICD, MOMENTUM EL ICD
 GEBRAUCHSANWEISUNG FÜR DEN ARZT RESONATE HF ICD, RESONATE EL ICD, PERCIVA HFICD, PERCIVA ICD, CHARISMA ELICD, VIGILANT ELICD, MOMENTUM EL ICD IMPLANTIERBARER CARDIOVERTER/ DEFIBRILLATOR REF D520, D521,
GEBRAUCHSANWEISUNG FÜR DEN ARZT RESONATE HF ICD, RESONATE EL ICD, PERCIVA HFICD, PERCIVA ICD, CHARISMA ELICD, VIGILANT ELICD, MOMENTUM EL ICD IMPLANTIERBARER CARDIOVERTER/ DEFIBRILLATOR REF D520, D521,
PlayStation Camera. Bedienungsanleitung CUH-ZEY
 PlayStation Camera Bedienungsanleitung CUH-ZEY2 7028416 DE Vor der Inbetriebnahme ˎˎLesen Sie diese Bedienungsanleitung und die Bedienungsanleitungen kompatibler Hardware bitte gründlich durch und bewahren
PlayStation Camera Bedienungsanleitung CUH-ZEY2 7028416 DE Vor der Inbetriebnahme ˎˎLesen Sie diese Bedienungsanleitung und die Bedienungsanleitungen kompatibler Hardware bitte gründlich durch und bewahren
AirPort Extreme Kart. Hinweis: Online-Anweisungen finden Sie unter der Adresse
 Deutsch Austausch Anleitung AirPort Extreme Kart AppleCare Bitte folgen Sie diesen Anweisungen gewissenhaft. Geschieht dies nicht, können die Geräte beschädigt werden, und Ihr Garantieanspruch kann verlorengehen.
Deutsch Austausch Anleitung AirPort Extreme Kart AppleCare Bitte folgen Sie diesen Anweisungen gewissenhaft. Geschieht dies nicht, können die Geräte beschädigt werden, und Ihr Garantieanspruch kann verlorengehen.
Operationstechnik MODUS MDO 1.5 Le Fort I Distraktor
 Operationstechnik MODUS MDO 1.5 Le Fort I Distraktor Der MODUS MDO 1.5 Le Fort I Distraktor ist Teil von MODUS MDO 1.5 und besteht aus Adaptionsplatten (M-4978/79), Schrauben, Distraktionszylindern, flexiblen
Operationstechnik MODUS MDO 1.5 Le Fort I Distraktor Der MODUS MDO 1.5 Le Fort I Distraktor ist Teil von MODUS MDO 1.5 und besteht aus Adaptionsplatten (M-4978/79), Schrauben, Distraktionszylindern, flexiblen
ÖNORM FprEN ISO 17664:2017. Vom Medizinprodukt-Hersteller bereitzustellende Informationen für die Aufbereitung von Medizinprodukten
 ÖNORM FprEN ISO 17664:2017 Vom Medizinprodukt-Hersteller bereitzustellende Informationen für die Aufbereitung von Medizinprodukten ÖGSV-Fachtagung 2017 EUROPÄISCHE NORM EUROPEAN STANDARD NORME EUROPÉENNE
ÖNORM FprEN ISO 17664:2017 Vom Medizinprodukt-Hersteller bereitzustellende Informationen für die Aufbereitung von Medizinprodukten ÖGSV-Fachtagung 2017 EUROPÄISCHE NORM EUROPEAN STANDARD NORME EUROPÉENNE
Patienteninformation Portsysteme
 Portsysteme Am Leben teilhaben schonend therapieren Jedes Jahr erhalten tausende Patienten ein implantierbares Portsystem kurz Port um im Rahmen ihrer Therapie auch über einen längeren Zeitraum schonend
Portsysteme Am Leben teilhaben schonend therapieren Jedes Jahr erhalten tausende Patienten ein implantierbares Portsystem kurz Port um im Rahmen ihrer Therapie auch über einen längeren Zeitraum schonend
Immer für Sie da. Hier können Sie Ihr Produkt registrieren und Unterstützung erhalten: SPA2100.
 Immer für Sie da Hier können Sie Ihr Produkt registrieren und Unterstützung erhalten: www.philips.com/welcome SPA2100 Benutzerhandbuch Inhaltsangabe 1 Sicherheit 2 Wichtige Sicherheitshinweise 2 2 Hinweis
Immer für Sie da Hier können Sie Ihr Produkt registrieren und Unterstützung erhalten: www.philips.com/welcome SPA2100 Benutzerhandbuch Inhaltsangabe 1 Sicherheit 2 Wichtige Sicherheitshinweise 2 2 Hinweis
Dieses Paket enthält die folgenden Sprachen:
 DE OSTEOSET XR KNOCHENHOHLRAUMFÜLLER 150841-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DE OSTEOSET XR KNOCHENHOHLRAUMFÜLLER 150841-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
Nokia Lautsprecher-Station MD-3
 Nokia Lautsprecher-Station MD-3 9253870/2 DEUTSCH Die Lautsprecher-Station MD-3 bieten eine qualitativ hochwertige Audiowiedergabe, wenn Sie mit einem kompatiblen Nokia Telefon oder Audiogerät Musik oder
Nokia Lautsprecher-Station MD-3 9253870/2 DEUTSCH Die Lautsprecher-Station MD-3 bieten eine qualitativ hochwertige Audiowiedergabe, wenn Sie mit einem kompatiblen Nokia Telefon oder Audiogerät Musik oder
1.1 Angefragte Untersuchungs- und Behandlungsmethode (Kurzbezeichnung, max. 200 Zeichen)
 NUB 1/4 1.1 Angefragte Untersuchungs- und Behandlungsmethode (Kurzbezeichnung, max. 200 Zeichen) Magenschrittmacher 1.2 Alternative Bezeichnunge(en) der Methode Enterra 1.3 Beschreibung der Methode Die
NUB 1/4 1.1 Angefragte Untersuchungs- und Behandlungsmethode (Kurzbezeichnung, max. 200 Zeichen) Magenschrittmacher 1.2 Alternative Bezeichnunge(en) der Methode Enterra 1.3 Beschreibung der Methode Die
Power Distribution Suitcase Botex PDS 16/s IP 44
 Betriebsanleitung Power Distribution Suitcase Botex PDS 16/s IP 44 Version: Draft () - de Thomann GmbH Hans-Thomann-Straße 1, 96138 Burgebrach, Germany www.thomann.de Inhalt Inhalt 1 Sicherheit...4 1.1
Betriebsanleitung Power Distribution Suitcase Botex PDS 16/s IP 44 Version: Draft () - de Thomann GmbH Hans-Thomann-Straße 1, 96138 Burgebrach, Germany www.thomann.de Inhalt Inhalt 1 Sicherheit...4 1.1
Ob ein Einkammer- oder Zweikammer-Schrittmacher notwendig ist, ergibt sich aus der Analyse der langsamen Rhythmusstörung des Herzens.
 Kantonsspital Uri CH-6460 Altdorf Telefon 041 875 51 51 Telefax 041 875 54 00 www.ksuri.ch Schrittmacher Schrittmacher sind Geräte, die eine zu langsame Herzaktion beheben. Ein Schrittmacher besteht aus
Kantonsspital Uri CH-6460 Altdorf Telefon 041 875 51 51 Telefax 041 875 54 00 www.ksuri.ch Schrittmacher Schrittmacher sind Geräte, die eine zu langsame Herzaktion beheben. Ein Schrittmacher besteht aus
