Vorläufige Notiz über eine etwas abgeänderte Betrachtungsweise der Alkohole und ihrer Derivate Von Privatdozent Erlenmeyer.
|
|
|
- Heinrich Hoch
- vor 7 Jahren
- Abrufe
Transkript
1 Vorläufige Notiz über eine etwas abgeänderte Betrachtungsweise der Alkohole und ihrer Derivate Von Privatdozent Erlenmeyer. Wir sind in der Entwicklungsgeschichte der Chemie zu einem Punkte der Erkenntnis gelangt, welche es uns für jetzt als erscheinen lässt, die wahre Konstitution der chemischen Verbindungen zu ermitteln. Die Wissenschaft hat, seitdem wir diesen Punkt erreicht haben, ungleich raschere und bedeutungsvollere Fortschritte gemacht, als in der Periode, in welcher man auf e i n e Bildungs- oder Zersetzungsweise eines zusammengesetzten Körpers die Formel der wirklichen Lagerung der kleinsten Teilchen der Bestandteile als unumstössliche Wahrheit gründen zu können glaubte. Wir sind jetzt so weit vorangeschritten, dass wir einer jeden Betrachtungsweise oder Form der Schreibweise der Bestandteile einer Verbindung volle Berechtigung zuerkennen, sobald sie nur ein Bild der chemischen Spaltbarkeit, wenn auch nur unter dem Einfluss eines einzigen Reagens zu geben geeignet ist. Die Betrachtungsweise, welche die chemische Spaltbarkeit einer Verbindung oder einer Reihe von Verbindungen unter möglichst verschiedenen Einflüssen erkennen lässt, ist gerechtermassen die am meistern bevorzugte. Einer solchen Stellung hat sich die typische Betrachtungsweise [Typentheorie] zu erfreuen. Seit ihrem ersten Erscheinen ist sie auf die mannigfaltigste Weise variiert worden und man muss gestehen, dass eine ihrer vorteilhaftesten Seiten ihre grosse Beweglichkeit ist. Die Betrachtungsweise, von der ich im Folgenden eine kurze Skizze entwerfen will, hat ihre Entstehung eben dieser Beweglichkeit zu danken. Bisher hat man h a u p t s ä ch l i ch drei Reihen von Alkoholen mit gleichem Kohlenstoffgehalt angenommen, die einsäurigen (Alkohole), die zweisäurigen (Glycole), die dreisäurigen (Glycerine). Die ersten leitete man von dem Typus 2, die zweiten von dem Typus 4 2, die letzten von dem Typus 6 3 ab 1. Derivierend von diesen nahm man ein- zwei- und dreiatomige etc. (in manchen Fällen auch bis mehr b a s i s ch e) Säuren an. Nach der folgenden Skizze lassen sich alle Alkohole und ihre Derivate als einatomige (die Säuren mitunter aber als mehrbasische) betrachten. Ich gebe vor der and nur die Formeln der aus den zwei ersten Alkoholen ableitbaren Verbindungsreihen, ohne die Tatsachen auf welche sie sich beziehen, hinzuzufügen. Der Leser wird leicht diesen Mangel ergänzen, da man, wie ich mich überzeugt habe, eine grosse Anzahl von Tatsachen durch diese Formeln nicht allein sehen sondern, wie ich meine, auch voraussehen kann. Sollte diese Betrachtungsweise für die Förderung der Wissenschaft trotz meiner Meinung keinen u n m i t t e l b a r e n Nutzen stiften, so wird sie doch m i t t e l b a r dadurch nützlich werden, dass sie wieder einmal daran erinnert, dass wird den Fortschritt der Wissenschaft hemmen, wenn wir uns fest an e i n e Schreibweise anklammern und sie verteidigen. Wir werden dadurch nach längerem Gebrauch unbewusst verleitet, sie für die Ausdrucksweise der wahren chemischen Konstitution zu halten und wir versperren uns selbst mehr oder weniger die Wege zur Aufsuchung neuer Beziehungen und zu neuen Entdeckungen. Ich meinerseits halte es für weit erspriesslicher für die Wissenschaft, we n n m a n d a r n a ch t r a cht e t d u r ch d a s E x p e r i m e nt s e l b s t a u f g e s t e l l t e B e t r a cht u n g s we i s e n z u w i d e r l e g e n, als sie durch gewalttätiges Anpassen an die Tatsachen, nur zur Rettung seines Geistesprodukts zu verteidigen. 1 In analoger Weise wurden die 4-, 5- und 6 atomigen von 4 mal, 5 mal und 6 mal 2 abgeleitet. 1
2 ier folgt meine Skizze: Alkohole und Glycole und Glycerine und Typus 2 Typus 2 Typus 2 Alkohole Aldehyde Säuren [Seitenwechsel im riginal] C 3 C C C 2 () C() C() (Kohlensäure) C() 2 Alkohole Aldehyde Säuren I. Dehyde der Säuren I. Säuren II. Alkohole und C 2 5 C 2 3 C 2 3 C 2 (Glycolid?) C 2 2 (Glycolid?) Glycole und C 2 4 () C 2 2 () C 2 2 () C 2 () (Glyoxal?) C 2 () 2 (xalsäure?) Glycerine und C 2 3 () 2 C 2 () 2 C 2 () 2 (Glyoxylsäure?) Diese Formeln mögen genügen um die Richtung dieser Betrachtungsweise anzudeuten. Es ist aus der Skizze von selbst einleuchtend, dass von dem Methyl noch ein Alkohol denkbar ist von C() der Formel 3. Von dem Aethyl können noch 3 weitere existieren: C 2 2 () 3 C, 2 () 4 und C 2() 5, von denen der erste auch noch ein Dehyd C 2 () 3 C und eine zugehörige Säure haben kann: 2 () 3. Bei den höheren o- 2
3 mologen wird natürlich die Mannigfaltigkeit der Alkohole, Säuren und Deyhde immer grösser. Wenn man dort die Abkömmlinge verfolgt, so wird man manche sehr einfache Beziehungen finden. Säuredehyde (Säuren minus 2 ) scheinen auch in den kohlenstoffreicheren Reihen schon bekannt zu sein. Ferner treten bei dieser Betrachtungsweise auch manche einfache Erklärungen von Isomerien zu Tag. (Noch will ich bemerken, dass man vom Wasser ausgehend mit Methyl, Sauerstoff und Wasserstoffhyperoxyd alle Formeln der verschiedenen Alkoholreihen und deren Derivate aufbauen kann.) e i d e l b e r g, im März 1861 Der vorangegangene Artikel ist wie folgt zu zitieren: Emil Erlenmeyer: Zeitschrift für Chemie und Pharmacie, 4, Verlag von Ferdinand Enke, Erlangen, 1861, S Die Rechtschreibung wurde auf den neusten Stand (2008) gebracht. Da der Verfasser Emil Erlenmeyer ( ) bereits vor mehr als 70 Jahren verstorben ist, darf der Artikel frei verwendet werden. Digitalisierung mittels L A TEX durch Joël Gubler. 3
4
5
Quadratische Gleichungen
 Quadratische Gleichungen Alle aufgezeigten Lösungswege gelten für Gleichungen, die schon vereinfacht und zusammengefasst wurden. Es darf nur noch + vorhanden sein!!! (Also nicht + und auch nicht 3 ; bitte
Quadratische Gleichungen Alle aufgezeigten Lösungswege gelten für Gleichungen, die schon vereinfacht und zusammengefasst wurden. Es darf nur noch + vorhanden sein!!! (Also nicht + und auch nicht 3 ; bitte
Organische Chemie. Kohlenwasserstoffe. Alkane. Alkane
 1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
Inhaltsverzeichnis. 3 Gesättigte Kohlenwasserstoffe (Alkane) 3.1 Offenkettige Alkane 3.2 Cyclische Alkane
 Inhaltsverzeichnis 1 Chemische Bindung in organischen Verbindungen 1.1 Einleitung 1.2 Grundlagen der chemischen Bindung 1.3 Die Atombindung (kovalente oder homöopolare Bindung) 1.4 Bindungslängen und Bindungsenergien
Inhaltsverzeichnis 1 Chemische Bindung in organischen Verbindungen 1.1 Einleitung 1.2 Grundlagen der chemischen Bindung 1.3 Die Atombindung (kovalente oder homöopolare Bindung) 1.4 Bindungslängen und Bindungsenergien
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 26.02.2018 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 2 H 4 O 2 ein, die die folgenden Eigenschaften
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 26.02.2018 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 2 H 4 O 2 ein, die die folgenden Eigenschaften
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
Repetitionen Chemie und Werkstoffkunde
 BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 2 Begriffe der Chemie und Werkstoffkunde Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1,
BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 2 Begriffe der Chemie und Werkstoffkunde Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1,
Repetitionen Chemie und Werkstoffkunde
 BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 2 Begriffe der Chemie und Werkstoffkunde Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1,
BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 2 Begriffe der Chemie und Werkstoffkunde Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1,
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 4 H 8 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung zeigt eine positive Fehling-Probe. -
Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 4 H 8 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung zeigt eine positive Fehling-Probe. -
Chemie-Tutorien zur Vorbereitung auf das Praktikum
 Seite 1 von 7 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie-Tutorien zur Vorbereitung auf das Praktikum 07.03.-18.03.2017 Dienstag, 07.03.2017 18.00-20.00 Uhr Grundlagen der Chemie I Donnerstag, 09.03.2017
Seite 1 von 7 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie-Tutorien zur Vorbereitung auf das Praktikum 07.03.-18.03.2017 Dienstag, 07.03.2017 18.00-20.00 Uhr Grundlagen der Chemie I Donnerstag, 09.03.2017
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 8 O 3 ein, die die folgenden Eigenschaften besitzt: - Die Verbindung ist vollständig mit Wasser mischbar.
Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 8 O 3 ein, die die folgenden Eigenschaften besitzt: - Die Verbindung ist vollständig mit Wasser mischbar.
RAHMENRICHTLINIEN SEKUNDARSCHULE CHEMIE KULTUSMINISTERIUM. Schuljahrgänge 7 10
 RAHMENRICHTLINIEN SEKUNDARSCHULE (Ergänzung der RRL Sekundarschule Schuljahrgänge 7 10 in Umsetzung der Bildungsstandards für das Fach Chemie für den Mittleren Schulabschluss) CHEMIE Schuljahrgänge 7 10
RAHMENRICHTLINIEN SEKUNDARSCHULE (Ergänzung der RRL Sekundarschule Schuljahrgänge 7 10 in Umsetzung der Bildungsstandards für das Fach Chemie für den Mittleren Schulabschluss) CHEMIE Schuljahrgänge 7 10
4. Reaktionsgeschwindigkeit und chemisches Gleichgewicht
 Chemie RG mit DG, Themenbereiche, Seite 1 von 4 Chemie im Realgymnasium mit DG, 5-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
Chemie RG mit DG, Themenbereiche, Seite 1 von 4 Chemie im Realgymnasium mit DG, 5-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
Verzeichnis der Wortabkürzungen... Verzeichnis der Zeichen und Symbole...XVII
 VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
Eine Einführung in die Organische Chemie
 Kapitel 10 Eine Einführung in die Organische Chemie Abb. 10.1: Das erste e Molekül. Seit der Begründung der Naturwissenschaft Chemie haben die Stoffe der belebten Natur, von Organismen, einen besonderen
Kapitel 10 Eine Einführung in die Organische Chemie Abb. 10.1: Das erste e Molekül. Seit der Begründung der Naturwissenschaft Chemie haben die Stoffe der belebten Natur, von Organismen, einen besonderen
Grundwissen Chemie Klasse
 Grundwissen Chemie 8. 10. Klasse Grundwissen Chemie 8I Chemie Reinstoff und Gemisch Atome und Moleküle Chemische Reaktionen Analyse und Synthese Katalysatoren Luft Sauerstoff und Wasserstoff Redoxreaktionen
Grundwissen Chemie 8. 10. Klasse Grundwissen Chemie 8I Chemie Reinstoff und Gemisch Atome und Moleküle Chemische Reaktionen Analyse und Synthese Katalysatoren Luft Sauerstoff und Wasserstoff Redoxreaktionen
Illustriert von Viktoria DUNAJEWA
 Axel, schau mal, womit diese Ausgabe der TROPINKA Warum beginnt! druckt man denn so ein Gedicht in einer christlichen Zeitschrift ab? Alle wissen doch, dass Gott die Welt geschaffen hat! Wissen das denn
Axel, schau mal, womit diese Ausgabe der TROPINKA Warum beginnt! druckt man denn so ein Gedicht in einer christlichen Zeitschrift ab? Alle wissen doch, dass Gott die Welt geschaffen hat! Wissen das denn
Inhaltsverzeichnis. 3 Organische Chemie. Vorwort Chemische Bindung Chemische Reaktionstypen Bindungen...
 VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
Schriftliche Abschlussprüfung Chemie
 Sächsisches Staatsministerium für Kultus Schuljahr 2004/2005 Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Sächsisches Staatsministerium für Kultus Schuljahr 2004/2005 Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Bist Du nicht "FIT", dann musst Du nacharbeiten.
 Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
chulportfolio 3. Schulkonzept 3.7 Kern- und Schulcurricula G9 (Klasse 5 11) Chemie Chemie Klasse 11
 Bildungsstandards Kerncurriculum Schulcurriculum Empfohlener Stundenumfang Die SuS können Stoffe beschreiben (Alkane, Alkene ); - die Verwendung Stoffe in Alltag und Technik (Methan, Ethen, ); - den Informationsgehalt
Bildungsstandards Kerncurriculum Schulcurriculum Empfohlener Stundenumfang Die SuS können Stoffe beschreiben (Alkane, Alkene ); - die Verwendung Stoffe in Alltag und Technik (Methan, Ethen, ); - den Informationsgehalt
Entwicklung der modernen Naturwissenschaft (speziell der Physik/Mechanik) in Abgrenzung von der mittelalterlich-scholastischen Naturphilosophie
 René Descartes (1596-1650) Meditationen über die Grundlagen der Philosophie (1641) Geistes- bzw. wissenschaftsgeschichtlicher Hintergrund Entwicklung der modernen Naturwissenschaft (speziell der Physik/Mechanik)
René Descartes (1596-1650) Meditationen über die Grundlagen der Philosophie (1641) Geistes- bzw. wissenschaftsgeschichtlicher Hintergrund Entwicklung der modernen Naturwissenschaft (speziell der Physik/Mechanik)
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 15.03.2017 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 7 H 8 ein, die die folgenden Eigenschaften
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 15.03.2017 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 7 H 8 ein, die die folgenden Eigenschaften
Wesentliche Bereiche für den Gegenstand Chemie
 Wesentliche Bereiche für den Gegenstand Chemie Semesterbezeichnungen laut Lehrplan: 6. Klasse Wintersemester: 3. Semester 6. Klasse Sommersemester: 4. Semester 7. Klasse Wintersemester: 5. Semester 7.
Wesentliche Bereiche für den Gegenstand Chemie Semesterbezeichnungen laut Lehrplan: 6. Klasse Wintersemester: 3. Semester 6. Klasse Sommersemester: 4. Semester 7. Klasse Wintersemester: 5. Semester 7.
Studien über Quercetin und seine Derivate
 198 Akademie d. Wissenschaften Wien; download unter www.biologiezentrum.at Studien über Quercetin und seine Derivate (VI. Abhandlung) von Dr. J. Herzig. Aus dem I. Chemischen Universitätslaboratorium in
198 Akademie d. Wissenschaften Wien; download unter www.biologiezentrum.at Studien über Quercetin und seine Derivate (VI. Abhandlung) von Dr. J. Herzig. Aus dem I. Chemischen Universitätslaboratorium in
Induktion im Lexikon: logische Herleitung allgemeiner Regeln von Einzelfällen zu allgemeinen Gesetzen aufsteigen
 Eine Induktionslogik gibt es nicht. Induktion im Lexikon: logische Herleitung allgemeiner Regeln von Einzelfällen zu allgemeinen Gesetzen aufsteigen Popper zitiert Einstein: Zu diesen Gesetzen führt kein
Eine Induktionslogik gibt es nicht. Induktion im Lexikon: logische Herleitung allgemeiner Regeln von Einzelfällen zu allgemeinen Gesetzen aufsteigen Popper zitiert Einstein: Zu diesen Gesetzen führt kein
ELEMENTARSTOFFE, VERBINDUNGEN und chemische Formeln LÖSUNG. Hinweis: In den Salzen kommen die Metallatome stets als einatomige Kationen vor.
 Hinweis: In den Salzen kommen die Metallatome stets als einatomige Kationen vor. Aufgabe 1: a) Tragen Sie die folgenden chemischen Formeln in die richtige Spalte der Tabelle ein. Beachten Sie, dass mehrere
Hinweis: In den Salzen kommen die Metallatome stets als einatomige Kationen vor. Aufgabe 1: a) Tragen Sie die folgenden chemischen Formeln in die richtige Spalte der Tabelle ein. Beachten Sie, dass mehrere
Die Stoffteilchen (II): Ionengruppen und ihre Ionen
 Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Flüssiggasfeuerzeug BIFIE
 Flüssiggasfeuerzeug Flüssiggasfeuerzeuge sind mit Butan befüllt. Seite 1 1. Ein solches Flüssiggasfeuerzeug wird vor dem Gebrauch gewogen (Bild 1) und gezündet (Bild 2). Bild 1 Bild 2 Wenn man es 20 Sekunden
Flüssiggasfeuerzeug Flüssiggasfeuerzeuge sind mit Butan befüllt. Seite 1 1. Ein solches Flüssiggasfeuerzeug wird vor dem Gebrauch gewogen (Bild 1) und gezündet (Bild 2). Bild 1 Bild 2 Wenn man es 20 Sekunden
 INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
Schwingungsspektroskopie
 Schwingungsspektroskopie In N-atomigen Molekülen haben wir 3N-5 (linear) bzw. 3N-6 (nichtlinear) Freiheitsgrade der Schwingung, welche die Position der Atome relativ zueinander beschreiben. Der Potentialterm
Schwingungsspektroskopie In N-atomigen Molekülen haben wir 3N-5 (linear) bzw. 3N-6 (nichtlinear) Freiheitsgrade der Schwingung, welche die Position der Atome relativ zueinander beschreiben. Der Potentialterm
Definiere den Begriff Orbital. Erkläre den ph-wert! Erkläre die Autoprotolyse des Wassers mit Hilfe der Reaktionsgleichung.
 Definiere den Begriff rbital. Das rbital ist ein Bereich, in dem sich ein Elektron mit großer Wahrscheinlichkeit befindet. In jedem rbital befinden sich maximal zwei Elektronen. Erkläre den pwert! Der
Definiere den Begriff rbital. Das rbital ist ein Bereich, in dem sich ein Elektron mit großer Wahrscheinlichkeit befindet. In jedem rbital befinden sich maximal zwei Elektronen. Erkläre den pwert! Der
Elektrophile Additionen von HX an die CC-Doppelbindung (Vollhardt, 3. Aufl., S , 4. Aufl., S ; Hart, S ; Buddrus, S.
 Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
Thema: Logik: 2. Teil. Übersicht logische Operationen Name in der Logik. Negation (Verneinung) Nicht
 Thema: Logik: 2. Teil Übersicht logische Operationen Name in der Logik Symbol Umgangssprachlicher Name Negation (Verneinung) Nicht Konjunktion ^ Und Disjunktion v Oder Subjunktion (Implikation) Bijunktion
Thema: Logik: 2. Teil Übersicht logische Operationen Name in der Logik Symbol Umgangssprachlicher Name Negation (Verneinung) Nicht Konjunktion ^ Und Disjunktion v Oder Subjunktion (Implikation) Bijunktion
4. Chemische Reaktionen und Energieumsatz, Thermochemie
 Chemie RG mit LS, Themenbereiche, Seite 1 von 4 Chemie im Realgymnasium mit LS, 6-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
Chemie RG mit LS, Themenbereiche, Seite 1 von 4 Chemie im Realgymnasium mit LS, 6-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
Chemisch-technologisches
 Chemisch-technologisches Rechnen Von Prof. Dr. Ferdinand Fiseber Bearbeitet von Fr. Hartner Fabrikduektor Dritte Auflage Mit 2 Diagrammen Springer-Verlag Berlin Heidelberg GmbH 1912 Springer-Verlag Berlin
Chemisch-technologisches Rechnen Von Prof. Dr. Ferdinand Fiseber Bearbeitet von Fr. Hartner Fabrikduektor Dritte Auflage Mit 2 Diagrammen Springer-Verlag Berlin Heidelberg GmbH 1912 Springer-Verlag Berlin
Erwartete Kompetenzen
 Stoffverteilungsplan Kerncurriculum für die Oberschule/Realschule in Niedersachsen (Schuljahrgänge 7/8) PRISMA Chemie Niedersachsen Differenzierende Ausgabe Band 7/8 Schule: Klettbuch ISBN 978-3-12-068537-1
Stoffverteilungsplan Kerncurriculum für die Oberschule/Realschule in Niedersachsen (Schuljahrgänge 7/8) PRISMA Chemie Niedersachsen Differenzierende Ausgabe Band 7/8 Schule: Klettbuch ISBN 978-3-12-068537-1
Sechster Brief. Schwefelwasserstoffsäure. Jodwasserstoffsäure. Schwefel 94,19 ; Jod 99,21 Wasserstoff 5,81 ; Wasserstoff 0,79 100,00 ; 100,00
 Sechster Brief. Bei diesen Zersetzungen und Verbindungen liegt die Frage ganz nahe, wie viel man von einem Körper nöthig hat, um mit einem zweiten eine chemische Verbindung hervorzubringen, wie viel man
Sechster Brief. Bei diesen Zersetzungen und Verbindungen liegt die Frage ganz nahe, wie viel man von einem Körper nöthig hat, um mit einem zweiten eine chemische Verbindung hervorzubringen, wie viel man
a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 8 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung ist zu Propansäure oxidierbar. - Die
Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 8 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung ist zu Propansäure oxidierbar. - Die
Chemie im Realgymnasium mit LS, 6-stündig Themenbereiche für die Reifeprüfung
 Chemie RG mit LS, Themenbereiche, Seite 1 von 5 Chemie im Realgymnasium mit LS, 6-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
Chemie RG mit LS, Themenbereiche, Seite 1 von 5 Chemie im Realgymnasium mit LS, 6-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
VERSTEHEN UND VERARBEITEN EINES LESETEXTES
 VERSTEHEN UND VERARBEITEN EINES LESETEXTES Justus Liebig einer der bedeutendsten deutschen Chemiker 1 2 3 4 5 6 Die deutsche Regierung und wichtige Chemieorganisationen haben das Jahr 2003 zum Jahr der
VERSTEHEN UND VERARBEITEN EINES LESETEXTES Justus Liebig einer der bedeutendsten deutschen Chemiker 1 2 3 4 5 6 Die deutsche Regierung und wichtige Chemieorganisationen haben das Jahr 2003 zum Jahr der
Kerncurriculum Inhalte Zeit Kompetenzen: die Schülerinnen und Schüler können Atome und Periodensystem
 Klassenstufe 9 BS (nach S. 196/197) Curriculum Fach: Chemie Klasse: 9 Hölderlin-Gymnasium Nürtingen Chemie Kerncurriculum Inhalte Zeit Kompetenzen: die Schülerinnen und Schüler können Atome und Periodensystem
Klassenstufe 9 BS (nach S. 196/197) Curriculum Fach: Chemie Klasse: 9 Hölderlin-Gymnasium Nürtingen Chemie Kerncurriculum Inhalte Zeit Kompetenzen: die Schülerinnen und Schüler können Atome und Periodensystem
Nichts als die mathematische Wahrheit
 1 Nichts als die mathematische Wahrheit Holger Stephan Weierstraß Institut für Angewandte Analysis und Stochastik (WIAS), Berlin Lange Nacht der Wissenschaften 10. Mai 2014 2 Anregungen zu folgenden Fragen
1 Nichts als die mathematische Wahrheit Holger Stephan Weierstraß Institut für Angewandte Analysis und Stochastik (WIAS), Berlin Lange Nacht der Wissenschaften 10. Mai 2014 2 Anregungen zu folgenden Fragen
CH-Matura TB 1 STOFFEIGENSCHAFTEN, ATOMBAU THEMENBEREICH 1: Themenbereiche Chemie
 TB 1 THEMENBEREICH 1: STOFFEIGENSCHAFTEN, ATOMBAU Der Kandidat/ die Kandidatin kennt die wichtigsten Stoffeigenschaften und einfache Methoden um diese zu bestimmen. Er/Sie kann den Atombau nach BOHR erklären
TB 1 THEMENBEREICH 1: STOFFEIGENSCHAFTEN, ATOMBAU Der Kandidat/ die Kandidatin kennt die wichtigsten Stoffeigenschaften und einfache Methoden um diese zu bestimmen. Er/Sie kann den Atombau nach BOHR erklären
Schwingungsspektroskopie
 In N atomigen Molekülen haben wir 3N 5 (linear) bzw. 3N 6 (nichtlinear) Freiheitsgrade der Schwingung, welche die Position der Atome relativ zueinander beschreiben. Der Potentialterm wird zu einer komplizierten
In N atomigen Molekülen haben wir 3N 5 (linear) bzw. 3N 6 (nichtlinear) Freiheitsgrade der Schwingung, welche die Position der Atome relativ zueinander beschreiben. Der Potentialterm wird zu einer komplizierten
STOFFE U N D STOFFTRENNUNG
 Inhalt WAS IST CHEMIE? 10 STOFFE U N D STOFFTRENNUNG 22 Chemie erlebt Chem ie-chancen und Gefahren...12 Umgang mit Chemikalien... 14 Chemie erlebt Chemie is t... 16 Methode Regeln beim Experimentieren...17
Inhalt WAS IST CHEMIE? 10 STOFFE U N D STOFFTRENNUNG 22 Chemie erlebt Chem ie-chancen und Gefahren...12 Umgang mit Chemikalien... 14 Chemie erlebt Chemie is t... 16 Methode Regeln beim Experimentieren...17
Frage 1. Klausuraufgaben Grundvorlesung Testat vom , Seite 1 Punkte. Bitte eintragen: Matrikelnummer: Bitte ankreuzen: Biotechnologie Pharmazie
 Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Punkte Matrikelnummer: Name: Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage 1 Skizzieren Sie die
Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Punkte Matrikelnummer: Name: Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage 1 Skizzieren Sie die
Die Stoffteilchen (II): Ionengruppen und ihre Ionen
 Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Selbsteinschätzung: Singletasking
 Devora Zack Die Multitasking-Falle Warum wir nicht alles gleichzeitig können ISBN 978-3-86936-663-0 Selbsteinschätzung: Singletasking Fragen Sie sich gerade, wo Sie selbst stehen? Finden Sie es heraus!
Devora Zack Die Multitasking-Falle Warum wir nicht alles gleichzeitig können ISBN 978-3-86936-663-0 Selbsteinschätzung: Singletasking Fragen Sie sich gerade, wo Sie selbst stehen? Finden Sie es heraus!
b. Lehre des vernünftigen Schlussfolgerns (1. System von Regeln von Aristoteles ( v. Chr.); sprachliche Argumente
 II. Zur Logik 1. Bemerkungen zur Logik a. Logisches Gebäude der Mathematik: wenige Axiome (sich nicht widersprechende Aussagen) bilden die Grundlage; darauf aufbauend Lehrsätze unter Berücksichtigung der
II. Zur Logik 1. Bemerkungen zur Logik a. Logisches Gebäude der Mathematik: wenige Axiome (sich nicht widersprechende Aussagen) bilden die Grundlage; darauf aufbauend Lehrsätze unter Berücksichtigung der
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 26.08.2014 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O 3 ein, die die folgenden Eigenschaften
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 26.08.2014 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O 3 ein, die die folgenden Eigenschaften
EINFÜHRUNG IN DIE ORGANISCHE CHEMIE
 rganische Chemie Lehrgang CEMIE FÜR BILGIELERKRÄFTE EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs
rganische Chemie Lehrgang CEMIE FÜR BILGIELERKRÄFTE EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs
Curriculum Chemie Klasse 10 Albert-Einstein-Gymnasium Ulm
 Curriculum Chemie Klasse 10 Albert-Einstein-Gymnasium Ulm Klasse 10 Themen Kohlenwasserstoffe Alkane - Vorkommen, Eigenschaften und Molekülstruktur - Isomerie und Nomenklatur Kohlenwasserstoffe - Energieträger
Curriculum Chemie Klasse 10 Albert-Einstein-Gymnasium Ulm Klasse 10 Themen Kohlenwasserstoffe Alkane - Vorkommen, Eigenschaften und Molekülstruktur - Isomerie und Nomenklatur Kohlenwasserstoffe - Energieträger
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 16.05.2014 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O 3 ein, die die folgenden Eigenschaften
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 16.05.2014 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O 3 ein, die die folgenden Eigenschaften
Bergische Universität Wuppertal Fachbereich C - Chemie Prof. Dr. Michael W. Tausch
 Bergische Universität Wuppertal Fachbereich C - Chemie Prof. Dr. Michael W. Tausch Klausur in Allgemeine Chemie für das 1. Semester, Studiengang GHR-Lehramt Zugelassene Hilfsmaterialien: Buchners Chemie-Begleiter,
Bergische Universität Wuppertal Fachbereich C - Chemie Prof. Dr. Michael W. Tausch Klausur in Allgemeine Chemie für das 1. Semester, Studiengang GHR-Lehramt Zugelassene Hilfsmaterialien: Buchners Chemie-Begleiter,
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 15.01.2018 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 2 H 2 O 2 ein, die die folgenden Eigenschaften
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 15.01.2018 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 2 H 2 O 2 ein, die die folgenden Eigenschaften
M U S T E R L Ö S U N G
 Prof. Dr.. Reiser Prof. Dr. A. Geyer 1. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 00 am Dienstag, dem 14. Mai 00 Name:...Vorname:... Matrikelnummer:...
Prof. Dr.. Reiser Prof. Dr. A. Geyer 1. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 00 am Dienstag, dem 14. Mai 00 Name:...Vorname:... Matrikelnummer:...
Paul Natorp. Philosophische Propädeutik. in Leitsätzen zu akademischen Vorlesungen
 Paul Natorp Philosophische Propädeutik (Allgemeine Einleitung in die Philosophie und Anfangsgründe der Logik, Ethik und Psychologie) in Leitsätzen zu akademischen Vorlesungen C e l t i s V e r l a g Bibliografische
Paul Natorp Philosophische Propädeutik (Allgemeine Einleitung in die Philosophie und Anfangsgründe der Logik, Ethik und Psychologie) in Leitsätzen zu akademischen Vorlesungen C e l t i s V e r l a g Bibliografische
Frage 1. Klausuraufgaben Grundvorlesung Testat vom , Seite 1 Musterlösung. Bitte eintragen: Matrikelnummer: 0815 Name: Musterstudi.
 Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Musterlösung Matrikelnummer: 0815 Name: Musterstudi Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage
Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Musterlösung Matrikelnummer: 0815 Name: Musterstudi Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage
Folien zur Vorlesung Perspektivität und Objektivität von Prof. Martin Seel. Sitzung vom 1. November 2004
 Folien zur Vorlesung Perspektivität und Objektivität von Prof. Martin Seel Sitzung vom 1. November 2004 1 Kant, Kritik der reinen Vernunft, B 74: Unsre Erkenntnis entspringt aus zwei Grundquellen des Gemüts,
Folien zur Vorlesung Perspektivität und Objektivität von Prof. Martin Seel Sitzung vom 1. November 2004 1 Kant, Kritik der reinen Vernunft, B 74: Unsre Erkenntnis entspringt aus zwei Grundquellen des Gemüts,
Chemie Tutorien zur Vorbereitung auf das Vorphysikum der Zahnmediziner Samstag, Uhr Allgemeine Chemie
 Seite 1 von 6 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie Tutorien zur Vorbereitung auf das Vorphysikum der Zahnmediziner 25.02. 04.03.2017 Samstag, 25.02.17 15.00 17.00 Uhr Allgemeine Chemie Mittwoch,
Seite 1 von 6 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie Tutorien zur Vorbereitung auf das Vorphysikum der Zahnmediziner 25.02. 04.03.2017 Samstag, 25.02.17 15.00 17.00 Uhr Allgemeine Chemie Mittwoch,
Erwartete Kompetenzen. Kompetenzbereich Erkenntnisgewinnung Die Schülerinnen und Schüler E1 E2 E3 E4 E5 E6 E7 E8 E9 E10 E11 E12 E13 E14 E15 E16 E17
 Stoffverteilungsplan Kerncurriculum für die Oberschule in Niedersachsen (Schuljahrgänge 7/8) PRISMA Chemie Niedersachsen Differenzierende Ausgabe Band 7/8 Schule: Klettbuch ISBN 978-3-12-068537-1 Lehrer:
Stoffverteilungsplan Kerncurriculum für die Oberschule in Niedersachsen (Schuljahrgänge 7/8) PRISMA Chemie Niedersachsen Differenzierende Ausgabe Band 7/8 Schule: Klettbuch ISBN 978-3-12-068537-1 Lehrer:
Klausur 1 Basiswissen I. Chemie. Klasse 11c. Erwartungshorizont
 Paula Fürst Schule (Gemeinschaftsschule) Berlin Klausur 1 Basiswissen I Chemie Klasse 11c Erwartungshorizont Vor und Nachname: Zeitvorgabe: 80 min Liebe Schülerin, lieber Schüler, tragen Sie bitte auf
Paula Fürst Schule (Gemeinschaftsschule) Berlin Klausur 1 Basiswissen I Chemie Klasse 11c Erwartungshorizont Vor und Nachname: Zeitvorgabe: 80 min Liebe Schülerin, lieber Schüler, tragen Sie bitte auf
Schriftliche Abschlussprüfung Chemie
 Sächsisches Staatsministerium für Kultus Schuljahr 1999/ Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Sächsisches Staatsministerium für Kultus Schuljahr 1999/ Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Chemie für Biologen, Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema ) iii) Carbonsäure iv) Dicarbonsäure
 Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
VII INHALTSVERZEICHNIS
 VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
Organik KOMPAKT Organik Blatt 1/5
 rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
BEKANNTE SPIELE: . - SO GILT DIE "GRUNDWAHRNEHMUNG" BZW. "DAS GRUNDVERHALTEN" DER
 BEKANNTE SPIELE:. - DIE DARSTELLUNG EINER "NUR FÜR DEN DARSTELLER WAHRNEHMBAREN WIRKLICHKEITSBESCHREIBUNG", - WIRD OFT ALS "SCHAUSPIELEREI" DEFINIERT, - WEIL "DAS BEKANNTE, BESTÄTIGTE VERHALTEN DER PERSON
BEKANNTE SPIELE:. - DIE DARSTELLUNG EINER "NUR FÜR DEN DARSTELLER WAHRNEHMBAREN WIRKLICHKEITSBESCHREIBUNG", - WIRD OFT ALS "SCHAUSPIELEREI" DEFINIERT, - WEIL "DAS BEKANNTE, BESTÄTIGTE VERHALTEN DER PERSON
Operatoren für das Fach Mathematik
 Operatoren für das Fach Mathematik Anforderungsbereich I Angeben, Nennen Sachverhalte, Begriffe, Daten ohne nähere Erläuterungen und Begründungen, ohne Lösungsweg aufzählen Geben Sie die Koordinaten des
Operatoren für das Fach Mathematik Anforderungsbereich I Angeben, Nennen Sachverhalte, Begriffe, Daten ohne nähere Erläuterungen und Begründungen, ohne Lösungsweg aufzählen Geben Sie die Koordinaten des
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 2,
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr., 6.04.11 1. Sie legen 100 ml einer 0, mol/l Natronlauge vor. Als Titrant verwenden Sie eine 0,8 mol/l Salzsäure. Berechnen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr., 6.04.11 1. Sie legen 100 ml einer 0, mol/l Natronlauge vor. Als Titrant verwenden Sie eine 0,8 mol/l Salzsäure. Berechnen
CH-Matura TB 1 STOFFEIGENSCHAFTEN, ATOMBAU THEMENBEREICH 1: Themenbereiche Chemie
 TB 1 THEMENBEREICH 1: STOFFEIGENSCHAFTEN, ATOMBAU Der Kandidat/ die Kandidatin kennt die wichtigsten Stoffeigenschaften und einfache Methoden um diese zu bestimmen. Er/Sie kann den Atombau nach BOHR erklären
TB 1 THEMENBEREICH 1: STOFFEIGENSCHAFTEN, ATOMBAU Der Kandidat/ die Kandidatin kennt die wichtigsten Stoffeigenschaften und einfache Methoden um diese zu bestimmen. Er/Sie kann den Atombau nach BOHR erklären
gleichermaßen gültig wären. Doch dies ist, wie ich zeigen werde, keineswegs der Fall. Es ist eines der Grundübel unserer Zeit, dass ein Großteil der
 gleichermaßen gültig wären. Doch dies ist, wie ich zeigen werde, keineswegs der Fall. Es ist eines der Grundübel unserer Zeit, dass ein Großteil der Menschen entweder nicht willens oder nicht fähig ist,
gleichermaßen gültig wären. Doch dies ist, wie ich zeigen werde, keineswegs der Fall. Es ist eines der Grundübel unserer Zeit, dass ein Großteil der Menschen entweder nicht willens oder nicht fähig ist,
Beispielaufgaben IChO 2. Runde 2019 Säurederivate. H2, Pd/C
 Beispielaufgaben Ih 2. Runde 2019 Säurederivate Beispiel 1 ligocarbonsäuren Gegeben sei folgendes Reaktionsschema: A H2, Pd/ H 2, Lindlar Na/NH 3(l) B D Base E A hat eine molare Masse von 118,09 g mol
Beispielaufgaben Ih 2. Runde 2019 Säurederivate Beispiel 1 ligocarbonsäuren Gegeben sei folgendes Reaktionsschema: A H2, Pd/ H 2, Lindlar Na/NH 3(l) B D Base E A hat eine molare Masse von 118,09 g mol
2. Seinsweise, die in der Angleichung von Ding und Verstand besteht. 3. Unmittelbare Wirkung dieser Angleichung: die Erkenntnis.
 THOMAS VON AQUIN - De veritate (Quaestio I) - Zusammenfassung Erster Artikel: Was ist Wahrheit?! Ziel ist die Erschließung des Wortes Wahrheit und der mit diesem Begriff verwandten Wörter.! 1. Grundlage
THOMAS VON AQUIN - De veritate (Quaestio I) - Zusammenfassung Erster Artikel: Was ist Wahrheit?! Ziel ist die Erschließung des Wortes Wahrheit und der mit diesem Begriff verwandten Wörter.! 1. Grundlage
Induktion im Lexikon: logische Herleitung allgemeiner Regeln von Einzelfällen zu allgemeinen Gesetzen aufsteigen
 Eine Induktionslogik gibt es nicht. Induktion im Lexikon: logische Herleitung allgemeiner Regeln von Einzelfällen zu allgemeinen Gesetzen aufsteigen Popper zitiert Einstein: Zu diesen Gesetzen führt kein
Eine Induktionslogik gibt es nicht. Induktion im Lexikon: logische Herleitung allgemeiner Regeln von Einzelfällen zu allgemeinen Gesetzen aufsteigen Popper zitiert Einstein: Zu diesen Gesetzen führt kein
CH-Matura TB 1 STOFFEIGENSCHAFTEN, ATOMBAU THEMENBEREICH 1: Themenbereiche Chemie
 TB 1 THEMENBEREICH 1: STOFFEIGENSCHAFTEN, ATOMBAU Der Kandidat/ die Kandidatin kennt die wichtigsten Stoffeigenschaften und einfache Methoden um diese zu bestimmen. Er/Sie kann den Atombau nach BOHR erklären
TB 1 THEMENBEREICH 1: STOFFEIGENSCHAFTEN, ATOMBAU Der Kandidat/ die Kandidatin kennt die wichtigsten Stoffeigenschaften und einfache Methoden um diese zu bestimmen. Er/Sie kann den Atombau nach BOHR erklären
Schriftliche Abschlussprüfung Chemie
 Sächsisches Staatsministerium für Kultus Schuljahr 2000/2001 Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Sächsisches Staatsministerium für Kultus Schuljahr 2000/2001 Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Statut der IVSS Sektion für Prävention in der chemischen Industrie (IVSS Sektion Chemie)
 Statut der IVSS Sektion für Prävention in der chemischen Industrie (IVSS Sektion Chemie) Kapitel 1: Name, Ziele und Aktionsmittel Artikel 1 Name Die Internationale Sektion führt den Namen "IVSS Sektion
Statut der IVSS Sektion für Prävention in der chemischen Industrie (IVSS Sektion Chemie) Kapitel 1: Name, Ziele und Aktionsmittel Artikel 1 Name Die Internationale Sektion führt den Namen "IVSS Sektion
Chemie Chemie - Klasse 9 - Version 1 (Juli 2004)
 Fehler! Kein Text mit angegebener Formatvorlage im Dokument. - Chemie Chemie Chemie - Klasse 9 - Version 1 (Juli 2004) Themenfeld Kerncurriculum
Fehler! Kein Text mit angegebener Formatvorlage im Dokument. - Chemie Chemie Chemie - Klasse 9 - Version 1 (Juli 2004) Themenfeld Kerncurriculum
Grundkurs Optische Aktivität 1983/I/1 1992/I/1 1994/III/3 1998/I/1
 Grundkurs Optische Aktivität 1983/I/1 1.1 Definieren Sie den Begriff "optische Aktivität"! 2BE 1.2 Erläutern Sie am Beispiel des Bromchloriodmethans, welche Form von Isomerie bei dieser Verbindung auftritt
Grundkurs Optische Aktivität 1983/I/1 1.1 Definieren Sie den Begriff "optische Aktivität"! 2BE 1.2 Erläutern Sie am Beispiel des Bromchloriodmethans, welche Form von Isomerie bei dieser Verbindung auftritt
Schriftliche Prüfung BSc Herbst 2007
 Prüfungen Analytische Chemie Montag, 3. September 2007 Schriftliche Prüfung BSc Herbst 2007 D CHAB/BIOL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Montag, 3. September 2007 Schriftliche Prüfung BSc Herbst 2007 D CHAB/BIOL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Übersicht über wichtige und häufig benötigte mathematische Operationen
 Bruchrechnung Übersicht über wichtige und häufig benötigte mathematische Operationen Addition/Subtraktion von (ungleichnamigen) Brüchen: Brüche erweitern, sodass die Nenner gleichnamig sind, indem Zähler
Bruchrechnung Übersicht über wichtige und häufig benötigte mathematische Operationen Addition/Subtraktion von (ungleichnamigen) Brüchen: Brüche erweitern, sodass die Nenner gleichnamig sind, indem Zähler
Eulersche Zahl und Exponentialfunktion
 Eulersche Zahl und Exponentialfunktion Raphael Dumhart 5. Juni 20 Inhaltsverzeichnis Vorwort 2 2 Die Eulersche Zahl 2 2. Einige Eigenschaften......................... 2 2.2 Die Entdeckung von e........................
Eulersche Zahl und Exponentialfunktion Raphael Dumhart 5. Juni 20 Inhaltsverzeichnis Vorwort 2 2 Die Eulersche Zahl 2 2. Einige Eigenschaften......................... 2 2.2 Die Entdeckung von e........................
Von der Besinnung und dem Verstand
 Das elfte Buch Hermetis Trismegisti Rede an Asclepium Von der Besinnung und dem Verstand estern, lieber Asclepi! habe ich eine vollkommene Rede geführt, jetzt halte ich nötig, solches zu verfolgen und
Das elfte Buch Hermetis Trismegisti Rede an Asclepium Von der Besinnung und dem Verstand estern, lieber Asclepi! habe ich eine vollkommene Rede geführt, jetzt halte ich nötig, solches zu verfolgen und
DIALOGE ÜBER NATÜRLICHE RELIGION
 DAVID HUME DIALOGE ÜBER NATÜRLICHE RELIGION NEUNTER TEIL, SEITEN 73-78 DER A PRIORI BEWEIS DER EXISTENZ GOTTES UND SEINER UNENDLICHEN ATTRIBUTE S. 73-74 Demea : Die Schwächen des a posteriori Beweises
DAVID HUME DIALOGE ÜBER NATÜRLICHE RELIGION NEUNTER TEIL, SEITEN 73-78 DER A PRIORI BEWEIS DER EXISTENZ GOTTES UND SEINER UNENDLICHEN ATTRIBUTE S. 73-74 Demea : Die Schwächen des a posteriori Beweises
Zugrunde gelegt wird ein Chemie-Unterricht mit zwei Wochenstunden. September. Oktober
 Vorschlag für einen Jahresplan Chemie-Unterricht im fünften Jahr mit dem Unterrichtswerk PRISMA Zugrunde gelegt wird ein Chemie-Unterricht mit zwei Wochenstunden Monat September Oktober Chemische Bindungen
Vorschlag für einen Jahresplan Chemie-Unterricht im fünften Jahr mit dem Unterrichtswerk PRISMA Zugrunde gelegt wird ein Chemie-Unterricht mit zwei Wochenstunden Monat September Oktober Chemische Bindungen
Blatt 10 Lösungshinweise
 Lineare Algebra und Geometrie I SS 05 Akad. Rätin Dr. Cynthia Hog-Angeloni Dr. Anton Malevich Blatt 0 Lösungshinweise 0 0 Aufgabe 0. Es seien die Vektoren u =, v = und w = in R gegeben. a # Finden Sie
Lineare Algebra und Geometrie I SS 05 Akad. Rätin Dr. Cynthia Hog-Angeloni Dr. Anton Malevich Blatt 0 Lösungshinweise 0 0 Aufgabe 0. Es seien die Vektoren u =, v = und w = in R gegeben. a # Finden Sie
Walter Orlov. Goldener Schnitt und Euleresche Zahl
 Walter Orlov Goldener Schnitt und Euleresche Zahl August 2004 Euklid (325-270 vor Christus) wird die Entdeckung des Streckenverhältnis Goldenen Schnittes zugeschrieben. Unter Goldenem Schnitt versteht
Walter Orlov Goldener Schnitt und Euleresche Zahl August 2004 Euklid (325-270 vor Christus) wird die Entdeckung des Streckenverhältnis Goldenen Schnittes zugeschrieben. Unter Goldenem Schnitt versteht
Aktuelle Beispiele aus der Forschung
 Vorlesung: Allgemeine Chemie Organische Chemie 05.12.; 08.12.; Prof. Dr. C. Meier Eine Einführung in die Organische Chemie Themen: Elektronenstruktur, kovalente Bindung, Säure-Basen-Eigenschaften in Abhängigkeit
Vorlesung: Allgemeine Chemie Organische Chemie 05.12.; 08.12.; Prof. Dr. C. Meier Eine Einführung in die Organische Chemie Themen: Elektronenstruktur, kovalente Bindung, Säure-Basen-Eigenschaften in Abhängigkeit
CH-Matura TB 1 THEMENBEREICH 1: Themenbereiche Chemie. AGMueller2014V3
 TB 1 THEMENBEREICH 1: STOFFEIGENSCHAFTEN, ATOMBAU Der Kandidat/ die Kandidatin kennt die wichtigsten Stoffeigenschaften und einfache Methoden um diese zu bestimmen. Er/Sie kann den Atombau nach BOHR erklären
TB 1 THEMENBEREICH 1: STOFFEIGENSCHAFTEN, ATOMBAU Der Kandidat/ die Kandidatin kennt die wichtigsten Stoffeigenschaften und einfache Methoden um diese zu bestimmen. Er/Sie kann den Atombau nach BOHR erklären
Boolesche Operationen und lokale Manipulationen
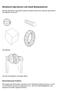 1 Boolesche Operationen und lokale Manipulationen Mit Hilfe Boolescher Operatoren werden komplexe Körper aus Instanzen generischer Grundkörper konstruiert.. Grundkörper Aus den Grundkörpern erzeugter Körper
1 Boolesche Operationen und lokale Manipulationen Mit Hilfe Boolescher Operatoren werden komplexe Körper aus Instanzen generischer Grundkörper konstruiert.. Grundkörper Aus den Grundkörpern erzeugter Körper
Organische Chemie I/II. Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter!
 Organische Chemie I/II Name: Fachprüfung Vorname: 5. Februar 2003, 15 30-18 30 h Matr.-Nr.: Raum 250 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10
Organische Chemie I/II Name: Fachprüfung Vorname: 5. Februar 2003, 15 30-18 30 h Matr.-Nr.: Raum 250 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen
 ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
Inhalt. Stoffe lassen sich ordnen - Elementfamilien. Der Bau der Atome. Kopiervorlagen. Kopiervorlagen. 0 Materialien zur Sprachbildung. aufgeführt.
 Inhalt 0 Materialien zur Sprachbildung Sofern sich die in eine besondere Rubrik einordnen lassen, ist dies jeweils aufgeführt. Stoffe lassen sich ordnen - Elementfamilien Diagnosebogen I - Selbsteinschätzung
Inhalt 0 Materialien zur Sprachbildung Sofern sich die in eine besondere Rubrik einordnen lassen, ist dies jeweils aufgeführt. Stoffe lassen sich ordnen - Elementfamilien Diagnosebogen I - Selbsteinschätzung
Die wichtigsten Tipps für eine effektive Suche in beck-online
 Dr. Rainer Dechsling und Dipl.-Kffr. Andrea Kepreda Die wichtigsten Tipps für eine effektive Suche in beck-online Ob in Studium oder Praxis: Trotz raumhoher Regale voll von Kommentaren, Gesetzen und Zeitschriften
Dr. Rainer Dechsling und Dipl.-Kffr. Andrea Kepreda Die wichtigsten Tipps für eine effektive Suche in beck-online Ob in Studium oder Praxis: Trotz raumhoher Regale voll von Kommentaren, Gesetzen und Zeitschriften
Vorlesung Chemie für Biologen: Klausur 1 WS Sa
 1 Vorlesung Chemie für Biologen: Klausur 1 WS 02-03 Sa 07.12.02 Name:... Ihre Unterschrift:... Vorname:... Matrikel-Nr.:... Studienbeginn: SS: WS:...... Tutor der Übungen: (Dort Klausureinsicht.) Punkteschlüssel
1 Vorlesung Chemie für Biologen: Klausur 1 WS 02-03 Sa 07.12.02 Name:... Ihre Unterschrift:... Vorname:... Matrikel-Nr.:... Studienbeginn: SS: WS:...... Tutor der Übungen: (Dort Klausureinsicht.) Punkteschlüssel
I. Chemische Bindung und Zwischenmolekulare Kräfte
 I. Chemische Bindung und Zwischenmolekulare Kräfte MINT-UNTERRICHTSEINHEIT A. Ausgangslage Die klare Unterscheidung der chemischen Bindung- und der Zwischenmolekularen Kräfte und die korrekte Zuordnung
I. Chemische Bindung und Zwischenmolekulare Kräfte MINT-UNTERRICHTSEINHEIT A. Ausgangslage Die klare Unterscheidung der chemischen Bindung- und der Zwischenmolekularen Kräfte und die korrekte Zuordnung

