Serazym Verotoxin 1+2
|
|
|
- Benjamin Waldfogel
- vor 7 Jahren
- Abrufe
Transkript
1 Serazym Verotoxin 1+2 Enzymimmunoassay zum Nachweis von Verotoxin 1 und 2 (Shiga Toxin 1 und 2) in Stuhlproben r E-030 n96 r E-030-A2 n2x 96 v In-vitro- Diagnostikum c Einführung Invasive und toxinbildende Escherichia coli- Stämme führen zu Durchfallerkrankungen bei Säuglingen und Erwachsenen. Unter den pathogenen E. coli Stämmen kommt der Gruppe der enterohämorrhagischen E. coli (EHEC) als Verursacher lebensbedrohender hämorrhagischer Kolitiden und des hämolytisch- urämischen Syndroms (HUS) mit Nierenversagen und hämolytischer Anämie mit Thrombozytopenie besondere Bedeutung zu (1, 2, 3). Diese Stämme wie E. coli O:157; O:26; O:111 und andere Serovare bilden Zytotoxine (Shiga Toxin 1 und 2, Shiga Toxin Varianten), die einen zytopathischen Effekt auf Verozellen haben, was zur Namensgebung als Verotoxin 1 und 2 führte. Methoden zum Nachweis der Enterotoxinbildung sind wie der Zytotoxizitätstest auf Verozellen und anschließendem Neutralisationstest sehr zeitaufwendig oder wie die Diagnostik mit Gensonden und Genamplifikation durch Polymerase Kettenreaktion (PCR) spezialisierten Laboratorien vorbehalten. Enzymimmunologische Methoden ermöglichen einen schnellen und spezifischen Verotoxin 1- und Verotoxin 2-Nachweis in Stuhlproben, wobei dem Verotoxin-Nachweis eine Anreicherungskultur vorausgehen sollte (4, 5, 6). GAL_E-030_ _DE Seite 1 von 16
2 Literatur: 1. Beutin, L.: Infektionen mit enterohämorrhagischen Escherichia coli (EHEC). Bundesgesundheitsbl. 39, 11 (1996): Bockemühl, J., Karch, H. und Tschäpe, H.: Infektionen des Menschen durch enterohämorrhagische Escherichia coli (EHEC) in Deutschland, Bundesgesundheitsbl. 6 (1997): Stock, I. und Wiedemann, B.: Infektionen durch enterohämorrhagische Escherichia coli-(ehec-) Stämme. MMP, 20. Jahrgang, Heft 3 (1997): Gerritzen, A.: Vergleichender Verotoxin-Nachweis im Stuhl mit zwei Enzymimmunoassays und dem Zytotoxizitätstest auf Verozellen. Lab. Med. 1998; 22 (12): Reissbrodt, R.: Enterohämorrhagic Escherichia coli: isolation and identification. Biotest Bulletin 6: (1998) 6. Fruth, A. et al.: Zur Verbesserung der gegenwärtigen bakteriologischen Diagnostik von enterohämorrhagischen Escherichia coli (EHEC). Bundesgesundheitsbl.-Gesundheitsforsch.- Gesundheitsschutz 4, (2000) Anwendungsbereich Der Serazym Verotoxin 1+2 ist ein in-vitro vitro-diagnostikum zum direkten Nachweis von Verotoxin 1 und 2 (Shiga Toxin 1 und 2) in Stuhlproben bzw. Stuhlkulturüberständen. Testprinzip Der Serazym Verotoxin 1+2 ist ein indirekter Zwei-Seiten-Assay auf der Basis polyklonaler und monoklonaler Antikörper gegen Verotoxin 1 (VT1) und 2 (VT2). Verdünnte unbehandelte Stuhlproben bzw. Kulturüberstände von Stuhlproben sowie negative und positive Kontrollproben werden in die mit polyklonalen anti-vt1- und anti-vt2-antikörpern beschichteten Vertiefungen der Mikrotitrationsstreifen dosiert. Nach 60 min Inkubation bei Raumtemperatur (RT) werden die ungebundenen Komponenten durch einen Waschschritt entfernt und biotinylierte, monoklonale anti-vt1- und anti- VT2-Antikörper in die Kavitäten dispensiert. Nach erneuter Inkubation für 30 min bei RT werden die ungebundenen biotinylierten Antikörper in einem Waschschritt entfernt. Die gebundenen biotinylierten Antikörper reagieren in einem weiteren Inkubationsschritt (30 min, RT) mit Streptavidin-poly- Peroxidase (POD)-Konjugat. Nach erneutem Waschen setzt die POD im folgenden enzymatischen Reaktionsschritt die farblose Substratlösung in ein blaues Endprodukt um. Diese Reaktion wird nach 15 min Inkubation durch Zugabe der Stopplösung abgebrochen, wodurch ein Farbumschlag der blauen Lösung zu gelb auftritt. Die bei 450 / 620 nm gemessene optische Dichte (OD) des Endprodukts ist zur Konzentration der spezifisch gebundenen Toxin-Antigene direkt proportional. GAL_E-030_ _DE Seite 2 von 16
3 Testkomponenten Für 96 Kavitäten Für 2x 96 Kavitäten 1 WELLS Mikrotiterplatte beschichtet mit polyklonalen anti- VT1 und anti-vt2- Antikörpern (Schaf) 12 teilbare Streifen zu je 8 Kavitäten Farbmarkierung orange vakuumversiegelt mit Trockenbeutel 2x 12 teilbare Streifen zu je 8 Kavitäten Farbmarkierung orange vakuumversiegelt mit Trockenbeutel 2 WASHBUF CONC 10x Waschpuffer 10-fach 100 ml Konzentrat für 1000 ml Lösung weiße Kappe 2x 100 ml Konzentrat für 2x 1000 ml Lösung weiße Kappe 3 DIL Verdünnungsmedium für Serazym Verotoxin ml gebrauchsfertig orange gefärbt schwarze Kappe 2x 100 ml gebrauchsfertig orange gefärbt schwarze Kappe 4 CONTROL + Positive Kontrolle inaktivierter, Verotoxin positiver E. coli Kulturüberstand 2,0 ml gebrauchsfertig blau gefärbt rote Kappe 4,0 ml gebrauchsfertig blau gefärbt rote Kappe 5 CONTROL Negative Kontrolle Verotoxin 1 und 2 negative Probe 2,0 ml gebrauchsfertig blau gefärbt grüne Kappe 4,0 ml gebrauchsfertig blau gefärbt grüne Kappe 6/1 CONJ BIOTIN Biotin-Konjugat Biotinylierte, monoklonale anti-vt1 und anti-vt2-antikörper (Maus) 15 ml gebrauchsfertig grün gefärbt weiße Kappe 30 ml gebrauchsfertig grün gefärbt weiße Kappe 6/2 CONJ STREPT Streptavidin-poly poly-pod POD-Konjugat 15 ml gebrauchsfertig rot gefärbt braune Kappe 30 ml gebrauchsfertig rot gefärbt braune Kappe 7 SUBSTR TMB Substrat 3,3,5,5 -Tetramethylbenzidin und Wasserstoffperoxid 15 ml gebrauchsfertig blaue Kappe 30 ml gebrauchsfertig blaue Kappe 8 STOP Stopplösung 0,25 M Schwefelsäure 15 ml gebrauchsfertig gelbe Kappe 30 ml gebrauchsfertig gelbe Kappe Vorbereitung und Lagerung der Proben Gewinnung und Lagerung Stuhlproben sollten sofort nach der Entnahme bei C gelagert und innerhalb von 72 h untersucht oder bei -20 C eingefroren werden. Beim direkten Nachweis von Verotoxin aus dem Stuhl ist die sofortige Untersuchung nach Ankunft im Labor zu bevorzugen. Stuhlproben für die Kultur innerhalb von ein bis zwei Stunden nach Ankunft im Labor in Kulturmedium überführen oder für einen späteren Ansatz sofort bei -20 C aufbewahren. Wiederholtes Einfrieren und Auftauen der Proben ist zu vermeiden. Vorbereitung und Verwendung Probenansatz bei direktem Einsatz der Stuhlproben. Eingefrorene Stuhlproben zügig auftauen und gut durchmischen. In ein Reaktionsgefäß 0,5 ml Verdünnungsmedium für Serazym Verotoxin 1+2 pipettieren. Bei festen Stuhlproben 200 mg (Durchmesser etwa 4 6 mm) mit einem Einmalstäbchen, bei flüssigen Stuhlproben 200 µl in das Probenverdünnungsmedium überführen und sorgfältig suspendieren. Wegen möglicher inhomogener Verotoxin Antigen- Verteilung wird die Probennahme von zwei differenten Stellen eines Stuhlganges empfohlen. GAL_E-030_ _DE Seite 3 von 16
4 Achtung: der direkte Einsatz von Stuhlproben im ELISA ohne vorherige Anreicherung kann nur als Vorscreening zum Erhalt eines schnellen ersten Ergebnisses gelten. Eine anschließende Untersuchung der entsprechenden Probe nach Voranreicherung sollte dann in jedem Fall zusätzlich erfolgen, um eine ausreichend hohe Sensitivität zu erhalten. Ein negatives ELISA Ergebnis bei Einsatz einer nicht vorangereicherten Stuhlprobe schließt aufgrund der geringeren Sensitivität eine EHEC-Infektion nicht aus! Probenansatz nach Anreicherung in einem Kulturmedium. Etwa 200 mg oder 200 µl der zu untersuchenden Stuhlprobe in 4 ml Anreicherungsbouillon, wie z. B. EHEC-Direktmedium (Haipha) oder mtsb (Mast) mit 50 ng/ml Mitomycin C überführen und möglichst unter Schütteln h bei 37 C inkubieren. Anschließend die festen Bestandteile sedimentieren lassen oder gegebenenfalls in einer Mikrozentrifuge eine Minute bei maximaler Drehzahl zentrifugieren. Der Kulturüberstand wird 1 : 2 verdünnt im ELISA getestet (100 µl / Vertiefung). Für die Testdurchführung zusätzlich benötigte Materialien und Hilfsmittel - Verstellbare Einkanal-Mikropipette 8-Kanalpipette bzw. Multipipetten mit Pipettenspitzen 8-Kanal- Handwaschkamm mit Vakuumpumpe und Abfallbehältern oder Mikrotiterplatten-Waschgerät Mikrotiterplatten-Photometer mit 450 nm Mess- und 620 nm Referenzfilter destilliertes oder deionisiertes Wasser Messzylinder Teströhrchen (2 ml) für die Probenverdünnung Anreicherungsmedium z.b. EHEC-Direktmedium (Haipha) oder m-tsb (Mast) mit 50 ng / ml Mitomycin C Vorbereitung und Lagerung der Reagenzien Testbesteckformat und Haltbarkeit Ein Testbesteck enthält Reagenzien für 1x 96 oder 2x 96 Bestimmungen. Das komplette Testbesteck mit verschlossenen Reagenzflaschen und Mikrotitrationsstreifen ist bei Lagerung bei 2 8 C bis zum aufgedruckten Verfallsdatum stabil. Alle geöffneten Testbesteckbestandteile sind bei ordnungsgemäßer Lagerung bei 2 8 C mindestens 2 Monate haltbar. Die gebrauchsfertig verdünnte Waschlösung ist bei Lagerung bei 2 8 C mindestens 1 Monat verwendbar. Vorbereitung und Verwendung Die Mikrotiterplatte mit teilbaren Streifen ist in einem aluminium-beschichteten Beutel zusammen mit Trockenmittel vakuumversiegelt. Öffnen der Verpackung erst nach Erreichen der Raumtemperatur. Nicht gebrauchte Kavitäten vor Feuchtigkeit schützen und zusammen mit dem Trockenmittel in den Beutel zurücklegen und verschließen. Waschpufferkonzentrat (10-fach) mit destilliertem oder deionisiertem Wasser verdünnen. Beispiel: 10 ml Waschpufferkonzentrat (2) + 90 ml destilliertes oder deionisiertes Wasser. Testdurchführung Stuhlproben mit Verdünnungsmedium für Serazym Verotoxin 1+2 (3) 1 + 2,5 verdünnen, z.b. 200 mg oder 200 µl Stuhlprobe + 0,5 ml Verdünnungsmedium (3) bzw. 200 mg Stuhlprobe in 4 ml Anreicherungsbouillon (z.b. EHEC-Direktmedium, oder mtsb mit 50 ng / ml Mitomycin C) für Stunden bei 37 C möglichst unter Schütteln bebrüten, Überstand (gegebenenfalls nach Zentrifugation) 1 : 2 in Verdünnungsmedium verdünnen und 100 µl pro Vertiefung im ELISA einsetzen. Die Reihenfolge der Pipettierschritte und deren Durchführung im Zeittakt sind einzuhalten! Beim Waschvorgang dispensierte Waschlösung mindestens 5 Sekunden einwirken lassen und Waschlösungsreste durch gründliches Absaugen oder Ausschlagen der Kavitäten entfernen! Substrat vor Licht geschützt aufbewahren! GAL_E-030_ _DE Seite 4 von 16
5 Arbeitsschritte 1. Die Testreagenzien und die benötigte Anzahl an Kavitäten auf Raumtemperatur (RT) erwärmen und alle Reagenzien vor Gebrauch leicht schütteln, Schaumbildung vermeiden. 2. Je 120 µl CONTROL + Positive Kontrolle (4) 120 µl CONTROL Negative Kontrolle (5) 100 µl verdünnte Probe bzw. verdünnten Kulturüberstand pipettieren. 3. Platte abkleben und 60 min bei RT inkubieren. 4. Dekantieren und 5 mal mit 300 µl Waschlösung (verdünnt aus (2 ) waschen. Restflüssigkeit durch Ausschlagen auf Zellstoff entfernen Tropfen (oder 120 µl) CONJ BIOTIN Biotin-Konjugat (6/1) pro Kavität. 6. Platte abkleben und 30 min bei RT inkubieren. 7. Dekantieren und 5 mal mit 300 µl Waschlösung (verdünnt aus (2 ) waschen. Restflüssigkeit durch Ausschlagen auf Zellstoff entfernen Tropfen (oder 120 µl) CONJ STREPT Streptavidin-poly-POD-Konjugat (6/2) pro Kavität. 9. Platte abkleben und 30 min bei RT inkubieren. 10. Dekantieren und 5 mal mit 300 µl Waschlösung (verdünnt aus (2 ) waschen. Restflüssigkeit durch Ausschlagen auf Zellstoff entfernen Tropfen (oder 120 µl) SUBSTR TMB Substrat (7) pro Kavität min lichtgeschützt bei RT inkubieren Tropfen (oder 120 µl) STOP Stopplösung (8) pro Kavität, kurz schütteln. 14. Messen der OD bei 450 nm / 620 nm mit einem Mikrotiterplatten-Photometer innerhalb von 30 Minuten. Berechnung der Ergebnisse Qualitative Evaluierung Cut-off Bestimmung: OD Negative Kontrolle + 0,20 Proben mit OD-Werten gleich oder höher als die des errechneten Grenzwertes sind als positiv, Proben mit OD-Werten unterhalb des errechneten Grenzwertes sind als negativ im Serazym Verotoxin 1+2 zu bewerten. Referenzwert Serazym Verotoxin 1+2 Positiv Cut-off Negativ < Cut-off Aufgrund von Unterschieden im Einsender-Klientel wird empfohlen, dass jedes Labor seine eigenen Referenzbereiche bestimmen sollte. Die genannten Werte sind deshalb nur als Empfehlung zu werten. Testvalidierung Der Test kann ausgewertet werden, wenn: OD-Mittelwert der negativen Kontrolle 0,20 (manuelle Abarbeitung) 0,30 (automatische Abarbeitung) OD-Mittelwert der positiven Kontrolle 1,00 Sind die o. g. Gültigkeitskriterien nicht erfüllt, muss der Testansatz wiederholt werden. Stellen Sie sicher, dass die Abarbeitung strikt gemäß Testanleitung erfolgt (korrekte Reagenzienvorbereitung, korrekte Inkubationszeiten und -temperaturen, sorgfältiges Waschen). Sollten die Gültigkeitskriterien auch nach wiederholtem Testansatz nicht erfüllt sein, kontaktieren Sie bitte den Hersteller. GAL_E-030_ _DE Seite 5 von 16
6 Grenzen der Methode Der Nachweis von VT 1 und VT 2 in Stuhlproben lässt keine Korrelation zwischen gemessener OD und Schweregrad der Infektion zu. Die OD der Proben darf auch nicht mit der OD der positiven Kontrolle in Korrelation gesetzt werden. Kreuzkontaminationen der Testbesteckreagenzien und Proben können zu falschen Ergebnissen führen. Unkorrekte Verdünnung, ungenügende Homogenisierung der Proben sowie nicht sedimentierte Festbestandteile in zentrifugierten Proben können sowohl zu falsch positiven als auch zu falsch negativen Ergebnissen führen. Ein negatives Ergebnis im Verotoxin 1+2 ELISA schließt eine Infektion nicht aus: Da der Toxingehalt der zu untersuchenden Stuhlproben häufig sehr niedrig ist, hat die selektive Anreicherung der VT produzierenden Erreger in einem dafür geeigneten Medium entscheidenden Einfluss auf die Sensitivität des Nachweises im ELISA. Die Gesamtinterpretation des ELISA-Testergebnisses sollte im Zusammenhang mit dem Erregernachweis und der Klinik erfolgen. Automatische Abarbeitung Bei Abarbeitung des Serazym Verotoxin 1+2 auf einem Mikrotitrationsplatten-Vollautomaten (wie z.b. DS2, DSX) können in Abhängigkeit vom verwendeten Gerät und von den individuellen Geräteeinstellungen im Vergleich zur manuellen Bearbeitung höhere OD-Werte gemessen werden. In diesen Fällen ist die Erhöhung des max. zulässigen Grenzwertes für die OD der Negativ-Kontrolle auf 0,3 zulässig. Für den Waschprozess ist die Einprogrammierung von Waschpuffer-Einwirkzeiten (mind. 10 sec pro Streifen und Waschschritt) gefolgt von einem Waschschritt mit destilliertem oder demineralisiertem Wasser und 10 sec Einwirkzeit zu empfehlen.gegebenenfalls kann die Anzahl der Waschschritte von 5x auf 7x bis 8x erhöht werden. Korrelation: manuelle automatische Abarbeitung Bei der parallelen Untersuchung von 188 Proben in manueller und automatischer Abarbeitung (DS2, Dynex Technologies) konnte ein Korrelationskoeffizient von 0,98 ermittelt werden. 4,0 Serazym Verotoxin 1+2 automatische Abarbeitung (DS2) 3,5 3,0 2,5 2,0 1,5 1,0 0,5 0,0 0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5 4,0 manuelle Abarbeitung Leistungsmerkmale Präzision Intra-Assay Variationskoeffizienten (VK) im Serazym Verotoxin 1+2 aus 12-fach Bestimmungen von Proben: VT 2 OD-Mittelwert Standard- VK (%) (pg/ml) abweichung ,268 0,051 2, ,799 0,037 4, ,262 0,013 5,1 0 0,056 0,006 11,3 Inter-Assay Variationskoeffizienten (VK) im Serazym Verotoxin 1+2 in 11 unterschiedlichen Testläufen aus 3-fach Bestimmungen von Proben: VT 2 OD-Mittelwert Standard- VK (%) (pg/ml) abweichung ,026 0,057 2, ,752 0,055 7, ,241 0,022 9,3 0 0,048 0,007 15,1 GAL_E-030_ _DE Seite 6 von 16
7 Untere Nachweisgrenze Die untere Nachweisgrenze wurde für VT 1 und VT 2 durch getrennte Titration der gereinigten Toxine im ELISA mit < 100 pg/ml bestimmt. Klinische Erprobung Im Rahmen einer Studie wurden insgesamt 825 Stuhlproben parallel im Serazym Verotoxin 1+2 sowie im Verozellzytotoxizitätstest untersucht. Dabei handelte es sich um 795 auf pathogene Darmerreger zu untersuchende Stuhlproben und 30 durch Shiga-Toxin-Gen-PCR und Kultur vorcharakterisierte und bis zur Testung bei -20 C gelagerte Stuhlproben. Die Testung im ELISA erfolgte nach Voranreicherung der Proben (mtsb; Stunden bei 37 C). Zytotoxizitätstest positiv negativ Serazym positiv 0 2 ELISA negativ Spezifität: 98,8% Zytotoxizitätstest positiv negativ Serazym positiv 11 0 ELISA negativ 2 17 Sensitivität: 84,6% Kreuzreaktivität Die mikrobiologische Routinediagnostik der im Rahmen der klinischen Studie untersuchten Stuhlproben ergab bei 141 Proben einen positiven Erregernachweis. Diese Erreger konnten insgesamt 12 verschiedenen Bakterien-Spezies zugeordnet werden (Staphylococcus aureus, Enterotoxin positive und negative Stämme; Clostridium difficile, Toxin positive Stämme; Pseudomonas aeruginosa; Salmonella typhimurium; Salmonella enteritidis; Salmonella spec.; Aeromonas hydrophila; Aeromonas caviae; Campylobacter spec.; Hafnia alvei; Yersinia enterocolitica O:3). Keiner dieser Erreger verursachte falsch positive Ergebnisse im Serazym Verotoxin 1+2. Allgemeine Hinweise und Vorsichtsmaßnahmen Dieses Testbesteck ist nur zum in-vitro Gebrauch bestimmt und darf nur von geschultem Laborfachpersonal durchgeführt werden. Die Arbeitsanleitung ist strikt einzuhalten. Das Testbesteck oder seine geöffneten Reagenzien sind nur innerhalb der angegebenen Haltbarkeitsfristen zu verwenden. Das Mischen von Testbesteckkomponenten verschiedener Chargen ist nicht erlaubt e mit Ausnahme von Verdünnungsmedium, Waschpuffer, TMB/Substratlösung und Stopplösung. Die Komplettierung eines geöffneten Testbestecks mit Reagenzien anderer Hersteller ist nicht erlaubt. Einige Reagenzien (2, 3, 4, 5, 6, 7) enthalten geringe Mengen Kathon (1,0% v/v) und Thimerosal (0,01% w/v) als Konservierungsmittel. Reagenzien nicht verschlucken und Kontakt mit Schleimhäuten vermeiden. Die Lagertemperatur der Reagenzien bis zur Wiederverwendung beträgt 2 8 C. Beim Umgang mit den Komponenten des Testbestecks sowie mit den Patientenproben und Kontrollen sind die Vorschriften zur Unfallverhütung beim Umgang mit potentiell infektiösem Material und gefährlichen Chemikalien zu beachten. Insbesondere sind folgende Regeln einzuhalten: Nicht essen, trinken oder rauchen! Nie mit dem Mund pipettieren! Handschuhe zur Vermeidung von Kontakt mit den Reagenzien und Proben tragen! Sicherheitshinweise zu den einzelnen Testkomponenten beachten! GAL_E-030_ _DE Seite 7 von 16
8 Inkubationsschema Serazym Verotoxin 1+2 (E-030) µl CONTROL + (4) 120 µl CONTROL (5) 100 µl verdünnte Stuhlkultur kulturprobe pipettieren 60 min Inkubation (Raumtemperatur) 5 x Waschen mit Waschlösung 2. 3 Tropfen (oder 120 µl) CONJ BIOTIN (6/1) 30 min Inkubation (Raumtemperatur) 5 x Waschen mit Waschlösung 3. 3 Tropfen (oder 120 µl) CONJ STREPT (6/2) 30 min Inkubation (Raumtemperatur) 5 x Waschen mit Waschlösung 4. 3 Tropfen (oder 120 µl) SUBSTR TMB (7) 15 min Inkubation (lichtgeschützt bei Raumtemperatur) 5. 3 Tropfen (oder 120 µl) STOP (8) Messung der OD bei 450 / 620 nm GAL_E-030_ _DE Seite 8 von 16
9 Serazym Verotoxin 1+2 Enzyme immunoassay for detection of Verotoxin 1+2 (Shiga-Toxin 1+2) in stool specimens r E-030 n96 r E-030-A2 n2x 96 v In-vitro- diagnostic device c Introduction Invasive and toxigenic Escherichia coli strains cause diarrhoea in infants and adults. Among pathogenic E. coli strains the group of enterohaemorrhagic E. coli (EHEC) can cause lifethreatening haemorrhagic colitis and haemolytic uraemic syndrome (HUS) leading to acute renal failure and haemolytic anaemia with thrombocytopenia (1, 2, 3). Strains like E. coli O:157; O:26; O:111 and other serovars are characterized by the production of cytotoxins (verotoxin 1 and 2 or shiga-toxin 1 and 2, shiga-toxin variants). The diagnosis of an EHEC infection is initially done by detection of the shigatoxins. Diagnostic methods can be direct toxin detection by cytotoxicity test on vero-cells and subsequent neutralization test or the detection of the encoding genes with probes or polymerase chain reaction (PCR). These methods are time-consuming and not suited for a routine diagnostic laboratory. Immunological methods like enzyme immunoassay enable a fast and specific shiga-toxin detection in stool specimens. It is commonly recommended to enrich the EHEC bacteria in selective broth media prior to the test run to enhance the sensitivity of the method (4, 5, 6). GAL_E-030_ _DE Page 9 of 16
10 References: 1. Beutin, L.: Infektionen mit enterohämorrhagischen Escherichia coli (EHEC). Bundesgesundheitsbl. 39, 11 (1996): Bockemühl, J., Karch, H. und Tschäpe, H.: Infektionen des Menschen durch enterohämorrhagische Escherichia coli (EHEC) in Deutschland, Bundesgesundheitsbl. 6 (1997): Stock, I. und Wiedemann, B.: Infektionen durch enterohämorrhagische Escherichia coli-(ehec-) Stämme. MMP, 20. Jahrgang, Heft 3 (1997): Gerritzen, A.: Vergleichender Verotoxin-Nachweis im Stuhl mit zwei Enzymimmunoassays und dem Zytotoxizitätstest auf Verozellen. Lab. Med. 1998; 22 (12): Reissbrodt, R.: Enterohämorrhagic Escherichia coli: isolation and identification. Biotest Bulletin 6: (1998) 6. Fruth, A. et al.: Zur Verbesserung der gegenwärtigen bakteriologischen Diagnostik von enterohämorrhagischen Escherichia coli (EHEC). Bundesgesundheitsbl.-Gesundheitsforsch.- Gesundheitsschutz 4, (2000) Intended Use The Serazym Verotoxin 1+2 is an in-vitro vitro-diagnostic device for direct detection of Verotoxin 1 and 2 (shiga-toxin 1 and 2) in faecal specimens and stool culture supernatants. Principle Of The Test Serazym Verotoxin 1+2 is an indirect two-site-immunoassay for the qualitative determination of verotoxin 1 and 2 based on polyclonal and monoclonal antibodies. Verotoxin 1 and/or 2 of specimens and the positive control react with polyclonal anti-verotoxin 1 and 2 antibodies coated on the solid phase of the microplate. After incubation for 60 minutes at room temperature (RT) non-bound material is removed by a washing step. Subsequently bound toxins specifically react with biotinylated monoclonal anti-verotoxin 1 and anti-verotoxin 2 antibodies during a second incubation period of 30 min at RT. Non-bound material is separated from the solid-phase immune complexes by a subsequent washing step. During the next incubation period of 30 min at RT horseradish peroxidase (HRP) conjugated streptavidin reacts with the bound biotinylated antibodies. Unbound conjugate is removed by a washing step. HRP converts the subsequently added colourless substrate solution of 3,3,5,5 -tetramethylbenzidine (TMB) into a blue product. The enzyme reaction is terminated by sulphuric acid dispensed into the wells after 15 min incubation at RT turning the solution from blue to yellow. The optical density (OD) of the solution read at 450 / 620 nm is directly proportional to the specifically bound amount of verotoxin 1 and/or verotoxin 2. Considering the cut-off value results are interpreted as positive or negative. GAL_E-030_ _DE Page 10 of 16
11 Test Components 1 WELLS 2 WASHBUF CONC 10x Wash buffer 10-fold 3 DIL 4 CONTROL + 5 CONTROL 6/1 CONJ BIOTIN 6/2 CONJ STREPT 7 SUBSTR TMB 8 STOP Microtitration plate coated with polyclonal anti- Verotoxin 1+2 antibodies (sheep) Sample diluent for Serazym Verotoxin 1+2 Positive control Inactivated Verotoxin positive culture supernatant Negative control Verotoxin negative sample Biotin-conjugate Biotinylated, monoclonal anti-verotoxin 1 and 2 antibodies (mouse) Streptavidin-poly poly-hrp HRP-conjugate Substrate 3,3,5,5 -Tetramethylbenzidine and hydrogen peroxide Stop solution 0.25 M sulphuric acid For 96 Wells For 2x 96 Wells 12 single breakable 8-well strips colour coding orange vacuum-sealed with desiccant 100 ml concentrate for 1000 ml solution white cap 100 ml ready to use coloured orange black cap 2.0 ml ready to use coloured blue red cap 2.0 ml ready to use coloured blue green cap 15 ml ready to use coloured green white cap 15 ml ready to use coloured red brown cap 15 ml ready to use blue cap 15 ml ready to use yellow cap 2x 12 single breakable 8-well strips colour coding orange vacuum-sealed with desiccant 2x 100 ml concentrate for 2x 1000 ml solution white cap 2x 100 ml ready to use coloured orange black cap 4.0 ml ready to use coloured blue red cap 4.0 ml ready to use coloured blue green cap 30 ml ready to use coloured green white cap 30 ml ready to use coloured red brown cap 30 ml ready to use blue cap 30 ml ready to use yellow cap Preparation And Storage Of Samples Collection and storage Stool samples should be stored at 2 8 C immediately after collection and processed within 72 hours. Longer storage is possible at -20 C. In case of direct verotoxin detection from stool suspension in sample diluent, testing immediately after the sample has arrived in the laboratory should be preferred. Stool specimens for enrichment culture should be transferred to the enrichment broth within 1-2 hours after the sample has arrived. Preparation Sample preparation for direct testing from diluted stool specimens Quickly thaw frozen stool specimens and mix them well. Samples treated with transport media should also be mixed before testing. Pipette 500 µl of Serazym Verotoxin 1+2 sample diluent into a clean tube. Transfer 200 mg (diameter about 4-6 mm) or 200 µl stool sample into the tube with the 500 µl of Serazym Verotoxin 1+2 sample diluent and mix thoroughly. Caution: the direct investigation of stool specimens with ELISA without prior enrichment should only serve as screening method for a fast preliminary result. A subsequent additional investigation of the concerning sample after enrichment is absolutely necessary to reach a sufficient sensitivity. A negative ELISA result does not necessarily exclude an infection with EHEC when stool samples are tested without enrichment culture. GAL_E-030_ _DE Page 11 of 16
12 Sample preparation for testing from enrichment culture Transfer about 200 mg or 200 µl of stool sample into a tube with 4 ml enrichment broth, e.g. EHEC-Direktmedium (Haipha) or mtsb (Mast) containing 50 ng/ml Mitomycin C and incubate for 18 to 20 hours at 37 C. If possible, use a shaker during sample incubation. Subsequently allow floating particles to sediment or if necessary sediment floating particles by a centrifugation step. Dilute the culture supernatant 1 : 2 with Serazym Verotoxin 1+2 sample diluent and dispense 100 µl diluted culture sample per well. Materials Required But Not Provided Adjustable one-channel micropipettes and pipette tips adjustable multi-channel pipette or multipipette and pipette tips Reagent container for multi-channel pipette 8-channel wash comb with vacuum pump and waste bottle or microplate washer microplate reader with 450 nm filter for measurement and 620 nm for reference distilled or deionized water glassware tubes (2 ml) for sample preparation enrichment broth, e. g. EHEC-Direktmedium (Haipha) or mtsb (Mast) containing 50 ng/ml Mitomycin C Preparation And Storage Of Reagents Kit size and expiry One kit is designed for 1x 96 or 2x 96 determinations. The expiry date of each component is reported on its respective label, that of the complete kit on the outer box label. Upon receipt, all test components have to be kept at 2 8 C, preferably in the original kit box. After opening all kit components are stable for at least 2 months, provided proper storage. The ready to use wash solution can be used for at least 1 month when stored at 2 8 C. Reagent preparation Allow all components to reach room temperature prior to use in the assay. The microtitration plate is vacuum-sealed in a foil with desiccant. The plate consists of a frame and strips with breakable wells. Allow the sealed plate to reach room temperature before opening. Unused wells should be stored refrigerated and protected from moisture in the original cover carefully resealed. Prepare a sufficient amount of wash solution by diluting the 10-fold concentrated wash buffer with distilled or deionized water. For Example: 10 ml wash buffer concentrate (2) + 90 ml distilled or deionized water. Assay Procedure Dilute stool samples with Serazym Verotoxin 1+2 sample diluent (3) , e.g. 200 mg or 200 µl stool ml Serazym Verotoxin 1+2 sample diluent (3). For enrichment culture: Transfer 200 mg or 200 µl stool sample to 4 ml enrichment broth (e.g. EHEC-Direktmedium or mtsb + 50 ng/ml Mitomycin C) and incubate for hours at 37 C if possible on a shaker. Dilute culture supernatant 1:2 with Serazym Verotoxin 1+2 sample diluent (3), mix thoroughly and use 100 µl / well for ELISA testing. Avoid any time shift during dispensing of reagents and samples. Make sure the soak time of the wash buffer in the wells is at least 5 seconds per wash cycle and that the remaining fluid is completely drained in every single wash cycle! Avoid light exposure of the TMB substrate solution! GAL_E-030_ _DE Page 12 of 16
13 Working steps 1. Warm all reagents to room temperature (RT) before use. Mix gently without causing foam. 2. Pipette: 120 µl CONTROL + positive control (4) 120 µl CONTROL negative control (5) 100 µl diluted stool specimen or diluted culture supernatant. 3. Cover plate and incubate for 60 min at RT. 4. Decant, then wash each well 5x with 300 µl wash solution (diluted from (2 ) and tap dry onto absorbent paper. 5. Dispense 3 drops (or 120 µl) CONJ BIOTIN biotin-conjugate (6/1) per well. 6. Cover plate and incubate for 30 min at RT. 7. Decant, then wash each well 5x with 300 µl wash solution (diluted from (2 ) and tap dry onto absorbent paper. 8. Dispense 3 drops (or 120 µl) CONJ STREPT streptavidin-poly-hrp-conjugate (6/2) per well. 9. Cover plate and incubate for 30 min at RT. 10. Decant, then wash each well 5x with 300 µl wash solution (diluted from (2 ) and tap dry onto absorbent paper. 11. Dispense 3 drops (or 120 µl) SUBSTR TMB substrate (7) per well. 12. Incubate for 15 min at RT protected from light. 13. Dispense 3 drops (or 120 µl) STOP stop solution (8) per well, mix gently. 14. Read OD at 450 nm / 620 nm with a microplate reader within 30 min after reaction stop. Result Interpretation Qualitative evaluation Cut-off determination: OD negative control Samples with OD values equal with or higher than the cut-off are considered positive, samples with OD values below the cut-off are considered negative in the Serazym Verotoxin 1+2. Reference Values Serazym Verotoxin 1+2 Positive Cut-off Negative < Cut-off It is recommended that each laboratory establishes its own normal and pathological reference ranges as usually done for other diagnostic parameters too. Therefore, the mentioned reference values provide a guide only to values which might be expected. GAL_E-030_ _DE Page 13 of 16
14 Test validity The test run is valid if: the mean OD of the negative control is 0.20 (manual performance) 0.30 (automatic performance) the mean OD of the positive control is 1.00 If the above mentioned quality criteria are not met, repeat the test and make sure that the test procedure is followed correctly (incubation times and temperatures, sample and wash buffer dilution, wash steps etc.). In case of repeated failure of the quality criteria contact your supplier. Limitations of the procedure There is no correlation between measured absorbance and seriousness of the infection. It is also not allowed to correlate absorbances of the samples with that of the positive control. Cross contamination of reagents and samples can produce false positive results. Incorrect dilutions, not sufficiently homogenized samples or solid particles after centrifugation of the suspension can cause false results. A negative test result in the Serazym Verotoxin 1+2 does not necessarily exclude an EHEC infection. Due to the usually low toxin concentrations in stool samples, the selective enrichment of EHEC bacteria in special culture media is of decisive influence on the sensitivity of the toxin detection with ELISA (6). The overall interpretation of the ELISA results should always consider the microbiological examination as well as clinical findings. Automatic Processing Performing the Serazym Verotoxin 1+2 on fully automated microplate processors (e.g. DS2, DSX) may cause elevated absorbances in comparison to the manual procedure due to individual differences concerning wash procedures and general technical specifications of the equipment. In these cases a maximum value of 0.3 absorbance units is permissible for the negative control. It is recommended to use a wash procedure including 10 seconds soak time per strip and wash step followed by a wash step with distilled or deionized water with 10 seconds of soak time after the final wash step of each wash cycle. If necessary the number of washing steps can be enhanced from 5x to 7x-8x. Correlation: manual automatic processing A panel of 188 specimens was investigated in parallel by manual and automatic processing method (DS2, Dynex Technologies) resp. The correlation was calculated with r = ,0 Serazym Verotoxin 1+2 3,5 automatic performance (DS2) 3,0 2,5 2,0 1,5 1,0 0,5 0,0 0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5 4,0 manual performance GAL_E-030_ _DE Page 14 of 16
15 Performance Characteristics Precision Intra-assay coefficient of variation (CV) in the Serazym Verotoxin 1+2 calculated from 12-fold determinations of samples: verotoxin 2 mean OD standard CV (%) (pg/ml) deviation Inter-assay coefficient of variation (CV) in the Serazym Verotoxin 1+2 in 11 different test runs from 3-fold determinations of samples: verotoxin 2 mean OD standard CV (%) (pg/ml) deviation Lower detection limit The lower detection limit of the Serazym Verotoxin 1+2 was determined with < 100 pg / ml (<10 pg / well) by separate titration of verotoxin 1 and 2. Specificity and sensitivity A total of 825 stool specimens were tested in parallel with the vero-cell cytotoxicity assay and the Serazym Verotoxin 1+2. The sample material consisted of 795 specimens sent for TPE-group diagnosis and 30 specimens that were already characterized by shiga-toxin gen PCR and culture and stored at -20 C until testing. Enrichment culture (mtsb; hours at 37 C) of all samples was carried out prior to ELISA testing. Vero-cell assay positive negative Serazym positive 0 2 ELISA negative Specificity: 98.8% Vero-cell assay positive negative Serazym positive 11 0 ELISA negative 2 17 Sensitivity: 84.6% Cross reactivity The routine diagnosis for TPE-group bacteria in this study revealed a positive pathogen detection in 141 samples. These pathogens belonged to 12 different bacterial species: Staphylococcus aureus, enterotoxin negative; Staphylococcus aureus, enterotoxin positive; EHEC; Pseudomonas aeruginosa; Salmonella typhimurium; Salmonella enteritidis; Salmonella spec. Aeromonas hydrophila; Aeromonas caviae; Campylobacter spec.; Hafnia alvei; Yersinia enterocolitica O:3. None of them caused false positive reactions in the Serazym Verotoxin 1+2. Common Advices and Precautions This kit is for in-vitro use only. Follow the working instructions carefully. The kit should be performed by trained technical staff only. The expiration dates stated on the respective labels are to be observed. Do not use or mix reagents from different lots except for sample diluent, wash buffer, TMB/substrate te solution and stop solution. Do not use reagents from other manufacturers. Avoid time shift during dispensing of reagents. All reagents should be kept at 2 8 C before use. Some of the reagents (2, 3, 4, 5, 6, 7) contain small amounts of Thimerosal (0.01% w/v) and Kathon (1.0% v/v) as preservative. They must not be swallowed or allowed to come into contact with skin or mucous membranes. Handle all components and all patient samples as if potentially hazardous. Since the kit contains potentially hazardous materials, the following precautions should generally be observed: Do not smoke, eat or drink while handling kit material! Always use protective gloves! Never pipette material by mouth! Note safety precautions of the single test components! GAL_E-030_ _DE Page 15 of 16
16 Incubation Scheme Serazym Verotoxin 1+2 (E-030) 1. pipette: 120 µl CONTROL + (4) 120 µl CONTROL (5) 100 µl diluted stool specimen or culture supernatant 60 min incubation (room temperature) 5 x wash with wash solution 2. 3 drops (or 120 µl) CONJ BIOTIN (6/1) 30 min incubation (room temperature) 5 x wash with wash solution 3. 3 drops (or 120 µl) CONJ STREPT (6/2) 30 min incubation (room temperature) 5 x wash with wash solution 4. 3 drops (or 120 µl) SUBSTR TMB (7) 15 min incubation (room temperature) protected from light 5. 3 drops (or 120 µl) STOP (8) Read OD at 450 / 620 nm GAL_E-030_ _DE Page 16 of 16
Serazym Clostridium difficile Toxin A+B
 Serazym Clostridium difficile Toxin A+B Enzymimmunoassay zum Nachweis von Clostridium difficile Toxin A+B in Stuhlproben und Kultursuspensionen r E-040 n96 r E-040-A2 n2x 96 v In-vitro- Diagnostikum c
Serazym Clostridium difficile Toxin A+B Enzymimmunoassay zum Nachweis von Clostridium difficile Toxin A+B in Stuhlproben und Kultursuspensionen r E-040 n96 r E-040-A2 n2x 96 v In-vitro- Diagnostikum c
Enzymimmunoassay zum Nachweis von Adenovirus in Stuhlproben
 Serazym Adenovirus Enzymimmunoassay zum Nachweis von Adenovirus in Stuhlproben r E-017 n96 r E-017-A2 n2x 96 v In-vitro- Diagnostikum c Einführung Adenoviren sind Ursache von Infektionskrankheiten der
Serazym Adenovirus Enzymimmunoassay zum Nachweis von Adenovirus in Stuhlproben r E-017 n96 r E-017-A2 n2x 96 v In-vitro- Diagnostikum c Einführung Adenoviren sind Ursache von Infektionskrankheiten der
Enzymimmunoassay zum Nachweis von IgG Antikörpern gegen zyklische citrullinierte Peptide (CCP) in humanem Serum oder Plasma
 Serazym Anti-CCP IgG Enzymimmunoassay zum Nachweis von IgG Antikörpern gegen zyklische citrullinierte Peptide (CCP) in humanem Serum oder Plasma r E-095 n96 v In-vitro- Diagnostikum c Einführung Die Bestimmung
Serazym Anti-CCP IgG Enzymimmunoassay zum Nachweis von IgG Antikörpern gegen zyklische citrullinierte Peptide (CCP) in humanem Serum oder Plasma r E-095 n96 v In-vitro- Diagnostikum c Einführung Die Bestimmung
Serazym Clostridium difficile GDH
 Serazym Clostridium difficile GDH Enzymimmunoassay zum Nachweis von Clostridium difficile GDH in Stuhlproben r E-107 n96 r E-107-A2 n2x 96 v In-vitro- Diagnostikum c Einführung Der anaerobe Sporenbildner
Serazym Clostridium difficile GDH Enzymimmunoassay zum Nachweis von Clostridium difficile GDH in Stuhlproben r E-107 n96 r E-107-A2 n2x 96 v In-vitro- Diagnostikum c Einführung Der anaerobe Sporenbildner
Enzymimmunoassay zum Nachweis von Adenovirus in Stuhlproben
 Serazym Adenovirus Enzymimmunoassay zum Nachweis von Adenovirus in Stuhlproben r E-017 n96 r E-017-A2 n2x 96 v In-vitro- Diagnostikum c Einführung Adenoviren sind Ursache von Infektionskrankheiten der
Serazym Adenovirus Enzymimmunoassay zum Nachweis von Adenovirus in Stuhlproben r E-017 n96 r E-017-A2 n2x 96 v In-vitro- Diagnostikum c Einführung Adenoviren sind Ursache von Infektionskrankheiten der
Serazym Giardia. Einführung. Enzymimmunoassay zum Nachweis von Giardia lamblia CWP-1 in Stuhlproben. r E-106-A n96 v In-vitro- Diagnostikum c
 Serazym Giardia Enzymimmunoassay zum Nachweis von Giardia lamblia CWP-1 in Stuhlproben r E-106-A n96 v In-vitro- Diagnostikum c Einführung Giardia lamblia (syn. Lamblia intestinalis) ist ein weltweit verbreitetes
Serazym Giardia Enzymimmunoassay zum Nachweis von Giardia lamblia CWP-1 in Stuhlproben r E-106-A n96 v In-vitro- Diagnostikum c Einführung Giardia lamblia (syn. Lamblia intestinalis) ist ein weltweit verbreitetes
Testanleitung. Quantitative Bestimmung der Tumor M2-PK Stuhltest Instruction Manual. Quantitative Determination of the Tumor M2-PK Stool Test
 Testanleitung Quantitative Bestimmung der Tumor M2-PK Stuhltest Instruction Manual Quantitative Determination of the Tumor M2-PK Stool Test Tumor M2-PK ELISA Stuhltest/Stool Test REF Artikel-Nr./Catalog
Testanleitung Quantitative Bestimmung der Tumor M2-PK Stuhltest Instruction Manual Quantitative Determination of the Tumor M2-PK Stool Test Tumor M2-PK ELISA Stuhltest/Stool Test REF Artikel-Nr./Catalog
BCA Protein Assay (Pierce)
 BCA Protein Assay (Pierce) BCA assay: geeignet für geringe Proteinmengen!!! Die Proteine bilden mit Cu2+-Ionen in alkalischer Lösung einen Komplex (Biuret-Reaktion). Die Cu2+-Ionen des Komplexes werden
BCA Protein Assay (Pierce) BCA assay: geeignet für geringe Proteinmengen!!! Die Proteine bilden mit Cu2+-Ionen in alkalischer Lösung einen Komplex (Biuret-Reaktion). Die Cu2+-Ionen des Komplexes werden
Serazym H. pylori 2nd Gen.
 Serazym H. pylori 2nd Gen. Enzymimmunoassay zum Nachweis von Helicobacter pylori Antigen in Stuhlproben r E-114-A n96 v In-vitro- Diagnostikum c Einführung Das Bakterium Helicobacter pylori (H. pylori)
Serazym H. pylori 2nd Gen. Enzymimmunoassay zum Nachweis von Helicobacter pylori Antigen in Stuhlproben r E-114-A n96 v In-vitro- Diagnostikum c Einführung Das Bakterium Helicobacter pylori (H. pylori)
Zink Transporter 8 (ZnT8) Ab ELISA
 Arbeitsanleitung Zink Transporter 8 (ZnT8) Ab ELISA Enzymimmunoassay für die quantitative Bestimmung von ZnT8-Autoantikörpern in Serum I V D REF EA102/96 12 x 8 2 8 C DLD Gesellschaft für Diagnostika und
Arbeitsanleitung Zink Transporter 8 (ZnT8) Ab ELISA Enzymimmunoassay für die quantitative Bestimmung von ZnT8-Autoantikörpern in Serum I V D REF EA102/96 12 x 8 2 8 C DLD Gesellschaft für Diagnostika und
Anti-ASGPR IgG ELISA
 Product information Information about other products is available at: www.demeditec.com Userś Manual Anti-ASGPR IgG ELISA Enzyme Immunoassay for the determination of IgG antibodies to asialoglycoprotein
Product information Information about other products is available at: www.demeditec.com Userś Manual Anti-ASGPR IgG ELISA Enzyme Immunoassay for the determination of IgG antibodies to asialoglycoprotein
Chymotrypsin ELISA Kit. Chymotrypsin ELISA Kit. Zur in vitro Bestimmung von Chymotrypsin in Stuhlproben
 Arbeitsanleitung/Manual ELISA Kit Zur in vitro Bestimmung von in Stuhlproben ELISA Kit For the in vitro determination of in stool Valid from 31.03.2010 +8 C K 6910 +2 C 96 Immundiagnostik AG, Stubenwald-Allee
Arbeitsanleitung/Manual ELISA Kit Zur in vitro Bestimmung von in Stuhlproben ELISA Kit For the in vitro determination of in stool Valid from 31.03.2010 +8 C K 6910 +2 C 96 Immundiagnostik AG, Stubenwald-Allee
CABLE TESTER. Manual DN-14003
 CABLE TESTER Manual DN-14003 Note: Please read and learn safety instructions before use or maintain the equipment This cable tester can t test any electrified product. 9V reduplicated battery is used in
CABLE TESTER Manual DN-14003 Note: Please read and learn safety instructions before use or maintain the equipment This cable tester can t test any electrified product. 9V reduplicated battery is used in
PIGTYPE Trichinella Ab
 PIGTYPE Trichinella Ab ELISA-Testkit zum Nachweis von Antikörpern gegen Trichinella spp. bei Schweinen Gebrauchsinformation Labor Diagnostik Leipzig in vitro-diagnostikum für Schweine Die deutsche Gebrauchsinformation
PIGTYPE Trichinella Ab ELISA-Testkit zum Nachweis von Antikörpern gegen Trichinella spp. bei Schweinen Gebrauchsinformation Labor Diagnostik Leipzig in vitro-diagnostikum für Schweine Die deutsche Gebrauchsinformation
Gebrauchsinformation. Neospora-p38 ELISA Cattle
 Gebrauchsinformation Neospora-p38 ELISA Cattle Test zum Nachweis von IgG-Antikörpern gegen den Erreger Neospora caninum bei Rindern In-vitro Diagnostikum für Tiere Bestandteile des Kits: 1 Mikrotiterplatte,
Gebrauchsinformation Neospora-p38 ELISA Cattle Test zum Nachweis von IgG-Antikörpern gegen den Erreger Neospora caninum bei Rindern In-vitro Diagnostikum für Tiere Bestandteile des Kits: 1 Mikrotiterplatte,
RIDASCREEN FAST Ei / Egg Protein
 RIDASCREEN FAST Ei / Egg Protein Enzymimmunoassay zur quantitativen Bestimmung von Eiklar-Proteinen Enzyme immunoassay for the quantitative analysis of egg white proteins Art. No.: R6402 In vitro Test
RIDASCREEN FAST Ei / Egg Protein Enzymimmunoassay zur quantitativen Bestimmung von Eiklar-Proteinen Enzyme immunoassay for the quantitative analysis of egg white proteins Art. No.: R6402 In vitro Test
Gebrauchsanweisung. Microbial Transglutaminase (MTG) ELISA
 Gebrauchsanweisung Microbial Transglutaminase (MTG) ELISA Enzymimmunoassay zur quantitativen Bestimmung von Mikrobieller Transglutaminase (MTG) Art.-Nr. E021 Für Forschungs & Entwicklungszwecke Revision
Gebrauchsanweisung Microbial Transglutaminase (MTG) ELISA Enzymimmunoassay zur quantitativen Bestimmung von Mikrobieller Transglutaminase (MTG) Art.-Nr. E021 Für Forschungs & Entwicklungszwecke Revision
Antikörper gegen TNFα-Blocker (ADA) ELISA Kit
 Antikörper gegen TNFα-Blocker (ADA) ELISA Kit Zur in vitro Bestimmung von freien humanen Antikörpern gegen den Wirkstoff (z. B. REMICADE) in EDTA-Plasma und Serum Antibodies against TNFα-Blocker (ADA)
Antikörper gegen TNFα-Blocker (ADA) ELISA Kit Zur in vitro Bestimmung von freien humanen Antikörpern gegen den Wirkstoff (z. B. REMICADE) in EDTA-Plasma und Serum Antibodies against TNFα-Blocker (ADA)
FLOCKTYPE Salmonella. Gebrauchsinformation
 FLOCKTYPE Salmonella ELISA-Testkit zum Nachweis von Antikörpern gegen Salmonellen im Huhn Gebrauchsinformation in vitro-diagnostikum für Tiere Die deutsche Gebrauchsinformation ist nach 17 c TierSG zugelassen.
FLOCKTYPE Salmonella ELISA-Testkit zum Nachweis von Antikörpern gegen Salmonellen im Huhn Gebrauchsinformation in vitro-diagnostikum für Tiere Die deutsche Gebrauchsinformation ist nach 17 c TierSG zugelassen.
TNFα-Blocker-ADA, Antikörper gegen Etanercept (z.b. ENBREL ) TNFα blocker ADA, antibodies against etanercept (e.g. ENBREL )
 Arbeitsanleitung TNFα-Blocker-ADA, Antikörper gegen Etanercept (z.b. ENBREL ) Zur in vitro Bestimmung von freien humanen Antikörpern gegen Etanercept (z.b. ENBREL ) in EDTA-Plasma und Serum TNFα blocker
Arbeitsanleitung TNFα-Blocker-ADA, Antikörper gegen Etanercept (z.b. ENBREL ) Zur in vitro Bestimmung von freien humanen Antikörpern gegen Etanercept (z.b. ENBREL ) in EDTA-Plasma und Serum TNFα blocker
Deceleration Technology. Rotary Dampers with high-torque range WRD-H 0607 WRD-H 0805 WRD-H 1208 WRD-H 1610 WRD-H
 Rotary Dampers with high-torque range WRD-H 67 WRD-H 85 WRD-H 128 WRD-H 161 WRD-H 21 Deceleration Technology ONLINE CALCULATION AND 2D / 3D CAD DOWNLOAD M m L F Benefits Applications: - Mechanical and
Rotary Dampers with high-torque range WRD-H 67 WRD-H 85 WRD-H 128 WRD-H 161 WRD-H 21 Deceleration Technology ONLINE CALCULATION AND 2D / 3D CAD DOWNLOAD M m L F Benefits Applications: - Mechanical and
Helicobacter pylori Antigen ELISA Kit
 Arbeitsanleitung / Manual Helicobacter pylori Antigen ELISA Kit Zur in vitro Bestimmung des Helicobacter pylori in Stuhl For the in vitro Determination of Helicobacter pylori in stool Gültig ab / Valid
Arbeitsanleitung / Manual Helicobacter pylori Antigen ELISA Kit Zur in vitro Bestimmung des Helicobacter pylori in Stuhl For the in vitro Determination of Helicobacter pylori in stool Gültig ab / Valid
POST MARKET CLINICAL FOLLOW UP
 POST MARKET CLINICAL FOLLOW UP (MEDDEV 2.12-2 May 2004) Dr. med. Christian Schübel 2007/47/EG Änderungen Klin. Bewertung Historie: CETF Report (2000) Qualität der klinischen Daten zu schlecht Zu wenige
POST MARKET CLINICAL FOLLOW UP (MEDDEV 2.12-2 May 2004) Dr. med. Christian Schübel 2007/47/EG Änderungen Klin. Bewertung Historie: CETF Report (2000) Qualität der klinischen Daten zu schlecht Zu wenige
TNF ELISA Kit. Zur in vitro Bestimmung des TNF in Serum, Plasma, Stuhl und Zellkulturüberständen
 TNF ELISA Kit Zur in vitro Bestimmung des TNF in Serum, Plasma, Stuhl und Zellkulturüberständen For the in vitro determination of TNF in serum, plasma, stool and cell culture supernatant Gültig ab / Valid
TNF ELISA Kit Zur in vitro Bestimmung des TNF in Serum, Plasma, Stuhl und Zellkulturüberständen For the in vitro determination of TNF in serum, plasma, stool and cell culture supernatant Gültig ab / Valid
Immunglobulin G ELISA Kit
 ELISA Kit Zur in vitro Bestimmung des in Serum, Plasma und Urin Immunoglobulin G ELISA Kit For the in vitro determination of Immunoglobulin G in serum, plasma and urine Gültig ab/valid from 16.06.2011
ELISA Kit Zur in vitro Bestimmung des in Serum, Plasma und Urin Immunoglobulin G ELISA Kit For the in vitro determination of Immunoglobulin G in serum, plasma and urine Gültig ab/valid from 16.06.2011
For the in vitro determination of Osteonectin in serum
 Arbeitsanleitung / Manual EIA Kit Zur in vitro Bestimmung von in Serum EIA Kit For the in vitro determination of in serum Nur zu wissenschaftlichen Zwecken / For research use only Gültig ab / Valid from
Arbeitsanleitung / Manual EIA Kit Zur in vitro Bestimmung von in Serum EIA Kit For the in vitro determination of in serum Nur zu wissenschaftlichen Zwecken / For research use only Gültig ab / Valid from
Testosteron ELISA, EIA
 Testosteron ELISA, EIA Enzymimmunoassay für Testosteron in porcinem Serum/Plasma Kurzbeschreibung der Assay-Durchführung 1. Testbestandteile und Lösungen auf Raumtemperatur bringen (Ausnahme: Tracer-Stammlösung
Testosteron ELISA, EIA Enzymimmunoassay für Testosteron in porcinem Serum/Plasma Kurzbeschreibung der Assay-Durchführung 1. Testbestandteile und Lösungen auf Raumtemperatur bringen (Ausnahme: Tracer-Stammlösung
Deceleration Technology. Rotary Dampers with high-torque range WRD-H 7550 WRD-H 9565 WRD-H
 Rotary Dampers with high-torque range WRD-H 7550 WRD-H 9565 WRD-H 12070 Deceleration Technology ONLINE CALCULATION AND 2D / 3D CAD DOWNLOAD M m L F Benefits Material: - Aluminium and steel Applications:
Rotary Dampers with high-torque range WRD-H 7550 WRD-H 9565 WRD-H 12070 Deceleration Technology ONLINE CALCULATION AND 2D / 3D CAD DOWNLOAD M m L F Benefits Material: - Aluminium and steel Applications:
anti-httg IgG ELISA Kit
 ELISA Kit Zur in vitro Bestimmung von anti-human- Gewebetransglutaminase IgG Antikörpern in Serum Gültig ab 20.06.2008 K 9398 +8 C +2 C 96 Immundiagnostik AG, Stubenwald-Allee 8a, D 64625 Bensheim Tel.:
ELISA Kit Zur in vitro Bestimmung von anti-human- Gewebetransglutaminase IgG Antikörpern in Serum Gültig ab 20.06.2008 K 9398 +8 C +2 C 96 Immundiagnostik AG, Stubenwald-Allee 8a, D 64625 Bensheim Tel.:
iid software tools QuickStartGuide iid USB base driver installation
 iid software tools QuickStartGuide iid software tools USB base driver installation microsensys Nov 2016 Introduction / Einleitung This document describes in short form installation of the microsensys USB
iid software tools QuickStartGuide iid software tools USB base driver installation microsensys Nov 2016 Introduction / Einleitung This document describes in short form installation of the microsensys USB
Gebrauchsinformation BABESIA-ELISA DOG
 Gebrauchsinformation BABESIA-ELISA DOG Test zum Nachweis von Antikörpern gegen den Erreger der Babesiose beim Hund, Babesia canis In-vitro Diagnostikum für Hunde Bestandteile des Kits: 1 Mikrotiterplatte,
Gebrauchsinformation BABESIA-ELISA DOG Test zum Nachweis von Antikörpern gegen den Erreger der Babesiose beim Hund, Babesia canis In-vitro Diagnostikum für Hunde Bestandteile des Kits: 1 Mikrotiterplatte,
WESAMIN GmbH & Co. KG
 WESAMIN GmbH & Co. KG Arbeitsanleitung Histamin - Lebensmittel ELISA Enzymimmunoassay für die quantitative Bestimmung von Histamin in Wein, Fischmehl, Fisch, Wurst, Käse und Milch REF HLM00 96 2 8 C WESAMIN
WESAMIN GmbH & Co. KG Arbeitsanleitung Histamin - Lebensmittel ELISA Enzymimmunoassay für die quantitative Bestimmung von Histamin in Wein, Fischmehl, Fisch, Wurst, Käse und Milch REF HLM00 96 2 8 C WESAMIN
Anti - Titin - Antikörper - ELISA
 Arbeitsanleitung Anti - Titin - Antikörper - ELISA Enzymimmunoassay für die quantitative Bestimmung von anti-titin-antikörpern in Serum und Plasma REF EA 601/48 6 x 8 2 8 C DLD Gesellschaft für Diagnostika
Arbeitsanleitung Anti - Titin - Antikörper - ELISA Enzymimmunoassay für die quantitative Bestimmung von anti-titin-antikörpern in Serum und Plasma REF EA 601/48 6 x 8 2 8 C DLD Gesellschaft für Diagnostika
PFBV - ELISA. Enzyme Linked Immuno Sorbent Assay. zum Nachweis des. Pelargonium flower break virus (PFBV)
 Baumgartenstr. 5 D-79285 Ebringen (FRG) Tel.: +49 7664 600254 Fax: +49 7664 600255 Email: info@steffens-biotec.com PFBV - ELISA Enzyme Linked Immuno Sorbent Assay zum Nachweis des Pelargonium flower break
Baumgartenstr. 5 D-79285 Ebringen (FRG) Tel.: +49 7664 600254 Fax: +49 7664 600255 Email: info@steffens-biotec.com PFBV - ELISA Enzyme Linked Immuno Sorbent Assay zum Nachweis des Pelargonium flower break
Immunglobulin G ELISA Kit
 ELISA Kit Zur in vitro Bestimmung des in Serum, Plasma und Urin Immunoglobulin G ELISA Kit For the in vitro determination of Immunoglobulin G in serum, plasma and urine Gültig ab/valid from 07.02.2013
ELISA Kit Zur in vitro Bestimmung des in Serum, Plasma und Urin Immunoglobulin G ELISA Kit For the in vitro determination of Immunoglobulin G in serum, plasma and urine Gültig ab/valid from 07.02.2013
Instruktionen Mozilla Thunderbird Seite 1
 Instruktionen Mozilla Thunderbird Seite 1 Instruktionen Mozilla Thunderbird Dieses Handbuch wird für Benutzer geschrieben, die bereits ein E-Mail-Konto zusammenbauen lassen im Mozilla Thunderbird und wird
Instruktionen Mozilla Thunderbird Seite 1 Instruktionen Mozilla Thunderbird Dieses Handbuch wird für Benutzer geschrieben, die bereits ein E-Mail-Konto zusammenbauen lassen im Mozilla Thunderbird und wird
Rat Control HZ-DEV99RC 001 2016-04. Rat control sera suitable for internal control quality of the following HOELZEL ELISAs:
 Rat Control Rat control sera suitable for internal control quality of the following HOELZEL ELISAs: Testosterone rat/mouse Corticosterone rat/mouse Prolactin rat TSH rat (HZ-DEV9911) (HZ-DEV9922) (HZ-DEV9966)
Rat Control Rat control sera suitable for internal control quality of the following HOELZEL ELISAs: Testosterone rat/mouse Corticosterone rat/mouse Prolactin rat TSH rat (HZ-DEV9911) (HZ-DEV9922) (HZ-DEV9966)
FIVNAT-CH. Annual report 2002
 FIVNAT-CH Schweizerische Gesellschaft für Reproduktionsmedizin Annual report 2002 Date of analysis 15.01.2004 Source: FileMaker Pro files FIVNAT_CYC.FP5 and FIVNAT_PAT.FP5 SUMMARY TABLE SUMMARY RESULTS
FIVNAT-CH Schweizerische Gesellschaft für Reproduktionsmedizin Annual report 2002 Date of analysis 15.01.2004 Source: FileMaker Pro files FIVNAT_CYC.FP5 and FIVNAT_PAT.FP5 SUMMARY TABLE SUMMARY RESULTS
p^db=`oj===pìééçêíáåñçêã~íáçå=
 p^db=`oj===pìééçêíáåñçêã~íáçå= Error: "Could not connect to the SQL Server Instance" or "Failed to open a connection to the database." When you attempt to launch ACT! by Sage or ACT by Sage Premium for
p^db=`oj===pìééçêíáåñçêã~íáçå= Error: "Could not connect to the SQL Server Instance" or "Failed to open a connection to the database." When you attempt to launch ACT! by Sage or ACT by Sage Premium for
Level 2 German, 2015
 91126 911260 2SUPERVISOR S Level 2 German, 2015 91126 Demonstrate understanding of a variety of written and / or visual German text(s) on familiar matters 2.00 p.m. Friday 4 December 2015 Credits: Five
91126 911260 2SUPERVISOR S Level 2 German, 2015 91126 Demonstrate understanding of a variety of written and / or visual German text(s) on familiar matters 2.00 p.m. Friday 4 December 2015 Credits: Five
The scientific approach of scale-up of a fluid bed
 Hüttlin Pharma Service The scientific approach of scale-up of a fluid bed Dr. Marcus Knöll November 2012 Objectives - Implementation of NIR in a fluid bed granulator Titel des Kapitels Case study The granulation
Hüttlin Pharma Service The scientific approach of scale-up of a fluid bed Dr. Marcus Knöll November 2012 Objectives - Implementation of NIR in a fluid bed granulator Titel des Kapitels Case study The granulation
RIDASCREEN Echinococcus IgG
 RIDASCREEN Echinococcus IgG Art. No.: K7621 R-Biopharm AG, An der neuen Bergstraße 17, D-64297 Darmstadt, Germany Tel.: +49 6151 8102-0 / Telefax: +49 6151 8102-20 1. Anwendungsbereich Für die in vitro
RIDASCREEN Echinococcus IgG Art. No.: K7621 R-Biopharm AG, An der neuen Bergstraße 17, D-64297 Darmstadt, Germany Tel.: +49 6151 8102-0 / Telefax: +49 6151 8102-20 1. Anwendungsbereich Für die in vitro
RealLine DNA Extraction 2
 RealLine Pathogen Diagnostic Kits Gebrauchsinformation RealLine DNA Extraction 2 KIT FÜR DIE EXTRAKTION VON DNA AUS KLINISCHEN PROBEN In-vitro Diagnostikum RealLine DNA-Extraction 2 VBC8897 96 Tests gültig
RealLine Pathogen Diagnostic Kits Gebrauchsinformation RealLine DNA Extraction 2 KIT FÜR DIE EXTRAKTION VON DNA AUS KLINISCHEN PROBEN In-vitro Diagnostikum RealLine DNA-Extraction 2 VBC8897 96 Tests gültig
Milenia Hybridetect. Detection of DNA and Protein
 Milenia Hybridetect Detection of DNA and Protein Firmenprofil und Produkte Milenia Biotec GmbH ist im Jahr 2000 gegründet worden. Die Firma entwickelt, produziert, vermarktet und verkauft diagnostische
Milenia Hybridetect Detection of DNA and Protein Firmenprofil und Produkte Milenia Biotec GmbH ist im Jahr 2000 gegründet worden. Die Firma entwickelt, produziert, vermarktet und verkauft diagnostische
PRO SCAN WASSERANALYSE PER SMARTPHONE WATER ANALYSIS BY SMARTPHONE ANALYSE DE L EAU PAR SMARTPHONE
 N02 WASSERANALYSE PER SMARTPHONE WATER ANALYSIS BY SMARTPHONE ANALYSE DE L EAU PAR SMARTPHONE NO 2 NO 3 ph Cl 2 CO 2 ANALYSE DIAGNOSE LÖSUNG ANALYSIS DIAGNOSIS SOLUTION THE NEW GENERATION ph KH GH N03
N02 WASSERANALYSE PER SMARTPHONE WATER ANALYSIS BY SMARTPHONE ANALYSE DE L EAU PAR SMARTPHONE NO 2 NO 3 ph Cl 2 CO 2 ANALYSE DIAGNOSE LÖSUNG ANALYSIS DIAGNOSIS SOLUTION THE NEW GENERATION ph KH GH N03
IDK Helicobacter pylori Antigen ELISA
 Arbeitsanleitung / Manual IDK Helicobacter pylori Antigen ELISA Zur in-vitro-bestimmung von Helicobacter pylori in Stuhl For the in vitro determination of Helicobacter pylori in stool Gültig ab / Valid
Arbeitsanleitung / Manual IDK Helicobacter pylori Antigen ELISA Zur in-vitro-bestimmung von Helicobacter pylori in Stuhl For the in vitro determination of Helicobacter pylori in stool Gültig ab / Valid
Cable Tester NS-468. Safety instructions
 Cable Tester NS-468 Safety instructions Do not use the cable tester NS-468 if it is damaged. This device is only for use inside dry and clean rooms. This device must be protected from moisture, splash
Cable Tester NS-468 Safety instructions Do not use the cable tester NS-468 if it is damaged. This device is only for use inside dry and clean rooms. This device must be protected from moisture, splash
Westfalia Bedienungsanleitung. Nr
 Westfalia Bedienungsanleitung Nr. 108610 Bedienungsanleitung Edelstahl Sicherheits-Brennbehälter Artikel Nr. 10 99 83 Sicherheitshinweise Der Sicherheits-Brennbehälter ist zur Verwendung in dem Westfalia
Westfalia Bedienungsanleitung Nr. 108610 Bedienungsanleitung Edelstahl Sicherheits-Brennbehälter Artikel Nr. 10 99 83 Sicherheitshinweise Der Sicherheits-Brennbehälter ist zur Verwendung in dem Westfalia
CA Enzyme immunoassay for the quantitative determination of CA 15-3 in human serum. English: Page 2 to 6 Deutsch: Seite 7 bis 11
 CA 15-3 Enzyme immunoassay for the quantitative determination of CA 15-3 in human serum Enzymimmunoassay zur quantitativen Bestimmung von CA 15-3 in humanem Serum Only for in-vitro diagnostic use English:
CA 15-3 Enzyme immunoassay for the quantitative determination of CA 15-3 in human serum Enzymimmunoassay zur quantitativen Bestimmung von CA 15-3 in humanem Serum Only for in-vitro diagnostic use English:
eurex rundschreiben 094/10
 eurex rundschreiben 094/10 Datum: Frankfurt, 21. Mai 2010 Empfänger: Alle Handelsteilnehmer der Eurex Deutschland und Eurex Zürich sowie Vendoren Autorisiert von: Jürg Spillmann Weitere Informationen zur
eurex rundschreiben 094/10 Datum: Frankfurt, 21. Mai 2010 Empfänger: Alle Handelsteilnehmer der Eurex Deutschland und Eurex Zürich sowie Vendoren Autorisiert von: Jürg Spillmann Weitere Informationen zur
Lehrstuhl für Allgemeine BWL Strategisches und Internationales Management Prof. Dr. Mike Geppert Carl-Zeiß-Str. 3 07743 Jena
 Lehrstuhl für Allgemeine BWL Strategisches und Internationales Management Prof. Dr. Mike Geppert Carl-Zeiß-Str. 3 07743 Jena http://www.im.uni-jena.de Contents I. Learning Objectives II. III. IV. Recap
Lehrstuhl für Allgemeine BWL Strategisches und Internationales Management Prof. Dr. Mike Geppert Carl-Zeiß-Str. 3 07743 Jena http://www.im.uni-jena.de Contents I. Learning Objectives II. III. IV. Recap
Level 1 German, 2014
 90886 908860 1SUPERVISOR S Level 1 German, 2014 90886 Demonstrate understanding of a variety of German texts on areas of most immediate relevance 9.30 am Wednesday 26 November 2014 Credits: Five Achievement
90886 908860 1SUPERVISOR S Level 1 German, 2014 90886 Demonstrate understanding of a variety of German texts on areas of most immediate relevance 9.30 am Wednesday 26 November 2014 Credits: Five Achievement
114-18867 09.Jan 2014 Rev C
 Application Specification 114-18867 09.Jan 2014 Rev C High Speed Data, Pin Headers 90 / 180 4pos., shie lded High Speed Data, Stiftleiste 90 / 180, geschirmt Description Beschreibung 1. Packaging of pin
Application Specification 114-18867 09.Jan 2014 Rev C High Speed Data, Pin Headers 90 / 180 4pos., shie lded High Speed Data, Stiftleiste 90 / 180, geschirmt Description Beschreibung 1. Packaging of pin
Bone Sialoprotein (BSP) ELISA Kit
 Arbeitsanleitung / Manual Bone Sialoprotein (BSP) ELISA Kit Zur in vitro Bestimmung von unterglykosyliertem Bone Sialoprotein in Serum For the in vitro determination of underglycosylated bone sialoprotein
Arbeitsanleitung / Manual Bone Sialoprotein (BSP) ELISA Kit Zur in vitro Bestimmung von unterglykosyliertem Bone Sialoprotein in Serum For the in vitro determination of underglycosylated bone sialoprotein
Level 2 German, 2013
 91126 911260 2SUPERVISOR S Level 2 German, 2013 91126 Demonstrate understanding of a variety of written and / or visual German text(s) on familiar matters 9.30 am Monday 11 November 2013 Credits: Five
91126 911260 2SUPERVISOR S Level 2 German, 2013 91126 Demonstrate understanding of a variety of written and / or visual German text(s) on familiar matters 9.30 am Monday 11 November 2013 Credits: Five
VGM. VGM information. HAMBURG SÜD VGM WEB PORTAL - USER GUIDE June 2016
 Overview The Hamburg Süd VGM-Portal is an application which enables to submit VGM information directly to Hamburg Süd via our e-portal web page. You can choose to insert VGM information directly, or download
Overview The Hamburg Süd VGM-Portal is an application which enables to submit VGM information directly to Hamburg Süd via our e-portal web page. You can choose to insert VGM information directly, or download
Gliadin - IgG - ELISA
 Arbeitsanleitung Gliadin - IgG - ELISA Enzymimmunoassay zur quantitativen Bestimmung von IgG-Antikörpern gegen Gliadin in Serum und Plasma I V D REF EA509/96 12 x 8 2 8 C DLD Gesellschaft für Diagnostika
Arbeitsanleitung Gliadin - IgG - ELISA Enzymimmunoassay zur quantitativen Bestimmung von IgG-Antikörpern gegen Gliadin in Serum und Plasma I V D REF EA509/96 12 x 8 2 8 C DLD Gesellschaft für Diagnostika
Bedienungsanleitung Instruction Manual K 106/1 & 2
 Auf dem Knapp 46 Tel.: ++49 (0)2191/907-0 D-42855 Remscheid Fax: ++49 (0)2191/907-141 Bedienungsanleitung Instruction Manual K 106/1 & 2 WE.3347_C Version 1.c 7/01 Auf dem Knapp 46 Tel.: ++49 (0)2191/907-0
Auf dem Knapp 46 Tel.: ++49 (0)2191/907-0 D-42855 Remscheid Fax: ++49 (0)2191/907-141 Bedienungsanleitung Instruction Manual K 106/1 & 2 WE.3347_C Version 1.c 7/01 Auf dem Knapp 46 Tel.: ++49 (0)2191/907-0
Packungsbeilage. Trypsin ELISA IVD 01-10-200 MAIER. analytik. Löhergasse 1. 74889 Sinsheim. Germany
 MAIER analytik g m b h Packungsbeilage Trypsin ELISA IVD 01-10-200 MAIER analytik g m b h Löhergasse 1 74889 Sinsheim Germany Tel.: 07261/655053 Fax.: 07261/979912 e-mail: intelact@t-online.de http://www.maier-analytik.de
MAIER analytik g m b h Packungsbeilage Trypsin ELISA IVD 01-10-200 MAIER analytik g m b h Löhergasse 1 74889 Sinsheim Germany Tel.: 07261/655053 Fax.: 07261/979912 e-mail: intelact@t-online.de http://www.maier-analytik.de
Manual. SureFood FISH ID Gadus chalcogrammus IAAC (R&D Version) (50 Reakt.) Art. Nr. S6313. Beschreibung
 Manual Seiten 1 bis 3 Pages 4 to 6 SureFood FISH ID Gadus chalcogrammus IAAC (R&D Version) (50 Reakt.) Art. Nr. S6313 Beschreibung Mit diesem Test wird Alaska-Seelachs-DNA (Gadus chalcogrammus oder Theragra
Manual Seiten 1 bis 3 Pages 4 to 6 SureFood FISH ID Gadus chalcogrammus IAAC (R&D Version) (50 Reakt.) Art. Nr. S6313 Beschreibung Mit diesem Test wird Alaska-Seelachs-DNA (Gadus chalcogrammus oder Theragra
Immunglobulin E ELISA Kit
 Immunglobulin E ELISA Kit Zur in vitro Bestimmung des in Serum und Stuhl Immunoglobulin E ELISA Kit For the in vitro determination of in serum and stool Gültig ab/valid from 02.08.2010 +8 C K 6511 +2 C
Immunglobulin E ELISA Kit Zur in vitro Bestimmung des in Serum und Stuhl Immunoglobulin E ELISA Kit For the in vitro determination of in serum and stool Gültig ab/valid from 02.08.2010 +8 C K 6511 +2 C
RIDASCREEN Leishmania Ab
 RIDASCREEN Leishmania Ab Art. No.: K7121 R-Biopharm AG, An der neuen Bergstraße 17, D-64297 Darmstadt, Germany Tel.: +49 (0) 6151 8102-0 / Telefax: +49 (0) 6151 8102-20 1. Anwendungsbereich Für die in
RIDASCREEN Leishmania Ab Art. No.: K7121 R-Biopharm AG, An der neuen Bergstraße 17, D-64297 Darmstadt, Germany Tel.: +49 (0) 6151 8102-0 / Telefax: +49 (0) 6151 8102-20 1. Anwendungsbereich Für die in
IDK Helicobacter pylori Antigen ELISA Kit
 Arbeitsanleitung / Manual IDK Helicobacter pylori Antigen ELISA Kit Zur in-vitro-bestimmung von Helicobacter pylori in Stuhl For the in vitro determination of Helicobacter pylori in stool Gültig ab / Valid
Arbeitsanleitung / Manual IDK Helicobacter pylori Antigen ELISA Kit Zur in-vitro-bestimmung von Helicobacter pylori in Stuhl For the in vitro determination of Helicobacter pylori in stool Gültig ab / Valid
Insulin ELISA. Instructions for use LDN-ME E-0900
 Li StarFish S.r.l. Via Cavour, 35-20063 Cernusco S/N (MI), Italy Tel. +39-02-92150794 - Fax. +39-02-92157285 info@listarfish.it -www.listarfish.it Instructions for use Insulin ELISA LDN-ME E-0900 Insulin
Li StarFish S.r.l. Via Cavour, 35-20063 Cernusco S/N (MI), Italy Tel. +39-02-92150794 - Fax. +39-02-92157285 info@listarfish.it -www.listarfish.it Instructions for use Insulin ELISA LDN-ME E-0900 Insulin
Albumin ELISA Kit. Super sensitiv Zur in-vitro-bestimmung von Albumin in Urin und Stuhl
 Arbeitsanleitung / Manual Albumin ELISA Kit Super sensitiv Zur in-vitro-bestimmung von Albumin in Urin und Stuhl Super sensitive For the in vitro determination of albumin in urine and stool Gültig ab /
Arbeitsanleitung / Manual Albumin ELISA Kit Super sensitiv Zur in-vitro-bestimmung von Albumin in Urin und Stuhl Super sensitive For the in vitro determination of albumin in urine and stool Gültig ab /
- Characteristic sensitive Small temperature differences. - Low Sensitivity 42,8 µv/k for Cu-Constantan
 Thermocouples + Lightweight Small backlash by deformations + No self heating + Physically defined Zero No calibration for control loops - Characteristic sensitive Small temperature differences to cable
Thermocouples + Lightweight Small backlash by deformations + No self heating + Physically defined Zero No calibration for control loops - Characteristic sensitive Small temperature differences to cable
TSH-R-Ab ELISA Enzyme Immunoassay for the quantitative determination of thyrotropin receptor autoantibodies (TRAb) in human serum
 Product information Information about other products is available at: www.demeditec.com Userś Manual TSH-R-Ab ELISA Enzyme Immunoassay for the quantitative determination of thyrotropin receptor autoantibodies
Product information Information about other products is available at: www.demeditec.com Userś Manual TSH-R-Ab ELISA Enzyme Immunoassay for the quantitative determination of thyrotropin receptor autoantibodies
Zur in-vitro-bestimmung von Histamin in EDTA-Plasma und Urin. For the in vitro determination of histamine in EDTA plasma and urine
 Arbeitsanleitung / Manual Histamin ELISA Zur in-vitro-bestimmung von Histamin in EDTA-Plasma und Urin For the in vitro determination of histamine in EDTA plasma and urine Gültig ab / Valid from 2017-01-10
Arbeitsanleitung / Manual Histamin ELISA Zur in-vitro-bestimmung von Histamin in EDTA-Plasma und Urin For the in vitro determination of histamine in EDTA plasma and urine Gültig ab / Valid from 2017-01-10
VGM. VGM information. HAMBURG SÜD VGM WEB PORTAL USER GUIDE June 2016
 Overview The Hamburg Süd VGM Web portal is an application that enables you to submit VGM information directly to Hamburg Süd via our e-portal Web page. You can choose to enter VGM information directly,
Overview The Hamburg Süd VGM Web portal is an application that enables you to submit VGM information directly to Hamburg Süd via our e-portal Web page. You can choose to enter VGM information directly,
TEST REPORT. 4. Identification no. of the product: 03FK10 03FK11 03FK16 03FK13 5. Manufacturer: Standard Diagnostics, Inc.
 Prüflabor für In-vitro-Diagnostika beim Paul-Ehrlich-Institut (PEI-IVD) Paul-Ehrlich-Straße 51-59 D-63225 Langen TEST REPORT 1. Test report no. (B.-Nr.): 0253/12 2. Customer: The Global Fund to Fight AIDS,
Prüflabor für In-vitro-Diagnostika beim Paul-Ehrlich-Institut (PEI-IVD) Paul-Ehrlich-Straße 51-59 D-63225 Langen TEST REPORT 1. Test report no. (B.-Nr.): 0253/12 2. Customer: The Global Fund to Fight AIDS,
Die Dokumentation kann auf einem angeschlossenen Sartorius Messwertdrucker erfolgen.
 Q-App: USP V2 Bestimmung des Arbeitsbereiches von Waagen gem. USP Kapitel 41. Determination of the operating range of balances acc. USP Chapter 41. Beschreibung Diese Q-App ist zur Bestimmung des Arbeitsbereiches
Q-App: USP V2 Bestimmung des Arbeitsbereiches von Waagen gem. USP Kapitel 41. Determination of the operating range of balances acc. USP Chapter 41. Beschreibung Diese Q-App ist zur Bestimmung des Arbeitsbereiches
RIDASCREEN FAST Ei / Egg Protein
 RIDASCREEN FAST Ei / Egg Protein Enzymimmunoassay zur quantitativen Bestimmung von Volleipulver Enzyme immunoassay for the quantitative analysis of whole egg powder Art. No.: R6402 In vitro Test Lagerung
RIDASCREEN FAST Ei / Egg Protein Enzymimmunoassay zur quantitativen Bestimmung von Volleipulver Enzyme immunoassay for the quantitative analysis of whole egg powder Art. No.: R6402 In vitro Test Lagerung
Enzymimmunoassay zur quantitativen Bestimmung von Haptoglobin (Schwein) Enzyme immunoassay for the quantitative analysis of Haptoglobin (pigs)
 RIDASCREEN Haptoglobin Enzymimmunoassay zur quantitativen Bestimmung von Haptoglobin (Schwein) Enzyme immunoassay for the quantitative analysis of Haptoglobin (pigs) Art. No.: R7501 In vitro Test Lagerung
RIDASCREEN Haptoglobin Enzymimmunoassay zur quantitativen Bestimmung von Haptoglobin (Schwein) Enzyme immunoassay for the quantitative analysis of Haptoglobin (pigs) Art. No.: R7501 In vitro Test Lagerung
Hazards and measures against hazards by implementation of safe pneumatic circuits
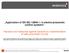 Application of EN ISO 13849-1 in electro-pneumatic control systems Hazards and measures against hazards by implementation of safe pneumatic circuits These examples of switching circuits are offered free
Application of EN ISO 13849-1 in electro-pneumatic control systems Hazards and measures against hazards by implementation of safe pneumatic circuits These examples of switching circuits are offered free
Mitglied der Leibniz-Gemeinschaft
 Methods of research into dictionary use: online questionnaires Annette Klosa (Institut für Deutsche Sprache, Mannheim) 5. Arbeitstreffen Netzwerk Internetlexikografie, Leiden, 25./26. März 2013 Content
Methods of research into dictionary use: online questionnaires Annette Klosa (Institut für Deutsche Sprache, Mannheim) 5. Arbeitstreffen Netzwerk Internetlexikografie, Leiden, 25./26. März 2013 Content
ReadMe zur Installation der BRICKware for Windows, Version 6.1.2. ReadMe on Installing BRICKware for Windows, Version 6.1.2
 ReadMe zur Installation der BRICKware for Windows, Version 6.1.2 Seiten 2-4 ReadMe on Installing BRICKware for Windows, Version 6.1.2 Pages 5/6 BRICKware for Windows ReadMe 1 1 BRICKware for Windows, Version
ReadMe zur Installation der BRICKware for Windows, Version 6.1.2 Seiten 2-4 ReadMe on Installing BRICKware for Windows, Version 6.1.2 Pages 5/6 BRICKware for Windows ReadMe 1 1 BRICKware for Windows, Version
LD BioScreen. Low Density Biochip Schnelltest-Systeme. Offenes System für Sandwich-Immunoassays. LD BioScreen
 LD BioScreen Low Density Biochip Schnelltest-Systeme Offenes System für Sandwich-Immunoassays LD BioScreen Die Alternative zur Mikrotiterplatte Für Assays im Forschungslabor Sie sparen Material, Zeit und
LD BioScreen Low Density Biochip Schnelltest-Systeme Offenes System für Sandwich-Immunoassays LD BioScreen Die Alternative zur Mikrotiterplatte Für Assays im Forschungslabor Sie sparen Material, Zeit und
Ingenics Project Portal
 Version: 00; Status: E Seite: 1/6 This document is drawn to show the functions of the project portal developed by Ingenics AG. To use the portal enter the following URL in your Browser: https://projectportal.ingenics.de
Version: 00; Status: E Seite: 1/6 This document is drawn to show the functions of the project portal developed by Ingenics AG. To use the portal enter the following URL in your Browser: https://projectportal.ingenics.de
Network premium POP UP Display
 Premium Pop Up System seamless graphic precision very compact and versatile pop-up system quick to set up at any location comes in a number of different shapes; straight, curved, wave-shaped, stair formations,
Premium Pop Up System seamless graphic precision very compact and versatile pop-up system quick to set up at any location comes in a number of different shapes; straight, curved, wave-shaped, stair formations,
TNFα-Blocker-ADA, Antikörper gegen Infliximab (z. B. REMICADE ) TNFα blocker ADA, antibodies against infliximab (e. g. REMICADE )
 Arbeitsanleitung / Manual TNFα-Blocker-ADA, Antikörper gegen Infliximab (z. B. REMICADE ) Zur in-vitro-bestimmung von freien humanen Antikörpern gegen Infliximab (z.b. REMICADE ) in EDTA-Plasma und Serum
Arbeitsanleitung / Manual TNFα-Blocker-ADA, Antikörper gegen Infliximab (z. B. REMICADE ) Zur in-vitro-bestimmung von freien humanen Antikörpern gegen Infliximab (z.b. REMICADE ) in EDTA-Plasma und Serum
RS232-Verbindung, RXU10 Herstellen einer RS232-Verbindung zwischen PC und Messgerät oder Modem und Messgerät
 Betriebsanleitung RS232-Verbindung, RXU10 Herstellen einer RS232-Verbindung zwischen PC und Messgerät oder Modem und Messgerät ä 2 Operating Instructions RS232 Connection, RXU10 Setting up an RS232 connection
Betriebsanleitung RS232-Verbindung, RXU10 Herstellen einer RS232-Verbindung zwischen PC und Messgerät oder Modem und Messgerät ä 2 Operating Instructions RS232 Connection, RXU10 Setting up an RS232 connection
Bedienungsanleitung Instruction Manual K103/1 WE.3221_F 7/03. Bedienungsanleitung Instruction Manual K103/1
 Bedienungsanleitung Instruction Manual K103/1 WE.3221_F 7/03 Bedienungsanleitung Instruction Manual K103/1 WE.3221_F 7/03 Bedienungsanleitung/Instruction Manual K103/1 Seite/page 2 Abb./Picture 1 bewegliches
Bedienungsanleitung Instruction Manual K103/1 WE.3221_F 7/03 Bedienungsanleitung Instruction Manual K103/1 WE.3221_F 7/03 Bedienungsanleitung/Instruction Manual K103/1 Seite/page 2 Abb./Picture 1 bewegliches
IDKmonitor Infliximab free ADA ELISA
 Arbeitsanleitung / Manual IDKmonitor Infliximab free ADA ELISA Zur in-vitro-bestimmung von freien humanen Antikörpern gegen Infliximab (z. B. REMICADE ) in EDTA-Plasma und Serum For the in vitro determination
Arbeitsanleitung / Manual IDKmonitor Infliximab free ADA ELISA Zur in-vitro-bestimmung von freien humanen Antikörpern gegen Infliximab (z. B. REMICADE ) in EDTA-Plasma und Serum For the in vitro determination
4M Economy INSTRUCTION MANUAL
 4M Economy INSTRUCTION MANUAL Part List Part no. Qty 4x4m 4x6m 4x8m 4x10m No.1 6 8 10 12 No.2 6 9 12 15 No.3 6 8 10 12 No.4 6 6 6 6 No.5 3 6 9 12 No.6 56 64 72 80 No.7 30 42 54 66 Nr.8 4 4 4 4 No.9 4 4
4M Economy INSTRUCTION MANUAL Part List Part no. Qty 4x4m 4x6m 4x8m 4x10m No.1 6 8 10 12 No.2 6 9 12 15 No.3 6 8 10 12 No.4 6 6 6 6 No.5 3 6 9 12 No.6 56 64 72 80 No.7 30 42 54 66 Nr.8 4 4 4 4 No.9 4 4
Calprotectin ELISA Kit. Calprotectin ELISA Kit. Zur in vitro Bestimmung von Calprotectin (MRP 8/14) in Stuhl
 Calprotectin ELISA Kit Zur in vitro Bestimmung von Calprotectin (MRP 8/14) in Stuhl Calprotectin ELISA Kit For the in vitro determination of Calprotectin (MRP 8/14) in stool Gültig ab / valid from 06.09.2005
Calprotectin ELISA Kit Zur in vitro Bestimmung von Calprotectin (MRP 8/14) in Stuhl Calprotectin ELISA Kit For the in vitro determination of Calprotectin (MRP 8/14) in stool Gültig ab / valid from 06.09.2005
Level 1 German, 2016
 90886 908860 1SUPERVISOR S Level 1 German, 2016 90886 Demonstrate understanding of a variety of German texts on areas of most immediate relevance 2.00 p.m. Wednesday 23 November 2016 Credits: Five Achievement
90886 908860 1SUPERVISOR S Level 1 German, 2016 90886 Demonstrate understanding of a variety of German texts on areas of most immediate relevance 2.00 p.m. Wednesday 23 November 2016 Credits: Five Achievement
Öl-Messstäbe Mercedes Benz
 Öl-Messstäbe Mercedes Benz Art. 1010 Anleitung und Vergleichsliste für Ölstandsmessung Messen der Ölstände bei Mercedes Fahrzeugen die ohne Ölmessstäbe ausgelieferte werden. Mercedes Getriebecode 716.5,
Öl-Messstäbe Mercedes Benz Art. 1010 Anleitung und Vergleichsliste für Ölstandsmessung Messen der Ölstände bei Mercedes Fahrzeugen die ohne Ölmessstäbe ausgelieferte werden. Mercedes Getriebecode 716.5,
FLACHSICHERUNGSDOSEN BLADE FUSE BOXES
 FLACHSICHERUNGSDOSEN ES Flachsicherungsdosen 15 00 00 und Varianten Die Flachsicherungsdosen und Zentralstecker gibt es in zwei-, vier-, sechs- und achtpoliger Ausführung und in den Farben schwarz, natur,
FLACHSICHERUNGSDOSEN ES Flachsicherungsdosen 15 00 00 und Varianten Die Flachsicherungsdosen und Zentralstecker gibt es in zwei-, vier-, sechs- und achtpoliger Ausführung und in den Farben schwarz, natur,
Das ist gut für die Gesundheit
 Exercise A: Label each picture in German. Exercise B: Complete the table with the English meanings. das ist weil das ist nicht da ist denn sind der Körper gut das Herz schlecht die Leber für die Haut ich
Exercise A: Label each picture in German. Exercise B: Complete the table with the English meanings. das ist weil das ist nicht da ist denn sind der Körper gut das Herz schlecht die Leber für die Haut ich
Guidelines for the efficient preparing for your colonoscopy
 Guidelines for the efficient preparing for your colonoscopy Information, Instructions and answers to your questions Dear patient, You`ve been scheduled for a colonoscopy in our clinic. For the success
Guidelines for the efficient preparing for your colonoscopy Information, Instructions and answers to your questions Dear patient, You`ve been scheduled for a colonoscopy in our clinic. For the success
Androstenedione ELISA
 Instructions for use Androstenedione ELISA AA E-1000 Androstenedione ELISA English INTRODUCTION Intended Use The Androstenedione ELISA is an enzyme immunoassay for the quantitative in vitro diagnostic
Instructions for use Androstenedione ELISA AA E-1000 Androstenedione ELISA English INTRODUCTION Intended Use The Androstenedione ELISA is an enzyme immunoassay for the quantitative in vitro diagnostic
Umschaltadapter/ Changeover / Trennadapter Disconnection Adapter für LSA-PLUS NT for LSA-PLUS NT. Montageanweisung Mounting Instructions
 Umschaltadapter/ Changeover / Trennadapter Disconnection Adapter für LSA-PLUS NT for LSA-PLUS NT Montageanweisung Mounting Instructions Der Umschalter dient zum unterbrechungsfreien Umschalten von Installations-drähten
Umschaltadapter/ Changeover / Trennadapter Disconnection Adapter für LSA-PLUS NT for LSA-PLUS NT Montageanweisung Mounting Instructions Der Umschalter dient zum unterbrechungsfreien Umschalten von Installations-drähten
Titelbild1 ANSYS. Customer Portal LogIn
 Titelbild1 ANSYS Customer Portal LogIn 1 Neuanmeldung Neuanmeldung: Bitte Not yet a member anklicken Adressen-Check Adressdaten eintragen Customer No. ist hier bereits erforderlich HERE - Button Hier nochmal
Titelbild1 ANSYS Customer Portal LogIn 1 Neuanmeldung Neuanmeldung: Bitte Not yet a member anklicken Adressen-Check Adressdaten eintragen Customer No. ist hier bereits erforderlich HERE - Button Hier nochmal
HybriScan I Pediococcus damnosus
 HybriScan I Pediococcus damnosus Molekularbiologisches Schnelltestsystem zur Identifizierung von Pediococcus damnosus Produkt-Nr.: 67289 Kontaktinformationen: HybriScan - Schnelltestsystem (F&E) Dr. Helmut
HybriScan I Pediococcus damnosus Molekularbiologisches Schnelltestsystem zur Identifizierung von Pediococcus damnosus Produkt-Nr.: 67289 Kontaktinformationen: HybriScan - Schnelltestsystem (F&E) Dr. Helmut
flocktype Mycoplasma Mg/Ms Ab Gebrauchsinformation
 Februar 2015 flocktype Mycoplasma Mg/Ms Ab Gebrauchsinformation 5 (Katalog-Nr. 274803) Zum Nachweis von Antikörpern gegen Mycoplasma gallisepticum und Mycoplasma synoviae 20 (Katalog-Nr. 274805) 274803,
Februar 2015 flocktype Mycoplasma Mg/Ms Ab Gebrauchsinformation 5 (Katalog-Nr. 274803) Zum Nachweis von Antikörpern gegen Mycoplasma gallisepticum und Mycoplasma synoviae 20 (Katalog-Nr. 274805) 274803,
Gebrauchsanleitung Histamin Elisa BA E - 1000
 Gebrauchsanleitung Elisa BA E - 1000 ELISA 1. Verwendungszweck und Testprinzip Enzymimmunoassay zur quantitativen Bestimmung von in Plasma und Urin In Kombination mit dem Zusatzkit e Release ELISA ( BA
Gebrauchsanleitung Elisa BA E - 1000 ELISA 1. Verwendungszweck und Testprinzip Enzymimmunoassay zur quantitativen Bestimmung von in Plasma und Urin In Kombination mit dem Zusatzkit e Release ELISA ( BA
Interleukin-12 (p70) ELISA
 Instructions for Use Interleukin-12 (p70) ELISA Enzyme immunoassay for the quantitative determination of human Interleukin-12(p70) in human serum, plasma and cell culture supernatants. BE53121 96 2-8 C
Instructions for Use Interleukin-12 (p70) ELISA Enzyme immunoassay for the quantitative determination of human Interleukin-12(p70) in human serum, plasma and cell culture supernatants. BE53121 96 2-8 C
Level 1 German, 2012
 90886 908860 1SUPERVISOR S Level 1 German, 2012 90886 Demonstrate understanding of a variety of German texts on areas of most immediate relevance 9.30 am Tuesday 13 November 2012 Credits: Five Achievement
90886 908860 1SUPERVISOR S Level 1 German, 2012 90886 Demonstrate understanding of a variety of German texts on areas of most immediate relevance 9.30 am Tuesday 13 November 2012 Credits: Five Achievement
PONS DIE DREI??? FRAGEZEICHEN, ARCTIC ADVENTURE: ENGLISCH LERNEN MIT JUSTUS, PETER UND BOB
 Read Online and Download Ebook PONS DIE DREI??? FRAGEZEICHEN, ARCTIC ADVENTURE: ENGLISCH LERNEN MIT JUSTUS, PETER UND BOB DOWNLOAD EBOOK : PONS DIE DREI??? FRAGEZEICHEN, ARCTIC ADVENTURE: Click link bellow
Read Online and Download Ebook PONS DIE DREI??? FRAGEZEICHEN, ARCTIC ADVENTURE: ENGLISCH LERNEN MIT JUSTUS, PETER UND BOB DOWNLOAD EBOOK : PONS DIE DREI??? FRAGEZEICHEN, ARCTIC ADVENTURE: Click link bellow
