IMPP. GEGENSTANDSKATALOG für den schriftlichen Teil der ÄRZTLICHEN VORPRÜFUNG (GK 1) Teilkatalog "CHEMIE FÜR MEDIZINER UND BIOCHEMIE
|
|
|
- Tobias Keller
- vor 8 Jahren
- Abrufe
Transkript
1 IMPP Institut für medizinische und pharmazeutische Prüfungsfragen Rechtsfähige Anstalt des öffentlichen Rechts GEGENSTANDSKATALOG für den schriftlichen Teil der ÄRZTLICHEN VORPRÜFUNG (GK 1) Teilkatalog "CHEMIE FÜR MEDIZINER UND BIOCHEMIE 4. Auflage Januar 2001
2 Institut für medizinische und pharmazeutische Prüfungsfragen Postfach 2528, Mainz
3 Die Neuauflage des Gegenstandskatalogs (GK) für den schriftlichen Teil der Ärztlichen Vorprüfung war seit langem überfällig. Die Aktualisierung wurde wiederholt zurückgestellt, weil eine Reform der Approbationsordnung für Ärzte (ÄAppO) mit veränderten Anforderungen an Struktur und Inhalte der GK mehrfach unmittelbar bevorzustehen schien. Weiteres Zuwarten war nun nicht länger vertretbar, weil einerseits die wissenschaftlichen Fortschritte, aber auch veränderte inhaltliche Akzente in manchen Stoffgebieten sich nun auch im GK wiederfinden sollen. Zur Funktion des Katalogs ist klarzustellen, dass Grundlage für den schriftlichen Teil der Ärztlichen Vorprüfung allein der in der jeweils gültigen Approbationsordnung für Ärzte festgelegte Prüfungsstoff (vgl. Anlage 10 zur ÄAppO) ist. Der GK ist als Erläuterung und Konkretisierung der dort in allgemeiner Form festgelegten Prüfungsthemen zu verstehen. Er ist damit als Hilfestellung sowohl bei der Prüfungsvorbereitung als auch bei der Gestaltung von Ausbildungsinhalten anzusehen und dient selbstverständlich auch als Richtschnur bei der Auswahl der Prüfungsthemen. Die Herleitung der Stoffsammlung aus den Bestimmungen der derzeit gültigen ÄAppO wirkt sich in mehrfacher Weise auf Struktur und Inhalte des Katalogs aus. So konnten sich Konzepte einer horizontalen Integration nicht in der vielfach gewünschten Weise niederschlagen, denn die ÄAppO sieht (noch?) fächerorientierte Prüfungen vor. Auch Ansätze zu einer vertikalen Integration, die der vorliegende Entwurf für eine Reform der ÄAppO durch eine teilweise Neugestaltung des ersten Prüfungsabschnittes in Aussicht stellt, können sich in diesem GK nur zu einem geringen Teil abbilden. Teilweise wurde die Hoffnung zum Ausdruck gebracht, der GK könne die humanbiologischen Grundlagen der Medizin ganzheitlich und gestützt auf eine oder wenige mächtige Theorien beschreiben. Dass ein solches Anliegen nicht nur von hohem intellektuellem Reiz wäre, sondern auch wichtige didaktische Perspektiven eröffnen könnte, ist unbestritten. Da der GK jedoch als pragmatisches Werkzeug für die berufszugangsregelnden schriftlichen Prüfungen nach ÄAppO verstanden werden muss, sieht er sich durch solche anspruchsvollen Erwartungen wenigstens derzeit noch überfordert. Erstmals wurde der Katalog durch eine vierte (rechte) Spalte ergänzt. Sie enthält stichwortartig Anwendungsbeispiele, mit denen der in Spalte 3 detaillierte Prüfungsstoff in Beziehung steht. Es kann sich hierbei im engeren Sinn um Bezüge handeln, die hohe klinische Relevanz besitzen oder denen wegen ihres Modellcharakters besonderer didaktischer Wert zukommt. Die rechte Spalte folgt weder einer eigenen Systematik, noch wird Vollständigkeit angestrebt. Stattdessen könnte sie als Anregung dafür dienen, noch mehr als bisher über sinnvolle Schnittstellen zwischen den grundlagenwissenschaftlichen und späteren Ausbildungsabschnitten nachzudenken. Ein Eintrag in der rechten Spalte erweitert also nicht den Prüfungsstoff des entsprechenden Items. Der Sachverhalt kann aber an anderer Stelle in einem der Teile des GK für den schriftlichen Teil der Ärztlichen Vorprüfung in den vorderen Spalten aufgeführt sein und somit beim dortigen Item zum Prüfungsstoff gehören. Um jeglichem Missverständnis vorzubeugen, sei daher wiederholt: Der in Betracht kommende Prüfungsstoff findet sich in den Spalten eins bis drei. Dessen ungeachtet können besonders wichtige Entwicklungen, wie sie in der lebendigen Wissenschaft ständig vor sich gehen, auch dann schon Prüfungsstoff sein, wenn sie dem Prüfungsstoffkatalog der Approbationsordnung für Ärzte zuzuordnen sind, im GK aber noch nicht aufgeführt werden. Im Sinne einer angemessenen Übergangszeit wird beim schriftlichen Teil der Ärztlichen Vorprüfung bis einschließlich Frühjahr 2002 noch der GK in der Fassung der 3. Auflage berücksichtigt. An dieser Stelle möchten wir uns sehr herzlich bei allen Hochschullehrerinnen und Hochschullehrern bedanken, die (auch durch ihre Bereitschaft, nicht durchweg schmerzlose Kompromisse zu schließen) zum Gelingen dieses GK beigetragen haben.
4 Chemie für Mediziner und Biochemie (Inhaltsübersicht) GRUNDLAGEN DER CHEMIE 1.1 Makroskopische Erscheinungsformen der Materie 2 Aufbau und Eigenschaften der Materie 2.1 Atome, Isotope, Periodensystem 2.2 Chemische Bindung 2.3 Acyclische Kohlenstoffverbindungen, einfache funktionelle Gruppen 2.4 Carbo- und Heterocyclen 2.5 Stereochemie 3 Stoffumwandlungen 3.1 Homogene Gleichgewichtsreaktionen 3.2 Heterogene Gleichgewichtsreaktionen 3.3 Säure/Base-Reaktionen 3.4 Redox-Reaktionen 3.5 Bildung und Eigenschaften der Salze 3.6 Ligandenaustausch-Reaktionen 3.7 Additions/Eliminierungs-Reaktionen 3.8 Substitutionsreaktionen 3.9 Sonstige Reaktionen CHEMIE BIOLOGISCH UND MEDIZINISCH RELEVANTER NATURSTOFFE 4 Kohlenhydrate 4.1 Monosaccharide 4.2 Disaccharide 4.3 Oligo- und Polysaccharide 5 Aminosäuren, Peptide, Proteine 5.1 Aminosäuren 5.2 Peptide 5.3 Proteine 6 Fettsäuren, Lipide 6.1 Fettsäuren 6.2 Acylglycerine 6.3 Sphingolipide 6.4 Steroide 7 Nukleotide, Nukleinsäuren, Chromatin 7.1 Nukleotide 7.2 Nukleinsäuren 7.3 Chromatin 8 Vitamine, Vitaminderivate, Coenzyme 8.1 Allgemeines 8.2 Biochemischer Mechanismus 8.3 Pathobiochemie 9 Grundlagen der Thermodynamik und Kinetik 9.1 Grundbegriffe der Energetik und Kinetik FUNKTIONELLE BIOCHEMIE 10 Bioenergetik und Biokatalyse 10.1 Energetik und Kinetik biochemischer Reaktionen 11 Prinzipien der Stoffwechselregulation 12 Kataboler Stoffwechsel und Energiegewinnung 12.1 "Energiereiche" Verbindungen 12.2 Kohlenhydratabbau 12.3 Triacylglycerin- und Fettsäureabbau 12.4 Ketonkörpersynthese und -abbau 12.5 Protein- und Aminosäureabbau 12.6 Ethanolabbau
5 12.7 Pyruvat-Dehydrogenase, Citratzyklus 12.8 Atmungskette und oxidative Phosphorylierung 12.9 Pathobiochemie 13 Bildung von Energiespeichern 13.1 Kohlenhydrate 13.2 Lipide 13.3 Proteine 13.4 Regulation der Energiespeicherbildung und -verwertung 13.5 Pathobiochemie MOLEKULARBIOLOGIE UND ZELLBIOLOGIE 14 Speicherung, Übertragung und Expression genetischer Information 14.1 Nukleotide 14.2 Nukleinsäuren 14.3 Faltung und Modifikation von Proteinen 14.4 Proteolyse 14.5 Tumorbiochemie 15 Zellstrukturen und interzelluläre Matrix; allgemeine Zytologie 15.1 Prokaryonte Zellen 15.2 Eukaryonte Zellen 15.3 Membranen 15.4 Zellkern 15.5 Mitochondrien 15.6 Lysosomen 15.7 Peroxisomen 15.8 Endoplasmatisches Retikulum (ER) 15.9 Golgi-Apparat Zytoskelett Extrazelluläre Matrix Zellzyklus Apoptose Pathobiochemie 16 Säure-Basenhaushalt, Wasser- und Elektrolythaushalt, Spurenelemente 16.1 Säure-Basen-Haushalt 16.2 Wasser- und Elektrolyt-Haushalt 16.3 Spurenelemente 16.4 Pathobiochemie 17 Bewegung 17.1 Kontraktile Systeme 17.2 Motile Systeme 17.3 Pathobiochemie 18 Hormone und Zytokine 18.1 Grundlagen 18.2 Stoffwechselregulation 18.3 Wachstum und Differenzierung, Fortpflanzung 18.4 Regulation von Verdauung und Resorption 18.5 Elektrolyt- und Wasserhaushalt 18.6 Calcium- und Phosphatstoffwechsel 18.7 Gewebshormone, Mediatoren 18.8 Zytokine 18.9 Pathobiochemie BIOCHEMIE VON ORGANEN UND GEWEBEN 19 Immunsystem 19.2 Störungen des Immunsystems
6 20 Blut 20.1 Erythropoiese und Erythrozyten 20.2 Pathobiochemie 20.3 Lymphozyten 20.4 Blutstillung, Blutgerinnung und Fibrinolyse 20.5 Pathobiochemie 20.6 Blutplasma 21 Leber 21.1 Energiestoffwechsel 21.2 Serviceleistungen 21.3 Cholesterin 21.4 Gallenflüssigkeit und Gallensäuren 21.5 Biotransformation 21.6 Endokrine Funktionen 22 Magen-Darm-Trakt 22.1 Grundlagen der Ernährung 22.2 Verdauung und Resorption 22.3 Wasser, Elektrolyte 22.4 Endokrine Funktionen 22.5 Pathobiochemie 23 Fettgewebe 23.1 Stoffwechselleistungen 23.2 Endokrine Funktion 24 Niere 24.1 Energiestoffwechsel 24.2 Endokrine Funktionen 24.3 Grundlagen der Harnbildung 24.4 Rückresorption 24.5 Ausscheidung von Säuren und Ammoniak 25 Muskulatur 25.1 Energiestoffwechsel 25.2 Kontraktion, Relaxation 25.3 Endokrine Funktionen 25.4 Pathobiochemie 26 Stützgewebe 26.1 Aufbau von Knorpel, Knochen, Zahnhartsubstanz 26.2 Extrazelluäre Matrix 26.3 Knorpelgewebe 26.4 Knochen, Zahnhartsubstanz 27 Nervensystem 27.1 Energiestoffwechsel 27.2 Liquor cerebrospinalis 27.3 Myelin 27.4 Erregungsleitung und -übertragung 28 Auge
7 CHEMIE FÜR MEDIZINER UND BIOCHEMIE Grundlagen der Chemie 1.1 Makroskopische Erscheinungsformen der Materie Aggregatzustände, Phasenumwandlungen 2 Aufbau und Eigenschaften der Materie 2.1 Atome, Isotope, Periodensystem Begriffe Elementarteilchen, Ordnungszahl, Kernladungszahl, Massenzahl, Elektronenhülle Ordnungszahl, Kernladungszahl, Massenzahl Identifizierung von Ordnungszahl, Kernladungszahl und Massenzahl an entsprechend gekennzeichneten Elementsymbolen Isotope Beispiele für stabile Isotope und Radio Elemente, Moleküle Periodensystem biochemisch wichtige Elemente 2.2 Chemische Bindung Ionenbindung, Atombindung Polarität von Molekülen isotope mit medizinischer Relevanz Element: Zuordnung von Name und Symbol biochemisch und medizinisch wichtiger Elemente, Molekül: relative Atom- und Molekülmasse, Avogadro-Konstante, Stoffmenge mol Ordnungsprinzipien des Periodensystems (Perioden 1 bis 7, Gruppen 1 bis 18), Einordnung biochemisch und medizinisch wichtiger Haupt- und Nebengruppenelemente, periodische Eigenschaften (z.b. Elektronegativität) Zuordnung von Elementen zu wichtigen Enzymen, Coenzymen und anderen biochemischen Verbindungen Ion, Ionen-Bindung; kovalente Bindung, koordinative Bindung, bindende und freie Elektronenpaare, Elektronegativität Dipolmoment von Molekülen, Assoziation durch H-Brücken und hydrophobe Wechselwirkungen, Beeinflussung physikalischer Eigenschaften durch H-Brücken sowie Hydratation von Ionen und Molekülen Beispiele Bindungsverhältnisse und Molekülformen bei den Grundelementen anhand einfacher Beispiele (C: Methan; H: H 2 ; O: Wasser, O 2, O 3, H 2 O 2 ; N: Ammoniak, N 2, Lachgas, NO, Cyanid), biochemisch relevante Sauerstoffradikale Begriffe, Definitionen und Zusammenhänge, die für das Verständnis des Aufbaus und der Eigenschaften biochemisch und medizinisch wichtiger Verbindungen sowie für die Beschreibung von Stoffumwandlungen im Stoffwechsel notwendig sind.
8 2.2.4 biochemisch wichtige Bindungen Metallkomplexe Erkennen biochemisch wichtiger Bindungen anhand einfacher Beispiele (keine Molekülorbital(MO)-Theorie), Unterschiede in den Bindungsenergien, Bindigkeit von H, C, O, N, S, Cl, P Aufbau von Metallkomplexen, Gesamtladung, Koordinationszahl von biochemisch wichtigen Metallionen in Metallkomplexen (Mg, Fe, Co, Zn, Cu), Chelatkomplexe, Erkennen von Chelatkomplexen bei Vorgabe biochemisch und medizinisch wichtiger Metallkomplexe 2.3 Acyclische Kohlenstoffverbindungen, einfache funktionelle Gruppen Kohlenwasserstoffe Unterscheidung gesättigte und ungesättigte Kohlenwasserstoffe, Alkylreste Formeln Definitionen: Summen- und Strukturformel Bindungen σ- und π-bindungen, konjugierte Doppelbindungen Isomerien Definition der Konstitution und der Konstitutionsisomerie (mit Beispielen) funktionelle Gruppen Struktur und Erkennen der funktionellen Gruppe bei Halogenalkanen, Alkoholen, Ethern, Thiolen, Thioethern (Sulfanen), Aminen, Aldehyden, Ketonen, Carbonsäuren und Carbonsäurederivaten, Carboxylatanion, Mesomerie homologe Definition Reihen Nomenklatur Nomenklatur bis maximal C 4, bei den Carbonsäuren auch C 16 /C 18 (ohne und mit Doppelbindungen) physikalische Eigenschaften 2.4 Carbo- und Heterocyclen Cycloalkane, Aromaten wichtige physikalische Eigenschaften im Vergleich (Siedepunkt, Löslichkeit in Wasser oder Kohlenwasserstoffen) Struktur, Summenformel und Molekülform von Cycloalkanen (C 5, C 6 ) und Aromaten (Benzol, Naphthalin) Heterocyclen nicht-aromatische und aromatische Heterocyclen mit O, N oder S (5- und 6-gliedrig): Erkennen von Pyrrol, Imidazol, Pyridin, Pyrimidin, Purin, Thiazol, Furan, Pyran in vorgegebenen Verbindungen 2.5 Stereochemie Konfiguration Definition der Konfiguration (mit einfachen Beispielen), Raumformeln
9 2.5.2 Stereoisomerie Stereoisomerie: Erkennen von Chiralitätszentren und cis/trans-isomerie in vorgegebenen Verbindungen, Prinzipien der R/S-Nomenklatur an einfachen Beispielen, Bestimmung der Anzahl möglicher Stereoisomere Enantiomere, Diastereomere Fischer-Projektion, D/L- Nomenklatur Definition, Beispiele, physikalische (optische Aktivität), chemische und pharmakologische Effekte der Enantio- und Diastereomerie bei α-hydroxysäuren, α-aminosäuren und Kohlenhydraten Konformation Definition, Beispiele: lineare Kohlenwasserstoffe und Cyclohexan/Steroide 3 Stoffumwandlungen 3.1 Homogene Gleichgewichtsreaktionen chemisches Gleichgewicht Kinetik, Thermodynamik gekoppelte Reaktionen Formulierung von Gleichgewichtsreaktionen: Massenwirkungsgesetz, Gleichgewichtskonstante K, Beeinflussung der Gleichgewichtslage kinetische und thermodynamische Aspekte von Gleichgewichtsreaktionen gekoppelte Reaktionen, Gesamtreaktionsgleichung, Gesamtgleichgewichtslage 3.2 Heterogene Gleichgewichtsreaktionen Begriffe Definition der Begriffe gesättigte Lösung, Suspension, Emulsion, Aerosol Verteilung Verteilung zwischen verschiedenen Phasen: Henry-Dalton sches Gesetz, Nernst scher Verteilungssatz Oberflächenprozesse Vorgänge an Oberflächen und Membranen: Adsorption, Osmose, Dialyse Abhängigkeit der Gleichgewichtslage von Temperatur, Art und Konzentration der Stoffe, Donnan-Gleichgewicht 3.3 Säure/Base-Reaktionen Definition von Brönsted-Säuren/Basen dissoziationsabhängige Größen ph-, pk s - und pk b -Werte, starke und schwache Säuren und Basen, Messung von ph-werten, Titrationskurven Beispiele, Anwendung Dissoziation von Schwefelsäure, Chlorwasserstoff, Kohlensäure, Phosphorsäure, Zitronensäure, Natriumhydroxid und Ammoniak in Wasser, Reaktionsgleichungen, konjugierte Säure/Base-Paare, Ampholyte
10 3.3.4 Neutralisation, Puffer Neutralisation, ph-werte von Salzlösungen, Pufferlösungen, ph-optimum, Puffergleichung des Phosphatpuffers (ph=7,2) und des Hydrogencarbonat/CO 2 -Puffers, Pufferkapazität Definition Lewis-Säuren /Basen 3.4 Redox-Reaktionen Definitionen Definition der Redox-Reaktion: Elektronenabgabe/Elektronenaufnahme, Oxidationsmittel/Reduktionsmittel, oxidiertes/reduziertes Produkt, Dehydrierung/Hydrierung einfache Reaktionsgleichungen elektrochemische Zellen Redox-Reaktionen biochemische Redoxreaktionen Erkennen von Redox-Reaktionen und Ergänzung einfacher Gleichungen, Aufstellen von Gleichungen unter Verwendung einfacher Oxidations- und Reduktionsmittel Beschreibung einfacher elektrochemischer Zellen, Elektrodenpotential, Normalwasserstoffelektrode, Spannungsreihe, Nernst sche Gleichung Knallgas-Reaktion, ph-abhängigkeit des Redox-Potentials, Energiebilanz, Atmungskette (s. 12.8) biologisch relevante Redoxreaktionen von Kohlenstoffverbindungen: Alkohole/Aldehyde/Carbonsäuren, Alkohole/Ketone, Hydrochinon/Chinon, Alkan/Alken, Thiole/Disulfide 3.5 Bildung und Eigenschaften der Salze Bildung Bildung aus den Elementen (einfache Beispiele) und durch Neutralisation Eigenschaften Löslichkeit in Wasser, Dissoziation, Hydratation, Lösungswärme, Seifen schwerlösliche Salze elektrochemische Anwendung biochemisch wichtige Salze Fällungs-Reaktionen Elektrolyse 3.6 Ligandenaustausch-Reaktionen Ligandenaustausch-Reaktionen, Eigenschaften Beispiele, die 10 am häufigsten vorkommenden Kationen und Anionen, Spurenelemente Erkennen von Ligandenaustausch- Reaktionen, Anwendung des Massenwirkungsgesetzes, Stabilität von Metallkomplexen, Komplexkonstanten, Chelat-Effekt, Veränderung der Eigenschaften von Metallionen durch Komplexierung, Ionenkanäle
11 3.6.3 Beispiele biochemische und medizinische Bedeutung an ausgewählten Beispielen 3.7 Additions/Eliminierungs-Reaktionen Additionen, Eliminationen Reaktionen der Carbonylgruppe Tautomerie, Kondensationen Lösen und Knüpfen kovalenter Bindungen: Radikal, Nucleophil, Elektro- 3.8 Substitutionsreaktionen Reaktionsablauf, reaktive Teilchen phil Reaktionen am gesättigten Kohlenstoffatom Reaktionen am ungesättigten Kohlenstoffatom Carbonsäureamide Hydrierung/Dehydrierung und Hydratisierung/Dehydratisierung an einfachen Beispielen, Erkennen bei vorgegebenen biochemischen Reaktionen von Aldehyden und Ketonen mit Wasser, Alkoholen und primären Aminen Keto-Enol-Tautomerie; Aldol-Kondensation, Ester-Kondensation, Bezug zur Mevalonsäure- bzw. Fettsäure-Biosynthese nucleophile Substitution zur Erzeugung der unter genannten funktionellen Gruppen; Bezug zur Funktion von S- Adenosyl-Methionin (SAM) als Methylierungsmittel Bildung/Hydrolyse von Carbonsäureestern und Carbonsäureamiden Säure-Base-Verhalten der Amide, partieller Doppelbindungscharakter; Thermodynamik vs. Kinetik der Amidhydrolyse in Wasser Aromaten Reaktionen an Aromaten (einfache Beispiele für Bromierung, Acylierung, Alkylierung, Sulfonierung) 3.9 Sonstige Reaktionen Nukleinsäuren Keto-Enol-Tautomerie: tautomere Formen der Nukleinbasen Carbonsäuren Decarboxylierung anorganische Säuren Veresterung und Amidbildung bei Schwefelsäure, Kohlensäure und Phosphorsäure (biochemische Beispiele) Chemie biologisch und medizinisch relevanter Naturstoffe 4 Kohlenhydrate 4.1 Monosaccharide Klassifizierung Triosen, Tetrosen, Pentosen, Hexosen, Aldosen, 2-Desoxyaldosen, Ketosen, Pyranosen, Furanosen, Aminozucker s. Anmerkung in 2.1
12 4.1.2 Beispiele Glycerinaldehyd, Ribose, Desoxyribose Glucose, Fructose, Mannose, Galaktose Glucosamin, Galaktosamin, N-Acetyl-Neuraminsäure Schreibweisen Erkennen von vorgegebenen Verbindungen (s. 2.5) in der Fischer-Projektion, Haworth-Formel und Sesselform-Schreibweise Stereochemie D- und L-Reihe, α- und β-anomere, C 1 -Konformation bei Pyranosen der D-Reihe Reaktionen Prinzip der Umsetzung mit: alkoholischen OH-Gruppen (Halbacetale und Acetale), Aminen, Oxidationsmitteln (-onsäuren, -uronsäuren), Reduktionsmitteln (Zuckeralkohole) 4.2 Disaccharide Klassifizierung, Aufbau 1,4-,1,6-Verknüpfung, α- und β- glykosidische Bindung (Haworthoder Sesselform- Schreibweise), Erkennen der enthaltenen Monosaccharide Beispiele Saccharose, Lactose, Maltose, Isomaltose Reaktionen Bildung durch Kondensation, säureoder enzymkatalysierte Hydrolyse zu Monosacchariden 4.3 Oligo- und Polysaccharide Klassifizierung, Aufbau Homo-, Heteroglykane, Erkennen der enthaltenen Monosaccharide, α- und β-glykosidische Bindung, Kennzeichnung von Hauptund Nebenketten, linearer oder helikaler Aufbau der Hauptkette Struktur Strukturprinzip von Glykogen, Stärke, Zellulose, Glykosaminoglykanen 5 Aminosäuren, Peptide, Proteine 5.1 Aminosäuren Klassifizierung L-Reihe (Fischer-Projektion, Stereoformel), α-aminogruppe, proteinogen - nicht proteinogen, essentiell - nicht essentiell, hydrophobe - hydrophile Reste
13 5.1.2 Eigenschaften Struktur in Abhängigkeit vom ph- Wert (Ampholyte), isoelektrischer Punkt, saure, neutrale, basische Aminosäuren, Wanderungsrichtung im elektrischen Feld bei vorgegebenem ph- Wert, Verhalten an Ionenaustauschern, Puffereigenschaften, Redoxverhalten (Cystein - Cystin) Beispiele die proteinogenen Aminosäuren, Ornithin, Citrullin, β-alanin, Homocystein Reaktionen Aminogruppe: Bildung von Schiff - schen Basen, Amiden, Carboxylgruppe: Bildung von Estern und Anhydriden, Amiden, Decarboxylierung, Disulfidbrücken, N- und O-Glykoside 5.2 Peptide Klassifizierung, Aufbau Di-, Tri-, Oligo- und Polypeptide, Erkennen der C- und N-terminalen Aminosäure, Sequenz, Erkennen der enthaltenen Aminosäuren bei vorgegebener Strukturformel Peptidbindung Erkennen in vorgegebenen Verbindungen, Ladungsverteilung, partieller Doppelbindungscharakter, herabgesetzte Basizität des N-Atoms Reaktionen Synthese durch Kondensation (Aktivierung der Carboxylgruppe), Hydrolyse unter dem Einfluss starker Säuren oder Basen 5.3 Proteine Klassifizierung, Aufbau einfache Proteine, zusammengesetzte Proteine (Glykoproteine, Metalloproteine, Proteine mit prosthetischen Gruppen, Lipoproteine), globuläre und fibrilläre Proteine, Primärstruktur (Sequenz), Sekundärstruktur (α-helix, Faltblattstruktur), Tertiär- und Quartärstruktur (Definition, Bindungsarten zur Stabilisierung der Proteinstruktur), native und denaturierte Proteine, Domänen und Strukturmotive
14 5.3.2 Eigenschaften Ampholyte, Puffer, hydrophile/hydrophobe Proteine, Beeinflussung der Löslichkeit (Temperatur, Salze, organische Lösungsmittel, ph-wert), Denaturierung, Wanderung im elektrischen Feld, analytische und präparative Trennung nach Ladung, Molmasse, Affinität Strukturaufklärung Hydrolyse, Bestimmung des N-Terminus, Prinzip der Sequenzierung 6 Fettsäuren, Lipide 6.1 Fettsäuren Klassifizierung geradzahlig ungeradzahlig, gesättigt ungesättigt, Nomenklaturprinzipien, essentiell - nicht essentiell Beispiele Palmitinsäure, Stearinsäure, Ölsäure, Linolsäure, Linolensäure, Arachidonsäure Eigenschaften Löslichkeit, Anionen als oberflächenaktive Stoffe, Seifen, Bildung von Phasengrenzflächen und Mizellen in Wasser Reaktionen Bildung von Estern und Amiden, Reaktivität der ungesättigten Fettsäuren an der Doppelbindung 6.2 Acylglycerine Klassifizierung, Struktur Triacylglycerine, Phosphoglycerine Eigenschaften Löslichkeit, Bildung von Phasengrenzflächen und Mizellen in Wasser, Bildung von Doppelschichten und Liposomen 6.3 Sphingolipide Klassifizierung, Struktur Sphingosin als der zugrunde liegende Alkohol, Strukturelemente von Sphingolipiden Eigenschaften Beteiligung von Sphingolipiden am Aufbau von Lipiddoppelschichten, Vorstufen für Signalmoleküle 6.4 Steroide Klassifizierung, Struktur Isopren als Grundstruktur der Isoprenlipide, strukturelle Merkmale von Cholesterin, Gallensäuren und Steroidhormonen
15 7 Nukleotide, Nukleinsäuren, Chromatin 7.1 Nukleotide Struktur Basen: Purin- und Pyrimidinbasen, Pentosen Nukleoside sowie deren Mono-, Diund Triphosphate, zyklische Nukleotide, N-glykosidische Bindungen, Phosphorsäureester- und -anhydridbindung Reaktionen Spaltung der glykosidischen Bindungen sowie der Phosphorsäureesterund -anhydridbindungen durch Hydrolyse 7.2 Nukleinsäuren Klassifizierung DNA, RNA (mrna, trna, rrna, snrna, hnrna) Struktur Prinzip des Aufbaus eines DNAbzw. RNA-Einzelstrangs, der DNA- Doppelhelix, 5'- und 3'-Ende, Phosphodiesterbindung, Gesetzmäßigkeiten der Basenpaarung, Wasserstoffbrücken, große und kleine Furche der DNA, DNA-Topologie Reaktionen Abbau durch enzymatische Hydrolyse, Hybridisierung, Denaturierung, Änderung der Viskosität, UV-Absorption 7.3 Chromatin Struktur Aufbau aus DNA, Histonen und Nicht-Histon-Proteinen, Struktur der Nukleosomen 8 Vitamine, Vitaminderivate, Coenzyme 8.1 Allgemeines Definition und Klassifikation Herkunft, Stabilität Vitaminbegriff, Zuordnung von Namen und Buchstabenkurzform, Einteilung in wasser- und lipidlöslich Vorkommen der in genannten Vitamine in wichtigen Nahrungsmitteln, Stabilität bei der Zubereitung von Nahrungsmitteln (Erhitzen, Licht- und Sauerstoffeinwirkung; s.a ) Beispiele Erkennen bei vorgegebener Struktur, bei zusammengesetzten Molekülen Erkennen der Bausteine: Cholecalciferol (D 3 ) und sein 1,25- Dihydroxyderivat (Calcitriol), Phyllochinone, Tocopherole, Retinsäure, Retinal, Retinol,
16 Thiamin und Thiamindiphosphat, Riboflavin, FMN, FAD, Nicotinsäureamid, NAD(P) +, NAD(P)H, Pyridoxin und Pyridoxalphosphat, Biotin, Cobalamin, Folsäure, Ascorbinsäure 8.2 Biochemischer Mechanismus Zusammenhang zwischen Vitamin und Coenzym, Kennzeichnung der funktionellen Gruppe, Beteiligung an Enzymreaktionen, Signaltransduktion, Antioxidation 8.3 Pathobiochemie Avitaminosen, Hypo- und Hypervitaminosen, Störungen des Vitaminmetabolismus 9 Grundlagen der Thermodynamik und Kinetik 9.1 Grundbegriffe der Energetik und Kinetik endergon/exergon,endotherm/ Definition der Begriffe exotherm Gibbs' freie Energie (=freie Reaktionsenthalpie) Reaktionsenthalpie Reaktionsentropie Gibbs-Helmholtz-Gleichung Änderung von Gibbs' freier Energie bei Konzentrationsänderungen Gibbs' freie Energie und EMK ( elektromotorische Kraft ) Reaktionsgeschwindigkeit G: maximal geleistete Arbeit bei reversibel isotherm und isobar geführten Prozessen in geschlossenen Systemen H: Reaktionswärme einer isotherm und isobar geführten Reaktion S: Maß für die Änderung des Ordnungszustandes eines Systems im Verlauf einer Reaktion Kenntnis, dass in geschlossenen Systemen (isotherm, isobar) G = H - T S gilt, Bedeutung der Gleichung Berechnung an biochemisch wichtigen Beispielen, Zusammenhang zwischen Gibbs' freier Energie ( G) und Gibbs' freier Standardenergie ( G 0 und G 0 ') Bedeutung der Gleichung G = zf E, Berechnungen an biochemisch wichtigen Beispielen zeitliche Änderung der Konzentration (dc/dt) als Maß für die Reaktionsgeschwindigkeit für eine gegebene Reaktion, Bedeutung des Vorzeichens Rachitis, Perniziosa, Nachtblindheit, Spina bifida s. Anmerkung in 2.1
17 9.1.9 Reaktionsordnung geschwindigkeitsbestimmender Teilschritt Definition des Begriffs Reaktionsordnung, Kriterien, an denen die Reaktionsordnung (0., 1., 2. sowie pseudonullte und -erste Ordnung) erkannt wird Erkennen des geschwindigkeitsbestimmenden Teilschritts in einer aus mehreren Teilreaktionen bestehenden Reaktionskette (bei Angabe entsprechender Größen) Energieprofil Erkennen von "Übergangszustand" (aktivierter Komplex), "Zwischenstufe", "Aktivierungsenergie" ( G ) und "Reaktionsenergie" ( G) anhand einer Skizze des Energieprofils einer Reaktion, Angabe der Ordinatenbezeichnung Parallelreaktionen Erkennen der bevorzugt ablaufenden Reaktion in einem System mit mehreren Reaktionswegen mit unterschiedlicher Aktivierungsenergie Katalyse Wirkungsweise eines Katalysators: Einfluss des Katalysators auf Reaktionsgeschwindigkeit, Aktivierungsenergie, Gleichgewichtslage Funktionelle Biochemie 10 Bioenergetik und Biokatalyse 10.1 Energetik und Kinetik biochemischer Reaktionen reversible Reaktionen Beurteilung der Reaktionsrichtung reversibler biochemischer Reaktionen bei Kenntnis der Gleichgewichtskonstanten, der Konzentrationen der Ausgangsstoffe und von Gibbs freier Energie Fließgleich- (dynamisches Gleichgewicht, "steady gewicht gekoppelte Reaktionen "energiereiche" Verbindungen, Gruppenübertragungspotential state"), Bedeutung in offenen Systemen Ablauf einer endergonen Reaktion durch energetische Kopplung mit einer exergonen Reaktion Größenordnung (kj/mol) der freien Energie der Hydrolyse "energiereicher" Verbindungen (z.b. ATP, GTP, Kreatinphosphat, Acetyl-CoA, PEP), Unterschied zwischen Phosphorsäureesterund Phosphorsäureanhydrid-Bindung Biokatalyse Enzyme als Biokatalysatoren, Proteinnatur von Enzymen, Isoenzyme, Ribozyme, Peptidyltransferase, Definition der Begriffe: Substratspezifität, Stereoselektivität - Stereospezifität, "aktives Zentrum" und "prosthetische Gruppe", Bedeutung von Coen- Enzymdiagnostik
18 zymen (Cosubstrate, Cofaktoren) Enzymkinetik Michaelis-Menten-Beziehung, kinetische Größen zur Kennzeichnung eines Enzyms (Definition, graphische Darstellung einer Enzymkinetik): Substratsättigung, Enzymaktivität, Enzymmenge, Halbsättigungskonzentration, Unit (µmol/min), Unit/Bezugsgröße (Serum: Volumen; Protein: Masse; Enzym: Molmenge) Hemmung von Enzymen kompetitive und nichtkompetitive Hemmung, Beispiele, Erkennen des Hemmtyps in graphischer Darstellung Enzymaktivität Einfluss des Milieus (Temperatur, ph- Wert, Ionen, Substrate, Produkte, Effektoren) photometrische Methoden Absorptionsspektrometrie zur Bestimmung kinetischer Größen, Lambert- Beer sches Gesetz (Berechnungen bei Vorgabe der Gleichung), Wellenlängenabhängigkeit der Extinktion (s.a. Physik Kap. 7), Prinzipien der enzymatischen Substratkonzentrationsbestimmung und der Enzymaktivitätsbestimmung 11 Prinzipien der Stoffwechselregulation Regulation der Enzymaktivität durch die Substratkonzentration negative Rückkopplung allosterische Regulation enzymgesteuerte chemische Modifikation von Enzymen Induktion und Repression der Enzymsynthese z.b. Regulation von Glucokinase und Hexokinase kompetitive Produkthemmung (z.b. Regulation der Hexokinase), Hemmung durch Endprodukt eines Synthesewegs (z.b. Regulation der ALA-Synthase) Enzyme mit hyperboler und sigmoider Kinetik ( z.b. Phosphofructokinase-1, Isocitratdehydrogenase) chemische Modifikation, Beeinflussung von Enzymaffinität und/oder - aktivität z.b. durch Phosphorylierung, Bedeutung interkonvertierender Enzyme bzw. von Enzymkaskaden z.b. Glykogen-Synthase und Phosphorylase, Pyruvat-Dehydrogenase, ADP-Ribosylierung z.b. von G-Proteinen Veränderung der Enzymkonzentration durch Steigerung/Drosselung der Enzymsynthese auf der Transkriptionsund Translationsebene (z.b. Regulation der Gluconeogenese und der Glykolyse ACE-Hemmer, Cyclooxygenasehemmer, Penicillin, Allopurinol, Schwermetallintoxikationen Hyperthermie, Verdauungsenzyme Photometrie in der klinisch-chemischen Diagnostik Blutglucoseregulation, Steuerung der Insulinsekretion Porphyrie Stoffwechsellage bei Diabetes mellitus Typ I Pertussis, Cholera Induktion des Cytochrom-P 450 -Systems durch Pharmaka, Steroid- Rezeptoren als pharmakologische Angriffspunkte
19 limitierte Proteolyse durch Hormone) und/oder des Enzymabbaus (z.b. Adaptation der hepatischen Arginase-Konzentration an unterschiedliche Ernährungssituationen), Begriff des Protein-Turnovers Bildung aktiver Enzyme aus inaktiven Vorstufen, z.b. Verdauungsproteasen, Gerinnungsfaktoren, Komplementfaktoren z.b. G-Proteine, Protein-Protein- Interaktion Hsps und Steroidhormon-Rezeptoren 12 Kataboler Stoffwechsel und Energiegewinnung 12.1 Energiereiche Verbindungen Säureanhydride, Thioester, Enolphosphat- und Phosphoamid-Verbindungen 12.2 Kohlenhydratabbau Glykogenolyse, Glykolyse, Abbau von Fructose, Galaktose, Zwischenprodukte, Cofaktoren, Prinzip der Energiegewinnung in der Glykolyse durch Substratkettenphosphorylierung, intrazelluläre Lokalisation, oxidativer Teil des Pentosephosphatwegs 12.3 Triacylglycerin- und Fettsäureabbau Triacylglycerinlipasen, Bedeutung der Nahrungskarenz, Aufnahme von Fettsäuren in die Zelle und in die Mitochondrien, Abbau von Fettsäuren (β-oxidation), Zwischenprodukte und Cofaktoren, intrazelluläre Lokalisation 12.4 Ketonkörpersynthese und abbau Synthese von Ketonkörpern in der Leber aus Acetyl-CoA, intrazelluläre Lokalisation, Ketonkörperbildung bei längerer Nahrungskarenz und bei Diabetes mellitus, Abbau von Ketonkörpern in extrahepatischen Geweben, Entstehung von Aceton, Ausscheidung durch die Nieren und die Lunge 12.5 Protein- und Aminosäureabbau Proteinabbau intrazelluläre Proteolyse: Lysosomen, Proteasomen Transaminierung und Desaminierung, Decarboxylierung Wege des Kohlenstoffs Substrate, Enzyme und Coenzyme Zuordnung proteinogener Aminosäuren zu Abbaufamilien, glucogene Aminosäuren, akute Pankreatitis, Gerinnungsstörungen Wirkung von Katecholaminen, Sehvorgang Hunger, Anpassung des Kohlenhydratstoffwechsels an kurzzeitige und Dauerleistungen, Glykogenosen, Galaktosämie, Fructose-Intoleranz, Glucose-6-phosphat-Dehydrogenase-Mangel Carnitin-Mangel ketoazidotisches Coma diabeticum lysosomale Speicherkrankheiten Störungen des Abbaus, z.b. bei Phenylketonurie
20 Wege des Stickstoffs 12.6 Ethanolabbau Organbeteiligung (Rolle von Leber, Muskel und Niere) Harnstoff- und Glutaminbildung: Bereitstellung von Ammoniak und Aspartat zur Einschleusung des Stickstoffs in den Harnstoffzyklus, Zwischenprodukte, Ammoniakbildung, Organbeteiligung, Aminosäuren als Ausgangssubstanz für Synthesen NAD + -abhängige Oxidation zu Acetat in der Leber, Acetat-Oxidation in extrahepatischen Organen 12.7 Pyruvat-Dehydrogenase, Citratzyklus Mechanismus und Stoffwechselbedeutung der Pyruvat-Dehydrogenase, Abbau von Acetyl-CoA zu CO 2, Zwischenprodukte, Cofaktoren, intrazelluläre Lokalisation, Funktion und Regulation des Zyklus, Entnahme und Einschleusung von Zwischenprodukten 12.8 Atmungskette und oxidative Phosphorylierung Aufbau Multienzymkomplexe in der inneren Mitochondrienmembran, Komplexe I - V: Strukturprinzip der Cytochrome, Schwefel-Eisen- und Flavo-Proteine sowie des Ubichinons Arbeitsweise Transport von Reduktionsäquivalenten durch die Mitochondrienmembran, mitochondriale Transportsysteme, Reoxidation von NADH und FADH 2, Kopplung zwischen Elektronentransport und Phosphorylierung, ATP-Bildung durch Aufbau und Ausnutzung des elektrochemischen Gradienten, Aufbau und Mechanismus der ATP- Synthase, ADP/ATP-Transport, Atmungskontrolle durch ADP, Möglichkeiten und Folgen der Entkopplung bzw. der Hemmung des Elektronentransports sowie der Hemmung der Phosphorylierung und des ATP-Transports, Entkopplungsproteine, Thermogenese 12.9 Pathobiochemie angeborene Enzymdefekte als Ursachen von Erkrankungen (z.b. Glucose- 6-phosphat-Dehydrogenase-Mangel, Pyruvatkinase-Mangel, Fructose-Intoleranz, Argininosuccinat-Lyase-Mangel, Phenylketonurie), Leberinsuffizienz, Hyperammonämien, Hepato-renale Kompensation von Azidosen und Alkalosen Alkoholkrankheit primär-biliäre Zirrhose Störungen bei Substratmangel oder Hypoxie, Myopathien, Enzephalopathien, Cyanid-Vergiftung
21 Defekte mitochondrialer Proteine, Wirkungen von Enzymgiften 13 Bildung von Energiespeichern 13.1 Kohlenhydrate Verwertung von Glucose Gluconeogenese Glykogensynthese 13.2 Lipide Verwertung von Lipoproteinen und Fettsäuren Fettsäuresynthese Triacyglycerinsynthese 13.3 Proteine Fluss und Verwertung von Glucose nach Nahrungsaufnahme und bei Nahrungskarenz, Mechanismen der Glucoseaufnahme in Zellen durch Glucosetransporter (GLUTs) und Na + -abhängigen sekundär aktiven Glucosetransport Bildung von Glucose aus Lactat, aus glucogenen Aminosäuren sowie aus Glycerin, Schlüsselenzyme der Gluconeogenese; Zwischenprodukte zwischen Pyruvat und Glucose, Cofaktoren, intrazelluläre Lokalisation, Organbeteiligung Bildung von Glykogen aus Glucose, Zwischenprodukte, Cofaktoren, Organbeteiligung Bildung, Fluss und Verwertung von Lipoproteinen sowie Fluss und Verwertung von Fettsäuren nach Nahrungsaufnahme aus Acetyl-CoA, Acetyl-CoA-Carboxylase, Beteiligung von Malonyl-CoA, Fettsäuresynthase-Komplex, Herkunft von Acetyl-CoA und NADPH, intrazelluläre Lokalisation Bildung von Triacylglycerinen, Zwischenprodukte, Cofaktoren, intrazelluläre Lokalisation, Organbeteiligung Synthese nicht-essentieller Aminosäuren aus α-ketosäuren, Aufnahme essentieller Aminosäuren durch die Nahrung, Proteine als Energiereserve 13.4 Regulation der Energiespeicherbildung und verwertung Bildung von Energiespeichern Speicherverwertung kurzfristige und langfristige Wirkung von Insulin auf die Bildung von Glykogen und Triacylglycerinen, Regulation der Glykogensynthase sowie der Acetyl-CoA-Carboxylase, Wirkung von Insulin und Wachstumsfaktoren auf die Proteinsynthese kurzfristige und langfristige Wirkung von Glukagon, Katecholaminen und Homöostase der Blutglucose Einfluss anaboler und kataboler Hormone Diabetes mellitus Gluconeogenese-steigernde Hormone und Pharmaka Hyperlipoproteinämien, Atherosklerose Adipositas Fettleber infolge von Alkoholabusus Lebererkrankungen, Vitaminmangel, Proteinmangelernährung Stoffwechselveränderungen bei Insulinmangel Sport, Gewichtreduktion
22 Energiegewinnung 13.5 Pathobiochemie Glucocorticoiden (s.a ), Regulation der Glykogenphosphorylase, der Hormon-sensitiven Lipase, der Fructosebisphosphatase, der Phosphoenolpyruvat-Carboxykinase Regulation von Teilschritten des Glucoseabbaus und des Citratzyklus (z.b. der Glucokinase-, der Hexokinase-, der Phosphofructokinase-, der Pyruvatkinase-, der Pyruvatdehydrogenase- sowie der Isocitratdehydrogenase-Reaktion) Stoffwechselveränderungen bei Nahrungskarenz sowie bei Diabetes mellitus Typ I und II, Adipositas, angeborene Störungen der Verwertung von Energiespeichern (z.b. Glykogenose Typ I, Lipoproteinlipase-Mangel) Pharmakotherapie, diätetische Maßnahmen Molekularbiologie und Zellbiologie 14 Speicherung, Übertragung und Expression genetischer Information 14.1 Nukleotide Synthese Schritte der Purin- und der Pyrimidinnukleotidsynthese, Bereitstellung von Pentosen (Pentosephosphatweg), Beteiligung von Folsäure, Wiederverwertung von Purin- und Pyrimidinbasen Funktion Cosubstrate (Coenzyme), Substrate der Nukleinsäuresynthese, Signalsubstanzen (zweite Boten), Aktivierung von Zuckern und Lipidbausteinen Abbau Wege und Endprodukte des Abbaus von Purin- und Pyrimidinnukleotiden Pathobiochemie Störungen des Stoffwechsels oder der Ausscheidung von Purinen 14.2 Nukleinsäuren Grundbegriffe Gen als Informationseinheit; Intron, Exon, Promotor, Genom als gesamte genetische Information (DNA-Gehalt) einer Zelle, Größe und Organisation des menschlichen Genoms (kodierend - nichtkodierend; einmal vorkommend - repetitiv), Fluß der genetischen Information: Replikation, Transkription, Translation, Rekombination, Transposition DNA- Replikation Mechanismen und Enzyme der DNA- Replikation, Komponenten der Replikationssysteme bei Pro- und Eukaryonten, Telomerase, Folsäureantagonisten, Antimetabolite, Sulfonamide Gicht, SCID, Adenosindesaminase- Mangel Pharmakotherapie, z.b. mit Allopurinol, Urikosurika Mutationen, Chromosomenaberrationen, diagnostische Verfahren Tumortherapie
23 DNA-Schädigung und Reparatur Hemmstoffe der Synthese von DNA und ihrer Bausteine (Folsäure-Antagonisten, Basenanaloge, Nukleosidanaloge wie z.b. Cytosinarabinosid), Polymerasekettenreaktion (s. a ), Synthese von cdna durch reverse Transkriptase DNA-verändernde chemische und physikalische Faktoren und ihre Effekte an DNA (Mutationen), Reparaturmechanismen, Defekte der DNA-Reparatur, Mutationen durch fehlerhafte Reparatur, Karzinogenese s Transkription Substrate und Mechanismen der RNA- Synthese, RNA-Polymerasen I, II, III und ihre Beziehung zur Synthese einzelner RNA-Typen, Transkriptionsfaktoren, Transkriptionskomplexe, Promotoren, Enhancer- Elemente, primäre Transkriptionsprodukte, posttranskriptionale Prozessierung von RNA (Cap-Struktur, Polyadenylierung, Spleissen), RNA-Editing, Hemmstoffe der Transkription (z.b. α- Amanitin, Actinomycin, Rifamycin), Hemmstoffe von Topoisomerasen Translation Proteinsynthese bei Pro- und Eukaryonten: Aktivierung von Aminosäuren, Initiation, Elongation, Termination der Proteinsynthese, Ribosomenstruktur, Polysomen, freie und ER-gebundene Ribosomen, Prinzip des genetischen Codes (Degeneration, Universalität), Hemmstoffe der Proteinsynthese, wie z.b. Streptomycin, Tetracycline, Chloramphenicol und ihre Angriffspunkte Regulation der Genexpression DNA- und RNA-Viren Induktion und Repression der Transkription von Genen, Signalkaskaden nach Aktivierung ektozellulärer Rezeptoren oder DNA-bindender Proteine, Induktion durch Fremdstoffe, Regulation der Translation, z.b. durch Häm Grundzüge der Struktur von DNA- und RNA-Viren, Tumorviren, Vermehrungszyklen von Viren, Aufbau von Retrovirus-Genomen, Onkogene, Inhibitoren der Virusreplikation (Nukleosidanaloge) Xeroderma pigmentosum, Teleangiektasie Anwendung in der Antibiotikatherapie, Thalassämien, Diphterietoxin, Vergiftung mit Knollenblätterpilzen Induktion des Cytochrom-P Systems Viruserkrankungen, AIDS, antivirale Therapie, virale Vektoren, Gentherapie DNA- Transformation, Konjugation, Trans- bakterielle Virulenz,
24 Übertragung duktion, Transfektion Gentherapie Restriktionsendonukleasen, reverse Transkriptase, cdna, Vektoren (z.b. Plasmide, Cosmide), Klonierung von Genen, Genbanken, Expressionsvektoren, Antibiotika-Resistenz, Knock-out- und transgene Tiere in-vitro-dna- Rekombination, Gentechnik Analyse von Nukleinsäuren Southern-Blot, Northern-Blot, Polymerase-Ketten-Reaktion (PCR), Restriktionsfragment-Längen-Polymorphismus (RFLP), genetischer Fingerabdruck, Prinzip der DNA-Sequenzierung Abbau Enzyme des DNA- und RNA-Abbaus 14.3 Faltung und Modifikation von Proteinen Proteinfaltung Bedeutung der Primärstruktur von Proteinen für die Raumstruktur, Denaturierung und Renaturierung von Proteinen, Bedeutung von Chaperonen, Protein- Disulfid-Isomerase und Prolyl-cistrans-Isomerase für die Proteinfaltung Adressierung von Proteinen limitierte Proteolyse Proteinglykosylierung Verankerung von Proteinen und Membranen nicht-enzymatische Glykierung 14.4 Proteolyse Signalsequenzen, Mechanismen der subzellulären Proteinlokalisierung und Proteinsekretion z.b. Prohormon-Konvertasen, z.b. Proenzym-Konvertasen (Enteropeptidase, Aktivierung des Blutgerinnungs- und Fibrinolysesystems) Prinzip des Aufbaus N- bzw. O-glykosidisch verknüpfter Kohlenhydrat- Seitenketten, Vorkommen von Glykoproteinen und Proteoglykanen Acylierung, Isoprenylierung und GPI- Anker Bildung von advanced glycation endproducts (AGE) Proteasen Einteilung, Mechanismen lysosomale Proteasen zytosolische Proteolyse Kathepsine; Bedeutung der Proteolyse in Phagolysosomen für Antigen-präsentierende Zellen Ubiquitinylierung von Proteinen, Abbau im Proteasom, Bedeutung für Antigenpräsentation mit MHC-I-Proteinen 14.5 Tumorbiochemie Kanzerogenese Mutationen durch chemische und physikalische Einwirkungen, Onkogene, Protoonkogene (Einteilung, Funktionen), gentechnische Synthese von Peptiden, z.b. Insulin, Wachstumshormon, Faktor VIII HIV-Diagnostik, Gendiagnostik, Mutations-Screening Prion-Krankheiten, Alzheimer-Krankheit Mukoviszidose Blutgerinnung, Fibrinolyse, Komplementsystem, Verdauungsenzyme, Apoptose, Hämophilien, Ehlers- Danlos-Syndrom Bedeutung für das Bindegewebe, Alterung, Blutgruppenantigene Diabetes mellitus, Vaskulopathien spezifische Immunabwehr strahlenbedingte maligne Erkrankungen, Retinoblastom, familiäre adenomatöse Polypose,
25 Tumorsuppressorgene (Retinoblastom- Gen/Protein; p53-gen/protein: Funktionen), Mehrschrittprozess der Tumorentstehung, Chromosomale Translokation Therapie Zytostatika (Hemmung des DNA- Stoffwechsels, der DNA-Topologie; Resistenzentwicklung) Apoptose Apoptose als programmierter Zelltod, zellbiologische Veränderungen (Chromatin-Kondensation, -Fragmentierung), Grundzüge der Signalkaskade, Caspasen, onkologische und entwicklungsbiologische Bedeutung 15 Zellstrukturen und interzelluläre Matrix; allgemeine Zytologie 15.1 Prokaryonte Zellen Bakterien (s.a. Biologie Kap. 3) 15.2 Eukaryonte Zellen Aufbau eukaryonter Zellen, subzelluläre Kompartimentierung von Stoffwechselprozessen, Stoffwechselregulation durch Kompartimentierung, Mechanismen des Stofftransportes durch Vesikeltransport, Transport durch Kanäle und Carrier-Moleküle, Prinzip der Auftrennung subzellulärer Partikel, Leitenzyme subzellulärer Partikel 15.3 Membranen Membrankomponenten Aufbau der Membran als Lipiddoppelschicht, Bausteine und Strukturprinzip von Glycerophospholipiden, Sphingolipiden und Cholesterin, integrale und periphere Membranproteine; Verankerung von Proteinen in der Membran, Bausteine und Strukturprinzip von Glykoproteinen, N- bzw. O-glykosidische Verknüpfung der Kohlenhydratseitenketten, N-Acetylneuraminsäure chronisch-myeloische Leukämie z.b. Cyclophosphamid, Busulfan Zelldifferenzierung, Immuntoleranz Rezeptordefekte, z.b. des LDL- Rezeptors, Sphärozytose, Muskeldystrophien, zystische Fibrose
26 Bildung und Abbau von Membranen Synthese von Membranlipiden am endoplasmatischen Retikulum, vesikulärer Transport von Membranen, Vesikelfusion, Membranfluss durch Exound Endozytose, Rezeptor-vermittelte Endozytose, Abbau von Membranlipiden durch Phospholipasen und lysosomale Hydrolasen, Bedeutung von Membranlipiden bei der Erzeugung von Signalmolekülen wie Eikosanoiden und Inositoltrisphosphaten Funktion Systeme für transmembranären Transport, Transzytose, Signalerkennung durch Rezeptoren, Informationsaustausch, Zell-Zell-Kontakte, beteiligte Komponenten, Zellidentität 15.4 Zellkern Chromatin Aufbau aus DNA und Histonen, Struktur von Nukleosomen und weiteren Verpackungsebenen Kernhülle Aufbau, Kernporen Funktionen DNA-Replikation, s , RNA-Synthese, s , NAD + -Synthese, Assemblierung ribosomaler Untereinheiten 15.5 Mitochondrien Aufbau äußere und innere Mitochondrienmembran, Intermembranraum, Matrixraum, Cristae Funktionen z.b. Citratzyklus, Atmungskette und oxidative Phosphorylierung, β-oxidation der Fettsäuren, s.a. 12.3, Lysosomen Entstehung, Aufbau Biogenese, Einbau lysosomaler Hydrolasen, Protonen-ATPase Funktionen Fusion mit Phagosomen, Abbau von Makromolekülen, Beziehung zur Antigenpräsentation mit MHC-II-Proteinen 15.7 Peroxisomen peroxisomale β-oxidation der Fettsäuren, Peroxidasen, Katalase 15.8 Endoplasmatisches Retikulum (ER) Aufbau und glattes und raues ER Zusammen- IgA-Sekretion Gentherapie mitochondriale Enzephalomyopathien lysosomale Speicherkrankheiten, z.b. Cystinose, Mucopolysaccharidosen, Gichtanfall Zellweger-Syndrom, Adrenoleukodystrophie
27 setzung Funktionen z.b. Synthese von Membranlipiden im glatten ER, Synthese von Membranoder Sekretproteinen am rauen ER, Adressierung von Proteinen s Golgi-Apparat Aufbau Cis-, medialer und Trans-Golgi, Trans- Golgi-Netzwerk, Vesikeltransport, Mechanismus Funktionen z.b. Reifung und Adressierung von Glykoproteinen, Recyclisierung von Membranbestandteilen Zytoskelett Aufbau und Funktion von Mikrotubuli, Actinfilamenten und Intermediärfilamenten Extrazelluläre Matrix Strukturprinzip, Vorkommen Synthese, Abbau Kollagene, Elastin, Proteoglykane, Glykosaminoglykane, Hyaluronat, Fibronektin Synthese von Kollagen einschl. posttranslationaler Modifikation, extrazelluläre Vernetzung, Grundzüge der Synthese und extrazellulären Vernetzung von Elastin, Grundzüge der Synthese von Glykosaminoglykanen, Abbau durch extrazellulär wirkende Proteasen und lysosomale Hydrolasen Funktion Funktion von Kollagenen, Elastin, Proteoglykanen, Hyaluronat und Fibronektin Zellzyklus Apoptose G 0, G 1, S-, G 2 -Phase des Zellzyklus, zeitlicher Ablauf der einzelnen Phasen, Vorgänge während dieser Phasen, Regulation des Übergangs in die verschiedenen Phasen durch Cycline und Cyclin-abhängige Proteinkinasen, Retinoblastom-Protein, Regulation des Zellzyklus durch Wachstumsfaktoren, Mitosehemmstoffe s Wirkung von Colchicin, Vinca- Alkaloiden Kollagenosen, Osteogenesis imperfecta, Marfan-Syndrom, Mucopolysaccharidosen Entstehung und Therapie von Malignomen Pathobiochemie Rezeptordefekte: Defekt des Apolipoprotein-B/E-Rezeptors, Transportstörungen: Cystinurie, Mukoviszidose, Kollagendefekte, Sphingolipidosen
28 16 Säure-Basenhaushalt, Wasser- und Elektrolythaushalt, Spurenelemente 16.1 Säure-Basen-Haushalt (s.a. Physiologie 5.10) Protonenbilanz Protonen-bildende und -verbrauchende Prozesse ph-regulation Henderson-Hasselbalch-Gleichung, Puffersysteme des Bluts, Bedeutung von Lunge, Leber und Nieren für die ph-regulation, Pufferkapazität im geschlossenen und offenen System am Beispiel des CO 2 /Hydrogencarbonat- Puffers 16.2 Wasser- und Elektrolyt-Haushalt Wasserhaushalt s. Physiologie Elektrolytstoffwechsel Funktionen der Elektrolyte s. Physiologie 9.1, Resorption, Transport, Speicherung und Ausscheidung von Natrium, Kalium, Calcium, Magnesium, Chlorid, Phosphat, Hydrogencarbonat Bedeutung wichtiger Elektrolyte für Osmoregulation, Membranpotential und Erregungsleitung, Enzymkatalyse und -regulation, transmembranären Transport, intrazelluläre Signalgebung, Elektroneutralität Regulation Regulation des Natrium/Kalium- sowie des Calcium- und Phosphat-Haushaltes (s.a. 18.6) 16.3 Spurenelemente Eisen Funktion des Eisens beim Elektronenund Sauerstofftransport, Grundzüge der Eisenresorption und des Eisenstoffwechsels, Bedeutung von Ferritin und Transferrin, Regulation des zellulären Eisenstoffwechsels Kupfer Bedeutung von Kupfer für die katalytische Aktivität von Oxidasen, Kupfer-Resorption und -Transport im Blut, Kupfer-ATPasen, Bedeutung der Superoxiddismutase Zink Cofaktor von Enzymen, Zinkfinger Iod Vorkommen von Iodid in der Nahrung, Resorption,Transport im Blut, Aufnahme und Speicherung in der Schilddrüse (s.a ) Selen Selenocystein als Bestandteil von Enzymen, oxidativer Stress 16.4 Pathobiochemie Grundzüge von Hypo- und Hyperaldosteronismus, Ursachen und Kompensationsmecha- Ursachen und Folgen von Azidosen und Alkalosen arterielle Hypertonie Eisenmangelanämie, Hämosiderose, Hämochromatose Morbus Wilson, Menkes-Erkrankung, German Childhood Cirrhosis Wundheilungsstörungen bei Zink- Mangel Iodmangelstruma
29 17 Bewegung 17.1 Kontraktile Systeme Actomyosin- System in Muskelzellen 17.2 Motile Systeme mikrotubuläres System Actin und Myosin in Nichtmuskelzellen nismen von metabolischen und respiratorischen Azidosen und Alkalosen (s.a. Physiologie ), Ursachen und Folgen von Hämosiderosen, Hämochromatosen und Eisenmangel Myosin, Actin, Tropomyosin und Troponin bzw. Calmodulin Untereinheiten des Troponins, Quartärstruktur der dicken und der dünnen Filamente, Aufbau des Sarkomers, Unterschiede zwischen glatter und quergestreifter Muskulatur, Energiebereitstellung s. 25.1, Kontraktion, Relaxation s mitotischer Spindelapparat, Zilien, Flagellen, axonaler Transport, Wechselwirkung von Tubulin mit Kinesin und Dynein, Wirkung von Colchicin und Vinblastin β- und γ-actin, Bedeutung von Actinfilamenten für die Struktur von Mikrovilli, Zytokinese in Nichtmuskelzellen, Akrosomenreaktion von Spermien, Motilität von Fibroblasten 17.3 Pathobiochemie Myasthenia gravis als Rezeptordefekt, Muskeldystrophien als Folge von Mutationen im Dystrophin-Gen, Carnitinmangel-Myopathien 18 Hormone und Zytokine 18.1 Grundlagen Aufbau des Hormonsystems und Grundlagen der hormonellen Kommunikation Hormone und Zytokine Hormon- und Zytokinrezep- Auto-, para- und endokrine Wirkungen, endokrine Drüsen, Hormon-produzierende Gewebe, Prinzip der neurohormonalen Kopplung, hormonelle Regelkreise, Transport, Rezeptoren, Inaktivierung Definition, Klassifizierung nach Bildungsort (glanduläre Hormone, Gewebshormone, Zytokine), nach chemischer Struktur (Proteine, Peptide, Aminosäurederivate, Steroide, Fettsäurederivate), nach Funktion, vesikuläre Speicherung oder Bedarfsgesteuerte Neusynthese, Transport im Blut, Grundzüge des Abbaus Liganden-aktivierte Transkriptionsfaktoren als intrazelluläre Hormonrezep- Kardiomyopathien, Diagnostik des Herzinfarkts
Inhaltsverzeichnis. I Stoffwechsel. 1 Vom Organismus zum Molekül Aminosäuren Peptide und Proteine Enzyme...
 XI I Stoffwechsel 1 Vom Organismus zum Molekül...................... 2 1.1 Aufbau des Organismus.............................. 2 1.2 Chemische Grundlagen des Stoffwechsels.................. 6 1.3 Informationsübertragung
XI I Stoffwechsel 1 Vom Organismus zum Molekül...................... 2 1.1 Aufbau des Organismus.............................. 2 1.2 Chemische Grundlagen des Stoffwechsels.................. 6 1.3 Informationsübertragung
IMPP-Gegenstandskatalog (IMPP-GK 1) Ersten Abschnitts der Ärztlichen Prüfung
 Institut für medizinische und pharmazeutische Prüfungsfragen Rechtsfähige Anstalt des öffentlichen Rechts Mainz IMPP-Gegenstandskatalog (IMPP-GK 1) für den schriftlichen Teil des Ersten Abschnitts der
Institut für medizinische und pharmazeutische Prüfungsfragen Rechtsfähige Anstalt des öffentlichen Rechts Mainz IMPP-Gegenstandskatalog (IMPP-GK 1) für den schriftlichen Teil des Ersten Abschnitts der
VII. Inhalt. Vorwort...
 VII Vorwort... V 1 Physikalische und chemische Grundlagen... 1 1.1 Reaktionskinetik... 1 1.2 Reaktionsgeschwindigkeit... 1 1.3 Reaktionsordnung... 2 1.4 Energie... 3 1.4.1 Reaktionsenergie... 3 1.4.2 Enthalpie......
VII Vorwort... V 1 Physikalische und chemische Grundlagen... 1 1.1 Reaktionskinetik... 1 1.2 Reaktionsgeschwindigkeit... 1 1.3 Reaktionsordnung... 2 1.4 Energie... 3 1.4.1 Reaktionsenergie... 3 1.4.2 Enthalpie......
1 Vom Organismus zum Molekül... 3
 I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
Übungsfragen Biochemie 1. Erklären Sie die Begriffe
 Übungsfragen Biochemie 1 Erklären Sie die Begriffe Adsorption Diffusion Dialyse Enantiomere Diastereomere Verseifung Fett Lipid essentielle Fettsäure essentielle Aminosäure Kohlenhydrat Disaccharid Peptid
Übungsfragen Biochemie 1 Erklären Sie die Begriffe Adsorption Diffusion Dialyse Enantiomere Diastereomere Verseifung Fett Lipid essentielle Fettsäure essentielle Aminosäure Kohlenhydrat Disaccharid Peptid
Organische Chemie I Chemie am 16.11.2012. Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2
 Organische Chemie I Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2 Verstehen was Organische Chemie heisst und die Entstehung von Kohlenstoffverbindungen kennen!... 2
Organische Chemie I Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2 Verstehen was Organische Chemie heisst und die Entstehung von Kohlenstoffverbindungen kennen!... 2
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Inhaltsverzeichnis. 1 Bioenergetik und Biokatalyse Prinzipien der Stoffwechselregulation Bildung von Energiespeichern...
 XI 1 Bioenergetik und Biokatalyse...... 2 1.1 Energetik und Kinetik biochemischer Reaktionen................... 4 1.1.1 Reversible Reaktionen............ 4 1.1.2 Fließgleichgewicht.............. 4 1.1.3
XI 1 Bioenergetik und Biokatalyse...... 2 1.1 Energetik und Kinetik biochemischer Reaktionen................... 4 1.1.1 Reversible Reaktionen............ 4 1.1.2 Fließgleichgewicht.............. 4 1.1.3
Wird vom Korrektor ausgefüllt: Aufgabe 1 2 3 4 5 6 7 8 9 10 11 12 Punkte
 Klausur zur Vorlesung Grundlagen der Chemie für Mediziner und Biologen & Chemie-Praktikum für Molekulare Medizin und Biologie Gehalten im Wintersemester 2008/2009 Bitte diese 3 Felder ausfüllem: Name Matrikelnummer
Klausur zur Vorlesung Grundlagen der Chemie für Mediziner und Biologen & Chemie-Praktikum für Molekulare Medizin und Biologie Gehalten im Wintersemester 2008/2009 Bitte diese 3 Felder ausfüllem: Name Matrikelnummer
Kompendium der allgemeinen und anorganischen Chemie
 Kompendium der allgemeinen und anorganischen Chemie Von Dr. rer. nat. habil. Peter Hermann Wissenschaftlicher Oberassistent am Physiologisch-Chemischen Institut der Martin-Luther-Universität Halle-Wittenberg
Kompendium der allgemeinen und anorganischen Chemie Von Dr. rer. nat. habil. Peter Hermann Wissenschaftlicher Oberassistent am Physiologisch-Chemischen Institut der Martin-Luther-Universität Halle-Wittenberg
Klausur zur Vorlesung Biochemie III im WS 2000/01
 Klausur zur Vorlesung Biochemie III im WS 2000/01 am 15.02.2001 von 15.30 17.00 Uhr (insgesamt 100 Punkte, mindestens 40 erforderlich) Bitte Name, Matrikelnummer und Studienfach unbedingt angeben (3 1.
Klausur zur Vorlesung Biochemie III im WS 2000/01 am 15.02.2001 von 15.30 17.00 Uhr (insgesamt 100 Punkte, mindestens 40 erforderlich) Bitte Name, Matrikelnummer und Studienfach unbedingt angeben (3 1.
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 Chemie für Biologen Vorlesung im WS 200/05 V2, Mi 10-12, S0 T01 A02 Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen (Teil : 03.11.200) MILESS: Chemie für Biologen 66 Chemische
Chemie für Biologen Vorlesung im WS 200/05 V2, Mi 10-12, S0 T01 A02 Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen (Teil : 03.11.200) MILESS: Chemie für Biologen 66 Chemische
Inhalt. Allgemeine Chemie
 Allgemeine Chemie Elementarteilchen 3 Aufbau eines Atoms 4 Isotope 5 Elemente 5 Atommasse, Stoffmenge Mol 6 Aufbau der Elektronenhülle 7 Allgemeines 7 Quantenzahlen 7 Elektronenkonfiguration 8 Atomorbitale
Allgemeine Chemie Elementarteilchen 3 Aufbau eines Atoms 4 Isotope 5 Elemente 5 Atommasse, Stoffmenge Mol 6 Aufbau der Elektronenhülle 7 Allgemeines 7 Quantenzahlen 7 Elektronenkonfiguration 8 Atomorbitale
Seminarplan zum. Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie. (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE
 Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Chemie Zusammenfassung KA 2
 Chemie Zusammenfassung KA 2 Wärmemenge Q bei einer Reaktion Chemische Reaktionen haben eine Gemeinsamkeit: Bei der Reaktion wird entweder Energie/Wärme frei (exotherm). Oder es wird Wärme/Energie aufgenommen
Chemie Zusammenfassung KA 2 Wärmemenge Q bei einer Reaktion Chemische Reaktionen haben eine Gemeinsamkeit: Bei der Reaktion wird entweder Energie/Wärme frei (exotherm). Oder es wird Wärme/Energie aufgenommen
Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6
 Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6 Thermodynamik und Gleichgewichte 1. a) Was sagt die Enthalpie aus? Die Enthalpie H beschreibt den Energiegehalt von Materie
Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6 Thermodynamik und Gleichgewichte 1. a) Was sagt die Enthalpie aus? Die Enthalpie H beschreibt den Energiegehalt von Materie
Inhalt. Atombau und Periodensystem ein untrennbarer Zusammenhang... 1. Chemische Bindung wie Teilchen zusammenhalten... 25
 Inhalt Vorwort Atombau und Periodensystem ein untrennbarer Zusammenhang... 1 1 Vorstellung über den Bau der Atome... 1 1.1 Erste Atommodelle Entwicklung aus Grundgesetzen und Versuchen... 1 1.2 Atomkern
Inhalt Vorwort Atombau und Periodensystem ein untrennbarer Zusammenhang... 1 1 Vorstellung über den Bau der Atome... 1 1.1 Erste Atommodelle Entwicklung aus Grundgesetzen und Versuchen... 1 1.2 Atomkern
6. Tag: Chemisches Gleichgewicht und Reaktionskinetik
 6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1 6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1. Das chemische Gleichgewicht Eine chemische Reaktion läuft in beiden Richtungen ab. Wenn
6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1 6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1. Das chemische Gleichgewicht Eine chemische Reaktion läuft in beiden Richtungen ab. Wenn
Fette und ihre Funktionen. Müssen Fette sein?
 Fette und ihre Funktionen Müssen Fette sein? Ja! Fette sind: Wichtiger Bestandteil unserer täglichen Nahrung Energieträger Nummer 1 Quelle für essentielle n Vehikel für die Aufnahme fettlöslicher Vitamine
Fette und ihre Funktionen Müssen Fette sein? Ja! Fette sind: Wichtiger Bestandteil unserer täglichen Nahrung Energieträger Nummer 1 Quelle für essentielle n Vehikel für die Aufnahme fettlöslicher Vitamine
Klausur zum Modul Molekularbiologie ILS, SS 2010 Freitag 6. August 10:00 Uhr
 Klausur zum Modul Molekularbiologie ILS, SS 2010 Freitag 6. August 10:00 Uhr Name: Matrikel-Nr.: Code Nummer: Bitte geben Sie Ihre Matrikel-Nr. und Ihren Namen an. Die Code-Nummer erhalten Sie zu Beginn
Klausur zum Modul Molekularbiologie ILS, SS 2010 Freitag 6. August 10:00 Uhr Name: Matrikel-Nr.: Code Nummer: Bitte geben Sie Ihre Matrikel-Nr. und Ihren Namen an. Die Code-Nummer erhalten Sie zu Beginn
SPEYER-KOLLEG AUGUST 2003 FACHKONFERENZ CHEMIE / BIOLOGIE
 STOFFPLAN CHEMIE GRUNDKURS 1. Halbjahr (K 1) 1. ATOMMODELL Kern- / Hülle-Modell (nach Bohr / Sommerfeld vereinfacht) Ergebnisse des "Wellenmechanischen Atommodells" Quantenzahlen, "Orbitale"(s-, p-, d-)
STOFFPLAN CHEMIE GRUNDKURS 1. Halbjahr (K 1) 1. ATOMMODELL Kern- / Hülle-Modell (nach Bohr / Sommerfeld vereinfacht) Ergebnisse des "Wellenmechanischen Atommodells" Quantenzahlen, "Orbitale"(s-, p-, d-)
Inhalt. Allgemeine Chemie. 5 Heterogene Gleichgewichte Gesättigte Lösungen und Löslichkeit Adsorption an Oberflächen
 Inhalt Allgemeine Chemie 1 Atombau 3 1.1 Elementarteilchen 3 Aufbau eines Atoms 4 Isotope 5 Elemente 5 Atommasse, Mol 6 Aufbau der Elektronen hülle 8 Allgemeines 8 Quantenzahlen 8 Elektronenkonfiguration
Inhalt Allgemeine Chemie 1 Atombau 3 1.1 Elementarteilchen 3 Aufbau eines Atoms 4 Isotope 5 Elemente 5 Atommasse, Mol 6 Aufbau der Elektronen hülle 8 Allgemeines 8 Quantenzahlen 8 Elektronenkonfiguration
Inhaltsverzeichnis. Organische Chemie und Biochemie 1. Proteine und Peptide 23. Enzyme 47. Coenzyme 71
 Inhaltsverzeichnis Organische Chemie und Biochemie 1 1. Die chemische Bindung 1 2. Das Wasser 2 3. Der Kohlenwasserstoff als Grandkörper 4 4. Die funktionellen Gruppen 6 5. Biochemisch wichtige Reaktionen
Inhaltsverzeichnis Organische Chemie und Biochemie 1 1. Die chemische Bindung 1 2. Das Wasser 2 3. Der Kohlenwasserstoff als Grandkörper 4 4. Die funktionellen Gruppen 6 5. Biochemisch wichtige Reaktionen
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
Naturwissenschaftliche Vorprüfung im Fach "Chemie für Zahnmediziner"
 Institut für Medizinische Physik und Biophysik Berlin, April 2006 10117 Berlin, Ziegelstraße 5/9 (CCM) Naturwissenschaftliche Vorprüfung im Fach "Chemie für Zahnmediziner" Allgemeine Hinweise zur Prüfung
Institut für Medizinische Physik und Biophysik Berlin, April 2006 10117 Berlin, Ziegelstraße 5/9 (CCM) Naturwissenschaftliche Vorprüfung im Fach "Chemie für Zahnmediziner" Allgemeine Hinweise zur Prüfung
Grundlagen Der 50 Die Biochemie und
 Inhalt Einleitung 13 Der 44 2.6.1 Der 45 1.1 Wozu Biochemie? 13 46 1.2 Der Intermediärstoffwechsel 13 2.6.3 Glykogenstoff- 1.3 Die Grundlagen der 13 46 1.4 Die Molekularbiologie 14 Der 48 1.5 Die Hormone
Inhalt Einleitung 13 Der 44 2.6.1 Der 45 1.1 Wozu Biochemie? 13 46 1.2 Der Intermediärstoffwechsel 13 2.6.3 Glykogenstoff- 1.3 Die Grundlagen der 13 46 1.4 Die Molekularbiologie 14 Der 48 1.5 Die Hormone
Inhaltsverzeichnis. a. Chemie der Aminosäuren und Peptide
 Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
Grundlagen- / Ergänzungs- / Präferenzfach
 3.11 Chemie Grundlagen / Ergänzungs / Präferenzfach Bildungsziel Der gymnasiale Chemieunterricht führt allgemein in die naturwissenschaftliche Denk und Arbeitsweise ein. Er zeigt die wesentliche Bedeutung
3.11 Chemie Grundlagen / Ergänzungs / Präferenzfach Bildungsziel Der gymnasiale Chemieunterricht führt allgemein in die naturwissenschaftliche Denk und Arbeitsweise ein. Er zeigt die wesentliche Bedeutung
Foliensatz; Arbeitsblatt; Internet. Je nach chemischem Wissen können die Proteine noch detaillierter besprochen werden.
 03 Arbeitsauftrag Arbeitsauftrag Ziel: Anhand des Foliensatzes soll die Bildung und der Aufbau des Proteinhormons Insulin erklärt werden. Danach soll kurz erklärt werden, wie man künstlich Insulin herstellt.
03 Arbeitsauftrag Arbeitsauftrag Ziel: Anhand des Foliensatzes soll die Bildung und der Aufbau des Proteinhormons Insulin erklärt werden. Danach soll kurz erklärt werden, wie man künstlich Insulin herstellt.
RNA und Expression RNA
 RNA und Expression Biochemie RNA 1) Die Transkription. 2) RNA-Typen 3) RNA Funktionen 4) RNA Prozessierung 5) RNA und Proteinexpression/Regelung 1 RNA-Typen in E. coli Vergleich RNA-DNA Sequenz 2 Die Transkriptions-Blase
RNA und Expression Biochemie RNA 1) Die Transkription. 2) RNA-Typen 3) RNA Funktionen 4) RNA Prozessierung 5) RNA und Proteinexpression/Regelung 1 RNA-Typen in E. coli Vergleich RNA-DNA Sequenz 2 Die Transkriptions-Blase
Allgemeine Chemie für Biologen
 Universität Regensburg Allgemeine Chemie für Biologen Rudolf Robelek Vorlesungsübersicht Ü Übersicht über die Kapitel der Vorlesung Kapitel 1: Materie - Elemente, Verbindungen, Mischungen Kapitel 2: Elektronenhülle,
Universität Regensburg Allgemeine Chemie für Biologen Rudolf Robelek Vorlesungsübersicht Ü Übersicht über die Kapitel der Vorlesung Kapitel 1: Materie - Elemente, Verbindungen, Mischungen Kapitel 2: Elektronenhülle,
Chemische Reaktionen
 Ein paar Worte zuvor 7 Stoffe und ihre Eigenschaften 1 Reine Stoffe und Gemische 10 2 Aggregatzustände, Dichte, Löslichkeit, Brennbarkeit und Leitfähigkeit 12 3 Trennverfahren 19 Auf einen Blick: Stoffe
Ein paar Worte zuvor 7 Stoffe und ihre Eigenschaften 1 Reine Stoffe und Gemische 10 2 Aggregatzustände, Dichte, Löslichkeit, Brennbarkeit und Leitfähigkeit 12 3 Trennverfahren 19 Auf einen Blick: Stoffe
Beispiele zur Multiple-Choice Prüfung in OC
 1 Beispiele zur Multiple-Choice Prüfung in C 10 Fragen Typ A Einfachauswahl Bezeichnen Sie nur eine Wahlantwort durch Umkreisen des betreffenden Buchstabens: - bei positiver Formulierung die einzig richtige
1 Beispiele zur Multiple-Choice Prüfung in C 10 Fragen Typ A Einfachauswahl Bezeichnen Sie nur eine Wahlantwort durch Umkreisen des betreffenden Buchstabens: - bei positiver Formulierung die einzig richtige
Musterlösung - Übung 5 Vorlesung Bio-Engineering Sommersemester 2008
 Aufgabe 1: Prinzipieller Ablauf der Proteinbiosynthese a) Erklären Sie folgende Begriffe möglichst in Ihren eigenen Worten (1 kurzer Satz): Gen Nukleotid RNA-Polymerase Promotor Codon Anti-Codon Stop-Codon
Aufgabe 1: Prinzipieller Ablauf der Proteinbiosynthese a) Erklären Sie folgende Begriffe möglichst in Ihren eigenen Worten (1 kurzer Satz): Gen Nukleotid RNA-Polymerase Promotor Codon Anti-Codon Stop-Codon
Vorlesung Anorganische Chemie
 Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 6 Entropie und Gibbs Enthalpie Gibbs-elmholtz-Gleichung Absolute Entropien Gibbs Standardbildungsenthalpien Kinetik
Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 6 Entropie und Gibbs Enthalpie Gibbs-elmholtz-Gleichung Absolute Entropien Gibbs Standardbildungsenthalpien Kinetik
Transgene Organismen
 Transgene Organismen Themenübersicht 1) Einführung 2) Komplementäre DNA (cdna) 3) Vektoren 4) Einschleusung von Genen in Eukaryontenzellen 5) Ausmaß der Genexpression 6) Genausschaltung (Gen-Knockout)
Transgene Organismen Themenübersicht 1) Einführung 2) Komplementäre DNA (cdna) 3) Vektoren 4) Einschleusung von Genen in Eukaryontenzellen 5) Ausmaß der Genexpression 6) Genausschaltung (Gen-Knockout)
P9 Kunststoffe Moleküle ohne Ende
 SLZB Fachbereich Naturwissenschaften Fachinternes Curriculum für das Fach Chemie Klasse 10 2014/15 P9 Kunststoffe Moleküle ohne Ende 10 Bedeutung Kunststoffe Monomer, Polymer, Makromoleküle Polymerisation
SLZB Fachbereich Naturwissenschaften Fachinternes Curriculum für das Fach Chemie Klasse 10 2014/15 P9 Kunststoffe Moleküle ohne Ende 10 Bedeutung Kunststoffe Monomer, Polymer, Makromoleküle Polymerisation
Ringvorlesung Bio(an)organische Chemie. Kofaktoren und Vitamine Die Moleküle des Lebens. Armin Geyer. Fachbereich Chemie Philipps-Universität
 Ringvorlesung Bio(an)organische Chemie Kofaktoren und Vitamine Die Moleküle des Lebens Armin Geyer Fachbereich Chemie Philipps-Universität 15. Apr. 2005 Inhalt Definition und Übersicht Antioxidantien:
Ringvorlesung Bio(an)organische Chemie Kofaktoren und Vitamine Die Moleküle des Lebens Armin Geyer Fachbereich Chemie Philipps-Universität 15. Apr. 2005 Inhalt Definition und Übersicht Antioxidantien:
Oxidation und Reduktion Redoxreaktionen Blatt 1/5
 Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Grundwissen Chemie. 8. Jahrgangsstufe, Gruppe I
 Grundwissen Chemie 8. Jahrgangsstufe, Gruppe I Stoffe, Experimente - Stoffe und Stoffgemische unterscheiden Stoffeigenschaften, Reinstoffe, Gemische, Trennverfahren - Teilchenmodell: Atome und Moleküle
Grundwissen Chemie 8. Jahrgangsstufe, Gruppe I Stoffe, Experimente - Stoffe und Stoffgemische unterscheiden Stoffeigenschaften, Reinstoffe, Gemische, Trennverfahren - Teilchenmodell: Atome und Moleküle
APP-GFP/Fluoreszenzmikroskop. Aufnahmen neuronaler Zellen, mit freund. Genehmigung von Prof. Stefan Kins, TU Kaiserslautern
 Über die Herkunft von Aβ42 und Amyloid-Plaques Heute ist sicher belegt, dass sich die amyloiden Plaques aus einer Vielzahl an Abbaufragmenten des Amyloid-Vorläufer-Proteins (amyloid-precursor-protein,
Über die Herkunft von Aβ42 und Amyloid-Plaques Heute ist sicher belegt, dass sich die amyloiden Plaques aus einer Vielzahl an Abbaufragmenten des Amyloid-Vorläufer-Proteins (amyloid-precursor-protein,
Schulcurriculum für die Qualifikationsphase im Fach Chemie
 Schulcurriculum für die Qualifikationsphase im Fach Chemie Fach: Chemie Klassenstufe: 11/12 Anzahl der zu unterrichtenden Wochenstunden: 3 Die Inhalte des Kerncurriculums wurden in Absprache mit den anderen
Schulcurriculum für die Qualifikationsphase im Fach Chemie Fach: Chemie Klassenstufe: 11/12 Anzahl der zu unterrichtenden Wochenstunden: 3 Die Inhalte des Kerncurriculums wurden in Absprache mit den anderen
Klausur zur Vorlesung Biochemie I im WS 2001/02
 (insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
(insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
Die Bedeutung der Kohlenhydrate für Leistung und Gesundheit
 Die Bedeutung der Kohlenhydrate für Leistung und Gesundheit glukosespiegel: enge Regelung zum Schutz vor Unterund Überzuckerung (Hypo- bzw. Hyperglykämie) abhängig von Nahrungszufuhr und Stoffwechsel bei
Die Bedeutung der Kohlenhydrate für Leistung und Gesundheit glukosespiegel: enge Regelung zum Schutz vor Unterund Überzuckerung (Hypo- bzw. Hyperglykämie) abhängig von Nahrungszufuhr und Stoffwechsel bei
Biomembranen Transportmechanismen
 Transportmechanismen Barrierewirkung der Membran: freie Diffusion von Stoffen wird unterbunden durch Lipidbilayer selektiver Stofftransport über spezielle Membranproteine = Translokatoren Semipermeabilität
Transportmechanismen Barrierewirkung der Membran: freie Diffusion von Stoffen wird unterbunden durch Lipidbilayer selektiver Stofftransport über spezielle Membranproteine = Translokatoren Semipermeabilität
Übungsblatt zu Säuren und Basen
 1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
Die Einheit der Atommasse m ist u. Das ist der 12. Teil der Masse eines Kohlenstoffatoms. 1 u = 1,6608 * 10-27 kg m(h) = 1 u
 Analytische Chemie Stöchiometrie Absolute Atommasse Die Einheit der Atommasse m ist u. Das ist der 12. Teil der Masse eines Kohlenstoffatoms. 1 u = 1,6608 * 10-27 kg m() = 1 u Stoffmenge n Die Stoffmenge
Analytische Chemie Stöchiometrie Absolute Atommasse Die Einheit der Atommasse m ist u. Das ist der 12. Teil der Masse eines Kohlenstoffatoms. 1 u = 1,6608 * 10-27 kg m() = 1 u Stoffmenge n Die Stoffmenge
Allgemeine Pathologie. Störungen im Kupfer- Stoffwechsel
 Allgemeine Pathologie Störungen im Kupfer- Stoffwechsel Physiologie (1): - das Übergangsmetall Kupfer ist als essentielles Spurenelement Bestandteil einer Reihe wichtiger Enzyme: - Ferro-oxidase I (Coeruloplasmin),
Allgemeine Pathologie Störungen im Kupfer- Stoffwechsel Physiologie (1): - das Übergangsmetall Kupfer ist als essentielles Spurenelement Bestandteil einer Reihe wichtiger Enzyme: - Ferro-oxidase I (Coeruloplasmin),
Studiengang Biowissenschaften Modulbegleitende Prüfung zum Praktikum in Organischer Chemie (gemäß MPO vom 12.09.2005) 21.07.2015
 Studiengang Biowissenschaften Modulbegleitende Prüfung zum Praktikum in Organischer Chemie (gemäß MPO vom 12.09.2005) 21.07.2015 Name: Vorname: Matrikel-Nr.: geborenam: in: Wiederholer dieser Klausur:
Studiengang Biowissenschaften Modulbegleitende Prüfung zum Praktikum in Organischer Chemie (gemäß MPO vom 12.09.2005) 21.07.2015 Name: Vorname: Matrikel-Nr.: geborenam: in: Wiederholer dieser Klausur:
8. Translation. Konzepte: Translation benötigt trnas und Ribosomen. Genetischer Code. Initiation - Elongation - Termination
 8. Translation Konzepte: Translation benötigt trnas und Ribosomen Genetischer Code Initiation - Elongation - Termination 1. Welche Typen von RNAs gibt es und welches sind ihre Funktionen? mouse human bacteria
8. Translation Konzepte: Translation benötigt trnas und Ribosomen Genetischer Code Initiation - Elongation - Termination 1. Welche Typen von RNAs gibt es und welches sind ihre Funktionen? mouse human bacteria
GRUNDWISSEN CHEMIE 9 - MuG erstellt von der Fachschaft Chemie
 Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 9 - MuG erstellt von der Fachschaft Chemie C 9.1 Stoffe und Reaktionen Reinstoff Element Kann chemisch nicht mehr zerlegt
Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 9 - MuG erstellt von der Fachschaft Chemie C 9.1 Stoffe und Reaktionen Reinstoff Element Kann chemisch nicht mehr zerlegt
Seminare Biochemie (2. Semester)
 Seminare Biochemie (2. Semester) im SoSe 2017: 1/1 Molekulare Funktion und Bedeutung von Nucleinsäuren (Teil 1) 1/2 Molekulare Funktion und Bedeutung von Nucleinsäuren (Teil 2) 2/1 Molekulare Funktion
Seminare Biochemie (2. Semester) im SoSe 2017: 1/1 Molekulare Funktion und Bedeutung von Nucleinsäuren (Teil 1) 1/2 Molekulare Funktion und Bedeutung von Nucleinsäuren (Teil 2) 2/1 Molekulare Funktion
Organische Chemie. Kohlenwasserstoffe. Alkane. Alkane
 1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
Chemie für Mediziner. Norbert Sträter
 Chemie für Mediziner Norbert Sträter Verlag Wissenschaftliche Scripten 2012 Inhaltsverzeichnis Allgemeine und Anorganische Chemie... 1 1 Atombau... 1 1.1 Fundamentale Begriffe... 1 1.2 Atome und Elemente...
Chemie für Mediziner Norbert Sträter Verlag Wissenschaftliche Scripten 2012 Inhaltsverzeichnis Allgemeine und Anorganische Chemie... 1 1 Atombau... 1 1.1 Fundamentale Begriffe... 1 1.2 Atome und Elemente...
Homologe Reihe. Alkane. Alkene. Alkine
 GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
Grundkurs Chemie 1und 11
 Arnold Arni Grundkurs Chemie 1und 11 Allgemeine, Anorganische und Organische Chemie für Fachunterricht und Selbststudium unter Mitarbeit von Klaus Neuenschwander @ WILEY YCH WILEY-VCH Verlag GmbH & Co.
Arnold Arni Grundkurs Chemie 1und 11 Allgemeine, Anorganische und Organische Chemie für Fachunterricht und Selbststudium unter Mitarbeit von Klaus Neuenschwander @ WILEY YCH WILEY-VCH Verlag GmbH & Co.
Curriculum Chemie Klasse 9 Albert-Einstein-Gymnasium Ulm
 Curriculum Chemie Klasse 9 Albert-Einstein-Gymnasium Ulm Klasse 9 Themen Das Kern-Hülle-Modell Modell des Atomkerns Die Atomhülle im Energiestufenmodell Elektrische Ladung im Atom Das Kern-Hülle-Modell
Curriculum Chemie Klasse 9 Albert-Einstein-Gymnasium Ulm Klasse 9 Themen Das Kern-Hülle-Modell Modell des Atomkerns Die Atomhülle im Energiestufenmodell Elektrische Ladung im Atom Das Kern-Hülle-Modell
Parotis Pankreas. Dünndarm Bürstensaum. Amylose Amylopektin Glykogen. Maltose. Glucose. Isomaltose. Saccharose. Fructose. Lactose. Galaktose.
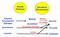 Parotis Pankreas Dünndarm Bürstensaum Amylose Amylopektin Glykogen Saccharose Lactose Maltose Isomaltose Saccharase (Sucrase) Lactase Maltase Isomaltase Glucose Fructose Galaktose Abbau von Stärke und
Parotis Pankreas Dünndarm Bürstensaum Amylose Amylopektin Glykogen Saccharose Lactose Maltose Isomaltose Saccharase (Sucrase) Lactase Maltase Isomaltase Glucose Fructose Galaktose Abbau von Stärke und
GRUNDWISSEN CHEMIE 10. KLASSE
 Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Taschenatlas Biochemie des Menschen
 Taschenatlas Biochemie des Menschen Bearbeitet von Jan Koolman, Klaus-Heinrich Röhm 4., vollständig überarbeitete und erweiterte Auflage 2009. Buch. XII, 529 S. Kartoniert ISBN 978 3 13 759404 8 Format
Taschenatlas Biochemie des Menschen Bearbeitet von Jan Koolman, Klaus-Heinrich Röhm 4., vollständig überarbeitete und erweiterte Auflage 2009. Buch. XII, 529 S. Kartoniert ISBN 978 3 13 759404 8 Format
Inhalt. 1 Einleitung Lipide Kohlenhydrate 19
 6 Inhalt 1 Einleitung 13 1.1 Wozu Biochemie? 13 1.2 Der Intermediärstoffwechsel 13 1.3 Die Grundlagen der Immunchemie 13 1.4 Die Molekularbiologie 14 1.5 Die Hormone 14 1.6 Die Biochemie und das Verständnis
6 Inhalt 1 Einleitung 13 1.1 Wozu Biochemie? 13 1.2 Der Intermediärstoffwechsel 13 1.3 Die Grundlagen der Immunchemie 13 1.4 Die Molekularbiologie 14 1.5 Die Hormone 14 1.6 Die Biochemie und das Verständnis
Hegel-Gymnasium Stuttgart-Vaihingen. Klasse 8
 24.September 2011 Hegel-Gymnasium Stuttgart-Vaihingen Curriculum Chemie Klasse 8 bis 10 Klasse 8 Kern- und Teilkompetenzen Kerncurriculum / Bildungsstandards / Teil der zentralen Jahrgangsarbeiten (ca.
24.September 2011 Hegel-Gymnasium Stuttgart-Vaihingen Curriculum Chemie Klasse 8 bis 10 Klasse 8 Kern- und Teilkompetenzen Kerncurriculum / Bildungsstandards / Teil der zentralen Jahrgangsarbeiten (ca.
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Wortschema Reaktionsschema Beispiel 1: Kupfer und Schwefel Vorzahlen
 6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
Expression der genetischen Information Skript: Kapitel 5
 Prof. A. Sartori Medizin 1. Studienjahr Bachelor Molekulare Zellbiologie FS 2013 12. März 2013 Expression der genetischen Information Skript: Kapitel 5 5.1 Struktur der RNA 5.2 RNA-Synthese (Transkription)
Prof. A. Sartori Medizin 1. Studienjahr Bachelor Molekulare Zellbiologie FS 2013 12. März 2013 Expression der genetischen Information Skript: Kapitel 5 5.1 Struktur der RNA 5.2 RNA-Synthese (Transkription)
Biochemie. Kurzes Lehrbuch der. für Mediziner und Naturwissenschaftler. Von Peter Karlson. 12., völlig neubearbeitete Auflage
 Kurzes Lehrbuch der Biochemie für Mediziner und Naturwissenschaftler Von Peter Karlson 12., völlig neubearbeitete Auflage 177 Abbildungen 323 Formelbilder und Schemata 37 Tabellen 2008 AGI-Information
Kurzes Lehrbuch der Biochemie für Mediziner und Naturwissenschaftler Von Peter Karlson 12., völlig neubearbeitete Auflage 177 Abbildungen 323 Formelbilder und Schemata 37 Tabellen 2008 AGI-Information
Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010
 1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
Selbst-Test zur Vorab-Einschätzung zum Vorkurs Chemie für Mediziner
 Liebe Studierende der Human- und Zahnmedizin, mithilfe dieses Tests können Sie selbst einschätzen, ob Sie den Vorkurs besuchen sollten. Die kleine Auswahl an Aufgaben spiegelt in etwa das Niveau des Vorkurses
Liebe Studierende der Human- und Zahnmedizin, mithilfe dieses Tests können Sie selbst einschätzen, ob Sie den Vorkurs besuchen sollten. Die kleine Auswahl an Aufgaben spiegelt in etwa das Niveau des Vorkurses
Aufbau, Struktur, Funktion von DNA, RNA und Proteinen
 Aufbau, Struktur, Funktion von DNA, RNA und Proteinen Mitarbeiterseminar der Medizinischen Fakultät Ruhr-Universität Bochum Andreas Friebe Abteilung für Pharmakologie und Toxikologie Aufbau, Struktur,
Aufbau, Struktur, Funktion von DNA, RNA und Proteinen Mitarbeiterseminar der Medizinischen Fakultät Ruhr-Universität Bochum Andreas Friebe Abteilung für Pharmakologie und Toxikologie Aufbau, Struktur,
Klonierung von S2P Rolle der M19-Zellen. POL-Seminar der Biochemie II 13.02.2007 Sebastian Gabriel
 Klonierung von S2P Rolle der M19-Zellen POL-Seminar der Biochemie II 13.02.2007 Sebastian Gabriel Inhalt 1. Was ist eine humane genomische DNA-Bank? 2. Unterschied zwischen cdna-bank und genomischer DNA-Bank?
Klonierung von S2P Rolle der M19-Zellen POL-Seminar der Biochemie II 13.02.2007 Sebastian Gabriel Inhalt 1. Was ist eine humane genomische DNA-Bank? 2. Unterschied zwischen cdna-bank und genomischer DNA-Bank?
2. Chemische Reaktionen und chemisches Gleichgewicht
 2. Chemische Reaktionen und chemisches Gleichgewicht 2.1 Enthalpie (ΔH) Bei chemischen Reaktionen reagieren die Edukte zu Produkten. Diese unterscheiden sich in der inneren Energie. Es gibt dabei zwei
2. Chemische Reaktionen und chemisches Gleichgewicht 2.1 Enthalpie (ΔH) Bei chemischen Reaktionen reagieren die Edukte zu Produkten. Diese unterscheiden sich in der inneren Energie. Es gibt dabei zwei
Lipide. Dr. med. Tamás Pándics. Biochemie I. SEMMELWEIS UNIVERSITÄT Institut für Medizinische Biochemie
 Lipide Biochemie I Dr. med. Tamás Pándics SEMMELWEIS UNIVERSITÄT Institut für Medizinische Biochemie Lipide Definition: hydrophobe Biomoleküle Heterogene Gruppe mit abwechslungsreichen Funktionen: Bestandteile
Lipide Biochemie I Dr. med. Tamás Pándics SEMMELWEIS UNIVERSITÄT Institut für Medizinische Biochemie Lipide Definition: hydrophobe Biomoleküle Heterogene Gruppe mit abwechslungsreichen Funktionen: Bestandteile
Christian-Ernst-Gymnasium
 Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 9 - MuG erstellt von der Fachschaft Chemie C 9.1 Stoffe und en Element kann chemisch nicht mehr zerlegt werden Teilchen
Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 9 - MuG erstellt von der Fachschaft Chemie C 9.1 Stoffe und en Element kann chemisch nicht mehr zerlegt werden Teilchen
Datenspeicherung und Datenfluß in der Zelle - Grundlagen der Biochemie
 Datenspeicherung und Datenfluß in der Zelle - Grundlagen der Biochemie Datenspeicherung und Datenfluß der Zelle Transkription DNA RNA Translation Protein Aufbau I. Grundlagen der organischen Chemie und
Datenspeicherung und Datenfluß in der Zelle - Grundlagen der Biochemie Datenspeicherung und Datenfluß der Zelle Transkription DNA RNA Translation Protein Aufbau I. Grundlagen der organischen Chemie und
Die DNA Replikation. Exakte Verdopplung des genetischen Materials. Musterstrang. Neuer Strang. Neuer Strang. Eltern-DNA-Doppelstrang.
 Die DNA Replikation Musterstrang Neuer Strang Eltern-DNA-Doppelstrang Neuer Strang Musterstrang Exakte Verdopplung des genetischen Materials Die Reaktion der DNA Polymerase 5`-Triphosphat Nächstes Desoxyribonucleosidtriphosphat
Die DNA Replikation Musterstrang Neuer Strang Eltern-DNA-Doppelstrang Neuer Strang Musterstrang Exakte Verdopplung des genetischen Materials Die Reaktion der DNA Polymerase 5`-Triphosphat Nächstes Desoxyribonucleosidtriphosphat
Grundkurs Chemie I und II
 Arnold Arni Grundkurs Chemie I und II Allgemeine, Anorganische und Organische Chemie für Fachunterricht und Selbststudium unter Mitarbeit von Klaus Neuenschwander WIEY- VCH WIEY-VCH Verlag GmbH & Co. KGaA
Arnold Arni Grundkurs Chemie I und II Allgemeine, Anorganische und Organische Chemie für Fachunterricht und Selbststudium unter Mitarbeit von Klaus Neuenschwander WIEY- VCH WIEY-VCH Verlag GmbH & Co. KGaA
Inhaltsverzeichnis. Proteins 37. Organisch Gftersi zr.ü??-3shq^is 1
 Inhaltsverzeichnis Organisch Gftersi zr.ü??-3shq^is 1 1. Die chemische Bindung 1 2. Das Wasser 2 3. Der Kohlenwasserstoff als Grundkörper 3 4. Die funktionellen Gruppen 6 5. Biochemisch wichtige Reaktionen
Inhaltsverzeichnis Organisch Gftersi zr.ü??-3shq^is 1 1. Die chemische Bindung 1 2. Das Wasser 2 3. Der Kohlenwasserstoff als Grundkörper 3 4. Die funktionellen Gruppen 6 5. Biochemisch wichtige Reaktionen
1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig?
 1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig? 1) Es sind alles Metalle. 2) In der äußeren Elektronenschale werden s- bzw. s- und p-orbitale aufgefüllt. 3) Sie stimmen
1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig? 1) Es sind alles Metalle. 2) In der äußeren Elektronenschale werden s- bzw. s- und p-orbitale aufgefüllt. 3) Sie stimmen
Inhaltsverzeichnis. Vorwort. xvii. Kapitel 1 Aufbau der Materie 1. Kapitel 2 Die chemische Bindung 39
 Vorwort xvii Kapitel 1 Aufbau der Materie 1 1.1 MateriebestehtausAtomen... 3 1.2 Elementarteilchen... 3 1.3 AufbaueinesAtoms... 4 1.4 AtommassenundStoffmengen... 5 1.5 Isotope... 7 1.6 Radioaktivität und
Vorwort xvii Kapitel 1 Aufbau der Materie 1 1.1 MateriebestehtausAtomen... 3 1.2 Elementarteilchen... 3 1.3 AufbaueinesAtoms... 4 1.4 AtommassenundStoffmengen... 5 1.5 Isotope... 7 1.6 Radioaktivität und
Q1 B1 KW 49. Genregulation
 Q1 B1 KW 49 Genregulation Transkription Posttranskription elle Modifikation Genregulation bei Eukaryoten Transkriptionsfaktoren (an TATA- Box) oder Silencer (verringert Transkription) und Enhancer (erhöht
Q1 B1 KW 49 Genregulation Transkription Posttranskription elle Modifikation Genregulation bei Eukaryoten Transkriptionsfaktoren (an TATA- Box) oder Silencer (verringert Transkription) und Enhancer (erhöht
Elektrolyte. (aus: Goldenberg, SOL)
 Elektrolyte Elektrolyte leiten in wässriger Lösung Strom. Zu den Elektrolyten zählen Säuren, Basen und Salze, denn diese alle liegen in wässriger Lösung zumindest teilweise in Ionenform vor. Das Ostwaldsche
Elektrolyte Elektrolyte leiten in wässriger Lösung Strom. Zu den Elektrolyten zählen Säuren, Basen und Salze, denn diese alle liegen in wässriger Lösung zumindest teilweise in Ionenform vor. Das Ostwaldsche
Kohlenhydrate C n. O) n (H 2. z.b. C 6 O 6 O) 6 H 12 : C 6. Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Monosaccharide
 Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Kontrolle der Genexpression auf mrna-ebene. Abb. aus Stryer (5th Ed.)
 Kontrolle der Genexpression auf mrna-ebene Abb. aus Stryer (5th Ed.) RNA interference (RNAi) sirna (small interfering RNA) mirna (micro RNA) Abb. aus Stryer (5th Ed.) Transcriptional silencing Inhibition
Kontrolle der Genexpression auf mrna-ebene Abb. aus Stryer (5th Ed.) RNA interference (RNAi) sirna (small interfering RNA) mirna (micro RNA) Abb. aus Stryer (5th Ed.) Transcriptional silencing Inhibition
3. Säure-Base-Beziehungen
 3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
Endstoffe (Produkte) Aus dem Reaktionsgemisch entweichendes Gas, z. B. 2 Welche Informationen kann man einer Reaktionsgleichung entnehmen?
 Reaktionsgleichungen Reaktionsgleichungen Blatt 1/5 1 Was ist eine Reaktionsgleichung? Eine Reaktionsgleichung beschreibt die Umwandlung von Stoffen, also einen chemischen Prozeß. Auf der einen Seite steht,
Reaktionsgleichungen Reaktionsgleichungen Blatt 1/5 1 Was ist eine Reaktionsgleichung? Eine Reaktionsgleichung beschreibt die Umwandlung von Stoffen, also einen chemischen Prozeß. Auf der einen Seite steht,
Chemische Evolution. Biologie-GLF von Christian Neukirchen Februar 2007
 Chemische Evolution Biologie-GLF von Christian Neukirchen Februar 2007 Aristoteles lehrte, aus Schlamm entstünden Würmer, und aus Würmern Aale. Omne vivum ex vivo. (Alles Leben entsteht aus Leben.) Pasteur
Chemische Evolution Biologie-GLF von Christian Neukirchen Februar 2007 Aristoteles lehrte, aus Schlamm entstünden Würmer, und aus Würmern Aale. Omne vivum ex vivo. (Alles Leben entsteht aus Leben.) Pasteur
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Musterklausur 1 zur Allgemeinen und Anorganischen Chemie
 Musterklausur 1 zur Allgemeinen und Anorganischen Chemie Achtung: Taschenrechner ist nicht zugelassen. Aufgaben sind so, dass sie ohne Rechner lösbar sind. Weitere Hilfsmittel: Periodensystem der Elemente
Musterklausur 1 zur Allgemeinen und Anorganischen Chemie Achtung: Taschenrechner ist nicht zugelassen. Aufgaben sind so, dass sie ohne Rechner lösbar sind. Weitere Hilfsmittel: Periodensystem der Elemente
Gliederung Thema Buch Heft 1. 1.1 1.2 1.3
 Themenblock: 1 A. Differenzierte quantitative Betrachtung chemischer Reaktionen Baustein: 1 A. I. Betrachtungen zum Verlauf chemischer Reaktionen (8) 2 3 Der unterschiedliche Verlauf chemischer Reaktionen
Themenblock: 1 A. Differenzierte quantitative Betrachtung chemischer Reaktionen Baustein: 1 A. I. Betrachtungen zum Verlauf chemischer Reaktionen (8) 2 3 Der unterschiedliche Verlauf chemischer Reaktionen
DNA Replikation ist semikonservativ. Abb. aus Stryer (5th Ed.)
 DNA Replikation ist semikonservativ Entwindung der DNA-Doppelhelix durch eine Helikase Replikationsgabel Eltern-DNA Beide DNA-Stränge werden in 5 3 Richtung synthetisiert DNA-Polymerasen katalysieren die
DNA Replikation ist semikonservativ Entwindung der DNA-Doppelhelix durch eine Helikase Replikationsgabel Eltern-DNA Beide DNA-Stränge werden in 5 3 Richtung synthetisiert DNA-Polymerasen katalysieren die
-Klausur Biochemie Name:
 -Klausur Biochemie -03.02.5 Name: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
-Klausur Biochemie -03.02.5 Name: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Seminar Biochemie. Lipide und Lipidstoffwechsel. Dr. Christian Hübbers
 Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, TG, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese, MalonylCoA,
Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, TG, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese, MalonylCoA,
Lernaufgabe: Richtigstellen von Reaktionsgleichungen
 Lernaufgabe: Richtigstellen von Reaktionsgleichungen Hilfreiche Angaben: Unterrichtsfach: Chemie Schultyp: Maturitätsschulen Jahrgangsstufe, Kurs: Grundlagenfach Bearbeitungsdauer: 20 Minuten Bearbeitung,
Lernaufgabe: Richtigstellen von Reaktionsgleichungen Hilfreiche Angaben: Unterrichtsfach: Chemie Schultyp: Maturitätsschulen Jahrgangsstufe, Kurs: Grundlagenfach Bearbeitungsdauer: 20 Minuten Bearbeitung,
Übungsklausur zum chemischen Praktikum für Studierende mit Chemie als Nebenfach
 Übungsklausur zum chemischen Praktikum für Studierende mit Chemie als Nebenfach 1. (10P) Was ist richtig (mehrere Richtige sind möglich)? a) Fructose besitzt 5 Kohlenstoffatome. FALSCH, Fructose besitzt
Übungsklausur zum chemischen Praktikum für Studierende mit Chemie als Nebenfach 1. (10P) Was ist richtig (mehrere Richtige sind möglich)? a) Fructose besitzt 5 Kohlenstoffatome. FALSCH, Fructose besitzt
Seminar Biochemie. Lipide und Lipidstoffwechsel. Dr. Christian Hübbers
 Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, Triglyceride, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese,
Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, Triglyceride, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese,
CURRICULUM AUS NATURWISSENSCHAFTEN Biologie/Erdwissenschaften/Chemie 1. Biennium SOGYM
 Allgemeine Ziele und Kompetenzen Der Unterricht der Biologie, Chemie und Erdwissenschaften soll den SchülerInnen eine naturwissenschaftliche Grundausbildung ermöglichen. Sie können sich mit naturwissenschaftliche
Allgemeine Ziele und Kompetenzen Der Unterricht der Biologie, Chemie und Erdwissenschaften soll den SchülerInnen eine naturwissenschaftliche Grundausbildung ermöglichen. Sie können sich mit naturwissenschaftliche
Übung 8. 1. Zellkommunikation. Vorlesung Bio-Engineering Sommersemester 2008. Kapitel 4. 4
 Bitte schreiben Sie Ihre Antworten direkt auf das Übungsblatt. Falls Sie mehr Platz brauchen verweisen Sie auf Zusatzblätter. Vergessen Sie Ihren Namen nicht! Abgabe der Übung bis spätestens 05. 05. 08
Bitte schreiben Sie Ihre Antworten direkt auf das Übungsblatt. Falls Sie mehr Platz brauchen verweisen Sie auf Zusatzblätter. Vergessen Sie Ihren Namen nicht! Abgabe der Übung bis spätestens 05. 05. 08
