JAHRESBERICHT DER KANTONALEN FORSCHUNGS- ETHIKKOMMISSION KEK BERN 2014
|
|
|
- Theresa Kaufer
- vor 6 Jahren
- Abrufe
Transkript
1 Kantonale Ethikkommission Bern (KEK) Postfach 56, 3010 Bern Präsident: Prof. Dr. Christian Seiler Tel.: +41-(0) Sekretariat: Tel.: +41-(0) Fax.: +41-(0) Bern, Juni 2015 JAHRESBERICHT DER KANTONALEN FORSCHUNGS- ETHIKKOMMISSION KEK BERN 2014 I. Allgemeines Die KEK prüft für den Kanton Bern die medizinischen Forschungsuntersuchungen am Menschen mit oder ohne therapeutischen Nutzen.. Über die Zuständigkeit entscheidet die KEK mit Hilfe ihrer juristischen Experten. Sie hat die vom Staat übertragene Entscheidungskompetenz, und sie hat, gestützt auf das eidgenössische Humanforschungsgesetz (HFG), das Statut einer Behördenkommission. Sie entscheidet selbständig und unabhängig mittels rechtsmittelfähigen Verfügungen. Ihre Rolle und Befugnisse sind in der Organisationsverordnung des Humanforschungsgesetz (OV-HFG) festgelegt. Die Aufsichtsbehörde der KEK ist die kantonale Gesundheits- und Fürsorgedirektion (GEF). Die KEK ist dem Kantonsapothekeramt administrativ zugeordnet (Art.1 KEKV). Personal- und, Finanzwesen sind ab der GEF untergeordnet. Die Kantonale Erziehungsdirektion ist im Interesse des Forschungsplatzes Bern mit einem Mitberichtsverfahren an der Aufsicht beteiligt. Die Kantonale Forschungsethikkommission (KEK) übt eine hoheitliche Kontrollfunktion aus: zum Schutz der Versuchspersonen zur Sicherung der wissenschaftlich-klinischen und bioethischen Qualität des einzelnen Versuchsprotokolls unter Berücksichtigung der örtlichen Voraussetzungen. Gesetzliche Grundlagen Seit 01. Januar 2014 arbeitet die KEK auf der Basis des eidgenössischen Humanforschungsgesetzes (HFG; SR ) vom 30. Sept. 2011, der eidgenössischen Verordnung über klinische Versuche (KlinV; SR ) vom 20. Sept. 2013, der eidgenössischen Humanforschungsverordnung (HFV; SR ) vom 20. Sept. 2013, der eidgenössischen Organisationsverordnung (OV-HFG; SR ) vom 20. Sept. 2013, der kantonalen Forschungsverordnung (KEKV; BSG , 20. Aug. 2014), des Bundesgesetzes über Arzneimittel und Medizinprodukte (Heilmittelgesetz, HMG; SR ) vom 15. Dez. 2000, Stand 1. Januar 2014, des Bundesgesetzes über den Datenschutz (SR 235.1) vom 19. Juni 1992 (1. Januar 2014), Generalsekretariat: Dr. sci.nat. Dorothy Pfiffner, pfiffner@kek.unibe.ch 1
2 Strahlenschutzgesetz (StSG ) vom 22. März 1991, Stand 1. Januar 2007, Strahlenschutzverordnung (StSV ), vom 22.Juni 94, Stand 1. Januar 2014, der ICH-Richtlinie for Good Clinical Practice (ICH-GCP), 1996, Deklaration von Helsinki 1964, Stand Zudem wurden auch folgende Erlasse in die Entscheide einbezogen: Bundesgesetz über genetische Untersuchungen beim Menschen (GUMG) vom 8. Oktober 2004, BV 119 Fortpflanzungsmedizin und Gentechnologie im Humanbereich, BG über die Forschung an embryonalen Stammzellen (Stammzellenforschungsgesetz StFG), BG über die medizinisch unterstützte Fortpflanzung (Fortpflanzungsmedizingesetz FMedG), BG über die Transplantation von Organen, Geweben und Zellen (Transplantationsgesetz TrG), Strafgesetzbuch (StGB). Bis 2014 wurden jährlich zwischen Gesuche eingereicht, unter dem HFG 2014 hat sich die Zahl auf >400 erhöht. Da die meisten Studien mehrere Jahre laufen (Archiv KEK), hat die KEK Ende 2014 total ca Studien zu betreuen (Protokoll-Amendments, Meldung unerwarteter Zwischenfälle, jährliche Sicherheitsberichte, Abschlussberichte etc.). Die KEK beurteilt die eingegangenen Studienprotokolle, die oft unvollständig und erst nach Rückfragen beurteilungsfähig sind, nach wissenschaftlich-technischen Kriterien auf der Basis der einschlägigen Gesetzgebung und sie bezieht grundlegende bioethische Kriterien (siehe Belmont revisited weiter unten) in ihre Erwägungen ein. Die Bewilligung für den Gesuchsteller zur Durchführung eines klinischen Versuchs der Kategorie B oder C verläuft parallel: 1. Verfügung mit Rechtsmittelbelehrung der KEK an den Gesuchsteller, 2. Verfügung durch Swissmedic/BAG. Für alle andern Studien fällt die zweite Prüfung weg. Klinische Versuche müssen registriert werden ( Klinische Versuche mit Heilmitteln können von Swissmedic inspiziert werden (auch Kategorie A Studien mit Heilmittel) Wissenschaftlich-technische Grundlagen Zweck der KEK als Entscheidungsinstanz ist es, den eingereichten Forschungsprotokollen eine tragfähige, rechtliche Legitimation zu verschaffen. 1. Klinische Versuche: Die fachlichen Grundlagen für das HFG und seine Folgeerlasse (in erster Linie die Verordnung über klinische Versuche, KlinV.) sind die internationalen Guidelines for Good Clinical Practice (GCP) der International Commission of Harmonisation (ICH). International Conference of Harmonization of Technical Requirements for Registration of Pharmaceuticals for Human Use, ICH Harmonised Tripartite Guideline Guideline for Good Clinical Practice (ICHGCP Guideline) Geneva Nicht-klinische Versuche: Hinzu kommen die HVF für alle anderen Forschungsprojekte, Ergebnisse des Belmont Reports (Belmont Revisited von 2005), die ethischen Kriterien von Emanuel et. al., (2000) und weitere wissenschaftliche Publikationen aus dem neuen universitären Gebiet Ethical and Regulatory Aspects of Clinical Research (NIH, Johns Hopkins University etc.). Durch wissenschaftliche Zusammenarbeit der KEK Bern mit den Arbeitsgemeinschaften europäischer Forschungsethikkommissionen (EURECNET) und u.a. dem Deutschen Referenzzentrum für Ethik in den Biowissenschaften in Bonn (DRZE) ist die Koordination und Auswertung auch aktueller gesamteuropäischer Erkenntnisse gesichert. Generalsekretariat: Dr. sci.nat. Dorothy Pfiffner, pfiffner@kek.unibe.ch 2
3 Verantwortlichkeiten Die KEK schützt die Rechte, die Sicherheit und das Wohl der Prüfungsteilnehmerinnen und Prüfungsteilnehmer. Sie widmet besonders schutzbedürftigen Versuchspersonen (Kinder, Unmündige/Entmündigte, gesunde Probandinnen und Probanden, nicht urteilsfähigen Versuchspersonen) spezielle Aufmerksamkeit. Sie beurteilt die Qualifikation des Prüfers, des Prüfortes, und die Art der Rekrutierung der Versuchspersonen und verlangt andere Informationen zum Forschungsprojekt, wenn das für deren Wohl und Sicherheit und zur Erhaltung des Selbstbestimmungsrechts erforderlich ist. Sie überprüft ebenso Umfang und Art und Weise der Entschädigungen an die Versuchspersonen. Bei den Beurteilungen der Studienprotokolle, den internen Beratungen sowie bei den Entscheiden sind die international anerkannten, mit dem Belmont revisited-bericht in Einklang stehenden Kriterien massgebend ( The 7 Requirements, Emanuel E.J., Wendler D., Grady C. JAMA ): 7 Erfordernisse VALUE (Ist die Studie erforderlich, kann sie neue Erkenntnisse gewinnen?) SCIENTIFIC VALIDITY (Kann die Hypothese geprüft werden? Ist die Methode geeignet?) FAIR SUBJECT SELECTION (Rekrutierung der Versuchspersonen? Ist Druck ausgeübt worden? werden Versuchspersonen mit Geld oder Geschenken angelockt?) FAVORABLE RISK BENEFIT RATIO (Gibt es eine Risikoanalyse? Ist die Studie den Versuchspersonen zumutbar?) INDEPENDENT REVIEW (Gibt es ein Monitoring? Werden die Ausstandsregeln der KEK eingehalten?) INFORMED CONSENT (Werden die Versuchspersonen umfassend, auch schriftlich und mit dem Protokoll übereinstimmend informiert? Ist die Patienten-bzw. Probandeninformation nach der Checkliste auf der Homepage abgefasst? Kann Überinformation im Einzelfall Desinformation bedeuten?) RESPECT FOR POTENTIAL AND ENROLLED SUBJECTS (Wird die Lebensqualität der Versuchspersonen berücksichtigt? Bleibt ihr Selbstbestimmungsrecht unangetastet?) Zusammensetzung der KEK, Aufgaben und Tätigkeit Die EK prüft gemäss HFG, Art. 51 im Rahmen ihrer Zuständigkeiten ob die Forschungsprojekte und deren Durchführung den ethischen, rechtlichen und wissenschaftlichen Anforderungen dieses Gesetzes entsprechen. Insbesondere überprüft sie, ob der Schutz der betroffenen Personen gewährleistet ist. Sie kann die Forscherinnen und Forscher insbesondere zu ethischen Fragen beraten und auf deren Anfrage hin Stellung nehmen zu nicht diesem Gesetz unterstehenden Forschungsvorhaben, namentlich zu solchen, die im Ausland durchgeführt werden.gemäss OV-HFG werden die Gesuche je nach Risiko und Komplexität im ordentlichen (mind. 7 Mitglieder), vereinfachten (3 Mitglieder) oder im präsidialen Verfahren begutachtet, und vom wissenschaftlichen Sekretariat formal und formal inhaltlich geprüft. Die KEK ist eine Expertenkommission mit Entscheidungskompetenz. Die Diskussionen finden interdisziplinär statt. So ist es möglich, den wissenschaftlichen, ethischen und gesetzlichen Anforderungen gerecht zu werden. Mitglieder und Mitarbeiterinnen der KEK Bern siehe Generalsekretariat: Dr. sci.nat. Dorothy Pfiffner, pfiffner@kek.unibe.ch 3
4 II. Jahresziele 2014 Interne Ziele 2014 Mitglieder: Antritt des neuen Präsidenten Prof. Dr. med. Christian Seiler per 1. Januar 2014 (Nachfolge Prof Dr. pharm. Niklaus Tüller); Wahlen: Prof. Dr. med. dent. Michael Bornstein (Zahnmedizin) ; Prof. Dr. med. Daniel Candinas (Chirurgie); Prof. Dr. Hansjörg Znoj (Psychologie) Dr. Dorothy Pfiffner(Biologie) ; Austritte: Prof. Dr. med. dent. Norbert Enkling; Prof. Dr. Arturo Hotz (Ethik); Dolores Krapf (Recht); Prof. Dr. med. Felix Stickel (Medizin), Prof. Dr. pharm. Niklaus Tüller (Pharmazie). Wissenschaftliches Sekretariat: Anstellung von 2 akademischen Mitarbeiterinnen/Mitarbeitern (Frau Dr. Nicole Gruber, Frau Manuela Tham) zur Umsetzung des HFG (160%) Administratives Sekretariat: Betrieb und Optimierung der spezifisch auf die KEK zugeschnittenen Datenbank Erneuerungen im IT-Bereich Fortbildungsveranstaltungen GCP-Kurs für sponsors/investigators für KEK-Mitglieder am 3. Juni 2014 Externe Ziele 2014 Inselspital/Medizinische Fakultät/Forschungsgruppen Optimierung der bestehenden Zusammenarbeit mit dem Dekanat der Medizinischen Fakultät (Prof. M. Arnold als Mittelbauvertreter und Prof. H.U. Simon, Vizedekan) Optimierung der Zusammenarbeit mit dem Inselspital: Sounding Board KEK Zusammenarbeit mit Direktor Lehre und Forschung des Inselspitals Zusammenarbeit mit CTU Bern Swissmedic Optimierung der Zusammenarbeit mit Swissmedic sowie den MitarbeiterInnen des GCP- Bereichs BAG HFG: Regelmässige Besprechungen zu prozeduralen Fragen nach Inkrafttreten HFG, zusammen mit Swissmedic KEK und Swissethics Optimieren der Arbeit von Swissethics. Koordination der Beurteilungskriterien und Formulare im Rahmen des HFG Fort- und Weiterbildung der Mitglieder der KEK Zusammenarbeit mit Prüfärzten und Study Nurses Direkte Kontakte mit den Studien einreichenden Prüfärzten (auch via Sounding Board KEK) Weiterführen von Anhörungen als Verständigungsmittel Beratung und Gespräche auf individueller Ebene Sitzungen Gesuche zu klinischen Versuchen mit minimalem Risiko (KlinV, Kategorie A) und solche zu nichtklinischen Versuchen mit minimalem Risiko (HFV, Kategorie A) werden in Sitzungen zum vereinfachten Verfahren behandelt. Gesuche der Kategorie B und C werden im ordentlichen Verfahren behandelt, alle andern Geschäfte werden im präsidialen Verfahren behandelt. Generalsekretariat: Dr. sci.nat. Dorothy Pfiffner, pfiffner@kek.unibe.ch 4
5 Damit alle eingereichten Studienprotokolle in nützlicher Frist unter Einhaltung der vorgeschriebenen Fristen einem Entscheid zugeführt werden können, sind mehrere Sitzungen pro Monat notwendig. 2014: 22 Sitzungen im ordentlichen Verfahren, 35 im vereinfachten Verfahren. Generalsekretariat: Dr. sci.nat. Dorothy Pfiffner, 5
6 III. Jahreszahlen 2014 Sitzungen Mitglieder Gesuche total 404 Gesuche investigator-initiated 304 Gesuche Industrie-sponsored 83 Gesuche im Präsidialverfahren 109 Gesuche im vereinfachten Verfahren 183 Gesuche im ordentlichen Verfahren 65 Studientyp Monozentrisch 181 Multizentrisch als LeitEK (total) 51(223) Klinische Versuche (ab 1.7.4) 73 -Kategorie A 28 -Kategorie B 11 -Kategorie C 34 Nicht-klinische Versuche (ab ) 94 -Kategorie A 31 -Kategorie B 1 Daten und Probenforschung (ab ) 62 Fristen Tage (median) Eingang Gesuch bis Bestätigung Vollständigkeit Tage (median) Bestätigung Vollständigkeit bis Votum (monozentrisch) Tage (median) Bestätigung Vollständigkeit bis Votum (multizentrisch) Aufteilung nach Votum (behandelte Gesuche 2014) Bewilligung (ohne Auflagen) 29 Ablehnen 3 Auflagen/Bedingungen 111 Nicht zuständig/nicht eintreten 43 Kein Votum erhalten 115 Die vergleichende Anzahl Studienprotokolle 2005 bis 2014 sind aus der folgenden Tabelle ersichtlich. Generalsekretariat: Dr. sci.nat. Dorothy Pfiffner, pfiffner@kek.unibe.ch 6
7 III. Jahreszahlen 2005 bis Anzahl Gesuche total Anzahl Gesuche Inselspital Anzahl Gesuche nicht Insel Versuchspersonen (geplante Einschlüsse) Patienten lokal '486 16'045 45'909 15'177 16'347 18'430 15' Patienten total CH 11'737 12'874 57' '994 39'584 39'382 33' Patienten international Probanden lokal Probanden CH Probanden international Internationalität 294' '659 89' '943 90' ' ' '188 2'845 7'710 1'404 4'755 7'678 2'788 3'276 3'162 4' '129 1'088 5'506 3'362 8' '000 8'970 16'306 3'392 12' Monozentrisch Multizentrisch International Aufteilung Votumstypen nach Positiv mit Auflage/Bedingung, ab /14 Negativ Aussetzen Nicht eintreten nicht zuständig Zurückweisen Kein Votum erhalten Generalsekretariat: Dr. sci.nat. Dorothy Pfiffner, pfiffner@kek.unibe.ch 7
8 Generalsekretariat: Dr. sci.nat. Dorothy Pfiffner, 8
9 IV. Finanzen Abrechnungsmodus 2014 wurden die Gebührenrichtlinien gesamtschweizerisch vereinheitlicht und neu herausgegeben ( Die Gebühren liegen im Rahmen der : Gebührenverordnung (GebV) vom 22. Februar 1995 (BSG ; Anhang III, Ziffer 8.4 des Gebührentarifs der Gesundheits- und Fürsorgedirektion) (Art. 4, 7GebV).. Innerhalb dieses Rahmentarifs bemisst sich eine Gebühr nach dem gesamten Zeit- und Arbeitsaufwand, nach der Bedeutung des Geschäfts für die Gebührenpflichtigen und deren Interesse an der Verrichtung sowie der wirtschaftlichen Leistungsfähigkeit der Gebührenpflichtigen (Art. 7 GebV). Das gesamte Rechnungs- und Mahnwesen wird über die Finanzabteilung der GEF abgewickelt. Der Rechnungsadressat erhält die Rechnung direkt von der GEF. Die Entschädigungen der Mitglieder erfolgt 3x jährlich aufgrund der Anzahl Begutachtungen, Sitzungsteilnahmen und anderen Aufwändungen für die KEK. Während die Einnahmen ausschliesslich von den Gesuchen abhängig sind (Anzahl Gesuche, Gebührenkategorie gemäss Gebührenreglement der KEK), sind die Ausgaben von einer Vielzahl von Faktoren abhängig: Anzahl Sitzungen, Anzahl Mitglieder, Dienstleistungen Dritter, Infrastrukturkosten inkl. EDV- und Büromaterial. Die Entschädigung des Präsidenten ist seit Entstehung der KEK unverändert, obwohl der Zeitaufwand für dieses Amt stark zugenommen hat, vor allem seit Inkrafttreten des HFG. Die Anzahl KEK- Mitglieder musste erhöht werden, um die verschiedenen Fachbereiche der Gesuche besser abdecken zu können, was mit einem grösseren Verwaltungsaufwand für die Entschädigungen im Sekretariat verbunden ist. Die Mitglieder werden durch RRB gewählt. Generalsekretariat: Dr. sci.nat. Dorothy Pfiffner, pfiffner@kek.unibe.ch 9
JAHRESBERICHT DER KANTONALEN FORSCHUNGS- ETHIKKOMMISSION KEK BERN 2009 MIT AUSBLICK AUF 2010
 Kantonale Ethikkommission Bern (KEK) Postfach 56, 3010 Bern Der Präsident Prof. Dr. Niklaus Tüller Tel.: +41-(0)31 311 29 88 Email: niklaus.tueller@swissonline.ch Sekretariat: Tel.: +41-(0)31 632 86 38
Kantonale Ethikkommission Bern (KEK) Postfach 56, 3010 Bern Der Präsident Prof. Dr. Niklaus Tüller Tel.: +41-(0)31 311 29 88 Email: niklaus.tueller@swissonline.ch Sekretariat: Tel.: +41-(0)31 632 86 38
JAHRESBERICHT DER KANTONALEN FORSCHUNGS- ETHIKKOMMISSION KEK BERN 2010 MIT AUSBLICK AUF 2011
 Kantonale Ethikkommission Bern (KEK) Postfach 56, 3010 Bern Der Präsident Prof. Dr. Niklaus Tüller Tel.: +41-(0)31 311 29 88 Email: niklaus.tueller@swissonline.ch Sekretariat: Tel.: +41-(0)31 632 86 38
Kantonale Ethikkommission Bern (KEK) Postfach 56, 3010 Bern Der Präsident Prof. Dr. Niklaus Tüller Tel.: +41-(0)31 311 29 88 Email: niklaus.tueller@swissonline.ch Sekretariat: Tel.: +41-(0)31 632 86 38
Das neue Humanforschungsgesetz Die wichtigsten Neuerung für Forschende
 Departement Klinische Forschung Clinical Trial Unit Das neue Humanforschungsgesetz Die wichtigsten Neuerung für Forschende Research Lunch Kardiologie Christiane Pauli-Magnus und Barbara Peters Das neuehumanforschungsgesetz
Departement Klinische Forschung Clinical Trial Unit Das neue Humanforschungsgesetz Die wichtigsten Neuerung für Forschende Research Lunch Kardiologie Christiane Pauli-Magnus und Barbara Peters Das neuehumanforschungsgesetz
Verordnung über die Kantonale Ethikkommission für die Forschung (KEKV) vom (Stand )
 8.05 Verordnung über die Kantonale Ethikkommission für die Forschung (KEKV) vom 0.08.04 (Stand 0.0.06) Der Regierungsrat des Kantons Bern, gestützt auf Artikel 54 des Bundesgesetzes vom 0. September 0
8.05 Verordnung über die Kantonale Ethikkommission für die Forschung (KEKV) vom 0.08.04 (Stand 0.0.06) Der Regierungsrat des Kantons Bern, gestützt auf Artikel 54 des Bundesgesetzes vom 0. September 0
TÄTIGKEITSBERICHT DER KANTONALEN FORSCHUNGS- ETHIKKOMMISSION KEK 2007/2008
 1 Kantonale Ethikkommission Bern (KEK) Postfach 56, 3010 Bern Der Präsident Prof. Dr. Niklaus Tüller Tel.: +41-(0)31 311 29 88 Email: niklaus.tueller@swissonline.ch Sekretariat: Tel.: +41-(0)31 632 86
1 Kantonale Ethikkommission Bern (KEK) Postfach 56, 3010 Bern Der Präsident Prof. Dr. Niklaus Tüller Tel.: +41-(0)31 311 29 88 Email: niklaus.tueller@swissonline.ch Sekretariat: Tel.: +41-(0)31 632 86
TÄTIGKEITSBERICHT DER KANTONALEN FORSCHUNGS- ETHIKKOMMISSION FÜR KLINISCHE VERSUCHE KEK 2004/2005/2006
 1 Kantonale Ethikkommission Bern (KEK) Postfach 56, Der Präsident Prof. Dr. Niklaus Tüller Tel.: +41-(0)31 311 29 88 Email: niklaus.tueller@swissonline.ch Sekretariat: Tel.: +41-(0)31 632 86 38 Fax.: +41-(0)31
1 Kantonale Ethikkommission Bern (KEK) Postfach 56, Der Präsident Prof. Dr. Niklaus Tüller Tel.: +41-(0)31 311 29 88 Email: niklaus.tueller@swissonline.ch Sekretariat: Tel.: +41-(0)31 632 86 38 Fax.: +41-(0)31
Erläuterungen Angaben zur Anzahl im Vollzugsjahr 2017 eingereichten Gesuche zur Bewilligung eines Forschungsprojekts
 Name Ethikkommission: KEK Zürich Erläuterungen Angaben zur Anzahl im Vollzugsjahr 217 eingereichten Gesuche zur Bewilligung eines Forschungsprojekts 2 3 Anzahl im Vollzugsjahr 217 als lokale Ethikkommission
Name Ethikkommission: KEK Zürich Erläuterungen Angaben zur Anzahl im Vollzugsjahr 217 eingereichten Gesuche zur Bewilligung eines Forschungsprojekts 2 3 Anzahl im Vollzugsjahr 217 als lokale Ethikkommission
Organisationsverordnung zum Humanforschungsgesetz
 Organisationsverordnung zum Humanforschungsgesetz (Organisationsverordnung HFG, OV-HFG) vom 20. September 2013 Der Schweizerische Bundesrat, gestützt auf die Artikel 49 Absätze 1 und 2, 53 Absatz 3, 59
Organisationsverordnung zum Humanforschungsgesetz (Organisationsverordnung HFG, OV-HFG) vom 20. September 2013 Der Schweizerische Bundesrat, gestützt auf die Artikel 49 Absätze 1 und 2, 53 Absatz 3, 59
Angaben zur Art und Anzahl im Vollzugsjahr 2016 eingereichten Gesuche zur Bewilligung eines Forschungsprojekts
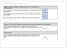 Angaben zur Anzahl im Vollzugsjahr 216 eingereichten Gesuche zur Bewilligung eines Forschungsprojekts Anzahl im Vollzugsjahr 216 als lokale Ethikkommission erhaltene Gesuche zur Bewilligung eines multizentrischen
Angaben zur Anzahl im Vollzugsjahr 216 eingereichten Gesuche zur Bewilligung eines Forschungsprojekts Anzahl im Vollzugsjahr 216 als lokale Ethikkommission erhaltene Gesuche zur Bewilligung eines multizentrischen
QMS Klinische Forschung
 Standard Operating Procedures (SOP) - Prozessbeschreibung ID P2_PM_01 Version: 1.0 Gültig ab: Erstellt von: Astrid Mattes (am 04. Februar 2013) Freigegeben von: Christiane Pauli-Magnus (am 05. März 2013)
Standard Operating Procedures (SOP) - Prozessbeschreibung ID P2_PM_01 Version: 1.0 Gültig ab: Erstellt von: Astrid Mattes (am 04. Februar 2013) Freigegeben von: Christiane Pauli-Magnus (am 05. März 2013)
Inspektion am Prüfzentrum Gute Vorbereitung = Gutes Ergebnis?
 D A CH Symposium für klinische Prüfungen 07. und 08. März 2016, Freiburg Inspektion am Prüfzentrum Gute Vorbereitung = Gutes Ergebnis? Alexander Mion, Leiter GCP/GVP Inspektorat - Abteilung Klinische Versuche,
D A CH Symposium für klinische Prüfungen 07. und 08. März 2016, Freiburg Inspektion am Prüfzentrum Gute Vorbereitung = Gutes Ergebnis? Alexander Mion, Leiter GCP/GVP Inspektorat - Abteilung Klinische Versuche,
Ethische Standards für die Physiotherapieforschung
 Ethische Standards für die Physiotherapieforschung Dr. rer. medic. Sandra Apelt, MSc. Phys. Dietmar Blohm, MSc. Phys. Philipps-Universität Marburg Fachbereich Medizin Studiengang Physiotherapie Ethik (k)ein
Ethische Standards für die Physiotherapieforschung Dr. rer. medic. Sandra Apelt, MSc. Phys. Dietmar Blohm, MSc. Phys. Philipps-Universität Marburg Fachbereich Medizin Studiengang Physiotherapie Ethik (k)ein
Vorwort Abkürzungen. Internationales Recht Internationaler Pakt über wirtschaftliche, soziale und kulturelle Rechte... 3
 Vorwort Abkürzungen V XIII Internationales Recht 1 11. Internationaler Pakt über wirtschaftliche, soziale und kulturelle Rechte... 3 I 2. Internationaler Pakt über bürgerliche und politische Rechte 6 I
Vorwort Abkürzungen V XIII Internationales Recht 1 11. Internationaler Pakt über wirtschaftliche, soziale und kulturelle Rechte... 3 I 2. Internationaler Pakt über bürgerliche und politische Rechte 6 I
Jahresberichterstattung der Ethikkommission Thurgau im Berichtjahr 2015
 Jahresberichterstattung der Ethikkommission Thurgau im Berichtjahr 2015 1 Rechtliche Grundlagen, Struktur und Organisation 1.1 Rechtliche Grundlagen Gesetz über das Gesundheitswesen (Gesundheitsgesetz)
Jahresberichterstattung der Ethikkommission Thurgau im Berichtjahr 2015 1 Rechtliche Grundlagen, Struktur und Organisation 1.1 Rechtliche Grundlagen Gesetz über das Gesundheitswesen (Gesundheitsgesetz)
Aktivitäten swissethics
 Aktivitäten swissethics Dr. med. Susanne Driessen Fortbildungsveranstaltung für Mitglieder von Ethikkommissionen 21. November 2017 Ethikkommissionen Schweiz swissethics Zweck des Vereins ist die Sicherstellung
Aktivitäten swissethics Dr. med. Susanne Driessen Fortbildungsveranstaltung für Mitglieder von Ethikkommissionen 21. November 2017 Ethikkommissionen Schweiz swissethics Zweck des Vereins ist die Sicherstellung
Jahresbericht Kanton Zürich Kantonale Ethikkommission Stampfenbachstrasse 121 Postfach 8090 Zürich. Prof. Dr. med. Peter Meier-Abt Präsident
 Kanton Zürich Kantonale Ethikkommission Stampfenbachstrasse 121 Postfach 8090 Zürich Prof. Dr. med. Peter Meier-Abt Präsident Dr. med. Peter Kleist Geschäftsführer Jahresbericht 2015 Version vom 28. Juli
Kanton Zürich Kantonale Ethikkommission Stampfenbachstrasse 121 Postfach 8090 Zürich Prof. Dr. med. Peter Meier-Abt Präsident Dr. med. Peter Kleist Geschäftsführer Jahresbericht 2015 Version vom 28. Juli
Forschungsethische Aspekte bei der Festlegung kontrazeptiver Methoden in klinischen Studien
 AGAH Diskussionsforum, Bonn, den 20.11.2015 Forschungsethische Aspekte bei der Festlegung kontrazeptiver Methoden in klinischen Studien Dr. phil. Dipl. Psych. Angelika Hüppe Ethikkommission der Universität
AGAH Diskussionsforum, Bonn, den 20.11.2015 Forschungsethische Aspekte bei der Festlegung kontrazeptiver Methoden in klinischen Studien Dr. phil. Dipl. Psych. Angelika Hüppe Ethikkommission der Universität
s w i s s e t h i c s
 Multizentrische Studien (Forschungsprojekte, welche nach einheitlichem Plan, aber in mehreren Zentren und unter Beteiligung mehrerer Ethikkommissionen durchgeführt werden): Konzept gemäss Humanforschungsgesetz
Multizentrische Studien (Forschungsprojekte, welche nach einheitlichem Plan, aber in mehreren Zentren und unter Beteiligung mehrerer Ethikkommissionen durchgeführt werden): Konzept gemäss Humanforschungsgesetz
Wenn eine Ethikkommission grünes Licht für Sozialforschung geben muss
 Die Folien erhalten Sie gerne als PDF. Wenn eine Ethikkommission grünes Licht für Sozialforschung geben muss Prof. Dr. Christian Liesen christian.liesen@hfh.ch DeGEval / SEVAL Methodenatelier, Raum LAA-K041
Die Folien erhalten Sie gerne als PDF. Wenn eine Ethikkommission grünes Licht für Sozialforschung geben muss Prof. Dr. Christian Liesen christian.liesen@hfh.ch DeGEval / SEVAL Methodenatelier, Raum LAA-K041
Bundesgesetz über das Schweizerische Institut für Rechtsvergleichung
 Bundesgesetz über das Schweizerische Institut für Rechtsvergleichung vom 6. Oktober 1978 (Stand am 1. Januar 2007) Die Bundesversammlung der Schweizerischen Eidgenossenschaft, gestützt auf Artikel 27 sexies
Bundesgesetz über das Schweizerische Institut für Rechtsvergleichung vom 6. Oktober 1978 (Stand am 1. Januar 2007) Die Bundesversammlung der Schweizerischen Eidgenossenschaft, gestützt auf Artikel 27 sexies
Häufige Rückstellungsgründe, Bedingungen und Auflagen
 Häufige Rückstellungsgründe, Bedingungen und Auflagen Dr. sc. nat. Dorothy Pfiffner Kantonale Ethikkommission Bern 12.01.2016 Rückstell/Bedingung/Auflagen 1 Übersicht 1. Bedeutung: Rückstellung, Bedingung,
Häufige Rückstellungsgründe, Bedingungen und Auflagen Dr. sc. nat. Dorothy Pfiffner Kantonale Ethikkommission Bern 12.01.2016 Rückstell/Bedingung/Auflagen 1 Übersicht 1. Bedeutung: Rückstellung, Bedingung,
Medizin- und Gesühdheitsrecht
 Medizin- und Gesühdheitsrecht Schweizerisches und internationales Recht Textausgabe von Thomas Gächter Bernhard Rutsche Brigitte Tag Helbing Lichtenhahn Verlag Internationales Recht I 1 I 2 I 3 I 4 Internationaler
Medizin- und Gesühdheitsrecht Schweizerisches und internationales Recht Textausgabe von Thomas Gächter Bernhard Rutsche Brigitte Tag Helbing Lichtenhahn Verlag Internationales Recht I 1 I 2 I 3 I 4 Internationaler
Humanforschungsgesetz und Ethikkommissionen für die Forschung. Faktenblatt der Koordinationsstelle Forschung am Menschen (kofam)
 Humanforschungsgesetz und Ethikkommissionen für die Forschung Faktenblatt der Koordinationsstelle Forschung am Menschen (kofam) 1 Einleitung Bevor unserem Gesundheitssystem neue Heilmittel, Operationen
Humanforschungsgesetz und Ethikkommissionen für die Forschung Faktenblatt der Koordinationsstelle Forschung am Menschen (kofam) 1 Einleitung Bevor unserem Gesundheitssystem neue Heilmittel, Operationen
Geschäftsordnung der Ethik-Kommission der Medizinischen Fakultät der Universität Duisburg-Essen vom
 Geschäftsordnung der Ethik-Kommission der Medizinischen Fakultät der Universität Duisburg-Essen vom 05.02.2018 Die Ethik-Kommission der Medizinischen Fakultät der Universität Duisburg-Essen gibt sich folgende
Geschäftsordnung der Ethik-Kommission der Medizinischen Fakultät der Universität Duisburg-Essen vom 05.02.2018 Die Ethik-Kommission der Medizinischen Fakultät der Universität Duisburg-Essen gibt sich folgende
12.AMG-Novelle Erfahrungen nach Inkrafttreten
 12.AMG-Novelle Erfahrungen nach Inkrafttreten Verfahren der Ethik-Kommissionen Ablauf und Kriterien Besonderheiten bei multizentrischen Studien Prof.Dr.med. Elmar Doppelfeld Vorsitzender des Arbeitskreises
12.AMG-Novelle Erfahrungen nach Inkrafttreten Verfahren der Ethik-Kommissionen Ablauf und Kriterien Besonderheiten bei multizentrischen Studien Prof.Dr.med. Elmar Doppelfeld Vorsitzender des Arbeitskreises
Good Clinical and Epidemiological Practice (GCP/GEP) Guido Grass
 Good Clinical and Epidemiological Practice () Guido Grass 2I 20 Good Clinical and Inhalte des Vortrags Entwicklung der Good Clincial Practice (GCP)-Leitlinie Grundlagen der GCP (GEP) 3I 20 Good Clinical
Good Clinical and Epidemiological Practice () Guido Grass 2I 20 Good Clinical and Inhalte des Vortrags Entwicklung der Good Clincial Practice (GCP)-Leitlinie Grundlagen der GCP (GEP) 3I 20 Good Clinical
Verordnung über die Krankenversicherung
 Verordnung über die Krankenversicherung (KVV) Änderung vom 9. Dezember 2016 Der Schweizerische Bundesrat verordnet: I Die Verordnung vom 27. Juni 1995 1 über die Krankenversicherung wird wie folgt geändert:
Verordnung über die Krankenversicherung (KVV) Änderung vom 9. Dezember 2016 Der Schweizerische Bundesrat verordnet: I Die Verordnung vom 27. Juni 1995 1 über die Krankenversicherung wird wie folgt geändert:
Einführungsgesetz zum Bundesgesetz über die Invalidenversicherung (EG IVG) vom (Stand )
 84. Einführungsgesetz zum Bundesgesetz über die Invalidenversicherung (EG IVG) vom.06.99 (Stand 0.0.008) Der Grosse Rat des Kantons Bern, gestützt auf Artikel 54 des Bundesgesetzes vom 9. Juni 959 über
84. Einführungsgesetz zum Bundesgesetz über die Invalidenversicherung (EG IVG) vom.06.99 (Stand 0.0.008) Der Grosse Rat des Kantons Bern, gestützt auf Artikel 54 des Bundesgesetzes vom 9. Juni 959 über
Das neue Portal für klinische Studien
 Das neue Portal für klinische Studien & Stephanie Züllig, PhD Sektion Forschung am Menschen und Ethik Hintergrund Forderung nach mehr Transparenz bei klinischen Studien (Motion Hubmann, 005) Registrierungspflicht
Das neue Portal für klinische Studien & Stephanie Züllig, PhD Sektion Forschung am Menschen und Ethik Hintergrund Forderung nach mehr Transparenz bei klinischen Studien (Motion Hubmann, 005) Registrierungspflicht
Ethische Aspekte der Forschung in der Onkologie
 Medizin-Ethik 19 Ethische Aspekte der Forschung in der Onkologie von Georg Marckmann, Johannes Meran 1. Auflage Ethische Aspekte der Forschung in der Onkologie Marckmann / Meran schnell und portofrei erhältlich
Medizin-Ethik 19 Ethische Aspekte der Forschung in der Onkologie von Georg Marckmann, Johannes Meran 1. Auflage Ethische Aspekte der Forschung in der Onkologie Marckmann / Meran schnell und portofrei erhältlich
vom 16. Januar/15. Februar 1995
 4.1.2 Verwaltungsvereinbarung zwischen dem Schweizerischen Bundesrat und der Schweizerischen Konferenz der kantonalen Erziehungsdirektoren (EDK) über die Anerkennung von Maturitätszeugnissen 1 vom 16.
4.1.2 Verwaltungsvereinbarung zwischen dem Schweizerischen Bundesrat und der Schweizerischen Konferenz der kantonalen Erziehungsdirektoren (EDK) über die Anerkennung von Maturitätszeugnissen 1 vom 16.
Klinische Prüfungen Internationale Rahmenbedingungen Ein Überblick 22 Mai 2014. Sabine Atzor, F. Hoffmann-La Roche Ltd
 Klinische Prüfungen Internationale Rahmenbedingungen Ein Überblick 22 Mai 2014 Sabine Atzor, F. Hoffmann-La Roche Ltd Klinische Prüfung/ Klinischer Versuch von Arzneimitteln am Menschen Untersuchung von
Klinische Prüfungen Internationale Rahmenbedingungen Ein Überblick 22 Mai 2014 Sabine Atzor, F. Hoffmann-La Roche Ltd Klinische Prüfung/ Klinischer Versuch von Arzneimitteln am Menschen Untersuchung von
Modul Forschung am Menschen, klinische Studien
 Curriculum Gute wissenschaftliche Praxis Modul Forschung am Menschen, klinische Studien Vorbemerkung Die Schwerpunkte dieses Moduls sind die Sensibilisierung der Teilnehmenden für das Konfliktfeld Forschung
Curriculum Gute wissenschaftliche Praxis Modul Forschung am Menschen, klinische Studien Vorbemerkung Die Schwerpunkte dieses Moduls sind die Sensibilisierung der Teilnehmenden für das Konfliktfeld Forschung
Einladung. GCP-Training. Auffrischungskurs. Klinische Prüfungen mit Arzneimitteln: GCP-Auffrischungskurs für Prüfer, Stellvertreter und Prüfgruppe
 Einladung GCP-Training Auffrischungskurs Klinische Prüfungen mit Arzneimitteln: GCP-Auffrischungskurs für Prüfer, Stellvertreter und Prüfgruppe CME-zertifiziert von der Landesärztekammer Samstag, den 09.12.2017-09:00-16:30
Einladung GCP-Training Auffrischungskurs Klinische Prüfungen mit Arzneimitteln: GCP-Auffrischungskurs für Prüfer, Stellvertreter und Prüfgruppe CME-zertifiziert von der Landesärztekammer Samstag, den 09.12.2017-09:00-16:30
Einladung. GCP-Training. Auffrischungskurs. Klinische Prüfungen mit Arzneimitteln: GCP-Auffrischungskurs für Prüfer, Stellvertreter und Prüfgruppe
 Einladung GCP-Training Auffrischungskurs Klinische Prüfungen mit Arzneimitteln: GCP-Auffrischungskurs für Prüfer, Stellvertreter und Prüfgruppe CME-zertifiziert von der Landesärztekammer Samstag, den 09.12.2017-09:00-16:30
Einladung GCP-Training Auffrischungskurs Klinische Prüfungen mit Arzneimitteln: GCP-Auffrischungskurs für Prüfer, Stellvertreter und Prüfgruppe CME-zertifiziert von der Landesärztekammer Samstag, den 09.12.2017-09:00-16:30
Verordnung über die Eidgenössische Fachkommission zur Beurteilung der Behandelbarkeit lebenslänglich verwahrter Straftäter
 Verordnung über die Eidgenössische Fachkommission zur Beurteilung der Behandelbarkeit vom 26. Juni 2013 Der Schweizerische Bundesrat, gestützt auf Artikel 387 Absatz 1 bis des Strafgesetzbuchs 1, verordnet:
Verordnung über die Eidgenössische Fachkommission zur Beurteilung der Behandelbarkeit vom 26. Juni 2013 Der Schweizerische Bundesrat, gestützt auf Artikel 387 Absatz 1 bis des Strafgesetzbuchs 1, verordnet:
Ethikkommissionen an Universitätskliniken Beispiele aus der Praxis
 Ethikkommissionen an Universitätskliniken Beispiele aus der Praxis Prof. Dr. H.D. Tröger Vorsitzender der Ethikkommission Carl-Neuberg-Str. 1 30625 Hannover Quelle: http://www.bundesaerztekammer.de/downloads/deklhelsinki2013.pdf
Ethikkommissionen an Universitätskliniken Beispiele aus der Praxis Prof. Dr. H.D. Tröger Vorsitzender der Ethikkommission Carl-Neuberg-Str. 1 30625 Hannover Quelle: http://www.bundesaerztekammer.de/downloads/deklhelsinki2013.pdf
Interkantonale Vereinbarung über den Salzverkauf in der Schweiz vom (Stand )
 68.- Interkantonale Vereinbarung über den Salzverkauf in der Schweiz vom..973 (Stand 0.0.975) Art. Zweck Diese Vereinbarung bezweckt die Schaffung einer einheitlichen Salzverkaufsordnung auf dem Gebiet
68.- Interkantonale Vereinbarung über den Salzverkauf in der Schweiz vom..973 (Stand 0.0.975) Art. Zweck Diese Vereinbarung bezweckt die Schaffung einer einheitlichen Salzverkaufsordnung auf dem Gebiet
s w i s s e t h i c s
 Forschung in Notfallsituationen (HFG Art. 30-31, KlinV Art.15-17; HFV Art.11) Gültig ab 1. Januar 2014 (Inkraftsetzung des Humanforschungsgesetzes und zugehöriger Verordnungen (vgl. Tabelle). Bei Forschung
Forschung in Notfallsituationen (HFG Art. 30-31, KlinV Art.15-17; HFV Art.11) Gültig ab 1. Januar 2014 (Inkraftsetzung des Humanforschungsgesetzes und zugehöriger Verordnungen (vgl. Tabelle). Bei Forschung
Interkantonale Vereinbarung über den Salzverkauf in der Schweiz
 38. Interkantonale Vereinbarung über den Salzverkauf in der Schweiz Vom. November 973 (Stand. Oktober 975) ) Art. Zweck Diese Vereinbarung bezweckt die Schaffung einer einheitlichen Salzverkaufsordnung
38. Interkantonale Vereinbarung über den Salzverkauf in der Schweiz Vom. November 973 (Stand. Oktober 975) ) Art. Zweck Diese Vereinbarung bezweckt die Schaffung einer einheitlichen Salzverkaufsordnung
Universität Zürich Ethik-Zentrum
 Geschäftsordnung des s der Universität Zürich 1. Teil Grundlagen Art. 1 Name und Zuordnung Das (EZ) ist ein interfakultäres Kompetenzzentrum zur Koordination und Förderung von Forschung und Lehre auf dem
Geschäftsordnung des s der Universität Zürich 1. Teil Grundlagen Art. 1 Name und Zuordnung Das (EZ) ist ein interfakultäres Kompetenzzentrum zur Koordination und Förderung von Forschung und Lehre auf dem
Der Weg zur erfolgreichen Klinischen Prüfung. Klinische Studien für Medizinprodukte und IVDs
 Der Weg zur erfolgreichen Klinischen Prüfung Klinische Studien für Medizinprodukte und IVDs Dr. Benjamin Reutterer KKS Gründung: April 2008 Beratungszentrum für klinische Forschung, Planung, Durchführung
Der Weg zur erfolgreichen Klinischen Prüfung Klinische Studien für Medizinprodukte und IVDs Dr. Benjamin Reutterer KKS Gründung: April 2008 Beratungszentrum für klinische Forschung, Planung, Durchführung
Bringt das HFG mehr Transparenzund wenn ja für wen?
 Bringt das HFG mehr Transparenzund wenn ja für wen? Prof. Dr. med. Robert Maurer Präsident em. KEK Zürich und Arbeitsgemeinschaft der Ethikkommissionen (AGEK) SCTO- FORUM KLINISCHE FORSCHUNG Bern 30.1.2013
Bringt das HFG mehr Transparenzund wenn ja für wen? Prof. Dr. med. Robert Maurer Präsident em. KEK Zürich und Arbeitsgemeinschaft der Ethikkommissionen (AGEK) SCTO- FORUM KLINISCHE FORSCHUNG Bern 30.1.2013
Was bedeutet die neue Gesetzgebung für mein Forschungsprojekt? Das neue Humanforschungsgesetz
 Was bedeutet die neue Gesetzgebung für mein Forschungsprojekt? Das neue Humanforschungsgesetz 6. Juni 2013 Brigitte Meier Leitung Sektion Forschung am Mensch und Ethik Bundesamt für Gesundheit Inhalt 1.
Was bedeutet die neue Gesetzgebung für mein Forschungsprojekt? Das neue Humanforschungsgesetz 6. Juni 2013 Brigitte Meier Leitung Sektion Forschung am Mensch und Ethik Bundesamt für Gesundheit Inhalt 1.
Synopse. 2016_04_VOL_Arbeitsmarktverordnung_AMV. Arbeitsmarktverordnung (AMV) Arbeitsmarktverordnung (AMV) Der Regierungsrat des Kantons Bern,
 Synopse 06_04_VOL_Arbeitsmarktverordnung_AMV Arbeitsmarktverordnung (AMV) Der Regierungsrat des Kantons Bern, auf Antrag der Volkswirtschaftsdirektion, beschliesst: I. Der Erlass 836. Arbeitsmarktverordnung
Synopse 06_04_VOL_Arbeitsmarktverordnung_AMV Arbeitsmarktverordnung (AMV) Der Regierungsrat des Kantons Bern, auf Antrag der Volkswirtschaftsdirektion, beschliesst: I. Der Erlass 836. Arbeitsmarktverordnung
Verordnung über die Gebühren im Gesundheitswesen
 Gebühren im Gesundheitswesen: Verordnung 0.70 Verordnung über die Gebühren im Gesundheitswesen Vom. Oktober 0 (Stand 7. Oktober 0) Der Regierungsrat des Kantons Basel-Stadt, gestützt auf Art. 4 Abs. 4
Gebühren im Gesundheitswesen: Verordnung 0.70 Verordnung über die Gebühren im Gesundheitswesen Vom. Oktober 0 (Stand 7. Oktober 0) Der Regierungsrat des Kantons Basel-Stadt, gestützt auf Art. 4 Abs. 4
Diese Verordnung regelt den Vollzug der eidgenössischen Betäubungsmittelgesetzgebung durch die kantonalen Behörden.
 83.3 Einführungsverordnung zur eidgenössischen Betäubungsmittelgesetzgebung (EV BetmG) vom 0.06.0 (Stand 0.09.0) Der Regierungsrat des Kantons Bern, gestützt auf Artikel 9d des Bundesgesetzes vom 3. Oktober
83.3 Einführungsverordnung zur eidgenössischen Betäubungsmittelgesetzgebung (EV BetmG) vom 0.06.0 (Stand 0.09.0) Der Regierungsrat des Kantons Bern, gestützt auf Artikel 9d des Bundesgesetzes vom 3. Oktober
Berner Fachhochschule Gesundheit. Detailinformation zum CAS-Studiengang
 Gesundheit Detailinformation zum CAS-Studiengang Study Nurse Durchführung 2014 / 2015 Kooperationspartner Überblick Die klinische Forschung leistet als Teilgebiet der Medizin einen wichtigen Beitrag zur
Gesundheit Detailinformation zum CAS-Studiengang Study Nurse Durchführung 2014 / 2015 Kooperationspartner Überblick Die klinische Forschung leistet als Teilgebiet der Medizin einen wichtigen Beitrag zur
Projekt HMV IV - Umteilung Abgabekategorien
 Projekt HMV IV - Umteilung Abgabekategorien Information für Fach- und Medizinalpersonen Dr. Bernhard Spörri, Projektleiter, Leiter Einheit-2, Abteilung Quality Review, Bereich Zulassung Swissmedic Schweizerisches
Projekt HMV IV - Umteilung Abgabekategorien Information für Fach- und Medizinalpersonen Dr. Bernhard Spörri, Projektleiter, Leiter Einheit-2, Abteilung Quality Review, Bereich Zulassung Swissmedic Schweizerisches
Einladung. GCP-Training. Grundlagen- und Aufbaukurs
 Einladung GCP-Training Grundlagen- und Aufbaukurs Klinische Prüfungen mit Arzneimitteln: GCP-Grundlagen- und Aufbaukurs für Prüfer, Stellvertreter und Prüfgruppe CME-zertifiziert von der Landesärztekammer
Einladung GCP-Training Grundlagen- und Aufbaukurs Klinische Prüfungen mit Arzneimitteln: GCP-Grundlagen- und Aufbaukurs für Prüfer, Stellvertreter und Prüfgruppe CME-zertifiziert von der Landesärztekammer
Ordnung zur ethischen Begutachtung von Forschungsprojekten des Fachbereichs Erziehungswissenschaft. der Freien Universität Berlin [RA III ]
![Ordnung zur ethischen Begutachtung von Forschungsprojekten des Fachbereichs Erziehungswissenschaft. der Freien Universität Berlin [RA III ] Ordnung zur ethischen Begutachtung von Forschungsprojekten des Fachbereichs Erziehungswissenschaft. der Freien Universität Berlin [RA III ]](/thumbs/58/42643911.jpg) Ordnung zur ethischen Begutachtung von Forschungsprojekten des Fachbereichs Erziehungswissenschaft und Psychologie der Freien Universität Berlin [RA III 2 210710] Präambel Aufgrund von 14 Abs.1 Nr. 2 Teilgrundordnung
Ordnung zur ethischen Begutachtung von Forschungsprojekten des Fachbereichs Erziehungswissenschaft und Psychologie der Freien Universität Berlin [RA III 2 210710] Präambel Aufgrund von 14 Abs.1 Nr. 2 Teilgrundordnung
Für die medizinische Forschung relevante Neuerungen im Strahlenschutzrecht
 Für die medizinische Forschung relevante Neuerungen im Strahlenschutzrecht 36. Jahrestagung des Arbeitskreises Medizinischer Ethik-Kommissionen in der Bundesrepublik Deutschland e.v. Berlin, 8. November
Für die medizinische Forschung relevante Neuerungen im Strahlenschutzrecht 36. Jahrestagung des Arbeitskreises Medizinischer Ethik-Kommissionen in der Bundesrepublik Deutschland e.v. Berlin, 8. November
Verordnung über die Aufsicht über die nachrichtendienstlichen Tätigkeiten
 Verordnung über die Aufsicht über die nachrichtendienstlichen Tätigkeiten (VAND) vom 16. August 2017 (Stand am 1. September 2017) Der Schweizerische Bundesrat, gestützt auf die Artikel 79 Absatz 4, 80
Verordnung über die Aufsicht über die nachrichtendienstlichen Tätigkeiten (VAND) vom 16. August 2017 (Stand am 1. September 2017) Der Schweizerische Bundesrat, gestützt auf die Artikel 79 Absatz 4, 80
Gestützt auf Art. 45 Abs. 1 und Art. 81 Abs. 1 der Kantonsverfassung 1)
 80.50 Kantonale Verordnung über die Umweltverträglichkeitsprüfung (KVUVP) Vom 7. Juli 009 (Stand 8. Dezember 05) Gestützt auf Art. 45 Abs. und Art. 8 Abs. der Kantonsverfassung ) von der Regierung erlassen
80.50 Kantonale Verordnung über die Umweltverträglichkeitsprüfung (KVUVP) Vom 7. Juli 009 (Stand 8. Dezember 05) Gestützt auf Art. 45 Abs. und Art. 8 Abs. der Kantonsverfassung ) von der Regierung erlassen
Studienregistrierung. Version: Gültig ab: 23. August Anmerkungen Das vorliegende Dokument ist eine Druckversion
 Studienregistrierung Version: 3.0.2 Gültig ab: 23. August 2016 Erstellt durch: Review durch: Freigabe durch: Ansprechperson: Astrid Mattes Emelie Müller, Julia Maurer Klaus Ehrlich Klaus Ehrlich Anmerkungen
Studienregistrierung Version: 3.0.2 Gültig ab: 23. August 2016 Erstellt durch: Review durch: Freigabe durch: Ansprechperson: Astrid Mattes Emelie Müller, Julia Maurer Klaus Ehrlich Klaus Ehrlich Anmerkungen
EU weite Genehmigung klinischer Prüfungen mit Humanarzneimitteln Welcher Regelungsbedarf besteht in Deutschland?
 EU weite Genehmigung klinischer Prüfungen mit Humanarzneimitteln Welcher Regelungsbedarf besteht in Deutschland? AGAH Workshop, 5. Dezember 2014 Nina Hammes Bundesministerium für Gesundheit 1 Verordnung
EU weite Genehmigung klinischer Prüfungen mit Humanarzneimitteln Welcher Regelungsbedarf besteht in Deutschland? AGAH Workshop, 5. Dezember 2014 Nina Hammes Bundesministerium für Gesundheit 1 Verordnung
Verordnung über die Organisation und die Aufgaben der Gesundheits- und Fürsorgedirektion (Organisationsverordnung GEF, OrV GEF) (Änderung)
 5.. Verordnung über die Organisation und die Aufgaben der Gesundheits- und Fürsorgedirektion (Organisationsverordnung GEF, OrV GEF) (Änderung) Der Regierungsrat des Kantons Bern, auf Antrag der Gesundheits-
5.. Verordnung über die Organisation und die Aufgaben der Gesundheits- und Fürsorgedirektion (Organisationsverordnung GEF, OrV GEF) (Änderung) Der Regierungsrat des Kantons Bern, auf Antrag der Gesundheits-
Fortpflanzungsmedizinverordnung
 Fortpflanzungsmedizinverordnung (FMedV) Änderung vom 21. Juni 2017 Der Schweizerische Bundesrat verordnet: I Die Fortpflanzungsmedizinverordnung vom 4. Dezember 2000 1 wird wie folgt geändert: Art. 1 Eine
Fortpflanzungsmedizinverordnung (FMedV) Änderung vom 21. Juni 2017 Der Schweizerische Bundesrat verordnet: I Die Fortpflanzungsmedizinverordnung vom 4. Dezember 2000 1 wird wie folgt geändert: Art. 1 Eine
Studierende müssen mindestens 15 Credits aus dem gesamten Angebot Qualifikatonsprofil Prüfarzt nachweisen.
 Institut für Medizinische Statistik Direktor: Univ.-Prof. Dr. rer. nat. Ralf-Dieter Hilgers Qualifikationsprofil Prüfarzt Sehr geehrte Damen und Herren, das Institut für Medizinische Statistik bietet den
Institut für Medizinische Statistik Direktor: Univ.-Prof. Dr. rer. nat. Ralf-Dieter Hilgers Qualifikationsprofil Prüfarzt Sehr geehrte Damen und Herren, das Institut für Medizinische Statistik bietet den
Richtlinien über die finanzielle Unterstützung von Fotoprojekten von gesamtschweizerischer Bedeutung
 Richtlinien über die finanzielle Unterstützung von Fotoprojekten vom 5. April 2004 Das Eidgenössische Departement des Innern erlässt folgende Richtlinien: 1. Abschnitt: Allgemeine Bestimmungen Art. 1 Gegenstand
Richtlinien über die finanzielle Unterstützung von Fotoprojekten vom 5. April 2004 Das Eidgenössische Departement des Innern erlässt folgende Richtlinien: 1. Abschnitt: Allgemeine Bestimmungen Art. 1 Gegenstand
Änderungen mit dem Humanforschungsgesetz Neue Vorlagen
 Departement Klinische Forschung Clinical Trial Unit Änderungen mit dem Humanforschungsgesetz Neue Vorlagen HFG News 3 Astrid Mattes 09. Januar 2014 -Seite 5 revidiert am 24.01.2014- Werkzeug zur Risikoklassifizierung
Departement Klinische Forschung Clinical Trial Unit Änderungen mit dem Humanforschungsgesetz Neue Vorlagen HFG News 3 Astrid Mattes 09. Januar 2014 -Seite 5 revidiert am 24.01.2014- Werkzeug zur Risikoklassifizierung
Evaluation und Optimierung der Biobank Governance
 Evaluation und Optimierung der Biobank Governance Prof. Dr. Daniel Strech 5. Nationales Biobanken-Symposium 2016 TMF/GBN, Berlin, 8.12.2016 Agenda 1. Was meint/umfasst Biobank-Governance? In Abgrenzung
Evaluation und Optimierung der Biobank Governance Prof. Dr. Daniel Strech 5. Nationales Biobanken-Symposium 2016 TMF/GBN, Berlin, 8.12.2016 Agenda 1. Was meint/umfasst Biobank-Governance? In Abgrenzung
Freiburger Ethik-Kommission International. Verfahrensordnung,
 Freiburger Ethik-Kommission International freiburg ethics commission international Verfahrensordnung, rev. am 30.Juni 1998 Dr. med. Dr. rer. nat. Hans-Peter Graf, Freiburg/Deutschland (Präsident der Kommission;
Freiburger Ethik-Kommission International freiburg ethics commission international Verfahrensordnung, rev. am 30.Juni 1998 Dr. med. Dr. rer. nat. Hans-Peter Graf, Freiburg/Deutschland (Präsident der Kommission;
Die Ethik-Kommission an der MedUni Wien
 Die Ethik-Kommission an der MedUni Wien Ernst Singer Ethik-Kommission MedUni Wien Juni 2014 Das Dilemma des klinischen Forschers... Als Arzt: Besorgt um die Gesundheit des Patienten Als Wissenschafter:
Die Ethik-Kommission an der MedUni Wien Ernst Singer Ethik-Kommission MedUni Wien Juni 2014 Das Dilemma des klinischen Forschers... Als Arzt: Besorgt um die Gesundheit des Patienten Als Wissenschafter:
Verordnung des WBF über die Gewährung von Steuererleichterungen im Rahmen der Regionalpolitik
 Verordnung des WBF über die Gewährung von Steuererleichterungen im Rahmen der Regionalpolitik vom 3. Juni 2016 (Stand am 1. Juli 2016) Das Eidgenössische Departement für Wirtschaft, Bildung und Forschung
Verordnung des WBF über die Gewährung von Steuererleichterungen im Rahmen der Regionalpolitik vom 3. Juni 2016 (Stand am 1. Juli 2016) Das Eidgenössische Departement für Wirtschaft, Bildung und Forschung
Forderungen der DGHO unter Berücksichtigung der Rolle von Ethik-Kommissionen und des Bundesamts für Strahlenschutz (BfS) bei Klinischen Studien
 Berlin, 17.6.2014: Pressekonferenz: Die neue EU-Verordnung zu klinischen Studien eine Chance für den Forschungsstandort Deutschland Forderungen der DGHO unter Berücksichtigung der Rolle von Ethik-Kommissionen
Berlin, 17.6.2014: Pressekonferenz: Die neue EU-Verordnung zu klinischen Studien eine Chance für den Forschungsstandort Deutschland Forderungen der DGHO unter Berücksichtigung der Rolle von Ethik-Kommissionen
1 Allgemeine Bestimmungen
 8.5. Verordnung über die Kontrolle der Feuerungsanlagen mit Heizöl «Extra leicht» und Gas (VKF) vom.0.00 (Stand 0.0.05) Der Regierungsrat des Kantons Bern, gestützt auf Artikel 7 Buchstabe d des Gesetzes
8.5. Verordnung über die Kontrolle der Feuerungsanlagen mit Heizöl «Extra leicht» und Gas (VKF) vom.0.00 (Stand 0.0.05) Der Regierungsrat des Kantons Bern, gestützt auf Artikel 7 Buchstabe d des Gesetzes
Kantonale Ethikkommission Zürich. Jahresbericht 2014
 Kantonale Ethikkommission Zürich Jahresbericht 2014 Zu Beginn des Jahres 2014 ist das Humanforschungsgesetz (HFG) mit den dazugehörenden drei Ausführungsverordnungen in Kraft getreten. Dies bedeutete für
Kantonale Ethikkommission Zürich Jahresbericht 2014 Zu Beginn des Jahres 2014 ist das Humanforschungsgesetz (HFG) mit den dazugehörenden drei Ausführungsverordnungen in Kraft getreten. Dies bedeutete für
Geschäftsordnung der unabhängigen Aufsichtsbehörde über die nachrichtendienstlichen Tätigkeiten
 Geschäftsordnung der unabhängigen Aufsichtsbehörde vom 26. Februar 2018 Die unabhängige Aufsichtsbehörde (AB-ND), gestützt auf Artikel 77 Absatz 3 des Nachrichtendienstgesetzes vom 25. September 2015 1
Geschäftsordnung der unabhängigen Aufsichtsbehörde vom 26. Februar 2018 Die unabhängige Aufsichtsbehörde (AB-ND), gestützt auf Artikel 77 Absatz 3 des Nachrichtendienstgesetzes vom 25. September 2015 1
Einführungsverordnung zur eidgenössischen Chemikaliengesetzgebung (EV ChemG) vom (Stand )
 83.5 Einführungsverordnung zur eidgenössischen Chemikaliengesetzgebung (EV ChemG) vom 24.05.2006 (Stand 0.0.2009) Der Regierungsrat des Kantons Bern, gestützt auf Artikel 32 des Bundesgesetzes vom 5. Dezember
83.5 Einführungsverordnung zur eidgenössischen Chemikaliengesetzgebung (EV ChemG) vom 24.05.2006 (Stand 0.0.2009) Der Regierungsrat des Kantons Bern, gestützt auf Artikel 32 des Bundesgesetzes vom 5. Dezember
Geschäftsordnung der unabhängigen Aufsichtsbehörde über die nachrichtendienstlichen Tätigkeiten
 Geschäftsordnung der unabhängigen Aufsichtsbehörde vom 26. Februar 2018 Die unabhängige Aufsichtsbehörde (AB-ND), gestützt auf Artikel 77 Absatz 3 des Nachrichtendienstgesetzes vom 25. September 2015 1
Geschäftsordnung der unabhängigen Aufsichtsbehörde vom 26. Februar 2018 Die unabhängige Aufsichtsbehörde (AB-ND), gestützt auf Artikel 77 Absatz 3 des Nachrichtendienstgesetzes vom 25. September 2015 1
Deutsches Hämophilieregister (DHR) Zur Notwendigkeit eines Ethikvotums
 Paul-Ehrlich-Institut Postfach 63207 Langen Birgit Haschberger Transfusionsmedizin / Deutsches Hämophilieregister (DHR) Telefon +49 (0) 6103 77 1860 Fax +49 (0) 6103 77 1276 E-Mail dhr@pei.de 28. Januar
Paul-Ehrlich-Institut Postfach 63207 Langen Birgit Haschberger Transfusionsmedizin / Deutsches Hämophilieregister (DHR) Telefon +49 (0) 6103 77 1860 Fax +49 (0) 6103 77 1276 E-Mail dhr@pei.de 28. Januar
Abgeschlossen durch Notenaustausch vom 11. Dezember 2001 Inkrafttreten: 1. Januar 2002
 0.812.101 Liechtensteinisches Landesgesetzblatt Jahrgang 2001 Nr. 190 ausgegeben am 20. Dezember 2001 Notenaustausch zwischen dem Fürstentum Liechtenstein und der Schweiz betreffend die Geltung der schweizeri-
0.812.101 Liechtensteinisches Landesgesetzblatt Jahrgang 2001 Nr. 190 ausgegeben am 20. Dezember 2001 Notenaustausch zwischen dem Fürstentum Liechtenstein und der Schweiz betreffend die Geltung der schweizeri-
zur Umsetzung der Mo. Eder "Swissmedic-Zulassung eines Arzneimittels als erlaubtes Werbeelement" in der Arzneimittel-Werbeverordnung (AWV)
 Eidgenössisches Departement des Innern EDI Bundesamt für Gesundheit BAG Dezember 2014 Erläuternder Bericht zur Umsetzung der Mo. Eder 13.3393 "Swissmedic-Zulassung eines Arzneimittels als erlaubtes Werbeelement"
Eidgenössisches Departement des Innern EDI Bundesamt für Gesundheit BAG Dezember 2014 Erläuternder Bericht zur Umsetzung der Mo. Eder 13.3393 "Swissmedic-Zulassung eines Arzneimittels als erlaubtes Werbeelement"
Wie funktioniert eine klinische Studie?
 Wie funktioniert eine klinische Studie? Bernhard Saller 3. Süddeutscher Hypophysen- und Nebennierentag München, 5. Mai 2007 Definitionen Ablauf klinischer Studien Klinische Arzneimittelprüfungen Zulassungsprozess
Wie funktioniert eine klinische Studie? Bernhard Saller 3. Süddeutscher Hypophysen- und Nebennierentag München, 5. Mai 2007 Definitionen Ablauf klinischer Studien Klinische Arzneimittelprüfungen Zulassungsprozess
Neubekanntmachung des Statuts einer Ethikkommission bei der Landesärztekammer Baden-Württemberg (ÄBW 2017, S.598)
 Neubekanntmachung des Statuts einer Ethikkommission bei der Landesärztekammer Baden-Württemberg (ÄBW 2017, S.598) Aufgrund von 2 der Satzung zur Änderung des Statuts einer Ethikkommission bei der Landesärztekammer
Neubekanntmachung des Statuts einer Ethikkommission bei der Landesärztekammer Baden-Württemberg (ÄBW 2017, S.598) Aufgrund von 2 der Satzung zur Änderung des Statuts einer Ethikkommission bei der Landesärztekammer
Informationen zur Ausnahmebewilligung für verbotene Betäubungsmittel des Bundesamtes für Gesundheit (BAG)
 Informationen zur Ausnahmebewilligung für verbotene Betäubungsmittel des Bundesamtes für Gesundheit (BAG) 1. Zweck dieses Merkblatts Dieses Merkblatt gibt eine Übersicht darüber, welche Tätigkeiten im
Informationen zur Ausnahmebewilligung für verbotene Betäubungsmittel des Bundesamtes für Gesundheit (BAG) 1. Zweck dieses Merkblatts Dieses Merkblatt gibt eine Übersicht darüber, welche Tätigkeiten im
Reglement des Naturhistorischen Museums
 8.6. Reglement des Naturhistorischen Museums vom. Februar 99 Der Staatsrat des Kantons Freiburg gestützt auf das Gesetz vom. Oktober 99 über die kulturellen Institutionen des Staates (KISG); gestützt auf
8.6. Reglement des Naturhistorischen Museums vom. Februar 99 Der Staatsrat des Kantons Freiburg gestützt auf das Gesetz vom. Oktober 99 über die kulturellen Institutionen des Staates (KISG); gestützt auf
Hohe Standards und liberale Normen
 Themendossier 1/10 Gesundheitspolitik Fakten zu gesundheitspolitischen Themen und die Position der Pharmaindustrie Bundesgesetz über die Forschung am Menschen Hohe Standards und liberale Normen Mit dem
Themendossier 1/10 Gesundheitspolitik Fakten zu gesundheitspolitischen Themen und die Position der Pharmaindustrie Bundesgesetz über die Forschung am Menschen Hohe Standards und liberale Normen Mit dem
GENERALCONSENT & HUMANRESEARCHACT
 SPHN Public Event Auditorium E. Rossi, Inselspital, Bern 28. August 2017 GENERALCONSENT & HUMANRESEARCHACT Prof. Dr. iur. Franziska Sprecher, Rechtsanwältin Institut für öffentliches Recht Universität
SPHN Public Event Auditorium E. Rossi, Inselspital, Bern 28. August 2017 GENERALCONSENT & HUMANRESEARCHACT Prof. Dr. iur. Franziska Sprecher, Rechtsanwältin Institut für öffentliches Recht Universität
Vereinbarung über die Vetsuisse-Fakultät der Universitäten Bern und Zürich vom (Stand )
 9.6- Vereinbarung über die Vetsuisse-Fakultät der Universitäten Bern und Zürich vom 0.05.005 (Stand 0.09.006) Die Kantone Zürich und Bern vereinbaren: Art. Ziel der Vereinbarung Ziel der vorliegenden Vereinbarung
9.6- Vereinbarung über die Vetsuisse-Fakultät der Universitäten Bern und Zürich vom 0.05.005 (Stand 0.09.006) Die Kantone Zürich und Bern vereinbaren: Art. Ziel der Vereinbarung Ziel der vorliegenden Vereinbarung
Fortpflanzungsmedizinverordnung (FMedV)
 Fortpflanzungsmedizinverordnung (FMedV) Änderung vom... Der Schweizerische Bundesrat verordnet: I Die Fortpflanzungsmedizinverordnung vom 4. Dezember 000 wird wie folgt geändert: Art. Einleitungssatz und
Fortpflanzungsmedizinverordnung (FMedV) Änderung vom... Der Schweizerische Bundesrat verordnet: I Die Fortpflanzungsmedizinverordnung vom 4. Dezember 000 wird wie folgt geändert: Art. Einleitungssatz und
Verordnung über die Organisation und den Betrieb des kantonalen Bildungszentrums für Gesundheitsberufe (BZG Kanton Solothurn)
 8.4. Verordnung über die Organisation und den Betrieb des kantonalen Bildungszentrums für Gesundheitsberufe (BZG Kanton Solothurn) RRB vom 7. März 00 Der Regierungsrat des Kantons Solothurn gestützt auf
8.4. Verordnung über die Organisation und den Betrieb des kantonalen Bildungszentrums für Gesundheitsberufe (BZG Kanton Solothurn) RRB vom 7. März 00 Der Regierungsrat des Kantons Solothurn gestützt auf
Rolle und Verantwortung der Ethik-Kommissionen bei klinischen Prüfungen
 Rolle und Verantwortung der Ethik-Kommissionen bei klinischen Prüfungen vfa /die achse: Teilnahme an klinischen Studien ja oder nein? Wissenswertes und Erfahrungen Prof. Dr. Joerg Berlin 28.1.2016 Arbeitskreis
Rolle und Verantwortung der Ethik-Kommissionen bei klinischen Prüfungen vfa /die achse: Teilnahme an klinischen Studien ja oder nein? Wissenswertes und Erfahrungen Prof. Dr. Joerg Berlin 28.1.2016 Arbeitskreis
Verordnung über besondere Fachprüfungen für Auslandschweizer und eingebürgerte Schweizer
 Verordnung 811.112.13 über besondere Fachprüfungen für Auslandschweizer und eingebürgerte Schweizer vom 18. November 1975 Das Eidgenössische Departement des Innern, gestützt auf die Artikel 115 Absatz
Verordnung 811.112.13 über besondere Fachprüfungen für Auslandschweizer und eingebürgerte Schweizer vom 18. November 1975 Das Eidgenössische Departement des Innern, gestützt auf die Artikel 115 Absatz
Vorsitzender der Ethikkommission der Bayerischen Landesärztekammer
 Prüferbewertung und Eignung von Prüfstellen Worauf achtet die Ethikkommission? Prof. Dr. Joerg Hasford Vorsitzender der Ethikkommission der Bayerischen Landesärztekammer Die nachfolgenden Ausführungen
Prüferbewertung und Eignung von Prüfstellen Worauf achtet die Ethikkommission? Prof. Dr. Joerg Hasford Vorsitzender der Ethikkommission der Bayerischen Landesärztekammer Die nachfolgenden Ausführungen
SWlSSmedic VERFÜGUNG. Bewilligung zur Herstellung von Arzneimitteln zum Grasshandel mit Arzneimitteln. Bewilligung Nr I Gesuch Nr.
 Seite 1/8 Bewilligung Nr. 506115 I Gesuch Nr. 1 02594165 VERFÜGUNG Bewilligung zur Herstellung von Arzneimitteln zum Grasshandel mit Arzneimitteln Sachverhalt - Erneuerung der Bewilligung Nr. 506115 basierend
Seite 1/8 Bewilligung Nr. 506115 I Gesuch Nr. 1 02594165 VERFÜGUNG Bewilligung zur Herstellung von Arzneimitteln zum Grasshandel mit Arzneimitteln Sachverhalt - Erneuerung der Bewilligung Nr. 506115 basierend
Generelle Bewilligung zur Offenbarung des Berufsgeheimnisses zu Forschungszwecken im Bereich der Medizin und des Gesundheitswesens
 Generelle Bewilligung zur Offenbarung des Berufsgeheimnisses zu Forschungszwecken im Bereich der Medizin und des Gesundheitswesens Die Expertenkommission für das Berufsgeheimnis in der medizinischen Forschung,
Generelle Bewilligung zur Offenbarung des Berufsgeheimnisses zu Forschungszwecken im Bereich der Medizin und des Gesundheitswesens Die Expertenkommission für das Berufsgeheimnis in der medizinischen Forschung,
Verordnung über besondere Fachprüfungen für Auslandschweizer und eingebürgerte Schweizer
 Verordnung über besondere Fachprüfungen für Auslandschweizer und eingebürgerte Schweizer vom 18. November 1975 Das Eidgenössische Departement des Innern, gestützt auf die Artikel 115 Absatz 2 bis und 116
Verordnung über besondere Fachprüfungen für Auslandschweizer und eingebürgerte Schweizer vom 18. November 1975 Das Eidgenössische Departement des Innern, gestützt auf die Artikel 115 Absatz 2 bis und 116
Gestützt auf Art. 45 der Kantonsverfassung vom 18. Mai / 14. September )
 500.50 Verordnung zum Einführungsgesetz zum Bundesgesetz über Arzneimittel und Medizinprodukte (Verordnung zum Einführungsgesetz zum Heilmittelgesetz; VOzEGzHMG) Vom. Dezember 00 (Stand. Juni 06) Gestützt
500.50 Verordnung zum Einführungsgesetz zum Bundesgesetz über Arzneimittel und Medizinprodukte (Verordnung zum Einführungsgesetz zum Heilmittelgesetz; VOzEGzHMG) Vom. Dezember 00 (Stand. Juni 06) Gestützt
Neuerstellung mit HMV4 fua
 Inhaltsverzeichnis 1 Definitionen, Begriffe, Abkürzungen... 1 Definitionen und Begriffe... 1 1.1.1 Radiopharmazeutika... 1 1.1.2 Formula-Radiopharmazeutika... 2 1.1.3 Wirkstoffe für Formula-Radiopharmazeutika
Inhaltsverzeichnis 1 Definitionen, Begriffe, Abkürzungen... 1 Definitionen und Begriffe... 1 1.1.1 Radiopharmazeutika... 1 1.1.2 Formula-Radiopharmazeutika... 2 1.1.3 Wirkstoffe für Formula-Radiopharmazeutika
Swissmedic Informationsanlass: Fach- und Medizinpersonen 20. Juni Jörg Schläpfer, Prozessentwicklung und Support, Projektleiter Umsetzung HMV IV
 Swissmedic Informationsanlass: Fach- und Medizinpersonen 20. Juni 2018 Befristete Zulassung Jörg Schläpfer, Prozessentwicklung und Support, Projektleiter Umsetzung HMV IV Swissmedic Schweizerisches Heilmittelinstitut
Swissmedic Informationsanlass: Fach- und Medizinpersonen 20. Juni 2018 Befristete Zulassung Jörg Schläpfer, Prozessentwicklung und Support, Projektleiter Umsetzung HMV IV Swissmedic Schweizerisches Heilmittelinstitut
15. Informationstagung der Fachkommission Haftpflicht Bern, 26. Mai Klinische Versuche. Ulrich Stalder Chubb Insurance Company of Europe SE
 15. Informationstagung der Fachkommission Haftpflicht Bern, 26. Mai 2014 Klinische Versuche Ulrich Stalder Chubb Insurance Company of Europe SE Agenda Wie war s bisher in der Schweiz? Neue Regelung in
15. Informationstagung der Fachkommission Haftpflicht Bern, 26. Mai 2014 Klinische Versuche Ulrich Stalder Chubb Insurance Company of Europe SE Agenda Wie war s bisher in der Schweiz? Neue Regelung in
Landesamt für Gesundheit und Soziales 1
 Landesamt für Gesundheit und Soziales 1 Ethik-Kommission des Landes Berlin Tätigkeitsbericht für das Jahr 2011 v. 30.04.2012 Das Jahr 2011 stand unter dem Zeichen der Wahrnehmung des erweiterten aufgrund
Landesamt für Gesundheit und Soziales 1 Ethik-Kommission des Landes Berlin Tätigkeitsbericht für das Jahr 2011 v. 30.04.2012 Das Jahr 2011 stand unter dem Zeichen der Wahrnehmung des erweiterten aufgrund
Gestützt auf Art. 45 der Kantonsverfassung vom 18. Mai / 14. September )
 500.50 Verordnung zum Einführungsgesetz zum Bundesgesetz über Arzneimittel und Medizinprodukte (Verordnung zum Einführungsgesetz zum Heilmittelgesetz; VOzEGzHMG) Vom. Dezember 00 (Stand. Januar 0) Gestützt
500.50 Verordnung zum Einführungsgesetz zum Bundesgesetz über Arzneimittel und Medizinprodukte (Verordnung zum Einführungsgesetz zum Heilmittelgesetz; VOzEGzHMG) Vom. Dezember 00 (Stand. Januar 0) Gestützt
Nr. 7 Verordnung zum Bundesgesetz über Aufenthalt und Niederlassung der Ausländer und zum Asylgesetz
 Nr. 7 Verordnung zum Bundesgesetz über Aufenthalt und Niederlassung der Ausländer und zum Asylgesetz vom. Dezember 000* (Stand. Januar 008) Der Regierungsrat des Kantons Luzern, gestützt auf Absatz des
Nr. 7 Verordnung zum Bundesgesetz über Aufenthalt und Niederlassung der Ausländer und zum Asylgesetz vom. Dezember 000* (Stand. Januar 008) Der Regierungsrat des Kantons Luzern, gestützt auf Absatz des
1 Allgemeine Bestimmungen
 8. Verordnung über die Anstellung der Assistenzärztinnen und Assistenzärzte sowie der Oberärztinnen und Oberärzte an den kantonalen Psychiatrieinstitutionen (AAOPV) vom 7.0.00 (Stand 0.04.00) Der Regierungsrat
8. Verordnung über die Anstellung der Assistenzärztinnen und Assistenzärzte sowie der Oberärztinnen und Oberärzte an den kantonalen Psychiatrieinstitutionen (AAOPV) vom 7.0.00 (Stand 0.04.00) Der Regierungsrat
