Einteilung der Vorlesung
|
|
|
- Werner Bayer
- vor 5 Jahren
- Abrufe
Transkript
1 Einteilung der Vorlesung VL1. Einleitung Die fundamentalen Bausteine und Kräfte der Natur VL2. Experimentelle Grundlagen der Atomphysik 2.1. Masse, Größe der Atome 2.2. Elementarladung, spezifische Ladung des Elektrons 2.3 Massenspektroskopie 2.4. Struktur der Atome, Rutherford-Streuversuch VL3. Photonen (Quanteneigenschaften des Lichts I) 3.1. Photoeffekt 3.2. Comptoneffekt VL4. Photonen (Quanteneigenschaften des Lichts II) 3.3. Gravitationseffekte des Photons 3.4. Temperaturstrahlung VL5. Materiewellen (Welleneigenschaften von Teilchen) 4.1. Beugung und Interferenz von Elektronen 4.2. Materiewellen und Wellenpakete 4.3. Heisenbergsche Unschärferelation Wim de Boer, Karlsruhe Atome und Moleküle,
2 Vorlesung 4: Das Photon Roter Faden: Eigenschaften des Photons Photoeffekt Comptonstreuung ->VL3 Gravitation Plancksche Temperaturstrahlung ->VL4 Folien auf dem Web: Teilweise benutzte Skripte: Wim de Boer, Karlsruhe Atome und Moleküle,
3 3.3. Gravitationseffekte des Photons Wim de Boer, Karlsruhe Atome und Moleküle,
4 Gravitationseffekt beim Photon Das Photon hat eine relativistische Masse m = E/c 2 = hv/c 2 und empfindet dementsprechend eine Gravitationskraft, die sich als Rotverschiebung (oder Blauverschiebung bei fallendem Photon) im Gravitationsfeld bemerkbar macht. Diese Rotverschiebung wurde im berühmten Experiment von Pound und Repka (1960) nachgewiesen: durch Gravitation verliert ein Photon bei der Höhe H nach Newtonscher Mechanik die Energie mgh = hδv und mit Photonmasse m=hv/c 2 folgt Δv/v=gH/c 2 Effekte jedoch sehr klein (Δ / für H=45m). Trick: benutze Mössbauer-Effekt um Frequenzverschiebungen sehr genau zu messen.(ps. Korrekte Beschreibung nach der Allgemeinen Relativitätstheorie ergibt für kleine Δv die gleiche Antwort) Wim de Boer, Karlsruhe Atome und Moleküle,
5 Mössbauer Effekt (Nobelpreis 1961) /tu-dresden.de/die_tu_dresden/fakultaeten/fakultaet_mathematik_und_naturwissenschaften/fachrichtung_physik/ifp/methoden/mb_spek/mb-effekt-guetlich.png Wim de Boer, Karlsruhe Atome und Moleküle,
6 Pound-Repka Versuch zur gravitativen Rotverschiebung der e.m. Strahlung 57 Co-> 57 Fe mit Emission eines Photons Pound und Repka benutzten die Schärfe der Mössbauer Linien um die sehr kleine Rotverschiebung der Photonen im Gravitationsfeld (Δ / ) in 1959 nachzuweisen durch den Abstand zwischen Quelle und Eisenabsorber bis zu 22 m zu varieren. Pound und Repka oben und unten Wim de Boer, Karlsruhe Atome und Moleküle,
7 Pound-Repka Versuch zur gravitativen Rotverschiebung der e.m. Strahlung Quelle wird sinusförmig variiert. Photondetektoren (NaI Szintlllator) messen Photonrate als Fkt. der Geschwindigkeit der Quelle. Wenn die Dopplerverschiebung Gravitationsverschiebung ausgleicht, werden Photonen absorbiert in Fe Folie und nimmt die Zählrate ab. Exp. beweist, dass für Photon gilt: m=e/c 2 =h /c 2 Wim de Boer, Karlsruhe Atome und Moleküle,
8 3.4. Temperaturstrahlung Wim de Boer, Karlsruhe Atome und Moleküle,
9 Temperaturstrahlung oder Hohlraumstrahlung oder Schwarzkörperstrahlung Strahlung eines sogenannten 'Schwarzen Körpers ist nichts anderes als ein System, das sämtliche einfallende Strahlung absorbieren soll. Am nähesten kommt man diesem Idealfall mit einem Hohlraumstrahler, der ungefähr so aussieht: klassisch Die austretende Strahlung ist unabh. vom Material und hat ein Maximum bei einer Wellenlänge, das - wie Wilhelm Wien zeigen konnte bei 2.898[ m]/t[k] liegt. D.h. je größer die Temperatur des schwarzen Körpers ist, desto weiter verschiebt sich das Maximum zu kleineren Wellenlängen hin. Das ist das Wiensche Verschiebungsgesetz. Klassisch nicht erklärbar, siehe Kurve. Wim de Boer, Karlsruhe Atome und Moleküle,
10 Rayleigh-Jeans Gesetz Die Spektralverteilungsfunktion lässt sich nach der klassischen Thermodynamik relativ einfach berechnen. Als Ergebnis erhält man die Gleichung von Rayleigh-Jeans: k B ist dabei die Boltzmannkonstante. Im vorigen Diagramm ist das als blaue Kurve dargestellt. Man sieht, dass diese Beziehung nur bei großen Wellenlängen halbwegs vernünftig mit der Spektralfunktion übereinstimmt. Je kleiner die Wellenlängen werden, desto deutlicher weicht die Rayleigh-Jeans- Kurve von der 'richtigen' Verteilung ab. Da im Nenner steht, strebt dieser Wert gegen unendlich, wenn gegen 0 geht, was man auch als 'Ultraviolettkatastrofe' bezeichnet hat. Wim de Boer, Karlsruhe Atome und Moleküle,
11 Schwarzkörperstrahlung nach Planck (ohne UV-Kat.) Für große Wellenlängen: exp(hc/ kt)=1+hc/ kt, d.h. I 1/ 4, wie vom klassischen Rayleigh _ Jeans Gesetz erwartet Wim de Boer, Karlsruhe Atome und Moleküle,
12 Das elektromagnetische Spektrum Wim de Boer, Karlsruhe Atome und Moleküle,
13 Aus Planck s Nobelpreis Rede Eventually after some weeks of the hardest work of my life, light entered the darkness, and a new inconceivable perspective opened up before me.... Because [a constant in the radiation law] represents the product of energy and time... I described it as the elementary quantum of action.... As long as it was looked on as infinitely small... everything was fine; but in the general case, however, a gap opened wide somewhere or other, which became more striking the weaker and faster the vibrations considered. Either the quantum of action was a fictional quantity, then the whole deduction of the radiation law was essentially an illusion or the derivation of the radiation law was based on a sound physical conception. In this case the quantum of action must play a fundamental role in physics, and here was something completely new, never heard of before,.. My futile attempts to put the elementary quantum of action into the classical theory continued for a number of years and they cost me a great deal of effort. Wim de Boer, Karlsruhe Atome und Moleküle,
14 Herleitung der Planckschen Strahlungsformel nach Einstein Planck erklärte seine Formel durch die Annahme, dass die Wellen in einem Hohlraum sich verhalten wie harmonische Oszillatoren, die nur diskrete Energiewerte E=nhv annehmen können und bei diesen Energien Strahlung absorbieren und emittieren. Einstein konnte in 1917, nach der Entdeckung der Photonen und die Quantisierung der Energieniveaus der Atome die Plancksche Strahlungsformel relativ einfach herleiten. Es gibt folgende Möglichkeiten für die Strahlung: a) Spontane Emission nach einem niedrigen Niveau unter Aussendung eines Photons (unabh. von Strahlungsdichte) b) Absorption eines Photons ( Photonendichte) und Übergang nach einem höheren Niveau c) Induzierte Emission ( Photonendichte) und Übergang nach einem höheren Niveau Nur nach dieser Verknüpfung von Photoeffekt, Comptonstreuung, Bohrsche Atommodell und Plancksche Strahlungsformel wurde Plancks Quantenhypothese akzeptiert. Er gilt als Gründer der Quantenmechanik. Wim de Boer, Karlsruhe Atome und Moleküle,
15 Bildliche Darstellung der möglichen Übergangen bei Schwarzkörperstrahlung N 1, N 2 sind die Besetzungszahlen 1 1 A 21, B 21, B 12 sind die Einsteinkoeffizienten Wim de Boer, Karlsruhe Atome und Moleküle,
16 Herleitung der Planckschen Streuformel nach Einstein Wim de Boer, Karlsruhe Atome und Moleküle,
17 Zusammenfassung Wim de Boer, Karlsruhe Atome und Moleküle,
18 Wiensches Verschiebungsgesetz Wim de Boer, Karlsruhe Atome und Moleküle,
19 Farbe und Helligkeit L der Sterne starke Fkt. der Temperatur: Freq. T und L T 4 Helligkeit im Bild prop. zur Fläche Blaufilter Kein Filter Rotfilter Durch Verschiebungsgesetz sind die Helligkeiten der Sterne eine starke Funktion der Farbe! Brauche mehrere Filter um Abstand zu bestimmen. Wim de Boer, Karlsruhe Atome und Moleküle,
20 Der Urknall und seine Teilchen Kosmologie Astrophysik Teilchenphysik seine Teilchen Der Urknall Siehe VL Kosmologie in WS Wim de Boer, Karlsruhe Atome und Moleküle,
21 Temperatur unseres Universums aus der kosmischen Hintergrundstrahlung Universum ist der perfekte Schwarzkörper- Strahler Wellenzahl wz=1/ in 1/cm T = ± K Dichte der Photonen 412 pro cm 3 Wellenlänge der Photonen ca. 1,5 mm, so dichteste Packung ca. (10 mm / 1.5 mm) 3 = ca. 300/cm 3, so 400 sind viele Photonen/cm 3 Wim de Boer, Karlsruhe Atome und Moleküle,
22 Temperaturentwicklung des Universums Wim de Boer, Karlsruhe Atome und Moleküle,
23 Zum Mitnehmen Planck postulierte in 1900 die Quantisierung der elektromagnetische Strahlung um die Spektralverteilung der Strahlung eines Schwarzen Körpers zu erklären. Damit war die Quantenmechanik gebohren. 18 J. später lieferte Einstein die Herleitung der Planckschen Strahlungsformel in der Form von Absorption und Emission von Photonen. Da Photonen Energie besitzen, haben sie nach E=mc 2 =hv eine Masse, die im Pound-Repka Versuch als Rotverschiebung im Gravitationsfeld beobachtet wurde. Wim de Boer, Karlsruhe Atome und Moleküle,
Vorlesung 4: Das Photon
 Vorlesung 4: Das Photon Roter Faden: Eigenschaften des Photons Photoeffekt Comptonstreuung ->VL3 Gravitation Plancksche Temperaturstrahlung ->VL4 Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/
Vorlesung 4: Das Photon Roter Faden: Eigenschaften des Photons Photoeffekt Comptonstreuung ->VL3 Gravitation Plancksche Temperaturstrahlung ->VL4 Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/
Vorlesung 4: Das Photon
 Vorlesung 4: Das Photon Roter Faden: Eigenschaften des Photons Photoeffekt Comptonstreuung ->VL3 Gravitation Plancksche Temperaturstrahlung ->VL4 Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/
Vorlesung 4: Das Photon Roter Faden: Eigenschaften des Photons Photoeffekt Comptonstreuung ->VL3 Gravitation Plancksche Temperaturstrahlung ->VL4 Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/
Einteilung der Vorlesung
 Einteilung der Vorlesung VL1. Einleitung Die fundamentalen Bausteine und Kräfte der Natur VL2. Experimentelle Grundlagen der Atomphysik 2.1. Masse, Größe der Atome 2.2. Elementarladung, spezifische Ladung
Einteilung der Vorlesung VL1. Einleitung Die fundamentalen Bausteine und Kräfte der Natur VL2. Experimentelle Grundlagen der Atomphysik 2.1. Masse, Größe der Atome 2.2. Elementarladung, spezifische Ladung
Vorlesung 3: Das Photon
 Vorlesung 3: Das Photon Roter Faden: Eigenschaften des Photons Photoeffekt Comptonstreuung ->VL3 Gravitation Plancksche Temperaturstrahlung ->VL4 Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/
Vorlesung 3: Das Photon Roter Faden: Eigenschaften des Photons Photoeffekt Comptonstreuung ->VL3 Gravitation Plancksche Temperaturstrahlung ->VL4 Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/
27. Wärmestrahlung. rmestrahlung, Quantenmechanik
 24. Vorlesung EP 27. Wärmestrahlung rmestrahlung, Quantenmechanik V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik Photometrie Plancksches Strahlungsgesetz Welle/Teilchen Dualismus für Strahlung
24. Vorlesung EP 27. Wärmestrahlung rmestrahlung, Quantenmechanik V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik Photometrie Plancksches Strahlungsgesetz Welle/Teilchen Dualismus für Strahlung
Einteilung der VL. 1. Einführung 2. Hubblesche Gesetz 3. Antigravitation 4. Gravitation 5. Entwicklung des Universums 6. Temperaturentwicklung
 Einteilung der VL 1. Einführung 2. Hubblesche Gesetz 3. Antigravitation 4. Gravitation 5. Entwicklung des Universums 6. Temperaturentwicklung HEUTE 7. Kosmische Hintergrundstrahlung 8. CMB kombiniert mit
Einteilung der VL 1. Einführung 2. Hubblesche Gesetz 3. Antigravitation 4. Gravitation 5. Entwicklung des Universums 6. Temperaturentwicklung HEUTE 7. Kosmische Hintergrundstrahlung 8. CMB kombiniert mit
Das plancksche Strahlungsgesetz Das plancksche Strahlungsgesetz
 Das plancksche Strahlungsgesetz 1 Historisch 164-177: Newton beschreibt Licht als Strom von Teilchen 1800 1900: Licht als Welle um 1900: Rätsel um die "Hohlraumstrahlung" Historisch um 1900: Rätsel um
Das plancksche Strahlungsgesetz 1 Historisch 164-177: Newton beschreibt Licht als Strom von Teilchen 1800 1900: Licht als Welle um 1900: Rätsel um die "Hohlraumstrahlung" Historisch um 1900: Rätsel um
Vorlesung 3: Das Photon
 Vorlesung 3: Das Photon Roter Faden: Eigenschaften des Photons Photoeffekt Comptonstreuung ->VL3 Gravitation Plancksche Temperaturstrahlung ->VL4 Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/
Vorlesung 3: Das Photon Roter Faden: Eigenschaften des Photons Photoeffekt Comptonstreuung ->VL3 Gravitation Plancksche Temperaturstrahlung ->VL4 Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/
Vorlesung 5: 5.1. Beugung und Interferenz von Elektronen 5.2. Materiewellen und Wellenpakete 5.3. Heisenbergsche Unschärferelation
 Vorlesung 5: Roter Faden: 5.1. Beugung und Interferenz von Elektronen 5.2. Materiewellen und Wellenpakete 5.3. Heisenbergsche Unschärferelation (Elektron: griechisch für Bernstein, der durch Reibung elektrostatisch
Vorlesung 5: Roter Faden: 5.1. Beugung und Interferenz von Elektronen 5.2. Materiewellen und Wellenpakete 5.3. Heisenbergsche Unschärferelation (Elektron: griechisch für Bernstein, der durch Reibung elektrostatisch
27. Wärmestrahlung. rmestrahlung, Quantenmechanik
 25. Vorlesung EP 27. Wärmestrahlung V. STRAHLUNG, ATOME, KERNE 27. Wä (Fortsetzung) Photometrie Plancksches Strahlungsgesetz Welle/Teilchen Dualismus für Strahlung und Materie Versuche: Quadratisches Abstandsgesetz
25. Vorlesung EP 27. Wärmestrahlung V. STRAHLUNG, ATOME, KERNE 27. Wä (Fortsetzung) Photometrie Plancksches Strahlungsgesetz Welle/Teilchen Dualismus für Strahlung und Materie Versuche: Quadratisches Abstandsgesetz
Vorlesung 6: Roter Faden: Schrödingergleichung als Wellengleichung der Materie. Messungen in der Quantenmechanik
 Vorlesung 6: Roter Faden: Schrödingergleichung als Wellengleichung der Materie Messungen in der Quantenmechanik Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Wim de Boer, Karlsruhe
Vorlesung 6: Roter Faden: Schrödingergleichung als Wellengleichung der Materie Messungen in der Quantenmechanik Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Wim de Boer, Karlsruhe
Einteilung der Vorlesung
 Einteilung der Vorlesung VL1. Einleitung Die fundamentalen Bausteine und Kräfte der Natur VL2. Experimentelle Grundlagen der Atomphysik 2.1. Masse, Größe der Atome 2.2. Elementarladung, spezifische Ladung
Einteilung der Vorlesung VL1. Einleitung Die fundamentalen Bausteine und Kräfte der Natur VL2. Experimentelle Grundlagen der Atomphysik 2.1. Masse, Größe der Atome 2.2. Elementarladung, spezifische Ladung
Vorlesung 9: Roter Faden: Wiederholung Quantisierung der Energien in QM. Franck-Hertz Versuch. Emissions- und Absorptionsspektren der Atome
 Vorlesung 9: Roter Faden: Wiederholung Quantisierung der Energien in QM Franck-Hertz Versuch Emissions- und Absorptionsspektren der Atome Spektren des Wasserstoffatoms Bohrsche Atommodell Folien auf dem
Vorlesung 9: Roter Faden: Wiederholung Quantisierung der Energien in QM Franck-Hertz Versuch Emissions- und Absorptionsspektren der Atome Spektren des Wasserstoffatoms Bohrsche Atommodell Folien auf dem
Elemente der Quantenmechanik III 9.1. Schrödingergleichung mit beliebigem Potential 9.2. Harmonischer Oszillator 9.3. Drehimpulsoperator
 VL 8 VL8. VL9. VL10. Das Wasserstoffatom in der klass. Mechanik 8.1. Emissions- und Absorptionsspektren der Atome 8.2. Quantelung der Energie (Frank-Hertz Versuch) 8.3. Bohrsches Atommodell 8.4. Spektren
VL 8 VL8. VL9. VL10. Das Wasserstoffatom in der klass. Mechanik 8.1. Emissions- und Absorptionsspektren der Atome 8.2. Quantelung der Energie (Frank-Hertz Versuch) 8.3. Bohrsches Atommodell 8.4. Spektren
Vorlesung 6: Roter Faden: Schrödingergleichung als Wellengleichung der Materie. Messungen in der Quantenmechanik
 Vorlesung 6: Roter Faden: Schrödingergleichung als Wellengleichung der Materie Messungen in der Quantenmechanik Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Wim de Boer, Karlsruhe
Vorlesung 6: Roter Faden: Schrödingergleichung als Wellengleichung der Materie Messungen in der Quantenmechanik Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Wim de Boer, Karlsruhe
CMB Echo des Urknalls. Max Camenzind Februar 2015
 CMB Echo des Urknalls Max Camenzind Februar 2015 Lemaître 1931: Big Bang des expandierenden Universums Big Bang : Photonenhintergrund + Neutrinohintergrund 3-Raum expandiert: dx a(t) dx ; Wellenlängen
CMB Echo des Urknalls Max Camenzind Februar 2015 Lemaître 1931: Big Bang des expandierenden Universums Big Bang : Photonenhintergrund + Neutrinohintergrund 3-Raum expandiert: dx a(t) dx ; Wellenlängen
Wim de Boer, Karlsruhe Kosmologie VL,
 Vorlesung 5: Roter Faden: 1. Temperaturentwicklung des Universums 2. Kernsynthese 3. CMB=cosmic microwave background = kosmische Hintergrundstrahlung. Wim de Boer, Karlsruhe Kosmologie VL, 16.11.2010 1
Vorlesung 5: Roter Faden: 1. Temperaturentwicklung des Universums 2. Kernsynthese 3. CMB=cosmic microwave background = kosmische Hintergrundstrahlung. Wim de Boer, Karlsruhe Kosmologie VL, 16.11.2010 1
Klassische Mechanik. Elektrodynamik. Thermodynamik. Der Stand der Physik am Beginn des 20. Jahrhunderts. Relativitätstheorie?
 Der Stand der Physik am Beginn des 20. Jahrhunderts Klassische Mechanik Newton-Axiome Relativitätstheorie? Maxwell-Gleichungen ok Elektrodynamik Thermodynamik Hauptsätze der Therm. Quantentheorie S.Alexandrova
Der Stand der Physik am Beginn des 20. Jahrhunderts Klassische Mechanik Newton-Axiome Relativitätstheorie? Maxwell-Gleichungen ok Elektrodynamik Thermodynamik Hauptsätze der Therm. Quantentheorie S.Alexandrova
Vorlesung 9: Roter Faden: Franck-Hertz Versuch. Emissions- und Absorptionsspektren der Atome. Spektren des Wasserstoffatoms. Bohrsche Atommodell
 Vorlesung 9: Roter Faden: Franck-Hertz Versuch Emissions- und Absorptionsspektren der Atome Spektren des Wasserstoffatoms Bohrsche Atommodell Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/
Vorlesung 9: Roter Faden: Franck-Hertz Versuch Emissions- und Absorptionsspektren der Atome Spektren des Wasserstoffatoms Bohrsche Atommodell Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/
2. Max Planck und das Wirkungsquantum h
 2. Max Planck und das Wirkungsquantum h Frequenzverteilung eines schwarzen Strahlers Am 6. Dezember 1900, dem 'Geburtsdatum' der modernen Physik, hatte Max Planck endlich die Antwort auf eine Frage gefunden,
2. Max Planck und das Wirkungsquantum h Frequenzverteilung eines schwarzen Strahlers Am 6. Dezember 1900, dem 'Geburtsdatum' der modernen Physik, hatte Max Planck endlich die Antwort auf eine Frage gefunden,
22. Wärmestrahlung. rmestrahlung, Quantenmechanik
 22. Wärmestrahlung rmestrahlung, Quantenmechanik Plancksches Strahlungsgesetz: Planck (1904): der Austausch von Energie zwischen dem strahlenden System und dem Strahlungsfeld kann nur in Einheiten von
22. Wärmestrahlung rmestrahlung, Quantenmechanik Plancksches Strahlungsgesetz: Planck (1904): der Austausch von Energie zwischen dem strahlenden System und dem Strahlungsfeld kann nur in Einheiten von
Moderne Physik. von Paul A. Tipler und Ralph A. LIewellyn. Oldenbourg Verlag München Wien
 Moderne Physik von Paul A. Tipler und Ralph A. LIewellyn Oldenbourg Verlag München Wien Inhaltsverzeichnis I Relativitätstheorie und Quantenmechanik: Die Grundlagen der modernen Physik 1 1 Relativitätstheorie
Moderne Physik von Paul A. Tipler und Ralph A. LIewellyn Oldenbourg Verlag München Wien Inhaltsverzeichnis I Relativitätstheorie und Quantenmechanik: Die Grundlagen der modernen Physik 1 1 Relativitätstheorie
Vorlesung 5: 5.1. Beugung und Interferenz von Elektronen 5.2. Materiewellen und Wellenpakete 5.3. Heisenbergsche Unschärferelation
 Vorlesung 5: Roter Faden: 5.1. Beugung und Interferenz von Elektronen 5.2. Materiewellen und Wellenpakete 5.3. Heisenbergsche Unschärferelation (Elektron: griechisch für Bernstein, der durch Reibung elektrostatisch
Vorlesung 5: Roter Faden: 5.1. Beugung und Interferenz von Elektronen 5.2. Materiewellen und Wellenpakete 5.3. Heisenbergsche Unschärferelation (Elektron: griechisch für Bernstein, der durch Reibung elektrostatisch
Vorlesung 5: 5.1. Beugung und Interferenz von Elektronen 5.2. Materiewellen und Wellenpakete 5.3. Heisenbergsche Unschärferelation
 Vorlesung 5: Roter Faden: 5.1. Beugung und Interferenz von Elektronen 5.2. Materiewellen und Wellenpakete 5.3. Heisenbergsche Unschärferelation (Elektron: griechisch für Bernstein, der durch Reibung elektrostatisch
Vorlesung 5: Roter Faden: 5.1. Beugung und Interferenz von Elektronen 5.2. Materiewellen und Wellenpakete 5.3. Heisenbergsche Unschärferelation (Elektron: griechisch für Bernstein, der durch Reibung elektrostatisch
Physik für Maschinenbau. Prof. Dr. Stefan Schael RWTH Aachen
 Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
Eigenschaften des Photons
 Eigenschaften des Photons Das Photon ist das Energiequant der elektromagnetischen Wellen, d.h. Licht hat wie von Einstein postuliert nicht nur Wellencharakter, sondern auch Teilchencharakter mit den oben
Eigenschaften des Photons Das Photon ist das Energiequant der elektromagnetischen Wellen, d.h. Licht hat wie von Einstein postuliert nicht nur Wellencharakter, sondern auch Teilchencharakter mit den oben
VL 20 VL Mehrelektronensysteme VL Periodensystem VL Röntgenstrahlung
 VL 20 VL 18 18.1. Mehrelektronensysteme VL 19 19.1. Periodensystem VL 20 20.1. Röntgenstrahlung Wim de Boer, Karlsruhe Atome und Moleküle, 27.06.2013 1 Vorlesung 20: Roter Faden: Röntgenstrahlung Folien
VL 20 VL 18 18.1. Mehrelektronensysteme VL 19 19.1. Periodensystem VL 20 20.1. Röntgenstrahlung Wim de Boer, Karlsruhe Atome und Moleküle, 27.06.2013 1 Vorlesung 20: Roter Faden: Röntgenstrahlung Folien
1. Auf dem Weg zur Quantentheorie Grundlegende Experimente und Erkenntnisse
 1. Auf dem Weg zur Quantentheorie Grundlegende Experimente und Erkenntnisse 1.1. Theorie der Wärmestrahlung Plancksche Strahlenhypothese Untersuchungen der Hohlraumstrahlung vor 1900 zeigten, dass das
1. Auf dem Weg zur Quantentheorie Grundlegende Experimente und Erkenntnisse 1.1. Theorie der Wärmestrahlung Plancksche Strahlenhypothese Untersuchungen der Hohlraumstrahlung vor 1900 zeigten, dass das
Eigenschaften des Photons
 Eigenschaften des Photons Das Photon ist das Energiequant der elektromagnetischen Wellen, d.h. Licht hat wie von Einstein postuliert nicht nur Wellencharakter, sondern auch Teilchencharakter mit den oben
Eigenschaften des Photons Das Photon ist das Energiequant der elektromagnetischen Wellen, d.h. Licht hat wie von Einstein postuliert nicht nur Wellencharakter, sondern auch Teilchencharakter mit den oben
Moderne Physik. von Paul A.Tipler und Ralph A. Liewellyn
 Moderne Physik von Paul A.Tipler und Ralph A. Liewellyn Aus dem Englischen von Dr. Anna Schleitzer Bearbeitet von Prof. Dr. Gerd Czycholl Prof. Dr. Cornelius Noack Prof. Dr. Udo Strohbusch 2., verbesserte
Moderne Physik von Paul A.Tipler und Ralph A. Liewellyn Aus dem Englischen von Dr. Anna Schleitzer Bearbeitet von Prof. Dr. Gerd Czycholl Prof. Dr. Cornelius Noack Prof. Dr. Udo Strohbusch 2., verbesserte
Vorlesung 19: Roter Faden: Röntgenstrahlung Laserprinzip. Siehe auch: Demtröder, Experimentalphysik 3, Springerverlag
 Vorlesung 19: Roter Faden: Röntgenstrahlung Laserprinzip Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: Demtröder, Experimentalphysik 3, Springerverlag Juni 21, 2005 Atomphysik
Vorlesung 19: Roter Faden: Röntgenstrahlung Laserprinzip Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: Demtröder, Experimentalphysik 3, Springerverlag Juni 21, 2005 Atomphysik
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung 18: Roter Faden: Röntgenstrahlung. Folien auf dem Web:
 Vorlesung 18: Roter Faden: Röntgenstrahlung Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ h i k h / d / Siehe auch: http://www.wmi.badw.de/teaching/lecturenotes/index.html http://www.uni-stuttgart.de/ipf/lehre/online-skript/
Vorlesung 18: Roter Faden: Röntgenstrahlung Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ h i k h / d / Siehe auch: http://www.wmi.badw.de/teaching/lecturenotes/index.html http://www.uni-stuttgart.de/ipf/lehre/online-skript/
23. Vorlesung EP. IV Optik 26. Beugung (Wellenoptik) V Strahlung, Atome, Kerne 27. Wärmestrahlung und Quantenmechanik
 23. Vorlesung EP IV Optik 26. Beugung (Wellenoptik) V Strahlung, Atome, Kerne 27. Wärmestrahlung und Quantenmechanik Strahlung: Stoff der Optik, Wärme-, Elektrizitätslehre u. Quantenphysik Photometrie
23. Vorlesung EP IV Optik 26. Beugung (Wellenoptik) V Strahlung, Atome, Kerne 27. Wärmestrahlung und Quantenmechanik Strahlung: Stoff der Optik, Wärme-, Elektrizitätslehre u. Quantenphysik Photometrie
Quantenmechanik. Eine Kurzvorstellung für Nicht-Physiker
 Quantenmechanik Eine Kurzvorstellung für Nicht-Physiker Die Quantenvorstellung Der Ursprung: Hohlraumstrahlung Das Verhalten eines Von Interesse: idealen Absorbers Energiedichte in Abhängigkeit zur Wellenlänge
Quantenmechanik Eine Kurzvorstellung für Nicht-Physiker Die Quantenvorstellung Der Ursprung: Hohlraumstrahlung Das Verhalten eines Von Interesse: idealen Absorbers Energiedichte in Abhängigkeit zur Wellenlänge
Max Planck: Das plancksche Wirkungsquantum
 Max Planck: Das plancksche Wirkungsquantum Überblick Person Max Planck Prinzip schwarzer Strahler Klassische Strahlungsgesetze Planck sches Strahlungsgesetz Beispiele kosmische Hintergrundstrahlung Sternspektren
Max Planck: Das plancksche Wirkungsquantum Überblick Person Max Planck Prinzip schwarzer Strahler Klassische Strahlungsgesetze Planck sches Strahlungsgesetz Beispiele kosmische Hintergrundstrahlung Sternspektren
Thema heute: Aufbau der Materie: Das Bohr sche Atommodell
 Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
SS 2015 Supplement to Experimental Physics 2 (LB-Technik) Prof. E. Resconi
 Quantenmechanik des Wasserstoff-Atoms [Kap. 8-10 Haken-Wolf Atom- und Quantenphysik ] - Der Aufbau der Atome Quantenmechanik ==> Atomphysik Niels Bohr, 1913: kritische Entwicklung, die schließlich Plancks
Quantenmechanik des Wasserstoff-Atoms [Kap. 8-10 Haken-Wolf Atom- und Quantenphysik ] - Der Aufbau der Atome Quantenmechanik ==> Atomphysik Niels Bohr, 1913: kritische Entwicklung, die schließlich Plancks
Grundlagen der Quantenmechanik wie sie in der Spektroskopie benötigt werden. Jürgen Stohner ZHW Winter 2007/8
 Grundlagen der Quantenmechanik wie sie in der Spektroskopie benötigt werden Jürgen Stohner ZHW Winter 2007/8 Inhaltsübersicht Kap. 1 von Welle und Teilchen Einleitung Welleneigenschaften von Licht: Beugung
Grundlagen der Quantenmechanik wie sie in der Spektroskopie benötigt werden Jürgen Stohner ZHW Winter 2007/8 Inhaltsübersicht Kap. 1 von Welle und Teilchen Einleitung Welleneigenschaften von Licht: Beugung
VL6. Elemente der Quantenmechanik I 6.1. Schrödingergleichung als Wellengleichung der Materie 6.2. Messungen in der Quantenmechanik
 VL7 VL6. Elemente der Quantenmechanik I 6.1. Schrödingergleichung als Wellengleichung der Materie 6.2. Messungen in der Quantenmechanik VL7. Elemente der Quantenmechanik II 7.1. Wellenpakete als Lösungen
VL7 VL6. Elemente der Quantenmechanik I 6.1. Schrödingergleichung als Wellengleichung der Materie 6.2. Messungen in der Quantenmechanik VL7. Elemente der Quantenmechanik II 7.1. Wellenpakete als Lösungen
Projektarbeit zur Schwarzkörperstrahlung
 Projektarbeit zur Schwarzkörperstrahlung Quantenmechanik SS 004 Gruppe 9 Gruppenmitglieder Simon Außerlechner Florian Hebenstreit Martin Horn Alexander Reinmüller Christoph Stieb Inhaltverzeichnis. Einleitung....
Projektarbeit zur Schwarzkörperstrahlung Quantenmechanik SS 004 Gruppe 9 Gruppenmitglieder Simon Außerlechner Florian Hebenstreit Martin Horn Alexander Reinmüller Christoph Stieb Inhaltverzeichnis. Einleitung....
Einführung in die Quantentheorie der Atome und Photonen
 Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
1 Physikalische Hintergrunde: Teilchen oder Welle?
 Skript zur 1. Vorlesung Quantenmechanik, Montag den 11. April, 2011. 1 Physikalische Hintergrunde: Teilchen oder Welle? 1.1 Geschichtliches: Warum Quantenmechanik? Bis 1900: klassische Physik Newtonsche
Skript zur 1. Vorlesung Quantenmechanik, Montag den 11. April, 2011. 1 Physikalische Hintergrunde: Teilchen oder Welle? 1.1 Geschichtliches: Warum Quantenmechanik? Bis 1900: klassische Physik Newtonsche
Einteilung der VL. Wim de Boer, Karlsruhe Kosmologie VL,
 Einteilung der VL 1. Einführung 2. Hubblesche Gesetz 3. Antigravitation 4. Gravitation und ART HEUTE 5. Entwicklung des Universums 6. Temperaturentwicklung 7. Kosmische Hintergrundstrahlung 8. CMB kombiniert
Einteilung der VL 1. Einführung 2. Hubblesche Gesetz 3. Antigravitation 4. Gravitation und ART HEUTE 5. Entwicklung des Universums 6. Temperaturentwicklung 7. Kosmische Hintergrundstrahlung 8. CMB kombiniert
VL 21 VL Mehrelektronensysteme VL Periodensystem VL Röntgenstrahlung.
 VL 21 VL 19 19.1. Mehrelektronensysteme VL 20 20.1. Periodensystem VL 21 21.1. Röntgenstrahlung. Wim de Boer, Karlsruhe Atome und Moleküle, 05.07.2012 1 Vorlesung 21: Roter Faden: Röntgenstrahlung Folien
VL 21 VL 19 19.1. Mehrelektronensysteme VL 20 20.1. Periodensystem VL 21 21.1. Röntgenstrahlung. Wim de Boer, Karlsruhe Atome und Moleküle, 05.07.2012 1 Vorlesung 21: Roter Faden: Röntgenstrahlung Folien
Einteilung der Vorlesung
 Einteilung der Vorlesung 1. Einleitung Die fundamentalen Bausteine und Kräfte der Natur 2. Experimentelle Grundlagen der Atomphysik 2.1. Größe der Atome 2.2. Elementarladung, spezifische Ladung des Elektrons
Einteilung der Vorlesung 1. Einleitung Die fundamentalen Bausteine und Kräfte der Natur 2. Experimentelle Grundlagen der Atomphysik 2.1. Größe der Atome 2.2. Elementarladung, spezifische Ladung des Elektrons
VL6. Elemente der Quantenmechanik I 6.1. Schrödingergleichung als Wellengleichung der Materie 6.2. Messungen in der Quantenmechanik
 VL7 VL6. Elemente der Quantenmechanik I 6.1. Schrödingergleichung als Wellengleichung der Materie 6.2. Messungen in der Quantenmechanik VL7. Elemente der Quantenmechanik II 7.1. Wellenpakete als Lösungen
VL7 VL6. Elemente der Quantenmechanik I 6.1. Schrödingergleichung als Wellengleichung der Materie 6.2. Messungen in der Quantenmechanik VL7. Elemente der Quantenmechanik II 7.1. Wellenpakete als Lösungen
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester #25 03/12/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
Physik für Mediziner im 1. Fachsemester #25 03/12/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
Vorlesung 21: Roter Faden: Das Elektron als Welle Heisenbergsche Unsicherheitsrelation. Versuch: Gasentladung
 Vorlesung 21: Roter Faden: Das Elektron als Welle Heisenbergsche Unsicherheitsrelation Versuch: Gasentladung Juli 7, 2006 Ausgewählte Kapitel der Physik, Prof. W. de Boer 1 Erste Experimente mit Elektronen
Vorlesung 21: Roter Faden: Das Elektron als Welle Heisenbergsche Unsicherheitsrelation Versuch: Gasentladung Juli 7, 2006 Ausgewählte Kapitel der Physik, Prof. W. de Boer 1 Erste Experimente mit Elektronen
Vorlesung 20: Roter Faden: Auswahlregeln. Folien auf dem Web:
 Vorlesung 20: Roter Faden: Auswahlregeln Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: http://www.uni-stuttgart.de/ipf/lehre/online-skript/ Wim de Boer, Karlsruhe Atome
Vorlesung 20: Roter Faden: Auswahlregeln Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: http://www.uni-stuttgart.de/ipf/lehre/online-skript/ Wim de Boer, Karlsruhe Atome
Vorlesung 14: Roter Faden: Wiederholung Lamb-Shift. Hyperfeinstruktur. Folien auf dem Web:
 Vorlesung 14: Roter Faden: Wiederholung Lamb-Shift Anomaler Zeeman-Effekt Hyperfeinstruktur Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ h i k h / d / Siehe auch: http://www.uni-stuttgart.de/ipf/lehre/online-skript/
Vorlesung 14: Roter Faden: Wiederholung Lamb-Shift Anomaler Zeeman-Effekt Hyperfeinstruktur Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ h i k h / d / Siehe auch: http://www.uni-stuttgart.de/ipf/lehre/online-skript/
VL 20 VL Mehrelektronensysteme VL Periodensystem VL Röntgenstrahlung
 VL 20 VL 18 18.1. Mehrelektronensysteme VL 19 19.1. Periodensystem VL 20 20.1. Röntgenstrahlung Wim de Boer, Karlsruhe Atome und Moleküle, 27.06.2013 1 Vorlesung 20: Roter Faden: Röntgenstrahlung Folien
VL 20 VL 18 18.1. Mehrelektronensysteme VL 19 19.1. Periodensystem VL 20 20.1. Röntgenstrahlung Wim de Boer, Karlsruhe Atome und Moleküle, 27.06.2013 1 Vorlesung 20: Roter Faden: Röntgenstrahlung Folien
Für Geowissenschaftler. EP WS 2009/10 Dünnweber/Faessler
 Für Geowissenschaftler Termin Nachholklausur Vorschlag Mittwoch 14.4.10 25. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung und Quantenmechanik Photometrie Plancksches Strahlungsgesetze, Welle/Teilchen
Für Geowissenschaftler Termin Nachholklausur Vorschlag Mittwoch 14.4.10 25. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung und Quantenmechanik Photometrie Plancksches Strahlungsgesetze, Welle/Teilchen
c. Bestimme die Gesamtenergie der im Objekt gespeicherten elektromagnetischen Strahlung durch Aufsummieren der Energie der einzelnen Moden.
 phys4.05 Page 1 3.5.1 Der 1D schwarze Strahler: Objekt der Länge L und Durchmesser D
phys4.05 Page 1 3.5.1 Der 1D schwarze Strahler: Objekt der Länge L und Durchmesser D
10 Teilchen und Wellen. 10.1 Strahlung schwarzer Körper
 10 Teilchen und Wellen Teilchen: m, V, p, r, E, lokalisierbar Wellen: l, f, p, E, unendlich ausgedehnt (harmonische Welle) Unterscheidung: Wellen interferieren 10.1 Strahlung schwarzer Körper JEDER Körper
10 Teilchen und Wellen Teilchen: m, V, p, r, E, lokalisierbar Wellen: l, f, p, E, unendlich ausgedehnt (harmonische Welle) Unterscheidung: Wellen interferieren 10.1 Strahlung schwarzer Körper JEDER Körper
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 007 Vladimir Dyakonov #16 am 0.0.007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 007 Vladimir Dyakonov #16 am 0.0.007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Einführung in die Astronomie und Astrophysik I
 Einführung in die Astronomie und Astrophysik I Teil 7 Jochen Liske Fachbereich Physik Hamburger Sternwarte jochen.liske@uni-hamburg.de Astronomische Nachricht der Woche Astronomische Nachricht der Woche
Einführung in die Astronomie und Astrophysik I Teil 7 Jochen Liske Fachbereich Physik Hamburger Sternwarte jochen.liske@uni-hamburg.de Astronomische Nachricht der Woche Astronomische Nachricht der Woche
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester #26 08/12/2010 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
Physik für Mediziner im 1. Fachsemester #26 08/12/2010 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
VL 12. VL11. Das Wasserstofatom in der QM II Energiezustände des Wasserstoffatoms Radiale Abhängigkeit (Laguerre-Polynome)
 VL 12 VL11. Das Wasserstofatom in der QM II 11.1. Energiezustände des Wasserstoffatoms 11.2. Radiale Abhängigkeit (Laguerre-Polynome) VL12. Spin-Bahn-Kopplung (I) 12.1 Bahnmagnetismus (Zeeman-Effekt) 12.2
VL 12 VL11. Das Wasserstofatom in der QM II 11.1. Energiezustände des Wasserstoffatoms 11.2. Radiale Abhängigkeit (Laguerre-Polynome) VL12. Spin-Bahn-Kopplung (I) 12.1 Bahnmagnetismus (Zeeman-Effekt) 12.2
Die seltsame Welt der Quanten
 Saturday Morning Physics Die seltsame Welt der Quanten Wie spielt Gott sein Würfelspiel? 12. 11. 2005 Gernot Alber und Gerhard Birkl Institut für Angewandte Physik Technische Universität Darmstadt gernot.alber@physik.tu-darmstadt.de
Saturday Morning Physics Die seltsame Welt der Quanten Wie spielt Gott sein Würfelspiel? 12. 11. 2005 Gernot Alber und Gerhard Birkl Institut für Angewandte Physik Technische Universität Darmstadt gernot.alber@physik.tu-darmstadt.de
Einführung in die Quantenphysik
 Einführung in die Quantenphysik Klassische Optik Der lichtelektrische Effekt Effekte elektromagnetischer Strahlung Kopenhagen-Interpretation Elektronen Quantenphysik und klassische Physik Atomphysik Klassische
Einführung in die Quantenphysik Klassische Optik Der lichtelektrische Effekt Effekte elektromagnetischer Strahlung Kopenhagen-Interpretation Elektronen Quantenphysik und klassische Physik Atomphysik Klassische
Spektren von Himmelskörpern
 Spektren von Himmelskörpern Inkohärente Lichtquellen Tobias Schulte 25.05.2016 1 Gliederung Schwarzkörperstrahlung Spektrum der Sonne Spektralklassen Hertzsprung Russell Diagramm Scheinbare und absolute
Spektren von Himmelskörpern Inkohärente Lichtquellen Tobias Schulte 25.05.2016 1 Gliederung Schwarzkörperstrahlung Spektrum der Sonne Spektralklassen Hertzsprung Russell Diagramm Scheinbare und absolute
PN 2 Einführung in die Experimentalphysik für Chemiker
 PN 2 Einführung in die Experimentalphysik für Chemiker 12. Vorlesung 4.7.08 Evelyn Plötz, Thomas Schmierer, Gunnar Spieß, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
PN 2 Einführung in die Experimentalphysik für Chemiker 12. Vorlesung 4.7.08 Evelyn Plötz, Thomas Schmierer, Gunnar Spieß, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
Einteilung der VL. Wim de Boer, Karlsruhe Kosmologie VL,
 Einteilung der VL 1. Einführung 2. Hubblesche Gesetz 3. Gravitation 4. Evolution des Universum 5. Temperaturentwicklung 6. Kosmische Hintergrundstrahlung 7. CMB kombiniert mit SN1a 8. Strukturbildung 9.
Einteilung der VL 1. Einführung 2. Hubblesche Gesetz 3. Gravitation 4. Evolution des Universum 5. Temperaturentwicklung 6. Kosmische Hintergrundstrahlung 7. CMB kombiniert mit SN1a 8. Strukturbildung 9.
Bohrsches Atommodell / Linienspektren. Experimentalphysik für Biologen und Chemiker, O. Benson & A. Peters, Humboldt-Universität zu Berlin
 Bohrsches Atommodell / Linienspektren Quantenstruktur der Atome: Atomspektren Emissionslinienspektren von Wasserstoffatomen im sichtbaren Bereich Balmer Serie (1885): 1 / λ = K (1/4-1/n 2 ) 656.28 486.13
Bohrsches Atommodell / Linienspektren Quantenstruktur der Atome: Atomspektren Emissionslinienspektren von Wasserstoffatomen im sichtbaren Bereich Balmer Serie (1885): 1 / λ = K (1/4-1/n 2 ) 656.28 486.13
Wärmestrahlung. Einfallende Strahlung = absorbierte Strahlung + reflektierte Strahlung
 Wärmestrahlung Gleichheit von Absorptions- und Emissionsgrad Zwei Flächen auf gleicher Temperatur T 1 stehen sich gegenüber. dunkelgrau hellgrau Der Wärmefluss durch Strahlung muss in beiden Richtungen
Wärmestrahlung Gleichheit von Absorptions- und Emissionsgrad Zwei Flächen auf gleicher Temperatur T 1 stehen sich gegenüber. dunkelgrau hellgrau Der Wärmefluss durch Strahlung muss in beiden Richtungen
Physik IV Einführung in die Atomistik und die Struktur der Materie
 Physik IV Einführung in die Atomistik und die Struktur der Materie Sommersemester 011 Vorlesung 04 1.04.011 Physik IV - Einführung in die Atomistik Vorlesung 4 Prof. Thorsten Kröll 1.04.011 1 Versuch OH
Physik IV Einführung in die Atomistik und die Struktur der Materie Sommersemester 011 Vorlesung 04 1.04.011 Physik IV - Einführung in die Atomistik Vorlesung 4 Prof. Thorsten Kröll 1.04.011 1 Versuch OH
Vorlesung 2: Roter Faden: Größe der Atome Massenspektroskopie Atomstruktur aus. Folien auf dem Web:
 Vorlesung 2: Roter Faden: Größe der Atome Massenspektroskopie p Atomstruktur aus Rutherfordstreuung (1911) Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Wim de Boer, Karlsruhe Atome
Vorlesung 2: Roter Faden: Größe der Atome Massenspektroskopie p Atomstruktur aus Rutherfordstreuung (1911) Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Wim de Boer, Karlsruhe Atome
Hallwachs-Experiment. Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe
 Hallwachs-Experiment Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe 20.09.2012 Skizziere das Experiment Notiere und Interpretiere die Beobachtungen Photoeffekt Bestrahlt
Hallwachs-Experiment Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe 20.09.2012 Skizziere das Experiment Notiere und Interpretiere die Beobachtungen Photoeffekt Bestrahlt
Von der kosmischen Hintergrundstrahlung zur Heisenbergschen Unbestimmtheitsrelation. eine Einführung in die Quantenmechanik
 Von der kosmischen Hintergrundstrahlung zur Heisenbergschen Unbestimmtheitsrelation eine Einführung in die Quantenmechanik 1) Die Hohlraumstrahlung: Geburt der Quantenmechanik Die kosmische Hintergrundstrahlung
Von der kosmischen Hintergrundstrahlung zur Heisenbergschen Unbestimmtheitsrelation eine Einführung in die Quantenmechanik 1) Die Hohlraumstrahlung: Geburt der Quantenmechanik Die kosmische Hintergrundstrahlung
Inhalt der Vorlesung PC2 WS2012_13
 Inhalt der Vorlesung PC2 WS2012_13 Nachtrag PC 1 11. Elektrochemie/Elektrochemische Zellen 11.1 Einführung 11.2 Elektrochemische Zellen 11.3 Zelldiagramme und Elektrodenreaktionen 11.4 Thermodynamische
Inhalt der Vorlesung PC2 WS2012_13 Nachtrag PC 1 11. Elektrochemie/Elektrochemische Zellen 11.1 Einführung 11.2 Elektrochemische Zellen 11.3 Zelldiagramme und Elektrodenreaktionen 11.4 Thermodynamische
Grundlagen der Quantentheorie
 Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Vorlesung 24: Roter Faden: Wiederholung Quantisierung der Energien in QM. Emissions- und Absorptionsspektren der Atome
 Vorlesung 24: Roter Faden: Wiederholung Quantisierung der Energien in QM Franck-Hertz Versuch Emissions- und Absorptionsspektren der Atome Spektren des Wasserstoffatoms Bohrsche Atommodell Lösung der Schrödingergleichung
Vorlesung 24: Roter Faden: Wiederholung Quantisierung der Energien in QM Franck-Hertz Versuch Emissions- und Absorptionsspektren der Atome Spektren des Wasserstoffatoms Bohrsche Atommodell Lösung der Schrödingergleichung
Vorlesung 2: Größe der Atome Massenspektroskopie Atomstruktur aus Rutherfordstreuung (1911)
 Vorlesung 2: Roter Faden: Größe der Atome Massenspektroskopie Atomstruktur aus Rutherfordstreuung (1911) Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Wim de Boer, Karlsruhe Atome
Vorlesung 2: Roter Faden: Größe der Atome Massenspektroskopie Atomstruktur aus Rutherfordstreuung (1911) Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Wim de Boer, Karlsruhe Atome
Elementarteilchenphysik
 Masterclass 2011 Elementarteilchenphysik Robert Harlander Bergische Universität Wuppertal 9. März 2011 Robert Harlander Masterclass Uni Wuppertal p. 1 Elementarteilchenphysik Zentrale Fragen: Was sind
Masterclass 2011 Elementarteilchenphysik Robert Harlander Bergische Universität Wuppertal 9. März 2011 Robert Harlander Masterclass Uni Wuppertal p. 1 Elementarteilchenphysik Zentrale Fragen: Was sind
14 Teilchen und Wellen
 14 Teilchen und Wellen 14.1 Teilchencharakter von elektromagnetischen Wellen 1411 14.1.1 Strahlung schwarzer Körper 14.1.2 Der Photoeffekt 14.1.3 Technische Anwendungen 14.2 Wellencharakter von Teilchen
14 Teilchen und Wellen 14.1 Teilchencharakter von elektromagnetischen Wellen 1411 14.1.1 Strahlung schwarzer Körper 14.1.2 Der Photoeffekt 14.1.3 Technische Anwendungen 14.2 Wellencharakter von Teilchen
Akkomodation des Auges
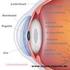 Das Auge Akkomodation des Auges 4 Kurzsichtiges Auge mit Zerstreuungslinse zur Korrektur (um entfernte Objekte scharf zu sehen): 5 Weitsichtiges Auge mit Sammellinse zur Korrektur (für nahe Objekte):
Das Auge Akkomodation des Auges 4 Kurzsichtiges Auge mit Zerstreuungslinse zur Korrektur (um entfernte Objekte scharf zu sehen): 5 Weitsichtiges Auge mit Sammellinse zur Korrektur (für nahe Objekte):
Atome - Moleküle - Kerne
 Atome - Moleküle - Kerne Band I Atomphysik Von Univ.-Professor Dr. Gerd Otter und Akad.-Direktor Dr. Raimund Honecker III. Physikalisches Institut der Rheinisch-Westfälischen Technischen Hochschule Aachen
Atome - Moleküle - Kerne Band I Atomphysik Von Univ.-Professor Dr. Gerd Otter und Akad.-Direktor Dr. Raimund Honecker III. Physikalisches Institut der Rheinisch-Westfälischen Technischen Hochschule Aachen
Physik III. Mit 154 Bildern und 13 Tabellen
 Physik III Optik, Quantenphänomene und Aufbau der Atome Einfuhrungskurs für Studierende der Naturwissenschaften und Elektrotechnik von Wolfgang Zinth und Hans-Joachim Körner 2., verbesserte Auflage Mit
Physik III Optik, Quantenphänomene und Aufbau der Atome Einfuhrungskurs für Studierende der Naturwissenschaften und Elektrotechnik von Wolfgang Zinth und Hans-Joachim Körner 2., verbesserte Auflage Mit
Inhaltsverzeichnis. Einleitung 1
 Inhaltsverzeichnis Einleitung 1 1 Licht und Materie 7 Was ist eigentlich Licht? 8 Aber was schwingt da wie? 9 Was sind Frequenz und Wellenlänge des Lichts? 11 Was ist eigentlich Materie? 12 Woraus besteht
Inhaltsverzeichnis Einleitung 1 1 Licht und Materie 7 Was ist eigentlich Licht? 8 Aber was schwingt da wie? 9 Was sind Frequenz und Wellenlänge des Lichts? 11 Was ist eigentlich Materie? 12 Woraus besteht
PROBLEME AUS DER PHYSIK
 Helmut Vogel PROBLEME AUS DER PHYSIK Aufgaben und Lösungen zur 16. Auflage von Gerthsen Kneser Vogel Physik Mit über 1100 Aufgaben, 158 Abbildungen und 16 Tabellen Springer-Verlag Berlin Heidelberg New
Helmut Vogel PROBLEME AUS DER PHYSIK Aufgaben und Lösungen zur 16. Auflage von Gerthsen Kneser Vogel Physik Mit über 1100 Aufgaben, 158 Abbildungen und 16 Tabellen Springer-Verlag Berlin Heidelberg New
Ferienkurs Experimentalphysik 3
 Ferienkurs Experimentalphysik 3 Übung Qi Li, Bernhard Loitsch, Hannes Schmeiduch Donnerstag, 08.03.2012 1 Schwarzer Körper Außerhalb der Erdatmosphäre misst man das Maximum des Sonnenspektrums bei einer
Ferienkurs Experimentalphysik 3 Übung Qi Li, Bernhard Loitsch, Hannes Schmeiduch Donnerstag, 08.03.2012 1 Schwarzer Körper Außerhalb der Erdatmosphäre misst man das Maximum des Sonnenspektrums bei einer
14. Teilchen und Wellen
 Inhalt 14.1 Strahlung schwarzer Körper 14.2 Der Photoeffekt 14.3 Der Comptoneffekt 14.4 Materiewellen 14.5 Interpretation von Teilchenwellen 14.6 Die Schrödingergleichung 14.7 Heisenberg sche Unschärferelation
Inhalt 14.1 Strahlung schwarzer Körper 14.2 Der Photoeffekt 14.3 Der Comptoneffekt 14.4 Materiewellen 14.5 Interpretation von Teilchenwellen 14.6 Die Schrödingergleichung 14.7 Heisenberg sche Unschärferelation
Vorlesung 2: Größe der Atome Massenspektroskopie Atomstruktur aus Rutherfordstreuung
 Vorlesung 2: Roter Faden: Größe der Atome Massenspektroskopie Atomstruktur aus Rutherfordstreuung Skripte und Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ April 14, 2005 Atomphysik
Vorlesung 2: Roter Faden: Größe der Atome Massenspektroskopie Atomstruktur aus Rutherfordstreuung Skripte und Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ April 14, 2005 Atomphysik
Vortragsthema: Die Unschärferelationen Ort/Impuls Energie/Zeit. An einigen Beispielen erläutern
 Vortragsthema: Die Unschärferelationen Ort/Impuls Energie/Zeit An einigen Beispielen erläutern 5. Das Photon: Welle und Teilchen 5.4. Die Plancksche Strahlungsformel Wichtige Punkte: u( ν, T ) = 8πh c
Vortragsthema: Die Unschärferelationen Ort/Impuls Energie/Zeit An einigen Beispielen erläutern 5. Das Photon: Welle und Teilchen 5.4. Die Plancksche Strahlungsformel Wichtige Punkte: u( ν, T ) = 8πh c
Bereich Schwierigkeit Thema Atomphysik X Atommodelle. Dalton, Thomson und Rutherford. Mögliche Lösung
 Atomphysik X Atommodelle Dalton, Thomson und Rutherford a) Formulieren Sie die Daltonsche Atomhypothese. b) Nennen Sie die wesentlichen Merkmale des Atommodells von Thomson. c) Beschreiben Sie die Rutherfordschen
Atomphysik X Atommodelle Dalton, Thomson und Rutherford a) Formulieren Sie die Daltonsche Atomhypothese. b) Nennen Sie die wesentlichen Merkmale des Atommodells von Thomson. c) Beschreiben Sie die Rutherfordschen
Elementarteilchenphysik
 Masterclass 2010 Elementarteilchenphysik Robert Harlander Bergische Universität Wuppertal 17. Februar 2010 Robert Harlander Masterclass Uni Wuppertal p. 1 Elementarteilchenphysik Zentrale Fragen: Was sind
Masterclass 2010 Elementarteilchenphysik Robert Harlander Bergische Universität Wuppertal 17. Februar 2010 Robert Harlander Masterclass Uni Wuppertal p. 1 Elementarteilchenphysik Zentrale Fragen: Was sind
Ein schwarzer Körper und seine Strahlung
 Quantenphysik 1. Hohlraumstrahlung und Lichtquanten 2. Max Planck Leben und Persönlichkeit 3. Das Bohrsche Atommodell 4. Niels Bohr Leben und Persönlichkeit 5. Wellenmechanik 6. Doppelspaltexperiment mit
Quantenphysik 1. Hohlraumstrahlung und Lichtquanten 2. Max Planck Leben und Persönlichkeit 3. Das Bohrsche Atommodell 4. Niels Bohr Leben und Persönlichkeit 5. Wellenmechanik 6. Doppelspaltexperiment mit
Der Welle-Teilchen-Dualismus
 Quantenphysik Der Welle-Teilchen-Dualismus Welle-Teilchen-Dualismus http://bluesky.blogg.de/2005/05/03/fachbegriffe-der-modernen-physik-ix/ Welle-Teilchen-Dualismus Alles ist gleichzeitig Welle und Teilchen.
Quantenphysik Der Welle-Teilchen-Dualismus Welle-Teilchen-Dualismus http://bluesky.blogg.de/2005/05/03/fachbegriffe-der-modernen-physik-ix/ Welle-Teilchen-Dualismus Alles ist gleichzeitig Welle und Teilchen.
7. Das Bohrsche Modell des Wasserstoff-Atoms. 7.1 Stabile Elektronbahnen im Atom
 phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
Teil II: Quantenmechanik
 Teil II: Quantenmechanik Historisches [Weinberg 1] Den ersten Hinweis auf die Unmöglichkeit der klassischen Physik fand man in der Thermodynamik des elektromagnetischen Feldes: Das klassische Strahulungsfeld
Teil II: Quantenmechanik Historisches [Weinberg 1] Den ersten Hinweis auf die Unmöglichkeit der klassischen Physik fand man in der Thermodynamik des elektromagnetischen Feldes: Das klassische Strahulungsfeld
