3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen.
|
|
|
- Philipp Langenberg
- vor 7 Jahren
- Abrufe
Transkript
1 Tuesday, January 30, 2001 Allgemeine Chemie B II Page: 1 Inhalt Index 3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der Alkene Eine C=C Doppelbindung ist die funktionelle Gruppe, die für die Alkene (Olefine) charakteristisch ist. Sie haben weniger H-Atome pro C-Atom als Alkane, und werden deshalb als ungesättigt bezeichnet. z.b.(trivialnamen): In der IUPAC-Nomenklatur wird die einfachere Endung -en anstatt -ylen benützt. Kompliziertere Systeme erfordern Anpassungen und Erweiterungen der Nomenklaturregeln für Alkene: i) Finden Sie die längste Kohlenstoff-Kette, die beide an der Doppelbindung beteiligte C-Atome enthält: ii) Die Nummerierung beginnt an dem Ende, das der Doppelbindung näher ist. In Cycloalkenen sind die Kohlenstoffatome 1 und 2 immer die, zwischen denen die Doppelbindung liegt: iii) Die Substituenten und ihre Positionen werden dem Namen des Alkens als Präfixe vorgestellt: iv) Zwei Substituenten können auf denselben oder auf entgegengesetzten Seiten der Doppelbindung stehen. Die erste stereochemische Anordung wird cis genannt, die zweite trans : Ein alternatives und allgemeineres System zur Benennung von cis/trans -Isomeren wurde von der IUPAC eingeführt: Das E,Z-System (später). v) Wenn andere funktionelle Gruppen vorhanden sind, können sie gegenüber der Doppelbindung Vorrang haben z.b Alkenole : vi) Substituenten, die eine Doppelbindung enthalten, werden Alkenyl genannt:
2 Tuesday, January 30, 2001 Allgemeine Chemie B II Page: E- und Z- Isomere Die Rotation um eine C=C Doppelbindung benötigt einen hohen Energiebetrag, weil die π-bindung (π-bindungsdissoziationsenergie 272 KJ/mol) gebrochen werden muss: Normalerweise sind unter 300 o C die meisten Doppelbindungen konfigurationsstabil. Aber mit einer starken Säure kann die Isomerisierung katalysiert werden, und beim Gleichgewicht steht das trans -Isomer im Überschuss. Die trans -Isomere sind stabiler als die cis -Isomere. Um bei den mehrfach substituierten Alkenen verschiedene Isomeren eindeutig kennzeichnen zu können, benutzt man die Sequenzregel von Cahn, Ingold und Prelog. Nach diesen Regeln sind alle möglichen Substituenten in einer Reihe nach abnehmender Priorität geordnet. Die Priorität der Substituenten ergibt sich aus der Abnahme der Ordungszahl der direkt an die Doppelbindung gebundenen Atome. z.b. : 35 Br > 17 Cl > 8 O > 7 N > 6 C > 1 H usw. Dasjenige Isomer, bei welchem die beiden Gruppen höherer Priorität auf derselben Seite der Doppelbindung liegen, wird als Z-Isomer, das andere als E-Isomer bezeichnet, z.b.: Sind zwei oder mehr mit der Doppelbindung verknüpfte Atome identisch, so bestimmt die Atomnummer des benachbarten Atoms die Prioritätenfolge : Doppelt gebundene Atome werden zweifach gezählt und alle Ligandenatome ausser Wasserstoff mit Phantomatomen zur Ligandenatomzahl 4 ergänzt :
3 Tuesday, January 30, 2001 Allgemeine Chemie B II Page: Allgemeines: Reaktionen nach Mechanismus eingeordnet Da verschiedene funktionelle Gruppen aber auch gleichartige chemische Reaktionen zeigen, ist es möglich, das Gesamtgebiet der Organischen Chemie nach Reaktionstypen zu gliedern. Betrachtet man nur die Veränderungen des Molekülskelettes und lässt den genauen Ablauf unberücksichtigt, so kann man vier Haupttypen von Reaktionen unterscheiden : Substitution: Dabei wird ein Atom oder eine Atomgruppe durch ein anderes Atom oder Atomgruppe ersetzt (substituiert) : Addition: Hier werden weitere Atome (Atomgruppen) an das Molekül angelagert : (nur an ungesättigten funktionellen Gruppen möglich) Eliminierung: Aus organischen Molekülen werden Moleküle abgespalten, wobei ungesättigte Verbindungen entstehen : Umlagerung: Wenn innerhalb eines Moleküls Atome oder Atomgruppen verschoben werden, so wird das Kohlenstoffgerüst verändert und es tritt eine Umlagerung ein: (Einige andere Reaktionen lassen sich oft nicht leicht in einen der erwähnten Reaktionstypen einordnen). Allgemeines über Reaktions-Mechanismen; In chemischen Reaktionen werden Kovalenzbindungen gebrochen und gebildet. Kovalenzbindungen können auf zwei Arten gebrochen werden: Bei der homolytischen Bindungstrennung entstehen Atome und/oder Radikale, während bei der heterolytischen Bindungstrennung Ionen, eventuell auch neutrale Molekule gebildet werden können. Umgekehrt, kann bei der Bindungsneubildung die Kovalenzbindung durch einen radikalischen oder durch einen polaren Prozess gebildet werden :
4 Tuesday, January 30, 2001 Allgemeine Chemie B II Page: 4 In polaren Reaktionen werden die Elektron-Bewegungen durch Pfeile gekennzeichnet, in dem ein Nucleophil ("nucleus-loving", ein elektronreiches Atom oder Atomgruppe) seine Elektronen auf ein Elektrophil ("electron-loving", ein elektronarmes Atom oder Atomgruppe) überträgt, um eine neue Kovalenzbindung zu bilden : 3.4 Struktur und Bindung in Alkenen Wie unser Orbital-Bild zeigt, besteht die Doppelbindung aus zwei unterschiedlichen Bindungen : einer σ- und einer π-bindung : Chemische Bindungen entstehen durch die Überlappung von Orbitalen, und die Bindungsstärke wird von der Effektivität dieser Überlappung bestimmt. Wegen der räumlichen Anordung der Orbitale ist zu erwarten, dass die Orbital-Überlappung in einer σ-bindung besser ist als in einer π-bindung. Weil die Überlappung in π-orbitalen geringer ist als in σ-orbitalen, sollte die Abspaltung eines Elektrons aus einem Alken aus dem energetisch höher liegenden π-niveau erfolgen, weil π-elektronen weniger stark gebunden sind als σ-elektronen : Dieser Unterschied hat chemische und physikalische Konsequenzen. 3.5 Elektrophile Addition an Alkene ; eine polare Additionsreaktion Eine C=C Doppelbindung (und ebenso eine Dreifachbindung) stellt ein Zentrum von relativ hoher negativer Ladungsdichte dar, und es ist deshalb verständlich, dass sie besonders leicht von elektrophilen Reagentien angreifbar ist: d.h. C=C Doppelbindungen sollten sich als Nucleophile verhalten. z.b. Addition von HCl : Mechanismus der Addition :
5 Tuesday, January 30, 2001 Allgemeine Chemie B II Page: 5 Ein Carbokation (Carbeniumion) entsteht als Zwischenprodukt. Zwischenprodukte treten oft in mehrstufigen Reaktionen auf und sind gewöhnlich instabil und reagieren rasch weiter. 3.6 Beschreibung einer Reaktion durch ein Energiediagramm Die chemische Thermodynamik befasst sich mit den Energieänderungen in Reaktanten und Produkten bei chemischen Reaktionen. Diese sind ein Mass dafür, wo ein chemisches Gleichgewicht liegt : K eq gross : Gleichgewicht liegt nach rechts : Energieniveau von Produkten ist niedriger als beim Reaktanten (exotherme Reaktion) K eq klein (<1) Gleichgewicht liegt nach links : Energieniveau von Produkten liegt höher als beim Reaktanten (endotherme Reaktion). Die Gleichgewichtslage wird durch G o, die Differenz zwischen den freien Enthalpien der Produkte und der Reaktanten, bestimmt. Die chemische Kinetik betrachtet die Geschwindigkeit, mit der die Reaktion abläuft. Die Geschwindigkeit einer Reaktion wird durch ihre freie Aktivierungsenergie G #, die Differenz zwischen der freien Enthalpie der Reaktanten und dem (oder dem höchsten, wenn es mehrere gibt) Übergangszustand (transition state). z.b. für A --> B Die Energie, die zur Überschreitung der Energiebarriere nötig ist, erlangt ein Molekül normalerweise durch Zusammenstösse mit anderen Molekülen. Die Häufigkeitsverteilung der kinetischen Energie bei einer gegebenen Temp. wird durch die Boltzmann-Verteilung angegeben. Bei RT beträgt die mittlere kinetische Energie der Moleküle einer organischen Verbindung nur etwa 2.5 KJ/mol. Viele organische Reaktionen besitzen Aktivierungsenergien von KJ/mol. Damit eine Reaktion bei Raumtemperatur abläuft, kann die Aktivierungsenergie bis auf etwa 80 KJ/mol liegen. Reaktionen mit höherer Aktivierungsenergie finden nur bei höherern Temperaturen statt. Für die Elektrophile-Addition von HCl an Alkene :
6 Tuesday, January 30, 2001 Allgemeine Chemie B II Page: 6 Die Strukturen, die auf Energiemaxima liegen, heissen Übergangszustände. Sie können weder isoliert noch beobachtet werden. Im ersten Übergangszustand ist die C=C Doppelbindung partiell gespalten und die neue C-H σ-bindung partiell gebildet: Das Zwischenprodukt, in diesem Fall ein Carbokation, liegt in einem Energieminimum, ist aber instabil weil es auf einem hohen Energieniveau liegt. Der zweite Übergangszustand benötigt nur einen sehr kleinen Energiebetrag und läuft deswegen sehr rasch ab: 3.7 Karotten, Alkene und das Sehvermögen Karotten stellen eine reiche Quelle von β-caroten dar, was für die körperliche Bildung von Vitamin A im Körper verwendet werden kann. β-caroten wird in der Leber durch Enzym-katalysierte Reaktionen in Vitamin A und 11-cis -Retinal umgewandelt : In unseren Augen findet man zwei besondere Zell Typen: Stäbchen und Zapfen (rod cells und cone cells). In den "Rod-cells" wird 11-cis -Retinal zum Protein Opsin gekuppelt, und dadurch wird Rhodopsin gebildet. Rhodopsin ist ein integrales Membranprotein und ist der Hauptphotorezeptor unseres Sehvermögens zeigten George Wald und Mitarbeiter, das Licht das 11-cis -Retinal des Rhodopsins zu all-trans -Retinal isomerisiert. Diese Isomerisierung, das Primärereignis des Sehvorgangs, ändert die Geometrie des Retinals und dadurch die Konformation des Opsin Moleküle wesentlich. Dadurch ist ein Photon in atomare Bewegung umgewandelt worden:
7 Tuesday, January 30, 2001 Allgemeine Chemie B II Page: 7 Danach wird all-trans -Retinal freigesetzt (durch eine Hydrolyse), und wird in einer Dunkelreaktion zu 11-cis -Retinal isomerisiert. Inhalt Index
3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen.
 Inhalt Index 3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der Alkene Eine C=C Doppelbindung ist die funktionelle Gruppe, die
Inhalt Index 3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der Alkene Eine C=C Doppelbindung ist die funktionelle Gruppe, die
Die Substituenten und ihre Positionen werden dem Namen des Alkens als Präfixe vorgestellt:
 23 3. Organische Reaktionen - Einordung nach chanismen. lkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der lkene Eine C=C Doppelbindung ist die funktionelle Gruppe, die für die lkene
23 3. Organische Reaktionen - Einordung nach chanismen. lkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der lkene Eine C=C Doppelbindung ist die funktionelle Gruppe, die für die lkene
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 CE 102.1: Grundlagen der Chemie - Organische Chemie Prof Dr. E. Landau und Prof. Dr. J.. Robinson 3. Organische Reaktionen - Einordung nach chanismen. lkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1
CE 102.1: Grundlagen der Chemie - Organische Chemie Prof Dr. E. Landau und Prof. Dr. J.. Robinson 3. Organische Reaktionen - Einordung nach chanismen. lkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1
CHE 172.1: Organische Chemie für die Life Sciences
 1 CE 172.1: Organische Chemie für die Life Sciences Prof Dr. J.. Robinson 3. Organische Reaktionen - Einordung nach chanismen. lkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der lkene
1 CE 172.1: Organische Chemie für die Life Sciences Prof Dr. J.. Robinson 3. Organische Reaktionen - Einordung nach chanismen. lkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der lkene
Reaktionstypen der Aliphate
 Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
KW Alkene. Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1
 KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
Übungen zur VL Chemie für Biologen und Humanbiologen Lösung Übung 9
 Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
4. Alkene und Alkine : Reaktionen und Darstellung
 Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
4. Alkene und Alkine : Reaktionen und Darstellung
 Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
Vorlesung Organische Chemie II Reaktionsmechanismen (3. Sem.)
 Vorlesung Organische Chemie II Reaktionsmechanismen (3. Sem.) Gliederung Grundlagen der physikalisch-organischen Chemie Radikalreaktionen Nukleophile und elektrophile Substitution am gesättigten C-Atom
Vorlesung Organische Chemie II Reaktionsmechanismen (3. Sem.) Gliederung Grundlagen der physikalisch-organischen Chemie Radikalreaktionen Nukleophile und elektrophile Substitution am gesättigten C-Atom
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Seminarplan zum. Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie. (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE
 Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Vorlesung Chemie für Biologen: Klausur 1 WS Sa
 1 Vorlesung Chemie für Biologen: Klausur 1 WS 02-03 Sa 07.12.02 Name:... Ihre Unterschrift:... Vorname:... Matrikel-Nr.:... Studienbeginn: SS: WS:...... Tutor der Übungen: (Dort Klausureinsicht.) Punkteschlüssel
1 Vorlesung Chemie für Biologen: Klausur 1 WS 02-03 Sa 07.12.02 Name:... Ihre Unterschrift:... Vorname:... Matrikel-Nr.:... Studienbeginn: SS: WS:...... Tutor der Übungen: (Dort Klausureinsicht.) Punkteschlüssel
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1. Grundwissen 10.Klasse NTG 2 Grundwissen 10.Klasse NTG 2
 Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Einführung in die Nomenklatur der organischen Chemie. Einteilung der Kohlenwasserstoffe
 organischen hemie Klasse 8 Einteilung der Kohlenwasserstoffe Alkane Alkene Alkine Kettenverbindungen Organische hemie socyclen ycloalkane ycloalkene ycloalkine Aromate Ringverbindungen eterocyclen Fünfringe
organischen hemie Klasse 8 Einteilung der Kohlenwasserstoffe Alkane Alkene Alkine Kettenverbindungen Organische hemie socyclen ycloalkane ycloalkene ycloalkine Aromate Ringverbindungen eterocyclen Fünfringe
v = - = - = = k [R] [S]
![v = - = - = = k [R] [S] v = - = - = = k [R] [S]](/thumbs/81/82977406.jpg) Vorlesung 7 Die hemische Kinetik (Vollhardt, 3 Aufl, S 70-72, 4 Aufl, S 54-58; art, S 107-110; Buddrus, S 26-29) befasst sich mit Geschwindigkeit, mit der eine Reaktion abläuft R S P Geschwindigkeit einer
Vorlesung 7 Die hemische Kinetik (Vollhardt, 3 Aufl, S 70-72, 4 Aufl, S 54-58; art, S 107-110; Buddrus, S 26-29) befasst sich mit Geschwindigkeit, mit der eine Reaktion abläuft R S P Geschwindigkeit einer
Drill&Practice: Alkene und Alkine
 Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME 1 Drill&Practice: Alkene und Alkine 1. Orbitalzeichnungen sind sehr aufwändig. Zeichnen Sie in die folgenden Strukturen mit rot die π -Bindungen und
Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME 1 Drill&Practice: Alkene und Alkine 1. Orbitalzeichnungen sind sehr aufwändig. Zeichnen Sie in die folgenden Strukturen mit rot die π -Bindungen und
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
 INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
Radikalische Substitution von Alkanen
 adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Organische Experimentalchemie
 PD Dr. Alexander Breder (abreder@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der umanmedizin, Zahnmedizin und
PD Dr. Alexander Breder (abreder@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der umanmedizin, Zahnmedizin und
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Chemie für Biologen, 2017
 Chemie für Biologen, 2017 Übung 11 Organisch chemische Reaktionen (Thema 12.1 12.6) Aufgabe 1: a) Erklären Sie folgende Begriffe: i) Übergangszustand Zustand der höchsten Energie in einer Reaktion, kann
Chemie für Biologen, 2017 Übung 11 Organisch chemische Reaktionen (Thema 12.1 12.6) Aufgabe 1: a) Erklären Sie folgende Begriffe: i) Übergangszustand Zustand der höchsten Energie in einer Reaktion, kann
VII INHALTSVERZEICHNIS
 VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!)
 . Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
. Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
Bundesrealgymnasium Imst. Chemie Klasse 8. Reaktionsmechanismen der Aliphate
 Bundesrealgymnasium Imst Chemie 2010-11 Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter aufgearbeitet
Bundesrealgymnasium Imst Chemie 2010-11 Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter aufgearbeitet
CHE 172.1: Organische Chemie für die Life Sciences
 1 E 172.1: Organische hemie für die Life Sciences Prof Dr. J. A. Robinson 4. Alkene und Alkine : Reaktionen und erstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken
1 E 172.1: Organische hemie für die Life Sciences Prof Dr. J. A. Robinson 4. Alkene und Alkine : Reaktionen und erstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken
Arzneistoff der Woche. Alkohole. Eliminierungen. Organische Chemie Agenda. Johann Wolfgang Goethe -Universität Frankfurt am Main
 Agenda Arzneistoff der Woche Alkohole Eliminierungen 1 Prof. Dr. Manfred Schubert-Zsilavecz Dabigatran - Struktur 2 Prof. Dr. Manfred Schubert-Zsilavecz Lucas-Test 3 Prof. Dr. Manfred Schubert-Zsilavecz
Agenda Arzneistoff der Woche Alkohole Eliminierungen 1 Prof. Dr. Manfred Schubert-Zsilavecz Dabigatran - Struktur 2 Prof. Dr. Manfred Schubert-Zsilavecz Lucas-Test 3 Prof. Dr. Manfred Schubert-Zsilavecz
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
(Anmerkung: Es sind weitere möglich. Spektren zeigen Diradikal.)
 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
c) Gleichzeitiger Bruch der C-X-Bindung und der C-H-Bindung
 Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
Übungen zur VL Chemie für Biologen und Humanbiologen Benennen Sie die folgenden Verbindungen nach IUPAC-Nomenklatur:
 Übungen zur VL Chemie für Biologen und Humanbiologen 21.01.2011 1. Benennen Sie die folgenden Verbindungen nach IUPAC-Nomenklatur: a) 3-Methyl-4-propylhexan Erklärung: Es liegt keine funktionelle Gruppe
Übungen zur VL Chemie für Biologen und Humanbiologen 21.01.2011 1. Benennen Sie die folgenden Verbindungen nach IUPAC-Nomenklatur: a) 3-Methyl-4-propylhexan Erklärung: Es liegt keine funktionelle Gruppe
Chemische Bindungen Atombindung
 Atombindung Das Lewis Modell der kovalenten Bindung Die Entstehung von Molekülen beruht auf der Bildung von gemeinsamen, bindenden Elektronenpaaren in dem Bestreben der Atome, eine energetisch stabile
Atombindung Das Lewis Modell der kovalenten Bindung Die Entstehung von Molekülen beruht auf der Bildung von gemeinsamen, bindenden Elektronenpaaren in dem Bestreben der Atome, eine energetisch stabile
Alkene / Additions-, Eliminierungsreaktionen
 2.2.2. Alkene / Additions-, Eliminierungsreaktionen 64 65 Struktur und Bindung in Ethen Ethen ist planar 2 trigonale C-Atome Bindungswinkel annähernd 120 o C ist sp2-hybridisiert Einfachbindung durch Überlapp
2.2.2. Alkene / Additions-, Eliminierungsreaktionen 64 65 Struktur und Bindung in Ethen Ethen ist planar 2 trigonale C-Atome Bindungswinkel annähernd 120 o C ist sp2-hybridisiert Einfachbindung durch Überlapp
Lernkarten CHE 172 Organische Chemie Kap 1-17
 Lernkarten CHE 172 Organische Chemie Kap 1-17 Lernkarten für Biologie und Biomedizinstudenten der Universität Zürich Die Karten basieren auf dem Skript von Prof. Dr. J. A. Robinson aus dem Jahr 2016, somit
Lernkarten CHE 172 Organische Chemie Kap 1-17 Lernkarten für Biologie und Biomedizinstudenten der Universität Zürich Die Karten basieren auf dem Skript von Prof. Dr. J. A. Robinson aus dem Jahr 2016, somit
Organische Chemie im Überblick
 Evelyne Chelain Nadeqe Lubin-Germain Jacques Uziel Organische Chemie im Überblick Grundwissen in Lerneinheiten Aus dem Französischen übersetzt von Karin Beifuss ~ Springer Spektrum Inhaltsverzeichnis 1
Evelyne Chelain Nadeqe Lubin-Germain Jacques Uziel Organische Chemie im Überblick Grundwissen in Lerneinheiten Aus dem Französischen übersetzt von Karin Beifuss ~ Springer Spektrum Inhaltsverzeichnis 1
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Reaktionstypen der Aromate
 Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Bundesrealgymnasium Imst. Chemie Klasse 8. Aliphate
 Bundesrealgymnasium Imst Chemie 2010-11 Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter aufgearbeitet
Bundesrealgymnasium Imst Chemie 2010-11 Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter aufgearbeitet
2. Übungsblatt. Organische Chemie für Studierende mit Nebenfach Chemie
 Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Elektrophile Additionen von HX an die CC-Doppelbindung (Vollhardt, 3. Aufl., S , 4. Aufl., S ; Hart, S ; Buddrus, S.
 Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
zur Vorlesung "Organische Chemie II (Aliphaten, Reaktionsmechanismen) für Studierende der Chemie und der Biochemie 3. Semester" WS 2002/2003
 J. aub/febr. 200 Klausur zur Vorlesung "rganische Chemie II (Aliphaten, Reaktionsmechanismen) für Studierende der Chemie und der Biochemie. Semester" Lösungsbogen WS 2002/200 ) Radikalreaktionen (2 Punkte):
J. aub/febr. 200 Klausur zur Vorlesung "rganische Chemie II (Aliphaten, Reaktionsmechanismen) für Studierende der Chemie und der Biochemie. Semester" Lösungsbogen WS 2002/200 ) Radikalreaktionen (2 Punkte):
Übung Nr. 13. Vorlesung Allgemeine Chemie II Teil Organische Chemie Frühjahrssemester Mi bzw. Fr
 Übung Nr. 13 Mi. 30.05.2012 bzw. Fr. 01.06.2012 1. Eliminierungen I Geben Sie für die untenstehenden Reaktionen die jeweiligen Produkte an! Um welche Namensreaktion handelt es sich? Welcher Typ Eliminierung
Übung Nr. 13 Mi. 30.05.2012 bzw. Fr. 01.06.2012 1. Eliminierungen I Geben Sie für die untenstehenden Reaktionen die jeweiligen Produkte an! Um welche Namensreaktion handelt es sich? Welcher Typ Eliminierung
Kapitel 4: Eliminierung - Übersicht
 » Reaktionstypen - 1,1-, 1,2-, 1,3-, 1,4-Eliminierung (α-, β-, γ-, δ- Eliminierung), thermische Fragmentierung, cis-eliminierung» Regel - Eliminierung wird begünstigt durch hohe Temperatur, starke Basen,
» Reaktionstypen - 1,1-, 1,2-, 1,3-, 1,4-Eliminierung (α-, β-, γ-, δ- Eliminierung), thermische Fragmentierung, cis-eliminierung» Regel - Eliminierung wird begünstigt durch hohe Temperatur, starke Basen,
4.1. Gesättigte Kohlenwasserstoffe (Alkane)
 4. Stoffgruppen 4.1. Gesättigte Kohlenwasserstoffe (Alkane) ffenkettige Alkane à für n C-Atome ergibt sich: C n 2n+2 Methan Ethan Propan Butan C 4 C 2 6 C 3 8 C 3 C C 3 3 C C 3 C 4 10 3 C C 3 à Es gibt
4. Stoffgruppen 4.1. Gesättigte Kohlenwasserstoffe (Alkane) ffenkettige Alkane à für n C-Atome ergibt sich: C n 2n+2 Methan Ethan Propan Butan C 4 C 2 6 C 3 8 C 3 C C 3 3 C C 3 C 4 10 3 C C 3 à Es gibt
6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und Herstellung
 6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und erstellung Moleküle, die nur Kohlenstoff und Wasserstoff enthalten, werden Kohlenwasserstoffe genannt Prof. Dr. Ivo C. Ivanov
6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und erstellung Moleküle, die nur Kohlenstoff und Wasserstoff enthalten, werden Kohlenwasserstoffe genannt Prof. Dr. Ivo C. Ivanov
Lebewesen enthalten weitaus mehr Molekülarten und beherbergen weitaus mehr chemische Reaktionsarten als die ganze anorganische Welt.
 Lebewesen enthalten weitaus mehr Molekülarten und beherbergen weitaus mehr chemische Reaktionsarten als die ganze anorganische Welt. Die aus Biomolekülen aufgebauten biologischen Strukturen sind äußerst
Lebewesen enthalten weitaus mehr Molekülarten und beherbergen weitaus mehr chemische Reaktionsarten als die ganze anorganische Welt. Die aus Biomolekülen aufgebauten biologischen Strukturen sind äußerst
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) OH H + - H 2 O. (aus H 3 PO 4 H 2 SO 4 ) - H + Stichpunkte zum E1-Mechanismus:
 Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
im Molekül eine Dreifachbindung (eine σ-bindung,
 1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
Chemie. Elektrochemie, Alkane und Alkene
 Zinkhalbzelle Mehr Zusammenfassungen von Malte Jakob findest du hier: hemie Elektrochemie, Alkane und Alkene Elektrochemie Galvanische Zelle: Anode Oxidation - e - e- e U - e - + Kathode Reduktion Zinkelektrode
Zinkhalbzelle Mehr Zusammenfassungen von Malte Jakob findest du hier: hemie Elektrochemie, Alkane und Alkene Elektrochemie Galvanische Zelle: Anode Oxidation - e - e- e U - e - + Kathode Reduktion Zinkelektrode
Thermodynamik & Kinetik
 Thermodynamik & Kinetik Inhaltsverzeichnis Ihr versteht die Begriffe offenes System, geschlossenes System, isoliertes System, Enthalpie, exotherm und endotherm... 3 Ihr kennt die Funktionsweise eines Kalorimeters
Thermodynamik & Kinetik Inhaltsverzeichnis Ihr versteht die Begriffe offenes System, geschlossenes System, isoliertes System, Enthalpie, exotherm und endotherm... 3 Ihr kennt die Funktionsweise eines Kalorimeters
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Reaktionsmechanismen der Organischen Chemie
 Peter Sykes Reaktionsmechanismen der Organischen Chemie Eine Einführung Mit einem Geleitwort von Lord A. R. Todd Übersetzt von Hans F. Ebel und Henning Hopf 9., überarbeitete Auflage Inhalt 1 Struktur,
Peter Sykes Reaktionsmechanismen der Organischen Chemie Eine Einführung Mit einem Geleitwort von Lord A. R. Todd Übersetzt von Hans F. Ebel und Henning Hopf 9., überarbeitete Auflage Inhalt 1 Struktur,
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Übung 13 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Ms: Mesyl-Gruppe (CH 3 SO 3 -), Tf: Triflyl-Gruppe (CF 3 SO 3 -), Ts:
1 Übung 13 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Ms: Mesyl-Gruppe (CH 3 SO 3 -), Tf: Triflyl-Gruppe (CF 3 SO 3 -), Ts:
Kapitel 3 Alkene Struktur, Nomenklatur, Reaktivität Thermodynamik und Kinetik
 Kapitel 3 Alkene Struktur, Nomenklatur, Reaktivität Thermodynamik und Kinetik 34 Geben Sie die systematischen Namen jeder der folgenden Verbindungen an: Welche der Verbindungen aus Übung besitzen E- und
Kapitel 3 Alkene Struktur, Nomenklatur, Reaktivität Thermodynamik und Kinetik 34 Geben Sie die systematischen Namen jeder der folgenden Verbindungen an: Welche der Verbindungen aus Übung besitzen E- und
S N 2, S N 1 E1, E2 S N 2, S N 1, E1, E2
 S N vs. E S N 2, S N 1 - B: E1, E2 H E1, E2 C C - : Nu L S N 2, S N 1, E1, E2 Die vier durch Pfeile angedeutenden Reaktionsmöglichkeiten laufen mit unterschiedlichen Geschwindigkeiten ab. Wichtigste Einflussfaktoren:
S N vs. E S N 2, S N 1 - B: E1, E2 H E1, E2 C C - : Nu L S N 2, S N 1, E1, E2 Die vier durch Pfeile angedeutenden Reaktionsmöglichkeiten laufen mit unterschiedlichen Geschwindigkeiten ab. Wichtigste Einflussfaktoren:
Organische Chemie, Reaktionsmechanismen
 , Reaktionen, Teil 3-1 - hemieskript Dr. R. Steiger rganische hemie, Reaktionsmechanismen Das Lernziel dieser Unterrichtseinheit beinhaltet folgende Punkte: Wie können funktionelle Gruppen ineinander überführt
, Reaktionen, Teil 3-1 - hemieskript Dr. R. Steiger rganische hemie, Reaktionsmechanismen Das Lernziel dieser Unterrichtseinheit beinhaltet folgende Punkte: Wie können funktionelle Gruppen ineinander überführt
σ-bindung beide Kohlenstoffatome sp-hybridisiert => Bindungswinkel 180 eine lineare Struktur
 VIII. Alkine Die C/C-Dreifachbindung als funktionelle Gruppe erste π-bindung σ-bindung zweite π-bindung orthogonal zur ersten beide Kohlenstoffatome sp-hybridisiert => Bindungswinkel 180 eine lineare Struktur
VIII. Alkine Die C/C-Dreifachbindung als funktionelle Gruppe erste π-bindung σ-bindung zweite π-bindung orthogonal zur ersten beide Kohlenstoffatome sp-hybridisiert => Bindungswinkel 180 eine lineare Struktur
Die Herstellung von Alkenen aus Chloralkanen bzw. aus anderen Estern oder Alkoholen durch E2- oder E1-Eliminierungen wurde bereits besprochen.
 Vorlesung 18. Alkene ie erstellung von Alkenen aus hloralkanen bzw. aus anderen Estern oder Alkoholen durch E2- oder E1-Eliminierungen wurde bereits besprochen. Technische erstellung von Ethylen (= Ethen)
Vorlesung 18. Alkene ie erstellung von Alkenen aus hloralkanen bzw. aus anderen Estern oder Alkoholen durch E2- oder E1-Eliminierungen wurde bereits besprochen. Technische erstellung von Ethylen (= Ethen)
Organische Chemie für Biologen und Wirtschaftsingenieure
 rganische hemie für Biologen und Wirtschaftsingenieure Lukas Gooßen, Vorlesung SS13 www.uni-kl.de Aufbau der Vorlesung rganische Verbindungen funktionellen Gruppen eaktionen Alkane: Alkene: Aromatische
rganische hemie für Biologen und Wirtschaftsingenieure Lukas Gooßen, Vorlesung SS13 www.uni-kl.de Aufbau der Vorlesung rganische Verbindungen funktionellen Gruppen eaktionen Alkane: Alkene: Aromatische
Übungssblatt 3: Alkene und weitere cyclische Kohlenwasserstoffe
 1 Übungssblatt 3: Alkene und weitere cyclische Kohlenwasserstoffe Warm Up 1) Erweitern Sie die Ihnen bekannten Regeln der Nomenklatur für Alkene und benennen danach folgende Verbindungen. Die Regel zur
1 Übungssblatt 3: Alkene und weitere cyclische Kohlenwasserstoffe Warm Up 1) Erweitern Sie die Ihnen bekannten Regeln der Nomenklatur für Alkene und benennen danach folgende Verbindungen. Die Regel zur
Grundlagen der organischen Chfemie
 Dr. sc. nat. Hans Rudolf Christen 'BHiGil.'liÜ ' \ Grundlagen der organischen Chfemie Verlag Sauerländer, Aarau Diesterweg Salle, Frankfurt am Main 9 Inhaltsverzeichnis Vorwort 7 I.Teil: Überblick über
Dr. sc. nat. Hans Rudolf Christen 'BHiGil.'liÜ ' \ Grundlagen der organischen Chfemie Verlag Sauerländer, Aarau Diesterweg Salle, Frankfurt am Main 9 Inhaltsverzeichnis Vorwort 7 I.Teil: Überblick über
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Grundlagen zum Verständnis chemischer Reaktionen = Handwerkszeug
 Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
13. Amine und ihre Derivate
 Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
ORGANISCHE CHEMIE. Struktur organischer Verbindungen: Formeln, Nomenklatur und Reaktionsmechanismen
 ORGANISE EMIE Struktur organischer Verbindungen: Formeln, Nomenklatur und Reaktionsmechanismen hemische Formeln Summenformeln Strukturformeln (Konstitutionsformeln) Ausführliche Strukturformeln Vereinfachte
ORGANISE EMIE Struktur organischer Verbindungen: Formeln, Nomenklatur und Reaktionsmechanismen hemische Formeln Summenformeln Strukturformeln (Konstitutionsformeln) Ausführliche Strukturformeln Vereinfachte
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 1. Klausur zum 2. Praktikumsteil (OC) vom 05.07.2014 NAME;
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 1. Klausur zum 2. Praktikumsteil (OC) vom 05.07.2014 NAME;
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Nachschreibklausur zum 2. Praktikumsteil (OC) vom 12.07.10
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Nachschreibklausur zum 2. Praktikumsteil (OC) vom 12.07.10
2. Übungsblatt. Organische Chemie für Studierende mit Nebenfach Chemie
 Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang
 Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
II. Halogenalkane, radikalische und nukleophile Substitution
 II. alogenalkane, radikalische und nukleophile Substitution Experimentelle Beobachtung: 36 n-c 6 14 RT n-c 6 13 Br + Br Allgemein formuliert: R- Br 2 -Br R-Br Wie geht das? 37 Mechanismus am besten mit
II. alogenalkane, radikalische und nukleophile Substitution Experimentelle Beobachtung: 36 n-c 6 14 RT n-c 6 13 Br + Br Allgemein formuliert: R- Br 2 -Br R-Br Wie geht das? 37 Mechanismus am besten mit
Alkene Struktur, Nomenklatur, Reaktivität Thermodynamik und Kinetik
 Alkene Struktur, Nomenklatur, Reaktivität Thermodynamik und Kinetik 3.1 Summenformeln und der ungesättigte harakter............................................. 151 3 3.2 Nomenklatur der Alkene..............................
Alkene Struktur, Nomenklatur, Reaktivität Thermodynamik und Kinetik 3.1 Summenformeln und der ungesättigte harakter............................................. 151 3 3.2 Nomenklatur der Alkene..............................
STRUKTUR UND REAKTION INDER CHEMIE
 STRUKTUR UND REAKTION INDER CHEMIE Ein Leitfaden für das Studium der Chemie 2., bearbeitete Auflage Mit 129 Bildern und 32 Tabellen INHALTSVERZEICHNIS Abkürzungen, Größen, Konstanten und Umrechnungsfaktoren
STRUKTUR UND REAKTION INDER CHEMIE Ein Leitfaden für das Studium der Chemie 2., bearbeitete Auflage Mit 129 Bildern und 32 Tabellen INHALTSVERZEICHNIS Abkürzungen, Größen, Konstanten und Umrechnungsfaktoren
Michael Pieper Universität-Oldenburg - SoSe 2003
 1. Klassifizierung (von : eliminare = aus dem Haus treiben). Allgemeinen Reaktionen bei denen zwei Gruppen (Atome, Ionen, Moleküle) aus einem Substrat abgespalten werden. Die Klassifizierung in α-, β-
1. Klassifizierung (von : eliminare = aus dem Haus treiben). Allgemeinen Reaktionen bei denen zwei Gruppen (Atome, Ionen, Moleküle) aus einem Substrat abgespalten werden. Die Klassifizierung in α-, β-
Organische Chemie der Freien Universität Berlin. Klausur SS 2008 Teil 2
 rganische Chemie der Freien Universität Berlin C I Grundlagen der rganischen Chemie (LV 21 21a) Klausur SS 28 Teil 2 Verfasser: Datum: 19.7.28 Prof. Dr. H.-U. Reißig Semester: SS 8 Höchstpunktzahl: 2 (in
rganische Chemie der Freien Universität Berlin C I Grundlagen der rganischen Chemie (LV 21 21a) Klausur SS 28 Teil 2 Verfasser: Datum: 19.7.28 Prof. Dr. H.-U. Reißig Semester: SS 8 Höchstpunktzahl: 2 (in
2. Klausur. 1. Aufgabe
 1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Bei der abschließenden
1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Bei der abschließenden
Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag)
 Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
6. Rechenübung Organik (27.01./ )
 1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
Basisprüfung Allgemeine Chemie (Teil OC) Montag, 3. September 2007
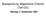 Basisprüfung Allgemeine Chemie (Teil C) Montag, 3. September 2007 1. omenklatur (20 Pt) 1.1 (10Pt) Benennen Sie die Verbindungen A - D nach IUPAC inkl. stereochemischer Deskriptoren. A B (2E,5E)4-Prop-1-inylhepta-2,5-dien
Basisprüfung Allgemeine Chemie (Teil C) Montag, 3. September 2007 1. omenklatur (20 Pt) 1.1 (10Pt) Benennen Sie die Verbindungen A - D nach IUPAC inkl. stereochemischer Deskriptoren. A B (2E,5E)4-Prop-1-inylhepta-2,5-dien
Lösungen zum Übungsblatt zur Schulaufgabe. 0. Aufgaben aus dem Buch, S. 34
 Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Verzeichnis der Wortabkürzungen... Verzeichnis der Zeichen und Symbole...XVII
 VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
Chemie für Biologen, Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema ) iii) Carbonsäure iv) Dicarbonsäure
 Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Organik KOMPAKT Organik Blatt 1/5
 rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
Decan Homologe Reihe der Alkane, unterschiedlich lange C-Ketten mit C- C (sp 3 /sp 3 ) und C-H (sp 3 /s)-bindungen (σ-bindungen) Beispiele: Butan
 1 30.09.005 0.1 Alkane Eine einfache Stoffgruppe der organischen Chemie sind die Alkane. Dabei handelt es sich um eine spezielle Gruppe der Kohlenwasserstoffe (KW). Alle Alkane gehorchen folgendem Prinzip:
1 30.09.005 0.1 Alkane Eine einfache Stoffgruppe der organischen Chemie sind die Alkane. Dabei handelt es sich um eine spezielle Gruppe der Kohlenwasserstoffe (KW). Alle Alkane gehorchen folgendem Prinzip:
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Cycloalkane enthalten eine oder mehrere gesättigte, ringförmige Kohlenstoffketten. Cycloalkane
 3. Cycloalkane Cycloalkane enthalten eine oder mehrere gesättigte, ringförmige Kohlenstoffketten. Einteilung: Cycloalkane Cycloaliphaten (Alicyclen, Carbocyclen) Polycyclen Cycloaliphaten (Alicyclen, Carbocyclen):
3. Cycloalkane Cycloalkane enthalten eine oder mehrere gesättigte, ringförmige Kohlenstoffketten. Einteilung: Cycloalkane Cycloaliphaten (Alicyclen, Carbocyclen) Polycyclen Cycloaliphaten (Alicyclen, Carbocyclen):
Grundkurs Chemie Alkane
 Grundkurs Chemie Alkane Abituraufgaben 1975/I Monobrompropan soll auf zwei verschiedenen Synthesewegen aus zwei verschiedenen Kohlenwasserstoffen hergestellt werden. 1. Bennen Sie die dafür geeigneten
Grundkurs Chemie Alkane Abituraufgaben 1975/I Monobrompropan soll auf zwei verschiedenen Synthesewegen aus zwei verschiedenen Kohlenwasserstoffen hergestellt werden. 1. Bennen Sie die dafür geeigneten
Konfigurationsisomerie
 Konfigurationsisomerie Enatiomerie, Diastereomerie (σ undπ). Prof.Dr. Ivo C. Ivanov 1 Optische Aktivität Zur Bestimmung des Drehwertes bedient man sich eines Polarimeters, dessen Aufbau nachfolgend schematisch
Konfigurationsisomerie Enatiomerie, Diastereomerie (σ undπ). Prof.Dr. Ivo C. Ivanov 1 Optische Aktivität Zur Bestimmung des Drehwertes bedient man sich eines Polarimeters, dessen Aufbau nachfolgend schematisch
2. Elektroneneffekte in den organischen Molekülen
 2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
Organische Chemie der Freien Universität Berlin. Klausur SS 2008 Teil 1
 rganische Chemie der Freien Universität Berlin C I Grundlagen der rganischen Chemie (LV 21 201a) Klausur SS 2008 Teil 1 Verfasser: Datum: 07.06.2008 Prof. Dr. H.-U. Reißig Semester: SS 08 Höchstpunktzahl:
rganische Chemie der Freien Universität Berlin C I Grundlagen der rganischen Chemie (LV 21 201a) Klausur SS 2008 Teil 1 Verfasser: Datum: 07.06.2008 Prof. Dr. H.-U. Reißig Semester: SS 08 Höchstpunktzahl:
Inhaltsverzeichnis. 3 Organische Chemie. Vorwort Chemische Bindung Chemische Reaktionstypen Bindungen...
 VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
Organische Chemie für Technische Biologen Organische Chemie für Lehramtskandidaten Sommersemester 2005 Prof. Dr. Stephen Hashmi.
 Organische Chemie für Technische Biologen Organische Chemie für Lehramtskandidaten Sommersemester 2005 Prof Dr Gliederung des Vorlesungsstoffes I Allgemeines II Chemische Bindung III Einteilung der Organischen
Organische Chemie für Technische Biologen Organische Chemie für Lehramtskandidaten Sommersemester 2005 Prof Dr Gliederung des Vorlesungsstoffes I Allgemeines II Chemische Bindung III Einteilung der Organischen
