Springer-Lehrbuch. Lehninger Biochemie. Bearbeitet von David Nelson, Michael Cox, A Held ISBN Zu Leseprobe
|
|
|
- Ernst Fleischer
- vor 7 Jahren
- Abrufe
Transkript
1 Springer-Lehrbuch Lehninger Biochemie Bearbeitet von David Nelson, Michael Cox, A Held erweitert, überarbeitet Buch. XXXVIII, 1342 S. Hardcover ISBN Zu Leseprobe schnell und portofrei erhältlich bei Die Online-Fachbuchhandlung beck-shop.de ist spezialisiert auf Fachbücher, insbesondere Recht, Steuern und Wirtschaft. Im Sortiment finden Sie alle Medien (Bücher, Zeitschriften, CDs, ebooks, etc.) aller Verlage. Ergänzt wird das Programm durch Services wie Neuerscheinungsdienst oder Zusammenstellungen von Büchern zu Sonderpreisen. Der Shop führt mehr als 8 Millionen Produkte.
2 Teil I Grundlagen der Biochemie 1 Die molekulare Logik des Lebens Die chemische Einheit der verschiedenen Lebewesen Die Biochemie erklärt verschiedenartige Lebensformen mit einheitlichen chemischen Begriffen Sämtliche Makromoleküle bestehen aus einigen wenigen einfachen Verbindungen Energie Produktion und Verbrauch im Stoffwechsel Organismen befinden sich nie im Gleichgewicht mit ihrer Umgebung In der molekularen Zusammensetzung spiegelt sich ein dynamisches Fließgleichgewicht wider Organismen wandeln Energie und Materie aus ihrer Umgebung um Organismen holen ihre Energie aus einem Fluss von Elektronen Biologische Reaktionen sind über Energiekopplung miteinander verbunden Enzyme ermöglichen eine Abfolge chemischer Reaktionen Die Regulation des Stoffwechsels sorgt für Balance und Ökonomie Biologischer Informationsaustausch In den DNA-Molekülen wird die genetische Kontinuität bewahrt Aufgrund ihrer Struktur kann die DNA nahezu perfekt repariert und repliziert werden Veränderungen in der Erbinformation ermöglichen die Evolution Die Molekülstruktur offenbart evolutionäre Verwandtschaften In der linearen DNA-Sequenz ist die Information für dreidimensionale Proteinstrukturen gespeichert Nicht-kovalente Wechselwirkungen stabilisieren dreidimensionale Strukturen Die physikalischen Wurzeln der biochemischen Welt Weiterführende Literatur Zellen Die Größenordnungen der Zelle Zellen und Gewebe, die in biochemischen Untersuchungen verwendet werden Evolution und Struktur prokaryotischer Zellen Evolution eukaryotischer Zellen Eukaryotische Zellen entwickelten sich in mehreren Phasen aus den Prokaryoten Aus den ersten eukaryotischen Zellen entstanden unterschiedliche Protisten Die wichtigsten Strukturen eukaryotischer Zellen Die Plasmamembran enthält Transportproteine und Rezeptoren Endocytose und Exocytose sorgen für den Transport durch die Plasmamembran Das endoplasmatische Reticulum steuert die Protein- und Lipidsynthese Im Golgi-Apparat werden Proteine verarbeitet und sortiert In den Lysosomen werden Substanzen abgebaut Vacuolen von Pflanzenzellen haben mehrere wichtige Funktionen Peroxisomen zerstören Wasserstoffperoxid, Glyoxysomen verwandeln Fette in Kohlenhydrate XIX
3 2.5.8 Im Zellkern befindet sich das Genom Mitochondrien sind die Kraftwerke aerober eukaryotischer Zellen Chloroplasten wandeln Sonnenenergie in chemische Energie um Mitochondrien und Chloroplasten sind wahrscheinlich aus endosymbiotischen Bakterien hervorgegangen Das Cytoskelett stabilisiert die Zellform, organisiert das Cytoplasma und dient der Bewegung Im Cytoplasma befinden sich viele Strukturen, die hochgradig geordnet sind und sich ständig verändern Untersuchung zellulärer Bestandteile Organellen lassen sich durch Zentrifugation isolieren Bei In-vitro-Studien werden unter Umständen wichtige Wechselwirkungen zwischen Molekülen übersehen Die Evolution vielzelliger Organismen und ihre Differenzierung auf Zellebene Viren, die Parasiten der Zelle Zusammenfassung Weiterführende Literatur Aufgaben Biomoleküle Chemische Zusammensetzung und chemische Bindung Biomoleküle sind Kohlenstoffverbindungen Funktionelle Gruppen bestimmen die chemischen Eigenschaften Dreidimensionale Struktur: Konformation und Konfiguration Die Konfiguration eines Moleküls kann sich nur ändern, wenn eine Bindung gelöst wird Die Konformation eines Moleküls ändert sich durch Drehung um Einfachbindungen EXKURS 3-1 Louis Pasteur und die optische Aktivität: In vino veritas Konfiguration und Konformation definieren zusammen die Struktur von Biomolekülen Wechselwirkungen zwischen Biomolekülen sind stereospezifisch Chemische Reaktivität Die Bindungsstärke hängt von den Eigenschaften der daran beteiligten Atome ab Es gibt fünf Klassen biochemischer Reaktionen Bei allen Oxidations-Reduktions- Reaktionen werden Elektronen übertragen In nucleophilen Substitutions - reaktionen werden Kohlenstoff Kohlenstoff Bindungen gespalten und neue gebildet Ein Elektronentransfer innerhalb eines Moleküls führt zu internen Umlagerungen Gruppenübertragungsreaktionen aktivieren Stoffwechselzwischenprodukte Durch Kondensation entstehen Biopolymere Makromoleküle und ihre monomeren Untereinheiten Die Hauptbestandteile der Zellen sind Makromoleküle Makromoleküle setzen sich aus monomeren Untereinheiten zusammen Monomere Untereinheiten sind einfach aufgebaut Die Kondensation von Untereinheiten erhöht den Ordnungsgrad, erfordert aber Energie In der Zelle herrscht eine strukturelle Hierarchie Die Evolution vor dem Beginn des Lebens Die ersten Biomoleküle entstanden im Verlauf einer chemischen Evolution Die chemische Evolution kann im Labor nachgeahmt werden RNA oder verwandte Vorstufen waren möglicherweise die ersten Gene und Katalysatoren Die biologische Evolution begann vor über 3,5 Milliarden Jahren Zusammenfassung Weiterführende Literatur Aufgaben Wasser Schwache Wechselwirkungen in wässrigen Systemen Wasserstoffbrücken verleihen Wasser seine ungewöhnlichen Eigenschaften Wasser bildet Wasserstoffbrücken mit polaren gelösten Stoffen Wasser geht mit gelösten Ionen elektrostatische Wechselwirkungen ein Beim Auflösen kristalliner Substanzen nimmt die Entropie zu XX
4 4.1.5 Unpolare Gase lösen sich schlecht in Wasser Unpolare Verbindungen erzwingen energetisch ungünstige Veränderungen der Wasserstruktur Van-der-Waals-Wechselwirkungen sind schwache interatomare Anziehungskräfte Schwache Wechselwirkungen sind für Struktur und Funktion von Makromolekülen ausschlaggebend Gelöste Stoffe beeinflussen die kolligativen Eigenschaften wässriger Lösungen Dissoziation von Wasser, schwachen Säuren und schwachen Basen EXKURS 4 1 Reaktion von Pflanzen auf Berührungen: Ein osmotischer Effekt Reines Wasser ist in geringem Umfang dissoziiert Die Dissoziation von Wasser lässt sich durch eine Gleichgewichtskonstante ausdrücken EXKURS 4 2 Das Ionenprodukt von Wasser: zwei Beispiele zur Veranschaulichung Die ph-skala gibt die H + - und OH -Konzentrationen an Schwache Säuren und Basen haben charakteristische Dissoziationskonstanten Titrationskurven zeigen den pk a -Wert schwacher Säuren Pufferung gegen ph-änderungen in biologischen Systemen Puffer sind Mischungen schwacher Säuren und ihrer konjugierten Basen Eine einfache Gleichung verbindet ph, pk a und Pufferkonzentration EXKURS 4 3 Berechnungen mit der Henderson-Hasselbalch-Gleichung Schwache Säuren oder Basen puffern Zellen und Gewebe gegen ph-änderungen EXKURS 4 4 Blut, Lungen und Puffer: Das Hydrogencarbonat-Puffersystem Wasser als Reaktant Die Eignung der wässrigen Umgebung für Lebewesen Zusammenfassung Weiterführende Literatur Aufgaben Teil II Struktur und Katalyse 5 Aminosäuren, Peptide und Proteine Aminosäuren Aminosäuren besitzen gemeinsame Strukturmerkmale Aminosäuren in Proteinen haben l-konfiguration Aminosäuren lassen sich durch ihre Seitenketten unterscheiden Nicht-Standardaminosäuren haben ebenfalls wichtige Funktionen Aminosäuren können als Säuren und Basen wirken EXKURS 5 1 Absorption von Licht durch Moleküle: Das Lambert-Beer-Gesetz Aminosäuren besitzen charakteristische Titrationskurven Aus der Titrationskurve lässt sich der isoelektrische Punkt einer Aminosäure bestimmen Aminosäuren haben unterschiedliche Säure-Base-Eigenschaften Peptide und Proteine Peptide sind Ketten aus Aminosäuren Peptide lassen sich anhand ihres Dissoziationsverhaltens unterscheiden Biologisch aktive Peptide und Polypeptide kommen in unterschiedlichen Größen vor Polypeptide haben charakteristische Aminosäurenzusammensetzungen Einige Proteine enthalten neben Aminosäuren noch andere chemische Gruppen Die Proteinstruktur kann auf vier Ebenen definiert werden Arbeiten mit Proteinen Proteine können isoliert und gereinigt werden Proteine können durch Elektrophorese getrennt und charakterisiert werden Nicht getrennte Proteine können quantitativ bestimmt werden Die kovalente Struktur der Proteine Die Funktion eines Proteins wird durch seine Aminosäuresequenz bestimmt Die Aminosäuresequenzen zahlreicher Proteine sind bekannt EXKURS 5 2 Homologe Proteine bei verschiedenen Arten XXI
5 5.4.3 Kurze Polypeptide werden mit automatisierten Verfahren sequenziert Große Proteine müssen in kleinen Abschnitten sequenziert werden Aminosäuresequenzen können auchmit anderen Methoden abgeleitet werden Aminosäuresequenzen liefern wichtige biochemische Informationen Kleine Peptide und Proteine können chemisch synthetisiert werden EXKURS 5 3 Massenspektrometrische Untersuchung von Proteinen Zusammenfassung Weiterführende Literatur Aufgaben Die dreidimensionale Struktur von Proteinen Übersicht über die Proteinstruktur Die Proteinkonformation wird hauptsächlich durch schwache Wechselwirkungen stabilisiert Die Peptidbindung ist starr und planar Sekundärstruktur von Proteinen Die a-helix ist eine häufige Sekundärstruktur in Proteinen EXKURS 6 1 Unterscheidung der rechten von der linken Hand Die Aminosäuresequenz beeinflusst die Stabilität von a-helices Die b-konformation ordnet Polypeptidketten zu Schichten b-schleifen kommen in Proteinen häufig vor Häufig auftretende Sekundärstrukturen besitzen charakteristische Bindungswinkel und Aminosäurenzusammensetzungen Tertiär- und Quartärstrukturen von Proteinen Faserproteine sind an ihre strukturelle Funktion angepasst EXKURS 6 2 Dauerwellen sind das Ergebnis eines biochemischen Prozesses Die strukturelle Vielfalt spiegelt die funktionelle Vielfalt globulärer Proteine wider Myoglobin lieferte frühe Hinweise auf die komplexe Struktur globulärer Proteine Globuläre Proteine besitzen vielfältige Tertiärstrukturen EXKURS 6 3 Methoden zur Bestimmung der dreidimensionalen Struktur eines Proteins Die Analyse vieler globulärer Proteine zeigt strukturelle Gemeinsamkeiten Proteinmotive sind die Grundlage für die Klassifizierung der Proteinstruktur Quartärstrukturen von Proteinen reichen von einfachen Dimerenbis zu großen Komplexen Die Größe von Proteinen ist begrenzt Denaturierung und Faltung von Proteinen Der Verlust der Proteinstruktur führt zum Verlust der Funktion Die Aminosäuresequenz bestimmt die Tertiärstruktur Polypeptide falten sich rasch in einem schrittweisen Prozess Bei einigen Proteinen wird die Faltung unterstützt EXKURS 6 4 Tod durch Fehlfaltung: Prionenerkrankungen Zusammenfassung Weiterführende Literatur Aufgaben Proteinfunktion Die reversible Bindung eines Proteins an einen Liganden: Sauerstoff bindende Proteine Sauerstoff kann an eine prosthetische Hämgruppe binden Myoglobin hat eine einzige Bindungsstelle für Sauerstoff Protein-Ligand-Wechselwirkungen können quantitativ beschrieben werden Die Proteinstruktur beeinflusst die Ligandenbindung Der Sauerstofftransport im Blut erfolgt durch Hämoglobin Hämoglobin-Untereinheiten ähneln in ihrer Struktur dem Myoglobin Bei Sauerstoffbindung erfährt Hämoglobin eine Strukturänderung Hämoglobin bindet Sauerstoff kooperativ Die kooperative Ligandenbindung kann quantitativ beschrieben werden Zwei Modelle zeigen die möglichen Mechanismen der kooperativen Bindung Hämoglobin transportiert auch H + und CO XXII
6 Die Sauerstoffbindung an Hämoglobin wird durch 2,3-Bisphosphoglycerat reguliert Sichelzellanämie ist eine molekulare Erkrankung des Hämoglobins Komplementäre Wechselwirkungen zwischen Proteinen und Liganden: Immunsystem und Immunglobuline Für die Immunantwort steht ein ganzes Heer spezialisierter Zellen und Moleküle zur Verfügung Die Unterscheidung von Selbst und Nicht-Selbst erfolgt durch Peptide auf der Zelloberfläche Molekulare Kontakte an der Zelloberfläche lösen die Immunreaktion aus Antikörper haben zwei identische Antigen-Bindungsstellen Antikörper binden fest und spezifisch an Antigene Die Antikörper-Antigen-Wechselwirkung ist Grundlage für eine Vielzahl wichtiger analytischer Verfahren Die Modulation von Proteinwechselwirkungen durch chemische Energie: Actin, Myosin und molekulare Motoren Myosin und Actin sind die wichtigsten Proteine des Muskels Weitere Proteine lassen aus den dünnen und dicken Filamenten geordnete Strukturen entstehen Dicke Myosinfilamente gleiten an dünnen Actinfilamenten entlang Zusammenfassung Weiterführende Literatur Aufgaben Enzyme Einführung Die meisten Enzyme sind Proteine Die Klassifizierung der Enzyme erfolgt nach den Reaktionen, die sie katalysieren Die Funktionsweise der Enzyme Enzyme beeinflussen die Geschwindigkeit, aber nicht das Gleichgewicht einer Reaktion Reaktionsgeschwindigkeiten und -gleichgewichte sind thermodynamisch genau definiert Wenige Prinzipien genügen, um die katalytische Leistung und Spezifität der Enzyme zu erklären Schwache Wechselwirkungen zwischen Enzym und Substratwerden im Übergangszustand optimiert Bindungsenergie leistet einen Beitrag zur Spezifität der Reaktion und zu ihrer Katalyse Spezifische katalytische Gruppen beteiligen sich an der Katalyse Durch Enzymkinetik zum Verständnis der Reaktionsmechanismen Die Substratkonzentration beeinflusst die Geschwindigkeit enzymkatalysierter Reaktionen Die Beziehung zwischen Substratkonzentration und Reaktionsgeschwindigkeit kann quantitativ ausgedrückt werden EXKURS 8 1 Transformationen der Michaelis-Menten-Gleichung: Die doppelt-reziproke Darstellung Kinetische Parameter werden zum Vergleich enzymatischer Aktivitäten herangezogen Viele Enzyme katalysieren Reaktionen mit zwei oder mehr Substraten Kinetische Daten des prästationären Zustands können Hinweise auf spezifische Reaktionsschritte liefern Enzyme können gehemmt werden Reversible Hemmung kann kompetitiv, unkompetitiv oder gemischt sein EXKURS 8 2 Kinetische Bestimmung der verschiedenen Hemmungsmechanismen Die irreversible Hemmung ist ein wichtiges Werkzeug in Enzymforschung und Pharmakologie Die Enzymaktivität wird vom ph-wert beeinflusst Beispiele enzymatischer Reaktionen Reaktionsmechanismen ausgewählter Enzyme EXKURS 8 3 Hinweise auf die Komplementarität von Enzym und Übergangszustand Regulatorische Enzyme Allosterische Enzyme reagieren auf die Bindung eines Modulators mit einer Konformationsänderung Der regulatorische Schritt vieler Stoffwechselwege wird von allosterischen Enzymen katalysiert Die kinetischen Eigenschaften allosterischer Enzyme weichen vom Michaelis-Menten-Verhalten ab XXIII
7 8.5.4 Einige regulatorische Enzyme erfahren reversible kovalente Modifikation Phosphatgruppen beeinflussen die Struktur und katalytische Aktivität von Proteinen Multiple Phosphorylierungen erlauben eine hervorragende regulatorische Kontrolle Die proteolytische Spaltung einer Enzymvorstufe als Regulationsmechanismus Einige regulatorische Enzyme verwenden multiple regulatorische Mechanismen Zusammenfassung Weiterführende Literatur Aufgaben Kohlenhydrate und Glycobiologie Monosaccharide und Disaccharide Die beiden Monosaccharidfamilien sind Aldosen und Ketosen Monosaccharide besitzen asymmetrische Zentren Die häufigen Monosaccharide haben eine ringförmige Struktur Lebewesen enthalten eine Vielzahl von Hexosederivaten Monosaccharide sind Reduktionsmittel Disaccharide enthalten eine glycosidische Bindung Polysaccharide Stärke und Glycogen sind gespeicherte Brennstoffe Cellulose und Chitin sind Struktur- Homopolysaccharide Bakterienzellwände enthalten Peptidoglycane Glycosaminoglycane sind Bestandteile der extrazellulären Matrix Glycokonjugate: Proteoglycane, Glycoproteine und Glycolipide Proteoglycane sind Glycosaminoglycanhaltige Makromoleküle der Zelloberfläche und der extrazellulären Matrix Glycoproteine sind informationsreiche Konjugate, die Oligosaccharide enthalten Glycolipide und Lipopolysaccharide sind Bestandteile von Membranen Wechselwirkungen zwischen Oligosacchariden und Lectinen vermitteln zahlreiche biologische Prozesse Analyse von Kohlenhydraten Zusammenfassung Weiterführende Literatur Aufgaben Nucleotide und Nucleinsäuren Einige Grundlagen Nucleotide und Nucleinsäuren enthalten charakteristische Basen und Pentosen In Nucleinsäuren sind die aufeinander folgenden Nucleotide über Phosphodiesterbindungen miteinander verbunden Die Eigenschaften der Nucleotidbasen beeinflussen die dreidimensionale Struktur der Nucleisäuren Die Struktur der Nucleinsäuren In der DNA ist die genetische Information gespeichert Jedes DNA-Molekül hat eine eindeutige Basenzusammensetzung Die DNA ist eine Doppelhelix Die DNA kann unterschiedliche dreidimensionale Formen annehmen Bestimmte DNA-Sequenzen nehmen ungewöhnliche Formen an Messenger-RNAs codieren Polypeptidketten Viele RNAs haben kompliziertere dreidimensionale Strukturen Die Chemie der Nucleinsäuren Doppelhelicale DNA und RNA kann denaturiert werden Nucleinsäuren aus unterschiedlichen Spezies können hybridisieren Nicht-enzymatische Veränderungen von Nucleotiden und Nucleinsäuren Einige DNA-Basen sind methyliert Sequenzierung langer DNA-Stränge Die chemische DNA-Synthese ist automatisiert Andere Funktionen der Nucleotide Nucleotide sind die Träger der chemischen Energie Viele Cofaktoren von Enzymen enthalten Adeninnucleotide Einige Nucleotide haben regulatorische Funktionen Zusammenfassung Weiterführende Literatur Aufgaben XXIV
8 11 Lipide Speicherlipide Fettsäuren leiten sich von Kohlenwasserstoffen ab Triacylglycerine sind Fettsäureester des Glycerins Triacylglycerine speichern Energie und sind gute Isolatoren EXKURS 11 1 Pottwale mit Köpfen voller Fett in die Tiefe Viele Nahrungsmittel enthalten Triacylglycerine Wachse speichern Energie und sind wasserabstoßend Strukturlipide in Membranen Glycerophospholipide leiten sich von Phosphatidsäure ab Bei einigen Phospholipiden sind die Fettsäuren mit dem Molekül verethert Sphingolipide stammen vom Sphingosin ab Biologische Erkennung erfolgt über Sphingolipide auf der Zelloberfläche Phospholipide und Sphingolipide werden in Lysosomen abgebaut Sterole enthalten vier fusionierte Kohlenstoffringe Lipide als Signale, Cofaktoren und Pigmente Phosphatidylinositole dienen als intrazelluläre Signale EXKURS 11 2 Menschliche Erbkrankheiten, die auf einer anomalen Anhäufung von Membranlipiden beruhen Eicosanoide übermitteln benachbarten Zellen Botschaften Steroidhormone überbringen Botschaften zwischen den Geweben Die Vitamine A und D sind Hormonvorstufen Die Vitamine E und K sowie die Lipidchinone sind Cofaktoren für Redoxreaktionen Dolichole aktivieren Zuckervorstufen für die Biosynthese Isolierung und Untersuchung von Lipiden Für eine Lipidextraktion benötigt man organische Lösungsmittel Mit Adsorptionschromatographie trennt man unterschiedlich polare Lipide Mit Gasflüssigkeitschromatographie trennt man Gemische von flüchtigen Lipidderivaten Eine spezifische Hydrolyse ist ein erster Schritt zur Bestimmung der Lipidstruktur Mithilfe der Massenspektrometrie lässt sich die gesamte Lipidstruktur entschlüsseln Zusammenfassung Weiterführende Literatur Aufgaben Biologische Membranen und Transport Die molekularen Bestandteile der Membran Die supramolekulare Membran architektur Das grundlegende Strukturelement der Membran ist eine Lipiddoppelschicht Membranlipide sind ständig in Bewegung Lateraldiffusion von Membranproteinen in der Doppelschicht EXKURS 12 1 Ein Blick auf Membranen Einige Membranproteine ziehen sich durch die Lipiddoppelschicht Periphere Membranproteine lassen sich leicht in Lösung bringen Einige periphere Membranproteine sind über kovalent gebundene Lipide verankert Integrale Proteine werden über hydrophobe Wechselwirkungen mit Lipiden in der Membran fixiert Manchmal kann man die Topologie eines integralen Membranproteins aufgrund seiner Sequenz vorhersagen Integrale Proteine sorgen für Interaktionen und Adhäsion zwischen Zellen Die Fusion von Membranen steht im Zentrum vieler biologischer Prozesse Transport gelöster Stoffe durch die Membran Membranproteine erleichtern den passiven Transport Aquaporine bilden hydrophile Kanäle, über die Wasser durch die Membran gelangt Der Glucosetransporter der Erythrocyten sorgt für einen passiven Transport Chlorid und Hydrogencarbonat werden zusammen durch die Erythrocytenmembran geschleust XXV
9 Durch aktiven Transport werden gelöste Stoffe gegen einen Konzentrations- oder elektrochemischen Gradienten bewegt. 438 EXKURS 12 2 Gestörter Glucoseund Wassertransport bei zwei Formen von Diabetes Es gibt mindestens vier allgemeine Arten von Transport-ATPasen EXKURS 12 3 Cystische Fibrose entsteht aufgrund eines defekten Ionenkanals Eine ATPase vom P-Typ katalysiert den aktiven Cotransport von Na + und K ATP-abhängige Ca 2+ -Pumpen sorgen für eine niedrige Calciumkonzentration im Cytosol Ionengradienten liefern die Energie für einen sekundären aktiven Transport Mithilfe von ionenselektiven Kanäle können Ionen schnell durch Membranen geschleust werden Anhand der Struktur eines K + -Kanals kann man erkennen, worauf seine Ionenspezifität beruht Der Acetylcholinrezeptor ist ein ligandengesteuerter Ionenkanal Der neuronale Na + -Kanal ist ein spannungsgesteuerter Ionenkanal Man kann die Funktion der Ionenkanäle elektrisch messen Defekte Ionenkanäle können erhebliche physiologische Folgen haben Porine sind Kanäle, die kleine Moleküle die Membran passieren lassen Zusammenfassung Weiterführende Literatur Aufgaben Biologische Signale Molekulare Mechanismen der Signalübertragung EXKURS 13 1 Scatchard-Analyse: Untersuchungen zu Wechselwirkungen zwischen Ligand und Rezeptor Gesteuerte Ionenkanäle Erregbare Zellen nutzen Jonenkanäle für die Übertragung elektrischer Signale Der nicotinische Acetylcholinrezeptor ist ein ligandengesteuerter Ionenkanal Spannungsgesteuerte Ionenkanäle erzeugen neuronale Aktionspotentiale Neuronen haben Rezeptorkanäle, die auf viele verschiedene Neurotransmitterreagieren Rezeptorenzyme Der Insulinrezeptor ist eine tyrosinspezifische Proteinkinase Die Guanylylcyclase ist ein Rezeptorenzym, das den second messenger cgmp herstellt Mit G-Proteinen gekoppelte Rezeptoren und Second-messenger-Moleküle Das b-adrenerge Rezeptorsystem wirkt über den second messenger camp Der b-adrenerge Rezeptor wird durch Phosphorylierung desensibilisiert Zyklisches AMP dient einer Reihe von regulatorischen Molekülen als second messenger Zwei second messenger stammen von Phosphatidylinositol ab Calcium wirkt bei vielen Signalübertragungreaktionen als second messenger Übertragung sensorischer Reize beim Sehen, Riechen und Schmecken Licht hyperpolarisiert Stäbchen- und Zapfenzellen im Auge von Wirbeltieren Licht löst im Rezeptor Rhodopsin Konformationsänderungen aus Angeregtes Rhodopsin senkt mithilfe des G-Proteins Transducin die cgmp-konzentration In den Stäbchen- und Zapfenzellen wird das Signal verstärkt Das visuelle Signal wird rasch abgeschaltet Rhodopsin wird durch Phosphorylierung desensibilisiert Zapfenzellen sind auf das Farbsehen spezialisiert EXKURS 13-2 Farbblindheit: Wie ein Experiment von John Dalton noch nach seinem Tod erfolgreich abgeschlossen wurde Beim Riechen und Schmecken nutzen Wirbeltiere ähnliche Mechanismen wie beim Sehen Sieben-Helix-Rezeptorsysteme, die an G-Proteine gekoppelt sind, haben einige gemeinsame Merkmale Eine Störung der Signalübertragung von G-Proteinen verursacht Krankheiten Regulation durch Phosphorylierung Die Lokalisation der Proteinkinasen und Phosphatasen beinflussen die Spezifität für ihre Zielproteine XXVI
10 13.7 Regulation der Transcription durch Steroidhormone Die Rolle der Proteinkinasen bei der Steuerung des Zellzyklus Der Zellzyklus besteht aus vier Phasen Die Konzentration an Cyclin-abhängigen Proteinkinasen oszilliert CDKs regulieren die Zellteilung durch Phosphorylierung bestimmter Proteine Oncogene, Tumorsuppressor-Gene und programmierter Zelltod Oncogene sind mutierte Formen von Genen für Proteine, die den Zellzyklus regulieren Fehler in Tumorsuppressor-Genen sorgen dafür, dass die normalen Kontrollen der Zellteilung entfallen Apoptose ist programmierter Zelltod Zusammenfassung Weiterführende Literatur Aufgaben Teil III Bioenergetik und Stoffwechsel 14 Prinzipien der Bioenergetik Bioenergetik und Thermodynamik Biologische Energieumwandlungen gehorchen den Gesetzen der Thermodynamik Zellen benötigen Quellen von Freier Enthalpie EXKURS 14 1 Entropie: Der Vorteil mangelnder Organisation Die Änderung der Freien Standardenthalpie steht in direkter Beziehung zur Gleichgewichtskonstante Die tatsächliche Änderung der Freien Enthalpie hängt von den Konzentrationen der Reaktanten und Produkte ab Änderungen der Freien Standardenthalpie sind additiv Phosphorylgruppenübertragungen und ATP Die Freie Enthalpieänderung der ATP-Hydrolyse ist groß und negativ Die Freie Enthalpie der Hydrolyse von anderen phosphorylierten Verbindungen und Thioestern ist ebenfalls groß EXKURS 14 2 Die Freie Enthalpie der ATP-Hydrolyse in Zellen: Die wahren Kosten des Stoffwechsels ATP liefert Energie durch Gruppenübertragungen, nicht durch einfache Hydrolyse ATP ist ein Donator von Phosphoryl-, Pyrophosphoryl- und Adenylatgruppen Der Aufbau von informationsreichen Makromolekülen erfordert Energie EXKURS 14 3 Leuchtkäferlicht macht ATP sichtbar ATP liefert die Energie für den aktiven Transport und die Muskelkontraktion Phosphorylgruppenübertragungen zwischen Nucleotiden kommen in allen Zelltypen vor Anorganisches Polyphosphat ist ein potentieller Phosphorylgruppendonator Biochemische und chemische Gleichungen sind nicht identisch Biologische Redoxreaktionen Der Elektronenfluss kann biologische Arbeit verrichten Redoxreaktionen können als Halbreaktionen formuliert werden Bei biologischen Oxidationen kommt es häufig zu Dehydrierung Reduktionspotentiale messen die Elektronenaffinität Standardreduktionspotentiale können für die Berechnung von Freien Enthalpieänderungen benutzt werden Für die zelluläre Oxidation von Glucose zu Kohlendioxid sind spezialisierte Elektronencarrier nötig Einige Arten von Coenzymen und Proteinen sind universelle Elektronencarrier NADH und NADPH wirken zusammen mit Dehydrogenasen als lösliche Elektronencarrier Flavinnucleotide sind fest an Flavoproteine gebunden Zusammenfassung Weiterführende Literatur Aufgaben Glycolyse und der Katabolismus der Hexosen Glycolyse Ein Überblick: Die Glycolyse verläuft in zwei Stufen Die erste Stufe der Glycolyse erfordert ATP In der zweiten Stufe der Glycolyse der Ertragsstufe werden ATP und NADH gebildet XXVII
11 Die Gesamtbilanz weist einen Netto - gewinn an ATP auf Die Zwischenprodukte der Glycolyse werden von Enzym zu Enzym weitergegeben Die Glycolyse ist streng reguliert Der Glucoseabbau gerät in Tumoren außer Kontrolle EXKURS 15 1 Glycolyse bei begrenzter Sauerstoffzufuhr: Athleten, Alligatoren und Quastenflosser Der Abbau von Pyruvat unter aeroben und anaeroben Bedingungen Pyruvat ist der endgültige Elektronenakzeptor bei der Milchsäuregärung EXKURS 15 2 Bierbrauen Ethanol ist das reduzierte Produkt der alkoholischen Gärung Thiaminpyrophosphat trägt aktive Aldehydgruppen Mikrobielle Fermentation liefert auch weitere, wirtschaftlich bedeutende Produkte Stoffwechselwege, die die Glycolyse speisen Glycogen und Stärke werden durch Phosphorolyse abgebaut Auch andere Monosaccharide treten in die Glycolyse ein allerdings an verschiedenen Punkten Poly- und Disaccharide aus der Nahrung werden hydrolytisch zu Monosacchariden abgebaut Die Regulation des Kohlenhydratstoffwechsels Regulatorische Enzyme wirken im Metabolismus als Ventile Glycolyse und Gluconeogenese werden koordiniert reguliert Phosphofructokinase-1 steht unter komplexer allosterischer Regulation Hexokinase wird von ihrem eigenen Produkt allosterisch gehemmt Pyruvatkinase wird durch ATP inhibiert. 598 EXKURS 15 3 Isoenzyme: Verschiedene Proteine die gleiche Reaktion Glycogen-Phosphorylase wird allosterisch und durch Hormone reguliert Glucose-Oxidation im Pentosephosphat-Weg EXKURS 15 4 Glucose-6-phosphat- Mangel: Warum Pythagoras keinen Falafel essen wollte Zusammenfassung Weiterführende Literatur Aufgaben Der Citratzyklus Bildung von Acetat Pyruvat wird zu Acetyl-CoA und CO 2 oxidiert Der Pyruvat-Dehydrogenase-Komplex benötigt fünf Coenzyme Der Pyruvat-Dehydrogenase-Komplex besteht aus drei unterschiedlichen Enzymen Zwischenprodukte bleiben an die Enzymoberfläche gebunden Reaktionen des Citratzyklus Der Citratzyklus umfasst acht Schritte EXKURS 16 1 Zur verwirrenden Nomenklatur von Synthasen und Synthetasen; Ligasen und Lyasen; Kinasen, Phosphatasen und Phosphorylasen Die Energie der Oxidationen im Zyklus Warum ist die Oxidation von Acetat so kompliziert? EXKURS 16 2 Citrat: Ein symmetrisches Molekül, das asymmetrisch reagiert Die Komponenten des Citratzyklus sind wichtige Zwischenprodukte der Biosynthese EXKURS 16 3 Citrat-Synthase, Limonadengetränke und Nahrungsmittel für die Welt Anaplerotische Reaktionen füllen die Zwischenprodukte des Citratzyklus wieder auf Biotin in Pyruvat-Carboxylase ist ein CO 2 -Carrier Regulation des Citratzyklus Die Produktion von Acetyl-CoA durch den Pyruvat-Dehydrogenase-Komplex wird durch allosterische und kovalente Mechanismen reguliert Der Citratzyklus wird auf Ebene seiner drei exergonen Schritte reguliert Der Glyoxylatzyklus Der Glyoxylatzyklus erzeugt aus Acetat C 4 -Verbindungen Der Citrat- und der Glyoxylatzyklus werden gemeinsam reguliert Zusammenfassung Weiterführende Literatur Aufgaben XXVIII
12 17 Die Oxidation von Fettsäuren Verdauung, Mobilisierung und Transport von Fetten Nahrungsfette werden im Dünndarm absorbiert Hormone mobilisieren gespeicherte Triacylglycerine Fettsäuren werden aktiviert und in die Mitochondrien transportiert b-oxidation Die b-oxidation von gesättigten Fettsäuren verläuft in vier Schritten Die vier Schritte werden zur Bildung von Acetyl-CoA und ATP wiederholt Acetyl-CoA kann im Citratzyklus weiter oxidiert werden EXKURS 17 1 b-oxidation bei Bären im Winterschlaf Die Oxidation ungesättigter Fettsäuren erfordert zwei zusätzliche Reaktionen Die vollständige Oxidation von Fettsäuren mit ungerader Kohlenstoffzahl erfordert drei zusätzliche Reaktionen Die Fettsäureoxidation ist streng reguliert EXKURS 17 2 Coenzym B 12 : eine radikale Lösung für ein kompliziertes Problem Peroxisomen führen ebenfalls b-oxidation aus Peroxisomen und Glyoxysomen in Pflanzen verwenden Acetyl-CoA aus der b-oxidation als Biosynthesevorstufen Die Enzyme der b-oxidation unterschiedlicher Organellen haben sich im Laufe der Evolution auseinander entwickelt Die Omega-Oxidation läuft im endoplasmatischen Reticulum ab Genetische Defekte von Fettsäureacyl- CoA-Dehydrogenasen verursachen schwere Erkrankungen Ketokörper In der Leber gebildete Ketokörper werden in andere Organe transportiert Extrahepatische Gewebe verwenden Ketokörper als Brennstoff Überproduktion von Ketokörpern bei Diabetes und längerem Fasten Zusammenfassung Weiterführende Literatur Aufgaben Aminosäureoxidation und die Produktion von Harnstoff Stoffwechselwege von Aminogruppen Nahrungsproteine werden enzymatisch zu Aminosäuren abgebaut Pyridoxalphosphat wirkt bei der Übertragung von a-aminogruppen auf a-ketoglutarat mit Glutamat setzt in der Leber Ammoniak frei Glutamin transportiert Ammoniak in den Blutkreislauf EXKURS 18 1 Untersuchungen auf Gewebeschäden Alanin transportiert Ammoniak von den Muskeln zur Leber Ammoniak ist für Tiere toxisch Stickstoffausscheidung und der Harnstoffzyklus Harnstoff entsteht aus Ammoniak in fünf enzymatischen Schritten Citrat- und Harnstoffzyklus sind miteinander verbunden Die Aktivität des Harnstoffzyklus wird in zwei Stufen reguliert Verknüpfungen von Reaktionswegen reduzieren den Energieaufwand für die Harnstoffsynthese Genetische Defekte im Harnstoffzyklus können lebensbedrohend sein Der natürliche Lebenraum bestimmt den Weg der Stickstoffausscheidung Wege des Aminosäureabbaus Beim Aminosäure-Katabolismus sind mehrere Enzym-Cofaktoren wichtig Zehn Aminosäuren werden zu Acetyl-CoA abgenaut Bei manchen Menschen weist der Phenylalanin-Katabolismus genetische Defekte auf Fünf Aminosäuren werden zu a-ketoglutarat umgesetzt Vier Aminosäuren werden zu Succinyl-CoA umgesetzt Verzweigte Aminosäuren werden nicht in der Leber abgebaut EXKURS 18 2 Wissenschaftliche Detektive klären einen rätselhaften Mordfall Asparagin und Aspartat werden zu Oxalacetat abgebaut Einige Aminosäuren können zu Glucose umgesetzt werden, andere zu Ketokörpern XXIX
13 Zusammenfassung Weiterführende Literatur Aufgaben Oxidative Phosphorylierung und Photophosphorylierung Elektronenübertragungen in Mitochondrien Elektronen werden zu universelle Elektronenakzeptoren geschleust Elektronen passieren eine Reihe von membrangebundenen Carriern Elektronen-Carrier wirken in Multienzymkomplexen Die Energie der Elektronenübertragung wird in einem Protonengradienten effizient gespeichert Bei pflanzlichen Mitochondrien folgt die Oxidation von NADH anderen Mechanismen ATP-Synthese EXKURS 19 1 Alternative Wege der Atmungskette und heiße, stinkende Pflanzen ATP-Synthase hat zwei funktionelle Bereiche: F o und F ATP wird an der Oberfläche von F 1 relativ zu ADP stabilisiert Der Protonengradient treibt die Freisetzung von ATP von der Enzymoberfläche Jede b-untereinheit der ATP-Synthase kann drei verschiedene Konformationen annehmen Die Rotationskatalyse ist entscheidend für den Bindungswechsel-Mechanismus bei der ATP-Synthese Chemiosmotische Kopplung erlaubt nicht-ganzzahlige Stöchiometrien von O 2 -Verbrauch und ATP-Synthese Die protonenmotorische Kraft liefert Energie für den aktiven Transport Shuttle-Systeme sind für die mitochondriale Oxidation von cytosolischem NADH nötig Regulation der oxidativen Phosphorylierung Die oxidative Phosphorylierung wird durch den Energiebedarf der Zelle reguliert Entkoppelte Mitochondrien in braunem Fettgewebe erzeugen Wärme ATP erzeugende Reaktionswege werden koordiniert reguliert Mutationen in mitochondrialen Genen verursachen Erkrankungen Mitochondrien entwickelten sich wahrscheinlich aus endo-symbiotischen Bakterien Allgemeine Merkmale der Photophosphorylierung Die Photosynthese findet bei höheren Pflanzen in den Chloroplasten statt Licht treibt den Elektronenfluss in Chloroplasten an Absorption von Licht Chlorophylle absorbieren Lichtenergie für die Photosynthese Hilfspigmente erweitern den Spektralbereich der Lichtabsorption Chlorophyll leitet absorbierte Energie durch Excitonentransfer an Reaktionszentren weiter Das zentrale photochemische Ereignis: der vom Licht getriebene Elektronenfluss Bakterien besitzen einen von zwei Typen einzelner photochemischer Reaktionszentren Kinetische und thermodynamische Faktoren verhindern Energieverlust durch innere Conversion In höheren Pflanzen wirken zwei Reaktionszentren als Tandem Die räumliche Trennung der Photosysteme I und II verhindert ein Leck für Excitonen Der Cytochrom b 6 f-komplex verknüpft die Photosysteme II und I miteinander Cyanobakterien nutzen den Cytochrom b 6 f-komplex und Cytochrom c bei der oxidativen Phosphorylierung und bei der Photophosphorylierung Wasser wird durch den Sauerstoff bildenden Komplex gespalten ATP-Synthese durch Photophosphorylierung Ein Protonengradient verknüpft Elektronenfluss und Phosphorylierung Die ungefähre Stöchiometrie der Photophosphorylierung konnte aufgeklärt werden Der zyklische Elektronenfluss erzeugt ATP, jedoch kein NADPH oder O Die ATP-Synthase von Chloroplasten ähnelt der von Mitochondrien Chloroplasten entwickelten sich wahrscheinlich aus endosymbiotischen Bakterien XXX
14 Verschiedene photosynthetisierende Organismen nutzen andere Wasserstoffdonatoren als Wasser In halophilen Bakterien nimmt ein einzelnes Protein Licht auf und pumpt Protonen, um die ATP-Synthese anzutreiben Zusammenfassung Weiterführende Literatur Aufgaben Biosynthese von Kohlenhydraten Gluconeogenese Für die Umsetzung von Pyruvat zu Phosphoenolpyruvat sind zwei exergone Reaktionen erforderlich Die Umsetzung von Fructose-1,6- bisphosphat zu Fructose-6-phosphat ist die zweite Umgehungsreaktion Die Umsetzung von Glucose-6-phosphat zu freier Glucose ist die dritte Umgehungsreaktion Die Gluconeogenese erfordert viel Energie Die Zwischenprodukte des Citrat-zyklus und viele Aminosäuren sind glucogen Leerlaufzyklen im Kohlenhydratstoffwechsel verbrauchen ATP Gluconeogenese und Glycolyse werden reziprok reguliert Die Gluconeogenese setzt in keimenden Samen Fette und Proteine zu Glucose um Biosynthese von Glycogen, Stärke, Saccharose und anderen Kohlenhydraten UDP-Glucose ist das Substrat für die Glycogensynthese Glycogen-Synthase und Glycogen-Phosphorylase werden reziprok reguliert ADP-Glucose ist das Substrat für die Stärkesynthese bei Pflanzen und für die Glycogensynthese bei Bakterien UDP-Glucose ist bei Pflanzen das Substrat für die Synthese von Saccharose Die Lactosesynthese wird auf eine ungewöhnliche Weise reguliert UDP-Glucose ist ein Zwischenprodukt bei der Bildung von Glucuronat und Vitamin C Zuckernucleotide sind Vorstufen beim Aufbau der Bakterienzellwand Synthese von Kohlenhydraten bei der Photosynthese Die CO 2 -Fixierung läuft in drei Stufen ab 807 EXKURS 20 1 Penicillin und b-lactamase: Wunderwaffe gegen kugelsichere Weste Pro Molekül Triosephosphat, das aus CO 2 synthetisiert wird, sind 6 NADPHund 9 ATP-Moleküle erforderlich Ein Transportsystem schleust Triosephosphate aus dem Chloroplasten heraus und Phosphat hinein Regulation des Kohlenhydratstoffwechsels bei Pflanzen Rubisco wird sowohl positiv als auch negativ reguliert Bestimmte Enzyme des Calvin-Zyklus werden durch Licht indirekt aktiviert Die Nutzung von Triosephosphaten für die Synthese von Saccharose und Stärke wird bei Pflanzen fein reguliert Photorespiration resultiert aus der Oxygenase-Aktivität von Rubisco Einige Pflanzen haben einen Mechanismus, mit dem die Photorespiration minimiert wird Zusammenfassung Weiterführende Literatur Aufgaben Biosynthese von Lipiden Biosynthese von Fettsäuren und Eicosanoiden Malonyl-CoA wird aus Acetyl-CoA und Hydrogencarbonat gebildet Fettsäuren werden in einer repetitiven Reaktionsfolge synthetisiert Der Fettsäure-Synthase-Komplex hat sieben verschiedene aktive Zentren Die Fettsäure-Synthase nimmt die Acetyl- und Malonylgruppen auf Die Fettsäure-Synthase-Reaktionen werden zur Bildung von Palmitat wiederholt Die Fettsäure-Synthase einiger Organismen besteht aus multifunktionellen Proteinen Die Fettsäure-Synthese erfolgt bei vielen Organismen im Cytosol, aber bei Pflanzen in den Chloroplasten Acetat wird als Citrat aus den Mitochondrien heraustransportiert Die Biosynthese von Fettsäuren wird strikt reguliert Langkettige gesättigte Fettsäuren werden aus Palmitat synthetisiert Einige Fettsäuren sind ungesättigt XXXI
1 Vom Organismus zum Molekül... 3
 I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
Stoffwechsel. Metabolismus (3)
 Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Inhaltsverzeichnis. I Stoffwechsel. 1 Vom Organismus zum Molekül Aminosäuren Peptide und Proteine Enzyme...
 XI I Stoffwechsel 1 Vom Organismus zum Molekül...................... 2 1.1 Aufbau des Organismus.............................. 2 1.2 Chemische Grundlagen des Stoffwechsels.................. 6 1.3 Informationsübertragung
XI I Stoffwechsel 1 Vom Organismus zum Molekül...................... 2 1.1 Aufbau des Organismus.............................. 2 1.2 Chemische Grundlagen des Stoffwechsels.................. 6 1.3 Informationsübertragung
Klausur zur Vorlesung Biochemie I im WS 2001/02
 (insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
(insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
Stoffwechsel. Die Chemie des Lebens ist in Stoffwechselwegen organisiert
 Die Chemie des Lebens ist in Stoffwechselwegen organisiert Der Stoffwechsel ist die Summe aller chemischen Reaktionen, die in den Zellen eines Organismus auftreten. Unter Mithilfe von Enzymen verläuft
Die Chemie des Lebens ist in Stoffwechselwegen organisiert Der Stoffwechsel ist die Summe aller chemischen Reaktionen, die in den Zellen eines Organismus auftreten. Unter Mithilfe von Enzymen verläuft
Regulation der Glykolyse: Phosphofructokinase
 Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine
 4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
Oxidative Phosphorylierung
 BICEMIE DER ERÄRUG II Grundzüge des Metabolismus xidative Phosphorylierung 24.04.2012 xidative Phosphorylierung xidative Phosphorylierung -Die Elektronen in AD und in FAD 2 (hohes Übertragungspotential)
BICEMIE DER ERÄRUG II Grundzüge des Metabolismus xidative Phosphorylierung 24.04.2012 xidative Phosphorylierung xidative Phosphorylierung -Die Elektronen in AD und in FAD 2 (hohes Übertragungspotential)
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Gluconeognese Neusynthese von Glucose aus Pyruvat
 Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!!
 Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!! Indirekte ATP synthese! Protonen können in wässriger Lösung sehr! schnell transportiert werden.! Ionen können biologische Membranen nicht spontan
Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!! Indirekte ATP synthese! Protonen können in wässriger Lösung sehr! schnell transportiert werden.! Ionen können biologische Membranen nicht spontan
Der Stoffwechsel: Konzepte und Grundmuster
 Der Stoffwechsel: Konzepte und Grundmuster 1 Lebende Organismen Was unterscheidet lebende Organismen von toter Materie? Lebende Organismen haben einen hohen Gehalt an chemischer Komplexität und Organisation
Der Stoffwechsel: Konzepte und Grundmuster 1 Lebende Organismen Was unterscheidet lebende Organismen von toter Materie? Lebende Organismen haben einen hohen Gehalt an chemischer Komplexität und Organisation
Lebewesen enthalten weitaus mehr Molekülarten und beherbergen weitaus mehr chemische Reaktionsarten als die ganze anorganische Welt.
 Lebewesen enthalten weitaus mehr Molekülarten und beherbergen weitaus mehr chemische Reaktionsarten als die ganze anorganische Welt. Die aus Biomolekülen aufgebauten biologischen Strukturen sind äußerst
Lebewesen enthalten weitaus mehr Molekülarten und beherbergen weitaus mehr chemische Reaktionsarten als die ganze anorganische Welt. Die aus Biomolekülen aufgebauten biologischen Strukturen sind äußerst
Biochemie II - Tutorium
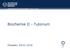 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Inhaltsverzeichnis. a. Chemie der Aminosäuren und Peptide
 Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
Was bisher geschah 1
 Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Funktion von Proteinen:
 Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
Organische Chemie der biologischen Stoffwechselwege
 Organische Chemie der biologischen Stoffwechselwege John McMurry / Tadhg Begley aus dem Amerikanischen übersetzt von Karin Beifuss ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum k_/l AKADEMISCHER VERLAG
Organische Chemie der biologischen Stoffwechselwege John McMurry / Tadhg Begley aus dem Amerikanischen übersetzt von Karin Beifuss ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum k_/l AKADEMISCHER VERLAG
Z 11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
Membranen. U. Albrecht
 Membranen Struktur einer Plasmamembran Moleküle gegeneinander beweglich -> flüssiger Charakter Fluidität abhängig von 1) Lipidzusammensetzung (gesättigt/ungesättigt) 2) Umgebungstemperatur Biologische
Membranen Struktur einer Plasmamembran Moleküle gegeneinander beweglich -> flüssiger Charakter Fluidität abhängig von 1) Lipidzusammensetzung (gesättigt/ungesättigt) 2) Umgebungstemperatur Biologische
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase
 Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Biologie für Mediziner
 Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Fettsäurebiosynthese
 Fettsäurebiosynthese Inhalt Fettsäuren Triacylglyceride FS-Biosynthese und einzelne Schritte Fettsäuren Lange CH-Ketten mit einer endständigen Carboxylgruppe 3 Gruppen: -> gesättigte FS -> einfach ungesättigte
Fettsäurebiosynthese Inhalt Fettsäuren Triacylglyceride FS-Biosynthese und einzelne Schritte Fettsäuren Lange CH-Ketten mit einer endständigen Carboxylgruppe 3 Gruppen: -> gesättigte FS -> einfach ungesättigte
Taschenatlas Biochemie des Menschen
 Taschenatlas Biochemie des Menschen Bearbeitet von Jan Koolman, Klaus-Heinrich Röhm 4., vollständig überarbeitete und erweiterte Auflage 2009. Buch. XII, 529 S. Kartoniert ISBN 978 3 13 759404 8 Format
Taschenatlas Biochemie des Menschen Bearbeitet von Jan Koolman, Klaus-Heinrich Röhm 4., vollständig überarbeitete und erweiterte Auflage 2009. Buch. XII, 529 S. Kartoniert ISBN 978 3 13 759404 8 Format
Biologie für Mediziner
 Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/ CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/ CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Einführung in die Biochemie Wirkungsweise von Enzymen
 Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Atmung Übersicht. Atmung der Mitochondrien
 Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
Beispiele für Prüfungsfragen zu den Einheiten. 2, 3, 5, 9-12, 15, 16, und 21 (Hartig)
 Beispiele für Prüfungsfragen zu den Einheiten 2, 3, 5, 9-12, 15, 16, und 21 (Hartig) Untenstehendes Molekül ist ein Peptidhormon. Wieviele Peptidbindungen besitzt dieses Molekül (zeichnen Sie diese ein)?
Beispiele für Prüfungsfragen zu den Einheiten 2, 3, 5, 9-12, 15, 16, und 21 (Hartig) Untenstehendes Molekül ist ein Peptidhormon. Wieviele Peptidbindungen besitzt dieses Molekül (zeichnen Sie diese ein)?
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Bioorganische Chemie Enzymatische Katalyse 2011
 Ringvorlesung Chemie B - Studiengang Molekulare Biotechnologie Bioorganische Chemie Enzymatische Katalyse 2011 Prof. Dr. A. Jäschke INF 364, Zi. 308, Tel. 54 48 51 jaeschke@uni-hd.de Lehrziele I Kenntnis
Ringvorlesung Chemie B - Studiengang Molekulare Biotechnologie Bioorganische Chemie Enzymatische Katalyse 2011 Prof. Dr. A. Jäschke INF 364, Zi. 308, Tel. 54 48 51 jaeschke@uni-hd.de Lehrziele I Kenntnis
Der Energiestoffwechsel eukaryotischer Zellen
 Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Hemmung der Enzym-Aktivität
 Hemmung der Enzym-Aktivität Substrat Kompetitiver Inhibitor Enzym Enzym Substrat Nichtkompetitiver Inhibitor Irreversibler Inhibitor Enzym Enzym Enzym - Kinetik Michaelis Menten Gleichung Lineweaver -
Hemmung der Enzym-Aktivität Substrat Kompetitiver Inhibitor Enzym Enzym Substrat Nichtkompetitiver Inhibitor Irreversibler Inhibitor Enzym Enzym Enzym - Kinetik Michaelis Menten Gleichung Lineweaver -
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Morphologische Grundlagen der Zelle Bakterienzelle
 Morphologische Grundlagen der Zelle Bakterienzelle Entstehung der Eukaryontenzelle Endosymbiontentheorie Tier-Zelle Pflanzen-Zelle Entstehung der Eukaryontenzelle Endosymbiontentheorie (aus Weiler/Nover:
Morphologische Grundlagen der Zelle Bakterienzelle Entstehung der Eukaryontenzelle Endosymbiontentheorie Tier-Zelle Pflanzen-Zelle Entstehung der Eukaryontenzelle Endosymbiontentheorie (aus Weiler/Nover:
Asmaa Mebrad Caroline Mühlmann Gluconeogenese
 Gluconeogenese Asmaa Mebrad Caroline Mühlmann 06.12.2004 Definition: wichtiger Stoffwechselweg, bei dem Glucose aus Nicht-Kohlenhydrat-Vorstufen synthetisiert wird Ablauf bei längeren Hungerperioden dient
Gluconeogenese Asmaa Mebrad Caroline Mühlmann 06.12.2004 Definition: wichtiger Stoffwechselweg, bei dem Glucose aus Nicht-Kohlenhydrat-Vorstufen synthetisiert wird Ablauf bei längeren Hungerperioden dient
Primärstoffwechsel. Prof. Dr. Albert Duschl
 Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Kohlenhydrate C n. O) n (H 2. z.b. C 6 O 6 O) 6 H 12 : C 6. Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Monosaccharide
 Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Biochemie. Kurzes Lehrbuch der. für Mediziner und Naturwissenschaftler. Von Peter Karlson. 12., völlig neubearbeitete Auflage
 Kurzes Lehrbuch der Biochemie für Mediziner und Naturwissenschaftler Von Peter Karlson 12., völlig neubearbeitete Auflage 177 Abbildungen 323 Formelbilder und Schemata 37 Tabellen 2008 AGI-Information
Kurzes Lehrbuch der Biochemie für Mediziner und Naturwissenschaftler Von Peter Karlson 12., völlig neubearbeitete Auflage 177 Abbildungen 323 Formelbilder und Schemata 37 Tabellen 2008 AGI-Information
In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit
 In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit in der Nucleotidsequenz der DNA verschlüsselt (codiert)
In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit in der Nucleotidsequenz der DNA verschlüsselt (codiert)
Entstehung der Eukaryontenzelle Endosymbiontentheorie
 Entstehung der Eukaryontenzelle Endosymbiontentheorie Tier-Zelle Pflanzen-Zelle Entstehung der Eukaryontenzelle Endosymbiontentheorie (aus Weiler/Nover: Allgemeine und molekulare Botanik) Tierzelle Morphologische
Entstehung der Eukaryontenzelle Endosymbiontentheorie Tier-Zelle Pflanzen-Zelle Entstehung der Eukaryontenzelle Endosymbiontentheorie (aus Weiler/Nover: Allgemeine und molekulare Botanik) Tierzelle Morphologische
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Membranen (3a) Membrane
 Membranen (3a) Biochemie Membrane Funktionen Abgrenzung der Zelle nach außen hin schaffen geeignete Voraussetzungen für einzelne enzymatische Reaktionen Signalübertragung tragen Signalstrukturen für die
Membranen (3a) Biochemie Membrane Funktionen Abgrenzung der Zelle nach außen hin schaffen geeignete Voraussetzungen für einzelne enzymatische Reaktionen Signalübertragung tragen Signalstrukturen für die
Praktikum Biochemie B.Sc. Water Science WS Enzymregulation. Marinja Niggemann, Denise Schäfer
 Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Kataboler und Anaboler Stoffwechsel
 Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Der Fettsäurestoffwechsel. Basierend auf Stryer Kapitel 22
 Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
Springer-Lehrbuch. Lehninger Biochemie
 Springer-Lehrbuch Lehninger Biochemie Bearbeitet von David Nelson, Michael Cox, Gerhard Heldmaier, Bärbel Häcker, Andreas Held, Gudrun Maxam, Claudia Schön, Nina Zellerhoff 4. Aufl. 2009, 3., korr. Nachdruck
Springer-Lehrbuch Lehninger Biochemie Bearbeitet von David Nelson, Michael Cox, Gerhard Heldmaier, Bärbel Häcker, Andreas Held, Gudrun Maxam, Claudia Schön, Nina Zellerhoff 4. Aufl. 2009, 3., korr. Nachdruck
Grundlagen der Molekularen Biophysik WS 2011/12 (Bachelor) Dozent: Prof Dr. Ulrike Alexiev (R , Tel /Sekretariat Frau Endrias Tel.
 Grundlagen der Molekularen Biophysik WS 2011/12 (Bachelor) Dozent: Prof Dr. Ulrike Alexiev (R.1.2.34, Tel. 55157/Sekretariat Frau Endrias Tel. 53337) Tutoren: Dr. Kristina Kirchberg, Alex Boreham 6-stündig
Grundlagen der Molekularen Biophysik WS 2011/12 (Bachelor) Dozent: Prof Dr. Ulrike Alexiev (R.1.2.34, Tel. 55157/Sekretariat Frau Endrias Tel. 53337) Tutoren: Dr. Kristina Kirchberg, Alex Boreham 6-stündig
Enzyme SPF BCH am
 Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Musterlösung. Frage Summe Note Punkte 1, ,5 1,0
 Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
6.3 Phospholipide und Signaltransduktion. Allgemeines
 6.3 Phospholipide und Signaltransduktion Allgemeines Bei der Signaltransduktion, das heißt der Weiterleitung von Signalen über die Zellmembran in das Innere der Zelle, denkt man zuerst einmal vor allem
6.3 Phospholipide und Signaltransduktion Allgemeines Bei der Signaltransduktion, das heißt der Weiterleitung von Signalen über die Zellmembran in das Innere der Zelle, denkt man zuerst einmal vor allem
Kohlenhydrate. spielen in der Natur eine sehr wichtige Rolle. dienen als Energiespeicher: Stärke, Glykogen
 Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
BIOCHEMIE. Prof. Manfred SUSSITZ. über(be)arbeitet und zusammengestellt nach Internetvorlagen:
 BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
Atmung Respiration 1
 Atmung Respiration 1 Atmung Die oxidative Phosphorylierung ist der letzte Schritt einer Serie von Energieumwandlungen, die insgesamt als Zellatmung oder einfach Atmung (Respiration) bezeichnet werden 2
Atmung Respiration 1 Atmung Die oxidative Phosphorylierung ist der letzte Schritt einer Serie von Energieumwandlungen, die insgesamt als Zellatmung oder einfach Atmung (Respiration) bezeichnet werden 2
Kohlenhydrate Aminosäuren Peptide
 Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
1. Die Bildung von Methan durch Mikroorganismen erfolgt (2 Punkte)
 Modul: Einführung in die Biochemie und Genetik Prüfungsleistung: Einführung in die Biochemie Welches Enzym katalysiert die dargestellte Reaktion? (2 Punkte) a) Hexokinase b) Glyceratkinase c) Mitogen-aktivierte
Modul: Einführung in die Biochemie und Genetik Prüfungsleistung: Einführung in die Biochemie Welches Enzym katalysiert die dargestellte Reaktion? (2 Punkte) a) Hexokinase b) Glyceratkinase c) Mitogen-aktivierte
Seminar Biochemie. Lipide und Lipidstoffwechsel. Dr. Christian Hübbers
 Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, TG, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese, MalonylCoA,
Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, TG, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese, MalonylCoA,
Hemmung der Enzym-Aktivität
 Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
Stoffwechselphysiologie. Zusammenfassung für das mündliche Abitur
 Naturwissenschaft Sarah Fuhrken Stoffwechselphysiologie. Zusammenfassung für das mündliche Abitur Zusammenfassung Stoffwechselphysiologie Lernzettel Biologie, 1. Semester Brown sche Molekularbewegung:
Naturwissenschaft Sarah Fuhrken Stoffwechselphysiologie. Zusammenfassung für das mündliche Abitur Zusammenfassung Stoffwechselphysiologie Lernzettel Biologie, 1. Semester Brown sche Molekularbewegung:
Mechanismen der ATP Synthese in Mitochondrien
 Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Aminosäuren 1. Aufbau der Aminosäuren
 Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Unterschied Tiere, Pflanzen, Bakterien u. Pilze und die Zellorganellen
 Unterschied Tiere, Pflanzen, Bakterien u. Pilze und die Zellorganellen Die Organellen der Zelle sind sozusagen die Organe die verschiedene Funktionen in der Zelle ausführen. Wir unterscheiden Tierische
Unterschied Tiere, Pflanzen, Bakterien u. Pilze und die Zellorganellen Die Organellen der Zelle sind sozusagen die Organe die verschiedene Funktionen in der Zelle ausführen. Wir unterscheiden Tierische
Bachelorstudiengang Biologie. Vorlesung Biochemie I Klausur am 11. Oktober 2012, 9:00 11:00, H18
 Bachelorstudiengang Biologie Vorlesung Biochemie I Klausur am 11. Oktober 2012, 9:00 11:00, H18 1. (a) Welche Aminosäuren mit positiv geladenen Seitenketten kennen Sie? Bitte geben Sie die Strukturformel
Bachelorstudiengang Biologie Vorlesung Biochemie I Klausur am 11. Oktober 2012, 9:00 11:00, H18 1. (a) Welche Aminosäuren mit positiv geladenen Seitenketten kennen Sie? Bitte geben Sie die Strukturformel
-Übersicht. 2. G-Protein-gekoppelte Rezeptoren. 5. Na + -K + -Pumpe REZEPTOREN. 1. Allgemeine Definition: Rezeptoren. 3. Tyrosin-Kinase Rezeptoren
 REZEPTOREN -Übersicht 1. Allgemeine Definition: Rezeptoren 2. G-Protein-gekoppelte Rezeptoren 3. Tyrosin-Kinase Rezeptoren Beispiel: Insulin 4. Steroidhormone 5. Na + -K + -Pumpe EINFÜHRUNG Definition
REZEPTOREN -Übersicht 1. Allgemeine Definition: Rezeptoren 2. G-Protein-gekoppelte Rezeptoren 3. Tyrosin-Kinase Rezeptoren Beispiel: Insulin 4. Steroidhormone 5. Na + -K + -Pumpe EINFÜHRUNG Definition
Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat
 Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus)
 Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Zellulärer Abbau von Proteinen in Aminosäuren:! Proteine werden in Zellen durch Proteasom-Komplexe in! einzelne Aminosäuren abgebaut.!
 Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
12. Oxidative Phosphorylierung
 12. Oxidative Phosphorylierung 303 Zweck: Gewinnung von ATP Regeneration von NAD + und FAD Gesamtreaktionen: 3 ADP + 3 P i 3 ATP NADH + 0,5 O 2 + H + NAD + + H-O-H 2 ADP + 2 P i 2 ATP FADH 2 + 0,5 O 2
12. Oxidative Phosphorylierung 303 Zweck: Gewinnung von ATP Regeneration von NAD + und FAD Gesamtreaktionen: 3 ADP + 3 P i 3 ATP NADH + 0,5 O 2 + H + NAD + + H-O-H 2 ADP + 2 P i 2 ATP FADH 2 + 0,5 O 2
1) Erklären sie die Begriffe Primär Sekundär und Tertiärstruktur von Proteinen. Nennen Sie drei typische Sekundärstrukturelemente (6P)
 1. Klausur zum Modul 5.3 Biochemie WS 09/10 12.2.2010 1) Erklären sie die Begriffe Primär Sekundär und Tertiärstruktur von Proteinen. Nennen Sie drei typische Sekundärstrukturelemente (6P) 2) Welche Funktion
1. Klausur zum Modul 5.3 Biochemie WS 09/10 12.2.2010 1) Erklären sie die Begriffe Primär Sekundär und Tertiärstruktur von Proteinen. Nennen Sie drei typische Sekundärstrukturelemente (6P) 2) Welche Funktion
Kohlenhydrate. Prof. Dr. Albert Duschl
 Kohlenhydrate Prof. Dr. Albert Duschl Kohlenhydrate in der Nahrung Kohlenhydrate sind in zwei Formen in unserer Nahrung vorhanden: Als komplexe Zucker, wie Stärke in Getreideprodukten, und als einfache
Kohlenhydrate Prof. Dr. Albert Duschl Kohlenhydrate in der Nahrung Kohlenhydrate sind in zwei Formen in unserer Nahrung vorhanden: Als komplexe Zucker, wie Stärke in Getreideprodukten, und als einfache
Übungsfragen zur Vorlesung Einführung in die Biologie, Zell- und Molekularbiologie Teil Biochemie PD Dr. Udo Rau. (Biomoleküle allgemein)
 Übungsfragen zur Vorlesung Einführung in die Biologie, Zell- und Molekularbiologie Teil Biochemie PD Dr. Udo Rau (Biomoleküle allgemein) 1) Aus welchen Elementen besteht die Zelle zu 99%? 2) Warum ist
Übungsfragen zur Vorlesung Einführung in die Biologie, Zell- und Molekularbiologie Teil Biochemie PD Dr. Udo Rau (Biomoleküle allgemein) 1) Aus welchen Elementen besteht die Zelle zu 99%? 2) Warum ist
Mitochondriale Elektronentransportkette (Atmungskette)
 Mitochondriale Elektronentransportkette (Atmungskette) Mitochondriale Elektronentransportkette (Atmungskette) Komplex I und II übetragen Elektronen auf Coenzym Q (Ubichinon) Gekoppelte Elektronen-Protonen
Mitochondriale Elektronentransportkette (Atmungskette) Mitochondriale Elektronentransportkette (Atmungskette) Komplex I und II übetragen Elektronen auf Coenzym Q (Ubichinon) Gekoppelte Elektronen-Protonen
Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail. Mag. Gerald Trutschl
 Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail Mag. Gerald Trutschl 1 Inhalt 1. Enzym Reaktion im Detail 2. Thermodynamische Reaktion 3. Katalysemechanismen 4. Michaelis-Menten-Konstante
Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail Mag. Gerald Trutschl 1 Inhalt 1. Enzym Reaktion im Detail 2. Thermodynamische Reaktion 3. Katalysemechanismen 4. Michaelis-Menten-Konstante
1. Biochemie-Klausur Zahnmediziner, WS 03/04
 1. Biochemie-Klausur Zahnmediziner, WS 03/04 1. Welche Aussage zur ß-Oxidation von Fettsäuren in Peroxisomen ist falsch? A) Die Aufnahme langkettiger Fettsäuren in die Peroxisomen erfolgt Carnitin-unabhängig!
1. Biochemie-Klausur Zahnmediziner, WS 03/04 1. Welche Aussage zur ß-Oxidation von Fettsäuren in Peroxisomen ist falsch? A) Die Aufnahme langkettiger Fettsäuren in die Peroxisomen erfolgt Carnitin-unabhängig!
Stoffklasse: LIPIDE Funktionen in der Zelle
 Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
Biochemie II. im Wintersemester 2009/2010. Joachim Wegener. Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg
 Biochemie II im Wintersemester 2009/2010 Joachim Wegener Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg 18.10.2010 1/14 Biochemie II im WS 2010 / 2011 All Dozenten auf einen
Biochemie II im Wintersemester 2009/2010 Joachim Wegener Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg 18.10.2010 1/14 Biochemie II im WS 2010 / 2011 All Dozenten auf einen
Stoffwechsel - Energiebereitstellung - Biomoleküle
 Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Grundlagen der Biochemie (BCh 5.3) Prof. Dr. Christoph Thiele WS 2014/15 1. Klausur ( )
 Grundlagen der Biochemie (BCh 5.3) Prof. Dr. Christoph Thiele WS 2014/15 1. Klausur (6.2.2015) Aufgabe 1: Erläutern Sie die Primär-, Sekundär- und die Tertiärstruktur von Proteinen. [3 P] Aufgabe 2: Erklären
Grundlagen der Biochemie (BCh 5.3) Prof. Dr. Christoph Thiele WS 2014/15 1. Klausur (6.2.2015) Aufgabe 1: Erläutern Sie die Primär-, Sekundär- und die Tertiärstruktur von Proteinen. [3 P] Aufgabe 2: Erklären
ENZYME. Teil 1: Grundlagen und Substratbestimmungen
 ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
und Pathobiochemie Detlef Doenecke Jan Koolman Georg Fuchs Wolfgang Gerok 15., komplett überarbeitete und neugestaltete Auflage
 Karlsons Biochemie und Pathobiochemie Detlef Doenecke Jan Koolman Georg Fuchs Wolfgang Gerok 15., komplett überarbeitete und neugestaltete Auflage Mehr als 800 Abbildungen, Formeln und Schemata 1 Falttafel
Karlsons Biochemie und Pathobiochemie Detlef Doenecke Jan Koolman Georg Fuchs Wolfgang Gerok 15., komplett überarbeitete und neugestaltete Auflage Mehr als 800 Abbildungen, Formeln und Schemata 1 Falttafel
Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016
 Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016 Fragen für die Übungsstunde 4 (20.06. 24.06.) Regulation der Transkription II, Translation
Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016 Fragen für die Übungsstunde 4 (20.06. 24.06.) Regulation der Transkription II, Translation
Autotrophe und heterotrophe Organismen
 Grundlagen der Umwelttechnik 5. Biomoleküle und Grundlagen des Stoffwechsels Vorlesung an der ochschule Augsburg Dr. Siegfried Kreibe 1 Autotrophe und heterotrophe rganismen Autotrophe rganismen: bauen
Grundlagen der Umwelttechnik 5. Biomoleküle und Grundlagen des Stoffwechsels Vorlesung an der ochschule Augsburg Dr. Siegfried Kreibe 1 Autotrophe und heterotrophe rganismen Autotrophe rganismen: bauen
Lipide und Zellmembranen. Stryer ed. 6, Kapitel 12
 Lipide und Zellmembranen Stryer ed. 6, Kapitel 12 Biologische Membranen Die Grenzen, die eine Zelle kennzeichnen, werden von biologischen i Membranen gebildet: sie definieren eine innere un eine äussere
Lipide und Zellmembranen Stryer ed. 6, Kapitel 12 Biologische Membranen Die Grenzen, die eine Zelle kennzeichnen, werden von biologischen i Membranen gebildet: sie definieren eine innere un eine äussere
Thematik der molekularen Zellbiologie Studienjahr 2004/05. I. Semester
 Thematik der molekularen Zellbiologie Studienjahr 2004/05 (Abkürzungen: V. = 45 Min. Vorlesung, S. = 45 Min. Seminar, ds. = doppeltes, 2 x 45 Min. Seminar, Ü. = 90 Min. Übung) I. Semester 1. Woche: d 1.
Thematik der molekularen Zellbiologie Studienjahr 2004/05 (Abkürzungen: V. = 45 Min. Vorlesung, S. = 45 Min. Seminar, ds. = doppeltes, 2 x 45 Min. Seminar, Ü. = 90 Min. Übung) I. Semester 1. Woche: d 1.
Grundzüge des Energiestoffwechsels I
 Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik
 Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik Der Metabolismus oder Stoffwechsel ist die Gesamtheit der in einem Organismus ablaufenden (bio)chemischen Prozesse Der
Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik Der Metabolismus oder Stoffwechsel ist die Gesamtheit der in einem Organismus ablaufenden (bio)chemischen Prozesse Der
Auswahlverfahren Medizin Prüfungsgebiet Chemie. 6.Termin Organische Chemie Naturstoffe
 Auswahlverfahren Medizin Prüfungsgebiet Chemie 6.Termin Organische Chemie Naturstoffe Kursleiter Mag. Wolfgang Mittergradnegger IFS Kurs 2009 Organische Chemie Naturstoffe Fette Kohlenhydrate Proteine
Auswahlverfahren Medizin Prüfungsgebiet Chemie 6.Termin Organische Chemie Naturstoffe Kursleiter Mag. Wolfgang Mittergradnegger IFS Kurs 2009 Organische Chemie Naturstoffe Fette Kohlenhydrate Proteine
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Gliederung. Puffersysteme. Wofür Puffersysteme? Wofür Puffersysteme? Wofür Puffersysteme? ph-verhältnisse im Körper. Puffersysteme
 Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
[Grundlagen der] Physiologie der [Mikro-]organismen
![[Grundlagen der] Physiologie der [Mikro-]organismen [Grundlagen der] Physiologie der [Mikro-]organismen](/thumbs/54/33395711.jpg) [Grundlagen der] Physiologie der [Mikro-]organismen Heribert Cypionka Folien: www.icbm.de/pmbio... Teaching... Was ist Physiologie? Vgl. Morphologie, Taxonomie... Themen der Vorlesung: Gundlegende physiologische
[Grundlagen der] Physiologie der [Mikro-]organismen Heribert Cypionka Folien: www.icbm.de/pmbio... Teaching... Was ist Physiologie? Vgl. Morphologie, Taxonomie... Themen der Vorlesung: Gundlegende physiologische
Biochemie (für Bioinformatiker) WS 2010/2011, 2. Klausur (50 Punkte)
 Datum: 07.02.2011 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 2. Klausur (50 Punkte) Modulnr.: FMI-BI0027 Hiermit bestätige ich meine Prüfungstauglichkeit.
Datum: 07.02.2011 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 2. Klausur (50 Punkte) Modulnr.: FMI-BI0027 Hiermit bestätige ich meine Prüfungstauglichkeit.
Die Zelle. Membranen: Struktur und Funktion
 Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
Mechanismus der Enzymkatalyse
 Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
Energie, Enzyme und Stoffwechsel
 Energie, Enzyme und Stoffwechsel 1 Physikalische Prinzipien der biologischen Energieumwandlung Physik: Energie Fähigkeit, Arbeit zu verrichten Biochemie: Energie Fähigkeit, Materie zu verändern 1 Physikalische
Energie, Enzyme und Stoffwechsel 1 Physikalische Prinzipien der biologischen Energieumwandlung Physik: Energie Fähigkeit, Arbeit zu verrichten Biochemie: Energie Fähigkeit, Materie zu verändern 1 Physikalische
Präsentation STOFFWECHSEL STOFFWECHSEL. Fettstoffwechsel im Sport. Biologische Oxidation Zitratzyklus und Atmungskette
 STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
1. Zeichnen und beschriften Sie die stereochemische Struktur von L- Threonin. Geben Sie an, ob R- oder S-Konfiguration vorliegt.
 Übung und Lösung zur Übung Aminosäuren 1. Zeichnen und beschriften Sie die stereochemische Struktur von L- Threonin. Geben Sie an, ob R- oder S-Konfiguration vorliegt. 2. Das Tripeptid Glutathion ( -Glu-Cys-Gly)
Übung und Lösung zur Übung Aminosäuren 1. Zeichnen und beschriften Sie die stereochemische Struktur von L- Threonin. Geben Sie an, ob R- oder S-Konfiguration vorliegt. 2. Das Tripeptid Glutathion ( -Glu-Cys-Gly)
Chemie für Mediziner. Norbert Sträter
 Chemie für Mediziner Norbert Sträter Verlag Wissenschaftliche Scripten 2012 Inhaltsverzeichnis Allgemeine und Anorganische Chemie... 1 1 Atombau... 1 1.1 Fundamentale Begriffe... 1 1.2 Atome und Elemente...
Chemie für Mediziner Norbert Sträter Verlag Wissenschaftliche Scripten 2012 Inhaltsverzeichnis Allgemeine und Anorganische Chemie... 1 1 Atombau... 1 1.1 Fundamentale Begriffe... 1 1.2 Atome und Elemente...
Zellbiologie! Privatdozent Dr. T. Kähne! Institut für Experimentelle Innere Medizin! Medizinische Fakultät
 Zellbiologie! Privatdozent Dr. T. Kähne! Institut für Experimentelle Innere Medizin! Medizinische Fakultät Grundlagen Lipid-Doppelschicht als Barriere für polare Moleküle! Abgrenzung für biochemische
Zellbiologie! Privatdozent Dr. T. Kähne! Institut für Experimentelle Innere Medizin! Medizinische Fakultät Grundlagen Lipid-Doppelschicht als Barriere für polare Moleküle! Abgrenzung für biochemische
BIOCHEMIE. Teil 2: Aminosäuren, Proteine, Enzyme. Urheberrechtlich geschütztes Material. Lernkarteikarten Veterinärmedizin - BIOCHEMIE
 Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
