Marc Thill, Marcus Schmidt, Michael Lux, Cornelia Liedtke, Andreas Schneeweiss, Christian Jackisch
|
|
|
- Norbert Kruse
- vor 6 Jahren
- Abrufe
Transkript
1 Persönliche PDF-Datei für Marc Thill, Marcus Schmidt, Michael Lux, Cornelia Liedtke, Andreas Schneeweiss, Christian Jackisch Mit den besten Grüßen vom Georg Thieme Verlag Einführung und Verwendung von biosimilaren Antikörpern in der Therapie des Mammakarzinoms Senologie 2018; 15: Nur für den persönlichen Gebrauch bestimmt. Keine kommerzielle Nutzung, keine Einstellung in Repositorien. Verlag und Copyright: 2018 by Georg Thieme Verlag KG Rüdigerstraße Stuttgart ISSN Nachdruck nur mit Genehmigung des Verlags
2 Aktuell diskutiert Einführung und Verwendung von biosimilaren Antikörpern in der Therapie des Mammakarzinoms b Einführung Biologische Arzneistoffe, sogenannte Biologika, sind komplexe Substanzen, die aus und mit lebendigen Systemen hergestellt werden. In der Therapie des Mammakarzinoms sind Biologika mit der Einführung der Antikörper bereits seit Jahren etabliert. Der erste Antikörper, der im August 2000 für die Indikation metastasiertes, HER2- positives Mammakarzinom in der EU zugelassen wurde, war das gegen den humanen epidermalen Wachstumsrezeptor-2 (HER2) gerichtete Trastuzumab. Im Mai 2006 erfolgte die Zulassung für Patientinnen mit einem frühen Mammakarzinom. Inzwischen wurde neben Trastuzumab auch der gegen die Dimerisierungsstelle des HER2-Rezeptors agierende Antikörper Pertuzumab für die Therapie von Patientinnen mit einem metastasierten Mammakarzinom (März 2013) sowie für die neoadjuvante Therapie von Patientinnen mit einem frühen Mammakarzinom (Juli 2015) zugelassen. Darüber hinaus erhielt im Jahre 2007 der gegen den vaskulären endothelialen Wachstumsrezeptor (VEGF) gerichtete Antikörper Bevacizumab die Zulassung für die Erstlinientherapie von Patientinnen mit einem metastasierten, HER2-negativen Mammakarzinom. Die Zulassung der genannten Antikörper hat in den letzten Jahren dazu geführt, dass sich die Therapieoptionen nachhaltig erweitert haben und es möglich wurde, zielgerichtet in die Pathophysiologie des Mammakarzinoms einzugreifen. Vor allem aber konnte das Überleben der Patientinnen mit einem HER2-positiven Mammakarzinom unter Inkaufnahme geringer Toxizitätsignifikantverbessertwerden. Die Einführung von Trastuzumab gilt daher als ein Meilenstein in der Mammakarzinomtherapie, der jedoch auch mit einer deutlichen Steigerung der Arzneimittelkosten assoziiert ist. Insgesamt sind seit der Einführung der biologischen Medikamente die Behandlungskosten deutlich gestiegen. Die Folge ist ein erheblicher Kostendruck. Gerade das Mammakarzinom hat aufgrund der hohen Inzidenz erhebliche gesundheitsökonomische Implikationen. Diagnostik, Therapie und Nachsorge von Patientinnen mit Mammakarzinom erfordern ein äußerst komplexes, zeit- und personalintensives Leistungsspektrum, wie es in dieser Form für kaum eine andere Erkrankung erforderlich ist. Für das Mammakarzinom werden in der Europäischen Union derzeit 13 pro Einwohner und Jahr ausgegeben. Dabei erkranken in Deutschland pro Jahr Frauen an einem invasiven Mammakarzinom, des Weiteren mindestens 5500 Frauen an einem duktalen Carcinoma in situ [1]. Während in Ländern wie Litauen und Bulgarien 2 pro Einwohner und Jahr für das Mammakarzinom ausgegeben werden, sind es in Deutschland bereits 29 je Einwohner und Jahr [2]. Für Trastuzumab ist nun im Jahre 2014 der Patentschutz in der EU abgelaufen und 2022 wird auch Bevacizumab seinen Patentschutz verlieren. Nicht zuletzt vor diesem Hintergrund haben verschiedene pharmazeutische Unternehmen bereits vor einigen Jahren damit begonnen, biosimilare Antikörper zu entwickeln, und in der Folge zahlreiche Studien initiiert [3]. Der erste biosimilare Antikörper, ein biosimilares Rituximab, wurde im Februar 2017 von der European Medicines Agency (EMA) bereits zugelassen. Im Gegensatz zu chemischen Arzneimitteln, die als Generika identisch kopierbar sind, können biosimilare Arzneimittel jedoch nicht identisch, sondern nur ähnlich (similar) kopiert werden. Der Grund dafür liegt in der Tatsache, dass biologische Arzneimittel mithilfe von lebenden Zellen (Hefen, Bakterien, Hamsterzellen) hergestellt werden. Zwar ist die Gen- bzw. Aminosäuresequenz von biosimilarem Antikörper und Originalpräparat (Originator) nahezu identisch, aber je nach Zelllinie, Nährmedium und Kulturbedingungen entstehen Proteine, bei denen im Rahmen der Synthese verschiedene posttranskriptionelle Modifikationen auftreten können, die eine Änderung der Tertiärstruktur, der Nukleinsäurevarianten und der Glykosylierung bedingen können [4]. Da die exakten Herstellungsprozesse des Originators nicht bekannt sind, ist nicht zu gewährleisten, dass der biosimilare Antikörper und das Originalpräparat in allen oben genannten Eigenschaften identisch sind. Sie sind nur ähnlich, also biosimilar. Dazu werden die mehr als 100 verschiedenen physikochemischen Charakteristika, wie Primär- (Aminosäuresequenz) und Tertiärstruktur, Glykosylierung, aber auch die biologische Aktivität (Bindungsfähigkeit, ADCC antibody-dependent cellmediated cytotoxicity) des biosimilaren Antikörpers mit dem Originator umfassend und detailliert überprüft. Auch die Originalpräparate werden, ausgehend von der Mastercell Bank, immer wieder neu produziert, sodass auch da mögliche posttranskriptionelle Modifikationen auftreten können (sog. batch-to-batch variability). Die Herstellungsprozesse der Originalpräparate sind daher einer äußerst strengen Kontrolle unterworfen. Mittlerweile ist in Europa bereits eine ganze Reihe an biosimilaren Medikamenten zugelassen wie Erythropoetine, Filgrastime und Somatropine ( de/embed/biosimilars-uebersicht-original praeparate.pdf., Stand August 2017). Neben den als Supportiva eingesetzten genannten Biosimilars wurde im Juni 2015 der erste biosimilare Antikörper, ein biosimilares Infliximab, von der EMA zugelassen. Der erste in der gynäkologischen Onkologie eingesetzte biosimilare Antikörper wird ein biosimilares Trastuzumab sein. Die Zulassung für mindestens 4 biosimilare Trastuzumabs wird für die kommenden 12 Monate erwartet. Weltweit werden im Jahre 2020 etwa 1,3 Billionen Euro für Medikamente ausgegeben werden [5]. Es wird erwartet, dass bis dahin etwa 225 neue onkologische Therapienzugelassenseinwerden.Die Einführung biosimilarer Medikamente ist daher hinsichtlich einer möglichen Kostenersparnis für die Gesundheitssysteme weltweit mehr als reizvoll. So wird erwartet, dass durch die Einführung von biosimilaren Medikamenten ein kumulatives Einsparpotenzial von Milliarden Euro innerhalb der nächsten 5 Jahre in den USA und Europa erreicht werden kann [6]. Für Europa werden dabei Preisreduktionen von % für möglich erachtet [6]. Thill M et al. Einführung und Verwendung Senologie 2018; 15:
3 Aktuell diskutiert Tab. 1 EMA-Anforderungen zum Erhalt der Marktreife eines biosimilaren Antikörpers (nach Daten aus [8]). 1. Vergleichbarkeit der Qualität 2. präklinische Vergleichbarkeit 3. klinische Vergleichbarkeit b Regulierung durch die European Medicines Agency (EMA) physikochemische Eigenschaften beschleunigte Stabilitätsstudien Belastungsstudien posttranslationale Modifikationsanalysen biologische Aktivität abhängig von biologischen Eigenschaften des Biosimilars Reinheit und Verunreinigung produktbezogene Verunreinigung prozessbezogene Verunreinigung Die Zulassung von biosimilaren Medikamenten für den europäischen Markt wird von der European Medicines Agency (EMA) reguliert, die zu diesem Zweck im Jahre 2005 eine Richtlinie in Kraft treten ließ. Mittlerweile existieren Überarbeitungen und Ergänzungen, die auf der Homepage der EMA eingesehen werden können und zum Download bereitstehen ( Im Jahre 2012 erfolgte die Erstellung der Richtlinie zur Entwicklung und Zulassung von biosimilaren Antikörpern (EMA/CHMP/BMWP/ /2010) [7]. Der in dieser Richtlinie festgelegte Zulassungsweg basiert auf präklinischen und Phase-I-Studien zu Pharmakokinetik und Pharmakodynamik, um Qualität, Wirksamkeit, Sicherheit und Verträglichkeit im Vergleich zum Originalpräparat nachzuweisen ( Tab. 1). Erst danach erfolgt im Rahmen einer Phase-III- Studie der Head-to-Head-Vergleich zwischen Biosimilar und Originator. Phase-II- Studien sind nicht vorgesehen. Ziel ist dabei, eine Ähnlichkeit mit dem Originator in Bezug auf Qualitätscharakteristika, biologische Aktivität und Effektivität in einer umfassenden Vergleichsuntersuchung zu zeigen, nicht eine therapeutische Äquivalenz und einen möglichen Patienten-Benefit per se. Studienpopulation und Endpunkte Die EMA empfiehlt für die klinische Überprüfung des biosimilaren Antikörpers im In-vitro-Studien Rezeptorbindungsassays funktionelle zelluläre Assays In-vivo-(Tiermodell-)Studien, falls angebracht Pharmakokinetik-/Pharmakodynamikstudien Aktivitätsstudien Toxizitätsassays Rahmen einer Phase-III-Studie eine sensitive und homogene Patientenpopulation und einen validierten und sensitiven klinischen Endpunkt. Da es bei dieser Studie um die Vergleichbarkeit und nicht um den therapeutischen Nutzen für die Patientin bzw. den Patienten geht, der bereits bei der Überprüfung des Originalpräparats gezeigt wurde, wird von der EMA die Gesamtansprechrate (overall response rate, ORR) oder die pathologische Komplettremission (pathologic complete remission, pcr) empfohlen. Mit dem Überleben assoziierte Endpunkte, wie das progressionsfreie (progression free survival, PFS) oder das Gesamtüberleben (overall survival, OS), sind keine empfohlenen Endpunkte, da sie von Einflussfaktoren wie Tumormasse, Tumorstadium und vorherigen Therapielinien und Therapien abhängen. Diese können allerdings im Rahmen der Studien, wenn möglich, dokumentiert werden [9]. Darüber hinaus sind die Endpunkte PFS und OS nicht wirklich realisierbar, da sie eine längere Nachbeobachtungszeit erfordern und somit (insbesondere bei Patienten im nicht metastasierten Stadium) eine Verzögerung des Zulassungsprozesses verursachen. Ermittlung der Sicherheit des biosimilaren Antikörpers Pharmakokinetikstudien unter Verwendung einer sensitiven und homogenen Population Dosis-Konzentration-Ansprechen vergleichende klinische Studien mit Untersuchung von Wirksamkeit Sicherheit Immunogenität Die Überprüfung der klinischen Sicherheit erfolgt durch das gesamte klinische Entwicklungsprogramm. Neben der Untersuchung der üblichen Sicherheitsparameter wird auch die Immunogenität, also eine mögliche Immunantwort des Immunsystems auf die Substanz, untersucht. Effekte der Immunogenität können starke Toxizität und anaphylaktische Reaktionen sein und bis zum Effektivitätsverlust des Medikaments und zur Resistenzentwicklung reichen. Aufgrund der stark verkürzten klinischen Überprüfung des biosimilaren Antikörpers mit im Vergleich zum Originalpräparat kleineren Patientenzahlen erfolgt die Erhebung von Verträglichkeitsdaten, Daten zur Immunogenität (Anti-Drug-Antikörper) und zu speziellen Nebenwirkungen wie der trastuzumabtypischen Kardiotoxizität im Rahmen eines Risk-Management-Plans zum größten Teil nach der Zulassung des biosimilaren Antikörpers. Extrapolation Ist ein biosimilarer Antikörper in einer Indikation zugelassen, dann ermöglicht die EMA eine Extrapolation für alle weiteren Indikationen, da von der nachgewiesenen Similarität auf die Daten zu anderen Indikationen geschlossen wird. Die Extrapolation ist einer der wesentlichen Punkte des Konzepts der Biosimilarität. Am Beispiel von Trastuzumab wären dies die Indikationen frühes und fortgeschrittenes/metastasiertes Mammakarzinom und metastasiertes Magenkarzinom, am Beispiel von Bevacizumab metastasiertes Mammakarzinom, fortgeschrittenes/metastasiertes nicht kleinzelliges Bronchialkarzinom, fortgeschrittenes/ metastasiertes Nierenzellkarzinom, fortgeschrittenes Ovarialkarzinom und rezidiviertes/metastasiertes Zervixkarzinom. 14 Thill M et al. Einführung und Verwendung Senologie 2018; 15: 13 17
4
5 Aktuell diskutiert Die Extrapolation für alle klinischen Indikationen ist grundsätzlich akzeptabel, falls genügend Effektivitäts- und Sicherheitsdaten erhoben wurden [10], kann aber aus 2 verschiedenen Gründen auch kritisch diskutiert werden. Zunächst bwird dies am Beispiel der Zulassung eines biosimilaren Infliximab deutlich. So erfolgte die Zulassung des biosimilaren Infliximab im September 2013 analog den EMA Guidelines nach einer Phase- I-Studie in der Indikation Morbus Bechterew und nach einer Phase-III- Studie in der Indikation Rheumatoide Arthritis für alle Indikationen: ankylosierende Spondylitis, rheumatoide Arthritis, Psoriasis und Psoriasisarthritis, aber auch für die inflammatorischen Darmerkrankungen Morbus Crohn und Colitis ulcerosa [11]. Aufgrund der unterschiedlichen Erkrankungsgruppen verlangte die kanadische Gesundheitsbehörde Daten für die Indikationen Morbus Crohn und Colitis ulcerosa als Voraussetzung für eine Extrapolation für diese Indikationen. Nach Erhalt der Daten erfolgte die Zulassung für alle Indikationen. Ein weiterer Diskussionspunkt ergibt sich aus der Patientenpopulation, die in der jeweiligen Studie untersucht wird. In der metastasierten Situation liegt bekannterweise ein vorbehandelter Zellklon vor, der sich hinsichtlich Rezeptorstatus und Immunogenität anders verhalten kann als ein therapienaiver Zellklon. Auch ist ein metastasiertes Patientenkollektiv aufgrund der Vorbehandlung und damit verbundener möglicher Toxizität komorbider. Folglich ist es, im Vergleich zu einem unbehandelten Kollektiv aus der neo-/adjuvanten Therapiesituation, möglicherweise weniger geeignet, wenn es darum geht, Biosimilarität zu zeigen. Pharmakovigilanz Nach der Zulassung des ersten und weiterer biosimilarer Trastuzumabs und im Hinblick auf weitere Substanzen ist eine strenge Pharmakovigilanz notwendig, um das gesamte Spektrum an Informationen zur Sicherheit der biosimilaren Antikörper dokumentieren und zuordnen zu können. Dazu gehören sowohl die Dokumentation unerwarteter Reaktionen als auch ein Anstieg der bekannten vorhersehbaren Nebenwirkungen. Um eine präzise Nachvollziehbarkeit der auftretenden Nebenwirkungen im Rahmen eines Risk-Management-Plans nach Zulassung gewährleisten zu können, bedarf es der Dokumentation des Handelsnamens und der Chargenbezeichnung, da verschiedene biosimilare Präparate mit einem identischen Wirkstoffnamen hinsichtlich des Nebenwirkungsspektrums unterschiedlich sein können. Das bedingt allerdings, dass uns als Therapeuten bekannt ist, welches Präparat von uns appliziert wird, und dass eine automatische Substitution des Originators nicht stattfindet [12, 13]. FAZIT Die Einführung sowie Verwendung biosimilarer Antikörper in der Onkologie ist, vor allem vor dem Hintergrund der erheblichen und weiter steigenden Kosten onkologischer Biologika, grundsätzlich zu befürworten. Zur Erhaltung der therapeutischen Qualität im Sinne der betroffenen Patient- (inn)en ist analog den EMA Guidelines jedoch die Einhaltung bestimmter Grundsätze notwendig, die wir im Folgenden erweitern und zum Teil etwas präzisieren wollen: Klinische Studien (mit adäquatem Äquivalenz-Studiendesign) sollten, wie den EMA Guidelines zu entnehmen ist, mit der homogensten und sensitivsten Patientenpopulation durchgeführt werden, um mögliche Unterschiede einwandfrei zu detektieren. Darüber hinaus sollte auch der sensitivste Endpunkt gewählt werden. Die EMA empfiehlt in der metastasierten Situation ORR (overall response rate) und in der neoadjuvanten die pcr (pathologic complete remission). Wir stimmen mit der EMA überein, Äquivalenzstudien in der sensitivsten Patientenpopulation durchzuführen, möchten aber die sensitivste Patientenpopulation, aufgrund der in unseren Augen höheren Sensitivität, präzisieren. In unseren Augen ist dies das therapienaive, frühe Mammakarzinom im neoadjuvanten Setting, mit tpcr (kein residualer Tumor in Mamma und axillären Lymphknoten) als Endpunkt. Aufgrund der Vorbehandlungen und möglicher Komorbiditäten ist, unserer Meinung nach, ein metastasiertes Patientenkollektiv nur suboptimal [14, 15]. Die Extrapolation ist analog den EMA Guidelines bei Vorliegen ausreichender Effektivitäts- und Sicherheitsdaten durchaus möglich; wir sehen jedoch die Extrapolation kritisch, insofern von Daten aus der metastasierten Situation mit einem heterogenen und vortherapierten Patientenkollektiv auf die therapienaive adjuvante Situation extrapoliert wird. Klinische Studien sollten eine Größe vorhalten, die ausreichend ist, um das bekannte Nebenwirkungsprofil sicher abbilden zu können und die Äquivalenz mit dem Originator zu belegen (Konfidenzintervall wenigstens 90 %, Äquivalenzbereich wenigstens ± 15 %). Die EMA gibt dazu keine detaillierten Empfehlungen ab. Klinische Studien sollten, wie von der EMA gefordert, umfassende Immunogenitätsdaten ermitteln, um Effektivitätsverluste durch fehlende Antikörperaffinität oder schwere Hypersensitivitätsreaktionen durch Anti-Drug-Antikörper detektieren zu können. Dabei sind selbst kleine Unterschiede zwischen Originator und biosimilarem Antikörper ausreichend, um schwere unerwartete Reaktionen hervorzurufen. Aufgrund des Zulassungsprozesses und der limitierten klinischen Datenlage ist nach erfolgter Zulassung eine vollständige Post- Market -Datendokumentation zur Untersuchung der Sicherheit des jeweiligen biosimilaren Trastuzumab obligat. Diese Empfehlung findet sich auch in den EMA Guidelines wieder. Die Erfassung von Nebenwirkungen sollte unseres Erachtens daher idealerweise mit präziser Zuordnung zu dem jeweiligen Präparat in zentralen Registern erfolgen, wobei die von den Firmen gesam- 16 Thill M et al. Einführung und Verwendung Senologie 2018; 15: 13 17
6 melten Daten zu ihren Produkten b in diese Register einfließen sollten. Jedes Biologikum und so auch jeder biosimilare Antikörper sollte einen eindeutig vom Originator unterscheidbaren internationalen Freinamen (international non-proprietary name, INN) haben, damit z. B. nicht alle Trastuzumab-Biosimilars als Trastuzumab firmieren und somit die Klarheit für die Anwender optimiert wird. Die Dokumentation in der Patientenakte muss neben dem INN auch den Handelsnamen und die Chargennummer enthalten. Die Entscheidung, den originalen Antikörper durch einen biosimilaren zu ersetzen, muss in der Hand der Therapeutin bzw. des Therapeuten liegen und darf nicht ohne ausdrückliche Zustimmung und Wissen der Patientin erfolgen. Die Apotheker sollten nicht ohne Wissen des Arztes und/oder Anordnung des Arztes das Originalpräparat auf einen biosimilaren Antikörper oder umgekehrt umstellen. Vorgeschriebene Verordnungsquoten für biosimilare Antikörper sollten zum jetzigen Zeitpunkt ohne Vorliegen von Langzeitdaten zur Sicherheit und Effektivität abgelehnt werden. Interessenkonflikt Vortrags-, Beraterhonorare und Reisekostenerstattung von Roche, Amgen, Pfizer. Autorinnen/Autoren Marc Thill 1, Marcus Schmidt 2, Michael Lux 3, Cornelia Liedtke 4, Andreas Schneeweiss 5, Christian Jackisch 6 1 Klinik für Gynäkologie und Geburtshilfe, Agaplesion Markus Krankenhaus, Frankfurt am Main 2 Klinik für Geburtshilfe und Frauengesundheit, Universitätsklinikum Mainz 3 Frauenklinik, Universitätsklinikum Erlangen 4 Klinik für Geburtshilfe und Frauenheilkunde, Universitätsklinikum Schleswig-Holstein, Campus Lübeck 5 Nationales Zentrum für Tumorerkrankungen und Klinik für Gynäkologie und Geburtshilfe, Universitätsklinikum Heidelberg 6 Klinik für Gynäkologie und Geburtshilfe, Sana Klinikum Offenbach Korrespondenzadresse Priv.-Doz. Dr. med. Marc Thill Klinik für Gynäkologie und Geburtshilfe, Agaplesion Markus, Krankenhaus Wilhelm-Epstein-Straße Frankfurt am Main marc.thill@fdk.info Erstveröffentlichung Dieser Beitrag wurde erstveröffentlicht in: Geburtshilfe Frauenheilkd 2018; 78(01): doi: /s Literatur [1] Robert Koch-Institut; Gesellschaft der epidemiologischen Krebsregister in Deutschland e. V Hrsg. Krebs in Deutschland 2011/ Ausgabe Berlin, 2015: [2] Luengo-Fernandez R, Leal J, Gray A et al. Economic burden of cancer across the European Union: a population-based cost analysis. Lancet Oncol 2013; 14: [3] Rugo HS, Linton KM, Cervi P et al. A clinicianʼs guide to biosimilars in oncology. Cancer Treat Rev 2016; 46: [4] Oh MJ, Hua S, Kim U et al. Analytical detection and characterization of biopharmaceutical glycosylation by MS. Bioanalysis 2016; 8: [5] IMS Institute forhealth Informatics. Global Medicines Use in 2020: Outlook and Implications. Parsippany: IMS Institute for Health Informatics 2015 [6] IMS Institute forhealth Informatics. Delivering on the Potential of biosimilar Medicines. Parsippany: IMS Institute for Health Informatics 2016 [7] European Medicines Agency. Guideline on similar biological medicinal products containing monoclonal antibodies non-clinical and clinical issues. Online: Scientific_guideline/2012/06/ WC pdf Stand: [8] Thill M. New frontiers in oncology: biosimilar antibodies for the treatment of breast cancer. Expert Rev Anticancer Ther 2015; 15: [9] Thill M. Biosimilare Antikörper als Herausforderung ist Evidenz übertragbar? Kompendium Biosimilars 2016; 1: [10] World HealthOrganization. Guidelines on Evaluation of monoclonal Antibodies as similar biotherapeutic Products (SBPs). Geneva, Switzerland: World Health Organization 2016 [11] European Medicines Agency. Remsima European Public Assessment Report Online human/002576/wc pdf Stand: [12] Cortes J, Curigliano G, Dieras V. Expert perspectives on biosimilar monoclonal antibodies in breast cancer. Breast Cancer Res Treat 2014; 144: [13] Tabernero J, Vyas M, Giuliani R et al. Biosimilars: a position paper of the European Society for Medical Oncology, with particular reference to oncology prescribers. ESMO Open 2016; 1: e doi: /esmoopen [14] Jackisch C, Lammers P, Jacobs I. Evolving landscape of human epidermal growth factor receptor 2-positive breast cancer treatment and the future of biosimilars. Breast 2017; 32: [15] Jackisch C, Scappaticci FA, Heinzmann D et al. Neoadjuvant breast cancer treatment as a sensitive setting for trastuzumab biosimilar development and extrapolation. Future Oncol 2015; 11: Bibliografie DOI Senologie 2018; 15: Georg Thieme Verlag KG, Stuttgart New York ISSN Thill M et al. Einführung und Verwendung Senologie 2018; 15:
Biosimilars ähnlich, aber nicht identisch!
 Biosimilars ähnlich, aber nicht identisch! München, 23. April 2007 Dr. Frank Mathias Geschäftsführer, AMGEN GmbH Deutschland Die Frage...... identisch - oder nur ähnlich? 2 Biotechnologisch hergestellte
Biosimilars ähnlich, aber nicht identisch! München, 23. April 2007 Dr. Frank Mathias Geschäftsführer, AMGEN GmbH Deutschland Die Frage...... identisch - oder nur ähnlich? 2 Biotechnologisch hergestellte
HER2-positiver Rezeptorstatus als signifikanter Überlebensvorteil
 10 Jahre Herceptin HER2-positiver Rezeptorstatus als signifikanter Überlebensvorteil Frankfurt am Main (27. September 2010) - Die Entwicklung von Trastuzumab (Herceptin) hat die Brustkrebstherapie revolutioniert.
10 Jahre Herceptin HER2-positiver Rezeptorstatus als signifikanter Überlebensvorteil Frankfurt am Main (27. September 2010) - Die Entwicklung von Trastuzumab (Herceptin) hat die Brustkrebstherapie revolutioniert.
Perjeta für die neoadjuvante Therapie zugelassen
 HER2-positives Mammakarzinom Perjeta für die neoadjuvante Therapie zugelassen Grenzach-Wyhlen (31. Juli 2015) - Die Europäische Arzneimittel-Agentur (EMA) hat Perjeta (Pertuzumab) in Kombination mit Herceptin
HER2-positives Mammakarzinom Perjeta für die neoadjuvante Therapie zugelassen Grenzach-Wyhlen (31. Juli 2015) - Die Europäische Arzneimittel-Agentur (EMA) hat Perjeta (Pertuzumab) in Kombination mit Herceptin
Ihre Therapie verstehen Fragen und Antworten zu Remsima kurz und verständlich
 Ihre Therapie verstehen Fragen und Antworten zu Remsima kurz und verständlich 1 2 Bei welchen Erkrankungen wird Remsima eingesetzt? Remsima ist ein Arzneimittel, das bei chronischent zündlichen Erkrankungen
Ihre Therapie verstehen Fragen und Antworten zu Remsima kurz und verständlich 1 2 Bei welchen Erkrankungen wird Remsima eingesetzt? Remsima ist ein Arzneimittel, das bei chronischent zündlichen Erkrankungen
Neue Studienkonzepte SUCCESS
 Campus Innenstadt für Frauenheilkunde und Geburtshilfe Neue Studienkonzepte SUCCESS PD Dr. med. Brigitte Rack für Frauenheilkunde und Geburtshilfe Ludwig-Maximilians-Universität München Campus Innenstadt
Campus Innenstadt für Frauenheilkunde und Geburtshilfe Neue Studienkonzepte SUCCESS PD Dr. med. Brigitte Rack für Frauenheilkunde und Geburtshilfe Ludwig-Maximilians-Universität München Campus Innenstadt
Meilenstein in der personalisierten Medizin FDA-Zulassung für Pertuzumab beim HER2-positiven metastasierten Mammakarzinom
 Meilenstein in der personalisierten Medizin FDA-Zulassung für Pertuzumab beim HER2-positiven metastasierten Mammakarzinom Frankfurt am Main (15. Juni 2012) - Die US-amerikanische Arzneimittelzulassungsbehörde
Meilenstein in der personalisierten Medizin FDA-Zulassung für Pertuzumab beim HER2-positiven metastasierten Mammakarzinom Frankfurt am Main (15. Juni 2012) - Die US-amerikanische Arzneimittelzulassungsbehörde
Positionspapier Biosimilars von monoklonalen Antikörpern in der Medizinischen Onkologie
 Positionspapier Biosimilars von monoklonalen Antikörpern in der Medizinischen Onkologie 3. Mai 2017 Zusammenfassung Nach Patentablauf der ersten therapeutisch eingesetzten, monoklonalen Antikörper in der
Positionspapier Biosimilars von monoklonalen Antikörpern in der Medizinischen Onkologie 3. Mai 2017 Zusammenfassung Nach Patentablauf der ersten therapeutisch eingesetzten, monoklonalen Antikörper in der
Ähnlich, aber nicht identisch Anforderungen an Biosimilars
 Ähnlich, aber nicht identisch Anforderungen an Biosimilars Dr. Frank Mathias, Vorsitzender VFA Bio Pressekonferenz 27. Oktober 2006 Sind wir identisch oder nur ähnlich? VFA Bio Oktober 2006 2 VFA Bio Oktober
Ähnlich, aber nicht identisch Anforderungen an Biosimilars Dr. Frank Mathias, Vorsitzender VFA Bio Pressekonferenz 27. Oktober 2006 Sind wir identisch oder nur ähnlich? VFA Bio Oktober 2006 2 VFA Bio Oktober
Was müssen therapeutische Biosimilars in der Onkologie leisten?
 Was müssen therapeutische Biosimilars in der Onkologie leisten? Prof. Dr. Hans Tesch Onkologische Gemeinschaftspraxis am Bethanien-Krankenhaus Frankfurt am Main AMGEN Satellitensymposium im Rahmen der
Was müssen therapeutische Biosimilars in der Onkologie leisten? Prof. Dr. Hans Tesch Onkologische Gemeinschaftspraxis am Bethanien-Krankenhaus Frankfurt am Main AMGEN Satellitensymposium im Rahmen der
Adjuvante zytostatische und zielgerichtete Therapien
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Versionen 2002 2017: Dall /
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Versionen 2002 2017: Dall /
Wie ist die Evidenzlage in Biosimilarstudien? Gibt es trotzdem Unterschiede?
 Wie ist die Evidenzlage in Biosimilarstudien? Gibt es trotzdem Unterschiede? Satellitensymposium während des DGHO-Kongresses: Biosimilars 3.0: therapeutische monoklonale Antikörper in der Onkologie - Chancen,
Wie ist die Evidenzlage in Biosimilarstudien? Gibt es trotzdem Unterschiede? Satellitensymposium während des DGHO-Kongresses: Biosimilars 3.0: therapeutische monoklonale Antikörper in der Onkologie - Chancen,
Biosimilars: Die Sicht der Ärzte (am Beispiel von Trastuzumab)
 Biosimilars: Die Sicht der Ärzte (am Beispiel von Trastuzumab) Veranstaltung für Patientenselbsthilfegruppen, Roche Diagnostics GmbH, Penzberg, 06.11.2013 PD Dr. M. Thill Klinik für Gynäkologie und Geburtshilfe
Biosimilars: Die Sicht der Ärzte (am Beispiel von Trastuzumab) Veranstaltung für Patientenselbsthilfegruppen, Roche Diagnostics GmbH, Penzberg, 06.11.2013 PD Dr. M. Thill Klinik für Gynäkologie und Geburtshilfe
Prof. Dr. Theodor Dingermann
 BIOSIMILARS Sicher keine Biologicals 2. Klasse Prof. Dr. Theodor Dingermann Institut für Pharmazeutische Biologie Dingermann@em.uni-frankfurt.de 19.02.2016 Biosimilars gibt es seit 10 Jahren Omnitrope
BIOSIMILARS Sicher keine Biologicals 2. Klasse Prof. Dr. Theodor Dingermann Institut für Pharmazeutische Biologie Dingermann@em.uni-frankfurt.de 19.02.2016 Biosimilars gibt es seit 10 Jahren Omnitrope
Neue Perspektiven für Frauen mit Brustkrebs Perjeta und Kadcyla in der Behandlung des HER2-positiven Mammakarzinoms
 Neue Perspektiven für Frauen mit Brustkrebs Perjeta und Kadcyla in der Behandlung des HER2-positiven Mammakarzinoms Berlin (19. Juni 2014) - Die Überlebensperspektiven für Frauen mit metastasiertem HER2-positivem
Neue Perspektiven für Frauen mit Brustkrebs Perjeta und Kadcyla in der Behandlung des HER2-positiven Mammakarzinoms Berlin (19. Juni 2014) - Die Überlebensperspektiven für Frauen mit metastasiertem HER2-positivem
Biosimilars : Wachstumsfaktoren und Antikörper in der Onkologie
 Biosimilars : Wachstumsfaktoren und Antikörper in der Onkologie Dr. med. Ursula Kronawitter www.onkologie - traunstein.de onkologie traunstein @ t-online.de Anforderungen des Arztes an ein Biosimilar Im
Biosimilars : Wachstumsfaktoren und Antikörper in der Onkologie Dr. med. Ursula Kronawitter www.onkologie - traunstein.de onkologie traunstein @ t-online.de Anforderungen des Arztes an ein Biosimilar Im
Adalimumab-Biosimilars: Ein Zwischenfazit. Wolf-Dieter Ludwig Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ)
 Adalimumab-Biosimilars: Ein Zwischenfazit Wolf-Dieter Ludwig Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ) Erklärung zu Interessenkonflikten Aufwandsentschädigung: A.I.D. (BÄK/ KBV); wissenschaftlicher
Adalimumab-Biosimilars: Ein Zwischenfazit Wolf-Dieter Ludwig Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ) Erklärung zu Interessenkonflikten Aufwandsentschädigung: A.I.D. (BÄK/ KBV); wissenschaftlicher
Biosimilars- Die Sicht der Patienten
 Ähnlich, aber eben doch nicht gleich - Biopharmazeutika: Der Unterschied liegt im Detail Biosimilars- Die Sicht der Patienten 27. November 2012 Ludwigshafen Renate Haidinger Medozinjournalistin 1.Vorsitzende
Ähnlich, aber eben doch nicht gleich - Biopharmazeutika: Der Unterschied liegt im Detail Biosimilars- Die Sicht der Patienten 27. November 2012 Ludwigshafen Renate Haidinger Medozinjournalistin 1.Vorsitzende
Neoadjuvante (Primäre) systemische Therapie
 Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
Die duale vertikale Blockade (VDB) als neue Therapieoption in der Zweitlinientherapie des metastasierten Her2neu positiven Mammakarzinoms
 Krebskongress 2014 Die duale vertikale Blockade (VDB) als neue Therapieoption in der Zweitlinientherapie des metastasierten Her2neu positiven Mammakarzinoms Prof. Dr. med. Christian Jackisch Berlin (21.
Krebskongress 2014 Die duale vertikale Blockade (VDB) als neue Therapieoption in der Zweitlinientherapie des metastasierten Her2neu positiven Mammakarzinoms Prof. Dr. med. Christian Jackisch Berlin (21.
kolorektalen Karzinoms
 Signifikante Lebensverlängerung durch Angiogenese-Hemmung Avastin in der First-Line-Therapie des metastasierten kolorektalen Karzinoms Berlin (24. März 2006) - Erhalten Patienten mit metastasiertem kolorektalen
Signifikante Lebensverlängerung durch Angiogenese-Hemmung Avastin in der First-Line-Therapie des metastasierten kolorektalen Karzinoms Berlin (24. März 2006) - Erhalten Patienten mit metastasiertem kolorektalen
Zulassung für Herceptin SC Mehr Freiraum für Frauen mit HER2-positivem Mammakarzinom
 Zulassung für Herceptin SC Mehr Freiraum für Frauen mit HER2-positivem Mammakarzinom Hamburg (12. September 2013) - Seit Ende August 2013 ist der Antikörper Herceptin (Trastuzumab, Roche) als subkutane
Zulassung für Herceptin SC Mehr Freiraum für Frauen mit HER2-positivem Mammakarzinom Hamburg (12. September 2013) - Seit Ende August 2013 ist der Antikörper Herceptin (Trastuzumab, Roche) als subkutane
Endokrine Therapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version 2002: Gerber / Friedrichs
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version 2002: Gerber / Friedrichs
Erbitux (Cetuximab) erhält Empfehlung des CHMP für den Erstlinieneinsatz in der Behandlung von Kopf-Hals-Tumoren
 Erbitux (Cetuximab) erhält Empfehlung des CHMP für den Erstlinieneinsatz in der Behandlung von Kopf Erbitux (Cetuximab) erhält Empfehlung des CHMP für den Erstlinieneinsatz in der Behandlung von Kopf-Hals-Tumoren
Erbitux (Cetuximab) erhält Empfehlung des CHMP für den Erstlinieneinsatz in der Behandlung von Kopf Erbitux (Cetuximab) erhält Empfehlung des CHMP für den Erstlinieneinsatz in der Behandlung von Kopf-Hals-Tumoren
Neoadjuvante (Primäre) systemische Therapie
 Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer AGO e. V. Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer AGO e. V. Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
Endokrine Therapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version 2002: Gerber / Friedrichs
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version 2002: Gerber / Friedrichs
Innovationen für Patienten
 Roche Innovationen für Patienten Penzberg (3. Mai 2017) - Roche zielt darauf, mit innovativen Lösungen neue Therapiestandards für Patienten zu schaffen. Beispielhaft für solche Durchbrüche in der Behandlung
Roche Innovationen für Patienten Penzberg (3. Mai 2017) - Roche zielt darauf, mit innovativen Lösungen neue Therapiestandards für Patienten zu schaffen. Beispielhaft für solche Durchbrüche in der Behandlung
Bevölkerungsbezogene Analysen neuer Therapieoptionen an einem regionalen Beispiel
 Bevölkerungsbezogene Analysen neuer Therapieoptionen an einem regionalen Beispiel Priv.- Doz. Dr. med. Monika Klinkhammer-Schalke Arbeitsgemeinschaft Deutscher Tumorzentren e.v., Berlin Kooperationsverbund
Bevölkerungsbezogene Analysen neuer Therapieoptionen an einem regionalen Beispiel Priv.- Doz. Dr. med. Monika Klinkhammer-Schalke Arbeitsgemeinschaft Deutscher Tumorzentren e.v., Berlin Kooperationsverbund
Nierenzellkarzinom: First-Line-Therapie mit Bevacizumab plus Interferon alfa-2a erhält Lebensqualität und. Therapieoptionen
 Nierenzellkarzinom First-Line-Therapie mit Bevacizumab plus Interferon alfa-2a erhält Lebensqualität und Therapieoptionen Düsseldorf (1.Oktober 2010) - Anlässlich der 62. Jahrestagung der Deutschen Gesellschaft
Nierenzellkarzinom First-Line-Therapie mit Bevacizumab plus Interferon alfa-2a erhält Lebensqualität und Therapieoptionen Düsseldorf (1.Oktober 2010) - Anlässlich der 62. Jahrestagung der Deutschen Gesellschaft
AMNOG: Wenn Innovation aufs System trifft: Ist das AMNOG System fit für Innovation- Beispiel Onkologie
 AMNOG: Wenn Innovation aufs System trifft: Ist das AMNOG System fit für Innovation- Beispiel Onkologie Dr. Jutta Wendel-Schrief Direktor Market Access MSD SHARP & DOHME GMBH Was sind Innovationen? Neue
AMNOG: Wenn Innovation aufs System trifft: Ist das AMNOG System fit für Innovation- Beispiel Onkologie Dr. Jutta Wendel-Schrief Direktor Market Access MSD SHARP & DOHME GMBH Was sind Innovationen? Neue
Neoadjuvante (Primäre) systemische Therapie
 Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer in der DGGG e.v. sowie Version 2009.1.0 2010.1.0D Neoadjuvante
Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer in der DGGG e.v. sowie Version 2009.1.0 2010.1.0D Neoadjuvante
Medikamentöse Therapie rheumatischer Erkrankungen
 Medikamentöse Therapie rheumatischer Erkrankungen Nichtsteroidale Antirheumatika/ Cox 2-Hemmer u. a. Diclofenac, Ibuprofen Celecoxib, Etoricoxib DMARDs/Basistherapeutika u. a. Hydroxychloroquin, Sulfasalazin,
Medikamentöse Therapie rheumatischer Erkrankungen Nichtsteroidale Antirheumatika/ Cox 2-Hemmer u. a. Diclofenac, Ibuprofen Celecoxib, Etoricoxib DMARDs/Basistherapeutika u. a. Hydroxychloroquin, Sulfasalazin,
Integrase-Hemmung mit ISENTRESS : Eine neue Klasse antiretroviraler Wirkstoffe zur Behandlung von HIV
 Integrase-Hemmung mit ISENTRESS : Eine neue Klasse antiretroviraler Wirkstoffe zur Behandlung von HIV Von Dr. med. Markus Rupp, MSD SHARP & DOHME GMBH, Haar München (20. September 2008) Der World-Aids-Report
Integrase-Hemmung mit ISENTRESS : Eine neue Klasse antiretroviraler Wirkstoffe zur Behandlung von HIV Von Dr. med. Markus Rupp, MSD SHARP & DOHME GMBH, Haar München (20. September 2008) Der World-Aids-Report
Refraktäres indolentes Non-Hodgkin-Lymphom Gazyvaro erzielt deutlich längeres progressionsfreies Überleben
 Refraktäres indolentes Non-Hodgkin-Lymphom: Gazyvaro erzielt deutlich längeres progressionsfreies Üb Refraktäres indolentes Non-Hodgkin-Lymphom Gazyvaro erzielt deutlich längeres progressionsfreies Überleben
Refraktäres indolentes Non-Hodgkin-Lymphom: Gazyvaro erzielt deutlich längeres progressionsfreies Üb Refraktäres indolentes Non-Hodgkin-Lymphom Gazyvaro erzielt deutlich längeres progressionsfreies Überleben
Update Systemtherapie. Mammakarzinom. Christoph Rochlitz
 Update Systemtherapie Mammakarzinom Christoph Rochlitz Themen Chemotherapie Hormontherapie Targeted Therapy Neoadjuvant Adjuvant Palliativ Themen Chemotherapie Hormontherapie Targeted Therapy Neoadjuvant
Update Systemtherapie Mammakarzinom Christoph Rochlitz Themen Chemotherapie Hormontherapie Targeted Therapy Neoadjuvant Adjuvant Palliativ Themen Chemotherapie Hormontherapie Targeted Therapy Neoadjuvant
Zielgerichtete Substanzen*
 Diagnostik und Therapie primärer und metastasierter Mammakarzinomr Zielgerichtete Substanzen* *Es werden nur Substanzen besprochen, von denen Daten aus mindestens einer publizierten Phase-III-Studie vorliegen
Diagnostik und Therapie primärer und metastasierter Mammakarzinomr Zielgerichtete Substanzen* *Es werden nur Substanzen besprochen, von denen Daten aus mindestens einer publizierten Phase-III-Studie vorliegen
ASCO 2015 Neues zur Therapie des HER2-positiven Mammakarzinoms
 ASCO 2015 Neues zur Therapie des HER2-positiven Mammakarzinoms Bonn (16. Juni 2015) - Ein Schwerpunkt des weltweit größten Krebskongresses, der 51. Jahrestagung der American Society of Clinical Oncology
ASCO 2015 Neues zur Therapie des HER2-positiven Mammakarzinoms Bonn (16. Juni 2015) - Ein Schwerpunkt des weltweit größten Krebskongresses, der 51. Jahrestagung der American Society of Clinical Oncology
Erhaltungstherapie mit Erlotinib verlängert Gesamtüberleben bei fortgeschrittenem NSCLC
 SATURN-Studie: Erhaltungstherapie mit Erlotinib verlängert Gesamtüberleben bei fortgeschrittenem NSCLC Grenzach-Wyhlen (13. August 2009) - Aktuelle Daten der SATURN-Studie bestätigen eine signifikante
SATURN-Studie: Erhaltungstherapie mit Erlotinib verlängert Gesamtüberleben bei fortgeschrittenem NSCLC Grenzach-Wyhlen (13. August 2009) - Aktuelle Daten der SATURN-Studie bestätigen eine signifikante
Von Originalen, Generika und Biosimilars. Marion Matousek-Wild Co-Leiterin Spitalapotheke 25. Juni 2015
 Von Originalen, Generika und Biosimilars Marion Matousek-Wild Co-Leiterin Spitalapotheke 25. Juni 2015 Generikum vs. Biosimilar Chemisches Produkt Chemische Synthese Biologisches Produkt Komplexer, mehrstufiger
Von Originalen, Generika und Biosimilars Marion Matousek-Wild Co-Leiterin Spitalapotheke 25. Juni 2015 Generikum vs. Biosimilar Chemisches Produkt Chemische Synthese Biologisches Produkt Komplexer, mehrstufiger
10 Jahre Biosimilars in Europa: Vom wissenschaftlichen Konzept zum wissenschaftlich-erfahrungsbasierten. Ansatz
 BfArM im Dialog zu Biosimilars 10 Jahre Biosimilars in Europa: Vom wissenschaftlichen Konzept zum wissenschaftlich-erfahrungsbasierten Andrea Laslop Scientific Office AGES Medizinmarktaufsicht, Wien, Austria
BfArM im Dialog zu Biosimilars 10 Jahre Biosimilars in Europa: Vom wissenschaftlichen Konzept zum wissenschaftlich-erfahrungsbasierten Andrea Laslop Scientific Office AGES Medizinmarktaufsicht, Wien, Austria
Version: V1.0 basierend auf Amendment 1 vom 15. Juli 2016
 Pertuzumab in First Line Treatment of HER2-positive metastatic breast Cancer patients: A cohort study of patients treated either with docetaxel and Trastuzumab or docetaxel, trastuzumab and, NCT02642458
Pertuzumab in First Line Treatment of HER2-positive metastatic breast Cancer patients: A cohort study of patients treated either with docetaxel and Trastuzumab or docetaxel, trastuzumab and, NCT02642458
internationalen SAiL Studie, in der die Sicherheit und Wirksamkeit des VEGF Antikörpers in der täglichen Routine analysiert werden.
 DGP Kongress in Lübeck Avastin überwindet Therapiestillstand beim fortgeschrittenen NSCLC Lübeck (11. April 2008) - Die zielgerichtete First Line -Therapie mit dem Angiogenese Hemmer Bevacizumab (Avastin
DGP Kongress in Lübeck Avastin überwindet Therapiestillstand beim fortgeschrittenen NSCLC Lübeck (11. April 2008) - Die zielgerichtete First Line -Therapie mit dem Angiogenese Hemmer Bevacizumab (Avastin
PROF. DR. MED. C. JACKISCH
 PROF. DR. MED. C. JACKISCH Versorgungslage beim Zervixkarzinom in Deutschland SANA KLINIKUM OFFENBACH Klinik für Gynäkologie und Geburtshilfe - Zertifiziertes Brust- und Genitalkrebszentrum mit Empfehlung
PROF. DR. MED. C. JACKISCH Versorgungslage beim Zervixkarzinom in Deutschland SANA KLINIKUM OFFENBACH Klinik für Gynäkologie und Geburtshilfe - Zertifiziertes Brust- und Genitalkrebszentrum mit Empfehlung
Erfolge der Immuntherapie beim Lungenkrebs. Martin Früh Klinik für Onkologie und Hämatologie Kantonsspital St. Gallen
 Erfolge der Immuntherapie beim Lungenkrebs Martin Früh Klinik für Onkologie und Hämatologie Kantonsspital St. Gallen Weltweite Krebsstatistik 2012 (Industrieländer) Neuerkrankungen/Jahr Mortalität/Jahr
Erfolge der Immuntherapie beim Lungenkrebs Martin Früh Klinik für Onkologie und Hämatologie Kantonsspital St. Gallen Weltweite Krebsstatistik 2012 (Industrieländer) Neuerkrankungen/Jahr Mortalität/Jahr
ASCO 2007 Kongressreflektionen Wo stehen wir heute Was bringt die Zukunft in der Therapie des Mammakarzinoms
 ASCO 2007 Kongressreflektionen Wo stehen wir heute Was bringt die Zukunft in der Therapie des Mammakarzinoms Prof. Dr. C. Jackisch Klinik für Gynäkologie und Geburtshilfe Klinikum Offenbach GmbH Das diesjährige
ASCO 2007 Kongressreflektionen Wo stehen wir heute Was bringt die Zukunft in der Therapie des Mammakarzinoms Prof. Dr. C. Jackisch Klinik für Gynäkologie und Geburtshilfe Klinikum Offenbach GmbH Das diesjährige
Endokrine Therapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2012.1D Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version
Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2012.1D Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version
Kein Hand-Fuß-Syndrom unter Behandlung mit UFT (Tegafur Uracil)
 ESMO: Kein Hand-Fuß-Syndrom unter Behandlung mit UFT (Tegafur Uracil) Darmstadt (8. Oktober 2008) Auf der 33. Jahrestagung der European Society for Medical Oncology (ESMO) wurden die Ergebnisse einer Untersuchung
ESMO: Kein Hand-Fuß-Syndrom unter Behandlung mit UFT (Tegafur Uracil) Darmstadt (8. Oktober 2008) Auf der 33. Jahrestagung der European Society for Medical Oncology (ESMO) wurden die Ergebnisse einer Untersuchung
Optimierung der Therapie des kolorektalen Karzinoms durch Panitumumab
 Neues und Wissenswertes aus der Onkologie Optimierung der Therapie des kolorektalen Karzinoms durch Panitumumab München (26. Juli 2012) - Deutliche Fortschritte in der Tumortherapie haben in den letzten
Neues und Wissenswertes aus der Onkologie Optimierung der Therapie des kolorektalen Karzinoms durch Panitumumab München (26. Juli 2012) - Deutliche Fortschritte in der Tumortherapie haben in den letzten
Biosimilars Produkt und Entwicklungsprozess
 Dr. med. Guido Würth, Global Program Medical Director, Hexal AG XI. Expertengespräch der PPH plus GmbH & Co. KG Frankfurt am Main, 29. April 2016 Biosimilars Produkt und Entwicklungsprozess Deklaration
Dr. med. Guido Würth, Global Program Medical Director, Hexal AG XI. Expertengespräch der PPH plus GmbH & Co. KG Frankfurt am Main, 29. April 2016 Biosimilars Produkt und Entwicklungsprozess Deklaration
Adjuvante zytostatische und zielgerichtete Therapien
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapie Version 2002: Möbus / Nitz Versionen
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapie Version 2002: Möbus / Nitz Versionen
Avastin wirkt unabhängig vom K-RAS-Mutationsstatus in der First-Line-Therapie des metastasierten kolorektalen Karzinoms
 Avastin wirkt unabhängig vom K-RAS-Mutationsstatus in der First-Line-Therapie des metastasierten kolorektalen Karzinoms Berlin / Grenzach-Wyhlen (3. Oktober 2008) - Avastin (Bevacizumab) ist das einzige
Avastin wirkt unabhängig vom K-RAS-Mutationsstatus in der First-Line-Therapie des metastasierten kolorektalen Karzinoms Berlin / Grenzach-Wyhlen (3. Oktober 2008) - Avastin (Bevacizumab) ist das einzige
Aktuelle Therapiestudien in der Klinik für Gynäkologie und Geburtshilfe Sana Klinikum Offenbach GmbH Stand Metastasiertes Mammakarzinom
 Klinikum GmbH Desiree Eine multizentrische, randomisierte doppelblinde, Phase-II-Studie zum Vergleich der Verträglichkeit bei einschleichender Dosierung von Everolimus bei Patienten mit metastasiertem
Klinikum GmbH Desiree Eine multizentrische, randomisierte doppelblinde, Phase-II-Studie zum Vergleich der Verträglichkeit bei einschleichender Dosierung von Everolimus bei Patienten mit metastasiertem
Antikörpertherapie beim Mammakarzinom
 Antikörpertherapie beim Mammakarzinom (Dr. S. Rückert) Trastuzumab (Herceptin ) ist ein gentechnisch hergestellter Antikörper, welcher gegen das HER2/neu-Protein gerichtet ist. Dieser Wachstumsfaktor kommt
Antikörpertherapie beim Mammakarzinom (Dr. S. Rückert) Trastuzumab (Herceptin ) ist ein gentechnisch hergestellter Antikörper, welcher gegen das HER2/neu-Protein gerichtet ist. Dieser Wachstumsfaktor kommt
Patientenseminar am Brustzentrum des Universitätsklinikums Leipzig 2019
 Patientenseminar am Brustzentrum des Universitätsklinikums Leipzig 2019 Prof. Dr. med. Bahriye Aktas Universitätsklinikum Leipzig Klinik und Poliklinik für Frauenheilkunde Leipzig 06.02.2019 Blitzlicht
Patientenseminar am Brustzentrum des Universitätsklinikums Leipzig 2019 Prof. Dr. med. Bahriye Aktas Universitätsklinikum Leipzig Klinik und Poliklinik für Frauenheilkunde Leipzig 06.02.2019 Blitzlicht
Positionierung der Deutschen Rheuma-Liga Bundesverband e.v. zur Einführung von Biosimilars in Deutschland
 Positionierung der Deutschen Rheuma-Liga Bundesverband e.v. zur Einführung von Biosimilars in Deutschland Die Deutsche Rheuma-Liga sieht es als erstrebenswert an, dass sichere und effektive Therapien möglichst
Positionierung der Deutschen Rheuma-Liga Bundesverband e.v. zur Einführung von Biosimilars in Deutschland Die Deutsche Rheuma-Liga sieht es als erstrebenswert an, dass sichere und effektive Therapien möglichst
Post St. Gallen Chemo- und Immuntherapie
 Post St. Gallen 2009 Chemo- und Immuntherapie Rupert Bartsch Universitätsklinik für Innere Medizin 1 Klinische Abteilung für Onkologie 1 Neue Daten von HERA und FinHER Empfehlungen des Panels zu Adjuvanten
Post St. Gallen 2009 Chemo- und Immuntherapie Rupert Bartsch Universitätsklinik für Innere Medizin 1 Klinische Abteilung für Onkologie 1 Neue Daten von HERA und FinHER Empfehlungen des Panels zu Adjuvanten
Erelzi und Rixathon : zwei Biosimilars als neue Therapieoptionen für rheumatologische Patienten
 Hexal: Erelzi und Rixathon : zwei Biosimilars als neue Therapieoptionen für rheumatologische Patiente Hexal Erelzi und Rixathon : zwei Biosimilars als neue Therapieoptionen für rheumatologische Patienten
Hexal: Erelzi und Rixathon : zwei Biosimilars als neue Therapieoptionen für rheumatologische Patiente Hexal Erelzi und Rixathon : zwei Biosimilars als neue Therapieoptionen für rheumatologische Patienten
Gute Überlebensqualität Trastuzumab beim metastasierten Magenkarzinom
 Gute Überlebensqualität Trastuzumab beim metastasierten Magenkarzinom München (24. April 2012) - Mit dem monoklonalen Antikörper Trastuzumab (Herceptin ) steht bislang die einzige zielgerichtete Substanz
Gute Überlebensqualität Trastuzumab beim metastasierten Magenkarzinom München (24. April 2012) - Mit dem monoklonalen Antikörper Trastuzumab (Herceptin ) steht bislang die einzige zielgerichtete Substanz
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien
 Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
Biosimilars - Die Sicht der Patienten Ulla Ohlms, Vorsitzende der Stiftung PATH Patients Tumorbank of Hope
 Biosimilars - Die Sicht der Patienten Ulla Ohlms, Vorsitzende der Stiftung PATH Patients Tumorbank of Hope Vfa-Tagung Ähnlich, aber eben doch nicht gleich Penzberg, 6. November 2013 März 2000, damals,
Biosimilars - Die Sicht der Patienten Ulla Ohlms, Vorsitzende der Stiftung PATH Patients Tumorbank of Hope Vfa-Tagung Ähnlich, aber eben doch nicht gleich Penzberg, 6. November 2013 März 2000, damals,
TNF-α-Inhibitoren zeigen Unterschiede in der Immunogenität
 Eine Klasse für sich TNF-α-Inhibitoren zeigen Unterschiede in der Immunogenität Berlin (26. April 2012) - Die Wirksamkeit und Sicherheit der TNF-α-Inhibitoren in der Behandlung der Rheumatoiden Arthritis
Eine Klasse für sich TNF-α-Inhibitoren zeigen Unterschiede in der Immunogenität Berlin (26. April 2012) - Die Wirksamkeit und Sicherheit der TNF-α-Inhibitoren in der Behandlung der Rheumatoiden Arthritis
Perspektiven mit Tarceva und Avastin
 Fortgeschrittenes NSCLC: Perspektiven mit Tarceva und Avastin Mannheim (20. März 2009) - Die Behandlung des fortgeschrittenen nicht-kleinzelligen Lungenkarzinoms (Non Small Cell Lung Cancer, NSCLC) mit
Fortgeschrittenes NSCLC: Perspektiven mit Tarceva und Avastin Mannheim (20. März 2009) - Die Behandlung des fortgeschrittenen nicht-kleinzelligen Lungenkarzinoms (Non Small Cell Lung Cancer, NSCLC) mit
Das tripelnegative. Mammakarzinom
 Das tripelnegative Mammakarzinom - eine therapeutische Herausforderung - Priv.-Doz. Dr. med. Cornelia Liedtke - Direktor: Prof. Dr. med. Achim Rody - Universitätsklinikum Schleswig-Holstein / Campus Lübeck
Das tripelnegative Mammakarzinom - eine therapeutische Herausforderung - Priv.-Doz. Dr. med. Cornelia Liedtke - Direktor: Prof. Dr. med. Achim Rody - Universitätsklinikum Schleswig-Holstein / Campus Lübeck
Positionspapier zu Biosimilars. Zusammenfassung
 Positionspapier zu Biosimilars Zusammenfassung Biotechnologisch hergestellte Medikamente, auch Biologika genannt, nehmen einen wichtigen Platz in der Behandlung von Krankheiten wie Krebs, rheumatoider
Positionspapier zu Biosimilars Zusammenfassung Biotechnologisch hergestellte Medikamente, auch Biologika genannt, nehmen einen wichtigen Platz in der Behandlung von Krankheiten wie Krebs, rheumatoider
HINTERGRUND-INFORMATION 2.7
 Biosimilars eine neue Generation von Arzneimitteln Biosimilars sind Nachfolgepräparate von Biopharmazeutika (Biologics), deren Patentschutz abgelaufen ist. Sie enthalten eine Wirksubstanz, die mit der
Biosimilars eine neue Generation von Arzneimitteln Biosimilars sind Nachfolgepräparate von Biopharmazeutika (Biologics), deren Patentschutz abgelaufen ist. Sie enthalten eine Wirksubstanz, die mit der
STUDIEN PRO UND CONTRA
 V) WEITERE THEMEN STUDIEN PRO UND CONTRA Die Erfahrung hat gezeigt, dass Behandlungsergebnisse an mehr oder weniger kleinen Patientenzahlen von Autor zu Autor auch bei Einsatz gleicher Zytostatika zu unterschiedlichen,
V) WEITERE THEMEN STUDIEN PRO UND CONTRA Die Erfahrung hat gezeigt, dass Behandlungsergebnisse an mehr oder weniger kleinen Patientenzahlen von Autor zu Autor auch bei Einsatz gleicher Zytostatika zu unterschiedlichen,
Chemotherapie bei metastasiertem Mammakarzinom
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Chemotherapie bei metastasiertem Mammakarzinom Chemotherapie bei metastasiertem Mammakarzinom Version 2002: von Minckwitz Version 2003
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Chemotherapie bei metastasiertem Mammakarzinom Chemotherapie bei metastasiertem Mammakarzinom Version 2002: von Minckwitz Version 2003
Neues zum fortgeschrittenen Mammakarzinom
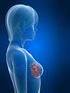 Neues zum fortgeschrittenen Mammakarzinom Ulrike Nitz Brustzentrum Niederrhein MBC OS Aktuelle Bestandsaufnahme OMEDCO nterims Analyse 2013; ABC Gruppe; n=1409/2250 Patients alive 100% 90% 80% 70% 60%
Neues zum fortgeschrittenen Mammakarzinom Ulrike Nitz Brustzentrum Niederrhein MBC OS Aktuelle Bestandsaufnahme OMEDCO nterims Analyse 2013; ABC Gruppe; n=1409/2250 Patients alive 100% 90% 80% 70% 60%
V. Grünwald 1, T. Steiner 2, L. Bergmann 3, B. Eberhardt 4, A. Hartmann 5. Onkologie und Stammzelltransplantation, Hannover.
 V. Grünwald 1, T. Steiner 2, L. Bergmann 3, B. Eberhardt 4, A. Hartmann 5 1 Medizinische Hochschule Hannover, Klinik für Hämatologie, Hämostaseologie, Onkologie und Stammzelltransplantation, 30625 Hannover.
V. Grünwald 1, T. Steiner 2, L. Bergmann 3, B. Eberhardt 4, A. Hartmann 5 1 Medizinische Hochschule Hannover, Klinik für Hämatologie, Hämostaseologie, Onkologie und Stammzelltransplantation, 30625 Hannover.
Biomarker beim KRK was kommt als nächstes in die Klinik?
 GI Oncology 2010 6. Interdisziplinäres Update 3. Juli 2010 Biomarker beim KRK was kommt als nächstes in die Klinik? Thomas Seufferlein Klinik für Innere Medizin I Martin-Luther-Universität Halle-Wittenberg
GI Oncology 2010 6. Interdisziplinäres Update 3. Juli 2010 Biomarker beim KRK was kommt als nächstes in die Klinik? Thomas Seufferlein Klinik für Innere Medizin I Martin-Luther-Universität Halle-Wittenberg
Alectinib wirksam bei ALK-positivem NSCLC
 Erste Ergebnisse der J-ALEX-Studie auf ASCO 2016 präsentiert Alectinib wirksam bei ALK-positivem NSCLC Hamburg (22. Juni 2016) Alectinib führt im Vergleich zu Crizotinib zu einer signifikanten Verlängerung
Erste Ergebnisse der J-ALEX-Studie auf ASCO 2016 präsentiert Alectinib wirksam bei ALK-positivem NSCLC Hamburg (22. Juni 2016) Alectinib führt im Vergleich zu Crizotinib zu einer signifikanten Verlängerung
EU-Kommission erteilt Zulassung für IRESSA
 Erste personalisierte Therapie von Lungenkrebs EU-Kommission erteilt Zulassung für IRESSA Frankfurt am Main (1.Juli 2009) - Die Europäische Kommission hat für das Krebsmedikament IRESSA (Gefitinib) die
Erste personalisierte Therapie von Lungenkrebs EU-Kommission erteilt Zulassung für IRESSA Frankfurt am Main (1.Juli 2009) - Die Europäische Kommission hat für das Krebsmedikament IRESSA (Gefitinib) die
Celgene GmbH Joseph-Wild-Straße München. Telefon: (089) PRESSEMITTEILUNG
 Celgene GmbH Joseph-Wild-Straße 20 81829 München Telefon: (089) 451519-010 info@celgene.de www.celgene.de PRESSEMITTEILUNG Zweiter AMNOG-Prozess für Orphan Drug IMNOVID (Pomalidomid) innerhalb der gesetzlichen
Celgene GmbH Joseph-Wild-Straße 20 81829 München Telefon: (089) 451519-010 info@celgene.de www.celgene.de PRESSEMITTEILUNG Zweiter AMNOG-Prozess für Orphan Drug IMNOVID (Pomalidomid) innerhalb der gesetzlichen
Herausforderungen in der individualisierten Therapie beim mcrc
 Erstlinientherapie des kolorektalen Karzinoms Herausforderungen in der individualisierten Therapie beim mcrc Berlin (2. Oktober 2010) Beim metastasierten kolorektalen Karzinom (mcrca) mit nicht-mutiertem
Erstlinientherapie des kolorektalen Karzinoms Herausforderungen in der individualisierten Therapie beim mcrc Berlin (2. Oktober 2010) Beim metastasierten kolorektalen Karzinom (mcrca) mit nicht-mutiertem
Immunogenität von Biosimilars
 www.pei.de Immunogenität von Biosimilars The views presented here are my own and do not necessarily reflect the views of the EMA or its committees and working parties. Jan Müller-Berghaus Überblick Was
www.pei.de Immunogenität von Biosimilars The views presented here are my own and do not necessarily reflect the views of the EMA or its committees and working parties. Jan Müller-Berghaus Überblick Was
Zirkulierende Tumorzellen (CTC) beim metastasierten Mammakarzinom
 Zirkulierende Tumorzellen (CTC) beim metastasierten Mammakarzinom Bahriye Aktas Universitätsfrauenklinik Essen Direktor: Prof. Dr. med. Rainer Kimmig Das Mammakarzinom- eine systemische Erkrankung! METASTASENBILDUNG
Zirkulierende Tumorzellen (CTC) beim metastasierten Mammakarzinom Bahriye Aktas Universitätsfrauenklinik Essen Direktor: Prof. Dr. med. Rainer Kimmig Das Mammakarzinom- eine systemische Erkrankung! METASTASENBILDUNG
Beschluss. im Alter von 5 Jahren und älter)
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Adjuvante zytostatische und zielgerichtete Therapien
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Version 2002: Möbus / Nitz Versionen
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Version 2002: Möbus / Nitz Versionen
EBM als Rationierungsprinzip. Medizinische Klinik III CBF und Charité Comprehensive Cancer Center Berlin
 EBM als Rationierungsprinzip????? UlihKilhl Ulrich Keilholz Medizinische Klinik III CBF und Charité Comprehensive Cancer Center Berlin Wie schaffe ich Bedingungen, die den Einsatz von Medikamenten und
EBM als Rationierungsprinzip????? UlihKilhl Ulrich Keilholz Medizinische Klinik III CBF und Charité Comprehensive Cancer Center Berlin Wie schaffe ich Bedingungen, die den Einsatz von Medikamenten und
Individuelle Therapieentscheidungen im Brustzentrum - zwischen Erfahrung und Laboranalyse -
 Individuelle Therapieentscheidungen im Brustzentrum - zwischen Erfahrung und Laboranalyse - Franz Edler von Koch Klinikum Dritter Orden Klinik für Gynäkologie und Geburtshilfe Brustzentrum Gynäkologisches
Individuelle Therapieentscheidungen im Brustzentrum - zwischen Erfahrung und Laboranalyse - Franz Edler von Koch Klinikum Dritter Orden Klinik für Gynäkologie und Geburtshilfe Brustzentrum Gynäkologisches
27. November 2012: Biosimilars: Ähnlich, aber eben doch nicht gleich
 Gladkova Svetlana Sarah Borowski / PIXELIO www.pixelio.de 27. November 2012: Biosimilars: Ähnlich, aber eben doch nicht gleich Dr. Sabine Sydow, Leiterin vfa bio Biotechnologie und Gentechnik eine Einführung
Gladkova Svetlana Sarah Borowski / PIXELIO www.pixelio.de 27. November 2012: Biosimilars: Ähnlich, aber eben doch nicht gleich Dr. Sabine Sydow, Leiterin vfa bio Biotechnologie und Gentechnik eine Einführung
Mammakarzinom - Zulassungsstatus von Medikamenten Leitlinie
 Mammakarzinom - Zulassungsstatus von Medikamenten Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft
Mammakarzinom - Zulassungsstatus von Medikamenten Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft
Vielversprechende Studiendaten zum Anti-PD-L1-Antikörper Atezolizumab
 ASCO-Jahrestagung 2016 Vielversprechende Studiendaten zum Anti-PD-L1-Antikörper Atezolizumab Hamburg (22. Juni 2016) - Die Krebsimmuntherapie war auf der 52. Jahrestagung der American Society of Clinical
ASCO-Jahrestagung 2016 Vielversprechende Studiendaten zum Anti-PD-L1-Antikörper Atezolizumab Hamburg (22. Juni 2016) - Die Krebsimmuntherapie war auf der 52. Jahrestagung der American Society of Clinical
Chemotherapie mit oder ohne zielgerichtete Substanzen beim
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Chemotherapie mit oder ohne zielgerichtete Substanzen beim metastasierten Mammakarzinom Chemotherapie mit oder ohne zielgerichtete Substanzen
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Chemotherapie mit oder ohne zielgerichtete Substanzen beim metastasierten Mammakarzinom Chemotherapie mit oder ohne zielgerichtete Substanzen
Medienmitteilung. Beschleunigtes FDA-Zulassungsverfahren für Perjeta von Roche zur Anwendung vor Operation bei frühem HER2-positivem Brustkrebs
 Medienmitteilung Basel, den 02. Juli 2013 Beschleunigtes FDA-Zulassungsverfahren für Perjeta von Roche zur Anwendung vor Operation bei frühem HER2-positivem Brustkrebs Zulassungsgesuch wird durch neues
Medienmitteilung Basel, den 02. Juli 2013 Beschleunigtes FDA-Zulassungsverfahren für Perjeta von Roche zur Anwendung vor Operation bei frühem HER2-positivem Brustkrebs Zulassungsgesuch wird durch neues
Endokrine und zielgerichtete Therapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2014.1D Endokrine und zielgerichtete Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten
Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2014.1D Endokrine und zielgerichtete Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten
Kolorektales Karzinom
 ASCO - Highlights Kolorektales Karzinom Henning Schulze-Bergkamen Nationales Centrum für Tumorerkrankungen (NCT) Abt. für Medizinische Onkologie Universitätsklinik Heidelberg ASCO Highlights Kolorektale
ASCO - Highlights Kolorektales Karzinom Henning Schulze-Bergkamen Nationales Centrum für Tumorerkrankungen (NCT) Abt. für Medizinische Onkologie Universitätsklinik Heidelberg ASCO Highlights Kolorektale
Zulassung von Arzneimitteln. Klinische Untersuchungen. Katalin Müllner
 Zulassung von Arzneimitteln. Klinische Untersuchungen Katalin Müllner Arzneimittel In gesetzlicher Definition sind Arzneimittel Stoffe oder Zubereitungen aus Stoffen, die vom Hersteller, der sie in den
Zulassung von Arzneimitteln. Klinische Untersuchungen Katalin Müllner Arzneimittel In gesetzlicher Definition sind Arzneimittel Stoffe oder Zubereitungen aus Stoffen, die vom Hersteller, der sie in den
Dossierbewertung A14-01 Version 1.0 Trastuzumab Emtansin Nutzenbewertung gemäß 35a SGB V
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Trastuzumab Emtansin gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Trastuzumab Emtansin gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf
Der Kampf gegen Krebs in Afrika. Maturin Tchoumi, Geschäftsführer Roche South Africa
 Der Kampf gegen Krebs in Afrika Maturin Tchoumi, Geschäftsführer Roche South Africa Eine stille Krise in afrikanischen Ländern unterhalb der Sahara Weltweit sterben in Entwicklungsländern mehr Menschen
Der Kampf gegen Krebs in Afrika Maturin Tchoumi, Geschäftsführer Roche South Africa Eine stille Krise in afrikanischen Ländern unterhalb der Sahara Weltweit sterben in Entwicklungsländern mehr Menschen
Personalisierte Medizin
 Personalisierte Medizin Möglichkeiten und Grenzen Prof. Dr. Friedemann Horn Universität Leipzig, Institut für Klinische Immunologie, Molekulare Immunologie Fraunhofer Institut für Zelltherapie und Immunologie
Personalisierte Medizin Möglichkeiten und Grenzen Prof. Dr. Friedemann Horn Universität Leipzig, Institut für Klinische Immunologie, Molekulare Immunologie Fraunhofer Institut für Zelltherapie und Immunologie
DGHO-Kongress Stuttgart,
 Klinische Praxisdaten zur pathologisch kompletten Remissionsrate und patientenberichteten Lebensqualität, nach neoadjuvanter Behandlung mit Pertuzumab, Trastuzumab und wöchentlichem Paclitaxel nach Anthrazyklinhaltiger
Klinische Praxisdaten zur pathologisch kompletten Remissionsrate und patientenberichteten Lebensqualität, nach neoadjuvanter Behandlung mit Pertuzumab, Trastuzumab und wöchentlichem Paclitaxel nach Anthrazyklinhaltiger
Jahrestagung der DGHO, OeGHO, SGMO und SGH 2017
 Der Einfluss von Zweit- und Drittliniengenerationen-TKI auf das Gesamtüberleben und das Progressionsfreie Überleben bei EGFR mutierten und ALK positiven Patienten: Ergebnisse des Lungennetzwerkes NOWEL
Der Einfluss von Zweit- und Drittliniengenerationen-TKI auf das Gesamtüberleben und das Progressionsfreie Überleben bei EGFR mutierten und ALK positiven Patienten: Ergebnisse des Lungennetzwerkes NOWEL
Sunitinib und Temsirolimus voll ausschöpfen
 Metastasiertes Nierenzellkarzinom (mrcc) Therapiemanagement beim mrcc: Potenziale von Sunitinib und Temsirolimus voll ausschöpfen Hannover (2. Mai 2011) Auf Basis überzeugender Phase-III-Zulassungsdaten
Metastasiertes Nierenzellkarzinom (mrcc) Therapiemanagement beim mrcc: Potenziale von Sunitinib und Temsirolimus voll ausschöpfen Hannover (2. Mai 2011) Auf Basis überzeugender Phase-III-Zulassungsdaten
Gelingt die tumorbiologische Subtypisierung bei Patientinnen mit primärem Mammakarzinom in der klinischen Routine?
 Gelingt die tumorbiologische Subtypisierung bei Patientinnen mit primärem Mammakarzinom in der klinischen Routine? Daten aus einem klinischen Krebsregister Elisabeth C. Inwald, Regensburg Offenlegung potentieller
Gelingt die tumorbiologische Subtypisierung bei Patientinnen mit primärem Mammakarzinom in der klinischen Routine? Daten aus einem klinischen Krebsregister Elisabeth C. Inwald, Regensburg Offenlegung potentieller
Kongress-Highlights Gynäkologische
 Kongress-Highlights Gynäkologische Onkologie vom ASCO 2017 Dr. med. Stefanie Zschäbitz Nationales Centrum für Tumorerkrankungen (NCT) Universitäts-Klinikum Heidelberg Post-ASCO am NCT Heidelberg, 28. Juni
Kongress-Highlights Gynäkologische Onkologie vom ASCO 2017 Dr. med. Stefanie Zschäbitz Nationales Centrum für Tumorerkrankungen (NCT) Universitäts-Klinikum Heidelberg Post-ASCO am NCT Heidelberg, 28. Juni
Psychoonkologie und Supportivtherapie
 Psychoonkologie und Supportivtherapie Rudolf Weide Praxisklinik für Hämatologie und Onkologie Koblenz PSO+SUPP: Metastasiertes Mammakarzinom Metastasiertes Mammakarzinom: Therapie versus BSC! 57 rumänische
Psychoonkologie und Supportivtherapie Rudolf Weide Praxisklinik für Hämatologie und Onkologie Koblenz PSO+SUPP: Metastasiertes Mammakarzinom Metastasiertes Mammakarzinom: Therapie versus BSC! 57 rumänische
BfArM im Dialog: Biosimilars 27. Juni 2016
 BfArM im Dialog: Biosimilars 27. Juni 216 Apothekerin Dr. Antje Behring Abteilung Arzneimittel des G-BA Inhaltsverzeichnis Marktzugang Regulierung und Erstattung von Biosimilars in Deutschland Frühe Nutzenbewertung
BfArM im Dialog: Biosimilars 27. Juni 216 Apothekerin Dr. Antje Behring Abteilung Arzneimittel des G-BA Inhaltsverzeichnis Marktzugang Regulierung und Erstattung von Biosimilars in Deutschland Frühe Nutzenbewertung
Roche-Medikament Perjeta verlängert das Leben von Patientinnen mit einer aggressiven Form von metas
 Roche-Medikament Perjeta verlängert das Leben von Patientinnen mit einer aggressiven Form von metas Roche-Medikament Perjeta verlängert das Leben von Patientinnen mit einer aggressiven Form von metastasierendem
Roche-Medikament Perjeta verlängert das Leben von Patientinnen mit einer aggressiven Form von metas Roche-Medikament Perjeta verlängert das Leben von Patientinnen mit einer aggressiven Form von metastasierendem
Haben Sie externe Hilfestellungen in Anspruch genommen? Wenn ja, bitte geben Sie an, welche Hilfestellung Sie in Anspruch genommen haben?
 Haben Sie externe Hilfestellungen in Anspruch genommen? Wenn ja, bitte geben Sie an, welche Hilfestellung Sie in Anspruch genommen haben? 1.1 Angefragte Untersuchungs- und Behandlungsmethode (Kurzbezeichnung
Haben Sie externe Hilfestellungen in Anspruch genommen? Wenn ja, bitte geben Sie an, welche Hilfestellung Sie in Anspruch genommen haben? 1.1 Angefragte Untersuchungs- und Behandlungsmethode (Kurzbezeichnung
Medizin und Krebsimmuntherapie
 Aktuelles vom Amerikanischen Krebskongress 2017 Roche präsentiert neue Daten zur personalisierten Medizin und Krebsimmuntherapie Düsseldorf (14. Juni 2017) - Fast 200 Abstracts zu 20 unterschiedlichen
Aktuelles vom Amerikanischen Krebskongress 2017 Roche präsentiert neue Daten zur personalisierten Medizin und Krebsimmuntherapie Düsseldorf (14. Juni 2017) - Fast 200 Abstracts zu 20 unterschiedlichen
