CML-V: Deutsche Prüfplanzusammenfassung
|
|
|
- Sigrid Hafner
- vor 8 Jahren
- Abrufe
Transkript
1 CML-V: Deutsche Prüfplanzusammenfassung Studientitel Behandlungsoptimierung bei neu diagnostizierten Ph- und/oder BCR-ABL-positiven Patienten mit chronischer myeloischer Leukämie (CML) in chronischer Phase mit Nilotinib- vs. Nilotinib plus Interferon alpha-induktion und Nilotinib- oder Interferon alpha-erhaltungsphase. TIGER-Studie. Ziele Primäre Ziele 1. Bewertung der Rate der guten molekularen Remission (Major Molecular Response, MMR) im Studienmonat 18 unter Nilotinib-Monotherapie im Vergleich zu der Kombinationstherapie mit Nilotinib und PEG-Interferon α2b. 2. Beurteilung des Anteils der Patienten in stabiler MMR nach Absetzen von Nilotinib und PEG-Interferon α2b. Sekundäre Ziele 1. Komplette zytogenetische Ansprechrate (CCyR) und MMR nach 12, 18 und 24 en 2. Dauer bis zum Erreichen von CCyR, MMR, MR 4 und MR 4,5 3. Rate der MR 4 und MR 4,5 während der Erhaltungstherapie und nach Absetzen der Medikation 4. Beurteilung des progressionsfreien Überlebens (Progression-Free Survival, PFS) und des Gesamt-Überlebens (Overall Survival, OS) zum Studienmonat 12, 24 und Vergleich des Anteils der Patienten ohne Therapie für mindestens 6 e 60 e nach Therapiestart in beiden Therapiearmen 6. Bewertung des Sicherheits- und Verträglichkeitsprofils von Nilotinib im Vergleich zu Nilotinib+PEG-IFN und PEG-IFN 7. Bewertung der Therapietreue der Patienten bei Nilotinib-basierten Therapien 8. Bewertung der Lebensqualität während der Induktionstherapie mit Nilotinib gegenüber der Induktion mit Nilotinib+PEG-IFN sowie während der Erhaltungstherapie mit Nilotinib im Vergleich zur Erhaltungstherapie mit PEG-IFN 9. Bewertung pharmakoökonomischer Aspekte der Behandlungsstrategien Prüfdesign Offene, multizentrische, randomisierte, Parallelgruppen-Studie mit neudiagnostizierten CML- Patienten in der chronischen Phase. Pilotphase (max. 24 Patienten) Die Studie startet mit einer sogenannten Pilotphase, um die optimale Dosierung der Kombination von Nilotinib mit Interferon zu finden. In die Pilotphase werden maximal 24 Patienten einbezogen. Anfänglich starten sechs Patienten nach 6-wöchiger Monotherapie mit Tyrosinkinaseinhibitoren mit der Kombinationstherapie: 2 x 300 mg Nilotinib täglich in Kombination mit einer Injektion (30 μg) pegyliertem Interferon alpha (PegIntron ) pro Woche. Sollte unter Version
2 dieser Dosierung bei 2 oder mehr Pateinten Nebenwirkungen Grad 3 oder 4 auftreten, werden 6 weitere Patienten untersucht. Falls diese Kohorte gut vertragen wird, wird die PEG-IFN Dosis in einer zweiten Kohorte auf 50 μg/woche gesteigert. Sollte die Dosierung der ersten Kohorte nicht vertragen werden, erfolgt bei 6 weiteren Patienten die Gabe von PEG-IFN in einer Dosierung von 30 μg alle 2 Wochen. Hauptphase Mindestens 628 erwachsene Patienten mit Ph und/oder BCR-ABL positiver CML in der chronischen Phase (CML-CP) sollen an 150 Zentren eingeschlossen werden. Eine Vorbehandlung mit Hydroxyurea und maximal sechswöchige Behandlung mit Imatinib oder Nilotinib ist zulässig. Patienten werden im Verhältnis 1:1 in die Behandlungsarme Nilotinib und Nilotinib + IFN randomisiert und für die Studiendauer von bis zu 5 Jahren behandelt. Die Randomisierung wird anhand des EUTOS-Scores stratifiziert. Nach bestätigter MMR, frühestens 24 e nach Behandlungsbeginn, wird die Erhaltungstherapie begonnen (Nilotinib-Monotherapie wird fortgeführt, bei der Kombinationstherapie wird Nilotinib abgesetzt). Die Patienten werden während der Erhaltungstherapie weiter beobachtet, um die Dauer der MMR und der MR 4 -Rate zu erfassen. Nach stabiler MR 4 für mindestens 12 e (d.h. gesamte Behandlungsdauer mindestens 36 e) wird die Beendigung der medikamentösen Behandlung gestattet und die rückfallfreie Zeit (ohne Verlust der MMR) der Patienten ohne Behandlung wird untersucht. Patienten, die gemäß ELN-Kriterien als Therapieversager gelten und die klinische Prüfung abbrechen müssen, sollten mit Dasatinib behandelt oder entsprechend der aktuellen Empfehlungen für eine allogene Stammzell-Transplantation in Erwägung gezogen werden. Patienten mit Nilotinib-Unverträglichkeit sollten mit Imatinib behandelt werden. Patienten, bei denen ein Therapieversagen während der IFN-Monotherapie auftritt (PCR- Anstieg >1% BCR-ABL), werden wieder mit der Kombinationstherapie Nilotinib+IFN behandelt. Version
3 >24 Mo. Therapie bestätigte MMR >36 Mo. Therapie >12 Mo. MR 4 Nilotinib 2x300 mg weiter Nilotinib --- R Nilotinib 2x300 mg + PEG-IFNα2b PEG-IFNα2b --- Nilotinib Intoleranz -> Imatinib Nilotinib-Resistenz -> Transplantation/Dasatinib empfohlen Suboptimales Ansprechen: -> Nilotinib 2x400mg Induktion Erhaltung Heilung? Abbildung 1: Prüfdesign Population: Die Prüfpopulation setzt sich aus erwachsenen männlichen und weiblichen Patienten mit neudiagnostizierter Ph und/oder BCR-ABL positiver chronischer myeloischer Leukämie in der chronischen Phase zusammen. Die Diagnosestellung muss innerhalb der letzten 6 e erfolgt sein und die Patienten dürfen bisher keine Behandlung erhalten haben (außer 6 e Hydroxyurea und max. 6 Wochen Imatinib oder Nilotinib). Insgesamt sollen 628 Patenten rekrutiert werden. Einschlusskriterien: Patienten müssen alle Einschlusskriterien innerhalb von 2 Wochen vor Baseline erfüllen. (Knochenmarkuntersuchungen können innerhalb von 12 Wochen vor Baseline durchgeführt werden.) Männliche oder weibliche Patienten mit diagnostizierter CML-CP und zytogenetischer Bestätigung des Ph-Chromosoms [t(9;22) Translokation]; CML-CP ist definiert als: - < 15 % Blasten im peripheren Blut und Knochenmark; - < 30 % Blasten plus Promyelozyten im peripheren Blut und Knochenmark; - < 20 % Basophile im peripheren Blut; 100/nl Blutplättchen; ECOG-Leistungsstatus 2. Version
4 Kein Nachweis einer extramedullären leukämischen Infiltration, mit Ausnahme einer Hepatosplenomegalie. Ph-negative Patienten mit Translokationsvarianten, die in der Multiplex-PCR positiv für BCR-ABL sind, können ebenfalls eingeschlossen werden. Vorbehandlung mit Hydroxyurea bis zu 6 en und Imatinib oder Nilotinib für max. 6 Wochen ist zulässig. Alter 18 Jahre Kalium, Magnesium und Kalzium LLN (lower limit of normal) im Serum; oder Korrektur in den Normbereich mittels oraler Medikation. ASAT und ALAT 2,5x ULN (upper limit of normal) oder 5,0x ULN, falls Leukämie bedingt. Alkalische Phosphatase 2,5x ULN, außer Leukämie bedingt Gesamt-Bilirubin 1,5x ULN, außer bei bekanntem Meulengracht-Syndrom Lipase und Amylase im Serum 1,5x ULN Serum-Kreatinin 2x ULN Unterschriebene Patienteninformation und Einwilligungserklärung vor Durchführung jeglicher studienbezogener Maßnahmen. Ausschlusskriterien Patienten, auf die eines der folgenden Kriterien zutrifft, können nicht in die klinische Prüfung eingeschlossen werden: Bekannte Beeinträchtigung der Herzfunktion, einschließlich: - LVEF < 45 % - kongenitales Long-QT-Syndrom - Vorgeschichte/Vorliegen einer signifikanten ventrikulären oder atrialen Tachyarrhythmie Klinisch signifikante Bradykardie (Ruhepuls < 50 Schläge / Minute) QT c > 450 ms beim EKG im Screening. Falls vor der Gabe von Nilotinib QT c > 450 ms und Abweichung der Elektrolyte vom Normbereich, sollten zunächst die Elektrolyte korrigiert werden und dann eine erneute Überprüfung des QT c -Kriteriums erfolgen. Myokardinfarkt innerhalb von 12 en vor Beginn der Prüfbehandlung. Andere klinisch signifikante Herzerkrankung (z.b. instabile Angina pectoris, Herzdekompensation, unkontrollierter Bluthochdruck). Vorgeschichte einer akuten (d.h. innerhalb eines Jahres vor Beginn der Prüfbehandlung) oder chronischen Pankreatitis. Andere derzeitige unkontrollierte Krankheiten (z.b. unkontrollierter Diabetes mellitus, aktive oder unkontrollierte Infektionen, akute oder chronische Leber- oder Nierenerkrankungen), die zu einem inakzeptablen Sicherheitsrisiko führen können oder eine Prüfplankonforme Durchführung gefährden. Beeinträchtigte Magen-Darm-Funktion oder Erkrankung, die die Absorption der Prüfmedikation beeinträchtigt (z. B. Geschwür, unkontrollierte Übelkeit, Erbrechen und Durchfall, Malabsorptions-Syndrom, Dünndarm-Resektion oder Magen-Bypass). Einnahme von Medikamenten, die zu einer Verlängerung der QT-Zeit führen können Einnahme von Medikamenten, die bekanntermaßen zu einer starken Induktion oder Inhibition des CYP450-Isoenzyms CYP3A4 führen. Version
5 Patienten die sich innerhalb von 2 Wochen vor Beginn der Prüfmedikation einer größeren Operation unterzogen haben, oder die sich von den Auswirkungen einer solchen O- peration noch nicht erholt haben. Patientinnen die schwanger sind oder stillen, oder Frauen im gebärfähigen Alter, die keine effektive Methode der Empfängnisverhütung anwenden. (Für Frauen im gebärfähigen Alter muss ein negativer Serum-Schwangerschaftstest innerhalb von 14 Tagen vor Beginn der Prüfbehandlung vorliegen). Bei post-menopausalen Frauen muss Amenorrhoe seit mindestens 12 en vorliegen, damit Sie als nicht gebärfähig gelten. Männliche und weibliche Patienten müssen für die gesamte Dauer der Einnahme und bis 3 e nach Absetzen der Prüfmedikation damit einverstanden sein, eine effektive Methode zur Empfängnisverhütung anzuwenden. Bekannte Infektion mit dem humanen Immundefizienzvirus (HIV). Aktive Autoimmunerkrankung, einschliesslich Autoimmunhepatitis Patienten mit einer Vorgeschichte einer anderen primären malignen Erkrankung, die zur Zeit klinisch signifikant ist oder zur Zeit eine Behandlung erfordert. Patenten, die nicht bereit oder nicht in der Lage sind, den Anforderungen des Prüfplans Folge zu leisten Der Prüfarzt sollte sicherstellen, dass nur Patienten, die alle Einschluss- und keines der Ausschlusskriterien aufweisen, eine Teilnahme an der klinischen Prüfung angeboten wird. Version
6 Studien- und Referenztherapie: Referenztherapie: Nilotinib (300 mg zweimal täglich) Studientherapie: PEG-Interferon alpha (parallel und als aufeinanderfolgende Kombinationstherapie) Primäre Endpunkte: 1. MMR nach 18 (Nilotinib gegenüber Nilotinib + PEG-IFN). 2. Anteil kontinuierlicher MMR 12 und 24 e nach Absetzen von Nilotinib und PEG- Interferon ( Heilung ). Sekundäre Endpunkte: 1. Zytogenetische Ansprechrate (CCyR) und MMR nach 12, 18 und 24 en. 2. Dauer bis zum Erreichen von CCyR, MMR, MR 4 und MR 4,5. 3. Rate der MR 4 und MR 4,5 während der Erhaltungstherapie und nach Absetzen der Medikation. 4. Progressionsfreies- und Gesamtüberleben nach 12, 24 und 60 en. 5. Anteil der Patienten ohne Therapie für mindestens 6 e nach 60 en nach Therapiestart. 6. Verträglichkeit und Sicherheit von Nilotinib im Vergleich mit Nilotinib+PEG-IFN und PEG- IFN. 7. Compliance der Patienten bezüglich der Nilotinib-basierten Therapien. 8. Beurteilung der Lebensqualität während der verschiedenen Behandlungen. 9. Pharmakoökonomie der Therapiestrategien. Visiten- und Behandlungsschema Die geplanten Visiten und Untersuchungen sind in Tabelle 1 aufgeführt. Eine komplette Visite zum Studienende muss für jeden Patienten durchgeführt werden, der mit oder früher als 2 Jahre nach Studienstart abbricht. Alle Daten, die durch die in Tabelle 1 aufgeführten Untersuchungen gewonnen werden, müssen als Quelldaten in die Patientenakte eingetragen werden. Version
7 Tabelle 1 Visiten- und Behandlungsschema Screening- Periode bis Baseline (Tag -14 bis 0) Einwilligungserklärung X Ein-/Ausschlusskriterien, relevante medizinische Vorgeschichte, frühere Erkrankungen, X Demografie, frühere Behandlungen, ECOG- Leistungsstatus Tag 1 1 und 2 (1) 3 6 9, 15, 21 12, 18, 24 Während Erhaltungstherapie Sokal-, Euro- (Hasford) und EUTOS-Score zur X Diagnose Serum-Schwangerschaftstest, falls zutreffend X X X Vitalparameter, körperliche Untersuchung, X X X X X X X X X extramedulläre Blutbildung, Gewicht (10,11) EKG (2) X X X X X X Hämatologie (12), Blutchemie (3) X X X X X X X X X Beurteilung des Knochenmarks / Zytogenetik X (7) X X X X (4,7) Analyse des peripheren Bluts mittels BCR-ABL X X X X X X X qrt-pcr (5, 7) und Mutationsanalysen (6, 7) Nilotinib-Konzentration im Blutplasma (X) X X X X +Tag 2 (8) Überprüfung der Therapietreue (9) X X X X X X X Fragebogen zur Lebensqualität X X X X X Unerwünschte Ereignisse/ Begleitmedikation fortlaufend Nach Absetzen (1) Ein entspricht einem Kalendermonat. Patientenvisiten innerhalb des ersten s der klinischen Prüfung sollten am vorbestimmten Tag (mit einem Visitenfenster von 2 Tagen) oder so nah wie möglich daran komplett abgeschlossen werden. Dies trifft für alle nachfolgenden Patientenvisiten ebenfalls zu (zulässiges Visitenfenster 14d). (2) Nach manuell gelesener EKG-Beurteilung: keine Prüfmedikamente für Patienten mit im Durchschnitt QTcF > 480 ms. (3) Detaillierte Parameter der Blutuntersuchungen sind im Prüfprotokoll (8.8.6, 8.8.7, 8.8.8) zu finden. (4) Zytogenetische Standarduntersuchung des Knochenmarks (nicht FISH) muss innerhalb von 8 Wochen vor dem Einschluss abgeschlossen sein. Knochenmarkaspirationen und/oder -Biopsien für die zytogenetischen Analysen werden zur Baseline, nach 3 en und dann alle 6 e durchgeführt, bis eine MMR erreicht wird. (5) Screening-Periode: Abnahme von 10 ml peripherem Blut für PCR. Anschließend alle 3 e bis zu 2 Jahre nach Studienstart: Abnahme von 20 ml peripherem Blut. Falls ein 5-facher Anstieg der BCR-ABL-Transkripte vorliegt (bezogen auf den geringsten Wert in der Studie) werden die Ergebnisse durch eine Wiederholung bestätigt: zweite Analyse der gleichen Probe und einer weiteren Probe innerhalb von 4 6 Wochen (ungeplante Visite) Version
8 (6) Mutationsanalysen im peripheren Blut (Prüfprotokoll 8.7.2). Eine Probe für Mutationsanalysen wird zur Baseline entnommen und nur bei Patienten analysiert, die im weiteren Verlauf kein oder ein abnehmendes Ansprechen zeigen. Falls Patienten kein oder ein abnehmendes Ansprechen zeigen, werden die Mutationsanalysen mit einer Probe durchgeführt, die zu diesem Zeitpunkt entnommen worden ist. Kontinuierliche Mutationsanalysen können nach einem Rückfall bei Bedarf alle 3 e durchgeführt werden. (7) Im Falle eines verlorenen Ansprechens muss eine Studienvisite innerhalb von 4 6 Wochen durchgeführt werden. Falls nötig wird eine ungeplante Visite durchgeführt. Eine körperliche Untersuchung einschließlich der Beurteilung extramedullärer Blutbildung, Gewicht, Vitalparameter (einschließlich Puls, Blutdruck und Körpertemperatur) und Blutuntersuchungen werden durchgeführt. Blutproben für PCR, Mutationsanalysen werden ebenfalls genommen. Falls erforderlich, findet auch eine Knochenmarkentnahme zur Bestätigung der zytogenetischen Remission statt. (8) Nicht verpflichtend (9) Der Überlebensstatus jedes Patienten wird nach Studienabbruch alle 3 e dokumentert. (10) Neuropsychiatrische Symptome müssen während der ersten 8 Therapiewochen mit PEG-IFN 3-wöchentlich kontrolliert werden. (11) Bei Patienten mit präexistenter Retinopathie soll zum Studienstart oder bei Visusänderungen eine Augenuntersuchung durchgeführt werden. (12) In den ersten 2 en der Therapie sollte alle 14 Tage, danach monatlich bzw. nach klinischer Notwendigkeit eines kleines Blutbild mit Hämoglobin, Leukozytenzahl und Thrombozytenzahl angefertigt werden. Version
9 Datenanalyse: Die Berechnung der notwendigen Patientenzahl stützt sich auf die Annahme, dass sich die beiden Behandlungsgruppen bezüglich der primären Variable MMR an 18 um 12 % unterscheiden (Nilotinib 60% vs. Nilotinib+IFN 72%). Um diesen Unterschied auf einem Siginifikanzniveau von 0,025 und mit einer Teststärke von 80 % detektieren zu können (unkorrigierter zweiseitiger Chi-Quadrat-Test), benötigt man in beiden Gruppen 295 Patienten. Aus Daten der CML-IV-Studie geht hervor, dass frühe allogene Stammzell-Transplantationen bei 3 4% der Patienten durchgeführt werden. Ausgehend von einem Patientenanteil von 4 % ohne Verlaufskontrolle und von 2% mit atypischen BCR-ABL-Transkripten ist eine Randomisierung von insgesamt 628 Patienten ausreichend. Wenn man eine Rekrutierungsrate von 200 Patienten / Jahr ausgeht, wird ein Rekrutierungszeitraum von 3 Jahren benötigt. Es besteht die Annahme, dass letztendlich 80% aller Patienten nach 18-monatiger oder längerer Behandlung eine MMR erreichen. Nach Erreichen dieses Remissionsstatus wird im Nilotinib-Monotherapiearm die Erhaltungstherapie fortgeführt, während im Kombinationsarm die Erhaltungstherapie nur noch aus IFN besteht (Nilotinib wird abgesetzt). Die molekularen Rückfallraten (>1% BCR-ABL) werden im Nilotinib-Monotherapiearm auf 5% und im IFN- Monotherapiearm auf 15 % geschätzt. Es wird erwartet, dass etwa 30% aller Patienten mit einer MMR zumindest über 1 Jahr eine bestätigte MR 4 haben und dass diese Patienten zwischen den beiden Behandlungsarmen etwa gleich verteilt sind. Diese 30% aller Patienten mit MMR sind für den zweiten primären Endpunkt geeignet: die stabile Remissionsrate nach Absetzen jeglicher Therapie. Bei mindestens 590 auswertbaren Patienten für das erste Ziel und 472 Patienten mit MMR stehen etwa 150 Patienten für die Analyse des zweiten Ziels zur Verfügung, 75 Patienten pro Arm. Es wird im früheren Nilotinib-Monotherapiearm eine molekulare Rückfallrate von 30% angenommen. Damit ist es möglich, einen statistisch signifikanten Unterschied (α = 0,025, unkorrigierter zweiseitiger Chi-Quadrat-Test) mit einer Teststärke von 80% im Hinblick auf den früheren IFN- Monotherapiearm zu detektieren, wenn die molekularen Rückfälle später zwischen 10% und 54% liegen. Alle Analysen sind Intent-to-treat -Analysen. Ethische Betrachtungen: Patienten werden erst nach einer schriftlichen Einverständniserklärung rekrutiert. Das Prüfprotokoll wird durch die verantwortliche Ethik-Kommission des Sponsors im Benehmen mit den Kommissionen aller teilnehmenden Institutionen beurteilt. Das Studiendesign zeigt einen hohen ethischen Anspruch es wird eine funktionelle Heilung von CML-Patienten nach einer Nilotinib- und IFN-Therapie angestrebt. Das Risiko der Studienteilnahme ist minimal. Jeder bevorstehende molekulare Rückfall nach Behandlungsunterbrechung wird durch regelmäßige RT-PCR-Analysen entdeckt und es wird ein Neustart der Nilotinib-Therapie durchgeführt, was in praktisch allen Fällen zu einem Ansprechen führt (Mahon et al., 2010; Burchert et al., 2010). Version
Chronisch myeloproliferative Syndrome - CML-V TIGER
 Innere Medizin I - Onkologie, Hämatologie, Klinische Infektiologie, Klinische Immunologie, Hämostaseologie, Internistische Intensivmedizin Chronisch myeloproliferative Syndrome - CML-V TIGER Prüfplancode
Innere Medizin I - Onkologie, Hämatologie, Klinische Infektiologie, Klinische Immunologie, Hämostaseologie, Internistische Intensivmedizin Chronisch myeloproliferative Syndrome - CML-V TIGER Prüfplancode
CML V Prof. Dr. med. G. Baerlocher
 Klinikdirektorin und Chefärztin Prof.Dr.med. Anne Angelillo- Scherrer AGEK Arbeitsgemeinschaft der Schweizerischen Forschungs-Ethikkommissionen für klinische Versuche Communauté de travail des Commissions
Klinikdirektorin und Chefärztin Prof.Dr.med. Anne Angelillo- Scherrer AGEK Arbeitsgemeinschaft der Schweizerischen Forschungs-Ethikkommissionen für klinische Versuche Communauté de travail des Commissions
Ziele der Hepatitis C-Therapie
 Behandlung der Hepatitis C Zur Behandlung der Hepatitis C stehen heute neben pegyliertem Interferon alfa (PEG-INF) und Ribavirin auch Proteaseinhibitoren (direkt antiviral wirksame Substanzen) zur Verfügung.
Behandlung der Hepatitis C Zur Behandlung der Hepatitis C stehen heute neben pegyliertem Interferon alfa (PEG-INF) und Ribavirin auch Proteaseinhibitoren (direkt antiviral wirksame Substanzen) zur Verfügung.
Ausfüllanleitung. zum indikationsspezifischen Datensatz. für das strukturierte Behandlungsprogramm KHK
 Ausfüllanleitung zum indikationsspezifischen Datensatz für das strukturierte Behandlungsprogramm KHK Stand der letzten Bearbeitung: 10-11-2014 Version 4.1 Anamnese- und Befunddaten Angina pectoris Bitte
Ausfüllanleitung zum indikationsspezifischen Datensatz für das strukturierte Behandlungsprogramm KHK Stand der letzten Bearbeitung: 10-11-2014 Version 4.1 Anamnese- und Befunddaten Angina pectoris Bitte
WAS finde ich WO im Beipackzettel
 WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
Richtlinie. des Gemeinsamen Bundesausschusses. zur Umsetzung der Regelungen in 62 für schwerwiegend chronisch Erkrankte ( Chroniker-Richtlinie )
 Richtlinie des Gemeinsamen Bundesausschusses zur Umsetzung der Regelungen in 62 für schwerwiegend chronisch Erkrankte ( Chroniker-Richtlinie ) in der Fassung vom 22. Januar 2004 veröffentlicht im Bundesanzeiger
Richtlinie des Gemeinsamen Bundesausschusses zur Umsetzung der Regelungen in 62 für schwerwiegend chronisch Erkrankte ( Chroniker-Richtlinie ) in der Fassung vom 22. Januar 2004 veröffentlicht im Bundesanzeiger
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen
 Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Patienteninformationsbroschüre Valproat
 Patienteninformationsbroschüre Valproat Informationen für Patientinnen Die Informationen in dieser Broschüre sind für Frauen bestimmt, denen Valproat verschrieben wird und die schwanger werden können (Frauen
Patienteninformationsbroschüre Valproat Informationen für Patientinnen Die Informationen in dieser Broschüre sind für Frauen bestimmt, denen Valproat verschrieben wird und die schwanger werden können (Frauen
Fragen und Antworten zur hämatopoetischen Stammzelle
 Fragen und Antworten zur hämatopoetischen Stammzelle Grundlagen, Indikationen, therapeutischer Nutzen von Rainer Haas, Ralf Kronenwett 1. Auflage Fragen und Antworten zur hämatopoetischen Stammzelle Haas
Fragen und Antworten zur hämatopoetischen Stammzelle Grundlagen, Indikationen, therapeutischer Nutzen von Rainer Haas, Ralf Kronenwett 1. Auflage Fragen und Antworten zur hämatopoetischen Stammzelle Haas
Diese Broschüre fasst die wichtigsten Informationen zusammen, damit Sie einen Entscheid treffen können.
 Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Fragebogen Kopfschmerzen
 Fragebogen Kopfschmerzen Fragen an Dich Fragen an Dich Fragen an die Eltern Bei diesen Fragen geht es um Deine Kopfschmerzen. Es wäre schön, wenn Du darüber etwas sagst. Deine Antworten helfen, für Deine
Fragebogen Kopfschmerzen Fragen an Dich Fragen an Dich Fragen an die Eltern Bei diesen Fragen geht es um Deine Kopfschmerzen. Es wäre schön, wenn Du darüber etwas sagst. Deine Antworten helfen, für Deine
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Legalon SIL - Trockensubstanz zur Infusionsbereitung
 PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Legalon SIL - Trockensubstanz zur Infusionsbereitung Wirkstoff: Silibinin-C-2,3-bis(hydrogensuccinat), Dinatriumsalz Lesen Sie die gesamte
PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Legalon SIL - Trockensubstanz zur Infusionsbereitung Wirkstoff: Silibinin-C-2,3-bis(hydrogensuccinat), Dinatriumsalz Lesen Sie die gesamte
PRÜFMODUL D UND CD. 1 Zweck. 2 Durchführung. 2.1 Allgemeines. 2.2 Antrag
 1 Zweck PRÜFMODUL D UND CD Diese Anweisung dient als Basis für unsere Kunden zur Information des Ablaufes der folgenden EG-Prüfung nach folgenden Prüfmodulen: D CD Es beschreibt die Aufgabe der benannten
1 Zweck PRÜFMODUL D UND CD Diese Anweisung dient als Basis für unsere Kunden zur Information des Ablaufes der folgenden EG-Prüfung nach folgenden Prüfmodulen: D CD Es beschreibt die Aufgabe der benannten
07.072. Forschung am Menschen. Verfassungsbestimmung ARGUMENTARIEN CONTRA
 07.072 Forschung am Menschen. Verfassungsbestimmung ARGUMENTARIEN CONTRA Verfassungsartikel über die Forschung am Menschen Art. 118b Hauptkritikpunkt: Abs 2,Bst c «Fremdnützige Forschung an urteilsunfähigen
07.072 Forschung am Menschen. Verfassungsbestimmung ARGUMENTARIEN CONTRA Verfassungsartikel über die Forschung am Menschen Art. 118b Hauptkritikpunkt: Abs 2,Bst c «Fremdnützige Forschung an urteilsunfähigen
Wenn Sie möchten, können Sie den Bogen auch anonym ausfüllen und an folgende Adresse senden:
 Der folgende Fragebogen ist bezogen auf das Krankheitsbild Netzhautablösung / Netzhautabspaltung sowie Riss- oder Lochbildung in der NH. Falls Sie noch keine NHA hatten, sondern nur Risse oder Löcher in
Der folgende Fragebogen ist bezogen auf das Krankheitsbild Netzhautablösung / Netzhautabspaltung sowie Riss- oder Lochbildung in der NH. Falls Sie noch keine NHA hatten, sondern nur Risse oder Löcher in
Minimale Resterkrankung, Hochdurchsatz-Sequenzierung und Prognose beim multiplen Myelom
 Minimale Resterkrankung, Hochdurchsatz-Sequenzierung und Prognose beim multiplen Myelom Von Navneet Ramesh und Maike Haehle, übersetzt von Sabine Schock Vom 8. Apr 2014 7:41 Uhr; aktualisiert am 8. Apr
Minimale Resterkrankung, Hochdurchsatz-Sequenzierung und Prognose beim multiplen Myelom Von Navneet Ramesh und Maike Haehle, übersetzt von Sabine Schock Vom 8. Apr 2014 7:41 Uhr; aktualisiert am 8. Apr
Änderung der ISO/IEC 17025 Anpassung an ISO 9001: 2000
 Änderung der ISO/IEC 17025 Anpassung an ISO 9001: 2000 Dr. Martin Czaske Sitzung der DKD-FA HF & Optik, GS & NF am 11. bzw. 13. Mai 2004 Änderung der ISO/IEC 17025 Anpassung der ISO/IEC 17025 an ISO 9001:
Änderung der ISO/IEC 17025 Anpassung an ISO 9001: 2000 Dr. Martin Czaske Sitzung der DKD-FA HF & Optik, GS & NF am 11. bzw. 13. Mai 2004 Änderung der ISO/IEC 17025 Anpassung der ISO/IEC 17025 an ISO 9001:
Screening Das Programm. zur Früherkennung von Brustkrebs
 Mammographie Screening Das Programm zur Früherkennung von Brustkrebs das Mammographie Screening Programm Wenn Sie zwischen 50 und 69 Jahre alt sind, haben Sie alle zwei Jahre Anspruch auf eine Mammographie-Untersuchung
Mammographie Screening Das Programm zur Früherkennung von Brustkrebs das Mammographie Screening Programm Wenn Sie zwischen 50 und 69 Jahre alt sind, haben Sie alle zwei Jahre Anspruch auf eine Mammographie-Untersuchung
!!! Folgeerkrankungen
 Ein zu hoher Blutzuckerspiegel kann Folgen auf Ihr Herzkreislaufsystem haben und zu Erkrankungen wie der Schaufensterkrankheit, einer Angina pectoris, einem Herzinfarkt oder einem Schlaganfall führen.
Ein zu hoher Blutzuckerspiegel kann Folgen auf Ihr Herzkreislaufsystem haben und zu Erkrankungen wie der Schaufensterkrankheit, einer Angina pectoris, einem Herzinfarkt oder einem Schlaganfall führen.
Sandoz Pharmaceuticals AG
 Die Pille danach. Was ist eine Notfallverhütung oder die sogenannte «Pille danach»? 1 Wann wird NorLevo Uno eingenommen? 2 Bei der «Pille danach» handelt es sich um eine Notfallverhütung, die eine unerwünschte
Die Pille danach. Was ist eine Notfallverhütung oder die sogenannte «Pille danach»? 1 Wann wird NorLevo Uno eingenommen? 2 Bei der «Pille danach» handelt es sich um eine Notfallverhütung, die eine unerwünschte
Besser leben mit Gicht. Seite 3 Seite 4 Seite 5 Seite 6. Zu starke Schweißbildung. besser natürlich behandeln. Gicht-Telegramm
 Besser leben mit Gicht GT II-2014 Seite 3 Seite 4 Seite 5 Seite 6 Purinrechner jetzt auf i-phone und Android Warnung vor dem Einsatz von NSAR wie Diclofenac Zu starke Schweißbildung besser natürlich behandeln
Besser leben mit Gicht GT II-2014 Seite 3 Seite 4 Seite 5 Seite 6 Purinrechner jetzt auf i-phone und Android Warnung vor dem Einsatz von NSAR wie Diclofenac Zu starke Schweißbildung besser natürlich behandeln
geben. Die Wahrscheinlichkeit von 100% ist hier demnach nur der Gehen wir einmal davon aus, dass die von uns angenommenen
 geben. Die Wahrscheinlichkeit von 100% ist hier demnach nur der Vollständigkeit halber aufgeführt. Gehen wir einmal davon aus, dass die von uns angenommenen 70% im Beispiel exakt berechnet sind. Was würde
geben. Die Wahrscheinlichkeit von 100% ist hier demnach nur der Vollständigkeit halber aufgeführt. Gehen wir einmal davon aus, dass die von uns angenommenen 70% im Beispiel exakt berechnet sind. Was würde
Patientenleitfaden für das Gespräch mit dem Arzt. Liebe Patientin, lieber Patient!
 Patientenleitfaden für das Gespräch mit dem Arzt Liebe Patientin, lieber Patient! Je besser Sie sich auf das Gespräch mit Ihrem Arzt vorbereiten, desto leichter wird es für sie/ihn sein, eine Diagnose
Patientenleitfaden für das Gespräch mit dem Arzt Liebe Patientin, lieber Patient! Je besser Sie sich auf das Gespräch mit Ihrem Arzt vorbereiten, desto leichter wird es für sie/ihn sein, eine Diagnose
Diabetes mellitus : Folgeschäden
 Diabetes mellitus : Folgeschäden Warum ist der Diabetes mellitus eine wichtige Erkrankung? a. Akute Probleme: Hypoglykämie Hyperglykämie Ketoazidose b. Chronische Probleme: Folgeschäden: Typische Schäden:
Diabetes mellitus : Folgeschäden Warum ist der Diabetes mellitus eine wichtige Erkrankung? a. Akute Probleme: Hypoglykämie Hyperglykämie Ketoazidose b. Chronische Probleme: Folgeschäden: Typische Schäden:
Cytomegalie & Co. Häufige Virusinfektionen in der Schwangerschaft. Deutsches Grünes Kreuz e.v.
 Cytomegalie & Co Häufige Virusinfektionen in der Schwangerschaft Schwangerschaft Eine ganz besondere Zeit der Vorfreude Verantwortung Sorge Die werdenden Eltern möchten alles richtig machen für das Wohl
Cytomegalie & Co Häufige Virusinfektionen in der Schwangerschaft Schwangerschaft Eine ganz besondere Zeit der Vorfreude Verantwortung Sorge Die werdenden Eltern möchten alles richtig machen für das Wohl
Bevölkerung mit Migrationshintergrund an der Gesamtbevölkerung 2012
 Statistische Übersicht inkl. dem Vergleich zwischen und zur (Aus-)Bildungssituation von jungen Menschen mit und ohne Migrationshintergrund 1 in den Bundesländern nach dem Mikrozensus Erstellt im Rahmen
Statistische Übersicht inkl. dem Vergleich zwischen und zur (Aus-)Bildungssituation von jungen Menschen mit und ohne Migrationshintergrund 1 in den Bundesländern nach dem Mikrozensus Erstellt im Rahmen
Künstlicher Hüftgelenksersatz
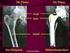 Künstlicher Hüftgelenksersatz Künstlicher Hüftgelenksersatz Was ist eine Hüftgelenk-Arthrose? Das Hüftgelenk ist eine bewegliche Verbindung zwischen dem Becken- und dem Oberschenkelknochen. Die am Gelenk
Künstlicher Hüftgelenksersatz Künstlicher Hüftgelenksersatz Was ist eine Hüftgelenk-Arthrose? Das Hüftgelenk ist eine bewegliche Verbindung zwischen dem Becken- und dem Oberschenkelknochen. Die am Gelenk
Diabetes. Zulassungserweiterung: Levemir (Insulin detemir) als Add-on Therapie zu Victoza (Liraglutid) bei Mens
 Zulassungserweiterung Levemir (Insulin detemir) als Add-on Therapie zu Victoza (Liraglutid) bei Menschen mit Typ 2 Diabetes Mainz (16. November 2011) Die Europäische Kommission hat die Zulassung des modernen
Zulassungserweiterung Levemir (Insulin detemir) als Add-on Therapie zu Victoza (Liraglutid) bei Menschen mit Typ 2 Diabetes Mainz (16. November 2011) Die Europäische Kommission hat die Zulassung des modernen
Indikationserweiterungen für JANUVIA (Sitagliptin, MSD) in der EU - Kombination mit Sulfonylharnstoff n
 Indikationserweiterungen für JANUVIA (Sitagliptin, MSD) in der EU Kombination mit Sulfonylharnstoff nun ebenfalls zugelassen Haar (März 2008) - Die europäische Arzneimittelbehörde EMEA hat JANUVIA für
Indikationserweiterungen für JANUVIA (Sitagliptin, MSD) in der EU Kombination mit Sulfonylharnstoff nun ebenfalls zugelassen Haar (März 2008) - Die europäische Arzneimittelbehörde EMEA hat JANUVIA für
3.9 Brustdrüse der Frau
 ICD-10 C50 Ergebnisse zur 77 3.9 Brustdrüse der Frau Kernaussagen Inzidenz und Mortalität: Die altersstandardisierte Inzidenz von Krebserkrankungen der weiblichen Brustdrüse (Mammakarzinom) ist seit den
ICD-10 C50 Ergebnisse zur 77 3.9 Brustdrüse der Frau Kernaussagen Inzidenz und Mortalität: Die altersstandardisierte Inzidenz von Krebserkrankungen der weiblichen Brustdrüse (Mammakarzinom) ist seit den
Informationen zum Thema Europäische Krankenversicherungskarte
 Gesundheitskarte AKTUELL Informationen zum Thema Europäische Krankenversicherungskarte Von Anfang an ist die Rückseite der elektronischen Gesundheitskarte für die Aufnahme der Europäischen Krankenversicherungskarte
Gesundheitskarte AKTUELL Informationen zum Thema Europäische Krankenversicherungskarte Von Anfang an ist die Rückseite der elektronischen Gesundheitskarte für die Aufnahme der Europäischen Krankenversicherungskarte
WEGWEISER ZUR EINLAGERUNG VON NABELSCHNURBLUT UND -GEWEBE
 WEGWEISER ZUR EINLAGERUNG VON NABELSCHNURBLUT UND -GEWEBE Nabelschnurblut ist wertvoll! Wenn sich Eltern dafür entscheiden, das Nabelschnurblut ihres Kindes aufzubewahren, können sie damit dem Kind selbst,
WEGWEISER ZUR EINLAGERUNG VON NABELSCHNURBLUT UND -GEWEBE Nabelschnurblut ist wertvoll! Wenn sich Eltern dafür entscheiden, das Nabelschnurblut ihres Kindes aufzubewahren, können sie damit dem Kind selbst,
Wie erleben Verbraucher IGeL? Ergebnisse einer Umfrage der Verbraucherzentralen
 Wie erleben Verbraucher IGeL? Ergebnisse einer Umfrage der Verbraucherzentralen Sperrfrist: 15.10.2012, 10 Uhr Berlin, 11.10.2012 Was sind IGeL? Individuelle Gesundheits-Leistungen (IGeL) sind medizinische
Wie erleben Verbraucher IGeL? Ergebnisse einer Umfrage der Verbraucherzentralen Sperrfrist: 15.10.2012, 10 Uhr Berlin, 11.10.2012 Was sind IGeL? Individuelle Gesundheits-Leistungen (IGeL) sind medizinische
KinderPlus. Mit KinderPlus wird Ihr Kind zum Privatpatienten im Krankenhaus.
 KinderPlus. Mit KinderPlus wird Ihr Kind zum Privatpatienten im Krankenhaus. Hubi, Junior und unsere Kunden empfehlen die Württembergische Krankenversicherung AG. Für Kinder bis 7 Jahre: Günstig in die
KinderPlus. Mit KinderPlus wird Ihr Kind zum Privatpatienten im Krankenhaus. Hubi, Junior und unsere Kunden empfehlen die Württembergische Krankenversicherung AG. Für Kinder bis 7 Jahre: Günstig in die
Scheper Ziekenhuis Emmen. Tel.: + 31 (0) 591-691 320 Fax: + 31 (0) 591-691 321 Web: www.plastici.nl
 Scheper Ziekenhuis Emmen Tel.: + 31 (0) 591-691 320 Fax: + 31 (0) 591-691 321 Web: www.plastici.nl PREISE Wir bieten Ihnen Brustvergrößerungen von 3000,- bis 5.500,- Euro an. ALLGEMEINE INFORMATIONEN Die
Scheper Ziekenhuis Emmen Tel.: + 31 (0) 591-691 320 Fax: + 31 (0) 591-691 321 Web: www.plastici.nl PREISE Wir bieten Ihnen Brustvergrößerungen von 3000,- bis 5.500,- Euro an. ALLGEMEINE INFORMATIONEN Die
Medizinische Rehabilitation bei Epilepsie
 Fachkliniken Wangen Medizinische Klinik Thoraxchirurgische Klinik Anästhesie und Intensivmedizin Neurologische Klinik Kinderklinik Rehabilitationskinderklinik www.fachkliniken-wangen.de Medizinische Rehabilitation
Fachkliniken Wangen Medizinische Klinik Thoraxchirurgische Klinik Anästhesie und Intensivmedizin Neurologische Klinik Kinderklinik Rehabilitationskinderklinik www.fachkliniken-wangen.de Medizinische Rehabilitation
Monitoring-Service Anleitung
 Anleitung 1. Monitoring in CrefoDirect Wie kann Monitoring über CrefoDirect bestellt werden? Bestellung von Monitoring beim Auskunftsabruf Beim Auskunftsabruf kann das Monitoring direkt mitbestellt werden.
Anleitung 1. Monitoring in CrefoDirect Wie kann Monitoring über CrefoDirect bestellt werden? Bestellung von Monitoring beim Auskunftsabruf Beim Auskunftsabruf kann das Monitoring direkt mitbestellt werden.
Wir sind für Sie da. Unser Gesundheitsangebot: Unterstützung im Umgang mit Ihrer Depression
 Wir sind für Sie da Unser Gesundheitsangebot: Unterstützung im Umgang mit Ihrer Depression Wir nehmen uns Zeit für Sie und helfen Ihnen Depressionen lassen sich heute meist gut behandeln. Häufig ist es
Wir sind für Sie da Unser Gesundheitsangebot: Unterstützung im Umgang mit Ihrer Depression Wir nehmen uns Zeit für Sie und helfen Ihnen Depressionen lassen sich heute meist gut behandeln. Häufig ist es
Hautkrebsscreening. 49 Prozent meinen, Hautkrebs sei kein Thema, das sie besorgt. Thema Hautkrebs. Ist Hautkrebs für Sie ein Thema, das Sie besorgt?
 Hautkrebsscreening Datenbasis: 1.004 gesetzlich Krankenversicherte ab 1 Jahren Erhebungszeitraum:. bis 4. April 01 statistische Fehlertoleranz: +/- Prozentpunkte Auftraggeber: DDG Hautkrebs ist ein Thema,
Hautkrebsscreening Datenbasis: 1.004 gesetzlich Krankenversicherte ab 1 Jahren Erhebungszeitraum:. bis 4. April 01 statistische Fehlertoleranz: +/- Prozentpunkte Auftraggeber: DDG Hautkrebs ist ein Thema,
Zweigbibliothek Medizin
 Sächsische Landesbibliothek - Staats- und Universitätsbibliothek Dresden (SLUB) Zweigbibliothek Medizin Diese Dissertation finden Sie original in Printform zur Ausleihe in der Zweigbibliothek Medizin Nähere
Sächsische Landesbibliothek - Staats- und Universitätsbibliothek Dresden (SLUB) Zweigbibliothek Medizin Diese Dissertation finden Sie original in Printform zur Ausleihe in der Zweigbibliothek Medizin Nähere
Vertrag zwischen. der AOK Berlin - Die Gesundheitskasse - und der Kassenärztlichen Vereinigung Berlin (KV)
 Vertrag zwischen der AOK Berlin - Die Gesundheitskasse - und der Kassenärztlichen Vereinigung Berlin (KV) über die Abgrenzung, Vergütung und Abrechnung der stationären vertragsärztlichen Tätigkeit 1) Dem
Vertrag zwischen der AOK Berlin - Die Gesundheitskasse - und der Kassenärztlichen Vereinigung Berlin (KV) über die Abgrenzung, Vergütung und Abrechnung der stationären vertragsärztlichen Tätigkeit 1) Dem
Anwenderdokumentation Prüfung nach dem Heilmittelkatalog
 Ausgabe August 2008 Anwenderdokumentation Prüfung nach dem Heilmittelkatalog 1 Einleitung... 2 2 Stammdateneinstellungen... 3 2.1 Zuordnung der Heilmittel... 3 3 Prüfung einer Verordnung... 7 3.1 Vorgehensweise
Ausgabe August 2008 Anwenderdokumentation Prüfung nach dem Heilmittelkatalog 1 Einleitung... 2 2 Stammdateneinstellungen... 3 2.1 Zuordnung der Heilmittel... 3 3 Prüfung einer Verordnung... 7 3.1 Vorgehensweise
Kundenregistrierung am egeodata Austria Portal
 Kundenregistrierung am egeodata Austria Portal Dieses Tutorial soll zeigen, wie sich ein neuer Kunde am egeodata Austria Portal registriert. Die Registrierung ist erforderlich, um fortgeschrittene oder
Kundenregistrierung am egeodata Austria Portal Dieses Tutorial soll zeigen, wie sich ein neuer Kunde am egeodata Austria Portal registriert. Die Registrierung ist erforderlich, um fortgeschrittene oder
1.1 Allgemeines. innerhalb der Nachtzeit (19:00 24:00) Gesamte Normalarbeitszeit (16:00 19:00)
 Abschnitt 1 Überstunden in der Nacht 11 1.1 Allgemeines # Die Ermittlung und Abrechnung von Überstunden unter der Woche, an Sonn- und Feiertagen wurde bereits im Band I, Abschnitt 3 behandelt. Sehen wir
Abschnitt 1 Überstunden in der Nacht 11 1.1 Allgemeines # Die Ermittlung und Abrechnung von Überstunden unter der Woche, an Sonn- und Feiertagen wurde bereits im Band I, Abschnitt 3 behandelt. Sehen wir
Fallstricke in der HIV-Diagnostik. Elisabeth Puchhammer-Stöckl Department für Virologie Medizinische Universität Wien
 Fallstricke in der HIV-Diagnostik Elisabeth Puchhammer-Stöckl Department für Virologie Medizinische Universität Wien HIV-Infektion: Diagnostik- Zeitverlauf Nach Pilcher et al, 2004 HIV-Infektion: Diagnostik-
Fallstricke in der HIV-Diagnostik Elisabeth Puchhammer-Stöckl Department für Virologie Medizinische Universität Wien HIV-Infektion: Diagnostik- Zeitverlauf Nach Pilcher et al, 2004 HIV-Infektion: Diagnostik-
Schritt für Schritt zur Krankenstandsstatistik
 Schritt für Schritt zur Krankenstandsstatistik Eine Anleitung zur Nutzung der Excel-Tabellen zur Erhebung des Krankenstands. Entwickelt durch: Kooperationsprojekt Arbeitsschutz in der ambulanten Pflege
Schritt für Schritt zur Krankenstandsstatistik Eine Anleitung zur Nutzung der Excel-Tabellen zur Erhebung des Krankenstands. Entwickelt durch: Kooperationsprojekt Arbeitsschutz in der ambulanten Pflege
Fragebogen zur Anforderungsanalyse
 Fragebogen zur Anforderungsanalyse Geschäftsprozess Datum Mitarbeiter www.seikumu.de Fragebogen zur Anforderungsanalyse Seite 6 Hinweise zur Durchführung der Anforderungsanalyse Bevor Sie beginnen, hier
Fragebogen zur Anforderungsanalyse Geschäftsprozess Datum Mitarbeiter www.seikumu.de Fragebogen zur Anforderungsanalyse Seite 6 Hinweise zur Durchführung der Anforderungsanalyse Bevor Sie beginnen, hier
Einleitende Bemerkungen
 Einleitende Bemerkungen EU-FORMBLATT LENKFREIE TAGE / KONTROLLGERÄT MANUELLER NACHTRAG ENTSCHEIDUNGSHILFE FÜR FAHRPERSONAL VON VERORDNUNGS-FAHRZEUGEN 1 BEI TÄTIGKEITEN IM INNERSTAATLICHEN VERKEHR Zur Frage,
Einleitende Bemerkungen EU-FORMBLATT LENKFREIE TAGE / KONTROLLGERÄT MANUELLER NACHTRAG ENTSCHEIDUNGSHILFE FÜR FAHRPERSONAL VON VERORDNUNGS-FAHRZEUGEN 1 BEI TÄTIGKEITEN IM INNERSTAATLICHEN VERKEHR Zur Frage,
Zeichen bei Zahlen entschlüsseln
 Zeichen bei Zahlen entschlüsseln In diesem Kapitel... Verwendung des Zahlenstrahls Absolut richtige Bestimmung von absoluten Werten Operationen bei Zahlen mit Vorzeichen: Addieren, Subtrahieren, Multiplizieren
Zeichen bei Zahlen entschlüsseln In diesem Kapitel... Verwendung des Zahlenstrahls Absolut richtige Bestimmung von absoluten Werten Operationen bei Zahlen mit Vorzeichen: Addieren, Subtrahieren, Multiplizieren
Für Patientinnen und Patienten. Blutdruckpass. Die mit dem Regenbogen
 Für Patientinnen und Patienten Blutdruckpass Die mit dem Regenbogen Patientendaten Vorname Name Geburtsdatum Adresse Strasse Hausnummer PLZ Stadt Tel. Nr. Allergien Medikamentenunverträglichkeit Andere
Für Patientinnen und Patienten Blutdruckpass Die mit dem Regenbogen Patientendaten Vorname Name Geburtsdatum Adresse Strasse Hausnummer PLZ Stadt Tel. Nr. Allergien Medikamentenunverträglichkeit Andere
Trockenes Auge. Haben Sie Trockene Augen?
 Trockenes Auge Jeder 3 bis 5 Patient, der den Augenarzt besucht, an der Krankheit Trockenes Auge leidet. Ein Trockenes Auge entsteht, wenn der Körper zu wenig Tränenflüssigkeit produziert oder die Zusammensetzung
Trockenes Auge Jeder 3 bis 5 Patient, der den Augenarzt besucht, an der Krankheit Trockenes Auge leidet. Ein Trockenes Auge entsteht, wenn der Körper zu wenig Tränenflüssigkeit produziert oder die Zusammensetzung
Behandlung und Beratung von Alkoholabhängigen
 Behandlung und Beratung von Alkoholabhängigen KURZBERICHT NR.1/2011 DEUTSCHE SUCHTHILFESTATISTIK 2009 1 Jutta Künzel Martin Steppan Tim Pfeiffer-Gerschel München, Mai 2011 IFT Institut für Therapieforschung,
Behandlung und Beratung von Alkoholabhängigen KURZBERICHT NR.1/2011 DEUTSCHE SUCHTHILFESTATISTIK 2009 1 Jutta Künzel Martin Steppan Tim Pfeiffer-Gerschel München, Mai 2011 IFT Institut für Therapieforschung,
Datenübernahme von HKO 5.9 zur. Advolux Kanzleisoftware
 Datenübernahme von HKO 5.9 zur Advolux Kanzleisoftware Die Datenübernahme (DÜ) von HKO 5.9 zu Advolux Kanzleisoftware ist aufgrund der von Update zu Update veränderten Datenbank (DB)-Strukturen in HKO
Datenübernahme von HKO 5.9 zur Advolux Kanzleisoftware Die Datenübernahme (DÜ) von HKO 5.9 zu Advolux Kanzleisoftware ist aufgrund der von Update zu Update veränderten Datenbank (DB)-Strukturen in HKO
Seite 1 von 14. Cookie-Einstellungen verschiedener Browser
 Seite 1 von 14 Cookie-Einstellungen verschiedener Browser Cookie-Einstellungen verschiedener Browser, 7. Dezember 2015 Inhaltsverzeichnis 1.Aktivierung von Cookies... 3 2.Cookies... 3 2.1.Wofu r braucht
Seite 1 von 14 Cookie-Einstellungen verschiedener Browser Cookie-Einstellungen verschiedener Browser, 7. Dezember 2015 Inhaltsverzeichnis 1.Aktivierung von Cookies... 3 2.Cookies... 3 2.1.Wofu r braucht
Informationen zur Prüfung Geprüfter Handelsfachwirt (IHK)/Geprüfte Handelsfachwirtin (IHK)
 Informationen zur Prüfung Geprüfter Handelsfachwirt (IHK)/Geprüfte Handelsfachwirtin (IHK) Die Prüfung zum Geprüften Handelsfachwirt (IHK)/zur Geprüften Handelsfachwirtin (IHK) ist eine öffentlich-rechtliche
Informationen zur Prüfung Geprüfter Handelsfachwirt (IHK)/Geprüfte Handelsfachwirtin (IHK) Die Prüfung zum Geprüften Handelsfachwirt (IHK)/zur Geprüften Handelsfachwirtin (IHK) ist eine öffentlich-rechtliche
10 Antworten zum Thema Generika
 10 Antworten zum Thema Generika Die mit dem Regenbogen Liebe Leserin, Lieber Leser Immer mehr Schweizerinnen und Schweizer leiden unter den jährlich steigenden Gesundheitskosten und Krankenkassenprämien.
10 Antworten zum Thema Generika Die mit dem Regenbogen Liebe Leserin, Lieber Leser Immer mehr Schweizerinnen und Schweizer leiden unter den jährlich steigenden Gesundheitskosten und Krankenkassenprämien.
Intraoperative Strahlentherapie bei Brustkrebs
 Intraoperative Strahlentherapie bei Brustkrebs Uniklinik Köln 1 Kein Grund für Verzweiflung Wenn die Diagnose Brustkrebs festgestellt wird, ist erst einmal die Sorge groß. Beruhigend zu wissen, dass es
Intraoperative Strahlentherapie bei Brustkrebs Uniklinik Köln 1 Kein Grund für Verzweiflung Wenn die Diagnose Brustkrebs festgestellt wird, ist erst einmal die Sorge groß. Beruhigend zu wissen, dass es
Abituraufgabe zur Stochastik, Hessen 2009, Grundkurs (TR)
 Abituraufgabe zur Stochastik, Hessen 2009, Grundkurs (TR) Eine Firma stellt USB-Sticks her. Sie werden in der Fabrik ungeprüft in Packungen zu je 20 Stück verpackt und an Händler ausgeliefert. 1 Ein Händler
Abituraufgabe zur Stochastik, Hessen 2009, Grundkurs (TR) Eine Firma stellt USB-Sticks her. Sie werden in der Fabrik ungeprüft in Packungen zu je 20 Stück verpackt und an Händler ausgeliefert. 1 Ein Händler
Leichte-Sprache-Bilder
 Leichte-Sprache-Bilder Reinhild Kassing Information - So geht es 1. Bilder gucken 2. anmelden für Probe-Bilder 3. Bilder bestellen 4. Rechnung bezahlen 5. Bilder runterladen 6. neue Bilder vorschlagen
Leichte-Sprache-Bilder Reinhild Kassing Information - So geht es 1. Bilder gucken 2. anmelden für Probe-Bilder 3. Bilder bestellen 4. Rechnung bezahlen 5. Bilder runterladen 6. neue Bilder vorschlagen
Versetzungsregeln in Bayern
 Grundschule Schüler der Jahrgangsstufen 1 und 2 rücken ohne besondere Entscheidung vor. Das Vorrücken in den Jahrgangsstufen 3 und 4 soll nur dann versagt werden, wenn der Schüler in seiner Entwicklung
Grundschule Schüler der Jahrgangsstufen 1 und 2 rücken ohne besondere Entscheidung vor. Das Vorrücken in den Jahrgangsstufen 3 und 4 soll nur dann versagt werden, wenn der Schüler in seiner Entwicklung
EINKAUFSLEITLINIE FÜR FETT-, ZUCKER
 EINKAUFSLEITLINIE FÜR FETT-, ZUCKER UND SALZREDUZIERTE PRODUKTE INHALT Grundsatz...2 1. Ziele und Geltungsbereich...3 2. Betroffene Warengruppen...3 3. Gestaltung des Eigenmarkensortiments...4 4. Verantwortlichkeiten...5
EINKAUFSLEITLINIE FÜR FETT-, ZUCKER UND SALZREDUZIERTE PRODUKTE INHALT Grundsatz...2 1. Ziele und Geltungsbereich...3 2. Betroffene Warengruppen...3 3. Gestaltung des Eigenmarkensortiments...4 4. Verantwortlichkeiten...5
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Viscosan - Augentropfen Wirkstoff: Hypromellose
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Viscosan - Augentropfen Wirkstoff: Hypromellose Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Viscosan - Augentropfen Wirkstoff: Hypromellose Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
PATIENTENINFORMATION UND EINVERSTÄNDNISERKLÄRUNG
 PATIENTENINFORMATION UND EINVERSTÄNDNISERKLÄRUNG Prüfstelle: Prüfarzt: (Name) Tel.: Gegenüberstellung von Imatinib (400mg täglich) und Nilotinib (2x 300mg täglich) bei Patienten mit chronischer myeloischer
PATIENTENINFORMATION UND EINVERSTÄNDNISERKLÄRUNG Prüfstelle: Prüfarzt: (Name) Tel.: Gegenüberstellung von Imatinib (400mg täglich) und Nilotinib (2x 300mg täglich) bei Patienten mit chronischer myeloischer
Güte von Tests. die Wahrscheinlichkeit für den Fehler 2. Art bei der Testentscheidung, nämlich. falsch ist. Darauf haben wir bereits im Kapitel über
 Güte von s Grundlegendes zum Konzept der Güte Ableitung der Gütefunktion des Gauss im Einstichprobenproblem Grafische Darstellung der Gütefunktionen des Gauss im Einstichprobenproblem Ableitung der Gütefunktion
Güte von s Grundlegendes zum Konzept der Güte Ableitung der Gütefunktion des Gauss im Einstichprobenproblem Grafische Darstellung der Gütefunktionen des Gauss im Einstichprobenproblem Ableitung der Gütefunktion
Aufgabe 1 Berechne den Gesamtwiderstand dieses einfachen Netzwerkes. Lösung Innerhalb dieser Schaltung sind alle Widerstände in Reihe geschaltet.
 Widerstandsnetzwerke - Grundlagen Diese Aufgaben dienen zur Übung und Wiederholung. Versucht die Aufgaben selbständig zu lösen und verwendet die Lösungen nur zur Überprüfung eurer Ergebnisse oder wenn
Widerstandsnetzwerke - Grundlagen Diese Aufgaben dienen zur Übung und Wiederholung. Versucht die Aufgaben selbständig zu lösen und verwendet die Lösungen nur zur Überprüfung eurer Ergebnisse oder wenn
How to do? Projekte - Zeiterfassung
 How to do? Projekte - Zeiterfassung Stand: Version 4.0.1, 18.03.2009 1. EINLEITUNG...3 2. PROJEKTE UND STAMMDATEN...4 2.1 Projekte... 4 2.2 Projektmitarbeiter... 5 2.3 Tätigkeiten... 6 2.4 Unterprojekte...
How to do? Projekte - Zeiterfassung Stand: Version 4.0.1, 18.03.2009 1. EINLEITUNG...3 2. PROJEKTE UND STAMMDATEN...4 2.1 Projekte... 4 2.2 Projektmitarbeiter... 5 2.3 Tätigkeiten... 6 2.4 Unterprojekte...
Die Invaliden-Versicherung ändert sich
 Die Invaliden-Versicherung ändert sich 1 Erklärung Die Invaliden-Versicherung ist für invalide Personen. Invalid bedeutet: Eine Person kann einige Sachen nicht machen. Wegen einer Krankheit. Wegen einem
Die Invaliden-Versicherung ändert sich 1 Erklärung Die Invaliden-Versicherung ist für invalide Personen. Invalid bedeutet: Eine Person kann einige Sachen nicht machen. Wegen einer Krankheit. Wegen einem
Dow Jones am 13.06.08 im 1-min Chat
 Dow Jones am 13.06.08 im 1-min Chat Dieser Ausschnitt ist eine Formation: Wechselstäbe am unteren Bollinger Band mit Punkt d über dem 20-er GD nach 3 tieferen Hoch s. Wenn ich einen Ausbruch aus Wechselstäben
Dow Jones am 13.06.08 im 1-min Chat Dieser Ausschnitt ist eine Formation: Wechselstäbe am unteren Bollinger Band mit Punkt d über dem 20-er GD nach 3 tieferen Hoch s. Wenn ich einen Ausbruch aus Wechselstäben
Auslesen der Fahrtdaten wiederholen Schritt für Schritt erklärt (Funktion Abfrage zur Datensicherung erstellen )
 + twinline GmbH + Am Heidekrug 28 + D-16727 Velten Auslesen der Fahrtdaten wiederholen Schritt für Schritt erklärt (Funktion Abfrage zur Datensicherung erstellen ) Der gewöhnliche Auslesevorgang der aktuellen
+ twinline GmbH + Am Heidekrug 28 + D-16727 Velten Auslesen der Fahrtdaten wiederholen Schritt für Schritt erklärt (Funktion Abfrage zur Datensicherung erstellen ) Der gewöhnliche Auslesevorgang der aktuellen
IHR PATIENTENDOSSIER IHRE RECHTE
 IHR PATIENTENDOSSIER IHRE RECHTE Im Spital, in der Klinik bestimmen Sie, wie Sie über Ihre Krankheit und deren Behandlung informiert werden wollen und wer informiert werden darf Information Patientendossier
IHR PATIENTENDOSSIER IHRE RECHTE Im Spital, in der Klinik bestimmen Sie, wie Sie über Ihre Krankheit und deren Behandlung informiert werden wollen und wer informiert werden darf Information Patientendossier
Hinweise zum Ausfüllen der Zeiterfassung
 Hinweise zum Ausfüllen der Zeiterfassung Generelle Hinweise zu Excel Ab Version VSA 4.50 wird die dezimale Schreibweise für Zeiteingaben verwendet. Die Zeiterfassung, die Sie erhalten haben wurde für Excel
Hinweise zum Ausfüllen der Zeiterfassung Generelle Hinweise zu Excel Ab Version VSA 4.50 wird die dezimale Schreibweise für Zeiteingaben verwendet. Die Zeiterfassung, die Sie erhalten haben wurde für Excel
Wege zur Patientensicherheit - Fragebogen zum Lernzielkatalog für Kompetenzen in der Patientensicherheit
 Wege zur Patientensicherheit - Fragebogen zum Lernzielkatalog für Kompetenzen in der Patientensicherheit der Arbeitsgruppe Bildung und Training des Aktionsbündnis Patientensicherheit e. V. Seit Dezember
Wege zur Patientensicherheit - Fragebogen zum Lernzielkatalog für Kompetenzen in der Patientensicherheit der Arbeitsgruppe Bildung und Training des Aktionsbündnis Patientensicherheit e. V. Seit Dezember
Der Gesundheitskompass für die junge Frau
 Haarausfall? Blutentnahme zu Hormonlabor, Eisenwerte, Schilddrüsenwerte, Biotin und Zink 86,87 EURO Wiederholte Scheideninfektionen? Mit dem Vaginalstatus können Infektionen durch spezielle Kulturen auf
Haarausfall? Blutentnahme zu Hormonlabor, Eisenwerte, Schilddrüsenwerte, Biotin und Zink 86,87 EURO Wiederholte Scheideninfektionen? Mit dem Vaginalstatus können Infektionen durch spezielle Kulturen auf
Greater occipital nerve block using local anaesthetics alone or with triamcinolone for transformed migraine: a randomised comparative study
 Greater occipital nerve block using local anaesthetics alone or with triamcinolone for transformed migraine: a randomised comparative study A. Ashkenazi, R. Matro, J.W. Shaw, M.A. Abbas, S.D. Silberstein
Greater occipital nerve block using local anaesthetics alone or with triamcinolone for transformed migraine: a randomised comparative study A. Ashkenazi, R. Matro, J.W. Shaw, M.A. Abbas, S.D. Silberstein
EMIS - Langzeitmessung
 EMIS - Langzeitmessung Every Meter Is Smart (Jeder Zähler ist intelligent) Inhaltsverzeichnis Allgemeines 2 Bedienung 3 Anfangstand eingeben 4 Endstand eingeben 6 Berechnungen 7 Einstellungen 9 Tarife
EMIS - Langzeitmessung Every Meter Is Smart (Jeder Zähler ist intelligent) Inhaltsverzeichnis Allgemeines 2 Bedienung 3 Anfangstand eingeben 4 Endstand eingeben 6 Berechnungen 7 Einstellungen 9 Tarife
In diesem Tutorial lernen Sie, wie Sie einen Termin erfassen und verschiedene Einstellungen zu einem Termin vornehmen können.
 Tutorial: Wie erfasse ich einen Termin? In diesem Tutorial lernen Sie, wie Sie einen Termin erfassen und verschiedene Einstellungen zu einem Termin vornehmen können. Neben den allgemeinen Angaben zu einem
Tutorial: Wie erfasse ich einen Termin? In diesem Tutorial lernen Sie, wie Sie einen Termin erfassen und verschiedene Einstellungen zu einem Termin vornehmen können. Neben den allgemeinen Angaben zu einem
Der HIV-Antikörper-Schnelltest aus Sicht des Labormediziners. Dr. Thomas Berg, Berlin www.bergdoctor.de
 Der HIV-Antikörper-Schnelltest aus Sicht des Labormediziners Was untersucht der HIV-Antikörper- Schnelltest? (am Beispiel Vitest HIV) Der HIV-Antikörper-Schnelltest ist ein SUCHTEST, der untersucht, ob
Der HIV-Antikörper-Schnelltest aus Sicht des Labormediziners Was untersucht der HIV-Antikörper- Schnelltest? (am Beispiel Vitest HIV) Der HIV-Antikörper-Schnelltest ist ein SUCHTEST, der untersucht, ob
Osteoporose. Ein echtes Volksleiden. Schon jetzt zählen die Osteoporose und die damit verbundene erhöhte Brüchigkeit der Knochen
 Osteoporose Osteoporose 9 Osteoporose Ein echtes Volksleiden Schon jetzt zählen die Osteoporose und die damit verbundene erhöhte Brüchigkeit der Knochen in den entwickelten Ländern zu den häufigsten Erkrankungen
Osteoporose Osteoporose 9 Osteoporose Ein echtes Volksleiden Schon jetzt zählen die Osteoporose und die damit verbundene erhöhte Brüchigkeit der Knochen in den entwickelten Ländern zu den häufigsten Erkrankungen
Häufig wiederkehrende Fragen zur mündlichen Ergänzungsprüfung im Einzelnen:
 Mündliche Ergänzungsprüfung bei gewerblich-technischen und kaufmännischen Ausbildungsordnungen bis zum 31.12.2006 und für alle Ausbildungsordnungen ab 01.01.2007 Am 13. Dezember 2006 verabschiedete der
Mündliche Ergänzungsprüfung bei gewerblich-technischen und kaufmännischen Ausbildungsordnungen bis zum 31.12.2006 und für alle Ausbildungsordnungen ab 01.01.2007 Am 13. Dezember 2006 verabschiedete der
Wie unsere Augen Erfahren Sie, wie wir sehen, und wie Sie Ihre Vision zu schützen.
 Wie unsere Augen Erfahren Sie, wie wir sehen, und wie Sie Ihre Vision zu schützen. Levobunolol ist ein Beta-Blocker, der den Druck im Inneren des Auges reduziert. Levobunolol Augen (Auge) ist für die Behandlung
Wie unsere Augen Erfahren Sie, wie wir sehen, und wie Sie Ihre Vision zu schützen. Levobunolol ist ein Beta-Blocker, der den Druck im Inneren des Auges reduziert. Levobunolol Augen (Auge) ist für die Behandlung
Berechnung der Erhöhung der Durchschnittsprämien
 Wolfram Fischer Berechnung der Erhöhung der Durchschnittsprämien Oktober 2004 1 Zusammenfassung Zur Berechnung der Durchschnittsprämien wird das gesamte gemeldete Prämienvolumen Zusammenfassung durch die
Wolfram Fischer Berechnung der Erhöhung der Durchschnittsprämien Oktober 2004 1 Zusammenfassung Zur Berechnung der Durchschnittsprämien wird das gesamte gemeldete Prämienvolumen Zusammenfassung durch die
Das große ElterngeldPlus 1x1. Alles über das ElterngeldPlus. Wer kann ElterngeldPlus beantragen? ElterngeldPlus verstehen ein paar einleitende Fakten
 Das große x -4 Alles über das Wer kann beantragen? Generell kann jeder beantragen! Eltern (Mütter UND Väter), die schon während ihrer Elternzeit wieder in Teilzeit arbeiten möchten. Eltern, die während
Das große x -4 Alles über das Wer kann beantragen? Generell kann jeder beantragen! Eltern (Mütter UND Väter), die schon während ihrer Elternzeit wieder in Teilzeit arbeiten möchten. Eltern, die während
Profil A 49,3 48,2 50,7 50,9 49,8 48,7 49,6 50,1 Profil B 51,8 49,6 53,2 51,1 51,1 53,4 50,7 50 51,5 51,7 48,8
 1. Aufgabe: Eine Reifenfirma hat für Winterreifen unterschiedliche Profile entwickelt. Bei jeweils gleicher Geschwindigkeit und auch sonst gleichen Bedingungen wurden die Bremswirkungen gemessen. Die gemessenen
1. Aufgabe: Eine Reifenfirma hat für Winterreifen unterschiedliche Profile entwickelt. Bei jeweils gleicher Geschwindigkeit und auch sonst gleichen Bedingungen wurden die Bremswirkungen gemessen. Die gemessenen
Behandlung von Diabetes
 04 Arbeitsanweisung Arbeitsauftrag Anhand des Foliensatzes werden die verschiedenen Behandlungsmethoden bei Diabetes Typ 1 und Typ 2 besprochen. Anschliessend werden noch kurz die Folgen bei einer Nichtbehandlung
04 Arbeitsanweisung Arbeitsauftrag Anhand des Foliensatzes werden die verschiedenen Behandlungsmethoden bei Diabetes Typ 1 und Typ 2 besprochen. Anschliessend werden noch kurz die Folgen bei einer Nichtbehandlung
Das NEUE Leistungspaket der Sozialversicherung. Mehr Zahngesundheit für Kinder und Jugendliche bis zum 18. Lebensjahr. Fragen und Antworten
 Das NEUE Leistungspaket der Sozialversicherung Mehr Zahngesundheit für Kinder und Jugendliche bis zum 18. Lebensjahr Fragen und Antworten Stand: Juni 2015 1 Grundsatzfragen zum neuen Leistungspaket 1.1
Das NEUE Leistungspaket der Sozialversicherung Mehr Zahngesundheit für Kinder und Jugendliche bis zum 18. Lebensjahr Fragen und Antworten Stand: Juni 2015 1 Grundsatzfragen zum neuen Leistungspaket 1.1
allensbacher berichte
 allensbacher berichte Institut für Demoskopie Allensbach 2006 / Nr. 8 ALTERSVORSORGE THEMA NUMMER 1 Allensbach am Bodensee, Mitte Mai 2006. - Das Thema Altersvorsorge beschäftigt die Bevölkerung immer
allensbacher berichte Institut für Demoskopie Allensbach 2006 / Nr. 8 ALTERSVORSORGE THEMA NUMMER 1 Allensbach am Bodensee, Mitte Mai 2006. - Das Thema Altersvorsorge beschäftigt die Bevölkerung immer
Das Persönliche Budget in verständlicher Sprache
 Das Persönliche Budget in verständlicher Sprache Das Persönliche Budget mehr Selbstbestimmung, mehr Selbstständigkeit, mehr Selbstbewusstsein! Dieser Text soll den behinderten Menschen in Westfalen-Lippe,
Das Persönliche Budget in verständlicher Sprache Das Persönliche Budget mehr Selbstbestimmung, mehr Selbstständigkeit, mehr Selbstbewusstsein! Dieser Text soll den behinderten Menschen in Westfalen-Lippe,
Leitfaden zur Durchführung eines Jahreswechsels in BüroWARE 5.x
 Leitfaden zur Durchführung eines Jahreswechsels in BüroWARE 5.x Je nach BüroWARE Version kann sich das Menü des Datenbankassistenten von den Bildschirmausdrucken in unserem Leitfaden unterscheiden. Der
Leitfaden zur Durchführung eines Jahreswechsels in BüroWARE 5.x Je nach BüroWARE Version kann sich das Menü des Datenbankassistenten von den Bildschirmausdrucken in unserem Leitfaden unterscheiden. Der
Fernausbildung Fachberater/in für holistische Gesundheit. Modul 6
 Fernausbildung Fachberater/in für holistische Gesundheit Modul 6 Vorwort Liebe(r) Teilnehmer/in Herzlich willkommen in Modul 6 Mit dem 6. Modul beenden Sie nun Ihre Ausbildung, denn einmal muss schliesslich
Fernausbildung Fachberater/in für holistische Gesundheit Modul 6 Vorwort Liebe(r) Teilnehmer/in Herzlich willkommen in Modul 6 Mit dem 6. Modul beenden Sie nun Ihre Ausbildung, denn einmal muss schliesslich
Rentenarten in der gesetzlichen Rentenversicherung + VBL-Rente
 Rentenarten in der gesetzlichen Rentenversicherung + VBL-Rente Im April 2007 wurde das Gesetz zur Anpassung der Regelaltersgrenze an die demografische Entwicklung und zur Stärkung der Finanzierungsgrundlagen
Rentenarten in der gesetzlichen Rentenversicherung + VBL-Rente Im April 2007 wurde das Gesetz zur Anpassung der Regelaltersgrenze an die demografische Entwicklung und zur Stärkung der Finanzierungsgrundlagen
Tutorium Klinische Psychologie I. Fragen zur Ausbildung und rechtlichen Grundlagen in der Klinischen Psychologie
 Tutorium Klinische Psychologie I Fragen zur Ausbildung und rechtlichen Grundlagen in der Klinischen Psychologie Fragen zur Ausbildung und rechtlichen Grundlagen in der Klinischen Psychologie Oswald David
Tutorium Klinische Psychologie I Fragen zur Ausbildung und rechtlichen Grundlagen in der Klinischen Psychologie Fragen zur Ausbildung und rechtlichen Grundlagen in der Klinischen Psychologie Oswald David
Fruchtbarkeit ist messbar!
 Fruchtbarkeit ist messbar! I n d i v i d u e l l & a u s s a g e k r ä f t i g Bestimmung der individuellen Fruchtbarkeitsreserve Hätten Sie s so genau gewusst? Weibliche Fruchtbarkeit und Lebensalter
Fruchtbarkeit ist messbar! I n d i v i d u e l l & a u s s a g e k r ä f t i g Bestimmung der individuellen Fruchtbarkeitsreserve Hätten Sie s so genau gewusst? Weibliche Fruchtbarkeit und Lebensalter
Fragebogen Weisse Liste-Ärzte
 www.weisse-liste.de Fragebogen Weisse Liste-Ärzte Der Fragebogen ist Teil des Projekts Weisse Liste-Ärzte. DIMENSION: Praxis & Personal trifft voll und ganz zu trifft eher zu trifft eher trifft überhaupt
www.weisse-liste.de Fragebogen Weisse Liste-Ärzte Der Fragebogen ist Teil des Projekts Weisse Liste-Ärzte. DIMENSION: Praxis & Personal trifft voll und ganz zu trifft eher zu trifft eher trifft überhaupt
