Elektrolythaushalt + Säure-Basen-Haushalt
|
|
|
- Anna Frank
- vor 7 Jahren
- Abrufe
Transkript
1 Elektrolythaushalt + Säure-Basen-Haushalt
2 Überblick Elektrolythaushalt Natrium Kalium Calcium Magnesium Phosphat Säure-Basen-Haushalt
3 Der Elektrolythaushalt Normwerte: Natrium mmol/l Kalium mmol/l Calcium mmol/l (als freies Ion) Magnesium mmol/l (als freies Ion) Phosphat mmol/l (als anorg. Phosphat)
4 Der Natriumhaushalt Mechanismen der Natriumresorption in der Niere
5 Der Natriumhasuhalt Mechanismen der Na + -Resorption im Darm Isoformen: Darm: SGLT1 Prox. Tubulus : SGLT2 Isoformen: apikal: NHE2/NHE3 basolateral: NHE1
6 Der Natriumhaushalt Mechanismen der Na + -Resorption im Darm Isoformen: apikal: NHE2/NHE3 basolateral: NHE1 Isoform im Sammelrohr der Niere! Aldosteron fördert diese Art der Resorption!!!
7 Der Kaliumhaushalt Mechanismen der renalen Kaliumresorption und -sekretion Abb. aus: S. Silbernagl : Die Funktion der Nieren. In : R. Klinke, S. Silbernagl : Lehrbuch der Physiologie, 3. Auflage, Georg Thieme Verlag, Stuttgart - New York 2001, S. 315.
8 Der Kaliumhaushalt K + -Transportmechanismen im Darm Abhängig von der ENaC-vermittelten Na + -Resorption!
9 Der Kaliumhaushalt K + -Transportmechanismen im Darm Das Verhältnis der apikalen und basolateralen Leitfähigkeiten entscheidet, ob K + nach basolateral rezirkuliert oder sezerniert wird. Aldosteron steigert die apikale Leitfähigkeit! Diese Isoform der H/K- Pumpe wird durch Omeprazol nicht gehemmt!
10 Der Calciumhaushalt Überblick
11 Der Calciumhaushalt Regulation der Calcium-Phosphathomöostase
12 Der Calciumhaushalt Bildung von Calcitriol
13 Der Säre-Basen-Haushalt Bedeutung des ph-wertes Der ph-wert hat eine große Bedeutung für nahezu alle physiologischen Vorgänge: 1. Biochemische Reaktionen 2. Enzyme 3. Ionenkanäle 4. Andere Ionen: insb. K + und Ca Kontraktion von Skelett- und Herzmuskel 6. Bindung von O 2 und CO 2 im Blut
14 Chemische Grundlagen Definition von Säuren und Basen Definition nach Brønsted und Lowry: Stoffe, die Protonen abgeben können, werden als Protonendonatoren oder Säuren bezeichnet. Stoffe, die Protonen aufnehmen können, werden als Protonenakzeptoren oder Basen bezeichnet.
15 Chemische Grundlagen Definition des ph-wertes ph = - log [H + ] d.h. bei einem ph-wert von 7.0 beträgt die Protonenkonzentration 100 nmol/l. Bei einem ph-wert von 7.4 liegt die Protonenkonzentration bei 40 nmol/l.
16 Der Säre-Basen-Haushalt Protonenkonzentration und ph-werte im Körper Intrazellulär Cytosol 7.2 Lysosomen 5.5 Extrazellulär arterielles Blutplasma 7.4 Magensaft 1.0 Harn (niedrigster Wert) 4.5 Pankreassekret 8.0
17 Regulation des ph-wertes im Blut Normalbereich der Blutplasmawerte Normalbereich ph 7,37 7,43 Azidose: ph < 7,37 Alkalose: ph > 7,43 lebensbedrohlich: ph < 7,0 oder ph > 7,8
18 Chemische Grundlagen Definition von Säuren und Basen Starke Säuren (z.b. Salzsäure oder Schwefelsäure) dissoziieren in Wasser vollständig und geben alle Protonen ab. Schwache Säuren (z.b. Essigsäure, Milchsäure) dissoziieren je nach vorliegendem ph-wert in unterschiedlichem Ausmaß
19 Chemische Grundlagen Dissoziationsverhalten schwacher Säuren Für die Dissoziation schwacher Säuren gilt das Massenwirkungsgesetz: HA H + + A - K D = [H+ ] [A - ] HA Logarithmieren liefert die Henderson-Hasselbalch- Gleichung: ph = pk + log [A- ] HA
20 Chemische Grundlagen Dissoziationsverhalten einiger physiologisch wichtiger Säuren/Basen-Paare Abb. aus: P. Scheid: Säure-Basen-Gleichgewicht. In : Klinke, Pape, Silbernagl, Physiologie, 5. Auflage, Thieme Verlag Stuttgart 2005, S. 314.
21 Chemische Grundlagen Puffer Puffer sind Substanzen, die H + - oder OH - -Ionen binden oder abgeben und dadurch die ph-veränderungen bei Zugabe oder Verlust von H + - oder OH - -Ionen gering halten.
22 Chemische Grundlagen Definition der Pufferkapazität Ein Puffersystem hat eine bestimmte Pufferkapazität. Diese hängt ab von: der Gesamtkonzentration des Puffers der Abweichung des ph-wertes vom pk-wert des Puffers
23 Chemische Grundlagen Definition der Pufferkapazität Abb. aus: P. Scheid: Säure-Basen-Gleichgewicht. In : Klinke, Pape, Silbernagl, Physiologie, 5. Auflage, Thieme Verlag Stuttgart 2005, S. 313.
24 Puffersysteme des Blutes Übersicht Gesamtpufferbasen (Normalwert: 48 mmol/l) Bicarbonatpuffer (25.2 mmol/l) Bicarbonat (H 2 CO 3 /HCO 3 - ) pk s =6.1 Nichtbicarbonatpuffer (22 mmol/l) Phosphat (H 2 PO 4 - /HPO 4 2- ) pk s =6.8 Plasmaproteine Erythrocyten (insb. Hämoglobin) Basenüberschuss = Differenz aus aktueller Konzentration der Pufferbasen und dem Normalwert = ± 2 mmol/l
25 Puffersysteme des Blutes pk-werte von Aminosäure-Seitenketten Aminosäure frei im Protein Asp Glu His Cys Tyr Lys Arg 12.48
26 Puffersysteme des Blutes Pufferung des ph-wertes durch die Erythrocyten Abb. aus G. Thews : Atemgastransport und Säure-Basen-Status des Blutes. In : R.F. Schmidt, G. Thews : Physiologie des Menschen, 26. Auflage, Springer Verlag, Berlin - Heidelberg - New York 1995, S. 614
27 Puffersysteme des Blutes Kapazität der geschlossenen Puffersysteme Bei einer Änderung des ph-wertes von 1 l Blut um eine Einheit werden gebunden: 1 mmol Protonen an Phosphat 5 mmol Protonen an Plasmaproteine 16 mmol Protonen an Hämoglobin
28 Puffersysteme des Blutes Übersicht Puffer Säure Base pks Bicarbonatpuffer Bicarbonat H 2 CO 3 - HCO Nichtbicarbonatpuffer Phosphat - H 2 PO 4 2- HPO Plasmaproteine Histidin HisH + His Cystein Cys-SH CysS Erythrocyten
29 Puffersysteme des Blutes Der Bikarbonatpuffer Abb. aus: P. Scheid: Säure-Basen-Gleichgewicht. In : Klinke, Pape, Silbernagl, Physiologie, 5. Auflage, Thieme Verlag Stuttgart 2005, S. 316.
30 Puffersysteme des Blutes Der Bikarbonatpuffer Allgemein gilt: ph = pk + log [A- ] [HA] Einsetzen der physiologischen Konzentrationen von HCO 3 - und CO 2 liefert: ph = log ph = log 20 ph = = mmol/l 1.2 mmol/l
31 Puffersysteme des Blutes Die CO 2 -Äquilibrierungslinie Abb. aus: P. Scheid: Säure-Basen-Gleichgewicht. In : Klinke, Pape, Silbernagl, Physiologie, 5. Auflage, Thieme Verlag Stuttgart 2005, S. 317.
32 Puffersysteme des Blutes Definition der Standardbikarbonat-Konzentration Aktuelle Bicarbonat-Konzentration = tatsächlich im Blutplasma des Patienten vorliegende HCO 3 - Konzentration Standardbikarbonat-Konzentration = HCO 3 - Konzentration, die sich nach Äquilibrieren mit p(co 2 ) = 5.3 kpa (40 mmhg) bei O 2 -Sättigung und 37 C einstellt. Normwert = 24 mmol/l
33 Regulation des intrazellulären ph Übersicht
34 Regulation des intrazellulären ph Protonen-Transportprozesse Quantitativ wichtigster Transporter: Na + -H + -Austauscher (treibende Kraft: Na- Gradient) Zur Überwindung größerer Gradienten wichtig: K + -H + -Pumpe H + -Pumpe (treibende Kraft: ATP- Hydrolyse)
35 Regulation des intrazellulären ph Bikarbonat-Transportprozesse Wichtigste Transportprozesse: HCO 3- /Cl Austauscher Na + /HCO 3- -Symporter
36 Das Säure-Basen-Gleichgewicht Übersicht 15 mol/d 50 mmol/d Abb. aus: P. Scheid: Säure-Basen-Gleichgewicht. In : Klinke, Pape, Silbernagl, Physiologie, 5. Auflage, Thieme Verlag Stuttgart 2005, S. 312.
37 Säure-Basen-Regulation durch die Niere Protonensekretion
38 Säure-Basen-Regulation durch die Niere Bikarbonat Resorption
39 Säure-Basen-Regulation durch die Niere Ammoniak-Ausscheidung
40 Säure-Basen-Regulation durch die Niere Ammoniak-Ausscheidung
41 Das Säure-Basen-Gleichgewicht Übersicht 15 mol/d 50 mmol/d
42 Regulation des ph-wertes im Blut Normalbereich der Blutplasmawerte Normalbereich ph 7,37 7,43 Azidose: ph < 7,37 Alkalose: ph > 7,43 lebensbedrohlich: ph < 7,0 oder ph > 7,8
43 Das Säure-Basen-Gleichgewicht Charakterisierung des Säure-Basen-Status
44 Das Säure-Basen-Gleichgewicht Normwerte Tabelle aus: P. Scheid: Säure-Basen-Gleichgewicht. In : Klinke, Pape, Silbernagl, Physiologie, 5. Auflage, Thieme Verlag Stuttgart 2005, S. 320.
45 Störungen des Säure-Basen- Gleichgewichtes Abb. aus: P. Scheid: Säure-Basen-Gleichgewicht. In : Klinke, Pape, Silbernagl, Physiologie, 5. Auflage, Thieme Verlag Stuttgart 2005, S. 321.
46 Störungen des Säure-Basen- Gleichgewichtes Tabelle aus: P. Scheid: Säure-Basen-Gleichgewicht. In : Klinke, Pape, Silbernagl, Physiologie, 5. Auflage, Thieme Verlag Stuttgart 2005, S. 321.
47 Störungen des Säure-Basen- Gleichgewichtes Ein Beispiel: Bei einem Patienten ergibt sich in einer arteriellen Blutprobe folgende Befundkonstellation: ph-wert 7,49 CO 2 -Partialdruck 4,1 kpa (31 mmhg) Standardbikarbonat 24 mmol Basenabweichung (base excess): 0 mmol/l Welche Störung des Säure-Basenhaushaltes liegt vor?
48 Störungen des Säure-Basen- Gleichgewichtes Bei der Untersuchung des Säure-Basen-Status im arteriellen Blut eines Patienten ergaben sich folgende Werte: ph: 7.50 CO 2 -Partialdruck: 50mmHg Basenüberschuß: +12mmol/l Es handelt sich hierbei um eine (A) voll kompensierte respiratorische Alkalose (B) teilweise kompensierte respiratorische Alkalose (C) respiratorische und nichtrespiratorische Alkalose (D) teilweise kompensierte nichtrespiratorische Alkalose (E) voll kompensierte nichtrespiratorische Alkalose
Elektrolythaushalt + Säure-Basen-Haushalt
 Elektrolythaushalt + Säure-Basen-Haushalt Überblick Elektrolythaushalt Natrium Kalium Calcium Magnesium Phosphat Säure-Basen-Haushalt Der Elektrolythaushalt Normwerte im Blut: Natrium 135-145 mmol/l Kalium
Elektrolythaushalt + Säure-Basen-Haushalt Überblick Elektrolythaushalt Natrium Kalium Calcium Magnesium Phosphat Säure-Basen-Haushalt Der Elektrolythaushalt Normwerte im Blut: Natrium 135-145 mmol/l Kalium
Säure-Basen- Haushalt
 Säure-Basen- Haushalt Folie Nr. 1 Grundlagen Normwerte Puffersysteme Störungen Grundlagen BGA Grundlagen: Ziel ist das Gleichgewicht zwischen sauren und alkalischen Substanzen Einheit des Säure-Basen-Gleichgewichts
Säure-Basen- Haushalt Folie Nr. 1 Grundlagen Normwerte Puffersysteme Störungen Grundlagen BGA Grundlagen: Ziel ist das Gleichgewicht zwischen sauren und alkalischen Substanzen Einheit des Säure-Basen-Gleichgewichts
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Gliederung. Puffersysteme. Wofür Puffersysteme? Wofür Puffersysteme? Wofür Puffersysteme? ph-verhältnisse im Körper. Puffersysteme
 Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Thema: Säure-Basen-Haushalt
 Säure-Basen-Haushalt Seite 1 Thema: Säure-Basen-Haushalt 1 Grundlagen Die ph-regulation des Körpers ist von grundlegender Bedeutung für seine Funktion. Der ph-wert ist ein Maß für die Wasserstoffionenkonzentration(Wasserstoffionen
Säure-Basen-Haushalt Seite 1 Thema: Säure-Basen-Haushalt 1 Grundlagen Die ph-regulation des Körpers ist von grundlegender Bedeutung für seine Funktion. Der ph-wert ist ein Maß für die Wasserstoffionenkonzentration(Wasserstoffionen
Kapitel 2.2 Kardiopulmonale Homöostase. Kohlendioxid
 Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Kurstag 3. Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers
 Kurstag Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung: Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Kurstag Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung: Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Thema: Säure-Basen-Haushalt
 Säure-Basen-Haushalt Seite 1 Thema: Säure-Basen-Haushalt 1 Grundlagen Die ph-regulation des Körpers ist von grundlegender Bedeutung für seine Funktion. Der ph-wert ist ein Maß für die Wasserstoffionenkonzentration(Wasserstoffionen
Säure-Basen-Haushalt Seite 1 Thema: Säure-Basen-Haushalt 1 Grundlagen Die ph-regulation des Körpers ist von grundlegender Bedeutung für seine Funktion. Der ph-wert ist ein Maß für die Wasserstoffionenkonzentration(Wasserstoffionen
HA + B A - + HB + Säuren und Basen. Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor!
 Säuren und Basen Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor! Die Tendenz ein Proton abzuspalten (Säure) bzw. aufzunehmen (Base) bezeichnet man als Säure-
Säuren und Basen Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor! Die Tendenz ein Proton abzuspalten (Säure) bzw. aufzunehmen (Base) bezeichnet man als Säure-
Das Säure-Basen- Gleichgewicht. Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung
 Das Säure-Basen- Gleichgewicht Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung BGA Blutgasanalyse Normalkost körpereigener Stoffwechsel Überschuss
Das Säure-Basen- Gleichgewicht Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung BGA Blutgasanalyse Normalkost körpereigener Stoffwechsel Überschuss
Säure-Basen-Haushalt
 Säure-Basen-Haushalt Voraussetzungen Kenntnisse über Gas-Partialdrücke und Formen des O 2 - bzw. CO 2 -Transportes im Blut, Rolle der Erythrozyten, Aufbau und Funktion des Hämoglobinmoleküls, Puffereigenschaften
Säure-Basen-Haushalt Voraussetzungen Kenntnisse über Gas-Partialdrücke und Formen des O 2 - bzw. CO 2 -Transportes im Blut, Rolle der Erythrozyten, Aufbau und Funktion des Hämoglobinmoleküls, Puffereigenschaften
Das Säure-Basen- Gleichgewicht. Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung
 Das Säure-Basen- Gleichgewicht Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung BGA Blutgasanalyse Normalkost körpereigener Stoffwechsel Überschuss
Das Säure-Basen- Gleichgewicht Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung BGA Blutgasanalyse Normalkost körpereigener Stoffwechsel Überschuss
Grundlagen der Chemie Säuren und Basen
 Säuren und Basen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Säure-Base-Theorien Die Begriffe Säure und Base
Säuren und Basen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Säure-Base-Theorien Die Begriffe Säure und Base
ph-wert Berechnung für starke Säuren / Basen starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1
![ph-wert Berechnung für starke Säuren / Basen starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 ph-wert Berechnung für starke Säuren / Basen starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1](/thumbs/33/16365353.jpg) ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
Einführung Aufgaben der Niere
 Die Niere Einführung Aufgaben der Niere Die Nieren haben verschiedene Aufgaben : 1. Ausscheidung von Stoffwechselprodukten und stoffwechselfremden Substanzen 2. Regulation des Elektrolythaushaltes 3. Regulation
Die Niere Einführung Aufgaben der Niere Die Nieren haben verschiedene Aufgaben : 1. Ausscheidung von Stoffwechselprodukten und stoffwechselfremden Substanzen 2. Regulation des Elektrolythaushaltes 3. Regulation
Protonenstoffwechsel. Puffersysteme des Blutes und des Organismus. Puffersysteme des Blutes und des Organismus Bicarbonat-Puffer
 Protonenstoffwechsel Puffersysteme des Blutes und des Organismus Die Summe aller im biologischen ph-bereich im Blut zur Aufnahme von H + befähigten Valenzen Anteil an Konzentration system % 50 pk a 6,1!
Protonenstoffwechsel Puffersysteme des Blutes und des Organismus Die Summe aller im biologischen ph-bereich im Blut zur Aufnahme von H + befähigten Valenzen Anteil an Konzentration system % 50 pk a 6,1!
12 Säure-Basen-Haushalt
 12.1 Der ph-wert in Körperflüssigkeiten 281 Gotthold Gäbel Der ph-wert der extrazellulären Flüssigkeit wird in einem sehr engen Bereich zwischen 7,36 und 7,44 gehalten. Dies geschieht über Puffersysteme,
12.1 Der ph-wert in Körperflüssigkeiten 281 Gotthold Gäbel Der ph-wert der extrazellulären Flüssigkeit wird in einem sehr engen Bereich zwischen 7,36 und 7,44 gehalten. Dies geschieht über Puffersysteme,
Prinzip der tubulären Transportprozesse. Vergleich von physiologischen und pathologischen Bedingungen
 Prinzip der tubulären Transportprozesse Vergleich von physiologischen und pathologischen Bedingungen Gliederung Physiologisch: Resorption (am Beispiel von Cl) Sekretion (am Beispiel von und H ) Pathologisch:
Prinzip der tubulären Transportprozesse Vergleich von physiologischen und pathologischen Bedingungen Gliederung Physiologisch: Resorption (am Beispiel von Cl) Sekretion (am Beispiel von und H ) Pathologisch:
Mehrprotonige Säuren (z.b. H 2 SO 4 )
 Mehrprotonige Säuren (z.b. H SO 4 ) Mehrprotonige Säuren protolysieren stufenweise. Jede Stufe hat eine eigene Säurekonstante, deren Werte von Stufe zu Stufe kleiner werden (die Protolyse wird immer unvollständiger).
Mehrprotonige Säuren (z.b. H SO 4 ) Mehrprotonige Säuren protolysieren stufenweise. Jede Stufe hat eine eigene Säurekonstante, deren Werte von Stufe zu Stufe kleiner werden (die Protolyse wird immer unvollständiger).
Aufgabe 1: Geben Sie die korrespondierenden Basen zu folgenden Verbindungen an: a) H 3 PO 4 b) H 2 PO 4
 Übungsaufgaben zum Thema Säuren, Basen und Puffer Säure/Base Definition nach Brǿnsted: Säuren sind Stoffe, die Protonen abgeben können (Protonendonatoren). Basen sind Stoffe, die Protonen aufnehmen können
Übungsaufgaben zum Thema Säuren, Basen und Puffer Säure/Base Definition nach Brǿnsted: Säuren sind Stoffe, die Protonen abgeben können (Protonendonatoren). Basen sind Stoffe, die Protonen aufnehmen können
Blutgasanalyse UNIVERSITÄT DES SAARLANDES. Probenahme, Parameter, usw. für MTAF-Schule. Jung R. 26. März 2015. Institut für Arbeitsmedizin der
 Probenahme, Parameter, usw. für MTAF-Schule Jung R. Institut für Arbeitsmedizin der UNIVERSITÄT DES SAARLANDES 26. März 2015 - ph - Werte Blutgasnormwerte Messung von ph-wert sowie den Partialdrücken po2
Probenahme, Parameter, usw. für MTAF-Schule Jung R. Institut für Arbeitsmedizin der UNIVERSITÄT DES SAARLANDES 26. März 2015 - ph - Werte Blutgasnormwerte Messung von ph-wert sowie den Partialdrücken po2
Säure - Base - Theorien
 Säure Base Theorien S. Arrhenius (1887) Säuren sind Stoffe, die in wässriger Lösung H + (aq) Ionen bilden, während Basen OH (aq) Ionen bilden. H 2 SO 4, HNO 3, HCl, NaOH, Ba(OH) 2, aber: NH 3, CH 3, OCH
Säure Base Theorien S. Arrhenius (1887) Säuren sind Stoffe, die in wässriger Lösung H + (aq) Ionen bilden, während Basen OH (aq) Ionen bilden. H 2 SO 4, HNO 3, HCl, NaOH, Ba(OH) 2, aber: NH 3, CH 3, OCH
Sauerstoffbindung im Blut
 Sauerstoffbindung im Blut Die Fähigkeit uns zu wundern, ist das Einzige, was wir brauchen, um gute Philosophen zu werden. Gaarder Jostein, Sofies Welt 1 Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung...
Sauerstoffbindung im Blut Die Fähigkeit uns zu wundern, ist das Einzige, was wir brauchen, um gute Philosophen zu werden. Gaarder Jostein, Sofies Welt 1 Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung...
KliChi. Klinische Chemie & Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Analytik und Blutgasanalytik. Dr. med. Bernhard Schlüter - 1 -
 Sommersemester 2012-1 - Klinische Chemie & Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Analytik und Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium Universitätsklinikum
Sommersemester 2012-1 - Klinische Chemie & Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Analytik und Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium Universitätsklinikum
Zusammenfassung der letzten Doppelstunde
 Die Niere Teil II Zusammenfassung der letzten Doppelstunde Prinzip der Harnbildung Definition der Clearance Filtration, Sekretion und Reabsorption Blut? Urin S U C V U S P Osmoregulation Struktur und Funktion
Die Niere Teil II Zusammenfassung der letzten Doppelstunde Prinzip der Harnbildung Definition der Clearance Filtration, Sekretion und Reabsorption Blut? Urin S U C V U S P Osmoregulation Struktur und Funktion
Ungefähre Zusammensetzung des Blutes und des Blutplasmas. Die häufigsten Bestandteile des Blutplasmas (Mittelwerte)
 Puffer /Zusammensetzung des Blutes 1 Zusammensetzung des Blutes Das Blut der Wirbeltiere besteht zu 55% aus flüssigem Blutplasma und zu 45% aus darin schwimmenden festen Bestandteilen, den Blutkörperchen.
Puffer /Zusammensetzung des Blutes 1 Zusammensetzung des Blutes Das Blut der Wirbeltiere besteht zu 55% aus flüssigem Blutplasma und zu 45% aus darin schwimmenden festen Bestandteilen, den Blutkörperchen.
Willy Bauhuber KfH Nierenzentrum im Klinikum Rosenheim
 Willy Bauhuber KfH Nierenzentrum im Klinikum Rosenheim über 5500 Fundstellen bei GOOGLE meist Alternativmedizin Fehlernärung, Bewegungsmangel, Stress... führen zu schädlicher Übersäuerung Behandlung durch
Willy Bauhuber KfH Nierenzentrum im Klinikum Rosenheim über 5500 Fundstellen bei GOOGLE meist Alternativmedizin Fehlernärung, Bewegungsmangel, Stress... führen zu schädlicher Übersäuerung Behandlung durch
Das chemische Gleichgewicht, Massenwirkungsgesetz, Löslichkeit von Salzen in Flüssigkeiten, Löslichkeitsprodukt, Chemische Gleichgewichte, Säuren und
 Wiederholung der letzten Vorlesungsstunde: Das chemische Gleichgewicht, Massenwirkungsgesetz, Löslichkeit von Salzen in Flüssigkeiten, Löslichkeitsprodukt, Thema heute: Chemische Gleichgewichte, Säuren
Wiederholung der letzten Vorlesungsstunde: Das chemische Gleichgewicht, Massenwirkungsgesetz, Löslichkeit von Salzen in Flüssigkeiten, Löslichkeitsprodukt, Thema heute: Chemische Gleichgewichte, Säuren
Säuren- und Basendefinition nach Arrhenius
 Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Säuren- und Basendefinition nach Arrhenius
 Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Säuren und Basen. 18 UE Präsenz - Selbststudium 1,3 ECTS
 Säuren und Basen 18 UE Präsenz - Selbststudium 1,3 ECTS Überblick 1. Schülervorstellungen Phänomenologische Begriffsbestimmung 2. Verschiedene Definitionen der Begriffe 3. Stärke von Säuren und Basen 4.
Säuren und Basen 18 UE Präsenz - Selbststudium 1,3 ECTS Überblick 1. Schülervorstellungen Phänomenologische Begriffsbestimmung 2. Verschiedene Definitionen der Begriffe 3. Stärke von Säuren und Basen 4.
Quantitative Säure-Basen Betrachtungen
 Quantitative Säure-Basen Betrachtungen Hilfedatei zu dem Tabellenkalkulationsprogramm Peter_Stewart_standard_including_P (Stand: 19.06.2009) Die grundlegende Einführung in dieses umfangreiche Gebiet ist:
Quantitative Säure-Basen Betrachtungen Hilfedatei zu dem Tabellenkalkulationsprogramm Peter_Stewart_standard_including_P (Stand: 19.06.2009) Die grundlegende Einführung in dieses umfangreiche Gebiet ist:
Wintersemester 2017 Seminar Stöchiometrie
 Wintersemester 2017 Seminar Stöchiometrie Themenüberblick Kurze Wiederholung der wichtigsten Formeln Neue Themen zur Abschlussklausur: 1. Elektrolytische Dissoziation 2. ph-wert Berechnung 3. Puffer Wiederholung
Wintersemester 2017 Seminar Stöchiometrie Themenüberblick Kurze Wiederholung der wichtigsten Formeln Neue Themen zur Abschlussklausur: 1. Elektrolytische Dissoziation 2. ph-wert Berechnung 3. Puffer Wiederholung
Die Blutgasanalyse Was ist außerklinisch tolerabel? KAI 2014 Dr. med. Günter Schrot
 Die Blutgasanalyse Was ist außerklinisch tolerabel? KAI 2014 Dr. med. Günter Schrot Normale Blutgasanalyse ph 7,36-7,44 po2 >80 mmhg pco2 35-45 mmhg HCO3-22 -26 mmol/l berechnet Das Säure-Basen-System
Die Blutgasanalyse Was ist außerklinisch tolerabel? KAI 2014 Dr. med. Günter Schrot Normale Blutgasanalyse ph 7,36-7,44 po2 >80 mmhg pco2 35-45 mmhg HCO3-22 -26 mmol/l berechnet Das Säure-Basen-System
BIOCHEMIE I. ure- Lernziele. Relevante Textbooks. für r Mediziner
 BIOCHEMIE I Institut für Klinische Chemie, Molekulare Diagnostik und Mitochondriale Genetik (M.F. Bauer) für r Mediziner Säure-Basen-Haushalt Relevante Textbooks Integrative Klinische Chemie und Laboratoriumsmedizin.
BIOCHEMIE I Institut für Klinische Chemie, Molekulare Diagnostik und Mitochondriale Genetik (M.F. Bauer) für r Mediziner Säure-Basen-Haushalt Relevante Textbooks Integrative Klinische Chemie und Laboratoriumsmedizin.
ph-wert Berechnung für starke Säuren / Basen
 ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
3.2. Aufgaben zu Säure-Base-Gleichgewichten
 .. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
.. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
BK07_Vorlesung Physiologie 29. Oktober 2012
 BK07_Vorlesung Physiologie 29. Oktober 2012 1 Schema des Membrantransports Silverthorn: Physiologie 2 Membranproteine Silverthorn: Physiologie Transportproteine Ionenkanäle Ionenpumpen Membranproteine,
BK07_Vorlesung Physiologie 29. Oktober 2012 1 Schema des Membrantransports Silverthorn: Physiologie 2 Membranproteine Silverthorn: Physiologie Transportproteine Ionenkanäle Ionenpumpen Membranproteine,
ph-wert Berechnung für starke Säuren / Basen
 ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH Na + aq + OH starke Base,
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH Na + aq + OH starke Base,
Puffersysteme. Diese Lerneinheit befasst sich mit den Grundlagen der Puffersysteme: Was ist der Pufferbereich und wovon ist er abhängig?
 Puffersysteme Diese Lerneinheit befasst sich mit den Grundlagen der Puffersysteme: Was ist ein Puffersystem? Wie wirkt ein Puffer? Was ist der Pufferbereich und wovon ist er abhängig? Welche biochemisch
Puffersysteme Diese Lerneinheit befasst sich mit den Grundlagen der Puffersysteme: Was ist ein Puffersystem? Wie wirkt ein Puffer? Was ist der Pufferbereich und wovon ist er abhängig? Welche biochemisch
Elektrolyte. (aus: Goldenberg, SOL)
 Elektrolyte Elektrolyte leiten in wässriger Lösung Strom. Zu den Elektrolyten zählen Säuren, Basen und Salze, denn diese alle liegen in wässriger Lösung zumindest teilweise in Ionenform vor. Das Ostwaldsche
Elektrolyte Elektrolyte leiten in wässriger Lösung Strom. Zu den Elektrolyten zählen Säuren, Basen und Salze, denn diese alle liegen in wässriger Lösung zumindest teilweise in Ionenform vor. Das Ostwaldsche
Physiologie der Atmung. Cem Ekmekcioglu
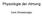 Physiologie der Atmung Cem Ekmekcioglu Übersicht über den Transportweg des Sauerstoffes beim Menschen Schmidt/Thews: Physiologie des Menschen, 27.Auflage, Kap.25, Springer (1997) Klinke, Pape, Silbernagl,
Physiologie der Atmung Cem Ekmekcioglu Übersicht über den Transportweg des Sauerstoffes beim Menschen Schmidt/Thews: Physiologie des Menschen, 27.Auflage, Kap.25, Springer (1997) Klinke, Pape, Silbernagl,
co2 arteriell venös arteriovenöse Differenz
 po2 arteriell venös pco2 arteriell venös ph arteriell venös O2-Sättigung so2 arteriell venös O2-Gehalt co2 arteriell venös arteriovenöse Differenz CO2-Gehalt cco2 arteriell venös Hypoxie Hypoxämie arteriell:
po2 arteriell venös pco2 arteriell venös ph arteriell venös O2-Sättigung so2 arteriell venös O2-Gehalt co2 arteriell venös arteriovenöse Differenz CO2-Gehalt cco2 arteriell venös Hypoxie Hypoxämie arteriell:
Sommersemester 2016 Seminar Stöchiometrie
 Sommersemester 2016 Seminar Stöchiometrie Themenüberblick Kurze Wiederholung der wichtigsten Formeln Neue Themen zur Abschlussklausur: 1. Elektrolytische Dissoziation 2. ph-wert Berechnung 3. Puffer Wiederholung
Sommersemester 2016 Seminar Stöchiometrie Themenüberblick Kurze Wiederholung der wichtigsten Formeln Neue Themen zur Abschlussklausur: 1. Elektrolytische Dissoziation 2. ph-wert Berechnung 3. Puffer Wiederholung
1/37. Das Protolysegleichgewicht. Wie könnte man die Stärke einer Säure quantitativ definieren?
 Das Protolysegleichgewicht 1/37 Wie könnte man die Stärke einer Säure quantitativ definieren? Das Protolysegleichgewicht 2/37 Wie könnte man die Stärke einer Säure quantitativ definieren? Ein erster Ansatz
Das Protolysegleichgewicht 1/37 Wie könnte man die Stärke einer Säure quantitativ definieren? Das Protolysegleichgewicht 2/37 Wie könnte man die Stärke einer Säure quantitativ definieren? Ein erster Ansatz
Säuren und Basen nach Brönsted
 Säuren und Basen nach Brönsted Es gibt versch. Definitionen von Säuren und Basen. Nach Brönsted ist eine Säure (HA) ein Protonendonator und eine Base (B) ein Protonenakzeptor, d.h. eine Säure reagiert
Säuren und Basen nach Brönsted Es gibt versch. Definitionen von Säuren und Basen. Nach Brönsted ist eine Säure (HA) ein Protonendonator und eine Base (B) ein Protonenakzeptor, d.h. eine Säure reagiert
Themen heute: Säuren und Basen, Redoxreaktionen
 Wiederholung der letzten Vorlesungsstunde: Massenwirkungsgesetz, Prinzip des kleinsten Zwangs, Löslichkeitsprodukt, Themen heute: Säuren und Basen, Redoxreaktionen Vorlesung Allgemeine Chemie, Prof. Dr.
Wiederholung der letzten Vorlesungsstunde: Massenwirkungsgesetz, Prinzip des kleinsten Zwangs, Löslichkeitsprodukt, Themen heute: Säuren und Basen, Redoxreaktionen Vorlesung Allgemeine Chemie, Prof. Dr.
Säuren und Basen. Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17.
 Säuren und Basen Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17 torsten.beweries@catalysis.de http://www.catalysis.de/forschung/koordinationschemische-katalyse/koordinationschemische-wasserspaltung/
Säuren und Basen Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17 torsten.beweries@catalysis.de http://www.catalysis.de/forschung/koordinationschemische-katalyse/koordinationschemische-wasserspaltung/
Übungsblatt zu Säuren und Basen
 1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
Kurstag 3. Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers
 Kurstag 3 Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Kurstag 3 Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Wintersemester 2016 Seminar Stöchiometrie
 Wintersemester 2016 Seminar Stöchiometrie Tutorien Raum Termin Hörsaal OSZ H5 Mo. 19.12., 18-20 Uhr Hörsaal OSZ H5 Fr. 13.1.,16-18 Uhr Hörsaal OSZ H5 Mo. 30.01., 18-20 Uhr Hörsaal OSZ H5 Mo. 06.02., 18-20
Wintersemester 2016 Seminar Stöchiometrie Tutorien Raum Termin Hörsaal OSZ H5 Mo. 19.12., 18-20 Uhr Hörsaal OSZ H5 Fr. 13.1.,16-18 Uhr Hörsaal OSZ H5 Mo. 30.01., 18-20 Uhr Hörsaal OSZ H5 Mo. 06.02., 18-20
Einteilung der Maßanalyse
 Einteilung der Maßanalyse Neutralisation (Säure-Base-Titration Acidimetrie Alkalimetrie Fällungstitration Redoxtitration Iodometrie Dichromatometrie Manganometrie etc. Komplexometrie Säure/Basen Theorien
Einteilung der Maßanalyse Neutralisation (Säure-Base-Titration Acidimetrie Alkalimetrie Fällungstitration Redoxtitration Iodometrie Dichromatometrie Manganometrie etc. Komplexometrie Säure/Basen Theorien
Zusammenfassung vom
 Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
3. Säure-Base-Beziehungen
 3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
Ein Puffer ist eine Mischung aus einer schwachen Säure/Base und ihrer Korrespondierenden Base/Säure.
 2.8 Chemische Stoßdämpfer Puffersysteme V: ph- Messung eines Gemisches aus HAc - /AC - nach Säure- bzw Basen Zugabe; n(naac) = n(hac) > Acetat-Puffer. H2O Acetat- Puffer H2O Acetat- Puffer Die ersten beiden
2.8 Chemische Stoßdämpfer Puffersysteme V: ph- Messung eines Gemisches aus HAc - /AC - nach Säure- bzw Basen Zugabe; n(naac) = n(hac) > Acetat-Puffer. H2O Acetat- Puffer H2O Acetat- Puffer Die ersten beiden
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
EinFaCh 4. Studienvorbereitung Chemie. Einstieg in Freibergs anschauliches Chemiewissen Teil 4: Säuren und Basen. tu-freiberg.de
 Studienvorbereitung Chemie EinFaCh Einstieg in Freibergs anschauliches Chemiewissen Teil : Säuren und Basen tu-freiberg.de tu-freiberg.de/fakultaet2/einfach Was ist eine Säure oder Base? Gemäß der heute
Studienvorbereitung Chemie EinFaCh Einstieg in Freibergs anschauliches Chemiewissen Teil : Säuren und Basen tu-freiberg.de tu-freiberg.de/fakultaet2/einfach Was ist eine Säure oder Base? Gemäß der heute
Chemie für Studierende der Biologie I
 SäureBaseGleichgewichte Es gibt verschiedene Definitionen für SäureBaseReaktionen, an dieser Stelle ist die Definition nach BrønstedLowry, die Übertragung eines H + Ions ( Proton ), gemeint. Nach BrønstedLowry
SäureBaseGleichgewichte Es gibt verschiedene Definitionen für SäureBaseReaktionen, an dieser Stelle ist die Definition nach BrønstedLowry, die Übertragung eines H + Ions ( Proton ), gemeint. Nach BrønstedLowry
BIOCHEMIE I Teil 5 und 6
 Titrationskurve einer schwachen Säure mit einer starken Base. BIOCHEMIE I Teil 5 und 6 13 Äquivalenzpunkt Äquivalenzpunkt: Essigsäure vollständig dissoziiert. Bei zunehmender Menge an NaOH nähert sich
Titrationskurve einer schwachen Säure mit einer starken Base. BIOCHEMIE I Teil 5 und 6 13 Äquivalenzpunkt Äquivalenzpunkt: Essigsäure vollständig dissoziiert. Bei zunehmender Menge an NaOH nähert sich
Homöostase der Mineralstoffe
 Mineralstoffversorgung auf dem Milchviehbetrieb Vetsuisse-Fakultät Zürich 24. November 2015 Homöostase der Mineralstoffe Maren Feldmann Klinik für Rinder Tierärztliche Hochschule Hannover Rindergesundheitsdienst
Mineralstoffversorgung auf dem Milchviehbetrieb Vetsuisse-Fakultät Zürich 24. November 2015 Homöostase der Mineralstoffe Maren Feldmann Klinik für Rinder Tierärztliche Hochschule Hannover Rindergesundheitsdienst
SS 2010. Thomas Schrader. der Universität Duisburg-Essen. (Teil 7: Säuren und Basen, Elektrolyte)
 Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 7: Säuren und Basen, Elektrolyte) Definition Säure/Base Konjugierte Säure/Base-Paare Konjugierte
Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 7: Säuren und Basen, Elektrolyte) Definition Säure/Base Konjugierte Säure/Base-Paare Konjugierte
Säure-Basen-Haushalt, Blutgase
 Säure-Basen-Haushalt, Blutgase Grundlagen Allgemeine Pathobiochemie Kohlendioxid CO 2, Kohlensäure H 2 CO 3 nichtflüchtige Säuren Puffersysteme renale Mechanismen Störungen und Kompensation Spezielle Pathobiochemie
Säure-Basen-Haushalt, Blutgase Grundlagen Allgemeine Pathobiochemie Kohlendioxid CO 2, Kohlensäure H 2 CO 3 nichtflüchtige Säuren Puffersysteme renale Mechanismen Störungen und Kompensation Spezielle Pathobiochemie
Der ph-wert des Blutplasmas zeigt an, ob das Gleichgewicht zwischen +
 Diagnostik Säure-Basen-Status Unter dem Säure-Basen-Status versteht man die Summe derjenigen Messund Rechengrößen, die eine Diagnostik der Störungen des Säure-Basen- Haushaltes ermöglichen. Dazu gehören
Diagnostik Säure-Basen-Status Unter dem Säure-Basen-Status versteht man die Summe derjenigen Messund Rechengrößen, die eine Diagnostik der Störungen des Säure-Basen- Haushaltes ermöglichen. Dazu gehören
Säure-Base Titrationen. (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen)
 Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Niere Salz-/Wasserhaushalt 2009
 Aus: Gray's Anatomy: Descriptive and Surgical Theory United Kingdom 1858 Zentrale Aufgaben der Nieren Regulation des Wasserhaushaltes Regulation des Mineralhaushaltes (Osmolarität) Regulation des Säure-Basen-Haushaltes
Aus: Gray's Anatomy: Descriptive and Surgical Theory United Kingdom 1858 Zentrale Aufgaben der Nieren Regulation des Wasserhaushaltes Regulation des Mineralhaushaltes (Osmolarität) Regulation des Säure-Basen-Haushaltes
AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7
 AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7 1. a) CH3COOH, C0=0.125 mol/l Schwache Säure pks = 4.75 (aus Tabelle) => ph = 0.5*(4.75-Log(0.125))= 2.83 b) H24, C0=0.1 mol/l Erste Protolysestufe starke
AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7 1. a) CH3COOH, C0=0.125 mol/l Schwache Säure pks = 4.75 (aus Tabelle) => ph = 0.5*(4.75-Log(0.125))= 2.83 b) H24, C0=0.1 mol/l Erste Protolysestufe starke
Grundlagen der Ernährungslehre
 Grundlagen der Ernährungslehre Wasser Elektrolyt Säuren-Basen Haushalt des Organismus Wasserhaushalt des Organismus Funktionen des Wassers im tierischen Organismus Bestandteil vieler zellulärer und subzellulärer
Grundlagen der Ernährungslehre Wasser Elektrolyt Säuren-Basen Haushalt des Organismus Wasserhaushalt des Organismus Funktionen des Wassers im tierischen Organismus Bestandteil vieler zellulärer und subzellulärer
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bislang geschah Kinetik Reaktionsgeschwindigkeit Konzentrationsabhängigkeit
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bislang geschah Kinetik Reaktionsgeschwindigkeit Konzentrationsabhängigkeit
Wiederholungen. Puffergleichung (Henderson-Hasselbalch) Ionenprodukt des Wassers. ph-wert-berechnungen. Titrationskurvenberechnung
 Vorlesung 22: Wiederholungen Puffergleichung (Henderson-Hasselbalch) Ionenprodukt des Wassers ph-wert-berechnungen Titrationskurvenberechnung Säuren und Basen Hydroxonium + Chlorid Ammonium + Hydroxid
Vorlesung 22: Wiederholungen Puffergleichung (Henderson-Hasselbalch) Ionenprodukt des Wassers ph-wert-berechnungen Titrationskurvenberechnung Säuren und Basen Hydroxonium + Chlorid Ammonium + Hydroxid
Wasser. Flora und Fauna. Wichtigste chemische Verbindung in Lebewesen. Menschen benötigt mindestens 1kg H 2 O pro Tag
 Wasser Flora und Fauna Wichtigste chemische Verbindung in Lebewesen Menschen benötigt mindestens 1kg H 2 O pro Tag Löslichkeit von Sauerstoff in Wasser in Abhängigkeit von der Temperatur mg/l Zustandsdiagramm
Wasser Flora und Fauna Wichtigste chemische Verbindung in Lebewesen Menschen benötigt mindestens 1kg H 2 O pro Tag Löslichkeit von Sauerstoff in Wasser in Abhängigkeit von der Temperatur mg/l Zustandsdiagramm
Die Nieren. Anatomie Physiologie Säure-/Basen-Haushalt Elektrolyte Wasserhaushalt. Copyright: T.Heinrich-RA-1997 1
 Die Nieren Anatomie Physiologie Säure-/Basen-Haushalt Elektrolyte Wasserhaushalt Copyright: T.Heinrich-RA-1997 1 Die Anatomie des Urogenital- Systems Copyright: T.Heinrich-RA-1997 2 Das harnproduzierende
Die Nieren Anatomie Physiologie Säure-/Basen-Haushalt Elektrolyte Wasserhaushalt Copyright: T.Heinrich-RA-1997 1 Die Anatomie des Urogenital- Systems Copyright: T.Heinrich-RA-1997 2 Das harnproduzierende
Teil 2. Puffersysteme. Puffersysteme. Puffersysteme. MTA-Schule
 Puffersysteme Säure-Basen-Haushalt Teil 2 MTA-Schule Lösungen, die die Fähigkeit besitzen, ihren -Wert trotz Zugabe von H + oder OH Ionen weitgehend konstant zu halten, nennt man Pufferlösungen. Puffersysteme:
Puffersysteme Säure-Basen-Haushalt Teil 2 MTA-Schule Lösungen, die die Fähigkeit besitzen, ihren -Wert trotz Zugabe von H + oder OH Ionen weitgehend konstant zu halten, nennt man Pufferlösungen. Puffersysteme:
NIERENPHYSIOLOGIE, HOMÖOSTASE DER EXTRAZELLULÄREN FLÜSSIGKEITSRÄUME
 NIERENPHYSIOLOGIE, HOMÖOSTASE DER EXTRAZELLULÄREN FLÜSSIGKEITSRÄUME (2) Dr. Attila Nagy 2017 Das Tubulussystem (Lernziele: 54-57) Das Tubulussystem besteht aus mehreren, morphologisch und funktionell unterschiedlichen
NIERENPHYSIOLOGIE, HOMÖOSTASE DER EXTRAZELLULÄREN FLÜSSIGKEITSRÄUME (2) Dr. Attila Nagy 2017 Das Tubulussystem (Lernziele: 54-57) Das Tubulussystem besteht aus mehreren, morphologisch und funktionell unterschiedlichen
2. Zusammensetzung des Körpers nach ausgewählten Elementen : Element Gew.-% ca. Masse ca.
 1 Teil C: Tabellen und Richtwerte (Körperzusammensetzung u. Energiehaushalt) Physiologie Cluster B4 Vegetative Regulation II 1. Elektolytkonzentrationen in den Flüssigkeitsräumen des Körpers ( aus Schmidt,Thews,Lang
1 Teil C: Tabellen und Richtwerte (Körperzusammensetzung u. Energiehaushalt) Physiologie Cluster B4 Vegetative Regulation II 1. Elektolytkonzentrationen in den Flüssigkeitsräumen des Körpers ( aus Schmidt,Thews,Lang
Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6
 Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6 Thermodynamik und Gleichgewichte 1. a) Was sagt die Enthalpie aus? Die Enthalpie H beschreibt den Energiegehalt von Materie
Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6 Thermodynamik und Gleichgewichte 1. a) Was sagt die Enthalpie aus? Die Enthalpie H beschreibt den Energiegehalt von Materie
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14
 Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 4: Isomerie, Gibbs-Helmholtz-Gleichung, Katalysator, Addition an Alkene, funktionelle Gruppen, Säure/Base 1) Ordnen Sie die folgenden
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 4: Isomerie, Gibbs-Helmholtz-Gleichung, Katalysator, Addition an Alkene, funktionelle Gruppen, Säure/Base 1) Ordnen Sie die folgenden
INSTITUT FÜR PHYSIOLOGIE
 INSTITUT FÜR PHYSIOLOGIE Anleitung zum Physiologie - Praktikum P - 1. Pufferung und Säure-Basen Analyse WS 2010/11 3. Semester 2 Inhalt I. VORBEMERKUNGEN... 3 II. THEORETISCHE GRUNDLAGEN... 4 1. Säuren
INSTITUT FÜR PHYSIOLOGIE Anleitung zum Physiologie - Praktikum P - 1. Pufferung und Säure-Basen Analyse WS 2010/11 3. Semester 2 Inhalt I. VORBEMERKUNGEN... 3 II. THEORETISCHE GRUNDLAGEN... 4 1. Säuren
HämofiltrationsLösungen für. Citrat-Antikoagulationsbehandlungen
 HämofiltrationsLösungen für Citrat-Antikoagulationsbehandlungen Die Citrat-Antikoagulationsbehandlung in der Hämodialyse Seit den 60er Jahren ist die Antikoagulation mit Citrat bekannt und seit 1980 klinisch
HämofiltrationsLösungen für Citrat-Antikoagulationsbehandlungen Die Citrat-Antikoagulationsbehandlung in der Hämodialyse Seit den 60er Jahren ist die Antikoagulation mit Citrat bekannt und seit 1980 klinisch
Übungen zur VL Chemie für Biologen und Humanbiologen 14.01.2011
 Übungen zur VL Chemie für Biologen und Humanbiologen 14.01.011 Redoxchemie 1. a) Was beobachten Sie, wenn Sie in getrennten Experimenten einen Eisen-, Kupfer-, Zink- und Goldstab in eine Salzsäurelösung
Übungen zur VL Chemie für Biologen und Humanbiologen 14.01.011 Redoxchemie 1. a) Was beobachten Sie, wenn Sie in getrennten Experimenten einen Eisen-, Kupfer-, Zink- und Goldstab in eine Salzsäurelösung
7. Tag: Säuren und Basen
 7. Tag: Säuren und Basen 1 7. Tag: Säuren und Basen 1. Definitionen für Säuren und Basen In früheren Zeiten wußte man nicht genau, was eine Säure und was eine Base ist. Damals wurde eine Säure als ein
7. Tag: Säuren und Basen 1 7. Tag: Säuren und Basen 1. Definitionen für Säuren und Basen In früheren Zeiten wußte man nicht genau, was eine Säure und was eine Base ist. Damals wurde eine Säure als ein
Berechnung des ph-wertes einer schwachen Säure
 Berechnung des ph-wertes einer schwachen Säure 1/32 Schwefelwasserstoff H2S hat einen pks-wert von 6,92. Wie groß ist der ph-wert einer 0,01-molaren H2S-Lösung? Berechnung des ph-wertes einer schwachen
Berechnung des ph-wertes einer schwachen Säure 1/32 Schwefelwasserstoff H2S hat einen pks-wert von 6,92. Wie groß ist der ph-wert einer 0,01-molaren H2S-Lösung? Berechnung des ph-wertes einer schwachen
Kapiteltest 1.1. Kapiteltest 1.2
 Kapiteltest 1.1 a) Perchlorsäure hat die Formel HClO 4. Was geschieht bei der Reaktion von Perchlorsäure mit Wasser? Geben Sie zuerst die Antwort in einem Satz. Dann notieren Sie die Reaktionsgleichung.
Kapiteltest 1.1 a) Perchlorsäure hat die Formel HClO 4. Was geschieht bei der Reaktion von Perchlorsäure mit Wasser? Geben Sie zuerst die Antwort in einem Satz. Dann notieren Sie die Reaktionsgleichung.
Klinische Chemie und Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Haushalt und Blutgasanalytik
 Klinische Chemie und Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Haushalt und Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium Universitätsklinikum Münster
Klinische Chemie und Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Haushalt und Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium Universitätsklinikum Münster
Regulation des Kalium- Calcium- und Phosphathaushalts
 Regulation des Kalium- Calcium- und Phosphathaushalts Lernziele: 80, 81 Dr. Attila Nagy 2019 1 Normalwerte K + -Aufnahme/Ausscheidung: 50-100 mmol/tag Ca 2+ -Aufnahme/Absorption: 1000/200 mg/tag; auch
Regulation des Kalium- Calcium- und Phosphathaushalts Lernziele: 80, 81 Dr. Attila Nagy 2019 1 Normalwerte K + -Aufnahme/Ausscheidung: 50-100 mmol/tag Ca 2+ -Aufnahme/Absorption: 1000/200 mg/tag; auch
Regulation des K + - Calcium- und Phosphathaushalts. Lernziele: 80, 81. Dr. Attila Nagy
 Regulation des K + - Calcium- und Phosphathaushalts Lernziele: 80, 81 Dr. Attila Nagy 2018 Normalwerte K + -Aufnahme/Ausscheidung: 50-100 mmol/tag Ca 2+ -Aufnahme/Absorption: 1000/200 mg/tag; auch 25/5
Regulation des K + - Calcium- und Phosphathaushalts Lernziele: 80, 81 Dr. Attila Nagy 2018 Normalwerte K + -Aufnahme/Ausscheidung: 50-100 mmol/tag Ca 2+ -Aufnahme/Absorption: 1000/200 mg/tag; auch 25/5
Säuren und Basen. Der ph-wert Zur Feststellung, ob eine Lösung sauer oder basisch ist genügt es, die Konzentration der H 3 O H 3 O + + OH -
 Der ph-wert Zur Feststellung, ob eine Lösung sauer oder basisch ist genügt es, die Konzentration der H 3 O + (aq)-ionen anzugeben. Aus der Gleichung: H 2 O + H 2 O H 3 O + + OH - c(h 3 O + ) c(oh - ) K
Der ph-wert Zur Feststellung, ob eine Lösung sauer oder basisch ist genügt es, die Konzentration der H 3 O + (aq)-ionen anzugeben. Aus der Gleichung: H 2 O + H 2 O H 3 O + + OH - c(h 3 O + ) c(oh - ) K
Der globale Kohlenstoffkreislauf
 Der globale Kohlenstoffkreislauf Eine wesentliche Motivation für die Untersuchung des globalen Kohlenstoffkreislaufs ist der anthropogen bedingte Anstieg der atmosphärischen Konzentration von klimarelevanten
Der globale Kohlenstoffkreislauf Eine wesentliche Motivation für die Untersuchung des globalen Kohlenstoffkreislaufs ist der anthropogen bedingte Anstieg der atmosphärischen Konzentration von klimarelevanten
CHEMIE KAPITEL 4 SÄURE- BASE. Timm Wilke. Georg- August- Universität Göttingen. Wintersemester 2013 / 2014
 CHEMIE KAPITEL 4 SÄURE- BASE Timm Wilke Georg- August- Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Historisches Im 17. Jahrhundert wurden von Robert Boyle Gemeinsamkeiten verschiedener Verbindungen
CHEMIE KAPITEL 4 SÄURE- BASE Timm Wilke Georg- August- Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Historisches Im 17. Jahrhundert wurden von Robert Boyle Gemeinsamkeiten verschiedener Verbindungen
1.5 Säuren und Basen und der ph-wert
 Seite 14 1.5 Säuren und Basen und der ph-wert 1.5.1 Säuren Geschichtlich bedingte Definition: Eine Säure ist ein Stoff, dessen wässrige Lösung sauer schmeckt oder ätzend wirkt, bzw. andere Stoffe angreift.
Seite 14 1.5 Säuren und Basen und der ph-wert 1.5.1 Säuren Geschichtlich bedingte Definition: Eine Säure ist ein Stoff, dessen wässrige Lösung sauer schmeckt oder ätzend wirkt, bzw. andere Stoffe angreift.
ABGA. Notfallpflegekongress 2008 Solothurn. Notfallpflege am Stadtspital Triemli Zürich
 ABGA Notfallpflegekongress 2008 Solothurn H. Zahner,, Fachschule für f r Intensiv- und Notfallpflege am Stadtspital Triemli Zürich Werte des pulmonalen Gasaustausches PaO 2 Sauerstoffpartialdruck im arteriellen
ABGA Notfallpflegekongress 2008 Solothurn H. Zahner,, Fachschule für f r Intensiv- und Notfallpflege am Stadtspital Triemli Zürich Werte des pulmonalen Gasaustausches PaO 2 Sauerstoffpartialdruck im arteriellen
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Teilnahmebescheinigungen Mail an christoph.woelper@uni-due.de
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Teilnahmebescheinigungen Mail an christoph.woelper@uni-due.de
Kapitel 17: Weitere Aspekt. wässriger Gleichgew. Einfluss gleicher Ionen: Gleichioniger Zusatz, Verschiebung des Gleichgewichtes nach Le-Châtelier.
 Ache2 Kapitel 17: Weitere Aspekt. wässriger Gleichgew. Einfluss gleicher Ionen: Gleichioniger Zusatz, Verschiebung des Gleichgewichtes nach Le-Châtelier. Bsp. ph berechnen einer 0.085 mol/l salpetriger
Ache2 Kapitel 17: Weitere Aspekt. wässriger Gleichgew. Einfluss gleicher Ionen: Gleichioniger Zusatz, Verschiebung des Gleichgewichtes nach Le-Châtelier. Bsp. ph berechnen einer 0.085 mol/l salpetriger
Vorkurs Chemie (NF) Säuren und Basen, Puffer Ulrich Keßler
 Vorkurs Chemie (NF) Säuren und Basen, Puffer Ulrich Keßler Alltagserfahrung: sauer Zitrone Essig junger Wein Welcher Stoff bewirkt saure Reaktion? http://www.simplyscience.ch/portal Data/1/Resources/Images_bis_10_
Vorkurs Chemie (NF) Säuren und Basen, Puffer Ulrich Keßler Alltagserfahrung: sauer Zitrone Essig junger Wein Welcher Stoff bewirkt saure Reaktion? http://www.simplyscience.ch/portal Data/1/Resources/Images_bis_10_
Was verstehen wir unter Säuren und Basen?
 Was verstehen wir unter Säuren und Basen? Säuren: Unter Säuren verstehen wir alle organischen und anorganischen Verbindungen, die in Lösungen Wasserstoffionen H + abgeben. Sie werden auch Protonen Donatoren
Was verstehen wir unter Säuren und Basen? Säuren: Unter Säuren verstehen wir alle organischen und anorganischen Verbindungen, die in Lösungen Wasserstoffionen H + abgeben. Sie werden auch Protonen Donatoren
Dr. Tobias Schafmeier, BZH
 Dr. Tobias Schafmeier, BZH Einführungsversuche A: Genauigkeit und Präzision des Pipettierens mit Kolbenhubpipette B: Bestimmung des Extinktionskoeffizienten von Methylenblau Absorptionsspektrum von NADH/NAD
Dr. Tobias Schafmeier, BZH Einführungsversuche A: Genauigkeit und Präzision des Pipettierens mit Kolbenhubpipette B: Bestimmung des Extinktionskoeffizienten von Methylenblau Absorptionsspektrum von NADH/NAD
Leitartikel Puffersysteme im Blut
 Zusammenfassung Ausgabe 30, Mai 2011 ISSN 2190-5118 Summary Hepatitis C Die Puffersysteme im Blut helfen dabei, den Säure-Basen-Haushalt aufrecht zu erhalten. Es geht um Azidose und Alkalose, aber. Welche
Zusammenfassung Ausgabe 30, Mai 2011 ISSN 2190-5118 Summary Hepatitis C Die Puffersysteme im Blut helfen dabei, den Säure-Basen-Haushalt aufrecht zu erhalten. Es geht um Azidose und Alkalose, aber. Welche
7. Chemische Reaktionen
 7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte Grundlagen Lösung: homogene Phase aus Lösungsmittel und gelösten Stoff Lösungsmittel liegt im Überschuss vor
7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte Grundlagen Lösung: homogene Phase aus Lösungsmittel und gelösten Stoff Lösungsmittel liegt im Überschuss vor
0.1 Protolyse-Gleichgewichte
 1 0.1 Protoyse-Geichgewichte 0.1.1 Protoysereaktionen Protonen-Donatoren Teichen, die bei einer Reaktion Protonen abgeben Protonen-Akzeptoren Teichen, die bei einer Reaktion Protonen aufnehmen Protoyse-Übergang
1 0.1 Protoyse-Geichgewichte 0.1.1 Protoysereaktionen Protonen-Donatoren Teichen, die bei einer Reaktion Protonen abgeben Protonen-Akzeptoren Teichen, die bei einer Reaktion Protonen aufnehmen Protoyse-Übergang
