co2 arteriell venös arteriovenöse Differenz
|
|
|
- Jobst Bieber
- vor 7 Jahren
- Abrufe
Transkript
1 po2 arteriell venös pco2 arteriell venös ph arteriell venös O2-Sättigung so2 arteriell venös O2-Gehalt co2 arteriell venös arteriovenöse Differenz CO2-Gehalt cco2 arteriell venös Hypoxie Hypoxämie
2 arteriell: 40 mmhg venös: 46 mmhg arteriell: 100 mmhg venös: 40 mmhg arteriell: > 97 % venös: 75% arteriell: 7,4 venös: 7,37 arteriell: 500 ml venös: 530 ml arteriell: 200 ml venös: 150 ml arteriovenöse Differenz: 50 ml verminderter co2 verminderter po2 Sauerstoffmangel im Blut
3 Hypoxigenation Henry-Gesetz Physikalische Löslichkeit O2 Hüfner-Zahl O2-Sättigung [%] 100 Linksverschiebung normal 80 Rechtsverschiebung 60 P50 50% 40 Halbsättigungsdruck po2 [mmhg] DR Die Sauerstoffbindungskurve Strukturen des Hämoglobins T- und R- Struktur Kooperativer Effekt
4 C = Konzentration des Gases α = (Bunsen)-Löslichkeitskoeffizient des Gases P = Partialdruck des Gases verminderte Sauerstoffsättigung Die Konzentration eines physikalisch gelösten Gases ist proportional zu seinem Partialdruck über der Flüssigkeit 1 Mol Häm bindet 4 Mol O2 1 g Hämoglobin kann 1,34 ml O2 binden (Hüfner-Zahl) in 1l Blut werden 200 ml O2 chemisch gebunden transportiert geringe physikalische Löslichkeit in 1 l Blut sind physikalisch gelöst: - 2,85 ml O2-1% des gesamt transportierten O2 der Rest des O2 wird chemisch an Hämoglobin gebunden transportiert O2-Sättigung [%] Linksverschiebung Rechtsverschiebung normal P50 = 27 mmhg po2, bei dem 50% aller Bindungsstellen des Häms von O2 besetzt sind 60 P50 50% po2 [mmhg] DR bei Anlagerung des ersten O2-Moleküls Lösung der Salzbindungen leichtere Anlagerung für weitere O2-Moleküle S-Verlauf der Sauerstoffbindungskurve T-Struktur: tense-struktur - desoxygeniertes Hämoglobin - durch 8 Salzbindungen gespannt R-Struktur: relaxed-struktur - oxygeniertes Hämoglobin - durch Anlagerung eines O2-Moleküls Zug auf das proximale Histidin des Globins Lösung der Salzbindungen
5 Sauerstoffbindungskurve von Myoglobin Pufferkraft des Hämoglobins Rechtsverschiebung der Sauerstoffbindungskurve Linksverschiebung der Sauerstoffbindungskurve Bohr-Effekt Carboxyhämoglobin Methämoglobin/Hämiglobin Häm- und Pulsoxymetrie
6 Vorteile: - hohe Konzentration - hoher Histidingehalt - viele negativ geladene Aminosäuren desoxygeniertes Hämoglobin puffert besonders stark Myoglobin besitzt nur 1 Bindungsstelle kein kooperativer Effekt möglich Bindungskurve = Hyperbel freie NH2-Gruppen binden CO2 (= Carbaminohämoglobin) Ursachen: - sinkender pco2 - sinkende H + -Konzentration (steigender ph) - sinkende 2,3-Bisphosphoglycerat-Konzentration (vernetzt β-ketten des Hämoglobins) - sinkende Temperatur Folge: - Affinitätszunahme des Hämoglobins - erschwerte Sauerstoffabgabe - erniedrigter P50-Wert Ursachen: - steigender pco2 - steigende H + -Konzentration (sinkender ph) - steigende 2,3-Bisphosphoglycerat-Konzentration (vernetzt β-ketten des Hämoglobins) - steigende Temperatur Folge: - Affinitätsabnahme des Hämoglobins - leichtere Sauerstoffabgabe - erhöhter P50-Wert angelagertes CO an Hämoglobin - hat 300 x höhere Affinität an Hb als O2 - entsteht in geringen Mengen beim Hämabbau Hämoglobin geht in R-Struktur über noch unblockiertes Hämoglobin weist eine erhöhte Affinität zu O2 auf erschwerte Sauerstoffabgabe im Gewebe physiologischer COHb-Anteil: 1% (Raucher: bis zu 10%) Die O2-Bindung an Hämoglobin ist abhängig vom ph und dem CO2-Partialdruck - ph-senkung und pco2-zunahme H + - H + stabilisiert die T-Struktur Stabilisierung der desoxygenierten Hämoglobinform Verminderung der Sauerstoffaffinität Prinzip: Photometrie Puls-Oxymetrie: partielle Sauerstoffsättigung - in-vivo - Messung bei 660 nm (rot) und 940 nm (infrarot) Häm-Oxymetrie: Bestimmung aller Hb-Derivate - in-vitro - 6 unterschiedliche Wellenlängen - genauer als Puls-Oxymetrie Hämoglobin mit oxidiertem Eisen (Fe 3+ ) Reduktion von Fe 3+ durch: NADH-abhängige-MetHb-Reduktase Affinität der restlichen nicht oxidierten Bindungsstellen erhöht physiologischer MetHb-Anteil: 1-2%
7 CO2-Transportformen Haldane-Effekt CO2-Diffusion vom Gewebe ins Blut innere Atmung CO2-Abgabe in den Lungenkapillaren äußere Atmung Die CO2-BIndungskurve po2 der Mitochondrien Prinzip der letzten Wiesen Henderson Hasselbalch-Gleichung
8 beschreibt die Fähigkeit des Hämoglobins, bei O2-Abgabe H + und CO2 aufzunehmen (und umgekehrt) 10 % physikalisch gelöst (= 26,75 ml/l Blut) 5-10 % an Aminogruppen des Hämoglobins gebunden = Carbamino-Hämoglobin 80 % als HCO3 - Gesamtkonzentration im Blut: 500 ml CO2/l Blut Alveole Kapillare Gewebe Kapillare Carboanhydrase H + HbO2 Carboanhydrase H + H + + HbO2 CO2 CO2 + H2O H2CO3 H + + HCO3 - HHb HCO3 - Cl - CO2 CO2 + H2O H2CO3 HCO3 - HHb HCO3 - O2 O2 HCO3 - O2 O2 Cl - SL SL CO2-Konzentration [mmol/l] physiologische Bindungskurve spo2 = 0% spo2 = 100% 1-3 mmhg CO2 chemisch gebunden 10 arteriell gemischt venös pco2 [mmhg] CO2 physikalisch gelöst hyperboler Verlauf ohne Sättigungsplateau SN Zellen am Kapillarende reagieren besonders leicht auf O2-Mangel
9 Pufferkapazität β Puffersysteme geschlossen offen Gesamtkonzentration aller Pufferbasen Bikarbonat-Puffer Konzentration von HCO3 - im Blut log(20) Proteinat-Puffersystem Phosphat-Puffersystem
10 [HA] bzw. [A - ] [mmol/l] geschlossenes Puffersystem: kein Reaktionspartner kann entweichen offenes Puffersystem: - ein Reaktionspartner kann konstant gehalten werden - größere Pufferkapazität Puffersäure [HA] ph 2 4 pks = Pufferkurve für einen Puffer mit pks = 5 β ph = pks Pufferbase! [A - ] SN Steigung der Pufferkurve bei bestimmtem ph beste Pufferkapazität bei ph = pks offenes Puffersystem pks = 6,1 (weit entfernt vom Blut-pH) Konzentration von HCO3 - im Blut: 24 mmol/l (hohe Konzentration wichtiger Puffer) ca. 50% des Gesamtpuffersystems 48 mmol/l (v.a. Bikarbonat- und Proteinatpuffer) Aussage über das metabolische System 1,3 24 mmol/l geschlossenes Puffersystem pks = 6,8 geringe Konzentration geringer Anteil am Gesamtpuffersystem geschlossenes Puffersystem puffert über ionisierbare Aminosäureketten wichtig: Albumin und Hämoglobin ca. 50% des Gesamtpuffersystems
11 Ammonium-Puffer ph-regulation durch die Niere ph-regulation durch die Leber Renale De-novo-Generierung von HCO3 - Atemzentrum Lokalisation Atemrhytmus, Atemfrequenz Chemorezeptoren zentral und peripher Intrazellulärer ph Hering-Breuer-Reflex
12 Ausscheidung fixer Säuren Sekretion von H + Reabsorption von HCO3 - Ausscheidung von NH4 + De-novo-Generierung von HCO3 - offenes Puffersystem pks = 9,1 kaum Bedeutung für die Blutpufferung durch Abbau von Glutamin (aus der Leber) vereinfachte Reaktion: Glutamin 2 NH Oxoglutarat 2 Oxoglutarat 2 HCO3 - Enzyme: - renale Glutaminase - Glutaminatdehydrogenase Aktivierung bei Azidose Bildung von Harnstoff: 2 NH4 + [...] Harnstoff + 2 H + Verbrauch von HCO3 - : 2 H HCO3 - Enzym: hepatische Glutaminase Aktivierung bei Alkalose Bildung von Glutamin: Glutamat + NH3 Glutamin ( Niere) Enzym: Glutamin-Synthetase Aktivierung bei Azidose Zentrale Chemorezeptoren: Lokalisation: Medulla oblongata Lokalisation: Medulla oblongata Messung: pco2 und ph im Liquor Vorgabe des Atemrhythmus: ventrale respiratorische Gruppe Periphere Chemorezeptoren: Lokalisation: Glomus aorticum und Vorgabe der Atemfrequenz: Glomus caroticum dorsale respiratorische Gruppe Messung: pco2, ph und po2 im Blut Leitung: N. vagus und glossopharyngeus Afferenzen: kortikal und peripher (z.b. Chemosensoren) Mechanismus: über Dehnungsrezeptoren im Lungenparenchym 1. Inspiration: Zunehmende Dehnung 2. Weiterleitung der Dehnungsinformation über N.vagus (über Ncl. tractus solitarii) 3. Hemmung der Inspiration ph = 7,2
13 Hyperventilation Hypoventilation Basenüberschuss (BE) Standardbikarbonatkonzentration Aktuelles Bikarbonat Anionenlücke Subtraktionsazidose/-alkalose Additionsazidose/-alkalose
14 verminderte CO2-Abatmung pco2 erhöht (Hyperkapnie) Zunahme von [H + ] Azidose vermehrte CO2-Abatmung pco2 erniedrigt (Hypokapnie) Abnahme von [H + ] Alkalose Definition: Bikarbonatkonzentration im Blut unter Standardbedingungen: - nach Blutbegasung mit pco2 = 40 mmhg, - bei 37 C - 100% O2-Sättigung Normalwert: mmol/l Menge an Säure/Base, die einer Blutprobe zugegeben werden muss, um ph = 7,4 zu erreichen Normalwert: - 3 bis + 3 mmol/l - positiv: Basenüberschuss Säurezugabe - negativ: Basenmangel Basenzugabe Aussage über das metabolische System Aussage über das metabolische System Definition: [Na + ] - ([Cl - ] + [HCO3 - ]) Normalwert: 10 ± 2 mmol/l Definition: Bikarbonatkonzentration unter Blutbedingungen Normalwert: mmol/l geringe Aussagekraft Ursache = erhöhter Säuren-/Basenanfall Ursache = erhöhter Basen-/Säurenverlust
15 Retentionsazidose Ablauf einer Störung des Säure-BaseHaushaltes Primär respiratorische Azidose Primär respiratorische Alkalose Primär metabolische Azidose Primär metabolische Alkalose Auswirkungen einer Azidose auf den Kaliumhaushalt
16 Akute Störung: - Parameter eines Systems verändert (v.a. BE oder pco2) - ph weicht von 7,4 ab Teilkompensierte Störung: - Parameter beider Systeme verändert - ph weicht von 7,4 ab Ursache = beeinträchtigte Säurenausscheidung Voll kompensierte Störung: - Parameter beider Systeme verändert - ph = 7,4 Ursache: Hyperventilation Ursache: Hypoventilation pco2 akut: pco2 akut: Folge: ph Folge: ph, Hypoxie BE akut: normal Standard-HCO3-: normal Kompensation: metabolisch (nach einigen h) BE akut: normal Standard-HCO3-: normal Kompensation: metabolisch (nach einigen h) BE kompensiert: BE kompensiert: pco2 kompensiert: pco2 kompensiert: Ursache: z.b. Verlust von Magensäure Ursache: Keto-/Laktatazidose u.a. BE akut: BE akut: Folge: ph Folge: ph pco2 akut: normal Standard-HCO3-: pco2 akut: normal Standard-HCO3-: Kompensation: respiratorisch (nach Minuten) BE kompensiert: Kompensation: respiratorisch (nach Minuten) BE kompensiert: pco2 kompensiert: pco2 kompensiert: Grundlage: H+/K+-Antiport bei Azidose: H+-Transport ins Zellinnere K+-Antiport ins Blut Hyperkaliämie bei Azidose
Säure-Basen- Haushalt
 Säure-Basen- Haushalt Folie Nr. 1 Grundlagen Normwerte Puffersysteme Störungen Grundlagen BGA Grundlagen: Ziel ist das Gleichgewicht zwischen sauren und alkalischen Substanzen Einheit des Säure-Basen-Gleichgewichts
Säure-Basen- Haushalt Folie Nr. 1 Grundlagen Normwerte Puffersysteme Störungen Grundlagen BGA Grundlagen: Ziel ist das Gleichgewicht zwischen sauren und alkalischen Substanzen Einheit des Säure-Basen-Gleichgewichts
Elektrolythaushalt + Säure-Basen-Haushalt
 Elektrolythaushalt + Säure-Basen-Haushalt Überblick Elektrolythaushalt Natrium Kalium Calcium Magnesium Phosphat Säure-Basen-Haushalt Der Elektrolythaushalt Normwerte: Natrium 135-145 mmol/l Kalium 3.5-5.5
Elektrolythaushalt + Säure-Basen-Haushalt Überblick Elektrolythaushalt Natrium Kalium Calcium Magnesium Phosphat Säure-Basen-Haushalt Der Elektrolythaushalt Normwerte: Natrium 135-145 mmol/l Kalium 3.5-5.5
Kapitel 2.2 Kardiopulmonale Homöostase. Kohlendioxid
 Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Laplace-Gesetz Aufteilung des Bronchialbaums Pneumozyten Intrapleuraler Druck Alveolardruck Transpulmonaler Druck
 Laplace-Gesetz Aufteilung des Bronchialbaums Pneumozyten Intrapleuraler Druck Alveolardruck Transpulmonaler Druck Atemzugvolumen Inspiratorisches Reservevolumen insgesamt 23 Verzweigungen Konduktionszone:
Laplace-Gesetz Aufteilung des Bronchialbaums Pneumozyten Intrapleuraler Druck Alveolardruck Transpulmonaler Druck Atemzugvolumen Inspiratorisches Reservevolumen insgesamt 23 Verzweigungen Konduktionszone:
ABGA. Notfallpflegekongress 2008 Solothurn. Notfallpflege am Stadtspital Triemli Zürich
 ABGA Notfallpflegekongress 2008 Solothurn H. Zahner,, Fachschule für f r Intensiv- und Notfallpflege am Stadtspital Triemli Zürich Werte des pulmonalen Gasaustausches PaO 2 Sauerstoffpartialdruck im arteriellen
ABGA Notfallpflegekongress 2008 Solothurn H. Zahner,, Fachschule für f r Intensiv- und Notfallpflege am Stadtspital Triemli Zürich Werte des pulmonalen Gasaustausches PaO 2 Sauerstoffpartialdruck im arteriellen
Die Blutgasanalyse Was ist außerklinisch tolerabel? KAI 2014 Dr. med. Günter Schrot
 Die Blutgasanalyse Was ist außerklinisch tolerabel? KAI 2014 Dr. med. Günter Schrot Normale Blutgasanalyse ph 7,36-7,44 po2 >80 mmhg pco2 35-45 mmhg HCO3-22 -26 mmol/l berechnet Das Säure-Basen-System
Die Blutgasanalyse Was ist außerklinisch tolerabel? KAI 2014 Dr. med. Günter Schrot Normale Blutgasanalyse ph 7,36-7,44 po2 >80 mmhg pco2 35-45 mmhg HCO3-22 -26 mmol/l berechnet Das Säure-Basen-System
Das Säure-Basen- Gleichgewicht. Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung
 Das Säure-Basen- Gleichgewicht Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung BGA Blutgasanalyse Normalkost körpereigener Stoffwechsel Überschuss
Das Säure-Basen- Gleichgewicht Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung BGA Blutgasanalyse Normalkost körpereigener Stoffwechsel Überschuss
Thema: Säure-Basen-Haushalt
 Säure-Basen-Haushalt Seite 1 Thema: Säure-Basen-Haushalt 1 Grundlagen Die ph-regulation des Körpers ist von grundlegender Bedeutung für seine Funktion. Der ph-wert ist ein Maß für die Wasserstoffionenkonzentration(Wasserstoffionen
Säure-Basen-Haushalt Seite 1 Thema: Säure-Basen-Haushalt 1 Grundlagen Die ph-regulation des Körpers ist von grundlegender Bedeutung für seine Funktion. Der ph-wert ist ein Maß für die Wasserstoffionenkonzentration(Wasserstoffionen
Kardiopulmonale Homöostase
 Kapitel 2 Kardiopulmonale Homöostase Primäre Funktion des Blutes im Rahmen der Atmung Transport von O 2 aus der Lunge zum peripheren Gewebe, CO 2 aus der Peripherie zu den Lungen, H + vom Gewebe zu den
Kapitel 2 Kardiopulmonale Homöostase Primäre Funktion des Blutes im Rahmen der Atmung Transport von O 2 aus der Lunge zum peripheren Gewebe, CO 2 aus der Peripherie zu den Lungen, H + vom Gewebe zu den
Das Säure-Basen- Gleichgewicht. Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung
 Das Säure-Basen- Gleichgewicht Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung BGA Blutgasanalyse Normalkost körpereigener Stoffwechsel Überschuss
Das Säure-Basen- Gleichgewicht Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung BGA Blutgasanalyse Normalkost körpereigener Stoffwechsel Überschuss
Elektrolythaushalt + Säure-Basen-Haushalt
 Elektrolythaushalt + Säure-Basen-Haushalt Überblick Elektrolythaushalt Natrium Kalium Calcium Magnesium Phosphat Säure-Basen-Haushalt Der Elektrolythaushalt Normwerte im Blut: Natrium 135-145 mmol/l Kalium
Elektrolythaushalt + Säure-Basen-Haushalt Überblick Elektrolythaushalt Natrium Kalium Calcium Magnesium Phosphat Säure-Basen-Haushalt Der Elektrolythaushalt Normwerte im Blut: Natrium 135-145 mmol/l Kalium
Thema: Säure-Basen-Haushalt
 Säure-Basen-Haushalt Seite 1 Thema: Säure-Basen-Haushalt 1 Grundlagen Die ph-regulation des Körpers ist von grundlegender Bedeutung für seine Funktion. Der ph-wert ist ein Maß für die Wasserstoffionenkonzentration(Wasserstoffionen
Säure-Basen-Haushalt Seite 1 Thema: Säure-Basen-Haushalt 1 Grundlagen Die ph-regulation des Körpers ist von grundlegender Bedeutung für seine Funktion. Der ph-wert ist ein Maß für die Wasserstoffionenkonzentration(Wasserstoffionen
Physiologie der Atmung. Cem Ekmekcioglu
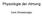 Physiologie der Atmung Cem Ekmekcioglu Übersicht über den Transportweg des Sauerstoffes beim Menschen Schmidt/Thews: Physiologie des Menschen, 27.Auflage, Kap.25, Springer (1997) Klinke, Pape, Silbernagl,
Physiologie der Atmung Cem Ekmekcioglu Übersicht über den Transportweg des Sauerstoffes beim Menschen Schmidt/Thews: Physiologie des Menschen, 27.Auflage, Kap.25, Springer (1997) Klinke, Pape, Silbernagl,
Blutgasanalyse UNIVERSITÄT DES SAARLANDES. Probenahme, Parameter, usw. für MTAF-Schule. Jung R. 26. März 2015. Institut für Arbeitsmedizin der
 Probenahme, Parameter, usw. für MTAF-Schule Jung R. Institut für Arbeitsmedizin der UNIVERSITÄT DES SAARLANDES 26. März 2015 - ph - Werte Blutgasnormwerte Messung von ph-wert sowie den Partialdrücken po2
Probenahme, Parameter, usw. für MTAF-Schule Jung R. Institut für Arbeitsmedizin der UNIVERSITÄT DES SAARLANDES 26. März 2015 - ph - Werte Blutgasnormwerte Messung von ph-wert sowie den Partialdrücken po2
Protonenstoffwechsel. Puffersysteme des Blutes und des Organismus. Puffersysteme des Blutes und des Organismus Bicarbonat-Puffer
 Protonenstoffwechsel Puffersysteme des Blutes und des Organismus Die Summe aller im biologischen ph-bereich im Blut zur Aufnahme von H + befähigten Valenzen Anteil an Konzentration system % 50 pk a 6,1!
Protonenstoffwechsel Puffersysteme des Blutes und des Organismus Die Summe aller im biologischen ph-bereich im Blut zur Aufnahme von H + befähigten Valenzen Anteil an Konzentration system % 50 pk a 6,1!
Säure-Basen-Haushalt
 Säure-Basen-Haushalt Voraussetzungen Kenntnisse über Gas-Partialdrücke und Formen des O 2 - bzw. CO 2 -Transportes im Blut, Rolle der Erythrozyten, Aufbau und Funktion des Hämoglobinmoleküls, Puffereigenschaften
Säure-Basen-Haushalt Voraussetzungen Kenntnisse über Gas-Partialdrücke und Formen des O 2 - bzw. CO 2 -Transportes im Blut, Rolle der Erythrozyten, Aufbau und Funktion des Hämoglobinmoleküls, Puffereigenschaften
Sauerstoffbindung im Blut
 Sauerstoffbindung im Blut Die Fähigkeit uns zu wundern, ist das Einzige, was wir brauchen, um gute Philosophen zu werden. Gaarder Jostein, Sofies Welt 1 Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung...
Sauerstoffbindung im Blut Die Fähigkeit uns zu wundern, ist das Einzige, was wir brauchen, um gute Philosophen zu werden. Gaarder Jostein, Sofies Welt 1 Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung...
Gliederung. Puffersysteme. Wofür Puffersysteme? Wofür Puffersysteme? Wofür Puffersysteme? ph-verhältnisse im Körper. Puffersysteme
 Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Atmung II Atemgastransport Pathophysiologie
 Atmung II Atemgastransport Pathophysiologie Einführung Äußere und Innere Atmung Atemgastransport Normwerte Atemgastransport Das Blut Eine wesentliche Aufgabe des Blutes ist der Atemgastransport : Das Blut
Atmung II Atemgastransport Pathophysiologie Einführung Äußere und Innere Atmung Atemgastransport Normwerte Atemgastransport Das Blut Eine wesentliche Aufgabe des Blutes ist der Atemgastransport : Das Blut
KliChi. Klinische Chemie & Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Analytik und Blutgasanalytik. Dr. med. Bernhard Schlüter - 1 -
 Sommersemester 2012-1 - Klinische Chemie & Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Analytik und Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium Universitätsklinikum
Sommersemester 2012-1 - Klinische Chemie & Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Analytik und Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium Universitätsklinikum
Der ph-wert des Blutplasmas zeigt an, ob das Gleichgewicht zwischen +
 Diagnostik Säure-Basen-Status Unter dem Säure-Basen-Status versteht man die Summe derjenigen Messund Rechengrößen, die eine Diagnostik der Störungen des Säure-Basen- Haushaltes ermöglichen. Dazu gehören
Diagnostik Säure-Basen-Status Unter dem Säure-Basen-Status versteht man die Summe derjenigen Messund Rechengrößen, die eine Diagnostik der Störungen des Säure-Basen- Haushaltes ermöglichen. Dazu gehören
Interpretation. Kapitel 4. Kasuistik 1 (1)
 Kapitel 4 Interpretation Kasuistik 1 (1) In der Notaufnahme werden Sie zu einem älteren Herrn gerufen, den seine Tochter gerade wegen Atemnot ins Krankenhaus gebracht hat. Anamnestisch ist ein chronischer
Kapitel 4 Interpretation Kasuistik 1 (1) In der Notaufnahme werden Sie zu einem älteren Herrn gerufen, den seine Tochter gerade wegen Atemnot ins Krankenhaus gebracht hat. Anamnestisch ist ein chronischer
12 Säure-Basen-Haushalt
 12.1 Der ph-wert in Körperflüssigkeiten 281 Gotthold Gäbel Der ph-wert der extrazellulären Flüssigkeit wird in einem sehr engen Bereich zwischen 7,36 und 7,44 gehalten. Dies geschieht über Puffersysteme,
12.1 Der ph-wert in Körperflüssigkeiten 281 Gotthold Gäbel Der ph-wert der extrazellulären Flüssigkeit wird in einem sehr engen Bereich zwischen 7,36 und 7,44 gehalten. Dies geschieht über Puffersysteme,
Atemgastransport im Blut
 Atemgastransport im Blut Institut für MTA-Ausbildung am Klinikum Osnabrück Fachgebiet Anatomie/Physiologie/Krankheitslehre - Dr. U. Krämer 1. Physikalische Löslichkeit der Atemgase Sauerstoff und Kohlendioxid
Atemgastransport im Blut Institut für MTA-Ausbildung am Klinikum Osnabrück Fachgebiet Anatomie/Physiologie/Krankheitslehre - Dr. U. Krämer 1. Physikalische Löslichkeit der Atemgase Sauerstoff und Kohlendioxid
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9)
 Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 1. Funktion des Hämoglobins Sauerstoff
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 1. Funktion des Hämoglobins Sauerstoff
Allgemeines: Konzentration des Hämoglobins im Blut: 160 g/l Verpackung im Erythrocyten -> kolloidosmotisch unwirksam -> beeinträchtigt nicht den Wasse
 Hämoglobin Allgemeines: Konzentration des Hämoglobins im Blut: 160 g/l Verpackung im Erythrocyten -> kolloidosmotisch unwirksam -> beeinträchtigt nicht den Wasseraustausch im Kapillarbereich Durch die
Hämoglobin Allgemeines: Konzentration des Hämoglobins im Blut: 160 g/l Verpackung im Erythrocyten -> kolloidosmotisch unwirksam -> beeinträchtigt nicht den Wasseraustausch im Kapillarbereich Durch die
Ungefähre Zusammensetzung des Blutes und des Blutplasmas. Die häufigsten Bestandteile des Blutplasmas (Mittelwerte)
 Puffer /Zusammensetzung des Blutes 1 Zusammensetzung des Blutes Das Blut der Wirbeltiere besteht zu 55% aus flüssigem Blutplasma und zu 45% aus darin schwimmenden festen Bestandteilen, den Blutkörperchen.
Puffer /Zusammensetzung des Blutes 1 Zusammensetzung des Blutes Das Blut der Wirbeltiere besteht zu 55% aus flüssigem Blutplasma und zu 45% aus darin schwimmenden festen Bestandteilen, den Blutkörperchen.
Klinische Chemie und Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Haushalt und Blutgasanalytik
 Klinische Chemie und Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Haushalt und Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium Universitätsklinikum Münster
Klinische Chemie und Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Haushalt und Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium Universitätsklinikum Münster
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Willy Bauhuber KfH Nierenzentrum im Klinikum Rosenheim
 Willy Bauhuber KfH Nierenzentrum im Klinikum Rosenheim über 5500 Fundstellen bei GOOGLE meist Alternativmedizin Fehlernärung, Bewegungsmangel, Stress... führen zu schädlicher Übersäuerung Behandlung durch
Willy Bauhuber KfH Nierenzentrum im Klinikum Rosenheim über 5500 Fundstellen bei GOOGLE meist Alternativmedizin Fehlernärung, Bewegungsmangel, Stress... führen zu schädlicher Übersäuerung Behandlung durch
Atemreiz und Schwimmbad-Blackout
 Thema: Atemreiz und Schwimmbad-Blackout Zielgruppe: Medizinisch interessierte Taucher Referent: Martijn Damen, TL1 Tauchsportklub Erlangen e.v. http://www.tske.de 1 Agenda Atemzentrum Steuerung der Atmung
Thema: Atemreiz und Schwimmbad-Blackout Zielgruppe: Medizinisch interessierte Taucher Referent: Martijn Damen, TL1 Tauchsportklub Erlangen e.v. http://www.tske.de 1 Agenda Atemzentrum Steuerung der Atmung
Kurstag 3. Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers
 Kurstag Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung: Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Kurstag Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung: Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Alveolo-arterielle Sauerstoffpartialdruckdifferenz, vereinfachte Berechnung
 A Druck A Alveolo-arterielle Sauerstoffpartialdruckdifferenz, vereinfachte Berechnung Synonyme nalveolo-arterielle Sauerstoffdruckdifferenz nalveolo-arterielle Sauerstoffdifferenz naad - (vereinfacht)
A Druck A Alveolo-arterielle Sauerstoffpartialdruckdifferenz, vereinfachte Berechnung Synonyme nalveolo-arterielle Sauerstoffdruckdifferenz nalveolo-arterielle Sauerstoffdifferenz naad - (vereinfacht)
Grundlagen der Chemie Säuren und Basen
 Säuren und Basen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Säure-Base-Theorien Die Begriffe Säure und Base
Säuren und Basen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Säure-Base-Theorien Die Begriffe Säure und Base
Blutgasanalyse & Säure-Basen-Status
 Blutgasanalyse & Säure-Basen-Status Präanalytik 1 3 Allgemein Einflussfaktoren wichtig für klinische Diagnostik Überwachung / Nachweis Diffusionsstörungen Ventilationsstörungen Perfusionsstörungen Störungen
Blutgasanalyse & Säure-Basen-Status Präanalytik 1 3 Allgemein Einflussfaktoren wichtig für klinische Diagnostik Überwachung / Nachweis Diffusionsstörungen Ventilationsstörungen Perfusionsstörungen Störungen
Ein erhöhter PaCO 2 in Verbindung mit einem erniedrigten ph-wert ist das Kennzeichen einer akuten respiratorischen Azidose.
 Respiratorische Azidose Akute respiratorische Azidose Ein erhöhter PaCO 2 in Verbindung mit einem erniedrigten phwert ist das Kennzeichen einer akuten respiratorischen Azidose. Chronische respiratorische
Respiratorische Azidose Akute respiratorische Azidose Ein erhöhter PaCO 2 in Verbindung mit einem erniedrigten phwert ist das Kennzeichen einer akuten respiratorischen Azidose. Chronische respiratorische
Mehrprotonige Säuren (z.b. H 2 SO 4 )
 Mehrprotonige Säuren (z.b. H SO 4 ) Mehrprotonige Säuren protolysieren stufenweise. Jede Stufe hat eine eigene Säurekonstante, deren Werte von Stufe zu Stufe kleiner werden (die Protolyse wird immer unvollständiger).
Mehrprotonige Säuren (z.b. H SO 4 ) Mehrprotonige Säuren protolysieren stufenweise. Jede Stufe hat eine eigene Säurekonstante, deren Werte von Stufe zu Stufe kleiner werden (die Protolyse wird immer unvollständiger).
HA + B A - + HB + Säuren und Basen. Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor!
 Säuren und Basen Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor! Die Tendenz ein Proton abzuspalten (Säure) bzw. aufzunehmen (Base) bezeichnet man als Säure-
Säuren und Basen Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor! Die Tendenz ein Proton abzuspalten (Säure) bzw. aufzunehmen (Base) bezeichnet man als Säure-
Niere Salz-/Wasserhaushalt 2009
 Aus: Gray's Anatomy: Descriptive and Surgical Theory United Kingdom 1858 Zentrale Aufgaben der Nieren Regulation des Wasserhaushaltes Regulation des Mineralhaushaltes (Osmolarität) Regulation des Säure-Basen-Haushaltes
Aus: Gray's Anatomy: Descriptive and Surgical Theory United Kingdom 1858 Zentrale Aufgaben der Nieren Regulation des Wasserhaushaltes Regulation des Mineralhaushaltes (Osmolarität) Regulation des Säure-Basen-Haushaltes
Grundlagen der Ernährungslehre
 Grundlagen der Ernährungslehre Wasser Elektrolyt Säuren-Basen Haushalt des Organismus Wasserhaushalt des Organismus Funktionen des Wassers im tierischen Organismus Bestandteil vieler zellulärer und subzellulärer
Grundlagen der Ernährungslehre Wasser Elektrolyt Säuren-Basen Haushalt des Organismus Wasserhaushalt des Organismus Funktionen des Wassers im tierischen Organismus Bestandteil vieler zellulärer und subzellulärer
Pneumologische Funktionsdiagnostik. Grundlagen I Anatomie und Physiologie
 Pneumologische Funktionsdiagnostik Grundlagen I Anatomie und Physiologie Inhalt 1.1 1.1.1 1.2.2 1.2 1.2.1 1.2.2 1.2.3 Anatomische Grundlagen obere Luftwege untere Luftwege Physiologische Grundlagen Atemmechanik
Pneumologische Funktionsdiagnostik Grundlagen I Anatomie und Physiologie Inhalt 1.1 1.1.1 1.2.2 1.2 1.2.1 1.2.2 1.2.3 Anatomische Grundlagen obere Luftwege untere Luftwege Physiologische Grundlagen Atemmechanik
Lungenfunktionstest. Die Spirometrie ("kleine Lungenfunktion", spirare (lat.): atmen) dient zur Messung des Lungen- bzw. Atemvolumens.
 Die Spirometrie ("kleine Lungenfunktion", spirare (lat.): atmen) dient zur Messung des Lungen- bzw. Atemvolumens. Beides sind wichtige Messgrößen, um Verlauf und Schwere von Lungenerkrankungen einzuschätzen.
Die Spirometrie ("kleine Lungenfunktion", spirare (lat.): atmen) dient zur Messung des Lungen- bzw. Atemvolumens. Beides sind wichtige Messgrößen, um Verlauf und Schwere von Lungenerkrankungen einzuschätzen.
ph-wert Berechnung für starke Säuren / Basen starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1
![ph-wert Berechnung für starke Säuren / Basen starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 ph-wert Berechnung für starke Säuren / Basen starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1](/thumbs/33/16365353.jpg) ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
Blutgasanalyse 03.06.14. Welche Konsequenzen hat das Ergebnis? Vortragsziele. ph-wert Puffersysteme im Blut. Bestandteile der Blutgasanalyse
 Blutgasanalyse Welche Konsequenzen hat das Ergebnis? Präsentation: Dr.R.Doppler Medizinische Abteilung LKH-Bruck/Mur Vortragsziele Interpretation der einzelnen Messwerte der Blutgasanalyse Erkennen von
Blutgasanalyse Welche Konsequenzen hat das Ergebnis? Präsentation: Dr.R.Doppler Medizinische Abteilung LKH-Bruck/Mur Vortragsziele Interpretation der einzelnen Messwerte der Blutgasanalyse Erkennen von
Azidosen, Alkalosen. Störungen der Regulation des Säure-Basen-Haushalts führen zu Alkalosen oder Azidosen.
 Allgemeine Pathologie: Azidosen, Alkalosen Störungen der Regulation des Säure-Basen-Haushalts führen zu Alkalosen oder Azidosen. Sie beruhen im wesentlichen auf Erkrankungen oder Funktionsstörungen der
Allgemeine Pathologie: Azidosen, Alkalosen Störungen der Regulation des Säure-Basen-Haushalts führen zu Alkalosen oder Azidosen. Sie beruhen im wesentlichen auf Erkrankungen oder Funktionsstörungen der
Physiologische Grundlagen der Ausdauer
 Lisa Maria Hirschfelder Aus der Reihe: e-fellows.net stipendiaten-wissen e-fellows.net (Hrsg.) Band 340 Physiologische Grundlagen der Ausdauer Leistungssport - Ausdauer-Grundlagen Skript Physiologische
Lisa Maria Hirschfelder Aus der Reihe: e-fellows.net stipendiaten-wissen e-fellows.net (Hrsg.) Band 340 Physiologische Grundlagen der Ausdauer Leistungssport - Ausdauer-Grundlagen Skript Physiologische
Klinische Chemie und Hämatologie Vorlesung: Blutgasanalyse
 Klinische Chemie und Hämatologie Vorlesung: Blutgasanalyse Dr. med. Bernhard Schlüter Institut für Klinische Chemie und Laboratoriumsmedizin/Zentrallaboratorium Westfälische Wilhelms-Universität Münster
Klinische Chemie und Hämatologie Vorlesung: Blutgasanalyse Dr. med. Bernhard Schlüter Institut für Klinische Chemie und Laboratoriumsmedizin/Zentrallaboratorium Westfälische Wilhelms-Universität Münster
Metabolische Alkalose
 Metabolische Alkalose PD Dr. Martin Bek, Medizinische Klinik und Poliklinik D, UKM, Münster 1) Diagnose einer metabolischen Alkalose A) Unterscheidung von Azidose/Alkalose Azidose (ph7.42)
Metabolische Alkalose PD Dr. Martin Bek, Medizinische Klinik und Poliklinik D, UKM, Münster 1) Diagnose einer metabolischen Alkalose A) Unterscheidung von Azidose/Alkalose Azidose (ph7.42)
BIOCHEMIE I Teil 5 und 6
 Titrationskurve einer schwachen Säure mit einer starken Base. BIOCHEMIE I Teil 5 und 6 13 Äquivalenzpunkt Äquivalenzpunkt: Essigsäure vollständig dissoziiert. Bei zunehmender Menge an NaOH nähert sich
Titrationskurve einer schwachen Säure mit einer starken Base. BIOCHEMIE I Teil 5 und 6 13 Äquivalenzpunkt Äquivalenzpunkt: Essigsäure vollständig dissoziiert. Bei zunehmender Menge an NaOH nähert sich
Physiologie der Respiration
 Physiologie der Respiration Margarethe Geiger, Zentrum für Biomolekulare Medizin und Pharmakologie, Institut für Gefäßbiologie und Thromboseforschung 1) Mechanik der Atmung Lungenvolumina Abbildung 1:
Physiologie der Respiration Margarethe Geiger, Zentrum für Biomolekulare Medizin und Pharmakologie, Institut für Gefäßbiologie und Thromboseforschung 1) Mechanik der Atmung Lungenvolumina Abbildung 1:
Proxima. pco 2 und berechnete Werte für HCO 3 und Basenüberschuss auf Proxima
 Funktionsprinzipien Der ProximaSensor wird als einzelner Multi ParameterChip hergestellt, der eine Reihe einzelner Sensoren beinhaltet, die jeweils einen anderen Parameter messen. Der pco 2 wird direktpotentiometrisch
Funktionsprinzipien Der ProximaSensor wird als einzelner Multi ParameterChip hergestellt, der eine Reihe einzelner Sensoren beinhaltet, die jeweils einen anderen Parameter messen. Der pco 2 wird direktpotentiometrisch
Säure-Basen-Haushalt, Blutgase
 Säure-Basen-Haushalt, Blutgase Grundlagen Allgemeine Pathobiochemie Kohlendioxid CO 2, Kohlensäure H 2 CO 3 nichtflüchtige Säuren Puffersysteme renale Mechanismen Störungen und Kompensation Spezielle Pathobiochemie
Säure-Basen-Haushalt, Blutgase Grundlagen Allgemeine Pathobiochemie Kohlendioxid CO 2, Kohlensäure H 2 CO 3 nichtflüchtige Säuren Puffersysteme renale Mechanismen Störungen und Kompensation Spezielle Pathobiochemie
Ein Puffer ist eine Mischung aus einer schwachen Säure/Base und ihrer Korrespondierenden Base/Säure.
 2.8 Chemische Stoßdämpfer Puffersysteme V: ph- Messung eines Gemisches aus HAc - /AC - nach Säure- bzw Basen Zugabe; n(naac) = n(hac) > Acetat-Puffer. H2O Acetat- Puffer H2O Acetat- Puffer Die ersten beiden
2.8 Chemische Stoßdämpfer Puffersysteme V: ph- Messung eines Gemisches aus HAc - /AC - nach Säure- bzw Basen Zugabe; n(naac) = n(hac) > Acetat-Puffer. H2O Acetat- Puffer H2O Acetat- Puffer Die ersten beiden
Säure-Basen Haushalt Samuel Fuchs
 Säure-Basen Haushalt 21.06.2013 Samuel Fuchs Inhaltsverzeichnis HERKUNFT DER SÄUREN IM KÖRPER... 4 WAS SIND SÄUREN?... 4 WAS SIND BASEN?... 4 PH-WERT... 4 KOHLENDIOXID CO2... 5 DIE PUFFERSYSTEME... 5 WIRKUNGSZEIT...
Säure-Basen Haushalt 21.06.2013 Samuel Fuchs Inhaltsverzeichnis HERKUNFT DER SÄUREN IM KÖRPER... 4 WAS SIND SÄUREN?... 4 WAS SIND BASEN?... 4 PH-WERT... 4 KOHLENDIOXID CO2... 5 DIE PUFFERSYSTEME... 5 WIRKUNGSZEIT...
Störungen des Säure-Basen-Haushalts
 3 Störungen des Säure-Basen-Haushalts Normalerweise wird der extrazelluläre ph-wert durch verschiedene Puffersysteme und Kompensationsmechanismen innerhalb sehr enger Grenzen (Norm: 7,38 7,42) reguliert,
3 Störungen des Säure-Basen-Haushalts Normalerweise wird der extrazelluläre ph-wert durch verschiedene Puffersysteme und Kompensationsmechanismen innerhalb sehr enger Grenzen (Norm: 7,38 7,42) reguliert,
Das oxygen window Tauchmedizinische Fortbildungen. Was ist das eigentlich? Dr.med. Stefan Wiese
 Das oxygen window Tauchmedizinische Fortbildungen Was ist das eigentlich? www.baromedizin.de Dr.med. Stefan Wiese intensive care Eindhoven, Netherlands vakanter Partialdruck Oxygen window window partial
Das oxygen window Tauchmedizinische Fortbildungen Was ist das eigentlich? www.baromedizin.de Dr.med. Stefan Wiese intensive care Eindhoven, Netherlands vakanter Partialdruck Oxygen window window partial
Säure-Basen-Status und Blutgase: Einleitung
 Institut für MTA-Ausbildung am Klinikum Osnabrück Fachgebiet Klinische Chemie Dr. Uwe Krämer Säure-Basen-Status und Blutgase: Einleitung Durch die Blutgasanalytik erfasst man: die Versorgung des Organismus
Institut für MTA-Ausbildung am Klinikum Osnabrück Fachgebiet Klinische Chemie Dr. Uwe Krämer Säure-Basen-Status und Blutgase: Einleitung Durch die Blutgasanalytik erfasst man: die Versorgung des Organismus
Pneumologische Funktionsdiagnostik. 7. Blutgasanalyse
 Pneumologische Funktionsdiagnostik 7. Blutgasanalyse Inhalt 7.1 Allgemeines 7.2 Säure-Base-Haushalt 7.3 Puffer-Systeme 7.4 Metabolische Einflüsse auf die BGA 7.5 Parameter Atemfunktion 7.6 Respiratorische
Pneumologische Funktionsdiagnostik 7. Blutgasanalyse Inhalt 7.1 Allgemeines 7.2 Säure-Base-Haushalt 7.3 Puffer-Systeme 7.4 Metabolische Einflüsse auf die BGA 7.5 Parameter Atemfunktion 7.6 Respiratorische
Atmungsphysiologie II.
 Atmungsphysiologie II. 29. Gasaustausch in der Lunge. 30. Sauerstofftransport im Blut. 31. Kohlendioxidtransport im Blut. prof. Gyula Sáry Gasaustausch in der Lunge Gasdiffusion findet durch die Kapillarmembrane
Atmungsphysiologie II. 29. Gasaustausch in der Lunge. 30. Sauerstofftransport im Blut. 31. Kohlendioxidtransport im Blut. prof. Gyula Sáry Gasaustausch in der Lunge Gasdiffusion findet durch die Kapillarmembrane
Physik für Mediziner und Zahnmediziner
 Physik für Mediziner und Zahnmediziner Vorlesung 21 Prof. F. Wörgötter (nach M. Seibt) -- Physik für Mediziner und Zahnmediziner 1 Gase (insbesondere: im Körper) aus: Klinke/Silbernagel: Lehrbuch der Physiologie
Physik für Mediziner und Zahnmediziner Vorlesung 21 Prof. F. Wörgötter (nach M. Seibt) -- Physik für Mediziner und Zahnmediziner 1 Gase (insbesondere: im Körper) aus: Klinke/Silbernagel: Lehrbuch der Physiologie
Nichtinvasive Notfallbeatmung. Aus : Der Notarzt, 5/2009, S.168ff; C. Dodt
 Nichtinvasive Notfallbeatmung Aus : Der Notarzt, 5/2009, S.168ff; C. Dodt Einleitung Häufigste Ursachen der respiratorischen Insuffizienz in der Präklinik : - akut exacerbierte COPD ( aecopd ) - Lungenödem
Nichtinvasive Notfallbeatmung Aus : Der Notarzt, 5/2009, S.168ff; C. Dodt Einleitung Häufigste Ursachen der respiratorischen Insuffizienz in der Präklinik : - akut exacerbierte COPD ( aecopd ) - Lungenödem
7. Biochemie Seminar
 7. Biochemie Seminar Regulation des Wasser und Elektrolythaushalts: Hormonelle Regulation durch ADH Die Funktion dieses Hormons liegt in einer Blutdrucksteigerung und einer Antidiurese. ADH (auch Vasopressin
7. Biochemie Seminar Regulation des Wasser und Elektrolythaushalts: Hormonelle Regulation durch ADH Die Funktion dieses Hormons liegt in einer Blutdrucksteigerung und einer Antidiurese. ADH (auch Vasopressin
ph-wert Berechnung für starke Säuren / Basen
 ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH Na + aq + OH starke Base,
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH Na + aq + OH starke Base,
NICHT INVASIVE HÄMOGLOBIN BESTIMMUNG BEI BLUTSPENDERN. Ariane Sümnig Abt. Transfusionsmedizin Universitätsmedizin Greifswald
 NICHT INVASIVE HÄMOGLOBIN BESTIMMUNG BEI BLUTSPENDERN Ariane Sümnig Abt. Transfusionsmedizin Universitätsmedizin Greifswald ZWEI STUDIEN > MASIMO PRONTO 7 > ähnlich der Pulsoxymetrie > Licht unterschiedlicher
NICHT INVASIVE HÄMOGLOBIN BESTIMMUNG BEI BLUTSPENDERN Ariane Sümnig Abt. Transfusionsmedizin Universitätsmedizin Greifswald ZWEI STUDIEN > MASIMO PRONTO 7 > ähnlich der Pulsoxymetrie > Licht unterschiedlicher
HYPOXIETRAINING WAS VERSTEHT MAN UNTER HYPOXIE? WAS IST IN DER HÖHE ANDERS?
 ???? IMSB-Austria 1 WAS VERSTEHT MAN UNTER? WAS IST IN DER HÖHE ANDERS? IMSB-Austria 2 1 WELCHE VERÄNDERUNGEN SIND ZU ERWARTEN? ARTEN DES S IMSB-Austria 3 ERFAHRUNGEN DISKUSSION IMSB-Austria 4 2 TRAINING
???? IMSB-Austria 1 WAS VERSTEHT MAN UNTER? WAS IST IN DER HÖHE ANDERS? IMSB-Austria 2 1 WELCHE VERÄNDERUNGEN SIND ZU ERWARTEN? ARTEN DES S IMSB-Austria 3 ERFAHRUNGEN DISKUSSION IMSB-Austria 4 2 TRAINING
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo
 Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de innere Energie U Energieumsatz bei
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de innere Energie U Energieumsatz bei
Sauerstofftransport im Blut. von Ralph Althoff Christoph Mittmann
 Sauerstofftransport im Blut von Ralph Althoff Christoph Mittmann Gliederung des Vortrags 1.) Geschichtliches 2.) Eigenschaften des Blutes 3.) Aufbau des Blutes 4.) Der Sauerstofftransporter 5.) Die Chemie
Sauerstofftransport im Blut von Ralph Althoff Christoph Mittmann Gliederung des Vortrags 1.) Geschichtliches 2.) Eigenschaften des Blutes 3.) Aufbau des Blutes 4.) Der Sauerstofftransporter 5.) Die Chemie
Elektrolyte. (aus: Goldenberg, SOL)
 Elektrolyte Elektrolyte leiten in wässriger Lösung Strom. Zu den Elektrolyten zählen Säuren, Basen und Salze, denn diese alle liegen in wässriger Lösung zumindest teilweise in Ionenform vor. Das Ostwaldsche
Elektrolyte Elektrolyte leiten in wässriger Lösung Strom. Zu den Elektrolyten zählen Säuren, Basen und Salze, denn diese alle liegen in wässriger Lösung zumindest teilweise in Ionenform vor. Das Ostwaldsche
ph-wert Berechnung für starke Säuren / Basen
 ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
Messverfahren. Entnahme von Proben für die Blutgasanalyse
 Kapitel 3 Messverfahren Entnahme von Proben für die Blutproben für die BGA werden in heparinisierten Spritzen oder Kapillaren entnommen (Heparin ist sauer: nur ganz geringe Mengen verwenden!) Luftblasen
Kapitel 3 Messverfahren Entnahme von Proben für die Blutproben für die BGA werden in heparinisierten Spritzen oder Kapillaren entnommen (Heparin ist sauer: nur ganz geringe Mengen verwenden!) Luftblasen
Säure - Base - Theorien
 Säure Base Theorien S. Arrhenius (1887) Säuren sind Stoffe, die in wässriger Lösung H + (aq) Ionen bilden, während Basen OH (aq) Ionen bilden. H 2 SO 4, HNO 3, HCl, NaOH, Ba(OH) 2, aber: NH 3, CH 3, OCH
Säure Base Theorien S. Arrhenius (1887) Säuren sind Stoffe, die in wässriger Lösung H + (aq) Ionen bilden, während Basen OH (aq) Ionen bilden. H 2 SO 4, HNO 3, HCl, NaOH, Ba(OH) 2, aber: NH 3, CH 3, OCH
Rationale Basisdiagnostik bei Elektrolytstörungen
 Rationale Basisdiagnostik bei Elektrolytstörungen Siegfried Waldegger Kindernephrologie Innsbruck Department für Kinder und Jugendheilkunde Elektrolytstörungen in Zusammenhang mit angeborenen Erkrankungen
Rationale Basisdiagnostik bei Elektrolytstörungen Siegfried Waldegger Kindernephrologie Innsbruck Department für Kinder und Jugendheilkunde Elektrolytstörungen in Zusammenhang mit angeborenen Erkrankungen
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Der globale Kohlenstoffkreislauf
 Der globale Kohlenstoffkreislauf Eine wesentliche Motivation für die Untersuchung des globalen Kohlenstoffkreislaufs ist der anthropogen bedingte Anstieg der atmosphärischen Konzentration von klimarelevanten
Der globale Kohlenstoffkreislauf Eine wesentliche Motivation für die Untersuchung des globalen Kohlenstoffkreislaufs ist der anthropogen bedingte Anstieg der atmosphärischen Konzentration von klimarelevanten
Aufgabengruppe BMS Chemie
 Aufgabengruppe BMS Chemie Zeitvorgabe: Bitte lösen Sie die folgenden 24 Aufgaben innerhalb von 18 Minuten! 1) Welche Aussagen treffen auf Proteine zu? I. Die Primärstruktur gibt die Aminosäurenabfolge
Aufgabengruppe BMS Chemie Zeitvorgabe: Bitte lösen Sie die folgenden 24 Aufgaben innerhalb von 18 Minuten! 1) Welche Aussagen treffen auf Proteine zu? I. Die Primärstruktur gibt die Aminosäurenabfolge
Säuren- und Basendefinition nach Arrhenius
 Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Säuren- und Basendefinition nach Arrhenius
 Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Herz und Kreislauf Teil 1
 24. TOGGENBURGER ANÄSTHESIE REPETITORIUM Herz und Kreislauf Teil 1 Aufgaben des Kreislaufs Salome Machaidze Miodrag Filipovic miodrag.filipovic@kssg.ch Anästhesiologie & Intensivmedizin Unter Verwendung
24. TOGGENBURGER ANÄSTHESIE REPETITORIUM Herz und Kreislauf Teil 1 Aufgaben des Kreislaufs Salome Machaidze Miodrag Filipovic miodrag.filipovic@kssg.ch Anästhesiologie & Intensivmedizin Unter Verwendung
DIE KLINISCHE BIOCHEMIE DES SÄURE-BASEN HAUSHALTES
 DIE KLINISCHE BIOCHEMIE DES SÄURE-BASEN HAUSHALTES Der Kampf des Lebens gegen Hydrogenionen. Hydrogenion(H + )-Homeostase Unverzichtbar für das Leben: Mitochondriale Funktion Aufladen und Form der Proteine
DIE KLINISCHE BIOCHEMIE DES SÄURE-BASEN HAUSHALTES Der Kampf des Lebens gegen Hydrogenionen. Hydrogenion(H + )-Homeostase Unverzichtbar für das Leben: Mitochondriale Funktion Aufladen und Form der Proteine
Danke für Ihr Interesse an dieser Präsentation! 2019 WK-Fortbildungen
 Danke für Ihr Interesse an dieser Präsentation! Wir möchten Sie darauf hinweisen, dass diese Präsentation das Eigentum des Erstellers ist. Jede Verwertung außerhalb der engen Grenzen des Urheberrechts
Danke für Ihr Interesse an dieser Präsentation! Wir möchten Sie darauf hinweisen, dass diese Präsentation das Eigentum des Erstellers ist. Jede Verwertung außerhalb der engen Grenzen des Urheberrechts
Metabolische Azidose
 Metabolische Azidose PD Dr. Martin Bek, Medizinische Klinik und Poliklinik D, UKM, Münster 1) Säure/Basenproduktion Normaler arterieller ph: 7.38 7.42 Normaler intrazellulärer ph: 7.0 7.3 Der körpereigene
Metabolische Azidose PD Dr. Martin Bek, Medizinische Klinik und Poliklinik D, UKM, Münster 1) Säure/Basenproduktion Normaler arterieller ph: 7.38 7.42 Normaler intrazellulärer ph: 7.0 7.3 Der körpereigene
Punktion der A. radialis + Blutgasanalyse
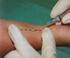 Punktion der A. radialis + Blutgasanalyse Wissenswertes: Allgemeines: Sinn dieser Station in unserem Skills Lab Innere ist nicht nur die arterielle Blutentnahme, sondern insbesondere auch die nachfolgende
Punktion der A. radialis + Blutgasanalyse Wissenswertes: Allgemeines: Sinn dieser Station in unserem Skills Lab Innere ist nicht nur die arterielle Blutentnahme, sondern insbesondere auch die nachfolgende
Aufgabe 1: Geben Sie die korrespondierenden Basen zu folgenden Verbindungen an: a) H 3 PO 4 b) H 2 PO 4
 Übungsaufgaben zum Thema Säuren, Basen und Puffer Säure/Base Definition nach Brǿnsted: Säuren sind Stoffe, die Protonen abgeben können (Protonendonatoren). Basen sind Stoffe, die Protonen aufnehmen können
Übungsaufgaben zum Thema Säuren, Basen und Puffer Säure/Base Definition nach Brǿnsted: Säuren sind Stoffe, die Protonen abgeben können (Protonendonatoren). Basen sind Stoffe, die Protonen aufnehmen können
INSTITUT FÜR PHYSIOLOGIE
 INSTITUT FÜR PHYSIOLOGIE Anleitung zum Physiologie - Praktikum P - 1. Pufferung und Säure-Basen Analyse WS 2010/11 3. Semester 2 Inhalt I. VORBEMERKUNGEN... 3 II. THEORETISCHE GRUNDLAGEN... 4 1. Säuren
INSTITUT FÜR PHYSIOLOGIE Anleitung zum Physiologie - Praktikum P - 1. Pufferung und Säure-Basen Analyse WS 2010/11 3. Semester 2 Inhalt I. VORBEMERKUNGEN... 3 II. THEORETISCHE GRUNDLAGEN... 4 1. Säuren
Blutgasanalytik eine Thematik zwischen Labor und Station
 Blutgasanalytik eine Thematik zwischen Labor und Station Xtra Vol. 14.2 2010 Nr. 11 Die Blutgasanalyse (BGA) ist ein fester Bestandteil heutiger Diagnostik und aus den Krankenhäusern und mittlerweile vielen
Blutgasanalytik eine Thematik zwischen Labor und Station Xtra Vol. 14.2 2010 Nr. 11 Die Blutgasanalyse (BGA) ist ein fester Bestandteil heutiger Diagnostik und aus den Krankenhäusern und mittlerweile vielen
Was verstehen wir unter Säuren und Basen?
 Was verstehen wir unter Säuren und Basen? Säuren: Unter Säuren verstehen wir alle organischen und anorganischen Verbindungen, die in Lösungen Wasserstoffionen H + abgeben. Sie werden auch Protonen Donatoren
Was verstehen wir unter Säuren und Basen? Säuren: Unter Säuren verstehen wir alle organischen und anorganischen Verbindungen, die in Lösungen Wasserstoffionen H + abgeben. Sie werden auch Protonen Donatoren
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9)
 Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 4. Allosterische Regulation Organismen
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 4. Allosterische Regulation Organismen
Anästhesie und Azidose
 Anästhesie und Azidose Monika Baumgartner Karin Gamma Kurs 2004 Universitätsspital Basel Vorwort Der SäureBasenHaushalt ist eines der komplexesten und feinsten Systeme überhaupt im menschlichen Organismus.
Anästhesie und Azidose Monika Baumgartner Karin Gamma Kurs 2004 Universitätsspital Basel Vorwort Der SäureBasenHaushalt ist eines der komplexesten und feinsten Systeme überhaupt im menschlichen Organismus.
Puffersysteme. Diese Lerneinheit befasst sich mit den Grundlagen der Puffersysteme: Was ist der Pufferbereich und wovon ist er abhängig?
 Puffersysteme Diese Lerneinheit befasst sich mit den Grundlagen der Puffersysteme: Was ist ein Puffersystem? Wie wirkt ein Puffer? Was ist der Pufferbereich und wovon ist er abhängig? Welche biochemisch
Puffersysteme Diese Lerneinheit befasst sich mit den Grundlagen der Puffersysteme: Was ist ein Puffersystem? Wie wirkt ein Puffer? Was ist der Pufferbereich und wovon ist er abhängig? Welche biochemisch
Blutgase. 3.1 Sauerstoff 55. 3.2 Kohlendioxid 64. Literatur 68
 Blutgase.1 Sauerstoff 55.1.1 O 2 -Kaskade 55.1.2 Transport von Sauerstoff im Blut 57.1. O 2 -Sättigung des Hämoglobins und O 2 -Bindungskurve 58.1.4 O 2 -Gehalt und O 2 -Status des Blutes 62.1.5 O 2 -Angebot
Blutgase.1 Sauerstoff 55.1.1 O 2 -Kaskade 55.1.2 Transport von Sauerstoff im Blut 57.1. O 2 -Sättigung des Hämoglobins und O 2 -Bindungskurve 58.1.4 O 2 -Gehalt und O 2 -Status des Blutes 62.1.5 O 2 -Angebot
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9)
 Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation A. Struktur von Myoglobin Strukturaufklärung
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation A. Struktur von Myoglobin Strukturaufklärung
I. Atemnot und deren Ursache
 Referat: Atmung I. Atemnot und deren Ursache II. Diagnostik bei Lungenerkrankungen - Auskultation/Perkussion/ BGA/ Röntgen III. Symptomatik bei Erkrankungen der Lunge (speziell Lungenentzündung) IV. Therapeutische
Referat: Atmung I. Atemnot und deren Ursache II. Diagnostik bei Lungenerkrankungen - Auskultation/Perkussion/ BGA/ Röntgen III. Symptomatik bei Erkrankungen der Lunge (speziell Lungenentzündung) IV. Therapeutische
EISENSTOFFWECHSEL. Maya Winter. M.Winter
 EISENSTOFFWECHSEL Maya Winter FE Eisen ein essentielles Element Aber: freies Eisen ist extrem giftig daher im Organismus immer in i gebundener Form hohe Toxizität t von freiem Eisen Komplexkonstante von
EISENSTOFFWECHSEL Maya Winter FE Eisen ein essentielles Element Aber: freies Eisen ist extrem giftig daher im Organismus immer in i gebundener Form hohe Toxizität t von freiem Eisen Komplexkonstante von
Vitalfunktionen - und ihre Werte. Volker Schelling
 Vitalfunktionen - und ihre Werte Volker Schelling 1 Definition Die Vitalfunktionen sind die Atmung, d i e Körpertemperatur und der Kreislauf, also arterieller Puls und arterieller Blutdruck, deren unterbrechungsfreie
Vitalfunktionen - und ihre Werte Volker Schelling 1 Definition Die Vitalfunktionen sind die Atmung, d i e Körpertemperatur und der Kreislauf, also arterieller Puls und arterieller Blutdruck, deren unterbrechungsfreie
A) Bei zweiprotonigen Säuren wird zur vollständigen Neutralisation exakt ein
 1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist richtig? A) Bei zweiprotonigen Säuren wird zur vollständigen Neutralisation exakt ein Äquivalent an Natronlauge
1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist richtig? A) Bei zweiprotonigen Säuren wird zur vollständigen Neutralisation exakt ein Äquivalent an Natronlauge
Einführung in die Biochemie Wirkungsweise von Enzymen
 Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Die Nieren. Anatomie Physiologie Säure-/Basen-Haushalt Elektrolyte Wasserhaushalt. Copyright: T.Heinrich-RA-1997 1
 Die Nieren Anatomie Physiologie Säure-/Basen-Haushalt Elektrolyte Wasserhaushalt Copyright: T.Heinrich-RA-1997 1 Die Anatomie des Urogenital- Systems Copyright: T.Heinrich-RA-1997 2 Das harnproduzierende
Die Nieren Anatomie Physiologie Säure-/Basen-Haushalt Elektrolyte Wasserhaushalt Copyright: T.Heinrich-RA-1997 1 Die Anatomie des Urogenital- Systems Copyright: T.Heinrich-RA-1997 2 Das harnproduzierende
Der Harnstoff ist das Endprodukt des Proteinstoffwechsels.
 Der Harnstoff ist das Endprodukt des Proteinstoffwechsels. Proteinabbau: Protein AS + Stickstoff Stickstoff zu Ammoniak (NH 3, Zellgift) Ammoniak wird an CO 2 gebunden Harnstoff entsteht (H 2 N- CO-NH
Der Harnstoff ist das Endprodukt des Proteinstoffwechsels. Proteinabbau: Protein AS + Stickstoff Stickstoff zu Ammoniak (NH 3, Zellgift) Ammoniak wird an CO 2 gebunden Harnstoff entsteht (H 2 N- CO-NH
