Call for Abstracts. VORPROgRAmm
|
|
|
- Frauke Bäcker
- vor 8 Jahren
- Abrufe
Transkript
1 Call for Abstracts VORPROgRAmm
2 Der richtige Partner besteht auch nach Jahren noch jede Prüfung. Die ARTEN-Studie belegt, was wir schon lange wissen: Viramune zeigte die Nicht-Unterlegenheit 1 gegenüber geboostetem Atazanavir/r (beide in Kombination mit Truvada ) nach 48 Wochen. 2 1 Die deutsche Fachinformation sieht die bid-gabe vor. 2 Soriano et al. IAS 2009, Cape Town, South Africa, Poster LBPE07.
3 10. Kongress für Infektionskrankheiten und Tropenmedizin Juni 2010 in Köln, Gürzenich gemeinsam mit dem 3. Deutschen Pflegetag Infektionsmedizin 23. Juni 2010 Unter der Schirmherrschaft von der Deutschen Gesellschaft für Wundheilung und Wundbehandlung e.v. (DGfW) Titelbild Bei dem Kunstwerk aus dem Jahr 1913 handelt es sich um einen Ausschnitt des Bildes Farbige Formen (III) von August Macke, der von 1887 bis 1914 lebte.
4 InHAlTSVeRZeICHnIS Grußwort Wissenschaftliche Leitung Wissenschaftlicher Beirat Allgemeine Hinweise Wissenschaftliches Programm Übersicht Fest- und Plenarvorträge Symposiumsthemen Reisemedizin-Symposium Pflegesymposium Hausärztetag Industriesymposien Get Together InHAlTSVeRZeICHnIS Hinweise zur Abstracteinreichung Sponsoren Aussteller Anfahrtsbeschreibung Gürzenich Hinweise zur Anmeldung Anmeldeformular ImPReSSum Herausgeber Konzeption, Layout Deutsche Gesellschaft für Infektiologie e.v. (DGI) c/o Medizinische Klinik II Campus-Virchow-Klinikum der Charité Augustenburger Platz Berlin vorstand@dgi-net.de Deep Thought Gesellschaft für Kommunikation mbh Kirschbaumweg Frankfurt am Main hl@deepthought.de Verlag, Satz Wecom Gesellschaft für Kommunikation mbh & Co. KG Lerchenkamp Hildesheim info@wecom.org Der Verlag übernimmt keine Garantie für die Richtigkeit der Angaben. 4
5 neue Ära Eine in der HIV-Therapie ATRIPLA 600 mg/200 mg/245mg Filmtabletten Zusammensetzung: Wirkstoffe: Jede ATRIPLA Filmtablette enthält 600 mg Efavirenz, 200 mg Emtricitabin und 245 mg Tenofovirdisoproxil (als Fumarat). Sonstige Bestandteile: Tablettenkern: Croscarmellose-Natrium, Hyprolose, Magnesiumstearat, mikrokristalline Cellulose, Natriumdodecysulfat; Filmüberzug: Eisen(II, III)-oxid, Eisen(III)-oxid, Macrogol 3350, Poly(vinylalkohol), Talkum, Titandioxid. Anwendungsgebiet: ATRIPLA dient zur Behandlung der HIV-1-Infektion bei Erwachsenen, die unter ihrer derzeitigen antiretroviralen Kombinationstherapie seit mehr als drei Monaten virussupprimiert sind, kein vorheriges virologisches Versagen erlitten haben und keine resistenzassoziierten Mutationen gegenüber den Substanzen in ATRIPLA aufweisen. Gegenanzeigen: Überempfindlichkeit gegen die Wirkstoffe oder einen der sonstigen Bestandteile von ATRIPLA, schwere Lebererkrankung (CPT Schweregrad C). Nicht gleichzeitig mit Terfenadin, Astemizol, Cisaprid, Midazolam, Triazolam, Pimozid, Bepridil, Mutterkorn-Alkaloiden (z.b. Ergotamin und derivate), Johanniskraut oder Voriconazol anwenden. Warnhinweise: ATRIPLA darf nicht in der Schwangerschaft angewendet werden, es sei denn, es gibt keine weiteren angemessenen Behandlungsoptionen. Tierstudien haben teratogene Wirkungen und den Übertritt in die Muttermilch gezeigt. Verkehrstüchtigkeit und Bedienen von Maschinen: Wenn ZNS-Symptome auftreten, wird von der Ausübung potentiell gefährlicher Tätigkeiten wie der Teilnahme am Straßenverkehr oder dem Bedienen von Maschinen abgeraten. Nebenwirkungen: Sehr häufig ( 1/10): Schwindel, Kopfschmerzen, Durchfall, Erbrechen, Übelkeit, Exantheme (alle Schweregrade), Hypophosphatämie, erhöhte Kreatinkinase-Werte im Blut. Häufig ( 1/100, <1/10): Urtikaria, Verfärbung der Haut (verstärkte Pigmentierung), Schmerzen, Bauchschmerzen, Schlafstörungen, abnorme Träume, Albträume, nächtliches Schwitzen, Konzentrationsstörungen, Benommenheit, Angst, Depression, Manie, Affektlabilität, Blähungen, Anorexie, Hitzewallungen, Schwächegefühl, Müdigkeit, Antriebslosigkeit, gesteigerte Energie, Juckreiz, Neutropenie, erhöhte Zucker-, Triglycerid- oder Bilirubinwerte im Blut, erhöhte Amylase-Werte, erhöhte Serum-Lipase-Werte, Dyspepsie, erhöhte Transaminase- Werte. Gelegentlich ( 1/1000, <1/100): Aggression, Selbstmordgedanken, abnormales Denken, Paranoia, Halluzination, Selbstmordversuch, Persönlichkeitsveränderungen, sich nicht normal Fühlen, Amnesie, Verwirrtheit, Ataxie, Krämpfe, Orientierungslosigkeit, zusammenhangloses Sprechen, Überspanntheitsgefühl, verschwommenes Sehen, Sehstörungen, Dyspnoe, Vertigo, Kribbeln oder Taubheit im Mund, Mundtrockenheit, allergische Reaktion, Stevens-Johnson-Syndrom, Erythema multiforme, akute Hepatitis, akute Pankreatitis, Fettumverteilung, Gewichtsverlust, gesteigerter Appetit, Gynäkomastie, Anämie, verminderte Libido, Muskelschmerzen, Frösteln. Andere mögliche Nebenwirkungen: Laktatazidose, Nierenversagen, akute tubuläre Nekrose, proximale renale Tubulopathie einschließlich Fanconi-Syndrom, Nephritis, Diabetes insipidus, erhöhte Kreatininwerte im Blut, Proteinurie, Rhabdomyolyse, Osteomalazie (Knochenschmerzen, selten Mitursache bei Frakturen), Muskelschwäche, Myopathie, Hypokaliämie, Wahnvorstellungen, Neurose, Psychose, Suizid, photoallergische Dermatitis, Hepatosteatose, Pankreatitis, Hepatitis, Leberversagen. Die antiretrovirale Kombinationstherapie kann Hyperlipidämie, Insulinresistenz, Hyperglykämie und Hyperlaktatämie verursachen. Unter antiretroviraler Kombinationstherapie ist das Auftreten eines Immun-Reaktivierungs-Syndroms beschrieben worden. Unter antiretroviraler Kombinationsbehandlung kann sich eine Osteonekrose (Absterben von Knochengewebe infolge unzureichender Blutversorgung des Knochens) entwickeln. Darreichungsform und Packungsgrößen: Packungen mit 30 und 3 x 30 Filmtabletten. Verschreibungspflichtig. Stand: Dezember Bristol-Myers Squibb and Gilead Sciences Ltd., Dublin, Irland.
6 SeHRgeeHRTedAmenundHeRRen, liebekolleginnenundkollegen, zum 10. Kongress für Infektionskrankheiten und Tropenmedizin (KIT) möchten wir Sie herzlich nach Köln einladen. Der KIT ist der größte deutschsprachige Kongress auf dem Gebiet der Infektionsmedizin und der einzige, der die unterschiedlichen Fachrichtungen in diesem Bereich vereint. Die Darstellung der Infektiologie als ein Fach mit breiter klinischer und wissenschaftlicher Ausrichtung ist eines unserer zentralen Anliegen für den KIT So freuen wir uns besonders darüber, dass der Kongress eine breite Unterstützung durch verschiedene Fachgesellschaften erfährt. Das Programm des KIT widmet sich insbesondere vier thematischen Schwerpunkten, der klinischen Infektiologie und Mikrobiologie, der klinischen Mykologie, der Reise- und Tropenmedizin und der HIV-Medizin. So wird jeder Teilnehmer die Möglichkeit haben, sich sowohl im Bereich seines besonderen Interessengebietes als auch in weiteren Gebieten der Infektiologie fortzubilden. Daneben sind Plenarvorträge von international ausgewiesenen Experten zu zentralen infektiologischen Themen vorgesehen, die sich an alle Teilnehmer richten. grusswort Jüngeren wissenschaftlich tätigen Kolleginnen und Kollegen soll mit dem KIT 2010 ein Forum zur Präsentation eigener Forschungsergebnisse geschaffen werden. Sowohl die Posterausstellung als auch mündliche Best Poster Sessions werden daher einen breiten Raum im Programm des Kongresses einnehmen. Während des KIT 2010 findet der 3. Deutsche Pflegetag in der Infektionsmedizin statt. Diese Veranstaltung wendet sich vor allem an Kolleginnen und Kollegen aus den Pflegeberufen und beinhaltet spezielle pflegerische Aspekte im Umgang mit Patienten mit Infektionskrankheiten. Neben dem Besuch des wissenschaftlichen Programms ist ein Aufenthalt in Köln in vielfältiger Weise interessant. Der Kongress wird inmitten der attraktiven Kölner Altstadt im historischen Gürzenich sowie im weltbekannten Wallraff-Richartz-Museum stattfinden. Die Stadt bietet eine Vielzahl von weiteren kulturellen Höhepunkten und Sehenswürdigkeiten sowie Möglichkeiten zur Freizeitgestaltung. Wir möchten Sie herzlich einladen, den KIT 2010 zu besuchen, wissenschaftliche Beiträge einzureichen und für den Kongress in Ihrem Kollegen- und Bekanntenkreis zu werben. Es würde uns sehr freuen, Sie im Juni 2010 in Köln begrüßen zu dürfen. Mit freundlichen Grüßen, Ihre Prof. Dr. Gerd Fätkenheuer Kongress präsident Prof. Dr. Harald Seifert Kongressvizepräsident 6
7 WISSenSCHAFTlICHeleITung Kongresspräsident Kongressvizepräsident Kongresssekretariat Prof. Dr. G. Fätkenheuer, Köln Prof. Dr. H. Seifert, Köln Dr. C. Wyen, Köln Gisela Kremer, Köln Tel Ausrichtende Fachgesellschaften Deutsche Gesellschaft für Infektiologie e.v. (DGI) Deutsche AIDS-Gesellschaft (DAIG) Beteiligte Fachgesellschaften Deutsche Gesellschaft für Tropenmedizin und Internationale Gesundheit e.v. (DTG) Paul-Ehrlich-Gesellschaft für Chemotherapie e.v. (PEG) Gesellschaft für Virologie e.v. (GfV) Deutsche Gesellschaft für Pädiatrische Infektiologie e.v. (DGPI) Deutsche Arbeitsgemeinschaft niedergelassener Ärzte in der Versorgung HIV-Infizierter e.v. (DAGNÄ) Deutschsprachige Mykologische Gesellschaft e.v. (DMykG) Deutsche Vereinigung zur Bekämpfung der Viruskrankheiten e.v. (DVV) Deutsche Gesellschaft für Hygiene und Mikrobiologie e.v. (DGHM) WISSenSCHAFTlICHeleITung 7
8 WISSenSCHAFTlICHeRBeIRAT Wissenschaftlicher Beirat Prof. Dr. R. Berner, Freiburg (DGPI) Prof. Dr. O. A. Cornely, Köln (DMykG) Prof. Dr. C. Drosten, Hamburg Prof. Dr. M. Herrmann, Homburg-Saar Priv.-Doz. Dr. M. Hölscher, München Prof. Dr. W.V. Kern, Freiburg (DGI) Dr. S. Klauke, Frankfurt (DAGNÄ) Prof. Dr. T. Löscher, München (DTG) Prof. T. Mertens, Ulm (GfV) Dr. R. Pape, Köln Prof. Dr. H. Pfister, Köln Prof. Dr. P. Rath, Essen Prof. Dr. J. Rockstroh, Bonn (DAIG) Prof. Dr. B. Salzberger, Regensburg Priv-Doz. Dr. K. Schröppel, Tübingen (DGHM) Prof. Dr. E. Straube, Jena (PEG) Priv.-Doz. Dr. J. van Lunzen, Hamburg Prof. Dr. T. Welte, Hannover Prof. Dr. P. Wutzler, Jena (DVV) 8 WISSenSCHAFTlICHeRBeIRAT Lokales Organisationskomitee Prof. Dr. Oliver A. Cornely, Köln PD Dr. Pia Hartmann, Köln Dr. Achim Kaasch, Köln Dr. Tim Kümmerle, Köln Dirk Küppers, Köln Dr. Rudolf Pape, Köln Frank Prison, Köln Dr. Maria Rüping. Köln Dr. Jan Rybniker, Köln Prof. Dr. Jörg W. Robertz, Köln Ellen Schaperdoth, Köln Dr. Janne Vehreschild, Köln
9 A FIRST IMPRESSION THAT LASTS Stark wirksam Gut verträglich Once Daily NEU 3-Monatspackung REYATAZ Bezeichnung Lauer-Taxe 90 Stück REYATAZ 300 mg Hartkapseln PZN-Nummer Packungsgröße N1 (90 Hartkapseln) SCHAFFT VERTRAUEN BIETET VORTEILE FÜR ARZT UND PATIENTEN EIN ARZTBESUCH EIN REZEPT EINE ZUZAHLUNG JE QUARTAL Quelle: 1. Molina J-M et al. CASTLE: atazanavir-ritonavir vs lopinavir in antiretroviral-naive HIV-1 infected patients: 96-week safety and effi cacy. Poster presented at joint ICAAC/IDSA meeting. Washington DC, United States, Poster #H-1250D. REYATAZ 100 mg / 150 mg / 200 mg / 300 mg Hartkapseln. Wirkstoff: Atazanavir. Zusammensetzung: 100 mg / 150 mg / 200 mg / 300 mg Atazanavir pro Kapsel. Sonstige Bestandteile: REYATAZ Hartkapsel: Crospovidon, Lactose-Monohydrat, Magnesiumstearat. Kapselhülle und Drucktinte: Gelatine, Indigocarmin (E132), Titandioxid (E171), Schellack, Ammoniumhydroxid, Propylenglycol, Simeticon. Anwendungsgebiete: Zur antiretroviralen Kombinationsbehandlung von HIV-1-infi zierten Erwachsenen. Gegenanzeigen: Überempfi ndlichkeit gegenüber Atazanavir oder einem der sonstigen Bestandteile. Patienten mit mäßiger bis schwerer Leberinsuffi zienz. Nicht gleichzeitig anwenden mit Arzneimitteln, die Johanniskraut enthalten. In Kombination mit Ritonavir nicht gleichzeitig anwenden mit Rifampicin und mit Arzneimitteln, die Substrate der Cytochrom P450-Isoform CYP3A4 sind und eine geringe therapeutische Breite haben (z. B. Astemizol, Terfenadin, Cisaprid, Pimozid, Chinidin, Bepridil, Triazolam, oral angewendetes Midazolam, Mutterkorn-Alkaloide, insbesondere Ergotamin, Dihydroergotamin, Ergometrin, Methylergometrin). Nebenwirkungen: Eine antiretrovirale Kombinationstherapie ist mit Lipodystrophie und Stoffwechsel anomalien (Hyperlipidämie, Hyperglykämie, Insulinresistenz) assoziiert worden. Bei HIV-Patienten mit schwerem Immundefekt Immun-Reaktivierungs-Syndrom möglich. Bei HIV-Patienten mit fortgeschrittener HIV-Erkrankung oder antiretroviraler Langzeittherapie Fälle von Osteonekrose beschrieben. Bei Patienten mit Hämophilie Typ A oder Typ B vermehrt Blutungen möglich. Unter einer Therapie mit Proteasehemmern wurden erhöhte Blutzuckerwerte, neu auftretender Diabetes mellitus oder Exarzerbationen eines bestehenden Diabetes mellitus beobachtet. Unter REYATAZ gab es Berichte über unregelmäßigen Herzschlag. Häufig (mind. 1 / 100 Pat.): Kopfschmerzen, Ikterus der Augen, Erbrechen, Diarrhoe, Bauchschmerzen, Übelkeit, Dyspepsie, Ausschlag, Lipodystrophie-Syndrom, Erschöpfung, Ikterus. Gelegentlich (mind. 1 / Pat.): periphere Neuropathie, Synkope, Amnesie, Schwindel, Benommenheit, Dysgeusie, Dyspnoe, Pankreatitis, Gastritis, aufgeblähtes Abdomen, aphthöse Stomatitis, Blähungen, Mundtrockenheit, Nierensteine, Hämaturie, Proteinurie, Pollakisurie, Urticaria, Alopezie, Juckreiz, Muskelatrophie, Arthralgie, Myalgie, Gewichtsabnahme, Gewichtszunahme, Anorexie, gesteigerter Appetit, Bluthochdruck, Brustschmerz, Unwohlsein, Fieber, Asthenie, allergische Reaktion, Hepatitis, Gynäkomastie, Depressionen, Orientierungslosigkeit, Angst, Schlafl osigkeit, Schlafstörungen, abnormale Träume. Selten (mind. 1 / Pat.): Ödem, Palpitation, Nierenschmerzen, vesikulobullöser Ausschlag, Ekzem, Gefäßerweiterung, Myopathie, abnormaler Gang, Hepatosplenomegalie. Nicht bekannte Häufigkeit: Torsades de pointes, QT-Verlängerung, Diabetes mellitus, Hyperglykämie, Nephrolithiasis, Gallenblasenfunktionsstörungen. Weitere Hinweise siehe Fachinformation. Verschreibungsstatus: Verschreibungspfl ichtig. Stand: Februar Pharmazeutischer Unternehmer: Bristol-Myers Squibb Pharma EEIG, Uxbridge Business Park, Sanderson Road, UB8 1DH Uxbridge, Middlesex, Vereinigtes Königreich.
10 AllgemeIneHInWeISe Kongresspräsident Kongressvizepräsident Kongresssekretär Professor Dr. Gerd Fätkenheuer Klinik I für Innere Medizin Uniklinik Köln Kerpener Straße Köln Professor Dr. Harald Seifert Institut für Medizinische Mikrobiologie, Immunologie und Hygiene Uniklinik Köln Goldfelsstraße Köln Dr. Christoph Wyen Klinik I für Innere Medizin Uniklinik Köln Kerpener Straße Köln christoph.wyen@uk-koeln.de AllgemeIneHInWeISe Tagungsort KIT 2010 c/o Frau Gisela Kremer Klinik I für Innere Medizin Uniklinik Köln Studienzentrum Infektiologie Kerpener Straße Köln gisela.kremer@uk-koeln.de Telefon: Fax: Gürzenich Köln Martinstraße Köln Tagungszeiten Mittwoch, 23. Juni Uhr Donnerstag, 24. Juni Uhr Freitag, 25. Juni Uhr Samstag, 26. Juni Uhr 10
11 Bei invasiven Candidosen: Mycamine * MYCAMINE ist zugelassen zur Behandlung invasiver Candidosen; zur Prophylaxe von Candida-Infektionen bei einer allogenen, hämatopoetischen Stammzelltransplantation oder wenn eine Neutropenie (absolute Neutrophilenzahl < 500/µl) von mindestens 10 oder mehr Tagen zu erwarten ist. Bei der Entscheidung, MYCAMINE anzuwenden, sollte in Betracht gezogen werden, dass ein Risiko zur Lebertumorbildung besteht. MYCAMINE ist daher nur anzuwenden, wenn andere Antimykotika nicht geeignet sind. MYCAMINE 50 mg Pulver zur Herstellung einer Infusionslösung, MYCAMINE 100 mg Pulver zur Herstellung einer Infusionslösung. Darreichung: Jede Durchstechflasche enthält nach der Rekonstitution pro Milliliter 10 mg bzw. 20 mg Micafungin als Natrium-Salz. Sonstige Bestandteile: Lactose-Monohydrat, Citronensäure, Natriumhydroxid. Anwendungsgebiete: Bei Erwachsenen (einschließlich älterer Patienten), Jugendlichen und Kindern (einschließlich Neugeborenen) mit invasiver Candidose, zur Prophylaxe von Candida-Infektionen bei einer allogenen, hämatopoetischen Stammzelltransplantation oder wenn eine Neutropenie (absolte Neutrophilenzahl < 500/µl) von mindestens 10 oder mehr Tagen zu erwarten ist. Behandlung der ösophagealen Candidose bei Erwachsenen (einschließlich älterer Patienten) und Jugendlichen. Die Entscheidung, Mycamine anzuwenden, sollte in Betracht ziehen, dass ein Risiko zur Lebertumorbildung besteht. Mycamine ist daher nur anzuwenden, wenn andere Antimykotika nicht geeignet sind. Dosierung und Anwendung: Die Behandlung mit Mycamine ist von einem Arzt einzuleiten, der Erfahrung mit der Behandlung von Pilzinfektionen hat. Zur Isolierung und Identifizierung der (des) Krankheitserreger(s) sind vor der Behandlung Pilzkulturen anzusetzen und andere relevante Laboruntersuchungen durchzuführen (einschließlich histopathologischer Untersuchungen). Die Behandlung kann noch vor Bekanntwerden der Ergebnisse solcher Kulturen oder Untersuchungen begonnen werden. Wenn die Ergebnisse bekannt sind, ist die antimykotische Therapie jedoch entsprechend anzupassen. Dosis: Zur Behand- lung invasiver Candidose 100 mg/tag (Körpergewicht > 40 kg) oder 2 mg/kg/tag (Körpergewicht 40 kg); Behandlung ösophagealer Candidose: 150 mg/tag (Körpergewicht > 40 kg) oder 3 mg/kg/tag (Körpergewicht 40 kg); Prophylaxe von Candida-Infektionen: 50 mg/tag (Körpergewicht > 40 kg) oder 1 mg/kg/tag (Körpergewicht 40 kg). Dosiserhöhung wegen nicht ausreichendem Ansprechen bei invasiver Candidose auf 200 mg/tag (Körpergewicht von > 40 kg) und auf 4 mg/kg/tag (Körpergewicht 40 kg) möglich. Behandlungsdauer: Invasive Candidose: mindestens 14 Tage. Nach zwei aufeinander folgenden negativen Blutkulturen und nach dem Abklingen der klinischen Anzeichen und Symptome der Infektion, Fortsetzung der Therapie noch mindestens 1 Woche lang. Ösophageale Candidose: Die Therapie sollte nach Abklingen der klinischen Anzeichen und Symptome noch mindestens 1 Woche fortgesetzt werden. Prophylaxe von Candida-Infektionen: nach Normalisierung der Neutrophilenzahl noch mindestens 1 Woche Therapie. Spezielle Bevölkerungsgruppen: Geschlecht, ethnische Zugehörigkeit, Nierenfunktionsstörung und leichte/mäßige Leberinsuffizienz erfordern keine Dosisanpassung. Die Behandlung von Patienten mit schwerer Leberinsuffizienz wird nicht empfohlen. Nach Rekonstitution tion und Verdünnung ist die Lösung über ca. 1 Stunde intravenös anzuwenden. Schnellere Infusionen können zu vermehrten histaminabhängigen Reaktionen führen. Gegenanzeigen: Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile. Warnhinweise und Vorsichtsmaßnahmen: Hepatische Wirkungen: Nach einer Behandlungsperiode von 3 Monaten wurden bei Ratten Foci präneoplastischer Hepatozyten und hepatozelluläre Tumore beobachtet und der vermutliche Schwellenwert befand sich in etwa im Bereich der klinischen Exposition. Die Relevanz für die therapeutische Anwendung kann nicht ausgeschlossen werden. Während der Behandlung ist die Leberfunktion sorgfältig zu kontrollieren und ein frühzeitiges Absetzen wird empfohlen, wenn die ALT/AST-Werte signifikant und dauerhaft erhöht sind. Die Behandlung sollte auf Basis einer sorgfältigen Nutzen-Risiko- Bewertung erfolgen, insbesondere bei Patienten mit Leberinsuffizienz oder chronischen Lebererkrankungen, welche bekanntermaßen präneoplastische Prozesse darstellen oder bei Patienten, die eine Begleittherapie erhalten insbesondere mit hepatotoxischen und/oder genotoxischen Eigenschaften. Signifikante Beeinträchtigungen der Leberfunktion traten sowohl bei Patienten als auch gesunden Probanden auf, einschließlich schwerer Störungen und Todesfällen. Kinder < 1 Jahr neigen möglicherweise eher zu Leberschäden. Mycamine kann auch Nierenprobleme und -insuffizienz verursachen. Anaphylaktoide Reaktionen einschließlich Schock können auftreten. Fälle von Hämolyse, einschließlich akuter intravasaler Hämolyse oder hämolytischer Anämie wurden selten berichtet. Patienten mit seltenen angeborenen Problemen von Galactoseintoleranz, Lapp-Lactase-Mangel oder Glucose-Galactose-Malabsorption sollten Mycamine nicht einnehmen. Wechselwirkungen: Die Wirkung anderer Arzneimittel kann beeinträchtigt oder verstärkt werden. Schwangerschaft und Stillzeit: Micafungin darf in der Schwangerschaft nicht angewendet werden, es sei denn dies ist unbedingt erforderlich. Micafungin kann möglicherweise die Fertilität bei Männern beeinträchtigen. Nebenwirkungen: Die häufigsten Nebenwirkungen waren Übelkeit, erhöhte ALP im Blut, Phlebitis, Erbrechen und erhöhte AST-Werte; allergieartige Symptome: Hautausschlag und Rigor wurden ebenfalls berichtet; hepatische Nebenwirkungen: die Mehrzahl der Nebenwirkungen waren leichten oder mäßigen Schweregrades. Am häufigsten waren ein Anstieg von AP, AST, ALT, Bilirubin im Blut sowie abnorme LFTs zu beobachten. Fälle von schwerwiegenden Leberfunktionsstörungen kamen gelegentlich vor; Reaktionen an der Einstichstelle: keine Einschränkung der Behandlung; Andere häufige Nebenwirkungen: Leukopenie, Neutropenie, Anämie, Hypokalämie, Hypomagnesämie, Hypokalzämie, Kopfschmerzen, Diarrhö, Bauchschmerzen, Fieber; Kinder: Einige der Nebenwirkungen traten bei Kindern häufiger auf als bei Erwachsenen. Kinder < 1 Jahr zeigten ca. zweimal häufiger einen Anstieg von ALT, AST und AP als ältere Kinder. Andere häufige Nebenwirkungen bei Kindern: Tachykardie, Hypertonie, Hypotonie, Hyperbilirubinämie, Hepatomegalie, akutes Nierenversagen, erhöhter Harnstoff im Blut. Weitere Angaben: siehe Fachinformation. Verschreibungspflichtig. Stand der Information: Oktober Astellas Pharma GmbH, Postfach , München
12 AllgemeIneHInWeISe Kongress-Organisation Pressebetreuung COCS GmbH - Congress Organisation C. Schäfer Franz-Joseph-Straße München katrin.lehmann@cocs.de Telefon: Fax: Sina Vogt Klinik I für Innere Medizin Uniklinik Köln Kerpener Straße Köln sinavogt@sinavogt.eu Telefon: AllgemeIneHInWeISe Konzeption, Layout Hotelreservierung Haftung Deep Thought Gesellschaft für Kommunikation mbh Kirschbaumweg Frankfurt am Main hl@deepthought.de Es sind Zimmerkontingente für die Teilnehmer des Kongresses unter dem Stichwort KIT2010 eingerichtet. Eine Hotelliste finden Sie unter Die Veranstalter bzw. Ausrichter des Kongresses können keine Haftung von Personenschäden, Verlust oder Beschädigung von Besitz der Kongressteilnehmer tragen, auch nicht während des Kongresses oder infolge der Kongressteilnahme. Bitte überprüfen Sie Ihre eigene Versicherung. 12
13 AllgemeIneHInWeISe Vorträge, Posterpräsentationen und Best Poster Session Fachausstellung Junge Wissenschaftler sollen auf dem KIT2010 eine breite Plattform zur Präsentation eigener Forschungsergebnisse erhalten. Eingereichte Abstracts werden von unabhängigen Gutachtern bewertet, und angenommene Beiträge werden als orale Präsentationen, als Poster und im Rahmen von Best Poster Sessions präsentiert. Bitte reichen Sie Ihren Beitrag als Abstract bis 01. Februar 2010 unter (Link Abstract-Einreichung ) ein. Hinweise zur Abstract-Einreichung siehe S. 26 Während des Kongresses findet eine begleitende Fachausstellung in den Foyers direkt vor den Vortragssälen statt. Für weitere Informationen wenden sie sich bitte an COCS GmbH, siehe Seite 12 Eröffnungsabend Mittwoch, 23. Juni 2010 Wissenschaftliche Preise Tagungsprogramm Im Anschluss an die Sitzungen (ab Uhr) sind alle Teilnehmer zu der Eröffnung mit Festvortrag und anschließendem Empfang im benachbarten Wallraf- Richartz-Museum eingeladen (ab ca Uhr). Eine Anmeldung ist erforderlich (siehe Anmeldeformular). Im Rahmen der KIT2010 werden insgesamt 5 Posterpreise verliehen. Der Preis für den ersten Platz beträgt 2.000,. Die European Society of Clinical Microbiology and Infections Diseases (ESCMID) stiftet als weiteren Posterpreis die Teilnahme an einer ESCMID-Summerschool. Darüber hinaus finden im Rahmen des KIT2010 die Preiverleihung des Rudolf-Ackermann-Preis für Infektiologie 2010 der Deutschen Gesellschaft für Infektiologie (DGI) und die Preisverleihung des Förderpreis Klinische Infektionsforschung 2010 der DGI statt. Das endgültige wissenschaftliche Programm wird allen Referenten, Moderatoren, angemeldeten Teilnehmern und Ausstellern vor Kongressbeginn zugeschickt. AllgemeIneHInWeISe 13
14 WISSenSCHAFTlICHeSPROgRAmm ÜBeRSICHT PROgRAmm Mittwoch 23. Juni 2010 Donnerstag 24. Juni 2010 Freitag 25. Juni 2010 Samstag 26. Juni Plenarvorträge Plenarvorträge Plenarvorträge Pause Pause Pause Symposium Infektiologie/ Klin. Mikrobiologie Tropenmedizin HIV/AIDS Symposium Infektiologie/ Klin. Mikrobiologie Tropenmedizin HIV/AIDS BMBF-Symposium Symposien Infektiologie/ Klin. Mikrobiologie Tropenmedizin Hausarzt- Symposium I Best paper session II Posterbegehung Posterbegehung Symposien Lunchsymposien Infektiologie/ Klin. Mikrobiologie Mykologie HIV/AIDS Lunchsymposien Infektiologie/ Klin. Mikrobiologie Mykologie HIV/AIDS Infektiologie/ Klin. Mikrobiologie HIV/AIDS Hausarzt- Symposium II Pause Pause Verabschiedung Symposien Symposien Begrüßung Infektiologie/ Infektiologie/ Klin. Mikrobiologie Klin. Mikrobiologie Plenarvortrag Tropenmedizin HIV/AIDS Pause Best Poster Session I Best Poster Session II Symposien GTZ-Symposium ESCMID-Symposium Infektiologie/ Klin. Mikrobiologie Pause Pause Tropenmedizin Reisemedizin- Symposium I Pflege-Symposium I Symposien Infektiologie/ Klin. Mikrobiologie Mykologie Best paper session I Symposien Infektiologie/ Klin. Mikrobiologie Tropenmedizin Mykologie Pause Pause Pause Symposien Symposien Mykologie HIV/AIDS Reisemedizin- Symposium II Pflege-Symposium II Eröffnung/ Festvortrag anschließend Empfang im Wallraf- Richartz-Museum Infektiologie/ Klin. Mikrobiologie HIV/AIDS Symposien Infektiologie/ Klin. Mikrobiologie Mitgliederversammlungen Mitgliederversammlungen 14
15 * Zyvoxid ist zugelassen zur Behandlung von Infektionen, wenn bekannt ist oder vermutet wird, dass sie durch empfindliche Gram-positive Erreger verursacht sind: nosokomiale Pneumonie, ambulant erworbene Pneumonie. Bei schweren Haut- und Weichteilinfektionen nur dann, wenn ein mikrobiol. Test ergeben hat, dass die Infektion durch empfindliche Gram-positive Erreger verursacht ist. Zyvoxid 600 mg Filmtabletten. Zyvoxid 100 mg/5 ml Granulat zur Herstellung einer Suspension zum Einnehmen. Zyvoxid 2 mg/ml Infusionslösung. Wirkstoff: Linezolid. Zusammensetzung: Zyvoxid 600 mg Filmtabletten: Arzneilich wirksamer Bestandteil: 1 Filmtablette enthält 600 mg Linezolid. Sonstige Bestandteile: Mikrokristalline Cellulose (E 460), Maisstärke, Carboxymethylstärke-Natrium (Typ A) (Ph.Eur.), Hyprolose (E 463), Magnesiumstearat (E 572), Hypromellose (E 464), Titandioxid (E 171), Macrogol 400, Carnaubawachs (E 903), rote Tinte, Eisen (III)-oxid (E 172). Zyvoxid 100 mg/5 ml Granulat zur Herstellung einer Suspension zum Einnehmen: Arzneilich wirksamer Bestandteil: Nach Herstellung mit 123 ml Wasser enthalten 5 ml Suspension 100 mg Linezolid. Sonstige Bestandteile: Sucrose, Mannitol (Ph.Eur.) (E 421), mikrokristalline Cellulose (E 460), Carmellose-Natrium (E 466), Aspartam (E 951), hochdisperses Siliciumdioxid (E 551), Natriumcitrat (E 331), Xanthangummi (E 415), Natriumbenzoat (E 221), Citronensäure (E 330), Natriumchlorid, Süßstoffe (Fructose, Maltodextrin, Monoammoniumglycyrrhizinat, Sorbitol), Orangenaroma, Orangencremearoma, Pfefferminzaroma und Vanillearoma. Zyvoxid 2 mg/ml Infusionslösung: Arzneilich wirksamer Bestandteil: 1 ml enthält 2 mg Linezolid. Der 300 ml- Infusionsbeutel enthält entsprechend 600 mg Linezolid. Sonstige Bestandteile: Glucose-Monohydrat (Ph.Eur.), Natriumcitrat (Ph.Eur.) (E 331), wasserfreie Citronensäure (Ph.Eur.) (E 330), Salzsäure 10 % (E 507), Natriumhydroxid (E 524), Wasser für Injektionszwecke. Anwendungsgebiete: Nosokomiale Pneumonie, ambulant erworbene Pneumonie, wenn bekannt ist oder vermutet wird, dass diese durch empfindliche Gram-positive Erreger verursacht sind. Bei schweren Haut- und Weichteilinfektionen nur dann, wenn ein mikrobiol. Test ergeben hat, dass die Infektion d. empfindliche Gram-positive Erreger verursacht ist. Behandlung mit Linezolid nur im Klinikumfeld beginnen unter Berücksichtigung der Empfehlungen eines Experten (Mikrobiologe, Spezialist f. Infektionskrankheiten). Linezolid ist nicht wirksam bei Infektionen durch Gram-negative Erreger. Bei gleichzeitigem Nachweis oder Verdacht eines Gram-negativen Krankheitserregers muss gleichzeitig eine spez. Therapie gegen Gram-negative Erreger eingeleitet werden. Offizielle Empfehlungen zum angemessenen Gebrauch von Antibiotika müssen berücksichtigt werden. Gegenanzeigen: Überempfindlichkeit gegen Linezolid oder einen der sonstigen Bestandteile des Arzneimittels. Patienten, die einen Hemmstoff der Monoaminoxidase A oder B einnehmen (z. B. Phenelzin, Isocarboxazid, Selegilin, Moclobemid), oder innerhalb der letzten 2 Wochen eingenommen haben. Patienten mit folgender zu Grunde liegender klinischer Symptomatik oder unter folgenden Begleitmedikationen, es sei denn es liegen Möglichkeiten zur genauen Beobachtung und Kontrolle des Blutdrucks vor: Patienten mit unkontrollierter Hypertonie, Phäochromozytom, Karzinoid, Thyreotoxikose, bipolarer Depression, schizoaffektiver Psychose, akuten Verwirrtheitszu ständen. Patienten, die eines der folgenden Medikamente einnehmen: Serotonin-Wiederaufnahmehemmer, trizyklische Antidepressiva, Serotonin-5HT1-Rezeptoragonisten (Triptane), direkt oder indirekt wirkende Sympathomimetika (einschließlich adrenerger Bronchodilatatoren, Pseudoephedrin oder Phenylpropanolamin), vasopressorische Mittel (z. B. Adrenalin, Noradrenalin), dopaminerge Mittel (z. B. Dopamin, Dobutamin), Pethidin oder Buspiron. Stillzeit: während der Therapie nicht stillen. Kinder und Jugendliche <18 Jahre (keine ausreichende Erfahrung). Nebenwirkungen: In klinischen Studien: Häufig: Candidiasis (insbesondere oral und vaginal) oder Mykose; Kopfschmerzen, Geschmacksstörungen (metallischer Geschmack); Diarrhoe (bei Verdacht auf pseudomembranöse Kolitis kann das Absetzen von Linezolid erforderlich sein!), Übelkeit, Erbrechen; veränderte Leberfunktionstests; erhöhte AST, ALT, LDH, alkalische Phosphatase, BUN, Kreatinkinase, Lipase, Amylase oder Glucose (nicht nüchtern), vermindertes Gesamteiweiß, Albumin, Natrium oder Kalzium, erhöhtes oder reduziertes Kalium oder Bicarbonat; erhöhte Neutrophilenzahl oder Eosinophilenzahl, reduziertes Hämoglobin, Hämatokrit oder reduzierte Erythrozytenzahl, erhöhte oder reduzierte Thrombozyten- oder Leukozytenzahlen. Gelegentlich: Vaginitis; Eosinophilie, Leukopenie, Neutropenie, Thrombozytopenie; Schlaflosigkeit; Schwindel, Hypästhesie, Parästhesie; verschwommenes Sehen; Tinnitus; Hypertonie, Phlebitis/Thrombophlebitis; lokalisierte oder allgemeine Abdominalschmerzen, Obstipation, Mundtrockenheit, Dyspepsie, Gastritis, Glossitis, weicher Stuhl, Pankreatitis, Stomatitis, Zungenverfärbung oder -veränderung; Dermatitis, Diaphorese, Pruritus, Hautausschlag, Urtikaria; Polyurie; vulvovaginale Störungen; Schüttelfrost, Müdigkeit, Fieber, Schmerzen an der Injektionsstelle, vermehrter Durst, lokalisierte Schmerzen; erhöhtes Gesamtbilirubin, Kreatinin, Natrium oder Kalzium, reduzierter Glucosespiegel (im nüchternen Zustand), erhöhtes oder reduziertes Chlorid; erhöhte Retikulozytenzahl, reduzierte Neutrophilenzahl. In Einzelfällen als schwerwiegend betrachtet: lokalisierte Abdominalschmerzen, transiente ischämische Attacken, Hypertonie, Pankreatitis und Nierenversagen. Während der klinischen Studien wurde ein Fall einer Arrhythmie (Tachykardie) im Zusammenhang mit der Linezolid-Einnahme berichtet. Bei Gabe bis zu 28 Tagen kam es bei weniger als 0,1 % der Patienten zu einer Anämie, in einem Compassionate-Use-Programm mit Patienten mit lebensbedrohlichen Infektionen und Begleiterkrankungen bei 2,5 % (bei Behandlungsdauer 28 Tage) bzw. 12,3 % (bei Behandlungsdauer über 28 Tage); der Anteil schwerer Anämien, die eine Bluttransfusion erforderlich machten, war höher bei Behandlungsdauer über 28 Tage. Die Sicherheitsdaten aus klinischen Studien bei mehr als 500 pädiatrischen Patienten (Alter bis zu 17 Jahren) haben keine Hinweise darauf erbracht, dass sich bei Linezolid das Nebenwirkungsprofil bei pädiatrischen Patienten von dem bei Erwachsenen unterscheidet. Nach Markteinführung: Antibiotika-assoziierte Kolitis einschließlich pseudomembranöse Kolitis, mit möglicherweise lebensbedrohlichen Begleitkomplikationen; Anämie (Notwendigkeit einer Bluttransfusion steigt bei Patienten mit Behandlungsdauer >28 Tage), Leukozytopenie, Neutropenie, Thrombozytopenie, Panzytopenie und Myelosuppression; Anaphylaxie; Lactatazidose; periphere Neuropathie (überwiegend bei Behandlungsdauer >28 Tage), Krämpfe (überwiegend bei Patienten mit epileptischen Anfällen oder Risikofaktoren für epileptische Anfälle in der Anamnese), Serotonin-Syndrom (Einzelfälle); optische Neuropathie (teilweise mit nachfolgender Erblindung; überwiegend bei Behandlungsdauer >28 Tage); superfizielle Zahnverfärbungen, Angioödem, bullöse Hauterscheinungen (z. B. Stevens-Johnson-Syndrom). Warnhinweise: Infusionslösung: Jeder ml der Lösung enthält 45,7 mg Glucose (entspricht 13,7 g/300 ml) und 0,38 mg Natrium (entspricht 114 mg/300 ml). Packungsbeilage beachten. Granulat: Enthält Sucrose, Mannitol und 8,5 mg Natrium pro 5 ml der Dosis. Die zubereitete Suspension enthält eine Phenylalanin-Quelle (Aspartam) mit einer Äquivalenz-Dosis von 20 mg/5 ml. Packungsbeilage beachten. Bitte beachten Sie außerdem die Fachinformation. Abgabestatus: Verschreibungspflichtig. Pharmazeutischer Unternehmer: PHARMACIA GmbH/PFIZER PHARMA GmbH, Berlin. Stand: Juni b-9v10zy-0-0
16 FeSTVORTRAgAmmITTWOCH,23.JunI2010,18.00uHR Unsterbliche Musik und tödliche Blutvergiftung der Sepsistod berühmter Komponisten Prof. Dr. Dr. h.c. E. Th. Rietschel, Berlin PlenARVORTRÄge Wie entziehen sich Immundefizienzviren der Kontrolle des Immunsystems? Prof. Dr. Dr. F. Kirchhoff, Ulm New Influenza Virus Infection Prof. Dr. R.A.M. Fouchier, Rotterdam, Niederlande Sinnvolle Hygienemaßnahmen bei multiresistenten Erregern (MRSA) muss alles evidenzbasiert sein? PD Dr. S. Harbarth, Genf, Schweiz Verteidigungsstrategien des intestinalen Immunsystems Dr. K. Brandl, La Jolla, CA, USA PROgRAmm Newer TB diagnostics and Biomarkers Prof. Dr. A. Zumla, London, Großbritannien 16
17 VIRUSLAST schnell und 1,2 dauerhaft SENKEN SUSTIVA NEU N3 Studie ACTG 5142: SUSTIVA + 2NRTIs virologisch überlegen durch signifi kant späteres virologisches Versagen als LPV/r + 2 NRTIs (p=0,006) 1 späteres virologisches Versagen bei Patienten mit Baseline HIV-1-RNA Kopien/ml als LPV/r + 2 NRTIs (p=0,01) 1 Studie ACTG 5160s: SUSTIVA + 2NRTIs senkt die Viruslast signifikant stärker in der First-Line-Therapie zu Tag 7 als LPV/r-haltige Regime (p<0,001), mit Korrelation von besseren virologischem Anspechen <50 Kopien/ml zu Woche 24 (p<0,001), 48 (p=0,036) und 96 (p=0,018) 2 For a life, for a future SUSTIVA 50 / 200 mg Hartkapseln, SUSTIVA 600 mg Filmtabletten, SUSTIVA 30 mg/ml Lösung zum Einnehmen. WIRKSTOFF: Efavirenz. ZUSAMMENSETZUNG: Arzneilich wirksamer Bestandteil: Efavirenz 50 mg / 200 mg pro Hartkapsel; 600 mg pro Filmtablette; 30 mg/ml Lösung. Sonstige Bestandteile: SUSTIVA Hartkapseln: Kapselkern: Natriumdodecylsulfat, Lactose-Monohydrat, Magnesiumstearat, Poly(O-carboxymethyl) stärke, Natriumsalz. Kapselhülle: Gelatine, Natriumdodecylsulfat, Titandioxid (E171), Siliciumdioxid, Eisenoxidhydrat (E172). Drucktinte: Carminsäure (E120), Indigocarmin (E132), Titandioxid (E171). SUSTIVA Filmtablette: Tablettenkern: Croscarmellose-Natrium, mikrokristalline Cellulose, Natriumdodecylsulfat, Hyprolose, Lactose-Monohydrat, Magnesiumstearat. Filmüberzug: Hypromellose (E464), Titandioxid (E171), Macrogol 400, Eisenoxidhydrat (E172), Carnaubawachs. Drucktinte: Hypromellose (E464), Propylenglykol, Carminsäure (E120), Indigocarmin (E132), Titandioxid (E171). SUSTIVA Lösung zum Einnehmen: mittelkettige Triglyzeride, Benzoesäure (E210), Erdbeer-/Pfefferminzaroma. ANWENDUNGSGEBIETE: Zur antiretroviralen Kombinationsbehandlung von HIV-1 infi zierten Erwachsenen, Jugendlichen und Kindern im Alter ab 3 Jahren. Sustiva-Lösung zum Einnehmen ist angezeigt bei Pat., die Hartkapseln oder Filmtabletten nicht schlucken können. GEGENANZEIGEN: Überempfi ndlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile. Nicht gleichzeitig mit Terfenadin, Astemizol, Cisaprid, Midazolam, Triazolam, Pimozid, Bepridil, Mutterkorn-Alkaloiden (z.b. Ergotamin und -derivate) oder Johanniskraut einnehmen. Schwere Leberschädigung (Child-Pugh-Klassifi kation C). NEBENWIRKUNGEN: Nach Beginn einer anti retroviralen Kombinationstherapie Immun-Reaktivierungs-Syndrom möglich. Unter Kombinationstherapie krankhafte Fettumverteilung (Lipodystrophie), Stoffwechselanomalien und Osteonekrose beschrieben. Sehr häufi g (mind. 1/10 Pat.): Hautausschlag. Häufi g (mind. 1/100 Pat.): abnormales Träumen, Konzentrationsstörungen, Schwindel, Kopfschmerzen, Schlafl osigkeit, Som nolenz, Bauchschmerzen, Durchfall, Übelkeit, Erbrechen, Juckreiz, Müdigkeit, Angst, Depressionen. Gelegentlich (mind. 1/1.000 Pat.): Unruhe, Amnesie, Ataxie, Koordinationsstörungen, Verwirrtheit, Konvulsionen, abnormales Denken, verschwommenes Sehen, Gleichgewichtsstörungen, akute Pankrea titis, Erythema multiforme, Stevens-Johnson-Syndrom, Überempfi ndlichkeit, akute Hepatitis, Gynäkomastie, Affektlabilität, Aggressionen, Euphorie, Hallu zinationen, Manie, Paranoia, Suizidversuch, Suizidgedanken. Nach Markt einführung traten zusätzliche Nebenwirkungen auf. Zerebelläre Koordinations- und Gleichgewichtsstörungen, Wahnvorstellungen, Leberversagen, Neurosen, photoallergische Dermatitis, Psychosen und vollendeter Selbstmord. VERSCHREIBUNGSSTATUS: Verschreibungspfl ichtig. PHARMAZEUTISCHER UNTERNEHMER: Bristol-Myers Squibb Pharma EEIG, Uxbridge Business Park, Sanderson Road, UB8 1 DH Uxbridge, Middlesex, Vereinigtes Königreich. STAND: Dezember QUELLEN: 1. Riddler SA et al. Class-sparing regimens for initial treatment of HIV-1 infection. NEJM 2008; 358: Haubrich RH, et al. Initial viral decay to assess the relative antiretrovial potency of PI-, NNRTI- and NRTIsparing regimens for first line therapy of HIV-1 infection ACTG 5160s (sub-study of A5142). 14th CROI, 2007; Abstract and Oral Presentation 137. Das SUSTIVA Sicherheitsprofil in diesen Studien stimmt mit bereits bekannten Daten überein.
18 SYmPOSIumSTHemen(AuSWAHl) PROgRAmm Erregerbedingte Tumore Hepatitis B/C HIV in den Tropen Infektionskontrolle Influenza Klinische Mykologie auf der Intensivstation Klinische Mykologie in der Hämatologie Malaria Multiresistente gramnegative Bakterien Neglected Tropical Diseases Neue Ansätze in der HIV-Therapie Neue Impfungen/Impfstoffe Neurologische Infektionen Opportunistische Infektionen Respiratorische Infektionen Sepsis Sexuell übertragene Erkrankungen Staphylococcus aureus Infektionen Tuberkulose Die oben aufgeführten Symposien werden u.a. von den DGI-Sektionen Antibiotic Stewardship, HIV-Medizin, Sepsisforschung/Infektionsimmunologie, Mykobakteriosen, Nosokomiale Infektionsprävention und Pulmonale Infektionen ausgerichtet. weitere Symposien: Symposium des BMBF Bundesministerium für Bildung und Forschung (Forschergruppen klinische Infektiologie) Symposium der GTZ-Esther Gesellschaft für Technische Zusammenarbeit GmbH (Hochschulpartnerschaften ein wichtiger Beitrag zur Krankenversorgung und Forschung in Entwicklungsländern) Symposium der ESCMID (European Society of Clinical Microbiology and Infections Diseases) 18
19 NEU: Zulassungserweiterung Jetzt First-Line. 1 x täglich. Überzeugend wirksam und verträglich. Hohe genetische Resistenzbarriere. PREZISTA 75 mg/- 150 mg/- 300 mg/- 400 mg/- 600 mg Filmtabletten. Wirkstoff: Darunavir. Zusammensetz.: 1 Filmtabl. enth. 75 mg, 150 mg, 300 mg, 400 mg bzw. 600 mg Darunavir (als Ethanolat). Sonst. Bestandt.: Jede Tabl. enth. 1,375 mg (300 mg Tabl.), 0,834 mg (400 mg Tabl.) bzw. 2,750 mg (600 mg Tabl.) Gelborange S (E110), mikrokristall. Cellulose, kol loidal. wasserfreies Siliciumdioxid, Crospovidon, Magne siumstearat, Polyvinyl alkohol - teilhydrolysiert, Macro gol 3350, Titandioxid (E171), Tal kum. Anw.geb.: Zusam men mit niedrig dosiertem Ritonavir in Kombination mit anderen antiretrovir. Arzneimittln. zur Therapie v. HIV-1 Infektionen b. antiretroviral nicht vorbeh. Erw. (400 mg) od. b. antiretrov. vorbeh. Erw., ein schl. derer, d. mehrf. vorbeh. wurden (300 mg/600 mg) u. zur Bhdlg. d. HIV-1 Infekt. b. ART-erfahr. Kindern u. Jugendl. ab 6 J. u. mind. 20 kg KG (75 mg, 150 mg) Gegen anz.: Überempfindl. gg. Daru navir o. ein. sonst. Bestandt. o. Ritonavir; schw. Leberfunkt.störg. (Child-Pugh-Klasse C); gleichzeitige Anw. v. Rifampicin, dem Kombinat.präp. Lopina vir/ritonavir, Johanniskraut u. AM, deren Clea rance in hohem Maße v. CYP3A abhän gig ist u. bei denen erhöh. Plasmakonz. m. schwerwieg. u./o. le bensbedrohl. Ereign. einher gehen. Wg. Unsicherheiten bzgl. d. Entwicklungsgr. d. Blut-Hirn-Schranke u. d. Leberenzyme b. Menschen ist PREZISTA m. niedrig dos. Ritonavir nicht b. pädiatr. Pat. unter 3 Jahren anzuw.. Bes. Warnhinw. u. Vorsichtsmaßn.: Behand lgs.abbruch bei schwe rem Ausschlag; Stillzeit, Kinder unter 6 J. od. weniger als 20 kg KG; Vorsicht bei: leichter o. mäßiger Leber fkts.störg. (Child-Pugh-Klasse A u. B), chron. Hep. B u. C, Alter über 65 J.; Sulfonamidallerg.; Hämophilie, Diab. mellitus/hyperglyk.; Schwangersch. nur bei ausdrückl. Verordng.. Möglichk. entzündl. Reakt. auf asympt. Infekt. o. Infekt. verurs. v. residualen opport. Erregern bei Pat., die zu Beginn der antiretrovir. Komb. therapie eine schwerw. Immunschwäche aufweisen. Nebenwirk.: Erwachs. Pat.: Sehr häufig: Diarrhö. Häufig: Kopfschmerz, Er brechen, Übelkeit, Bauchschm., Alaninaminotrans ferase erhöht, Aspartataminotransferase erhöht, erhöhte Amylase i. Blut, Hautausschlag (inkl. makulärer, makulo papul., papul., erythemat. u. juckender Ausschlag), Hypertriglycerid., Hypercholesterin., Hyperlipid., Er schöpfg., periph. Neuropathie, Schwindel, aufgeblähter Bauch, Dyspepsie, Flatulenz, Pruritus, Lipohyperthroph., Lipodystroph., Lipoatroph., Asthenie, Schlaflosigkeit. Gelegentlich: Myokardinfarkt (akuter Myokardinfarkt), Angina pect., im EKG verläng., korrig. QT-Intervall, Thrombozyto penie, Neutropenie, Leukopenie, Eosino philenzahl erhöht, Anämie, Lethargie, Parästhesie, Hyp ästhesie, Schläf rigk., konjunkt. Hyperämie, Sehstörung, trockenes Auge, Drehschwindel, Dyspnoe, Husten, Epistaxis, Rhinorrhö, Halsirritation, Pan kreatitis, Gastritis, gastroösophag. Refluxkrankheit, (aphtöse) Stomatitis, Würgereiz, Mundtrockenh., Hämatemesis, Aufstoßen, Empfindungsstörung im Mund, Cheilitis, trockene Lippen, belegte Zunge, abdominelle Beschwerden, Bauchbeschw., Obstipat., erhöhte Lipase, (akutes) Nierenvers., Nephrolithiasis, erhöhtes Kreatinin i. Blut, vermind. renale Kreatinin-Clearance, Proteinurie, Bilirubinurie, Dysurie, Nykturie, Pollakisurie, schwerer Hautausschlag, generalis. Hautausschlag, allerg. Dermatitis, Dermatitis, Ekzem, Erythem, Akne, seborr h. Dermatitis, Hautläsionen, Xerodermie, trockene Haut, Nagelpigmentierung, Gesichtsödem, Urtikaria, Hyperhi drose, Nachtschweiß, Alopezie, Myalgie, Muskelspasmen, Muskelschwäche, musculo skelettale Steifigkeit, Arthritis, Gelenksteife, Arthral gie, Extremitätenschmerz., Osteoporose, erhöhte Kreatinin-Phosphokinase i. Blut, Diab. mell., Insulinresistenz, Polydipsie, Gicht, Anorexie, Ge wichts abnahme, Ge wichtszunahme, Hyperglykämie, Hypertonie, Pyrexie, Brust schmerz, periph. Ödem, Schüttelfrost, anomales Gefühl, Hitzegefühl, Reiz bark., Schmerz, Trockenheit, allg. Unwohlsein, Im mun rekonsti tutionssyndr., Hepatitis, zytolyt. Hepatitis, Steatosis hepatis, Transaminasen erhöht, Hepatomegalie, Bilirubin im Blut erhöht, alk. Phosph. im Blut erhöht, Gammaglutamyltransferase erhöht, erekt. Dysfunkt., Gynäkomastie, Depression, Ver wirrth.zustän de, Desorien tierth., Angstzustände, Stimmungs ver änderg., Schlaflosigk., Schlafstörg., anomale Träume, Hypothyreose, TSH-Blutspiegel erhöht, vermind. Appetit, vermehrter Appetit, vermind. HDL, Lactatdehydro genase im Blut erhöht, Alpträume, vermind. Libido, Unruhe, Herpes simplex, Synkope, Krampf anfall, Ageusie, Dysgeusie, Aufmerksamkeitsstörg., Einschränkg. d. Gedächtnisleistung, Störg. d. Schlaf rhythmus, Erröten. Selten: Erythema multiforme, Stevens-John son-syndrom. Zusätzl. od. abweichend bei nicht vorbeh. erwachs. Pat.: Sehr häufig: Übelkeit Häufig: Anorexie, Dysgeusie, abdominelle Beschw., Alopezie, trockene Haut, Er schöpfg.. Gelegentlich: Hyperlipidämie, Dys pepsie, Aspartataminotransferase erhöht, Asthenie. Zusätzl. bei antiretrov. Kombtherapie: Lipodystrophie, Stoffwech selstör. (u.a. Hypertri glyc.ämie, Hyper chol.ämie, Insulin resist., Hyperglyk. u. Hyperlaktatämie), er höh te CPK, Myalgie, Myo sitis, selten Rhabdo myolyse, Fälle v. Osteonekrose, Berichte v. Spontanblutg. bei Hämophilie-Pat.. Möglichk. entzündl. Reakt. auf asympt. Infekt. o. Infekt. verurs. v. residualen opport. Erregern bei Pat., die zu Beginn der antiretrovir. Komb. therapie eine schwerw. Immunschwäche aufweisen. Kinder und Jugendl.: Sicherheitsdaten der Phase-II-Studie DELPHI zeigten bei Kdrn. und Jugendl. ein vergleichb. Sicherheitsprofil mit dem d. Erwachsenenpopulation. Enthält Gelborange S (E 110) (nur 300 mg/- 400 mg/- 600 mg Tabl.) Stand d. Inform.: 06/09. Ver schreibungs pflichtig. Janssen-Cilag International NV, Beerse, Belgien. JANSSEN-CILAG GmbH, Neuss.
20 ReISemedIZInSYmPOSIum Mittwoch, 23. Juni 2010, ab Uhr Am Mittwoch Nachmittag, Uhr ist ein Reisemedizin-Symposium geplant. Hier werden ausgewiesene Experten über neue Entwicklungen bei Reiseimpfungen, Malaria-Prophylaxe und Reisediarrhoe informieren. Die Veranstaltung richtet sich an die Kongressteilnehmer und interessierte Ärzte im Raum Köln. Bei Interesse wenden Sie sich bitte an Das Reisemedizin-Symposium ist bei vorheriger Anmeldung kostenfrei. PFlegeSYmPOSIum deutscherpflegetag InFeKTIOnSmedIZIn Mittwoch, 23. Juni 2010, ab Uhr Am Mittwochnachmittag findet im Rahmen des KIT2010 ein integriertes Pflege-Symposium zu infektiologischen Problemen in der Krankenpflege statt, welches sich an Pflegefachkräfte der stationären und ambulanten Alten- und Krankenpflege richtet. PROgRAmm Schwerpunktthemen werden unter anderem sein: Aktuelle Behandlungskonzepte bei infizierten Wunden Multiresistente Erreger im stationären und ambulanten Sektor Die Schirmherrschaft übernimmt die Deutsche Gesellschaft für Wundheilung und Wundbehandlung e.v. (DGfW). Das Pflegesymposium ist in der normalen Kongressgebühr enthalten. Die Teilnahme ist für Pflegefachkräfte bei vorheriger Anmeldung kostenfrei. HAuSÄRZTeTAg Samstag, 26. Juni 2010, ab Uhr Im Rahmen des KIT2010 wird am Samstagvormittag ein Hausärztetag durchgeführt, welcher sich speziell an infektiologisch interessierte niedergelassene Kollegen richtet. Dieses Symposium hat infektiologische Probleme bei der ambulanten Versorgung zum Inhalt. Eine Zertifizierung wird beantragt. Hauptthemen sind u.a.: Ambulante Antibiotikatherapie Respiratorische Infektionen Resistente Erreger im ambulanten Bereich Borreliose Der Hausärztetag ist bei vorheriger Anmeldung kostenfrei. 20
21 InduSTRIeSYmPOSIen Neurologische Infektionen / HIV und Haut / ART bei Malaria und anderen Infektionskrankheiten Abbott GmbH & Co. KG, Wiesbaden Diagnose und Therapie von Candidainfektionen: Strategien im klinischen Alltag Astellas Pharma GmbH, München Prophylaxe und Therapie Antimykotische Behandlungsstrategien im klinischen Alltag Essex Pharma GmbH, München CCR5-Rezeptorantagonisten was haben sie der klassischen ART voraus? Essex Pharma GmbH, München Initialtherapie der HIV-Infektion: Was? Wann? Für wen? Gilead Sciences GmbH, Martinsried Spondylodiscitis und Diabetischer Fuß mit Infektion: Wie soll der Infektiologe reagieren? Infectopharm Arzneimittel GmbH, Heppenheim Sepsis auf der Intensivstation Janssen-Cilag GmbH, Neuss Infektionen mit grampositiven Erregern Novartis Pharma GmbH, Nürnberg Update Infektionsprävention: Gegenwart und Zukunft des Pneumokokken- Konjugatimpfstoffs Wyeth Pharma GmbH, Münster Antiretrovirale Therapie weiter gedacht Tibotec A Division of Janssen-Cilag, Neuss PROgRAmm Was bedeutet Qualität in der antiinfektiven Therapie und wie können wir sie uns leisten? Pfizer Pharma GmbH, Berlin 21
22 Die dgi stellt sich vor Die dgi ist ein Forum für den Austausch zwischen Ärzten und Wissenschaftlern, die sich für Forschung, Aus- und Weiterbildung, exzellente Krankenversorgung und Prävention im Bereich Infektionskrankheiten engagieren. Die dgi möchte infektiologisches Wissen und Verständnis vermehren und fördert Öffentlichkeitsarbeit zu Infektionskrankheiten. Sie unterstützt Interdisziplinarität und bekennt sich zur Verantwortung von Wissenschaft, Medizin und Politik für die nationale wie internationale öffentliche Gesundheit. Die dgi will... die ärztliche Weiterbildung in der Infektiologie verbessern, in Deutschland hierin internationales Niveau erreichen und eine europäische Harmonisierung der infektiologischen Weiterbildung erreichen grundlagennahe und anwendungsorientierte Forschung zu Infektionskrankheiten und infektionsmedizinischen Problemen fördern und deren Ergebnisse umsetzen helfen durch geeignete Programme und Aktivitäten eine hohe Qualität in der medizinischen Versorgung von Patienten mit Infektionskrankheiten erreichen und sichern die Aus- und Fortbildung zu infektiologischen Themen kontinuierlich und frei von kommerziellen Interessen verbessern und dabei verwandte Disziplinen und Nachbargebiete miteinbeziehen das infektiologische Wissen und Verständnis in der Öffentlichkeit und Politik vermehren und mehr Bewusstsein für Prävention und Problemlösungen im Sinne internationaler Gesundheit schaffen dgi-geschäftstelle Frau Marianne Fellhauer c/o Klinik für Infektiologie und Pneumologie Charité Campus Virchow-Klinikum Augustenburger Platz 1 D Berlin Tel./Fax: administration@dgi-net.de dgi-vorstandssekretariat Frau Gabriele Peyerl-Hoffmann Frau Anja Ludolph-Donislawski c/o Zentrum Infektiologie und Reisemedizin Medizinische Universitätsklinik Hugstetter Strasse 55 D Freiburg i.br. Tel./Fax: vorstand@dgi-net.de Erster Vorsitzender Prof. Dr. Winfried V. Kern Stellv. Vorsitzender/ Geschäftsführer Prof. Dr. Bernd Salzberger Schatzmeister Prof. Dr. Bernhard R. Ruf Beisitzer Prof. Dr. Norbert Suttorp Beisitzer Prof. Dr. Christian Drosten Sprecher des Beirats/ KIT2010-Präsident Prof. Dr. Gerd Fätkenheuer Unterstützen Sie Infektionsforschung und eine leistungsfähige, patientengerechte Infektionsmedizin DGI DGI-Förderverein/-Akademie Meta-Alexander-Stiftung Walter-Marget-Vereinigung BDI-Sektion Infektiologie die Infrastruktur und Kooperationen zur Erreichung obiger Ziele verbessern. Wenn Sie Interesse an einer Mitgliedschaft haben:
11. Kölner Antibiotika-Tag: Was gibt es Neues in der Klinischen Infektiologie?
 11. Kölner Antibiotika-Tag: Was gibt es Neues in der Klinischen Infektiologie? Samstag, 18. Januar 2014 9.00-13.30 Uhr Tagungsort (geändert): Hörsaal I LFI der Universität zu Köln Joseph-Stelzmann-Straße
11. Kölner Antibiotika-Tag: Was gibt es Neues in der Klinischen Infektiologie? Samstag, 18. Januar 2014 9.00-13.30 Uhr Tagungsort (geändert): Hörsaal I LFI der Universität zu Köln Joseph-Stelzmann-Straße
WAS finde ich WO im Beipackzettel
 WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Heumann s Blasen- und Nierentee Solubitrat Wirkstoffe: Dickextrakt aus Birkenblättern, Dickextrakt aus Riesengoldrutenkraut Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Heumann s Blasen- und Nierentee Solubitrat Wirkstoffe: Dickextrakt aus Birkenblättern, Dickextrakt aus Riesengoldrutenkraut Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Legalon SIL - Trockensubstanz zur Infusionsbereitung
 PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Legalon SIL - Trockensubstanz zur Infusionsbereitung Wirkstoff: Silibinin-C-2,3-bis(hydrogensuccinat), Dinatriumsalz Lesen Sie die gesamte
PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Legalon SIL - Trockensubstanz zur Infusionsbereitung Wirkstoff: Silibinin-C-2,3-bis(hydrogensuccinat), Dinatriumsalz Lesen Sie die gesamte
Rationaler Einsatz von Antibiotika in der Humanmedizin
 Rationaler Einsatz von Antibiotika in der Humanmedizin Werner Handrick September 2011 Einsatz von Antibiotika in der Humanmedizin Antibiotika spielen eine wichtige Rolle in der klinischen Infektionsmedizin
Rationaler Einsatz von Antibiotika in der Humanmedizin Werner Handrick September 2011 Einsatz von Antibiotika in der Humanmedizin Antibiotika spielen eine wichtige Rolle in der klinischen Infektionsmedizin
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. PROGESTOGEL 1 % Gel. Progesteron
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER PROGESTOGEL 1 % Gel Progesteron Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. Heben
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER PROGESTOGEL 1 % Gel Progesteron Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. Heben
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Viscosan - Augentropfen Wirkstoff: Hypromellose
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Viscosan - Augentropfen Wirkstoff: Hypromellose Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Viscosan - Augentropfen Wirkstoff: Hypromellose Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
Sidroga Blasentee akut Wirkstoffe: Bärentraubenblätter, Birkenblätter, Goldrutenkraut, Orthosiphonblätter
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Sidroga Blasentee akut Wirkstoffe: Bärentraubenblätter, Birkenblätter, Goldrutenkraut, Orthosiphonblätter Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Sidroga Blasentee akut Wirkstoffe: Bärentraubenblätter, Birkenblätter, Goldrutenkraut, Orthosiphonblätter Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Patienten. Desloratadin Genericon 5 mg Filmtabletten. Wirkstoff: Desloratadin
 Gebrauchsinformation: Information für Patienten Desloratadin Genericon 5 mg Filmtabletten Wirkstoff: Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Patienten Desloratadin Genericon 5 mg Filmtabletten Wirkstoff: Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Nasa Rhinathiol 0,1 %ige Nasenspray, Lösung Xylometazolinhydrochlorid
 Seite 1/5 Packungsbeilage Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mir der Anwendung dieses Arzneimittels beginnen. Sie enthält wichtige Informationen für Ihre Behandlung. Wenn
Seite 1/5 Packungsbeilage Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mir der Anwendung dieses Arzneimittels beginnen. Sie enthält wichtige Informationen für Ihre Behandlung. Wenn
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Tantum Verde 3 mg Pastillen mit Minzgeschmack Wirkstoff: Benzydaminhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tantum Verde 3 mg Pastillen mit Minzgeschmack Wirkstoff: Benzydaminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tantum Verde 3 mg Pastillen mit Minzgeschmack Wirkstoff: Benzydaminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. AERIUS 5 mg Filmtabletten Desloratadin
 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN AERIUS 5 mg Filmtabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN AERIUS 5 mg Filmtabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Kamillosan -Mundspray. Kamillenblütenauszug Pfefferminzöl Anisöl
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Kamillosan -Mundspray Kamillenblütenauszug Pfefferminzöl Anisöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Kamillosan -Mundspray Kamillenblütenauszug Pfefferminzöl Anisöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. ALLEGRATAB 120 mg Filmtabletten Fexofenadinhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER ALLEGRATAB 120 mg Filmtabletten Fexofenadinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER ALLEGRATAB 120 mg Filmtabletten Fexofenadinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
www.kit2010.de PROGRAMMÜBERSICHT
 www.kit2010.de PROGRAMMÜBERSICHT PROGRAMMÜBERSICHT MITTWOCH, 23. JUNI 2010 Großer Saal Kleiner Saal Isabellen-Saal Stifter-Saal 14:00 14:15 Kongresseröffnung 14:15 14:45 Plenarvortrag 1, PLE 01 Aktuelle
www.kit2010.de PROGRAMMÜBERSICHT PROGRAMMÜBERSICHT MITTWOCH, 23. JUNI 2010 Großer Saal Kleiner Saal Isabellen-Saal Stifter-Saal 14:00 14:15 Kongresseröffnung 14:15 14:45 Plenarvortrag 1, PLE 01 Aktuelle
Gebrauchsinformation: Information für Patienten
 Gebrauchsinformation: Information für Patienten Esberitox -Tabletten Trockenextrakt aus einer Mischung von Lebensbaumspitzen und -blättern, Purpursonnenhutwurzel, Blassfarbener Sonnenhutwurzel und Färberhülsenwurzel
Gebrauchsinformation: Information für Patienten Esberitox -Tabletten Trockenextrakt aus einer Mischung von Lebensbaumspitzen und -blättern, Purpursonnenhutwurzel, Blassfarbener Sonnenhutwurzel und Färberhülsenwurzel
Erratum Benkert, Pocket Guide, Psychopharmaka von A bis Z. 3.Aufl. ISBN (print): 978-3-642-54766-9/ DOI 10.1007/978-3-642-54767-6
 Erratum Benkert, Pocket Guide, Psychopharmaka von A bis Z. 3.Aufl. ISBN (print): 978-3-642-54766-9/ DOI 10.1007/978-3-642-54767-6 Trotz sorgfältiger Erstellung des Buchs Benkert, Pocket Guide, Psychopharmaka
Erratum Benkert, Pocket Guide, Psychopharmaka von A bis Z. 3.Aufl. ISBN (print): 978-3-642-54766-9/ DOI 10.1007/978-3-642-54767-6 Trotz sorgfältiger Erstellung des Buchs Benkert, Pocket Guide, Psychopharmaka
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Tebofortan 40 mg - Filmtabletten. Wirkstoff: Trockenextrakt aus Ginkgo-biloba-Blättern
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tebofortan 40 mg - Filmtabletten Wirkstoff: Trockenextrakt aus Ginkgo-biloba-Blättern Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tebofortan 40 mg - Filmtabletten Wirkstoff: Trockenextrakt aus Ginkgo-biloba-Blättern Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
1. Was sind Dorithricin Halstabletten und wofür werden sie angewendet?
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Dorithricin - Halstabletten Wirkstoffe: Tyrothricin, Benzalkoniumchlorid, Benzocain Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Dorithricin - Halstabletten Wirkstoffe: Tyrothricin, Benzalkoniumchlorid, Benzocain Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
Gebrauchsinformation: Information für den Anwender
 Wortlaut der für die Gebrauchsinformation vorgesehenen Angaben Stand: Mai 2008 1 Gebrauchsinformation: Information für den Anwender Harntee-Steiner, Teeaufgusspulver Zur Anwendung bei Heranwachsenden ab
Wortlaut der für die Gebrauchsinformation vorgesehenen Angaben Stand: Mai 2008 1 Gebrauchsinformation: Information für den Anwender Harntee-Steiner, Teeaufgusspulver Zur Anwendung bei Heranwachsenden ab
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. AERIUS 5 mg Schmelztabletten Desloratadin
 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN AERIUS 5 mg Schmelztabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN AERIUS 5 mg Schmelztabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Wie unsere Augen Erfahren Sie, wie wir sehen, und wie Sie Ihre Vision zu schützen.
 Wie unsere Augen Erfahren Sie, wie wir sehen, und wie Sie Ihre Vision zu schützen. Levobunolol ist ein Beta-Blocker, der den Druck im Inneren des Auges reduziert. Levobunolol Augen (Auge) ist für die Behandlung
Wie unsere Augen Erfahren Sie, wie wir sehen, und wie Sie Ihre Vision zu schützen. Levobunolol ist ein Beta-Blocker, der den Druck im Inneren des Auges reduziert. Levobunolol Augen (Auge) ist für die Behandlung
!!! Folgeerkrankungen
 Ein zu hoher Blutzuckerspiegel kann Folgen auf Ihr Herzkreislaufsystem haben und zu Erkrankungen wie der Schaufensterkrankheit, einer Angina pectoris, einem Herzinfarkt oder einem Schlaganfall führen.
Ein zu hoher Blutzuckerspiegel kann Folgen auf Ihr Herzkreislaufsystem haben und zu Erkrankungen wie der Schaufensterkrankheit, einer Angina pectoris, einem Herzinfarkt oder einem Schlaganfall führen.
Packungsbeilage CORSODYL Mundspüllösung / Spray 03-2012 Seite 1/5 BE106802 / BE191764 Belgien GEBRAUCHINFORMATION: INFORMATION FÜR DEN ANWENDER
 Seite 1/5 BE106802 / BE191764 Belgien GEBRAUCHINFORMATION: INFORMATION FÜR DEN ANWENDER CORSODYL 200mg/100ml mundwasser CORSODYL 200mg/100ml spray zur Anwendung in der Mundhöhle Chlorhexidindigluconat
Seite 1/5 BE106802 / BE191764 Belgien GEBRAUCHINFORMATION: INFORMATION FÜR DEN ANWENDER CORSODYL 200mg/100ml mundwasser CORSODYL 200mg/100ml spray zur Anwendung in der Mundhöhle Chlorhexidindigluconat
Welche der aufgeführten zahnmedizinischen relevanten Erscheinungen treffen auf Sie zu?
 Ihre Wünsche sind uns wichtig. Grund Ihres Besuches?... Worauf legen Sie besonderen Wert?... Was haben Sie bisher beim Zahnarztbesuch besonders vermisst?.. Welche der aufgeführten zahnmedizinischen relevanten
Ihre Wünsche sind uns wichtig. Grund Ihres Besuches?... Worauf legen Sie besonderen Wert?... Was haben Sie bisher beim Zahnarztbesuch besonders vermisst?.. Welche der aufgeführten zahnmedizinischen relevanten
Gebrauchsinformation: Information für Patienten. Urgenin Tropfen Tinktur aus Serenoa repens (Bartram Small) ; Saft aus Echinacea purpurea (Moench)
 Gebrauchsinformation: Information für Patienten Urgenin Tropfen Tinktur aus Serenoa repens (Bartram Small) ; Saft aus Echinacea purpurea (Moench) Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für Patienten Urgenin Tropfen Tinktur aus Serenoa repens (Bartram Small) ; Saft aus Echinacea purpurea (Moench) Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Clarityn 10 mg - Brausetabletten Wirkstoff: Loratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Clarityn 10 mg - Brausetabletten Wirkstoff: Loratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
Sandoz Pharmaceuticals AG
 Die Pille danach. Was ist eine Notfallverhütung oder die sogenannte «Pille danach»? 1 Wann wird NorLevo Uno eingenommen? 2 Bei der «Pille danach» handelt es sich um eine Notfallverhütung, die eine unerwünschte
Die Pille danach. Was ist eine Notfallverhütung oder die sogenannte «Pille danach»? 1 Wann wird NorLevo Uno eingenommen? 2 Bei der «Pille danach» handelt es sich um eine Notfallverhütung, die eine unerwünschte
Gebrauchsinformation: Information für Anwender. LOMUSOL Augentropfen. Wirkstoff: Dinatriumcromoglicat
 Gebrauchsinformation: Information für Anwender LOMUSOL Augentropfen Wirkstoff: Dinatriumcromoglicat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Gebrauchsinformation: Information für Anwender LOMUSOL Augentropfen Wirkstoff: Dinatriumcromoglicat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen
 Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Wirkstoffe: Trockenextrakt aus Birkenblättern, Trockenextrakt aus Goldrutenkraut
 Gebrauchsinformation: Information für Anwender HEUMANN Blasen- und Nierentee SOLUBITRAT uro Teeaufgusspulver Wirkstoffe: Trockenextrakt aus Birkenblättern, Trockenextrakt aus Goldrutenkraut Lesen Sie die
Gebrauchsinformation: Information für Anwender HEUMANN Blasen- und Nierentee SOLUBITRAT uro Teeaufgusspulver Wirkstoffe: Trockenextrakt aus Birkenblättern, Trockenextrakt aus Goldrutenkraut Lesen Sie die
Ankündigung. Heidelberger Onkologietage Gynäkologie und Senologie. 20. - 21. Februar 2009
 Ankündigung Heidelberger Onkologietage Gynäkologie und Senologie 20. - 21. Februar 2009 Vorsitz Prof. Dr. med. Ch. Sohn Prof. Dr. med. O. D. Wiestler Prof. Dr. med. Ch. von Kalle Prof. Dr. med. D. Jäger
Ankündigung Heidelberger Onkologietage Gynäkologie und Senologie 20. - 21. Februar 2009 Vorsitz Prof. Dr. med. Ch. Sohn Prof. Dr. med. O. D. Wiestler Prof. Dr. med. Ch. von Kalle Prof. Dr. med. D. Jäger
Atronase 0,3 mg/ml Nasenspray, Lösung (Ipratropiumbromid)
 GEBRAUCHSINFORMATION ATRONASE 0,3 MG/ML NASENSPRAY, LÖSUNG Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel ist auch ohne Verschreibung
GEBRAUCHSINFORMATION ATRONASE 0,3 MG/ML NASENSPRAY, LÖSUNG Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel ist auch ohne Verschreibung
Packungsbeilage GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. NUSO-SAN Menthol 1mg/ml Nasenspray, Lösung. Xylometazolinhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER NUSO-SAN Menthol 1mg/ml Nasenspray, Lösung Xylometazolinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER NUSO-SAN Menthol 1mg/ml Nasenspray, Lösung Xylometazolinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
10 Antworten zum Thema Generika
 10 Antworten zum Thema Generika Die mit dem Regenbogen Liebe Leserin, Lieber Leser Immer mehr Schweizerinnen und Schweizer leiden unter den jährlich steigenden Gesundheitskosten und Krankenkassenprämien.
10 Antworten zum Thema Generika Die mit dem Regenbogen Liebe Leserin, Lieber Leser Immer mehr Schweizerinnen und Schweizer leiden unter den jährlich steigenden Gesundheitskosten und Krankenkassenprämien.
1. WAS IST DAFALGAN Zäpfchen UND WOFÜR WIRD ES ANGEWENDET?
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER DAFALGAN Säuglinge 80 mg Zäpfchen DAFALGAN Kleinkinder 150 mg Zäpfchen DAFALGAN große Kinder 300 mg Zäpfchen Paracetamol Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER DAFALGAN Säuglinge 80 mg Zäpfchen DAFALGAN Kleinkinder 150 mg Zäpfchen DAFALGAN große Kinder 300 mg Zäpfchen Paracetamol Lesen Sie die gesamte Packungsbeilage
Hepatyrix Injektionssuspension Hepatitis-A-(inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert) ab dem vollendeten 15.
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER 22.07.2009 Hepatyrix Injektionssuspension Hepatitis-A-(inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert) ab dem vollendeten 15. Lebensjahr
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER 22.07.2009 Hepatyrix Injektionssuspension Hepatitis-A-(inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert) ab dem vollendeten 15. Lebensjahr
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Normhydral - lösliches Pulver
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Normhydral - lösliches Pulver p 1/5 Wirkstoffe: Wasserfreie Glucose, Natriumchlorid, Natriumcitrat, Kaliumchlorid Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Normhydral - lösliches Pulver p 1/5 Wirkstoffe: Wasserfreie Glucose, Natriumchlorid, Natriumcitrat, Kaliumchlorid Lesen Sie die gesamte Packungsbeilage
Faltschachtel. Unverkäufliches Muster (Eindruck auf Linie) Teil einer Klinikpackung, Einzelverkauf unzulässig (Eindruck auf Linie)
 Packmittelmanuskript Nr. 64000/009/94/6 Seite 2 Faltschachtel HEUMANN PHARMA GmbH & Co. Generica KG Südwestpark 50 90449 Nürnberg Urso 400 Heumann Filmtabletten mit 400 mg Ursodeoxycholsäure Zur Auflösung
Packmittelmanuskript Nr. 64000/009/94/6 Seite 2 Faltschachtel HEUMANN PHARMA GmbH & Co. Generica KG Südwestpark 50 90449 Nürnberg Urso 400 Heumann Filmtabletten mit 400 mg Ursodeoxycholsäure Zur Auflösung
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER SINUTAB 500/30 mg Tabletten SINUTAB FORTE 500/60 mg Tabletten Paracetamol und Pseudoephedrinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER SINUTAB 500/30 mg Tabletten SINUTAB FORTE 500/60 mg Tabletten Paracetamol und Pseudoephedrinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender. Delphi 0,1 % Creme Triamcinolonacetonid
 Gebrauchsinformation: Information für Anwender Delphi 0,1 % Creme Triamcinolonacetonid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Anwender Delphi 0,1 % Creme Triamcinolonacetonid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für den Anwender. Zur Anwendung bei Erwachsenen. Wirkstoff: Sumatriptan
 Gebrauchsinformation: Information für den Anwender sumatriptan-biomo 50 mg überzogene Tabletten Zur Anwendung bei Erwachsenen Wirkstoff: Sumatriptan Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für den Anwender sumatriptan-biomo 50 mg überzogene Tabletten Zur Anwendung bei Erwachsenen Wirkstoff: Sumatriptan Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Bijsluiter DE versie Imaverol 100 mg (glas) B. PACKUNGSBEILAGE 1
 B. PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION Imaverol 100 mg, Konzentrat zur örtlichen Anwendung 1.NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
B. PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION Imaverol 100 mg, Konzentrat zur örtlichen Anwendung 1.NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Zur Anwendung bei postmenopausalen Frauen Wirkstoff: Letrozol
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER letrozol-biomo 2,5 mg Filmtabletten Zur Anwendung bei postmenopausalen Frauen Wirkstoff: Letrozol Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER letrozol-biomo 2,5 mg Filmtabletten Zur Anwendung bei postmenopausalen Frauen Wirkstoff: Letrozol Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Magnevist 2 mmol/l Injektionslösung. Gadopentetsäure, Dimeglumin
 1 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Magnevist 2 mmol/l Injektionslösung Gadopentetsäure, Dimeglumin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor dieses Arzneimittel bei
1 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Magnevist 2 mmol/l Injektionslösung Gadopentetsäure, Dimeglumin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor dieses Arzneimittel bei
DAS GRÜNE REZEPT. Für eine sichere Medikation mit rezeptfreien Arzneimitteln
 DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
ANWEISUNGSKARTE FÜR DEN PATIENTEN
 Der Plan zur Risikobegrenzung in Belgien, zu dem diese Information gehört, ist eine Maßnahme, die ergriffen wurde, um eine sichere und wirksame Anwendung fon ZypAdhera TM zu garantieren. (RMA modifizierte
Der Plan zur Risikobegrenzung in Belgien, zu dem diese Information gehört, ist eine Maßnahme, die ergriffen wurde, um eine sichere und wirksame Anwendung fon ZypAdhera TM zu garantieren. (RMA modifizierte
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Postinor 750 Mikrogramm Tabletten Levonorgestrel
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Postinor 750 Mikrogramm Tabletten Levonorgestrel Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Postinor 750 Mikrogramm Tabletten Levonorgestrel Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Postinor 1500 Mikrogramm - Tablette Wirkstoff: Levonorgestrel
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Postinor 1500 Mikrogramm - Tablette Wirkstoff: Levonorgestrel Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Postinor 1500 Mikrogramm - Tablette Wirkstoff: Levonorgestrel Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
Patienteninformationsbroschüre Valproat
 Patienteninformationsbroschüre Valproat Informationen für Patientinnen Die Informationen in dieser Broschüre sind für Frauen bestimmt, denen Valproat verschrieben wird und die schwanger werden können (Frauen
Patienteninformationsbroschüre Valproat Informationen für Patientinnen Die Informationen in dieser Broschüre sind für Frauen bestimmt, denen Valproat verschrieben wird und die schwanger werden können (Frauen
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Vitagutt Vitamin E 670 mg, Weichkapsel Zur Anwendung bei Erwachsenen Wirkstoff: 1000 mg all-rac-alpha-tocopherolacetat (entsprechend 670 mg RRR-alpha- Tocopherol-Äquivalente).
Gebrauchsinformation: Information für Anwender Vitagutt Vitamin E 670 mg, Weichkapsel Zur Anwendung bei Erwachsenen Wirkstoff: 1000 mg all-rac-alpha-tocopherolacetat (entsprechend 670 mg RRR-alpha- Tocopherol-Äquivalente).
AUFKLÄRUNGSBLATT* ZUR IMPFUNG GEGEN DIE FSME (Frühsommer-Meningoenzephalitis) *(Auszug aus den jeweiligen Packungsinformationen)
 AUFKLÄRUNGSBLATT* ZUR IMPFUNG GEGEN DIE FSME (Frühsommer-Meningoenzephalitis) *(Auszug aus den jeweiligen Packungsinformationen) Lesen Sie die gesamte Information sorgfältig durch, bevor Sie sich bzw.
AUFKLÄRUNGSBLATT* ZUR IMPFUNG GEGEN DIE FSME (Frühsommer-Meningoenzephalitis) *(Auszug aus den jeweiligen Packungsinformationen) Lesen Sie die gesamte Information sorgfältig durch, bevor Sie sich bzw.
Künstlicher Hüftgelenksersatz
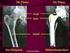 Künstlicher Hüftgelenksersatz Künstlicher Hüftgelenksersatz Was ist eine Hüftgelenk-Arthrose? Das Hüftgelenk ist eine bewegliche Verbindung zwischen dem Becken- und dem Oberschenkelknochen. Die am Gelenk
Künstlicher Hüftgelenksersatz Künstlicher Hüftgelenksersatz Was ist eine Hüftgelenk-Arthrose? Das Hüftgelenk ist eine bewegliche Verbindung zwischen dem Becken- und dem Oberschenkelknochen. Die am Gelenk
10.000 10.000. an Masern erkrankt. an Mumps erkrankt. mit Röteln infiziert
 Nutzen: Bei Viruskontakt ist mein geimpftes Kind auch künftig besser gegen Masern, Mumps und Röteln geschützt. Je mehr Menschen geimpft sind, desto unwahrscheinlicher werden Kontakte mit dem Virus. ohne
Nutzen: Bei Viruskontakt ist mein geimpftes Kind auch künftig besser gegen Masern, Mumps und Röteln geschützt. Je mehr Menschen geimpft sind, desto unwahrscheinlicher werden Kontakte mit dem Virus. ohne
LANSOYL Paraffine Gel zum Einnehmenv3.0_B2.0 1/5
 PIL September 2015 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER LANSOYL PARAFFINE 78,230 g/100 g Gel zum Einnehmen Paraffinöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
PIL September 2015 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER LANSOYL PARAFFINE 78,230 g/100 g Gel zum Einnehmen Paraffinöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
APOTHEKIA SPECIAL DIE PILLE DANACH
 APOTHEKIA SPECIAL DIE PILLE DANACH Die zwei Pillen danach In Deutschland sind aktuell zwei Wirkstoffe für die Pille danach zugelassen, Ulipristalacetat (Handelsname ellaone) und Levonorgestrel (Handelsname
APOTHEKIA SPECIAL DIE PILLE DANACH Die zwei Pillen danach In Deutschland sind aktuell zwei Wirkstoffe für die Pille danach zugelassen, Ulipristalacetat (Handelsname ellaone) und Levonorgestrel (Handelsname
Gefährlich hohe Blutzuckerwerte
 Gefährlich hohe Blutzuckerwerte In besonderen Situationen kann der Blutzuckerspiegel gefährlich ansteigen Wenn in Ausnahmefällen der Blutzuckerspiegel sehr hoch ansteigt, dann kann das für Sie gefährlich
Gefährlich hohe Blutzuckerwerte In besonderen Situationen kann der Blutzuckerspiegel gefährlich ansteigen Wenn in Ausnahmefällen der Blutzuckerspiegel sehr hoch ansteigt, dann kann das für Sie gefährlich
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Aricept 5 mg Filmtabletten Wirkstoff: Donepezilhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Aricept 5 mg Filmtabletten Wirkstoff: Donepezilhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Aricept 5 mg Filmtabletten Wirkstoff: Donepezilhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender. Cevitol 500 mg-kautabletten Wirkstoff: Ascorbinsäure (Vitamin C)
 Gebrauchsinformation: Information für Anwender Cevitol 500 mg-kautabletten Wirkstoff: Ascorbinsäure (Vitamin C) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender Cevitol 500 mg-kautabletten Wirkstoff: Ascorbinsäure (Vitamin C) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Patienten. Letrofam 2,5 mg-filmtabletten Wirkstoff: Letrozol
 Gebrauchsinformation: Information für Patienten Letrofam 2,5 mg-filmtabletten Wirkstoff: Letrozol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Patienten Letrofam 2,5 mg-filmtabletten Wirkstoff: Letrozol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
1. WAS SIND Bicalutamid Winthrop 150 mg Filmtabletten, UND WOFÜR WERDEN SIE ANGEWENDET?
 Gebrauchsinformation: Information für den Anwender Bicalutamid Winthrop 150 mg Filmtabletten Wirkstoff: Bicalutamid Für erwachsene Männer Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
Gebrauchsinformation: Information für den Anwender Bicalutamid Winthrop 150 mg Filmtabletten Wirkstoff: Bicalutamid Für erwachsene Männer Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
WAS TUN BEI ANGST & DEPRESSION? von. Hans Kottke
 Hans Kottke Blasiusstr.10 38114, Braunschweig mail@hanskottke.de ca. 701 Wörter WAS TUN BEI ANGST & DEPRESSION? von Hans Kottke Mai 2012 Die Ausgangslage Kottke / Was tun bei Angst & Depression / 2 Es
Hans Kottke Blasiusstr.10 38114, Braunschweig mail@hanskottke.de ca. 701 Wörter WAS TUN BEI ANGST & DEPRESSION? von Hans Kottke Mai 2012 Die Ausgangslage Kottke / Was tun bei Angst & Depression / 2 Es
PACKUNGSBEILAGE. CORSODYL Zahngel, 10 mg Chlorhexidin digluconat pro g Zahngel
 Seite 1/5 981 IS 153 F7 Belgien PACKUNGSBEILAGE Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Wenn Sie weitere Fragen haben, wenden Sie sich an
Seite 1/5 981 IS 153 F7 Belgien PACKUNGSBEILAGE Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Wenn Sie weitere Fragen haben, wenden Sie sich an
Durchfall in der Pflege. Der kleine Ratgeber von Aplona
 Durchfallerkrankungen Durchfall in der Pflege Der kleine von Aplona Der kleine von Aplona 3 Fotos: Titel, Seite 2, 3 und 4: Fotolia.com Durchfall in der Pflege Akute Durchfallerkrankungen stellen eine
Durchfallerkrankungen Durchfall in der Pflege Der kleine von Aplona Der kleine von Aplona 3 Fotos: Titel, Seite 2, 3 und 4: Fotolia.com Durchfall in der Pflege Akute Durchfallerkrankungen stellen eine
INFORMATIONEN ZUR NACHSORGE VON ZAHNIMPLANTATEN
 INFORMATIONEN ZUR NACHSORGE VON ZAHNIMPLANTATEN WORIN BESTEHT DIE NACHSORGE? Straumann-Implantate sind eine moderne Möglichkeit für Zahnersatz, wenn ein oder mehrere Zähne fehlen. Diese bekannte und hochwertige
INFORMATIONEN ZUR NACHSORGE VON ZAHNIMPLANTATEN WORIN BESTEHT DIE NACHSORGE? Straumann-Implantate sind eine moderne Möglichkeit für Zahnersatz, wenn ein oder mehrere Zähne fehlen. Diese bekannte und hochwertige
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Ibuprofen Sandoz 200 mg Filmtabletten Ibuprofen Sandoz 400 mg Filmtabletten Ibuprofen
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Ibuprofen Sandoz 200 mg Filmtabletten Ibuprofen Sandoz 400 mg Filmtabletten Ibuprofen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Ibuprofen Sandoz 200 mg Filmtabletten Ibuprofen Sandoz 400 mg Filmtabletten Ibuprofen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie
Neue Patientenleitlinie zu Colitis Ulcerosa erschienen
 Entzündliche Darmerkrankung wirksam behandeln Neue Patientenleitlinie zu Colitis Ulcerosa erschienen Berlin (15. November 2012) Über den aktuellen Wissenstand rund um die chronisch-entzündliche Darmerkrankung
Entzündliche Darmerkrankung wirksam behandeln Neue Patientenleitlinie zu Colitis Ulcerosa erschienen Berlin (15. November 2012) Über den aktuellen Wissenstand rund um die chronisch-entzündliche Darmerkrankung
7. Würzburger Infektiologisches Symposium
 Samstag, 14. Juli 2012 7. Würzburger Infektiologisches Symposium Antiinfektive Strategien 2012 Zentrum Innere Medizin (ZIM), Großer Hörsaal Oberdürrbacher Str. 6, 97080 Würzburg Schwerpunkt Infektiologie
Samstag, 14. Juli 2012 7. Würzburger Infektiologisches Symposium Antiinfektive Strategien 2012 Zentrum Innere Medizin (ZIM), Großer Hörsaal Oberdürrbacher Str. 6, 97080 Würzburg Schwerpunkt Infektiologie
Betreff: Citalopram hältige Arzneispezialitäten Änderungen der Fach- und Gebrauchsinformationen
 Datum: 15.11.2011 Kontakt: Mag. pharm. Dr. Ulrike Rehberger Abteilung: Tel. / Fax: +43(0)505 55 36258, DW.Fax-36207 E-Mail: ulrike.rehberger@ages.at Unser Zeichen: 16c-111114-23425-A-PHV Ihr Zeichen: Betreff:
Datum: 15.11.2011 Kontakt: Mag. pharm. Dr. Ulrike Rehberger Abteilung: Tel. / Fax: +43(0)505 55 36258, DW.Fax-36207 E-Mail: ulrike.rehberger@ages.at Unser Zeichen: 16c-111114-23425-A-PHV Ihr Zeichen: Betreff:
Europäische Arzneimittelbehörde empfiehlt Aussetzung der Marktzulassung für Raptiva
 Europäische Arzneimittelbehörde empfiehlt Aussetzung der Marktzulassung für Raptiva Darmstadt (19. Februar 2009) Die Merck KGaA hat heute bekannt gegeben, dass die europäische Arzneimittelbehörde EMEA
Europäische Arzneimittelbehörde empfiehlt Aussetzung der Marktzulassung für Raptiva Darmstadt (19. Februar 2009) Die Merck KGaA hat heute bekannt gegeben, dass die europäische Arzneimittelbehörde EMEA
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER ISOPTO CARPINE 1% Augentropfen ISOPTO CARPINE 2% Augentropfen ISOPTO CARPINE 3% Augentropfen ISOPTO CARPINE 4% Augentropfen Pilocarpinhydrochlorid Lesen
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER ISOPTO CARPINE 1% Augentropfen ISOPTO CARPINE 2% Augentropfen ISOPTO CARPINE 3% Augentropfen ISOPTO CARPINE 4% Augentropfen Pilocarpinhydrochlorid Lesen
EINVERSTÄNDISERKLÄRUNG ZUR SCHUTZIMPFUNG
 EINVERSTÄNDISERKLÄRUNG ZUR SCHUTZIMPFUNG Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff BITTE
EINVERSTÄNDISERKLÄRUNG ZUR SCHUTZIMPFUNG Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff BITTE
Krank durch Schlafstörungen
 Seite 1 von 6 I n f o r m a t i o n s m a t e r i a l v o m 1 2. 0 1. 2 0 1 2 Krank durch Schlafstörungen "Die meisten Menschen sterben an ihren Medikamenten und nicht an ihren Krankheiten", meinte der
Seite 1 von 6 I n f o r m a t i o n s m a t e r i a l v o m 1 2. 0 1. 2 0 1 2 Krank durch Schlafstörungen "Die meisten Menschen sterben an ihren Medikamenten und nicht an ihren Krankheiten", meinte der
Diabetes mellitus : Folgeschäden
 Diabetes mellitus : Folgeschäden Warum ist der Diabetes mellitus eine wichtige Erkrankung? a. Akute Probleme: Hypoglykämie Hyperglykämie Ketoazidose b. Chronische Probleme: Folgeschäden: Typische Schäden:
Diabetes mellitus : Folgeschäden Warum ist der Diabetes mellitus eine wichtige Erkrankung? a. Akute Probleme: Hypoglykämie Hyperglykämie Ketoazidose b. Chronische Probleme: Folgeschäden: Typische Schäden:
Die bewegte Frau. HIV-infizierte Frauen in Deutschland: eine Standortbestimmung 2006. Dr.med. Christiane Cordes Berlin
 Die bewegte Frau HIV-infizierte Frauen in Deutschland: eine Standortbestimmung 2006 Dr.med. Christiane Cordes Berlin HIV im Dialog 2006 Epidemiologie Deutschland 2006 49.000 HIV-Infizierte Infizierte insgesamt
Die bewegte Frau HIV-infizierte Frauen in Deutschland: eine Standortbestimmung 2006 Dr.med. Christiane Cordes Berlin HIV im Dialog 2006 Epidemiologie Deutschland 2006 49.000 HIV-Infizierte Infizierte insgesamt
Lungenentzündung gehören Sie zu einer Risikogruppe?
 copy 11pt Lungenentzündung gehören Sie zu einer Risikogruppe? Wo viele Menschen zusammenkommen, können sie besonders leicht übertragen werden: Die Erreger der Lungenentzündung. Niesen und Husten, ein Händedruck
copy 11pt Lungenentzündung gehören Sie zu einer Risikogruppe? Wo viele Menschen zusammenkommen, können sie besonders leicht übertragen werden: Die Erreger der Lungenentzündung. Niesen und Husten, ein Händedruck
Patientenleitfaden für das Gespräch mit dem Arzt. Liebe Patientin, lieber Patient!
 Patientenleitfaden für das Gespräch mit dem Arzt Liebe Patientin, lieber Patient! Je besser Sie sich auf das Gespräch mit Ihrem Arzt vorbereiten, desto leichter wird es für sie/ihn sein, eine Diagnose
Patientenleitfaden für das Gespräch mit dem Arzt Liebe Patientin, lieber Patient! Je besser Sie sich auf das Gespräch mit Ihrem Arzt vorbereiten, desto leichter wird es für sie/ihn sein, eine Diagnose
GEBRAUCHSINFORMATION
 GEBRAUCHSINFORMATION 1. Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen. Heben Sie die Packungsbeilage auf. Vielleicht möchten Sie diese
GEBRAUCHSINFORMATION 1. Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen. Heben Sie die Packungsbeilage auf. Vielleicht möchten Sie diese
Was ist AURORIX und wofür wird es angewendet? Was müssen Sie vor der Einnahme von AURORIX beachten?
 Was ist AURORIX und wofür wird es angewendet? AURORIX ist ein Arzneimittel zur Behandlung von Depressionen und bestimmten Angstzuständen (Sozialphobie). Moclobemid, der Wirkstoff von AURORIX, wirkt antriebssteigernd
Was ist AURORIX und wofür wird es angewendet? AURORIX ist ein Arzneimittel zur Behandlung von Depressionen und bestimmten Angstzuständen (Sozialphobie). Moclobemid, der Wirkstoff von AURORIX, wirkt antriebssteigernd
Methicillin Resistenter Staphylococcus Aureus (MRSA)
 Methicillin Resistenter Staphylococcus Aureus (MRSA) Allgemein Ihr Kind wurde in das UMC St Radboud in Nijmegen aufgenommen, nachdem es einige Zeit in einem anderen, wahrscheinlich ausländischen Krankenhaus
Methicillin Resistenter Staphylococcus Aureus (MRSA) Allgemein Ihr Kind wurde in das UMC St Radboud in Nijmegen aufgenommen, nachdem es einige Zeit in einem anderen, wahrscheinlich ausländischen Krankenhaus
INFORMATIONSBROSCHÜRE FÜR PATIENTEN/BEZUGSPERSONEN. Bitte lies die Packungsbeilage vor der Anwendung des Arzneimittels ABILIFY sorgfältig durch.
 Die Europäischen Gesundheitsbehörden haben die Vermarktung des Arzneimittels ABILIFY an bestimmte Bedingungen geknüpft. Die vorliegenden Informationen sind Teil des obligatorischen Risikomanagementplans
Die Europäischen Gesundheitsbehörden haben die Vermarktung des Arzneimittels ABILIFY an bestimmte Bedingungen geknüpft. Die vorliegenden Informationen sind Teil des obligatorischen Risikomanagementplans
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Levetiracetam +pharma 500 mg Filmtabletten. Wirkstoff: Levetiracetam
 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Levetiracetam +pharma 500 mg Filmtabletten Wirkstoff: Levetiracetam Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Levetiracetam +pharma 500 mg Filmtabletten Wirkstoff: Levetiracetam Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender. DAFALGAN CODEINE 500mg/30mg, Brausetabletten DAFALGAN CODEINE 500mg/30mg Filmtabletten
 Gebrauchsinformation: Information für Anwender DAFALGAN CODEINE 500mg/30mg, Brausetabletten DAFALGAN CODEINE 500mg/30mg Filmtabletten Paracetamol, halb entwässertes Codeinphosphat Lesen Sie die gesamte
Gebrauchsinformation: Information für Anwender DAFALGAN CODEINE 500mg/30mg, Brausetabletten DAFALGAN CODEINE 500mg/30mg Filmtabletten Paracetamol, halb entwässertes Codeinphosphat Lesen Sie die gesamte
Faktenbox Kombinationsbehandlung (Antidepressiva und Psychotherapie) bei schweren Depressionen
 Faktenbox (Antidepressiva und Psychotherapie) bei schweren Depressionen Nutzen und Risiken im Überblick Was ist eine? Was passiert bei einer? Bei einer werden mehrere Therapien miteinander gekoppelt: Antidepressiva
Faktenbox (Antidepressiva und Psychotherapie) bei schweren Depressionen Nutzen und Risiken im Überblick Was ist eine? Was passiert bei einer? Bei einer werden mehrere Therapien miteinander gekoppelt: Antidepressiva
Datum: Kontakt: Abteilung: Tel. / Fax: E-Mail: Unser Zeichen: Ihr Zeichen:
 BASG / AGES Institut LCM Traisengasse 5, A-1200 Wien Datum: Kontakt: Abteilung: Tel. / Fax: E-Mail: Unser Zeichen: Ihr Zeichen: 06.11.2014 Veronika Iro REGA +43 (0) 505 55 36247 pv-implementation@ages.at
BASG / AGES Institut LCM Traisengasse 5, A-1200 Wien Datum: Kontakt: Abteilung: Tel. / Fax: E-Mail: Unser Zeichen: Ihr Zeichen: 06.11.2014 Veronika Iro REGA +43 (0) 505 55 36247 pv-implementation@ages.at
Tag der Seltenen Erkrankungen Aktionstag im Uniklinikum Aachen
 Tag der Seltenen Erkrankungen Aktionstag im Uniklinikum Aachen Am 28. Februar 2015 hatten wir den Tag der seltenen Erkrankungen. Die Deutsche GBS Initiative e.v. hatte an diesem Tag die Gelegenheit, zusammen
Tag der Seltenen Erkrankungen Aktionstag im Uniklinikum Aachen Am 28. Februar 2015 hatten wir den Tag der seltenen Erkrankungen. Die Deutsche GBS Initiative e.v. hatte an diesem Tag die Gelegenheit, zusammen
Gebrauchsinformation: Information für Patienten. Candeblo 16 mg-tabletten Wirkstoff: Candesartan Cilexetil
 Gebrauchsinformation: Information für Patienten Candeblo 16 mg-tabletten Wirkstoff: Candesartan Cilexetil Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Patienten Candeblo 16 mg-tabletten Wirkstoff: Candesartan Cilexetil Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Fallstricke in der HIV-Diagnostik. Elisabeth Puchhammer-Stöckl Department für Virologie Medizinische Universität Wien
 Fallstricke in der HIV-Diagnostik Elisabeth Puchhammer-Stöckl Department für Virologie Medizinische Universität Wien HIV-Infektion: Diagnostik- Zeitverlauf Nach Pilcher et al, 2004 HIV-Infektion: Diagnostik-
Fallstricke in der HIV-Diagnostik Elisabeth Puchhammer-Stöckl Department für Virologie Medizinische Universität Wien HIV-Infektion: Diagnostik- Zeitverlauf Nach Pilcher et al, 2004 HIV-Infektion: Diagnostik-
Intraoperative Strahlentherapie bei Brustkrebs
 Intraoperative Strahlentherapie bei Brustkrebs Uniklinik Köln 1 Kein Grund für Verzweiflung Wenn die Diagnose Brustkrebs festgestellt wird, ist erst einmal die Sorge groß. Beruhigend zu wissen, dass es
Intraoperative Strahlentherapie bei Brustkrebs Uniklinik Köln 1 Kein Grund für Verzweiflung Wenn die Diagnose Brustkrebs festgestellt wird, ist erst einmal die Sorge groß. Beruhigend zu wissen, dass es
Dontisolon D Mundheilpaste
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER 5 mg/g Paste Wirkstoff: Prednisolonacetat (Ph.Eur.) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER 5 mg/g Paste Wirkstoff: Prednisolonacetat (Ph.Eur.) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Gründe für fehlende Vorsorgemaßnahmen gegen Krankheit
 Gründe für fehlende Vorsorgemaßnahmen gegen Krankheit politische Lage verlassen sich auf Familie persönliche, finanzielle Lage meinen, sich Vorsorge leisten zu können meinen, sie seien zu alt nicht mit
Gründe für fehlende Vorsorgemaßnahmen gegen Krankheit politische Lage verlassen sich auf Familie persönliche, finanzielle Lage meinen, sich Vorsorge leisten zu können meinen, sie seien zu alt nicht mit
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Candesartan Zentiva 16 mg Tabletten Wirkstoff: Candesartancilexetil Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender Candesartan Zentiva 16 mg Tabletten Wirkstoff: Candesartancilexetil Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Übersicht Verständnisfragen
 Übersicht Verständnisfragen Herz-Kreislauf-Erkrankungen Chronisch-obstruktive Lungenerkrankung (COPD) Übergewicht und Adipositas Diabetes mellitus Krebserkrankungen HIV und AIDS Rheumatische Erkrankungen
Übersicht Verständnisfragen Herz-Kreislauf-Erkrankungen Chronisch-obstruktive Lungenerkrankung (COPD) Übergewicht und Adipositas Diabetes mellitus Krebserkrankungen HIV und AIDS Rheumatische Erkrankungen
zur Verfügung gestellt von Gebrauchs.info GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 2,5 mg/g Wirkstoff: Prednicarbat GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. Heben
2,5 mg/g Wirkstoff: Prednicarbat GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. Heben
TOP 3: Loperamid (flüssige Darreichungsformen)
 TOP 3: Loperamid (flüssige Darreichungsformen) Antrag auf Ausweitung der Ausnahme von der Verschreibungspflicht auch für flüssige Darreichungsformen 1 Historie und aktuell: Seit 1993 D. h. folgende Darreichungsformen
TOP 3: Loperamid (flüssige Darreichungsformen) Antrag auf Ausweitung der Ausnahme von der Verschreibungspflicht auch für flüssige Darreichungsformen 1 Historie und aktuell: Seit 1993 D. h. folgende Darreichungsformen
Wortlaut der für die Packungsbeilage vorgesehenen Angaben. Gebrauchsinformation: Information für den Anwender
 Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation: Information für den Anwender Olanzapin axcount 20 mg Filmtabletten Filmtabletten Wirkstoff: Olanzapin Zur Anwendung bei Erwachsenen
Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation: Information für den Anwender Olanzapin axcount 20 mg Filmtabletten Filmtabletten Wirkstoff: Olanzapin Zur Anwendung bei Erwachsenen
Einladung. 3. bis 5. Dezember 2015 Berlin. Klinik, Diagnostik und Therapie bei aktuellen Infektionserregern
 17. Klinisch-Mikrobiologisch- Infektiologisches Symposium Klinik, Diagnostik und Therapie bei aktuellen Infektionserregern Claudia Paulussen / 123RF Einladung 3. bis 5. Dezember 2015 Berlin [ 17. KMIS
17. Klinisch-Mikrobiologisch- Infektiologisches Symposium Klinik, Diagnostik und Therapie bei aktuellen Infektionserregern Claudia Paulussen / 123RF Einladung 3. bis 5. Dezember 2015 Berlin [ 17. KMIS
IMPLANON NXT Erläuternde Broschüre für Patientinnen
 Die Markteinführung von IMPLANON NXT wurde von den belgischen Gesundheitsbehörden an bestimmte Bedingungen geknüpft. Der vorgeschriebene Plan zur Risikominimierung in Belgien, der auch das vorliegende
Die Markteinführung von IMPLANON NXT wurde von den belgischen Gesundheitsbehörden an bestimmte Bedingungen geknüpft. Der vorgeschriebene Plan zur Risikominimierung in Belgien, der auch das vorliegende
Kopf dicht? Nase zu? Husten?
 Kopf dicht? Nase zu? Husten? Inhalt 2 Inhalt 2-3 Wunderwerk Atemwege 4-7 Kopf dicht, Nase zu, Husten was im Körper passiert 8-11 Wie hilft GeloMyrtol forte? 12-15 Wirksamkeit klinisch bestätigt 16-17 Wie
Kopf dicht? Nase zu? Husten? Inhalt 2 Inhalt 2-3 Wunderwerk Atemwege 4-7 Kopf dicht, Nase zu, Husten was im Körper passiert 8-11 Wie hilft GeloMyrtol forte? 12-15 Wirksamkeit klinisch bestätigt 16-17 Wie
