Phasen, Komponenten, Freiheitsgrade
|
|
|
- Harry Schuster
- vor 6 Jahren
- Abrufe
Transkript
1 Phasendiagramme
2 Lernziele: Phasen, Komonenten, Freiheitsgrade Die Phasenregel Zweikomonentensysteme: Damfdruckdiagramme, Hebelgesetz Zweikomonentensysteme: Siedediagramme (die Destillation von Mischungen, Azeotroe) Flüssig-Flüssig-Phasendiagramme P. Atkins, J. de Paula, Physikalische Chemie, Wiley-VCH Verlag GmbH& Co, 2013, G. Wedler, H-J. Freund, Lehrbuch der Physikalischen Chemie, Wiley-VCH Verlag GmbH& Co, 2004,
3 Phasen, Komonenten, Freiheitsgrade Kennzeichen : P Anzahl der Phasen / System Beisiel: P = 1 Gas; Gasmischung ; Kristall ; (vollständig mischbare) Flüssigkeiten P = 3 CaCO 3 : (CaCO 3 + CaO) [2 feste Phasen ] + CO 2 [gasförmige Phase] P = 2 Legierung 2 Metalle : Al + Cu Kennzeichen : N B Bestandteil einer Mischung (chemische Sezies : Ion / Molekül) Beisiel: N B = 2 Mischung Ethanol / Wasser N B = 3 NaCl - wässrige Lösung :(H 2 O + Na + + Cl - )
4 Phasen, Komonenten, Freiheitsgrade Komonente Bestandteil des Systems (chemisch unabhängig) Kennzeichen : C Anzahl der Komonenten: minimale Anzahl unabhängiger Sezies N B = C keine chemische Reaktion / keine sonstige Einschränkung (z.b. Ladungsneutralität) Beisiel: C = 1 reines Wasser C = 2 Mischung Ethanol / Wasser: C 2 H 3 OH + H 2 O C = 2 NaCl - wässrige Lösung (Ladungsneutralität) H 2 O + (Na + + Cl - ) N B C C = 3 (O 2 + H 2 + H 2 O) [T 25 C]
5 Phasen, Komonenten, Freiheitsgrade Chemische Reaktion minimale Anzahl der Sezies Beisiel: (1): CaCO 3 (s) CaO (s) + CO 2 (g) P = 3 C = 2 CO 2 ; CaO N B = 3 (2): NH 4 Cl (s) NH 3 (g) + HCl (g) P = 2 (s) ; (g) C = 1 NH 4 Cl N B = 3 C = 2 überschüssig: NH 3 / HCl
6 Phasen, Komonenten, Freiheitsgrade Varianz (F) Anzahl der intensiven Zustandsvariablen unabhängig voneinander änderbar Anzahl der Phasen (Gleichgewicht) = Konstant Beisiel: (1): System : Gas C = 1 ; P = 1 F = 2 ; T (2): System : reine Stoffe (Flüssigkeit + Damf) C = 1 ; P = 2 F = 1 = f(t) T = f()
7 Die Phasenregel Phasenregel (Gibbs) ein allgemeiner Zusammenhang: F = f(c,p) F = C P + 2 Einkomonentensystem: C = 1 (1): P = 1 F = 2 f(t) : Fläche in (P,T) (2): P = 2 F = 1 = f(t) : Linie in (P,T) (3): P = 3 F = 0 = Konstant, T = Konstant : Punkt in (P,T) Beisiel: Wasser
8 Zweikomonentensysteme C = 2 F = 4 P ; T = Konstant F = 3 P = 2 Damfdruckdiagramme Ideale Mischung 2 (flüchtige) Flüssigkeiten: Raoult sches Gesetz x A x B A B * A * B * B * A * B x A
9 Zweikomonentensysteme Gashase Konzentration der flüchtigen Komonente * höher in Damf A Dalton sches Gesetz * B 1 A x A Flüchtigkeit A > Flüchtigkeit B B B g A = A A A * x A B * + A * - B * ( ) x A =1-g B A (Molenbruch A im Damf) = f(molenbruch A in der flüssigen Phase)
10 Zweikomonentensysteme Gashase B nicht flüchtig B * = 0 B = 0 kein Beitrag zur Zusammensetzung des Damfes * B * B * A * A * B A (Damfdruck der Mischung) = f(zusammensetzung der Gashase)
11 Zweikomonentensysteme Interretation (1): Kennzeichen : a Damfdruck: Mischung der Zusammensetzung x A b Zusammensetzung: Gashase + flüssige Phase (Gleichgewicht) P = 2 F = 1 T = Konstant (F man verzichtet auf Freiheitsgrad T) Kennzeichen : z A Zusammensetzung des Gesamtsystems oberhalb Diagonale flüssige Phase z A = x A unterhalb der unteren Kurve Gashase z A = A zwischen den Kurven Gas + Flüssigkeit
12 Interretation (2): Zweikomonentensysteme (a) Zusammensetzung: flüssige Phase P = 1 F = 2 z A = Konstant ; ( sinkt ) (a 1 ) Zusammensetzung: flüssige Phase + (Gashase 0) ( sinkt ) (a 2 ) Zusammensetzung: flüssige Phase + Gashase (Gleichgewicht) Verdamfung: 2 P = 2 F = 1 ( sinkt ) (a 3 ) Zusammensetzung: (flüssige Phase 0)+ Gashase Verdamfung: 3 P = 2 F = 1 ( sinkt ) (a 4 ) Zusammensetzung: Gashase
13 Zweikomonentensysteme Interretation (3): die Region zwischen beiden Kurven z A Konstant vertikale Linie: Isolethe (gleiche Menge) (a) Zusammensetzung: Gashase + flüssige Phase (Gleichgewicht) P = 2 F = 1 ( sinkt ) (b) Zusammensetzung: verschiebt sich Konnode ( beide Phasen koexistieren) ( sinkt ) (c) Flüssigkeit verdamft Kolben: noch weiter heraus sinkt Gashase
14 Das Hebelgesetz Punkt im Zweihasengebiet die Anteile beider Phasen Hebelgesetz die Stoffmenge, (Gleichgewicht): Begründung: n l = n l n = n + n n z A = n z A + n z A Beide Phasen: n z A = n x A + n A n (x A - z A )= n (z A - A )
15 Die Siedediagramme Hilft bei Destillationsrozessen ideale Mischung: A flüchtiger als B a) Die Destillation von Mischungen: Zweihasengebiet F = 1 ( Konstant, T = Konstant) T T 2 : Flüssigkeit sieden (es gibt infinitesimale Menge Damf) Die flüchtigere Komonente (niedriger Siedeunkt) Gashase
16 Die Siedediagramme Hilft bei Destillationsrozessen ideale Mischung: A flüchtiger als B Destillationsaaratur der Damf zur Kondensation gekühlt. Fraktionierte Destillation Kreislauf Siede- und Kondensationsrozess Kondensat: reines A
17 Die Siedediagramme: Azeotroe 1. Azeotro mit Siedeunktmaximum - das Siedediagramm ein Maximum wenn der Damfdruck durch zwischenmolekulare Anziehungskräfte A-B unter den idealen Wert fällt. die flüssige Phase wird stabilisiert Beisiel: Chloroform/Aceton Saletersäure/Wasser Anfangszustand: flüssige Phase mit einer Zusammensetzung (a) Destillationsrozess Zusammensetzung flüssige Phase Zusammensetzung Damf (b) Die Mischung kann durch Destillation nicht weiter aufgetrennt werden.
18 Die Siedediagramme: Azeotroe 2. Azeotro mit Siedeunktminimum - das Siedediagramm ein Minimum (zwischenmolekulare Wechselwirkungen A B sind eher unvorteilhaft) Die Mischung wird destabilisiert relativ zum idealen Verhalten Beisiel: Dioxan/Wasser Ethanol/Wasser Anfangszustand: flüssige Phase mit einer Zusammensetzung (a) Destillationsrozess Zusammensetzung des Damfs in der Kolonne konstant (b).
19 Die Siedediagramme: Nicht mischbare Flüssigkeiten Nicht mischbare Flüssigkeiten im Gleichgewicht eine winzige Menge A liegt in B gelöst vor (und umgekehrt). Beide Flüssigkeiten mit der jeweils anderen Komonente gesättigt. Die Destillation zweier nicht mischbarer Flüssigkeiten (a) gemeinsame Destillation der getrennten Komonenten (b) der Damfdruck der Mischung * * A B T > wenn = atm beginnt die Flüssigkeit zu sieden : die gelössten Stoffe werden ausgetrieben
20 Die Siedediagramme: Nicht mischbare Flüssigkeiten Das Sieden intensive Durchmischung : die Sättigung beider Lösungen bleibt erhalten die gelössten Stoffe ständig ausgetrieben 2 nicht mischbare Flüssigkeiten sieden nicht bei der gleichen T massgeblich für den Beginn des Siedens Die Anwesenheit 2. Komonente Herabsetzung T Siede Beisiel: Oktan/Wasser
21 Flüssig/Flüssig-Phasendiagramme Binäre Mischung begrenzt mischbare Flüssigkeiten = f(t) Beisiel: Hexan/Nitrobenzol (C = 2) (1): P = 2 F = 1 f(t) : bei einer T ist z A (die Zusammensetzung) exakt bestimmt (2): P = 1 F = 2 beide Flüssigkeiten mischen sich vollständig sowohl T und z A (die Zusammensetzung der Mischung) können beliebig gewählt werden!
22 Schliesslich wenn es so viel B gibt die gesamte Menge A löst sich darin 1 Phase Flüssig/Flüssig-Phasendiagramme: Entmischung Anfangzustand B (kleine Menge) gemischt mit Flüssigkeit A (mehr B hinzugefügt) es gibt einen Punkt in A kein weiteres B mehr löst 2 Phasen (Gleichgewicht): a an B gesättigten A a an Sur B, gesättigt an A Hebelgesetz relative Anteile kleine Menge A lösst sich in B (mehr B hinzugefügt) Der Anteil einer der beiden Phasen nimmt auf Kosten der anderen zu.
23 Flüssig/Flüssig-Phasendiagramme: Entmischung Beisiel: Siedediagramm Hexan/Nitrobenzol ( = 0.1 MPa) unter der Kurve z = f(t) A,B mischen sich nur teilweise oberhalb der oberen T ok mischbar A,B: in beliebigem Verhältnis T = 290C 50g (0.59 mol) C 6 H g (0.41 mol) C 6 H 5 NO 3 2 Phase Zusammensetzung: x N = (0.41 mol, 290C) An den Schnittunkten der entsrechenden Konnode : x N = 0.35 / x N = 0.83 «Hebelarme»: l = / l = Hebelgesetz n n l l 7
24 Kritische Temeraturen Obere kritische Temeratur : T ok T > T ok die Komonenten mischen sich in beliebigem Verhältnis vollständig mischbar (P = 1) T < T ok Entmischung der Komonenten (P = 2) Begründung T ok eine intensive thermische Bewegung der Teilchen, die dem Zusammenhalt der Moleküle eines Stoffs interhalb einer Phase entgegenwirkt. Beisiel: Palladium/Wasserstof
25 Kritische Temeraturen Freie Mischungsenthalie reale Lösung M G nrt x A ln x A x B ln > 2 M G ein doeltes Minimum 2 Phasen x B x x Zusammensetzung die Minima: 0 A M G x B sinkt bewegen sich die Minima aufeinander zu > 2 die Minima fallen zusammen
26 Kritische Temeraturen Untere kritische Temeratur: T uk T < T uk die Komonenten mischen sich in beliebigem Verhältnis (P = 1) T > T uk Entmischung der Komonenten (P = 2) niedrige T die Flüssigkeiten besser mischbar einen schwach gebundenen Komlex T > T uk der Komlex zerfällt Beisiel: Triethilamin/Wasser
27 Kritische Temeraturen Zwei kritische Temeraturen: T ok und T uk Beide Flüssigkeiten nach Aufbrechen der Komlexe gewöhnliche artiell mischbare Flüssigkeiten. T > T uk bildet einen Komlex T > T ok wieder homogenisiert (durch thermische Bewegung der Moleküle). Beisiel: Nicotin/Wasser
28 Lernziele: Phasen, Komonenten, Freiheitsgrade Die Phasenregel Zweikomonentensysteme: Damfdruckdiagramme, Hebelgesetz Zweikomonentensysteme: Siedediagramme (die Destillation von Mischungen, Azeotroe) Flüssig-Flüssig-Phasendiagramme P. Atkins, J. de Paula, Physikalische Chemie, Wiley-VCH Verlag GmbH& Co, 2013, G. Wedler, H-J. Freund, Lehrbuch der Physikalischen Chemie, Wiley-VCH Verlag GmbH& Co, 2004,
Phasen, Komponenten, Freiheitsgrade
 Phasendiagramme 1 Lernziele: Ø Phasen, Komponenten, Freiheitsgrade Ø Die Phasenregel Ø Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Ø Zweikomponentensysteme: Siedediagramme (die Destillation
Phasendiagramme 1 Lernziele: Ø Phasen, Komponenten, Freiheitsgrade Ø Die Phasenregel Ø Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Ø Zweikomponentensysteme: Siedediagramme (die Destillation
Lernziele: Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme,
 Phasendiagramme Lernziele: ee Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Zweikomponentensysteme: Siedediagramme (die Distillation von Mischungen,
Phasendiagramme Lernziele: ee Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Zweikomponentensysteme: Siedediagramme (die Distillation von Mischungen,
Destillation und Rektifikation: Vorlesung am : Zusammenfassung des zweiten Teils. Siedediagramm
 Destillation und Rektifikation: Vorlesung am 27.1.211: Zusammenfassung des zweiten eils llgemeine Bemerkung zu den Berechnungen und bleitungen der Formeln: Die Vorgänge werden in der Regel für ideale Zustände
Destillation und Rektifikation: Vorlesung am 27.1.211: Zusammenfassung des zweiten eils llgemeine Bemerkung zu den Berechnungen und bleitungen der Formeln: Die Vorgänge werden in der Regel für ideale Zustände
Kolligative Eigenschaften
 Kolligative Eigenschaften Kolligative (lat. colligare, sammeln) Eigenschaften (in verdünnter Lösung): f(nzahl der eilchen des gelösten Stoffs) f(rt der eilchen des gelösten Stoffs) eispiel: Gefrierpunkt,
Kolligative Eigenschaften Kolligative (lat. colligare, sammeln) Eigenschaften (in verdünnter Lösung): f(nzahl der eilchen des gelösten Stoffs) f(rt der eilchen des gelösten Stoffs) eispiel: Gefrierpunkt,
PC I Thermodynamik und Transportprozesse
 20.06.2006 15:19 1 PC I Thermodynamik und Transportprozesse Kapitel 5 20.06.2006 15:19 2 V. Lösungen und Mischungen Im Winter des Jahres 1729 setzte ich Bier, Wein, Essig und Salzwasser in großen offenen
20.06.2006 15:19 1 PC I Thermodynamik und Transportprozesse Kapitel 5 20.06.2006 15:19 2 V. Lösungen und Mischungen Im Winter des Jahres 1729 setzte ich Bier, Wein, Essig und Salzwasser in großen offenen
Zustandsbeschreibungen
 Aggregatzustände fest Kristall, geordnet Modifikationen Fernordnung flüssig teilgeordnet Fluktuationen Nahordnung gasförmig regellose Bewegung Unabhängigkeit ngigkeit (ideales Gas) Zustandsbeschreibung
Aggregatzustände fest Kristall, geordnet Modifikationen Fernordnung flüssig teilgeordnet Fluktuationen Nahordnung gasförmig regellose Bewegung Unabhängigkeit ngigkeit (ideales Gas) Zustandsbeschreibung
PartiellemolareVolumina. Chloroform/Aceton
 PartiellemlareVlumina Chlrfrm/cetn Ezessgrößen ( ) ( ) E E m m Mi Mi E V n V n V V n V V n ideal V real V V 2 2 1 1 0,2 0 2 2 0,1 0 1 1 ) ( ) ( Δ Δ Δ Δ Δ E E Mi Mi E H n H n ideal H real H H 2 2 1 1 )
PartiellemlareVlumina Chlrfrm/cetn Ezessgrößen ( ) ( ) E E m m Mi Mi E V n V n V V n V V n ideal V real V V 2 2 1 1 0,2 0 2 2 0,1 0 1 1 ) ( ) ( Δ Δ Δ Δ Δ E E Mi Mi E H n H n ideal H real H H 2 2 1 1 )
Musterlösung Klausur Physikalische Chemie I: Thermodynamik (Januar 2009)
 Musterlösung Klausur Physikalische Chemie I: Thermodynamik (Januar 2009) Aufgabe 1: Reaktionsthermodynamik a) möglichst niedrige Temeratur (begünstigt exotherme Reaktionen) möglichst hoher Druck (begünstigt
Musterlösung Klausur Physikalische Chemie I: Thermodynamik (Januar 2009) Aufgabe 1: Reaktionsthermodynamik a) möglichst niedrige Temeratur (begünstigt exotherme Reaktionen) möglichst hoher Druck (begünstigt
212 - Siedepunktserhöhung
 1 - Siedeunktserhöhung 1. Aufgabe Es ist für verschiedene in Wasser lösliche Stoffe die Siedeunktserhöhung ihrer Lösung zu messen und daraus die molare Masse zu bestimmen.. Grundlagen Stichworte: Damfdruck,
1 - Siedeunktserhöhung 1. Aufgabe Es ist für verschiedene in Wasser lösliche Stoffe die Siedeunktserhöhung ihrer Lösung zu messen und daraus die molare Masse zu bestimmen.. Grundlagen Stichworte: Damfdruck,
Modul: Allgemeine Chemie
 Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Phasengleichgewicht (Destillation)
 Phasengleichgewicht (Destillation) Labor für Thermische Verfahrenstechnik bearbeitet von Prof. Dr.-Ing. habil. R. Geike 1. Grundlagen für das Phasengleichgewicht Damf - Flüssigkeit Die unterschiedliche
Phasengleichgewicht (Destillation) Labor für Thermische Verfahrenstechnik bearbeitet von Prof. Dr.-Ing. habil. R. Geike 1. Grundlagen für das Phasengleichgewicht Damf - Flüssigkeit Die unterschiedliche
Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 11
 Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 11 Prof. Dr. Norbert Hampp Jens Träger Sommersemester 2007 02. 07. 2007 Aufgabe 1 a) Die Dampfdrücke nach dem Raoult schen
Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 11 Prof. Dr. Norbert Hampp Jens Träger Sommersemester 2007 02. 07. 2007 Aufgabe 1 a) Die Dampfdrücke nach dem Raoult schen
Berechnen Sie die Wärmemenge in kj, die erforderlich ist, um 750g H 2 O von
 Aufgabe 1: Berechnen Sie die Wärmemenge in kj, die erforderlich ist, um 750g H O von 0 C bis zum Siedepunkt (100 C) zu erwärmen. Die spezifische Wärmekapazität von Wasser c = 4.18 J K - 1 g -1. Lösung
Aufgabe 1: Berechnen Sie die Wärmemenge in kj, die erforderlich ist, um 750g H O von 0 C bis zum Siedepunkt (100 C) zu erwärmen. Die spezifische Wärmekapazität von Wasser c = 4.18 J K - 1 g -1. Lösung
Physikalische Chemie I
 Physikalische Chemie I 2017 Physikalische Chemie I Dozenten: Vorlesung Prof. Dr. Cornelia Palivan (Tel: 0612673839 [email protected]) Prof. Dr. Wolfgang Meier (Tel: 0612673802 [email protected])
Physikalische Chemie I 2017 Physikalische Chemie I Dozenten: Vorlesung Prof. Dr. Cornelia Palivan (Tel: 0612673839 [email protected]) Prof. Dr. Wolfgang Meier (Tel: 0612673802 [email protected])
Institut für Technische Chemie Technische Universität Clausthal. Technisch-chemisches Praktikum TCB. Versuch: Rektifikation
 Institut für Technische Chemie Technische Universität Clausthal Technisch-chemisches Praktikum TCB Versuch: Rektifikation Einleitung In einer Vielzahl von chemischen Produktionsanlagen besteht die Notwendigkeit,
Institut für Technische Chemie Technische Universität Clausthal Technisch-chemisches Praktikum TCB Versuch: Rektifikation Einleitung In einer Vielzahl von chemischen Produktionsanlagen besteht die Notwendigkeit,
Kolligative Eigenschaften
 Prof. Dr. Norbert Hampp 1/8 11. Kolligative Eigenschaften Kolligative Eigenschaften Unter kolligativen Eigenschaften versteht man die Eigenschaften eines Systems die auf der Mischung unterschiedlicher
Prof. Dr. Norbert Hampp 1/8 11. Kolligative Eigenschaften Kolligative Eigenschaften Unter kolligativen Eigenschaften versteht man die Eigenschaften eines Systems die auf der Mischung unterschiedlicher
Versuch 10. Rektifikation und Rektifizierkolonne
 Praktikum Physikalische Chemie Versuch 1 Rektifikation und Rektifizierkolonne Bestimmung der theoretischen Bodenzahl einer Rektifikationskolonne am Beispiel eines binären Gemisches ktualisiertes Versuchsskript,
Praktikum Physikalische Chemie Versuch 1 Rektifikation und Rektifizierkolonne Bestimmung der theoretischen Bodenzahl einer Rektifikationskolonne am Beispiel eines binären Gemisches ktualisiertes Versuchsskript,
Wir wollen unsere folgenden Betrachtung auf die drei Phasen - fest, - flüssig, - gasförmig beschränken.
 8.4 Phasenübergänge und Phasengleichgewichte 8.4.1 Phasenübergang bei reinem Stoff Wir wollen unsere folgenden Betrachtung auf die drei Phasen - fest, - flüssig, - gasförmig beschränken. Die Erfahrung
8.4 Phasenübergänge und Phasengleichgewichte 8.4.1 Phasenübergang bei reinem Stoff Wir wollen unsere folgenden Betrachtung auf die drei Phasen - fest, - flüssig, - gasförmig beschränken. Die Erfahrung
Musterlösung Übung 10
 Musterlösung Übung 10 Aufgabe 1: Phasendiagramme Abbildung 1-1: Skizzen der Phasendiagramme von Wasser links) und Ethanol rechts). Die Steigung der Schmelzkurven sind zur besseren Anschaulichkeit überzogen
Musterlösung Übung 10 Aufgabe 1: Phasendiagramme Abbildung 1-1: Skizzen der Phasendiagramme von Wasser links) und Ethanol rechts). Die Steigung der Schmelzkurven sind zur besseren Anschaulichkeit überzogen
Spezialfälle. BOYLE-MARIOTT`sches Gesetz p V = n R T bei T, n = konstant: p V = const. GAY-LUSSAC`sches Gesetz. bei V, n = konstant: p = const.
 Spezialfälle BOYLE-MARIOTT`sches Gesetz p V = n R T bei T, n = konstant: p V = const. GAY-LUSSAC`sches Gesetz p V = n R T bei V, n = konstant: p = const. T Druck Druck V = const. Volumen T 2 T 1 Temperatur
Spezialfälle BOYLE-MARIOTT`sches Gesetz p V = n R T bei T, n = konstant: p V = const. GAY-LUSSAC`sches Gesetz p V = n R T bei V, n = konstant: p = const. T Druck Druck V = const. Volumen T 2 T 1 Temperatur
DAMPFDRUCK EINER REINEN FLÜSSIGKEIT. 1. Versuchsplatz. 2. Allgemeines zum Versuch
 DAMPFDRUCK EINER REINEN FLÜSSIGKEI 1. ersuchslatz Komonenten: - hermostat - Woulffsche Flasche - Dreihalskolben mit ersuchssubstanz - hermometer - Druckmesser - Druckanzeige 2. Allgemeines zum ersuch Befindet
DAMPFDRUCK EINER REINEN FLÜSSIGKEI 1. ersuchslatz Komonenten: - hermostat - Woulffsche Flasche - Dreihalskolben mit ersuchssubstanz - hermometer - Druckmesser - Druckanzeige 2. Allgemeines zum ersuch Befindet
11. Der Phasenübergang
 11. Der Phasenübergang - Phasendiagramme, Kritischer Punkt und ripelpunkt - Gibbssche Phasenregel - Phasenübergänge 1. und 2. Ordnung - Das Phasengleichgewicht - Clausius-Clapeyron-Gleichung - Pictet-routon-Regel,
11. Der Phasenübergang - Phasendiagramme, Kritischer Punkt und ripelpunkt - Gibbssche Phasenregel - Phasenübergänge 1. und 2. Ordnung - Das Phasengleichgewicht - Clausius-Clapeyron-Gleichung - Pictet-routon-Regel,
Verflüssigung von Gasen / Joule-Thomson-Effekt
 Sieden und Kondensation: T p T p S S 0 1 RTSp0 1 ln p p0 Dampfdrucktopf, Autoklave zur Sterilisation absolute Luftfeuchtigkeit relative Luftfeuchtigkeit a ( g/m 3 ) a pw rel S ps rel 1 Taupunkt erflüssigung
Sieden und Kondensation: T p T p S S 0 1 RTSp0 1 ln p p0 Dampfdrucktopf, Autoklave zur Sterilisation absolute Luftfeuchtigkeit relative Luftfeuchtigkeit a ( g/m 3 ) a pw rel S ps rel 1 Taupunkt erflüssigung
Grundlagen der Allgemeinen und Anorganischen Chemie. Atome
 Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 361 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 361 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
- Chemisches Potential der idealen Gasphase: Phasengleichgewichte nichtidealer Gemische
 Inhalt von Abschnitt 3.3 3.3-0 3.3 Phasenübergänge und Phasengleichgewichte 3.3.1 Phasenübergang bei reinem Stoff 3.3.2 Phasengleichgewichte reiner Stoffe 3.3.3 Phasengleichgewichte von Stoffgemischen
Inhalt von Abschnitt 3.3 3.3-0 3.3 Phasenübergänge und Phasengleichgewichte 3.3.1 Phasenübergang bei reinem Stoff 3.3.2 Phasengleichgewichte reiner Stoffe 3.3.3 Phasengleichgewichte von Stoffgemischen
8.4.3 Phasengleichgewichte von Stoffgemischen
 8.4.3 Phasengleichgewichte von Stoffgemischen In einer reinen Flüssigkeit überwinden einige der höher energetischen Moleküle die molekularen Anziehungskräfte und entweichen in die Gasphase. Je kleiner
8.4.3 Phasengleichgewichte von Stoffgemischen In einer reinen Flüssigkeit überwinden einige der höher energetischen Moleküle die molekularen Anziehungskräfte und entweichen in die Gasphase. Je kleiner
Physikalische Chemie 0 Klausur, 22. Oktober 2011
 Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Protokoll zum Versuch 4.2
 Grundpraktikum Physikalische Chemie Studiengang: Chemie-Ingenieurwesen Technische Universität München SS 2003 Protokoll zum Versuch 4.2 Entmischungsgleichgewicht Gruppe 3 Kim Langbein Oliver Gobin 07 April
Grundpraktikum Physikalische Chemie Studiengang: Chemie-Ingenieurwesen Technische Universität München SS 2003 Protokoll zum Versuch 4.2 Entmischungsgleichgewicht Gruppe 3 Kim Langbein Oliver Gobin 07 April
Die Eigenschaften einfacher Mischungen
 Die Eigenschaften einfacher Mischungen Lernziele: ee Thermodynamische eschreibung von Mischungen Partielle molare Grössen, TD von MIschhasen Chemische Potenzial flüssiger Phasen Eigeschaften von Lösungen,
Die Eigenschaften einfacher Mischungen Lernziele: ee Thermodynamische eschreibung von Mischungen Partielle molare Grössen, TD von MIschhasen Chemische Potenzial flüssiger Phasen Eigeschaften von Lösungen,
Lösungen, Stoffmengen und Konzentrationen
 12 Lösungen, Stoffmengen und Konzentrationen Lösungen sind homogene Mischungen reiner Stoffe, aber umgekehrt sind nicht alle homogenen Mischungen echte Lösungen. Echte Lösungen weisen nur zum Teil die
12 Lösungen, Stoffmengen und Konzentrationen Lösungen sind homogene Mischungen reiner Stoffe, aber umgekehrt sind nicht alle homogenen Mischungen echte Lösungen. Echte Lösungen weisen nur zum Teil die
A 2.6 Wie ist die Zusammensetzung der Flüssigkeit und des Dampfes eines Stickstoff-Sauerstoff-Gemischs
 A 2.1 Bei - 10 o C beträgt der Dampfdruck des Kohlendioxids 26,47 bar, die Dichte der Flüssigkeit 980,8 kg/m 3 und die Dichte des Dampfes 70,5 kg/m 3. Bei - 7,5 o C beträgt der Dampfdruck 28,44 bar. Man
A 2.1 Bei - 10 o C beträgt der Dampfdruck des Kohlendioxids 26,47 bar, die Dichte der Flüssigkeit 980,8 kg/m 3 und die Dichte des Dampfes 70,5 kg/m 3. Bei - 7,5 o C beträgt der Dampfdruck 28,44 bar. Man
Physikalische Umwandlungen reiner Stoffe
 Physikalische Umwandlungen reiner Stoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagrame Phasenübergänge, die D Gleichgewichtkriterium Die Abhängigkeit der
Physikalische Umwandlungen reiner Stoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagrame Phasenübergänge, die D Gleichgewichtkriterium Die Abhängigkeit der
Der Zweite Hauptsatz der TD- Lernziele
 Der Zweite Hautsatz der D- Lernziele o Einleitung o Entroie (Definition, Entroie als Zustandsfunktion, die Clausius sche Ungleichung) o Der Zweite Hautzatz der D o Die Entroieänderungen bei seziellen Prozessen
Der Zweite Hautsatz der D- Lernziele o Einleitung o Entroie (Definition, Entroie als Zustandsfunktion, die Clausius sche Ungleichung) o Der Zweite Hautzatz der D o Die Entroieänderungen bei seziellen Prozessen
14 Destillation Grundlagen Destillation
 72 4 Destillation 4 Destillation 4. Grundlagen Mit dem wichtigen rennverfahren der Destillation (die entscheidende Modifikation der Destillation stellt dabei die Rektifikation dar) lässt sich aus einem
72 4 Destillation 4 Destillation 4. Grundlagen Mit dem wichtigen rennverfahren der Destillation (die entscheidende Modifikation der Destillation stellt dabei die Rektifikation dar) lässt sich aus einem
Zentralprüfung SwissChO 2016
 PROBLEM 1 - VERSCHIEDENE FRAGEN 9.5 PUNKTE a 6 N A = 3.61 10 4 mol 1 Punkt b Aufgrund der Verdünnung hat man 0.05M Br Ionen, 0.05M I Ionen und 0.1M Br + Ionen. 1/ Punkt wenn Br und I richtig, 1/ Punkt
PROBLEM 1 - VERSCHIEDENE FRAGEN 9.5 PUNKTE a 6 N A = 3.61 10 4 mol 1 Punkt b Aufgrund der Verdünnung hat man 0.05M Br Ionen, 0.05M I Ionen und 0.1M Br + Ionen. 1/ Punkt wenn Br und I richtig, 1/ Punkt
Inhalt der Vorlesung. 1. Eigenschaften der Gase. 0. Einführung
 Inhalt der Vorlesung 0. Einführung 0.1 Themen der Physikal. Chemie 0.2 Grundbegriffe/ Zentrale Größe: Energie 0.3 Molekulare Deutung der inneren Energie U Molekülstruktur, Energieniveaus und elektromagn.
Inhalt der Vorlesung 0. Einführung 0.1 Themen der Physikal. Chemie 0.2 Grundbegriffe/ Zentrale Größe: Energie 0.3 Molekulare Deutung der inneren Energie U Molekülstruktur, Energieniveaus und elektromagn.
Name: Punktzahl: von 57 Note:
 Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
Multiple-Choice Test. Alle Fragen können mit Hilfe der Versuchsanleitung richtig gelöst werden.
 PCG-Grundpraktikum Versuch 1- Dampfdruckdiagramm Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Dampfdruckdiagramm wird dieses Vorgespräch durch einen Multiple-Choice
PCG-Grundpraktikum Versuch 1- Dampfdruckdiagramm Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Dampfdruckdiagramm wird dieses Vorgespräch durch einen Multiple-Choice
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum Übungsblatt 4 zur Vorlesung Physikalische Chemie II WS 2008/09 Prof. E. Bartsch 4.1 Der Siedepunkt einer flüssigen Mischung
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum Übungsblatt 4 zur Vorlesung Physikalische Chemie II WS 2008/09 Prof. E. Bartsch 4.1 Der Siedepunkt einer flüssigen Mischung
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I Dr. Helge Klemmer
 Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
! #!! % & ( )! ! +, +,# # !.. +, ) + + /) # %
 ! #! #!! % & ( )!! +, +,# #!.. +, ) + + /)!!.0. #+,)!## 2 +, ) + + 3 4 # )!#!! ), 5 # 6! # &!). ) # )!#! #, () # # ) #!# #. # ) 6 # ) )0 4 )) #, 7) 6!!. )0 +,!# +, 4 / 4, )!#!! ))# 0.(! & ( )!! 8 # ) #+,
! #! #!! % & ( )!! +, +,# #!.. +, ) + + /)!!.0. #+,)!## 2 +, ) + + 3 4 # )!#!! ), 5 # 6! # &!). ) # )!#! #, () # # ) #!# #. # ) 6 # ) )0 4 )) #, 7) 6!!. )0 +,!# +, 4 / 4, )!#!! ))# 0.(! & ( )!! 8 # ) #+,
Schmelzdiagramm eines binären Stoffgemisches
 Praktikum Physikalische Chemie I 30. Oktober 2015 Schmelzdiagramm eines binären Stoffgemisches Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1. Theorie hinter dem Versuch Ein Schmelzdiagramm zeigt
Praktikum Physikalische Chemie I 30. Oktober 2015 Schmelzdiagramm eines binären Stoffgemisches Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1. Theorie hinter dem Versuch Ein Schmelzdiagramm zeigt
 Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Chemisches Praktikum für TUM-BWL Praxisseminar II Grundoperationen und Reinigungstechniken
 Chemisches Praktikum für TUM-BWL Praxisseminar II Grundoperationen und Reinigungstechniken Inhalt: Wiederholung Azeotrop-Destillation Extraktion Kontinuierliche Feststoffextraktion Dr. Andreas Bauer, Dr.
Chemisches Praktikum für TUM-BWL Praxisseminar II Grundoperationen und Reinigungstechniken Inhalt: Wiederholung Azeotrop-Destillation Extraktion Kontinuierliche Feststoffextraktion Dr. Andreas Bauer, Dr.
Repetitorium Physikalische Chemie für Lehramt
 Repetitorium Physikalische Chemie für Lehramt Anfangstext bei der Prüfung. Hier nicht relevant. Zu jeder der 10 Fragen werden maximal 12,5 Punkte vergeben. Höchstens 100 Punkte können erreicht werden,
Repetitorium Physikalische Chemie für Lehramt Anfangstext bei der Prüfung. Hier nicht relevant. Zu jeder der 10 Fragen werden maximal 12,5 Punkte vergeben. Höchstens 100 Punkte können erreicht werden,
Hauptsätze der Thermodynamik
 Platzhalter für Bild, Bild auf Titelfolie hinter das Logo einsetzen Hauptsätze der Thermodynamik Dominik Pfennig, 31.10.2012 Inhalt 0. Hauptsatz Innere Energie 1. Hauptsatz Enthalpie Satz von Hess 2. Hauptsatz
Platzhalter für Bild, Bild auf Titelfolie hinter das Logo einsetzen Hauptsätze der Thermodynamik Dominik Pfennig, 31.10.2012 Inhalt 0. Hauptsatz Innere Energie 1. Hauptsatz Enthalpie Satz von Hess 2. Hauptsatz
Themen heute: Reaktionsgleichungen, chemische Gleichgewichte
 Wiederholung der letzten Vorlesungsstunde: Ionenbindung, Coulomb-Gesetz, Ionen- (Kristall-)strukturen, NaCl, CsCl, ZnS, Elementarzelle, 7 Kristallsysteme Themen heute: Reaktionsgleichungen, chemische Gleichgewichte
Wiederholung der letzten Vorlesungsstunde: Ionenbindung, Coulomb-Gesetz, Ionen- (Kristall-)strukturen, NaCl, CsCl, ZnS, Elementarzelle, 7 Kristallsysteme Themen heute: Reaktionsgleichungen, chemische Gleichgewichte
Planung, Bau und Betrieb von Chemieanlagen - Übung Allgemeine Chemie. Allgemeine Chemie. Rückblick auf vorherige Übung
 Planung, Bau und Betrieb von Chemieanlagen - Übung Allgemeine Chemie 1 Allgemeine Chemie Rückblick auf vorherige Übung 2 Löslichkeit Was ist eine Lösung? - Eine Lösung ist ein einphasiges (homogenes) Gemisch
Planung, Bau und Betrieb von Chemieanlagen - Übung Allgemeine Chemie 1 Allgemeine Chemie Rückblick auf vorherige Übung 2 Löslichkeit Was ist eine Lösung? - Eine Lösung ist ein einphasiges (homogenes) Gemisch
1 I. Thermodynamik. 1.1 Ideales Gasgesetz. 1.2 Vereinfachte kinetische Gastheorie. 1.3 Erster Hauptsatz der Thermodynamik.
 1 I. hermodynamik 1.1 Ideales Gasgesetz eilchenzahl N Stoffmenge: n [mol], N A = 6.022 10 23 mol 1 ; N = nn A molare Größen: X m = X/n ideales Gasgesetz: V = nr, R = 8.314JK 1 mol 1 Zustandsgrößen:, V,,
1 I. hermodynamik 1.1 Ideales Gasgesetz eilchenzahl N Stoffmenge: n [mol], N A = 6.022 10 23 mol 1 ; N = nn A molare Größen: X m = X/n ideales Gasgesetz: V = nr, R = 8.314JK 1 mol 1 Zustandsgrößen:, V,,
Die 4 Phasen des Carnot-Prozesses
 Die 4 Phasen des Carnot-Prozesses isotherme Expansion: A B V V T k N Q ln 1 1 isotherme Kompression: adiabatische Kompression: adiabatische Expansion: 0 Q Q 0 C D V V T k N Q ln 2 2 S Q 1 1 /T1 T 1 T 2
Die 4 Phasen des Carnot-Prozesses isotherme Expansion: A B V V T k N Q ln 1 1 isotherme Kompression: adiabatische Kompression: adiabatische Expansion: 0 Q Q 0 C D V V T k N Q ln 2 2 S Q 1 1 /T1 T 1 T 2
Gefrierpunktserniedrigung
 Gefrierpunktserniedrigung Zur Darstellung der möglichen Phasen einer Substanz wird deren Verhalten bei verschiedenen Drücken und Temperaturen gemessen und in ein Druck-Temperatur- Diagramm eingetragen.
Gefrierpunktserniedrigung Zur Darstellung der möglichen Phasen einer Substanz wird deren Verhalten bei verschiedenen Drücken und Temperaturen gemessen und in ein Druck-Temperatur- Diagramm eingetragen.
Lernzielkontrolle Sekunda
 Lernzielkontrolle Sekunda Hilfsmittel: PSE, Taschenrechner 1 Stoffklassen / Bindungslehre / Zwischenmolekulare Kräfte (15) Richtzeit: 25 Minuten 1.1 Elektrische Leitfähigkeit verschiedener Stoffe (3) Manche
Lernzielkontrolle Sekunda Hilfsmittel: PSE, Taschenrechner 1 Stoffklassen / Bindungslehre / Zwischenmolekulare Kräfte (15) Richtzeit: 25 Minuten 1.1 Elektrische Leitfähigkeit verschiedener Stoffe (3) Manche
-Reaktionsordnung- Referat zur Vorlesung Reaktionsdynamik. 31. Oktober 2012 Nils Wilharm Reaktionsordnung Seite 1
 -Reaktionsordnung- Referat zur Vorlesung Reaktionsdynamik 31. Oktober 2012 Nils Wilharm Reaktionsordnung Seite 1 Reaktionsordnung Allgemeines Reaktionsgeschwindigkeit/-ordnung 0. Ordnung 1. Ordnung 2.
-Reaktionsordnung- Referat zur Vorlesung Reaktionsdynamik 31. Oktober 2012 Nils Wilharm Reaktionsordnung Seite 1 Reaktionsordnung Allgemeines Reaktionsgeschwindigkeit/-ordnung 0. Ordnung 1. Ordnung 2.
Mischungslücke in der flüssigen Phase
 Übungen in physikalischer Chemie für B. Sc.-Studierende Versuch Nr.: S05 Version 2018 (260218) Kurzbezeichnung: Mischungslücke Mischungslücke in der flüssigen Phase Aufgabenstellung Die Entmischungskurven
Übungen in physikalischer Chemie für B. Sc.-Studierende Versuch Nr.: S05 Version 2018 (260218) Kurzbezeichnung: Mischungslücke Mischungslücke in der flüssigen Phase Aufgabenstellung Die Entmischungskurven
Der Zweite Hauptsatz der TD- Lernziele
 Der Zweite Hautsatz der D- Lernziele o Einleitung o Entroie (Definition, Entroie als Zustandsfunktion, die Clausius sche Ungleichung) o Der Zweite Hautzatz der D o Die Entroieänderungen bei seziellen Prozessen
Der Zweite Hautsatz der D- Lernziele o Einleitung o Entroie (Definition, Entroie als Zustandsfunktion, die Clausius sche Ungleichung) o Der Zweite Hautzatz der D o Die Entroieänderungen bei seziellen Prozessen
4. Freie Energie/Enthalpie & Gibbs Gleichungen
 4. Freie Energie/Enthalpie & Gibbs Gleichungen 1. Eigenschaften der Materie in der Gasphase 2. Erster Hauptsatz: Arbeit und Wärme 3. Entropie und Zweiter Hauptsatz der hermodynamik 4. Freie Enthalpie G,
4. Freie Energie/Enthalpie & Gibbs Gleichungen 1. Eigenschaften der Materie in der Gasphase 2. Erster Hauptsatz: Arbeit und Wärme 3. Entropie und Zweiter Hauptsatz der hermodynamik 4. Freie Enthalpie G,
Physikalisch-chemische Grundlagen der thermischen Verfahrenstechnik
 Lüdecke Lüdecke Thermodynamik Physikalisch-chemische Grundlagen der thermischen Verfahrenstechnik Grundlagen der Thermodynamik Grundbegriffe Nullter und erster Hauptsatz der Thermodynamik Das ideale Gas
Lüdecke Lüdecke Thermodynamik Physikalisch-chemische Grundlagen der thermischen Verfahrenstechnik Grundlagen der Thermodynamik Grundbegriffe Nullter und erster Hauptsatz der Thermodynamik Das ideale Gas
Taschenbuch der Verfahrenstechnik Herausgegeben von Karl Schwister
 aschenbuch der Verfahrenstechnik Herausgegeben von Karl Schwister ISBN-: 3-446-458-9 ISBN-3: 978-3-446-458-9 Leseprobe Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-458-9
aschenbuch der Verfahrenstechnik Herausgegeben von Karl Schwister ISBN-: 3-446-458-9 ISBN-3: 978-3-446-458-9 Leseprobe Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-458-9
Bestimmung des Phasendiagramms eines binären Systems mit Mischungslücke
 Bestimmung des Phasendiagramms eines binären Systems mit Mischungslücke Themenbereiche Gibbssches Phasengesetz, Phasendiagramme, Mischbarkeit im flüssigen und festen Zustand, thermodynamische Stabilitätsbedingungen.
Bestimmung des Phasendiagramms eines binären Systems mit Mischungslücke Themenbereiche Gibbssches Phasengesetz, Phasendiagramme, Mischbarkeit im flüssigen und festen Zustand, thermodynamische Stabilitätsbedingungen.
5.6 Zusammenfassung / Merkpunkte zu Kapitel 5: Thermodynamisches Gleichgewicht
 5.6 Zusammenfassung / Merkpunkte zu Kapitel 5: Thermodynamisches Gleichgewicht Ein Teilchen, oder auch ein ganzes System von Teilchen, befindet sich im Gleichgewicht, falls sich "nichts" mehr ändert. Bei
5.6 Zusammenfassung / Merkpunkte zu Kapitel 5: Thermodynamisches Gleichgewicht Ein Teilchen, oder auch ein ganzes System von Teilchen, befindet sich im Gleichgewicht, falls sich "nichts" mehr ändert. Bei
Phasengleichgewichte (VLE)
 Phasengleichgewichte (VLE) Gibbs sche Phasenregel Clausius-Claeyron-Gleichung Antoine-Gleichung Nichtideales Phasenverhalten Van der Waals-Gleichung Phasenverhalten von Gemischen (VLE) Raoult sches Gesetz
Phasengleichgewichte (VLE) Gibbs sche Phasenregel Clausius-Claeyron-Gleichung Antoine-Gleichung Nichtideales Phasenverhalten Van der Waals-Gleichung Phasenverhalten von Gemischen (VLE) Raoult sches Gesetz
NH 3. CCl 4 CO 2. Lösungen zur Lernzielkontrolle Sekunda. Hilfsmittel: PSE, Taschenrechner
 Lösungen zur Lernzielkontrolle Sekunda Hilfsmittel: PSE, Taschenrechner 1 Stoffklassen / Bindungslehre / Zwischenmolekulare Kräfte (1) 1.1 Elektrische Leitfähigkeit verschiedener Stoffe (3) leitfähig,
Lösungen zur Lernzielkontrolle Sekunda Hilfsmittel: PSE, Taschenrechner 1 Stoffklassen / Bindungslehre / Zwischenmolekulare Kräfte (1) 1.1 Elektrische Leitfähigkeit verschiedener Stoffe (3) leitfähig,
Amphiphile Moleküle vereinen zwei inkompatible Molekülteile mit unterschiedlicher Löslichkeit (meist: hydrophil + hydrophob)
 3. Amhihile 3.1. Allgemeines Amhihile Moleküle vereinen zwei inkomatible Molekülteile mit unterschiedlicher Löslichkeit (meist: hydrohil + hydrohob) Tenside, Detergentien, surfactant, Liide, Blockcoolymere,...
3. Amhihile 3.1. Allgemeines Amhihile Moleküle vereinen zwei inkomatible Molekülteile mit unterschiedlicher Löslichkeit (meist: hydrohil + hydrohob) Tenside, Detergentien, surfactant, Liide, Blockcoolymere,...
Inhalt 1 Grundlagen der Thermodynamik
 Inhalt 1 Grundlagen der Thermodynamik..................... 1 1.1 Grundbegriffe.............................. 2 1.1.1 Das System........................... 2 1.1.2 Zustandsgrößen........................
Inhalt 1 Grundlagen der Thermodynamik..................... 1 1.1 Grundbegriffe.............................. 2 1.1.1 Das System........................... 2 1.1.2 Zustandsgrößen........................
Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol
![Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol](/thumbs/50/26795947.jpg) 2. Zustandsgrößen 2.1 Die thermischen Zustandsgrößen 2.1.1. Masse und Molzahl Reine Stoffe: Ein Mol eines reinen Stoffes enthält N A = 6,02214. 10 23 Atome oder Moleküle, N A heißt Avogadro-Zahl. Molzahl:
2. Zustandsgrößen 2.1 Die thermischen Zustandsgrößen 2.1.1. Masse und Molzahl Reine Stoffe: Ein Mol eines reinen Stoffes enthält N A = 6,02214. 10 23 Atome oder Moleküle, N A heißt Avogadro-Zahl. Molzahl:
Mischphasenthermodynamik Prüfung
 Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Mischphasenthermodynamik Prüfung 06. 03. 2017 Teil 1 : Fragenteil Gesamte Bearbeitungszeit
Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Mischphasenthermodynamik Prüfung 06. 03. 2017 Teil 1 : Fragenteil Gesamte Bearbeitungszeit
EDUKTE PRODUKTE. Bei einer chemischen Reaktion wandeln sich Stoffe in neue Stoffe mit anderen Eigenschaften um. Symbolische Schreibweise: Reagiert zu
 L2 1 Chemische Reaktion, Energetik Bei einer chemischen Reaktion wandeln sich Stoffe in neue Stoffe mit anderen Eigenschaften um. Symbolische Schreibweise: Ausgangsstoff e EDUKTE Reagiert zu Endstoffe
L2 1 Chemische Reaktion, Energetik Bei einer chemischen Reaktion wandeln sich Stoffe in neue Stoffe mit anderen Eigenschaften um. Symbolische Schreibweise: Ausgangsstoff e EDUKTE Reagiert zu Endstoffe
Grundlagen der Chemie Lösungen Prof. Annie Powell
 Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Azeotrope. Viele binäre flüssige Mischungen zeigen das vorhin diskutierte Siedediagramm, doch
 Azeotrope B A Viele binäre flüssige Mischungen zeigen das vorhin diskutierte Siedediagramm, doch zahl- reiche wichtige Systeme weichen davon ab. Ein solches Verhalten kann auftreten, a wenn die Wechselwirkungen
Azeotrope B A Viele binäre flüssige Mischungen zeigen das vorhin diskutierte Siedediagramm, doch zahl- reiche wichtige Systeme weichen davon ab. Ein solches Verhalten kann auftreten, a wenn die Wechselwirkungen
PhysikalischeUmwandlungen
 PhysikalischeUmwandlungen reinerstoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagramme Phasenübergänge, die D Gleichgewichtkriterien Die Abhängigkeit der Stabilität
PhysikalischeUmwandlungen reinerstoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagramme Phasenübergänge, die D Gleichgewichtkriterien Die Abhängigkeit der Stabilität
Chemie aquatischer Systeme. Herbstsemester 2013
 Chemie aquatischer Systeme Herbstsemester 2013 Ziele der Vorlesung Verständnis der chemischen Zusammensetzung der Gewässer aufgrund chemischer Prozesse Verknüpfung chemischer Prozesse mit biologischen
Chemie aquatischer Systeme Herbstsemester 2013 Ziele der Vorlesung Verständnis der chemischen Zusammensetzung der Gewässer aufgrund chemischer Prozesse Verknüpfung chemischer Prozesse mit biologischen
Lehrbuch Chemische Technologie
 C. Herbert Vogel Lehrbuch Chemische Technologie Grundlagen Verfahrenstechnischer Anlagen WILEY- VCH WILEY-VCH Verlag GmbH & Co. KGaA IX Inhaltsverzeichnis 1 Einführung 1 1.1 Das Ziel industrieller Forschung
C. Herbert Vogel Lehrbuch Chemische Technologie Grundlagen Verfahrenstechnischer Anlagen WILEY- VCH WILEY-VCH Verlag GmbH & Co. KGaA IX Inhaltsverzeichnis 1 Einführung 1 1.1 Das Ziel industrieller Forschung
Endersch, Jonas 09./
 Endersch, Jonas 09./10.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.2: Destillation 1 Versuch 1.3: Destillation 2 Einleitung und Theorie: In diesen Versuchen
Endersch, Jonas 09./10.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.2: Destillation 1 Versuch 1.3: Destillation 2 Einleitung und Theorie: In diesen Versuchen
Vorlesung Anorganische Chemie
 Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 5 Verhalten von Lösungen Konzentrationen Solvatation und Solvatationsenthalpie Kolligative Eigenschaften Kryoskopie/Ebullioskopie
Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 5 Verhalten von Lösungen Konzentrationen Solvatation und Solvatationsenthalpie Kolligative Eigenschaften Kryoskopie/Ebullioskopie
1. Wärmelehre 1.1. Temperatur. Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités)
 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
LMPG1 ÜB3-Lösungen Grundlagen der Destillation Seite 1 von 12
 LMPG1 ÜB3-Lösungen Grundlagen der Destillation Seite 1 von 12 LMPG1 ÜB3-Lösungen Grundlagen der Destillation Seite 2 von 12 a. Nennen Sie eine Bedingung, damit eine Gleichstromdestillation zum Einsatz
LMPG1 ÜB3-Lösungen Grundlagen der Destillation Seite 1 von 12 LMPG1 ÜB3-Lösungen Grundlagen der Destillation Seite 2 von 12 a. Nennen Sie eine Bedingung, damit eine Gleichstromdestillation zum Einsatz
Siedediagramm binärer Gemische und Rektifikation
 Versuch Nr. 14: Siedediagramm binärer Gemische und Rektifikation 1. Ziel des Versuchs Ziel des Versuches, ist es die Siedekurve eines Methanol-Wasser-Gemisches aufzunehmen. Im zweiten Versuchsteil soll
Versuch Nr. 14: Siedediagramm binärer Gemische und Rektifikation 1. Ziel des Versuchs Ziel des Versuches, ist es die Siedekurve eines Methanol-Wasser-Gemisches aufzunehmen. Im zweiten Versuchsteil soll
LMPG1 ÜB Grundlagen der Destillation Lösungen Seite 1 von 12
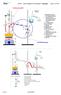 LMPG1 ÜB Grundlagen der Destillation Lösungen Seite 1 von 12 LMPG1 ÜB Grundlagen der Destillation Lösungen Seite 2 von 12 a. Nennen Sie eine Bedingung, damit eine Gleichstromdestillation zum Einsatz kommt.
LMPG1 ÜB Grundlagen der Destillation Lösungen Seite 1 von 12 LMPG1 ÜB Grundlagen der Destillation Lösungen Seite 2 von 12 a. Nennen Sie eine Bedingung, damit eine Gleichstromdestillation zum Einsatz kommt.
TU Ilmenau Chemisches Praktikum Versuche Binäres Phasendiagramm. Siedediagramm
 TU Ilmenau Chemisches Praktikum Versuche Binäres Phasendiagramm V3 Fachgebiet Chemie Siedediagramm 1. Aufgabenstellung A. Ermitteln Sie das Siedediagramm des binären Systems der Substanzen "A und B (diese
TU Ilmenau Chemisches Praktikum Versuche Binäres Phasendiagramm V3 Fachgebiet Chemie Siedediagramm 1. Aufgabenstellung A. Ermitteln Sie das Siedediagramm des binären Systems der Substanzen "A und B (diese
STÖCHIOMETRIE. die Lehre von der mengenmäßigen Zusammensetzung chemischer Verbindungen und den Mengenverhältnissen bei chemischen Reaktionen
 1 STÖCHIOMETRIE die Lehre von der mengenmäßigen Zusammensetzung chemischer Verbindungen und den Mengenverhältnissen bei chemischen Reaktionen 1) STOFFMENGE n(x) reine Zählgröße Menge der Elementarteilchen
1 STÖCHIOMETRIE die Lehre von der mengenmäßigen Zusammensetzung chemischer Verbindungen und den Mengenverhältnissen bei chemischen Reaktionen 1) STOFFMENGE n(x) reine Zählgröße Menge der Elementarteilchen
