Musterlösung Klausur Physikalische Chemie I: Thermodynamik (Januar 2009)
|
|
|
- Wilhelmine Ackermann
- vor 5 Jahren
- Abrufe
Transkript
1 Musterlösung Klausur Physikalische Chemie I: Thermodynamik (Januar 2009) Aufgabe 1: Reaktionsthermodynamik a) möglichst niedrige Temeratur (begünstigt exotherme Reaktionen) möglichst hoher Druck (begünstigt Reaktionen, bei denen sich die Zahl der gasförmigen Teilchen verringert) b) c) d) n SO3 = 2.3 mol = ξ (1.1) n SO2 = 3 ξ (1.2) n O2 = ξ (1.3) n ges = ξ (1.4) K x = n n x ν i i = n ν i i n ν n SO3 ges = i=1 i=1 n SO2 n 1/2 O 2 n 1/2 ges = (1.5) ( ) ν 1 K = K x = K x 15 = (1.6) r G = RT ln K = kj/mol (1.7) r G = r H T r S (1.8) r S = rh r G T = J K 1 mol 1 (1.9) Die Entroie nimmt im Laufe der Reaktion ab, da die Zahl der Teilchen abnimmt. e) Es wird die integrierte Form der Clausius-Claeyron-Gleichung für ideale Gase verwendet (mit der Näherung va = gas ). Für 1 und T 1 werden Standarddruck (1 bar) und Siedetemeratur verwendet. ( ) 2 ln = ( ) vah 1 (1.10) 1 T 2 = [ ln R ( T 2 T 1 ) R va H + 1 T 1 ] 1 = K (1.11) 1
2 Aufgabe 2: Mischungslücken a) Die allgemeine Formel für die Mischungsentroie einer idealen Mischung lautet: n mix S = R n ges x i ln x i (2.1) Für das gegebene System betragen die Molenbrüche x P henol = 0.2 und x W asser = 0.8. Die Gesamtstoffmenge beträgt 5 mol. i=1 mix S = R 5 mol (0.2 ln ln 0.8) = J K 1 mol 1 (2.2) b) Die Wärmekaazität des Systems, C, setzt sich aus den Wärmekaazitäten der Komonenten zusammen. C = 1 mol c P henol + 4 mol c W asser = JK 1 (2.3) Die aufzubringende Mischungsenthalie wird dem System in Form von Wärme entzogen. Bei bekannter Wärmekaazität kann diese Wärme mit der Temeraturänderung in Beziehung gesetzt werden. mix H = Q (2.4) Q = C T (2.5) mix H = T C = ( 13.4 K) JK 1 = kj (2.6) c) Aussagen über die Sontanität von Prozessen werden mit Hilfe der freien Enthalie mix G getroffen. Eine sontane Entmischung entsricht einer ositiven freien Mischungsenthalie. Die dafür benötigte Mischungsentroie mix S ist aus (2a) bekannt und die Mischungsenthalie mix H aus (2b). Es wird angenommen, dass diese Grössen für den betrachteten Temeraturbereich konstant sind. mix G = mix H T mix S (2.7) mix G 0 (2.8) T mixh mix S = K = 63.2 C (2.9) Diesen Wert liest man in etwa auch aus Abb. 1 ab. d) Bei 60 C mischen sich die beiden Flüssigkeiten nicht mehr vollständig. Dementsrechend ist die Mischungsenthalie geringer. e) Aus dem Phasendiagramm kann abgelesen werden, dass bei 60 C für einen Molenbruch x P henol kleiner 0.05 oder grösser 0.25 gerade eine vollständige Mischung erfolgt. Die Stoffmenge an Phenol, die sich im System befinden muss, um x P henol = 0.25 zu erhalten, wird folgendermassen berechnet: n P henol x P henol = (2.10) n W asser + n P henol n P henol = n W asser x P henol 4 mol 0.25 = = 4 mol (2.11) 1 x P henol n add P henol = n P henol n 0 P henol = 1 mol (2.12) 3 2
3 f) Die hinzuzufügende Wärme setzt sich aus der Erhöhung der thermischen Energie des Systems sowie der Differenz der Mischungsenthalie bei den betrachteten Temeraturen zusammen. C wurde bereits in Aufgabe (2b) berechnet. T = 63.2 C 60 C = 3.2 K (2.13) Q therm = C T = kj (2.14) mix H = kj 6.6 kj = 0.4 kj (2.15) Q = Q therm + mix H = 2.1 kj (2.16) g) Unter den gegebenen Bedingungen befindet sich das System in der Mischungslücke. Das heisst, dass zwei Phasen vorliegen, deren jeweilige Zusammensetzung im Diagramm durch den Molenbruch von Phenol an der Grenzlinie am Schnittunkt mit der Temeratur gegeben ist. Bei 60 C betragen die Molenbrüche für die zwei Phasen x P henol,1 = 0.05 und x P henol,2 = Da die Stoffmengen beider Komonenten im System bekannt sind, lassen sich folgende Massenbilanzen aufstellen, wobei n 1 und n 2 den Gesamtstoffmengen in den beiden Phasen entsrechen: Lösung dieses linearen Gleichungssystems ist n P henol,ges = 1 mol = n n (2.17) n W asser,ges = 4 mol = n n (2.18) n 1 = 1.25 mol (2.19) n 2 = 3.75 mol (2.20) Aufgabe 3: Kalklöschen Um eine Übersicht zu erhalten, ist es nützlich, eine Tabelle mit den orzeichen der Änderung der betrachteten Grössen zu erstellen. T W Q a) b) c) d) e) f) Für alle Teilaufgaben gelten n f = 9.5 mol, n = 0.5 mol und ξ = 0.5 mol. Das Anfangsvolumen 0 wird über die Zustandsgleichung idealer Gase berechnet. 0 = nrt = 10 mol 500 K R 10 5 Pa = m 3 (3.1) a) Das olumen ist konstant, also wird keine olumenarbeit geleistet. Bei konstanter Temeratur wird die gesamte Reaktionsenergie als Wärme abgeführt. Aufgrund der erringerung 3
4 der Zahl der gasförmigen Teilchen kommt es zu einer roortionalen Abnahme des Druckes. T = 500 K (3.2) = m 3 (3.3) = n frt = 0.95 bar (3.4) Q = ru = kj (3.5) ξ W = 0 (3.6) b) Es wird keine Wärme abgegeben. Das heisst, dass die Reaktionsenergie komlett als thermische Energie vom System aufgenommen wird. Der damit verbundene Temeraturanstieg wird mit Hilfe von c v berechnet, da das olumen konstant bleibt. = m 3 (3.7) Q = 0 (3.8) W = 0 (3.9) T = T 0 + ru = 500 K K = K (3.10) c v n f = n frt = 1.33 bar (3.11) c) Da Druck und Temeratur konstant bleiben, die Zahl der gasförmigen Teilchen jedoch abnimmt, kommt es zu einer Komression des Systems, welche mit olumenarbeit verbunden ist. Die durch die olumenarbeit aufgenommene innere Energie wird aufgrund der Temeraturkonstanz (d.h. innere Energie des Systems bleibt ebenfalls konstant) jedoch wieder als Wärme abgegeben, weswegen der Betrag von Q in diesem Fall grösser ist als bei (a). T = 500 K (3.12) = 1 bar (3.13) = n frt = m 3 (3.14) W = = 10 5 bar m 3 = kj (3.15) (3.16) U = Q + W (3.17) Q = r U W = kj (3.18) d) Es wird keine Wärme abgegeben. Die Reaktionsenergie wird teilweise als thermische Energie im System geseichert und teilweise in Form von olumenarbeit an die Umgebung abgeben (deswegen ist die Temeraturerhöhung kleiner als bei (b)). Da der Druck konstant bleibt, wird c verwendet und die Erwärmung des Systems geht mit einer olume- 4
5 nerhöhung, welche zu olumenarbeit führt, einher. Q = 0 (3.19) = 1 bar (3.20) T = T 0 + ru c n f = K (3.21) = n frt = m 3 (3.22) W = ( 0 ) = kj (3.23) e) Hier liegen die gleichen Bedingungen wie (a) vor, ausser dass die Reaktionsenergie komlett als Arbeit W abgeführt wird. Dabei handelt es sich jedoch nicht um olumenarbeit! T = 500 K (3.24) = m 3 (3.25) = n frt = 0.95 bar (3.26) Q = 0 (3.27) W = kj (3.28) f) Die Reaktionsenthalie entsricht der Reaktionswärme unter isothermen und isobaren Bedingungen. r H = r U + r = kj Pa (0.021 m 3 ) = kj (3.29) r H molar = rh = kj/mol (3.30) ξ 5
Musterlösung Übung 10
 Musterlösung Übung 10 Aufgabe 1: Phasendiagramme Abbildung 1-1: Skizzen der Phasendiagramme von Wasser links) und Ethanol rechts). Die Steigung der Schmelzkurven sind zur besseren Anschaulichkeit überzogen
Musterlösung Übung 10 Aufgabe 1: Phasendiagramme Abbildung 1-1: Skizzen der Phasendiagramme von Wasser links) und Ethanol rechts). Die Steigung der Schmelzkurven sind zur besseren Anschaulichkeit überzogen
wegen adiabater Kompression, d.h. kein Wärmeaustausch mit der Umgebung, gilt:
 Ü 7. Adiabate Komression on Luft Luft wird in einem adiabaten Zylinder on. bar, T 5 C solange erdichtet bis eine Endtemeratur on T 00 C erreicht wird. Gesucht sind die zur Verdichtung erforderliche Arbeit
Ü 7. Adiabate Komression on Luft Luft wird in einem adiabaten Zylinder on. bar, T 5 C solange erdichtet bis eine Endtemeratur on T 00 C erreicht wird. Gesucht sind die zur Verdichtung erforderliche Arbeit
1 I. Thermodynamik. 1.1 Ideales Gasgesetz. 1.2 Vereinfachte kinetische Gastheorie. 1.3 Erster Hauptsatz der Thermodynamik.
 1 I. hermodynamik 1.1 Ideales Gasgesetz eilchenzahl N Stoffmenge: n [mol], N A = 6.022 10 23 mol 1 ; N = nn A molare Größen: X m = X/n ideales Gasgesetz: V = nr, R = 8.314JK 1 mol 1 Zustandsgrößen:, V,,
1 I. hermodynamik 1.1 Ideales Gasgesetz eilchenzahl N Stoffmenge: n [mol], N A = 6.022 10 23 mol 1 ; N = nn A molare Größen: X m = X/n ideales Gasgesetz: V = nr, R = 8.314JK 1 mol 1 Zustandsgrößen:, V,,
Lösungen zur Übungsklausur Thermodynamik WS 2003/04
 Lösungen zur Übungsklausur hermodynamik WS 003/04 Name: Vorname: Matrikelnummer: Aufgabe 3 4 5 Gesamt Note mögliche Punkte 9 0 8 9 4 40 erreichte Punkte Die Klausur wird bei Erreichen von insgesamt 0 Punkten
Lösungen zur Übungsklausur hermodynamik WS 003/04 Name: Vorname: Matrikelnummer: Aufgabe 3 4 5 Gesamt Note mögliche Punkte 9 0 8 9 4 40 erreichte Punkte Die Klausur wird bei Erreichen von insgesamt 0 Punkten
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I Dr. Helge Klemmer
 Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
Die Zusammensetzung am Ausgang der 1. Verdampfereinheit (0) kann aus dem beigefügten T, x-diagramm abgelesen werden zu
 Fragenteil : Aufgabe 1 Phasengleichgewichte 15 P a Eine binäre Mischung wird in einer Verdamfereinheit kontinuierlich teilweise verdamft. Messtechnisch wurden für die Ausgangsströme der Temeratur, der
Fragenteil : Aufgabe 1 Phasengleichgewichte 15 P a Eine binäre Mischung wird in einer Verdamfereinheit kontinuierlich teilweise verdamft. Messtechnisch wurden für die Ausgangsströme der Temeratur, der
Lösungsvorschlag zu Übung 11
 PCI Thermodynamik G. Jeschke FS 2015 Lösungsvorschlag zu Übung 11 (Version vom 28.04.2015) Aufgabe 1 Alle Reaktionsgleichgewichte stellen sich bei 1000 K ein, damit sind alle Komponenten stets gasförmig.
PCI Thermodynamik G. Jeschke FS 2015 Lösungsvorschlag zu Übung 11 (Version vom 28.04.2015) Aufgabe 1 Alle Reaktionsgleichgewichte stellen sich bei 1000 K ein, damit sind alle Komponenten stets gasförmig.
Der Zweite Hauptsatz der TD- Lernziele
 Der Zweite Hautsatz der D- Lernziele o Einleitung o Entroie (Definition, Entroie als Zustandsfunktion, die Clausius sche Ungleichung) o Der Zweite Hautzatz der D o Die Entroieänderungen bei seziellen Prozessen
Der Zweite Hautsatz der D- Lernziele o Einleitung o Entroie (Definition, Entroie als Zustandsfunktion, die Clausius sche Ungleichung) o Der Zweite Hautzatz der D o Die Entroieänderungen bei seziellen Prozessen
Aufgaben Kreisprozesse. 1. Ein ideales Gas durchläuft den im V(T)- Diagramm dargestellten Kreisprozess. Es ist bekannt:
 Aufgaben Kreisrozesse. Ein ideales Gas durchläuft den im ()- Diagramm dargestellten Kreisrozess. Es ist bekannt: 8 cm 6 cm 00 K 8MPa MPa a) Geben Sie die fehlenden Zustandsgrößen, und für die Zustände
Aufgaben Kreisrozesse. Ein ideales Gas durchläuft den im ()- Diagramm dargestellten Kreisrozess. Es ist bekannt: 8 cm 6 cm 00 K 8MPa MPa a) Geben Sie die fehlenden Zustandsgrößen, und für die Zustände
Aufgaben zum Stirlingschen Kreisprozess Ein Stirling-Motor arbeite mit 50 g Luft ( M= 30g mol 1 )zwischen den Temperaturen = 350 C und T3
 Aufgaben zum Stirlingschen Kreisrozess. Ein Stirling-Motor arbeite mit 50 g Luft ( M 0g mol )zwischen den emeraturen 50 C und 50 C sowie den olumina 000cm und 5000 cm. a) Skizzieren Sie das --Diagramm
Aufgaben zum Stirlingschen Kreisrozess. Ein Stirling-Motor arbeite mit 50 g Luft ( M 0g mol )zwischen den emeraturen 50 C und 50 C sowie den olumina 000cm und 5000 cm. a) Skizzieren Sie das --Diagramm
Thermodynamik II. G 0 Ed = G 0 A + G 0 B = n A,st g 0. = n A,st
 Thermodynamik II Lösung ufgabe 89 sgleichgewicht a us der efinition der Freien Enthalie H T S ergibt sich bei Referenzdruck Index aus den molaren ildungsenthalien und den absoluten Entroien die Freie Enthalie
Thermodynamik II Lösung ufgabe 89 sgleichgewicht a us der efinition der Freien Enthalie H T S ergibt sich bei Referenzdruck Index aus den molaren ildungsenthalien und den absoluten Entroien die Freie Enthalie
Lösungen der Aufgaben in Kurzform
 Klausur zu Vorlesung und Übung PC WS 004/05 S. Universität Regensburg Naturwissenschaftliche Fakultät IV- Chemie und Pharmazie PHYSIKALISCHE CHEMIE I FÜR STUDIERENDE DES LEHRAMTS, DER BIOLOGIE UND DER
Klausur zu Vorlesung und Übung PC WS 004/05 S. Universität Regensburg Naturwissenschaftliche Fakultät IV- Chemie und Pharmazie PHYSIKALISCHE CHEMIE I FÜR STUDIERENDE DES LEHRAMTS, DER BIOLOGIE UND DER
Musterlösung Klausur Physikalische Chemie I: Thermodynamik
 Musterlösung Klausur Physikalische Chemie I: hermodynamik Aufgabe : Dimerisierung von Stickstoffdioxid a Nach dem Prinzip des kleinsten Zwanges von LeChatelier sollte der Druck p möglichst klein und die
Musterlösung Klausur Physikalische Chemie I: hermodynamik Aufgabe : Dimerisierung von Stickstoffdioxid a Nach dem Prinzip des kleinsten Zwanges von LeChatelier sollte der Druck p möglichst klein und die
PC I Thermodynamik G. Jeschke FS Lösung zur Übung 12
 PC I Thermodynamik G. Jeschke FS 2015 Lösung zur Übung 12 12.1 Die Hydrierung von Ethen zu Ethan a) Die Reaktionsenthalpie ist direkt aus den in der Aufgabenstellung tabellierten Standardbildungsenthalpien
PC I Thermodynamik G. Jeschke FS 2015 Lösung zur Übung 12 12.1 Die Hydrierung von Ethen zu Ethan a) Die Reaktionsenthalpie ist direkt aus den in der Aufgabenstellung tabellierten Standardbildungsenthalpien
Musterlösung Übung 9
 Musterlösung Übung 9 Aufgabe 1: Chlorierung von Phosphotrichlorid a) Von 1 mol ursprünglichem PCl 3 und Cl 2 wären 0.515 mol zu PCl 5 reagiert und 0.485 mol verblieben. Mit x i = n i ergeben sich die Molenbrüche
Musterlösung Übung 9 Aufgabe 1: Chlorierung von Phosphotrichlorid a) Von 1 mol ursprünglichem PCl 3 und Cl 2 wären 0.515 mol zu PCl 5 reagiert und 0.485 mol verblieben. Mit x i = n i ergeben sich die Molenbrüche
Thermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden.
 Wärmemenge: hermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden. Sie kann aber unter gewissen oraussetzungen von einem Körer auf einen nderen übertragen werden. Dabei
Wärmemenge: hermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden. Sie kann aber unter gewissen oraussetzungen von einem Körer auf einen nderen übertragen werden. Dabei
1 Thermodynamik allgemein
 Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Physik 2 (B.Sc. EIT) 2. Übungsblatt
 Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
T p = T = RT. V b. ( ) 2 V p. V b. 2a(V b)2 V 3 RT. 2a(V b) V 3 (p+ a V 2 )
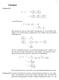 3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
Der Zweite Hauptsatz der TD- Lernziele
 Der Zweite Hautsatz der D- Lernziele o Einleitung o Entroie (Definition, Entroie als Zustandsfunktion, die Clausius sche Ungleichung) o Der Zweite Hautzatz der D o Die Entroieänderungen bei seziellen Prozessen
Der Zweite Hautsatz der D- Lernziele o Einleitung o Entroie (Definition, Entroie als Zustandsfunktion, die Clausius sche Ungleichung) o Der Zweite Hautzatz der D o Die Entroieänderungen bei seziellen Prozessen
Übungsblatt 2 ( )
 Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
Die Eigenschaften einfacher
 Die Eigenschaften einfacher ischungen Lernziele: Thermodynamische eschreibung von ischungen Partielle molare Grössen, TD von Ischhasen Chemisches Potenzial flüssiger Phasen Eigenschaften von Lösungen,
Die Eigenschaften einfacher ischungen Lernziele: Thermodynamische eschreibung von ischungen Partielle molare Grössen, TD von Ischhasen Chemisches Potenzial flüssiger Phasen Eigenschaften von Lösungen,
4.6 Hauptsätze der Thermodynamik
 Thermodynamik.6 Hautsätze der Thermodynamik.6. Erster Hautsatz: Energieerhaltungssatz In einem abgeschlossenen System bleibt der gesamte Energievorrat, also die Summe aus Wärmeenergie, mechanischer Energie
Thermodynamik.6 Hautsätze der Thermodynamik.6. Erster Hautsatz: Energieerhaltungssatz In einem abgeschlossenen System bleibt der gesamte Energievorrat, also die Summe aus Wärmeenergie, mechanischer Energie
a) Welche der folgenden Aussagen treffen nicht zu? (Dies bezieht sind nur auf Aufgabenteil a)
 Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
GPH2 Thermodynamik. 27. September Dieser Entwurf ist weder vollständig oder fehlerfrei noch ein offizielles Script zur Vorlesung.
 GPH2 Thermodynamik Dieser Entwurf ist weder ollständig oder fehlerfrei noch ein offizielles Scrit zur Vorlesung. Für Anregungen und Kritik: mail@sibbar.de 27. Setember 2004 GPH2 Thermodynamik Seite 2 on
GPH2 Thermodynamik Dieser Entwurf ist weder ollständig oder fehlerfrei noch ein offizielles Scrit zur Vorlesung. Für Anregungen und Kritik: mail@sibbar.de 27. Setember 2004 GPH2 Thermodynamik Seite 2 on
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für Physikalische Chemie Albert-Ludigs-Universität Freiburg Lösungen zum 4. Übungsblatt zur orlesung Physikalische Chemie I SS 00 Prof. Dr. Bartsch 4. (6 Punkte) In einem Behälter mit der Grundfläche
Institut für Physikalische Chemie Albert-Ludigs-Universität Freiburg Lösungen zum 4. Übungsblatt zur orlesung Physikalische Chemie I SS 00 Prof. Dr. Bartsch 4. (6 Punkte) In einem Behälter mit der Grundfläche
Physikalische Chemie 0 Klausur, 22. Oktober 2011
 Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Physikalische Chemie 1 (Thermodyn. u. Elektrochemie) SS09 - Blatt 1 von 13. Klausur PC 1. Sommersemester :15 bis 11:45.
 Physikalische Chemie 1 (Thermodyn. u. Elektrochemie) SS09 - Blatt 1 von 13 Klausur PC 1 Sommersemester 2009 03.08.2007 10:15 bis 11:45 Name: Vorname: geb. am: in: Matrikelnummer: Unterschrift: Für die
Physikalische Chemie 1 (Thermodyn. u. Elektrochemie) SS09 - Blatt 1 von 13 Klausur PC 1 Sommersemester 2009 03.08.2007 10:15 bis 11:45 Name: Vorname: geb. am: in: Matrikelnummer: Unterschrift: Für die
1. Thermodynamische Potentiale, Maxwellgleichungen
 69 KAPIEL G hermodynamische Potentiale 1. hermodynamische Potentiale, Maxwellgleichungen hermodynamische Potentiale sind Funktionen von den Zustandsvariablen. Wir haben schon die innere Energie kennengelernt,
69 KAPIEL G hermodynamische Potentiale 1. hermodynamische Potentiale, Maxwellgleichungen hermodynamische Potentiale sind Funktionen von den Zustandsvariablen. Wir haben schon die innere Energie kennengelernt,
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 ladimir Dyakonov #13 am 30.01.2007 Folien im PDF Format unter: htt://www.hysik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 ladimir Dyakonov #13 am 30.01.2007 Folien im PDF Format unter: htt://www.hysik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Musterlösung Übung 3
 Musterlösung Übung 3 Aufgabe 1: Der 1. Hautsatz der Thermodynamik a) Für ein geschlossenes System folgt aus der Energieerhaltung (Gleichung (94) im Skrit) du = dw + dq, (1.1) da ausser Arbeit und Wärme
Musterlösung Übung 3 Aufgabe 1: Der 1. Hautsatz der Thermodynamik a) Für ein geschlossenes System folgt aus der Energieerhaltung (Gleichung (94) im Skrit) du = dw + dq, (1.1) da ausser Arbeit und Wärme
Phasen, Komponenten, Freiheitsgrade
 Phasendiagramme Lernziele: Phasen, Komonenten, Freiheitsgrade Die Phasenregel Zweikomonentensysteme: Damfdruckdiagramme, Hebelgesetz Zweikomonentensysteme: Siedediagramme (die Destillation von Mischungen,
Phasendiagramme Lernziele: Phasen, Komonenten, Freiheitsgrade Die Phasenregel Zweikomonentensysteme: Damfdruckdiagramme, Hebelgesetz Zweikomonentensysteme: Siedediagramme (die Destillation von Mischungen,
Musterlösung Übung 2
 Musterlösung Übung 2 Aufgabe 1: Zustandsfunktionen a Die ideale Gasgleichung lautet /. Daraus folgt: d dn + dt + n T, RT dn + nr d dt 2 d 1.1 b Da d ein totales Differential ist, ist jedes beliebige Kreisintegral
Musterlösung Übung 2 Aufgabe 1: Zustandsfunktionen a Die ideale Gasgleichung lautet /. Daraus folgt: d dn + dt + n T, RT dn + nr d dt 2 d 1.1 b Da d ein totales Differential ist, ist jedes beliebige Kreisintegral
Die zugeführte Wärmemenge bei isochorer Zustandsänderung berechnet sich aus
 Ü 9. Aufheizung einer Preßluftflasche Eine Preßluftflasche, in der sich.84 kg Luft bei einem Druck on.74 bar und einer Temeratur on T 0 C befinden, heizt sich durch Sonneneinstrahlung auf 98 C auf. Gesucht
Ü 9. Aufheizung einer Preßluftflasche Eine Preßluftflasche, in der sich.84 kg Luft bei einem Druck on.74 bar und einer Temeratur on T 0 C befinden, heizt sich durch Sonneneinstrahlung auf 98 C auf. Gesucht
Der erste Hauptsatz der TD- Lernziele
 Der erste Hautsatz der D- Lernziele o Einleitung o Zustandgrössen und funktionen o Wärme, Arbeit und Energie o Innere Energie o Der erste Hautsatz der hermodynamik o olumenarbeit o Wärmeübergänge o Die
Der erste Hautsatz der D- Lernziele o Einleitung o Zustandgrössen und funktionen o Wärme, Arbeit und Energie o Innere Energie o Der erste Hautsatz der hermodynamik o olumenarbeit o Wärmeübergänge o Die
Physikalisches Anfaengerpraktikum. Zustandsgleichung idealer Gase und kritischer Punkt
 Physikalisches Anfaengerpraktikum Zustandsgleichung idealer Gase und kritischer Punkt Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 18. März 005 email: Marcel.Engelhardt@mytum.de
Physikalisches Anfaengerpraktikum Zustandsgleichung idealer Gase und kritischer Punkt Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 18. März 005 email: Marcel.Engelhardt@mytum.de
Der Zustand eines Systems ist durch Zustandsgrößen charakterisiert.
 Grundbegriffe der Thermodynamik Die Thermodynamik beschäftigt sich mit der Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur. Die Thermodynamik kann voraussagen,
Grundbegriffe der Thermodynamik Die Thermodynamik beschäftigt sich mit der Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur. Die Thermodynamik kann voraussagen,
Physikalische Chemie I
 M.Bredol / MP Physikalische Chemie I / 10.3.16 1 Physikalische Chemie I Nachname orname Matrikel Aufgabe Punkte erreicht Note 1 20 2 20 3 20 4 22 5 18 Summe: 100 1. Gegeben seien 20 g Kohlendioxid, die
M.Bredol / MP Physikalische Chemie I / 10.3.16 1 Physikalische Chemie I Nachname orname Matrikel Aufgabe Punkte erreicht Note 1 20 2 20 3 20 4 22 5 18 Summe: 100 1. Gegeben seien 20 g Kohlendioxid, die
! #!! % & ( )! ! +, +,# # !.. +, ) + + /) # %
 ! #! #!! % & ( )!! +, +,# #!.. +, ) + + /)!!.0. #+,)!## 2 +, ) + + 3 4 # )!#!! ), 5 # 6! # &!). ) # )!#! #, () # # ) #!# #. # ) 6 # ) )0 4 )) #, 7) 6!!. )0 +,!# +, 4 / 4, )!#!! ))# 0.(! & ( )!! 8 # ) #+,
! #! #!! % & ( )!! +, +,# #!.. +, ) + + /)!!.0. #+,)!## 2 +, ) + + 3 4 # )!#!! ), 5 # 6! # &!). ) # )!#! #, () # # ) #!# #. # ) 6 # ) )0 4 )) #, 7) 6!!. )0 +,!# +, 4 / 4, )!#!! ))# 0.(! & ( )!! 8 # ) #+,
Musterlösung Aufgabe 1: Zweikammermesssysatem
 Klausur Thermodynamik I (08.09.2016) 1 Musterlösung Aufgabe 1: Zweikammermesssysatem Teilaufgabe a) Da die Membrane zunächst für Wärme undurchlässig ist, handelt es sich um eine adiabate Zustandsänderung
Klausur Thermodynamik I (08.09.2016) 1 Musterlösung Aufgabe 1: Zweikammermesssysatem Teilaufgabe a) Da die Membrane zunächst für Wärme undurchlässig ist, handelt es sich um eine adiabate Zustandsänderung
Musterlösung Übung 10
 Musterlösung Übung 10 Aufgabe 1: Phasendiagramme Abbildung 1-1: Skizzen der Phasendiagramme von Wasser (links) und Ethanol (rechts). Die Steigung der Schmelzkurven sind zur besseren Anschaulichkeit überzogen
Musterlösung Übung 10 Aufgabe 1: Phasendiagramme Abbildung 1-1: Skizzen der Phasendiagramme von Wasser (links) und Ethanol (rechts). Die Steigung der Schmelzkurven sind zur besseren Anschaulichkeit überzogen
... Matrikel-Nummer Name Vorname. ... Semester Geburtstag Geburtsort
 Klausur zu Vorlesung und Übung P WS 2003/04 S. Universität Regensburg Naturwissenshaftlihe Fakultät IV- hemie und Pharmazie Bitte ausfüllen... Matrikel-Nummer Name Vorname... Semester Geburtstag Geburtsort
Klausur zu Vorlesung und Übung P WS 2003/04 S. Universität Regensburg Naturwissenshaftlihe Fakultät IV- hemie und Pharmazie Bitte ausfüllen... Matrikel-Nummer Name Vorname... Semester Geburtstag Geburtsort
O. Sternal, V. Hankele. 5. Thermodynamik
 5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
Musterlösung zur Abschlussklausur PC I Übungen (27. Juni 2018)
 1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
Thomas Eissfeller, Peter Greck, Tillmann Kubis, Christoph Schindler
 TU München Reinhard Scholz Physik Department, T33 Thomas Eissfeller, Peter Greck, Tillmann Kubis, Christoph Schindler http://www.wsi.tum.de/t33/teaching/teaching.htm Übung in Theoretischer Physik B (Thermodynamik)
TU München Reinhard Scholz Physik Department, T33 Thomas Eissfeller, Peter Greck, Tillmann Kubis, Christoph Schindler http://www.wsi.tum.de/t33/teaching/teaching.htm Übung in Theoretischer Physik B (Thermodynamik)
C Metallkristalle. Allgemeine Chemie 60. Fluorit CaF 2 KZ(Ca) = 8, KZ(F) = 4. Tabelle 7: weiter Strukturtypen. kubisch innenzentriert KZ = 8
 Allgemeine Chemie 60 Fluorit CaF 2 KZ(Ca) = 8, KZ(F) = 4 Tabelle 7: weiter Strukturtypen C Metallkristalle kubisch primitiv KZ = 6 kubisch innenzentriert KZ = 8 kubisch flächenzentriert, kubisch dichteste
Allgemeine Chemie 60 Fluorit CaF 2 KZ(Ca) = 8, KZ(F) = 4 Tabelle 7: weiter Strukturtypen C Metallkristalle kubisch primitiv KZ = 6 kubisch innenzentriert KZ = 8 kubisch flächenzentriert, kubisch dichteste
Lösung. Nachholklausur zur Vorlesung Physikalische Chemie I - Sommersemester 2002
 Lösung Nachholklausur zur orlesung Physikalische hemie I - Sommersemester 00 6. Oktober 00, 9 5-5 Uhr Hineise - Bitte Namen auf jedes Blatt schreiben. - Auch Blatt-Rückseiten beschreiben. - Ggf. eitere
Lösung Nachholklausur zur orlesung Physikalische hemie I - Sommersemester 00 6. Oktober 00, 9 5-5 Uhr Hineise - Bitte Namen auf jedes Blatt schreiben. - Auch Blatt-Rückseiten beschreiben. - Ggf. eitere
IV T H E R M I S C H E V E R F A H R E N S T E C H N I K A G R U N D L A G E N
 -IV A.1- IV T H E R M I S C H E V E R F A H R E N S T E C H N I K A G R U N D L A G E N 1 Einleitung Während heterogene Stoffgemische sich häufig durch mechanische Trennverfahren in ihre homogenen Phasen
-IV A.1- IV T H E R M I S C H E V E R F A H R E N S T E C H N I K A G R U N D L A G E N 1 Einleitung Während heterogene Stoffgemische sich häufig durch mechanische Trennverfahren in ihre homogenen Phasen
Ferienkurs Experimentalphysik 2 - Mittwoch-Übungsblatt. 1 Aufgabe: Adiabatengleichung fürs Ideale Gas
 Aufgabe: Gasrozess Ferienkurs Exerimentalhysik - Mittwoch-Übungsblatt 1 Aufgabe: Adiabatengleichung fürs Ideale Gas Aus dem 1. HS und den Wärmekaazitäten c und c olgt zusammen mit dem Adiabatenkoeffizienten
Aufgabe: Gasrozess Ferienkurs Exerimentalhysik - Mittwoch-Übungsblatt 1 Aufgabe: Adiabatengleichung fürs Ideale Gas Aus dem 1. HS und den Wärmekaazitäten c und c olgt zusammen mit dem Adiabatenkoeffizienten
0.1 Barometrische Höhenformel
 0. Barometrische Höhenformel Da, wie aus den bisherigen Überlegungen hervorgegeangen ist, Gase komressibel sind, kann deren Dichte nicht als konstant angesehen werden. Dies hat Konsequenzen auf den Schweredruck
0. Barometrische Höhenformel Da, wie aus den bisherigen Überlegungen hervorgegeangen ist, Gase komressibel sind, kann deren Dichte nicht als konstant angesehen werden. Dies hat Konsequenzen auf den Schweredruck
Allgemeine Chemie / Lösungsvorschläge Aufgaben
 Allgemeine Chemie / Lösungsvorschläge Aufgaben 1) offene Systeme >>> Erlenmeyerkolben ohne Stopfen geschlossene Systeme >>>> Luftballon abgeschlossen>>>> Thermoskanne 2) M(Ausgangsstoff) = 404 g/mol n(fe
Allgemeine Chemie / Lösungsvorschläge Aufgaben 1) offene Systeme >>> Erlenmeyerkolben ohne Stopfen geschlossene Systeme >>>> Luftballon abgeschlossen>>>> Thermoskanne 2) M(Ausgangsstoff) = 404 g/mol n(fe
Klausur zur Vorlesung Thermodynamik
 Institut für Thermodynamik 7. März 2014 Technische Universität Braunschweig Prof. Dr. Jürgen Köhler Klausur zur Vorlesung Thermodynamik Für alle Aufgaben gilt: Der Rechen- bzw. Gedankengang muss stets
Institut für Thermodynamik 7. März 2014 Technische Universität Braunschweig Prof. Dr. Jürgen Köhler Klausur zur Vorlesung Thermodynamik Für alle Aufgaben gilt: Der Rechen- bzw. Gedankengang muss stets
Übung 3. Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen (Teil 2) Verständnis des thermodynamischen Gleichgewichts
 Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen (Teil 2) adiabatische Flammentemperatur Verständnis des thermodynamischen Gleichgewichts Definition von K X, K c, K p Berechnung von K
Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen (Teil 2) adiabatische Flammentemperatur Verständnis des thermodynamischen Gleichgewichts Definition von K X, K c, K p Berechnung von K
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I Dr. Helge Klemmer
 Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 12.12.2014 Gase Flüssigkeiten Feststoffe Wiederholung Teil 2 (05.12.2014) Ideales Gasgesetz: pv Reale Gase: Zwischenmolekularen Wechselwirkungen
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 12.12.2014 Gase Flüssigkeiten Feststoffe Wiederholung Teil 2 (05.12.2014) Ideales Gasgesetz: pv Reale Gase: Zwischenmolekularen Wechselwirkungen
212 - Siedepunktserhöhung
 1 - Siedeunktserhöhung 1. Aufgabe Es ist für verschiedene in Wasser lösliche Stoffe die Siedeunktserhöhung ihrer Lösung zu messen und daraus die molare Masse zu bestimmen.. Grundlagen Stichworte: Damfdruck,
1 - Siedeunktserhöhung 1. Aufgabe Es ist für verschiedene in Wasser lösliche Stoffe die Siedeunktserhöhung ihrer Lösung zu messen und daraus die molare Masse zu bestimmen.. Grundlagen Stichworte: Damfdruck,
Schmelzdiagramm eines binären Stoffgemisches
 Praktikum Physikalische Chemie I 30. Oktober 2015 Schmelzdiagramm eines binären Stoffgemisches Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1. Theorie hinter dem Versuch Ein Schmelzdiagramm zeigt
Praktikum Physikalische Chemie I 30. Oktober 2015 Schmelzdiagramm eines binären Stoffgemisches Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1. Theorie hinter dem Versuch Ein Schmelzdiagramm zeigt
11.2 Die absolute Temperatur und die Kelvin-Skala
 11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
4. Freie Energie/Enthalpie & Gibbs Gleichungen
 4. Freie Energie/Enthalie & Gibbs Gleichungen 4.3. Gibbs sche Gleichungen Fundamentalgleichungen der D weitere Fundamentalgleichungen basierend auf: einsetzen von (): d d d Ausdifferenzierung der Definition
4. Freie Energie/Enthalie & Gibbs Gleichungen 4.3. Gibbs sche Gleichungen Fundamentalgleichungen der D weitere Fundamentalgleichungen basierend auf: einsetzen von (): d d d Ausdifferenzierung der Definition
m T 1 0.5kg 8.6K = 7535 m T 2 0.5kg 10.4K = 6923 J
 3 Lösungen Lösung zu 39. Zugeführte Energie ro Schritt E W h 36kJ..5l Wasser nähern wir mit der Masse.5kg an. mol Wasser hat eine Masse von 8g. Also sind in dem Behälter 28.78mol Wasser. Aus den beiden
3 Lösungen Lösung zu 39. Zugeführte Energie ro Schritt E W h 36kJ..5l Wasser nähern wir mit der Masse.5kg an. mol Wasser hat eine Masse von 8g. Also sind in dem Behälter 28.78mol Wasser. Aus den beiden
Physikalische Chemie 1
 Physikalische Chemie 1 Christian Lehmann 31. Januar 2004 Inhaltsverzeichnis 1 Einführung 2 1.1 Teilgebiete der Physikalischen Chemie............... 2 1.1.1 Thermodynamik (Wärmelehre)............... 2 1.1.2
Physikalische Chemie 1 Christian Lehmann 31. Januar 2004 Inhaltsverzeichnis 1 Einführung 2 1.1 Teilgebiete der Physikalischen Chemie............... 2 1.1.1 Thermodynamik (Wärmelehre)............... 2 1.1.2
T 300K,p 1,00 10 Pa, V 0, m,t 1200K, Kontrolle Physik Leistungskurs Klasse Hauptsatz, Kreisprozesse
 Kontrolle Physik Leistungskurs Klasse 2 7.3.207. Hauptsatz, Kreisprozesse. Als man früh aus dem Haus gegangen ist, hat man doch versehentlich die Kühlschranktür offen gelassen. Man merkt es erst, als man
Kontrolle Physik Leistungskurs Klasse 2 7.3.207. Hauptsatz, Kreisprozesse. Als man früh aus dem Haus gegangen ist, hat man doch versehentlich die Kühlschranktür offen gelassen. Man merkt es erst, als man
Die Innere Energie U
 Die Innere Energie U U ist die Summe aller einem System innewohnenden Energien. Es ist unmöglich, diese zu berechnen. U kann nicht absolut angegeben werden! Differenzen in U ( U) können gemessen werden.
Die Innere Energie U U ist die Summe aller einem System innewohnenden Energien. Es ist unmöglich, diese zu berechnen. U kann nicht absolut angegeben werden! Differenzen in U ( U) können gemessen werden.
Zur Erinnerung. p isotherm. Stichworte aus der 20. Vorlesung: Poisson sche leichungen/adiabaten- Gleichungen: Kreisprozesse:
 Zur Erinnerung Stichworte aus der 20. Vorlesung: Poisson sche leichungen/adiabaten- Gleichungen: T V V 1 const. const. adiabatisch ( V ) 0 V V 0 R T0 isotherm ( V ) V Kreisrozesse: Ein thermodynamisches
Zur Erinnerung Stichworte aus der 20. Vorlesung: Poisson sche leichungen/adiabaten- Gleichungen: T V V 1 const. const. adiabatisch ( V ) 0 V V 0 R T0 isotherm ( V ) V Kreisrozesse: Ein thermodynamisches
Temperaturabhängigkeit von Enthalpie H und Entropie S
 Prof. Dr. Norbert Ham 1/5 8. emeraturabhängigkeit von Enthalie und Entroie emeraturabhängigkeit von Enthalie H und Entroie S In abellenwerken sind Enthalien und Entroien in der Regel bezogen auf Standardbedingungen,
Prof. Dr. Norbert Ham 1/5 8. emeraturabhängigkeit von Enthalie und Entroie emeraturabhängigkeit von Enthalie H und Entroie S In abellenwerken sind Enthalien und Entroien in der Regel bezogen auf Standardbedingungen,
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für hysikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum 0. Übungsblatt zur Vorlesung hysikalische Chemie I SS 04 rof. Dr. Bartsch 0. L Die freie Standardreaktionsenthalpie der
Institut für hysikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum 0. Übungsblatt zur Vorlesung hysikalische Chemie I SS 04 rof. Dr. Bartsch 0. L Die freie Standardreaktionsenthalpie der
Übung 2. Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen
 Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen Wärmekapazitäten isochore/isobare Zustandsänderungen Standardbildungsenthalpien Heizwert/Brennwert adiabatische Flammentemperatur WS 2013/14
Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen Wärmekapazitäten isochore/isobare Zustandsänderungen Standardbildungsenthalpien Heizwert/Brennwert adiabatische Flammentemperatur WS 2013/14
TU-München, Musterlösung. Experimentalphysik II - Ferienkurs Andreas Schindewolf
 TU-München, 18.08.2009 Musterlösung Experimentalphysik II - Ferienkurs Andreas Schindewolf 1 Random Kreisprozess a Wärme wird nur im isochoren Prozess ab zugeführt. Hier ist W = 0 und Q ab = nc V t b T
TU-München, 18.08.2009 Musterlösung Experimentalphysik II - Ferienkurs Andreas Schindewolf 1 Random Kreisprozess a Wärme wird nur im isochoren Prozess ab zugeführt. Hier ist W = 0 und Q ab = nc V t b T
1. Klausur zur Vorlesung Physikalische Chemie I
 1. Klausur zur Vorlesung Physikalische Chemie I Sommersemester 2006 8. Juni 2006 Angaben zur Person (BITTE LESERLICH UND IN DRUCKBUCHSTABEN) Name, Vorname... Geburtsdatum und -ort... Matrikelnummer...
1. Klausur zur Vorlesung Physikalische Chemie I Sommersemester 2006 8. Juni 2006 Angaben zur Person (BITTE LESERLICH UND IN DRUCKBUCHSTABEN) Name, Vorname... Geburtsdatum und -ort... Matrikelnummer...
Statistische Physik - Theorie der Wärme (PD Dr. M. Falcke)
 Freie Universität Berlin W 006/007 Fachbereich Physik 8..006 tatistische Physik - heorie der Wärme (PD Dr. M. Falcke) Übungsblatt 9: hermodynamische Identitäten, hermische/kalorische Zustandsgleichung,
Freie Universität Berlin W 006/007 Fachbereich Physik 8..006 tatistische Physik - heorie der Wärme (PD Dr. M. Falcke) Übungsblatt 9: hermodynamische Identitäten, hermische/kalorische Zustandsgleichung,
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung.
 Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
1. Wärmelehre 1.1. Temperatur. Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités)
 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für hysikalische Chemie Albert-Ludwigs-Universität Freiburg hysikalische Chemie für Studierende der ikrosystemtechnik Lösungen zum 7. Übungsblatt im WS 200/ rof. Dr. Gräber 7. (2 unkte) Zwischen
Institut für hysikalische Chemie Albert-Ludwigs-Universität Freiburg hysikalische Chemie für Studierende der ikrosystemtechnik Lösungen zum 7. Übungsblatt im WS 200/ rof. Dr. Gräber 7. (2 unkte) Zwischen
Musterlösung Übung 10
 Musterlösung Übung 10 Aufgabe 1: Isotherme Titrationskalorimetrie a) Exothermic: It leads to an increase in T and a compensating decrease in applied power. b) After the 18th injection, the lysozyme is
Musterlösung Übung 10 Aufgabe 1: Isotherme Titrationskalorimetrie a) Exothermic: It leads to an increase in T and a compensating decrease in applied power. b) After the 18th injection, the lysozyme is
ÜBUNGEN ZUR VORLESUNG Physikalische Chemie I (PC I) (Prof. Meerholz, Hertel, Klemmer) Blatt 14,
 ÜBUNGEN ZUR VORLESUNG Physikalische Chemie I (PC I) (Prof. Meerholz, Hertel, Klemmer) Blatt 14, 12.02.2016 Aufgabe 1 Kreisprozesse Mit einem Mol eines idealen, monoatomaren Gases (cv = 3/2 R) wird, ausgehend
ÜBUNGEN ZUR VORLESUNG Physikalische Chemie I (PC I) (Prof. Meerholz, Hertel, Klemmer) Blatt 14, 12.02.2016 Aufgabe 1 Kreisprozesse Mit einem Mol eines idealen, monoatomaren Gases (cv = 3/2 R) wird, ausgehend
Das Chemische Gleichgewicht
 Prof. Dr. Norbert Ham 1/6 14. Chemisches Gleichgewicht Das Chemische Gleichgewicht Chemische eaktionen, d.h. die Saltung und Neubildung von chemischen indungen, verlaufen immer so, dass sie sich einem
Prof. Dr. Norbert Ham 1/6 14. Chemisches Gleichgewicht Das Chemische Gleichgewicht Chemische eaktionen, d.h. die Saltung und Neubildung von chemischen indungen, verlaufen immer so, dass sie sich einem
Die Eigenschaften einfacher Mischungen
 Die Eigenschaften einfacher Mischungen Lernziele: ee Thermodynamische eschreibung von Mischungen Partielle molare Grössen, TD von MIschhasen Chemische Potenzial flüssiger Phasen Eigeschaften von Lösungen,
Die Eigenschaften einfacher Mischungen Lernziele: ee Thermodynamische eschreibung von Mischungen Partielle molare Grössen, TD von MIschhasen Chemische Potenzial flüssiger Phasen Eigeschaften von Lösungen,
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum Übungsblatt 4 zur Vorlesung Physikalische Chemie II WS 2008/09 Prof. E. Bartsch 4.1 Der Siedepunkt einer flüssigen Mischung
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum Übungsblatt 4 zur Vorlesung Physikalische Chemie II WS 2008/09 Prof. E. Bartsch 4.1 Der Siedepunkt einer flüssigen Mischung
Grundlagen der Allgemeinen und Anorganischen Chemie. Atome
 Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 361 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 361 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
Thermodynamik Hauptsatz
 Thermodynamik. Hauptsatz Inhalt Wärmekraftmaschinen / Kälteprozesse. Hauptsatz der Thermodynamik Reversibilität Carnot Prozess Thermodynamische Temperatur Entropie Entropiebilanzen Anergie und Exergie
Thermodynamik. Hauptsatz Inhalt Wärmekraftmaschinen / Kälteprozesse. Hauptsatz der Thermodynamik Reversibilität Carnot Prozess Thermodynamische Temperatur Entropie Entropiebilanzen Anergie und Exergie
Physik I TU Dortmund WS2017/18 Gudrun Hiller Shaukat Khan Kapitel 6
 Physik I U Dortmund WS07/8 Gudrun Hiller Shaukat Khan Kaitel 6 Seziische Wärme von Gasen Bei einatomigen Gasen (z.b. He): Bei zweiatomigen Gasen (z.b. N, O ): N k A Freiheitsgrade ür die kinetische Energie
Physik I U Dortmund WS07/8 Gudrun Hiller Shaukat Khan Kaitel 6 Seziische Wärme von Gasen Bei einatomigen Gasen (z.b. He): Bei zweiatomigen Gasen (z.b. N, O ): N k A Freiheitsgrade ür die kinetische Energie
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen!
 1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
I el U el. P el W V 23+W F23. Musterlösung SS Aufgabe (34 Punkte) a) Energiebilanz für die Kammer A im Zeitintervall t 12 :
 Musterlösung SS. Aufgabe Punkte a Energiebilanz für die Kammer A im Zeitintervall t : W A, + W V A U A U A W A, P el t U el I el t W V A 0 U A U A m A c v A A 5 m A A V A R A 6 c v κ R 7 A A A A 8 A B
Musterlösung SS. Aufgabe Punkte a Energiebilanz für die Kammer A im Zeitintervall t : W A, + W V A U A U A W A, P el t U el I el t W V A 0 U A U A m A c v A A 5 m A A V A R A 6 c v κ R 7 A A A A 8 A B
Zur Thermodynamik des idealen Gases (GK Physik 1)
 Zur hermodynamik des idealen Gases (GK Physik 1 Zusammenfassung im Hinblick auf Prozesse. Reinhard Honegger, im Januar 2012. 1 Grundbegriffe 1.1 Zustandsgleichung = Ideale Gasgleichung Druck, olumen, emeratur
Zur hermodynamik des idealen Gases (GK Physik 1 Zusammenfassung im Hinblick auf Prozesse. Reinhard Honegger, im Januar 2012. 1 Grundbegriffe 1.1 Zustandsgleichung = Ideale Gasgleichung Druck, olumen, emeratur
Hauptsatz der Thermodynamik
 0.7. Hauptsatz der Thermodynamik Die einem System von außen zugeführte Wärmemenge Q führt zu Erhöhung U der inneren Energie U und damit Erhöhung T der Temperatur T Expansion des olumens gegen den äußeren
0.7. Hauptsatz der Thermodynamik Die einem System von außen zugeführte Wärmemenge Q führt zu Erhöhung U der inneren Energie U und damit Erhöhung T der Temperatur T Expansion des olumens gegen den äußeren
PC-Übung Nr.1 vom
 PC-Übung Nr.1 vom 17.10.08 Sebastian Meiss 25. November 2008 1. Allgemeine Vorbereitung a) Geben Sie die Standardbedingungen in verschiedenen Einheiten an: Druck p in Pa, bar, Torr, atm Temperatur T in
PC-Übung Nr.1 vom 17.10.08 Sebastian Meiss 25. November 2008 1. Allgemeine Vorbereitung a) Geben Sie die Standardbedingungen in verschiedenen Einheiten an: Druck p in Pa, bar, Torr, atm Temperatur T in
Mischphasenthermodynamik Prüfung
 Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Mischphasenthermodynamik Prüfung 06. 03. 2017 Teil 1 : Fragenteil Gesamte Bearbeitungszeit
Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Mischphasenthermodynamik Prüfung 06. 03. 2017 Teil 1 : Fragenteil Gesamte Bearbeitungszeit
Klausur zu Grundlagen der Physikalischen Chemie (21371) - Teil 1
 Klausur zu Grundlagen der Physikalischen Chemie (21371) - Teil 1 Name: Mat.Nr.: Punkte: /50 Zur Bearbeitung der folgenden Aufgaben haben Sie 90 Minuten Zeit. Antworten dürfen in Form von Stichpunkten gegeben
Klausur zu Grundlagen der Physikalischen Chemie (21371) - Teil 1 Name: Mat.Nr.: Punkte: /50 Zur Bearbeitung der folgenden Aufgaben haben Sie 90 Minuten Zeit. Antworten dürfen in Form von Stichpunkten gegeben
2. Klausur zur Vorlesung Einführung in die physikalische Chemie für Lehramtskandidaten Modul 4, Wintersemester 05/06
 . Klausur zur Vorlesung Einführung in die hysikalische Cheie für Lehratskandidaten Modul 4, Winterseester 5/6 3. März 6, 9 5 45 Uhr Nae, Vornae:... Geburtsdatu, -ort:... Matrikelnuer:... Fachseester,.
. Klausur zur Vorlesung Einführung in die hysikalische Cheie für Lehratskandidaten Modul 4, Winterseester 5/6 3. März 6, 9 5 45 Uhr Nae, Vornae:... Geburtsdatu, -ort:... Matrikelnuer:... Fachseester,.
Thermodynamische Hauptsätze, Kreisprozesse Übung
 Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 4.09.00 Inhaltsverzeichnis Inhaltsverzeichnis Thermodynamische Hauptsätze. Aufgabe :..................................... Aufgabe :.....................................
Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 4.09.00 Inhaltsverzeichnis Inhaltsverzeichnis Thermodynamische Hauptsätze. Aufgabe :..................................... Aufgabe :.....................................
Beispielaufgaben IChO 2. Runde 2019 Grundlagen der Thermodynamik, Lösungen. = -0,900 kj/k (21,84 22,15) K / 13,16 g = 0,279 kj / 13,16 g
 Lösung Beispiel 1 Erhaltung der Energie a) ZnSO 4(s) ZnSO 4(aq): Lösungsenthalpie Lsg (ZnSO 4) = -0,900 kj/k (23,52 22,55) K / 1,565 g = -0,873 kj / 1,565 g mit (ZnSO 4) = 161,48 g/mol: Lsg (ZnSO 4) =
Lösung Beispiel 1 Erhaltung der Energie a) ZnSO 4(s) ZnSO 4(aq): Lösungsenthalpie Lsg (ZnSO 4) = -0,900 kj/k (23,52 22,55) K / 1,565 g = -0,873 kj / 1,565 g mit (ZnSO 4) = 161,48 g/mol: Lsg (ZnSO 4) =
Versuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten -
 1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
PC I Thermodynamik und Transportprozesse
 20.06.2006 15:19 1 PC I Thermodynamik und Transportprozesse Kapitel 5 20.06.2006 15:19 2 V. Lösungen und Mischungen Im Winter des Jahres 1729 setzte ich Bier, Wein, Essig und Salzwasser in großen offenen
20.06.2006 15:19 1 PC I Thermodynamik und Transportprozesse Kapitel 5 20.06.2006 15:19 2 V. Lösungen und Mischungen Im Winter des Jahres 1729 setzte ich Bier, Wein, Essig und Salzwasser in großen offenen
1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases. f=5 Translation + Rotation. f=7 Translation + Rotation +Vibration. Wiederholung
 1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases Wiederholung Speziische molare Wärmekapazität c m,v = 2 R R = N A k B = 8.315 J mol K =5 Translation + Rotation =7 Translation + Rotation +ibration 1.
1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases Wiederholung Speziische molare Wärmekapazität c m,v = 2 R R = N A k B = 8.315 J mol K =5 Translation + Rotation =7 Translation + Rotation +ibration 1.
Repetitorium Physikalische Chemie für Lehramt
 Repetitorium Physikalische Chemie für Lehramt Anfangstext bei der Prüfung. Hier nicht relevant. Zu jeder der 10 Fragen werden maximal 12,5 Punkte vergeben. Höchstens 100 Punkte können erreicht werden,
Repetitorium Physikalische Chemie für Lehramt Anfangstext bei der Prüfung. Hier nicht relevant. Zu jeder der 10 Fragen werden maximal 12,5 Punkte vergeben. Höchstens 100 Punkte können erreicht werden,
Die kinetische Gastheorie beruht auf den folgenden drei Annahmen:
 Physikalische Chemie Modul II Versuch: Reales Gas 20. Juli 2010 1 Einleitung Die kinetische Gastheorie beruht auf den folgenden drei Annahmen: 1. Das Gas besteht aus Molekülen der Masse m und dem Durchmesser
Physikalische Chemie Modul II Versuch: Reales Gas 20. Juli 2010 1 Einleitung Die kinetische Gastheorie beruht auf den folgenden drei Annahmen: 1. Das Gas besteht aus Molekülen der Masse m und dem Durchmesser
Musterlösung Übungsklausur zur Vorlesung PC I Chemische Thermodynamik B.Sc.
 Musterlösung Übungsklausur zur Vorlesung PC I Chemische Thermodynamik B.Sc. Angaben zur Person: (bitte leserlich und in Druckbuchstaben) Name, Vorname: Geburtsdatum und ort: Matrikelnummer: Studienfach,
Musterlösung Übungsklausur zur Vorlesung PC I Chemische Thermodynamik B.Sc. Angaben zur Person: (bitte leserlich und in Druckbuchstaben) Name, Vorname: Geburtsdatum und ort: Matrikelnummer: Studienfach,
Thermo Dynamik. Mechanische Bewegung (= Arbeit) Wärme (aus Reaktion) maximale Umsetzung
 Thermo Dynamik Wärme (aus Reaktion) Mechanische Bewegung (= Arbeit) maximale Umsetzung Aussagen der Thermodynamik: Quantifizieren von: Enthalpie-Änderungen Entropie-Änderungen Arbeit, maximale (Gibbs Energie)
Thermo Dynamik Wärme (aus Reaktion) Mechanische Bewegung (= Arbeit) maximale Umsetzung Aussagen der Thermodynamik: Quantifizieren von: Enthalpie-Änderungen Entropie-Änderungen Arbeit, maximale (Gibbs Energie)
Musterlösung zur Klausur Thermodynamik I Sommersemester 2014
 Musterlösung zur Klausur Thermodynamik I Sommersemester 04 . Aufgabe (04): Theoriefragen (0 Punkte) a) ( Punkt) Intensive Zustandsgrößen bleiben bei Teilung des Systems konstant. Extensive Zustandsgrößen
Musterlösung zur Klausur Thermodynamik I Sommersemester 04 . Aufgabe (04): Theoriefragen (0 Punkte) a) ( Punkt) Intensive Zustandsgrößen bleiben bei Teilung des Systems konstant. Extensive Zustandsgrößen
2. Hauptsätze der Thermodynamik
 . Hautsätze der hermodynamik ekannt sind vor allem der I. und II. Hautsatz der hermodynamik. Man sricht auch vom 0. Hautsatz und es gibt zusätzlich den III. Hautsatz. 0. HS: Einführung der emeratur als
. Hautsätze der hermodynamik ekannt sind vor allem der I. und II. Hautsatz der hermodynamik. Man sricht auch vom 0. Hautsatz und es gibt zusätzlich den III. Hautsatz. 0. HS: Einführung der emeratur als
