4.1. Fette und Seifen
|
|
|
- Lorenz Fiedler
- vor 7 Jahren
- Abrufe
Transkript
1 4.1. Fette und Seifen Aufbau und physikalische Eigenschaften der Fette Pflanzliche und tierische Fette und Öle vergleichen Fette sind Ester langkettiger arbonsäuren (Fettsäuren) mit Propantriol (Glycerin). Das Depotfett der warmblütigen Säugetiere enthält hauptsächlich langkettige gesättigte Fettsäuren, während wechselwarme Fische und Echsen sowie die Pflanzen vor allem kurzkettigere und ungesättigte Fettsäuren enthalten: Zusammensetzung verschiedener Fette in Massenprozent Butter -fett Schweine -fett Kokos -fett liven -öl Sonnenblumen -öl Leinsamen -öl Buttersäure Butansäure Laurinsäure Dodekansäure Myristinsäure Tetradekansäure Palmtinsäure exadekansäure Stearinsäure ctadekansäure Ölsäure cis-9-ctadecensäure Linolsäure cis, cis-9,1-ctadecadiensäure Linolensäure all-cis-9,1,15-ctadecatriensäure Arachidonsäure all-cis-5,8,11,14-eicosatetraensäure Iodzahl (g Iod / 100 g Fett) Schmelzbereich ( ) 31 bis bis 4 3 bis 8 3 bis 0 18 bis 11 0 bis 16 Beispiele Tristearinsäure-glycerin-ester Tri-Linolensäure-Glycerin-Ester 1
2 Physikalische Eigenschaften: Die starren cis-doppelbindungen der ungesättigten Fettsäuren behindern den Kontakt der langen Alkylreste und schwächen dadurch die Van-der-Waals-Kräfte. Fette mit ungesättigten Fettsäuren haben infolgedessen geringere Schmelzpunkte als solche mit gesättigten Fettsäuren. Fette, die bei aumtemperatur flüssig sind, werden auch Öle genannt. Aufgrund der starken Van-der-Waals-Kräfte zwischen den langen Ketten sind Fette bei Normaldruck nicht unzersetzt verdampfbar Verhalten der Fette beim Erhitzen 1. Bildung von Acrolein: livenöl mit etwas KS 4 im G erhitzen und die entstehenden Gase durch fuchsinschweflige Säure leiten.. Fettexplosion mit Wachs und Teelichten Zersetzung: Zunächst werden die Esterbindungen durch den aus dem Fleisch austretenden Wasserdampf hydrolysiert. Nachdem das Wasser verdampft ist, eliminiert das Glycerin zwei weitere Wassermoleküle, wobei das krebserregende Propenal (Acrolein) entsteht und verdampft. Die langen Ketten der Fettsäuren werden radikalisch gespalten und oxidieren zu ebenfalls krebserregenden Aldehyden. (s.u.) Fettexplosion mit Wasser Die kurzkettigen Zersetzungsprodukte verdampfen und können sich leicht entzünden. Beim Löschversuch mit Wasser kommt es zur Explosion, da die Wassertropfen auf den heißen Gefäßboden sinken und dort schlagartig verdampft. Dadurch werden Fetttröpfchen emporgeschleudert, die sich infolge ihres großen Verteilungsgrades ebenfalls entzünden. Tristearinsäure-glycerin-ester 3 3 Stearinsäure Glycerin 3 Decyl-adikal 8-arboxy-ctyl-adikal 3 Decanal 8-xo-ctansäure Propenal (Acrolein) Übungen: Aufgaben zu Fetten und Seifen Aufgaben 1 und
3 Verhalten der Fette beim Stehen lassen Altes Fritierfett mit fuchsinschwefliger Säure schütteln Beim Stehen lassen werden Fette durch die Luftfeuchtigkeit allmählich hydrolisiert, wobei u.a. Buttersäure freigesetzt wird. Die Doppelbindungen der ungesättigten Fettsäuren bilden leicht mesomeriestabilisierte adikale, die durch Luftsauerstoff zu ydroperoxiden oxidiert werden. Durch Spaltung können wie beim Erhitzen übelriechend und gesundheitsschädliche Aldehyde entstehen. ungesättigte Fettsäure mesomeriestabilisiertes Fettsäureradikal Fettsäureperoxidradikal Aldehyd Enol Aldehyd Fettsäurehydroperoxid Biologische Bedeutung der Fette Fette als Energiespeicher Fette dienen dem Körper als Energiespeicher und Wärmeisolierung für längere ungerzeiten. Fette mit langen gesättigten Fettsäuren sind bei aumtemperatur fest und können daher nur durch Warmblüter genutzt werden Da der Transport der wasserunlöslichen Fette im Blut durch speziell herzustellende Transportlipoproteine für den Körper sehr aufwendig ist, werden die Fettvorräte aber erst angegriffen, wenn die Glykogenvorräte in der Leber und die Aminosäurenvorräte in den Zellen und Muskeln zur Neige gehen. Je nach Konstitution und Versorgung kann es bis zu zwei Wochen dauern, bis der Fettabbau in Gang kommt! Pflanzliche Fette in Früchten dienen als Energiespeicher und xidationsschutz für den Samen. Sie sind aufgrund ihrer geringeren Schmelzpunkte auch bei Boden- bzw. Wassertemperaturen von 5-10 durch die Pflanzen abbaubar. Die Doppelbindungen der ungesättigten Fettsäuren fangen den Luftsauerstoff ab und dienen daher als xidationsschutz für den empfindlichen Samen (Autoxidation): Fette als Nehrungsmittel Tierische Fette müssen im Verdauungstrakt unter beträchtlichem Energieaufwand zunächst geschmolzen werden, um dann verdaut und abgebaut werden zu können Pflanzliche Fette sind aufgrund ihrer geringeren Schmelzpunkte leichter verdaulich als tierische Fette und enthalten mehrfach ungesättigte Fettsäuren, die vom Körper (u.a. zur Synthese der Prostaglandin-ormone) benötigt, aber nicht selbst hergestellt werden können. Diese Fettsäuren haben Vitamincharakter und heißen auch essentielle Fettsäuren. Sie können im menschlichen Körper nicht nur Sauerstoff, sondern auch andere potentiell krebserregende adikale abfangen Übungen: Aufgaben zu Fetten und Seifen Aufgabe 3 Margarineherstellung: In ein Becherglas gibt man 15 g Kokosfett und bringt das Fett über kleiner Flamme zum Schmelzen. Man nimmt das Becherglas von der Flamme und fügt unter kräftigem ühren einen Eßlöffel livenöl zu. Man stellt das Becherglas in eine Schüssel mit Eiswasser und fügt unter ständigem ühren je einen Teelöffel gut gekühlte fettarme Milch und Eigelb sowie eine Prise Salz zu. Man rührt kräftig, bis die Masse steif ist. 3
4 Margarine und Fetthärtung Pflanzliche Öle sind gesünder als tierische Fette und außerdem durch Auspressen oder Extrahieren der Pflanzensamenleichter leichter und billiger zu gewinnen. Sie sind daher seit Ende des 0. Jahrhunderts auch in nördlichen Ländern als Nahrungsbestandteil beliebt geworden. Um ein butterähnliches und streichfähiges Produkt (Margarine) herzustellen, werden die Doppelbindungen teilweise katalytisch hydriert (Fetthärtung), wodurch allerdings auch der physiologische Wert der entsprechenden Fettsäuren gemindert wird. Wie bei der Butterherstellung gibt man außerdem etwas Wasser und einen Emulgator (s.u.) hinzu, um durch Emulsionsbildung eine weitere Verfestigung zu erreichen. Übungen: Aufgaben zu Fetten und Seifen Aufgabe Untersuchung von Fetten Bromlösung in livenöl geben Iodzahl Die Iodzahl gibt an, wieviel g Iod maximal an 100 g Fett addiert werden kann und ist ein Maß für die durchschnittliche Zahl der Doppelbindungen pro Molekül. Die Iodzahl läßt sich schnell und einfach bestimmen und wird in der Lebensmittelchemie häufig verwendet, da die Zahl der Doppelbindungen für den physiologischen Wert eines Fettes entscheidend ist. Verseifungszahl Die Verseifungszahl gibt an, wieviel mg K für die Verseifung von 1 g Fett verbraucht werden. Sie ist ein Maß für die Zahl der Esterbindungen bzw. Fettsäuren pro g Fett. ohe Verseifungszahlen bedeuten also viele kurzkettige Fettsäuren, niedrige Verseifungszahlen dagegen wenige langkettige Fettsäuren pro g Fett. Da kurzkettige Fettsäuren leichter verdaulich sind, ist die Verseifungszahl ebenfalls eine wichtige Kennzahl in der Lebensmittelchemie. Säurezahl Die Säurezahl gibt an, wieviel mg K für die Neutralisation der freien Fettsäuren in 1 g Fett verbraucht werden. Da die Zahl der freien Fettsäuren mit zunehmendem Alter des Fettes ansteigt, ist sie ein Maß für den Frischegrad des Fettes Übungen: Aufgaben zu Fetten und Seifen Aufgaben 5-9 Gaschromatograph auseinander bauen Gsachromatographie Für genauere Untersuchungen verwendet man die Gaschromatographie. Ein Gaschromatograph besteht aus einer langen Metallröhre (Trennsäule), die innen mit einem porösen Material beschichtet ist, welches mit einer mehr oder weniger polaren Flüssigkeit wie z.b. Wasser oder Glycerin (stationäre Phase) getränkt ist. Durch die Trennsäure wird ein inertes Trägergas wie Wasserstoff oder elium (mobile Phase) gepumpt. Am Kopf der Säule wird das zu trennende Gemisch injiziert und vom Trägergas in die Säule eingebracht. Je nach Polarität und Molmasse werden die zu trennenden Stoff unterschiedlich stark von der stationären Phase zurückgehalten und treten daher nach unterschiedlicher etentionszeit am Säulenende wieder aus. Sie werden dort durch einen Detektor nachgewiesen, der ihre Wärmeleitfähigkeit misst. Die Temperatur in der Trennsäule kann bis zu 400 betragen, so dass auch weniger flüchtige Stoffe untersucht werden können. Da sich Fette nicht unzersetzt verdampfen lassen, werden sie zunächst hydrolysiert und die Fettsäuren dann mit Methanol verestert, um die Siedepunkte herabzusetzen. Die Fettsäuremethanolester können dann in den Gaschromatograph eingespritzt und mit ilfe von Vergleichssubstanzen identifiziert werden. Übungen: Aufgaben zu Fetten und Seifen Aufgabe 10 4
5 Dispersionen Tyndall-Effekt mit Seifenlösung Dispersionen Dispersionen sind Verteilungen von kleinen Teilchen in einem Dispersionsmittel. Je nach Durchmesser d der dispergierten Teilchen unterscheidet man 1. molekulardisperse (echte) Lösungen mit d < 1 nm. Da der Teilchendurchmesser deutlich kleiner ist als die Wellenlänge des sichtbaren Lichtes, findet keine eflektion statt. Die Teilchen sind unsichtbar und die Lösung ist klar.. kolloiddisperse (kolloidale) Lösung mit 1 < d < 1000 nm. Da der Teilchendurchmesser im Bereich der Wellenlänge des sichtbaren Lichtes liegt, findet eflektion statt, aber der Umriss der Teilchen ist nicht auflösbar. Die Lösungen sind klar und zeigen den Tyndall-Effekt (Streuung von durchscheinendem Licht) 3. grobdisperse Lösungen mit d > 1000 nm, in denen die Umrisse der Teilchen erkennbar sind und zu einer trüben Lösung führen. Beispiele: Aggregatzustände Bezeichnung Beispiel fest in fest feste Suspension ubinglas fest in flüssig flüssige Suspension Kaffee fest in gasförmig festes Aerosol auch flüssig in fest feste Emulsion Butter flüssig in flüssig flüssige Emulsion Milch flüssig in gasförmig flüssiges Aerosol Nebel gasförmig in fest fester Schaum Bimsstein gasförmig in flüssig flüssiger Schaum Schlagsahne Tenside und Emulgatoren Tenside bzw. Emulgatoren sind Moleküle, die aus einem längeren unpolaren Schwanz (Alkylrest) und einem polaren Kopf (meist eine ydroxyl-, arboxylat oder Sulfonat-Gruppe) bestehen. Dadurch sind sie in der Lage, unpolare und polare Stoffe kolloidal ineinander zu lösen. Die Bildung einer Dispersion erfolgt in mehreren Schritten. 1. Benetzung der unpolaren Teilchen durch erabsetzung der berflächenspannung des Wassers. Petrischale randvoll mit Wasser füllen, Baumwolle oder Büroklammer auflegen und Spülmittel dazugeben. Petrischale mit Wasser auf P, Schwefel oder Aktivkohle aufstreuen, 1 Tropfen Spülmittel dazugeben. Die Tensidmoleküle ordnen sich wegen der mangelnden Löslichkeit ihrer unpolaren Schwänze an der Wasseroberfläche an. Sie schwächen dort die starken Dipol-Dipol-Kräfte zwischen den Wassermolekülen und bewirken so das Zerfließen der Wassertropfen. Das Wasser kann in Gewebe und kleine Zwischenräume vordringen und die Fettteilchen umhüllen.. Ablösewirkung Die unpolaren Schwänze der Tenside werden durch van-der-waals- Kräfte von unpolaren Fasern und Fetteilchen angezogen. Die nach außen stehenden negativ geladenen polaren Köpfe stoßen sich gegenseitig ab und bewirken die Ablösung und Aufspaltung der Fettteilchen. 3. Emulgier- bzw. Dispergierwirkung Je 1 Teelöffel Aktivkohle in 100 ml Wasser und 100 ml Tensidlösung geben und filtrieren. In G jeweils ml mit Sudanrot gefärbtes livenöl geben und Wasser bzw. Tensidlösung hnzufügen. Die Fetteilchen werden von den Tensidmolekülen umhüllt, wobei die unpolaren Schwänze in die Fetteilchen eindringen und die polaren Köpfe dem Wasser zugewandt sind. Die so gebildeten Micellen haben nach außen hin polaren harakter und bilden eine Dispersion 5
6 Übungen: Aufgaben zu Fetten und Seifen Aufgabe Seifen livenöl und Wasser in G geben, festes Na hinzufügen, erwärmen (Schutzbrille!) und Schaumbildung beobachten Die einfachsten und ältesten Tenside erhält man durch Kochen von tierischen oder pflanzlichen Fetten mit konzentrierten Alkalilaugen (Seifensieden). Dabei werden die Fette zu Glycerin und Alkalisalzen der Fettsäuren (Seifen) hydrolysiert. Mit Natronlauge erhält man feste Kernseifen, mit Kalilauge flüssige Schmierseifen: 3 Na (aq) Tripalmitinsäure-glycerin-ester Natronlauge Na Na Na Natriumpalmitat (Kernseife) Glycerin Nachteile der Seifen: 1. Seifen reagieren als Salze schwacher Säuren stark basisch, wodurch Textilien und auch die menschliche aut angegriffen werden: Na Na.. Starke Säuren neutralisieren die Seifen zu wasserunlöslichen Fettsäuren. Aus diesem Grund können Seifen für stark saure Verschmutzungen, wie sie zum Beispiel häufig in der Industrie auftreten, nicht verwendet werden: Na 3 Na. 3. Die ärtebildner des Wassers, hauptsächlich a - und Mg -Ionen, bilden mit Seifen schwerlösliche Salze, die Kalkseifen. In hartem Wasser wird dadurch unnötig mehr Seife verbraucht. Außerdem lagert sich die Kalkseife auf Textilien ab, wodurch diese grau und spröde werden: Na a ( ) a Na. Übungen: Versuche zu Seifen und Tensiden artes Wasser und Waschwirkung Natürliches Quellwasser enthält im Gegensatz zu egenwasser je nach erkunft unterschiedliche Mengen an a, Mg, 3 und S 4 -Ionen. Diese Ionen sind einerseits für den Eigengeschmack verantwortlich, vermindern aber andererseits die Waschwirkung der meisten Seifen Na und anionischen Tenside S 3 Na, mit denen sie schwerlösliche Salze wie z.b. Kalkseifen a( ) bilden. Diese schwerlösliche Salze setzen sich beim Waschvorgang am Boden des Waschgefäßes ab, wodurch sowohl die ärtebildner a und Mg als auch die Seifen und S 3 aus der Waschlauge entfernt werden. a und Mg führen also zu einem Mehrverbrauch an (teurer und umweltbelastender) Seife und sollten daher vor dem Waschvorgang entfernt werden. Früher entfernte man einen Teil des a und Mg durch Erhitzen oder Zugabe von Lauge. Dabei werden die 3 -Ionen zu 3 deprotoniert: Beim Erhitzen wird aus der Waschlauge ausgetrieben, wodurch sich das Gleichgewicht 3 3 stark nach rechts verschiebt. (Prinzip vom kleinsten Zwang) Zugabe von Lauge: 3 3. Die 3 -Ionen bilden mit a und (in geringerem Maße) Mg schwerlösliche Salze, die sich als Kesselstein a 3 und Mg 3 auf dem Boden absetzen. Dadurch kann jedes ursprünglich enthaltene 3 ein a bzw. Mg aus der Lauge entfernen. Der Gehalt an 3 wird daher temporäre ärte genannt, während der Gehalt an S 4 permanente ärte heißt. 6
7 eute werden a und Mg beim Waschvorgang durch Komplexbildner wie Na 5 P 3 11 oder Na EDTA entfernt bzw. durch Na ersetzt. Nach dem Gesetz über Einheiten im Messwesen vom darf von den vielen früher gebräuchlichen Einheiten eigentlich nur noch die Einheit mmol/l verwendet werden. Auf den Waschmittelpackungen wird neben dem ärtebereich aber oft noch der Deutsche ärtegrad angegeben. Ein Deutscher Grad (1 d) entspricht 10 mg alciumoxid pro Liter oder 0,18 mmol/l Erdalkali-Ionen. Dabei muss beachtet werden, dass in wässeriger Lösung kein alciumoxid vorliegt, aber alle ärtebildner (auch die Anionen 3 und S 4!) auf alciumoxid umgerechnet werden. Beispiel: Berechnung der temporären und permanenten Wasserhärte 1 l einer Wasserprobe enthält 467 mg a -Ionen und 8 mg 3 -Ionen. a) Wie viel g Kesselstein a 3 können beim Erhitzen dieser Wasserprobe maximal entstehen? b) Berechnen Sie die temporäre und die permanente ärte in deutschen ärtegraden. c) Die permanente ärte wurde früher auch durch Zugabe von Na 3 oder Na 3 und nachfolgenden Erhitzen entfernt. Erklären Sie diese beiden Methoden mit ilfe je einer eaktionsgleichung. Lösung: a) Man rechnet die eaktionsgleichung zunächst auf mg um: 1 mmol a (aq) mmol 3 (aq) 1 mmol a 3 (s) 1 mmol (g) 1 mmol 40 mg a (aq) 1 mg 3 (aq) 100 mg a 3 (s) 1 mmol (g) 1 mmol Am Massenverhältnis sieht man jetzt schon, dass die 8 mg 3 vollständig reagieren können, wobei aber nur ein Teil der 467 mg a verbraucht werden. Daher rechnet man auf 8 mg 3 um : 74,7 mg a 8 mg 3 186,9 mg a3 (s) ::: b) Die in a) verbrauchten 74,4 mg a = 1,86 mmol a 10,3 d bilden die temporäre ärte, die übrig gebliebenen ,4 = 39,6 mg a = 9,8 mmol a 54,5 d bilden die permanente ärte. c) In beiden Fällen wird der Gehalt an 3 erhöht, wodurch die restliche a und Mg ausgefällt werden. Übungen: Aufgaben zu Fetten und Seifen Aufgabe 1 Versuche zur Wasserhärte Anionische und nichtionische Tenside Anionische Tenside. Zu den wichtigsten Vertretern dieses Typs gehören die in Waschmitteln verwendeten Natriumsalze von Schwefelsäuremonoalkylester, die man auch als Alkylsulfate" bezeichnet und die Alkylbenzolsulfonate. Alkylsulfate erhält man durch Addition von Schwefelsäure an höhere 1-Alkene aus dem rackprozeß und Neutralisation der entstehenden Schwefelsäuremonoalkylester: S 4 Na Dodeken-1 elektrophile Addition S Säure-Basereaktion S Na Schwefelsäure-dodekyl - -ester Natrium-Dodekyl-sulfat 7
8 Bei der erstellung von Alkylbenzolsulfonaten wird zunächst Benzol an höhere 1-Alkene addiert. Durch Sulfonierung der entstehenden Alkylbenzole mit Schwefelsäure erhält man Alkylbenzolsulfonsäuren, deren Neutralisation mit Natronlauge Alkytbenzolsulfonate ergibt: 10 1 Dodeken-1 Benzol elektrophile Addition 10 1 Dodekyl-benzol S 4 elektrophile Substitution 10 1 S Na Dodekyl-benzol-sulfonsäure Säure-Basereaktion 10 1 S Na Natrium-Dodekyl-benzol-sulfonat Da die teilweise veresterte Schwefelsäuren aufgrund des I-Effektes der Alkylrste schwächere Säuren als unveresterte Schwefelsäuren sind und mit a ebenfalls schwerlsliche Salze bilden, treten die oben genannten Nachteile in abgeschwächter Form bei diesen Tensiden leider ebenfalls auf. Nichtionische Tenside. Diese Art von Tensiden erhält im hydrophilen Molekülteil mehrere, zur ydratisierung befähigte Ethergruppen und eine endständige polare ydroxylgruppe. Die erstellung erfolgt häufig durch Addition von Fettsäuren oder höheren primären Alkoholen an Ethylenoxid. Nichtionische Tenside neigen bei ausgezeichneter einigungswirkung weniger zur Schaumbildung als Anion-Tenside und werden in Geschirrspülmitteln verwendet. Beispiel: ktyl-tetraglykol-ether Übungen: Versuche zu Seifen und Tensiden Waschmittel Versuche zu Waschmitteln Enthärter entfernen die ärtbildner a - und Mg aus der Waschlösung. Sie verhindern dadurch die Bildung von Kalkseifen und die Verkalkung der Waschmaschine. Pentanatriumtriphosphat Na 5 P 3 10 bildet mit den ärtebildnern lösliche Komplexe, führt aber zu einer Eutrophierung (Überdüngung übermäßiges Algenwachstum Sauerstoffmangel) der Gewässer und wird daher kaum noch verwendet. Das Natriumaluminiumsilicat Zeolith A Na 1 [Al 1 Si 1 8 ] 7 (zeon = kochen und lithos = Stein, da das Mineral beim Erhitzen durch Wasserabgabe zu kochen scheint) ist ein Ionentauscher, der die in seinen ohlräumen lose gebundenen Na - und K - Ionen gegen a - und Mg austauschen kann. 8
9 Bleichmittel wie z.b. Natriumperborat Na B 8 4 oder Natriumpercarbonat Na 3 3 hydrolysieren in Wasser unter Bildung von, welches die Farbstoffe in bst- und otweinflecken durch xidation zerstört. Die Farbstoffe von maschinenwaschbaren Textilien müssen gegenüber Luftsauerstoff beständig sein und werden nicht angegriffen. Schwermetallionen katalysieren den Zerfall des Perborates, was zu Faserschädigungen durch überhöhte -Konzentrationen führen kann. Man setzt daher Komplexbildner wie EDTA (Ethylendiamintetraacetat) hinzu, die die Schwermetallionen aus der Waschlösung entfernen. Das ähnlich aufgebaute TAED (Tetraacetylethylenediamin) ist im Gegensatz zu EDTA ein Ethansäureamid, welches mit sehr leicht zu Peressigsäure hydrolisiert und die Freisetzung von kontrolliert beschleunigt, so dass die Waschtemperatur ohne Verzicht auf Bleichwirkung herabgesetzt werden kann. Weißtöner. Wiederholt gewaschene Wäsche erhält mit der Zeit einen Gelbstich. Gelbliches Weiß wird jedoch als Schmutz empfunden. Weißtöner, wie das rechts abgebildete Blankophor sind Fluoreszenzfarbstoffe, die die UV-Strahlung, die zu etwa 4 % im Tageslicht enthalten ist, absorbieren und als sichtbares" blaues Licht wieder abstrahlen. Das emittierte, blaue Licht kompensiert den Gelbstich der Wäsche zu weiß Enzyme (Proteasen) dienen zur Auflösung eiweißhaltiger Flecken aus Kakao, Blut oder Milch. Stellmittel wie Natriumsulfat Na S 4 oder Natriumsilikat Na 4 Si 4 dienen als Trockenmittel, um die ieselfähigkeit und Dosierbarkeit des Waschpulvers zu verbessern. Soda Na 3 sorgt für einen leicht basischen p der Waschlauge, um die Protonierung der anionischen Tenside zu verhindern. Übungen: Aufgaben zu Fetten und Seifen Aufgabe 13 9
CoA H C 6 H C 10. Die Trivialnamen der fett geschriebenen Carbonsäuren sollten Sie kennen.
 Vorlesung 42 Fette und Öle sind mit Glycerin veresterte arbonsäuren. Sie sind die energiereichsten Nahrungsmittel und bilden die Energiereserve des tierischen und pflanzlichen rganismus. 2 R R 2 R 1 2
Vorlesung 42 Fette und Öle sind mit Glycerin veresterte arbonsäuren. Sie sind die energiereichsten Nahrungsmittel und bilden die Energiereserve des tierischen und pflanzlichen rganismus. 2 R R 2 R 1 2
Versuch: Seifenherstellung aus Kokosfett
 Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
Welche Aufgaben haben Fette im Körper?
 Einleitung Welche Aufgaben haben Fette im Körper? 1 Fette... Einleitung Welche Aufgaben haben Fette im Körper? 2 Fette... sind wichtige Energielieferanten (38-39 kj/g) Einleitung Welche Aufgaben haben
Einleitung Welche Aufgaben haben Fette im Körper? 1 Fette... Einleitung Welche Aufgaben haben Fette im Körper? 2 Fette... sind wichtige Energielieferanten (38-39 kj/g) Einleitung Welche Aufgaben haben
Fachdidaktik Chemie ETH Waschmittel S. 1
 Fachdidaktik Chemie ETH Waschmittel S. 1 Waschmittel Weshalb lohnt es sich im Chemie-Unterricht über Waschmittel zu sprechen? Die Wirkung von Seite lässt sich auf die Struktur zurückführen Es lassen sich
Fachdidaktik Chemie ETH Waschmittel S. 1 Waschmittel Weshalb lohnt es sich im Chemie-Unterricht über Waschmittel zu sprechen? Die Wirkung von Seite lässt sich auf die Struktur zurückführen Es lassen sich
Kohlenhydrate, Proteine, Fette und Öle
 Kohlenhydrate, Proteine, Fette und Öle Kohlenhydrate: albacetale oder Acetale von Aldehyden und Ketonen Proteine: arbonsäureamide Fette, Öle: arbonsäureester N Fette und Öle die Triester des Glycerins
Kohlenhydrate, Proteine, Fette und Öle Kohlenhydrate: albacetale oder Acetale von Aldehyden und Ketonen Proteine: arbonsäureamide Fette, Öle: arbonsäureester N Fette und Öle die Triester des Glycerins
Lernzirkel WAS Station 1 Herstellung von Seife aus Kokosfett
 Station 1 Herstellung von Seife aus Kokosfett Zeitbedarf: 35 min. Durchführung 10 g Kokosfett und 5 ml destilliertes Wasser werden langsam in einem Becherglas erhitzt. Unter Rühren werden 10 ml Natronlauge
Station 1 Herstellung von Seife aus Kokosfett Zeitbedarf: 35 min. Durchführung 10 g Kokosfett und 5 ml destilliertes Wasser werden langsam in einem Becherglas erhitzt. Unter Rühren werden 10 ml Natronlauge
Fette und fettähnliche Substanzen
 Fette und fettähnliche Substanzen Fette und fettähnliche Substanzen (letztere wurden früher als Lipoide bezeichnet) bilden die Gruppe der Lipide. Sie sind unlöslich in Wasser, aber gut löslich in organischen
Fette und fettähnliche Substanzen Fette und fettähnliche Substanzen (letztere wurden früher als Lipoide bezeichnet) bilden die Gruppe der Lipide. Sie sind unlöslich in Wasser, aber gut löslich in organischen
Versuch: Emulgierende und dispergierende Wirkung von Tensiden
 Philipps-Universität Marburg 18.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Emulgierende
Philipps-Universität Marburg 18.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Emulgierende
c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
 Carbonsäuren schriftliche Ausarbeitungen zu folgenden Themen: a) Eigenschaften von organischen Säuren b) Begriff der homologen Reihe der Carbonsäuren c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
Carbonsäuren schriftliche Ausarbeitungen zu folgenden Themen: a) Eigenschaften von organischen Säuren b) Begriff der homologen Reihe der Carbonsäuren c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
Waschmittel. Cl - CH 3
 Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvorträge im Sommersemester 2011 08.06.2011 Betreuung: Dr. M. Andratschke Referentinnen: Susanne Gumminger
Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvorträge im Sommersemester 2011 08.06.2011 Betreuung: Dr. M. Andratschke Referentinnen: Susanne Gumminger
Versuchsprotokoll. Nachweis von Tensiden in Kernseife, Spülmittel und Waschmittel
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 5.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Nachweis von Tensiden in
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 5.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Nachweis von Tensiden in
Aromaten, Fette und Tenside Seminar zu chem2010 Stephan Bernt
 , Fette und Tenside 12.05.2010 Seminar zu chem2010 Stephan Bernt Kriterien für Aromatizität: cyclisch planar vollständig konjugiertes π-elektronensystem Hückel-Regel: 4n+2 π-elektronen Prototyp des Aromaten:
, Fette und Tenside 12.05.2010 Seminar zu chem2010 Stephan Bernt Kriterien für Aromatizität: cyclisch planar vollständig konjugiertes π-elektronensystem Hückel-Regel: 4n+2 π-elektronen Prototyp des Aromaten:
Wachmittelchemie Und Zeolithen
 Wachmittelchemie Und Zeolithen Gliederung Geschichte Inhaltsstoffe eines Waschmittels Waschenzymen Tensiden Optische aufheller Bleichmittel Stabilisatoren Schaumregulatoren Wasserenthärter Zeolithen Quelle
Wachmittelchemie Und Zeolithen Gliederung Geschichte Inhaltsstoffe eines Waschmittels Waschenzymen Tensiden Optische aufheller Bleichmittel Stabilisatoren Schaumregulatoren Wasserenthärter Zeolithen Quelle
Alkohole Brüder des Wassers
 6. Alkohole Brüder des Wassers 6.1 Alkohole Brüder des Wassers entsteht aus Zucker durch die alkoholische Gärung. Dabei werden Glucosemoleküle mit ilfe von efezellen in und Kohlendioxid umgewandelt. NS29
6. Alkohole Brüder des Wassers 6.1 Alkohole Brüder des Wassers entsteht aus Zucker durch die alkoholische Gärung. Dabei werden Glucosemoleküle mit ilfe von efezellen in und Kohlendioxid umgewandelt. NS29
FETTE UND ÖLE. Allgemeines
 FETTE UND ÖLE Allgemeines Fette und Öle sind chemisch gesehen gemischte Fettsäureglycerinester. Alle drei OH-Gruppen des Glycerins sind dabei verestert, weshalb Fette auch als Triglyceride bezeichnet werden.
FETTE UND ÖLE Allgemeines Fette und Öle sind chemisch gesehen gemischte Fettsäureglycerinester. Alle drei OH-Gruppen des Glycerins sind dabei verestert, weshalb Fette auch als Triglyceride bezeichnet werden.
Gase sind in Wasser löslich Solche Lösungen können auch gesättigt sein
 4. TRENNEN UND MISCHEN ARBEITSBLATT 4.1 DIE LÖSLICHKEIT VON GASEN IN FLÜSSIGKEITEN Können sich Gase wie Festkörper in Flüssigkeiten lösen? Was lässt sich über die Löslichkeit von Kohlendioxid in Wasser
4. TRENNEN UND MISCHEN ARBEITSBLATT 4.1 DIE LÖSLICHKEIT VON GASEN IN FLÜSSIGKEITEN Können sich Gase wie Festkörper in Flüssigkeiten lösen? Was lässt sich über die Löslichkeit von Kohlendioxid in Wasser
Lebensmitteltechnologische Praktikum
 Lebensmitteltechnologische Praktikum Protokollabgabe: - persönlich - meckl@wzw.tum.de - adamski@wzw.tum.de Aufbau: Deckblatt (Name, e-mail-adresse) Einleitung (Hintergrund, Vorgehensweise) Ergebnisse (Messwert,
Lebensmitteltechnologische Praktikum Protokollabgabe: - persönlich - meckl@wzw.tum.de - adamski@wzw.tum.de Aufbau: Deckblatt (Name, e-mail-adresse) Einleitung (Hintergrund, Vorgehensweise) Ergebnisse (Messwert,
Grundlagen der Chemie Lösungen Prof. Annie Powell
 Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Einfache und kleine Versuche mit Lebensmitteln
 Cours central de chimie Biel-Bienne 2003 Zentralkurs Chemie Einfache und kleine Versuche mit Lebensmitteln Margarine, Kunsthonig und Caramel im Grundlagenunterricht. Dr. Daniel Hirschi Deutsches Gymnasium
Cours central de chimie Biel-Bienne 2003 Zentralkurs Chemie Einfache und kleine Versuche mit Lebensmitteln Margarine, Kunsthonig und Caramel im Grundlagenunterricht. Dr. Daniel Hirschi Deutsches Gymnasium
Zusammensetzung der Waschmittel
 Zusammensetzung der Waschmittel Als Waschmittel werden Gemische verschiedener Substanzen in flüssiger, gelartiger oder pulverförmiger Art bezeichnet, die zum Reinigen von Textilien verwendet werden. Sie
Zusammensetzung der Waschmittel Als Waschmittel werden Gemische verschiedener Substanzen in flüssiger, gelartiger oder pulverförmiger Art bezeichnet, die zum Reinigen von Textilien verwendet werden. Sie
Waschmittel auf Bäumen
 Datum:.11.015 Schüler: Daniel Tetla Schule: Gymnasium Friedrich Ebert Klasse: T1 Waschmittel auf Bäumen 1a. Versuch Herstellen einer Waschlauge aus Kastanien und Untersuchung ihrer Geräte: Material: Waage
Datum:.11.015 Schüler: Daniel Tetla Schule: Gymnasium Friedrich Ebert Klasse: T1 Waschmittel auf Bäumen 1a. Versuch Herstellen einer Waschlauge aus Kastanien und Untersuchung ihrer Geräte: Material: Waage
Schulversuchspraktikum. Mona-Christin Maaß. Sommersemester Klassenstufen 11 & 12. Tenside
 Schulversuchspraktikum Mona-Christin Maaß Sommersemester 2013 Klassenstufen 11 & 12 Tenside 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Es werden ein Lehrerversuch V1 und acht
Schulversuchspraktikum Mona-Christin Maaß Sommersemester 2013 Klassenstufen 11 & 12 Tenside 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Es werden ein Lehrerversuch V1 und acht
Carbonsäuren (Vollhardt, 3. Aufl., S. 893 ff, 4. Aufl., S. 967 ff; Hart, S. 345 ff; Buddrus, S. 501 ff)
 Vorlesung 39 arbonsäuren (Vollhardt, 3 Aufl, S 893 ff, 4 Aufl, S 967 ff; art, S 345 ff; Buddrus, S 501 ff) Die funktionelle Gruppe der arbonsäuren (= Fettsäuren) ist die arboxyl- (bzw arboxy-) Gruppe In
Vorlesung 39 arbonsäuren (Vollhardt, 3 Aufl, S 893 ff, 4 Aufl, S 967 ff; art, S 345 ff; Buddrus, S 501 ff) Die funktionelle Gruppe der arbonsäuren (= Fettsäuren) ist die arboxyl- (bzw arboxy-) Gruppe In
Chemie Alkohole, Aldehyde & Ketone, Carbonsäuren
 Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Handseife. Praktikumsbericht vom Labor SPF 4. Klasse. Erstellt von Fabian Wohlfender, 4Mc, und Benjamin Baumann, 4Md
 Handseife Praktikumsbericht vom 21.12.09 Labor SPF 4. Klasse Erstellt von Fabian Wohlfender, 4Mc, und Benjamin Baumann, 4Md 1 Einleitung Ziel dieses Praktikums ist es, selbständig eine Seife herzustellen.
Handseife Praktikumsbericht vom 21.12.09 Labor SPF 4. Klasse Erstellt von Fabian Wohlfender, 4Mc, und Benjamin Baumann, 4Md 1 Einleitung Ziel dieses Praktikums ist es, selbständig eine Seife herzustellen.
Welche Vorteile besitzt Margarine im Vergleich mit/zu Butter? Welche Zutaten findet man hauptsächlich in einer Margarine? Erstellt eine Zutatenliste.
 Emulsionsherstellung Chronologischer Überblick: Margarine ist ein industriell hergestelltes Streichfett. Margarine wurde zum ersten Mal in Frankreich im Jahr 1869 hergestellt. Butter war eine Rarität und
Emulsionsherstellung Chronologischer Überblick: Margarine ist ein industriell hergestelltes Streichfett. Margarine wurde zum ersten Mal in Frankreich im Jahr 1869 hergestellt. Butter war eine Rarität und
Wie funktionieren Waschmittel?
 Wie funktionieren Waschmittel? Das sind die wesentliche Bestandteile von Waschmitteln und so funktionieren sie. habelfrank - Pixabay.com Stand: 08.01.2018 Tenside Tenside sind der wichtigste Bestandteil
Wie funktionieren Waschmittel? Das sind die wesentliche Bestandteile von Waschmitteln und so funktionieren sie. habelfrank - Pixabay.com Stand: 08.01.2018 Tenside Tenside sind der wichtigste Bestandteil
Waschmittelinhaltsstoffe und ihre Funktion beim Waschprozess
 21 Waschmittelinhaltsstoffe und ihre Funktion beim Waschprozess Inhaltsstoffe Funktion Inhaltsstoffe Funktion Tenside Enthärter (Gerüststoffe) lösen den Schmutz von der Faser (Primärwaschwirkung) und verhindern
21 Waschmittelinhaltsstoffe und ihre Funktion beim Waschprozess Inhaltsstoffe Funktion Inhaltsstoffe Funktion Tenside Enthärter (Gerüststoffe) lösen den Schmutz von der Faser (Primärwaschwirkung) und verhindern
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Lösung der Beispielaufgaben IChO 2. Runde 2019 Säurederivate
 Lösung der Beispielaufgaben Ih 2. Runde 2019 Säurederivate Lösung Beispiel 1 ligocarbonsäuren a, b, c) A 464 Butandisäure Succinate B 444 (Z)-Butendisäure Maleate 424 Butindisäure D 444 (E)-Butendisäure
Lösung der Beispielaufgaben Ih 2. Runde 2019 Säurederivate Lösung Beispiel 1 ligocarbonsäuren a, b, c) A 464 Butandisäure Succinate B 444 (Z)-Butendisäure Maleate 424 Butindisäure D 444 (E)-Butendisäure
Waschmittel. - Erklärung: Durch Spül-/ Waschmittel wird die Grenz- bzw. Oberflächenspannung herabgesetzt.
 Universität Regensburg Institut für Anorganische Chemie: Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvorträge in anorganischer Chemie im Wintersemester 2007/2008 23.11.2007 Betreuung: Dr. M. Andratschke
Universität Regensburg Institut für Anorganische Chemie: Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvorträge in anorganischer Chemie im Wintersemester 2007/2008 23.11.2007 Betreuung: Dr. M. Andratschke
Chemie ist eine naturwissenschaftliche Disziplin, welche sich mit den Stoffen, den Stoffeigenschaften und den Stoffumwandlungen beschäftigt.
 1 Definition: Chemie ist eine naturwissenschaftliche Disziplin, welche sich mit den Stoffen, den Stoffeigenschaften und den Stoffumwandlungen beschäftigt. 2 Erscheinungsformen der Materie Homogen oder
1 Definition: Chemie ist eine naturwissenschaftliche Disziplin, welche sich mit den Stoffen, den Stoffeigenschaften und den Stoffumwandlungen beschäftigt. 2 Erscheinungsformen der Materie Homogen oder
Fette, Öle und Tenside
 Schulversuchspraktikum Thomas Polle Sommersemester 2015 Klassenstufen 11 & 12 Fette, Öle und Tenside Kurzprotokoll Inhalt Inhaltsverzeichnis 1Weitere Lehrerversuche... 3 V1 Verseifungszahl... 3 2Weitere
Schulversuchspraktikum Thomas Polle Sommersemester 2015 Klassenstufen 11 & 12 Fette, Öle und Tenside Kurzprotokoll Inhalt Inhaltsverzeichnis 1Weitere Lehrerversuche... 3 V1 Verseifungszahl... 3 2Weitere
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Versuchsprotokoll. Untersuchung der Waschwirkung
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 17.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Untersuchung der Waschwirkung
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 17.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Untersuchung der Waschwirkung
Fette und Seifen. Die Fettsäuren können
 Fette und Seifen 1. Zur Einführung Fette und Öle sind Stoffe, die aus einem oder mehreren Triglyceriden bestehen. Triglyceride sind Verbindungen (Ester) aus langkettigen Carbonsäuren und Glycerin, ein
Fette und Seifen 1. Zur Einführung Fette und Öle sind Stoffe, die aus einem oder mehreren Triglyceriden bestehen. Triglyceride sind Verbindungen (Ester) aus langkettigen Carbonsäuren und Glycerin, ein
Organische Chemie 10C1. Funktionelle Gruppen 10C2. Homologe Reihe der Alkane 10C3. Nomenklatur der Alkane (gesättigte Kohlenwasserstoffe) 10C4
 Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Reak%onen an der Carbonylgruppe
 Reak%onen an der Carbonylgruppe H. Wünsch 2013 1.1 Struktur der Carbonylgruppe Die Carbonylgruppe entsteht bei der OxidaBon primärer und sekundärer Alkohole. Kohlenstoff und Sauerstoff sind doppelt gebunden,
Reak%onen an der Carbonylgruppe H. Wünsch 2013 1.1 Struktur der Carbonylgruppe Die Carbonylgruppe entsteht bei der OxidaBon primärer und sekundärer Alkohole. Kohlenstoff und Sauerstoff sind doppelt gebunden,
Die Biochemie der Fette und deren Bedarfsempfehlungen für den Menschen
 Autor: Dr. Ulrike Jambor de Sousa Klinik, Institut: Titel: Die Biochemie der Fette und deren Bedarfsempfehlungen für den Menschen Inhaltsverzeichnis Einleitung Triglyceride Fett-Verdauung Lipoproteine
Autor: Dr. Ulrike Jambor de Sousa Klinik, Institut: Titel: Die Biochemie der Fette und deren Bedarfsempfehlungen für den Menschen Inhaltsverzeichnis Einleitung Triglyceride Fett-Verdauung Lipoproteine
CHEMIEPRAKTIKUM SPF/EGF KANTONSSCHULE BADEN. Einleitung
 EMIEPRAKTIKUM SPF/EGF KATSSULE BADE erstellung von Indigo, Färbevorgang Einleitung Indigo ist einer der ältesten und wichtigsten aturfarbstoffe, mit dem schon vor Jahrtausenden in der ganzen Welt - in
EMIEPRAKTIKUM SPF/EGF KATSSULE BADE erstellung von Indigo, Färbevorgang Einleitung Indigo ist einer der ältesten und wichtigsten aturfarbstoffe, mit dem schon vor Jahrtausenden in der ganzen Welt - in
Seifen und Waschmittel
 Lernwerkstatt Schülerlabor Chemie Experimentiermappe zum Thema Seifen und Waschmittel Friedrich-Schiller-Universität Jena Arbeitsgruppe Chemiedidaktik August-Bebel-Straße 6-8 07743 Jena Fonds der Chemischen
Lernwerkstatt Schülerlabor Chemie Experimentiermappe zum Thema Seifen und Waschmittel Friedrich-Schiller-Universität Jena Arbeitsgruppe Chemiedidaktik August-Bebel-Straße 6-8 07743 Jena Fonds der Chemischen
3.1 Waschmittelinhaltsstoffe und ihre Funktion beim Waschprozess
 3.1 Waschmittelinhaltsstoffe und ihre Funktion beim Waschprozess Inhaltsstoffe Funktion Inhaltsstoffe Funktion Tenside Enthärter (Gerüststoffe) Bleichmittel lösen den Schmutz von der Faser (Primärwaschwirkung)
3.1 Waschmittelinhaltsstoffe und ihre Funktion beim Waschprozess Inhaltsstoffe Funktion Inhaltsstoffe Funktion Tenside Enthärter (Gerüststoffe) Bleichmittel lösen den Schmutz von der Faser (Primärwaschwirkung)
Versuchsprotokoll. Herstellung von Seife
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. eiß WS 08/09 5.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Herstellung von Seife Gruppe
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. eiß WS 08/09 5.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Herstellung von Seife Gruppe
Beispielaufgaben IChO 2. Runde 2019 Säurederivate. H2, Pd/C
 Beispielaufgaben Ih 2. Runde 2019 Säurederivate Beispiel 1 ligocarbonsäuren Gegeben sei folgendes Reaktionsschema: A H2, Pd/ H 2, Lindlar Na/NH 3(l) B D Base E A hat eine molare Masse von 118,09 g mol
Beispielaufgaben Ih 2. Runde 2019 Säurederivate Beispiel 1 ligocarbonsäuren Gegeben sei folgendes Reaktionsschema: A H2, Pd/ H 2, Lindlar Na/NH 3(l) B D Base E A hat eine molare Masse von 118,09 g mol
1. Sie wissen, wie sich die Seifenherstellung im Laufe der Jahrhunderte verändert hat.
 Seifen Übersicht Zitat von Justus von Liebig (1803-1873): "Die Seife ist ein Massstab für den Wohlstand und die Kultur der Staaten. Es ist gewiss, dass man bei der Vergleichung zweier Staaten bei gleicher
Seifen Übersicht Zitat von Justus von Liebig (1803-1873): "Die Seife ist ein Massstab für den Wohlstand und die Kultur der Staaten. Es ist gewiss, dass man bei der Vergleichung zweier Staaten bei gleicher
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
GERADE RICHTIG WASCHEN
 Material: GERADE RICHTIG WASCHEN Moderne Waschmaschinen und Waschmittel erleichtern den Reinigungsprozess unserer Wäsche. In der vorliegenden Unterrichtseinheit erfahren SchülerInnen mehr über die chemischen
Material: GERADE RICHTIG WASCHEN Moderne Waschmaschinen und Waschmittel erleichtern den Reinigungsprozess unserer Wäsche. In der vorliegenden Unterrichtseinheit erfahren SchülerInnen mehr über die chemischen
Eigenschaften von Tensidlösungen
 V17 Eigenschaften von Tensidlösungen Fach Klasse Überthema Feinthema Zeit Chemie Q4 Grenzflächenaktive Substanzen Eigenschaften von Tenisden 30 Minuten Zusammenfassung Bei dem Versuch werden die Eigenschaften
V17 Eigenschaften von Tensidlösungen Fach Klasse Überthema Feinthema Zeit Chemie Q4 Grenzflächenaktive Substanzen Eigenschaften von Tenisden 30 Minuten Zusammenfassung Bei dem Versuch werden die Eigenschaften
Putz- und Waschmittel
 Putz- und Waschmittel Principles Dietmar Pflumm: KSR/MSE April 2008 Putz-/Waschmittel Definition Die Aufgabe von Putz- und Waschmitteln ist die Reinigung und Pflege diverser Gegenstände in Haushalt, Betrieb
Putz- und Waschmittel Principles Dietmar Pflumm: KSR/MSE April 2008 Putz-/Waschmittel Definition Die Aufgabe von Putz- und Waschmitteln ist die Reinigung und Pflege diverser Gegenstände in Haushalt, Betrieb
Wozu werden Emulgatoren bei der Herstellung von Lebensmitteln verwendet?
 Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P788700) 8.6 Emulgatoren Experiment von: Anouch Gedruckt: 28.02.204 :8:54 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe Wozu
Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P788700) 8.6 Emulgatoren Experiment von: Anouch Gedruckt: 28.02.204 :8:54 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe Wozu
Organische Chemie für Mediziner WS 2016/2017. Übungsblatt 3: Ausgewählte Substanzklassen
 1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
Die Zelle. Membranen: Struktur und Funktion
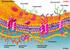 Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
28 Lipide Überblick über die Lipid-Gruppe
 28 Lipide 28.1 Überblick über die Lipid-Gruppe Die Ester langkettiger, meist unverzweigter Carbonsäuren wie Fette, Wachse u.a. werden unter dem Begriff Lipide zusammengefasst. Manchmal rechnet man auch
28 Lipide 28.1 Überblick über die Lipid-Gruppe Die Ester langkettiger, meist unverzweigter Carbonsäuren wie Fette, Wachse u.a. werden unter dem Begriff Lipide zusammengefasst. Manchmal rechnet man auch
Elektrophile Additionen von HX an die CC-Doppelbindung (Vollhardt, 3. Aufl., S , 4. Aufl., S ; Hart, S ; Buddrus, S.
 Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
2.3 Herstellung von Seife. Aufgabe. Wie lässt sich aus Fett Seife herstellen? Naturwissenschaften - Chemie - Lebensmittelchemie - 2 Fette
 Naturwissenschaften - Chemie - Lebensmittelchemie - 2 Fette (P785500) 2.3 Herstellung von Seife Experiment von: Anouch Gedruckt: 28.02.204 0:50:52 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Lebensmittelchemie - 2 Fette (P785500) 2.3 Herstellung von Seife Experiment von: Anouch Gedruckt: 28.02.204 0:50:52 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Totipotent: Pluripotent:
 E BIO 1 KW 39 Totipotent: Pluripotent: Zellorganellen Stadtzeitung Lübeck (Ausgabe vom 13. Januar 2003) Salzstreuen verboten - Bereich warnt vor Umweltschäden Streusalz als Auftaumittel zu nehmen, ist
E BIO 1 KW 39 Totipotent: Pluripotent: Zellorganellen Stadtzeitung Lübeck (Ausgabe vom 13. Januar 2003) Salzstreuen verboten - Bereich warnt vor Umweltschäden Streusalz als Auftaumittel zu nehmen, ist
Kl.10 LB2. Kl.10 LB2. Kl.10 LB2. Kl.10 LB2. Nenne 2 Vorkommen von Fetten.
 Nenne 2 Vorkommen von Fetten. Es gibt pflanzliche Fette (Kokosöl, livenöl) und tierische Fette (Schweinefett, Milchfett). Beschreibe die Löslichkeit der Fette. Fette sind nicht in Wasser aber in Benzin
Nenne 2 Vorkommen von Fetten. Es gibt pflanzliche Fette (Kokosöl, livenöl) und tierische Fette (Schweinefett, Milchfett). Beschreibe die Löslichkeit der Fette. Fette sind nicht in Wasser aber in Benzin
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Welcher Indikator ist für die Titration von Essigsäure (pks =4.76) mit Natronlauge am besten geeignet?
 1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist falsch? A) Säuren erhöhen durch Abgabe eines Protons an Wasser die H3O + -Konzentration einer Lösung. B)
1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist falsch? A) Säuren erhöhen durch Abgabe eines Protons an Wasser die H3O + -Konzentration einer Lösung. B)
Eigenschaften von Alkanolen (Alkohole) und deren Erklärung aus der Struktur
 Versuchsanweisung: Eigenschaften von Alkoholen, die ydroxylgruppe als funktionelle Gruppe Eigenschaften von Alkanolen (Alkohole) und deren Erklärung aus der Struktur Organische Substanzen bestehen zum
Versuchsanweisung: Eigenschaften von Alkoholen, die ydroxylgruppe als funktionelle Gruppe Eigenschaften von Alkanolen (Alkohole) und deren Erklärung aus der Struktur Organische Substanzen bestehen zum
FETTREICHE NAHRUNGSMITTEL
 7 FETTREICHE NAHRUNGSMITTEL Fettreiche Nahrungsmittel können sowohl.. als auch.. Ursprung sein. Durch die Verarbeitung der Rohprodukte kann sich der Fettanteil.. Wir unterscheiden pflanzliche und tierische
7 FETTREICHE NAHRUNGSMITTEL Fettreiche Nahrungsmittel können sowohl.. als auch.. Ursprung sein. Durch die Verarbeitung der Rohprodukte kann sich der Fettanteil.. Wir unterscheiden pflanzliche und tierische
1.9. Zwischenmolekulare Kräfte
 1.9. Zwischenmolekulare Kräfte 1.9.1. Schmelzen und Verdampfen von Stoffen fester Zustand geordnetes Kristallgitter Teilchen schwingen um Ruhelage flüssiger Zustand Teilchen sind im Tropfen frei beweglich
1.9. Zwischenmolekulare Kräfte 1.9.1. Schmelzen und Verdampfen von Stoffen fester Zustand geordnetes Kristallgitter Teilchen schwingen um Ruhelage flüssiger Zustand Teilchen sind im Tropfen frei beweglich
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Sarah Henkel Name: Johannes Hergt Datum: 9.12.2010 Gruppe 8: Ester, Fette, Seifen und
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Sarah Henkel Name: Johannes Hergt Datum: 9.12.2010 Gruppe 8: Ester, Fette, Seifen und
13.1. Struktur der Carbonyl-Gruppe, Prinzipielle Reaktivität
 13. arbonyl -Verbindungen 13.1. Struktur der arbonyl-gruppe, Prinzipielle Reaktivität 13.2. Aldehyde & Ketone 13.2.1 Nomenklatur 13.2.2 Darstellungen xidationen 13.2.3 Reaktionen Additionen an der = Acetale
13. arbonyl -Verbindungen 13.1. Struktur der arbonyl-gruppe, Prinzipielle Reaktivität 13.2. Aldehyde & Ketone 13.2.1 Nomenklatur 13.2.2 Darstellungen xidationen 13.2.3 Reaktionen Additionen an der = Acetale
Funktionelle Gruppen Alkohol
 Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Struktur und Chemie von Fetten
 Struktur und Chemie von Fetten Definition Lipide oder Rohfett = Lebensmittelbestandteile, die nicht in Wasser, sondern nur in organischen Lösungsmitteln löslich sind Beinhalten Triglyceride, Phosphatide,
Struktur und Chemie von Fetten Definition Lipide oder Rohfett = Lebensmittelbestandteile, die nicht in Wasser, sondern nur in organischen Lösungsmitteln löslich sind Beinhalten Triglyceride, Phosphatide,
A) Bei zweiprotonigen Säuren wird zur vollständigen Neutralisation exakt ein
 1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist richtig? A) Bei zweiprotonigen Säuren wird zur vollständigen Neutralisation exakt ein Äquivalent an Natronlauge
1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist richtig? A) Bei zweiprotonigen Säuren wird zur vollständigen Neutralisation exakt ein Äquivalent an Natronlauge
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt: Organische Chemie II. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Stoffklasse Alkane Alkene/Alkine Aromaten
 Stoffklasse Alkane Alkene/Alkine Aromaten funktionelle Gruppe Bezeichnung Einfachbindung Doppel-/Dreifachbindung aromatisches System Präfix Alkyl- Alkenyl/Alkinyl- Phenyl- Suffix -alkan -en/-in -Benzol
Stoffklasse Alkane Alkene/Alkine Aromaten funktionelle Gruppe Bezeichnung Einfachbindung Doppel-/Dreifachbindung aromatisches System Präfix Alkyl- Alkenyl/Alkinyl- Phenyl- Suffix -alkan -en/-in -Benzol
Detergenzien [BAD_1093101.DOC]
![Detergenzien [BAD_1093101.DOC] Detergenzien [BAD_1093101.DOC]](/thumbs/25/6804836.jpg) Detergenzien [BAD_1093101.DOC] Die Funktion der Tenside lässt sich durch ihren molekularen Aufbau erklären. Tenside bestehen allgemein aus einem hydrophoben ( wasserabweisenden ) Kohlenwasserstoffrest
Detergenzien [BAD_1093101.DOC] Die Funktion der Tenside lässt sich durch ihren molekularen Aufbau erklären. Tenside bestehen allgemein aus einem hydrophoben ( wasserabweisenden ) Kohlenwasserstoffrest
Waschmittel. 1. Historisches
 Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Sommersemester 2009 27.05.2009 Gruppenversuche in Anorganischer Chemie mit Demonstrationen Betreuung: Dr. M. Andratschke
Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Sommersemester 2009 27.05.2009 Gruppenversuche in Anorganischer Chemie mit Demonstrationen Betreuung: Dr. M. Andratschke
Trennverfahren (c) by Gerald Trutschl
 Trennverfahren (c) by Gerald Trutschl Inhalt Einteilung der Materie Homogene vs. Heterogene Gemische Trennverfahren Materie Materie by GT Gemische Reinstoffe heterogene Elemente homogene Verbindungen Gemische
Trennverfahren (c) by Gerald Trutschl Inhalt Einteilung der Materie Homogene vs. Heterogene Gemische Trennverfahren Materie Materie by GT Gemische Reinstoffe heterogene Elemente homogene Verbindungen Gemische
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
Anorganische Chemie! der unbelebten Natur keine Kohlenstoffverbindung (Kohlenstoffatome C) Metall Nichtmetallverbindungen Ionenbindung
 3 Chemie / Physik 3.1 Eigenheiten der Chemie und Physik Chemie ist die Lehre von den Stoffen, ihrer Zusammensetzung, dem Aufbau, der Struktur und ihrer Umwandlung Die Chemie untersucht und beschreibt die
3 Chemie / Physik 3.1 Eigenheiten der Chemie und Physik Chemie ist die Lehre von den Stoffen, ihrer Zusammensetzung, dem Aufbau, der Struktur und ihrer Umwandlung Die Chemie untersucht und beschreibt die
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
STUDIENBÜCHER CHEMIE. Lipide und Tenside. Lore Fischer-Blunk. Ein Praktikum
 STUDIENBÜCHER CHEMIE 2008 AGI-Information Management Consultants May be used for personal purporses only or by libraries associated to dandelon.com network. Lore Fischer-Blunk Lipide und Tenside Ein Praktikum
STUDIENBÜCHER CHEMIE 2008 AGI-Information Management Consultants May be used for personal purporses only or by libraries associated to dandelon.com network. Lore Fischer-Blunk Lipide und Tenside Ein Praktikum
Grundwissen Chemie 8. Klasse NTG
 Grundwissen Chemie 8. Klasse NTG Reinstoff hat gleich bleibende Eigenschaften (Stoffebene) besteht aus einer Sorte gleichartiger Teilchen z.b.: dest. Wasser, Kupfer, Gold, Salz 8.1 C NTG Element sind nicht
Grundwissen Chemie 8. Klasse NTG Reinstoff hat gleich bleibende Eigenschaften (Stoffebene) besteht aus einer Sorte gleichartiger Teilchen z.b.: dest. Wasser, Kupfer, Gold, Salz 8.1 C NTG Element sind nicht
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
Stoffgemisch. Reinstoff. Homogenes Gemisch. Heterogenes Gemisch. ( 8. Klasse NTG 1 / 48 ) ( 8. Klasse NTG 2 / 48 ) ( 8. Klasse NTG 3 / 48 )
 Stoffgemisch ( 8. Klasse NTG 1 / 48 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 8. Klasse
Stoffgemisch ( 8. Klasse NTG 1 / 48 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 8. Klasse
Philipps-Universität Marburg
 Philipps-Universität Marburg 4.12.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistent: Tobias Gerhardt Schulversuch (Gruppe 8/Verseifung): Verseifung
Philipps-Universität Marburg 4.12.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistent: Tobias Gerhardt Schulversuch (Gruppe 8/Verseifung): Verseifung
2. Übung Grundlagen der Hauptgruppenchemie AC02
 Allgemeine und Anorganische Chemie 2. Übung Grundlagen der Hauptgruppenchemie AC02 Aufgabe 1: Vervollständigen und gleichen Sie die folgenden Gleichungen aus: a) CaO + H 2 O Ca(OH) 2 b) Al 2 O 3 + 6 H
Allgemeine und Anorganische Chemie 2. Übung Grundlagen der Hauptgruppenchemie AC02 Aufgabe 1: Vervollständigen und gleichen Sie die folgenden Gleichungen aus: a) CaO + H 2 O Ca(OH) 2 b) Al 2 O 3 + 6 H
Becherglas mit Wasser, 4 Reagenzgläser, Thermometer, Brenner. Proben von Schweineschmalz, Butter, Kokosfett, Sonnenblumenöl
 Station 1: Schmelztemperatur der Fette Becherglas mit Wasser, 4 Reagenzgläser, Thermometer, Brenner Proben von Schweineschmalz, Butter, Kokosfett, Sonnenblumenöl Geben Sie Proben verschiedener Fette in
Station 1: Schmelztemperatur der Fette Becherglas mit Wasser, 4 Reagenzgläser, Thermometer, Brenner Proben von Schweineschmalz, Butter, Kokosfett, Sonnenblumenöl Geben Sie Proben verschiedener Fette in
DÜNGE- LEHRE Abendschule für Gartenbau 2003/2004
 DÜNGE- LERE Abendschule für Gartenbau 2003/2004 ELEMENTE die für Pflanzen wichtig sind Na Wasserstoff in Form von Wasser Natrium K Kalium für die Wiederstandsfähigkeit, Wasserhaushalt Mg Magnesium Zentralatom
DÜNGE- LERE Abendschule für Gartenbau 2003/2004 ELEMENTE die für Pflanzen wichtig sind Na Wasserstoff in Form von Wasser Natrium K Kalium für die Wiederstandsfähigkeit, Wasserhaushalt Mg Magnesium Zentralatom
Grundwissen Chemie Klasse
 Grundwissen Chemie 8. 10. Klasse Grundwissen Chemie 8I Chemie Reinstoff und Gemisch Atome und Moleküle Chemische Reaktionen Analyse und Synthese Katalysatoren Luft Sauerstoff und Wasserstoff Redoxreaktionen
Grundwissen Chemie 8. 10. Klasse Grundwissen Chemie 8I Chemie Reinstoff und Gemisch Atome und Moleküle Chemische Reaktionen Analyse und Synthese Katalysatoren Luft Sauerstoff und Wasserstoff Redoxreaktionen
Grundwissenkarten Hans-Carossa- Gymnasium
 Grundwissenkarten Hans-Carossa- Gymnasium 10. Klasse Chemie SG Es sind insgesamt 20 Karten für die 10. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundwissenkarten Hans-Carossa- Gymnasium 10. Klasse Chemie SG Es sind insgesamt 20 Karten für die 10. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
3. STOFFE MISCHEN UND TRENNEN
 CHEMIE / 4.0S Seite - 3.1-3. STOFFE MISCHEN UND TRENNEN 3.1. Herstellung von Gemischen: Die genaue Mischung von Farben, Kosmetika, Reinigungsmitteln u.s.w. sind wohlgehütete Betriebsgeheimnisse der Herstellerfirmen.
CHEMIE / 4.0S Seite - 3.1-3. STOFFE MISCHEN UND TRENNEN 3.1. Herstellung von Gemischen: Die genaue Mischung von Farben, Kosmetika, Reinigungsmitteln u.s.w. sind wohlgehütete Betriebsgeheimnisse der Herstellerfirmen.
Waschmittel und Waschvorgang
 Universität Regensburg Lehrstuhl für Anorganische Chemie Übungen im Vortragen mit Demonstrationen Sommersemester 2011 Dozentin: Dr. Andratschke Referentinnen: Bodenschatz, Katharina; Meier, Stefanie Datum:
Universität Regensburg Lehrstuhl für Anorganische Chemie Übungen im Vortragen mit Demonstrationen Sommersemester 2011 Dozentin: Dr. Andratschke Referentinnen: Bodenschatz, Katharina; Meier, Stefanie Datum:
SVEN-DAVID MÜLLER. Gesünder leben mit pflanzlichen Fetten und Ölen
 SVEN-DAVID MÜLLER Gesünder leben mit pflanzlichen Fetten und Ölen Was Sie über Fette wissen müssen Fette sind ein wichtiger Bestandteil unserer Nahrung, der Mensch braucht sie zum Überleben. Dennoch haben
SVEN-DAVID MÜLLER Gesünder leben mit pflanzlichen Fetten und Ölen Was Sie über Fette wissen müssen Fette sind ein wichtiger Bestandteil unserer Nahrung, der Mensch braucht sie zum Überleben. Dennoch haben
Waschmittel und Zeolithe. Eine Präsentation von Benedikt Daumann und Stefan Fischer
 Waschmittel und Zeolithe vs. Eine Präsentation von Benedikt Daumann und Stefan Fischer Inhaltsverzeichnis I II III Einführung / Geschichte Inhaltsstoffe eines Waschmittels Funktionsweise eines Waschmittels
Waschmittel und Zeolithe vs. Eine Präsentation von Benedikt Daumann und Stefan Fischer Inhaltsverzeichnis I II III Einführung / Geschichte Inhaltsstoffe eines Waschmittels Funktionsweise eines Waschmittels
Gruppe 8 eigener Versuch. Hydrolyse der Seife
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 23.06.09 SS 09 Gruppe 8 eigener Versuch ydrolyse der Seife Reaktion:
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 23.06.09 SS 09 Gruppe 8 eigener Versuch ydrolyse der Seife Reaktion:
Chemie 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter Wasser (= 1000g)?
 Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Der waschaktive Bestandteil eines Waschmittels: herabsetzten (lat. Tensio = Spannung). So kann eine bessere Benetzung
 Der waschaktive Bestandteil eines Waschmittels: Tenside Einleitung: Tenside sind Stoffe die, die Grenzflächenspannung im Wasser herabsetzten (lat. Tensio = Spannung). So kann eine bessere Benetzung realisiert
Der waschaktive Bestandteil eines Waschmittels: Tenside Einleitung: Tenside sind Stoffe die, die Grenzflächenspannung im Wasser herabsetzten (lat. Tensio = Spannung). So kann eine bessere Benetzung realisiert
Untersuche die Wirkung von Seife auf Trinkwasser und destilliertes Wasser.
 Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P755200) 3.8 Wasserhärte Experiment von: Seb Gedruckt: 24.03.204 :37:47 intertess (Version 3.2 B24,
Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P755200) 3.8 Wasserhärte Experiment von: Seb Gedruckt: 24.03.204 :37:47 intertess (Version 3.2 B24,
Saubere Sache! Ein Gruppenpuzzle zum Thema Seifen
 1 von 18 Saubere Sache! Ein Gruppenpuzzle zum Thema Seifen Ein Beitrag von Markus Tepner, Dortmund, und Insa Melle, Dortmund Mit Illustrationen von Dr. Wolfgang Zettlmeier, Barbing Wir benutzen sie jeden
1 von 18 Saubere Sache! Ein Gruppenpuzzle zum Thema Seifen Ein Beitrag von Markus Tepner, Dortmund, und Insa Melle, Dortmund Mit Illustrationen von Dr. Wolfgang Zettlmeier, Barbing Wir benutzen sie jeden
Name: Klasse: Datum:
 Arbeitsblatt 10.1 Versuch 1: Man füllt eine mittelgroße Glasschale mit Wasser und legt vorsichtig eine Büroklammer auf die Oberfläche des Wassers. Anschließend gibt man mit einer Pipette am Rand der Glasschale
Arbeitsblatt 10.1 Versuch 1: Man füllt eine mittelgroße Glasschale mit Wasser und legt vorsichtig eine Büroklammer auf die Oberfläche des Wassers. Anschließend gibt man mit einer Pipette am Rand der Glasschale
17. Biomoleküle : Lipide, Terpene, Steroide, Alkaloide
 Inhalt Index 17. Biomoleküle : Lipide, Terpene, Steroide, Alkaloide Eine grosse Anzahl von Naturstoffen ist wasserunlöslich oder wenig wasserlöslich, löst sich jedoch in Ether oder anderen unpolaren Lösungsmitteln.
Inhalt Index 17. Biomoleküle : Lipide, Terpene, Steroide, Alkaloide Eine grosse Anzahl von Naturstoffen ist wasserunlöslich oder wenig wasserlöslich, löst sich jedoch in Ether oder anderen unpolaren Lösungsmitteln.
Beispiele: Laurinsäure, Myristinsäure, Palmitinsäure, Stearinsäure. Funktion: Gesättigte Fettsäuren dienen dem Körper vorwiegend als Energiequelle.
 Zusatzinformationen Fette Gesättigte Fettsäuren Beispiele: Laurinsäure, Myristinsäure, Palmitinsäure, Stearinsäure. Funktion: Gesättigte Fettsäuren dienen dem Körper vorwiegend als Energiequelle. Empfehlungen
Zusatzinformationen Fette Gesättigte Fettsäuren Beispiele: Laurinsäure, Myristinsäure, Palmitinsäure, Stearinsäure. Funktion: Gesättigte Fettsäuren dienen dem Körper vorwiegend als Energiequelle. Empfehlungen
