Protonenstoffwechsel. Puffersysteme des Blutes und des Organismus. Puffersysteme des Blutes und des Organismus Bicarbonat-Puffer
|
|
|
- Ulrich Ritter
- vor 7 Jahren
- Abrufe
Transkript
1 Protonenstoffwechsel Puffersysteme des Blutes und des Organismus Die Summe aller im biologischen ph-bereich im Blut zur Aufnahme von H + befähigten Valenzen Anteil an Konzentration system % 50 pk a 6,1! Die biologische Wertigkeit eines Puffers hängt ab von: 1. seiner Konzentration 2. seiner Verteilung in den Körperflüssigkeiten 3. seiner Beziehung zu Eliminationsprozessen Nicht-systeme 50 Hb - / O 2 Hb - 8,25 / 6, ,8 Pufferbase Σ 48 mmol/l Puffersysteme des Blutes und des Organismus H 2 O + H 2 CO 3 H + + HCO 3 - Im Plasma werden 25,2 mmol/l Gesamtkohlensäure transportiert. Davon entfallen 1,2 mmol/l auf die freie Kohlensäure (= [H 2 CO 3 ] + [ ]) und 24 mmol/l auf das Bicarbonat. [HCO 3 - ] [H 2 CO 3 ] Puffersysteme des Blutes und des Organismus Gasaustausch und Zirkulation in der Lunge unter normalen Bedingungen
2 Puffersysteme des Blutes und des Organismus Puffersysteme des Blutes und des Organismus Im Plasma werden 25,2 mmol Gesamtkohlensäure (= [H 2 CO 3 ] + [ ]) transportiert. Davon entfallen 1,2 mmol/l auf die freie Kohlensäure und 24 mmol/l auf das Bicarbonat. [HCO 3 - ] [H 2 CO 3 ] Konzentrationsverhältnis von [HCO 3- ] und [ ] und daraus resultierendem ph bzw. Protonenkonzentration. Scheinbare Dissoziationskonstante der Kohlensäure [HCO - 3 ] S pco CO mmol/l [HCO 3 - ] p 24 ph = 6,1 + log = 7,4 1,2 40 mmhg : 20:1 oder 24 : 1,2 ph 7,4 Puffersysteme des Blutes und des Organismus Puffersysteme des Blutes und des Organismus Konzentrationsverhältnis von [HCO 3- ] und [ ] und daraus resultierender ph-wert bzw. Protonenkonzentration. + H 2 O H 2 CO 3 H + + HCO 3 - Alveole Blut Verhältnis HCO - 3 / 10:1 12,5:1 16:1 20:1 25:1 32:1 40:1 Resultierender ph-wert 7,1 7,2 7,3 7,4 7,5 7,6 7,7 [H + ] nmol/l physiol. Bedingungen ph = 6,1 + log = 7,4 1,2 d.h. es kann kein abgeatmet werden! Geschlossenes System: Zugabe von mM Milchsäure ph = 6,1 + log = 6,1 + log 1, ,2 = 7,12 Zur Erinnerung: [H + ]=10 -ph
3 Puffersysteme des Blutes und des Organismus + H 2 O H 2 CO 3 H + + HCO 3-24 physiol. Bedingungen ph = 6,1 + log = 7,4 1,2 Alveole Blut Geschlossenes System Offenes System Die Bedeutung der Konstanthaltung der -Konzentration für die Menge Base, die benötigt wird, um den ph-wert eines Bicarbonatpuffers von 7,4 auf 7,7 zu erhöhen. Links: Der ursprüngliche Zustand bei einem ph von 7,4. Geschlossenes System: Zugabe von mM Milchsäure ph = 6,1 + log = 6,1 + log = 7,12 1, ,2 Offenes System: Zugabe von 1mM Milchsäure d.h. es kann kein abgeatmet werden! d.h. kann über die Lunge abgeatmet werden! ph = 6,1 + log = 6,1 + log 1,2 1,2 = 7,38 Mitte: Die Änderung nach Zugabe von Base im abgeschlossenen System. Rechts: Die Änderung nach Zugabe von Base im offenen System. (Modifiziert nach Hills AG, Reid EL (1967) John Hopkins Med J 120: 368) Zusammenwirken der Blutpuffer Nicht- Kopplung der Eliminationswege für und H + aus nicht-flüchtigen Säuren Überwiegend im Plasma wirksam Säurekomponente gut eliminierbar, da im offenen System an Alveolarluft gekoppelt. Gesamtkonzentration des Systems sehr anpassungsfähig, da die Elimination der laufend entstehenden Komponente variiert werden kann. pk S mit 6,1 relativ ungünstig zum physiol. ph-wert gelegen. Überwiegend in Erythrozyten. Säurekomponenten praktisch nicht eliminierbar. Gesamtkonzentration des Systems nichtvariabel. pk S mit 6,8 bis etwa 8,25 günstig zum physiol. ph-wert gelegen. Puffergleichung: [HCO - 3 ] S CO2 p Puffergleichung: ph = pk s + log [NB-Puffer] [NB-Puffer-H]
4 Diagnostische Messgrößen des Säure-Basen Status Klinisch wird des Säure-Basen-Gleichgewicht im Blut zumindest durch drei Parameter charakterisiert: 1. Parameter für die freie Protonenkonzentration: ph-wert 2. Parameter für die respiratorische Komponente: p 3. Parameter für die metabolische Komponente einer der folgenden Größen Plasmabicarbonat HCO Standardbicarbonat, StHCO Basenabweichung, BE Diagnostische Meßgrößen des Säure-Basen Status - Basenabweichung- Die Basenabweichung (base excess; BE) ist definiert als Basenkonzentration des Vollbluts, gemessen durch Titration bis zum Endpunkt ph 7,40 bei einem pc0 2 von 40 mmhg (5,33 kpa) und 37 C. Bei BE = 0 besteht keine Abweichung vom physiol. Zustand. Bei einem Überschuß an nicht-flüchtiger Säure im Blut wird BE negativ und damit zu base deficit (= es fehlen Basenäquivalente). metabolischer Einfluß Sie liefert die direkte Aussage, wieviel mmol Base pro Liter Blut überschüssig oder zu wenig vorhanden sind. [HCO - 3 ] S CO2 p respiratorischer Einfluß Die Basenabweichung ist daher hervorragend geeignet für Dosisberechnungen bei therapeutischen Massnahmen. Diagnostische Meßgrößen des Säure-Basen Status - Referenzbereiche - ph < 7,36 ph > 7,45 Azidose Alkalose (Säurezunahme (H + ) oder Basenverlust (B - )) Basenzunahme (B - ) oder (Säureverlust (H + ) ) metabolisch respiratorisch respiratorisch metabolisch primär bedingt durch Veränderung des p durch nicht-respiratorische Ursachen ; primär normaler p p [mmol/l] = (0,0304 mmol L -1 mmhg -1 ) ( 40 mmhg) = 1,2 mmol/l
5 - respiratorische Azidose - Klinisch: Mangelnde Abatmung von stärkster zentraler Atemstimulus meist hervorgerufen durch eine alveoläre Hypoventilation Partialinsuffizienz: d.h. pco2 ph Globalinsuffizienz: d.h. p + po 2 ph Hyperkapnie und Hypoxämie Ursachen: ZNS-Störungen (Hirntumor, Enzephalitis, SHT, Narkotika, etc.) Muskelstörungen (Muskelrelaxantien, Operationstrauma, etc.) Traumata (Rippenserienfraktur, etc.) Atemwege (Fremdkörper, Asthma, Brochialstenosen, etc.) Lunge (Pneumonie, Lungenödem, Emphysem, etc.) - Hypoventilation - - respiratorische Azidose - HHG: [HCO - 3 ] S CO2 p Hypoventilation -> p > 40 mmhg [ ]= 78 mmhg 0,0304 mmol/l -1 mmhg -1 = 2,37 mmol/l 24 ph = 6,1 + log = 7,10 2,37 Respiratorische Azidose
6 - respiratorische Azidose - - respiratorische Azidose - (erhöht durch alveoläre Hypoventilation) Ausgleichsmechanismen H + werden von NBP abgefangen - respiratorische Azidose - - respiratorische Azidose - HHG: [HCO - 3 ] S CO2 p Hypoventilation -> p > 40 mmhg [ ]= 78 mmhg 0,0304 mmol/l -1 mmhg -1 = 2,37 mmol/l Ausgleichsmechanismen 24 ph = 6,1 + log = 7,10 2,37 Respiratorische Azidose (zusätzlich renale Mechanismen zur Erhöhung der H + -Ausscheidung über den Urin) H + werden von NBP abgefangen Fehlen renaler Kompensationsmechanismen -> ph -Anstieg erreicht sofort intrazellulären Raum (gute Diffusion des ) Ggf. alveoläre Hypoventilation -> Sauerstoffminderversorgung. Die akute resp. Azidose = lebensbedrohlicher Zustand Sofortige Maßnahmen erforderlich!
7 - respiratorische Alkalose - - respiratorische Alkalose - Klinisch: Erhöhte Abatmung von durchalveoläre Hyperventilation Hypokapnie: p ph alkalisch Ursachen: Direkte Reizung des Atemzentrums (z.b. Hyperventilation durch emotionale Ursachen, Enzephalitis, Meningitis,SHT, Aspirin- Intox., Bakt. Toxine, Schilddrüsenüberfunktion). Reflektorische Reizung des Atemzentrums (Lungenfibrose, Pneumonie, Hypoxie bei Höhenaufenthalt). Mechanische Überbeatmung. - respiratorische Alkalose - - respiratorische Alkalose -
8 - respiratorische Alkalose - Blutgasanalysator HHG: [HCO - 3 ] S CO2 p Hyperventilation -> p < 40 mmhg [ ]= 30 mmhg 0,0304 mmol/l -1 mmhg -1 = 0,91 mmol/l 24 ph = 6,1 + log = 7,52 0,91 Respiratorische Alkalose Die akute resp. Alkalose ist im Ggs. zur Azidose meist kein akut lebensbedrohlicher Zustand, zieht aber bei Nichtbeseitigung schwere Folgen nach sich. Hauptfolge: zerebralen Durchblutung Maßnahmen: Beseitigung des Grundgeschehens (z.b. Beruhigen, ggf. Pneumonie- Behandlung, ordnungsgemäße maschinelle Beatmung. Ggf. Rückatmung, um den p zu erhöhen. Typische Befundberichte der Blutgasanalyse
9
10
11 Gewebezelle Der Abtransport Gewebekapillare H 2 O ca. 45% als Na + HCO 3- im Plasma ca. 20% an Hb gebunden ca. 25% als K + HCO 3- im Ery. ca. 10% physikalisch gelöst O 2 Carbonanhydratase HHb H 2 CO 3 (20%) Hb H + HCO 3 (25%) O 2 Hb K + Cl (10%) HCO 3 Na + Cl (45%) Na + HCO 3
12 Die Abgabe pco 2 - Abatmung Alveole O 2 (10%) (45%) Na + HCO 3 Lungenkapillare Cl O 2 HHb HCO H + 3 Carbonanhydratase O 2 Hb +H 2 O Erythrozyt Die flüchtige Säure wird als Abfallprodukt des Stoffwechsels über die Lunge abgeatmet diffundiert von den Lungenkapillaren in die Alveolen und wird dann ausgeatmet Alveole p = 40 mmhg Kapillare p = 45 mmhg Der relativ langsame Spontanzerfall von Kohlensäure in Wasser und Kohlendioxyd wird durch die Carboanhydratase mit hoher Geschwindigkeit katalysiert. Die Kontaktzeit des Blutes mit den Lungenbläschen von ca. 1 Sekunde reicht aus, um das im Plasma als Bicarbonat transportierte wieder in und H 2 O umzusetzen und das Gleichgewicht der Partialdrücke der Blut-und der Alveolargase herzustellen. Säure-Basen Regulation Die Stellglieder für die Säure-Basen-Regulation sind die Ventilation der Lunge und die Bicarbonatrückresorption der Niere.
13 Enstehung Entsorgung von und H + Protonen Stoffwechsel als flüchtige Protonen in Form CO Extrazelluläres 2 H + Bett ph 7,4 ph 6,8 Säure nichtflüchtiger Säuren Blut u. ERZ + H 2 O H 2 CO 3 HCO H + + NBP- NBP - H Das Kohlensäure - Bikarbonat System Enzym Carbonanhydratase schnell und spontan Lunge H + Niere NBP = Eiweiß, Hämoglobin Oxihämoglobin Phosphatpuffer + H 2 O H 2 CO 3 H + + HCO mmol/24 h 60 mmol/24 h (NBP = Nichtbicarbonat Puffer neutralsiert Protonen durch Bindung an freie negative Ladungsstellen) Die Stoffwechselprodukte und H + werden getrennt über Lunge und Niere ausgeschieden. Beim Transport im Blut kommunizieren sie über die Puffersysteme wird ausgeatmet H 2 O bleibt zurück! Steuerung der HCO 3 Konzentration in der Niere Blut Nierenzelle Urin Die Regulation von HCO 3 vollzieht sich innerhalb von Stunden/Tagen
BIOCHEMIE I Teil 5 und 6
 Titrationskurve einer schwachen Säure mit einer starken Base. BIOCHEMIE I Teil 5 und 6 13 Äquivalenzpunkt Äquivalenzpunkt: Essigsäure vollständig dissoziiert. Bei zunehmender Menge an NaOH nähert sich
Titrationskurve einer schwachen Säure mit einer starken Base. BIOCHEMIE I Teil 5 und 6 13 Äquivalenzpunkt Äquivalenzpunkt: Essigsäure vollständig dissoziiert. Bei zunehmender Menge an NaOH nähert sich
Kapitel 2.2 Kardiopulmonale Homöostase. Kohlendioxid
 Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
BIOCHEMIE I. ure- Lernziele. Relevante Textbooks. für r Mediziner
 BIOCHEMIE I Institut für Klinische Chemie, Molekulare Diagnostik und Mitochondriale Genetik (M.F. Bauer) für r Mediziner Säure-Basen-Haushalt Relevante Textbooks Integrative Klinische Chemie und Laboratoriumsmedizin.
BIOCHEMIE I Institut für Klinische Chemie, Molekulare Diagnostik und Mitochondriale Genetik (M.F. Bauer) für r Mediziner Säure-Basen-Haushalt Relevante Textbooks Integrative Klinische Chemie und Laboratoriumsmedizin.
Das Säure-Basen- Gleichgewicht. Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung
 Das Säure-Basen- Gleichgewicht Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung BGA Blutgasanalyse Normalkost körpereigener Stoffwechsel Überschuss
Das Säure-Basen- Gleichgewicht Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung BGA Blutgasanalyse Normalkost körpereigener Stoffwechsel Überschuss
Das Säure-Basen- Gleichgewicht. Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung
 Das Säure-Basen- Gleichgewicht Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung BGA Blutgasanalyse Normalkost körpereigener Stoffwechsel Überschuss
Das Säure-Basen- Gleichgewicht Warum wichtig? Optimierung des/der: Metabolismus Eiweißtransport über Membranen hinweg Signalübertragung BGA Blutgasanalyse Normalkost körpereigener Stoffwechsel Überschuss
Die Blutgasanalyse Was ist außerklinisch tolerabel? KAI 2014 Dr. med. Günter Schrot
 Die Blutgasanalyse Was ist außerklinisch tolerabel? KAI 2014 Dr. med. Günter Schrot Normale Blutgasanalyse ph 7,36-7,44 po2 >80 mmhg pco2 35-45 mmhg HCO3-22 -26 mmol/l berechnet Das Säure-Basen-System
Die Blutgasanalyse Was ist außerklinisch tolerabel? KAI 2014 Dr. med. Günter Schrot Normale Blutgasanalyse ph 7,36-7,44 po2 >80 mmhg pco2 35-45 mmhg HCO3-22 -26 mmol/l berechnet Das Säure-Basen-System
ABGA. Notfallpflegekongress 2008 Solothurn. Notfallpflege am Stadtspital Triemli Zürich
 ABGA Notfallpflegekongress 2008 Solothurn H. Zahner,, Fachschule für f r Intensiv- und Notfallpflege am Stadtspital Triemli Zürich Werte des pulmonalen Gasaustausches PaO 2 Sauerstoffpartialdruck im arteriellen
ABGA Notfallpflegekongress 2008 Solothurn H. Zahner,, Fachschule für f r Intensiv- und Notfallpflege am Stadtspital Triemli Zürich Werte des pulmonalen Gasaustausches PaO 2 Sauerstoffpartialdruck im arteriellen
Elektrolythaushalt + Säure-Basen-Haushalt
 Elektrolythaushalt + Säure-Basen-Haushalt Überblick Elektrolythaushalt Natrium Kalium Calcium Magnesium Phosphat Säure-Basen-Haushalt Der Elektrolythaushalt Normwerte im Blut: Natrium 135-145 mmol/l Kalium
Elektrolythaushalt + Säure-Basen-Haushalt Überblick Elektrolythaushalt Natrium Kalium Calcium Magnesium Phosphat Säure-Basen-Haushalt Der Elektrolythaushalt Normwerte im Blut: Natrium 135-145 mmol/l Kalium
KliChi. Klinische Chemie & Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Analytik und Blutgasanalytik. Dr. med. Bernhard Schlüter - 1 -
 Sommersemester 2012-1 - Klinische Chemie & Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Analytik und Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium Universitätsklinikum
Sommersemester 2012-1 - Klinische Chemie & Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Analytik und Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium Universitätsklinikum
Ungefähre Zusammensetzung des Blutes und des Blutplasmas. Die häufigsten Bestandteile des Blutplasmas (Mittelwerte)
 Puffer /Zusammensetzung des Blutes 1 Zusammensetzung des Blutes Das Blut der Wirbeltiere besteht zu 55% aus flüssigem Blutplasma und zu 45% aus darin schwimmenden festen Bestandteilen, den Blutkörperchen.
Puffer /Zusammensetzung des Blutes 1 Zusammensetzung des Blutes Das Blut der Wirbeltiere besteht zu 55% aus flüssigem Blutplasma und zu 45% aus darin schwimmenden festen Bestandteilen, den Blutkörperchen.
Der ph-wert des Blutplasmas zeigt an, ob das Gleichgewicht zwischen +
 Diagnostik Säure-Basen-Status Unter dem Säure-Basen-Status versteht man die Summe derjenigen Messund Rechengrößen, die eine Diagnostik der Störungen des Säure-Basen- Haushaltes ermöglichen. Dazu gehören
Diagnostik Säure-Basen-Status Unter dem Säure-Basen-Status versteht man die Summe derjenigen Messund Rechengrößen, die eine Diagnostik der Störungen des Säure-Basen- Haushaltes ermöglichen. Dazu gehören
Gliederung. Puffersysteme. Wofür Puffersysteme? Wofür Puffersysteme? Wofür Puffersysteme? ph-verhältnisse im Körper. Puffersysteme
 Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Klinische Chemie und Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Haushalt und Blutgasanalytik
 Klinische Chemie und Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Haushalt und Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium Universitätsklinikum Münster
Klinische Chemie und Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Haushalt und Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium Universitätsklinikum Münster
Lungenfunktionstest. Die Spirometrie ("kleine Lungenfunktion", spirare (lat.): atmen) dient zur Messung des Lungen- bzw. Atemvolumens.
 Die Spirometrie ("kleine Lungenfunktion", spirare (lat.): atmen) dient zur Messung des Lungen- bzw. Atemvolumens. Beides sind wichtige Messgrößen, um Verlauf und Schwere von Lungenerkrankungen einzuschätzen.
Die Spirometrie ("kleine Lungenfunktion", spirare (lat.): atmen) dient zur Messung des Lungen- bzw. Atemvolumens. Beides sind wichtige Messgrößen, um Verlauf und Schwere von Lungenerkrankungen einzuschätzen.
Klinische Chemie und Hämatologie Vorlesung: Blutgasanalyse
 Klinische Chemie und Hämatologie Vorlesung: Blutgasanalyse Dr. med. Bernhard Schlüter Institut für Klinische Chemie und Laboratoriumsmedizin/Zentrallaboratorium Westfälische Wilhelms-Universität Münster
Klinische Chemie und Hämatologie Vorlesung: Blutgasanalyse Dr. med. Bernhard Schlüter Institut für Klinische Chemie und Laboratoriumsmedizin/Zentrallaboratorium Westfälische Wilhelms-Universität Münster
Elektrolythaushalt + Säure-Basen-Haushalt
 Elektrolythaushalt + Säure-Basen-Haushalt Überblick Elektrolythaushalt Natrium Kalium Calcium Magnesium Phosphat Säure-Basen-Haushalt Der Elektrolythaushalt Normwerte: Natrium 135-145 mmol/l Kalium 3.5-5.5
Elektrolythaushalt + Säure-Basen-Haushalt Überblick Elektrolythaushalt Natrium Kalium Calcium Magnesium Phosphat Säure-Basen-Haushalt Der Elektrolythaushalt Normwerte: Natrium 135-145 mmol/l Kalium 3.5-5.5
Säure-Basen- Haushalt
 Säure-Basen- Haushalt Folie Nr. 1 Grundlagen Normwerte Puffersysteme Störungen Grundlagen BGA Grundlagen: Ziel ist das Gleichgewicht zwischen sauren und alkalischen Substanzen Einheit des Säure-Basen-Gleichgewichts
Säure-Basen- Haushalt Folie Nr. 1 Grundlagen Normwerte Puffersysteme Störungen Grundlagen BGA Grundlagen: Ziel ist das Gleichgewicht zwischen sauren und alkalischen Substanzen Einheit des Säure-Basen-Gleichgewichts
Säure-Basen-Haushalt, Blutgase
 Säure-Basen-Haushalt, Blutgase Grundlagen Allgemeine Pathobiochemie Kohlendioxid CO 2, Kohlensäure H 2 CO 3 nichtflüchtige Säuren Puffersysteme renale Mechanismen Störungen und Kompensation Spezielle Pathobiochemie
Säure-Basen-Haushalt, Blutgase Grundlagen Allgemeine Pathobiochemie Kohlendioxid CO 2, Kohlensäure H 2 CO 3 nichtflüchtige Säuren Puffersysteme renale Mechanismen Störungen und Kompensation Spezielle Pathobiochemie
Grundlagen der Ernährungslehre
 Grundlagen der Ernährungslehre Wasser Elektrolyt Säuren-Basen Haushalt des Organismus Wasserhaushalt des Organismus Funktionen des Wassers im tierischen Organismus Bestandteil vieler zellulärer und subzellulärer
Grundlagen der Ernährungslehre Wasser Elektrolyt Säuren-Basen Haushalt des Organismus Wasserhaushalt des Organismus Funktionen des Wassers im tierischen Organismus Bestandteil vieler zellulärer und subzellulärer
Blutgasanalyse UNIVERSITÄT DES SAARLANDES. Probenahme, Parameter, usw. für MTAF-Schule. Jung R. 26. März 2015. Institut für Arbeitsmedizin der
 Probenahme, Parameter, usw. für MTAF-Schule Jung R. Institut für Arbeitsmedizin der UNIVERSITÄT DES SAARLANDES 26. März 2015 - ph - Werte Blutgasnormwerte Messung von ph-wert sowie den Partialdrücken po2
Probenahme, Parameter, usw. für MTAF-Schule Jung R. Institut für Arbeitsmedizin der UNIVERSITÄT DES SAARLANDES 26. März 2015 - ph - Werte Blutgasnormwerte Messung von ph-wert sowie den Partialdrücken po2
Atemgastransport im Blut
 Atemgastransport im Blut Institut für MTA-Ausbildung am Klinikum Osnabrück Fachgebiet Anatomie/Physiologie/Krankheitslehre - Dr. U. Krämer 1. Physikalische Löslichkeit der Atemgase Sauerstoff und Kohlendioxid
Atemgastransport im Blut Institut für MTA-Ausbildung am Klinikum Osnabrück Fachgebiet Anatomie/Physiologie/Krankheitslehre - Dr. U. Krämer 1. Physikalische Löslichkeit der Atemgase Sauerstoff und Kohlendioxid
Ein erhöhter PaCO 2 in Verbindung mit einem erniedrigten ph-wert ist das Kennzeichen einer akuten respiratorischen Azidose.
 Respiratorische Azidose Akute respiratorische Azidose Ein erhöhter PaCO 2 in Verbindung mit einem erniedrigten phwert ist das Kennzeichen einer akuten respiratorischen Azidose. Chronische respiratorische
Respiratorische Azidose Akute respiratorische Azidose Ein erhöhter PaCO 2 in Verbindung mit einem erniedrigten phwert ist das Kennzeichen einer akuten respiratorischen Azidose. Chronische respiratorische
Thema: Säure-Basen-Haushalt
 Säure-Basen-Haushalt Seite 1 Thema: Säure-Basen-Haushalt 1 Grundlagen Die ph-regulation des Körpers ist von grundlegender Bedeutung für seine Funktion. Der ph-wert ist ein Maß für die Wasserstoffionenkonzentration(Wasserstoffionen
Säure-Basen-Haushalt Seite 1 Thema: Säure-Basen-Haushalt 1 Grundlagen Die ph-regulation des Körpers ist von grundlegender Bedeutung für seine Funktion. Der ph-wert ist ein Maß für die Wasserstoffionenkonzentration(Wasserstoffionen
Proxima. pco 2 und berechnete Werte für HCO 3 und Basenüberschuss auf Proxima
 Funktionsprinzipien Der ProximaSensor wird als einzelner Multi ParameterChip hergestellt, der eine Reihe einzelner Sensoren beinhaltet, die jeweils einen anderen Parameter messen. Der pco 2 wird direktpotentiometrisch
Funktionsprinzipien Der ProximaSensor wird als einzelner Multi ParameterChip hergestellt, der eine Reihe einzelner Sensoren beinhaltet, die jeweils einen anderen Parameter messen. Der pco 2 wird direktpotentiometrisch
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Lungenkrankheiten und Funktionsdiagnostik
 Lungenkrankheiten und Funktionsdiagnostik Krankheitsbilder, Untersuchungsmethoden und Parameter für MTAF-Schule Jung R. Institut für Arbeitsmedizin der UNIVERSITÄT DES SAARLANDES 10. Oktober 2013 Schnittbild
Lungenkrankheiten und Funktionsdiagnostik Krankheitsbilder, Untersuchungsmethoden und Parameter für MTAF-Schule Jung R. Institut für Arbeitsmedizin der UNIVERSITÄT DES SAARLANDES 10. Oktober 2013 Schnittbild
Interpretation. Kapitel 4. Kasuistik 1 (1)
 Kapitel 4 Interpretation Kasuistik 1 (1) In der Notaufnahme werden Sie zu einem älteren Herrn gerufen, den seine Tochter gerade wegen Atemnot ins Krankenhaus gebracht hat. Anamnestisch ist ein chronischer
Kapitel 4 Interpretation Kasuistik 1 (1) In der Notaufnahme werden Sie zu einem älteren Herrn gerufen, den seine Tochter gerade wegen Atemnot ins Krankenhaus gebracht hat. Anamnestisch ist ein chronischer
Säure-Basen Haushalt Samuel Fuchs
 Säure-Basen Haushalt 21.06.2013 Samuel Fuchs Inhaltsverzeichnis HERKUNFT DER SÄUREN IM KÖRPER... 4 WAS SIND SÄUREN?... 4 WAS SIND BASEN?... 4 PH-WERT... 4 KOHLENDIOXID CO2... 5 DIE PUFFERSYSTEME... 5 WIRKUNGSZEIT...
Säure-Basen Haushalt 21.06.2013 Samuel Fuchs Inhaltsverzeichnis HERKUNFT DER SÄUREN IM KÖRPER... 4 WAS SIND SÄUREN?... 4 WAS SIND BASEN?... 4 PH-WERT... 4 KOHLENDIOXID CO2... 5 DIE PUFFERSYSTEME... 5 WIRKUNGSZEIT...
Kardiopulmonale Homöostase
 Kapitel 2 Kardiopulmonale Homöostase Primäre Funktion des Blutes im Rahmen der Atmung Transport von O 2 aus der Lunge zum peripheren Gewebe, CO 2 aus der Peripherie zu den Lungen, H + vom Gewebe zu den
Kapitel 2 Kardiopulmonale Homöostase Primäre Funktion des Blutes im Rahmen der Atmung Transport von O 2 aus der Lunge zum peripheren Gewebe, CO 2 aus der Peripherie zu den Lungen, H + vom Gewebe zu den
Willy Bauhuber KfH Nierenzentrum im Klinikum Rosenheim
 Willy Bauhuber KfH Nierenzentrum im Klinikum Rosenheim über 5500 Fundstellen bei GOOGLE meist Alternativmedizin Fehlernärung, Bewegungsmangel, Stress... führen zu schädlicher Übersäuerung Behandlung durch
Willy Bauhuber KfH Nierenzentrum im Klinikum Rosenheim über 5500 Fundstellen bei GOOGLE meist Alternativmedizin Fehlernärung, Bewegungsmangel, Stress... führen zu schädlicher Übersäuerung Behandlung durch
Thema: Säure-Basen-Haushalt
 Säure-Basen-Haushalt Seite 1 Thema: Säure-Basen-Haushalt 1 Grundlagen Die ph-regulation des Körpers ist von grundlegender Bedeutung für seine Funktion. Der ph-wert ist ein Maß für die Wasserstoffionenkonzentration(Wasserstoffionen
Säure-Basen-Haushalt Seite 1 Thema: Säure-Basen-Haushalt 1 Grundlagen Die ph-regulation des Körpers ist von grundlegender Bedeutung für seine Funktion. Der ph-wert ist ein Maß für die Wasserstoffionenkonzentration(Wasserstoffionen
BGA geschafft! Und jetzt?
 BGA geschafft! Und jetzt? Peter Krisper Medizinische Universitätsklinik Abt. f. Nephrologie & Hämodialyse Lernziele Sicheres Erkennen einfacher Störungen des Säure Basenhaushaltes an Hand einer Blutgasanalyse
BGA geschafft! Und jetzt? Peter Krisper Medizinische Universitätsklinik Abt. f. Nephrologie & Hämodialyse Lernziele Sicheres Erkennen einfacher Störungen des Säure Basenhaushaltes an Hand einer Blutgasanalyse
HA + B A - + HB + Säuren und Basen. Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor!
 Säuren und Basen Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor! Die Tendenz ein Proton abzuspalten (Säure) bzw. aufzunehmen (Base) bezeichnet man als Säure-
Säuren und Basen Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor! Die Tendenz ein Proton abzuspalten (Säure) bzw. aufzunehmen (Base) bezeichnet man als Säure-
Physiologie der Atmung. Cem Ekmekcioglu
 Physiologie der Atmung Cem Ekmekcioglu Übersicht über den Transportweg des Sauerstoffes beim Menschen Schmidt/Thews: Physiologie des Menschen, 27.Auflage, Kap.25, Springer (1997) Klinke, Pape, Silbernagl,
Physiologie der Atmung Cem Ekmekcioglu Übersicht über den Transportweg des Sauerstoffes beim Menschen Schmidt/Thews: Physiologie des Menschen, 27.Auflage, Kap.25, Springer (1997) Klinke, Pape, Silbernagl,
Störungen des Säure-Basen-Haushalts
 3 Störungen des Säure-Basen-Haushalts Normalerweise wird der extrazelluläre ph-wert durch verschiedene Puffersysteme und Kompensationsmechanismen innerhalb sehr enger Grenzen (Norm: 7,38 7,42) reguliert,
3 Störungen des Säure-Basen-Haushalts Normalerweise wird der extrazelluläre ph-wert durch verschiedene Puffersysteme und Kompensationsmechanismen innerhalb sehr enger Grenzen (Norm: 7,38 7,42) reguliert,
DIE KLINISCHE BIOCHEMIE DES SÄURE-BASEN HAUSHALTES
 DIE KLINISCHE BIOCHEMIE DES SÄURE-BASEN HAUSHALTES Der Kampf des Lebens gegen Hydrogenionen. Hydrogenion(H + )-Homeostase Unverzichtbar für das Leben: Mitochondriale Funktion Aufladen und Form der Proteine
DIE KLINISCHE BIOCHEMIE DES SÄURE-BASEN HAUSHALTES Der Kampf des Lebens gegen Hydrogenionen. Hydrogenion(H + )-Homeostase Unverzichtbar für das Leben: Mitochondriale Funktion Aufladen und Form der Proteine
Leitartikel Puffersysteme im Blut
 Zusammenfassung Ausgabe 30, Mai 2011 ISSN 2190-5118 Summary Hepatitis C Die Puffersysteme im Blut helfen dabei, den Säure-Basen-Haushalt aufrecht zu erhalten. Es geht um Azidose und Alkalose, aber. Welche
Zusammenfassung Ausgabe 30, Mai 2011 ISSN 2190-5118 Summary Hepatitis C Die Puffersysteme im Blut helfen dabei, den Säure-Basen-Haushalt aufrecht zu erhalten. Es geht um Azidose und Alkalose, aber. Welche
12 Säure-Basen-Haushalt
 12.1 Der ph-wert in Körperflüssigkeiten 281 Gotthold Gäbel Der ph-wert der extrazellulären Flüssigkeit wird in einem sehr engen Bereich zwischen 7,36 und 7,44 gehalten. Dies geschieht über Puffersysteme,
12.1 Der ph-wert in Körperflüssigkeiten 281 Gotthold Gäbel Der ph-wert der extrazellulären Flüssigkeit wird in einem sehr engen Bereich zwischen 7,36 und 7,44 gehalten. Dies geschieht über Puffersysteme,
Pneumologische Funktionsdiagnostik. 7. Blutgasanalyse
 Pneumologische Funktionsdiagnostik 7. Blutgasanalyse Inhalt 7.1 Allgemeines 7.2 Säure-Base-Haushalt 7.3 Puffer-Systeme 7.4 Metabolische Einflüsse auf die BGA 7.5 Parameter Atemfunktion 7.6 Respiratorische
Pneumologische Funktionsdiagnostik 7. Blutgasanalyse Inhalt 7.1 Allgemeines 7.2 Säure-Base-Haushalt 7.3 Puffer-Systeme 7.4 Metabolische Einflüsse auf die BGA 7.5 Parameter Atemfunktion 7.6 Respiratorische
Alveolo-arterielle Sauerstoffpartialdruckdifferenz, vereinfachte Berechnung
 A Druck A Alveolo-arterielle Sauerstoffpartialdruckdifferenz, vereinfachte Berechnung Synonyme nalveolo-arterielle Sauerstoffdruckdifferenz nalveolo-arterielle Sauerstoffdifferenz naad - (vereinfacht)
A Druck A Alveolo-arterielle Sauerstoffpartialdruckdifferenz, vereinfachte Berechnung Synonyme nalveolo-arterielle Sauerstoffdruckdifferenz nalveolo-arterielle Sauerstoffdifferenz naad - (vereinfacht)
Azidosen, Alkalosen. Störungen der Regulation des Säure-Basen-Haushalts führen zu Alkalosen oder Azidosen.
 Allgemeine Pathologie: Azidosen, Alkalosen Störungen der Regulation des Säure-Basen-Haushalts führen zu Alkalosen oder Azidosen. Sie beruhen im wesentlichen auf Erkrankungen oder Funktionsstörungen der
Allgemeine Pathologie: Azidosen, Alkalosen Störungen der Regulation des Säure-Basen-Haushalts führen zu Alkalosen oder Azidosen. Sie beruhen im wesentlichen auf Erkrankungen oder Funktionsstörungen der
INSTITUT FÜR PHYSIOLOGIE
 INSTITUT FÜR PHYSIOLOGIE Fallbeispiel 1 zum Physiologie Praktikum P 1. Pufferung und SäureBasen Analyse Fallbeispiel Praktikum Säuren/Basen Alle Daten stammen von einem/r Patienten/in der Bochumer Universitätskliniken
INSTITUT FÜR PHYSIOLOGIE Fallbeispiel 1 zum Physiologie Praktikum P 1. Pufferung und SäureBasen Analyse Fallbeispiel Praktikum Säuren/Basen Alle Daten stammen von einem/r Patienten/in der Bochumer Universitätskliniken
Was verstehen wir unter Säuren und Basen?
 Was verstehen wir unter Säuren und Basen? Säuren: Unter Säuren verstehen wir alle organischen und anorganischen Verbindungen, die in Lösungen Wasserstoffionen H + abgeben. Sie werden auch Protonen Donatoren
Was verstehen wir unter Säuren und Basen? Säuren: Unter Säuren verstehen wir alle organischen und anorganischen Verbindungen, die in Lösungen Wasserstoffionen H + abgeben. Sie werden auch Protonen Donatoren
Pflege bei Erkrankungen der Niere
 ?... 13 1. a) Nennen Sie die Ursachen, Symptome und Therapie bei Hyperhydratation. b) Unterscheiden Sie Hyperkaliämie und Hypokaliämie hinsichtlich Ursachen, Symptome und Therapie voneinander. ...! 1.
?... 13 1. a) Nennen Sie die Ursachen, Symptome und Therapie bei Hyperhydratation. b) Unterscheiden Sie Hyperkaliämie und Hypokaliämie hinsichtlich Ursachen, Symptome und Therapie voneinander. ...! 1.
Kurstag 3. Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers
 Kurstag 3 Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Kurstag 3 Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
CHEMIE KAPITEL 4 SÄURE-BASE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2013 / 2014
 CHEMIE KAPITEL 4 SÄURE-BASE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Aufgaben In einen Liter Wasser werden 2 g NH - 2 (starke Base) eingeleitet welchen ph-wert hat
CHEMIE KAPITEL 4 SÄURE-BASE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Aufgaben In einen Liter Wasser werden 2 g NH - 2 (starke Base) eingeleitet welchen ph-wert hat
Atmungsphysiologie II.
 Atmungsphysiologie II. 29. Gasaustausch in der Lunge. 30. Sauerstofftransport im Blut. 31. Kohlendioxidtransport im Blut. prof. Gyula Sáry Gasaustausch in der Lunge Gasdiffusion findet durch die Kapillarmembrane
Atmungsphysiologie II. 29. Gasaustausch in der Lunge. 30. Sauerstofftransport im Blut. 31. Kohlendioxidtransport im Blut. prof. Gyula Sáry Gasaustausch in der Lunge Gasdiffusion findet durch die Kapillarmembrane
Blutgasanalyse 03.06.14. Welche Konsequenzen hat das Ergebnis? Vortragsziele. ph-wert Puffersysteme im Blut. Bestandteile der Blutgasanalyse
 Blutgasanalyse Welche Konsequenzen hat das Ergebnis? Präsentation: Dr.R.Doppler Medizinische Abteilung LKH-Bruck/Mur Vortragsziele Interpretation der einzelnen Messwerte der Blutgasanalyse Erkennen von
Blutgasanalyse Welche Konsequenzen hat das Ergebnis? Präsentation: Dr.R.Doppler Medizinische Abteilung LKH-Bruck/Mur Vortragsziele Interpretation der einzelnen Messwerte der Blutgasanalyse Erkennen von
Säuren- und Basendefinition nach Arrhenius
 Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Säuren- und Basendefinition nach Arrhenius
 Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Puffersysteme. Diese Lerneinheit befasst sich mit den Grundlagen der Puffersysteme: Was ist der Pufferbereich und wovon ist er abhängig?
 Puffersysteme Diese Lerneinheit befasst sich mit den Grundlagen der Puffersysteme: Was ist ein Puffersystem? Wie wirkt ein Puffer? Was ist der Pufferbereich und wovon ist er abhängig? Welche biochemisch
Puffersysteme Diese Lerneinheit befasst sich mit den Grundlagen der Puffersysteme: Was ist ein Puffersystem? Wie wirkt ein Puffer? Was ist der Pufferbereich und wovon ist er abhängig? Welche biochemisch
5.5. α-toxin Zeit [min] Zeit [min] Kontrolle α-tox α-tox+adm ADM ADM $ $
![5.5. α-toxin Zeit [min] Zeit [min] Kontrolle α-tox α-tox+adm ADM ADM $ $ 5.5. α-toxin Zeit [min] Zeit [min] Kontrolle α-tox α-tox+adm ADM ADM $ $](/thumbs/72/66328153.jpg) 5. Ergebnisse 5.1. Mittlerer arterieller Blutdruck und Gefäßwiderstand des Ileumpräparats Bei flusskonstanter Perfusion stand der Blutgefässwiderstand des Ileumsegmentes in direkter Korrelation mit den
5. Ergebnisse 5.1. Mittlerer arterieller Blutdruck und Gefäßwiderstand des Ileumpräparats Bei flusskonstanter Perfusion stand der Blutgefässwiderstand des Ileumsegmentes in direkter Korrelation mit den
ph-wert Berechnung für starke Säuren / Basen
 ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
Chemie 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter Wasser (= 1000g)?
 Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Kapitel 17: Weitere Aspekt. wässriger Gleichgew. Einfluss gleicher Ionen: Gleichioniger Zusatz, Verschiebung des Gleichgewichtes nach Le-Châtelier.
 Ache2 Kapitel 17: Weitere Aspekt. wässriger Gleichgew. Einfluss gleicher Ionen: Gleichioniger Zusatz, Verschiebung des Gleichgewichtes nach Le-Châtelier. Bsp. ph berechnen einer 0.085 mol/l salpetriger
Ache2 Kapitel 17: Weitere Aspekt. wässriger Gleichgew. Einfluss gleicher Ionen: Gleichioniger Zusatz, Verschiebung des Gleichgewichtes nach Le-Châtelier. Bsp. ph berechnen einer 0.085 mol/l salpetriger
Physiologische Grundlagen der Ausdauer
 Lisa Maria Hirschfelder Aus der Reihe: e-fellows.net stipendiaten-wissen e-fellows.net (Hrsg.) Band 340 Physiologische Grundlagen der Ausdauer Leistungssport - Ausdauer-Grundlagen Skript Physiologische
Lisa Maria Hirschfelder Aus der Reihe: e-fellows.net stipendiaten-wissen e-fellows.net (Hrsg.) Band 340 Physiologische Grundlagen der Ausdauer Leistungssport - Ausdauer-Grundlagen Skript Physiologische
Blutgasanalytik eine Thematik zwischen Labor und Station
 Blutgasanalytik eine Thematik zwischen Labor und Station Xtra Vol. 14.2 2010 Nr. 11 Die Blutgasanalyse (BGA) ist ein fester Bestandteil heutiger Diagnostik und aus den Krankenhäusern und mittlerweile vielen
Blutgasanalytik eine Thematik zwischen Labor und Station Xtra Vol. 14.2 2010 Nr. 11 Die Blutgasanalyse (BGA) ist ein fester Bestandteil heutiger Diagnostik und aus den Krankenhäusern und mittlerweile vielen
Die Atmung. Die Atmung des Menschen. Die Atmung des Menschen
 Die Atmung Die Atmung ist ein lebenswichtiger Vorgang. Dabei wird der Körper mit Sauerstoff aus der eingeatmeten Luft versorgt. Den Sauerstoff benötigt der Körper zur lebenserhaltenden Energiegewinnung
Die Atmung Die Atmung ist ein lebenswichtiger Vorgang. Dabei wird der Körper mit Sauerstoff aus der eingeatmeten Luft versorgt. Den Sauerstoff benötigt der Körper zur lebenserhaltenden Energiegewinnung
Pneumologische Funktionsdiagnostik. 6. Diffusionsmessung
 Pneumologische Funktionsdiagnostik 6. Diffusionsmessung Inhalt 6.1 physiologische Grundlagen 6.2 Indikationen 6.3 Prinzip 6.4 Durchführung 6.5 Interpretation der Parameter 6.6 Qualitätskriterien Abbildung
Pneumologische Funktionsdiagnostik 6. Diffusionsmessung Inhalt 6.1 physiologische Grundlagen 6.2 Indikationen 6.3 Prinzip 6.4 Durchführung 6.5 Interpretation der Parameter 6.6 Qualitätskriterien Abbildung
ph-wert Berechnung für starke Säuren / Basen
 ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH Na + aq + OH starke Base,
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH Na + aq + OH starke Base,
Natriumhydrogencarbonat-Lösung 4,2 %/8.4 % AlleMan Pharma. Fachinformation FACHINFORMATION
 Natriumhydrogencarbonat-Lösung 4,2 %/8.4 % AlleMan Pharma Fachinformation FACHINFORMATION 1. Bezeichnung der Arzneimittel Wirkstoff: Natriumhydrogencarbonat 2. Qualitative und quantitative Zusammensetzung
Natriumhydrogencarbonat-Lösung 4,2 %/8.4 % AlleMan Pharma Fachinformation FACHINFORMATION 1. Bezeichnung der Arzneimittel Wirkstoff: Natriumhydrogencarbonat 2. Qualitative und quantitative Zusammensetzung
Physiologie der Atmung
 Beatmungstherapie Grundlagen der maschinellen Beatmung Ambulanter Pflegedienst Holzminden Nordstr. 23 37603 Holzminden 1 Physiologie der Atmung Ventilation (Belüftung der Alveolen) Inspiration (aktiv)
Beatmungstherapie Grundlagen der maschinellen Beatmung Ambulanter Pflegedienst Holzminden Nordstr. 23 37603 Holzminden 1 Physiologie der Atmung Ventilation (Belüftung der Alveolen) Inspiration (aktiv)
3.2. Aufgaben zu Säure-Base-Gleichgewichten
 .. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
.. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
Blutgasanalyse & Säure-Basen-Status
 Blutgasanalyse & Säure-Basen-Status Präanalytik 1 3 Allgemein Einflussfaktoren wichtig für klinische Diagnostik Überwachung / Nachweis Diffusionsstörungen Ventilationsstörungen Perfusionsstörungen Störungen
Blutgasanalyse & Säure-Basen-Status Präanalytik 1 3 Allgemein Einflussfaktoren wichtig für klinische Diagnostik Überwachung / Nachweis Diffusionsstörungen Ventilationsstörungen Perfusionsstörungen Störungen
Säuren und Basen. Säure-Base- Definition n. Arrhenius
 Säuren und Basen Säure-Base- Definition n. Arrhenius Säuren sind Verbindungen, die in Wasser in Protonen (H +, positiv geladene Wasserstoffionen) und in negativ geladene Säurerestionen dissoziieren (zerfallen).
Säuren und Basen Säure-Base- Definition n. Arrhenius Säuren sind Verbindungen, die in Wasser in Protonen (H +, positiv geladene Wasserstoffionen) und in negativ geladene Säurerestionen dissoziieren (zerfallen).
Danke für Ihr Interesse an dieser Präsentation! 2019 WK-Fortbildungen
 Danke für Ihr Interesse an dieser Präsentation! Wir möchten Sie darauf hinweisen, dass diese Präsentation das Eigentum des Erstellers ist. Jede Verwertung außerhalb der engen Grenzen des Urheberrechts
Danke für Ihr Interesse an dieser Präsentation! Wir möchten Sie darauf hinweisen, dass diese Präsentation das Eigentum des Erstellers ist. Jede Verwertung außerhalb der engen Grenzen des Urheberrechts
Handout Die Atmung. Anatomie
 Handout Die Atmung Anatomie Obere Atemwege Zu den oberen Atemwegen zählen die Nase, der Mund und der Rachenraum. Die Trennung zu den unteren Atemwegen gilt der Kehlkopf und dort genauer die Stimmritze.
Handout Die Atmung Anatomie Obere Atemwege Zu den oberen Atemwegen zählen die Nase, der Mund und der Rachenraum. Die Trennung zu den unteren Atemwegen gilt der Kehlkopf und dort genauer die Stimmritze.
INSTITUT FÜR PHYSIOLOGIE
 INSTITUT FÜR PHYSIOLOGIE Anleitung zum Physiologie - Praktikum P - 1. Pufferung und Säure-Basen Analyse WS 2010/11 3. Semester 2 Inhalt I. VORBEMERKUNGEN... 3 II. THEORETISCHE GRUNDLAGEN... 4 1. Säuren
INSTITUT FÜR PHYSIOLOGIE Anleitung zum Physiologie - Praktikum P - 1. Pufferung und Säure-Basen Analyse WS 2010/11 3. Semester 2 Inhalt I. VORBEMERKUNGEN... 3 II. THEORETISCHE GRUNDLAGEN... 4 1. Säuren
Modul 39: Säure-Basen-Haushalt
 Modul 39: Säure-Basen-Haushalt Stichworte: ph-wert - Pufferung - offenes versus geschlossenes Puffersystem - CO 2 /HCO 3 - -Puffer - [HCO 3 - ] Standard - [HCO 3 - ] aktuell - Henderson-Hasselbalch- Gleichung
Modul 39: Säure-Basen-Haushalt Stichworte: ph-wert - Pufferung - offenes versus geschlossenes Puffersystem - CO 2 /HCO 3 - -Puffer - [HCO 3 - ] Standard - [HCO 3 - ] aktuell - Henderson-Hasselbalch- Gleichung
Inhaltsverzeichnis. Vormann: Säure-Basen-Haushalt: latente Azidose als Ursache chronischer Erkrankungen... 25
 Vorwort Die Konzentration freier Wasserstoffionen in den verschiedenen Flüssigkeitsräumen des menschlichen Organismus gehört zu jenen Größen die in einem relativ engen Bereich konstant gehalten werden.
Vorwort Die Konzentration freier Wasserstoffionen in den verschiedenen Flüssigkeitsräumen des menschlichen Organismus gehört zu jenen Größen die in einem relativ engen Bereich konstant gehalten werden.
Zusammenfassung vom
 Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Teil 2. Puffersysteme. Puffersysteme. Puffersysteme. MTA-Schule
 Puffersysteme Säure-Basen-Haushalt Teil 2 MTA-Schule Lösungen, die die Fähigkeit besitzen, ihren -Wert trotz Zugabe von H + oder OH Ionen weitgehend konstant zu halten, nennt man Pufferlösungen. Puffersysteme:
Puffersysteme Säure-Basen-Haushalt Teil 2 MTA-Schule Lösungen, die die Fähigkeit besitzen, ihren -Wert trotz Zugabe von H + oder OH Ionen weitgehend konstant zu halten, nennt man Pufferlösungen. Puffersysteme:
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9)
 Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 1. Funktion des Hämoglobins Sauerstoff
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 1. Funktion des Hämoglobins Sauerstoff
Themen : Allgemeine Zellphysiologie Atmung & Säure / Basen
 Zentrum der Physiologie Seminar Pathophysiologie zum Praktikum Physiologie SS 2013 Themen : Allgemeine Zellphysiologie Atmung & Säure / Basen Dozenten : Jochen Roeper / Katrin Schröder Kennung der ausgewählten
Zentrum der Physiologie Seminar Pathophysiologie zum Praktikum Physiologie SS 2013 Themen : Allgemeine Zellphysiologie Atmung & Säure / Basen Dozenten : Jochen Roeper / Katrin Schröder Kennung der ausgewählten
Alveolo-arterielle Sauerstoffpartialdruckdifferenz, vereinfachte Berechnung
 Alveolo-arterielle Sauerstoffpartialdruckdifferenz, vereinfachte Berechnung alveolo-arterielle Sauerstoffdruckdifferenz alveolo-arterielle Sauerstoffdifferenz AaDO 2 - (vereinfacht) AaDO 2 - (Schätzwert)
Alveolo-arterielle Sauerstoffpartialdruckdifferenz, vereinfachte Berechnung alveolo-arterielle Sauerstoffdruckdifferenz alveolo-arterielle Sauerstoffdifferenz AaDO 2 - (vereinfacht) AaDO 2 - (Schätzwert)
Aus dem Institut für Veterinär-Physiologie sowie der Klinik für Pferde, Allgemeine Chirurgie und Radiologie der Freien Universität Berlin
 Aus dem Institut für Veterinär-Physiologie sowie der Klinik für Pferde, Allgemeine Chirurgie und Radiologie der Freien Universität Berlin Bedeutung der Stewart-Variablen des Säuren-Basen-Status für die
Aus dem Institut für Veterinär-Physiologie sowie der Klinik für Pferde, Allgemeine Chirurgie und Radiologie der Freien Universität Berlin Bedeutung der Stewart-Variablen des Säuren-Basen-Status für die
Anorganisch-chemisches Praktikum für Human- und Molekularbiologen
 Anorganisch-chemisches Praktikum für uman- und Molekularbiologen. Praktikumstag Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Säure-Base-Definition
Anorganisch-chemisches Praktikum für uman- und Molekularbiologen. Praktikumstag Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Säure-Base-Definition
K Den Säure-Basen-Haushalt verstehen
 Ihr Einkaufsführer: handlich, sicher, gut K Den Säure-Basen-Haushalt verstehen K Vorwort 6 K Was sind Säuren? 10 K Was sind Basen? 11 K Wechselwirkungen im Körper 12 Stadieneinteilung der Azidose (Übersäuerung)
Ihr Einkaufsführer: handlich, sicher, gut K Den Säure-Basen-Haushalt verstehen K Vorwort 6 K Was sind Säuren? 10 K Was sind Basen? 11 K Wechselwirkungen im Körper 12 Stadieneinteilung der Azidose (Übersäuerung)
Physiologie Kurs VI Funktionen der Lunge Regulation der Blutgase und des Säure-Base Status
 Physiologie Kurs VI Funktionen der Lunge Regulation der Blutgase und des Säure-Base Status Pharmakologisches Institut für Naturwissenschaftler Katharina Metzner Lehrbuchbeispiele: Titel Autoren Ausgabe
Physiologie Kurs VI Funktionen der Lunge Regulation der Blutgase und des Säure-Base Status Pharmakologisches Institut für Naturwissenschaftler Katharina Metzner Lehrbuchbeispiele: Titel Autoren Ausgabe
Herz und Kreislauf Teil 1
 24. TOGGENBURGER ANÄSTHESIE REPETITORIUM Herz und Kreislauf Teil 1 Aufgaben des Kreislaufs Salome Machaidze Miodrag Filipovic miodrag.filipovic@kssg.ch Anästhesiologie & Intensivmedizin Unter Verwendung
24. TOGGENBURGER ANÄSTHESIE REPETITORIUM Herz und Kreislauf Teil 1 Aufgaben des Kreislaufs Salome Machaidze Miodrag Filipovic miodrag.filipovic@kssg.ch Anästhesiologie & Intensivmedizin Unter Verwendung
Säure - Base - Theorien
 Säure Base Theorien S. Arrhenius (1887) Säuren sind Stoffe, die in wässriger Lösung H + (aq) Ionen bilden, während Basen OH (aq) Ionen bilden. H 2 SO 4, HNO 3, HCl, NaOH, Ba(OH) 2, aber: NH 3, CH 3, OCH
Säure Base Theorien S. Arrhenius (1887) Säuren sind Stoffe, die in wässriger Lösung H + (aq) Ionen bilden, während Basen OH (aq) Ionen bilden. H 2 SO 4, HNO 3, HCl, NaOH, Ba(OH) 2, aber: NH 3, CH 3, OCH
Aufgabe 1: Geben Sie die korrespondierenden Basen zu folgenden Verbindungen an: a) H 3 PO 4 b) H 2 PO 4
 Übungsaufgaben zum Thema Säuren, Basen und Puffer Säure/Base Definition nach Brǿnsted: Säuren sind Stoffe, die Protonen abgeben können (Protonendonatoren). Basen sind Stoffe, die Protonen aufnehmen können
Übungsaufgaben zum Thema Säuren, Basen und Puffer Säure/Base Definition nach Brǿnsted: Säuren sind Stoffe, die Protonen abgeben können (Protonendonatoren). Basen sind Stoffe, die Protonen aufnehmen können
Musteraufgaben. Was verstehen Sie im Zusammenhang mit der Hämatopoese unter einer "pluripotenten Stammzelle"? Welche Aufgabe hat diese Zelle?
 Fach: Immunologie - 32001_Immunologie-Blut Anzahl Aufgaben: 25 Musteraufgaben Diese Aufgabensammlung wurde mit KlasseDozent erstellt. Sie haben diese Aufgaben zusätzlich als KlasseDozent-Importdatei (.xml)
Fach: Immunologie - 32001_Immunologie-Blut Anzahl Aufgaben: 25 Musteraufgaben Diese Aufgabensammlung wurde mit KlasseDozent erstellt. Sie haben diese Aufgaben zusätzlich als KlasseDozent-Importdatei (.xml)
Gastransport Tierreich
 Gastransport Einstiegsfragen: - Sind Verbrennungen exotherm oder endotherm? - Welches Gas wird dafür benötigt? - Wo kommt es vor? - Wo wird es benötigt? - Wie kann es dorthin gelangen? - Was braucht es
Gastransport Einstiegsfragen: - Sind Verbrennungen exotherm oder endotherm? - Welches Gas wird dafür benötigt? - Wo kommt es vor? - Wo wird es benötigt? - Wie kann es dorthin gelangen? - Was braucht es
Stewart-Approach. Approach zur Beurteilung des SäureS Haushaltes. Der. Doch leicht zu verstehen, oder?
 Der Stewart-Approach Approach zur Beurteilung des SäureS ure-basen- Haushaltes Doch leicht zu verstehen, oder? Georg-Christian Funk Erste Interne Lungenabteilung Otto Wagner Spital - Wien Fragen: Was ist
Der Stewart-Approach Approach zur Beurteilung des SäureS ure-basen- Haushaltes Doch leicht zu verstehen, oder? Georg-Christian Funk Erste Interne Lungenabteilung Otto Wagner Spital - Wien Fragen: Was ist
Pressemitteilung. Neue Placebo-kontrollierte Doppelblind-Studie bestätigt: Entsäuerung mit Basica Direkt bringt mehr Energie
 Pressemitteilung Neue Placebo-kontrollierte Doppelblind-Studie bestätigt: Entsäuerung mit Basica Direkt bringt mehr Energie In der heutigen Zeit muss man leistungsfähig sein für alle Anforderungen, die
Pressemitteilung Neue Placebo-kontrollierte Doppelblind-Studie bestätigt: Entsäuerung mit Basica Direkt bringt mehr Energie In der heutigen Zeit muss man leistungsfähig sein für alle Anforderungen, die
Kapnometrie in der außerklinischen Beatmung sinnvoll oder nur ein teures Spielzeug?
 Kapnometrie in der außerklinischen Beatmung sinnvoll oder nur ein teures Spielzeug? S. Tiedemann, R. Thietje, S. Hirschfeld Quelle: Wikimedia Autor: Yikrazuul Lizenz: Gemeinfrei Quelle: Wikimedia Autor:
Kapnometrie in der außerklinischen Beatmung sinnvoll oder nur ein teures Spielzeug? S. Tiedemann, R. Thietje, S. Hirschfeld Quelle: Wikimedia Autor: Yikrazuul Lizenz: Gemeinfrei Quelle: Wikimedia Autor:
Sauerstoffbindung im Blut
 Sauerstoffbindung im Blut Die Fähigkeit uns zu wundern, ist das Einzige, was wir brauchen, um gute Philosophen zu werden. Gaarder Jostein, Sofies Welt 1 Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung...
Sauerstoffbindung im Blut Die Fähigkeit uns zu wundern, ist das Einzige, was wir brauchen, um gute Philosophen zu werden. Gaarder Jostein, Sofies Welt 1 Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung...
Niere Salz-/Wasserhaushalt 2009
 Aus: Gray's Anatomy: Descriptive and Surgical Theory United Kingdom 1858 Zentrale Aufgaben der Nieren Regulation des Wasserhaushaltes Regulation des Mineralhaushaltes (Osmolarität) Regulation des Säure-Basen-Haushaltes
Aus: Gray's Anatomy: Descriptive and Surgical Theory United Kingdom 1858 Zentrale Aufgaben der Nieren Regulation des Wasserhaushaltes Regulation des Mineralhaushaltes (Osmolarität) Regulation des Säure-Basen-Haushaltes
Blutgasanalyse in der präklinischen Notfallmedizin
 Gliederung Ortsstelle Mayrhofen Blutgasanalyse in der präklinischen Notfallmedizin Einführung Meßparameter Grundlagen Blutgasanalyse Störungen Fallbeispiele Therapeutische Überlegungen Anwendung am Standort
Gliederung Ortsstelle Mayrhofen Blutgasanalyse in der präklinischen Notfallmedizin Einführung Meßparameter Grundlagen Blutgasanalyse Störungen Fallbeispiele Therapeutische Überlegungen Anwendung am Standort
Laplace-Gesetz Aufteilung des Bronchialbaums Pneumozyten Intrapleuraler Druck Alveolardruck Transpulmonaler Druck
 Laplace-Gesetz Aufteilung des Bronchialbaums Pneumozyten Intrapleuraler Druck Alveolardruck Transpulmonaler Druck Atemzugvolumen Inspiratorisches Reservevolumen insgesamt 23 Verzweigungen Konduktionszone:
Laplace-Gesetz Aufteilung des Bronchialbaums Pneumozyten Intrapleuraler Druck Alveolardruck Transpulmonaler Druck Atemzugvolumen Inspiratorisches Reservevolumen insgesamt 23 Verzweigungen Konduktionszone:
Säurekapazität in der Belebung einer Kläranlage
 LV Bayern, Besprechung der Lehrer Kläranlagen-Nachbarschaft 2014 Säurekapazität in der Belebung einer Kläranlage Dipl.-Ing. Annette Schlicher, Struktur- und Genehmigungsdirektion Süd, Regionalstelle Wasserwirtschaft,
LV Bayern, Besprechung der Lehrer Kläranlagen-Nachbarschaft 2014 Säurekapazität in der Belebung einer Kläranlage Dipl.-Ing. Annette Schlicher, Struktur- und Genehmigungsdirektion Süd, Regionalstelle Wasserwirtschaft,
Rationale Basisdiagnostik bei Elektrolytstörungen
 Rationale Basisdiagnostik bei Elektrolytstörungen Siegfried Waldegger Kindernephrologie Innsbruck Department für Kinder und Jugendheilkunde Elektrolytstörungen in Zusammenhang mit angeborenen Erkrankungen
Rationale Basisdiagnostik bei Elektrolytstörungen Siegfried Waldegger Kindernephrologie Innsbruck Department für Kinder und Jugendheilkunde Elektrolytstörungen in Zusammenhang mit angeborenen Erkrankungen
Seminar: Blutgasanalytik
 Seminar: Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin - Zentrallaboratorium - Universitätsklinikum Münster Wintersemester 2015/16 Gliederung 1. Anwendungen der Blutgasanalytik
Seminar: Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin - Zentrallaboratorium - Universitätsklinikum Münster Wintersemester 2015/16 Gliederung 1. Anwendungen der Blutgasanalytik
Einteilung der Maßanalyse
 Einteilung der Maßanalyse Neutralisation (Säure-Base-Titration Acidimetrie Alkalimetrie Fällungstitration Redoxtitration Iodometrie Dichromatometrie Manganometrie etc. Komplexometrie Säure/Basen Theorien
Einteilung der Maßanalyse Neutralisation (Säure-Base-Titration Acidimetrie Alkalimetrie Fällungstitration Redoxtitration Iodometrie Dichromatometrie Manganometrie etc. Komplexometrie Säure/Basen Theorien
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Natriumhydrogencarbonat-Lösung 8,4 % DELTAMEDICA Infusionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1000 ml
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Natriumhydrogencarbonat-Lösung 8,4 % DELTAMEDICA Infusionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1000 ml
Punktion der A. radialis + Blutgasanalyse
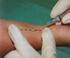 Punktion der A. radialis + Blutgasanalyse Wissenswertes: Allgemeines: Sinn dieser Station in unserem Skills Lab Innere ist nicht nur die arterielle Blutentnahme, sondern insbesondere auch die nachfolgende
Punktion der A. radialis + Blutgasanalyse Wissenswertes: Allgemeines: Sinn dieser Station in unserem Skills Lab Innere ist nicht nur die arterielle Blutentnahme, sondern insbesondere auch die nachfolgende
co2 arteriell venös arteriovenöse Differenz
 po2 arteriell venös pco2 arteriell venös ph arteriell venös O2-Sättigung so2 arteriell venös O2-Gehalt co2 arteriell venös arteriovenöse Differenz CO2-Gehalt cco2 arteriell venös Hypoxie Hypoxämie arteriell:
po2 arteriell venös pco2 arteriell venös ph arteriell venös O2-Sättigung so2 arteriell venös O2-Gehalt co2 arteriell venös arteriovenöse Differenz CO2-Gehalt cco2 arteriell venös Hypoxie Hypoxämie arteriell:
