Prävention/Impfen, M. Pfleiderer
|
|
|
- Silke Biermann
- vor 8 Jahren
- Abrufe
Transkript
1 Seite 2 7 PRÄVENTION/IMPFEN 7.1 Influenzaimpfstoffe Entwicklungsgeschichte Saisonale Influenzaimpfstoffe Herstellung Klinische Prüfung und Zulassung Jährliche Stammanpassung Immunologische Eigenschaften Verträglichkeit Neue Technologien 7.2 Pandemische Influenzaimpfstoffe Allgemeine Anmerkungen Das Prinzip der Musterimpfstoffe Herstellung Präklinische Anforderungen Klinische Anforderungen Adjuvanssysteme Andere Inhaltsstoffe Anpassung der Musterimpfstoffe an H1N1v Verträglichkeit 7.3 Nutzen-Risiko-Analyse 7.4 Literatur
2 Seite Influenzaimpfstoffe Entwicklungsgeschichte Die Entwicklungsgeschichte der Influenzaimpfstoffe erstreckt sich bereits über viele Jahrzehnte. Mit der Charakterisierung der Influenzaviren als verursachende Erreger der Influenza Mitte der 1930er Jahre begannen fast zeitgleich Entwicklungsarbeiten mit dem Ziel, eine Impfstoffproduktion zu etablieren. Wesentliche Voraussetzung für den Erfolg dieser Bemühungen war die Tatsache, dass die Influenzatypen A und B, die für Erkrankungen im Menschen ursächlich verantwortlich sind, in bebrüteten Hühnereiern vermehrbar sind. Das bebrütete Hühnerei ist eines der wenigen Substrate zur Virusanzucht, das zum damaligen Zeitpunkt verfügbar und kontrollierbar war. Influenzaviren vermehren sich im Atmungstrakt des Hühnerembryos zu hohen Titern und können direkt aus der Allantoisflüssigkeit gewonnen werden. Die erste Generation der Influenzaimpfstoffe bestand demzufolge aus relativ kruden Viruspräparationen. Uncharakterisierte produkt- und prozessspezifische Verunreinigungen aus den Herstellungsprozessen bedingten jedoch hohe Nebenwirkungsraten, die im Rahmen der zunehmenden Erkenntnisse zur Wirksamkeit der Influenzaimpfstoffe und der damit verbundenen immer breiter werdenden Anwendung nicht länger toleriert werden konnten. Mit anderen Worten: Die Impfrisiken und der Nutzen der frühen Influenzaimpfstoffe hielten sich nicht länger in der Balance, sodass ein positives Nutzen-Risiko-Verhältnis nur schwer darzustellen war. Mit zunehmender Technisierung der Herstellungsprozesse, insbesondere durch die Integration moderner Zentrifugationstechniken, war es in der Folge möglich, die Impfviren immer besser aufzureinigen und von Verunreinigungen aus den Herstellungsprozessen, die hauptsächlich für die starke Reaktogenität verantwortlich waren, zu trennen. Eine weitere Evolutionsstufe in der Entwicklungsgeschichte der Influenzaimpfstoffe bestand in der Spaltung der Impfviren, d. h. in der Trennung von denjenigen Viruskomponenten, die für die Entwicklung einer protektiven Immunität benötigt werden, von den dazu nichtbenötigten Virusbestandteilen. Wie später noch näher ausgeführt wird, richtet sich eine effektive Immunantwort primär gegen die auf der Virusoberfläche prominenten Glykoproteine Hämagglutinin (HA) und Neuraminidase (NA). In modernen Spaltimpfstoffen sind diese Komponenten nur noch von geringen Mengen anderer Virusproteine begleitet; in Untereinheitenimpfstoffen sind auch diese fast zur Gänze entfernt. Auf der aktuellen Evolutionsstufe präsentieren sich Influenzaimpfstoffe in allen Personengruppen als sehr verträgliche Produkte, eine unabdingbare Voraussetzung für die jährliche Anwendung sowie dem aktuellen Anlass entsprechend für die massenweise Anwendung im Rahmen einer Pandemie Saisonale Influenzaimpfstoffe Das Verständnis zur Funktionsweise von Pandemieimpfstoffen erschließt sich am einfachsten über die saisonalen Influenzaimpfstoffe. Bereits an dieser Stelle ist es notwendig, auf einige Besonderheiten der Influenzaimpfstoffe hinzuweisen, die sie von anderen Impfstoffen unterscheiden. Bedingt durch die optimale Anpassung an den menschlichen Wirt verändert sich die Oberfläche der Influenzaviren, in erster Linie das HA-Protein, in dem Maß, wie
3 Seite 4 die individuelle und die kollektive (entspricht Herden-)Immunität innerhalb einer Population zunehmen. Dieses Phänomen wird als antigene drift bezeichnet; die daraus hervorgehenden veränderten Influenzaviren sind die Drift-Varianten. Eine funktionale Antikörperantwort infolge einer Exposition, Infektion oder Impfung richtet sich gegen exponierte Epitope des HA-Proteins und ermöglicht die Virusneutralisation. Je nachdem, wie ausgeprägt und spezifisch diese Anti-HA- Antikörpertiter sind, werden eine Neuinfektion und Erkrankung verhindert. Je niedriger bzw. je unspezifischer die Antikörper sind, umso mehr wächst das Infektions- und Erkrankungsrisiko. Antikörpertiter, die einen bestimmten Schwellenwert unterschreiten, können eine Infektion nicht mehr verhindern, wohl aber die Schwere der Erkrankung mildern. Wird dieser Schwellenwert weiter unterschritten, entfaltet sich das volle klinische Bild einer Influenza mit hohen Morbiditäts- und Mortalitätsraten. Die Plastizität der Oberfläche der Influenzaviren erfordert fast jedes Jahr die saisonale Anpassung der Stammzusammensetzung der Influenzaimpfstoffe, um über die jährliche Wiederimpfung die Anti-HA-Antikörpertiter über dem Schwellenwert zu halten, der als Korrelat für eine protektive Immunität akzeptiert ist, und um darüber hinaus die Spezifität dieser Antikörper den zirkulierenden Influenzaviren anzupassen. Saisonale Influenzaimpfstoffe sind trivalent, d. h. sie enthalten eine definierte Menge der HA-Antigene und eine nichtdefinierte Menge der NA-Antigene der aktuellen Drift-Varianten der Influenza-A-Subtypen H1N1 und H3N2 sowie das HA eines Influenza-B-Virus. Nachdem sich der Wirkstoff die Zusammensetzung der Impfviren fast jedes Jahr ändert, handelt es sich bei den saisonalen Influenzaimpfstoffen um neue Produkte, die im Prinzip eine jährliche Neuzulassung notwendig machen. Wie im Abschn genauer erläutert wird, ist aufgrund der kurzen Zeitspanne zwischen der Festlegung der für die neue Impfsaison relevanten Impfstämme und dem Beginn der Impfkampagne eine jährliche Neuzulassung nicht möglich. Deswegen gilt für Influenzaimpfstoffe die Besonderheit, dass die Daten zur Qualität sowie zu den präklinischen und klinischen Untersuchungen, auf denen eine einmal erteilte Zulassung basiert, auch für alle zukünftigen Influenzavirustypen und -subtypen relevant sind. Das Prinzip der Übertragbarkeit von einmal erhobenen Daten ist auch für die Pandemieimpfstoffe relevant (s. Abschn ) Herstellung Influenzaimpfstoffe werden traditionell in Bruteiern und seit wenigen Jahren auch in Zellkulturen hergestellt: Hundenierenzellen (Optaflu, saisonal, Novartis; Madin Darby Canine Kidney Cells, MDCK): [1]. Verozellen (Celvapan, pandemisch, Baxter; Affennierenzellen): [2]. Beide Herstellungsprozesse stehen gleichwertig nebeneinander. Die immer wieder geäußerte Vermutung, dass bruteibasierte Influenzaimpfstoffe veraltet seien und
4 Seite 5 durch neue Technologien ersetzt werden müssten, trifft nicht zu. Die Herstellung dieser Impfstoffe ist dem Stand der Technik und des Wissens angepasst. Die klinischen Eigenschaften der eibasierten Impfstoffe unterscheiden sich nicht von denen der zellbasierten Influenzaimpfstoffe. Die überwiegende Mehrzahl der saisonalen und der pandemischen Influenzaimpfstoffe wird unverändert im Brutei hergestellt. Die zellbasierten Impfstoffe spielen derzeit nur für die Versorgung mit pandemischen Influenzaimpfstoffen eine Rolle. Die Herstellung von Influenzaimpfstoffen kann in mehrere charakteristische Phasen untergliedert werden [3]: Virusanzucht (Fermentation), Virusreinigung, Virusinaktivierung, Virusspaltung, Herstellung der monovalenten bulks (gereinigter monovalenter Wirkstoff: HA-Antigene der Influenza-A-Subtypen H1N1, H3N2 bzw. des Influenza-B- Virus), Herstellung der trivalenten bulks (trivalenter Wirkstoff: Mischung der 3 monovalenten HA-Antigene mit den anderen Impfstoffkomponenten) sowie Abfüllung, Kennzeichnung und Verpackung (Endprodukt). Alle saisonalen Influenzaimpfstoffe enthalten je 15 µg der HA-Antigene der 3 saisonal relevanten Influenzaviren. Saisonale Ganzvirusimpfstoffe sind in Deutschland seit mehr als zehn Jahren nicht mehr im Gebrauch und auch nicht mehr zugelassen Klinische Prüfung und Zulassung Saisonale Influenzaimpfstoffe unterliegen den gleichen Anforderungen bezüglich der Qualität, der präklinischen und klinischen Untersuchungen wie andere Impfstoffe auch. Neben der Eignung des Herstellungsverfahrens und der Herstellungsstätte müssen insbesondere die klinischen Eigenschaften über geeignete Studien nachgewiesen werden. Für etablierte inaktivierte Influenzaimpfstoffe, d. h. solche, die auf Bruteiern oder Gewebekulturen hergestellt werden und je 15 µg HA-Antigen der 3 relevanten Influenzaviren enthalten, sind keine echten Wirksamkeitsstudien vorgeschrieben. Vielmehr ist für derartige Influenzaimpfstoffe ein immunologisches Korrelat akzeptiert. So wird beispielsweise ein Hämagglutinationsinhibitions- (HAI-)Titer von 1:40 als Korrelat für protektive Immunität akzeptiert. Als alternative Testverfahren sind ein Immundiffusionstest, der Single-Radial-Hemolysis- (SRH-)Test sowie Virusneutralisationstests anerkannt (Harmonisation of Requirements for Influenza Vaccines; CPMP/BWP/214/96 [4]). Die Akzeptanzkriterien für den HAI-Test sind in Tabelle 1 zusammengefasst.
5 Seite 6 Altersgruppe (Jahre) Über 60 Serokonversionsfaktor a 2,5 2,0 Serokonversionsrate b (%) Seroprotektionsrate c (%) a Mittlerer Anstieg der HAI-Antikörpertiter. b Anteil der Personen mit einem HAI-Titer <1:40 vor der Impfung und 1:40 nach der Impfung bzw. mit einem HAI-Titer von 1:40 vor der Impfung und einem mindestens vierfachen Titeranstieg nach der Impfung. c Anteil der Personen mit einem HAI-Titer von 1:40 nach der Impfung. Tabelle 1 Immunologische Akzeptanzkriterien für saisonale Influenzaimpfstoffe am Beispiel des Hämagglutinationsinhibitions-(HAI)-Tests Diese Vorgaben berücksichtigen, dass bei den meisten Personen, die älter als etwa 8 bis 10 Jahre sind, bereits eine durch den mehr oder weniger regelmäßigen Kontakt mit zirkulierenden Influenzaviren oder durch frühere Impfungen bedingte Grundimmunität unterschiedlichen Ausmaßes vorliegt. Somit ist es möglich, die Immunogenität saisonaler Influenzaimpfstoffe in einer bezüglich ihrer individuellen Basisimmunität höchst heterogenen Bevölkerung hinreichend gut zu beschreiben. Neue saisonale Influenzaimpfstoffe, also solche, die mit neuen Verfahren (z. B. gentechnisch) hergestellt werden, über alternative Routen (z. B. nasal) verabreicht werden oder auf anderen Wirkprinzipien (z. B. lebend attenuiert) beruhen, können nur über den Nachweis der Wirksamkeit in kontrollierten Studien zugelassen werden, da bei solchen Konzepten die Eignung der in Tabelle 1 beschriebenen Akzeptanzkriterien nicht belegt ist [5] Jährliche Stammanpassung Die Anpassung einmal zugelassener saisonaler Influenzaimpfstoffe erfolgt in einem engen Zeitrahmen. Im Februar eines jeden Jahres legt die World Health Organization (WHO) in Zusammenarbeit mit ihren Kollaborationszentren für Influenza die Zusammensetzung der Impfstoffe für die kommende Saison für die nördliche Hemisphäre fest. Gleichermaßen wird im September eines jeden Jahres eine Empfehlung für die südliche Hemisphäre ausgesprochen [6]. Die WHO-Empfehlung für die nördliche Hemisphäre wird von den zuständigen wissenschaftlichen Gremien der Europäischen Union (EU) der Ad Hoc Influenza Working Party der Biologics Working Party (BWP) des Committee for Medicinal Products for Human Use (CHMP) der European Medicines Agency (EMEA), London, unter Einbeziehung der europäischen Hersteller überprüft und ggf. modifiziert übernommen. Wichtig ist, dass die von der WHO empfohlenen Stämme in die Herstellungsprozesse der Hersteller passen, d. h. hohe Virusausbeuten erlauben. Dies ist ein Kriterium, das für die rechtzeitige Bereitstellung ausreichender Mengen an saisonalen und pandemischen Influenzaimpfstoffen von fundamentaler Bedeutung ist. Im Rahmen der Stammanpassung müssen die Hersteller nachweisen, dass die Herstellung des neuen Impfstoffs im Einklang mit der zugrunde liegenden Zulassung steht und sich somit keine Abweichungen von der ursprünglich zugelassenen Impfstoffqualität einschleichen. In der EU wird, anders als etwa in den USA oder in Kanada, zudem noch eine Immunogenitätsstudie mit 60 Probanden unter 60 Jahren sowie weiteren
6 Seite 7 60 Probanden über 60 Jahren verlangt, um die Wirksamkeit der neuen Impfstoffe anhand der in Tabelle 1 zusammengestellten Kriterien überprüfen zu können. Zum Nachweis der Eignung der saisonalen Influenzaimpfstoffe muss allerdings nur eines der 3 beschriebenen Kriterien erfüllt werden. Der Grund für diese Regelung liegt darin, dass im Vergleich zum Vorjahr nur leicht veränderte Drift-Varianten entsprechend exponierte Immunsysteme ggf. kaum mehr stimulieren können, sodass insbesondere das Kriterium des Seroprotektionsfaktors nicht mehr erfüllt werden kann. Die Praxis zeigt aber, dass die in Deutschland und in der EU zugelassenen saisonalen Influenzaimpfstoffe regelmäßig alle 3 Akzeptanzkriterien erfüllen und dies sogar mit den unteren Konfidenzintervallen, d. h. sehr gut zur regelmäßigen Auffrischimpfung geeignet sind Immunologische Eigenschaften Wie im Abschn bereits erwähnt, gibt es in Deutschland nur noch saisonale Spalt- oder Untereinheitenimpfstoffe. Eine Liste der zugelassenen bzw. aktualisierten Impfstoffe findet sich auf der Homepage des Paul-Ehrlich-Instituts (PEI, -saisonal/influenza-saisonal-node.html? nnn=true, [7]). Die bessere Verträglichkeit dieser Impfstoffklassen im Vergleich zu den Ganzvirusimpfstoffen hat jedoch ihren Preis. Mit zunehmender Aufreinigung des HA-Impfantigens nimmt dessen Immunogenität ab. Dies bedeutet, dass in der Reihenfolge: Ganzvirusimpfstoff Spaltimpfstoff Untereinheitenimpfstoff zunehmend geringere Antikörpertiter erzielt werden. Die Reduktion der immunogenen Eigenschaften liegt darin begründet, dass insbesondere in Ganzvirusimpfstoffen andere Influenzavirusproteine einen adjuvantierenden Effekt auf das HA-Antigen ausüben, der mit zunehmender Aufreinigung zunehmend wegfällt. Diese Tendenz hat im Rahmen der regelmäßigen saisonalen Impfung vermutlich keine klinischen Konsequenzen, denn eine ausreichend hohe Grundimmunität benötigt nur einen geringen Stimulus, um vervollständigt zu werden. Wie sich im Rahmen der umfangreichen Studien zu pandemischen Kandidatimpfstoffen aber herausgestellt hat, wird es immer schwieriger, naive, also zuvor gegenüber einem neuen Antigen noch nie exponierte Immunsysteme, mit hoch gereinigten Impfantigenen effektiv zu stimulieren. Zumindest kann dies nicht über eine einzige Teildosis erreicht werden. Eine vergleichsweise geringere Immunogenität von Impfantigenen kann entweder durch die Verabreichung mehrerer Teildosen oder durch die Verwendung geeigneter Adjuvanssysteme, mit deren Hilfe die Immunogenität gereinigter Influenzavirusantigene signifikant verbessert werden kann, kompensiert werden. In der Tat kann dies am Beispiel des seit vielen Jahren zugelassenen saisonalen Impfstoffs Fluad (Novartis Vaccines and Diagnostics, Siena, Italien), der ein squalenölbasiertes Öl-in-Wasser-Adjuvanssystem enthält, eindrucksvoll bestätigt werden. Fluad ist somit ein adjuvantierter Untereinheitenimpfstoff, der im Vergleich zu seinem nichtadjuvantierten Gegenstück eine geringere Restimmunität wesentlich effektiver auffrischen kann. Je ausgeprägter eine vorhandene Restimmunität beim Impfling jedoch ist, umso weniger Vorteile haben adjuvantierte im Vergleich zu den nichtadjuvantierten saisonalen Influenzaimpfstoffen.
7 Seite 8 Diese Erkenntnisse haben fundamental zur Entwicklung geeigneter Pandemieimpfstoffe beigetragen, wie im Abschn. 7.2 noch ausführlich dargelegt wird Verträglichkeit Daten zur Verträglichkeit von saisonalen Influenzaimpfstoffen werden über die Spontanerfassung (Pharmakovigilanz) sowie über die von den Herstellern und Zulassungsinhabern zweimal jährlich zu verfassenden Periodic Safety Update Reports (PSUR) erfasst und ausgewertet. Für die saisonalen Influenzaimpfstoffe ergeben sich über die Jahre hinweg keine besonderen Nebenwirkungsprofile, die über das zu erwartende und zu tolerierende Maß hinausgehen. Das PEI bietet seit einiger Zeit eine Onlinedatenbank zur Meldung von Verdachtsfällen unerwünschter Arzneimittelwirkungen und Impfkomplikationen an, mit deren Hilfe spezifisch nach bestimmten Nebenwirkungen recherchiert werden kann: a52u21ad3 [8] Neue Technologien Nachdem zumindest die saisonalen Influenzaimpfstoffe seit Langem etabliert sind, wird in regelmäßigen Abständen über vermeintlich verbesserte Impfkonzepte berichtet. Überwiegend beziehen sich solche Berichte auf die gentechnische Herstellung der Impfantigene in diversen Expressionssystemen. Solche Forschungsansätze basieren zumeist auf der Annahme, dass Influenzaimpfstoffe, die nicht auf Hühnereiern produziert werden, besser und schneller hergestellt werden können. Insbesondere wird die Bereitstellung ausreichender Mengen an Bruteiern zur Herstellung saisonaler und pandemischer Influenzaimpfstoffe gerne als besonderer Engpass dargestellt, durch den die rechtzeitige Versorgung mit Impfstoffen gefährdet werden könnte. Solche Überlegungen basieren allerdings nicht auf einer realen Grundlage. Die Logistikketten zur Bereitstellung von Bruteiern für die Abdeckung des Bedarfs an Influenzaimpfstoffen funktionieren reibungslos, sowohl in interpandemischen als auch in pandemischen Zeiten, wie die gegenwärtige Situation zweifelsfrei verdeutlicht. Lediglich Seuchenzüge hoch pathogener aviärer Influenzaviren könnten die Produktion von Bruteiern gefährden, aber auch diese Bedenken sind angesichts der fortdauernden Zirkulation des aviären Influenza-A-Virussubtyps H1N1 eher hypothetisch. Die Verbesserung von Influenzaimpfstoffen aller Art kann nur über die Erhöhung der Immunogenität der Impfantigene erfolgen. Der alleinige Wechsel in der Herstellungsmethode, z. B. von traditionell auf rekombinant, wird kaum in immunogeneren Influenzavirusantigenen resultieren, denn, wie bereits im Abschn ausgeführt wurde, nimmt die Immunogenität des HA-Antigens ab, je besser dieses von anderen Influenzavirusproteinen abgetrennt werden kann. Dieser Sachverhalt trifft insbesondere auf rekombinant hergestellte Influenzavirusantigene zu, bei deren Produktion andere Virusproteine naturgemäß nicht vorkommen. Die Verbesserung der Immunogenität von Spalt- oder Untereinheitenimpfstoffen, v. a. in immunologisch naiven Personen, kann nach derzeitiger Einschätzung nur über den Zusatz geeigneter Adjuvanssysteme erreicht werden (s. Abschn ). Alternativ bieten sich die nasal verabreichten lebend attenuierten Influenzaimpfstoffe an, mit denen insbesondere in Kindern eine sehr gute Wirksamkeit belegt werden konnte. Ein solcher saisonaler Impfstoff wird in der EU
8 Seite 9 voraussichtlich ab dem Jahr 2010 zur Verfügung stehen. In welchen Altersgruppen der lebend attenuierte Influenzaimpfstoff in der EU angewendet werden darf, kann derzeit noch nicht genau abgeschätzt werden. 7.2 Pandemische Influenzaimpfstoffe Allgemeine Anmerkungen Pandemische Influenzaimpfstoffe unterliegen demselben Dilemma wie die saisonalen Influenzaimpfstoffe, d. h. die Zeitspanne zwischen der Identifizierung des relevanten pandemischen Influenzavirus und dem Eintreffen der ersten Pandemiewelle, vor der eine betroffene Bevölkerung durch die rechtzeitige Impfung mit geeigneten Impfstoffen geschützt werden soll, ist sehr knapp bemessen. Diese ohnehin schon schwierige Situation wird dadurch noch verschärft, dass Pandemieimpfstoffe zum Anbeginn einer pandemischen Welle in ausreichenden Quantitäten zur Verfügung stehen und an besonders gefährdete Bevölkerungsteile im Wesentlichen synchron verimpft werden müssen. Trotzdem ist es notwendig, dass auch Pandemieimpfstoffe unter strikter wissenschaftlicher und regulatorischer Kontrolle gehalten werden sowie hinsichtlich ihrer Qualität und ihrer klinischen Eigenschaften genauso sorgfältig geprüft werden wie andere Impfstoffe auch Das Prinzip der Musterimpfstoffe Das einleitend zitierte Dilemma wird durch das Prinzip der Musterzulassungen bzw. der Musterimpfstoffe umgangen. Dieses Prinzip ist eng an die Kriterien der Zulassung und Stammanpassung der saisonalen Influenzaimpfstoffe angelehnt. Es berücksichtigt den in wissenschaftlichen und medizinischen Kreisen anerkannten Sachverhalt, dass die für einen oder mehrere Influenzavirustypen akzeptierten Daten zu Herstellung (Qualität), präklinischen und klinischen Untersuchungen auf andere neue Influenzavirustypen bzw. -subtypen übertragbar sind (s. Abschn ). Für pandemische Influenzaimpfstoffe bedeutet dies, dass Erkenntnisse, die im Rahmen von Zulassungsverfahren mit Influenzavirus-A-Subtypen generiert wurden, von denen man annimmt, dass sie ein mögliches pandemisches Potenzial besitzen, sich jedoch noch nicht zu einem Pandemievirus weiterentwickelt haben, zukünftig auf ein tatsächliches pandemisches Influenzavirus übertragbar sind. Dieser Ansatz erlaubt es, dass bei der Zulassung nur noch die Herstellung des eigentlichen pandemischen Impfstoffs geprüft werden muss, genau wie dies bei den saisonalen Impfstoffen der Fall ist. Eine erneute klinische Prüfung ist unter diesen Voraussetzungen nicht mehr notwendig und unter Berücksichtigung der schnellen Ausbreitung eines pandemischen Influenzavirus auch gar nicht möglich. Die wissenschaftlichen und regulatorischen Grundlagen der Musterzulassungen/Musterimpfstoffe (mock-up vaccines) wurden 2003 von der Vaccine Working Party (VWP) des CHMP, dem Ausschuss für Humanarzneimittel der EMEA in London erarbeitet. Pandemische Musterimpfstoffe besitzen somit EU- Zulassungen und repräsentieren einen breit gefächerten wissenschaftlichen Konsens [9]. Während die ersten klinischen Untersuchungen mit Musterimpfstoffen auf der Basis der Influenzavirus-A-Subtypen H2N2, H7N7 oder H9N2, denen ein mögliches pandemisches Potenzial zugeschrieben worden war, durchgeführt
9 Seite 10 wurden, beruht der Großteil unseres Wissens zu Pandemieimpfstoffen mittlerweile auf Impfstoffen, die das HA-Antigen des hoch pathogenen aviären Subtyps H5N1 enthalten. Eine Übersicht zu den derzeit zugelassenen H5N1-basierten Musterimpfstoffen zeigt Tabelle 2 [10]. Name Hersteller Anwendung Produktbeschreibung Focetria Novartis WHO-Phase 6 7,5 µg H5N1, Oberflächenantigen, adjuvantiert mit MF59.1 Daronrix a GSK WHO-Phase 6 3,75 µg H5N1 Ganzvirus, adjuvantiert mit AlOH Pandemrix GSK WHO-Phase 6 Celvapan Baxter WHO-Phase 6 Emerflu b Sanofi Pasteur WHO-Phase 6 3,75 µg H5N1, Spaltantigen, adjuvantiert mit AS03 7,5 µg H5N1 Ganzvirus, nichtadjuvantiert 30 µg H5N1 Spaltantigen adjuvantiert mit AlOH AlOH Aluminiumhydroxid, AS03 Adjuvant System 03, GSK GlaxoSmithKline. a Wird nicht hergestellt. b Zulassungsverfahren noch nicht abgeschlossen. Tabelle 2 Zusammenstellung der in der EU zugelassenen Musterimpfstoffe. (Nach [10]) Die Tabelle 2 verdeutlicht, dass sich alle namhaften Hersteller von saisonalen Influenzaimpfstoffen mit unterschiedlichen Impfstoffformulierungen an dem Konzept der Zulassung von Musterimpfstoffen beteiligt haben. GlaxoSmithKline (GSK) besitzt als einziger Hersteller sogar 2 Musterzulassungen, für die Impfstoffe Daronrix und Pandemrix. Aus Gründen, die in den Abschn , und noch näher erläutert werden, spielt nur Pandemrix, nicht aber Daronrix, für den Pandemiefall eine Rolle. Der pharmazeutischen und klinischen Entwicklung dieser Musterimpfstoffe lagen die im Abschn erläuterten immunologischen Eigenschaften des Influenzavirus-HA-Antigens zugrunde. Die Produktbeschreibungen in Tabelle 2 weisen bereits an dieser Stelle darauf hin, dass dem Prinzip der Antigeneinsparung nur über den Zusatz von Adjuvanzien bzw. über Ganzvirusimpfstoffe gefolgt werden kann. Dieses Prinzip ist für eine effiziente Pandemieplanung von fundamentaler Bedeutung. Je weniger Antigen pro Dosis benötigt wird bzw. je weniger Teildosen zum Erreichen einer protektiven Immunität benötigt werden, umso besser können die vorhandenen Herstellungsressourcen genutzt werden und umso mehr dringend benötigter Impfstoff steht für die zu impfenden Bevölkerungsgruppen zum Anbeginn und während einer Pandemie zur Verfügung. Die Anwendung pandemischer Influenzaimpfstoffe im Rahmen der Zulassung ist an die Phase 6 bezüglich der WHO-Definition pandemischer Phasen und deren offizieller Verlautbarung durch die WHO gebunden.
10 Seite Herstellung Die Herstellung pandemischer Musterimpfstoffe bzw. des tatsächlichen Pandemieimpfstoffs unterscheidet sich bis zur Endformulierung nicht von der Herstellung der saisonalen Influenzaimpfstoffe. Es gilt an dieser Stelle erneut hervorzuheben, dass die bisher erteilten Musterzulassungen ausschließlich Hersteller betreffen, die auch Zulassungen für saisonale Impfstoffe in Deutschland oder in der EU besitzen. Diese Hersteller stellen saisonale Influenzaimpfstoffe in einer konsistenten Qualität und, darüber definiert, mit immer gleichbleibenden klinischen Eigenschaften her. Lediglich in der Zusammensetzung, also dem allerletzten Prozessschritt, d. h. der Mischung des HA-Antigens mit den anderen Impfstoffkomponenten, unterscheidet sich die Herstellung der pandemischen von der der saisonalen Influenzaimpfstoffe. Die Unterschiede ergeben sich durch den niedrigeren Antigengehalt und durch den Zusatz der bereits mehrfach erwähnten Adjuvanssysteme, die in den meisten saisonalen Influenzaimpfstoffen nicht enthalten sind Präklinische Anforderungen Im Gegensatz zu den saisonalen Influenzaimpfstoffen können die Effizienz und die Effektivität von H5N1-basierten Musterimpfstoffen nicht in kontrollierten klinischen Studien erfasst werden, da das dem Impfantigen entsprechende aviäre Influenzavirus des Subtyps H5N1 nicht in der menschlichen Population zirkuliert. Solche Studien sind nur im Rahmen der breiten Anwendung gegenüber einem tatsächlich zirkulierenden pandemischen Influenzavirus, wie derzeit dem H1N1v- Virus, möglich. Die Erfassung der Wirksamkeit von pandemischen Musterimpfstoffen a priori ist ausschließlich über die Bestimmung der serologischen Parameter gemäß Abschn möglich. Umso wichtiger ist unter solchen Voraussetzungen die sorgfältige präklinische Untersuchung von Musterimpfstoffen, insbesondere hinsichtlich ihrer Schutzeigenschaften. Glücklicherweise gibt es für die Prüfung von Influenzaimpfstoffen ein relevantes Tiermodell, das Frettchen, mit dem die Wirksamkeit von Influenzaimpfstoffen, über die reine Bestimmung serologischer Parameter hinaus, untersucht werden kann. Frettchen entwickeln nach einer Infektion mit Influenzaviren ähnliche Symptome wie der Mensch. Die Infektion mit dem hoch pathogenen aviären Influenzavirus-A-Subtyp H5N1 führt, wie beim Menschen, zu schwersten Krankheitsverläufen und zum Tod. Somit lassen sich mit diesem Tiermodell verlässliche Daten zur möglichen Schutzwirkung von H5N1-basierten Musterimpfstoffen generieren. Insgesamt ergibt sich aus der präklinischen Untersuchung der in Tabelle 2 aufgelisteten Musterimpfstoffe folgender Sachverhalt: Geimpfte Frettchen überleben eine tödliche H5N1-Belastungsdosis. Seren von Personen, die im Rahmen von klinischen Studien mit H5N1- Impfstoffen geimpft und nachfolgend auf Frettchen transferiert wurden, schützen diese ebenfalls vor einer ansonsten tödlichen H5N1-Belastungsdosis. Seren geimpfter Frettchen kreuzreagieren mit H5N1-Varianten, deren HA- Antigen nicht im Impfstoff enthalten ist. Geimpfte Frettchen überleben eine tödliche Belastungsdosis mit H5N1- Varianten, deren HA-Antigen nicht im Impfstoff enthalten ist.
11 Seite 12 Frettchen, die eine Dosis eines H5N1-Impfstoffs erhalten haben, reagieren anamnestisch, wenn ihnen eine zweite Dosis eines Impfstoffs verabreicht wird, der das HA-Antigen einer Drift-Variante des ursprünglichen H5N1- Impfstamms enthält. Auch wenn diese Resultate nicht vorschnell und zur Gänze auf den Menschen übertragen werden sollten, geben die präklinischen Erkenntnisse doch genügend Hinweise, dass die einzelnen H5N1-basierten Musterimpfstoffe effiziente Impfkonzepte repräsentieren Klinische Anforderungen Die klinische Minimalanforderung für pandemische Influenzaimpfstoffe entspricht der für die saisonalen Influenzaimpfstoffe, d. h. beispielsweise allen in der Tabelle 1 genannten Akzeptanzkriterien zu genügen. Allerdings sind die Impfziele von saisonaler und pandemischer Impfung unterschiedlich. Während bei der saisonalen Impfung die Auffrischung bzw. Anpassung einer bestehenden Grundimmunität beabsichtigt ist, geht es bei der Pandemieimpfung in erster Linie um die Grundimmunisierung bisher nichtexponierter und somit immunologisch naiver Personengruppen. Daher sind insbesondere die Seroprotektionsraten ein wichtiges Kriterium, die Antikörpertiter repräsentieren, von denen angenommen wird, dass sie mit einer Schutzwirkung korrelieren. Über diese klinischen Minimalanforderungen hinaus wird von geeigneten pandemischen Musterimpfstoffen verlangt, dass zum Erreichen solcher Seroprotektionsraten nicht mehr als 2 Teildosen notwendig sind. Impfkonzepte, die mehr als 2 Teildosen für eine effektive Grundimmunisierung benötigen, lassen sich nicht in die Logistik pandemischer Impfkampagnen integrieren. Wünschenswert ist zudem, dass nach der zweiten Impfung Seroprotektionsraten erzielt werden, die die Minimalanforderung 70% für Erwachsene von 18 bis 60 Jahren bzw. 60% für Personen, die älter als 60 Jahre sind, signifikant übertreffen. Tabelle 3 vergleicht die bisher veröffentlichten Daten bezüglich der Seroprotektionsraten, die mit 3 zugelassenen H5N1-basierten Musterimpfstoffen erzielt werden. Sie sind repräsentativ für andere Impfstoffe, die derselben Impfstoffklasse angehören (Ganzvirus, Spalt- oder Untereinheitenimpfstoff). Nicht aufgeführt sind die Seroprotektionsraten, die mit nichtadjuvantierten bzw. mit Aluminiumhydroxid- (AlOH-) adjuvantierten H5N1-Spalt- oder -Untereinheitenimpfstoffen erzielt werden. Solche H5N1-Impfstoffe entsprechen bei Weitem nicht den Minimalanforderungen, sind also zu wenig immunogen.
12 Seite 13 Impfstoff Seroprotektionsraten (SPR, %) Tag nach der ersten Impfung Tag nach der zweiten Impfung Celvapan (Baxter) H5N1-Ganzvirusimpfstoff 1 55,5 2 57,9 a 1 65,4 2 67,7 a 7,5 µg HA-Antigen, nichtadjuvantiert Focetria (Novartis) H5N1-Untereinheitenimpfstoff 7,5 µg HA-Antigen, mit MF b 1 86 b adjuvantiert Pandemrix (GSK) H5N1-Spaltimpfstoff 3,75 µg HA-Antigen, mit AS ,5 a 1 94,3 a adjuvantiert AS03 Adjuvant System 03, GSK GlaxoSmithKline. a Hämagglutinationsinhibitions- (HAI-)Test. b Single-Radial-Hemolysis- (SRH-)Test. 1 Erwachsene (18 bis 60 Jahre). 2 Ältere (>60 Jahre). Tabelle 3 Seroprotektionsraten nach ein- oder zweimaliger Impfung mit unterschiedlichen zugelassenen H5N1-Musterimpfstoffen [2, 11, 12] Die in Tabelle 3 und im Text zusammengestellten Daten bestätigen einige schon früher erwähnte Sachverhalte, nämlich die direkte Korrelation zwischen der Antigenpräparation und den immunogenen Eigenschaften des HA-Antigens. Unadjuvantierte H5N1-Ganzvirusimpfstoffe sind erheblich immunogener als die entsprechenden H5N1-Spalt- oder -Untereinheitenimpfstoffe. Dieses Defizit kann jedoch über den Zusatz geeigneter Adjuvanssysteme, z. B. MF59 oder AS03, kompensiert werden. Derart formulierte H5N1-HA-Antigene übertreffen dann in ihrer Immunogenität die entsprechenden Ganzvirusimpfstoffe. Bemerkenswert ist auch, dass die unterschiedliche Immunogenität der Spalt- und Untereinheitenimpfstoffe trotz des Zusatzes der leistungsstarken Adjuvanssysteme MF59 bzw. AS03 bestehen bleibt. Bei keinem der Studienteilnehmer wurden signifikante Basisimmunitätstiter für den Subtyp H5N1 festgestellt. Dies war auch nicht zu erwarten, denn Influenza-A-Viren des Subtyps H5N1 können nur Vögel, nicht jedoch den Menschen über natürliche Infektketten infizieren. Impfungen gegen H5N1 erfordern deshalb eine Grundimmunisierung. Die Auffrischung einer vorbestehenden Grundimmunität ist nicht möglich. Dies bestätigt sich durch die Beobachtung, dass eine einzige Dosis der beschriebenen H5N1-Musterimpfstoffe nicht ausreicht, um die erforderlichen Seroprotektionsraten zu erreichen (Tabelle 3, mittlere Spalte). Die in Tabelle 3 erwähnten Testsysteme, HAI- und SRH-Test, zur Bestimmung der Immunantwort nach der ersten und zweiten Teilimpfung wurden im Abschn bereits vorgestellt. An dieser Stelle soll allerdings auch darauf hingewiesen werden, dass die gezeigten Unterschiede in der Immunogenität der einzelnen H5N1- Musterimpfstoffe, zumindest teilweise, auch auf Unterschiedlichkeiten und Schwankungen in den von den Herstellern verwendeten Testsystemen zurückgeführt werden könnten. Alle Hersteller von H5N1-Musterimpfstoffen mussten deshalb die erzielten HAI- oder SRH-Testergebnisse durch Resultate aus
13 Seite 14 sog. Mikroneutralisationstests, mit denen die Titer funktionaler, d. h. virusneutralisierender Antikörper bestimmt werden können, bestätigen. Der für die Versorgung Deutschlands vorgesehene Pandemieimpfstoff Pandemrix von GSK und der Pandemieimpfstoff Focetria von Novartis stellen den derzeitigen Goldstandard dar. Pandemieimpfstoffe, die immunologisch naive Immunsysteme noch effektiver stimulieren können, sind weltweit nicht verfügbar Adjuvanssysteme Im Zuge der Entwicklung der H5N1-Musterimpfstoffe hat sich sehr bald und deutlich gezeigt, dass das ansonsten vielfach bewährte Adjuvans AlOH zur Verbesserung der Immunogenität des Influenzavirus-HA-Antigens in immunologisch naiven Immunsystemen nur unzureichend oder gar nicht geeignet ist. Aluminiumhydroxid bewirkt bei H5N1-Spalt- oder -Untereinheitenantigenen eine marginale Erhöhung der Immunogenität, bei H5N1-Ganzvirusimpfstoffen ist im Vergleich zum unadjuvantierten Antigen kein Effekt mehr feststellbar; in einem Fall bewirkte der Zusatz von AlOH sogar die Verschlechterung der immunogenen Eigenschaften. Allerdings muss auch betont werden, dass das Konzept der Antigeneinsparung über die Verwendung von AlOH bei der Auffrischung einer vorbestehenden Grundimmunität entwickelt wurde. In geprimten Immunsystemen, also bei bestehender Grundimmunität gegenüber Influenzavirusantigenen, kann ein reduzierter Antigengehalt durch den Zusatz von AlOH kompensiert werden [13, 14]. Auf ungeprimte Immunsysteme, wie dies für H5N1-Antigene der Fall ist, lässt sich dieser Ansatz jedoch nicht übertragen. Somit fokussierte sich die Weiterentwicklung der H5N1-Musterimpfstoffe auf die Verwendung neuer Adjuvanssystme, den Öl-in-Wasser-basierten Adjuvanzien. Mit einem solchen Adjuvanssystem, MF59 von Novartis, ergab sich im Rahmen der Verwendung in einem zugelassenen saisonalen Influenzaimpfstoff (Fluad, Novartis, Siena, Italien) bereits eine Reihe von Hinweisen, dass Impfstoffformulierungen dieser Art auch dann effektiv sind, wenn keine oder eine ansonsten nur unzureichende Grundimmunität vorliegt. Wie in den vorhergehenden Abschnitten bereits ausführlich beschrieben wurde, ergeben sich über solche Formulierungen hervorragende Pandemieimpfstoffe, die trotz eines niedrigeren HA-Antigengehalts sehr hohe Seroprotektionsraten (85 95%) nach nur 2 Teildosen bewirken. Die Zusammensetzung der von GSK (AS03) und Novartis (MF59) verwendeten neuen Adjuvanssysteme ist in Tabelle 4 gegenübergestellt.
14 Seite 15 Funktion der Adjuvanskomponenten MF59 AS03 Ölphase Squalen (9,75 mg) Squalen (10,68 mg) α-tocopherol (11,68 mg) Lipophiler Oberflächenfaktor Sorbitoltrioleat (1,175 mg) Hydrophiler Oberflächenfaktor Polysorbat 80 (1,175 mg) Polysorbat 80 (4,85 mg) Wasserphase Zitratpuffer PBS Herstellungsverfahren Mikrofluidisierung Mikrofluidisierung Durchschnittliche Partikelgröße (nm) PBS phosphate buffered saline Tabelle 4 Zusammensetzung der Öl-in-Wasser-basierten Adjuvanssysteme MF59 (Novartis) und AS03 (GSK) sowie Funktion der Komponenten Grundsätzlich sind die Adjuvanskomponenten MF59 und AS03 biologische Substanzen, die auch in anderen Arzneimitteln, in Kosmetika und in Lebensmitteln Verwendung finden. Die Annahme, es handle hierbei um Nanopartikel und somit um eine vollständig neue Substanzgruppe, deren Unbedenklichkeit noch nicht geklärt ist, ist unzutreffend. Partikel mit einer Größe von nm entsprechen nicht der Definition von Nanopartikeln, deren Größe nur wenige Nanometer umfasst und die deshalb gänzlich andere und im Vergleich zu den Adjuvanspartikeln unbekannte pharmakologische Eigenschaften haben können. Eine ausführliche Risikoanalyse betreffend die Öl-in-Wasser-basierten Adjuvanssysteme, insbesondere was deren Anwendung in der Schwangerschaft anbelangt, findet sich auf der Homepage des PEI ( cln_116/nn_ /de/infos/fachkreise/impf-fach/schweine influenza/pand-impf/ schweineinfluenza-impfstoffe-schwangerschaft.html [15]) Andere Inhaltsstoffe Mit Ausnahme der Antigenzusammensetzung und im Einzelfall der Verwendung eines Adjuvanssystems unterscheiden sich die Inhaltstoffe der Pandemieimpfstoffe nicht von denen der saisonalen Influenzaimpfstoffe. Soweit Pandemieimpfstoffe nicht in Einzelspritzen, sondern in Mehrdosenbehältnissen abgefüllt werden, folgen einige Hersteller der Empfehlung der WHO und verwenden das Konservierungsmittel Thiomersal. Obwohl Thiomersal aufgrund von Sicherheitsbedenken aus nahezu allen in Deutschland verfügbaren Impfstoffen entfernt wurde, ist die Verwendung in Mehrdosenverhältnissen vertretbar. Die Vermeidung mikrobiologischer Kontaminationen während der Entnahme der Einzeldosen überwiegt nämlich die vermuteten oder tatsächlichen Risiken, die mit der Verabreichung quecksilberhaltiger Substanzen verbunden sind. Die am Ende des Abschn zitierte Risikoanalyse des PEI erstreckt sich auch auf die Verwendung von Thiomersal. Der für Deutschland zunächst zur Verfügung stehende Pandemieimpfstoff Pandemrix von GSK enthält 5 µg Thiomersal/Dosis. Der zweite für Deutschland vorgesehene Pandemieimpfstoff ist ein zellbasierter H1N1v-Impfstoff von Novartis (Celtura). Dieser wird für Deutschland in Einzelspritzen bereitgestellt und benötigt
15 Seite 16 demzufolge kein Thiomersal. Das PEI wird den Bewertungsbericht zu diesem Impfstoff voraussichtlich Ende Oktober 2009 auf seiner Homepage ( veröffentlichen, sobald das nationale Zulassungsverfahren erfolgreich beendet wurde Anpassung der Musterimpfstoffe an H1N1v Die Anpassungen der H5N1-Musterzulassungen für Celvapan, Focetria und Pandemrix an den pandemischen H1N1v-Influenzavirusstamm wurden Ende September/Anfang Oktober 2009 infolge der positiven Empfehlung des CHMP auch formal von der EU-Kommission genehmigt ( Inhaltlicher Schwerpunkt dieser Änderungsverfahren war der Nachweis, dass die Herstellung und somit die Qualität der H1N1v-Impfstoffe der ursprünglichen Zulassung für die H5N1-Musterimpfstoffe entspricht. Die Bewertung der dazu notwendigen Daten erfolgte in einem sog. rollierenden Verfahren, d. h. einzelne Datensegmente wurden von den zuständigen Behörden geprüft, sobald diese von den Herstellern eingereicht worden waren. Dieses Verfahren ist an den Pandemiefall angepasst und bedeutet eine enorme Zeitersparnis, da sich die Vollständigkeit der Genehmigungsunterlagen während des Verfahrens ergibt und nicht erst abgewartet werden muss, bis ein Hersteller alle geforderten Daten und Unterlagen gemäß den Vorgaben für ein normales Zulassungsverfahren zusammengestellt und zur Prüfung eingereicht hat. Neben den Daten zur Herstellung gibt es mittlerweile auch erste veröffentlichte Ergebnisse aus klinischen Studien mit den tatsächlichen H1N1v- Pandemieimpfstoffen in gesunden Erwachsenen im Alter von 18 bis 60 Jahren. Diese Resultate sind einigermaßen überraschend, denn sie weichen doch erheblich von den klinischen Erkenntnissen und Erwartungen ab, die mit den H5N1-Impfstoffen gewonnen wurden und in zwei Punkten zusammengefasst werden können: Es besteht offenbar eine relative hohe Grundimmunität gegenüber H1N1- Antigenen bei Erwachsenen im Alter von 18 bis 60 Jahren. Eine einmalige Impfung mit antigenreduzierten und adjuvantierten bzw. nichtantigenreduzierten und unadjuvantierten H1N1v-Impfstoffen induziert Seroprotektionsraten in einer Größenordnung von 80 90%, die mit den H5N1-Musterimpfstoffen nur mit 2 Teildosen erreicht werden konnte. Tabelle 5 beschreibt diesen Sachverhalt für einen nichtadjuvantierten H1N1v- Impfstoff eines australischen Herstellers (CSL) von Influenzaspaltimpfstoffen. Die in dieser Studie vor der Impfung gemessenen HAI-Titer sind nicht unbedingt repräsentativ für Europa. Die Influenzasaison auf der südlichen Hemisphäre geht gerade ihrem Ende entgegen und wurde fast ausschließlich von dem pandemischen Influenzavirus H1N1v bestimmt, sodass von hohen Seroprävalenzraten ausgegangen werden muss. Deshalb sind die mittleren HAI- Titer vor der Impfung bei australischen Probanden derzeit etwa doppelt bis dreimal so hoch wie bei Probanden der nördlichen Hemisphäre. Sehr wohl vergleichbar sind jedoch die HAI-Titer nach der ersten Impfung. Unabhängig davon, wo (Australien, China, Europa) und mit welchem Impfstoff H1N1v-spezifische klinische Daten verfügbar gemacht werden, bestätigten sich die in Australien generierten Daten.
16 Seite 17 Impfstoff H1N1v (CSL, Australien) H1N1v-Spaltimpfstoff 15 µg HA-Antigen, nichtadjuvantiert H1N1v (CSL, Australien) H1N1v-Spaltimpfstoff 30 µg HA-Antigen, nichtadjuvantiert a Hämagglutinationsinhibitions- (HAI-)Test. Seroprotektionsraten (SPR, %) H1N1v-Basistiter (vor der Impfung) Tag 21 nach der ersten Impfung 1 32,8 2 33,9 a 2 93, a 2 20,7 1 38,7 a 2 87,9 1 98,4 a 1 Erwachsene (18 bis 49 Jahre). 2 Erwachsene (50 bis 64 Jahre). Tabelle 5 Seroprotektionsraten vor der Impfung und nach der ersten Dosis eines H1N1v- Impfstoffs [16] Ob auch eine im Vergleich zum H5N1-HA-Antigen höhere natürliche Immunogenität des HA-Antigens des H1N1v-Influenzavirus-A-Subtyps zu diesen Ergebnissen beiträgt, kann derzeit noch nicht abgeschätzt werden. Hier sind insbesondere die Ergebnisse der klinischen Studien an Kindern, die noch keine Grundimmunität aufgebaut haben, abzuwarten. Somit muss die optimale Anwendung der H1N1v-Impfstoffe (1 oder 2 Dosen) im Bezug auf die einzelnen Produkte (adjuvantiert oder nichtadjuvantiert, Ganzvirus-, Spalt- oder Untereinheitenimpfstoff) sowie hinsichtlich der unterschiedlichen Altersund Risikokategorien (z. B. Kinder, Schwangere, Ältere) auf der Basis der neu hinzukommenden H1N1v-Daten fortlaufend präzisiert werden. Die für Deutschland zur Verfügung stehenden Impfstoffoptionen lassen ein solches flexibles Vorgehen problemlos zu Verträglichkeit Die Pandemieimpfstoffe sind hinsichtlich des Nebenwirkungsprofils nicht von den saisonalen Influenzaimpfstoffen zu unterscheiden. Dennoch werden immer wieder Zweifel geäußert, ob insbesondere die adjuvantierten Pandemieimpfstoffe ausreichend im Bezug auf ihre Verträglichkeit geprüft worden sind. Für Erwachsene sind die diesbezüglich verfügbaren Daten zur Erfassung der Nebenwirkungen umfangreich. Für Kinder stehen erheblich weniger direkte und indirekte Datensätze zur Verfügung. Für Risikogruppierungen, an erster Stelle Schwangere, gibt es für adjuvantierte Pandemieimpfstoffe keine klinischen Daten. Tabelle 6 fasst die bisher generierten Daten zur klinischen Überprüfung der Verträglichkeit pandemischer Musterimpfstoffe und, soweit zutreffend, deren nichtadjuvantierter Pendants zusammen.
17 Seite 18 Impfstoff (Adjuvans) Erwachsene 18 bis 60 Jahre Erwachsene >60 Jahre Kinder Andere Verträglichkeitsdaten Celvapan (unadjuvantiert) Noch nicht verfügbar Nicht zutreffend Focetria (MF59) Kleinkinder, Kinder, Heranwachsende und Jugendliche von 6 Monaten bis 17 Jahren Fluad ist seit 1997 als MF59-haltiger saisonaler Influenzaimpfstoff zugelassen Pandemrix (AS03) Kinder im Alter von 3 bis 6 Jahren AS03 wird derzeit in Erwachsenen mit HA- Antigenen saisonaler Influenzaviren in ausgedehnten klinischen Studien untersucht Tabelle 6 Zusammenstellung der für unterschiedliche Altersgruppen insgesamt verfügbaren Verträglichkeitsdaten für adjuvantierte und nichtadjuvantierte H5N1-Musterimpfstoffe In Abhängigkeit von der verfügbaren Datenlage muss im Bezug auf die einzelnen Alters- und Personengruppen eine kontinuierliche Nutzen-Risiko-Analyse der einzelnen H1N1v-Impfstoffe durchgeführt werden. Neu hinzukommende Daten aus kontrollierten klinischen Studien, die derzeit mit allen H1N1v-Impfstoffen durchgeführt werden, ermöglichen eine immer präzisere Verrechnung des Nutzens der Impfung mit den möglichen Impfrisiken. An die Zulassungen der H1N1v-Impfstoffe sind zudem Risikomanagement- und Pharmakovigilanzpläne geknüpft, in denen u. a. die engmaschige Überwachung von mindestens 9000 Impflingen aller Alters- und Risikogruppen pro Impfstoff gefordert ist. Mit diesen Systemen lassen sich auch seltene Nebenwirkungen erfassen, die in klinischen Studien nicht erkannt werden können. 7.3 Nutzen-Risiko-Analyse Alle Planungen zur Entwicklung, Herstellung und Anwendung von Pandemieimpfstoffen haben sich am schlimmsten anzunehmenden Fall orientiert, also einer pandemischen Situation, die mit der Spanischen Grippe ab dem Jahr 1918 zu vergleichen ist. Die Resultate dieser Bemühungen wurden in den vorangegangenen Abschnitten ausführlich beschrieben. Es stehen nunmehr antigenreduzierte und hoch immunogene Pandemieimpfstoffe zur Verfügung, mit denen sich die Auswirkungen einer aggressiven Pandemie kontrollieren lassen. Die Anwendung der H1N1v-Impfstoffe muss nun dem tatsächlichen, also derzeit viel milderen pandemischen Szenario angepasst werden. Abbildung 1 soll verdeutlichen, wie Pandemieimpfstoffe unter den realen Voraussetzungen optimal angewendet werden können. Der gegenwärtige Pandemieverlauf ist für die individuellen Alters- und Risikogruppierungen zwischen den beiden Extremen milde WHO-Phase 6 und schwere WHO-Phase 6 einzuordnen. In Abhängigkeit vom Risiko, das eine Infektion mit dem H1N1v-Virus für die genannten
18 Seite 19 Personengruppen darstellt, muss die Anwendung der Impfstoffe durch den Umfang der verfügbaren klinischen Daten begründet werden. Sind die gesundheitlichen Folgen einer Infektion gering bis mäßig, kann die Anwendung eines Pandemieimpfstoffs nur über ausreichende klinische Daten begründet werden. Bedeutet eine Infektion ein erhebliches Gesundheitsrisiko, kann sie auch auf der Basis von wenigeren oder gar keinen alters- bzw. risikogruppenspezifischen klinischen Daten begründet werden. In jedem Fall überwiegt dann der Nutzen der Impfung die bekannten und unbekannten Impfrisiken. Auf der Basis einer solchen dynamischen Nutzen-Risiko-Analyse ergibt sich für jede Personengruppe zu jedem beliebigen Zeitpunkt der fortlaufenden Pandemie eine Anleitung zur optimalen Anwendung der verfügbaren H1N1v-Impfstoffe. Individuelles Risiko (z.b. Krankheitsverlauf) Schwere WHO Phase 6 Klinische Daten?? Hohes Risiko Klinische Daten??? Milde WHO Phase 6 Moderates Risiko H1N1v gegenwärtige Situation? Minimum???? Maximum Erforderliche klinische Daten zur optimalen Anwendung eines Pandemieimpfstoffs Abbildung 1 Dynamische Nutzen-Risiko-Analyse zur optimalen Anwendung von pandemischen H1N1v-Impfstoffen Aus diesem Konzept leitet sich auch die Schlussfolgerung ab, dass Überlegungen zur Beschaffung von Pandemieimpfstoffen nicht unbedingt deckungsgleich mit Überlegungen zu deren optimaler Anwendung sind. Wichtig ist zunächst, dafür Sorge zu tragen, dass die Pandemieimpfstoffe in ausreichendem Maß verfügbar sind. Wie sie am sinnvollsten angewendet werden, hängt hauptsächlich von der weiteren Entwicklung der derzeitigen Pandemie ab, die nicht verlässlich vorherbestimmt werden kann und somit abgewartet werden muss.
19 Seite Literatur Pfleiderer M (2007) Herstellung und Qualitätskontrolle von Impfstoffen. Pharm Unserer Zeit 37(1): Pfleiderer M (2009) Kap. 6: Influenzaimpfstoffe. In: Haas W (Hrsg) Influenza. Prävention, Diagnostik, Therapie und öffentliche Gesundheit. Elsevier Urban & Fischer, München, S nnn=true Dossier Structure and Content for Pandemic Influenza Vaccine Marketing Authorisation Application, CPMP/4717/03; Submission of Marketing Authorisation Applications for Pandemic Influenza Vaccines through the Centralised Procedure, EMEA/CPMP/4986/ Hehme N, Engelmann H, Künzel W, Neumeier E, Sänger R (2002) Pandemic preparedness: lessons learnt from H2N2 and H9N2 candidate vaccines. Med Microbiol Immunol 191(3-4): Hehme N, Engelmann H, Kuenzel W, Neumeier E, Saenger R (2004) Immunogenicity of a monovalent, aluminium adjuvanted influenza whole virus vaccine for pandemic use. Virus Res 103(1-2): Greenberg ME, Lai MH, Hartel GF, Wichems CH, Gittleson C, Bennet J, Dawson G, Hu W, Leggio C, Washington D, Basser RL (2009) Response after one dose of a monovalent influenza A (H1N1) 2009 vaccine preliminary report. N Engl J Med, DOI /NEJMMoa
InVo. Information zu Verordnungen in der GKV. Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen. Stand: Februar 2010
 Nr. 1 2010 InVo Information zu Verordnungen in der GKV Stand: Februar 2010 Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen Bisher konnten Sie als Arzt Arzneimittel (z. B.
Nr. 1 2010 InVo Information zu Verordnungen in der GKV Stand: Februar 2010 Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen Bisher konnten Sie als Arzt Arzneimittel (z. B.
WAS finde ich WO im Beipackzettel
 WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
Die Sicht der EMEA. für Zulassungs-, Therapie- und. Berlin-Brandenburgische Akademie der
 Lebensqualität und Patientennutzen Die Sicht der EMEA PMS-Workshop: Lebensqualität als Kriterium für Zulassungs-, Therapie- und Erstattungsentscheidungen. Berlin-Brandenburgische Akademie der Wissenschaften
Lebensqualität und Patientennutzen Die Sicht der EMEA PMS-Workshop: Lebensqualität als Kriterium für Zulassungs-, Therapie- und Erstattungsentscheidungen. Berlin-Brandenburgische Akademie der Wissenschaften
RECHT AKTUELL. GKS-Rechtsanwalt Florian Hupperts informiert über aktuelle Probleme aus dem Beamten- und Disziplinarrecht
 RECHT AKTUELL GKS-Rechtsanwalt Florian Hupperts informiert über aktuelle Probleme aus dem Beamten- und Disziplinarrecht Rechtsanwalt Florian Hupperts Was muss eigentlich in einer Konkurrentenmitteilung
RECHT AKTUELL GKS-Rechtsanwalt Florian Hupperts informiert über aktuelle Probleme aus dem Beamten- und Disziplinarrecht Rechtsanwalt Florian Hupperts Was muss eigentlich in einer Konkurrentenmitteilung
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren
 Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
10.000 10.000. an Masern erkrankt. an Mumps erkrankt. mit Röteln infiziert
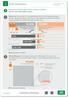 Nutzen: Bei Viruskontakt ist mein geimpftes Kind auch künftig besser gegen Masern, Mumps und Röteln geschützt. Je mehr Menschen geimpft sind, desto unwahrscheinlicher werden Kontakte mit dem Virus. ohne
Nutzen: Bei Viruskontakt ist mein geimpftes Kind auch künftig besser gegen Masern, Mumps und Röteln geschützt. Je mehr Menschen geimpft sind, desto unwahrscheinlicher werden Kontakte mit dem Virus. ohne
infach Geld FBV Ihr Weg zum finanzellen Erfolg Florian Mock
 infach Ihr Weg zum finanzellen Erfolg Geld Florian Mock FBV Die Grundlagen für finanziellen Erfolg Denn Sie müssten anschließend wieder vom Gehaltskonto Rückzahlungen in Höhe der Entnahmen vornehmen, um
infach Ihr Weg zum finanzellen Erfolg Geld Florian Mock FBV Die Grundlagen für finanziellen Erfolg Denn Sie müssten anschließend wieder vom Gehaltskonto Rückzahlungen in Höhe der Entnahmen vornehmen, um
Häufig wiederkehrende Fragen zur mündlichen Ergänzungsprüfung im Einzelnen:
 Mündliche Ergänzungsprüfung bei gewerblich-technischen und kaufmännischen Ausbildungsordnungen bis zum 31.12.2006 und für alle Ausbildungsordnungen ab 01.01.2007 Am 13. Dezember 2006 verabschiedete der
Mündliche Ergänzungsprüfung bei gewerblich-technischen und kaufmännischen Ausbildungsordnungen bis zum 31.12.2006 und für alle Ausbildungsordnungen ab 01.01.2007 Am 13. Dezember 2006 verabschiedete der
GeoPilot (Android) die App
 GeoPilot (Android) die App Mit der neuen Rademacher GeoPilot App machen Sie Ihr Android Smartphone zum Sensor und steuern beliebige Szenen über den HomePilot. Die App beinhaltet zwei Funktionen, zum einen
GeoPilot (Android) die App Mit der neuen Rademacher GeoPilot App machen Sie Ihr Android Smartphone zum Sensor und steuern beliebige Szenen über den HomePilot. Die App beinhaltet zwei Funktionen, zum einen
Wie funktioniert ein Mieterhöhungsverlangen?
 Wie funktioniert ein Mieterhöhungsverlangen? Grundsätzlich steht einem Vermieter jederzeit die Möglichkeit offen, die gegenwärtig bezahlte Miete gemäß 558 BGB an die ortsübliche Miete durch ein entsprechendes
Wie funktioniert ein Mieterhöhungsverlangen? Grundsätzlich steht einem Vermieter jederzeit die Möglichkeit offen, die gegenwärtig bezahlte Miete gemäß 558 BGB an die ortsübliche Miete durch ein entsprechendes
Mobile Intranet in Unternehmen
 Mobile Intranet in Unternehmen Ergebnisse einer Umfrage unter Intranet Verantwortlichen aexea GmbH - communication. content. consulting Augustenstraße 15 70178 Stuttgart Tel: 0711 87035490 Mobile Intranet
Mobile Intranet in Unternehmen Ergebnisse einer Umfrage unter Intranet Verantwortlichen aexea GmbH - communication. content. consulting Augustenstraße 15 70178 Stuttgart Tel: 0711 87035490 Mobile Intranet
Mitteilung der Kommission. Muster für eine Erklärung über die zur Einstufung als KMU erforderlichen Angaben (2003/C 118/03)
 20.5.2003 Amtsblatt der Europäischen Union C 118/5 Mitteilung der Kommission Muster für eine Erklärung über die zur Einstufung als KMU erforderlichen Angaben (2003/C 118/03) Durch diese Mitteilung soll
20.5.2003 Amtsblatt der Europäischen Union C 118/5 Mitteilung der Kommission Muster für eine Erklärung über die zur Einstufung als KMU erforderlichen Angaben (2003/C 118/03) Durch diese Mitteilung soll
Service-Angebote des BPI
 Pharmakovigilanz Service-Angebote des BPI BPI-Pharmakovigilanz Knowledge Base Mit dem EU-Pharmapackage und dem Zweiten Gesetz zur Änderung arzneimittelrechtlicher und anderer Vorschriften vom 19. Oktober
Pharmakovigilanz Service-Angebote des BPI BPI-Pharmakovigilanz Knowledge Base Mit dem EU-Pharmapackage und dem Zweiten Gesetz zur Änderung arzneimittelrechtlicher und anderer Vorschriften vom 19. Oktober
e-book Garantie und Gewährleistung bei Insolvenz eines Automobilherstellers Autor: Dr. jur. Götz Knoop
 e-book Garantie und Gewährleistung bei Insolvenz eines Autor: Dr. jur. Götz Knoop Inhaltsverzeichnis: 1. GARANTIEN BEI INSOLVENZ EINES AUTOMOBILHERSTELLERS 3 1.1. Garantie des Herstellers 3 1.2. Garantie
e-book Garantie und Gewährleistung bei Insolvenz eines Autor: Dr. jur. Götz Knoop Inhaltsverzeichnis: 1. GARANTIEN BEI INSOLVENZ EINES AUTOMOBILHERSTELLERS 3 1.1. Garantie des Herstellers 3 1.2. Garantie
Osteoporose. Ein echtes Volksleiden. Schon jetzt zählen die Osteoporose und die damit verbundene erhöhte Brüchigkeit der Knochen
 Osteoporose Osteoporose 9 Osteoporose Ein echtes Volksleiden Schon jetzt zählen die Osteoporose und die damit verbundene erhöhte Brüchigkeit der Knochen in den entwickelten Ländern zu den häufigsten Erkrankungen
Osteoporose Osteoporose 9 Osteoporose Ein echtes Volksleiden Schon jetzt zählen die Osteoporose und die damit verbundene erhöhte Brüchigkeit der Knochen in den entwickelten Ländern zu den häufigsten Erkrankungen
geben. Die Wahrscheinlichkeit von 100% ist hier demnach nur der Gehen wir einmal davon aus, dass die von uns angenommenen
 geben. Die Wahrscheinlichkeit von 100% ist hier demnach nur der Vollständigkeit halber aufgeführt. Gehen wir einmal davon aus, dass die von uns angenommenen 70% im Beispiel exakt berechnet sind. Was würde
geben. Die Wahrscheinlichkeit von 100% ist hier demnach nur der Vollständigkeit halber aufgeführt. Gehen wir einmal davon aus, dass die von uns angenommenen 70% im Beispiel exakt berechnet sind. Was würde
1.1 Allgemeines. innerhalb der Nachtzeit (19:00 24:00) Gesamte Normalarbeitszeit (16:00 19:00)
 Abschnitt 1 Überstunden in der Nacht 11 1.1 Allgemeines # Die Ermittlung und Abrechnung von Überstunden unter der Woche, an Sonn- und Feiertagen wurde bereits im Band I, Abschnitt 3 behandelt. Sehen wir
Abschnitt 1 Überstunden in der Nacht 11 1.1 Allgemeines # Die Ermittlung und Abrechnung von Überstunden unter der Woche, an Sonn- und Feiertagen wurde bereits im Band I, Abschnitt 3 behandelt. Sehen wir
Fragebogen: Abschlussbefragung
 Fragebogen: Abschlussbefragung Vielen Dank, dass Sie die Ameise - Schulung durchgeführt haben. Abschließend möchten wir Ihnen noch einige Fragen zu Ihrer subjektiven Einschätzung unseres Simulationssystems,
Fragebogen: Abschlussbefragung Vielen Dank, dass Sie die Ameise - Schulung durchgeführt haben. Abschließend möchten wir Ihnen noch einige Fragen zu Ihrer subjektiven Einschätzung unseres Simulationssystems,
Soja-Lebensmittel - Quelle von hochwertigem Eiweiß
 Soja-Lebensmittel - Quelle von hochwertigem Eiweiß Thesenpapier des wissenschaftlichen Beirats der ENSA Einleitung Eiweiß ist ein wichtiger Grundnährstoff, der für das Wachstum und die Reparatur aller
Soja-Lebensmittel - Quelle von hochwertigem Eiweiß Thesenpapier des wissenschaftlichen Beirats der ENSA Einleitung Eiweiß ist ein wichtiger Grundnährstoff, der für das Wachstum und die Reparatur aller
Verband der TÜV e. V. STUDIE ZUM IMAGE DER MPU
 Verband der TÜV e. V. STUDIE ZUM IMAGE DER MPU 2 DIE MEDIZINISCH-PSYCHOLOGISCHE UNTERSUCHUNG (MPU) IST HOCH ANGESEHEN Das Image der Medizinisch-Psychologischen Untersuchung (MPU) ist zwiespältig: Das ist
Verband der TÜV e. V. STUDIE ZUM IMAGE DER MPU 2 DIE MEDIZINISCH-PSYCHOLOGISCHE UNTERSUCHUNG (MPU) IST HOCH ANGESEHEN Das Image der Medizinisch-Psychologischen Untersuchung (MPU) ist zwiespältig: Das ist
Energetische Klassen von Gebäuden
 Energetische Klassen von Gebäuden Grundsätzlich gibt es Neubauten und Bestandsgebäude. Diese Definition ist immer aktuell. Aber auch ein heutiger Neubau ist in drei (oder vielleicht erst zehn?) Jahren
Energetische Klassen von Gebäuden Grundsätzlich gibt es Neubauten und Bestandsgebäude. Diese Definition ist immer aktuell. Aber auch ein heutiger Neubau ist in drei (oder vielleicht erst zehn?) Jahren
Gründe für fehlende Vorsorgemaßnahmen gegen Krankheit
 Gründe für fehlende Vorsorgemaßnahmen gegen Krankheit politische Lage verlassen sich auf Familie persönliche, finanzielle Lage meinen, sich Vorsorge leisten zu können meinen, sie seien zu alt nicht mit
Gründe für fehlende Vorsorgemaßnahmen gegen Krankheit politische Lage verlassen sich auf Familie persönliche, finanzielle Lage meinen, sich Vorsorge leisten zu können meinen, sie seien zu alt nicht mit
Der ohne sachlichen Grund befristete Arbeitsvertrag
 Der ohne sachlichen Grund befristete Arbeitsvertrag 1. Allgemeines Die Befristung von Arbeitsverträgen ist im Teilzeit- und Befristungsgesetz (TzBfG) geregelt. Zu unterscheiden sind Befristungen des Arbeitsverhältnisses
Der ohne sachlichen Grund befristete Arbeitsvertrag 1. Allgemeines Die Befristung von Arbeitsverträgen ist im Teilzeit- und Befristungsgesetz (TzBfG) geregelt. Zu unterscheiden sind Befristungen des Arbeitsverhältnisses
Monitoring-Service Anleitung
 Anleitung 1. Monitoring in CrefoDirect Wie kann Monitoring über CrefoDirect bestellt werden? Bestellung von Monitoring beim Auskunftsabruf Beim Auskunftsabruf kann das Monitoring direkt mitbestellt werden.
Anleitung 1. Monitoring in CrefoDirect Wie kann Monitoring über CrefoDirect bestellt werden? Bestellung von Monitoring beim Auskunftsabruf Beim Auskunftsabruf kann das Monitoring direkt mitbestellt werden.
Grundfunktionen und Bedienung
 Kapitel 13 Mit der App Health ist eine neue Anwendung in ios 8 enthalten, die von vorangegangenen Betriebssystemen bislang nicht geboten wurde. Health fungiert dabei als Aggregator für die Daten von Fitness-
Kapitel 13 Mit der App Health ist eine neue Anwendung in ios 8 enthalten, die von vorangegangenen Betriebssystemen bislang nicht geboten wurde. Health fungiert dabei als Aggregator für die Daten von Fitness-
Was ist clevere Altersvorsorge?
 Was ist clevere Altersvorsorge? Um eine gute Altersvorsorge zu erreichen, ist es clever einen unabhängigen Berater auszuwählen Angestellte bzw. Berater von Banken, Versicherungen, Fondsgesellschaften und
Was ist clevere Altersvorsorge? Um eine gute Altersvorsorge zu erreichen, ist es clever einen unabhängigen Berater auszuwählen Angestellte bzw. Berater von Banken, Versicherungen, Fondsgesellschaften und
DAS GRÜNE REZEPT. Für eine sichere Medikation mit rezeptfreien Arzneimitteln
 DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
Anleitung zum Computercheck Windows Firewall aktivieren oder eine kostenlose Firewall installieren
 Anleitung zum Computercheck Windows Firewall aktivieren oder eine kostenlose Firewall installieren Ziel der Anleitung Sie möchten ein modernes Firewallprogramm für Ihren Computer installieren, um gegen
Anleitung zum Computercheck Windows Firewall aktivieren oder eine kostenlose Firewall installieren Ziel der Anleitung Sie möchten ein modernes Firewallprogramm für Ihren Computer installieren, um gegen
PTV VISWALK TIPPS UND TRICKS PTV VISWALK TIPPS UND TRICKS: VERWENDUNG DICHTEBASIERTER TEILROUTEN
 PTV VISWALK TIPPS UND TRICKS PTV VISWALK TIPPS UND TRICKS: VERWENDUNG DICHTEBASIERTER TEILROUTEN Karlsruhe, April 2015 Verwendung dichte-basierter Teilrouten Stellen Sie sich vor, in einem belebten Gebäude,
PTV VISWALK TIPPS UND TRICKS PTV VISWALK TIPPS UND TRICKS: VERWENDUNG DICHTEBASIERTER TEILROUTEN Karlsruhe, April 2015 Verwendung dichte-basierter Teilrouten Stellen Sie sich vor, in einem belebten Gebäude,
PRÜFMODUL D UND CD. 1 Zweck. 2 Durchführung. 2.1 Allgemeines. 2.2 Antrag
 1 Zweck PRÜFMODUL D UND CD Diese Anweisung dient als Basis für unsere Kunden zur Information des Ablaufes der folgenden EG-Prüfung nach folgenden Prüfmodulen: D CD Es beschreibt die Aufgabe der benannten
1 Zweck PRÜFMODUL D UND CD Diese Anweisung dient als Basis für unsere Kunden zur Information des Ablaufes der folgenden EG-Prüfung nach folgenden Prüfmodulen: D CD Es beschreibt die Aufgabe der benannten
Zeichen bei Zahlen entschlüsseln
 Zeichen bei Zahlen entschlüsseln In diesem Kapitel... Verwendung des Zahlenstrahls Absolut richtige Bestimmung von absoluten Werten Operationen bei Zahlen mit Vorzeichen: Addieren, Subtrahieren, Multiplizieren
Zeichen bei Zahlen entschlüsseln In diesem Kapitel... Verwendung des Zahlenstrahls Absolut richtige Bestimmung von absoluten Werten Operationen bei Zahlen mit Vorzeichen: Addieren, Subtrahieren, Multiplizieren
Die vorliegende Arbeitshilfe befasst sich mit den Anforderungen an qualitätsrelevante
 ISO 9001:2015 Die vorliegende Arbeitshilfe befasst sich mit den Anforderungen an qualitätsrelevante Prozesse. Die ISO 9001 wurde grundlegend überarbeitet und modernisiert. Die neue Fassung ist seit dem
ISO 9001:2015 Die vorliegende Arbeitshilfe befasst sich mit den Anforderungen an qualitätsrelevante Prozesse. Die ISO 9001 wurde grundlegend überarbeitet und modernisiert. Die neue Fassung ist seit dem
Kleine Anfrage mit Antwort
 Niedersächsischer Landtag 16. Wahlperiode Drucksache 16/1659 Kleine Anfrage mit Antwort Wortlaut der Kleinen Anfrage der Abgeordneten Ina Korter (GRÜNE), eingegangen am 29.07.2009 Zwischenbilanz nach vier
Niedersächsischer Landtag 16. Wahlperiode Drucksache 16/1659 Kleine Anfrage mit Antwort Wortlaut der Kleinen Anfrage der Abgeordneten Ina Korter (GRÜNE), eingegangen am 29.07.2009 Zwischenbilanz nach vier
Patienteninformationsbroschüre Valproat
 Patienteninformationsbroschüre Valproat Informationen für Patientinnen Die Informationen in dieser Broschüre sind für Frauen bestimmt, denen Valproat verschrieben wird und die schwanger werden können (Frauen
Patienteninformationsbroschüre Valproat Informationen für Patientinnen Die Informationen in dieser Broschüre sind für Frauen bestimmt, denen Valproat verschrieben wird und die schwanger werden können (Frauen
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Viscosan - Augentropfen Wirkstoff: Hypromellose
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Viscosan - Augentropfen Wirkstoff: Hypromellose Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Viscosan - Augentropfen Wirkstoff: Hypromellose Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
Auswertung des Fragebogens zum CO2-Fußabdruck
 Auswertung des Fragebogens zum CO2-Fußabdruck Um Ähnlichkeiten und Unterschiede im CO2-Verbrauch zwischen unseren Ländern zu untersuchen, haben wir eine Online-Umfrage zum CO2- Fußabdruck durchgeführt.
Auswertung des Fragebogens zum CO2-Fußabdruck Um Ähnlichkeiten und Unterschiede im CO2-Verbrauch zwischen unseren Ländern zu untersuchen, haben wir eine Online-Umfrage zum CO2- Fußabdruck durchgeführt.
Schritt für Schritt zur Krankenstandsstatistik
 Schritt für Schritt zur Krankenstandsstatistik Eine Anleitung zur Nutzung der Excel-Tabellen zur Erhebung des Krankenstands. Entwickelt durch: Kooperationsprojekt Arbeitsschutz in der ambulanten Pflege
Schritt für Schritt zur Krankenstandsstatistik Eine Anleitung zur Nutzung der Excel-Tabellen zur Erhebung des Krankenstands. Entwickelt durch: Kooperationsprojekt Arbeitsschutz in der ambulanten Pflege
Änderung des IFRS 2 Anteilsbasierte Vergütung
 Änderung IFRS 2 Änderung des IFRS 2 Anteilsbasierte Vergütung Anwendungsbereich Paragraph 2 wird geändert, Paragraph 3 gestrichen und Paragraph 3A angefügt. 2 Dieser IFRS ist bei der Bilanzierung aller
Änderung IFRS 2 Änderung des IFRS 2 Anteilsbasierte Vergütung Anwendungsbereich Paragraph 2 wird geändert, Paragraph 3 gestrichen und Paragraph 3A angefügt. 2 Dieser IFRS ist bei der Bilanzierung aller
Ein neues System für die Allokation von Spenderlungen. LAS Information für Patienten in Deutschland
 Ein neues System für die Allokation von Spenderlungen LAS Information für Patienten in Deutschland Ein neues System für die Allokation von Spenderlungen Aufgrund des immensen Mangels an Spenderorganen
Ein neues System für die Allokation von Spenderlungen LAS Information für Patienten in Deutschland Ein neues System für die Allokation von Spenderlungen Aufgrund des immensen Mangels an Spenderorganen
«Eine Person ist funktional gesund, wenn sie möglichst kompetent mit einem möglichst gesunden Körper an möglichst normalisierten Lebensbereichen
 18 «Eine Person ist funktional gesund, wenn sie möglichst kompetent mit einem möglichst gesunden Körper an möglichst normalisierten Lebensbereichen teilnimmt und teilhat.» 3Das Konzept der Funktionalen
18 «Eine Person ist funktional gesund, wenn sie möglichst kompetent mit einem möglichst gesunden Körper an möglichst normalisierten Lebensbereichen teilnimmt und teilhat.» 3Das Konzept der Funktionalen
Das Wachstum der deutschen Volkswirtschaft
 Institut für Wachstumsstudien www.wachstumsstudien.de IWS-Papier Nr. 1 Das Wachstum der deutschen Volkswirtschaft der Bundesrepublik Deutschland 1950 2002.............Seite 2 Relatives Wachstum in der
Institut für Wachstumsstudien www.wachstumsstudien.de IWS-Papier Nr. 1 Das Wachstum der deutschen Volkswirtschaft der Bundesrepublik Deutschland 1950 2002.............Seite 2 Relatives Wachstum in der
Arbeitshilfen zur Auftragsdatenverarbeitung
 Arbeitshilfen zur Auftragsdatenverarbeitung 1 Abgrenzung Die vorliegenden Excel-Tabellen dienen nur als Beispiel, wie anhand von Checklisten die datenschutzrechtlichen Voraussetzungen für die Vergabe einer
Arbeitshilfen zur Auftragsdatenverarbeitung 1 Abgrenzung Die vorliegenden Excel-Tabellen dienen nur als Beispiel, wie anhand von Checklisten die datenschutzrechtlichen Voraussetzungen für die Vergabe einer
Was meinen die Leute eigentlich mit: Grexit?
 Was meinen die Leute eigentlich mit: Grexit? Grexit sind eigentlich 2 Wörter. 1. Griechenland 2. Exit Exit ist ein englisches Wort. Es bedeutet: Ausgang. Aber was haben diese 2 Sachen mit-einander zu tun?
Was meinen die Leute eigentlich mit: Grexit? Grexit sind eigentlich 2 Wörter. 1. Griechenland 2. Exit Exit ist ein englisches Wort. Es bedeutet: Ausgang. Aber was haben diese 2 Sachen mit-einander zu tun?
Pflegende Angehörige Online Ihre Plattform im Internet
 Pflegende Angehörige Online Ihre Plattform im Internet Wissen Wichtiges Wissen rund um Pflege Unterstützung Professionelle Beratung Austausch und Kontakt Erfahrungen & Rat mit anderen Angehörigen austauschen
Pflegende Angehörige Online Ihre Plattform im Internet Wissen Wichtiges Wissen rund um Pflege Unterstützung Professionelle Beratung Austausch und Kontakt Erfahrungen & Rat mit anderen Angehörigen austauschen
Charakteristikum des Gutachtenstils: Es wird mit einer Frage begonnen, sodann werden die Voraussetzungen Schritt für Schritt aufgezeigt und erörtert.
 Der Gutachtenstil: Charakteristikum des Gutachtenstils: Es wird mit einer Frage begonnen, sodann werden die Voraussetzungen Schritt für Schritt aufgezeigt und erörtert. Das Ergebnis steht am Schluß. Charakteristikum
Der Gutachtenstil: Charakteristikum des Gutachtenstils: Es wird mit einer Frage begonnen, sodann werden die Voraussetzungen Schritt für Schritt aufgezeigt und erörtert. Das Ergebnis steht am Schluß. Charakteristikum
Prozessbewertung und -verbesserung nach ITIL im Kontext des betrieblichen Informationsmanagements. von Stephanie Wilke am 14.08.08
 Prozessbewertung und -verbesserung nach ITIL im Kontext des betrieblichen Informationsmanagements von Stephanie Wilke am 14.08.08 Überblick Einleitung Was ist ITIL? Gegenüberstellung der Prozesse Neuer
Prozessbewertung und -verbesserung nach ITIL im Kontext des betrieblichen Informationsmanagements von Stephanie Wilke am 14.08.08 Überblick Einleitung Was ist ITIL? Gegenüberstellung der Prozesse Neuer
Abweichungen. Anforderungen / Zitate aus den Rechtsvorschriften
 Abweichungen Anforderungen / Zitate aus den Rechtsvorschriften AMWHV [...] Alle Abweichungen im Prozess und von der Festlegung der Spezifikation sind zu dokumentieren und gründlich zu untersuchen. [...]
Abweichungen Anforderungen / Zitate aus den Rechtsvorschriften AMWHV [...] Alle Abweichungen im Prozess und von der Festlegung der Spezifikation sind zu dokumentieren und gründlich zu untersuchen. [...]
EU-Verordnung Nr. 1907/2006 (REACH)
 Was bedeutet REACH? REACH ist die EG-Verordnung Nr. 1907/2006 zur Registration, Evaluation, Authorization and Restriction of CHemicals (Registrierung, Bewertung und Zulassung von Chemikalien). Mit dieser
Was bedeutet REACH? REACH ist die EG-Verordnung Nr. 1907/2006 zur Registration, Evaluation, Authorization and Restriction of CHemicals (Registrierung, Bewertung und Zulassung von Chemikalien). Mit dieser
allensbacher berichte
 allensbacher berichte Institut für Demoskopie Allensbach 2006 / Nr. 8 ALTERSVORSORGE THEMA NUMMER 1 Allensbach am Bodensee, Mitte Mai 2006. - Das Thema Altersvorsorge beschäftigt die Bevölkerung immer
allensbacher berichte Institut für Demoskopie Allensbach 2006 / Nr. 8 ALTERSVORSORGE THEMA NUMMER 1 Allensbach am Bodensee, Mitte Mai 2006. - Das Thema Altersvorsorge beschäftigt die Bevölkerung immer
Fragen und Antworten zur Prüfmöglichkeit für ausländische Investitionen (Änderung des Außenwirtschaftsgesetzes und der Außenwirtschaftsverordnung)
 Fragen und Antworten zur Prüfmöglichkeit für ausländische Investitionen (Änderung des Außenwirtschaftsgesetzes und der Außenwirtschaftsverordnung) 1. Welche Investitionen können geprüft werden? Einer Prüfung
Fragen und Antworten zur Prüfmöglichkeit für ausländische Investitionen (Änderung des Außenwirtschaftsgesetzes und der Außenwirtschaftsverordnung) 1. Welche Investitionen können geprüft werden? Einer Prüfung
Diese Broschüre fasst die wichtigsten Informationen zusammen, damit Sie einen Entscheid treffen können.
 Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Allensbach: Das Elterngeld im Urteil der jungen Eltern
 August 2007 Allensbach: Das Elterngeld im Urteil der jungen Eltern Allensbach befragte im Juni 2007 eine repräsentative Stichprobe von 1000 Müttern und Vätern, deren (jüngstes) Kind ab dem 1.1.2007 geboren
August 2007 Allensbach: Das Elterngeld im Urteil der jungen Eltern Allensbach befragte im Juni 2007 eine repräsentative Stichprobe von 1000 Müttern und Vätern, deren (jüngstes) Kind ab dem 1.1.2007 geboren
Die neue Aufgabe von der Monitoring-Stelle. Das ist die Monitoring-Stelle:
 Die neue Aufgabe von der Monitoring-Stelle Das ist die Monitoring-Stelle: Am Deutschen Institut für Menschen-Rechte in Berlin gibt es ein besonderes Büro. Dieses Büro heißt Monitoring-Stelle. Mo-ni-to-ring
Die neue Aufgabe von der Monitoring-Stelle Das ist die Monitoring-Stelle: Am Deutschen Institut für Menschen-Rechte in Berlin gibt es ein besonderes Büro. Dieses Büro heißt Monitoring-Stelle. Mo-ni-to-ring
How to do? Projekte - Zeiterfassung
 How to do? Projekte - Zeiterfassung Stand: Version 4.0.1, 18.03.2009 1. EINLEITUNG...3 2. PROJEKTE UND STAMMDATEN...4 2.1 Projekte... 4 2.2 Projektmitarbeiter... 5 2.3 Tätigkeiten... 6 2.4 Unterprojekte...
How to do? Projekte - Zeiterfassung Stand: Version 4.0.1, 18.03.2009 1. EINLEITUNG...3 2. PROJEKTE UND STAMMDATEN...4 2.1 Projekte... 4 2.2 Projektmitarbeiter... 5 2.3 Tätigkeiten... 6 2.4 Unterprojekte...
Die Forschung mit embryonalen Stammzellen ist ethisch nicht akzeptabel
 Die Forschung mit embryonalen Stammzellen ist ethisch nicht akzeptabel Das Schweizer Volk soll sich selber äussern bezüglich der Gesetzgebung zur embryonalen Stammzellenforschung. Die ethische Bedeutung
Die Forschung mit embryonalen Stammzellen ist ethisch nicht akzeptabel Das Schweizer Volk soll sich selber äussern bezüglich der Gesetzgebung zur embryonalen Stammzellenforschung. Die ethische Bedeutung
Handbuch ECDL 2003 Basic Modul 5: Datenbank Grundlagen von relationalen Datenbanken
 Handbuch ECDL 2003 Basic Modul 5: Datenbank Grundlagen von relationalen Datenbanken Dateiname: ecdl5_01_00_documentation_standard.doc Speicherdatum: 14.02.2005 ECDL 2003 Basic Modul 5 Datenbank - Grundlagen
Handbuch ECDL 2003 Basic Modul 5: Datenbank Grundlagen von relationalen Datenbanken Dateiname: ecdl5_01_00_documentation_standard.doc Speicherdatum: 14.02.2005 ECDL 2003 Basic Modul 5 Datenbank - Grundlagen
Leseauszug DGQ-Band 14-26
 Leseauszug DGQ-Band 14-26 Einleitung Dieser Band liefert einen Ansatz zur Einführung von Prozessmanagement in kleinen und mittleren Organisationen (KMO) 1. Die Erfolgskriterien für eine Einführung werden
Leseauszug DGQ-Band 14-26 Einleitung Dieser Band liefert einen Ansatz zur Einführung von Prozessmanagement in kleinen und mittleren Organisationen (KMO) 1. Die Erfolgskriterien für eine Einführung werden
1. Man schreibe die folgenden Aussagen jeweils in einen normalen Satz um. Zum Beispiel kann man die Aussage:
 Zählen und Zahlbereiche Übungsblatt 1 1. Man schreibe die folgenden Aussagen jeweils in einen normalen Satz um. Zum Beispiel kann man die Aussage: Für alle m, n N gilt m + n = n + m. in den Satz umschreiben:
Zählen und Zahlbereiche Übungsblatt 1 1. Man schreibe die folgenden Aussagen jeweils in einen normalen Satz um. Zum Beispiel kann man die Aussage: Für alle m, n N gilt m + n = n + m. in den Satz umschreiben:
Wie oft soll ich essen?
 Wie oft soll ich essen? Wie sollen Sie sich als Diabetiker am besten ernähren? Gesunde Ernährung für Menschen mit Diabetes unterscheidet sich nicht von gesunder Ernährung für andere Menschen. Es gibt nichts,
Wie oft soll ich essen? Wie sollen Sie sich als Diabetiker am besten ernähren? Gesunde Ernährung für Menschen mit Diabetes unterscheidet sich nicht von gesunder Ernährung für andere Menschen. Es gibt nichts,
Keniaurlaub (nach OLG Stuttgart, VersR 2002, 148)
 Keniaurlaub (nach OLG Stuttgart, VersR 2002, 148) F plant, im Sommer 2003 nach Kenia zu reisen. Deshalb lässt sie sich bereits am 04.05.2002 zur Hepatitis-A-Prophylaxe von ihrem Hausarzt mit dem Impfstoff
Keniaurlaub (nach OLG Stuttgart, VersR 2002, 148) F plant, im Sommer 2003 nach Kenia zu reisen. Deshalb lässt sie sich bereits am 04.05.2002 zur Hepatitis-A-Prophylaxe von ihrem Hausarzt mit dem Impfstoff
Berechnung der Erhöhung der Durchschnittsprämien
 Wolfram Fischer Berechnung der Erhöhung der Durchschnittsprämien Oktober 2004 1 Zusammenfassung Zur Berechnung der Durchschnittsprämien wird das gesamte gemeldete Prämienvolumen Zusammenfassung durch die
Wolfram Fischer Berechnung der Erhöhung der Durchschnittsprämien Oktober 2004 1 Zusammenfassung Zur Berechnung der Durchschnittsprämien wird das gesamte gemeldete Prämienvolumen Zusammenfassung durch die
Ärzte befürchten Engpässe bei der Patientenversorgung
 allensbacher berichte Institut für Demoskopie Allensbach November 2010 Ärzte befürchten Engpässe bei der Patientenversorgung Die Ärzte in Deutschland sind außerordentlich besorgt, dass es in Zukunft verstärkt
allensbacher berichte Institut für Demoskopie Allensbach November 2010 Ärzte befürchten Engpässe bei der Patientenversorgung Die Ärzte in Deutschland sind außerordentlich besorgt, dass es in Zukunft verstärkt
Vermögensbildung: Sparen und Wertsteigerung bei Immobilien liegen vorn
 An die Redaktionen von Presse, Funk und Fernsehen 32 02. 09. 2002 Vermögensbildung: Sparen und Wertsteigerung bei Immobilien liegen vorn Das aktive Sparen ist nach wie vor die wichtigste Einflussgröße
An die Redaktionen von Presse, Funk und Fernsehen 32 02. 09. 2002 Vermögensbildung: Sparen und Wertsteigerung bei Immobilien liegen vorn Das aktive Sparen ist nach wie vor die wichtigste Einflussgröße
REACH-CLP-Helpdesk. Zulassung in der Lieferkette. Matti Sander, Bundesanstalt für Arbeitsschutz und Arbeitsmedizin
 REACH-CLP-Helpdesk Zulassung in der Lieferkette Matti Sander, Bundesanstalt für Arbeitsschutz und Arbeitsmedizin Inhaltsangabe Grundsatz Verschiedene Konstellationen 1. Der Hersteller/Importeur 2. Der
REACH-CLP-Helpdesk Zulassung in der Lieferkette Matti Sander, Bundesanstalt für Arbeitsschutz und Arbeitsmedizin Inhaltsangabe Grundsatz Verschiedene Konstellationen 1. Der Hersteller/Importeur 2. Der
Primzahlen und RSA-Verschlüsselung
 Primzahlen und RSA-Verschlüsselung Michael Fütterer und Jonathan Zachhuber 1 Einiges zu Primzahlen Ein paar Definitionen: Wir bezeichnen mit Z die Menge der positiven und negativen ganzen Zahlen, also
Primzahlen und RSA-Verschlüsselung Michael Fütterer und Jonathan Zachhuber 1 Einiges zu Primzahlen Ein paar Definitionen: Wir bezeichnen mit Z die Menge der positiven und negativen ganzen Zahlen, also
Der wachsende Berufsunfähigkeitsschutz SV Start-Easy-BU.
 SV STart-easy-bu Der wachsende Berufsunfähigkeitsschutz für junge Leute. SV Start-Easy-BU. Was auch passiert: Sparkassen-Finanzgruppe www.sparkassenversicherung.de Weiter mit im Leben dabei auch bei Berufsunfähigkeit.
SV STart-easy-bu Der wachsende Berufsunfähigkeitsschutz für junge Leute. SV Start-Easy-BU. Was auch passiert: Sparkassen-Finanzgruppe www.sparkassenversicherung.de Weiter mit im Leben dabei auch bei Berufsunfähigkeit.
Maintenance & Re-Zertifizierung
 Zertifizierung nach Technischen Richtlinien Maintenance & Re-Zertifizierung Version 1.2 vom 15.06.2009 Bundesamt für Sicherheit in der Informationstechnik Postfach 20 03 63 53133 Bonn Tel.: +49 22899 9582-0
Zertifizierung nach Technischen Richtlinien Maintenance & Re-Zertifizierung Version 1.2 vom 15.06.2009 Bundesamt für Sicherheit in der Informationstechnik Postfach 20 03 63 53133 Bonn Tel.: +49 22899 9582-0
Erfolgreiche Webseiten: Zur Notwendigkeit die eigene(n) Zielgruppe(n) zu kennen und zu verstehen!
 Erfolgreiche Webseiten: Zur Notwendigkeit die eigene(n) Zielgruppe(n) zu kennen und zu verstehen! www.wee24.de. info@wee24.de. 08382 / 6040561 1 Experten sprechen Ihre Sprache. 2 Unternehmenswebseiten
Erfolgreiche Webseiten: Zur Notwendigkeit die eigene(n) Zielgruppe(n) zu kennen und zu verstehen! www.wee24.de. info@wee24.de. 08382 / 6040561 1 Experten sprechen Ihre Sprache. 2 Unternehmenswebseiten
Nicht über uns ohne uns
 Nicht über uns ohne uns Das bedeutet: Es soll nichts über Menschen mit Behinderung entschieden werden, wenn sie nicht mit dabei sind. Dieser Text ist in leicht verständlicher Sprache geschrieben. Die Parteien
Nicht über uns ohne uns Das bedeutet: Es soll nichts über Menschen mit Behinderung entschieden werden, wenn sie nicht mit dabei sind. Dieser Text ist in leicht verständlicher Sprache geschrieben. Die Parteien
TOP SELECT PLUS Newsletter Nr.2
 TOP SELECT PLUS Newsletter Nr.2 Anspruch und Wirklichkeit - TOP SELECT PLUS Montag, 4. Juni 2012 Vermögensverwaltungen gibt es wie Sand am Meer. Darunter befinden sich solche, die ihrem Namen alle Ehre
TOP SELECT PLUS Newsletter Nr.2 Anspruch und Wirklichkeit - TOP SELECT PLUS Montag, 4. Juni 2012 Vermögensverwaltungen gibt es wie Sand am Meer. Darunter befinden sich solche, die ihrem Namen alle Ehre
SEPA-Anleitung zum Release 3.09
 Hier folgt nun eine kurze Information was sich mit dem neuen Release 3.08 zum Thema SEPA alles ändert. Bitte diese Anleitung sorgfältig lesen, damit bei der Umsetzung keine Fragen aufkommen. Bitte vor
Hier folgt nun eine kurze Information was sich mit dem neuen Release 3.08 zum Thema SEPA alles ändert. Bitte diese Anleitung sorgfältig lesen, damit bei der Umsetzung keine Fragen aufkommen. Bitte vor
Zulassung nach MID (Measurement Instruments Directive)
 Anwender - I n f o MID-Zulassung H 00.01 / 12.08 Zulassung nach MID (Measurement Instruments Directive) Inhaltsverzeichnis 1. Hinweis 2. Gesetzesgrundlage 3. Inhalte 4. Zählerkennzeichnung/Zulassungszeichen
Anwender - I n f o MID-Zulassung H 00.01 / 12.08 Zulassung nach MID (Measurement Instruments Directive) Inhaltsverzeichnis 1. Hinweis 2. Gesetzesgrundlage 3. Inhalte 4. Zählerkennzeichnung/Zulassungszeichen
Moderne Behandlung des Grauen Stars
 Katarakt Moderne Behandlung des Grauen Stars Sehr geehrte Patientin, sehr geehrter Patient, Bei Ihnen wurde eine Trübung der Augenlinse festgestellt, die umgangssprachlich auch Grauer Star genannt wird.
Katarakt Moderne Behandlung des Grauen Stars Sehr geehrte Patientin, sehr geehrter Patient, Bei Ihnen wurde eine Trübung der Augenlinse festgestellt, die umgangssprachlich auch Grauer Star genannt wird.
Jugendschutzgesetz (JuSchG) Die Besonderheit der "erziehungsbeauftragten" Person am Beispiel Diskotheken- und Gaststättenbesuch
 Jugendschutzgesetz (JuSchG) Die Besonderheit der "erziehungsbeauftragten" Person am Beispiel Diskotheken- und Gaststättenbesuch Einleitung Das Jugendschutzgesetz enthält im zweiten Abschnitt Reglementierungen
Jugendschutzgesetz (JuSchG) Die Besonderheit der "erziehungsbeauftragten" Person am Beispiel Diskotheken- und Gaststättenbesuch Einleitung Das Jugendschutzgesetz enthält im zweiten Abschnitt Reglementierungen
Lösung Fall 8 Anspruch des L auf Lieferung von 3.000 Panini á 2,-
 Lösung Fall 8 Anspruch des L auf Lieferung von 3.000 Panini á 2,- L könnte gegen G einen Anspruch auf Lieferung von 3.000 Panini á 2,- gem. 433 I BGB haben. Voraussetzung dafür ist, dass G und L einen
Lösung Fall 8 Anspruch des L auf Lieferung von 3.000 Panini á 2,- L könnte gegen G einen Anspruch auf Lieferung von 3.000 Panini á 2,- gem. 433 I BGB haben. Voraussetzung dafür ist, dass G und L einen
Reporting Services und SharePoint 2010 Teil 1
 Reporting Services und SharePoint 2010 Teil 1 Abstract Bei der Verwendung der Reporting Services in Zusammenhang mit SharePoint 2010 stellt sich immer wieder die Frage bei der Installation: Wo und Wie?
Reporting Services und SharePoint 2010 Teil 1 Abstract Bei der Verwendung der Reporting Services in Zusammenhang mit SharePoint 2010 stellt sich immer wieder die Frage bei der Installation: Wo und Wie?
Forschen - Schreiben - Lehren
 Forschen - Schreiben - Lehren Kontakt: Mareike Gronich mgronich@uni-bielefeld.de Fach/Fachgebiet: Germanistik Art der Lehrveranstaltung: Seminar Ausgangspunkt Geschütztes konstruktives Peer-Feedback in
Forschen - Schreiben - Lehren Kontakt: Mareike Gronich mgronich@uni-bielefeld.de Fach/Fachgebiet: Germanistik Art der Lehrveranstaltung: Seminar Ausgangspunkt Geschütztes konstruktives Peer-Feedback in
Letzte Krankenkassen streichen Zusatzbeiträge
 Zusatzbeiträge - Gesundheitsfonds Foto: D. Claus Einige n verlangten 2010 Zusatzbeiträge von ihren Versicherten. Die positive wirtschaftliche Entwicklung im Jahr 2011 ermöglichte den n die Rücknahme der
Zusatzbeiträge - Gesundheitsfonds Foto: D. Claus Einige n verlangten 2010 Zusatzbeiträge von ihren Versicherten. Die positive wirtschaftliche Entwicklung im Jahr 2011 ermöglichte den n die Rücknahme der
Wir sind für Sie da. Unser Gesundheitsangebot: Unterstützung im Umgang mit Ihrer Depression
 Wir sind für Sie da Unser Gesundheitsangebot: Unterstützung im Umgang mit Ihrer Depression Wir nehmen uns Zeit für Sie und helfen Ihnen Depressionen lassen sich heute meist gut behandeln. Häufig ist es
Wir sind für Sie da Unser Gesundheitsangebot: Unterstützung im Umgang mit Ihrer Depression Wir nehmen uns Zeit für Sie und helfen Ihnen Depressionen lassen sich heute meist gut behandeln. Häufig ist es
40-Tage-Wunder- Kurs. Umarme, was Du nicht ändern kannst.
 40-Tage-Wunder- Kurs Umarme, was Du nicht ändern kannst. Das sagt Wikipedia: Als Wunder (griechisch thauma) gilt umgangssprachlich ein Ereignis, dessen Zustandekommen man sich nicht erklären kann, so dass
40-Tage-Wunder- Kurs Umarme, was Du nicht ändern kannst. Das sagt Wikipedia: Als Wunder (griechisch thauma) gilt umgangssprachlich ein Ereignis, dessen Zustandekommen man sich nicht erklären kann, so dass
MS und Impfungen. DAS KLEINE IMPF-1x1. DAS KLEINE IMPF-1x1. Christian Lampl. Abteilung für Allgemeine Neurologie und Schmerzmedizin
 MS und Impfungen Christian Lampl Abteilung für Allgemeine Neurologie und Schmerzmedizin DAS KLEINE IMPF-1x1 Impfungen stellen sehr wirksame und wichtige präventivmedizinische Maßnahmen dar. Das unmittelbare
MS und Impfungen Christian Lampl Abteilung für Allgemeine Neurologie und Schmerzmedizin DAS KLEINE IMPF-1x1 Impfungen stellen sehr wirksame und wichtige präventivmedizinische Maßnahmen dar. Das unmittelbare
Vor- und Nachteile der Kastration
 Vor- und Nachteile der Kastration Was versteht man unter Kastration? Unter Kastration versteht man die chirugische Entfernung der Keimdrüsen. Bei der Hündin handelt es sich dabei um die Eierstöcke, beim
Vor- und Nachteile der Kastration Was versteht man unter Kastration? Unter Kastration versteht man die chirugische Entfernung der Keimdrüsen. Bei der Hündin handelt es sich dabei um die Eierstöcke, beim
Wann ist eine Software in Medizinprodukte- Aufbereitungsabteilungen ein Medizinprodukt?
 DGSV-Kongress 2009 Wann ist eine Software in Medizinprodukte- Aufbereitungsabteilungen ein Medizinprodukt? Sybille Andrée Betriebswirtin für und Sozialmanagement (FH-SRH) Prokuristin HSD Händschke Software
DGSV-Kongress 2009 Wann ist eine Software in Medizinprodukte- Aufbereitungsabteilungen ein Medizinprodukt? Sybille Andrée Betriebswirtin für und Sozialmanagement (FH-SRH) Prokuristin HSD Händschke Software
Ihren Kundendienst effektiver machen
 Ihren Kundendienst effektiver machen Wenn Sie einen neuen Kundendienstauftrag per Handy an Ihrem Monteur senden mag das ja funktionieren, aber hat Ihr Kunde nicht schon darüber gemeckert? Muss der Kunde
Ihren Kundendienst effektiver machen Wenn Sie einen neuen Kundendienstauftrag per Handy an Ihrem Monteur senden mag das ja funktionieren, aber hat Ihr Kunde nicht schon darüber gemeckert? Muss der Kunde
Informationsblatt Induktionsbeweis
 Sommer 015 Informationsblatt Induktionsbeweis 31. März 015 Motivation Die vollständige Induktion ist ein wichtiges Beweisverfahren in der Informatik. Sie wird häufig dazu gebraucht, um mathematische Formeln
Sommer 015 Informationsblatt Induktionsbeweis 31. März 015 Motivation Die vollständige Induktion ist ein wichtiges Beweisverfahren in der Informatik. Sie wird häufig dazu gebraucht, um mathematische Formeln
Erfahrungsbericht zur Eignung verschiedener ELISA Kits zum Nachweis von Antikörpern gegen Aviäre Influena für das Routinelabor
 Erfahrungsbericht zur Eignung verschiedener ELISA Kits zum Nachweis von Antikörpern gegen Aviäre Influena für das Routinelabor Dr. Hans-C. Philipp Lohmann Tierzucht GmbH Veterinär-Labor Abschnede 64 27472
Erfahrungsbericht zur Eignung verschiedener ELISA Kits zum Nachweis von Antikörpern gegen Aviäre Influena für das Routinelabor Dr. Hans-C. Philipp Lohmann Tierzucht GmbH Veterinär-Labor Abschnede 64 27472
Schweizer Verordnung über Bedarfsgegenstände in Kontakt mit Lebensmitteln (SR 817.023.21) Zugelassene Stoffe für Verpackungstinten
 Schweizer Verordnung über Bedarfsgegenstände in Kontakt mit Lebensmitteln (SR 817.023.21) Zugelassene Stoffe für Verpackungstinten Fragen und Antworten Seite 1 von 6 Das Eidgenössische Department des Innern
Schweizer Verordnung über Bedarfsgegenstände in Kontakt mit Lebensmitteln (SR 817.023.21) Zugelassene Stoffe für Verpackungstinten Fragen und Antworten Seite 1 von 6 Das Eidgenössische Department des Innern
Methodische Fragen zur frühen Nutzenbewertung nach 35a SGB V
 Die frühe Nutzenbewertung nach AMNOG Rechtssymposium des G-BA, Berlin, 16. Nov. 2010 Methodische Fragen zur frühen Nutzenbewertung nach 35a SGB V Jürgen Windeler AMNOG Nutzenbewertung für Arzneimittel
Die frühe Nutzenbewertung nach AMNOG Rechtssymposium des G-BA, Berlin, 16. Nov. 2010 Methodische Fragen zur frühen Nutzenbewertung nach 35a SGB V Jürgen Windeler AMNOG Nutzenbewertung für Arzneimittel
Übungsaufgaben Prozentrechnung und / oder Dreisatz
 Übungsaufgaben Prozentrechnung und / oder Dreisatz 1. Bei der Wahl des Universitätssprechers wurden 800 gültige Stimmen abgegeben. Die Stimmen verteilten sich so auf die drei Kandidat/innen: A bekam 300,
Übungsaufgaben Prozentrechnung und / oder Dreisatz 1. Bei der Wahl des Universitätssprechers wurden 800 gültige Stimmen abgegeben. Die Stimmen verteilten sich so auf die drei Kandidat/innen: A bekam 300,
200,- Euro am Tag gewinnen Konsequenz Silber Methode Warum machen die Casinos nichts dagegen? Ist es überhaupt legal?
 Mit meiner Methode werden Sie vom ersten Tag an Geld gewinnen. Diese Methode ist erprobt und wird von vielen Menschen angewendet! Wenn Sie es genau so machen, wie es hier steht, werden Sie bis zu 200,-
Mit meiner Methode werden Sie vom ersten Tag an Geld gewinnen. Diese Methode ist erprobt und wird von vielen Menschen angewendet! Wenn Sie es genau so machen, wie es hier steht, werden Sie bis zu 200,-
Unterschiede bei den Produktionsfunktionen zurückzuführen und können sich auf partielle Produktivitäten (Arbeitsproduktivität, Kapitalproduktivität,
 20 Etappe 1: Reale Außenwirtschaft Unterschiede bei den Produktionsfunktionen zurückzuführen und können sich auf partielle Produktivitäten (Arbeitsproduktivität, Kapitalproduktivität, Bodenproduktivität
20 Etappe 1: Reale Außenwirtschaft Unterschiede bei den Produktionsfunktionen zurückzuführen und können sich auf partielle Produktivitäten (Arbeitsproduktivität, Kapitalproduktivität, Bodenproduktivität
Lernaufgabe Industriekauffrau/Industriekaufmann Angebot und Auftrag: Arbeitsblatt I Auftragsbeschreibung
 Angebot und Auftrag: Arbeitsblatt I Auftragsbeschreibung Ein Kunde hat Interesse an einem von Ihrem Unternehmen hergestellten Produkt gezeigt. Es handelt sich dabei um einen batteriebetriebenen tragbaren
Angebot und Auftrag: Arbeitsblatt I Auftragsbeschreibung Ein Kunde hat Interesse an einem von Ihrem Unternehmen hergestellten Produkt gezeigt. Es handelt sich dabei um einen batteriebetriebenen tragbaren
Ergebnisse der NOVIBEL-Kundenzufriedenheitsanalyse 2002
 Ergebnisse der NOVIBEL-Kundenzufriedenheitsanalyse 2002 1. Grundlagen zum Verständnis der Befragung NOVIBEL führt die Kundenzufriedenheitsanalyse seit dem Jahr 2000 in Zusammenarbeit mit dem Lehrstuhl
Ergebnisse der NOVIBEL-Kundenzufriedenheitsanalyse 2002 1. Grundlagen zum Verständnis der Befragung NOVIBEL führt die Kundenzufriedenheitsanalyse seit dem Jahr 2000 in Zusammenarbeit mit dem Lehrstuhl
Bei der Tagung werden die Aspekte der DLRL aus verschiedenen Perspektiven dargestellt. Ich habe mich für die Betrachtung der Chancen entschieden,
 Bei der Tagung werden die Aspekte der DLRL aus verschiedenen Perspektiven dargestellt. Ich habe mich für die Betrachtung der Chancen entschieden, weil dieser Aspekt bei der Diskussion der Probleme meist
Bei der Tagung werden die Aspekte der DLRL aus verschiedenen Perspektiven dargestellt. Ich habe mich für die Betrachtung der Chancen entschieden, weil dieser Aspekt bei der Diskussion der Probleme meist
DAS PARETO PRINZIP DER SCHLÜSSEL ZUM ERFOLG
 DAS PARETO PRINZIP DER SCHLÜSSEL ZUM ERFOLG von Urs Schaffer Copyright by Urs Schaffer Schaffer Consulting GmbH Basel www.schaffer-consulting.ch Info@schaffer-consulting.ch Haben Sie gewusst dass... >
DAS PARETO PRINZIP DER SCHLÜSSEL ZUM ERFOLG von Urs Schaffer Copyright by Urs Schaffer Schaffer Consulting GmbH Basel www.schaffer-consulting.ch Info@schaffer-consulting.ch Haben Sie gewusst dass... >
Guide DynDNS und Portforwarding
 Guide DynDNS und Portforwarding Allgemein Um Geräte im lokalen Netzwerk von überall aus über das Internet erreichen zu können, kommt man um die Themen Dynamik DNS (kurz DynDNS) und Portweiterleitung(auch
Guide DynDNS und Portforwarding Allgemein Um Geräte im lokalen Netzwerk von überall aus über das Internet erreichen zu können, kommt man um die Themen Dynamik DNS (kurz DynDNS) und Portweiterleitung(auch
In diesem Tutorial lernen Sie, wie Sie einen Termin erfassen und verschiedene Einstellungen zu einem Termin vornehmen können.
 Tutorial: Wie erfasse ich einen Termin? In diesem Tutorial lernen Sie, wie Sie einen Termin erfassen und verschiedene Einstellungen zu einem Termin vornehmen können. Neben den allgemeinen Angaben zu einem
Tutorial: Wie erfasse ich einen Termin? In diesem Tutorial lernen Sie, wie Sie einen Termin erfassen und verschiedene Einstellungen zu einem Termin vornehmen können. Neben den allgemeinen Angaben zu einem
Ziel- und Qualitätsorientierung. Fortbildung für die Begutachtung in Verbindung mit dem Gesamtplanverfahren nach 58 SGB XII
 Ziel- und Qualitätsorientierung Fortbildung für die Begutachtung in Verbindung mit dem Gesamtplanverfahren nach 58 SGB XII Qualität? In der Alltagssprache ist Qualität oft ein Ausdruck für die Güte einer
Ziel- und Qualitätsorientierung Fortbildung für die Begutachtung in Verbindung mit dem Gesamtplanverfahren nach 58 SGB XII Qualität? In der Alltagssprache ist Qualität oft ein Ausdruck für die Güte einer
