Physikalische Grundlagen der zahnäzrtlichen Materialkunde. Einführung
|
|
|
- Marie Waltz
- vor 5 Jahren
- Abrufe
Transkript
1 Physikalische Grundlagen der zahnäzrtlichen Materialkunde 1. Einführung 1
2 Warum? Herstellung Struktur Z.B.: Eigenschaften Zahnärztliche Verwendung alle: Al 2 O 3! 2
3 Was? Wie? 3
4 "Sage es mir, und ich vergesse es; zeige es mir, und ich erinnere mich; lass es mich tun, und ich verstehe es. (Konfuzius) The most exciting phrase to hear in science, the one that heralds new discoveries, is not Eureka! (I found it!), but That s funny (Isaac Asimov) 4
5 Nützliche Infos o Tölgyesi Ferenc, Dozent (ferenc.tolgyesi@eok.sote.hu) Institut für Biophysik und Strahlenbiologie o Webseite: o W.D. Callister: Materials Science and Engineering. An Introduction (7th ed.), Wiley&Sons, 2007 o K.J. Anusavice: Phillips Science of Dental Materials (11th ed.), Saunders, 2003 o Damjanovich, Fidy, Szöllősi: Medizinische Biophysik, Medicina 2008 o 2 Zwischenprüfungen: 7. und 13. Woche o Prüfungsform: Kolloquium (mündlich) Note: 1. Test 2. Test 20 Punkte + 20 Punkte + Kolloquium 50 Punkte = insgesamt Min. 20 Punkte!! 90 Punkte Ab 40 Punkte: 2 Ab 55 Punkte: 3 Ab 70 Punkte: 4 Ab 80 Punkte: 5 5
6 Physikalische Grundlagen der zahnärztlichen Materialkunde 1. Struktur der Materie Atomare Wechselwirkungen. Multiatomare Systeme - Gase 6
7 Allgemeine Prinzipien Ekin 1 mv 2 2 Wechselwirkungen Bewegungen abstoßend anziehend E pot E Z.B. elektrisch r Unordnung E kin q1 q2 E pot k r Ordnung E E pot E kin E E pot E kin 0 0 gebundenes Elektron freies Elektron 7
8 Atomarer Aufbau der Materie o Demokritos 5.Jht v.chr. o Daltonsches Gesetz 1803 o Moderne Mikroskope: Graphit Si Kristall mit Defekten m Ordnungszah Elementarladung ll Atomkern, elektr. Ladung: Ze Z Elektronen, elektr. Ladung Ze Elektronenwolken m Bewegungen Elektrische Anziehung 8
9 Gebundene Zustände o Energieminimum o Diskrete Energiezustände o Pauli-Prinzip Eine neue Maßeinheit: Elektronenvolt (ev), es gilt 1 ev = 1, J Freie Zustände Elektronenzahl 2 K-Schale Hauptquantenzahl (n) 1 8 L-Schale 2 18 M-Schale 3 9
10 Periodensystem 10
11 Elektronegativität Ionisationsenergie (I): Zur Entfernung des äußersten Elektrons benötigte Energie (ev/atom; kj/mol) Elektronaffinitás (A): Elektronaffinität (A): Bei der Aufnahme eines Elektrons freigesetzte Energie (ev/atom; kj/mol) Elektronegativität = I A 11
12 Pauling-Skala (ev): 12
13 Atomare Wechselwirkungen Abstoßende Ww (E pot > 0) (Abstoß zw. den Kernen, Pauli-Prinzip) Bindungslänge (r 0 ) Bindungsenergie (E) 0,1 nm kj/mol Anziehende Ww (E pot < 0) E ~ x 2 F ~ x gemeinsame Elektronenbahnen elektrische Anziehung (Ion-Ion, Ion-Dipol, Dipol-Dipol) x Hookesches Gesetz 13
14 Bindungstypen primäre 100 kj/mol kovalente metallische ionische ionische Bindung Z.B. NaCl metallische Bindung kovalente Bindung Z.B. Na Z.B. H 2 14
15 Differenz der Elektronegativität Metallbindung Ionenbindung kovalente Bindung primäre chemische Bindung Summe der Elektronegativität 15
16 sekundäre 10 kj/mol van der Waals (Orientierung, Induktion, Dispersion) H-Brückenbindung van der Waals Bindung (Dispersionskräfte) H-Brückenbindung Temporärer Dipol Induzierter Dipol Zwischen 2 Atomen von hoher Elektronegativität (Z.B. O, N,...) Z.B. Edelgas Z.B. Wasser 16
17 Aggregatzustände Anziehende Ww Abstoßende Ww + Bewegungen T ( ~ E kin ) Fest Flüssig Gasförmig Eigenvolumen Eigenform Kristallin (Festkörper) Amorf Fernordnung Kristallgitter Nahordnung ungeordnet Dichte (r): ρ m V kg 3 m Spezifisches Volumen (v): v 1 r 3 m kg 17
18 Dichtewerte: Stoff r (g/cm 3 ) Weitere Maßeinheit: 1 g/cm 3 = 1000 kg/m 3 Zahnschmelz 2,2 Dentin 1,9 Wasser 1 Amalgam 12 Gold 19,3 Goldlegierungen Pd-Ag Legierungen Co-Cr Legierungen 8-9 Ni-Cr Legierungen 8 Glas 2,2-2,7 Keramiken 1,6-3,9 Porzelan 2,2-2,4 Gips 2,31-2,76 PMMA (Polimethyllmetakrilat) 1,2 Silikon 1,4 18
19 Gase Makroskopische Beschreibung: Kein Eigenvolumen und keine Eigenform Isotrop Messbare Größen: Druck p, V,, T pv Volumen RT (für ideale Gase) Stoffmenge Temperatur Mikroskopische Beschreibung: Ungeordnet Starke und fast freie Bewegung 1 mv kt Maxwell-Boltzmann- Verteilung 19
20 Gas im Gravitationsfeld barometrische Höhenformel: p? Im thermischen Gleichgewicht: p p 0 e mgh kt p h p Luft p p h 20
21 21
22 Boltzmann-Verteilung im Allgemeinen Die Verteilung der Teilchen auf die Energiezustände im thermischen Gleichgewicht (T = konstant): n i i n 0 0 n i n 0 e i 0 kt n i i n e kt n e kt 0 0 n0 e E RT E R k N A N A 22
23 Anwendungen: Barometrische Höhenformel Thermische Elektronenemission von Metallen Konzentrationselemente, Nernst-Gleichung Chemische Reaktionen (Geschwindigkeits- und Gleichgewichtskonstante) Konzentration von thermischen Punktdefekten (in Kristallen und Makromolekülen) Elektrische Leitfähigkeit von Halbleitern... K n n A B e A B kt Arrhenius- Plot: gát A k kt AB konst.e Zustände 23
24 Hausaufgaben 1.1. CO 2 -Gas befindet sich in einem Behälter, die Anzahl der Moleküle beträgt 3, Berechnen Sie die Stoffmenge und die Masse des Gases! 1.3. Die Ionisationsenergie von Na-Atom beträgt 496 kj/mol. a) Was ist die Ionisationsenergie für ein einziges Atom in ev-einheit? b) Was ist die Wellenlänge des Lichtes, dessen Photonenenergie gerade diesen Wert beträgt? 1.9. Das Volumen einer Amalgamfüllung beträgt 12 mm 3. Berechnen Sie die Masse! Haben H 2 O-Moleküle Platz in einem Glas des Volumens 2 dl? Die Temperatur von N 2 -Gas beträgt 25 C, die Stoffmenge ist 1 mol. a) Was sind durchschnittliche kinetische Energie und Geschwindigkeit von N 2 -Molekülen? b) Was ist gesamte kinetische Energie der Moleküle in dem Gas? Wenn die Atmosphäre ruhig und ihre Temperatur 0 C wäre, in welcher Höhe würde die Sauerstoffkonzentration auf die Hälfte sinken? (5 km) Wenn die Atmosphäre ruhig und ihre Temperatur 0 C wäre, in welcher Höhe würde a) die Kohlenstoffdioxydkonzentration b) die Konzentration von Toluol (Zivilisationsverunreinigung; molare Masse: 92,1 g/mol) auf die Hälfte sinken? Lösungen: ,98 mmol und 263 mg 1.3. a) 5,15 ev; b) 241 nm mg nein a) 0,00617 aj und 515 m/s; b) 3710 J/mol m a) 3640 m; b) 1740 m 24
Biophysik für Pharmazeuten I.
 Biohysik für Pharmazeuten I. Allgemeine Prinziien Wechselwirkungen Bewegungen abstoßend anziehend Ekin = 1 mv 015/16 Vorlesung 3 E ot E Z.B. elektrisch r Struktur der Materie Unordnung + E kin q1 q = k
Biohysik für Pharmazeuten I. Allgemeine Prinziien Wechselwirkungen Bewegungen abstoßend anziehend Ekin = 1 mv 015/16 Vorlesung 3 E ot E Z.B. elektrisch r Struktur der Materie Unordnung + E kin q1 q = k
Medizinische Biophysik
 2. Gasförmiger Aggregatzustand Medizinische Biophysik c) Kinetische Deutung der Temperatur: d) Maxwell-Boltzmann-Verteilung e) Barometrische Höhenformel (Gas im Gravitationsfeld) f) Boltzmann-Verteilung
2. Gasförmiger Aggregatzustand Medizinische Biophysik c) Kinetische Deutung der Temperatur: d) Maxwell-Boltzmann-Verteilung e) Barometrische Höhenformel (Gas im Gravitationsfeld) f) Boltzmann-Verteilung
Biophysik für Pharmazeuten I Struktur der Materie Tölgyesi Ferenc
 Biophysik für Pharmazeuten I. 014. 09.. Struktur der Materie Tölgyesi Ferenc Atomarer Aufbau der Materie o Demokritos 5.Jht v.chr. o Daltonsches Gesetz 180 o Moderne Mikroskope: Hausaufgaben: Neue Aufgabensammlung
Biophysik für Pharmazeuten I. 014. 09.. Struktur der Materie Tölgyesi Ferenc Atomarer Aufbau der Materie o Demokritos 5.Jht v.chr. o Daltonsches Gesetz 180 o Moderne Mikroskope: Hausaufgaben: Neue Aufgabensammlung
Physikalische Grundlagen der zahnäzrtlichen Materialkunde
 Waum? Hestellung Stuktu Z.B.: Eigenschaften Zahnäztliche Vewendung Physikalische Gundlagen de zahnäztlichen Mateialkunde 1. Einfühung 1 alle: Al O! Was? "Sage es mi, und ich vegesse es; zeige es mi, und
Waum? Hestellung Stuktu Z.B.: Eigenschaften Zahnäztliche Vewendung Physikalische Gundlagen de zahnäztlichen Mateialkunde 1. Einfühung 1 alle: Al O! Was? "Sage es mi, und ich vegesse es; zeige es mi, und
Medizinische Biophysik
 2. Gasförmiger Aggregatzustand a) Makroskopische Beschreibung b) Mikroskopische Beschreibung Medizinische Biophysik c) Kinetische Deutung der Temperatur d) Maxwell-Boltzmann-Verteilung e) Barometrische
2. Gasförmiger Aggregatzustand a) Makroskopische Beschreibung b) Mikroskopische Beschreibung Medizinische Biophysik c) Kinetische Deutung der Temperatur d) Maxwell-Boltzmann-Verteilung e) Barometrische
- + E A. N m. Wasser. Oberflächenspannung, oder spezifische Oberflächenenergie ( ): Stoff (J/m 2 )* c) Oberflächenspannung
 Medizinische Biophysik Struktur der Materie Aggregatzustände: Gase, Flüssigkeiten, feste Körper 2. Vorlesung 12. 09. 2016 e) Barometrische Höhenformel (Gas im Gravitationsfeld) Gravitation (ohne Bewegungen,
Medizinische Biophysik Struktur der Materie Aggregatzustände: Gase, Flüssigkeiten, feste Körper 2. Vorlesung 12. 09. 2016 e) Barometrische Höhenformel (Gas im Gravitationsfeld) Gravitation (ohne Bewegungen,
Medizinische Biophysik
 4. Flüssiger Aggregatzustand Medizinische Biophysik a) Makroskopische Beschreibung b) Mikroskopische Beschreibung c) Oberflächenspannung Struktur der Materie Aggregatzustände: Gase, Flüssigkeiten, feste
4. Flüssiger Aggregatzustand Medizinische Biophysik a) Makroskopische Beschreibung b) Mikroskopische Beschreibung c) Oberflächenspannung Struktur der Materie Aggregatzustände: Gase, Flüssigkeiten, feste
Hier: Beschränkung auf die elektrische Eigenschaften
 IV. Festkörperphysik Hier: Beschränkung auf die elektrische Eigenschaften 3 Aggregatzustände: fest, flüssig, gasförmig: Wechselspiel Anziehungskräfte der Teilchen gegen die thermische Energie kt. Zustand
IV. Festkörperphysik Hier: Beschränkung auf die elektrische Eigenschaften 3 Aggregatzustände: fest, flüssig, gasförmig: Wechselspiel Anziehungskräfte der Teilchen gegen die thermische Energie kt. Zustand
4 Thermodynamik mikroskopisch: kinetische Gastheorie makroskopisch: System:
 Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Medizinische Biophysik I.
 Physik in de Medizin Medizinische Biophysik I. D. Feenc Tölgyesi tolgyesi.feenc @med.semmelweis-univ.hu Institut fü Biophysik und Stahlenbiologie 0 Diagnostik Röntgendiagnostik Sonogaphie Optische Tomogaphie
Physik in de Medizin Medizinische Biophysik I. D. Feenc Tölgyesi tolgyesi.feenc @med.semmelweis-univ.hu Institut fü Biophysik und Stahlenbiologie 0 Diagnostik Röntgendiagnostik Sonogaphie Optische Tomogaphie
Grundlagen der statistischen Physik und Thermodynamik
 Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Medizinische Biophysik I.
 P H Y S I K Physik in de Medizin Medizinische Biophysik I. D. Feenc Tölgyesi tolgyesi.feenc @med.semmelweis-univ.hu Institut fü Biophysik und Stahlenbiologie 0 Diagnostik Röntgendiagnostik Sonogaphie Optische
P H Y S I K Physik in de Medizin Medizinische Biophysik I. D. Feenc Tölgyesi tolgyesi.feenc @med.semmelweis-univ.hu Institut fü Biophysik und Stahlenbiologie 0 Diagnostik Röntgendiagnostik Sonogaphie Optische
Festkörper. Festkörper
 Festkörper Einteilung der Materie in drei Aggregatszustände: fest, flüssig, gasförmig Unterscheidung Festkörper behält seine Form Nachteil: Ungenaue Abgrenzung Beispiel: Ist Butter Festkörper oder Flüssigkeit
Festkörper Einteilung der Materie in drei Aggregatszustände: fest, flüssig, gasförmig Unterscheidung Festkörper behält seine Form Nachteil: Ungenaue Abgrenzung Beispiel: Ist Butter Festkörper oder Flüssigkeit
Flüssigkeiten. Viskosität (h) v h. A h. víz. (Fluidität~ 1/h) [h] = Pa s. Newtonsches Reibungsgesetz: Dynamische Nahordnung.
![Flüssigkeiten. Viskosität (h) v h. A h. víz. (Fluidität~ 1/h) [h] = Pa s. Newtonsches Reibungsgesetz: Dynamische Nahordnung. Flüssigkeiten. Viskosität (h) v h. A h. víz. (Fluidität~ 1/h) [h] = Pa s. Newtonsches Reibungsgesetz: Dynamische Nahordnung.](/thumbs/66/56374829.jpg) Flüssigkeiten flüssig Keine Eigenform (nach Deformieren bleibt so, es gibt keine rückstellende cherkräfte) fest Eigenform (nach Deformieren stellt sich zurück, da es rückstellende cherkräftegibt ) Physikalische
Flüssigkeiten flüssig Keine Eigenform (nach Deformieren bleibt so, es gibt keine rückstellende cherkräfte) fest Eigenform (nach Deformieren stellt sich zurück, da es rückstellende cherkräftegibt ) Physikalische
Medizinische Biophysik I.
 Thematik de Volesungen Medizinische Biophysik I. 0 D. Feenc Tölgyesi tolgyesi.feenc @med.semmelweis-univ.hu Institut fü Biophysik und Stahlenbiologie 1 Abweichung fü Zahnmedizine in den esten dei Wochen:
Thematik de Volesungen Medizinische Biophysik I. 0 D. Feenc Tölgyesi tolgyesi.feenc @med.semmelweis-univ.hu Institut fü Biophysik und Stahlenbiologie 1 Abweichung fü Zahnmedizine in den esten dei Wochen:
Atome und Bindungen. Was sollen Sie mitnehmen?
 Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
Atome und Bindungen. Was sollen Sie mitnehmen?
 Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
Lernmaterial Lernfeld 1 Grundlagen Physik und Chemie. Chemische Grundlagen, Bindungsarten. Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms
 Chemische Grundlagen, Bindungsarten Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms Hier ist ein Lithiumatom schematisch dargestellt. Elektronen umkreisen den Kern in diskreten Bahnen IQ Technikum
Chemische Grundlagen, Bindungsarten Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms Hier ist ein Lithiumatom schematisch dargestellt. Elektronen umkreisen den Kern in diskreten Bahnen IQ Technikum
1. Wärmelehre 1.1. Temperatur. Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités)
 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
Besetzung der Orbitale
 Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Grenzflächenphänomene. Physikalische Grundlagen der zahnärztlichen Materialkunde 3. Struktur der Materie. J m. N m. 1. Oberflächenspannung
 Grenzflächenphänomene 1. Oberflächenspannung Physikalische Grundlagen der zahnärztlichen Materialkunde 3. Struktur der Materie Grenzflächenphänomene Phase/Phasendiagramm/Phasenübergang Schwerpunkte: Oberflächenspannung
Grenzflächenphänomene 1. Oberflächenspannung Physikalische Grundlagen der zahnärztlichen Materialkunde 3. Struktur der Materie Grenzflächenphänomene Phase/Phasendiagramm/Phasenübergang Schwerpunkte: Oberflächenspannung
Skript zur Vorlesung
 Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Name: Punktzahl: von 57 Note:
 Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
Atomaufbau. Elektronen e (-) Atomhülle
 Atomaufbau Institut für Elementarteilchen Nukleonen Protonen p (+) Neutronen n (o) Elektronen e (-) Atomkern Atomhülle Atom WIBA-NET 2005 Prof. Setzer 1 Elementarteilchen Institut für Name Symbol Masse
Atomaufbau Institut für Elementarteilchen Nukleonen Protonen p (+) Neutronen n (o) Elektronen e (-) Atomkern Atomhülle Atom WIBA-NET 2005 Prof. Setzer 1 Elementarteilchen Institut für Name Symbol Masse
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle
 2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
Gesetz von Boyle. Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V.
 Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
O. Sternal, V. Hankele. 5. Thermodynamik
 5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
Physikalische Chemie 0 Klausur, 22. Oktober 2011
 Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Wechselwirkungen zwischen Atomen Was bisher geschah Quantenmechanisches
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Wechselwirkungen zwischen Atomen Was bisher geschah Quantenmechanisches
Basiskenntnistest - Chemie
 Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
1. Wärmelehre 1.1. Temperatur Wiederholung
 1. Wärmelehre 1.1. Temperatur Wiederholung a) Zur Messung der Temperatur verwendet man physikalische Effekte, die von der Temperatur abhängen. Beispiele: Volumen einer Flüssigkeit (Hg-Thermometer), aber
1. Wärmelehre 1.1. Temperatur Wiederholung a) Zur Messung der Temperatur verwendet man physikalische Effekte, die von der Temperatur abhängen. Beispiele: Volumen einer Flüssigkeit (Hg-Thermometer), aber
f) Ideales Gas - mikroskopisch
 f) Ideales Gas - mikroskopisch i) Annahmen Schon gehabt: Massenpunkte ohne Eigenvolumen Nur elastische Stöße, keine Wechselwirkungen Jetzt dazu: Wände vollkommen elastisch, perfekte Reflektoren Zeitliches
f) Ideales Gas - mikroskopisch i) Annahmen Schon gehabt: Massenpunkte ohne Eigenvolumen Nur elastische Stöße, keine Wechselwirkungen Jetzt dazu: Wände vollkommen elastisch, perfekte Reflektoren Zeitliches
Physik III im Studiengang Elektrotechnik
 Physik III im Studiengang lektrotechnik - kinetische Gastheorie - Prof. Dr. Ulrich Hahn WS 008/09 Molekularbewegung kleine sichtbare Teilchen in Flüssigkeiten oder Gasen: unregelmäß äßige Zitterbewegung
Physik III im Studiengang lektrotechnik - kinetische Gastheorie - Prof. Dr. Ulrich Hahn WS 008/09 Molekularbewegung kleine sichtbare Teilchen in Flüssigkeiten oder Gasen: unregelmäß äßige Zitterbewegung
Musterlösung zur Abschlussklausur PC I Übungen (27. Juni 2018)
 1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie
 Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie DIE CHEMISCHE BINDUNG Ionische Bindung, Beispiel Natriumchlorid Trifft
Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie DIE CHEMISCHE BINDUNG Ionische Bindung, Beispiel Natriumchlorid Trifft
1.1 Chemie in Karlsruhe - Karl Weltzien & Lothar Meyer, Karlsruher Kongress ( ) Periodensystem der Elemente
 Chemie Vorkurs 2014 1. Allgemeine Grundlagen 1.1 Chemie in Karlsruhe - Karl Weltzien & Lothar Meyer, Karlsruher Kongress (03.-05.09.1860) Periodensystem der Elemente - Fritz Haber, Nobelpreis 1918 Ammoniaksynthese
Chemie Vorkurs 2014 1. Allgemeine Grundlagen 1.1 Chemie in Karlsruhe - Karl Weltzien & Lothar Meyer, Karlsruher Kongress (03.-05.09.1860) Periodensystem der Elemente - Fritz Haber, Nobelpreis 1918 Ammoniaksynthese
Kinetische Energie der Moleküle / Aggregatzustand
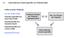 2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kräfte zwischen Molekülen - Van-der-Waals-Kräfte Orientierungskräfte bzw. Dipol-Dipol-Kräfte Induktionskräfte bzw. induzierte Dipole Dispersionskräfte
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kräfte zwischen Molekülen - Van-der-Waals-Kräfte Orientierungskräfte bzw. Dipol-Dipol-Kräfte Induktionskräfte bzw. induzierte Dipole Dispersionskräfte
Allgemeines Gasgesetz. PV = K o T
 Allgemeines Gasgesetz Die Kombination der beiden Gesetze von Gay-Lussac mit dem Gesetz von Boyle-Mariotte gibt den Zusammenhang der drei Zustandsgrößen Druck, Volumen, und Temperatur eines idealen Gases,
Allgemeines Gasgesetz Die Kombination der beiden Gesetze von Gay-Lussac mit dem Gesetz von Boyle-Mariotte gibt den Zusammenhang der drei Zustandsgrößen Druck, Volumen, und Temperatur eines idealen Gases,
Stoffgemisch. Reinstoff. Homogenes Gemisch. Heterogenes Gemisch. ( 9. Kl. SG - WSG 1 / 56 ) ( 9. Kl. SG - WSG 2 / 56 ) ( 9. Kl.
 Stoffgemisch ( 9. Kl. SG - WSG 1 / 56 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 9. Kl.
Stoffgemisch ( 9. Kl. SG - WSG 1 / 56 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 9. Kl.
Das Ideale Gas Kinetische Gastheorie (auf atomarer Ebene)
 Das Ideale Gas Kinetische Gastheorie (auf atomarer Ebene) Wir haben gesehen, dass ein sogenanntes 'ideales Gas' durch die Zustandsgleichung pv = νr T [1] beschrieben wird; wir wollen nun verstehen, welchen
Das Ideale Gas Kinetische Gastheorie (auf atomarer Ebene) Wir haben gesehen, dass ein sogenanntes 'ideales Gas' durch die Zustandsgleichung pv = νr T [1] beschrieben wird; wir wollen nun verstehen, welchen
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Struktur von Festkörpern
 Struktur von Festkörpern Wir wollen uns zunächst mit der Struktur von Festkörpern, daß heißt mit der Geometrie in der sie vorliegen beschäftigen Kovalent gebundene Festkörper haben wir bereits in Form
Struktur von Festkörpern Wir wollen uns zunächst mit der Struktur von Festkörpern, daß heißt mit der Geometrie in der sie vorliegen beschäftigen Kovalent gebundene Festkörper haben wir bereits in Form
Inhalt. Vorlesung Werkstoffe des Leichtbaus I. 0. Einführung in den Leichtbau
 Inhalt Vorlesung Werkstoffe des Leichtbaus I 0. Einführung in den Leichtbau 1. Leichtbau im Überblick 2. Konstruktion und Gestaltung von Leichtbaustrukturen 3. Beanspruchung und Auslegung von Leichtbaustrukturen
Inhalt Vorlesung Werkstoffe des Leichtbaus I 0. Einführung in den Leichtbau 1. Leichtbau im Überblick 2. Konstruktion und Gestaltung von Leichtbaustrukturen 3. Beanspruchung und Auslegung von Leichtbaustrukturen
HÖHERE PHYSIK SKRIPTUM VORLESUNGBLATT XI
 Prof. Dr. F. Koch Dr. H. E. Porteanu fkoch@ph.tum.de porteanu@ph.tum.de WS 4-5 HÖHEE PHYSIK SKIPTUM VOLESUNGBLATT XI 4..5 Molekülphysik Atome binden zu Molekülen und Festkörpern durch interatomare Kräfte
Prof. Dr. F. Koch Dr. H. E. Porteanu fkoch@ph.tum.de porteanu@ph.tum.de WS 4-5 HÖHEE PHYSIK SKIPTUM VOLESUNGBLATT XI 4..5 Molekülphysik Atome binden zu Molekülen und Festkörpern durch interatomare Kräfte
A. Erhaltungsgrößen (17 Punkte) Name: Vorname: Matr. Nr.: Studiengang: ET Diplom ET Bachelor TI WI. Platz Nr.: Tutor:
 Prof. Dr. O. Dopfer Prof. Dr. A. Hese Priv. Doz. Dr. S. Kröger Cand.-Phys. A. Kochan Technische Universität Berlin A. Erhaltungsgrößen (17 Punkte) 1. Unter welcher Bedingung bleiben a) der Impuls b) der
Prof. Dr. O. Dopfer Prof. Dr. A. Hese Priv. Doz. Dr. S. Kröger Cand.-Phys. A. Kochan Technische Universität Berlin A. Erhaltungsgrößen (17 Punkte) 1. Unter welcher Bedingung bleiben a) der Impuls b) der
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen!
 1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
Vorlesung Theoretische Chemie I
 Institut für Physikalische and Theoretische Chemie, Goethe-Universität, Frankfurt am Main 20. Dezember 2013 Teil I Energieeinheiten Joule E kin = 1 2 mv 2 E pot = mgh [E] = kg m2 s 2 = J Verwendung: Energie/Arbeit
Institut für Physikalische and Theoretische Chemie, Goethe-Universität, Frankfurt am Main 20. Dezember 2013 Teil I Energieeinheiten Joule E kin = 1 2 mv 2 E pot = mgh [E] = kg m2 s 2 = J Verwendung: Energie/Arbeit
Grundwissen 9.Klasse SG 1 Grundwissen 9.Klasse SG 1. Grundwissen 9.Klasse SG 2 Grundwissen 9.Klasse SG 2. Stoffebene.
 Grundwissen 9.Klasse SG 1 Grundwissen 9.Klasse SG 1 Stoff Reinstoff mischen Gemisch Einteilung der Stoffe Bei gleichen Bedingungen (Temp., Druck) immer gleiche Eigenschaften (z.b. Schmelz- /Siedetemp.,
Grundwissen 9.Klasse SG 1 Grundwissen 9.Klasse SG 1 Stoff Reinstoff mischen Gemisch Einteilung der Stoffe Bei gleichen Bedingungen (Temp., Druck) immer gleiche Eigenschaften (z.b. Schmelz- /Siedetemp.,
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I Dr. Helge Klemmer
 Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
Chemie-Grundwissen der 9.Klasse
 Chemie-Grundwissen der 9.Klasse Stoffebene = Makroskopische (sichtbare) Ebene Betrachtung einer Stoffportion mit den erkennbaren und messbaren Eigenschaften Teilchenebene = Submikroskopische Ebene Betrachtung
Chemie-Grundwissen der 9.Klasse Stoffebene = Makroskopische (sichtbare) Ebene Betrachtung einer Stoffportion mit den erkennbaren und messbaren Eigenschaften Teilchenebene = Submikroskopische Ebene Betrachtung
Hochschule Düsseldorf University of Applied Sciences. 20. April 2016 HSD. Energiespeicher Wärme
 Energiespeicher 02 - Wärme Wiederholung Energiearten Primärenergie Physikalische Energie Kernenergie Chemische Energie Potentielle Energie Kinetische Energie Innere Energie Quelle: Innere Energie Innere
Energiespeicher 02 - Wärme Wiederholung Energiearten Primärenergie Physikalische Energie Kernenergie Chemische Energie Potentielle Energie Kinetische Energie Innere Energie Quelle: Innere Energie Innere
Chemische Bindung. Wie halten Atome zusammen? Welche Atome können sich verbinden? Febr 02
 Chemische Bindung locker bleiben Wie halten Atome zusammen? positiv Welche Atome können sich verbinden? power keep smiling Chemische Bindung Die chemischen Reaktionen spielen sich zwischen den Hüllen der
Chemische Bindung locker bleiben Wie halten Atome zusammen? positiv Welche Atome können sich verbinden? power keep smiling Chemische Bindung Die chemischen Reaktionen spielen sich zwischen den Hüllen der
Klaus Stierstadt. Physik. der Materie VCH
 Klaus Stierstadt Physik der Materie VCH Inhalt Vorwort Tafelteil hinter Inhaltsverzeichnis (Seiten TI-T XVII) V Teil I Mikrophysik - Die Bausteine der Materie... l 1 Aufbau und Eigenschaften der Materie
Klaus Stierstadt Physik der Materie VCH Inhalt Vorwort Tafelteil hinter Inhaltsverzeichnis (Seiten TI-T XVII) V Teil I Mikrophysik - Die Bausteine der Materie... l 1 Aufbau und Eigenschaften der Materie
Grundlagen der Allgemeinen und Anorganischen Chemie. Atome
 Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 361 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 361 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
22. Chemische Bindungen
 .05.03. Chemische Bindungen Molekül: System aus zwei oder mehr Atomen Kleinste Einheit einer Substanz, die deren chemische Eigenschaften ausweist Quantenmechanisches Vielteilchensystem: Exakte explizite
.05.03. Chemische Bindungen Molekül: System aus zwei oder mehr Atomen Kleinste Einheit einer Substanz, die deren chemische Eigenschaften ausweist Quantenmechanisches Vielteilchensystem: Exakte explizite
Wasser à. Nachweis: Wasser ist
 Arbeitsblatt zu Kap. 5. Atome Bausteine der Stoffe 5.1 Elemente und Verbindungen Elektrolyse des Reinstoffes Wasser Wasser à Nachweis: Wasser ist Stoffeinteilung 5.2 Von den Elementen zu den Atomen Synthese
Arbeitsblatt zu Kap. 5. Atome Bausteine der Stoffe 5.1 Elemente und Verbindungen Elektrolyse des Reinstoffes Wasser Wasser à Nachweis: Wasser ist Stoffeinteilung 5.2 Von den Elementen zu den Atomen Synthese
Potential und Spannung
 Potential und Spannung Arbeit bei Ladungsverschiebung: Beim Verschieben einer Ladung q im elektrischen Feld E( r) entlang dem Weg C wird Arbeit geleistet: W el = F C d s = q E d s Vorzeichen: W el > 0
Potential und Spannung Arbeit bei Ladungsverschiebung: Beim Verschieben einer Ladung q im elektrischen Feld E( r) entlang dem Weg C wird Arbeit geleistet: W el = F C d s = q E d s Vorzeichen: W el > 0
Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung
 Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion 16. Phasenübergänge (Verdampfen, Schmelzen, Sublimieren) Versuche: Wärmeleitung
Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion 16. Phasenübergänge (Verdampfen, Schmelzen, Sublimieren) Versuche: Wärmeleitung
Vorlesung Allgemeine Chemie: Chemische Bindung
 Vorlesung Allgemeine Chemie: Chemische Bindung Inhalte Gruppentendenzen: Alkalimetalle, Halogene, Reaktion mit H 2 und H 2 O, basische und saure Oxide, Ionenbindung, Gitterenergie, Tendenzen in Abhängigkeit
Vorlesung Allgemeine Chemie: Chemische Bindung Inhalte Gruppentendenzen: Alkalimetalle, Halogene, Reaktion mit H 2 und H 2 O, basische und saure Oxide, Ionenbindung, Gitterenergie, Tendenzen in Abhängigkeit
Biophysik für Pharmazeuten I.
 Thematik Biophysik für Pharmazeuten I. Woche Vorlesungen: Thema Einführung Mechanik Struktur der Materie Vortragende Tölgyesi Woche Praktika: Thema Einführung, Sicherheitsvorschriften Refraktometer Mikroskop
Thematik Biophysik für Pharmazeuten I. Woche Vorlesungen: Thema Einführung Mechanik Struktur der Materie Vortragende Tölgyesi Woche Praktika: Thema Einführung, Sicherheitsvorschriften Refraktometer Mikroskop
Grundtypen der Bindung. Grundtypen chemischer Bindung. Oktettregel. A.8.1. Atombindung
 Grundtypen der Bindung Grundtypen chemischer Bindung Oktettregel A.8.1. Atombindung 1 A.8.1 Atombindung Valenz (Zahl der Bindungen) Atombindung auch: kovalente Bindung, ElektronenpaarBindung Zwei Atome
Grundtypen der Bindung Grundtypen chemischer Bindung Oktettregel A.8.1. Atombindung 1 A.8.1 Atombindung Valenz (Zahl der Bindungen) Atombindung auch: kovalente Bindung, ElektronenpaarBindung Zwei Atome
E2: Wärmelehre und Elektromagnetismus 7. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 7. Vorlesung 30.04.2018 Heute: - 2. Hauptsatz - Boltzmann-Verteilung https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 30.04.2018 Prof. Dr. Jan Lipfert
E2: Wärmelehre und Elektromagnetismus 7. Vorlesung 30.04.2018 Heute: - 2. Hauptsatz - Boltzmann-Verteilung https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 30.04.2018 Prof. Dr. Jan Lipfert
Inhaltsverzeichnis. 1. Chemische Grundbegriffe...9
 sverzeichnis 3 1. Chemische Grundbegriffe...9 1.1. Sinn und Zweck dieser Lehreinheit... 9 1.2. Das Wesen der Naturwissenschaften... 10 1.3. Stoffe und Körper...12 1.4. Physikalische und chemische Vorgänge...
sverzeichnis 3 1. Chemische Grundbegriffe...9 1.1. Sinn und Zweck dieser Lehreinheit... 9 1.2. Das Wesen der Naturwissenschaften... 10 1.3. Stoffe und Körper...12 1.4. Physikalische und chemische Vorgänge...
Kristallchemie. Atome Ionen Moleküle Chemische Bindungen
 Zirkon Kristallchemie Atome Ionen Moleküle Chemische Bindungen Bohr sches Atommodell Kernteilchen: p: Proton n: Neutron Elektronenhülle: e - Elektron Nukleus: Massenzahl A = p + n, Ordnungszahl Z = p =
Zirkon Kristallchemie Atome Ionen Moleküle Chemische Bindungen Bohr sches Atommodell Kernteilchen: p: Proton n: Neutron Elektronenhülle: e - Elektron Nukleus: Massenzahl A = p + n, Ordnungszahl Z = p =
Vorlesung Allgemeine Chemie: Chemische Bindung
 Vorlesung Allgemeine Chemie: Chemische Bindung Inhalte Gruppentendenzen: Alkalimetalle, Halogene, Reaktion mit H 2 und H 2 O, basische und saure Oxide, Ionenbindung, Gitterenergie, Tendenzen in Abhängigkeit
Vorlesung Allgemeine Chemie: Chemische Bindung Inhalte Gruppentendenzen: Alkalimetalle, Halogene, Reaktion mit H 2 und H 2 O, basische und saure Oxide, Ionenbindung, Gitterenergie, Tendenzen in Abhängigkeit
Grundlagen der Physik 2 Schwingungen und Wärmelehre Othmar Marti.
 (c) Ulm University p. 1/1 Grundlagen der Physik 2 Schwingungen und Wärmelehre 14. 05. 2007 Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik Universität Ulm (c) Ulm University p.
(c) Ulm University p. 1/1 Grundlagen der Physik 2 Schwingungen und Wärmelehre 14. 05. 2007 Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik Universität Ulm (c) Ulm University p.
Elektrizitätslehre 3.
 Elektrizitätslehre 3. Elektrischer Strom Strom = geordnete Bewegung der Ladungsträgern Ladungsträgern: Elektronen Ionen Strom im Vakuum Strom im Gas Strom in Flüssigkeit (Lösung) Strom im Festkörper Leiter
Elektrizitätslehre 3. Elektrischer Strom Strom = geordnete Bewegung der Ladungsträgern Ladungsträgern: Elektronen Ionen Strom im Vakuum Strom im Gas Strom in Flüssigkeit (Lösung) Strom im Festkörper Leiter
Stoffgemisch. Reinstoff. Homogenes Gemisch. Heterogenes Gemisch. ( 8. Klasse NTG 1 / 48 ) ( 8. Klasse NTG 2 / 48 ) ( 8. Klasse NTG 3 / 48 )
 Stoffgemisch ( 8. Klasse NTG 1 / 48 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 8. Klasse
Stoffgemisch ( 8. Klasse NTG 1 / 48 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 8. Klasse
Arbeit = Kraft Weg ; W = F s ; 1 Joule = 1 Newton Meter ; 1 J = 1 N m
 GRATIS-Übungsdokument Gymnasium Klasse 8 Physik Thema: Mechanik, Wärmelehre, Elektrizitätslehre CATLUX de Energie Arbeit = Kraft Weg ; W = F s ; 1 Joule = 1 Newton Meter ; 1 J = 1 N m Energie ist gespeicherte
GRATIS-Übungsdokument Gymnasium Klasse 8 Physik Thema: Mechanik, Wärmelehre, Elektrizitätslehre CATLUX de Energie Arbeit = Kraft Weg ; W = F s ; 1 Joule = 1 Newton Meter ; 1 J = 1 N m Energie ist gespeicherte
Aufgabenübersicht für tägliche Übungen mit zugehörigen Klassenstufen:
 Aufgabenübersicht für tägliche Übungen mit zugehörigen Klassenstufen: Größen mit Formelzeichen, Einheiten und Umrechnungen: Bsp.: 520 mm : 10 = 52 cm Bsp.: 120 h : 24 = 5 d 6 Weg FZ: s Einheiten: mm; cm;
Aufgabenübersicht für tägliche Übungen mit zugehörigen Klassenstufen: Größen mit Formelzeichen, Einheiten und Umrechnungen: Bsp.: 520 mm : 10 = 52 cm Bsp.: 120 h : 24 = 5 d 6 Weg FZ: s Einheiten: mm; cm;
Medizinische Biophysik I.
 P H Y S I K Physik in de Medizin Medizinische Biophysik I. D. Feenc Tölgyesi feenc.tolgyesi@eok.sote.hu Institut fü Biophysik und Stahlenbiologie 0 Diagnostik Röntgendiagnostik Sonogaphie Optische Tomogaphie
P H Y S I K Physik in de Medizin Medizinische Biophysik I. D. Feenc Tölgyesi feenc.tolgyesi@eok.sote.hu Institut fü Biophysik und Stahlenbiologie 0 Diagnostik Röntgendiagnostik Sonogaphie Optische Tomogaphie
Hochschule Düsseldorf University of Applied Sciences. 26. April 2017 HSD. Energiespeicher Wärme
 Energiespeicher 02 - Wärme Wiederholung Energiearten Primärenergie Physikalische Energie Kernenergie Chemische Energie Potentielle Energie Kinetische Energie Innere Energie Quelle: Innere Energie Innere
Energiespeicher 02 - Wärme Wiederholung Energiearten Primärenergie Physikalische Energie Kernenergie Chemische Energie Potentielle Energie Kinetische Energie Innere Energie Quelle: Innere Energie Innere
1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen!
 1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen! Aggregatzustände Fest, flüssig, gasförmig Schmelz -wärme Kondensations -wärme Die Umwandlung von Aggregatzuständen
1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen! Aggregatzustände Fest, flüssig, gasförmig Schmelz -wärme Kondensations -wärme Die Umwandlung von Aggregatzuständen
Federkraft: F 1 = -bx (b = 50 N/m) Gravitationskraft: F 2 = mg (g = 9,8 m/s 2 )
 Aufgabe: Schwingung An eine Stahlfeder wird eine Kugel mit der Masse 500g gehängt. Federkraft: F 1 -b (b 50 N/m) Gravitationskraft: F mg (g 9,8 m/s ) m 500g F ma W 1 F( ) d W kin 1 mv b ( t + ϕ ) Acos(
Aufgabe: Schwingung An eine Stahlfeder wird eine Kugel mit der Masse 500g gehängt. Federkraft: F 1 -b (b 50 N/m) Gravitationskraft: F mg (g 9,8 m/s ) m 500g F ma W 1 F( ) d W kin 1 mv b ( t + ϕ ) Acos(
Physikalische. Grundlagen. L. Kölling, Fw Minden
 Physikalische Grundlagen L. Kölling, Fw Minden Radioaktivität kann man weder sehen, hören, fühlen, riechen oder schmecken. Daher muss sie der FA (SB) zumindest verstehen, um im Einsatzfall die erforderlichen
Physikalische Grundlagen L. Kölling, Fw Minden Radioaktivität kann man weder sehen, hören, fühlen, riechen oder schmecken. Daher muss sie der FA (SB) zumindest verstehen, um im Einsatzfall die erforderlichen
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg
 TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg GRUNDLAGEN Modul: Versuch: Gießen von Metallen (Änderung von Volumen und
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg GRUNDLAGEN Modul: Versuch: Gießen von Metallen (Änderung von Volumen und
Onsagersche Gleichung. Energetische Beziehungen
 Onsagersche Gleichung. Energetische Beziehungen R I 4 V t t 1 r 8... D A p l J LX c x Zustandsgrössen sind Grössen, die zur Beschreibung des Zustandes eines stofflichen Systems dienen, T, V, p, m,... T,
Onsagersche Gleichung. Energetische Beziehungen R I 4 V t t 1 r 8... D A p l J LX c x Zustandsgrössen sind Grössen, die zur Beschreibung des Zustandes eines stofflichen Systems dienen, T, V, p, m,... T,
Allgemeine Chemie I Herbstsemester 2012
 Lösung 4 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Im Vorlesungsskript sind für Xenon die Werte σ(xe) = 406 pm und ε = 236 kjmol 1 tabelliert. ( ) 12 ( ) 6 σ σ E i j = 4ε (1) r i j r i j r i j
Lösung 4 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Im Vorlesungsskript sind für Xenon die Werte σ(xe) = 406 pm und ε = 236 kjmol 1 tabelliert. ( ) 12 ( ) 6 σ σ E i j = 4ε (1) r i j r i j r i j
Physik III im Studiengang Elektrotechnik
 Physik III im Studiengang Elektrotechnik - Einführung in die Wärmelehre - Prof. Dr. Ulrich Hahn WS 2008/09 Entwicklung der Wärmelehre Sinnesempfindung: Objekte warm kalt Beschreibung der thermische Eigenschaften
Physik III im Studiengang Elektrotechnik - Einführung in die Wärmelehre - Prof. Dr. Ulrich Hahn WS 2008/09 Entwicklung der Wärmelehre Sinnesempfindung: Objekte warm kalt Beschreibung der thermische Eigenschaften
Grundwissen Chemie 9. Jahrgangsstufe G8
 Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Basiswissen Physikalische Chemie
 Claus Czeslik Heiko Seemann Roland.Winter Basiswissen Physikalische Chemie 4., aktualisierte Auflage STUDIUM VIEWEG+ TEUBNER Inhaltsverzeichnis Vorwort Liste der wichtigsten Symbole V XI 1 Aggregatzustände.
Claus Czeslik Heiko Seemann Roland.Winter Basiswissen Physikalische Chemie 4., aktualisierte Auflage STUDIUM VIEWEG+ TEUBNER Inhaltsverzeichnis Vorwort Liste der wichtigsten Symbole V XI 1 Aggregatzustände.
= n + + Thermodynamik von Elektrolytlösungen. Wdhlg: Chemisches Potential einer Teilchenart: Für Elektrolytlösungen gilt: wobei : und
 Elektrolyte Teil III Solvatation, elektrische Leitfähigkeit, starke und schwache Elektrolyte, Ionenstärke, Debye Hückeltheorie, Migration, Diffusion, Festelektrolyte Thermodynamik von Elektrolytlösungen
Elektrolyte Teil III Solvatation, elektrische Leitfähigkeit, starke und schwache Elektrolyte, Ionenstärke, Debye Hückeltheorie, Migration, Diffusion, Festelektrolyte Thermodynamik von Elektrolytlösungen
Modelle zur Beschreibung von Gasen und deren Eigenschaften
 Prof. Dr. Norbert Hampp 1/7 1. Das Ideale Gas Modelle zur Beschreibung von Gasen und deren Eigenschaften Modelle = vereinfachende mathematische Darstellungen der Realität Für Gase wollen wir drei Modelle
Prof. Dr. Norbert Hampp 1/7 1. Das Ideale Gas Modelle zur Beschreibung von Gasen und deren Eigenschaften Modelle = vereinfachende mathematische Darstellungen der Realität Für Gase wollen wir drei Modelle
Physik 4: Skalen und Strukturen
 Physik 4: Skalen und Strukturen.5: Kleine Skalen Chemische Bindung Aggregatszustände Kristallstrukturen und Streuung Bildung des Lebens Kovalente Molekülbindungen Ladungsdichteverteilungen: CH 4 NH 3 H
Physik 4: Skalen und Strukturen.5: Kleine Skalen Chemische Bindung Aggregatszustände Kristallstrukturen und Streuung Bildung des Lebens Kovalente Molekülbindungen Ladungsdichteverteilungen: CH 4 NH 3 H
PROBLEME AUS DER PHYSIK
 Helmut Vogel PROBLEME AUS DER PHYSIK Aufgaben und Lösungen zur 16. Auflage von Gerthsen Kneser Vogel Physik Mit über 1100 Aufgaben, 158 Abbildungen und 16 Tabellen Springer-Verlag Berlin Heidelberg New
Helmut Vogel PROBLEME AUS DER PHYSIK Aufgaben und Lösungen zur 16. Auflage von Gerthsen Kneser Vogel Physik Mit über 1100 Aufgaben, 158 Abbildungen und 16 Tabellen Springer-Verlag Berlin Heidelberg New
Kondensationswärme. Verdampfungswärme. Resublimationswärme. Sublimationswärme. Erstarrungswärme. Schmelzwärme. Energie (Enthalpie) Energie (Enthalpie)
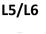 A. Soi 2017 18 81 Energie (Enthalpie) Energie (Enthalpie) Gasförmig Flüssig Schmelzwärme (Schmelzenthalpie) Verdampfungswärme (Schmelzenthalpie) Sublimationswärme (Sublimationsenthalpie) Fest Gasförmig
A. Soi 2017 18 81 Energie (Enthalpie) Energie (Enthalpie) Gasförmig Flüssig Schmelzwärme (Schmelzenthalpie) Verdampfungswärme (Schmelzenthalpie) Sublimationswärme (Sublimationsenthalpie) Fest Gasförmig
Die kinetische Gastheorie beruht auf den folgenden drei Annahmen:
 Physikalische Chemie Modul II Versuch: Reales Gas 20. Juli 2010 1 Einleitung Die kinetische Gastheorie beruht auf den folgenden drei Annahmen: 1. Das Gas besteht aus Molekülen der Masse m und dem Durchmesser
Physikalische Chemie Modul II Versuch: Reales Gas 20. Juli 2010 1 Einleitung Die kinetische Gastheorie beruht auf den folgenden drei Annahmen: 1. Das Gas besteht aus Molekülen der Masse m und dem Durchmesser
Physik 4: Skalen und Strukturen
 Physik 4: Skalen und Strukturen Kapitel : Festkörperphysik.1 Aggregatszustände. Kristallstrukturen.3 Chemische Bindung.4 Gitterschwingungen.5 Elektronen im Festkörper Phasendiagramm von CO Klassisches
Physik 4: Skalen und Strukturen Kapitel : Festkörperphysik.1 Aggregatszustände. Kristallstrukturen.3 Chemische Bindung.4 Gitterschwingungen.5 Elektronen im Festkörper Phasendiagramm von CO Klassisches
Definiere den Begriff Chemischer Vorgang! Definiere den Begriff Physikalischer Vorgang!
 Chemischer Vorgang! Stoffänderung, keine Zustandsänderung, mit Energiebeteiligung Physikalischer Vorgang! Zustandsänderung, keine Stoffänderung (z.b. Lösen, Aggregatzustände,...) Erkläre die Begriffe heterogenes
Chemischer Vorgang! Stoffänderung, keine Zustandsänderung, mit Energiebeteiligung Physikalischer Vorgang! Zustandsänderung, keine Stoffänderung (z.b. Lösen, Aggregatzustände,...) Erkläre die Begriffe heterogenes
Grundpraktikum für Biologen 2016
 Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
1902-KLAUSURVORBEREITUNG ALLGEMEINE CHEMIE
 1902-KLAUSURVORBEREITUNG ALLGEMEINE CHEMIE ATOMBAU 1) (6 Punkte) Der Atomkern eines Reinelements enthält 78 Neutronen. a) Geben Sie ein vollständiges Elementsymbol für dieses Reinelement an. b) Geben Sie
1902-KLAUSURVORBEREITUNG ALLGEMEINE CHEMIE ATOMBAU 1) (6 Punkte) Der Atomkern eines Reinelements enthält 78 Neutronen. a) Geben Sie ein vollständiges Elementsymbol für dieses Reinelement an. b) Geben Sie
Biophysik für Pharmazeuten I.
 Biophysik für Pharmazeuten I. Prof. László Smeller laszlo.smeller@eok.sote.hu Dr. Attila Bérces attila.berces@eok.sote.hu Dr. Pál Gróf pal.grof@eok.sote.hu 1 Thematik 13 Vorlesungen: Woche Thema Vortragende
Biophysik für Pharmazeuten I. Prof. László Smeller laszlo.smeller@eok.sote.hu Dr. Attila Bérces attila.berces@eok.sote.hu Dr. Pál Gróf pal.grof@eok.sote.hu 1 Thematik 13 Vorlesungen: Woche Thema Vortragende
Ferienkurs Experimentalphysik II Thermodynamik Grundlagen
 Ferienkurs Experimentalphysik II Thermodynamik Grundlagen Lennart Schmidt 08.09.2011 Inhaltsverzeichnis 1 Grundlagen 3 1.1 Temperatur und Wärme............................ 3 1.2 0. und 1. Hauptsatz..............................
Ferienkurs Experimentalphysik II Thermodynamik Grundlagen Lennart Schmidt 08.09.2011 Inhaltsverzeichnis 1 Grundlagen 3 1.1 Temperatur und Wärme............................ 3 1.2 0. und 1. Hauptsatz..............................
1.2 Zustandsgrößen, Zustandsänderungen, Gleichgewichtszustand
 1.2 Zustandsgrößen, Zustandsänderungen, Gleichgewichtszustand Wie erfolgt die Beschreibung des Zustands eines Systems? über Zustandsgrößen (makroskopische Eigenschaften, die den Zustand eines Systems kennzeichnen)
1.2 Zustandsgrößen, Zustandsänderungen, Gleichgewichtszustand Wie erfolgt die Beschreibung des Zustands eines Systems? über Zustandsgrößen (makroskopische Eigenschaften, die den Zustand eines Systems kennzeichnen)
Bohrsches Atommodell
 Atome und ihre Bindungen Atomaufbau Im Atomkern befinden sich die Protonen (positiv geladen) und die Neutronen (neutral). P und N sind ungefähr gleich schwer und machen 99% der Atommasse aus. Um den Kern
Atome und ihre Bindungen Atomaufbau Im Atomkern befinden sich die Protonen (positiv geladen) und die Neutronen (neutral). P und N sind ungefähr gleich schwer und machen 99% der Atommasse aus. Um den Kern
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C?
 A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
Zustandsbeschreibungen
 Aggregatzustände fest Kristall, geordnet Modifikationen Fernordnung flüssig teilgeordnet Fluktuationen Nahordnung gasförmig regellose Bewegung Unabhängigkeit ngigkeit (ideales Gas) Zustandsbeschreibung
Aggregatzustände fest Kristall, geordnet Modifikationen Fernordnung flüssig teilgeordnet Fluktuationen Nahordnung gasförmig regellose Bewegung Unabhängigkeit ngigkeit (ideales Gas) Zustandsbeschreibung
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bislang geschah Kovalente Bindung Oktett-Regel Valence-Bond-Theorie
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bislang geschah Kovalente Bindung Oktett-Regel Valence-Bond-Theorie
Alle Atome haben Massen ungefähr einem vielfachen der Masse des Wasserstoff Atoms.
 02. Atom Page 1 2. Das Atom Atom: kleinster unveränderbarer Bestandteil eines chemischen Elements Charakteristische Eigenschaften von Atomen: Masse, Volumen, Ladung 2.1 Bestimmung der Atommasse expt. Befund:
02. Atom Page 1 2. Das Atom Atom: kleinster unveränderbarer Bestandteil eines chemischen Elements Charakteristische Eigenschaften von Atomen: Masse, Volumen, Ladung 2.1 Bestimmung der Atommasse expt. Befund:
