Medizinische Biophysik I.
|
|
|
- Hedwig Schulz
- vor 6 Jahren
- Abrufe
Transkript
1 P H Y S I K Physik in de Medizin Medizinische Biophysik I. D. Feenc Tölgyesi Institut fü Biophysik und Stahlenbiologie 0 Diagnostik Röntgendiagnostik Sonogaphie Optische Tomogaphie MRI KG ndosko Theapie Gamma-Messe Phototheapie Lasechiugie Defibillato Nieensteinzetümm Medizinische Foschung Röntgendiffaktion Optische Spektoskopie Mikoskopie Massenspektometie Lebenspozesse Diffusion Stömungen Hebelfunktion Wämestahlung elektische Stöme... 1 Physik in dem medizinischen Cuiculum Thematik de Volesungen Physiologie Chemie Biostatistik Biochemie Molekulabiologie Radiologie Chiugie Othopädie Kiefeothopädie usw. 4 1
2 Paktika Abweichung fü Zahnmedizine in den esten dei Wochen: Potokolle! Hilfsmittel: Paktikum medizinische Biophysik, 015, Semmelweis Velag, Budapest Biophysik fü Medizine, 008, Medicina Velag, Budapest Physikalische Gundkenntnisse, heunteladba von de Webseite des Instituts Aufgabensammlung zu medizinischen Biophysik, heunteladba von de Webseite des Instituts 5 6 Studienegel Voaussetzungen de Anekennung des Semestes Püfungen Anekennung von Scheinen aus füheen Studien Webseite: Medizinische Biophysik Stuktu de Mateie I. Atome, Moleküle und ihe Wechselwikungen 1. Allgemein übe Wechselwikungen a) Beispiele: b) Bescheibung de Wechselwikungen:. lektische Wechselwikung a) Coulomb-Gesetz: b) elektische potenzielle negie ( pot ). Aufbau des Atoms a) Bauelemente und ihe Wechselwikungen b) negiezustände c) lektonegativität 4. Atomae, molekulae Wechselwikungen a) negiekuve b) Pimäe Bindungen c) Sekundäe Bindungen 5. negiezustände in Molekülen II. Aggegatzustände 1. Allgemeine Bescheibung. inige gundlegenden Gößen zu Bescheibung von Köpen. Gasfömige Aggegatzustand a) Makoskopische Bescheibung b) Mikoskopische Bescheibung c) Kinetische Deutung de Tempeatu d) Maxwell-Boltzmann-Veteilung e) Baometische Höhenfomel (Gas im Gavitationsfeld) f) Boltzmann-Veteilung 7 8
3 I. Atome, Moleküle und ihe Wechselwikungen 1. Allgemein übe Wechselwikungen a) Beispiele: Stake Wechselwikung (Kenkaft) Kontakt (molekulae Wechselwikungen im Hintegund) lektische Wechselwikung Gavitation Magnetische Wechselwikung 9 10 b) Bescheibung de Wechselwikungen: Symmetie! Stäke d. Ww Themische Wechselwikung (Wäme) Bei fenwikenden Ww: Abklingen mit wachsendem Abstand Gößen und Gesetze: Kaft, die newtonschen Gesetze und Beispiele fü Kaftgesetze Abeit und negie negieehaltung Leistung Duck Abstand Kaft negie Chemische, biologische, Wechselwikungen 11 1
4 Gebundene Zustände ntstehung von stabilen Stuktuen - allgemeine Pinzipien WCHSLWIRKUNGN abstoßend anziehend. lektische Wechselwikung q q a) Coulomb-Gesetz: Fel k F q F q 1 1 F + + Abstoß Anziehung + UNORDNUNG ORDNUNG s entstehen keine stabile Stuktuen, fühe entstandene Stuktuen lösen sich auf. BWGUNGN Wechselwikungsenegie Wie können die zwei Seiten miteinande quantitativ veglichen weden? negie Stabile Stuktuen entstehen und weden ehalten. Wechselwikungsenegie b) elektische potenzielle negie ( pot ): q1 q pot k Bewegungsenegie 1 14 pot + + Abstoß Anziehung +. Aufbau des Atoms a) Bauelemente und ihe Wechselwikungen Z lektonen, ihe Gesamtladung ist Ze b) negiezustände Spezielle igenschaft de Mikowelt: diskete negiezustände Feie Zustände Zum Beispiel: H-Atom elekt. Ladung des Kenes: Ze, (Z ist die Odnungszahl (Kenladungszahl)) Schalen kin 1 mv Bewegungen pot anziehende Wechselwikung = elektische Ww. q1 q pot k gesamt Hauptquantenzahl (n) kin gesamt pot kin 0 gebundenes lekton Statt Bahnen ehe lektonenwolken veschiedene Fomen gesamt pot kin 0 feies lekton
5 negie negie Nebenquantenzahl (l) Unteschalen Z.B. 11 Na Z.B. 17 Cl l = 0 s s shap; 1 p p pincipal; d diffuse; f fundamental d Weitee Pinzipien bei de Besetzung de negiezuständen (Schalen, Unteschalen): negieminimum Pauli-Pinzip f 17 1s s p 6 s 1 Ionisationsenegie (I): Zu ntfenung des äußesten lektons benötigte negie (ev/atom; kj/mol) c) lektonegativität (N) = I A 1s s p 6 s p 5 lektonenaffinität (A): Bei de Aufnahme eines lektons feigesetzte negie (ev/atom; kj/mol) 18 lektonegativitität - Pauling-Skala: 4. Atomae, molekulae Wechselwikungen a) negiekuve Abstoß zw. den Kenen, Pauli-Pinzip Bindung Bindungslänge ( 0 ) 0,1 nm Bindungsenegie ( 0 ) 0,-1000 kj/mol Bindungstypen gemeinsame lektonenbahnen elektische Anziehung (Ion-Ion, Ion-Dipol, Dipol-Dipol) lektonegativität
6 b) Pimäe Bindungen Ionenbindung Kovalente Bindung Metallbindung kj/mol 1 c) Sekundäe Bindungen 0,-50 kj/mol van de Waals (Dipol-Dipol) Oientieung ( pemanente Dipole) Pimäe und sekundäe Bindungen 5. negiezustände in Molekülen Moleküle Aggegatzustände (flüssige und feste Köpe) Induktion (1 pemanente und 1 induziete Dipol) Dispesion H-Bückenbindung Molekül lekton Vibation Rotation 1 ev 0,1 ev 0,01 ev alle negiefomen sind quantiet Bindungsstäke Bindungstyp Mateial Bindungsenegie (kj/mol) van de Waals Neon (Ne) 0,6 schwach Agon (A) 7,7 (sekundä) H-Bindung Wasse (H O) stak (pimä) Metallbindung Quecksilbe (Hg) 68 Aluminium (Al) 4 Wolfam (W) 849 Ionenbindung NaCl 640 MgO 1000 kovalente Bindung Silizium (Si) 450 Kohlenstoff (C, Diamant) 71 Z. B. Vibationen lektonenniveaus Vibationsniveaus (Rotationsniveaus sind nicht gezeigt.) 4 6
7 Dichte (g/cm ) II. Aggegatzustände 1. Allgemeine Bescheibung Fest Flüssig Gasfömig T. inige gundlegenden Gößen zu Bescheibung von Köpen: Zahl de Bauelemente (Atome ode Moleküle) im Köpe (N) igenvolumen igenfom Stoffmenge (n ) in Mol: 1 mol enthält 6,0 10 Bauelemente ν = N N A Avogado-Konstante (N A ): N A = 6,0 10 1/mol Masse (m) Molae Masse (M): die Masse von einem Mol m = ν M Volumen (V) 5 6 m kg Dichte (): ρ V m Anziehende Wechselwikungen Abstoßende Wechselwikungen + Bewegungen T Stoff (g/cm ) Wasse 1 Fettgewebe 0,9 Blut 1,05 Knochen 1,8 Köpegewebe 1,04 (Mittelwet) Wasse T(K) = t( C) + 7 Tempeatuabhängigkeit: is (T) : Tempeatu ( C) 7 8 7
8 . Gasfömige Aggegatzustand a) Makoskopische Bescheibung: Kein igenvolumen und keine igenfom Isotop Tempeatu Messbae Gößen: b) Mikoskopische Bescheibung: Ungeodnet Stake und fast feie Bewegungen p, V, n, T pv n RT (fü ideale Gase) Duck Volumen Stoffmenge allgemeine Gaskonstante R = 8,1 J/(molK) ine andee Fom: duchschnittliche kinetische negie von einem Mol kin, mol 1 Mv RT Molae Masse d) Maxwell-Boltzmann-Veteilung Allgemeine Gaskonstante R = 8,4 J/(mol K) RT = molae themische negie c) Kinetische Deutung de Tempeatu: duchschnittliche kinetische negie eines Teilchens kin 1 mv kt Masse eines Teilchens Geschwindigkeit des Teilchens Boltzmann-Konstante k = 1,8 10 J/K Tempeatu kt = themische negie 9 0 e) Baometische Höhenfomel (Gas im Gavitationsfeld) Gavitation (ohne Bewegungen, d. h. T = 0) Bewegung (ohne Gavitation) p p 0 p e mgh kt Duck bei h = 0 p 0 p e mgh kt h (km) Nu im themischen Gleichgewicht!! 1 8
9 f) Boltzmann-Veteilung Die Veteilung de Teilchen auf die negiezustände im themischen Gleichgewicht (T = konstant). n i 0 kt i n0 e n0 n i n 0 e RT e kt NA R k N A Hausaufgaben: Aufgabensammlung : 1.1,, 4, 5, 8, 9, 17, 0, 1,, 6, 7, 1, 4, 6, 8, 40 nomale Besetzung siehe Besetzungsinvesion späte bei dem Lase Anwendungen de Boltzmann-Veteilung: Baometische Höhenfomel Themische lektonenemission von Metallen Konzentationselemente, Nenst-Gleichung Chemische Reaktionen (Geschwindigkeits- und Gleichgewichtskonstante) Konzentation von themischen Punktdefekten (in Kistallen und Makomolekülen) lektische Leitfähigkeit von Halbleiten... (Gilt abe nicht z. B. bei de Besetzung de lektonenschalen in einem Atom!) 4 9
Medizinische Biophysik I.
 Physik in de Medizin Medizinische Biophysik I. D. Feenc Tölgyesi tolgyesi.feenc @med.semmelweis-univ.hu Institut fü Biophysik und Stahlenbiologie 0 Diagnostik Röntgendiagnostik Sonogaphie Optische Tomogaphie
Physik in de Medizin Medizinische Biophysik I. D. Feenc Tölgyesi tolgyesi.feenc @med.semmelweis-univ.hu Institut fü Biophysik und Stahlenbiologie 0 Diagnostik Röntgendiagnostik Sonogaphie Optische Tomogaphie
Medizinische Biophysik I.
 Thematik de Volesungen Medizinische Biophysik I. 0 D. Feenc Tölgyesi tolgyesi.feenc @med.semmelweis-univ.hu Institut fü Biophysik und Stahlenbiologie 1 Abweichung fü Zahnmedizine in den esten dei Wochen:
Thematik de Volesungen Medizinische Biophysik I. 0 D. Feenc Tölgyesi tolgyesi.feenc @med.semmelweis-univ.hu Institut fü Biophysik und Stahlenbiologie 1 Abweichung fü Zahnmedizine in den esten dei Wochen:
Medizinische Biophysik I.
 P H Y S I K Physik in de Medizin Medizinische Biophysik I. D. Feenc Tölgyesi tolgyesi.feenc @med.semmelweis-univ.hu Institut fü Biophysik und Stahlenbiologie 0 Diagnostik Röntgendiagnostik Sonogaphie Optische
P H Y S I K Physik in de Medizin Medizinische Biophysik I. D. Feenc Tölgyesi tolgyesi.feenc @med.semmelweis-univ.hu Institut fü Biophysik und Stahlenbiologie 0 Diagnostik Röntgendiagnostik Sonogaphie Optische
Medizinische Biophysik I.
 P H Y S I K Physik in de Medizin Medizinische Biophysik I. D. Feenc Tölgyesi feenc.tolgyesi@eok.sote.hu Institut fü Biophysik und Stahlenbiologie 0 Diagnostik Röntgendiagnostik Sonogaphie Optische Tomogaphie
P H Y S I K Physik in de Medizin Medizinische Biophysik I. D. Feenc Tölgyesi feenc.tolgyesi@eok.sote.hu Institut fü Biophysik und Stahlenbiologie 0 Diagnostik Röntgendiagnostik Sonogaphie Optische Tomogaphie
Medizinische Biophysik 4
 I. Atomae, molekulae Wechselwikungen. Im Allgemeinen übe Wechselwikungen a) Kaft omändeung (Defomation) Medizinische Biophysik 4 Stuktu de Mateie Wechselwikung!! Bewegungsändeung (Beschleunigung, a) a
I. Atomae, molekulae Wechselwikungen. Im Allgemeinen übe Wechselwikungen a) Kaft omändeung (Defomation) Medizinische Biophysik 4 Stuktu de Mateie Wechselwikung!! Bewegungsändeung (Beschleunigung, a) a
Physikalische Grundlagen der zahnäzrtlichen Materialkunde
 Waum? Hestellung Stuktu Z.B.: Eigenschaften Zahnäztliche Vewendung Physikalische Gundlagen de zahnäztlichen Mateialkunde 1. Einfühung 1 alle: Al O! Was? "Sage es mi, und ich vegesse es; zeige es mi, und
Waum? Hestellung Stuktu Z.B.: Eigenschaften Zahnäztliche Vewendung Physikalische Gundlagen de zahnäztlichen Mateialkunde 1. Einfühung 1 alle: Al O! Was? "Sage es mi, und ich vegesse es; zeige es mi, und
Physikalische Grundlagen der zahnäzrtlichen Materialkunde. Einführung
 Physikalische Grundlagen der zahnäzrtlichen Materialkunde 1. Einführung 1 Warum? Herstellung Struktur Z.B.: Eigenschaften Zahnärztliche Verwendung alle: Al 2 O 3! 2 Was? Wie? 3 "Sage es mir, und ich vergesse
Physikalische Grundlagen der zahnäzrtlichen Materialkunde 1. Einführung 1 Warum? Herstellung Struktur Z.B.: Eigenschaften Zahnärztliche Verwendung alle: Al 2 O 3! 2 Was? Wie? 3 "Sage es mir, und ich vergesse
Elektrizitätslehre. Elektrische Ladungen und Felder. Aufbau des Stoffes. Elektrisches Feld Elektrische Ww. Elektrische Ladung. Dauermagnet.
 lektizitätslehe lektische Ladungen und elde Aufbau des Stoffes lektische Ladung lektisches eld lektische Ww Stomkeise Stom Induziete Stom Magnetfeld magnetische Ww Dauemagnet lektomagnetische Schwingungen
lektizitätslehe lektische Ladungen und elde Aufbau des Stoffes lektische Ladung lektisches eld lektische Ww Stomkeise Stom Induziete Stom Magnetfeld magnetische Ww Dauemagnet lektomagnetische Schwingungen
Elektrizitätslehre. Elektrische Ladungen und Felder. Aufbau des Stoffes. Elektrisches Feld Elektrische Ww. Elektrische Ladung. Dauermagnet.
 lektizitätslehe lektische Ladungen und elde Aufbau des Stoffes lektische Ladung lektisches eld lektische Ww Stomkeise Stom Induziete Stom Magnetfeld magnetische Ww Dauemagnet lektomagnetische Schwingungen
lektizitätslehe lektische Ladungen und elde Aufbau des Stoffes lektische Ladung lektisches eld lektische Ww Stomkeise Stom Induziete Stom Magnetfeld magnetische Ww Dauemagnet lektomagnetische Schwingungen
Biophysik für Pharmazeuten I Struktur der Materie Tölgyesi Ferenc
 Biophysik für Pharmazeuten I. 014. 09.. Struktur der Materie Tölgyesi Ferenc Atomarer Aufbau der Materie o Demokritos 5.Jht v.chr. o Daltonsches Gesetz 180 o Moderne Mikroskope: Hausaufgaben: Neue Aufgabensammlung
Biophysik für Pharmazeuten I. 014. 09.. Struktur der Materie Tölgyesi Ferenc Atomarer Aufbau der Materie o Demokritos 5.Jht v.chr. o Daltonsches Gesetz 180 o Moderne Mikroskope: Hausaufgaben: Neue Aufgabensammlung
Medizinische Biophysik 3
 II. Wellenoptik. Im Allgemeinen übe Schwingungen und Wellen c) Mechanische Wellen Medizinische Biophysik 3 Licht in de Medizin (otsetzung) Polaisation (lineae Polaisation) nichtpolaisiete Welle Nu bei
II. Wellenoptik. Im Allgemeinen übe Schwingungen und Wellen c) Mechanische Wellen Medizinische Biophysik 3 Licht in de Medizin (otsetzung) Polaisation (lineae Polaisation) nichtpolaisiete Welle Nu bei
Medizinische Biophysik
 2. Gasförmiger Aggregatzustand Medizinische Biophysik c) Kinetische Deutung der Temperatur: d) Maxwell-Boltzmann-Verteilung e) Barometrische Höhenformel (Gas im Gravitationsfeld) f) Boltzmann-Verteilung
2. Gasförmiger Aggregatzustand Medizinische Biophysik c) Kinetische Deutung der Temperatur: d) Maxwell-Boltzmann-Verteilung e) Barometrische Höhenformel (Gas im Gravitationsfeld) f) Boltzmann-Verteilung
Warum? Elektrizitätslehre. Elektrische Erscheinungen. Logik des Aufbaues des Lehrstoffes der Elektrizitätslehre
 lektizitätslehe aum? lektische scheinungen in lebende Mateie: Ruhepotential, Aktionspotential, KG, MG t lektische Geäte in de äztlichen Paxis: KG, MG, ltaschall, Defibillato, T, NMR, ämetheapie t Logik
lektizitätslehe aum? lektische scheinungen in lebende Mateie: Ruhepotential, Aktionspotential, KG, MG t lektische Geäte in de äztlichen Paxis: KG, MG, ltaschall, Defibillato, T, NMR, ämetheapie t Logik
Kerne und Teilchen. Kernkraft. Moderne Experimentalphysik III Vorlesung 16. MICHAEL FEINDT INSTITUT FÜR EXPERIMENTELLE KERNPHYSIK
 Kene und Teilchen Modene Expeimentalphysik III Volesung 16 MICHAEL FEINDT INSTITUT FÜ EXPEIMENTELLE KENPHYSIK Kenkaft KIT Univesität des Landes Baden-Wüttembeg und nationales Foschungszentum in de Helmholtz-Gemeinschaft
Kene und Teilchen Modene Expeimentalphysik III Volesung 16 MICHAEL FEINDT INSTITUT FÜ EXPEIMENTELLE KENPHYSIK Kenkaft KIT Univesität des Landes Baden-Wüttembeg und nationales Foschungszentum in de Helmholtz-Gemeinschaft
Elektrostatik. Salze lösen sich in Wasser um Lösungen geladener Ionen zu bilden, die drei Viertel der Erdoberfläche bedecken.
 Elektostatik Elektische Wechselwikungen zwischen Ladungen bestimmen gosse Teile de Physik, Chemie und Biologie. z.b. Sie sind die Gundlage fü stake wie schwache chemische Bindungen. Salze lösen sich in
Elektostatik Elektische Wechselwikungen zwischen Ladungen bestimmen gosse Teile de Physik, Chemie und Biologie. z.b. Sie sind die Gundlage fü stake wie schwache chemische Bindungen. Salze lösen sich in
Kap. 8 Thermodynamik
 Kap. 8 Themodynamik 1. Tempeatu und Wämeenegie 2. Wämeleitung und Diffusion 3. Hauptsätze de Themodynamik 4. Reale Gase M. zu Nedden / S. Kowaik Volesung 23 Mechanik und Themodynamik (Physik I) Seite 1
Kap. 8 Themodynamik 1. Tempeatu und Wämeenegie 2. Wämeleitung und Diffusion 3. Hauptsätze de Themodynamik 4. Reale Gase M. zu Nedden / S. Kowaik Volesung 23 Mechanik und Themodynamik (Physik I) Seite 1
Medizinische Biophysik
 2. Gasförmiger Aggregatzustand a) Makroskopische Beschreibung b) Mikroskopische Beschreibung Medizinische Biophysik c) Kinetische Deutung der Temperatur d) Maxwell-Boltzmann-Verteilung e) Barometrische
2. Gasförmiger Aggregatzustand a) Makroskopische Beschreibung b) Mikroskopische Beschreibung Medizinische Biophysik c) Kinetische Deutung der Temperatur d) Maxwell-Boltzmann-Verteilung e) Barometrische
Biophysik für Pharmazeuten I.
 Biophysik fü Phamazeuten I. Biomechanik 04. 09. 5. Mechanik Tölgyesi eenc Mechanik Kinematik (Bewegungslehe) Tanslation Veschiebung Rotation Dehung Allgemeine Bewegung = Tanslation + Rotation Bezugssystem
Biophysik fü Phamazeuten I. Biomechanik 04. 09. 5. Mechanik Tölgyesi eenc Mechanik Kinematik (Bewegungslehe) Tanslation Veschiebung Rotation Dehung Allgemeine Bewegung = Tanslation + Rotation Bezugssystem
Biophysik für Pharmazeuten I.
 Biohysik für Pharmazeuten I. Allgemeine Prinziien Wechselwirkungen Bewegungen abstoßend anziehend Ekin = 1 mv 015/16 Vorlesung 3 E ot E Z.B. elektrisch r Struktur der Materie Unordnung + E kin q1 q = k
Biohysik für Pharmazeuten I. Allgemeine Prinziien Wechselwirkungen Bewegungen abstoßend anziehend Ekin = 1 mv 015/16 Vorlesung 3 E ot E Z.B. elektrisch r Struktur der Materie Unordnung + E kin q1 q = k
Wiederholung: elektronische Eigenschaften
 Wiedeholung: elektonische igenschaten Die igenschaten des elektonischen Systems eines Mateiales haben inluss au: + Leitähigkeit + Optische igenschaten + Magnetische igenschaten + Adsoption und Adhäsion
Wiedeholung: elektonische igenschaten Die igenschaten des elektonischen Systems eines Mateiales haben inluss au: + Leitähigkeit + Optische igenschaten + Magnetische igenschaten + Adsoption und Adhäsion
BIOPHYSIK. Thematik der Vorlesungen. Mikrowelt. Praktikum. 03. Sept. Atome. Gas. Flüssigkeit 10. Sept. Festkörper.
 BIOPHYSIK Die Rolle de Biopysik in de Veteinämedizin pysikalisce Gundlagen von Lebenspozessen pysikalisce Metoden in de Teapie und Diagnostik Hilfsmittel KAD 007.09.03 Hebstsemeste Fülingssemeste Biopysik
BIOPHYSIK Die Rolle de Biopysik in de Veteinämedizin pysikalisce Gundlagen von Lebenspozessen pysikalisce Metoden in de Teapie und Diagnostik Hilfsmittel KAD 007.09.03 Hebstsemeste Fülingssemeste Biopysik
4.11 Wechselwirkungen und Kräfte
 4.11 Wechselwikungen und Käfte Kaft Wechselwikung Reichweite (m) Relative Stäke Gavitationskaft zwischen Massen Gavitationsladung (Anziehend) 1-22 Schwache Kaft Wechselwikung beim β-zefall schwache Ladung
4.11 Wechselwikungen und Käfte Kaft Wechselwikung Reichweite (m) Relative Stäke Gavitationskaft zwischen Massen Gavitationsladung (Anziehend) 1-22 Schwache Kaft Wechselwikung beim β-zefall schwache Ladung
4.3 Magnetostatik Beobachtungen
 4.3 Magnetostatik Gundlegende Beobachtungen an Magneten Auch unmagnetische Köpe aus Fe, Co, Ni weden von Magneten angezogen. Die Kaftwikung an den Enden, den Polen, ist besondes goß. Eine dehbae Magnetnadel
4.3 Magnetostatik Gundlegende Beobachtungen an Magneten Auch unmagnetische Köpe aus Fe, Co, Ni weden von Magneten angezogen. Die Kaftwikung an den Enden, den Polen, ist besondes goß. Eine dehbae Magnetnadel
Physikalische Chemie I - Klassische Thermodynamik SoSe 2006 Prof. Dr. Norbert Hampp 1/7 3. Das reale Gas. Das reale Gas
 Pof. D. Nobet Ham 1/7. Das eale Gas Das eale Gas Fü die Bescheibung des ealen Gases weden die Gasteilchen betachtet als - massebehaftet - kugelfömig mit Duchmesse d - Wechselwikungen auf Gund von Diol-Diol-Wechselwikungen
Pof. D. Nobet Ham 1/7. Das eale Gas Das eale Gas Fü die Bescheibung des ealen Gases weden die Gasteilchen betachtet als - massebehaftet - kugelfömig mit Duchmesse d - Wechselwikungen auf Gund von Diol-Diol-Wechselwikungen
Kerne sind stark gebundene Systeme aus farbneutralen Nukleonen:
 X. Kenphysik. ukleonen und Kenkaft Kene sind stak gebundene Systeme aus fabneutalen ukleonen: Impuls de ukleonen aufgund Unschäfeelationen elativ goß (s. späte). Bild feie ukleonen in einem effektiven
X. Kenphysik. ukleonen und Kenkaft Kene sind stak gebundene Systeme aus fabneutalen ukleonen: Impuls de ukleonen aufgund Unschäfeelationen elativ goß (s. späte). Bild feie ukleonen in einem effektiven
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern?
 An welche Stichwöte von de letzten Volesung können Sie sich noch einnen? Positive und negative Ladung Das Coulombsche Gesetz F 1 4πε q q 1 Quantisieung und haltung de elektischen Ladung e 19 1, 6 1 C Das
An welche Stichwöte von de letzten Volesung können Sie sich noch einnen? Positive und negative Ladung Das Coulombsche Gesetz F 1 4πε q q 1 Quantisieung und haltung de elektischen Ladung e 19 1, 6 1 C Das
Abbildung 9: zweiatomiges Molekül mit Bindungselektron. 2 e e e H
 Physik de kondensieten Mateie WS 00/0 5.0.00 c) Kovalente Kopplung Bei de kovalenten Kopplung handelt es sich um die Elektonenpaabildung zwischen nicht voll besetzten Obitalen. Zu Veanschaulichung diese
Physik de kondensieten Mateie WS 00/0 5.0.00 c) Kovalente Kopplung Bei de kovalenten Kopplung handelt es sich um die Elektonenpaabildung zwischen nicht voll besetzten Obitalen. Zu Veanschaulichung diese
Einführung in die Physik I. Elektromagnetismus 1
 infühung in die Physik I lektomagnetismus O. von de Lühe und. Landgaf lektische Ladung lektische Ladung bleibt in einem abgeschlossenen System ehalten s gibt zwei Aten elektische Ladung positive und negative
infühung in die Physik I lektomagnetismus O. von de Lühe und. Landgaf lektische Ladung lektische Ladung bleibt in einem abgeschlossenen System ehalten s gibt zwei Aten elektische Ladung positive und negative
PN 2 Einführung in die Experimentalphysik für Chemiker und Biologen
 PN 2 Einfühung in die Expeimentalphysik fü Chemike und Biologen 1. Volesung 20.4.07 Nadja Regne, Thomas Schmiee, Gunna Spieß, Pete Gilch Lehstuhl fü BioMolekulae Optik Depatment fü Physik Ludwig-Maximilians-Univesität
PN 2 Einfühung in die Expeimentalphysik fü Chemike und Biologen 1. Volesung 20.4.07 Nadja Regne, Thomas Schmiee, Gunna Spieß, Pete Gilch Lehstuhl fü BioMolekulae Optik Depatment fü Physik Ludwig-Maximilians-Univesität
Grundlagen der statistischen Physik und Thermodynamik
 Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Hier: Beschränkung auf die elektrische Eigenschaften
 IV. Festkörperphysik Hier: Beschränkung auf die elektrische Eigenschaften 3 Aggregatzustände: fest, flüssig, gasförmig: Wechselspiel Anziehungskräfte der Teilchen gegen die thermische Energie kt. Zustand
IV. Festkörperphysik Hier: Beschränkung auf die elektrische Eigenschaften 3 Aggregatzustände: fest, flüssig, gasförmig: Wechselspiel Anziehungskräfte der Teilchen gegen die thermische Energie kt. Zustand
Quantitative Bestimmung von anorganischen Arznei-, Hilfs- und Schadstoffen
 Semina zum Paktikum Quantitative Bestimmung von anoganischen Aznei-, Hilfs- und Schadstoffen im. Fachsemeste Phamazie I. Pinzipien de quantitativen Analyse Do, 10.4.008 Einfühung Ziel de quantitativen
Semina zum Paktikum Quantitative Bestimmung von anoganischen Aznei-, Hilfs- und Schadstoffen im. Fachsemeste Phamazie I. Pinzipien de quantitativen Analyse Do, 10.4.008 Einfühung Ziel de quantitativen
Materie in einem Kondensator
 Mateie in einem Kondensato In einen geladen Kondensato (Q konst.) wid a) eine Metallplatte b) isolieende Mateialien (Dielektika) eingebacht Metallplatte in einem Kondensato Die Metallplatte hat den gleichen
Mateie in einem Kondensato In einen geladen Kondensato (Q konst.) wid a) eine Metallplatte b) isolieende Mateialien (Dielektika) eingebacht Metallplatte in einem Kondensato Die Metallplatte hat den gleichen
PN 2 Einführung in die Experimentalphysik für Chemiker und Biologen
 PN 2 Einfühung in die alphysik fü Chemike und Biologen 2. Volesung 27.4.07 Nadja Regne, Thomas Schmiee, Gunna Spieß, Pete Gilch Lehstuhl fü BioMolekulae Optik Depatment fü Physik LudwigMaximiliansUnivesität
PN 2 Einfühung in die alphysik fü Chemike und Biologen 2. Volesung 27.4.07 Nadja Regne, Thomas Schmiee, Gunna Spieß, Pete Gilch Lehstuhl fü BioMolekulae Optik Depatment fü Physik LudwigMaximiliansUnivesität
- + E A. N m. Wasser. Oberflächenspannung, oder spezifische Oberflächenenergie ( ): Stoff (J/m 2 )* c) Oberflächenspannung
 Medizinische Biophysik Struktur der Materie Aggregatzustände: Gase, Flüssigkeiten, feste Körper 2. Vorlesung 12. 09. 2016 e) Barometrische Höhenformel (Gas im Gravitationsfeld) Gravitation (ohne Bewegungen,
Medizinische Biophysik Struktur der Materie Aggregatzustände: Gase, Flüssigkeiten, feste Körper 2. Vorlesung 12. 09. 2016 e) Barometrische Höhenformel (Gas im Gravitationsfeld) Gravitation (ohne Bewegungen,
Biophysik für Pharmazeuten I. 2016/17
 .09.06. Biophysik fü Phaazeuten I. 06/7 Mechanik Bioechanik Volesung Mechanik László Selle http://biofiz.sote.hu undlegende Begiffe de Physik, wie Kaft, Enegie,... Mechanik Kineatik (Bewegungslehe) Tanslation
.09.06. Biophysik fü Phaazeuten I. 06/7 Mechanik Bioechanik Volesung Mechanik László Selle http://biofiz.sote.hu undlegende Begiffe de Physik, wie Kaft, Enegie,... Mechanik Kineatik (Bewegungslehe) Tanslation
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I Dr. Helge Klemmer
 Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
Bezugssysteme neu beleuchtet
 Bezugssysteme neu beleuchtet D. Holge Hauptmann Euopa-Gymnasium Wöth Bezugsysteme neu beleuchtet, Folie 1 Kleine Vobemekung Beim Bezugssystemwechsel: ändet sich die mathematische Bescheibung das physikalische
Bezugssysteme neu beleuchtet D. Holge Hauptmann Euopa-Gymnasium Wöth Bezugsysteme neu beleuchtet, Folie 1 Kleine Vobemekung Beim Bezugssystemwechsel: ändet sich die mathematische Bescheibung das physikalische
II Wärmelehre 16. Phasenübergänge (Verdampfen, Schmelzen, Sublimieren) pt-diagramm
 16. Volesung EP II Wämelehe 16. Phasenübegänge (Vedampfen, Schmelzen, Sublimieen) pv-diagamm pt-diagamm III. Elektizität und Magnetismus 17. Elektostatik Elektische Ladung q Elektisches Feld E Potential
16. Volesung EP II Wämelehe 16. Phasenübegänge (Vedampfen, Schmelzen, Sublimieen) pv-diagamm pt-diagamm III. Elektizität und Magnetismus 17. Elektostatik Elektische Ladung q Elektisches Feld E Potential
1. Wärmelehre 1.1. Temperatur Wiederholung
 1. Wärmelehre 1.1. Temperatur Wiederholung a) Zur Messung der Temperatur verwendet man physikalische Effekte, die von der Temperatur abhängen. Beispiele: Volumen einer Flüssigkeit (Hg-Thermometer), aber
1. Wärmelehre 1.1. Temperatur Wiederholung a) Zur Messung der Temperatur verwendet man physikalische Effekte, die von der Temperatur abhängen. Beispiele: Volumen einer Flüssigkeit (Hg-Thermometer), aber
MECHANIK OHNE FERNWIRKUNG - mit Impuls und Impulsströmen
 MECHANIK OHNE FERNWIRKUNG - mit Impuls und Impulsstömen Holge Hauptmann Euopa-Gymnasium, Wöth am Rhein holge.hauptmann@gmx.de Mechanik mit Impuls und Impulsstömen 1 Impuls als Gundgöße de Mechanik De Impuls
MECHANIK OHNE FERNWIRKUNG - mit Impuls und Impulsstömen Holge Hauptmann Euopa-Gymnasium, Wöth am Rhein holge.hauptmann@gmx.de Mechanik mit Impuls und Impulsstömen 1 Impuls als Gundgöße de Mechanik De Impuls
Medizinische Biophysik 13
 Medizinische Biophysik 3 Kuze Rekapitulation de lektizitätslehe lektische Ladung Ladung: ist an Mateie gebunden, eine wesentliche igenschaft de Mateie (wie die Masse). Makoskopische Objekte sind im allgemeinen
Medizinische Biophysik 3 Kuze Rekapitulation de lektizitätslehe lektische Ladung Ladung: ist an Mateie gebunden, eine wesentliche igenschaft de Mateie (wie die Masse). Makoskopische Objekte sind im allgemeinen
Atome und Bindungen. Was sollen Sie mitnehmen?
 Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
PN 2 Einführung in die Experimentalphysik für Chemiker. 4. Vorlesung Evelyn Plötz, Thomas Schmierer, Gunnar Spieß, Peter Gilch
 PN 2 Einfühung in die alphysik fü Chemike 4. Volesung 9.5.08 Evelyn Plötz, Thomas Schmiee, Gunna Spieß, Pete Gilch Lehstuhl fü BioMolekulae Optik Depatment fü Physik Ludwig-Maximilians-Univesität München
PN 2 Einfühung in die alphysik fü Chemike 4. Volesung 9.5.08 Evelyn Plötz, Thomas Schmiee, Gunna Spieß, Pete Gilch Lehstuhl fü BioMolekulae Optik Depatment fü Physik Ludwig-Maximilians-Univesität München
Physikalische Chemie 0 Klausur, 22. Oktober 2011
 Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
4 Thermodynamik mikroskopisch: kinetische Gastheorie makroskopisch: System:
 Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung
 Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion 16. Phasenübergänge (Verdampfen, Schmelzen, Sublimieren) Versuche: Wärmeleitung
Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion 16. Phasenübergänge (Verdampfen, Schmelzen, Sublimieren) Versuche: Wärmeleitung
Besetzung der Orbitale
 Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Physik II TU Dortmund SS2018 Götz Uhrig Shaukat Khan Kapitel 5
 6 lektomagnetische Wellen egeben sich als Lösungen fü - und B-Felde aus den Maxwel-Gleichungen. Veschiedene Fomen: - Radio- und Mikowellen (Sende): Wellenlängen l 1 3 bis 1 - m, Fequenzen f 1 5 bis 1 11
6 lektomagnetische Wellen egeben sich als Lösungen fü - und B-Felde aus den Maxwel-Gleichungen. Veschiedene Fomen: - Radio- und Mikowellen (Sende): Wellenlängen l 1 3 bis 1 - m, Fequenzen f 1 5 bis 1 11
Atome und Bindungen. Was sollen Sie mitnehmen?
 Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
Arbeit in Kraftfeldern
 Abeit in Kaftfelden In einem Kaftfeld F ( ) ist F( )d die vom Feld bei Bewegung eines Köps entlang dem Weg geleistete Abeit. Achtung: Vozeichenwechsel bzgl. voheigen Beispielen Konsevative Kaftfelde Ein
Abeit in Kaftfelden In einem Kaftfeld F ( ) ist F( )d die vom Feld bei Bewegung eines Köps entlang dem Weg geleistete Abeit. Achtung: Vozeichenwechsel bzgl. voheigen Beispielen Konsevative Kaftfelde Ein
1. Wärmelehre 1.1. Temperatur. Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités)
 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
T T T T. Wärmeleitung. Zwei Reservoirs mit unterschiedlicher Temperatur werden in Kontakt gebracht. Die Gesamtentropien ändert sich wie: T 1 T 2
 Wämeleitung Zwei Resevois mit unteschieliche empeatu ween in Kontakt gebacht. Die Gesamtentopien änet sich wie: S S + 1 S 1 Die Äneung e Entopie S 1 ist Q S 1 integieen liefet: C m 1 ΔS1 C C ln 1 m 1 m
Wämeleitung Zwei Resevois mit unteschieliche empeatu ween in Kontakt gebacht. Die Gesamtentopien änet sich wie: S S + 1 S 1 Die Äneung e Entopie S 1 ist Q S 1 integieen liefet: C m 1 ΔS1 C C ln 1 m 1 m
Medizinische Biophysik
 4. Flüssiger Aggregatzustand Medizinische Biophysik a) Makroskopische Beschreibung b) Mikroskopische Beschreibung c) Oberflächenspannung Struktur der Materie Aggregatzustände: Gase, Flüssigkeiten, feste
4. Flüssiger Aggregatzustand Medizinische Biophysik a) Makroskopische Beschreibung b) Mikroskopische Beschreibung c) Oberflächenspannung Struktur der Materie Aggregatzustände: Gase, Flüssigkeiten, feste
5.5 Effekte an Flüssigkeitsgrenzflächen
 Physik I TU Dotmund WS017/18 Gudun Hille Shaukat Khan Kapitel 5 5.5 Effekte an Flüssigkeitsgenzflächen Genzfläche Flüssigkeit - Gas Moleküle an de Obefläche eine Flüssigkeit sind nicht von allen Seiten
Physik I TU Dotmund WS017/18 Gudun Hille Shaukat Khan Kapitel 5 5.5 Effekte an Flüssigkeitsgenzflächen Genzfläche Flüssigkeit - Gas Moleküle an de Obefläche eine Flüssigkeit sind nicht von allen Seiten
Lösungen zum Übungsblatt 5 zur Vorlesung Physikalische Chemie WS 2009/2010 Prof. Dr. Bartsch
 1 Lösungen zum Übungsblatt 5 zu Volesung hysikalische Chemie WS 29/21 o. D. Batsch 5.1 L (5 unkte Geben Sie die Deinition de Enthalpie an und zeigen Sie, dass die bei konstantem Duck zwischen System und
1 Lösungen zum Übungsblatt 5 zu Volesung hysikalische Chemie WS 29/21 o. D. Batsch 5.1 L (5 unkte Geben Sie die Deinition de Enthalpie an und zeigen Sie, dass die bei konstantem Duck zwischen System und
Um was geht es in dieser Vorlesung wirklich?
 Inhalt de Volesung 1. Elektostatik 2. Elektische Stom 3. Leitungsmechanismen 4. Magnetismus 5. Elektomagnetismus 6. Induktion 7. Maxwellsche Gleichungen 8. Wechselstom 9. Elektomagnetische Wellen 1 Um
Inhalt de Volesung 1. Elektostatik 2. Elektische Stom 3. Leitungsmechanismen 4. Magnetismus 5. Elektomagnetismus 6. Induktion 7. Maxwellsche Gleichungen 8. Wechselstom 9. Elektomagnetische Wellen 1 Um
Elektrizitätslehre 3.
 Elektrizitätslehre 3. Elektrischer Strom Strom = geordnete Bewegung der Ladungsträgern Ladungsträgern: Elektronen Ionen Strom im Vakuum Strom im Gas Strom in Flüssigkeit (Lösung) Strom im Festkörper Leiter
Elektrizitätslehre 3. Elektrischer Strom Strom = geordnete Bewegung der Ladungsträgern Ladungsträgern: Elektronen Ionen Strom im Vakuum Strom im Gas Strom in Flüssigkeit (Lösung) Strom im Festkörper Leiter
Gesetz von Boyle. Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V.
 Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
Bei der Wärmeübertragung kann man drei Transportvorgänge voneinander unterscheiden:
 6 ämeübetagung Bei de ämeübetagung kann man dei Tanspotvogänge voneinande untescheiden: ämeleitung ämeübegang / onvektion ämestahlung De ämetanspot duch Leitung ode onvektion benötigt einen stofflichen
6 ämeübetagung Bei de ämeübetagung kann man dei Tanspotvogänge voneinande untescheiden: ämeleitung ämeübegang / onvektion ämestahlung De ämetanspot duch Leitung ode onvektion benötigt einen stofflichen
Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie
 Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie DIE CHEMISCHE BINDUNG Ionische Bindung, Beispiel Natriumchlorid Trifft
Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie DIE CHEMISCHE BINDUNG Ionische Bindung, Beispiel Natriumchlorid Trifft
Elektrostatik. Arbeit und potenzielle Energie
 Elektostatik. Ladungen Phänomenologie. Eigenschaften von Ladungen 3. Käfte zwischen Ladungen, quantitativ 4. Elektisches Feld 5. De Satz von Gauß 6. Potenzial und Potenzialdiffeenz i. Abeit im elektischen
Elektostatik. Ladungen Phänomenologie. Eigenschaften von Ladungen 3. Käfte zwischen Ladungen, quantitativ 4. Elektisches Feld 5. De Satz von Gauß 6. Potenzial und Potenzialdiffeenz i. Abeit im elektischen
Chemische Bindung. Wie halten Atome zusammen? Welche Atome können sich verbinden? Febr 02
 Chemische Bindung locker bleiben Wie halten Atome zusammen? positiv Welche Atome können sich verbinden? power keep smiling Chemische Bindung Die chemischen Reaktionen spielen sich zwischen den Hüllen der
Chemische Bindung locker bleiben Wie halten Atome zusammen? positiv Welche Atome können sich verbinden? power keep smiling Chemische Bindung Die chemischen Reaktionen spielen sich zwischen den Hüllen der
Zur Erinnerung. Winkelmaße: Radiant und Steradiant. Stichworte aus der 3. Vorlesung:
 Zu inneung Stichwote aus de 3. Volesung: inkelaße: Radiant und Steadiant die (gleichföige) Keisbewegung als beschleunigte Bewegung (Richtungsändeung von v) Dastellung de kineatischen Gößen duch die inheitsvektoen
Zu inneung Stichwote aus de 3. Volesung: inkelaße: Radiant und Steadiant die (gleichföige) Keisbewegung als beschleunigte Bewegung (Richtungsändeung von v) Dastellung de kineatischen Gößen duch die inheitsvektoen
Der elektrische Dipol Sind zwei unterschiedliche Ladungen in einem Abstand d angeordnet, dann liegt ein elektrischer Dipol vor.
 De elektische Dipol Sind zwei unteschiedliche Ladungen in einem Abstand d angeodnet, dann liegt ein elektische Dipol vo. +q d q Man definiet das Dipolmoment: p q d Das Diplomoment ist ein Vekto, de entlang
De elektische Dipol Sind zwei unteschiedliche Ladungen in einem Abstand d angeodnet, dann liegt ein elektische Dipol vo. +q d q Man definiet das Dipolmoment: p q d Das Diplomoment ist ein Vekto, de entlang
11.2 Die absolute Temperatur und die Kelvin-Skala
 11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
= n + + Thermodynamik von Elektrolytlösungen. Wdhlg: Chemisches Potential einer Teilchenart: Für Elektrolytlösungen gilt: wobei : und
 Elektrolyte Teil III Solvatation, elektrische Leitfähigkeit, starke und schwache Elektrolyte, Ionenstärke, Debye Hückeltheorie, Migration, Diffusion, Festelektrolyte Thermodynamik von Elektrolytlösungen
Elektrolyte Teil III Solvatation, elektrische Leitfähigkeit, starke und schwache Elektrolyte, Ionenstärke, Debye Hückeltheorie, Migration, Diffusion, Festelektrolyte Thermodynamik von Elektrolytlösungen
Inhalt der Vorlesung Experimentalphysik II
 xpeimentalphysik II (Kip SS 9) Inhalt e Volesung xpeimentalphysik II Teil : lektiitätslehe, lektoynamik. lektische Laung un elektische Fele. Kapaität 3. lektische Stom 4. Magnetostatik 5. lektoynamik 6.
xpeimentalphysik II (Kip SS 9) Inhalt e Volesung xpeimentalphysik II Teil : lektiitätslehe, lektoynamik. lektische Laung un elektische Fele. Kapaität 3. lektische Stom 4. Magnetostatik 5. lektoynamik 6.
b) Drehimpuls r r Für Massenpunkt auf Kreisbahn: L=r p Für Massenpunkt auf beliebiger Bahn im Raum:
 b) Dehimpuls De Bewegungszustand eines otieenden Köpes wid duch seinen Dehimpuls L beschieben. Analog zum Dehmoment nimmt de Dehimpuls mit dem Impuls p und dem Bahnadius zu. Fü Massenpunkt auf Keisbahn:
b) Dehimpuls De Bewegungszustand eines otieenden Köpes wid duch seinen Dehimpuls L beschieben. Analog zum Dehmoment nimmt de Dehimpuls mit dem Impuls p und dem Bahnadius zu. Fü Massenpunkt auf Keisbahn:
Kern- und Teilchenphysik. Einführung in die Teilchenphysik: Schwache Wechselwirkung - Paritätsverletzung - verschiedene Prozesse der schwachen WW
 Ken- und Teilchenphysik Einfühung in die Teilchenphysik: Schwache Wechselwikung - Paitätsveletzung - veschiedene Pozesse de schwachen WW Noethe Theoem: Wiedeholung: Noethe-Theoem Jede Symmetie impliziet
Ken- und Teilchenphysik Einfühung in die Teilchenphysik: Schwache Wechselwikung - Paitätsveletzung - veschiedene Pozesse de schwachen WW Noethe Theoem: Wiedeholung: Noethe-Theoem Jede Symmetie impliziet
Kapitel 4 Energie und Arbeit
 Kapitel 4 negie und Abeit Kaftfelde Wenn wi jedem unkt des Raums eindeutig einen Kaft-Vekto zuodnen können, ehalten wi ein Kaftfeld F ( ) Häufig tauchen in de hysik Zental-Kaftfelde auf : F( ) f ( ) ˆ
Kapitel 4 negie und Abeit Kaftfelde Wenn wi jedem unkt des Raums eindeutig einen Kaft-Vekto zuodnen können, ehalten wi ein Kaftfeld F ( ) Häufig tauchen in de hysik Zental-Kaftfelde auf : F( ) f ( ) ˆ
Einführung in die Physik I. Wärme 3
 Einfühung in die Physik I Wäme 3 O. von de Lühe und U. Landgaf Duckabeit Mechanische Abeit ΔW kann von einem Gas geleistet weden, wenn es sein olumen um Δ gegen einen Duck p ändet. Dies hängt von de At
Einfühung in die Physik I Wäme 3 O. von de Lühe und U. Landgaf Duckabeit Mechanische Abeit ΔW kann von einem Gas geleistet weden, wenn es sein olumen um Δ gegen einen Duck p ändet. Dies hängt von de At
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle
 2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
Allgemeines Gasgesetz. PV = K o T
 Allgemeines Gasgesetz Die Kombination der beiden Gesetze von Gay-Lussac mit dem Gesetz von Boyle-Mariotte gibt den Zusammenhang der drei Zustandsgrößen Druck, Volumen, und Temperatur eines idealen Gases,
Allgemeines Gasgesetz Die Kombination der beiden Gesetze von Gay-Lussac mit dem Gesetz von Boyle-Mariotte gibt den Zusammenhang der drei Zustandsgrößen Druck, Volumen, und Temperatur eines idealen Gases,
E4 - Physik kondensierter Materie Mitschrift zur Vorlesung von Prof. Bogdan Sepiol und Prof. Gero Vogl
 E4 - Physik kondensierter Materie Mitschrift zur Vorlesung von Prof. Bogdan Sepiol und Prof. Gero Vogl Markus Drapalik und Bernhard Reiter Version vom 14.03.2006 Einleitung Literatur: Kittel, Charles:...,
E4 - Physik kondensierter Materie Mitschrift zur Vorlesung von Prof. Bogdan Sepiol und Prof. Gero Vogl Markus Drapalik und Bernhard Reiter Version vom 14.03.2006 Einleitung Literatur: Kittel, Charles:...,
EP WS 2009/10 Dünnweber/Faessler
 6.Volesung 6. Volesung EP I) Mechanik. Kinematik. Dynamik 3. a) Abeit b) Enegie (Wiedeholung): Enegie- und Impulsehaltung c) Stöße 4. Stae Köpe a) Dehmoment b) Schwepunkt Vesuche: Hüpfende Stahlkugel Veküztes
6.Volesung 6. Volesung EP I) Mechanik. Kinematik. Dynamik 3. a) Abeit b) Enegie (Wiedeholung): Enegie- und Impulsehaltung c) Stöße 4. Stae Köpe a) Dehmoment b) Schwepunkt Vesuche: Hüpfende Stahlkugel Veküztes
Physik - Gravitation. 8.1 Weltbilder. Ptolemaios: Geozentrisches Weltbild (Modell mit Epizyklen) R. Girwidz 1. R. Girwidz 2
 Physik - avitation. iwidz 8. Weltbilde Ptolemaios: eozentisches Weltbild (odell mit pizyklen). iwidz 8. Weltbilde. iwidz 3 8. Weltbilde Histoisch: Die Bewegung de Planeten wa übe Jahhundete nicht zu ekläen
Physik - avitation. iwidz 8. Weltbilde Ptolemaios: eozentisches Weltbild (odell mit pizyklen). iwidz 8. Weltbilde. iwidz 3 8. Weltbilde Histoisch: Die Bewegung de Planeten wa übe Jahhundete nicht zu ekläen
3. Elektrostatik (Motivation) Nervenzelle
 3. Elektostatik (Motivation) Nevenzelle 18 Jh.: Neuone wie elektische Leite. ABER: Widestand des Axoplasmas seh hoch 2,5 10 8 Ω (vegleichba Holz) Weiteleitung duch Pozesse senkecht zu Zellmemban Zellmemban
3. Elektostatik (Motivation) Nevenzelle 18 Jh.: Neuone wie elektische Leite. ABER: Widestand des Axoplasmas seh hoch 2,5 10 8 Ω (vegleichba Holz) Weiteleitung duch Pozesse senkecht zu Zellmemban Zellmemban
Vorbereitungsunterlagen 4. Kleingruppe GEMB- Dielektrische Polarisation
 Vobeeitungsuntelagen 4. Kleinguppe GEMB- Dielektische Polaisation HINWEIS ZU DEN NACHFOLGENDEN LERNMATERIALIEN Nachfolgende Lenmateialien sind ausdücklich als institutsfemde Mateialien zu vestehen. Sämtliche
Vobeeitungsuntelagen 4. Kleinguppe GEMB- Dielektische Polaisation HINWEIS ZU DEN NACHFOLGENDEN LERNMATERIALIEN Nachfolgende Lenmateialien sind ausdücklich als institutsfemde Mateialien zu vestehen. Sämtliche
6.Vorlesung 6. Vorlesung EP b) Energie (Fortsetzung): Energie- und Impulserhaltung c) Stöße 4. Starre Körper a) Drehmoment b) Schwerpunkt Versuche:
 6. Volesung EP I) Mechanik. Kinematik. Dynamik 3. a) Abeit b) Enegie (Fotsetzung): Enegie- und Impulsehaltung c) Stöße 4. Stae Köpe a) Dehmoment b) Schwepunkt 6.Volesung Vesuche: Hüpfende Stahlkugel Veküztes
6. Volesung EP I) Mechanik. Kinematik. Dynamik 3. a) Abeit b) Enegie (Fotsetzung): Enegie- und Impulsehaltung c) Stöße 4. Stae Köpe a) Dehmoment b) Schwepunkt 6.Volesung Vesuche: Hüpfende Stahlkugel Veküztes
Grundpraktikum für Biologen 2016
 Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
CHEMIE KAPITEL 1 AUFBAU DER MATERIE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2014 / 2015
 CHEMIE KAPITEL 1 AUFBAU DER MATERIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2014 / 2015 Folie 2 Atombau und Elementarteilchen Folie 3 Atommasse und Stoffmenge Stoffmenge [mol]: 12,000
CHEMIE KAPITEL 1 AUFBAU DER MATERIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2014 / 2015 Folie 2 Atombau und Elementarteilchen Folie 3 Atommasse und Stoffmenge Stoffmenge [mol]: 12,000
Festkörper. Festkörper
 Festkörper Einteilung der Materie in drei Aggregatszustände: fest, flüssig, gasförmig Unterscheidung Festkörper behält seine Form Nachteil: Ungenaue Abgrenzung Beispiel: Ist Butter Festkörper oder Flüssigkeit
Festkörper Einteilung der Materie in drei Aggregatszustände: fest, flüssig, gasförmig Unterscheidung Festkörper behält seine Form Nachteil: Ungenaue Abgrenzung Beispiel: Ist Butter Festkörper oder Flüssigkeit
Zusammenfassung magnetische Kraft auf elektrische Ladung
 24b Magnetismus 1 Zusammenfassung magnetische Kaft auf elektische Ladung Kaftwikung am elektisch geladenen Isolato ist otsunabhängig Kaftwikung am Magneten ist otsabhängig Maximale Kaft an den Enden Magnete
24b Magnetismus 1 Zusammenfassung magnetische Kaft auf elektische Ladung Kaftwikung am elektisch geladenen Isolato ist otsunabhängig Kaftwikung am Magneten ist otsabhängig Maximale Kaft an den Enden Magnete
Der typische erwachsene Mensch probiert die Dinge nur 2-3 x aus und gibt dann entnervt oder frustriert auf!
 De typische ewachsene Mensch pobiet die Dinge nu -3 x aus und gibt dann entnevt ode fustiet auf! Haben Sie noch die Hatnäckigkeit eines Kleinkindes welches laufen lent? Wie viel Zeit haben Sie mit dem
De typische ewachsene Mensch pobiet die Dinge nu -3 x aus und gibt dann entnevt ode fustiet auf! Haben Sie noch die Hatnäckigkeit eines Kleinkindes welches laufen lent? Wie viel Zeit haben Sie mit dem
Grundlagen der Allgemeinen und Anorganischen Chemie. Atome
 Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 361 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 361 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
F63 Gitterenergie von festem Argon
 1 F63 Gitteenegie von festem Agon 1. Einleitung Die Sublimationsenthalpie von festem Agon kann aus de Dampfduckkuve bestimmt weden. Dazu vewendet man die Clausius-Clapeyon-Gleichung. Wenn außedem noch
1 F63 Gitteenegie von festem Agon 1. Einleitung Die Sublimationsenthalpie von festem Agon kann aus de Dampfduckkuve bestimmt weden. Dazu vewendet man die Clausius-Clapeyon-Gleichung. Wenn außedem noch
22. Chemische Bindungen
 .05.03. Chemische Bindungen Molekül: System aus zwei oder mehr Atomen Kleinste Einheit einer Substanz, die deren chemische Eigenschaften ausweist Quantenmechanisches Vielteilchensystem: Exakte explizite
.05.03. Chemische Bindungen Molekül: System aus zwei oder mehr Atomen Kleinste Einheit einer Substanz, die deren chemische Eigenschaften ausweist Quantenmechanisches Vielteilchensystem: Exakte explizite
Dynamik. 4.Vorlesung EP
 4.Volesung EP I) Mechanik. Kinematik.Dynamik a) Newtons Axiome (Begiffe Masse und Kaft) b) Fundamentale Käfte c) Schwekaft (Gavitation) d) Fedekaft e) Reibungskaft Vesuche: Raketenvesuche: Impulsehaltung
4.Volesung EP I) Mechanik. Kinematik.Dynamik a) Newtons Axiome (Begiffe Masse und Kaft) b) Fundamentale Käfte c) Schwekaft (Gavitation) d) Fedekaft e) Reibungskaft Vesuche: Raketenvesuche: Impulsehaltung
1.2.4 Das elektrostatische Potenzial, Spannung
 peimentalphsik II U Dotmund SS Shaukat Khan @ U - Dotmund. de Kapitel..4 Das elektostatische otenial Spannung Benötigte Abeit um eine Ladung im -Feld u bewegen W Kaft Weg F ds q ds Fü die Ladung q im Feld
peimentalphsik II U Dotmund SS Shaukat Khan @ U - Dotmund. de Kapitel..4 Das elektostatische otenial Spannung Benötigte Abeit um eine Ladung im -Feld u bewegen W Kaft Weg F ds q ds Fü die Ladung q im Feld
Kapitel 13. Das Wasserstoff-Atom Energiewerte des Wasserstoff-Atoms durch Kastenpotential-Näherung
 Kapitel 13 Das Wassestoff-Atom 13.1 negiewete des Wassestoff-Atoms duch Kastenpotential-Näheung Das gobe Atommodell des im Potentialtopf eingespeten Atoms vemag in qualitative Weise das Aufteten von Linienspekten
Kapitel 13 Das Wassestoff-Atom 13.1 negiewete des Wassestoff-Atoms duch Kastenpotential-Näheung Das gobe Atommodell des im Potentialtopf eingespeten Atoms vemag in qualitative Weise das Aufteten von Linienspekten
Atomaufbau. Elektronen e (-) Atomhülle
 Atomaufbau Institut für Elementarteilchen Nukleonen Protonen p (+) Neutronen n (o) Elektronen e (-) Atomkern Atomhülle Atom WIBA-NET 2005 Prof. Setzer 1 Elementarteilchen Institut für Name Symbol Masse
Atomaufbau Institut für Elementarteilchen Nukleonen Protonen p (+) Neutronen n (o) Elektronen e (-) Atomkern Atomhülle Atom WIBA-NET 2005 Prof. Setzer 1 Elementarteilchen Institut für Name Symbol Masse
Kinetische Energie der Moleküle / Aggregatzustand
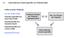 2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kräfte zwischen Molekülen - Van-der-Waals-Kräfte Orientierungskräfte bzw. Dipol-Dipol-Kräfte Induktionskräfte bzw. induzierte Dipole Dispersionskräfte
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kräfte zwischen Molekülen - Van-der-Waals-Kräfte Orientierungskräfte bzw. Dipol-Dipol-Kräfte Induktionskräfte bzw. induzierte Dipole Dispersionskräfte
Kerne und Teilchen. Kernkraft. Moderne Experimentalphysik III Vorlesung 16.
 Kerne und Teilchen Moderne Experimentalphysik III Vorlesung 16 MICHAEL FEINDT & THOMAS KUH INSTITUT FÜ EXPEIMENTELLE KENPHYSIK Kernkraft KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum
Kerne und Teilchen Moderne Experimentalphysik III Vorlesung 16 MICHAEL FEINDT & THOMAS KUH INSTITUT FÜ EXPEIMENTELLE KENPHYSIK Kernkraft KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum
3.5 Potential an der Zellmembran eines Neurons
 VAK 5.04.900, WS03/04 J.L. Vehey, (CvO Univesität Oldenbug ) 3.5 Potential an de Zellmemban eines Neuons Goldmann Gleichung fü mehee Ionen allgemein E R T F ln n k 1 n k 1 z z k k P k P k m [ X ] + z P[
VAK 5.04.900, WS03/04 J.L. Vehey, (CvO Univesität Oldenbug ) 3.5 Potential an de Zellmemban eines Neuons Goldmann Gleichung fü mehee Ionen allgemein E R T F ln n k 1 n k 1 z z k k P k P k m [ X ] + z P[
Kap. 0 Mathematische Grundlagen
 Kap. 0 Mathematische Gundlagen 1. Vektoen 1. Vektoopeationen (Skala- und Vektopodukt) 2. Diffeentialopeatoen (Nabla- und Laplace-Opeato) 2. Tigonometische Beziehungen 3. Komplexe Zahlen und komplexe Zahlenebene
Kap. 0 Mathematische Gundlagen 1. Vektoen 1. Vektoopeationen (Skala- und Vektopodukt) 2. Diffeentialopeatoen (Nabla- und Laplace-Opeato) 2. Tigonometische Beziehungen 3. Komplexe Zahlen und komplexe Zahlenebene
Einführung in die Physik I. Mechanik deformierbarer Körper 1
 Einfühung in die Physik I Mechanik defomiebae Köe O. von de Lühe und U. Landgaf Defomationen Defomationen, die das Volumen änden Dehnung Stauchung Defomationen, die das Volumen nicht änden Scheung Dillung
Einfühung in die Physik I Mechanik defomiebae Köe O. von de Lühe und U. Landgaf Defomationen Defomationen, die das Volumen änden Dehnung Stauchung Defomationen, die das Volumen nicht änden Scheung Dillung
Skript zur Vorlesung
 Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
