Medizinische Biophysik
|
|
|
- Leonard Voss
- vor 5 Jahren
- Abrufe
Transkript
1 4. Flüssiger Aggregatzustand Medizinische Biophysik a) Makroskopische Beschreibung b) Mikroskopische Beschreibung c) Oberflächenspannung Struktur der Materie Aggregatzustände: Gase, Flüssigkeiten, feste Körper d) Wasser und seine günstige 5. Fester Aggregatzustand - Kristalle a) Makroskopische Beschreibung b) Mikroskopische Beschreibung c) Kristalltypen d) Apatit e) Gitterfehler 2. Vorlesung f) Elektronenstruktur (Bändermodell) 6. Fester Aggregatzustand - amorphe Stoffe b) Mikroskopische Beschreibung: 4. Flüssiger Aggregatzustand Eigenvolumen aber keine Eigenform Isotrop Viskosität (s. später bei Transportprozessen) flüssig Keine Eigenform: Nach Deformieren bleibt so, es gibt keine rückstellende Scherkräfte. b) Mikroskopische Beschreibung: Dynamische Nahordnung Mittelstarke Bewegungen Wasser fest Eigenform: Nach Deformieren stellt sich zurück, da es rückstellende Scherkräfte gibt. 1 H-Brücken Isotropie 2 c) Oberflächenspannung Anziehende Wechselwirkungen zwischen den Molekülen Oberflächenspannung, oder spezifische Oberflächenenergie (): Stoff (J/m 2 )* E A Zur Flächenvergrößerung von A nötige Energie J 2 m N m Oberflächenvergrößerung Wasser Wasser 0,073 Blut 0,06 Speichel 0,05 Alkohol 0,023 Quecksilber 0,484 * In Bezug auf Luft, 20 C 3 4 1
2 Die hohe Oberflächenspannung des Wassers kann Probleme verursachen! Neonatales Atemnotsyndrom RDS=respiratory distress syndrome d) Wasser und seine günstige : hohe spezifische Wärmekapazität, Schmelzwärme und Verdampfungswärme (s. später) hohe Oberflächenspannung gutes Lösungsmittel für viele Stoffe Wassermolekül H-Brücke Weitere Erscheinungen, wobei die Oberflächenspannung eine Rolle spielt: - + Dipol Benetzung Kapillareffekt 5 6 feste Stoffe Kristalle (Festkörper) amorphe Stoffe Mikrokristalline Stoffe 5. Fester Aggregatzustand - Kristalle Eigenvolumen, Eigenform Einkristalle: oft anisotrop; Polykristalle: isotrop z. B. Tantal (Metall) ein Korn Unter dem Mikroskop mehrere Körner Nanokristalline Stoffe Einkristall z. B. Al 2 O 3 Polykristall Polykristall Einkristall (besteht aus mehreren Kristallen) 7 oft anisotrop oft isotrop 8 2
3 b) Mikroskopische Beschreibung: Fernordnung Periodizität Kristallgitter Schwache Bewegungen (Schwingungen) c) Kristalltypen: Atomkristall (kovalente Bindung) Ionenkristall (Ionenbindung) Diamant Salz Metallkristall (Metallbindung) Molekülkristall (sekundäre Bindung) Gold Eis Zum Beispiel: kubisch hexagonal Bindungsenergie (E 0 ), wie Schmelzpunkt, Schmelzwärme, Steifigkeit, Wärmeausdehnungskoeffizient, 9 10 d) Apatit Ca 10 (PO 4 ) 6 (X) 2 Ca 5 (PO 4 ) 3 X X = OH : Hydroxiapatit F : Fluorapatit ein hexagonales Ionenkristall anorganische Substanz der harten Gewebe (Knochen, Dentin, Zahnschmelz) etwa 2/3 des Knochengewebes e) Gitterfehler: Punktfehler Thermische Fehler Leerstelle (Vakanz, Schottky-Defekt) Interstitium (Zwischengitteratom) Frenkel-Defekt Fremdatome (chemische Fehler, Dotierung) Substitutionsatom Interstitielles Atom (Interstitium) Zahl der Schottky- Defekte (n S ): Aktivierungsenergie ( Bindungsenergie) n N e S S kt Zahl der besetzten Gitterstelle ( Zahl der Atome) Dentin, Knochen: nm x 6 nm große Kristalle Zahnschmelz: nm x 30 nm große Kristalle
4 Thermische Fehler in biologischen Makromolekülen: Zahl der aufgespalteten H- Brücken n N e S S kt Zahl der intakten H- Brücken Gitterfehler!! z. B. optische Al 2 O 3 + Cr 3+ + V2+ Fe 2+ +Ti 4+ +Fe 2+ Versetzungen (Dislokationen) Rubin siehe Rubinlaser NaI NaI + Tl 13 (unter Röntgenbestrahlung) siehe Szintillationskristall in der Nuklearmedizin Praktikum Nukleare Grundmessung 14 z. B. mechanische f) Elektronenstruktur (Bändermodell): z. B. chemische Ca 10 (PO 4 ) 6 (OH) 2 Hydroxiapatit Ca 10 (PO 4 ) 6 F 2 Fluorapatit Kleinere Löslichkeit in Säuren Leitungsband: Von oben gesehen das unterste Energieband, das nicht vollbesetzt ist. Valenzband: Von unten gesehen das oberste Energieband, das noch Elektronen enthält. z. B. elektrische siehe reine und dotierte Halbleiter
5 Elektrische der Festkörper Bei T = 0 K : Elektrischer Strom = kollektive Wanderung von elektrischen Ladungsträgern (Elektronen, Ionen, ) Dazu sind freie (quasifreie) Ladungsträger nötig. Z. B. Bewegung von Elektronen in einem Metallgitter: zufällige thermische Bewegung + kollektive Wanderung elektrische Kraft + U elektrische Spannung + abwechselnd: Beschleunigung, Abbremsen ständige Energieaufnahme, -abgabe Elektrischer Strom, elektrische Leitung ist nur dann möglich, wenn die Elektronen Ihren Energiezustand um eine geringe Energiemenge ständig ändern können. Breite der Bandlücke (verbotenen Zone): z.b. Al 2 O 3 : = 6,5 ev NaI: = 5 ev z.b. Si: = 1,1 ev Ge: = 0,7 ev 17 siehe die optischen später 18 Eigenhalbleiter (intrinsic Halbleiter) Bei T = 0 K : keine elektrische Leitung Dotierte Halbleiter Grundkristall z.b. Si n-halbleiter 14Si: 1s 2 2s 2 2p 6 3s 2 3p 2 p-halbleiter z. B. + P z. B. + B 15P: 1s 2 2s 2 2p 6 3s 2 3p 3 5B: 1s 2 2s 2 2p 1 Licht Photoleitung Bei T = 273 K : Annähernd Boltzmann-Verteilung! Elektronen (negative Ladungsträger) Zahl der freien Ladungsträger Defektelektronen, Löcher (virtuelle positive Ladungsträger) σ~ N~e ε 2kT elektrische Leitfähigkeit 19 Elektronenleitung (n-leitung) Löcherleitung (p-leitung) 20 5
6 6. Fester Aggregatzustand - amorphe Stoffe Eigenvolumen aber keine Eigenform Isotrop sehr hohe Viskosität Z.B. Glas, Harz, Wachs, Bitumen,... Hausaufgaben: Aufgabensammlung 1.43, 44, 47, 49, 50, 52 b) Mikroskopische Beschreibung: Nahordnung Schwache Bewegungen = gefrorene unterkühlte Flüssigkeiten, Gläser! Quartz Glas
Medizinische Biophysik
 2. Gasförmiger Aggregatzustand Medizinische Biophysik c) Kinetische Deutung der Temperatur: d) Maxwell-Boltzmann-Verteilung e) Barometrische Höhenformel (Gas im Gravitationsfeld) f) Boltzmann-Verteilung
2. Gasförmiger Aggregatzustand Medizinische Biophysik c) Kinetische Deutung der Temperatur: d) Maxwell-Boltzmann-Verteilung e) Barometrische Höhenformel (Gas im Gravitationsfeld) f) Boltzmann-Verteilung
Medizinische Biophysik
 2. Gasförmiger Aggregatzustand a) Makroskopische Beschreibung b) Mikroskopische Beschreibung Medizinische Biophysik c) Kinetische Deutung der Temperatur d) Maxwell-Boltzmann-Verteilung e) Barometrische
2. Gasförmiger Aggregatzustand a) Makroskopische Beschreibung b) Mikroskopische Beschreibung Medizinische Biophysik c) Kinetische Deutung der Temperatur d) Maxwell-Boltzmann-Verteilung e) Barometrische
Biophysik für Pharmazeuten I Struktur der Materie Tölgyesi Ferenc
 Biophysik für Pharmazeuten I. 014. 09.. Struktur der Materie Tölgyesi Ferenc Atomarer Aufbau der Materie o Demokritos 5.Jht v.chr. o Daltonsches Gesetz 180 o Moderne Mikroskope: Hausaufgaben: Neue Aufgabensammlung
Biophysik für Pharmazeuten I. 014. 09.. Struktur der Materie Tölgyesi Ferenc Atomarer Aufbau der Materie o Demokritos 5.Jht v.chr. o Daltonsches Gesetz 180 o Moderne Mikroskope: Hausaufgaben: Neue Aufgabensammlung
Flüssigkeiten. Viskosität (h) v h. A h. víz. (Fluidität~ 1/h) [h] = Pa s. Newtonsches Reibungsgesetz: Dynamische Nahordnung.
![Flüssigkeiten. Viskosität (h) v h. A h. víz. (Fluidität~ 1/h) [h] = Pa s. Newtonsches Reibungsgesetz: Dynamische Nahordnung. Flüssigkeiten. Viskosität (h) v h. A h. víz. (Fluidität~ 1/h) [h] = Pa s. Newtonsches Reibungsgesetz: Dynamische Nahordnung.](/thumbs/66/56374829.jpg) Flüssigkeiten flüssig Keine Eigenform (nach Deformieren bleibt so, es gibt keine rückstellende cherkräfte) fest Eigenform (nach Deformieren stellt sich zurück, da es rückstellende cherkräftegibt ) Physikalische
Flüssigkeiten flüssig Keine Eigenform (nach Deformieren bleibt so, es gibt keine rückstellende cherkräfte) fest Eigenform (nach Deformieren stellt sich zurück, da es rückstellende cherkräftegibt ) Physikalische
Biophysik für Pharmazeuten I.
 Biohysik für Pharmazeuten I. Allgemeine Prinziien Wechselwirkungen Bewegungen abstoßend anziehend Ekin = 1 mv 015/16 Vorlesung 3 E ot E Z.B. elektrisch r Struktur der Materie Unordnung + E kin q1 q = k
Biohysik für Pharmazeuten I. Allgemeine Prinziien Wechselwirkungen Bewegungen abstoßend anziehend Ekin = 1 mv 015/16 Vorlesung 3 E ot E Z.B. elektrisch r Struktur der Materie Unordnung + E kin q1 q = k
Grenzflächenphänomene. Physikalische Grundlagen der zahnärztlichen Materialkunde 3. Struktur der Materie. J m. N m. 1. Oberflächenspannung
 Grenzflächenphänomene 1. Oberflächenspannung Physikalische Grundlagen der zahnärztlichen Materialkunde 3. Struktur der Materie Grenzflächenphänomene Phase/Phasendiagramm/Phasenübergang Schwerpunkte: Oberflächenspannung
Grenzflächenphänomene 1. Oberflächenspannung Physikalische Grundlagen der zahnärztlichen Materialkunde 3. Struktur der Materie Grenzflächenphänomene Phase/Phasendiagramm/Phasenübergang Schwerpunkte: Oberflächenspannung
Hier: Beschränkung auf die elektrische Eigenschaften
 IV. Festkörperphysik Hier: Beschränkung auf die elektrische Eigenschaften 3 Aggregatzustände: fest, flüssig, gasförmig: Wechselspiel Anziehungskräfte der Teilchen gegen die thermische Energie kt. Zustand
IV. Festkörperphysik Hier: Beschränkung auf die elektrische Eigenschaften 3 Aggregatzustände: fest, flüssig, gasförmig: Wechselspiel Anziehungskräfte der Teilchen gegen die thermische Energie kt. Zustand
Festkörper. Festkörper
 Festkörper Einteilung der Materie in drei Aggregatszustände: fest, flüssig, gasförmig Unterscheidung Festkörper behält seine Form Nachteil: Ungenaue Abgrenzung Beispiel: Ist Butter Festkörper oder Flüssigkeit
Festkörper Einteilung der Materie in drei Aggregatszustände: fest, flüssig, gasförmig Unterscheidung Festkörper behält seine Form Nachteil: Ungenaue Abgrenzung Beispiel: Ist Butter Festkörper oder Flüssigkeit
Grundlagen der Allgemeinen und Anorganischen Chemie. Atome. Chemische Reaktionen. Verbindungen
 Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 284 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 284 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
11. Elektronen im Festkörper
 11. Elektronen im Festkörper 11.1 Elektrische Leitung in Festkörpern 11.2 Freies Elektronengas im Sommerfeld- Modell 11.3 Bändermodell des Festkörpers 11.4 Metalle, Isolatoren und Halbleiter WS 2013/14
11. Elektronen im Festkörper 11.1 Elektrische Leitung in Festkörpern 11.2 Freies Elektronengas im Sommerfeld- Modell 11.3 Bändermodell des Festkörpers 11.4 Metalle, Isolatoren und Halbleiter WS 2013/14
11. Elektronen im Festkörper
 11. Elektronen im Festkörper 11.1 Elektrische Leitung in Festkörpern 11.2 Freies Elektronengas im Sommerfeld- Modell 11.3 Bändermodell des Festkörpers 11.4 Metalle, Isolatoren und Halbleiter 1 11.4 Metalle,
11. Elektronen im Festkörper 11.1 Elektrische Leitung in Festkörpern 11.2 Freies Elektronengas im Sommerfeld- Modell 11.3 Bändermodell des Festkörpers 11.4 Metalle, Isolatoren und Halbleiter 1 11.4 Metalle,
2.4 Metallische Bindung und Metallkristalle. Unterteilung in Metalle, Halbmetalle, Nicht metalle. Li Be B C N O F. Na Mg Al Si P S Cl
 2.4 Metallische Bindung und Metallkristalle Li Be B C N O F Na Mg Al Si P S Cl K Ca Ga Ge As Se Br Rb Sr In Sn Sb Te I Cs Ba Tl Pb Bi Po At Unterteilung in Metalle, Halbmetalle, Nicht metalle Metalle etwa
2.4 Metallische Bindung und Metallkristalle Li Be B C N O F Na Mg Al Si P S Cl K Ca Ga Ge As Se Br Rb Sr In Sn Sb Te I Cs Ba Tl Pb Bi Po At Unterteilung in Metalle, Halbmetalle, Nicht metalle Metalle etwa
Spezifischer Widerstand fester Körper. Leiter Halbleiter Isolatoren. Kupferoxid
 R. Brinkmann http://brinkmann-du.de Seite 1 26.11.2013 Halbleiter Widerstandsbestimmung durch Strom - Spannungsmessung Versuch: Widerstandsbestimmung durch Strom und Spannungsmessung. 1. Leiter : Wendel
R. Brinkmann http://brinkmann-du.de Seite 1 26.11.2013 Halbleiter Widerstandsbestimmung durch Strom - Spannungsmessung Versuch: Widerstandsbestimmung durch Strom und Spannungsmessung. 1. Leiter : Wendel
Anorganische Chemie III
 Seminar zu Vorlesung Anorganische Chemie III Wintersemester 2013/14 Christoph Wölper Universität Duisburg-Essen # Elektronengas # Bändermodell Bindungsmodelle Metallbindung > Bindungsmodelle Elektronengas
Seminar zu Vorlesung Anorganische Chemie III Wintersemester 2013/14 Christoph Wölper Universität Duisburg-Essen # Elektronengas # Bändermodell Bindungsmodelle Metallbindung > Bindungsmodelle Elektronengas
Anorganische Chemie III - Festkörperchemie
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Festkörperchemie
Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Festkörperchemie
Werkstoffe der Elektrotechnik im Studiengang Elektrotechnik
 Werkstoffe der Elektrotechnik im Studiengang Elektrotechnik - Festkörper - Prof. Dr. Ulrich Hahn WS 2008/2009 Grundtypen Gläser, amorphe Festkörper Nahordnung der Teilchen 5 10 Atom- unterkühlte Flüssigkeiten
Werkstoffe der Elektrotechnik im Studiengang Elektrotechnik - Festkörper - Prof. Dr. Ulrich Hahn WS 2008/2009 Grundtypen Gläser, amorphe Festkörper Nahordnung der Teilchen 5 10 Atom- unterkühlte Flüssigkeiten
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Festkörper. Flüssigkristalle. Festkörper = Kristalle. Gitterstruktur. Elementarzelle
 Festkörper. Flüssigkristalle Festkörper = Kristalle och höhere Dichte periodische Struktur i große Bereiche, Ferordug stark begrezte Bewegug freie Schwigug ud Rotatio, aber fast keie Traslatio Volume-
Festkörper. Flüssigkristalle Festkörper = Kristalle och höhere Dichte periodische Struktur i große Bereiche, Ferordug stark begrezte Bewegug freie Schwigug ud Rotatio, aber fast keie Traslatio Volume-
FAKULTÄT FÜR ELEKTROTECHNIK UND INFORMATIONSTECHNIK
 Elektronik 1 - Bauelemente Vorlesung 5, 09.11.2017 Nils Pohl FAKULTÄT FÜR ELEKTROTECHNIK UND INFORMATIONSTECHNIK Lehrstuhl für Integrierte Systeme Organisatorisches Terminübersicht 02.11. 12:15 Vorlesung
Elektronik 1 - Bauelemente Vorlesung 5, 09.11.2017 Nils Pohl FAKULTÄT FÜR ELEKTROTECHNIK UND INFORMATIONSTECHNIK Lehrstuhl für Integrierte Systeme Organisatorisches Terminübersicht 02.11. 12:15 Vorlesung
3. Struktur des Festkörpers
 3. Struktur des Festkörpers 3.1 Kristalline und amorphe Strukturen Amorphe Struktur - Atombindung ist gerichtet - unregelmäßige Anordnung der Atome - keinen exakten Schmelzpunkt, sondern langsames Erweichen,
3. Struktur des Festkörpers 3.1 Kristalline und amorphe Strukturen Amorphe Struktur - Atombindung ist gerichtet - unregelmäßige Anordnung der Atome - keinen exakten Schmelzpunkt, sondern langsames Erweichen,
 2.2.2 Mechanismen der elektrischen Leitung Ohm sches Verhalten (U I bei T = const ) zeigen verschiedenste Materialien mit unterschiedlichen mikroskopischen Mechanismen der elektrischen Leitung: Metalle
2.2.2 Mechanismen der elektrischen Leitung Ohm sches Verhalten (U I bei T = const ) zeigen verschiedenste Materialien mit unterschiedlichen mikroskopischen Mechanismen der elektrischen Leitung: Metalle
Grundlagen der Rechnertechnologie Sommersemester Vorlesung Dr.-Ing. Wolfgang Heenes
 Grundlagen der Rechnertechnologie Sommersemester 2010 5. Vorlesung Dr.-Ing. Wolfgang Heenes 18. Mai 2010 TechnischeUniversitätDarmstadt Dr.-Ing. WolfgangHeenes 1 Inhalt 1. Aufbau der Materie 2. Energiebändermodell
Grundlagen der Rechnertechnologie Sommersemester 2010 5. Vorlesung Dr.-Ing. Wolfgang Heenes 18. Mai 2010 TechnischeUniversitätDarmstadt Dr.-Ing. WolfgangHeenes 1 Inhalt 1. Aufbau der Materie 2. Energiebändermodell
Freie Elektronen bilden ein Elektronengas. Feste positive Aluminiumionen. Abb. 1.1: Metallbindung: Feste Atomrümpfe und freie Valenzelektronen
 1 Grundlagen 1.1 Leiter Nichtleiter Halbleiter 1.1.1 Leiter Leiter sind generell Stoffe, die die Eigenschaft haben verschiedene arten weiterzuleiten. Im Folgenden steht dabei die Leitfähigkeit des elektrischen
1 Grundlagen 1.1 Leiter Nichtleiter Halbleiter 1.1.1 Leiter Leiter sind generell Stoffe, die die Eigenschaft haben verschiedene arten weiterzuleiten. Im Folgenden steht dabei die Leitfähigkeit des elektrischen
Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung / Salzstrukturen
 Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung / Salzstrukturen Der metallische Zustand, Dichtestpackung von Kugeln, hexagonal-, kubischdichte Packung, Oktaeder-, Tetraederlücken, kubisch-innenzentrierte
Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung / Salzstrukturen Der metallische Zustand, Dichtestpackung von Kugeln, hexagonal-, kubischdichte Packung, Oktaeder-, Tetraederlücken, kubisch-innenzentrierte
Klaus Stierstadt. Physik. der Materie VCH
 Klaus Stierstadt Physik der Materie VCH Inhalt Vorwort Tafelteil hinter Inhaltsverzeichnis (Seiten TI-T XVII) V Teil I Mikrophysik - Die Bausteine der Materie... l 1 Aufbau und Eigenschaften der Materie
Klaus Stierstadt Physik der Materie VCH Inhalt Vorwort Tafelteil hinter Inhaltsverzeichnis (Seiten TI-T XVII) V Teil I Mikrophysik - Die Bausteine der Materie... l 1 Aufbau und Eigenschaften der Materie
Typische Eigenschaften von Metallen
 Typische Eigenschaften von Metallen hohe elektrische Leitfähigkeit (nimmt mit steigender Temperatur ab) hohe Wärmeleitfähigkeit leichte Verformbarkeit metallischer Glanz Elektronengas-Modell eines Metalls
Typische Eigenschaften von Metallen hohe elektrische Leitfähigkeit (nimmt mit steigender Temperatur ab) hohe Wärmeleitfähigkeit leichte Verformbarkeit metallischer Glanz Elektronengas-Modell eines Metalls
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle
 2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
E 2 Temperaturabhängigkeit elektrischer Widerstände
 E 2 Temperaturabhängigkeit elektrischer Widerstände 1. Aufgaben 1. Für die Stoffe - Metall (Kupfer) - Legierung (Konstantan) - Halbleiter (Silizium, Galliumarsenid) ist die Temperaturabhängigkeit des elektr.
E 2 Temperaturabhängigkeit elektrischer Widerstände 1. Aufgaben 1. Für die Stoffe - Metall (Kupfer) - Legierung (Konstantan) - Halbleiter (Silizium, Galliumarsenid) ist die Temperaturabhängigkeit des elektr.
Die kovalente Bindung
 Die kovalente Bindung Atome, die keine abgeschlossene Elektronenschale besitzen, können über eine kovalente Bindung dieses Ziel erreichen. Beispiel: 4 H H + C H H C H H Die Wasserstoffatome erreichen damit
Die kovalente Bindung Atome, die keine abgeschlossene Elektronenschale besitzen, können über eine kovalente Bindung dieses Ziel erreichen. Beispiel: 4 H H + C H H C H H Die Wasserstoffatome erreichen damit
Atomverband mit festem Atomzahlverhältnis. Anzahl der Atome veränderlich? (bei festem Atomzahlverhältnis) Elektrisch Leitend?
 L3 1 Atomverband mit festem Atomzahlverhältnis. Ja Anzahl der Atome veränderlich? (bei festem Atomzahlverhältnis) Nein Ja Elektrisch Leitend? Nur in der Schmelze? Nein Ionenkristall Beliebig erweiterbar
L3 1 Atomverband mit festem Atomzahlverhältnis. Ja Anzahl der Atome veränderlich? (bei festem Atomzahlverhältnis) Nein Ja Elektrisch Leitend? Nur in der Schmelze? Nein Ionenkristall Beliebig erweiterbar
Physik 4: Skalen und Strukturen
 Physik 4: Skalen und Strukturen Kapitel : Festkörperphysik.1 Aggregatszustände. Kristallstrukturen.3 Chemische Bindung.4 Gitterschwingungen.5 Elektronen im Festkörper Phasendiagramm von CO Klassisches
Physik 4: Skalen und Strukturen Kapitel : Festkörperphysik.1 Aggregatszustände. Kristallstrukturen.3 Chemische Bindung.4 Gitterschwingungen.5 Elektronen im Festkörper Phasendiagramm von CO Klassisches
Detektoren in der Kern- und Teilchenphysik Szintillationsdetektoren Ionisationsdetektoren Halbleiterdetektoren
 Wechselwirkung geladener Teilchen in Materie Physik VI Sommersemester 2008 Detektoren in der Kern- und Teilchenphysik Szintillationsdetektoren Ionisationsdetektoren Halbleiterdetektoren Szintillationsdetektoren
Wechselwirkung geladener Teilchen in Materie Physik VI Sommersemester 2008 Detektoren in der Kern- und Teilchenphysik Szintillationsdetektoren Ionisationsdetektoren Halbleiterdetektoren Szintillationsdetektoren
Inhaltsverzeichnis. Vorwort. Wie man dieses Buch liest. Periodensystem der Elemente
 Inhaltsverzeichnis Vorwort Wie man dieses Buch liest Periodensystem der Elemente v vii xiv 1 Flüssigkristalle 1 1.1 Motivation und Phänomenologie.................. 1 1.2 Was ist ein Flüssigkristall?.....................
Inhaltsverzeichnis Vorwort Wie man dieses Buch liest Periodensystem der Elemente v vii xiv 1 Flüssigkristalle 1 1.1 Motivation und Phänomenologie.................. 1 1.2 Was ist ein Flüssigkristall?.....................
4. Fehleranordnung und Diffusion
 4. Fehleranordnung und Diffusion 33 4. Fehleranordnung und Diffusion Annahme: dichtes, porenfreies Oxid Materialtransport nur durch Festkörperdiffusion möglich Schematisch: Mögliche Teilreaktionen:. Übergang
4. Fehleranordnung und Diffusion 33 4. Fehleranordnung und Diffusion Annahme: dichtes, porenfreies Oxid Materialtransport nur durch Festkörperdiffusion möglich Schematisch: Mögliche Teilreaktionen:. Übergang
16 Festkörper Physik für E-Techniker. 16 Festkörper
 16 Festkörper 16.1 Arten der Festkörper 16.2 Kristalle 16.3 Bindungskräfte im Festkörper 16.3.1 Van der Waals-Bindung 16.3.2 Ionenbindung 16.3.3 Atombindung 16.3.4 Metallbindung 16.4 Vom Atom zum Festkörper
16 Festkörper 16.1 Arten der Festkörper 16.2 Kristalle 16.3 Bindungskräfte im Festkörper 16.3.1 Van der Waals-Bindung 16.3.2 Ionenbindung 16.3.3 Atombindung 16.3.4 Metallbindung 16.4 Vom Atom zum Festkörper
= e kt. 2. Halbleiter-Bauelemente. 2.1 Reine und dotierte Halbleiter 2.2 der pn-übergang 2.3 Die Diode 2.4 Schaltungen mit Dioden
 2. Halbleiter-Bauelemente 2.1 Reine und dotierte Halbleiter 2.2 der pn-übergang 2.3 Die Diode 2.4 Schaltungen mit Dioden Zu 2.1: Fermi-Energie Fermi-Energie E F : das am absoluten Nullpunkt oberste besetzte
2. Halbleiter-Bauelemente 2.1 Reine und dotierte Halbleiter 2.2 der pn-übergang 2.3 Die Diode 2.4 Schaltungen mit Dioden Zu 2.1: Fermi-Energie Fermi-Energie E F : das am absoluten Nullpunkt oberste besetzte
Spezifischer Widerstand fester Körper. Leiter Halbleiter Isolatoren. Kupferoxid
 R. Brinkmann http://brinkmann-du.de Seite 1 26.11.2013 Halbleiter Widerstandsbestimmung durch Strom - Spannungsmessung Versuch: Widerstandsbestimmung durch Strom und Spannungsmessung. 1. Leiter : Wendel
R. Brinkmann http://brinkmann-du.de Seite 1 26.11.2013 Halbleiter Widerstandsbestimmung durch Strom - Spannungsmessung Versuch: Widerstandsbestimmung durch Strom und Spannungsmessung. 1. Leiter : Wendel
Kinetische Energie der Moleküle / Aggregatzustand
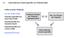 2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kräfte zwischen Molekülen - Van-der-Waals-Kräfte Orientierungskräfte bzw. Dipol-Dipol-Kräfte Induktionskräfte bzw. induzierte Dipole Dispersionskräfte
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kräfte zwischen Molekülen - Van-der-Waals-Kräfte Orientierungskräfte bzw. Dipol-Dipol-Kräfte Induktionskräfte bzw. induzierte Dipole Dispersionskräfte
Struktur von Festkörpern
 Struktur von Festkörpern Wir wollen uns zunächst mit der Struktur von Festkörpern, daß heißt mit der Geometrie in der sie vorliegen beschäftigen Kovalent gebundene Festkörper haben wir bereits in Form
Struktur von Festkörpern Wir wollen uns zunächst mit der Struktur von Festkörpern, daß heißt mit der Geometrie in der sie vorliegen beschäftigen Kovalent gebundene Festkörper haben wir bereits in Form
Norbert Koch. Polymer gegen Silizium: Wer wird in der Elektronik gewinnen?
 Polymer gegen Silizium: Wer wird in der Elektronik gewinnen? Norbert Koch Humboldt Universität zu Berlin, Institut für Physik & IRIS Adlershof Helmholtz Zentrum Berlin für Materialien und Energie GmbH
Polymer gegen Silizium: Wer wird in der Elektronik gewinnen? Norbert Koch Humboldt Universität zu Berlin, Institut für Physik & IRIS Adlershof Helmholtz Zentrum Berlin für Materialien und Energie GmbH
Elektrische und Thermische Leitfähigkeit von Metallen
 Elektrische und Thermische Leitfähigkeit von Metallen Virtueller Vortrag von Andreas Kautsch und Andreas Litschauer im Rahmen der VO Festkörperphysik Grundlagen Outline elektrische Leitfähigkeit Gründe
Elektrische und Thermische Leitfähigkeit von Metallen Virtueller Vortrag von Andreas Kautsch und Andreas Litschauer im Rahmen der VO Festkörperphysik Grundlagen Outline elektrische Leitfähigkeit Gründe
Dielektrizitätskonstante
 Dielektrizitätskonstante Spannung am geladenen Plattenkondensator sinkt, wenn nichtleitendes Dielektrikum eingeschoben wird Ladung bleibt konstant : Q = C 0 U 0 = C D U D Q + + + + + + + + + + + - - -
Dielektrizitätskonstante Spannung am geladenen Plattenkondensator sinkt, wenn nichtleitendes Dielektrikum eingeschoben wird Ladung bleibt konstant : Q = C 0 U 0 = C D U D Q + + + + + + + + + + + - - -
Universität Regensburg
 Universität Regensburg Fakultät für Chemie und Pharmazie Institut für Anorganische Chemie Prof. Dr. R. Winter 93040 Regensburg Musterlösungen Übung 7. 1. Geben Sie an, ob die folgenden Orbitalüberlappungen
Universität Regensburg Fakultät für Chemie und Pharmazie Institut für Anorganische Chemie Prof. Dr. R. Winter 93040 Regensburg Musterlösungen Übung 7. 1. Geben Sie an, ob die folgenden Orbitalüberlappungen
Halbleiterarten. Technische Universität Ilmenau Institut für Werkstofftechnik. Halbleiter. elektronische Halbleiter
 Halbleiterarten Halbleiter kristalline Halbleiter amorphe Halbleiter elektronische Halbleiter Ionenhalbleiter elektronische Halbleiter Ionenhalbleiter Element Halbleiter Verbindungshalbleiter Eigen Halbleiter
Halbleiterarten Halbleiter kristalline Halbleiter amorphe Halbleiter elektronische Halbleiter Ionenhalbleiter elektronische Halbleiter Ionenhalbleiter Element Halbleiter Verbindungshalbleiter Eigen Halbleiter
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Biologie Arbeitsblätter mit Lösungen - Biochemie
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Biologie Arbeitsblätter mit Lösungen - Biochemie Das komplette Material finden Sie hier: Download bei School-Scout.de B201 LÖSUNG:
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Biologie Arbeitsblätter mit Lösungen - Biochemie Das komplette Material finden Sie hier: Download bei School-Scout.de B201 LÖSUNG:
Thema heute: Chemische Bindungen - Ionenbindung
 Wiederholung der letzten Vorlesungsstunde: Chemische Bindungen, Doppelbindungsregel, VSEPR-Theorie Thema heute: Chemische Bindungen - Ionenbindung Vorlesung Allgemeine Chemie, Prof. Dr. Martin Köckerling
Wiederholung der letzten Vorlesungsstunde: Chemische Bindungen, Doppelbindungsregel, VSEPR-Theorie Thema heute: Chemische Bindungen - Ionenbindung Vorlesung Allgemeine Chemie, Prof. Dr. Martin Köckerling
Materie ist die Gesamtheit aller Stoffe: Energie bei chemischen Reaktionen:
 A.1.1 1 Stoffbegriff / Materie / Energie Materie ist die Gesamtheit aller Stoffe: Jeder Stoff füllt einen Raum V (Einheit: m³) aus Jeder Stoff besitzt eine Masse m (Einheit: kg) Dichte = Masse / Volumen
A.1.1 1 Stoffbegriff / Materie / Energie Materie ist die Gesamtheit aller Stoffe: Jeder Stoff füllt einen Raum V (Einheit: m³) aus Jeder Stoff besitzt eine Masse m (Einheit: kg) Dichte = Masse / Volumen
Konzepte der anorganischen und analytischen Chemie II II
 Konzepte der anorganischen und analytischen Chemie II II Marc H. Prosenc Inst. für Anorganische und Angewandte Chemie Tel: 42838-3102 prosenc@chemie.uni-hamburg.de Outline Einführung in die Chemie fester
Konzepte der anorganischen und analytischen Chemie II II Marc H. Prosenc Inst. für Anorganische und Angewandte Chemie Tel: 42838-3102 prosenc@chemie.uni-hamburg.de Outline Einführung in die Chemie fester
3.4. Leitungsmechanismen
 a) Metalle 3.4. Leitungsmechanismen - Metall besteht aus positiv geladenen Metallionen und frei beweglichen Leitungselektronen (freie Elektronengas), Bsp.: Cu 2+ + 2e - - elektrische Leitung durch freie
a) Metalle 3.4. Leitungsmechanismen - Metall besteht aus positiv geladenen Metallionen und frei beweglichen Leitungselektronen (freie Elektronengas), Bsp.: Cu 2+ + 2e - - elektrische Leitung durch freie
Medizinische Biophysik Struktur der Materie II. Aggregatzustände: feste Körper, Flüssigkristalle 5. Fester Aggregatzustand - amorphe Stoffe
 Medizinische Biphysik Struktur der Materie II. Aggregatzustände: feste Körper, Flüssigkristalle 5. Fester Aggregatzustand - amrphe Stffe a) Makrskpische Beschreibung: b) Mikrskpische Beschreibung: 6. Flüssigkristalle
Medizinische Biphysik Struktur der Materie II. Aggregatzustände: feste Körper, Flüssigkristalle 5. Fester Aggregatzustand - amrphe Stffe a) Makrskpische Beschreibung: b) Mikrskpische Beschreibung: 6. Flüssigkristalle
Atom-, Molekül- und Festkörperphysik
 Atom-, Molekül- und Festkörperphysik für LAK, SS 2013 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 10. Vorlesung, 27. 6. 2013 Halbleiter, Halbleiter-Bauelemente Diode, Solarzelle,
Atom-, Molekül- und Festkörperphysik für LAK, SS 2013 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 10. Vorlesung, 27. 6. 2013 Halbleiter, Halbleiter-Bauelemente Diode, Solarzelle,
Die chemische Bindung
 Die chemische Bindung Die Valenz-Bond Theorie Molekülorbitale Die Bänder Theorie der Festkörper bei einer ionischen Bindung bildet bildet sich ein Dipol aus ('Übertragung von Elektronen') Eine kovalente
Die chemische Bindung Die Valenz-Bond Theorie Molekülorbitale Die Bänder Theorie der Festkörper bei einer ionischen Bindung bildet bildet sich ein Dipol aus ('Übertragung von Elektronen') Eine kovalente
Ulrich Schwarz Experimentelle Sensorik Institut für Physik, TU Chemnitz. Sommersemester Physik der kondensierten Materie
 Physik der kondensierten Materie Kapitel 8 Elektronen im periodischen Potential Ulrich Schwarz Experimentelle Sensorik Institut für Physik, TU Chemnitz In Vertretung von Carsten Deibel Optik & Photonik
Physik der kondensierten Materie Kapitel 8 Elektronen im periodischen Potential Ulrich Schwarz Experimentelle Sensorik Institut für Physik, TU Chemnitz In Vertretung von Carsten Deibel Optik & Photonik
Halbleiter. Das Herz unserer multimedialen Welt. Bastian Inselmann - LK Physik
 Halbleiter Das Herz unserer multimedialen Welt Inhalt Bisherig Bekanntes Das Bändermodell Halbleiter und ihre Eigenschaften Dotierung Anwendungsbeispiel: Funktion der Diode Bisher Bekanntes: Leiter Isolatoren
Halbleiter Das Herz unserer multimedialen Welt Inhalt Bisherig Bekanntes Das Bändermodell Halbleiter und ihre Eigenschaften Dotierung Anwendungsbeispiel: Funktion der Diode Bisher Bekanntes: Leiter Isolatoren
Physikalische Chemie 1 Struktur und Materie Wintersemester 2015/16
 Vorlesung: Kontakt: Physikalische Chemie 1 Struktur und Materie Wintersemester 2015/16 5., 7., 12., 19., 21., 28. Oktober und 4., 11., 13., 18. November Hörsaal 10.01 Daran anschließend Physikalische Chemie
Vorlesung: Kontakt: Physikalische Chemie 1 Struktur und Materie Wintersemester 2015/16 5., 7., 12., 19., 21., 28. Oktober und 4., 11., 13., 18. November Hörsaal 10.01 Daran anschließend Physikalische Chemie
4 Thermodynamik mikroskopisch: kinetische Gastheorie makroskopisch: System:
 Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Kristallstruktur 1 Tetraederwinkel Die Millerschen Indizes Die hcp-struktur Bravais-Gitter 3
 In ha Itsverzeichn is Vorwort V 1 ALl Al.2 A1.3 Al.4 Al.5 Al.6 Al.7 Al.8 Kristallstruktur 1 Tetraederwinkel.............................................................. 1 Die Millerschen Indizes......................................................
In ha Itsverzeichn is Vorwort V 1 ALl Al.2 A1.3 Al.4 Al.5 Al.6 Al.7 Al.8 Kristallstruktur 1 Tetraederwinkel.............................................................. 1 Die Millerschen Indizes......................................................
1 Leitfähigkeit in Festkörpern
 1 Leitfähigkeit in Festkörpern Elektrische Leitfähigkeit ist eine physikalische Größe, die die Fähigkeit eines Stoffes angibt, elektrischen Strom zu leiten. Bändermodell Die Leitfähigkeit verschiedener
1 Leitfähigkeit in Festkörpern Elektrische Leitfähigkeit ist eine physikalische Größe, die die Fähigkeit eines Stoffes angibt, elektrischen Strom zu leiten. Bändermodell Die Leitfähigkeit verschiedener
Grundpraktikum für Biologen 2016
 Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
Zur Erinnerung. Trägheitsmomente, Kreisel, etc. Stichworte aus der 11. Vorlesung:
 Zur Erinnerung Stichworte aus der 11. Vorlesung: Zusammenfassung: Trägheitsmomente, Kreisel, etc. allgemeine Darstellung des Drehimpulses für Drehung von beliebig geformtem Körper um beliebige Drehachse
Zur Erinnerung Stichworte aus der 11. Vorlesung: Zusammenfassung: Trägheitsmomente, Kreisel, etc. allgemeine Darstellung des Drehimpulses für Drehung von beliebig geformtem Körper um beliebige Drehachse
Opto-elektronische. Materialeigenschaften VL # 4
 Opto-elektronische Materialeigenschaften VL # 4 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und Bayerisches Zentrum für Angewandte
Opto-elektronische Materialeigenschaften VL # 4 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und Bayerisches Zentrum für Angewandte
Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde. Sommersemester 2007
 Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde Sommersemester 2007 VL #35 am 28.06.2007 Vladimir Dyakonov Leitungsmechanismen Ladungstransport in Festkörpern Ladungsträger
Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde Sommersemester 2007 VL #35 am 28.06.2007 Vladimir Dyakonov Leitungsmechanismen Ladungstransport in Festkörpern Ladungsträger
sind Stoffe, die je nach Verwendungszweck aus Rohstoffen durch Bearbeitung und Veredelung gewonnen werden. Einteilung der Werkstoffe
 Werkstoffe sind Arbeitsmittel rein stofflicher Natur, die in Produktionsprozessen weiter verarbeitet werden und entweder in die jeweiligen Endprodukte eingehen oder während deren Herstellung verbraucht
Werkstoffe sind Arbeitsmittel rein stofflicher Natur, die in Produktionsprozessen weiter verarbeitet werden und entweder in die jeweiligen Endprodukte eingehen oder während deren Herstellung verbraucht
1.1. Baustoffarten Atombau und Periodensystem
 1. Allgemeine Grundlagen 1.1. Baustoffarten 1.2. Atombau und Periodensystem 1.3. Chemische Bindungen Betrachtungsebene der Baustoffe Submikroskopischer Bereich Atome (kleinste Bausteine der Stoffe) Chemische
1. Allgemeine Grundlagen 1.1. Baustoffarten 1.2. Atombau und Periodensystem 1.3. Chemische Bindungen Betrachtungsebene der Baustoffe Submikroskopischer Bereich Atome (kleinste Bausteine der Stoffe) Chemische
Vom Atom zum Molekül
 Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
3. Struktur des Festkörpers
 3. Struktur des Festkörpers 3.1 Kristalline und amorphe Strukturen Amorphe Struktur - Atombindung ist gerichtet - unregelmäßige Anordnung der Atome - keinen exakten Schmelzpunkt, sondern langsames Erweichen,
3. Struktur des Festkörpers 3.1 Kristalline und amorphe Strukturen Amorphe Struktur - Atombindung ist gerichtet - unregelmäßige Anordnung der Atome - keinen exakten Schmelzpunkt, sondern langsames Erweichen,
Strahlungsdetektoren. Strahlungsdetektoren. Szintillationsdetektor. Strahlungsdetektoren. Tl-haltiges NaI. ionisierende Strahlung << >> Materie
 Strahlungsdetektoren Strahlungsdetektoren ionisierende Strahlung > Materie elektromagnetische Wechselwirkung Wechselwirkung nicht elektromagnetische Wechselwirkung Die Basis aller Messungen (auch Beobachtungen)
Strahlungsdetektoren Strahlungsdetektoren ionisierende Strahlung > Materie elektromagnetische Wechselwirkung Wechselwirkung nicht elektromagnetische Wechselwirkung Die Basis aller Messungen (auch Beobachtungen)
Strahlungsdetektoren. Strahlungsdetektoren. Szintillationsdetektor. Szintillationsdetektor. Tl-haltiges NaI. ionisierende Strahlung << >> Materie
 Strahlungsdetektoren ionisierende Strahlung > Materie elektromagnetische Wechselwirkung Wechselwirkung nicht elektromagnetische Wechselwirkung Strahlungsdetektoren Nachweis über elektromagnetische
Strahlungsdetektoren ionisierende Strahlung > Materie elektromagnetische Wechselwirkung Wechselwirkung nicht elektromagnetische Wechselwirkung Strahlungsdetektoren Nachweis über elektromagnetische
INSTITUT FÜR ANGEWANDTE PHYSIK Physikalisches Praktikum für Studierende der Ingenieurswissenschaften Universität Hamburg, Jungiusstraße 11
 INSTITUT FÜR ANGEWANDTE PHYSIK Physikalisches Praktikum für Studierende der Ingenieurswissenschaften Universität Hamburg, Jungiusstraße 11 Halleffekt 1 Ziel Durch Messungen des Stroms und der Hallspannung
INSTITUT FÜR ANGEWANDTE PHYSIK Physikalisches Praktikum für Studierende der Ingenieurswissenschaften Universität Hamburg, Jungiusstraße 11 Halleffekt 1 Ziel Durch Messungen des Stroms und der Hallspannung
Kondensationswärme. Verdampfungswärme. Resublimationswärme. Sublimationswärme. Erstarrungswärme. Schmelzwärme. Energie (Enthalpie) Energie (Enthalpie)
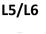 A. Soi 2017 18 81 Energie (Enthalpie) Energie (Enthalpie) Gasförmig Flüssig Schmelzwärme (Schmelzenthalpie) Verdampfungswärme (Schmelzenthalpie) Sublimationswärme (Sublimationsenthalpie) Fest Gasförmig
A. Soi 2017 18 81 Energie (Enthalpie) Energie (Enthalpie) Gasförmig Flüssig Schmelzwärme (Schmelzenthalpie) Verdampfungswärme (Schmelzenthalpie) Sublimationswärme (Sublimationsenthalpie) Fest Gasförmig
Festkörperphysik. Aufgaben und Lösun
 Festkörperphysik. Aufgaben und Lösun von Prof. Dr. Rudolf Gross Dr. Achim Marx Priv.-Doz. Dr. Dietrich Einzel Oldenbourg Verlag München Inhaltsverzeichnis Vorwort V 1 Kristallstruktur 1 ALI Tetraederwinkel
Festkörperphysik. Aufgaben und Lösun von Prof. Dr. Rudolf Gross Dr. Achim Marx Priv.-Doz. Dr. Dietrich Einzel Oldenbourg Verlag München Inhaltsverzeichnis Vorwort V 1 Kristallstruktur 1 ALI Tetraederwinkel
Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie
 Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie DIE CHEMISCHE BINDUNG Ionische Bindung, Beispiel Natriumchlorid Trifft
Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie DIE CHEMISCHE BINDUNG Ionische Bindung, Beispiel Natriumchlorid Trifft
ELEMENTARSTOFFE, VERBINDUNGEN und chemische Formeln LÖSUNG. Hinweis: In den Salzen kommen die Metallatome stets als einatomige Kationen vor.
 Hinweis: In den Salzen kommen die Metallatome stets als einatomige Kationen vor. Aufgabe 1: a) Tragen Sie die folgenden chemischen Formeln in die richtige Spalte der Tabelle ein. Beachten Sie, dass mehrere
Hinweis: In den Salzen kommen die Metallatome stets als einatomige Kationen vor. Aufgabe 1: a) Tragen Sie die folgenden chemischen Formeln in die richtige Spalte der Tabelle ein. Beachten Sie, dass mehrere
Versuch 2. Physik für (Zahn-)Mediziner. c Claus Pegel 13. November 2007
 Versuch 2 Physik für (Zahn-)Mediziner c Claus Pegel 13. November 2007 1 Wärmemenge 1 Wärme oder Wärmemenge ist eine makroskopische Größe zur Beschreibung der ungeordneten Bewegung von Molekülen ( Schwingungen,
Versuch 2 Physik für (Zahn-)Mediziner c Claus Pegel 13. November 2007 1 Wärmemenge 1 Wärme oder Wärmemenge ist eine makroskopische Größe zur Beschreibung der ungeordneten Bewegung von Molekülen ( Schwingungen,
Chemische Bindungen Atombindung
 Atombindung Das Lewis Modell der kovalenten Bindung Bildung von Molekülen (Einfachbindungen) Aus jeweils einem ungepaarten Elektron eines Atoms bildet sich ein gemeinsames Elektronenpaar als Molekülorbital
Atombindung Das Lewis Modell der kovalenten Bindung Bildung von Molekülen (Einfachbindungen) Aus jeweils einem ungepaarten Elektron eines Atoms bildet sich ein gemeinsames Elektronenpaar als Molekülorbital
Physikalische Chemie 1 Struktur und Materie Wintersemester 2016/17
 Physikalische Chemie 1 Struktur und Materie Wintersemester 2016/17 Vorlesung: Hörsaal 10.01 Daran anschließend Physikalische Chemie 2 (Prof. Falcaro, TU): Materie im elektr./magn. Feld, Wechselwirkungen,
Physikalische Chemie 1 Struktur und Materie Wintersemester 2016/17 Vorlesung: Hörsaal 10.01 Daran anschließend Physikalische Chemie 2 (Prof. Falcaro, TU): Materie im elektr./magn. Feld, Wechselwirkungen,
Lage des Ferminiveaus beim intrinsischen HL
 9.1 Lage des Ferminiveaus beim intrinsischen HL n W L W F = NL exp exp kt B kt B W V W F = p = NV exp exp kt B kt B Auflösen nach der exp-funktion: Mit Auflösen nach W F : 3 * N 2 V m h = * NL me 2W F
9.1 Lage des Ferminiveaus beim intrinsischen HL n W L W F = NL exp exp kt B kt B W V W F = p = NV exp exp kt B kt B Auflösen nach der exp-funktion: Mit Auflösen nach W F : 3 * N 2 V m h = * NL me 2W F
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Welche Zustände sind denn eigentlich besetzt?
 elche Zustände sind denn eigentlich besetzt? elche Zustände sind denn eigentlich besetzt? ( 0 ) 12 9 -im Prinzip sollte das Ganze ähnlich wie beim Atom erfolgen 6 - Besetzung von unten nach oben 3 -...wie
elche Zustände sind denn eigentlich besetzt? elche Zustände sind denn eigentlich besetzt? ( 0 ) 12 9 -im Prinzip sollte das Ganze ähnlich wie beim Atom erfolgen 6 - Besetzung von unten nach oben 3 -...wie
Kristallchemie. Atome Ionen Moleküle Chemische Bindungen
 Zirkon Kristallchemie Atome Ionen Moleküle Chemische Bindungen Bohr sches Atommodell Kernteilchen: p: Proton n: Neutron Elektronenhülle: e - Elektron Nukleus: Massenzahl A = p + n, Ordnungszahl Z = p =
Zirkon Kristallchemie Atome Ionen Moleküle Chemische Bindungen Bohr sches Atommodell Kernteilchen: p: Proton n: Neutron Elektronenhülle: e - Elektron Nukleus: Massenzahl A = p + n, Ordnungszahl Z = p =
2. Struktur von Festkörpern
 . Struktur von Festkörpern Energie-Minimum wird erreicht, wenn jedes Atom möglichst dieselbe Umgebung hat Periodische Anordnung von Atomen. Periodische Anordnung erleichtert theoretische Beschreibung erheblich.
. Struktur von Festkörpern Energie-Minimum wird erreicht, wenn jedes Atom möglichst dieselbe Umgebung hat Periodische Anordnung von Atomen. Periodische Anordnung erleichtert theoretische Beschreibung erheblich.
Vorlesung Anorganische Chemie
 Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 4 Molekülstruktur Ausnahmen von der Oktettregel Hypervalente Verbindungen VSEPR Hybridisierung Molekülorbitale
Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 4 Molekülstruktur Ausnahmen von der Oktettregel Hypervalente Verbindungen VSEPR Hybridisierung Molekülorbitale
6/2 Halbleiter Ganz wichtige Bauteile
 Elektronik 6/2 Seite 1 6/2 Halbleiter Ganz wichtige Bauteile Erforderlicher Wissensstand der Schüler Begriffe: Widerstand, Temperatur, elektrisches Feld, Ionen, Isolator Lernziele der Unterrichtssequenz
Elektronik 6/2 Seite 1 6/2 Halbleiter Ganz wichtige Bauteile Erforderlicher Wissensstand der Schüler Begriffe: Widerstand, Temperatur, elektrisches Feld, Ionen, Isolator Lernziele der Unterrichtssequenz
Physik IV Einführung in die Atomistik und die Struktur der Materie
 Physik IV Einführung in die Atomistik und die Struktur der Materie Sommersemester 2011 Vorlesung 21 30.06.2011 Physik IV - Einführung in die Atomistik Vorlesung 21 Prof. Thorsten Kröll 30.06.2011 1 H 2
Physik IV Einführung in die Atomistik und die Struktur der Materie Sommersemester 2011 Vorlesung 21 30.06.2011 Physik IV - Einführung in die Atomistik Vorlesung 21 Prof. Thorsten Kröll 30.06.2011 1 H 2
4.2 Metallkristalle. 4.2.1 Bindungsverhältnisse
 4.2 Metallkristalle - 75 % aller Elemente sind Metalle - hohe thermische und elektrische Leitfähigkeit - metallischer Glanz - Duktilität (Zähigkeit, Verformungsvermögen): Fähigkeit eines Werkstoffs, sich
4.2 Metallkristalle - 75 % aller Elemente sind Metalle - hohe thermische und elektrische Leitfähigkeit - metallischer Glanz - Duktilität (Zähigkeit, Verformungsvermögen): Fähigkeit eines Werkstoffs, sich
EDUKTE PRODUKTE. Bei einer chemischen Reaktion wandeln sich Stoffe in neue Stoffe mit anderen Eigenschaften um. Symbolische Schreibweise: Reagiert zu
 L2 1 Chemische Reaktion, Energetik Bei einer chemischen Reaktion wandeln sich Stoffe in neue Stoffe mit anderen Eigenschaften um. Symbolische Schreibweise: Ausgangsstoff e EDUKTE Reagiert zu Endstoffe
L2 1 Chemische Reaktion, Energetik Bei einer chemischen Reaktion wandeln sich Stoffe in neue Stoffe mit anderen Eigenschaften um. Symbolische Schreibweise: Ausgangsstoff e EDUKTE Reagiert zu Endstoffe
Halbleiter, Dioden. wyrs, Halbleiter, 1
 Halbleiter, Dioden Halbleiter, 1 Inhaltsverzeichnis Aufbau & physikalische Eigenschaften von Halbleitern Veränderung der Eigenschaften mittels Dotierung Vorgänge am Übergang von dotierten Materialen Verhalten
Halbleiter, Dioden Halbleiter, 1 Inhaltsverzeichnis Aufbau & physikalische Eigenschaften von Halbleitern Veränderung der Eigenschaften mittels Dotierung Vorgänge am Übergang von dotierten Materialen Verhalten
Versuch 1.3 Hall-Effekt
 F-Praktikum: Versuch Hall-Effekt Seite 1/9 F-Praktikum Versuch 1.3 Hall-Effekt Diego Semmler, Nils Höres Inhaltsverzeichnis F-Praktikum...1 Motivation...2 Aufgabenstellung...2 Theorie...2 Das Bändermodell...2
F-Praktikum: Versuch Hall-Effekt Seite 1/9 F-Praktikum Versuch 1.3 Hall-Effekt Diego Semmler, Nils Höres Inhaltsverzeichnis F-Praktikum...1 Motivation...2 Aufgabenstellung...2 Theorie...2 Das Bändermodell...2
Learn4Med. Es gibt in der Chemie drei verschiedene Arten von Bindungen: Metallische Bindung: zwischen zwei Metallen, es entsteht ein Metall
 6. Chemische Bindung Es gibt in der Chemie drei verschiedene Arten von Bindungen: Metallische Bindung: zwischen zwei Metallen, es entsteht ein Metall Atombindung: zwischen zwei Nichtmetallen, es entsteht
6. Chemische Bindung Es gibt in der Chemie drei verschiedene Arten von Bindungen: Metallische Bindung: zwischen zwei Metallen, es entsteht ein Metall Atombindung: zwischen zwei Nichtmetallen, es entsteht
Magische Kristalle Prof. Dr. R. Glaum
 Magische Kristalle Prof. Dr. R. Glaum Institut für Anorganische Chemie Universität Bonn http://www.glaum.chemie.uni-bonn.de email: rglaum@uni-bonn.de Dank Herr Michael Kortmann Herr Andreas Valder Deutsche
Magische Kristalle Prof. Dr. R. Glaum Institut für Anorganische Chemie Universität Bonn http://www.glaum.chemie.uni-bonn.de email: rglaum@uni-bonn.de Dank Herr Michael Kortmann Herr Andreas Valder Deutsche
Physik I Mechanik und Thermodynamik
 Physik I Mechanik und hermodynamik 1 Einführung: 1.1 Was ist Physik? 1.2 Experiment - Modell - heorie 1.3 Geschichte der Physik 1.4 Physik und andere Wissenschaften 1.5 Maßsysteme 1.6 Messfehler und Messgenauigkeit
Physik I Mechanik und hermodynamik 1 Einführung: 1.1 Was ist Physik? 1.2 Experiment - Modell - heorie 1.3 Geschichte der Physik 1.4 Physik und andere Wissenschaften 1.5 Maßsysteme 1.6 Messfehler und Messgenauigkeit
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Grundlagen der statistischen Physik und Thermodynamik
 Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Seebeck-/Peltier-Effekt: thermoelektrische Materialien
 Seebeck-/Peltier-Effekt: thermoelektrische (Seebeck-Effekt) [1] Matthias Neumann, Sebastian Paulik Folie 1 1. Seebeck-Effekt 1.1 Einführung 1.2 Theorie 1.3 Anwendung Thomas Johann Seebeck (1770-1831) 2.
Seebeck-/Peltier-Effekt: thermoelektrische (Seebeck-Effekt) [1] Matthias Neumann, Sebastian Paulik Folie 1 1. Seebeck-Effekt 1.1 Einführung 1.2 Theorie 1.3 Anwendung Thomas Johann Seebeck (1770-1831) 2.
Physikalisches Praktikum II Bachelor Physikalische Technik: Lasertechnik Prof. Dr. H.-Ch. Mertins, MSc. M. Gilbert
 Physikalisches Praktikum II Bachelor Physikalische Technik: Lasertechnik Prof. Dr. H.-Ch. Mertins, MSc. M. Gilbert FK05 Solarzelle und Photowiderstand (Pr_PhII_FK05_Solarzelle_7, 25.10.2015) 1. 2. Name
Physikalisches Praktikum II Bachelor Physikalische Technik: Lasertechnik Prof. Dr. H.-Ch. Mertins, MSc. M. Gilbert FK05 Solarzelle und Photowiderstand (Pr_PhII_FK05_Solarzelle_7, 25.10.2015) 1. 2. Name
E2: Wärmelehre und Elektromagnetismus 6. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 6. Vorlesung 26.04.2018 Heute: - Kondensationskerne - Van der Waals-Gas - 2. Hauptsatz https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 26.04.2018 Prof.
E2: Wärmelehre und Elektromagnetismus 6. Vorlesung 26.04.2018 Heute: - Kondensationskerne - Van der Waals-Gas - 2. Hauptsatz https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 26.04.2018 Prof.
Grundlagen der Technischen Informatik
 Grundlagen der Technischen Informatik Dr. Wolfgang Koch Friedrich Schiller Universität Jena Fakultät für Mathematik und Informatik Rechnerarchitektur wolfgang.koch@uni-jena.de Inhalt Grundlagen der Techn.
Grundlagen der Technischen Informatik Dr. Wolfgang Koch Friedrich Schiller Universität Jena Fakultät für Mathematik und Informatik Rechnerarchitektur wolfgang.koch@uni-jena.de Inhalt Grundlagen der Techn.
Exkurs: Wasser Das Elixier des Lebens
 Exkurs: Wasser Das Elixier des Lebens Wasser Anatomie eines Moleküls VSEPR-Modell sp3-hybridorbital Sigma-Bindung Elektronenkonfiguration Sauerstoff Das vollbesetzte 2s-Orbital sowie die drei p-orbitale
Exkurs: Wasser Das Elixier des Lebens Wasser Anatomie eines Moleküls VSEPR-Modell sp3-hybridorbital Sigma-Bindung Elektronenkonfiguration Sauerstoff Das vollbesetzte 2s-Orbital sowie die drei p-orbitale
