Minerale und Kristalle: Bausteine der Erde
|
|
|
- Angelika Gehrig
- vor 7 Jahren
- Abrufe
Transkript
1 STEOP: System Erde (LV ) Unterstützendes Handoutmaterial zum Themenkomplex 3: Minerale und Kristalle: Bausteine der Erde Dieses Handoutmaterial ergänzt die Vorlesungsinhalte. Zur Prüfungsvorbereitung wird weiters empfohlen Kapitel 3 Die Baustoffe der Erde: Minerale und Gesteine des Lehrbuchs Press/Siever - Allgemeine Geologie (J. Grotzinger et al.), 5. Aufl., Springer Spektrum, 2008 (hier insbesondere die Kapitelzusammenfassung). Dieses Handout beinhaltet weitere für die STEOP-Prüfung relevante Inhalte, welche im o.g. Lehrbuchkapitel nicht hinreichend enthalten sind. Bei Fragen bitte zu kontaktieren: Prof. Lutz Nasdala, Institut für Mineralogie und Kristallographie der Universität Wien UZA2 Raum 2A251 / Telefon / lutz.nasdala@univie.ac.at
2 Empfohlene Literatur Mineralogie/Kristallographie: Allgemeines zur Mineralogie / Kristallographie ( easy ): Matthes, Lehrbuch der Allgemeinen Mineralogie (aktuelle Aufl. Okrusch/Matthes) Rösler, Lehrbuch der Mineralogie weiter allgemeine Mineralogie-Lehrbücher zur Mineral-Systematik: Strunz, Mineralogische Tabellen (nicht notwendig für Studienanfänger bzw. BSc) Mineralogie ( advanced ): Putnis, Introduction to mineral sciences (ab MSc bzw. PhD) Kristallographie: Kleber, Einführung in die Kristallographie
3 Mineralogie = Naturwissenschaft von den überwiegend kristallinen Bausteinen der uns umgebenden geologischen Materie, den Mineralen (Mineralogie = Lehre von den Mineralen) alter Begriff: Oryktognosie Allgemeines zur Mineralogie auch (eher ungebräuchlich): Lithurgik (Lehre von Verwendung und Bearbeitung von Mineralen und Gesteinen) Geologie Chemie Mineralogie = materialwiss. Geowissenschaft Physik Werkstoffwissenschaft
4 Allgemeines zur Mineralogie Allgemeine Mineralogie = allgemeingültige Gesetzmäßigkeiten vom Bau der Minerale, ihren physikalische und chemischen Eigenschaften, ihrer Bildung / Alteration / Vergehen, ihrem Vorkommen / paragenetischen Verhältnissen und ihrer Nutzung Spezielle Mineralogie = Beschreibung der einzelnen Minerale (Stellung im Mineralsystem, Bildung, Eigenschaften, etc.) Teilbereiche der Mineralogie: Historische Mineralogie Regionale Mineralogie Mineralchemie, Kristallchemie, Geochemie Mineralphysik, Kristallographie Mineralanalytik Technische Mineralogie / Angewandte Mineralogie / Synthesen Kosmische Mineralogie Mineralogie der Lagerstätten / genetische Mineralogie Mineralogie gesteinsbildender Spezies: Petrologie Mineralsystematik / systematische Mineralogie
5 Allgemeines zur Mineralogie Mineraldefinition: Minerale sind stofflich homogene, feste und kristalline anorganische Körper der natürlichen Materie der Erde Begriffsherkunft: minera (altdeutsch für Erz, Erzstufe), urspr. von mina (lat. Schacht); bzw. minare (lateinisch Bergbautreiben) Beispiele für Abweichungen von der Mineraldefinition: stoffliche Homogenität (= definierter Chemismus und definierte Kristallstruktur): z.b. Zonierungen, Verunreinigungen, Baufehler fester Aggregatzustand: z.b. Hg ist flüssig aber dennoch ein Mineral Kristallinität: amorphe Minerale (z.b. Opal, Gläser, metamikte Min.) anorganische Zusammensetzung: organische Minerale natürliche Minerale (= irdisch und kosmisch): z.b. technische Minerale, Mineralsynthesen terrestrische Entstehung: z.b. Minerale in Meteoriten
6 Zum Vergleich: Allgemeines zur Mineralogie Mineraldefinition: Minerale sind stofflich homogene, feste und kristalline anorganische Körper der natürlichen Materie der Erde Gestein = feste Vereinigung von Mineralen (sowie von Bruchstücken anderer Gesteine, Organismenrückständen, etc.); i.d.r. fest, i.d.r. natürlich auftretend, oft makroskopisch homogen aber i.d.r. mikroskopisch heterogen Stein = Körper oder Objekt, bestehend aus einem (oder mehreren) Mineral(en) oder Gestein(en) Kristall = homogener Festkörper definierter Zusammensetzung mit natürlich gewachsener polyedrischer Form, der durch (dreidimensional unendlich) regelmäßige Anordnung der Bausteine (Atome / Ionen / Moleküle) im sog. Kristallgitter charakterisiert ist Quasikristall = Körper, bei dem die Bausteine geordnet, aber nicht periodisch angeordnet sind
7 Allgemeines zur Mineralogie Mineralart: Mineralindividuen, deren chemische Zusammensetzung und Struktur gleich ist ACHTUNG: Zu vielen Mineralen gibt es neben den anerkannten Bezeichnungen auch veraltete, wenngleich immer noch gebräuchliche Begriffe! Beispiele: Kalkspat (= Calcit), Bleiglanz (= Galenit), Zinkblende (= Sphalerit), Roteisenstein (= Hämatit), Schwerspat (= Baryt) Mineralvarietät: alle Mineralinidividuen (einer Mineralart), die eine zusätzliche, spezifische Besonderheit aufweisen Beispiele: Amethyst = violetter Quarz; Achat = lagig-gebänderter, mikrokristalliner Quarz; Chalkotrichit = nadelig ausgebildeter Cuprit; Smaragd = grüner Beryll; Aquamarin = blauer Beryll; Rubin = roter Korund; Amazonit = grüner Mikroklin Mineralgruppe: umfasst mehrere Mineralarten, welche weitgehende Ähnlichkeiten (sind oft isostrukturell) aufweisen Beispiele: Granat-Gruppe; Turmalin-Gruppe; Feldspäte; Zeolithe (Gerüstsilikate mit strukturellen Kanälen, in denen Wasser eingelagert wird); Olivine
8 Polymorphe (bzw. polymorphe Mineralarten) = Minerale mit gleichem Chemismus, aber unterschiedlichen Kristallstrukturen ( Vielgestaltigkeit ) Beispiele: C (Graphit, Diamant) SiO 2 (Quarz, Tridymit, Coesit, Stishovit,...) KAlSi 3 O 8 (Sanidin, Orthoklas, Mikroklin) CaCO 3 (Calcit, Aragonit, Vaterit) Isotype Minerale = Minerale mit gleichem Strukturtyp, aber unterschiedlichem Chemismus Beispiele: Strontianit, SrCO 3 (im Aragonit-Strukturtyp) Sylvin, KCl; Galenit, PbS (beide im Halit-Strukturtyp) Kassiterit ( Zinnstein ), SnO 2 (im Rutil-Strukturtyp) Isomorphe Minerale = sehr ähnliche Strukturen, dadurch chemische Mischbarkeit bzw. Mischkristallbildung ( Gleichgestaltigkeit ) Beispiele: Allgemeines zur Mineralogie Fayalit (Fe 2 SiO 4 ) Forsterit (Mg 2 SiO 4 ) = Olivine Albit (NaAlSi 3 O 8 ) Anorthit (CaAl 2 Si 2 O 8 ) = Plagioklase
9 Mineralstruktur Die Struktur ist i.d.r. bestimmt durch Anordnung von Atomen in einem dreidimensional unendlichen Kristallgitter mit Translationssymmetrie ; daraus resultierend Kristalle (= makroskopisch ebenflächig begrenzte Körper): Fluorit, CaF 2 (Z=4): kub. Elementarzelle Translationsgitter kubische Kristalle (würfeliger Habitus)
10 Bau von Kristallen: Beispiel Halit (I) Anordnung von Na + - (rot) und Cl - -Ionen (blau) im kubischen Halitgitter Gleiche Darstellung, mit Ionenradien auf 25% reduziert. Schwarz: Elementarzelle Gleiche Darstellung, mit Cl-Koordinationspolyeder Oktaedrische (6er-) Koordination: Jedes Cl ist von sechs Na umgeben) Diese Seite beinhaltet ergänzende Informationen (nicht prüfungsrelevant im ersten Semester)
11 Bau von Kristallen: Beispiel Halit (II) Analoge Darstellung, plus hälftige darüberliegende Elementarzelle Gleiche Darstellung, mit Na- Koordinationspolyeder Oktaedrische (6er-) Koordination: Jedes Na ist von sechs Cl umgeben) Diese Seite beinhaltet ergänzende Informationen (nicht prüfungsrelevant im ersten Semester)
12 Bau von Kristallen: Beispiel Korund Blick entlang c-achse Blick perspektivisch gekippt Tetraedrische Koordination O-Al Oktaedrische Koordination Al-O Diese Seite beinhaltet ergänzende Informationen (nicht prüfungsrelevant im ersten Semester)
13 Bau von Kristallen: Beispiel Diopsid CaMg[Si 2 O 6 ] Anordnung von Ionen im monoklinen Diopsidgitter: rot = Ca grün = Mg blau = Si grau = O Gleiche Darstellung, mit Koordinationspolyedern Si-O = 4 Mg-O = 6 Ca-O = 8 Gleiche Darstellung, nur Koordinationspolyeder Diese Seite beinhaltet ergänzende Informationen (nicht prüfungsrelevant im ersten Semester)
14 Bau von Kristallen: Beispiel Ca-Zeolith Mordenit, Ca[AlSi 5 O 12 ] 2 6H 2 O Anordnung von Ionen im rhombischen Mordenitgitter: rot & grün = Ca, dunkelblau = Si, hellblau = H, grau = O Werden nur die Si-O-Tetraeder dargestellt, sind die typischen strukturellen Kanäle wesentlich besser erkennbar Diese Seite beinhaltet ergänzende Informationen (nicht prüfungsrelevant im ersten Semester)
15 Bau von Kristallen: Koordination Interatomare Bindung und Koordination: Radienverhältnis Koordination Beispiel 0,155-0,225 3 CO 3 in Calcit 0,225-0,414 4 SiO 4 in Olivin 0,414-0,732 6 NaCl 6 in Halit 0, CaO 8 in Diopsid > 1 12 KO 12 in Muskovit Diese Seite beinhaltet ergänzende Informationen (nicht prüfungsrelevant im ersten Semester)
16 Mineralchemismus Klassifikation in zehn Mineralklassen (welche wiederum nach chemischen oder strukturellen Gesichtspunkten in Abteilungen unterteilt werden): 1. Element-Minerale (z.b. Eisen, Fe; Diamant, C; Graphit, C) 2. Sulfide (z.b. Pyrit, FeS 2 ; Galenit, PbS; Sphalerit, ZnS) 3. Halide / Halogenide (z.b. Halit, NaCl; Fluorit, CaF 2 ) 4. Oxide / Hydroxide (z.b. Quarz, SiO 2 ; Magnetit, Fe 3 O 4 ) 5. Karbonate / Nitrate (z.b. Calcit, CaCO 3 ; Malachit, Cu 2 [(OH) 2 /CO 3 ]) 6. Borate 7. Sulfate (z.b. Gips, CaSO 4 2H 2 O; Baryt, BaSO 4 ) 8. Phosphate / Arsenate/ Vanadate (z.b. Apatit, Ca 5 [PO 4 ] 3 F) 9. Silikate (z.b. Forsterit, MgSiO 4 ; Pyrop, Mg 3 Al 2 [SiO 4 ] 3 ; Topas, Al 2 [F 2 /SiO 4 ]; Muscovit, KAl 2 [(OH,F) 2 /AlSi 3 O 10 ]; Orthoklas, K[AlSi 3 O 8 ]) 10. organische Minerale
17 Mineralchemismus: Silikate Sub-Klassifikation der Silikate nach kristallstrukturellen Gesichtspunkten in Abteilungen: Art der Vernetzung der SiO 4 -Tetraeder 1. bis 3. Keine unendliche Vernetzung: Nesosilikate (Insel) keine direkte Verknüpfung der Tetraeder; daher [SiO 4 ] Sorosilikate (Gruppe) Verknüpfung zweier Tetraeder zu [Si 2 O 7 ] Cyclosilikate (Ring) Verknüpfung über zwei Ecken (z.b. [Si 3 O 9,], [Si 6 O 18 ]) 4. Unendliche Vernetzung in einer Richtung: Inosilikate (Kette), weiter unterteilt in Einfachketten / Doppelketten und Einer-, Zweier-, Dreierketten etc. Einfachkette: Verknüpfung über zwei Ecken (z.b. [Si 2 O 6 ], [Si 5 O 15 ]) Doppelkette: Verknüpfung über zwei oder drei Ecken (z.b. Si 8 O 22 ]) 5. Unendliche Vernetzung in zwei Richtungen: Phyllosilikate (Schicht), weiter unterteilt in Zweischicht-, Dreischicht-, Vierschicht-silikate (mit und ohne Zwischenschichten etc.). Verknüpfung über drei Ecken. 6. Unendliche Vernetzung in drei Richtungen: Tektosilikate (Gerüst). Direkte Verknüpfung der Tetraeder über alle vier Ecken. Achtung: In manchen Lehrbüchern wird Quarz (Oxid!) als Tektosilikat behandelt. Diese Seite beinhaltet ergänzende Informationen (nicht prüfungsrelevant im ersten Semester)
18 Kristallsymmetrie Klassifikation in sieben (acht) Kristallsysteme (welche wiederum nach strukturellen Gesichtspunkten in Kristallklassen und Raumgruppen unterteilt werden) 1. Kubisches System (z.b. Diamant, C; Galenit, PbS; Pyrit, FeS 2; Halit, NaCl; Magnetit, Fe 3 O 4 ; Fluorit, CaF 2 ) 2. Tetragonales System (z.b. Chalkopyrit, CuFeS 2 ) 3. Rhombisches / orthorhombisches System (z.b. Olivine, (Mg,Fe) 2 SiO 4 ; Topas, Al 2 [F 2 /SiO 4 ]; Baryt, BaSO 4 ) 4. Hexagonales System (z.b. Apatit, Ca 5 [PO 4 ] 3 F) 5. Trigonales System (z.b. Calcit, CaCO 3 ; Korund, Al 2 O 3 ; Quarz, SiO 2 ) 6. Monoklines System (z.b. Gips, CaSO 4 2H 2 O; Malachit, Cu 2 [(OH) 2 /CO 3 ]; Muscovit, KAl 2 [(OH,F) 2 /AlSi 3 O 10 ]) 7. Triklines System (z.b. Mikroklin, K[AlSi 3 O 8 ]) [8. Amorphe Minerale; Beispiele Opal, Bernstein (?), Lechatelierit]
19 Kristallformen Geschlossene Formen: gleichwertige (besser symmetrieäquivalente) Kristallflächen können einen geschlossenen Körper aufbauen Beispiele: Tetraeder, Rhombendodekaeder, Dipyramide, Skalenoeder Offene Formen: gleichwertige (besser symmetrieäquivalente) Kristallflächen können NICHT einen geschlossenen Körper aufbauen Beispiele: Prisma (hex., tetrag.), Pinakoid (hex., tetrag.), Doma Einfache Formen: Kristalle bestehen aus nur einer Flächenart (besser: bestehen aus einer geschlossennen Form) Beispiele: Rhombendodekaeder, Oktaeder, Würfel, Dipyramide,... Kombinierte Formen: Kristalle weisen Flächen mehrerer (geschlossener und/oder offener) Formen auf Beispiel 1: Kombination rhombisches Disphenoid und zwei Pinakoide Beispiel 2: Kombination von sechs Pinakoiden (triklin) Beispiel 3: Kombination von hexagonalem Prisma und Basis-Pinakoid Diese Seite beinhaltet ergänzende Informationen (nicht prüfungsrelevant im ersten Semester)
20 Morphologie Kristallform idiomorph = eigengestaltig, xenomorph = fremdgestaltig (Zwischenstufe: hypidiomorph) Kristalltracht; Tracht = Gesamtheit der Flächen (Beispiele: oktaedrisch, würfelig, hexagonal-prismatisch, pyramidal) Kristallhabitus; Habitus = äußere Kristallgestalt (Beispiele: isometrisch, gedrungen, prismatisch, stängelig, nadelig, faserig, plattig; dabei oft Begriffe, welche die Zahl gleichwertiger Dimensionen beschreiben) Aggregatform = Art der Miteinender-Verwachsung von Kristallindividuen (Beispiele: massig, radialstrahlig, blättrig, verfilzt, nierig, traubig, oolithisch, stalaktitisch, gebändert; auch typische Verzwillingungen)
21 Morphologie: Tracht und Habitus Beispiel : gleiche Tracht bei unterschiedlichem Habitus (hier: Kombination des di-trigonalen Prismas mit Dipyramide) Quarzkristalle: oben kurzsäuliger (nahezu isometrischer) Habitus unten säuliger bzw. prismatischer Habitus Beispiel : gleicher Habitus (hier: säulig-prismatisch) bei unterschiedlicher Kristalltracht links: Quarzkristall (Kombination von Prisma und aufgesetzter Dipyramide) rechts: Aragonitkristall (Kombination von Prisma und Basis-Pinakoid)
22 Morphologie: Verwachsungen Reguläre Mineralverwachsungen: (a) Zwillinge: Individuen einer Mineralart mit unterschiedlicher kristallographischer Orientierung (b) Parallelverwachsungen: Individuen einer Mineralart mit übereinstimmender kristallographischer Orientierung (c) Epitaxie: Individuen verschiedener Mineralarten mit orientierter Verwachsung (durch Übereinstimmungen in den Gittersymmetrien bedingt)
23 Optische Eigenschaften Farbe im homogenen Festkörper eine kooperative Eigenschaft von Chemie und Struktur, verursacht durch wellenlängenspezifische Licht-Absorption (Wellenlängenbereich nm) i.d.r. anisotrop (Pleochroismus, Dichroismus) Strichfarbe, Strich im Pulver ( Strichfarbe ) reale Streu-/Absorptionsfarbe = Eigenfarbe, i.d.r. ohne Vorherrschaft kooperativer Effekte des homogenen makroskopischen Festkörpers Beispiele: Pyrit, FeS 2 Farbe goldgelb, Strich schwarz Malachit, Cu 2 (OH) 2 CO 3 Farbe grün, Strich grün Amazonit, KAlSi 3 O 8 Farbe grün, Strich weiß/farblos Transparenz transparent (durchsichtig), translucent (durchscheinend), trüb, milchig, opak (undurchsichtig) Diese Seite beinhaltet ergänzende Informationen (nicht prüfungsrelevant im ersten Semester)
24 Optische Eigenschaften Lichtbrechung optische Dichte; erkennbar anhand der Wechselwirkung von elektromagnetischer Strahlung mit Materie in kristalliner Materie i.d.r. anisotrop; beschrieben durch das Snellius sche Brechungsgesetz Glanz = visuell erkennbarer Effekt der Lichtbrechung sehr hohe Lichtbrechung: metallischer Glanz (bei opaken Festkörpern incl. Quecksilber; Bsp. Pyrit, Chalkopyrit) mittelhohe Lichtbrechung: halbmetallischer Glanz, Diamantglanz, Fettglanz (Bsp. Sphalerit, Rutil, Titanit) niedrige Lichtbrechung: Glasglanz, matter Glanz (Bsp. Halit, Quarz) weitere Begriffe für genauere Beschreibung: blendeartiger, harzartiger, seidiger Glanz (bergmännisch: Kiese - Glanze - Blenden - Fahle ) weitere Lichtwirkungen Doppelbrechung (Beispiel Calcit) sowie besondere Effekte (Opaleszenz - Labradorisieren - Chatoyance - Asterismus) Diese Seite beinhaltet ergänzende Informationen (nicht prüfungsrelevant im ersten Semester)
25 Optische Eigenschaften Doppelbrechung: Vermögen von Mineralen, einen Lichtstrahl in zwei Teilstrahlen aufzuspalten, welche sich dann hinsichtlich Lichtbrechung, Ausbreitungsrichtung, Absorption (Farbe), etc. unterschiedlich verhalten. Bei allen Mineralen, außer kubischen und amorphen Spezies. zweifach zu sehen. Calcit (CaCO 3 ): Großer Kristall im Gegenlicht, naturhistorisches Museum Wien. Als Resultat der starken Doppelbrechung ist die Kreuzblende zweifach zu sehen. Diese Seite beinhaltet ergänzende Informationen (nicht prüfungsrelevant im ersten Semester)
26 Mechanische Eigenschaften von Mineralen Härte = Widerstand, den ein Mineral dem mechanischen Eindringen eines anderen Minerals entgegensetzt; in kristalliner Materie immer anisotrop (uneinheitlich: Ritzhärte, Eindruckhärte, Schleifhärte) Ritzhärte: Mohs sche Härteskala = 10 Normminerale, bei denen das folgende (härtere) immer das vorhergehende von Einkristall zu Einkristall ritzt 1. Talk (mit dem Fingernagel schabbar) 2. Gips, Halit (mit dem Fingernagel ritzbar) 3. Calcit 4. Fluorit 5. Apatit (mit dem Messer ritzbar) 6. Orthoklas 7. Quarz (ritzt Fensterglas) 8. Topas 9. Korund 10. Diamant Diese Seite beinhaltet ergänzende Informationen (nicht prüfungsrelevant im ersten Semester)
27 Mechanische Eigenschaften von Mineralen Spaltbarkeit (bzw. Teilbarkeit) bzw. Bruch Verhalten eines Minerals / Kristalls bei mechanischer Zerstörung; strukturabhängig, daher in kristalliner Materie immer anisotrop Spaltbarkeit (bzw. Teilbarkeit) = entlang kristallographisch bestimmter Schwächezonen in der Struktur Bruch = Richtung nahezu beliebig, nicht kristallographisch vorbestimmt Beschreibung der Spaltbarkeit nach der Form (z.b. würfelig, spätig, blättrig) bzw. der Richtung (z.b. nach der Oktaederfläche, parallel zur Basis, senkrecht zum Prisma etc.) Beschreibung der Spaltbarkeit nach der Qualität (z.b. sehr vollkommmen, vollkommen, sehr gut, gut, mäßig, schlecht) Beschreibung des Bruchs nach der Topographie der entstehenden Oberfläche (z.b. uneben, muschelig, hakig,splittrig) Tenazität (Verformbarkeit) z.b. hämmerbar, schneidbar, duktil, flexibel, spröde Diese Seite beinhaltet ergänzende Informationen (nicht prüfungsrelevant im ersten Semester)
28 Mechanische Eigenschaften von Mineralen Dichte (angegeben in Gramm pro Kubikzentimeter) - orts- und richtungsunabhängige Konstante, D - Berechnung D = M/V ( M = Masse; V = Volumen) - bzw. Berechnung als sog. Röntgendichte : D = Z M / N V Z = Zahl der Formeleinheiten pro Elementarzelle M = molekulare Masse bzw. Summe der Atommassen pro Formeleinheit N = Loschmidt sche Zahl: 6, Atome pro g V = Volumen der Elementarzelle Beispiele (Angaben in g/cm 3 ): Eis 0.9 Halit 2.17 Graphit 2.22 Orthoklas 2.55 Quarz 2.65 Calcit 2.72 Biotit 2.98 Apatit 3.18 Topas 3.57 Rutil 4.30 Baryt 4.48 Hämatit 5.3 Galenit 7.6 Quecksilber 13.5 Gold 19.3 Platin 21.5 Diese Seite beinhaltet ergänzende Informationen (nicht prüfungsrelevant im ersten Semester)
29 Zusatz zur Terminologie Organogene Minerale vs. organische Minerale: - organogen: durch Tätigkeit lebender Organismen entstanden Beispiele: Muscheln, Radiolarien, Diatomeen (Calcit, Aragonit, auch Strontianit); Otolithe, Perlen (Aragonit, Vaterit); Knochen, Zahnmaterial (Ca-Apatit) - organisch: organische chemische Zusammensetzung = C-H-O-Verbindung Beispiele: Ravatit (C 14 H 10 ); Whewellit (CaC 2 O 4 H 2 O) Beispiel für eine organogene sedimentäre Lagerstätte: Muschelkalkabbau bei Shark Bay, WA. Fotos privat.
30 Mineralgenese 1. Magmatische Bildung: Entstehung aus einem meist silikatischen Magma (= glutheiße Schmelze, meist silikatisch) liquidmagmatische Bildungen = Phasen entstehen direkt aus dem (flüssigen) Magma Pegmatite = Spätkristallisate, riesenkörnig postmagmatische Bildungen = Phasen entstehen aus Fluida (Gasen und/oder Flüssigkeiten), die aus dem Magma entwichen sind bzw. sich aus diesem entwickelt haben pneumatolytische Bildungen = aus überkritischen Fluida hydrothermale Bildungen = aus unterkritischen Fluida 2. Metamorphe / metamorphogene Bildung: Entstehung durch Metamorphose (= Umwandlung eines Minerals in ein anderes etc.) Metamorphose (= Umwandlung eines Minerals in ein anderes etc.) 3. Sedimentäre Bildung: Entstehung durch exogene Prozesse (mechanische, chemische oder biogene Verwitterung) Seifen = sekundäre sedimentäre Mineralanreicherungen
31 Allgemeine Termini: Mineralgenese Paragenese = typische, weil gesetzmäßige Mineralvergesellschaftung Assoziation = zufällige Mineralvergesellschaftung Akzessorien = weit verbreitete, aber in Gesteinen nur in geringen Konzentrationen vorkommende Minerale (Gegensatz zu Hauptgesteinsbestandteilen) genesekritische Minerale = Minerale, welche nur in einem relativ schmalen Bildungsbereich entstehen (auch Faziesanzeiger) Bsp.: Diamant, Coesit für HP-HT Bsp.: Sylvin für Evaporite Bsp.: Auripigment (As 2 S 3 ) für niedrigstthermale Hydrothermen Durchläuferminerale = Gegensatz zu oben: Minerale, die in sehr vielen Bildungsbereichen entstehen bzw. vorkommen Bsp.: Quarz (liquidmagmatisch, pegmatitisch, pneumatolytisch, hydrothermal, biogen, metamorph, etc.)
32 Pseudomorphosen Mineralalteration Pseudomorphose = ein Mineral in der äußeren Gestalt eines anderen Minerals (durch sekundäre Mineralumwandlung bei Beibehaltung der äußeren Form) Beispiel: Hämatit pseudomorph nach Magnetit durch Umwandlungsreaktion 2 Fe 3 O 4 + ½ O 2 3 Fe 2 O 3 Monazit pseudomorph nach Apatit Paramorphose = Pseudomorphose ohne chemische Änderung (ein Polymorph nach einem anderen Polymorph der selben chemischen Substanz) Beispiel: graphitisierter Diamant, Tief-Quarz nach Hoch-Quarz Perimorphose = Umhüllungs-Pseudomorphose
Allgemeines zur Mineralogie / wichtige Definitionen:
 Allgemeines zur Mineralogie / wichtige Definitionen: Mineralogie = Lehre von den überwiegend kristallinen Bausteinen der uns umgebenden geologischen Materie, den Mineralen (Mineralogie = Lehre von den
Allgemeines zur Mineralogie / wichtige Definitionen: Mineralogie = Lehre von den überwiegend kristallinen Bausteinen der uns umgebenden geologischen Materie, den Mineralen (Mineralogie = Lehre von den
Übungen zur Allgemeinen Geologie, Nebenfach. Erta Ale, Afrika
 Übungen zur Allgemeinen Geologie, Nebenfach Erta Ale, Afrika Minerale anorganisch, (natürlich) Festkörper definierte chemische Zusammensetzung homogen definiert durch chemische Formel kristallin Physikalische
Übungen zur Allgemeinen Geologie, Nebenfach Erta Ale, Afrika Minerale anorganisch, (natürlich) Festkörper definierte chemische Zusammensetzung homogen definiert durch chemische Formel kristallin Physikalische
Einführung in die Geologie
 Einführung in die Geologie Teil 4: Minerale - Baustoffe der Gesteine Prof. Dr. Rolf Bracke International Geothermal Centre Lennershofstraße 140 44801 Bochum Übersicht Definition der Minerale Minerale und
Einführung in die Geologie Teil 4: Minerale - Baustoffe der Gesteine Prof. Dr. Rolf Bracke International Geothermal Centre Lennershofstraße 140 44801 Bochum Übersicht Definition der Minerale Minerale und
Einführung in die Geowissenschaften I Geomaterialien Teil II WS 2016/2017
 Einführung in die Geowissenschaften I Geomaterialien Teil II WS 2016/2017 13. Dez. Kristallchemie der Silikate Was ist ein Mineral? Was ist ein Gestein? Gesteinsbildende Minerale 20. Dez Das System Erde:
Einführung in die Geowissenschaften I Geomaterialien Teil II WS 2016/2017 13. Dez. Kristallchemie der Silikate Was ist ein Mineral? Was ist ein Gestein? Gesteinsbildende Minerale 20. Dez Das System Erde:
Gesteinskunde Einführung
 Gesteinskunde Einführung Christopher Giehl, Uni Tübingen 13.10.2011 Christopher Giehl (Universität Tübingen) 13.10.2011 1 / 23 1 Organisatorisches 2 Kursinhalte und -ziele 3 Grundbegriffe und Definitionen
Gesteinskunde Einführung Christopher Giehl, Uni Tübingen 13.10.2011 Christopher Giehl (Universität Tübingen) 13.10.2011 1 / 23 1 Organisatorisches 2 Kursinhalte und -ziele 3 Grundbegriffe und Definitionen
Klausur vom
 Klausur vom 18.07.2006 1. Nennen sie die Mineralklassen der folgenden Minerale: Augit Azurit Halit Galenit Chromit Anhydrit 2. Warum schwankt die Dichte von Platin zwischen 15 und 21 g/cm 3? 3. Nennen
Klausur vom 18.07.2006 1. Nennen sie die Mineralklassen der folgenden Minerale: Augit Azurit Halit Galenit Chromit Anhydrit 2. Warum schwankt die Dichte von Platin zwischen 15 und 21 g/cm 3? 3. Nennen
Einführung in die Geologie. Mark Feldmann Dr.sc.nat. ETH
 Geologie & Tourismus Einführung in die Geologie Mark Feldmann Dr.sc.nat. ETH Ihr Profi für geo-kulturelle Führungen und Exkursionen Buchholzstrasse 58 8750 Glarus 078 660 01 96 www.geo-life.ch Inhalt Aufbau
Geologie & Tourismus Einführung in die Geologie Mark Feldmann Dr.sc.nat. ETH Ihr Profi für geo-kulturelle Führungen und Exkursionen Buchholzstrasse 58 8750 Glarus 078 660 01 96 www.geo-life.ch Inhalt Aufbau
Prinzipien des Kristallbaus
 Zirkon Prinzipien des Kristallbaus 1. Pauling sche Regel: Kationen umgeben sich mit Anionen, wobei Anionen annähernd regelmässige Polyeder bilden. Die Koordinationszahl der Kationen, d.h. die Anzahl Anionen
Zirkon Prinzipien des Kristallbaus 1. Pauling sche Regel: Kationen umgeben sich mit Anionen, wobei Anionen annähernd regelmässige Polyeder bilden. Die Koordinationszahl der Kationen, d.h. die Anzahl Anionen
STEOP: System Erde (LV ) Unterstützendes Handoutmaterial zum Themenkomplex 4: Magmatite:
 STEOP: System Erde (LV 280001) Unterstützendes Handoutmaterial zum Themenkomplex 4: Magmatite: Gesteine und Minerale entstanden aus Schmelzen und ihren Folgeprodukten Dieses Handoutmaterial ergänzt die
STEOP: System Erde (LV 280001) Unterstützendes Handoutmaterial zum Themenkomplex 4: Magmatite: Gesteine und Minerale entstanden aus Schmelzen und ihren Folgeprodukten Dieses Handoutmaterial ergänzt die
Die Bestimmung gesteinsbildender Minerale
 7 2 Die Bestimmung gesteinsbildender Minerale 2.1 Definition 8 2.2 Mineralgliederung 8 2.3 Mineraleigenschaften 8 2.4 Gesteinsbildende Minerale 9 U. Sebastian, Gesteinskunde, DOI 10.1007/978-3-642-41757-3_2,
7 2 Die Bestimmung gesteinsbildender Minerale 2.1 Definition 8 2.2 Mineralgliederung 8 2.3 Mineraleigenschaften 8 2.4 Gesteinsbildende Minerale 9 U. Sebastian, Gesteinskunde, DOI 10.1007/978-3-642-41757-3_2,
Wiederholung der letzten Vorlesungsstunde
 Wiederholung der letzten Vorlesungsstunde Festkörper, ausgewählte Beispiele spezieller Eigenschaften von Feststoffen, Kohlenstoffmodifikationen, Nichtstöchiometrie, Unterscheidung kristalliner und amorpher
Wiederholung der letzten Vorlesungsstunde Festkörper, ausgewählte Beispiele spezieller Eigenschaften von Feststoffen, Kohlenstoffmodifikationen, Nichtstöchiometrie, Unterscheidung kristalliner und amorpher
Allgemeines zu Mineraleigenschaften:
 Allgemeines zu Mineraleigenschaften: Wichtigste Gruppen von physikalischen Eigenschaften: - mechanische Eigenschaften - optische Eigenschaften - magnetische Eigenschaften - thermische Eigenschaften - elektrische
Allgemeines zu Mineraleigenschaften: Wichtigste Gruppen von physikalischen Eigenschaften: - mechanische Eigenschaften - optische Eigenschaften - magnetische Eigenschaften - thermische Eigenschaften - elektrische
Grundlagen der Geowissenschaften
 Übungen zur Lehrveranstaltung: Grundlagen der Geowissenschaften Jörg A. Pfänder, TU Freiberg Die Folien (in Farbe & ungekürzt) sind auch zu finden unter: http://www.geo.tu-freiberg.de/tektono/privatesites/pfaender/index.html
Übungen zur Lehrveranstaltung: Grundlagen der Geowissenschaften Jörg A. Pfänder, TU Freiberg Die Folien (in Farbe & ungekürzt) sind auch zu finden unter: http://www.geo.tu-freiberg.de/tektono/privatesites/pfaender/index.html
Beispielklausur Geochemie I Mineralogie (Anteil Schertl)
 Beispielklausur Geochemie I Mineralogie (Anteil Schertl) 1. Wichtig zum Verständnis der Kristallchemie von Mineralen sind Wertigkeiten und Ionenradien von Elementen. a. Geben Sie die Wertigkeiten folgender
Beispielklausur Geochemie I Mineralogie (Anteil Schertl) 1. Wichtig zum Verständnis der Kristallchemie von Mineralen sind Wertigkeiten und Ionenradien von Elementen. a. Geben Sie die Wertigkeiten folgender
Anorganische Chemie III - Festkörperchemie
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Festkörperchemie
Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Festkörperchemie
Mineralogie Wissenschaft zwischen den Stühlen
 Mineralogie Wissenschaft zwischen den Stühlen Lehrerfortbildung des HZDR 2013 Dr. Robert Möckel 08. Februar 2013 Inhalt Was ist Mineralogie? Was ist ein Mineral? Wie kann man Minerale unterscheiden? Beispiel
Mineralogie Wissenschaft zwischen den Stühlen Lehrerfortbildung des HZDR 2013 Dr. Robert Möckel 08. Februar 2013 Inhalt Was ist Mineralogie? Was ist ein Mineral? Wie kann man Minerale unterscheiden? Beispiel
Einführung in die Geologie Teil 4: Minerale - Baustoffe der Gesteine
 Einführung in die Geologie Teil 4: Minerale - Baustoffe der Gesteine Prof. Dr. Rolf Bracke FH Bochum GeothermieZentrum Lennershofstraße 140 44801 Bochum Übersicht Definition der Minerale Minerale und Kristalle
Einführung in die Geologie Teil 4: Minerale - Baustoffe der Gesteine Prof. Dr. Rolf Bracke FH Bochum GeothermieZentrum Lennershofstraße 140 44801 Bochum Übersicht Definition der Minerale Minerale und Kristalle
Nachbesprechung. Übung 6
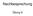 Nachbesprechung Übung 6 Mischungsdreieck Alamandin (Fe) X möglich Pyrop (Mg) X nicht möglich Spessartin (Mn) Phasendiagramm V (Andalusit) > V (Sillimanit) > V (Kyanit) S (Sillimanit) > S (Andalusit) >
Nachbesprechung Übung 6 Mischungsdreieck Alamandin (Fe) X möglich Pyrop (Mg) X nicht möglich Spessartin (Mn) Phasendiagramm V (Andalusit) > V (Sillimanit) > V (Kyanit) S (Sillimanit) > S (Andalusit) >
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Kupfermineralien (Teil-2)
 Kupfermineralien (Teil-2) Helmut Kuhle, Mitglied der Arbeitsgemeinschaft Bergbau und Geowissenschaften e.v. Oxide Cuprit (veraltet Rotkupfererz, chemisch Kupfer(l)-oxid) ist ein eher selten vorkommendes
Kupfermineralien (Teil-2) Helmut Kuhle, Mitglied der Arbeitsgemeinschaft Bergbau und Geowissenschaften e.v. Oxide Cuprit (veraltet Rotkupfererz, chemisch Kupfer(l)-oxid) ist ein eher selten vorkommendes
Vorlesung. Geomaterialien. Eigenschaften von Mineralen
 Vorlesung Geomaterialien Eigenschaften von Mineralen Prof. Dr. Frank E. Brenker Institut für Geowissenschaften Mineralogie JWG-Universität Frankfurt Ziele der heutigen Vorlesung Kennenlernen der Eigenschaften
Vorlesung Geomaterialien Eigenschaften von Mineralen Prof. Dr. Frank E. Brenker Institut für Geowissenschaften Mineralogie JWG-Universität Frankfurt Ziele der heutigen Vorlesung Kennenlernen der Eigenschaften
Vorlesung. Geomaterialien. 1. Doppelstunde Chemische Grundlagen der Minerale Glossar. Prof. Dr. F.E. Brenker
 Vorlesung Geomaterialien 1. Doppelstunde Chemische Grundlagen der Minerale Glossar Prof. Dr. F.E. Brenker Institut für Geowissenschaften FE Mineralogie JWG-Universität Frankfurt AG Brenker Planetare und
Vorlesung Geomaterialien 1. Doppelstunde Chemische Grundlagen der Minerale Glossar Prof. Dr. F.E. Brenker Institut für Geowissenschaften FE Mineralogie JWG-Universität Frankfurt AG Brenker Planetare und
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Häufige Kristallformen der Granate. Rösler 1984
 Häufige Kristallformen der Granate Rösler 1984 Deer, Howie, Zussman 1996 Granat Granat in pegmatitischer Lage im Plattengneis, Koralpe, Österreich Grossular ( Demantoid ), Idria, California Granat Granat-Glimmerschiefer
Häufige Kristallformen der Granate Rösler 1984 Deer, Howie, Zussman 1996 Granat Granat in pegmatitischer Lage im Plattengneis, Koralpe, Österreich Grossular ( Demantoid ), Idria, California Granat Granat-Glimmerschiefer
Metamorphe Gesteine und Minerale
 STEOP: System Erde (LV 280001) Unterstützendes Handoutmaterial zum Themenkomplex 6: Metamorphe Gesteine und Minerale Dieses Handoutmaterial ergänzt die Vorlesungsinhalte. Zur Prüfungsvorbereitung wird
STEOP: System Erde (LV 280001) Unterstützendes Handoutmaterial zum Themenkomplex 6: Metamorphe Gesteine und Minerale Dieses Handoutmaterial ergänzt die Vorlesungsinhalte. Zur Prüfungsvorbereitung wird
Gesteinskunde. Bestimmung magmatischer Minerale. Christopher Giehl, Uni Tübingen 20.10.2011
 Gesteinskunde Bestimmung magmatischer Minerale Christopher Giehl, Uni Tübingen 20.10.2011 Christopher Giehl (Universität Tübingen) 20.10.2011 1 / 18 1 Wiederholung 2 Klassifikation magmatischer Gesteine
Gesteinskunde Bestimmung magmatischer Minerale Christopher Giehl, Uni Tübingen 20.10.2011 Christopher Giehl (Universität Tübingen) 20.10.2011 1 / 18 1 Wiederholung 2 Klassifikation magmatischer Gesteine
Handout zum Vorlesungsteil Physikalische Eigenschaften von Mineralen
 Handout zum Vorlesungsteil Physikalische Eigenschaften von Mineralen Wichtigste Gruppen von physikalischen Eigenschaften: - mechanische Eigenschaften - optische Eigenschaften - magnetische Eigenschaften
Handout zum Vorlesungsteil Physikalische Eigenschaften von Mineralen Wichtigste Gruppen von physikalischen Eigenschaften: - mechanische Eigenschaften - optische Eigenschaften - magnetische Eigenschaften
Unterrichtsmaterial zur Stoff-Separation einer heterogenen Mischung am Beispiel von Granit
 Unterrichtsmaterial zur Stoff-Separation einer heterogenen Mischung am Beispiel von Granit Inhalt (je 6x) Granit Schraubdeckelgläser mit Granitsplitter Quarz Alkalifeldspat Plagioklas Schraubdeckelgläser
Unterrichtsmaterial zur Stoff-Separation einer heterogenen Mischung am Beispiel von Granit Inhalt (je 6x) Granit Schraubdeckelgläser mit Granitsplitter Quarz Alkalifeldspat Plagioklas Schraubdeckelgläser
Talk Apatit Feldspat Topas. Granat Halit Magnetit Turmalin Härte (Mohs): Härte (Mohs):
 Talk Apatit Feldspat Topas mittlere Volumen Lichtbrechung: Elementarzelle:.-. Talk ist das weichste Mineral, man kann es sogar mit dem Fingernagel ritzen. Zähne und Knochen des Körpers bestehen zu einem
Talk Apatit Feldspat Topas mittlere Volumen Lichtbrechung: Elementarzelle:.-. Talk ist das weichste Mineral, man kann es sogar mit dem Fingernagel ritzen. Zähne und Knochen des Körpers bestehen zu einem
LV Materialwissenschaftliche Mineralogie Handout zum Vorlesungsteil Physikalische Eigenschaften von Mineralen
 LV Materialwissenschaftliche Mineralogie Handout zum Vorlesungsteil Physikalische Eigenschaften von Mineralen Wichtigste Gruppen von physikalischen Eigenschaften: - mechanische Eigenschaften - optische
LV Materialwissenschaftliche Mineralogie Handout zum Vorlesungsteil Physikalische Eigenschaften von Mineralen Wichtigste Gruppen von physikalischen Eigenschaften: - mechanische Eigenschaften - optische
Grundlagen der Geowissenschaften: Mineralogie
 Grundlagen der Geowissenschaften: Mineralogie Gerhard Heide Institut für Mineralogie Professur für Allgemeine und Angewandte Mineralogie Direktor der Geowissenschaftlichen Sammlungen Brennhausgasse 14
Grundlagen der Geowissenschaften: Mineralogie Gerhard Heide Institut für Mineralogie Professur für Allgemeine und Angewandte Mineralogie Direktor der Geowissenschaftlichen Sammlungen Brennhausgasse 14
LV Mikroskopie I Kurs 6 1/10
 LV 620.108 Mikroskopie I Kurs 6 1/10 Olivin-Gruppe Als Vorbereitung für die Übungen sind die Kapitel über Nesosilikate (Olivin) und Inosilikate (Pyroxene) in Matthes Mineralogie (oder einem vergleichbaren
LV 620.108 Mikroskopie I Kurs 6 1/10 Olivin-Gruppe Als Vorbereitung für die Übungen sind die Kapitel über Nesosilikate (Olivin) und Inosilikate (Pyroxene) in Matthes Mineralogie (oder einem vergleichbaren
Anorganische Chemie III - Festkörperchemie
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Wiederholung
Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Wiederholung
Grundlagen der Geowissenschaften: Mineralogie
 Grundlagen der Geowissenschaften: Mineralogie Mineralbildung Stoffbestand der Erde Mineralsystematik Gesteinsbildene Minerale Gerhard Heide Institut für Mineralogie Professur für Allgemeine und Angewandte
Grundlagen der Geowissenschaften: Mineralogie Mineralbildung Stoffbestand der Erde Mineralsystematik Gesteinsbildene Minerale Gerhard Heide Institut für Mineralogie Professur für Allgemeine und Angewandte
Unterrichtsmaterial zum Modul Symmetrie
 Unterrichtsmaterial zum Modul Symmetrie Inhalt (je 4x) Alkalifeldspat (Prisma - monoklin) Kalkspat/Calcit (Rhomboeder - trigonal) Apatit (Prisma & Pyramide - hexagonal) Quarz (Prisma & Pyramide - trigonal)
Unterrichtsmaterial zum Modul Symmetrie Inhalt (je 4x) Alkalifeldspat (Prisma - monoklin) Kalkspat/Calcit (Rhomboeder - trigonal) Apatit (Prisma & Pyramide - hexagonal) Quarz (Prisma & Pyramide - trigonal)
Grundlagen der Chemie Ionenradien
 Ionenradien Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Ionenradien In einem Ionenkristall halten benachbarte
Ionenradien Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Ionenradien In einem Ionenkristall halten benachbarte
Modul: Allgemeine Chemie
 Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Mensch und Umwelt; Lagerstätten und Rohstoffe
 STEOP: System Erde (LV 280001) Unterstützendes Handoutmaterial zum Themenkomplex 23: Mensch und Umwelt; Lagerstätten und Rohstoffe Dieses Handoutmaterial ergänzt die Vorlesungsinhalte. Zur Prüfungsvorbereitung
STEOP: System Erde (LV 280001) Unterstützendes Handoutmaterial zum Themenkomplex 23: Mensch und Umwelt; Lagerstätten und Rohstoffe Dieses Handoutmaterial ergänzt die Vorlesungsinhalte. Zur Prüfungsvorbereitung
Thema heute: Aufbau fester Stoffe - Kristallographie
 Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung Ionenbindung, Kationen, Anionen, Coulomb-Kräfte Thema heute: Aufbau fester Stoffe - Kristallographie 244 Aufbau fester Materie Im Gegensatz
Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung Ionenbindung, Kationen, Anionen, Coulomb-Kräfte Thema heute: Aufbau fester Stoffe - Kristallographie 244 Aufbau fester Materie Im Gegensatz
Grundriß der Mineralogie und Petrographie
 Grundriß der Mineralogie und Petrographie Eine Einführung für Studierende und zum Selbstunterricht Begründet von Gottlob Linck und Hermann Jung Dritte, neubearbeitete Auflage von Dr. phil. Hermann Jung
Grundriß der Mineralogie und Petrographie Eine Einführung für Studierende und zum Selbstunterricht Begründet von Gottlob Linck und Hermann Jung Dritte, neubearbeitete Auflage von Dr. phil. Hermann Jung
Beim Symmetriezentrum = Inversionszentrum wird jeder Punkt des Kristalls an einem gedachten Mittelpunkt gespiegelt.
 Mineralien : Glitzernde Kostbarkeiten Allgemeines Ein Mineral ist ein homogener, meist fester, kristalliner und anorganischer Grundbaustein der natürlichen Materie. Eine Mineralart ist durch ihre chemischer
Mineralien : Glitzernde Kostbarkeiten Allgemeines Ein Mineral ist ein homogener, meist fester, kristalliner und anorganischer Grundbaustein der natürlichen Materie. Eine Mineralart ist durch ihre chemischer
Enstatit Bamle, N. Kettensilikate
 Enstatit Bamle, N Kettensilikate Silikat-Strukturen Klassifikation nach Polymerisierungsgrad der SiO 4 -Tetraeder Kettensilikate / Inosilikate [SiO 3 ] 2- Einfachketten [Si 4 O 11 ] 6- Doppelketten Pyroxene,
Enstatit Bamle, N Kettensilikate Silikat-Strukturen Klassifikation nach Polymerisierungsgrad der SiO 4 -Tetraeder Kettensilikate / Inosilikate [SiO 3 ] 2- Einfachketten [Si 4 O 11 ] 6- Doppelketten Pyroxene,
Struktur von Festkörpern
 Struktur von Festkörpern Wir wollen uns zunächst mit der Struktur von Festkörpern, daß heißt mit der Geometrie in der sie vorliegen beschäftigen Kovalent gebundene Festkörper haben wir bereits in Form
Struktur von Festkörpern Wir wollen uns zunächst mit der Struktur von Festkörpern, daß heißt mit der Geometrie in der sie vorliegen beschäftigen Kovalent gebundene Festkörper haben wir bereits in Form
Kristallchemie. Atome Ionen Moleküle Chemische Bindungen
 Kristallchemie Atome Ionen Moleküle Chemische Bindungen Metalle, Metalloide, Nichtmetalle Metalle: E-neg < 1.9 - e - Abgabe Kationen Nichtmetalle: E-neg > 2.1 - e - Aufnahme Anionen Metalloide: B, Si,
Kristallchemie Atome Ionen Moleküle Chemische Bindungen Metalle, Metalloide, Nichtmetalle Metalle: E-neg < 1.9 - e - Abgabe Kationen Nichtmetalle: E-neg > 2.1 - e - Aufnahme Anionen Metalloide: B, Si,
Na 2 [Si 3 Al 2 O 10 ] 2H 2 O. KCa[Si 5 Al 3 O 16 ] 6H 2 O. Ca[Si 7 Al 2 O 18 ] 7H 2 O. Na 6 [Si 30 Al 6 O 72 ] 24H 2 O
![Na 2 [Si 3 Al 2 O 10 ] 2H 2 O. KCa[Si 5 Al 3 O 16 ] 6H 2 O. Ca[Si 7 Al 2 O 18 ] 7H 2 O. Na 6 [Si 30 Al 6 O 72 ] 24H 2 O Na 2 [Si 3 Al 2 O 10 ] 2H 2 O. KCa[Si 5 Al 3 O 16 ] 6H 2 O. Ca[Si 7 Al 2 O 18 ] 7H 2 O. Na 6 [Si 30 Al 6 O 72 ] 24H 2 O](/thumbs/62/47486773.jpg) 1 Tektosilikate Überblick 1. SiO 2 -Gruppe Quarz (hoch - tief) Tridymit Cristobalit Coesite Stishovit Opal 2. Feldspat-Gruppe Alkalifeldspäte K[Si 3 AlO 8 ] Plagioklasreihe Na[Si 3 AlO 8 ] Ca[Si 2 Al 2
1 Tektosilikate Überblick 1. SiO 2 -Gruppe Quarz (hoch - tief) Tridymit Cristobalit Coesite Stishovit Opal 2. Feldspat-Gruppe Alkalifeldspäte K[Si 3 AlO 8 ] Plagioklasreihe Na[Si 3 AlO 8 ] Ca[Si 2 Al 2
Thema heute: Chemische Bindungen - Ionenbindung
 Wiederholung der letzten Vorlesungsstunde: Chemische Bindungen, Doppelbindungsregel, VSEPR-Theorie Thema heute: Chemische Bindungen - Ionenbindung Vorlesung Allgemeine Chemie, Prof. Dr. Martin Köckerling
Wiederholung der letzten Vorlesungsstunde: Chemische Bindungen, Doppelbindungsregel, VSEPR-Theorie Thema heute: Chemische Bindungen - Ionenbindung Vorlesung Allgemeine Chemie, Prof. Dr. Martin Köckerling
Erich Offermann. Kristalle. und ihre Formen. Band 1: Theoretische Kristallmorphologie - Leseprobe S KristalloGrafik Verlag
 Erich Offermann Kristalle und ihre Formen Band 1: Theoretische Kristallmorphologie - Leseprobe S. 94- KristalloGrafik Verlag Allgemeines Formenkombinationen 3.1 Allgemeines zu Formenkombinationen 3.1.1
Erich Offermann Kristalle und ihre Formen Band 1: Theoretische Kristallmorphologie - Leseprobe S. 94- KristalloGrafik Verlag Allgemeines Formenkombinationen 3.1 Allgemeines zu Formenkombinationen 3.1.1
Konzepte der anorganischen und analytischen Chemie II II
 Konzepte der anorganischen und analytischen Chemie II II Marc H. Prosenc Inst. für Anorganische und Angewandte Chemie Tel: 42838-3102 prosenc@chemie.uni-hamburg.de Outline Einführung in die Chemie fester
Konzepte der anorganischen und analytischen Chemie II II Marc H. Prosenc Inst. für Anorganische und Angewandte Chemie Tel: 42838-3102 prosenc@chemie.uni-hamburg.de Outline Einführung in die Chemie fester
6. Die Chemische Bindung
 6. Die Chemische Bindung Hauptbindungsarten Kovalente Bindung I Kovalente Bindung II Ionenbindung Metallische Bindung Nebenbindungsarten Van der Waals Wechselwirkung Wasserstoffbrückenbindung Salzartige
6. Die Chemische Bindung Hauptbindungsarten Kovalente Bindung I Kovalente Bindung II Ionenbindung Metallische Bindung Nebenbindungsarten Van der Waals Wechselwirkung Wasserstoffbrückenbindung Salzartige
Auf n-kugeln einer dichtesten Packung kommen n-oktaederlücken und 2n-Tetraederlücken
 2.1 Kugelpackungen In einer Verbindung A m X n haben die X-Atome die Anordnung einer dichtesten Kugelpackung und A-Atome besetzen die Oktaederlücken (OL). Geben Sie die resultierenden Formeln A m X n an,
2.1 Kugelpackungen In einer Verbindung A m X n haben die X-Atome die Anordnung einer dichtesten Kugelpackung und A-Atome besetzen die Oktaederlücken (OL). Geben Sie die resultierenden Formeln A m X n an,
Ökopedologie I + II. Einführung in die Mineralogie und Gesteinskunde
 Ökopedologie I + II Einführung in die Mineralogie und Gesteinskunde Minerale - Definition Minerale sind stofflich einheitliche (physikalisch und chemisch homogene), feste, anorganische, meist natürlich
Ökopedologie I + II Einführung in die Mineralogie und Gesteinskunde Minerale - Definition Minerale sind stofflich einheitliche (physikalisch und chemisch homogene), feste, anorganische, meist natürlich
Gesteine. Die. und ihre Mineralien. Ein Einführungs- und Bestimmungsbuch. Richard V. Dietrich Brian J. Skinner
 Richard V. Dietrich Brian J. Skinner Die Gesteine und ihre Mineralien Ein Einführungs- und Bestimmungsbuch Aus dem Amerikanischen übersetzt und bearbeitet von: Dipl. Geol. Werner Knorr und Dr. Helmuth
Richard V. Dietrich Brian J. Skinner Die Gesteine und ihre Mineralien Ein Einführungs- und Bestimmungsbuch Aus dem Amerikanischen übersetzt und bearbeitet von: Dipl. Geol. Werner Knorr und Dr. Helmuth
Faszination der Kristalle
 B&U 3 PLUS Infos für Lehrerinnen und Lehrer Allgemeine Informationen B&U PLUS ist ein frei zugängliches, speziell auf die Inhalte der Schulbuchreihe B&U abgestimmtes ONLINE-Zusatzmaterial ( http://bu3.veritas.at
B&U 3 PLUS Infos für Lehrerinnen und Lehrer Allgemeine Informationen B&U PLUS ist ein frei zugängliches, speziell auf die Inhalte der Schulbuchreihe B&U abgestimmtes ONLINE-Zusatzmaterial ( http://bu3.veritas.at
Einführung in die Mineralogie- Kristallographie
 Einführung in die Mineralogie- Kristallographie Dozent: R. Abart AB Mineralogie-Petrologie Inst. für Geologische Wissenschaften FB Geowissenschaften Assistenz H-P. Nabein E. Petrishcheva J. Wanderer Zustandsformen
Einführung in die Mineralogie- Kristallographie Dozent: R. Abart AB Mineralogie-Petrologie Inst. für Geologische Wissenschaften FB Geowissenschaften Assistenz H-P. Nabein E. Petrishcheva J. Wanderer Zustandsformen
Magische Kristalle Prof. Dr. R. Glaum
 Magische Kristalle Prof. Dr. R. Glaum Institut für Anorganische Chemie Universität Bonn http://www.glaum.chemie.uni-bonn.de email: rglaum@uni-bonn.de Dank Herr Michael Kortmann Herr Andreas Valder Deutsche
Magische Kristalle Prof. Dr. R. Glaum Institut für Anorganische Chemie Universität Bonn http://www.glaum.chemie.uni-bonn.de email: rglaum@uni-bonn.de Dank Herr Michael Kortmann Herr Andreas Valder Deutsche
Vorlesung. Geomaterialien. 16. Stunde Halogenide und Elemente. Prof. Dr. F.E. Brenker
 Vorlesung Geomaterialien 16. Stunde Halogenide und Elemente Prof. Dr. F.E. Brenker Institut für Geowissenschaften FE Mineralogie JWG-Universität Frankfurt Halogenide Evaporitische Bildung Halit NaCl Sylvin
Vorlesung Geomaterialien 16. Stunde Halogenide und Elemente Prof. Dr. F.E. Brenker Institut für Geowissenschaften FE Mineralogie JWG-Universität Frankfurt Halogenide Evaporitische Bildung Halit NaCl Sylvin
LEHRBUCH DER MINERALOGIE
 LEHRBUCH DER MINERALOGIE Von Prof. em. Dr. rer. nat. habil. HANS JÜRGEN RÖSLER Bergakademie Freiberg 4., durchgesehene und erweiterte Auflage Mit 685 Bildern, 65 Tabellen und drei Beilagen VEB Deutscher
LEHRBUCH DER MINERALOGIE Von Prof. em. Dr. rer. nat. habil. HANS JÜRGEN RÖSLER Bergakademie Freiberg 4., durchgesehene und erweiterte Auflage Mit 685 Bildern, 65 Tabellen und drei Beilagen VEB Deutscher
2 Allgemeine Mineralogie
 2 Allgemeine Mineralogie 2.1 Einführung DieMineralogieisteinesehralteWissenschaft, denn seit Menschen versuchen, aus Steinen Werkzeuge, Farben oder Metalle zu gewinnen, beschäftigen sie sich mit Mineralien.
2 Allgemeine Mineralogie 2.1 Einführung DieMineralogieisteinesehralteWissenschaft, denn seit Menschen versuchen, aus Steinen Werkzeuge, Farben oder Metalle zu gewinnen, beschäftigen sie sich mit Mineralien.
Zweite Folie (Ziel der Einführung): Ziel der Einführung soll sein: Einführung in die Kristallmorphologie Klaus Schilling, Speyer
 Einführung in die Kristallmorphologie 2008-2018 Klaus Schilling, Speyer 1 Erste Folie (Titel): Die Präsentation zeigt keine wissenschaftliche Ausarbeitung. Es ist ein Versuch, dem Thema den Nimbus der
Einführung in die Kristallmorphologie 2008-2018 Klaus Schilling, Speyer 1 Erste Folie (Titel): Die Präsentation zeigt keine wissenschaftliche Ausarbeitung. Es ist ein Versuch, dem Thema den Nimbus der
Gibbssche Phasenregel und Einführung in Phasendiagramme F = C P + 2
 Petrologie der Magmatite und Metamorphite: Teil Metamorphite - Vorlesung 3 1/6 Gibbssche Phasenregel und Einführung in Phasendiagramme Bei Vorliegen eines thermodynamischen Gleichgewichts (thermodynamic
Petrologie der Magmatite und Metamorphite: Teil Metamorphite - Vorlesung 3 1/6 Gibbssche Phasenregel und Einführung in Phasendiagramme Bei Vorliegen eines thermodynamischen Gleichgewichts (thermodynamic
Kristallchemie. Atome Ionen Moleküle Chemische Bindungen
 Zirkon Kristallchemie Atome Ionen Moleküle Chemische Bindungen Bohr sches Atommodell Kernteilchen: p: Proton n: Neutron Elektronenhülle: e - Elektron Nukleus: Massenzahl A = p + n, Ordnungszahl Z = p =
Zirkon Kristallchemie Atome Ionen Moleküle Chemische Bindungen Bohr sches Atommodell Kernteilchen: p: Proton n: Neutron Elektronenhülle: e - Elektron Nukleus: Massenzahl A = p + n, Ordnungszahl Z = p =
k.com Vorlesung Geomaterialien 2. Doppelstunde Kristallographische Grundlagen Prof. Dr. F.E. Brenker
 k.com Vorlesung Geomaterialien 2. Doppelstunde Kristallographische Grundlagen Prof. Dr. F.E. Brenker Institut für Geowissenschaften FE Mineralogie JWG-Universität Frankfurt Netzebene Translation: Verschiebung,
k.com Vorlesung Geomaterialien 2. Doppelstunde Kristallographische Grundlagen Prof. Dr. F.E. Brenker Institut für Geowissenschaften FE Mineralogie JWG-Universität Frankfurt Netzebene Translation: Verschiebung,
Modifikationen einer polymorphen Substanz
 Zirkon Polymorphie Polymorphe Substanzen sind Elemente oder Verbindungen, die bei verschiedenen Druckund Temperaturbedingungen Festkörper mit unterschiedlichen Kristallstrukturen ausbilden. Beispiel SiO
Zirkon Polymorphie Polymorphe Substanzen sind Elemente oder Verbindungen, die bei verschiedenen Druckund Temperaturbedingungen Festkörper mit unterschiedlichen Kristallstrukturen ausbilden. Beispiel SiO
Freiwillige Übungsaufgaben zum Stoff vorangegangener Vorlesungen zur Selbstkontrolle für den 2. April 2008 (wird nicht bewertet)
 AC II - 2. April 2008 Übungen Anke Zürn Zusammenfassung & Wiederholung Dichteste Kugelpackungen (KP) Freiwillige Übungsaufgaben zum Stoff vorangegangener Vorlesungen zur Selbstkontrolle für den 2. April
AC II - 2. April 2008 Übungen Anke Zürn Zusammenfassung & Wiederholung Dichteste Kugelpackungen (KP) Freiwillige Übungsaufgaben zum Stoff vorangegangener Vorlesungen zur Selbstkontrolle für den 2. April
2. Mineralische Bestandteile der Böden
 BODENBESTANDTEILE 2. Mineralische Bestandteile der Böden S 9 Das Programm 1. Einführung BODENBESTANDTEILE 2. Mineralische Bodenbestandteile 3. Organische Bodenbestandteile BODENBILDUNG 4. Faktoren und
BODENBESTANDTEILE 2. Mineralische Bestandteile der Böden S 9 Das Programm 1. Einführung BODENBESTANDTEILE 2. Mineralische Bodenbestandteile 3. Organische Bodenbestandteile BODENBILDUNG 4. Faktoren und
Kristallstruktur und Mikrostruktur Teil I Vorlesung 2
 Kristallstruktur und Mikrostruktur Teil I Vorlesung 2 1 Kristallstruktur und Teil I Scripte Mikrostruktur http://www.uni-stuttgart.de/mawi/aktuelles_lehrangebot/lehrangebot.html 2 Wiederholung Koordinatensysteme
Kristallstruktur und Mikrostruktur Teil I Vorlesung 2 1 Kristallstruktur und Teil I Scripte Mikrostruktur http://www.uni-stuttgart.de/mawi/aktuelles_lehrangebot/lehrangebot.html 2 Wiederholung Koordinatensysteme
SOROSILIKATE - ÜBERBLICK
 Sorosilikate 1 SOROSILIKATE - ÜBERBLICK Silikatische Gruppenstrukturen; Verknüpfung von 2 SiO 4 -Tetraedern zu [Si 2 O 7 ] 6- -Gruppe Einige Vertreter Hemimorphit Zn 4 [Si 2 O 7 ] (OH) 2 *H 2 O, o.rhombisch;
Sorosilikate 1 SOROSILIKATE - ÜBERBLICK Silikatische Gruppenstrukturen; Verknüpfung von 2 SiO 4 -Tetraedern zu [Si 2 O 7 ] 6- -Gruppe Einige Vertreter Hemimorphit Zn 4 [Si 2 O 7 ] (OH) 2 *H 2 O, o.rhombisch;
A. N. Danilewsky 1. Inhalt des 1. Kapitels
 A. N. Danilewsky 1 Inhalt des 1. Kapitels 1 Vom Raumgitter zur Kristallstruktur... 2 1.1 Definition und Nomenklatur... 2 1.2 Gittergerade...4 1.3 Gitterebene...4 1.4 Raumgitter...5 1.5 Kristallsysteme...
A. N. Danilewsky 1 Inhalt des 1. Kapitels 1 Vom Raumgitter zur Kristallstruktur... 2 1.1 Definition und Nomenklatur... 2 1.2 Gittergerade...4 1.3 Gitterebene...4 1.4 Raumgitter...5 1.5 Kristallsysteme...
Einführung in die Kristallographie
 Einführung in die Kristallographie Gerhard Heide Institut für Mineralogie Professur für Allgemeine und Angewandte Mineralogie Brennhausgasse 14 03731-39-2665 oder -2628 gerhard.heide@mineral.tu-freiberg.de
Einführung in die Kristallographie Gerhard Heide Institut für Mineralogie Professur für Allgemeine und Angewandte Mineralogie Brennhausgasse 14 03731-39-2665 oder -2628 gerhard.heide@mineral.tu-freiberg.de
AC II Übung 3 Abgabe Mittwoch, 11. März 2009
 3.1 Rotes PbO a) Skizzieren Sie die idealisierte Struktur von PbO (rot) in perspektivischer Darstellung (eine Elementarzelle). Pb-Atome: weiss, O-Atome: orange. b) Geben Sie die Koordinationspolyeder und
3.1 Rotes PbO a) Skizzieren Sie die idealisierte Struktur von PbO (rot) in perspektivischer Darstellung (eine Elementarzelle). Pb-Atome: weiss, O-Atome: orange. b) Geben Sie die Koordinationspolyeder und
Inselsilikate (Nesosilikate)
 Almandin Fe 3 Al 2 [SiO 4 3 6 ½ - 7 ½ fehlend kubisch Kristallform Rhombendodekaeder {110} Metapelite, Granatglimmerschiefer Granatgruppe Grossular Ca 3 Al 2 [SiO 4 3 6 ½ - 7 ½ fehlend kubisch grünlich
Almandin Fe 3 Al 2 [SiO 4 3 6 ½ - 7 ½ fehlend kubisch Kristallform Rhombendodekaeder {110} Metapelite, Granatglimmerschiefer Granatgruppe Grossular Ca 3 Al 2 [SiO 4 3 6 ½ - 7 ½ fehlend kubisch grünlich
KRISTALLE. Franz Langsam BRG/BORG St. Pölten
 KRISTALLE Franz Langsam BRG/BORG St. Pölten Allgemeines Versuche Einteilung Beispiele Quellen Heuristische Annäherung an das Themengebiet Individuelle Analyse: Welcher dieser Stoffe ist kristallin? Bernstein
KRISTALLE Franz Langsam BRG/BORG St. Pölten Allgemeines Versuche Einteilung Beispiele Quellen Heuristische Annäherung an das Themengebiet Individuelle Analyse: Welcher dieser Stoffe ist kristallin? Bernstein
Silikat Strukturen. Klassifikationskriterium Polymerisierungsgrad der SiO 4 Tetraeder. [SiO 4 ] 4- Tetraeder
![Silikat Strukturen. Klassifikationskriterium Polymerisierungsgrad der SiO 4 Tetraeder. [SiO 4 ] 4- Tetraeder Silikat Strukturen. Klassifikationskriterium Polymerisierungsgrad der SiO 4 Tetraeder. [SiO 4 ] 4- Tetraeder](/thumbs/94/121633583.jpg) Zirkon Silikat Strukturen Klassifikationskriterium Polymerisierungsgrad der SiO 4 Tetraeder [SiO 4 ] 4- Tetraeder Silikat Strukturen Klassifikation nach Polymerisierungsgrad der SiO 4 Tetraeder [SiO 4
Zirkon Silikat Strukturen Klassifikationskriterium Polymerisierungsgrad der SiO 4 Tetraeder [SiO 4 ] 4- Tetraeder Silikat Strukturen Klassifikation nach Polymerisierungsgrad der SiO 4 Tetraeder [SiO 4
Helmut Schrecke Karl-Ludwig Weiner. Mineralogie. Ein Lehrbuch auf systematischer Grundlage W DE. Walter de Gruyter Berlin New York 1981
 Helmut Schrecke Karl-Ludwig Weiner Mineralogie Ein Lehrbuch auf systematischer Grundlage W DE G Walter de Gruyter Berlin New York 1981 Inhalt Einführung 1. Mineral, Kristall, Gestein 1 2. Einige Bemerkungen
Helmut Schrecke Karl-Ludwig Weiner Mineralogie Ein Lehrbuch auf systematischer Grundlage W DE G Walter de Gruyter Berlin New York 1981 Inhalt Einführung 1. Mineral, Kristall, Gestein 1 2. Einige Bemerkungen
Typisch metallische Eigenschaften:
 Typisch metallische Eigenschaften: hohe elektrische Leitfähigkeit hohe thermische Leitfähigkeit bei Energiezufuhr (Wärme, elektromagnetische Strahlung) können Elektronen emittiert werden metallischer Glanz
Typisch metallische Eigenschaften: hohe elektrische Leitfähigkeit hohe thermische Leitfähigkeit bei Energiezufuhr (Wärme, elektromagnetische Strahlung) können Elektronen emittiert werden metallischer Glanz
... Willkommen zum Schotterkurs!
 Übungen zur Lehrveranstaltung: Grundlagen der Geowissenschaften... Willkommen zum Schotterkurs! Petra Maissenbacher, TU Freiberg Die Folien (in Farbe & ungekürzt) sind auch zu finden unter: Die Folien
Übungen zur Lehrveranstaltung: Grundlagen der Geowissenschaften... Willkommen zum Schotterkurs! Petra Maissenbacher, TU Freiberg Die Folien (in Farbe & ungekürzt) sind auch zu finden unter: Die Folien
Anorganische Chemie III - Festkörperchemie
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Wiederholung
Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Wiederholung
Zeolithe Minerale mit außergewöhnlichen Fähigkeiten
 Zeolithe Minerale mit außergewöhnlichen Fähigkeiten Inhaltsverzeichnis 1 Mineralogie als Wissenschaft 1 2 Der atomare Aufbau von Kristallen 2 2.1 Chemische Bindung.....................................
Zeolithe Minerale mit außergewöhnlichen Fähigkeiten Inhaltsverzeichnis 1 Mineralogie als Wissenschaft 1 2 Der atomare Aufbau von Kristallen 2 2.1 Chemische Bindung.....................................
Kristallstruktur und Mikrostruktur Teil I Vorlesung 2
 Kristallstruktur und Mikrostruktur Teil I Vorlesung 2 1 Kristallstruktur und Teil I Scripte Mikrostruktur http://www.uni-stuttgart.de/mawi/aktuelles_lehrangebot/lehrangebot.html 2 Wiederholung Koordinatensysteme
Kristallstruktur und Mikrostruktur Teil I Vorlesung 2 1 Kristallstruktur und Teil I Scripte Mikrostruktur http://www.uni-stuttgart.de/mawi/aktuelles_lehrangebot/lehrangebot.html 2 Wiederholung Koordinatensysteme
Generelle Definition. Kristallklassen im kubischen Kristallsystem. Kristallformen im kubischen Kristallsystem
 Generelle Definition Seite 1 von Alle Kristalle des kubischen Systems lassen sich auf ein Achsenkreuz beziehen mit drei senkrecht aufeinanderstehenden Achsen und gleichlangen Achsenabschnitten. Also: Alpha
Generelle Definition Seite 1 von Alle Kristalle des kubischen Systems lassen sich auf ein Achsenkreuz beziehen mit drei senkrecht aufeinanderstehenden Achsen und gleichlangen Achsenabschnitten. Also: Alpha
Physik 4: Skalen und Strukturen
 Physik 4: Skalen und Strukturen Kapitel : Festkörperphysik.1 Aggregatszustände. Kristallstrukturen.3 Chemische Bindung.4 Gitterschwingungen.5 Elektronen im Festkörper Phasendiagramm von CO Klassisches
Physik 4: Skalen und Strukturen Kapitel : Festkörperphysik.1 Aggregatszustände. Kristallstrukturen.3 Chemische Bindung.4 Gitterschwingungen.5 Elektronen im Festkörper Phasendiagramm von CO Klassisches
Nachbesprechung. Übung 3
 Nachbesprechung Übung 3 Form (a) Pinakoid, (b) allgemeine Fläche (Pfeil) wird durch eine Spiegelebene in ein Doma überführt, (c) Sphenoid (Pfeil), generiert durch die Wirkung einer 2-zähligen Achse, (d)
Nachbesprechung Übung 3 Form (a) Pinakoid, (b) allgemeine Fläche (Pfeil) wird durch eine Spiegelebene in ein Doma überführt, (c) Sphenoid (Pfeil), generiert durch die Wirkung einer 2-zähligen Achse, (d)
Marta Kubiak & Ewelina Kuczera
 Marta Kubiak & Marta Kubiak & Ewelina Kuczera Was ist Keramik und Porzellan Geschichte Einteilung der Keramik : Grobkeramik Feinkeramik Rohstoffe zur Silikatkeramikherstellung Silikate Verfahrensschritte
Marta Kubiak & Marta Kubiak & Ewelina Kuczera Was ist Keramik und Porzellan Geschichte Einteilung der Keramik : Grobkeramik Feinkeramik Rohstoffe zur Silikatkeramikherstellung Silikate Verfahrensschritte
Hier: Beschränkung auf die elektrische Eigenschaften
 IV. Festkörperphysik Hier: Beschränkung auf die elektrische Eigenschaften 3 Aggregatzustände: fest, flüssig, gasförmig: Wechselspiel Anziehungskräfte der Teilchen gegen die thermische Energie kt. Zustand
IV. Festkörperphysik Hier: Beschränkung auf die elektrische Eigenschaften 3 Aggregatzustände: fest, flüssig, gasförmig: Wechselspiel Anziehungskräfte der Teilchen gegen die thermische Energie kt. Zustand
LV Mikroskopie I Kurs 7 1/7. Calcische-Amphibole (Ca >Na): Tremolit-Ferroaktinolit-Reihe, Hornblende, Kärsutit etc.
 LV 620.108 Mikroskopie I Kurs 7 1/7 Amphibole Inosilikate (Bandsilikate; abgeleitet von der [Si 4 O 11 -Doppelkette]. Es lassen sich zahlreiche Mischungsreihen unterscheiden. Allgemeine Formel der Amphibole
LV 620.108 Mikroskopie I Kurs 7 1/7 Amphibole Inosilikate (Bandsilikate; abgeleitet von der [Si 4 O 11 -Doppelkette]. Es lassen sich zahlreiche Mischungsreihen unterscheiden. Allgemeine Formel der Amphibole
ANORGANISCHE GLASCHEMIE
 ANORGANISCHE GLASCHEMIE Fabian Immink, Thomas Seidel, Manuel Westbomke 18.05.2012 GLIEDERUNG Was ist Glas? Eigenschaften Glassorten Färbung von Gläsern Einsatzgebiete von Glas Herstellungsprozess Zahlen
ANORGANISCHE GLASCHEMIE Fabian Immink, Thomas Seidel, Manuel Westbomke 18.05.2012 GLIEDERUNG Was ist Glas? Eigenschaften Glassorten Färbung von Gläsern Einsatzgebiete von Glas Herstellungsprozess Zahlen
Übungen zur Allgemeinen Geologie, Nebenfach
 zur Allgemeinen Geologie, Nebenfach Erta Ale, Afrika Übungstermine und Themen Termine Einführungsstunde Übung 26.10.2010 Einführung + Mineral- Eigenschaften Gruppeneinteilung 02.11. 2010 Minerale 1 Eigenschaften
zur Allgemeinen Geologie, Nebenfach Erta Ale, Afrika Übungstermine und Themen Termine Einführungsstunde Übung 26.10.2010 Einführung + Mineral- Eigenschaften Gruppeneinteilung 02.11. 2010 Minerale 1 Eigenschaften
Gesteinskunde. Skript für die Übungen zur Dynamik der Erde
 Gesteinskunde Skript für die Übungen zur Dynamik der Erde Martina Kölbl-Ebert (1994) 2. ergänzte Auflage von Franz Moser (1999) 3. Auflage von Joachim Kuhlemann und Wolfgang Frisch (2002) 4. überarbeitete
Gesteinskunde Skript für die Übungen zur Dynamik der Erde Martina Kölbl-Ebert (1994) 2. ergänzte Auflage von Franz Moser (1999) 3. Auflage von Joachim Kuhlemann und Wolfgang Frisch (2002) 4. überarbeitete
Edelsteinkunde. Zweijährige Berufsfachschule für Goldschmiede. Schuljahr 1 und 2. Landesinstitut für Erziehung und Unterricht Abteilung III
 Zweijährige Berufsfachschule für Goldschmiede Schuljahr 1 und 2 152 Vorbemerkungen Im Fach befassen sich die Schüler mit den Grundlagen der Mineralogie und der Petrographie, den daraus resultierenden Eigenschaften
Zweijährige Berufsfachschule für Goldschmiede Schuljahr 1 und 2 152 Vorbemerkungen Im Fach befassen sich die Schüler mit den Grundlagen der Mineralogie und der Petrographie, den daraus resultierenden Eigenschaften
Rohstoffe (stark vereinfachte Übersicht)
 Rohstoffe (stark vereinfachte Übersicht) Rohstoffe (primär) = natürliche Ressourcen, die (abgesehen vom Herauslösen aus ihrer natürlichen Quelle) noch keine Bearbeitung erfahren haben Rohstoffe (sekundär)
Rohstoffe (stark vereinfachte Übersicht) Rohstoffe (primär) = natürliche Ressourcen, die (abgesehen vom Herauslösen aus ihrer natürlichen Quelle) noch keine Bearbeitung erfahren haben Rohstoffe (sekundär)
Strukturr. Cs Cl. Na Cl. Zn S. Struktur. Koordinationn [ : ] 21 / 44
![Strukturr. Cs Cl. Na Cl. Zn S. Struktur. Koordinationn [ : ] 21 / 44 Strukturr. Cs Cl. Na Cl. Zn S. Struktur. Koordinationn [ : ] 21 / 44](/thumbs/94/121643787.jpg) 2.2. 7 2.2. 7.1 Beispiele AX-Systeme Cs Cl Strukturr Koordination [ : ] Basis: Na Cl Struktur Koordination [ : ] Basis: Zn S Strukturr Koordinationn [ : ] Basis: Koordinationn [ : ] Basis: 21 / 44 2.2.
2.2. 7 2.2. 7.1 Beispiele AX-Systeme Cs Cl Strukturr Koordination [ : ] Basis: Na Cl Struktur Koordination [ : ] Basis: Zn S Strukturr Koordinationn [ : ] Basis: Koordinationn [ : ] Basis: 21 / 44 2.2.
Übungen zur Mineral- und Gesteinsbestimmung
 Übungen zur Mineral- und Gesteinsbestimmung für Studierende der Geologie und der Mineralogie Schriftgranit aus Südnorwegen H.-G. Stosch 1, R. Hollerbach 2, J.-D. Eckhardt 1 und R. Kleinschrodt 2 1 Institut
Übungen zur Mineral- und Gesteinsbestimmung für Studierende der Geologie und der Mineralogie Schriftgranit aus Südnorwegen H.-G. Stosch 1, R. Hollerbach 2, J.-D. Eckhardt 1 und R. Kleinschrodt 2 1 Institut
Systematik Geowissenschaften: Reduzierte Fassung
 Systematik Geowissenschaften: Reduzierte Fassung (modifizierte Fassung; Stand: 7/2006) ALLG 0 ALLGEMEINES GEOL 1 GEOL 10 GEOL 10.100 GEOL 10.102 GEOL 10.103 GEOL 10.104 GEOL 10.105 GEOL 10.106 GEOL 10.107
Systematik Geowissenschaften: Reduzierte Fassung (modifizierte Fassung; Stand: 7/2006) ALLG 0 ALLGEMEINES GEOL 1 GEOL 10 GEOL 10.100 GEOL 10.102 GEOL 10.103 GEOL 10.104 GEOL 10.105 GEOL 10.106 GEOL 10.107
Anorganische Chemie III - Festkörperchemie
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Wiederholung
Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Wiederholung
Medizinische Biophysik
 4. Flüssiger Aggregatzustand Medizinische Biophysik a) Makroskopische Beschreibung b) Mikroskopische Beschreibung c) Oberflächenspannung Struktur der Materie Aggregatzustände: Gase, Flüssigkeiten, feste
4. Flüssiger Aggregatzustand Medizinische Biophysik a) Makroskopische Beschreibung b) Mikroskopische Beschreibung c) Oberflächenspannung Struktur der Materie Aggregatzustände: Gase, Flüssigkeiten, feste
Vorlesung. Geomaterialien. 8. Stunde Gruppen- und Ringsilikate
 Vorlesung Geomaterialien 8. Stunde Gruppen- und Ringsilikate Prof. Dr. Frank E. Brenker Institut für Geowissenschaften FE Mineralogie JWG-Universität Frankfurt Gruppensilikate Sorosilikate Die wichtigsten
Vorlesung Geomaterialien 8. Stunde Gruppen- und Ringsilikate Prof. Dr. Frank E. Brenker Institut für Geowissenschaften FE Mineralogie JWG-Universität Frankfurt Gruppensilikate Sorosilikate Die wichtigsten
M. W. Tausch. 3.Teil Ionenbindung
 Ionenbildung bei der NaCl-Synthese Energie als Funktion des Ionenabstands Gitterenergie Born-Haber Kreisprozess Gitterenergie und Gittergeometrie Koordinationszahlen Dichteste Kugelpackungen Elementarzellen
Ionenbildung bei der NaCl-Synthese Energie als Funktion des Ionenabstands Gitterenergie Born-Haber Kreisprozess Gitterenergie und Gittergeometrie Koordinationszahlen Dichteste Kugelpackungen Elementarzellen
