EudraCT-Nr.: Protokoll-Nr.: D-V
|
|
|
- Alexander Kolbe
- vor 5 Jahren
- Abrufe
Transkript
1 EudraCT-Nr.: Protokoll-Nr.: D-V Studientitel Eine multizentrische, randomisierte Phase III-Studie zum Vergleich einer Chemo- versus einer endokrinen Behandlung in Kombination mit einer dualen HER2-gerichteten Herceptin (Trastuzumab)/ Perjeta (Pertuzumab)-Therapie plus Kisqali (Ribociclib) bei Patientinnen mit HER2-positivem und hormonrezeptorpositivem metastasiertem Brustkrebs. Sponsor Universitätsklinikum Ulm, Prof. Dr. Wolfgang Janni Leiter der klinischen Prüfung Prof. Dr. Jens Huober, Universitätsklinikum Ulm Studiendesign Prospektive, offene, multizentrische, randomisierte klinische Phase IIIa-Studie FDA covered study ja nein Prüfzentren Bis zu 120 Prüfzentren deutschlandweit Start Studieneinschluss: Q3 / 2015 Ende Studieneinschluss: Q2 / 2020 Geplante Studiendauer Rationale der Studie Studienbehandlungssdauer: 12 Monate Ende Behandlungsperiode: Q2/ 2021 Follow-up Dauer: 24 Monate Ende Follow-up Periode: Q2 / 2023 Primärer Studienendpunkt (vor Inkrafttreten des Amendments): Das primäre Zielkriterium dieser Studie ist, die Verträglichkeit der dualen HER2-gerichteten Therapie (Trastuzumab plus Pertuzumab) in Kombination mit einer endokrinen Therapie versus der dualen HER2-gerichteten Therapie in Kombination mit einer Chemotherapie bei Patientinnen mit HER2-positivem, hormon-rezeptor positivem metastasiertem Brustkrebs zu evaluieren. Sicherheit/Verträglichkeit wird über den Anteil an Patientinnen mit unerwünschten Ereignissen (adverse events) während des Behandlungszeitraums definiert (Definition nach dem modifizierten adverse event score ). Der modifizierte adverse event score beinhaltet alle unerwünschten Ereignisse mit Grad 3 oder höher, mit der Ausnahme von Neutropenie, welche nur bei Grad 4 gewertet wird, und Haarausfall, Hautausschlag, periphere Neuropathie sowie Hand-Fuß-Syndrom, welche schon ab Grad 2 gewertet werden.
2 Neuer primärer Studienendpunkt: Mit Inkrafttreten des Amendments bekommen neu eingeschlossene Patientinnen in beiden Randomisierungsarmen zusätzlich den CDK4/6 Inhibitor Kisquali (Ribociclib). Daher wird als neues primäres Studienziel die Verträglichkeit der dualen HER2-gerichteten Therapie (Trastuzumab plus Pertuzumab) in Kombination mit Ribociclib und endokriner Therapie versus der dualen HER2-gerichteten Therapie in Kombination mit einer Chemotherapie (gefolgt von einer Erhaltungstherapie mit Trastuzumab und Pertuzumab plus Ribociclib und endokrine Therapie) verglichen. Sicherheit/Verträglichkeit wird über die Anzahl an unerwünschten Ereignissen (adverse events) während des Behandlungs-zeitraums definiert (Definition nach dem modifizierten adverse event score ; siehe oben). Sekundäre Hauptendpunkte: Vergleich der Verträglichkeit der dualen HER2-gerichteten Therapie (Trastuzumab plus Pertuzumab) in Kombination mit einer endokrinen Therapie versus der dualen HER2-gerichteten Therapie in Kombination mit einer Chemotherapie bei Patientinnen, die vor Inkrafttreten des Amendments in die Studie eingeschlossen wurden (diese Patientinnen haben kein Ribociclib im Rahmen ihrer Studienbehandlung erhalten). Sicherheit/Verträglichkeit wird über die Anzahl an unerwünschten Ereignissen (adverse events) während des Behandlungszeitraums definiert (Definition nach dem modifizierten adverse event score ; siehe oben). Vergleich der Verträglichkeit der dualen HER2-gerichteten Therapie (Trastuzumab plus Pertuzumab) in Kombination mit einer endokrinen Therapie versus der dualen HER2-gerichteten Therapie in Kombination mit einer Chemotherapie bei allen in die Studie eingeschlossenen Patientinnen (unabhängig davon, ob sie vor oder nach Inkrafttreten des Amendments eingeschlossenwurden). Sicherheit/Verträglichkeit wird über die Anzahl an unerwünschten Ereignissen (adverse events) während des Behandlungszeitraums definiert (Definition nach dem modifizierten adverse event score ; siehe oben). Weitere sekundäre Endpunkte: Vergleich der Verträglichkeit der dualen HER2-gerichteten Therapie (Trastuzumab plus Pertuzumab) in Kombination mit Ribociclib und endokriner Therapie versus der dualen HER2-gerichteten Therapie in Kombination mit einer Chemotherapie
3 Geplante Patientenzahl Patientenauswahl Behandlungschema Dosierung und (gefolgt von einer Erhaltungstherapie mit Trastuzumab und Pertuzumab plus Ribociclib und endokrine Therapie), wobei Sicherheit/Verträglichkeit anhand eines speziellen adverse event score evaluiert wird, der zusätzlich zu den im modifizierten adverse event score beinhalteten unerwünschten Ereignissen (siehe oben) auch Übelkeit, Erbrechen, Durchfall und Stomatitis ab Grad 2 beinhaltet. Bestimmung des quality-adjusted survival (Auswertung nach der Q-TWiST Methode) und der Unterschied des quality-adjusted survival im Vergleich zwischen den Behandlungsarmen Unterschiede zwischen den Behandlungsarmen hinsichtlich der Allgemeinen Ansprechrate (ORR), der klinischen Erfolgsrate (DCR), des Progressionsfreien Überlebens (PFS) und des Gesamtüberlebens (OS) entsprechend den RECIST Leitlinien Version 1.1., basierend auf lokaler Beurteilung. Beurteilung der Inzidenz von ZNS-Metastasen, mittels CT oder vorzugsweise MRT entsprechend den RECIST Leitlinien Version 1.1., basierend auf lokaler Beurteilung. Weitere Beurteilung zusätzlicher Lebensqualitätsaspekte auf Basis der EORTC QLQ-C30 und EORTC QLQ-BR23 Fragebögen Vorkommen und Anzahl der CTCs im peripheren Blut vor Behandlungsbeginn, 6 Wochen nach Randomisierung, und nach der 12-monatigen Studienbehandlungsdauer oder bei Progress (falls dieser vor Ende der 12-monatigen Studienbehandlungsdauer eintritt) zur Evaluierung der Aussagekraft der CTCs hinsichtlich des Therapieansprechens/- erfolgs. Bestimmung des endocrine responsiveness score (ERS) der CTCs vor Behandlungsbeginn, 6 Wochen nach Randomisierung, und nach der 12-monatigen Studienbehandlungsdauer oder bei Progress (falls dieser vor Ende der 12-monatigen Studienbehandlungsdauer eintritt) zur Evaluierung der Aussagekraft der ERS hinsichtlich des Therapieansprechens/- erfolgs Toxizitätsanalyse und Vergleich der Toxizität beider Behandlungsarme Evaluation der Sicherheit und Verträglichkeit der Studienmedikation Insgesamt 270 Patientinnen Einschlusskriterien: Patientinnen können nur eingeschlossen werden, wenn alle der folgenden Kriterien erfüllt werden: Schriftliches Einverständnis zur Studienteilnahme Bestimmung des HER2-Status des primären
4 Mammakarzinoms und/oder einer Metastase mit HER2-Positivität der Gewebsproben, d.h. Immunhistochmie 3+ oder Fluoreszenz in situ Hybridisierung (FISH) positiv sowie histopathologisch bestätigter Hormonrezeptorpositivität Metastasiertes Mammakarzinom, das einer Operation oder Strahlentherapie alleine nicht zugänglich ist Nicht mehr als 2 vorrangegangenen Chemotherapielinien in der metastasierten Situation Prä- oder postmenapausaler Status Mindestens eine nach RECIST auswertbare metastatische Läsion, entsprechend den RECIST Leitlinien Version 1.1., basierend auf lokaler Beuerteilung. Tumorevaluation nach RECIST Version 1.1 innerhalb von 4 Wochen vor Studienrandomisierung Alter 18 Jahre 12-Kanal-EKG: -QTcF Interval bei der Einschlussvisite < 450 msec -Ruheherzfrequenz s/min Echokardiografischer Nachweis einer linksventrikulären Ejaktionsfraktion (LVEF) 50% zu Studienbeginn ECOG Score 2 Adäquate Knochenmarksreserve und Organfunktion 14 Tage vor dem Zeitpunkt der Rekrutierung, durch folgende Laborparameter bestätigt: - Absolute Neutrophile 1500/µL, - Thrombozyten /µL, - Hämoglobin 9 g/dl, - ALT (SGPT) 2.0 ULN ( 3.0 ULN bei Lebermetastasierung) - AST (SGOT) 2.0 ULN ( 3.0 ULN bei Lebermetastasierung) - Bilirubin (gesamt) 1.5 ULN (Ausnahme Gilbert s Syndrom) - Kreatinin 2.0 mg/dl oder 177µmol/L - INR 1,5 Unauffällige Laborwerte für: Natrium, Kalium, Kalzium (Ribociclib-Therapie) Bei Patientinnen im gebärfähigen Alter gilt: Negativer Schwangerschaftstest innerhalb von 7 Tagen vor Randomisierung und sichere Kontrazeption (d.h. einfache oder kombinierte nicht-hormonelle Kontrazeption mit einer Versagerquote < 1% oder komplette sexuelle Abstinenz) während der Behandlungsdauer bis einschließlich 7 Monate nach Einnahmeende der Studienmedikation.
5 Ausschlusskriterien: Patientinnen können nicht in die Studie eingeschlossen werden, wenn einer der folgenden Punkte zutrifft: Anamnestisch bekannte Überempfindlichkeit gegenüber Trastuzumab, Pertuzumab oder Ribociclib oder chemisch verwandten Bestandteilen bzw. weiteren Bestandteilen der Medikation Vortherapie mit mtor- oder CDK4/6-Inhibotoren. Zwingende Indikation zur Durchführung einer Chemotherapie Polyneuropathie (PNP) 2 für Taxantherapie ZNS Metastasen Vorliegen von Erkrankungen oder besonderen sozialen oder psychiatrischen Bedingung, die die adäquate Einschätzung oder Evaluation der Studiendaten gefährden oder die Einhaltung des Studienprotokolls stören oder nach Ansicht des behandelnden Arztes zu einer unverhältnismäßigen Gefährdung der Patientin bei Studienteilnahme führen würde Progress unter Pertuzumab Therapie Behandlung mit Pertuzumab innerhalb der letzten 12 Monate Behandlung mit anderen Prüfsubstanzen während der Studie Unverträglichkeit gegen Soyalecithin und Erdnüsse Lebenserwartung < 6 Monate Manifeste kardiale Vorerkrankungen, einschließlich: Symptomatische Herzinsuffizenz oder LVEF < 50 % Therapiebedürftige oder klinisch relevante Arrhythmien, z.b. Vorhoftachykardien mit einem Ruhepuls 100/min, relevante ventrikuläre Arrhythmien (ventrikuläre Tachykardie), höhergradiger AV-Block (2 AV-Block Typ 2 [Mobitz 2] oder 3 AV-Block) behandlungsbedürftige Angina Pectoris klinisch relevante Herzklappenerkrankungen Nachweis einer transmuralen Infarzierung im EKG schlecht kontrollierte art. Hypertonie (z.b. systolisch >180 mm Hg oder diastolisch >100 mm Hg) jede andere kardiale Begleiterkrankung, die nach Ansicht des behandelnden Arztes zu einer unverhältnismäßigen Gefährdung der Patientin bei Studienteilnahme führen würde Ruhedyspnoe oder andere Erkrankungen, die eine kontinuierliche Sauerstofftherapie erfordern Schlecht eingestellter Diabetes mellitus oder Nachweis
6 einer klinisch relevanten diabetischen Vaskulopathie Bekannte HIV-, Hepatitis B- oder Hepatitis C-Erkrankung Männlicher Patient Schwangerschaft oder Stillzeit sowie gebärfähige Patientinnen ohne negativen Schwangerschaftstest in den letzten 7 Tagen vor Studienrandomisierung oder mit unsicheren Verhütungsmethoden Medizinische oder psychologische Gegebenheiten, die das Verständnis oder die Wiedergabe der informierten Einwilligung verhindern oder die Beendigung der Studie stören. Teilnahme an einer anderen klinischen Studien innerhalb der letzten 30 Tage vor Studienregistration Vollständige oder teilweise Geschäftsunfähigkeit
7 Behandlung: Patientinnen werden abhängig von der Randomisierung mit Trastuzumab/ Pertuzumab und Chemotherapie oder Trastuzumab/ Pertuzumab (plus Ribociclib nach Inkrafttreten des Amendments) und endokriner Therapie behandelt. Ein Wechsel von Chemotherapie zu endokriner Therapie oder umgekehrt ist nicht erlaubt. Ein Wechsel der Medikation auch innerhalb der Behandlungsarme ist nicht möglich. Drei Wochen nach Abschluss der Chemotherapie soll mit endokriner Therapie begonnen werden. Spätenstens sechs Wochen nach Abschluss der Chemotherapie, bei guten Laborwerten und unauffälligem EKG, werden die Patientinnen mit einer endokrinen Erhaltungstherapie (plus Ribociclib nach Inkrafttreten des Amendments) behandelt. Trastuzumab/ Pertuzumab muss vor der Chemotherapie intravenös verabreicht werden. Empfohlene Dosierung für Pertuzumab: Initiale Dosis: 840 mg Pertuzumab als intravenöse Infusion über 60 Minuten, d1; für die nachfolgenden Infusionen: 420 mg Pertuzumab als intravenöse Infusion über Minuten, q3w Empfohlene Dosierung für Trastuzumab: Initiale Dosis: 8 mg/kg Körpergewicht Trastuzumab als intravenöse Infusion über 90 Minuten, d1; für die nachfolgenden Infusionen: 6 mg/kg Körpergewicht Trastuzumab als intravenöse Infusion über 30 Minuten, q3w Empfohlene Dosierung für Ribociclib: Ribociclib wird in Form vontabletten 3 x 200 mg 1-21 d q28d verabreicht. Empfohlene Dosierung für Chemo- oder endokrine Therapie
8 Chemotherapie Docetaxel Empfohlene Dosierung 75 mg/m 2 i.v. d1 q3w Paclitaxel Zwei Chemotherapieregimen sind möglich: 90 mg/m 2 i.v. d1, 8, 15 q4w oder 80 mg/m 2 i.v. d1, 8, 15, 22 q4w; Behandlungsdauer mit Paclitaxel im Ermessen des behandelnden Prüfarztes, jedoch empfohlene Mindesttherapiedauer 4 Monate oder bis inakzeptabler Toxizität oder Krankheitsprogression Capecitabine 2 x 1000 mg/m 2 p.o. d1-14 q3w; Behandlungsdauer mit Capecitabine im Ermessen des behandelnden Prüfarztes. Mindesttherapiedauer 4 Monate oder bis inakzeptabler Toxizität oder Krankheitsprogression. Vinorelbine 30 mg/m 2 i.v.. d1+d8 q3w; Behandlungsdauer mit Vinorelbine im Ermessen des behandelnden Prüfarztes, jedoch Mindesttherapiedauer 4 Monate oder bis inakzeptabler Toxizität oder Krankheitsprogression nab-paclitaxel 125 mg/m² d1, 8, 15 q4w; Behandlungsdauer mit Nab-Paclitaxel im Ermessen des behandelnden Prüfarztes, jedoch Mindesttherapiedauer 4 Monate oder bis inakzeptabler Toxizität oder Krankheitsprogression Eribulin 1,23 mg/m² i.v. d1, 8 q3w, Behandlungsdauer mit Eribulin im Ermessen des behandelnden Prüfarztes. Mindesttherapiedauer 4 Monate oder bis inakzeptabler Toxizität oder Krankheitsprogression endokrine Therapie Exemestan Letrozol Anastrozol Fulvestrant Leuprorelin Goserelin Empfohlene Dosierung 25 mg/d p.o. 2,5 mg/d p.o. 1 mg/d p.o. 500 mg i.m. d , dann q28d 3,75 mg 1 M Depot s.c. q4w, 11,25 mg 3 M Depot s.c. 3,6 mg s.c. q4w
9 Dauer der Studienbehandlung: Abhängig vom gewählten Präparat und dem gewählten Behandlungschema Abhängig von Tumorprogress, unerwünschter Toxizität sowie weiteren Situationen, die einen Therapieabbruch erfordern Für Chemotherapie wird eine Mindestdauer von 4 Monaten empfohlen (soweit es nicht medizinische Gründe für einen vorzeitigen Abbruch der Behandlung gibt). Drei Wochen nach Abschluss der Chemotherapie soll mit endokriner Therapie begonnen werden. Spätestens sechs Wochen nach Abschluss der Chemotherapie, bei guten Laborwerten und unauffälligem EKG, werden die Patientinnen mit einer endokrinen Erhaltungstherapie (plus Ribociclib nach Inkrafttreten des Amendments) behandelt. Begrenzt auf die 12-monatige Studienbehandlungsperiode; eine Verlängerung der Behandlung über die Dauer der Studienbehandlungsperiode hinaus ist bei medizinischer Indikation für alle Therapien möglich Behandlung in der Follow-Up-Phase: Die Therapie in der Follow-Up-Phase, d.h. nach Abschluss der Studientherapie erfolgt gemäß den Empfehlungen des Prüfarztes. Alle in der Studienbehandlungsperiode gegebenen Therapien können bei medizinischer Indikation unbegrenzt verlängert werden. Die Studienmedikation wird bis zum Ende der Follow-Up-Phase gestellt.
10 Patientinnenkollektive Intention to Treat (ITT) Kollektiv: Alle randomisierten Patientinnen. Tolerability Kollektiv: Alle randomisierten Patientinnen, welche die Studienmedikation mindestens einmal erhalten haben und für die mindestens eine Sicherheitsauswertung nach Studienbeginn durchgeführt wurde. Per Protocol (PP) Kollektiv: Alle Patientinnen des ITT-Kollektivs, welche weder Ein- noch Ausschlusskriterien verletzt haben und welche nach Studienplan behandelt wurden. Falls notwendig, können modifizierte oder zusätzliche Patientinnenkollektive für weitere spezifische Auswertungen in einem Statistical Analysis Plan (SAP) definiert werden. Patientinnenkollektive, statistische Methoden und Fallzahlberechnung Statistische Methoden In der konfirmatorischen Primäranalyse (sowie den explorativen Analysen zu den beiden sekundären Hauptendpunkten) wird der Anteil an Patientinnen mit während der Behandlungsphase aufgetretenen unerwünschten Ereignissen (definiert nach dem modifizierten adverse event score ) zwischen beiden Behandlungsarmen mit einem χ 2 Test verglichen, wobei die relativen Risiken, das relative Risikoverhältnis sowie die entsprechenden 95% Vertrauens-bereiche berichtet werden. Zusätzlich werden in explorativen Analysen die Vergleiche der Anteile an Patientinnen mit während der Behandlungsphase aufgetretenen unerwünschten Ereignissen zwischen beiden Behandlungsarmen auch für die durch die Stratifizierungsfaktoren vorgegebenen Subgruppen (mit vs. ohne viszerale Metastasen; erste vs. höhere Chemotherapie-Linie; mit vs. ohne vorangegangener Trastuzumabbehandlung; mit vs. ohne vorangegangener Pertuzumabbehandlung) durchgeführt. Für die konfirmatorische Primäranalyse werden alle Patientinnen eingeschlossen, welche nach Inkrafttreten des Amendments (d.h. nach der Hinzunahme von Ribociclib in beide Studienarme) randomisiert worden sind (siehe Rationale der Studie). Entsprechend der zwei sekundären Hauptendpunkte (siehe Rationale der Studie) wird diese Analyse auch für Patientinnen, die vor Inkrafttreten des Amendments in die Studie eingeschlossen worden sind (d.h., Patientinnen, welche kein Ribociclib im Rahmen ihrer Studienbehandlung erhalten haben) und für alle in die Studie eingeschlossenen Patientinnen
11 (unabhängig davon, ob sie vor oder nach Inkrafttreten des Amendments eingeschlossen wurden; ITT und/oder Safety-Kollektiv) durchgeführt. Alle statistischen Analysen welche die sekundären Studienziele betreffen haben nur explorativen Charakter und werden sowohl mit dem gesamten Safety bzw. ITT Kollektiv als auch mit den Subkollektiven der Patientinnen mit und ohne zusätzliche Ribociclib-Behandlung durchgeführt. Der sekundäre Endpunkt qualitäts-adjustiertes Überleben (quality-adjusted survival, QAS) wird mittels der Q-TWiST-Methode (quality-adjusted time without symptoms and toxicity) analysiert (siehe Goldhirsch et al. 1989; Glasziou et al. 1990; Gelber et al. 1993). Alle auf Häufigkeiten bzw. Raten basierenden sekundären Endpunkte und Parameter (ORR, DCR, CR, PR, SD) werden mit Hilfe von absoluten und relativen Häufigkeiten in Häufigkeitstabellen sowie den entsprechenden Vertrauens-intervallen beschrieben. Die entsprechenden Gruppenvergleiche werden mittels geeigneter nicht-parametrischer statistischer Verfahren wie Fisher s exakter Test, χ 2 -Test, oder Cochran-Mantel-Haenszel Test durchgeführt. Progressionsfreies und Gesamtüberleben werden mit der Kaplan Meier Product Limit Methode bestimmt und anhand von Medianen, 95% Vertrauensintervallen und Überlebenskurven beschrieben bzw. dargestellt; Gruppenvergleiche werden mit dem Log-Rank Test durchgeführt. Für multivariate Überlebensanalysen werden geeignete Regressionsmodelle verwendet (z.b. Cox-Regression, logistische Regression). Vorhandensein und Anzahl zirkulierender Tumorzellen (circulating tumor cells, CTCs) an verschiedenen Zeitpunkten werden beschreibend dargestellt, und die Änderung der Anzahl CTCs über die Zeit wird mit geeigneten linearen Modellen (z.b. Generalized linear mixed models) untersucht. Zusätzlich sollen verschiedene Maße der CTC Dynamik (basierend auf verschiedenen Schwellenwertkritierien; relative oder absolute Änderungen der CTC-Anzahl) explorativ auf ihre Eignung als prognostische oder prediktive Marker evaluiert werden. Mehr Details zur den statistischen Auswertemethoden werden in einem Statistical Analysis Plan (SAP) dargestellt, welcher vor dem Data Base Lock finalisiert wird. Soweit nicht anders angegeben, werden alle statistischen Analysen mit dem Statistikprogramm IBM SPSS Statistics durchgeführt.
12 Fallzahlberechnung DETECT V/CHEVENDO ist angelegt als eine zweiarmige, randomisierte Phase III Überlegenheitsstudie. Das primäre Studienziel ist der Vergleich des Anteils an Patientinnen mit unerwünschten Ereignissen (definiert nach dem modifizierten adverse event score ; evaluiert basierend auf NCI CTCAE Version 4.03) zwischen dem Behandlungsarm mit dualer HER2 gerichteter Therapie plus Chemotherapie und dem Behandlungsarm mit dualer HER2 gerichteter Therapie plus endokriner Therapie (χ 2 Test). Die Fallzahlberechnungen basieren auf der Annahme, dass für Patientinnen mit HER2-positivem metastasiertem Brustkrebs, die mit einer dualen HER2-zielgerichteten Therapie plus Chemotherapie behandelt werden, der Anteil an nach dem modifizierten adverse event score definierten unerwünschten Ereignissen 86.3% beträgt (Ergebnisse der CLEOPATRA-Studie, Daten von Roche). Basierend auf dieser Annahme sind mindestens 121 Patientinnen pro Behandlungsarm notwendig, um ein um 20% reduziertes Risiko eines unerwünschten Ereignisses für Patientinnen mit dualer HER2-zielgerichteter Therapie plus endokriner Therapie im Vergleich zu Patientinnen mit dualer HER2-zielgerichteter Therapie plus Chemotherapie nachweisen zu können (90% Power, zweiseitiger Test, α = 0.05). Unter der Annahme einer loss to follow-up Rate von ca. 10% müssen 270 Patientinnen mit HER2-positivem und hormonrezeptor-positivem metastasiertem Brustkrebs für diese Studie rekrutiert werden. Für das Inkrafttreten des Amendments mit der Hinzunahme des CDK4/6 Inhibitors Ribociclib in beiden Randomisierungsarmen wurde eine separate Fallzahlkalkulation durchgeführt um die statistische Power der Analyse des neuen primären Endpunkts für die Ribociclib-Kohorte zu ermitteln. Hierfür wird angenommen, dass 90 Patientinnen vor Inkrafttreten des Amendments in die Studie rekrutiert werden (diese Patientinnen erhalten kein Ribociclib). Dementsprechend wird davon ausgegangen, dass 180 Patientinnen nach Inkrafttreten des Amendments rekrutiert werden und demzufolge Ribociclib erhalten. Basierend auf der Annahme, dass für Patientinnen mit HER2-positivem metastasiertem Brustkrebs, die mit einer dualen HER2-zielgerichteten Therapie plus Chemotherapie behandelt werden, der Anteil an nach dem modifizierten adverse event score definierten unerwünschten Ereignissen 86.3% beträgt (siehe oben), ergibt eine Fallzahl von 80 Patientinnen pro Behandlungsarm (180 Patientinnen, die Ribociclib erhalten, loss to follow-up Rate von ca. 10%) eine statistische Power von 76% (zweiseitiger Test, α = 0.05) für die Detektion eines um 20%
13 reduziertes Risikos eines unerwünschten Ereignisses für Patientinnen mit dualer HER2-zielgerichteter Therapie plus Ribociclib und endokriner Therapie im Vergleich zu Patientinnen mit dualer HER2-zielgerichteter Therapie plus Chemotherapie (gefolgt von einer Erhaltungstherapie mit dualer HER2 Blockade plus Ribociclib und endokriner Therapie).
Vorstellung der aktuellen DETECT Studiendesigns. S. Krause Studienkoordinatorin Studienzentrale UFK Ulm
 Vorstellung der aktuellen DETECT Studiendesigns S. Krause Studienkoordinatorin Studienzentrale UFK Ulm Aktuelles Design der DETECT-Studien DETECT III DETECT IV a und b DETECT V Meeting-Mappen: Übersichtsfolien
Vorstellung der aktuellen DETECT Studiendesigns S. Krause Studienkoordinatorin Studienzentrale UFK Ulm Aktuelles Design der DETECT-Studien DETECT III DETECT IV a und b DETECT V Meeting-Mappen: Übersichtsfolien
DETECT Studien: Multizentrische Studien bei Patientinnen mit HER2-negativem metastasiertem Brustkrebs und zirkulierenden Tumorzellen
 DETECT Studien: Multizentrische Studien bei Patientinnen mit HER2-negativem metastasiertem Brustkrebs und zirkulierenden Tumorzellen Sponsor: Universitätsklinikum Ulm (AöR), Albert-Einstein-Allee 29, 89081
DETECT Studien: Multizentrische Studien bei Patientinnen mit HER2-negativem metastasiertem Brustkrebs und zirkulierenden Tumorzellen Sponsor: Universitätsklinikum Ulm (AöR), Albert-Einstein-Allee 29, 89081
APPENDIX I GERMAN PROTOCOL-SYNOPSIS & GERMAN STUDY FLOW SHEET
 APPENDIX I GERMAN PROTOCOL-SYNOPSIS & GERMAN STUDY FLOW SHEET EUDRACT-NR.: 2010-024238-46 Protokoll-Nr.: D-III Sponsor: Universitätsklinikum Ulm, Albert-Einstein-Allee 29, D-89081 Ulm Wissenschaftliche
APPENDIX I GERMAN PROTOCOL-SYNOPSIS & GERMAN STUDY FLOW SHEET EUDRACT-NR.: 2010-024238-46 Protokoll-Nr.: D-III Sponsor: Universitätsklinikum Ulm, Albert-Einstein-Allee 29, D-89081 Ulm Wissenschaftliche
DETECT-STUDIEN: MULTIZENTRISCHE STUDIEN BEI PATIENTINNEN MIT HER2-NEGATIVEM METASTASIERTEM BRUSTKREBS UND ZIRKULIERENDEN TUMORZELLEN (CTCs)
 DEUTSCHES KURZPROTOKOLL DETECT III UND DETECT IV In Kooperation mit Deutsche Gesellschaft für Senologie DETECT-STUDIEN: MULTIZENTRISCHE STUDIEN BEI PATIENTINNEN MIT HER2-NEGATIVEM METASTASIERTEM BRUSTKREBS
DEUTSCHES KURZPROTOKOLL DETECT III UND DETECT IV In Kooperation mit Deutsche Gesellschaft für Senologie DETECT-STUDIEN: MULTIZENTRISCHE STUDIEN BEI PATIENTINNEN MIT HER2-NEGATIVEM METASTASIERTEM BRUSTKREBS
APPENDIX I GERMAN PROTOCOL-SYNOPSIS & GERMAN STUDY FLOW SHEET
 APPENDIX I GERMAN PROTOCOL-SYNOPSIS & GERMAN STUDY FLOW SHEET EUDRACT-NR.: 2013-001269-18 Protokoll-Nr.: D-IV Sponsor: Universitätsklinikum Ulm, Albert-Einstein-Allee 29, D-89081 Ulm Wissenschaftliche
APPENDIX I GERMAN PROTOCOL-SYNOPSIS & GERMAN STUDY FLOW SHEET EUDRACT-NR.: 2013-001269-18 Protokoll-Nr.: D-IV Sponsor: Universitätsklinikum Ulm, Albert-Einstein-Allee 29, D-89081 Ulm Wissenschaftliche
1. Neoadjuvante Therapie. 2. Adjuvante Therapie. 3. Metastasiertes Mamma-Ca. 4. Mamma-Ca. in der Schwangerschaft. 5. Nicht-interventionelle Studien
 1. Neoadjuvante Therapie GeparOcto-Studie Penelope-Studie 2. Adjuvante Therapie GAIN II-Studie Katherine-Studie TREAT CTC-Studie OLYMPIA Studie 3. Metastasiertes Mamma-Ca. First-line Therapie: Ab Second-line
1. Neoadjuvante Therapie GeparOcto-Studie Penelope-Studie 2. Adjuvante Therapie GAIN II-Studie Katherine-Studie TREAT CTC-Studie OLYMPIA Studie 3. Metastasiertes Mamma-Ca. First-line Therapie: Ab Second-line
APPENDIX I GERMAN PROTOCOL-SYNOPSIS & GERMAN STUDY FLOW SHEET
 APPENDIX I GERMAN PROTOCOL-SYNOPSIS & GERMAN STUDY FLOW SHEET EUDRACT-NR.: 2013-001269-18 Protokoll-Nr.: D-IV Sponsor: Universitätsklinikum Ulm, Albert-Einstein-Allee 29, D-89081 Ulm Wissenschaftliche
APPENDIX I GERMAN PROTOCOL-SYNOPSIS & GERMAN STUDY FLOW SHEET EUDRACT-NR.: 2013-001269-18 Protokoll-Nr.: D-IV Sponsor: Universitätsklinikum Ulm, Albert-Einstein-Allee 29, D-89081 Ulm Wissenschaftliche
Die duale vertikale Blockade (VDB) als neue Therapieoption in der Zweitlinientherapie des metastasierten Her2neu positiven Mammakarzinoms
 Krebskongress 2014 Die duale vertikale Blockade (VDB) als neue Therapieoption in der Zweitlinientherapie des metastasierten Her2neu positiven Mammakarzinoms Prof. Dr. med. Christian Jackisch Berlin (21.
Krebskongress 2014 Die duale vertikale Blockade (VDB) als neue Therapieoption in der Zweitlinientherapie des metastasierten Her2neu positiven Mammakarzinoms Prof. Dr. med. Christian Jackisch Berlin (21.
Studiendesign. Gute Gründe für die Teilnahme an den DETECT-Studien
 Studiendesign Gute Gründe für die Teilnahme an den DETECT-Studien NEU: Neue Beurteilung der CTCs in DETECT III (HER2-Positivität von CTCs bei Immunhistochemie 1+, 2+, 3+) NEU: Aufnahme des CDK4/6 Inhibitors
Studiendesign Gute Gründe für die Teilnahme an den DETECT-Studien NEU: Neue Beurteilung der CTCs in DETECT III (HER2-Positivität von CTCs bei Immunhistochemie 1+, 2+, 3+) NEU: Aufnahme des CDK4/6 Inhibitors
GBG Jahrestreffen 2018
 GBG 97- AMICA Antihormonelle Erhaltungstherapie nach First-Line-Chemotherapie mit oder ohne CDK4/6-Inhibitor Ribociclib bei Hormonrezeptorpositivem / HER2 negativem, metastasiertem Brustkrebs: Eine Phase-II-Studie
GBG 97- AMICA Antihormonelle Erhaltungstherapie nach First-Line-Chemotherapie mit oder ohne CDK4/6-Inhibitor Ribociclib bei Hormonrezeptorpositivem / HER2 negativem, metastasiertem Brustkrebs: Eine Phase-II-Studie
Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid
 10 CLL4-Protokoll der deutschen CLL-Studiengruppe Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid - CLL4-Protokoll
10 CLL4-Protokoll der deutschen CLL-Studiengruppe Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid - CLL4-Protokoll
Aktuelle Therapiestudien in der Klinik für Gynäkologie und Geburtshilfe Sana Klinikum Offenbach GmbH Stand Metastasiertes Mammakarzinom
 Klinikum GmbH Desiree Eine multizentrische, randomisierte doppelblinde, Phase-II-Studie zum Vergleich der Verträglichkeit bei einschleichender Dosierung von Everolimus bei Patienten mit metastasiertem
Klinikum GmbH Desiree Eine multizentrische, randomisierte doppelblinde, Phase-II-Studie zum Vergleich der Verträglichkeit bei einschleichender Dosierung von Everolimus bei Patienten mit metastasiertem
GBG 54 - MALE. Eine prospektive, randomisierte, multizentrische Phase II Studie zur Evaluierung der Östradiolsuppression unter Tamoxifen alleine
 GBG 54 - MALE Eine prospektive, randomisierte, multizentrische Phase II Studie zur Evaluierung der Östradiolsuppression unter Tamoxifen alleine versus Tamoxifen plus GnRH-Analogon versus Aromatase-Inhibitor
GBG 54 - MALE Eine prospektive, randomisierte, multizentrische Phase II Studie zur Evaluierung der Östradiolsuppression unter Tamoxifen alleine versus Tamoxifen plus GnRH-Analogon versus Aromatase-Inhibitor
Therapie von Patienten über 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Chlorambucil
 CLL5-Protokoll der deutschen CLL-Studiengruppe 15 Therapie von Patienten über 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Chlorambucil - CLL5-Protokoll der
CLL5-Protokoll der deutschen CLL-Studiengruppe 15 Therapie von Patienten über 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Chlorambucil - CLL5-Protokoll der
Protokol ID: AGO-OVAR OP.4 (AGO DESKTOP OVAR III)
 EINE RANDOMISIERTE, MULTIZENTRISCHE STUDIE ZUM VERGLEICH DER WIRKSAMKEIT EINER ZUSÄTZLICHEN TUMORDEBULKING-OPERATION GEGEN EINE ALLEINIGE CHEMOTHERAPIE BEI PATIENTINNEN MIT EINEM PLATIN-SENSIBLEN OVARIALKARZINOM-REZIDIV
EINE RANDOMISIERTE, MULTIZENTRISCHE STUDIE ZUM VERGLEICH DER WIRKSAMKEIT EINER ZUSÄTZLICHEN TUMORDEBULKING-OPERATION GEGEN EINE ALLEINIGE CHEMOTHERAPIE BEI PATIENTINNEN MIT EINEM PLATIN-SENSIBLEN OVARIALKARZINOM-REZIDIV
Pank n reaszent n r t um u M ü M n ü c n he h n: Opt p i t mierun u g n g de d r Pati t ent n e t nv n ersor o gu g n u g
 Pankreaszentrum München: Optimierung der Patientenversorgung Biomarker-Studie : Rash-basierte Therapiestrategie Dr. med. Stefan Böck Prof. Dr. med. Volker Heinemann Medizinische Klinik und Poliklinik III
Pankreaszentrum München: Optimierung der Patientenversorgung Biomarker-Studie : Rash-basierte Therapiestrategie Dr. med. Stefan Böck Prof. Dr. med. Volker Heinemann Medizinische Klinik und Poliklinik III
Endokrine und zielgerichtete Therapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2016.1D Endokrine und zielgerichtete Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten
Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2016.1D Endokrine und zielgerichtete Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten
KURZFASSUNG DES PRÜFPROTOKOLLS 1839IL/0079 VOM
 KURZFASSUNG DES PRÜFPROTOKOLLS 1839IL/0079 VOM 11.11.02 RANDOMISIERTE, OFFENE, NICHT-KOMPARATIVE PHASE II STUDIE ZUR BEURTEILUNG DER WIRKSAMKEIT UND VERTRÄGLICHKEIT VON ZWEI DOSIERUNGEN ZD1839 BEI PATIENTEN
KURZFASSUNG DES PRÜFPROTOKOLLS 1839IL/0079 VOM 11.11.02 RANDOMISIERTE, OFFENE, NICHT-KOMPARATIVE PHASE II STUDIE ZUR BEURTEILUNG DER WIRKSAMKEIT UND VERTRÄGLICHKEIT VON ZWEI DOSIERUNGEN ZD1839 BEI PATIENTEN
Neues zum fortgeschrittenen Mammakarzinom
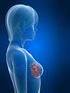 Neues zum fortgeschrittenen Mammakarzinom Ulrike Nitz Brustzentrum Niederrhein MBC OS Aktuelle Bestandsaufnahme OMEDCO nterims Analyse 2013; ABC Gruppe; n=1409/2250 Patients alive 100% 90% 80% 70% 60%
Neues zum fortgeschrittenen Mammakarzinom Ulrike Nitz Brustzentrum Niederrhein MBC OS Aktuelle Bestandsaufnahme OMEDCO nterims Analyse 2013; ABC Gruppe; n=1409/2250 Patients alive 100% 90% 80% 70% 60%
1. Neoadjuvante Therapie. 2. Adjuvante Therapie. 3. Metastasiertes Mamma-Ca. 4. Mamma-Ca. in der Schwangerschaft. 5. Nicht-interventionelle Studien
 1. Neoadjuvante Therapie GeparOcto-Studie Penelope-Studie 2. Adjuvante Therapie GAIN II-Studie Adapt-Studie Katherine-Studie TREAT CTC-Studie 3. Metastasiertes Mamma-Ca. First-line Therapie: Ab Second-line
1. Neoadjuvante Therapie GeparOcto-Studie Penelope-Studie 2. Adjuvante Therapie GAIN II-Studie Adapt-Studie Katherine-Studie TREAT CTC-Studie 3. Metastasiertes Mamma-Ca. First-line Therapie: Ab Second-line
AGO-OVAR 19 / TRUST. (platinfreies Intervall 6-12 Monate) Intermediär-platinsensibles Rezidiv. Erstdiagnose FIGO IIIB-IV
 Ovarialkarzinom Aktuelle Studien in der Klinik für Gynäkologie des UKE Kontakt Studiensekretariat: Sylke Krenkel (040/7410-57970, skrenkel@uke.de) Stand juni 2017 Intermediär-platinsensibles Rezidiv (platinfreies
Ovarialkarzinom Aktuelle Studien in der Klinik für Gynäkologie des UKE Kontakt Studiensekretariat: Sylke Krenkel (040/7410-57970, skrenkel@uke.de) Stand juni 2017 Intermediär-platinsensibles Rezidiv (platinfreies
Endokrine Therapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version 2002: Gerber / Friedrichs
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version 2002: Gerber / Friedrichs
1.4. Protokoll-Synopse
 EudraCT-Nr.: 2005-005473-29 Protokoll Version 2.3 vom 20.12.2006 Seite - 13-1.4. Protokoll-Synopse Protokoll-Nr.: OSHO # 70 (FL-OSHO/GLSG-M3-2005-01) Protokoll-Version und Datum.: 2.3 vom 20.12.2006 Titel
EudraCT-Nr.: 2005-005473-29 Protokoll Version 2.3 vom 20.12.2006 Seite - 13-1.4. Protokoll-Synopse Protokoll-Nr.: OSHO # 70 (FL-OSHO/GLSG-M3-2005-01) Protokoll-Version und Datum.: 2.3 vom 20.12.2006 Titel
Chemotherapie bei metastasiertem Mammakarzinom
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Chemotherapie bei metastasiertem Mammakarzinom Chemotherapie bei metastasiertem Mammakarzinom Version 2002: von Minckwitz Version 2003
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Chemotherapie bei metastasiertem Mammakarzinom Chemotherapie bei metastasiertem Mammakarzinom Version 2002: von Minckwitz Version 2003
Zusammenfassung des Prüfplans
 Studientitel Studiencode GBG 97 EudraCT Number 2017-003667-35 Zusammenfassung des Prüfplans EudraCT-Nr. 2017-003667-35 Antihormonelle Erhaltungstherapie nach First-Line-Chemotherapie mit oder ohne CDK4/6-Inhibitor
Studientitel Studiencode GBG 97 EudraCT Number 2017-003667-35 Zusammenfassung des Prüfplans EudraCT-Nr. 2017-003667-35 Antihormonelle Erhaltungstherapie nach First-Line-Chemotherapie mit oder ohne CDK4/6-Inhibitor
Neue Studienkonzepte SUCCESS
 Campus Innenstadt für Frauenheilkunde und Geburtshilfe Neue Studienkonzepte SUCCESS PD Dr. med. Brigitte Rack für Frauenheilkunde und Geburtshilfe Ludwig-Maximilians-Universität München Campus Innenstadt
Campus Innenstadt für Frauenheilkunde und Geburtshilfe Neue Studienkonzepte SUCCESS PD Dr. med. Brigitte Rack für Frauenheilkunde und Geburtshilfe Ludwig-Maximilians-Universität München Campus Innenstadt
Erhaltungstherapie mit Erlotinib verlängert Gesamtüberleben bei fortgeschrittenem NSCLC
 SATURN-Studie: Erhaltungstherapie mit Erlotinib verlängert Gesamtüberleben bei fortgeschrittenem NSCLC Grenzach-Wyhlen (13. August 2009) - Aktuelle Daten der SATURN-Studie bestätigen eine signifikante
SATURN-Studie: Erhaltungstherapie mit Erlotinib verlängert Gesamtüberleben bei fortgeschrittenem NSCLC Grenzach-Wyhlen (13. August 2009) - Aktuelle Daten der SATURN-Studie bestätigen eine signifikante
Endokrine Therapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2012.1D Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version
Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2012.1D Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version
Endokrine und zielgerichtete Therapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2014.1D Endokrine und zielgerichtete Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten
Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2014.1D Endokrine und zielgerichtete Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten
Meilenstein in der personalisierten Medizin FDA-Zulassung für Pertuzumab beim HER2-positiven metastasierten Mammakarzinom
 Meilenstein in der personalisierten Medizin FDA-Zulassung für Pertuzumab beim HER2-positiven metastasierten Mammakarzinom Frankfurt am Main (15. Juni 2012) - Die US-amerikanische Arzneimittelzulassungsbehörde
Meilenstein in der personalisierten Medizin FDA-Zulassung für Pertuzumab beim HER2-positiven metastasierten Mammakarzinom Frankfurt am Main (15. Juni 2012) - Die US-amerikanische Arzneimittelzulassungsbehörde
Endokrine Therapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version 2002: Gerber / Friedrichs
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version 2002: Gerber / Friedrichs
Adjuvante zytostatische und zielgerichtete Therapien
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Versionen 2002 2017: Dall /
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Versionen 2002 2017: Dall /
1.4. Protokoll-Synopse
 EudraCT-Nr.: 2005-005473-29 Protokoll Version 2.4 vom 20.7.2009 Seite - 13-1.4. Protokoll-Synopse Protokoll-Nr.: OSHO # 70 (FL-OSHO/GLSG-M3-2005-01) Protokoll-Version und Datum.: 2.4 vom 20.07.2009 Titel
EudraCT-Nr.: 2005-005473-29 Protokoll Version 2.4 vom 20.7.2009 Seite - 13-1.4. Protokoll-Synopse Protokoll-Nr.: OSHO # 70 (FL-OSHO/GLSG-M3-2005-01) Protokoll-Version und Datum.: 2.4 vom 20.07.2009 Titel
Zirkulierende Tumorzellen (CTC) beim metastasierten Mammakarzinom
 Zirkulierende Tumorzellen (CTC) beim metastasierten Mammakarzinom Bahriye Aktas Universitätsfrauenklinik Essen Direktor: Prof. Dr. med. Rainer Kimmig Das Mammakarzinom- eine systemische Erkrankung! METASTASENBILDUNG
Zirkulierende Tumorzellen (CTC) beim metastasierten Mammakarzinom Bahriye Aktas Universitätsfrauenklinik Essen Direktor: Prof. Dr. med. Rainer Kimmig Das Mammakarzinom- eine systemische Erkrankung! METASTASENBILDUNG
A Randomized, Prospective, Double-Blind, Placebocontrolled Trial of Terlipressin for Type 1 Hepatorenal Syndrome
 A Randomized, Prospective, Double-Blind, Placebocontrolled Trial of Terlipressin for Type 1 Hepatorenal Syndrome Sanyal et al, Gastroenterology 2008;134:1360-1368 WISSENSCHAFTLICHE GRUNDLAGEN UND ALLGEMEINE
A Randomized, Prospective, Double-Blind, Placebocontrolled Trial of Terlipressin for Type 1 Hepatorenal Syndrome Sanyal et al, Gastroenterology 2008;134:1360-1368 WISSENSCHAFTLICHE GRUNDLAGEN UND ALLGEMEINE
Chemotherapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Chemotherapie des metastasierten Mammakarzinoms Chemotherapie bei metastasiertem Mammakarzinom Version 2002: von Minckwitz Version 2003
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Chemotherapie des metastasierten Mammakarzinoms Chemotherapie bei metastasiertem Mammakarzinom Version 2002: von Minckwitz Version 2003
Deutsche Synopse. Studienphase und Titel:
 MEL001-Studie Seite 1 Deutsche Synopse Studienphase und Titel: Eine prospektive Phase I und fortlaufende Phase II, zweiarmige, randomisierte, multizentrische Studie von Temsirolimus in Kombination mit
MEL001-Studie Seite 1 Deutsche Synopse Studienphase und Titel: Eine prospektive Phase I und fortlaufende Phase II, zweiarmige, randomisierte, multizentrische Studie von Temsirolimus in Kombination mit
internationalen SAiL Studie, in der die Sicherheit und Wirksamkeit des VEGF Antikörpers in der täglichen Routine analysiert werden.
 DGP Kongress in Lübeck Avastin überwindet Therapiestillstand beim fortgeschrittenen NSCLC Lübeck (11. April 2008) - Die zielgerichtete First Line -Therapie mit dem Angiogenese Hemmer Bevacizumab (Avastin
DGP Kongress in Lübeck Avastin überwindet Therapiestillstand beim fortgeschrittenen NSCLC Lübeck (11. April 2008) - Die zielgerichtete First Line -Therapie mit dem Angiogenese Hemmer Bevacizumab (Avastin
Mammakarzinom - Zulassungsstatus von Medikamenten Leitlinie
 Mammakarzinom - Zulassungsstatus von Medikamenten Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft
Mammakarzinom - Zulassungsstatus von Medikamenten Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft
Dossierbewertung A18-72 Version 1.0 Abemaciclib (Mammakarzinom; Kombination mit einem Aromatasehemmer)
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Abemaciclib in Kombination mit einem Aromatasehemmer gemäß 35a SGB V beauftragt.
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Abemaciclib in Kombination mit einem Aromatasehemmer gemäß 35a SGB V beauftragt.
DETECT III DETECT III
 DETECT III Eine prospektive, randomisierte, zweiarmige, multizentrische Phase III Studie zum Vergleich Standardtherapie versusstandardtherapie mit Lapatinib bei metastasierten Patientinnen mit initial
DETECT III Eine prospektive, randomisierte, zweiarmige, multizentrische Phase III Studie zum Vergleich Standardtherapie versusstandardtherapie mit Lapatinib bei metastasierten Patientinnen mit initial
Entscheidungsfindung in der Erstlinientherapie welche Daten helfen weiter? Stefan Siemer
 Entscheidungsfindung in der Erstlinientherapie welche Daten helfen weiter? Stefan Siemer EAU (Ljungberg et al. 2014) Guidelines on Renal Cell Carcinoma, Update 2014,:www.uroweb.org/guidelines/online-guidelines/
Entscheidungsfindung in der Erstlinientherapie welche Daten helfen weiter? Stefan Siemer EAU (Ljungberg et al. 2014) Guidelines on Renal Cell Carcinoma, Update 2014,:www.uroweb.org/guidelines/online-guidelines/
Dossierbewertung A13-41 Version 1.0 Afatinib Nutzenbewertung gemäß 35a SGB V
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Afatinib gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis eines
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Afatinib gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis eines
Dossierbewertung A16-11 Version 1.0 Ramucirumab (Lungenkarzinom)
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Ramucirumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Ramucirumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
Helios Amper-Klinikum Dachau
 Helios Amper-Klinikum Dachau Dachau, 25.05.2018 Bei der Suche nach immer besseren Therapiemöglichkeiten für Krebspatienten kommt klinischen eine besondere Bedeutung zu. Im Onkologischen Zentrum Dachau
Helios Amper-Klinikum Dachau Dachau, 25.05.2018 Bei der Suche nach immer besseren Therapiemöglichkeiten für Krebspatienten kommt klinischen eine besondere Bedeutung zu. Im Onkologischen Zentrum Dachau
Adjuvante zytostatische und zielgerichtete Therapien
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Version 2002: Möbus / Nitz Versionen
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Version 2002: Möbus / Nitz Versionen
Ovarialkarzinom Aktuelle Studien in der Klinik für Gynäkologie des UKE Kontakt Studiensekretariat: Sylke Krenkel (040/ ,
 Ovarialkarzinom Aktuelle Studien in der Klinik für Gynäkologie des UKE Kontakt Studiensekretariat: Sylke Krenkel (040/7410-57970, skrenkel@uke.de) Stand Dezember 2017, A.Jaeger 1 Erstdiagnose FIGO IIIB-IV
Ovarialkarzinom Aktuelle Studien in der Klinik für Gynäkologie des UKE Kontakt Studiensekretariat: Sylke Krenkel (040/7410-57970, skrenkel@uke.de) Stand Dezember 2017, A.Jaeger 1 Erstdiagnose FIGO IIIB-IV
Gute Überlebensqualität Trastuzumab beim metastasierten Magenkarzinom
 Gute Überlebensqualität Trastuzumab beim metastasierten Magenkarzinom München (24. April 2012) - Mit dem monoklonalen Antikörper Trastuzumab (Herceptin ) steht bislang die einzige zielgerichtete Substanz
Gute Überlebensqualität Trastuzumab beim metastasierten Magenkarzinom München (24. April 2012) - Mit dem monoklonalen Antikörper Trastuzumab (Herceptin ) steht bislang die einzige zielgerichtete Substanz
O f f e n e S t u d i e n - August 2013 -
 Sehr geehrte Patientinnen und Angehörige, sehr geehrte Ärztinnen und Ärzte, Klinische Studien zur Behandlung des Ovarial-, Tuben-, Endometrium- und Peritonealkarzinoms: bevor antihormonelle, chemotherapeutische
Sehr geehrte Patientinnen und Angehörige, sehr geehrte Ärztinnen und Ärzte, Klinische Studien zur Behandlung des Ovarial-, Tuben-, Endometrium- und Peritonealkarzinoms: bevor antihormonelle, chemotherapeutische
Neoadjuvante (Primäre) systemische Therapie
 Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
Metastasiertes kolorektales Karzinom palliative Therapie, 1st-line
 Metastasiertes kolorektales Karzinom palliative Therapie, 1st-line AIO-KRK-0110: Capecitabin plus Bevacizumab versus Capecitabin plus Irinotecan plus Bevacizumab als Erstlinien-Therapie beim metastasierten
Metastasiertes kolorektales Karzinom palliative Therapie, 1st-line AIO-KRK-0110: Capecitabin plus Bevacizumab versus Capecitabin plus Irinotecan plus Bevacizumab als Erstlinien-Therapie beim metastasierten
Originalarbeit: James et al., N Engl J Med 2012; 366:
 Originalarbeit: James et al., N Engl J Med 2012; 366: 1477-1488 Kommentar zur Originalarbeit: Shipley & Zietman N Engl J Med 2012; 366: 1540-41 Meilenstein BC2001-Studie: Design randomisierte Studie mit
Originalarbeit: James et al., N Engl J Med 2012; 366: 1477-1488 Kommentar zur Originalarbeit: Shipley & Zietman N Engl J Med 2012; 366: 1540-41 Meilenstein BC2001-Studie: Design randomisierte Studie mit
Endokrine und zielgerichtete Therapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2015.1D Endokrine und zielgerichtete Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten
Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2015.1D Endokrine und zielgerichtete Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten
Neoadjuvante (Primäre) systemische Therapie
 Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer AGO e. V. Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer AGO e. V. Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
Chemotherapie mit oder ohne zielgerichtete Substanzen beim
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Chemotherapie mit oder ohne zielgerichtete Substanzen beim metastasierten Mammakarzinom Chemotherapie mit oder ohne zielgerichtete Substanzen
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Chemotherapie mit oder ohne zielgerichtete Substanzen beim metastasierten Mammakarzinom Chemotherapie mit oder ohne zielgerichtete Substanzen
Chronische lymphatische Leukämien - CLL2-BCG
 Innere Medizin I - Onkologie, Hämatologie, Klinische Infektiologie, Klinische Immunologie, Hämostaseologie, Internistische Intensivmedizin Chronische lymphatische Leukämien - CLL2-BCG Prüfplancode ISRCTN
Innere Medizin I - Onkologie, Hämatologie, Klinische Infektiologie, Klinische Immunologie, Hämostaseologie, Internistische Intensivmedizin Chronische lymphatische Leukämien - CLL2-BCG Prüfplancode ISRCTN
Analyse von Ereigniszeiten
 Survivalanalyse Analyse von Ereigniszeiten Lebensdauer = Zeit zwischen einem Startpunkt (Anfangsdatum) und einem aufgetretenen Ereignis (Enddatum) Startpunkte Diagnose einer Krankheit Beginn einer Behandlung
Survivalanalyse Analyse von Ereigniszeiten Lebensdauer = Zeit zwischen einem Startpunkt (Anfangsdatum) und einem aufgetretenen Ereignis (Enddatum) Startpunkte Diagnose einer Krankheit Beginn einer Behandlung
Endokrine Therapie des Mammakarzinoms. Bernd Hanswille Klinikum Dortmund Frauenklinik
 Endokrine Therapie des Mammakarzinoms Bernd Hanswille Klinikum Dortmund Frauenklinik Grundlagen Stufe-3-Leitlinie Brustkrebs-Früherkennung in Deutschland www.senologie.org\leitlinien.html S2/S3-Leitlinie
Endokrine Therapie des Mammakarzinoms Bernd Hanswille Klinikum Dortmund Frauenklinik Grundlagen Stufe-3-Leitlinie Brustkrebs-Früherkennung in Deutschland www.senologie.org\leitlinien.html S2/S3-Leitlinie
Dossierbewertung A17-67 Version 1.0 Alectinib (nicht kleinzelliges Lungenkarzinom)
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Alectinib gemäß 35a SGB V beauftragt. Die Bewertung erfolgt auf Basis eines
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Alectinib gemäß 35a SGB V beauftragt. Die Bewertung erfolgt auf Basis eines
Laufende Studien in unserem Zentrum
 Klinik für Senologie / Interdisziplinäres Brustzentrum Laufende Studien in unserem Zentrum Palliative Therapie Therapie, die auf Erhaltung von Lebensqualität bzw. auf die Lebensverlängerung bei unheilbaren
Klinik für Senologie / Interdisziplinäres Brustzentrum Laufende Studien in unserem Zentrum Palliative Therapie Therapie, die auf Erhaltung von Lebensqualität bzw. auf die Lebensverlängerung bei unheilbaren
Therapie der älteren Patientin
 Therapie der älteren Patientin P. Wimberger, F. Hilpert Universitätsklinikum Essen Universitätsklinikum Kiel Ovarialkarzinom - State of the Art AGO-Symposium München 20.Juni 2009 Lebenserwartung von Frauen
Therapie der älteren Patientin P. Wimberger, F. Hilpert Universitätsklinikum Essen Universitätsklinikum Kiel Ovarialkarzinom - State of the Art AGO-Symposium München 20.Juni 2009 Lebenserwartung von Frauen
Therapie des HER2 negativen und Hormonrezeptorpositiven. Volkmar Müller
 DETECT Investigatormeeting Therapie des HER2 negativen und Hormonrezeptorpositiven Mammakarzinoms Volkmar Müller Klinik für Gynäkologie, Brustzentrum am UKE Hubertus Wald Tumorzentrum Universitätsklinikum
DETECT Investigatormeeting Therapie des HER2 negativen und Hormonrezeptorpositiven Mammakarzinoms Volkmar Müller Klinik für Gynäkologie, Brustzentrum am UKE Hubertus Wald Tumorzentrum Universitätsklinikum
SABCS 2011: Metastasierte Situation
 Dr. med. Johannes Ettl Interdisziplinäres Brustzentrum und Frauenklinik rechts der Isar, Technische Universität München, Direktorin: Prof. Dr. M. Kiechle SABCS 2011: Metastasierte Situation München, Projektgruppe
Dr. med. Johannes Ettl Interdisziplinäres Brustzentrum und Frauenklinik rechts der Isar, Technische Universität München, Direktorin: Prof. Dr. M. Kiechle SABCS 2011: Metastasierte Situation München, Projektgruppe
Studienübersicht Brustzentrum Neckar-Donau
 HERA Eine randomisierte, multizentrische Studie zum Vergleich von einem Jahr und 2 Jahren Herceptin gegenüber keinem Herceptin bei Frauen mit Her2- positivem primären Mammakarzinom, die eine adjuvante
HERA Eine randomisierte, multizentrische Studie zum Vergleich von einem Jahr und 2 Jahren Herceptin gegenüber keinem Herceptin bei Frauen mit Her2- positivem primären Mammakarzinom, die eine adjuvante
Synopse AGO OVAR OP.7 TRUST/AGO OVAR 19 nationaler Part / Deutschland
 Synopse Protokolltitel Studie zur primären radikalen Operation bei fortgeschrittenem Ovarialkarzinom Erweiterung für Deutschland mit Evaluation von Fragilität und Langzeit Lebensqualität Protokollnummer
Synopse Protokolltitel Studie zur primären radikalen Operation bei fortgeschrittenem Ovarialkarzinom Erweiterung für Deutschland mit Evaluation von Fragilität und Langzeit Lebensqualität Protokollnummer
Antikörpertherapie beim Mammakarzinom
 Antikörpertherapie beim Mammakarzinom (Dr. S. Rückert) Trastuzumab (Herceptin ) ist ein gentechnisch hergestellter Antikörper, welcher gegen das HER2/neu-Protein gerichtet ist. Dieser Wachstumsfaktor kommt
Antikörpertherapie beim Mammakarzinom (Dr. S. Rückert) Trastuzumab (Herceptin ) ist ein gentechnisch hergestellter Antikörper, welcher gegen das HER2/neu-Protein gerichtet ist. Dieser Wachstumsfaktor kommt
Analyse von Ereignisdaten Univ.-Prof. DI Dr. Andrea Berghold Institut für Med. Informatik, Statistik und Dokumentation
 Analyse von Ereignisdaten Univ.-Prof. DI Dr. Andrea Berghold Institut für Med. Informatik, Statistik und Dokumentation Analyse von Ereigniszeiten Lebensdauer = Zeit zwischen einem Startpunkt (Anfangsdatum)
Analyse von Ereignisdaten Univ.-Prof. DI Dr. Andrea Berghold Institut für Med. Informatik, Statistik und Dokumentation Analyse von Ereigniszeiten Lebensdauer = Zeit zwischen einem Startpunkt (Anfangsdatum)
Dossierbewertung A18-41 Version 1.0 Pertuzumab (Mammakarzinom)
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Pertuzumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgt auf Basis eines
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Pertuzumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgt auf Basis eines
Dossierbewertung A16-10 Version 1.0 Ramucirumab (Kolorektalkarzinom)
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Ramucirumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Ramucirumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
Decitabin Beschluss vom: 2. Mai 2013 gültig bis: unbefristet In Kraft getreten am: 2. Mai 2013 BAnz AT B6
 Beschluss vom: 2. Mai 2013 gültig bis: unbefristet In Kraft getreten am: 2. Mai 2013 BAnz AT 29.05.2013 B6 Zugelassenes Anwendungsgebiet Dacogen ist indiziert zur Behandlung erwachsener Patienten ab einem
Beschluss vom: 2. Mai 2013 gültig bis: unbefristet In Kraft getreten am: 2. Mai 2013 BAnz AT 29.05.2013 B6 Zugelassenes Anwendungsgebiet Dacogen ist indiziert zur Behandlung erwachsener Patienten ab einem
Erste Taxan-basierte Anthrazyklin-freie Chemotherapie
 Erste Taxan-basierte Anthrazyklin-freie Chemotherapie in Kombination mit Herceptin (TCH) für Patientinnen mit HER2-positivem frühem Brustkrebs erhält FDA-Zulassung Edmonton, Kanada (31. Mai 2008, ots/prnewswire)
Erste Taxan-basierte Anthrazyklin-freie Chemotherapie in Kombination mit Herceptin (TCH) für Patientinnen mit HER2-positivem frühem Brustkrebs erhält FDA-Zulassung Edmonton, Kanada (31. Mai 2008, ots/prnewswire)
Dossierbewertung A18-80 Version 1.0 Enzalutamid (Prostatakarzinom)
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Enzalutamid gemäß 35a SGB V beauftragt. Die Bewertung erfolgt auf Basis eines
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Enzalutamid gemäß 35a SGB V beauftragt. Die Bewertung erfolgt auf Basis eines
Das Neuste weltweit zur Antihormontherapie. Prof. Dr. Tanja Fehm Universitätsfrauenklinik Düsseldorf
 Das Neuste weltweit zur Antihormontherapie UpDat e Prof. Dr. Tanja Fehm Universitätsfrauenklinik Düsseldorf Zunächst einige Anmerkungen zur Antihormontherapie Ihre Frage kurz beantwortet Antihormontherapie
Das Neuste weltweit zur Antihormontherapie UpDat e Prof. Dr. Tanja Fehm Universitätsfrauenklinik Düsseldorf Zunächst einige Anmerkungen zur Antihormontherapie Ihre Frage kurz beantwortet Antihormontherapie
Zielgerichtete Substanzen*
 Diagnostik und Therapie primärer und metastasierter Mammakarzinomr Zielgerichtete Substanzen* *Es werden nur Substanzen besprochen, von denen Daten aus mindestens einer publizierten Phase-III-Studie vorliegen
Diagnostik und Therapie primärer und metastasierter Mammakarzinomr Zielgerichtete Substanzen* *Es werden nur Substanzen besprochen, von denen Daten aus mindestens einer publizierten Phase-III-Studie vorliegen
Mistelextrakt in der Instillationstherapie des Urothelkarzinoms der Blase
 Mistelextrakt in der Instillationstherapie des Urothelkarzinoms der Blase Dr. med. Achim Rose, Helios Kliniken Duisburg Epidemiologie in Deutschland: ca. 16.000 ED/a, über 25.000 Diagnosen/a 75 % bei ED
Mistelextrakt in der Instillationstherapie des Urothelkarzinoms der Blase Dr. med. Achim Rose, Helios Kliniken Duisburg Epidemiologie in Deutschland: ca. 16.000 ED/a, über 25.000 Diagnosen/a 75 % bei ED
ER+, PR+ und Her2/neu-positives Mammakarzinom mit Änderung des Rezeptorstatus
 G. Schaller, München. 03. Juni 2014 ER+, PR+ und Her2/neu-positives Mammakarzinom mit Änderung des Rezeptorstatus Dargestellt wird die Kasuistik einer 57-jährigen Patientin mit einem primär Hormonrezeptorpositiven
G. Schaller, München. 03. Juni 2014 ER+, PR+ und Her2/neu-positives Mammakarzinom mit Änderung des Rezeptorstatus Dargestellt wird die Kasuistik einer 57-jährigen Patientin mit einem primär Hormonrezeptorpositiven
Studienzentrum der Deutschen Gesellschaft für f. SYNCHRONOUS Trial
 Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
PROTOKOLL SYNOPSE Version 3.1 (Protokollversion 3.1 Amendment 1):
 T-PLL2-Protokoll der Deutschen CLL Studiengruppe (DCLLSG) Phase II Trial of Combined Immunochemotherapy with Fludarabine, Mitoxantrone, Cyclophosphamide and Alemtuzumab (FMC-Alemtuzumab) in Patients with
T-PLL2-Protokoll der Deutschen CLL Studiengruppe (DCLLSG) Phase II Trial of Combined Immunochemotherapy with Fludarabine, Mitoxantrone, Cyclophosphamide and Alemtuzumab (FMC-Alemtuzumab) in Patients with
Update Onkologie - Gynäkologie und Senologie- Prof. Dr. Dorothea Fischer Klinikum Ernst von Bergmann Potsdam
 Update Onkologie - Gynäkologie und Senologie- Prof. Dr. Dorothea Fischer Klinikum Ernst von Bergmann Potsdam Agenda Ovar/ Tube/ Peritoneum Endometrium Zervix Vulva Mamma Ovarial- /Tuben- /Peritonealkarzinom
Update Onkologie - Gynäkologie und Senologie- Prof. Dr. Dorothea Fischer Klinikum Ernst von Bergmann Potsdam Agenda Ovar/ Tube/ Peritoneum Endometrium Zervix Vulva Mamma Ovarial- /Tuben- /Peritonealkarzinom
Neoadjuvante Pertuzumab-Gabe bei HER2-positivem Brustkrebs
 Anhaltspunkt für geringeren Nutzen Neoadjuvante Pertuzumab-Gabe bei HER2-positivem Brustkrebs - Keine positiven Effekte belegt / Mehr Therapieabbrüche wegen Nebenwirkungen Köln (1. Dezember 2015) - Pertuzumab
Anhaltspunkt für geringeren Nutzen Neoadjuvante Pertuzumab-Gabe bei HER2-positivem Brustkrebs - Keine positiven Effekte belegt / Mehr Therapieabbrüche wegen Nebenwirkungen Köln (1. Dezember 2015) - Pertuzumab
FIRE-3 3 Studie. Studientreffen am
 FIRE-3 3 Studie Studientreffen am 26.06.2009 in MünchenM FIRE-3 3 Studie n = 294 Patienten randomisierte deutsche Mulitizenterstudie FOLFIRI + Cetuximab R FOLFIRI + Bevacizumab Primärer Endpunkt = ORR
FIRE-3 3 Studie Studientreffen am 26.06.2009 in MünchenM FIRE-3 3 Studie n = 294 Patienten randomisierte deutsche Mulitizenterstudie FOLFIRI + Cetuximab R FOLFIRI + Bevacizumab Primärer Endpunkt = ORR
Version: V1.0 basierend auf Amendment 1 vom 15. Juli 2016
 Pertuzumab in First Line Treatment of HER2-positive metastatic breast Cancer patients: A cohort study of patients treated either with docetaxel and Trastuzumab or docetaxel, trastuzumab and, NCT02642458
Pertuzumab in First Line Treatment of HER2-positive metastatic breast Cancer patients: A cohort study of patients treated either with docetaxel and Trastuzumab or docetaxel, trastuzumab and, NCT02642458
Highlights aus der medizinischen Onkologie
 Highlights aus der medizinischen Onkologie ESIO-Fortbildung 15.09.16 Susanna Stoll Klinik für Medizinische Onkologie USZ / Stadtspital Triemli Uebersicht Neue Substanzen: - Palbociclib - Olaparib Adjuvante
Highlights aus der medizinischen Onkologie ESIO-Fortbildung 15.09.16 Susanna Stoll Klinik für Medizinische Onkologie USZ / Stadtspital Triemli Uebersicht Neue Substanzen: - Palbociclib - Olaparib Adjuvante
Prüfplan. MCL Rezidiv-Studie des European MCL Network und der GLSG Protokoll Version 1.5
 Prüfplan MCL Rezidiv-Studie des und der GLSG Protokoll Version 1.5 Vollständiger Titel: Wirksamkeit und Sicherheit einer Kombinationstherapie mit Rituximab, hochdosiertem Ara-C und Dexamethason (R-HAD)
Prüfplan MCL Rezidiv-Studie des und der GLSG Protokoll Version 1.5 Vollständiger Titel: Wirksamkeit und Sicherheit einer Kombinationstherapie mit Rituximab, hochdosiertem Ara-C und Dexamethason (R-HAD)
1 von :09
 1 von 5 09.06.2011 15:09 2 von 5 09.06.2011 15:09 Klinische Studien CAI Prüfplancode ISRCTN EudraCT Clinicaltrials.gov DRKS CAI n/a NCT00126321 Therapie von Patienten mit rezidivierter akuter myeloischer
1 von 5 09.06.2011 15:09 2 von 5 09.06.2011 15:09 Klinische Studien CAI Prüfplancode ISRCTN EudraCT Clinicaltrials.gov DRKS CAI n/a NCT00126321 Therapie von Patienten mit rezidivierter akuter myeloischer
Second-line Chemotherapie. Prostatakarzinoms
 Second-line Chemotherapie des metastasierten, hormonrefraktären Prostatakarzinoms 1st-line Therapie TAX-327 & SWOG 99-16: Docetaxel q3wks Update 2008: Berthold et al, JCO 2008; 26:242-245 2nd-line Therapien
Second-line Chemotherapie des metastasierten, hormonrefraktären Prostatakarzinoms 1st-line Therapie TAX-327 & SWOG 99-16: Docetaxel q3wks Update 2008: Berthold et al, JCO 2008; 26:242-245 2nd-line Therapien
Dossierbewertung A14-01 Version 1.0 Trastuzumab Emtansin Nutzenbewertung gemäß 35a SGB V
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Trastuzumab Emtansin gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Trastuzumab Emtansin gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf
Efficacy and safety of recombinant human activated protein C for severe sepsis Bernard, G.et al. N Engl J Med 2001; 344:
 RCT: Efficacy and safety of recombinant human activated protein C for severe sepsis Bernard, G.et al. Eignung der Studie für critical appraisal im Rahmen eines EbM Kurses: - typisches Beispiel für Arzneimittelstudie
RCT: Efficacy and safety of recombinant human activated protein C for severe sepsis Bernard, G.et al. Eignung der Studie für critical appraisal im Rahmen eines EbM Kurses: - typisches Beispiel für Arzneimittelstudie
Primär-systemische Therapie Studien (neo-adjuvante Therapie Studien)
 Übersicht der aktuellen n beim Mamma-Carcinom Stand: Juli 2009 Primär-systemische Therapie n (neo-adjuvante Therapie n) A: Her-2-negativ 4 x EC +/- Bev A1 bei CR/PR 4 x T +/- Bev OP A2 bei NC P weekly
Übersicht der aktuellen n beim Mamma-Carcinom Stand: Juli 2009 Primär-systemische Therapie n (neo-adjuvante Therapie n) A: Her-2-negativ 4 x EC +/- Bev A1 bei CR/PR 4 x T +/- Bev OP A2 bei NC P weekly
Wirksamkeit und Sicherheit von Thalidomid in der primären Therapie des multiplen Myeloms
 AMB 2006, 40, 89 Wirksamkeit und Sicherheit von Thalidomid in der primären Therapie des multiplen Myeloms Mit Thalidomid, Lenalidomid und Bortezomib (Velcade ) stehen inzwischen neue Wirkstoffe für die
AMB 2006, 40, 89 Wirksamkeit und Sicherheit von Thalidomid in der primären Therapie des multiplen Myeloms Mit Thalidomid, Lenalidomid und Bortezomib (Velcade ) stehen inzwischen neue Wirkstoffe für die
Rezidiv eines invasiven eptihelialem Ovarial-, Tuben- oder primären Peritonealkarzinom
 STUDIENÜBERSICHT Laufende Studien Sphero NEO: (Brustzentrum) Neoadjuvant Mamma-CA Kurzbeschreibung: prospektive Kohortenstudie zur Prädiktion des Effektes der medikamentösen Therapie am multizellulären
STUDIENÜBERSICHT Laufende Studien Sphero NEO: (Brustzentrum) Neoadjuvant Mamma-CA Kurzbeschreibung: prospektive Kohortenstudie zur Prädiktion des Effektes der medikamentösen Therapie am multizellulären
Pasireotid Beschluss vom: 6. Dezember 2012 gültig bis: unbefristet In Kraft getreten am: 6. Dezember 2012 BAnz AT B3
 Beschluss vom: 6. Dezember 01 gültig bis: unbefristet In Kraft getreten am: 6. Dezember 01 BAnz AT 1.01.013 B3 Zugelassenenes Anwendungsgebiet Signifor ist indiziert für die Behandlung von erwachsenen
Beschluss vom: 6. Dezember 01 gültig bis: unbefristet In Kraft getreten am: 6. Dezember 01 BAnz AT 1.01.013 B3 Zugelassenenes Anwendungsgebiet Signifor ist indiziert für die Behandlung von erwachsenen
Zielgerichtete Therapie Ob Ihr wollt oder nicht
 Zielgerichtete Therapie Ob Ihr wollt oder nicht Ziad Atassi Universitätsfrauenklinik Ulm Direktor: Prof.Dr.R.Kreienberg inedome Ulm 08.07.2009 ADECATUMUMAB N = 22 NERATINIB N = 37 PERTUZUMAB N = 29 TRASTUZUMAB
Zielgerichtete Therapie Ob Ihr wollt oder nicht Ziad Atassi Universitätsfrauenklinik Ulm Direktor: Prof.Dr.R.Kreienberg inedome Ulm 08.07.2009 ADECATUMUMAB N = 22 NERATINIB N = 37 PERTUZUMAB N = 29 TRASTUZUMAB
Chronisch myeloproliferative Syndrome - CML-V TIGER
 Innere Medizin I - Onkologie, Hämatologie, Klinische Infektiologie, Klinische Immunologie, Hämostaseologie, Internistische Intensivmedizin Chronisch myeloproliferative Syndrome - CML-V TIGER Prüfplancode
Innere Medizin I - Onkologie, Hämatologie, Klinische Infektiologie, Klinische Immunologie, Hämostaseologie, Internistische Intensivmedizin Chronisch myeloproliferative Syndrome - CML-V TIGER Prüfplancode
Aktuelle Aspekte der PARP-Inhibition: Wer profitiert, wer nicht?
 Ovarialkarzinom State of the Art AGO-Symposium Aktuelle Aspekte der PARP-Inhibition: Wer profitiert, wer nicht? Pauline Wimberger Klinik und Poliklinik für Gynäkologie und Geburtshilfe Technische Universität
Ovarialkarzinom State of the Art AGO-Symposium Aktuelle Aspekte der PARP-Inhibition: Wer profitiert, wer nicht? Pauline Wimberger Klinik und Poliklinik für Gynäkologie und Geburtshilfe Technische Universität
Kardiale Toxizität beim Mamma-Ca
 Kardiale Toxizität beim Mamma-Ca René Baumann, Jürgen Dunst Klinik für Strahlentherapie Christian-Albrechts-Universität Kiel/ UKSH Kiel seit 350 Jahren ganz weit oben 1. Daten aus historischen Studien
Kardiale Toxizität beim Mamma-Ca René Baumann, Jürgen Dunst Klinik für Strahlentherapie Christian-Albrechts-Universität Kiel/ UKSH Kiel seit 350 Jahren ganz weit oben 1. Daten aus historischen Studien
Dossierbewertung A18-69 Version 1.0 Durvalumab (lokal fortgeschrittenes, inoperables NSCLC)
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Durvalumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgt auf Basis eines
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Durvalumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgt auf Basis eines
Wege ärztlicher Therapieentscheidung beim Mammakarzinom. Berlin, März Dr. med. Peter Klare Gynäkologische Onkologie
 beim Mammakarzinom Berlin, März 2015 Dr. med. Peter Klare Gynäkologische Onkologie Der Arzt das unbekannte Wesen Aufgeschlossener streng Konservativer Richtliniengläubiger Studienfetischist Angsthase Alchemist
beim Mammakarzinom Berlin, März 2015 Dr. med. Peter Klare Gynäkologische Onkologie Der Arzt das unbekannte Wesen Aufgeschlossener streng Konservativer Richtliniengläubiger Studienfetischist Angsthase Alchemist
Neues vom ASCO beim metastasierten Mammakarzinom
 Neues vom ASCO 2008 beim metastasierten Mammakarzinom 04.07.2008 Dorit Lässig Medizinische Klinik und Poliklinik III (Direktor: Prof. Dr. med. W. Hiddemann) Universität München - Standort Großhadern Übersicht
Neues vom ASCO 2008 beim metastasierten Mammakarzinom 04.07.2008 Dorit Lässig Medizinische Klinik und Poliklinik III (Direktor: Prof. Dr. med. W. Hiddemann) Universität München - Standort Großhadern Übersicht
