Wissen kompakt: Spektralphotometrie. Flexibel. Verlässlich. Persönlich.
|
|
|
- Klaus Heidrich
- vor 7 Jahren
- Abrufe
Transkript
1 K O M P E T E N Z I M L A B O R Wissen kompakt: Spektralphotometrie Flexibel. Verlässlich. Persönlich.
2 Zur Untersuchung von molekularen Eigenschaften ist die Wechselwirkung von Licht mit Molekülen eine grundlegende und sehr gut untersuchte Methode. Mit der Methode, die als Spektralphotometrie bezeichnet wird, können verschiedene Moleküle sowohl identifiziert als auch quantifiziert werden. Bei der photometrischen Messung wird die Menge der sichtbaren (VIS) und ultravioletten (UV) elektromagnetischen Strahlung (Licht) gemessen, die von den Molekülen reflektiert oder absorbiert bzw. durch die Moleküle hindurch gelassen wird. Es stellt sich die Frage, was genau gemessen werden kann bzw. was Licht absorbiert. Die Antwort ist: Alles. Messprinzip Die chemische Struktur von Molekülen führt dazu, dass elektromagnetische Strahlung spezifisch in Abhängigkeit davon absorbiert wird. Spektralphotometer werden in vielen Laboren zur Probenbeschreibung und Bestimmung unterschiedlichster Faktoren eingesetzt: Qualität von Lebensmitteln. Konzentration von DNA. Verunreiniung von Wasserproben. UV-Durchlässigkeit von Kleidung und Sonnenbrillen. UV / VIS Spektralphotometer sind so aufgebaut, dass die notwendige Lichtenergie im benötigten Spektrum im sichtbaren oder ultravioletten Bereich (~ 200 bis nm) erzeugt wird. Sichtbares Licht ist im Bereich von 400 bis 750 nm (blau bis rot) und beschreibt in der Tat den Teil des Spektrums, den ein Mensch sehen kann. Daher haben Substanzen, die in diesem Bereich absorbieren eine charakteristische Farbe, die als Komplementärfarbe bezeichnet wird. Es gibt sehr unterschiedliche Wege, auf denen Licht mit Proben wechselwirken kann. Der bekannteste ist die Absorption. Licht kann die Probe aber auch durchdringen (Transmission) oder durch die Probe gebrochen werden. Ebenso kann Licht an der Oberfläche reflektiert oder gestreut werden. Die Lichtabsorption einer Probe ist die Folge der spezifischen Elektronenkonfiguration des Moleküls. Licht einer bestimmten Wellenlänge hat genau die Energie, die gebraucht wird, um Elektronen innerhalb des Moleküls von ihrem Grundniveau auf ein angeregtes Niveau anzuheben. Viele Moleküle haben Energiezwischenniveaus, die dazu führen, dass nicht nur exakt eine Wellenlänge absorbiert wird, sondern benachbarte Wellenlägen gleich mit. Das führt zu den charakteristischen runden Peaks in einem UV / VIS-Spektrum (Abb. 1). Der größte Teil der Absorptionsspektrometrie basiert auf elektronischen Übergängen innerhalb einer verbundenen Gruppe von Atomen. Zum Beispiel hat die -OH-Gruppe des Ethanols ein Absorptionsmaximum bei 210 nm. Die funktionelle Gruppe, die die Absorption verursacht, wird als Chromophor bezeichnet. Ein Großteil aller Moleküle hat mehr als einen Chromophor, welches zu komplexen Spektren führen kann. Diese Spektren sind charakterisch für dieses spezifische Molekül und können zur Identifizierung genutzt werden. Viele organische Verbindungen mit einfachen Doppelbindungen zwischen Nichtmetallatomen wie Kohlenstoff, Sauerstoff oder Stickstoff sowie kleine konjugierte Ringstrukturen wie Proteine und Nukleinsäuren absorbieren Licht im UV-Bereich. Größere aromatische Strukturen verschieben das Absorbtionsmaximum in Richtung des sichtbaren Lichts. Ein Beispiel ist TMB, welches oft als Substrat in ELISA-Assays genutzt wird, um Antigene nachzuweisen. Gesetz von Lambert-Beer Wie wird nun die Absorbtion von Licht in einer Probe genau gemessen? Um das zu verstehen, schauen wir uns die von Lambert und Beer aufgestellten Gesetzmäßigkeiten zur Lichtabsorbtion an. Das Lambertsche Gesetz Das Beersche Gesetz Abb. 2 Das Lambertsche Gesetz besagt, dass die von einem transparenten Medium absorbierte Lichtmenge nicht von der Intensität des einfallenden Lichts beeinflusst wird. Die Anzahl der Schichten ist für die Absorption unerheblich, solange die Gesamtdicke gleich bleibt. Die von einer Probe absorbierte Menge an Licht wird sowohl als Transmission wie auch als Extinktion angegeben. Transmission (T) beschreibt das Verhältnis der Menge an Licht (I) in %, das die Probe komplett durchdringt zur ursprünglich eingestrahlten Menge an Licht (I 0 ) von l T = l * 100% 0 Wenn die Konzentration des gesuchten Moleküls in der Proben lösung ansteigt, fällt als Folge dessen der Transmissionswert exponentiell ab. Für eine etwas einfachere Betrachtung beschreibt das Beersche Gesetz die Absorption des Lichtes in der Probe: Es besagt, dass der dekadische Logarithmus der Transmission proportional der Absorption (A) ist, da das Verhältnis von Absorption zu Konzentration des absorbierenden Moleküls Abb. 1: Elektronenniveau und UV-Spektrum Abb.3: Der molare Extinktionskoeffizient ε
3 linear verläuft. Absorption entspricht dabei der Konzentration, multipliziert mit der Wellenlänge des Lichts, multipliziert mit dem molaren Extink - tionskoeffizienten (ε). Der molare Extinktionskoeffizient eines Moleküls ist dabei abhängig vom ph-wert und der Wellenlänge. Der Auftragung von Absorbtion (A) gegen Konzentration (c) ergibt eine Gerade mit der Steigung (ε), welches die lineare Beziehung zwischen Lichttransmission und Probenkonzentration des Beerschen Gesetzes beschreibt. Als Resultat ergibt sich das Lambert-Beersche Gesetz: Die mit Abstand am häufigsten verwendeten Lichtquellen sind die Wolfram-Halogenlampe für den sichtbaren Bereich (VIS-Bereich), die Deuteriumlampe für den ultravioletten Bereich (UV-Bereich) sowie die Xenon-Blitzlampe (UV / VIS-Bereich). Für die Arbeit im VIS-Bereich bzw. für reine VIS-Photometer genügt eine Halogenlampe, da das abgestrahlte Licht im Bereich von nm liegt und somit den gesamten sichtbaren Bereich abdeckt. Photometer, die auch im UV-Bereich messen, nutzen entweder Deuteriumlampen, um Licht im Bereich von nm zu erlg l 0 = εcd l Schickt man Licht durch ein absorbierendes Medium, so nimmt seine Intensität dabei exponentiell ab. Deutlich wird, dass mit steigender Absorption die Menge des trans - mittierten Lichtes extrem abfällt. Das führt dazu, dass Messungen bei hoher Absorption oft außerhalb des linearen Messbereichs der Geräte durchgeführt werden. Diese Messungen sind kein verlässlicher Indikator für die Konzentration der absorbierenden Moleküle und weichen damit vom Beerschen Gesetz ab. Ein weiterer Faktor, der eine korrekte Messung beeinträchtigen kann, ist Streulicht. Als Streulicht bezeichnet man Strahlung, die außerhalb der für die Messung ausgewählten bzw. gewünschten Wellenlängen auf die Probe trifft. Eine potentielle Fehlerquelle ist auch die Probe, in der verschiedene Effekte wie Polymerisation oder Ionisation auftreten können. All die genannten Faktoren können der Grund für ein ungenaues Messergebnis sein. Optischer Aufbau Zunächst muss ein Photometer folgende Ausstattung besitzen: Lichtquelle Möglichkeit Wellenlängen auszuwählen bzw. zu filtern Probenhalter Detektor Auswertungsmöglichkeit Abb.4: Lambert-Beersches Gesetz In welchem Verhältnis stehen nun Absorption und Transmission: 1A Absorption entspricht 10 % transmittiertem Licht 2A Absorption entspricht 1 % transmittiertem Licht 3A Absorption entspricht 0,1 % transmittiertem Licht 4A Absorption entspricht 0,01 % transmittiertem Licht Abb. 5: Aufbau eines Photometers
4 halten oder Xenon-Blitzlampen, welche das Spektrum von nm abdecken können. Eine Deuteriumlampe emittiert nach Einschalten des Photometers UV-Licht mit sehr konstanter Stärke, während die Xenon-Blitzlampe nur während der Messung per Gasentladung Licht erzeugt. Aufgrund des konstanten Lichtstroms gilt die Deuteriumlampe als präziser. Sie muss jedoch in regelmäßigen Abständen ausgewechselt werden. Die Xenon- Blitzlampe hingegen zeichnet sich durch eine extrem lange Lebensdauer aus, hat jedoch durch die notwendige Integration über die Zeit aufgrund der vielen einzelnen Lichtblitze eine etwas niedrigere Reproduzierbarkeit. Das von der Lichtquelle erzeugte Licht muss nun gefiltert oder speziell ausgewählt werden, damit nur die gewünschten Wellenlängen auf die Probe treffen. Eine einfache Methode der Filterung ist die Nutzung eines Absorptionsfilters aus gefärbtem Glas, der nur für bestimmte Wellenlängen durchlässig ist und alle anderen Wellenlängen absorbiert. Photometer mit Absorptionsfiltern werden auch Kolorimeter genannt. Anspruchsvoller und leistungsfähiger ist bereits der Interferenzfilter, der den Effekt der Interferenz nutzt, um Licht bestimmter Wellenlägen zu brechen und schmale Bandbreiten auszustrahlen. Küvetten Der klassische Probenhalter in einem Photometer ist für eine 10 mm Küvette, in der Regel aus Quarzglas, ausgelegt. Die besondere Eigenschaft von Quarzglas, weder im VIS noch im UV-Bereich, Licht zu absorbieren, kommt hier zum Tragen. Die meisten Arten von Plastikküvetten absorbieren Licht im UV-Bereich und sind daher nicht universell geeignet (Ausnahme z. B. BRAND UV-Küvette ab 220 nm einsetzbar). Neben den weit verbreiteten 10 mm Küvetten gibt es auch andere Modelle, wie die 40 mm Küvette, für stark verdünnte Proben wie Gewässerproben oder die Mikrovolumen-Küvetten für DNA Messungen (z.b. Hellma TrayCell). Ebenso existiert mittlerweile eine Vielzahl verschiedener Küvetten- und Probenhalter für besondere Anforderungen. Bei der Durchflussmessung etwa wird mittels einer Pumpe, ein soge nann - ter Sipper, ein kontinuierlicher Probenstrom durch die Küvette gepumpt, um einen repräsentativen Durchschnittswert oder auch Kinetiken, also Veränderungen über die Zeit, zu erhalten. Folienhalter erlauben die Messung größerer lichtdurchlässiger Objekte, wie u. a. Sonnenbrillengläser auf deren UVA / UVB Durchlässigkeit. Temperierbare Küvettenhalter sind ebenso erhältlich wie Küvettenwechsler mit z. B. 8 Plätzen. Der Küvettenwechsler erlaubt die schnelle Messung einer größeren Anzahl Proben. Abb. 6: Auflösung und Abhängigkeit der optischen Bandbreite Moderne Laborphotometer nutzen hingegen einen Monochromator, der über ein Prisma bzw. ein optisches Gitter bestimmte Wellenlängen sehr effizient emittiert. Ein Monochromator liefert Licht mit einer deutlich höheren aufgelösten, schmaleren Bandbreite als ein konventioneller Absorptionsfilter. Da beliebige Wellenlängen ausgewählt werden können, erlaubt er auch die Messung eines Spektrums, d.h. das Absorptionsverhaltens einer Probe über alle Wellenlängen im Messbereich. Die Analyse von Spektren ergibt viele Information über die vermessenen Proben. Während einer Konzentrationsbestimmung von DNA wird beispielswiese die Probe im Bereich von nm gemessen. Das Absorptionsmaximum von DNA liegt bei 260 nm. Der ausgegebene Wert dient als Grundlage für die Bestimmung der Konzentration. Absorption bei Werten über oder unter 260 nm gibt dem Anwender darüber hinaus Aufschluss über die Reinheit der DNA. Absorption bei Werten unterhalb von 260 nm weist auf Reste von Substanzen wie Phenol oder Guanidin HCl hin, die während der Probenvorbereitung genutzt wurden. Absorption bei Werten über 260 nm ist ein Indiz für die Kontamination der DNA mit Proteinen. Unabhängig von der Art die gewünschte Wellenlänge auszuwählen ist es wichtig, die Funktion der spektralen Bandbreite zu verstehen. Je nach Anwendung kann eine kleinere Bandbreite nötig sein, um schmale Peaks in einer Probe zu finden (Abb. 6). Abb. 7: Küvettenwechsler Detektor Sobald das Licht die Probe durchdrungen hat, muss es reproduzierbar gemessen werden. Hierzu gibt es viele verschiedene Methoden. Bei der Detektion mittels Photodiode wird das auf das aktive Zentrum der Elektrode fallende Licht in einen kleinen Elektronenfluss umgewandelt, der als elektrischer Strom gemessen werden kann. Ebenfalls eine gängige Methode ist die Messung per Diodenarray oder CCD Sensor. In einem Diodenarray sind viele optisch aktive Elemente linear oder in eine Matrix angebracht. So kann das gesamte optische Spektrum gleichzeitig gemessen werden. Eine Siliziumphotodiode ist empfindlicher für kleine Lichtmengen, ein Diodenarry ist wesentlich robuster, da keine beweglichen Teile verbaut werden. Zudem dauert eine Messung nur wenige Sekunden. Wie kommen nun all diese Elemente in einem Kolorimeter oder UV / VIS Spektrophotometer zusammen? Ein einfaches Photometer verfügt über eine Halogenlampe als Lichtquelle, einen Absorptionsfilter und einen 10 mm Küvettenhalter. Mit dieser Ausstattung können Routinemessungen im VIS Bereich durchgeführt werden.
5 Libra S12 Die Lichtleitung kann auch über Glasfaser erfolgen. Abb. 10: Einstrahlphotometer mit Glasfaser und Referenzstrahl Ein komplexerer Aufbau wird dagegen im Einstrahlphotometer realisiert (Abb. 8). Als Lichtquelle kommt hier neben der Halogenlampe auch eine Deuteriumlampe zum Einsatz, um im UV-Bereich messen zu können. Die Wellenlängenauswahl erfolgt über einen Monochromator während ein Photodioden-Detektor das aufgefangene Licht misst. Als Probenhalter stehen hier neben dem 10 mm Küvettenhalter auch beheizbare Probenhalter sowie ein Rundküvettenhalter für Reagenzgläser zur Auswahl. FoodALYT Photometer Abb. 8: Aufbau eines Einstrahlphotometers Noch eine Stufe höher stehen die Einstrahlphotometer mit Referenzstrahl (eng: Split Beam). In diesem Fall ist eine Xenon-Blitzlampe verbaut, um sowohl Licht im UV als auch im VIS Bereich zu erzeugen. Ein Monochromator regelt die Wellenlängenauswahl. Das Licht der Lampe wird hier vor Auftreffen auf die Probe geteilt (gesplittet). Der so abgespaltene Teil des Lichts, der nicht auf die Probe trifft, wird mit einem separaten Detek - tor gemessen und dient zur Korrektur des Mess ergebnisses (Abb. 9). Für höchste Ansprüche, wie z. B. in der Pharmaindustrie, werden Zweistrahlphotometer (eng. Double Beam) verwendet (Abb. 11). Als Lichtquelle ist hier wieder eine Halogenlampe für den VIS- und eine Deuteriumlampe für den UV-Bereich verbaut. Der hochpräzise Monochromator erlaubt es, die Bandbreite zwischen 0,5 und 4 mm zu variieren. Besonders schmale Bandbreiten wie 0,5 mm werden bei komplexen Proben mit sehr steilen und schmalen Absorptionsmaxima genutzt, um diese sauber zu trennen. Da eine Halbierung der Bandbreite immer auch eine Viertelung der Lichtenergie bedeutet, ist es oft sinnvoll, nicht mit der kleinsten technisch möglichen Bandbreite zu messen, um ein besseres, rauschärmeres Spektrum zu bekommen. Größere Bandbreiten verbessern das Signal- / Rauschverhältnis. Doppelstrahlphotometer messen gleichzeitig die tatsächliche Probe und eine Referenzprobe. Sie eignen sich dadurch insbesondere für komplexe Messungen bei denen sehr präzise gemessen werden muss oder solche mit ständig wechselnder Referenzprobe. Abb. 9: Biochrom Photometer mit Referenzstrahl Abb. 11: Zweistrahlphotometer
6 Moderne Geräte werden zunehmend auch mit einer leistungsfähigen internen Software ausgestattet, die oft mit Touchscreens direkt am Gerät bedient werden kann. Daneben gibt es leistungsfähige Software für die Steuerung und Datenaufnahme, die auf einem separaten PC installiert ist und verschiedene Anforderungen erfüllt (z. B. 21 CFR Part 11). Die Auswahl des richtigen Gerätes, ob Kolorimeter oder UV / VIS Spektralphotometer, erfordert ein gutes Verständnis für die Anwendung und die technischen Eigenschaften des Gerätes. Libra S80 Zusammenfassung Wenn die Ansprüche an die Messung relativ gering sind, wie etwa bei der Messung von farbigen Lösungen, ist ein einfaches Einstrahlphotometer oder Kolorimeter ausreichend. Ein höherwertiges Gerät würde ebenfalls präzise Ergebnisse liefern, die eigentlichen Anforderungen der Anwendung aber bei weitem übersteigen. Dieses führt zu unnötig höheren Anschaffungs- und Unterhaltskosten. Einfache Geräte eignen sich gut für die Demonstration chemischer und physikalischer Grundprinzipien, z. B. in Schullaboren. Komplexere Messungen, wie etwa Konzentrations- und Reinheitsbestimmung von DNA, erfordern leistungs - stärkere Geräte, die auch im UV-Bereich messen und Spektren aufnehmen können. Die Transmission von Strahlung durch Sonnenbrillengläser benötigt zudem den nötigen Platz im Probenraum. Pharmazeutische und andere spezielle Anwendungen sind dann die Domäne der High- End Zweistrahlphotometer mit variabler Bandbreite, die höchsten Ansprüchen gerecht werden Gehrden / Hannover Elbingeröder Straße 1 Telefon / Hamburg Neuer Höltigbaum 30 Telefon 040 / Markkleeberg Hauptstraße 130 Telefon / VERTRIEBSBÜROS Berlin Telefon / Braunschweig Telefon / Essen Telefon 0201 / Frankfurt Telefon 0160 / Göttingen Telefon 0551 / Heidelberg Telefon 0151 / Kiel Telefon 040 / Magdeburg Telefon / Münster Telefon 0421 / Nürnberg Telefon 089 / Osnabrück Telefon 0421 / Rostock Telefon / Ruhrgebiet Telefon / Ulm Telefon 089 / Gerne stehen wir Ihnen auch persönlich für eine Beratung zur Verfügung. Schubert & Weiss OMNILAB München Fromundstraße 34 Telefon 089 / OMNILAB baltic 1002, Riga / Lettland Maza Nometnu iela 45A Telefon Robert-Hooke-Straße Bremen Telefon 0421 / info@omnilab.de Flexibel. Verlässlich. Persönlich. OMNILAB Laboratuvar Malzemeleri San. ve Tic. Ltd. Sti Mersinli / Izmir / Türkei 1201 / 1 Sk. No:2 Su Plaza K:5 / 502 Telefon
Seminar: Photometrie
 Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
 Die Farbstofflösung in einer Küvette absorbiert 90% des einfallenden Lichtes. Welche Extinktion hat diese Lösung? 0 0,9 1,9 keine der Aussagen ist richtig Eine Küvette mit einer wässrigen Farbstofflösung
Die Farbstofflösung in einer Küvette absorbiert 90% des einfallenden Lichtes. Welche Extinktion hat diese Lösung? 0 0,9 1,9 keine der Aussagen ist richtig Eine Küvette mit einer wässrigen Farbstofflösung
Laborpraktikum Sensorik. Versuch. Optische Konzentrations- bestimmung MS 2
 Otto-von-Guericke-Universität Magdeburg Fakultät für Elektrotechnik und Informationstechnik Institut für Mikro- und Sensorsysteme (IMOS) Laborpraktikum Sensorik Versuch Optische Konzentrations- bestimmung
Otto-von-Guericke-Universität Magdeburg Fakultät für Elektrotechnik und Informationstechnik Institut für Mikro- und Sensorsysteme (IMOS) Laborpraktikum Sensorik Versuch Optische Konzentrations- bestimmung
Wechselwirkung zwischen Licht und chemischen Verbindungen
 Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
GRUNDLAGEN DER SPEKTROPHOTOMETRIE
 11 GRUNDLAGEN DER SPEKTROPHOTOMETRE Materie erscheint uns farbig, wenn sie aus dem einfallenden weißen Licht einen bestimmten spektralen Teil absorbiert. Als Farbe nehmen wir den reflektierten Anteil des
11 GRUNDLAGEN DER SPEKTROPHOTOMETRE Materie erscheint uns farbig, wenn sie aus dem einfallenden weißen Licht einen bestimmten spektralen Teil absorbiert. Als Farbe nehmen wir den reflektierten Anteil des
Protokoll zum Versuch 50: Photometrie vom Thema: Photometrische Fe 2+ -Konzentrationsbestimmung mit Phenanthrolin
 Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
Grundlagen der photometrischen Messung
 Grundlagen der photometrischen Messung Teil 1: Grundlagen, Optik, AQS, Testsätze (I) 2015 WTW GmbH. [ Juni 2015] Einführung Phos (griech.) für Licht => Photometrie ist ein Messverfahren, bei dem mit Hilfe
Grundlagen der photometrischen Messung Teil 1: Grundlagen, Optik, AQS, Testsätze (I) 2015 WTW GmbH. [ Juni 2015] Einführung Phos (griech.) für Licht => Photometrie ist ein Messverfahren, bei dem mit Hilfe
Spektroskopie-Seminar SS UV-Vis-Spektroskopie. UV-Vis-Spektroskopie
 UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1. Lambert Beer sches Gesetz - Zerfall des Manganoxalations
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Physikalische Chemie: Kinetik
 Physikalische Chemie: Kinetik Prof. Thiemann SS 2002 Protokoll Versuch 2 «Die ph-abhängigkeit der Solvolysegeschwindigkeit von Malachitgrün» 1 Inhalt: 1. Theorie 2. Zusatzfragen Bau eines UV-Spektralphotometers
Physikalische Chemie: Kinetik Prof. Thiemann SS 2002 Protokoll Versuch 2 «Die ph-abhängigkeit der Solvolysegeschwindigkeit von Malachitgrün» 1 Inhalt: 1. Theorie 2. Zusatzfragen Bau eines UV-Spektralphotometers
1. Blue-curacao 1.1. Die durchgelassene Lichtintensität I ist bei konstanter Konzentration von der Schichtdicke abhängig: d 1 < d 2
 1. Blue-curacao 1.1 Viele Getränke sind aus rein optischen Gründen mit Lebensmittelfarbstoffen angefärbt. So auch Blue-curacao. Der Likör enthält den Lebensmittelfarbstoff E 133. (Erioglaucin A (Brillant
1. Blue-curacao 1.1 Viele Getränke sind aus rein optischen Gründen mit Lebensmittelfarbstoffen angefärbt. So auch Blue-curacao. Der Likör enthält den Lebensmittelfarbstoff E 133. (Erioglaucin A (Brillant
Photom etrieren Photometrie Fraunhofer sche Linien
 17 Photometrieren Die Spektroskopie, auch Spektralphotometrie, Spektrophotometrie oder einfach nur Photometrie genannt, umfasst eine Anzahl experimenteller Messverfahren, die generell die Wechselwirkung
17 Photometrieren Die Spektroskopie, auch Spektralphotometrie, Spektrophotometrie oder einfach nur Photometrie genannt, umfasst eine Anzahl experimenteller Messverfahren, die generell die Wechselwirkung
Versuch K2 Photometrische Messung
 Versuch K2 Photometrische Messung Aufgaben: 1. Messung der Extinktion von Mangan(III)-oxalat bei verschiedenen Wellenlängen. 2. Bestimmung der Geschwindigkeitskonstanten des Zerfalls des komplexen Mangan(III)-oxalations
Versuch K2 Photometrische Messung Aufgaben: 1. Messung der Extinktion von Mangan(III)-oxalat bei verschiedenen Wellenlängen. 2. Bestimmung der Geschwindigkeitskonstanten des Zerfalls des komplexen Mangan(III)-oxalations
Wie Heavy Metal ist der Boden?
 Wie Heavy Metal ist der Boden? Inhaltsverzeichnis 1. Entstehung und Ausbreitung von Schwermetallen im Boden 2. Analytische Aufschlussverfahren 3. Grundlagen der UV-VIS- und AAS-Spektroskopie 2 Schwermetalle
Wie Heavy Metal ist der Boden? Inhaltsverzeichnis 1. Entstehung und Ausbreitung von Schwermetallen im Boden 2. Analytische Aufschlussverfahren 3. Grundlagen der UV-VIS- und AAS-Spektroskopie 2 Schwermetalle
Flüssigkeitschromatographie
 Flüssigkeitschromatographie Flüssigkeitschromatographie Einteilung nach Druck: LC MPLC: HPLC: Liquid chromatography Flüssigkeitschromatographie Medium performance (pressure) LC Mittelleistungs (druck)
Flüssigkeitschromatographie Flüssigkeitschromatographie Einteilung nach Druck: LC MPLC: HPLC: Liquid chromatography Flüssigkeitschromatographie Medium performance (pressure) LC Mittelleistungs (druck)
Kontrollaufgaben zur Optik
 Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
So messen Sie die Absorption
 Versuch 9 b Absorptionsspektroskopie, Beer-Lambert-Gesetz Einleitung Das Spektrophotometer ist ein wichtiges Hilfsmittel für den Lebenswissenschaftler. Wenn wir die molekularen Grundlagen biologischer
Versuch 9 b Absorptionsspektroskopie, Beer-Lambert-Gesetz Einleitung Das Spektrophotometer ist ein wichtiges Hilfsmittel für den Lebenswissenschaftler. Wenn wir die molekularen Grundlagen biologischer
Spektroskopie im sichtbaren und UV-Bereich
 Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
1. Ziel des Versuchs. 2. Versuchsaufbau und Durchführung. Dennis Fischer Gruppe 9 Magdalena Boeddinghaus
 Versuch Nr. 7: Lambert-Beersches Gesetz 1. Ziel des Versuchs Ziel des Versuches ist es, die Abhängigkeiten der Absorption eines Stoffes von der Konzentration, der Schichtdicke und der Wellenlänge zu ermitteln.
Versuch Nr. 7: Lambert-Beersches Gesetz 1. Ziel des Versuchs Ziel des Versuches ist es, die Abhängigkeiten der Absorption eines Stoffes von der Konzentration, der Schichtdicke und der Wellenlänge zu ermitteln.
2 Einführung in Licht und Farbe
 2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
UviLine 9100/9400: Die neue Spektralphotometer-Serie von SCHOTT Instruments
 UviLine 9100/9400: Die neue Spektralphotometer-Serie von SCHOTT Instruments Zwei komplett neue Hochleistungs- Einstrahlphotometer: UviLine 9100 für Messungen im VIS Bereich von 320 1100 nm UviLine 9400
UviLine 9100/9400: Die neue Spektralphotometer-Serie von SCHOTT Instruments Zwei komplett neue Hochleistungs- Einstrahlphotometer: UviLine 9100 für Messungen im VIS Bereich von 320 1100 nm UviLine 9400
Flexibel. Verlässlich. Persönlich.
 K O M P E T E N Z I M L A B O R Flexibel. Verlässlich. Persönlich. Wir versprechen nur, was wir auch halten können und halten, was wir versprechen. Kompetenz im Labor Kompetente Beratung, innovative Produkte
K O M P E T E N Z I M L A B O R Flexibel. Verlässlich. Persönlich. Wir versprechen nur, was wir auch halten können und halten, was wir versprechen. Kompetenz im Labor Kompetente Beratung, innovative Produkte
21-1. K=f c I=I0 e f c d
 21-1 Lichtabsorption 1. Vorbereitung : Extinktions- und Absorptionskonstante, mittlere Reichweite, Unterscheidung zwischen stark und schwach absorbierenden Stoffen, Lambert-Beersches Gesetz, Erklärung
21-1 Lichtabsorption 1. Vorbereitung : Extinktions- und Absorptionskonstante, mittlere Reichweite, Unterscheidung zwischen stark und schwach absorbierenden Stoffen, Lambert-Beersches Gesetz, Erklärung
Quantenphysik in der Sekundarstufe I
 Quantenphysik in der Sekundarstufe I Atomphysik Dr. Holger Hauptmann Europa-Gymnasium Wörth holger.hauptmann@gmx.de Quantenphysik in der Sek I, Folie 1 Inhalt 1. Der Aufbau der Atome 2. Größe und Dichte
Quantenphysik in der Sekundarstufe I Atomphysik Dr. Holger Hauptmann Europa-Gymnasium Wörth holger.hauptmann@gmx.de Quantenphysik in der Sek I, Folie 1 Inhalt 1. Der Aufbau der Atome 2. Größe und Dichte
TrayCell Faseroptische Ultra-Mikro-Messzelle für die UV/Vis-basierte Bioanalytik. Hellma. Where precision becomes an art.
 Hellma. Where precision becomes an art. TrayCell Faseroptische Ultra-Mikro-Messzelle für die UV/Vis-basierte Bioanalytik 2008 by Hellma www.hellma-worldwide.com Die TrayCell Einzigartig. Präzise. Flexibel.
Hellma. Where precision becomes an art. TrayCell Faseroptische Ultra-Mikro-Messzelle für die UV/Vis-basierte Bioanalytik 2008 by Hellma www.hellma-worldwide.com Die TrayCell Einzigartig. Präzise. Flexibel.
. Nur wenn ε m (λ 1 ) = ε m (λ 2 ), dann ist E = ε m c d.
 Das Lambert-Beersche Gesetz gilt nur für monochromatisches Licht: Wird eine Substanz mit dem molaren Extinktionskoeffizienten ε m (λ) bei der Wellenlänge λ 1 mit der Intensität I 1 und bei der Wellenlänge
Das Lambert-Beersche Gesetz gilt nur für monochromatisches Licht: Wird eine Substanz mit dem molaren Extinktionskoeffizienten ε m (λ) bei der Wellenlänge λ 1 mit der Intensität I 1 und bei der Wellenlänge
Praktikum Optische Technologien, Protokoll Versuch Absorptionsmessung
 Praktikum Optische Technologien, Protokoll Versuch Absorptionsmessung 09.0.204 Ort: Laserlabor der Fachhochschule Aachen Campus Jülich Inhaltsverzeichnis Einleitung 2 Fragen zur Vorbereitung 2 3 Geräteliste
Praktikum Optische Technologien, Protokoll Versuch Absorptionsmessung 09.0.204 Ort: Laserlabor der Fachhochschule Aachen Campus Jülich Inhaltsverzeichnis Einleitung 2 Fragen zur Vorbereitung 2 3 Geräteliste
K1: Lambert-Beer`sches Gesetz
 K1: Lambert-Beer`sches Gesetz Einleitung In diesem Versuch soll die Entfärbung von Kristallviolett durch atronlauge mittels der Absorptionsspektroskopie untersucht werden. Sowohl die Reaktionskinetik als
K1: Lambert-Beer`sches Gesetz Einleitung In diesem Versuch soll die Entfärbung von Kristallviolett durch atronlauge mittels der Absorptionsspektroskopie untersucht werden. Sowohl die Reaktionskinetik als
K O M P E T E N Z I M L A B O R. Flexibel. Verlässlich. Persönlich.
 K O M P E T E N Z I M L A B O R Flexibel. Verlässlich. Persönlich. Wir versprechen nur, was wir auch halten können und halten, was wir versprechen. Kompetenz im Labor Kompetente Beratung, innovative Produkte
K O M P E T E N Z I M L A B O R Flexibel. Verlässlich. Persönlich. Wir versprechen nur, was wir auch halten können und halten, was wir versprechen. Kompetenz im Labor Kompetente Beratung, innovative Produkte
Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2
 Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2 9. Spektralphotometrische Bestimmung einer Gleichgewichtskonstanten: Lambert-Beer und Massenwirkungsgesetz
Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2 9. Spektralphotometrische Bestimmung einer Gleichgewichtskonstanten: Lambert-Beer und Massenwirkungsgesetz
Physik für Maschinenbau. Prof. Dr. Stefan Schael RWTH Aachen
 Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
Elektromagnetische Strahlung
 Elektromagnetische Strahlung 1 Absorptionsmethoden - Grundlagen Als Absorptionsmethoden bezeichnet man die Konzentrationsbestimmung einer Substanz, indem gemessen wird, wie sie die Intensität elektromagnetischer
Elektromagnetische Strahlung 1 Absorptionsmethoden - Grundlagen Als Absorptionsmethoden bezeichnet man die Konzentrationsbestimmung einer Substanz, indem gemessen wird, wie sie die Intensität elektromagnetischer
Lösungen zu den Übungen zur Einführung in die Spektroskopie für Studenten der Biologie (SS 2011)
 Universität Konstanz Fachbereich Biologie Priv.-Doz. Dr. Jörg H. Kleinschmidt http://www.biologie.uni-konstanz.de/folding/home.html Datum: 26.5.211 Lösungen zu den Übungen zur Einführung in die Spektroskopie
Universität Konstanz Fachbereich Biologie Priv.-Doz. Dr. Jörg H. Kleinschmidt http://www.biologie.uni-konstanz.de/folding/home.html Datum: 26.5.211 Lösungen zu den Übungen zur Einführung in die Spektroskopie
7. Das Bohrsche Modell des Wasserstoff-Atoms. 7.1 Stabile Elektronbahnen im Atom
 phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
Quantenphysik in der Sekundarstufe I
 Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
AnC I Protokoll: 6.1 Extraktionsphotometrische Bestimmung von Cobalt mit HDEHP! SS Analytische Chemie I. Versuchsprotokoll
 Analytische Chemie I Versuchsprotokoll 6.1 Extraktionsphotometrische Bestimmung von Mikromengen an Cobalt mit Phosphorsäure-bis- (2-ethylhexylester) (HDEHP) 1.! Theoretischer Hintergrund Zur Analyse wird
Analytische Chemie I Versuchsprotokoll 6.1 Extraktionsphotometrische Bestimmung von Mikromengen an Cobalt mit Phosphorsäure-bis- (2-ethylhexylester) (HDEHP) 1.! Theoretischer Hintergrund Zur Analyse wird
23. Mai 2000 Physikalisch-Chemisches Praktikum Versuch Nr. 2
 23. Mai 2000 Physikalisch-Chemisches Praktikum Versuch Nr. 2 Thema: Aufgabenstellung: Material: ph-abhängigkeit einer Solvolysereaktion 1. Bestimmung der Geschwindigkeitskonstanten für die Reaktion von
23. Mai 2000 Physikalisch-Chemisches Praktikum Versuch Nr. 2 Thema: Aufgabenstellung: Material: ph-abhängigkeit einer Solvolysereaktion 1. Bestimmung der Geschwindigkeitskonstanten für die Reaktion von
Konzentrationsbestimmung von Calcium und Cadmium in Meerwasser mittels Atomabsorptionsspektroskopie
 Praktikum Physikalische und Analytische Chemie Versuch Atomabsorptionsspektroskopie (AAS) Frühjahrssemester 2012 Konzentrationsbestimmung von Calcium und Cadmium in Meerwasser mittels Atomabsorptionsspektroskopie
Praktikum Physikalische und Analytische Chemie Versuch Atomabsorptionsspektroskopie (AAS) Frühjahrssemester 2012 Konzentrationsbestimmung von Calcium und Cadmium in Meerwasser mittels Atomabsorptionsspektroskopie
NG Brechzahl von Glas
 NG Brechzahl von Glas Blockpraktikum Frühjahr 2007 25. April 2007 Inhaltsverzeichnis 1 Einführung 2 2 Theoretische Grundlagen 2 2.1 Geometrische Optik und Wellenoptik.......... 2 2.2 Linear polarisiertes
NG Brechzahl von Glas Blockpraktikum Frühjahr 2007 25. April 2007 Inhaltsverzeichnis 1 Einführung 2 2 Theoretische Grundlagen 2 2.1 Geometrische Optik und Wellenoptik.......... 2 2.2 Linear polarisiertes
Medizinische Biophysik Licht in der Medizin.
 4. Transmission Medizinische Biophysik Licht in der Medizin. VI. Wechselwirkungen des Lichts mit der Materie 3. Absorption e) Schwächungsgesetz f) Anwendungen (Absorptionsspektrometrie, Lambert-Beer-Gesetz)
4. Transmission Medizinische Biophysik Licht in der Medizin. VI. Wechselwirkungen des Lichts mit der Materie 3. Absorption e) Schwächungsgesetz f) Anwendungen (Absorptionsspektrometrie, Lambert-Beer-Gesetz)
2.) Welcher Kurvenverlauf deutet auf eine Abweichung vom Lambert-Beerschen Gesetz infolge Assoziation der absorbierenden Moleküle hin?
 Fragen zum Gesamtthemenbereich Analytik Spektroskopische Verfahren 1.) Welche Aussage trifft zu? a) Die Absorption A wächst proportional zur Konzentration. b) Die Transmission T wächst proportional zur
Fragen zum Gesamtthemenbereich Analytik Spektroskopische Verfahren 1.) Welche Aussage trifft zu? a) Die Absorption A wächst proportional zur Konzentration. b) Die Transmission T wächst proportional zur
Das Spektrum elektromagnetischer Strahlung
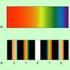 Druckversion: Virtuelles Labor: UV-Vis-Spektroskopie 1 Versuchsziel ufnahme eines Spektrums von Sulfanilamid (SN) und Sulfathiazol (ST) zur Ermittlung der maximalen Wellenlänge max und der entsprechenden
Druckversion: Virtuelles Labor: UV-Vis-Spektroskopie 1 Versuchsziel ufnahme eines Spektrums von Sulfanilamid (SN) und Sulfathiazol (ST) zur Ermittlung der maximalen Wellenlänge max und der entsprechenden
Biostatistik, Winter 2018/19
 1/32 Biostatistik, Winter 2018/19 Folgen, Summen,, Lambert-Beer Prof. Dr. Achim Klenke http://www.aklenke.de 2. Vorlesung: 26.10.2018 2/32 Inhalt 1 Folgen Begriffsbildung Grenzwerte 2 Summen und Produkte
1/32 Biostatistik, Winter 2018/19 Folgen, Summen,, Lambert-Beer Prof. Dr. Achim Klenke http://www.aklenke.de 2. Vorlesung: 26.10.2018 2/32 Inhalt 1 Folgen Begriffsbildung Grenzwerte 2 Summen und Produkte
Photometrische Analyse der Reduktion von Methylenblau mit Ascorbinsäure, Salzsäure und Lösungsmittel Einfluss
 Kinetik Physikalische Chemie Praktikum Photometrische Analyse der Reduktion von Methylenblau mit Ascorbinsäure, Salzsäure und Lösungsmittel Einfluss Author: Mark Hardmeier markh@student.ethz.ch D-BIOL
Kinetik Physikalische Chemie Praktikum Photometrische Analyse der Reduktion von Methylenblau mit Ascorbinsäure, Salzsäure und Lösungsmittel Einfluss Author: Mark Hardmeier markh@student.ethz.ch D-BIOL
FRICKE-Dosimetrie. Laborpraktikum IKTP, SS2014. Betreuer: C.Zech. Größen der Dosimetrie
 FRICKE-Dosimetrie Laborpraktikum IKTP, SS2014 Betreuer: C.Zech Dosen in der Größenordnung von kgy werden hauptsächlich bei der Modifikation von Materialien, in der Lebensmittelkonservierung, sowie in der
FRICKE-Dosimetrie Laborpraktikum IKTP, SS2014 Betreuer: C.Zech Dosen in der Größenordnung von kgy werden hauptsächlich bei der Modifikation von Materialien, in der Lebensmittelkonservierung, sowie in der
Versuch: Reaktionskinetik
 Versuch: Reaktionskinetik Befindet sich eine chemische Reaktion im thermodynamischen Gleichgewicht, so lassen sich die Bedingungen für diesen Zustand durch eine energetische Betrachtungsweise mithilfe
Versuch: Reaktionskinetik Befindet sich eine chemische Reaktion im thermodynamischen Gleichgewicht, so lassen sich die Bedingungen für diesen Zustand durch eine energetische Betrachtungsweise mithilfe
Medizinische Biophysik 6
 Eigenschaften des Lichtes Medizinische Biophysik 6 Geradlinige Ausbreitung Energietransport Licht in der Medizin. 1 Geometrische Optik Wellennatur Teilchennatur III. Teilchencharakter des Lichtes a) Lichtelektrischer
Eigenschaften des Lichtes Medizinische Biophysik 6 Geradlinige Ausbreitung Energietransport Licht in der Medizin. 1 Geometrische Optik Wellennatur Teilchennatur III. Teilchencharakter des Lichtes a) Lichtelektrischer
3 Elektronengas-Modell und Polyene
 3.1 Lernziele 1. Sie können die Anregungsenergie ΔE für den Ügang vom höchsten besetzten (HOMO) zum niedrigsten unbesetzten (LUMO) Niveau von Polyenen mit dem Elektronengas-Modell echnen. 2. Sie sind in
3.1 Lernziele 1. Sie können die Anregungsenergie ΔE für den Ügang vom höchsten besetzten (HOMO) zum niedrigsten unbesetzten (LUMO) Niveau von Polyenen mit dem Elektronengas-Modell echnen. 2. Sie sind in
Photometrie mit Pyridinnucleotiden
 Photometrie mit Pyridinnucleotiden Grundlagen der Photometrie Photometer-Arten Eppendorf-Photometer Struktur und Funktion des NADH Beispiele des optischen Tests Berechnungsverfahren Biochemie - "Photometrie
Photometrie mit Pyridinnucleotiden Grundlagen der Photometrie Photometer-Arten Eppendorf-Photometer Struktur und Funktion des NADH Beispiele des optischen Tests Berechnungsverfahren Biochemie - "Photometrie
UV/VIS-Spektroskopie
 UV/VIS-Spektroskopie Version 2, Gruppe M 14 Jorge Ferreiro, Studiengang Chemieingenieur, 4. Semester, fjorge@student.ethz.ch Natalja Früh, Studiengang Interdisziplinäre Naturwissenschaften, 4. Semester
UV/VIS-Spektroskopie Version 2, Gruppe M 14 Jorge Ferreiro, Studiengang Chemieingenieur, 4. Semester, fjorge@student.ethz.ch Natalja Früh, Studiengang Interdisziplinäre Naturwissenschaften, 4. Semester
SCHWEIZER JUGEND FORSCHT. Chemie und Materialwissenschaften
 SCHWEIZER JUGEND FORSCHT Chemie und Materialwissenschaften Studie einer ultraschnellen Fotochemischen Reaktion mit Laserspektroskopie Gianluca Schmoll Widmer Betreuer: Dr. Sandra Mosquera Vazquez, Dr.
SCHWEIZER JUGEND FORSCHT Chemie und Materialwissenschaften Studie einer ultraschnellen Fotochemischen Reaktion mit Laserspektroskopie Gianluca Schmoll Widmer Betreuer: Dr. Sandra Mosquera Vazquez, Dr.
UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie
 Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2018/19 www.ruhr-uni-bochum.de/chirality 1 Komplementärfarben Absorbiert eine Probe gelbes
Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2018/19 www.ruhr-uni-bochum.de/chirality 1 Komplementärfarben Absorbiert eine Probe gelbes
UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie
 Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Reminder: MO-Diagramm von O 2 2- MdS-1 UV/Vis-Spektroskopie
Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Reminder: MO-Diagramm von O 2 2- MdS-1 UV/Vis-Spektroskopie
Physikpraktikum für Pharmazeuten Universität Regensburg Fakultät Physik. 9. Versuch: Spektralphotometer
 Physikpraktikum für Pharmazeuten Universität Regensburg Fakultät Physik 9. Versuch: Spektralphotometer 1 Einführung Im achten Versuch haben wir gelernt, dass ein Lichtstrahl, welcher durch ein Ensemble
Physikpraktikum für Pharmazeuten Universität Regensburg Fakultät Physik 9. Versuch: Spektralphotometer 1 Einführung Im achten Versuch haben wir gelernt, dass ein Lichtstrahl, welcher durch ein Ensemble
Farbstoffe Einleitung
 Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Aufnahme einer Extinktionskurve. Themen. Prinzip. Material TEAS Photometrie, Extinktion, Verdünnung, Extinktionskurve
 Aufnahme einer TEAS Themen Photometrie, Extinktion, Verdünnung, Prinzip Eine Farbstofflösung wird zunächst hergestellt und anschließend die Extinktion bei verschiedenen Wellenlängen gemessen. Anschließend
Aufnahme einer TEAS Themen Photometrie, Extinktion, Verdünnung, Prinzip Eine Farbstofflösung wird zunächst hergestellt und anschließend die Extinktion bei verschiedenen Wellenlängen gemessen. Anschließend
12.8 Eigenschaften von elektronischen Übergängen. Übergangsfrequenz
 phys4.024 Page 1 12.8 Eigenschaften von elektronischen Übergängen Übergangsfrequenz betrachte die allgemeine Lösung ψ n der zeitabhängigen Schrödinger-Gleichung zum Energieeigenwert E n Erwartungswert
phys4.024 Page 1 12.8 Eigenschaften von elektronischen Übergängen Übergangsfrequenz betrachte die allgemeine Lösung ψ n der zeitabhängigen Schrödinger-Gleichung zum Energieeigenwert E n Erwartungswert
Welche Strahlen werden durch die Erdatmosphäre abgeschirmt? Welche Moleküle beeinflussen wesentlich die Strahlendurchlässigkeit der Atmosphäre?
 Spektren 1 Welche Strahlen werden durch die Erdatmosphäre abgeschirmt? Welche Moleküle beeinflussen wesentlich die Strahlendurchlässigkeit der Atmosphäre? Der UV- und höherenergetische Anteil wird fast
Spektren 1 Welche Strahlen werden durch die Erdatmosphäre abgeschirmt? Welche Moleküle beeinflussen wesentlich die Strahlendurchlässigkeit der Atmosphäre? Der UV- und höherenergetische Anteil wird fast
 Die Lage der Emissionsbanden der charakteristischen Röntgenstrahlung (anderer Name: Eigenstrahlung) wird bestimmt durch durch das Material der Kathode durch das Material der Anode die Größe der Anodenspannung
Die Lage der Emissionsbanden der charakteristischen Röntgenstrahlung (anderer Name: Eigenstrahlung) wird bestimmt durch durch das Material der Kathode durch das Material der Anode die Größe der Anodenspannung
Physikalisches Anfängerpraktikum Teil 2 Versuch PII 22: Lichtstreuung Auswertung
 Physikalisches Anfängerpraktikum Teil 2 Versuch PII 22: Lichtstreuung Auswertung Gruppe Mi-14: Marc A. Donges , 1060028 Tanja Pfister, 14846 05 07 12 1 1 Versuchsaufbau Der Versuch wurde
Physikalisches Anfängerpraktikum Teil 2 Versuch PII 22: Lichtstreuung Auswertung Gruppe Mi-14: Marc A. Donges , 1060028 Tanja Pfister, 14846 05 07 12 1 1 Versuchsaufbau Der Versuch wurde
Fluoreszenz. Abb. 1: Möglicher Versuchsaufbau
 Fluoreszenz Abb. 1: Möglicher Versuchsaufbau Geräteliste: UV-Lampe Geldscheintester, Schwarzlicht-Leuchtstofflampe, Halogenlampe, UV- Bandpass, Granulat mit fluoreszierendem Farbstoff, Fluoreszenzproben,
Fluoreszenz Abb. 1: Möglicher Versuchsaufbau Geräteliste: UV-Lampe Geldscheintester, Schwarzlicht-Leuchtstofflampe, Halogenlampe, UV- Bandpass, Granulat mit fluoreszierendem Farbstoff, Fluoreszenzproben,
UV/VIS-Spektroskopie
 UV/VIS-Spektroskopie 1 UV/VIS-Spektroskopie Im ersten Teil dieses Versuchs werden mittels optischer Messungen die Absolutkonzentrationen der Komponenten eines Gemischs mit einem Demonstrations-Spektrometer
UV/VIS-Spektroskopie 1 UV/VIS-Spektroskopie Im ersten Teil dieses Versuchs werden mittels optischer Messungen die Absolutkonzentrationen der Komponenten eines Gemischs mit einem Demonstrations-Spektrometer
Sensorlabor II. Versuch: FFT-IR Spektroskopie. Gruppe 1: Oliver Knaus Rodrigo Kuhfs
 Sensorlabor II Versuch: FFT-IR Spektroskopie Gruppe : Oliver Knaus Inhaltsverzeichnis Inhaltsverzeichnis... 2 2 Aufbau und Meßprinzip eines FFT IR Spektrometers... 3 2. Nachweisbare Stoffe... 4 2.2 Verwendete
Sensorlabor II Versuch: FFT-IR Spektroskopie Gruppe : Oliver Knaus Inhaltsverzeichnis Inhaltsverzeichnis... 2 2 Aufbau und Meßprinzip eines FFT IR Spektrometers... 3 2. Nachweisbare Stoffe... 4 2.2 Verwendete
Konzentrationsbestimmung von Zink, Natrium und Calcium in verschiedenen Mineralwassern mittels Atom-Absorptions-Spektroskopie
 Analytisches Physikalisches Praktikum SS 07 AAS Konzentrationsbestimmung von Zink, Natrium und Calcium in verschiedenen Mineralwassern mittels Atom-Absorptions-Spektroskopie Assistent: Markus Wälle, waelle@inorg.chem.ethz.ch
Analytisches Physikalisches Praktikum SS 07 AAS Konzentrationsbestimmung von Zink, Natrium und Calcium in verschiedenen Mineralwassern mittels Atom-Absorptions-Spektroskopie Assistent: Markus Wälle, waelle@inorg.chem.ethz.ch
Spektroskopie im sichtbaren und UV-Bereich
 Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
Fortgeschrittenenpraktikum: Ausarbeitung - Versuch 14 Optische Absorption Durchgeführt am 13. Juni 2002
 Fortgeschrittenenpraktikum: Ausarbeitung - Versuch 14 Optische Absorption Durchgeführt am 13. Juni 2002 30. Juli 2002 Gruppe 17 Christoph Moder 2234849 Michael Wack 2234088 Sebastian Mühlbauer 2218723
Fortgeschrittenenpraktikum: Ausarbeitung - Versuch 14 Optische Absorption Durchgeführt am 13. Juni 2002 30. Juli 2002 Gruppe 17 Christoph Moder 2234849 Michael Wack 2234088 Sebastian Mühlbauer 2218723
Enzymatische Katalyse
 VERSUCHSZIEL Die natürliche Braunfärbung einer aufgeschnittenen Kartoffel ist nichts anderes, als die enzymatisch oxydative Umsetzung der darin anwesenden Phenolverbindungen mit Sauerstoff zu Chinonverbindungen.
VERSUCHSZIEL Die natürliche Braunfärbung einer aufgeschnittenen Kartoffel ist nichts anderes, als die enzymatisch oxydative Umsetzung der darin anwesenden Phenolverbindungen mit Sauerstoff zu Chinonverbindungen.
Wellenlängen bei Strahlungsmessungen. im Gebiet der Meteorologie nm nm
 Die Solarstrahlung Die Sonne sendet uns ein breites Frequenzspektrum. Die elektromagnetische Strahlung der Sonne, die am oberen Rand der Erdatmosphäre einfällt, wird als extraterrestrische Sonnenstrahlung
Die Solarstrahlung Die Sonne sendet uns ein breites Frequenzspektrum. Die elektromagnetische Strahlung der Sonne, die am oberen Rand der Erdatmosphäre einfällt, wird als extraterrestrische Sonnenstrahlung
Absorptionsspektrometer im UV/VIS bestehen im wesentlichen aus 4 Bauteilen:
 2.4.2 Aufbau eines Absorptionsspektrometers N072_Absorptionsspektrometrie2_a_BAneu.doc - 1/11 Absorptionsspektrometer im UV/VIS bestehen im wesentlichen aus 4 Bauteilen: S = Strahlungsquelle M = Monochromator
2.4.2 Aufbau eines Absorptionsspektrometers N072_Absorptionsspektrometrie2_a_BAneu.doc - 1/11 Absorptionsspektrometer im UV/VIS bestehen im wesentlichen aus 4 Bauteilen: S = Strahlungsquelle M = Monochromator
KAISERSLAUTERN. Untersuchung von Lichtspektren. Lampen mit eigenem Versuchsaufbau. ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht
 ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht KAISERSLAUTERN Untersuchung von Lichtspektren bei verschiedenen Lampen mit eigenem Versuchsaufbau Johannes Kührt Schule: Burggymnasium Burgstraße
ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht KAISERSLAUTERN Untersuchung von Lichtspektren bei verschiedenen Lampen mit eigenem Versuchsaufbau Johannes Kührt Schule: Burggymnasium Burgstraße
Versuch O08: Polarisation des Lichtes
 Versuch O08: Polarisation des Lichtes 5. März 2014 I Lernziele Wellenoptik Longitudinal- und Transversalwellen Elektromagnetische Wellen II Physikalische Grundlagen Nachweismethode Elektromagnetische Wellen
Versuch O08: Polarisation des Lichtes 5. März 2014 I Lernziele Wellenoptik Longitudinal- und Transversalwellen Elektromagnetische Wellen II Physikalische Grundlagen Nachweismethode Elektromagnetische Wellen
Atomabsorptionsspektrometrie (AAS)
 Atomabsorptionsspektrometrie (AAS) Zusammenfassung Mit Hilfe eines Atomabsorptionsspektrometers wurden die Konzentrationen von Arsen und Lithium in drei verschieden Mineralwässern bestimmt. Resultate Konzentrationen
Atomabsorptionsspektrometrie (AAS) Zusammenfassung Mit Hilfe eines Atomabsorptionsspektrometers wurden die Konzentrationen von Arsen und Lithium in drei verschieden Mineralwässern bestimmt. Resultate Konzentrationen
Die Grundlagen der Spektroskopie: Theorie FÜR EINE BESSERE WISSENSCHAFT AGILENT AND YOU
 Die Grundlagen der Spektroskopie: Theorie FÜR EINE BESSERE WISSENSCHAFT AGILENT AND YOU 1 Agilent engagiert sich für Ausbildung und Lehre und möchte den Zugang zu firmeneigenem Material ermöglichen. Diese
Die Grundlagen der Spektroskopie: Theorie FÜR EINE BESSERE WISSENSCHAFT AGILENT AND YOU 1 Agilent engagiert sich für Ausbildung und Lehre und möchte den Zugang zu firmeneigenem Material ermöglichen. Diese
Lehrerinformation Brillantblau
 Lehrerinformation: Allgemeines zu Triarylmethylfarbstoffen Viele Gegenstände, mit denen wir tagtäglich in Berührung kommen, sind farbig. Letztlich ist aber all diese Farbenpracht auf die chemischen Verbindungen
Lehrerinformation: Allgemeines zu Triarylmethylfarbstoffen Viele Gegenstände, mit denen wir tagtäglich in Berührung kommen, sind farbig. Letztlich ist aber all diese Farbenpracht auf die chemischen Verbindungen
5 Elektronengas-Modell und Polyene
 5.1 Übersicht und Lernziele Übersicht Im vorherigen Kapitel haben Sie gelernt, das Elektronengas-Modell am Beispiel der Cyanin-Farbstoffe anzuwenden. Sie konnten überprüfen, dass die Berechnungen für die
5.1 Übersicht und Lernziele Übersicht Im vorherigen Kapitel haben Sie gelernt, das Elektronengas-Modell am Beispiel der Cyanin-Farbstoffe anzuwenden. Sie konnten überprüfen, dass die Berechnungen für die
Versuchsprotokoll Kapitel 6
 Versuchsprotokoll Kapitel 6 Felix, Sebastian, Tobias, Raphael, Joel 1. Semester 21 Inhaltsverzeichnis Einleitung...3 Versuch 6.1...3 Einwaagen und Herstellung der Verdünnungen...3 Photospektrometrisches
Versuchsprotokoll Kapitel 6 Felix, Sebastian, Tobias, Raphael, Joel 1. Semester 21 Inhaltsverzeichnis Einleitung...3 Versuch 6.1...3 Einwaagen und Herstellung der Verdünnungen...3 Photospektrometrisches
Wärmestrahlung. Einfallende Strahlung = absorbierte Strahlung + reflektierte Strahlung
 Wärmestrahlung Gleichheit von Absorptions- und Emissionsgrad Zwei Flächen auf gleicher Temperatur T 1 stehen sich gegenüber. dunkelgrau hellgrau Der Wärmefluss durch Strahlung muss in beiden Richtungen
Wärmestrahlung Gleichheit von Absorptions- und Emissionsgrad Zwei Flächen auf gleicher Temperatur T 1 stehen sich gegenüber. dunkelgrau hellgrau Der Wärmefluss durch Strahlung muss in beiden Richtungen
Versuchsprotokoll: Aminosäure- und Proteinbestimmung
 Versuchsprotokoll: Aminosäure- und Proteinbestimmung a) Proteinbestimmung mit Biuret-Reagenz 1.1. Einleitung Das Ziel des Versuchs ist es nach Aufstellen einer Eichgerade mit gegeben Konzentrationen, die
Versuchsprotokoll: Aminosäure- und Proteinbestimmung a) Proteinbestimmung mit Biuret-Reagenz 1.1. Einleitung Das Ziel des Versuchs ist es nach Aufstellen einer Eichgerade mit gegeben Konzentrationen, die
Seminar zum Praktikumsversuch: Optische Spektroskopie. Tilman Zscheckel Otto-Schott-Institut
 Seminar zum Praktikumsversuch: Optische Spektroskopie Tilman Zscheckel Otto-Schott-Institut Optische Spektroskopie Definition: - qualitative oder quantitative Analyse, die auf der Wechselwirkung von Licht
Seminar zum Praktikumsversuch: Optische Spektroskopie Tilman Zscheckel Otto-Schott-Institut Optische Spektroskopie Definition: - qualitative oder quantitative Analyse, die auf der Wechselwirkung von Licht
Besprechung am
 PN2 Einführung in die Physik für Chemiker 2 Prof. J. Lipfert SS 2016 Übungsblatt 10 Übungsblatt 10 Besprechung am 27.6.2016 Aufgabe 1 Interferenz an dünnen Schichten. Weißes Licht fällt unter einem Winkel
PN2 Einführung in die Physik für Chemiker 2 Prof. J. Lipfert SS 2016 Übungsblatt 10 Übungsblatt 10 Besprechung am 27.6.2016 Aufgabe 1 Interferenz an dünnen Schichten. Weißes Licht fällt unter einem Winkel
Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: Die Essentials der letzten Vorlesung Funktionelle Gruppen
Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: Die Essentials der letzten Vorlesung Funktionelle Gruppen
Kimble Laborglas. Flexibel. Verlässlich. Persönlich.
 K O M P E T E N Z I M L A B O R Kimble Laborglas Flexibel. Verlässlich. Persönlich. Kimble Chase Als führender Hersteller von Laborglasartikeln ist Kimble Chase Europe unser kompetenter Partner für qualitativ
K O M P E T E N Z I M L A B O R Kimble Laborglas Flexibel. Verlässlich. Persönlich. Kimble Chase Als führender Hersteller von Laborglasartikeln ist Kimble Chase Europe unser kompetenter Partner für qualitativ
Lernziele zu Farbigkeit von Stoffen
 Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Fluoreszenzspektroskopie
 A 60 Fluoreszenzspektroskopie Aufgabe: Bestimmen Sie das Absorptions- und Fluoreszenzspektrum des Farbstoffs Rhodamin 6G in ethanolischer Lösung. Bestimmen Sie in beiden Spektren jeweils die Wellenlänge
A 60 Fluoreszenzspektroskopie Aufgabe: Bestimmen Sie das Absorptions- und Fluoreszenzspektrum des Farbstoffs Rhodamin 6G in ethanolischer Lösung. Bestimmen Sie in beiden Spektren jeweils die Wellenlänge
9. GV: Atom- und Molekülspektren
 Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
4. Optische Spektroskopie I
 1 Absorption einfallendes Licht reflektiertes Streulicht direkt reflektiertes Licht Lumineszenz etc. transmittiertes Streulicht direkt transmittiertes Licht Lumineszenz etc. Reflexion Werkstoff/ Material
1 Absorption einfallendes Licht reflektiertes Streulicht direkt reflektiertes Licht Lumineszenz etc. transmittiertes Streulicht direkt transmittiertes Licht Lumineszenz etc. Reflexion Werkstoff/ Material
Weitere Eigenschaften von Licht
 Weitere Eigenschaften von Licht In welcher Richtung (Ebene) schwingen die Lichtwellen? Querwelle (Transversalwelle)? Längswelle (Longitudinalwelle)? Untersuchung! Betrachtung einer Seilwelle (Querwelle):
Weitere Eigenschaften von Licht In welcher Richtung (Ebene) schwingen die Lichtwellen? Querwelle (Transversalwelle)? Längswelle (Longitudinalwelle)? Untersuchung! Betrachtung einer Seilwelle (Querwelle):
1. Aufgabe a) Beschreibe den Schülerversuchsaufbau zur Dispersion von Licht. Notiere insbesondere die Namen und Aufgaben der einzelnen Objekte.
 1. Aufgabe a) Beschreibe den Schülerversuchsaufbau zur Dispersion von Licht. Notiere insbesondere die Namen und Aufgaben der einzelnen Objekte. Linie Wellenlänge /nm eigene Beobachtung Flint Kron Quarz
1. Aufgabe a) Beschreibe den Schülerversuchsaufbau zur Dispersion von Licht. Notiere insbesondere die Namen und Aufgaben der einzelnen Objekte. Linie Wellenlänge /nm eigene Beobachtung Flint Kron Quarz
Grundpraktikum Humanbiologie I - Spektroskopie. Spektroskopie. Verfahren verwendete Strahlung Übergang Bioch. Anwendungen. Absorptionsverfahren
 Spektroskopie Grundlagen Spektroskopische Verfahren gehören zu den wichtigsten analytischen Methoden der Biochemie. Sie sind im allgemeinen empfindlich, benötigen also nur geringe Substanzmengen, und sind
Spektroskopie Grundlagen Spektroskopische Verfahren gehören zu den wichtigsten analytischen Methoden der Biochemie. Sie sind im allgemeinen empfindlich, benötigen also nur geringe Substanzmengen, und sind
Physik 3 exp. Teil. 30. Optische Reflexion, Brechung und Polarisation
 Physik 3 exp. Teil. 30. Optische Reflexion, Brechung und Polarisation Es gibt zwei Möglichkeiten, ein Objekt zu sehen: (1) Wir sehen das vom Objekt emittierte Licht direkt (eine Glühlampe, eine Flamme,
Physik 3 exp. Teil. 30. Optische Reflexion, Brechung und Polarisation Es gibt zwei Möglichkeiten, ein Objekt zu sehen: (1) Wir sehen das vom Objekt emittierte Licht direkt (eine Glühlampe, eine Flamme,
V1: Methoden der Proteinbestimmung
 V1: Methoden der Proteinbestimmung Methodik: Proteinkonzentrationsbestimmung mittels Bradford sowie der Korrekturverfahren nach Warburg & Christian sowie Kalb & Bernlohr UV-Spektren von Protein- und Nukleinsäurelösungen
V1: Methoden der Proteinbestimmung Methodik: Proteinkonzentrationsbestimmung mittels Bradford sowie der Korrekturverfahren nach Warburg & Christian sowie Kalb & Bernlohr UV-Spektren von Protein- und Nukleinsäurelösungen
Spektroskopische Methoden
 Spektroskopische Methoden OCIfolie367 MS - Massenspektroskopie (Bestimmung von Molekulargewichten, charakteristischen Fragmentierungen von Molekülen) Absorptionsspektroskopische Methoden (Absorption =
Spektroskopische Methoden OCIfolie367 MS - Massenspektroskopie (Bestimmung von Molekulargewichten, charakteristischen Fragmentierungen von Molekülen) Absorptionsspektroskopische Methoden (Absorption =
Absorptionsspektren von Farbstoffen
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 50 Absorptionsspektren von Farbstoffen Aufgabe Es sind die Absorptionsspektren verschiedener Cyanin-Farbstoffe im Wellenlängenbereich
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 50 Absorptionsspektren von Farbstoffen Aufgabe Es sind die Absorptionsspektren verschiedener Cyanin-Farbstoffe im Wellenlängenbereich
UV/VIS- Spektroskopie für Anwender
 UV/VIS- Spektroskopie für Anwender Wolfgang Gottwald Kurt Herbert Heinrich WILEY-VCH Weinheim New York Chichester Brisbane Singapore Toronto Inhaltsverzeichnis 1 Einführung 1 1.1 Einsatzmöglichkeiten der
UV/VIS- Spektroskopie für Anwender Wolfgang Gottwald Kurt Herbert Heinrich WILEY-VCH Weinheim New York Chichester Brisbane Singapore Toronto Inhaltsverzeichnis 1 Einführung 1 1.1 Einsatzmöglichkeiten der
= 6,63 10 J s 8. (die Plancksche Konstante):
 35 Photonen und Materiefelder 35.1 Das Photon: Teilchen des Lichts Die Quantenphysik: viele Größen treten nur in ganzzahligen Vielfachen von bestimmten kleinsten Beträgen (elementaren Einheiten) auf: diese
35 Photonen und Materiefelder 35.1 Das Photon: Teilchen des Lichts Die Quantenphysik: viele Größen treten nur in ganzzahligen Vielfachen von bestimmten kleinsten Beträgen (elementaren Einheiten) auf: diese
Auswertung. D07: Photoeffekt
 Auswertung zum Versuch D07: Photoeffekt Alexander Fufaev Partner: Jule Heier Gruppe 434 1 Einleitung In diesem Versuch geht es darum, den Photoeffekt auf verschiedene Weisen zu untersuchen. In Versuchsteil
Auswertung zum Versuch D07: Photoeffekt Alexander Fufaev Partner: Jule Heier Gruppe 434 1 Einleitung In diesem Versuch geht es darum, den Photoeffekt auf verschiedene Weisen zu untersuchen. In Versuchsteil
Licht als Teilchenstrahlung
 Der Photoeffekt: die auf die Materie einfallende Strahlung löst ein Elektron aus. Es gibt eine Grenzfrequenz, welche die Strahlung haben muss, um das Atom gerade zu ionisieren. Licht als Teilchenstrahlung
Der Photoeffekt: die auf die Materie einfallende Strahlung löst ein Elektron aus. Es gibt eine Grenzfrequenz, welche die Strahlung haben muss, um das Atom gerade zu ionisieren. Licht als Teilchenstrahlung
Versuch 2: Das Spektrometer
 Versuch : Das Spektrometer Funktionsweise des Spektrometers Das Spektrometer zerlegt die am Eingang auftreffende Strahlungsleistung und mißt die Anteile in Abhängigkeit von der Wellenlänge. Das Ergebnis
Versuch : Das Spektrometer Funktionsweise des Spektrometers Das Spektrometer zerlegt die am Eingang auftreffende Strahlungsleistung und mißt die Anteile in Abhängigkeit von der Wellenlänge. Das Ergebnis
