Better Medicines for Children Perspektive der EMEA nach 2 Jahren EU-Kinderarzneimittelverordnung
|
|
|
- Alexander Grosse
- vor 8 Jahren
- Abrufe
Transkript
1 Better Medicines for Children 2007 Perspektive der EMEA nach 2 Jahren EU-Kinderarzneimittelverordnung Ralph Bax EMEA London Arzneimittelforschung in der Pädiatrie Strategien und Chancen Symposium München
2 European Medicines Agency (EMEA) Dezentrales Organ der EU mit Sitz in London Haupttätigkeitsfelder Schutz und Foerderung von public health (human und vet.) durch Evaluation und Supervision von Arzneimitteln fuer Mernschen und Tiere, Wissenschaftliche Evaluierung von Anträgen auf Arzneimittelzulassungen (zentralisiertes Verfahren) Sicherheitsmonitoring mit Hilfe eines Pharmakovigilanznetzwerks Stimulierung von Innovation und Forschung im pharmazeutischen Sektor (wissenschaftliche Beratung scientific advice)
3 European Medicines Agency (EMEA) Wissenschaftliche Tätigkeit 6 wissenschaftliche Kommittes (aus EU, EEA-EFTA Mitgliedsstaaten, Vertreter von Patientenverbänden und Aerzteschaft) EMEA umfasst ein Netzwerk von über 40 NCAs in 30 EU/EEA-EFTA Mitgliedsstaaten mit 4500 Experten.
4 EMEA and the EU Regulatory Network RO EL BE LV BG DK Committees EMEA Secretariat Working Parties SK CZ ES AT LT FR UK IT IE SI NL LU HU PL DE PT MT FI EE CY SE Competent National Authorities
5 CAT Advanced therapies COMP Orphan drugs Landscape CHMP Committee for Medicinal Products for Human Use HMPC Herbal med. products PDCO Paediatric Committee Committee for Orphan Medicinal Products 13 WPs 7SAGs Working Parties Scientific Advisory Groups CVMP
6 Die bekannte Ausgangssituation 20 % der EU Bevölkerung = 100 Millionen sind jünger als 16 Jahre Frühgeborene Kinder, reifgeborene Kinder, Säuglinge, Kleinkinder, Kinder, Schulkinder, Jugendliche 50-90% der in der Pädiatrie gebrauchten Arzneimittel sind (dafür) nicht untersucht und evaluiert worden Beispiele für sich daraus ergebende Risiken: Unerwünschte Arzeimittelwirkungen (Überdosierung) Unwirksamkeit (Unterdosierung) Ungeeignete Darreichungsform Später Zugang zu innovativen Medikanten
7 Why innovation in Paediatric development? Hard to use tools for kids that were meant for others (eg endpoints ) Ron Portman
8 Why innovation in Paediatric development? Child... Infant... Preterm... Not a small adult Not a small child Not a small infant
9 Empirismus Falldarstellungen Medizinische Praxis in der Kinderheilkunde Unkontrollierte Studien, die einen Nutzen suggerieren Extrapolation von Ergebnissen bei Erwachsenen Individuelle Richtlinien, Kochrezepte. Standard für viele Jahre
10 Warum Innovation in der Entwicklung von Kinderarzneimitteln? Studien bei Erwachsenen nicht ausreichend Spezifität der kindlichen Erkrankung Kinetische Charakteristika Auswirkungen auf Wachstum, Entwicklung und Reifung Spezifische unerwünschte Nebenwirkungen Zusätzliche Probleme Ethische Herausforderungen Größtmöglicher Schutz Minimierung von Schmerzen, Angst und Stress Darreichungsformen Studien bei Kindern sind schwieriger durchzufuehren, dauern laenger, kosten mehr und sollen in den Augen viler unethisch sein. Verbreiteter off-label Gebrauch Schwierigkeiten bei der Rekrutierung Neue Forschungsansätze! (small sample size, PK-Methodik)
11 Herausforderungen Qualität Altersgerechte Darreichungsformen Zusatzstoffe, Alkoholgehalt, Geschmack globale Unterschiede Non-clinical Sind zusätzliche Studien bei Tieren notwendig? Sicherheit (Studien bei juvenilen Tieren, Tox., Auswirkungen auf Wachstum und Entwicklung) Timing Robuste klinische Studien Small numbers Statistische power Neue Methoden (adaptive design, modelling) Adäquate Rekrutierung in alen Altersgruppen Monitoring: zusätzlich für Wachstum/Entwicklung, Langzeit Wirksamkeit und Sicherheit, chronische Erkrankungen.
12 Nicht unmöglich: Sind Arzneimittelstudien bei Kindern unmöglich? - Eltern geben die Einwilligung auch bei Neugeborenen - Auschluss der Kinder von der Forschung (falschverstandener Schutz?!) versus zuverlässige wissenschaftliche Daten - Schutz der Kinder bei Studien hat oberste Priorität - Marktkräfte unzureichend (US Erfahrung) - Carrot and stick approach (Zuckerbrot und Peitsche)
13 Impact of clinical trials with children: paediatric cancer survival rates Data from St. Jude Children s Research Hospital
14 Ziele: EU Kinderarzneimittelverordnung Verbesserung der Gesundheit von Kindern Förderung der qualitativ hochwertigen, ethischen Erforschung von Arzneimitteln für Kinder Förderung der Verfügbarkeit von zugelassenen Medikamenten für Kinder Mehr und bessere Informationen über Arzneimittel Erreichung der Ziele Unter Vermeidung unnötiger Studien mit Kindern Ohne Verzögerung der Zulassung für Erwachsene Entry into force 26 January 2007
15 Eckpfeiler der Kinderarzneimittel- Verordnung Wissenschaftliches Expertenkommittee: Pädiatrieausschuss (Paediatric Committee PDCO) Pädiatrischer (reifender) Entwicklungsplan: Pädiatrisches Prüfkonzept (Paediatric Investigation Plan = PIP) Verpflichtungen, Bonusse und Anreize: Für neue und für patentgeschützte Arzneimittel Für Arzneimittel ohne Basispatentschutz Maßnahmen zur Information und für die Forschung Öffentlich zugängliche Studieninformationen in EudraCT Leitlinien (z. B. zu Ethik); Förderprogramme (RP7) Europäisches Netzwerk zum Kompetenzaufbau und zur Studien-Unterstützung
16 Paediatric Committee (PDCO) 1 Chair 5 CHMP members 22 other Member States representatives 3 Patients/families representatives* 3 Health Professionals representatives* Each member has an alternate *to be appointed
17 Paediatric Committee Created in July 2007 All 27 (+2) members but some alternates missing Competences: Neonatology, paediatric cardiovascular diseases, immunology, transplantation, respiratory, ICU, vaccines, pharmacology, PK, haematology, oncology, endocrinology and diabetes, adolescent medicine, pharmacovigilance, anaesthesiology, infectious diseases, gastroenterology and nutrition, general paediatrics, Formulations (plus permanent external experts) Adult internal medicine, non-clinical toxicology Additional methodologist Ethicist
18 Eckpfeiler der Kinderarzneimittel- Verordnung Wissenschaftliches Expertenkommittee: Pädiatrieausschuss (Paediatric Committee PDCO) Pädiatrischer (reifender) Entwicklungsplan: Pädiatrisches Prüfkonzept (Paediatric Investigation Plan = PIP) Verpflichtungen, Bonusse und Anreize: Für neue und für patentgeschützte Arzneimittel Für Arzneimittel ohne Basispatentschutz Maßnahmen zur Information und für die Forschung Öffentlich zugängliche Studieninformationen in EudraCT Leitlinien (z. B. zu Ethik); Förderprogramme (RP7) Europäisches Netzwerk zum Kompetenzaufbau und zur Studien-Unterstützung
19 Paediatric Investigation Plan- PIP (Pädiatrisches Prüfkonzept) Grundlage für die Entwicklung und Zulassung von Arzneimitteln für pädiatrische Bevölkerungsgruppen Beinhaltet Einzelheiten zum Zeitplan und zu den Maßnahmen zum Nachweis der Qualität Sicherheit Wirksamkeit Wird auf Antrag durch Zulassungskriterie n zur Genehmigung (PDCO) gebilligt/abgelehnt Ist für Antragsteller verpflichtend
20 Gliederung eines Antrags auf Billigung eines PIP Verschiedene allgemeine Informationen (Zulassung, Hintergrund, Zustand, Produkt) Antrag auf Freistellung Strategie der Entwicklung des Arzneimittels für Kinder Einzelheiten der einzelnen Studien Geplante zeitliche Abfolge der Studien (gegebenenfalls mit Antrag auf Zurückstellung) Wissenschaftliche Dokumentation und Referenzen
21 Timing of PIP application (new products) CTA CTA SA MA Non-clin Phase 1 Phase 2 Phase 3 Post approval 1 Paed. Investig. Plan PIP Amendments Paediatric Committee Compliance Deferral Waiver
22 Warum ist ein PIP notwendig? Pharmazeutische Unternehmen müssen Daten von Studien an Kindern gemäss des genehmigten PIP nachweisen, beim Antrag auf Arzneimittelzulassung (MAA) Bei zugelassenen Arzneimitteln fuer neue Indikationen, Verabreichungswege und Darreichungsformen. Andernfalls benötigen sie - eine komplette Freistellung ( full waiver ) - oder eine Zurückstellung ( deferral ) PIP
23 Waivers (Freistellungen) 3 gesetzliche Gründe Krankheit tritt nur bei Erwachsenen auf Arzneimittel ist wahrscheinlich unwirksam oder bedenklich Fragliches Arzneimittel bietet gegenüber bestehenden pädiatrischen Behandlungen keinen signifikanten therapeutischen Nutzen
24 Wer macht was? Europäische Kommission: DG Enterprise: Gesetzgebung, Richtlinien, Zulassung DG Research: Förderung von Studien patentfreier Arzneimittel (with a view for a PUMA) EMEA / Pädiatrisches Team: Erstellt ersten wissenschaftlichen Bericht über PIPs Koordiniert die Implementierung und Aktivitäten Hostet Pädiatrieausschuss: wissentschaftliche Evaluation von PIP; CHMP: Evaluation von Genehmigungsanträgen PDCO (EMEA) Evaluierung der PIPs Beratung CHMP, guidelines, Stellungnahmen Mitgliedsstaaten: Beratung; Gestellung Ausschuss-Mitglieder; Forschungsförderung; Studienzulassung
25 Eckpfeiler der Kinderarzneimittel- Verordnung Wissenschaftliches Expertenkommittee: Pädiatrieausschuss (Paediatric Committee PDCO) Pädiatrischer (reifender) Entwicklungsplan: Pädiatrisches Prüfkonzept (Paediatric Investigation Plan = PIP) Verpflichtungen, Bonusse und Anreize: Für neue und für patentgeschützte Arzneimittel Für Arzneimittel ohne Basispatentschutz Maßnahmen zur Information und für die Forschung Öffentlich zugängliche Studieninformationen in EudraCT Leitlinien (z. B. zu Ethik); Förderprogramme (RP7) Europäisches Netzwerk zum Kompetenzaufbau und zur Studien-Unterstützung
26 Obligations versus Incentives Obligation Incentive Comments New Medicines Paediatric Investigation Plan or Waiver 6 months extension of patent * Necessary for validation of application On Patent and Approved Medicines Orphan Medicines Paediatric Investigation Plan or Waiver Paediatric Investigation Plan or Waiver 6 months extension of patent* 2 years of market exclusivity* When New indication, new route, new formulation Necessary for validation In addition to 10 years Off patent Medicines VOLUNTARY PIP 10 years of data protection Research funds Paediatric Use MA *if compliance with PIP, information, approval EU-wide
27 Paediatric Committee
28 Paediatric Committee
29 Neonatal research -Least knowledge -Most challenging -Most safety concerns -Most needed -Most difficult to do -Research no one wants to do or no one wants to approve
30 Eckpfeiler der Kinderarzneimittel- Verordnung Wissenschaftliches Expertenkommittee: Pädiatrieausschuss (Paediatric Committee PDCO) Pädiatrischer (reifender) Entwicklungsplan: Pädiatrisches Prüfkonzept (Paediatric Investigation Plan = PIP) Verpflichtungen, Bonusse und Anreize: Für neue und für patentgeschützte Arzneimittel Für Arzneimittel ohne Basispatentschutz Maßnahmen zur Information und für die Forschung Öffentlich zugängliche Studieninformationen in EudraCT Leitlinien (z. B. zu Ethik); Förderprogramme (RP7) Europäisches Netzwerk zum Kompetenzaufbau und zur Studien-Unterstützung
31 Europäische Förderung Studien zu patentfreien Arzneimitteln Innerhalb des Europäischen Rahmenprogramms 3. Ausschreibung FP7 (deadline: November 2009) 6 Mio /Antrag Bezug auf die Prioritäten-Liste für Studien zu patentfreien Arzneimitteln für Kinder ( Zusammen mit FDA/NIH Prioritaeten: Neonaologie, Onkologie-junge Kinder WHO list of essential medicines
32 European Paediatric Network Objectives to coordinate studies relating to paediatric medicinal products to build up competence at a EU level to avoid unnecessary duplication of studies and testing in the paediatric population
33 Symbol? To be included on the packaging of medicinal products with paediatric indication Paediatric Committee considered there was no symbol for which benefits outweighed risks (of medication error) Commission decided not to implement
34 Symbol: One proposal CHILD BABY
35 But BABY!
36 Information und Transparenz Datenbank pädiatrischer Studien (EudraCT) Protokollinformationen Ergebnisinformationen Abgeschlossene Studien (publiziert oder nicht) Studien in Drittstaaten (in PIP) Datenbank zugelassener Arzneimittel (EudraPharm) Medizinische Informationen (SmPC, Packungsbeilage; mit Ergebnissen) EMEA-Entscheidung über PIP Billigung und Freistellungen öffentlich zugänglich Name and Praise / Name and Shame (EC)
37 Making it work... EC FORMULATIONS CLINICAL TRIALS HCP, ACADEMICS, NETWORKS SCIENTIFIC ADVICE PIP ORPHAN DESIGNATION SME PATIENTS /Parents EMEA, NCAs INDUSTRY INNOVATIVE DEVELOPMENT EMEA EUROPEAN NETWORK
38
39 Zusammenfassung Verordnung betrifft neue und alte Arzneimittel Unterstützung auch von akademischen Initiativen und Generikaherstellern steht zur Verfügung Ausschreibungen im 7. RP sollten beachtet werden Transparenz und Information dienen Patienten, Health Care Professionals, Netzen und der Industrie Hohe Herausforderung fuer alle Beteiligten Das Europäische Netzwerk wird eine praktische Wirkung für Studien mit Kindern und Jugendlichen entfalten Sollte ein gemeinsames Anliegen der kommenden Jahre sein Das Europäische Netzwerk sollte ein gemeinsames Anliegen der kommenden Jahre sein
40 better medicines for children
41
42 Timeline of Implementation as of Entry into force, 26 January 2007: Free Scientific Advice as of July 2007: Establishment of Paediatric Committee Submission of Paediatric Investigation Plan (PIP) request as of 26 July 2008: Obligation to submit results of studies according to agreed PIP with applications for Marketing Authorisation (new products) Or EMEA decision granting a waiver or deferral as of 26 January 2009: Obligation to submit results of studies according to agreed PIP with application for new indications, new routes of administration, new pharmaceutical forms Or EMEA decision granting a waiver or deferral
43 Applicant s request for a PIP YES PIP ± ± Partial waiver deferr al PIP ± Partial waiver ± deferr al PDCO NO REFUSAL new PIP ± ± Partial waiver deferr al PDCO agreement Full WAIVER NB: full waiver= no reward
44 Applicant s request for a Waiver YES Waiver Full Waiver PDCO NO REFUSAL PIP Partial waiver ± deferr al NB: full waiver= no reward
45 Timeline of Implementation as of Entry into force, 26 January 2007: Free Scientific Advice as of July 2007: Establishment of Paediatric Committee Submission of Paediatric Investigation Plan (PIP) request as of 26 July 2008: Obligation to submit results of studies according to agreed PIP with applications for Marketing Authorisation (new products) Or EMEA decision granting a waiver or deferral as of 26 January 2009: Obligation to submit results of studies according to agreed PIP with application for new indications, new routes of administration, new pharmaceutical forms Or EMEA decision granting a waiver or deferral
46 30% 25% 20% 15% 10% 5% 0% Therapeutic areas PIP/waivers 2008 nephro onco infection cardiov endocrino-metab hemato immuno psychiatry others vaccines
47 Timing of Consultation of Paediatric Committee Scientific advice MA Non-clin Phase 1 Phase 2 Phase 3 Post approval Paed. Investig. Plan 1 Amendments Compliance Paediatric Committee (PDCO)
48 CAT Advanced therapies COMP Orphan drugs Landscape CHMP Committee for Medicinal Products for Human Use HMPC Herbal med. products PDCO Paediatric Committee Committee for Orphan Medicinal Products 13 WPs 7SAGs Working Parties Scientific Advisory Groups CVMP
Die neue Rolle von Kindern im Arzneimittelrecht und ihre praktischen Konsequenzen. Was hat mein Kind von der EU? Prof. Dr. med. Joachim Boos, Münster
 Die neue Rolle von Kindern im Arzneimittelrecht und ihre praktischen Konsequenzen Was hat mein Kind von der EU? Prof. Dr. med. Joachim Boos, Münster Bayer Werbung um 1900: Heroin, das ideale Sedativum
Die neue Rolle von Kindern im Arzneimittelrecht und ihre praktischen Konsequenzen Was hat mein Kind von der EU? Prof. Dr. med. Joachim Boos, Münster Bayer Werbung um 1900: Heroin, das ideale Sedativum
Die Sicht der EMEA. für Zulassungs-, Therapie- und. Berlin-Brandenburgische Akademie der
 Lebensqualität und Patientennutzen Die Sicht der EMEA PMS-Workshop: Lebensqualität als Kriterium für Zulassungs-, Therapie- und Erstattungsentscheidungen. Berlin-Brandenburgische Akademie der Wissenschaften
Lebensqualität und Patientennutzen Die Sicht der EMEA PMS-Workshop: Lebensqualität als Kriterium für Zulassungs-, Therapie- und Erstattungsentscheidungen. Berlin-Brandenburgische Akademie der Wissenschaften
Pädiatrischer Prüfplan (PIP)
 Pädiatrischer Prüfplan (PIP) AGES - Gespräch Arzneimittel in der Pädiatrie: Heute und Morgen 27. Mai 2008 Dr. Doris Tschabitscher, PharmMed Austrian Alternate PDCO Pädiatrische Pharmakotherapie: Wie alles
Pädiatrischer Prüfplan (PIP) AGES - Gespräch Arzneimittel in der Pädiatrie: Heute und Morgen 27. Mai 2008 Dr. Doris Tschabitscher, PharmMed Austrian Alternate PDCO Pädiatrische Pharmakotherapie: Wie alles
Die Schweiz liegt in Forschung und Innovation an der Spitze, die Forschungsförderung muss Schritt halten Nationalrätin Tiana Moser, Glp
 Die Schweiz liegt in Forschung und Innovation an der Spitze, die Forschungsförderung muss Schritt halten Nationalrätin Tiana Moser, Glp Parlamentarisches Seminar des Netzwerks FUTURE 11. Januar 2012 Zahlreiche
Die Schweiz liegt in Forschung und Innovation an der Spitze, die Forschungsförderung muss Schritt halten Nationalrätin Tiana Moser, Glp Parlamentarisches Seminar des Netzwerks FUTURE 11. Januar 2012 Zahlreiche
Intelligente Energie Europa Beteiligungsergebnisse 2007-2012
 Intelligente Energie Europa Beteiligungsergebnisse 2007-2012 31. Januar 2013 Nationaler Informationstag Intelligente Energie Europa - Aufruf 2013 Ute Roewer, NKS Energie www.nks-energie.de eu-energie@fz-juelich.de
Intelligente Energie Europa Beteiligungsergebnisse 2007-2012 31. Januar 2013 Nationaler Informationstag Intelligente Energie Europa - Aufruf 2013 Ute Roewer, NKS Energie www.nks-energie.de eu-energie@fz-juelich.de
bíüáâ=eáåf=çéê=éü~êã~òéìíáëåüéå=fåçìëíêáé= téäåüéå=fåíéêéëëéå=çáéåí=çáé=^êòåéáãáííéäñçêëåüìåö\=
 EVANGELISCHE AKADEMIE bíüáâeáåfçéêéü~êã~òéìíáëåüéåfåçìëíêáé téäåüéåfåíéêéëëéåçáéåíçáé^êòåéáãáííéäñçêëåüìåö\ q~öìåöçéêbî~åöéäáëåüéå^â~çéãáéiçååìãîçãskäáëukkçîéãäéêomms fåhççééê~íáçåãáíçéãwéåíêìãñ êdéëìåçüéáíëéíüáâ
EVANGELISCHE AKADEMIE bíüáâeáåfçéêéü~êã~òéìíáëåüéåfåçìëíêáé téäåüéåfåíéêéëëéåçáéåíçáé^êòåéáãáííéäñçêëåüìåö\ q~öìåöçéêbî~åöéäáëåüéå^â~çéãáéiçååìãîçãskäáëukkçîéãäéêomms fåhççééê~íáçåãáíçéãwéåíêìãñ êdéëìåçüéáíëéíüáâ
Erstattung für Arzneimittel in Europa. Dr. Sabine Vogler CMI-Workshop, Bundesministerium für Gesundheit, 17.1.2011
 Erstattung für Arzneimittel in Europa Dr. Sabine Vogler CMI-Workshop, Bundesministerium für Gesundheit, 17.1.2011 Pharmaceutical Pricing and Reimbursement Information (PPRI)» Aus einem EU-Projekt (2005-2007)
Erstattung für Arzneimittel in Europa Dr. Sabine Vogler CMI-Workshop, Bundesministerium für Gesundheit, 17.1.2011 Pharmaceutical Pricing and Reimbursement Information (PPRI)» Aus einem EU-Projekt (2005-2007)
Maßnahmen zur Vermeidung von Umsatzsteuerbetrug und Evaluierung bestehender Strategien zur Minimierung der Umsatzsteuerlücke
 Deutscher Bundestag Drucksache 17/5751 17. Wahlperiode 05. 05. 2011 Antwort der Bundesregierung auf die Kleine Anfrage der Abgeordneten Dr. Thomas Gambke, Britta Haßelmann, Lisa Paus, weiterer Abgeordneter
Deutscher Bundestag Drucksache 17/5751 17. Wahlperiode 05. 05. 2011 Antwort der Bundesregierung auf die Kleine Anfrage der Abgeordneten Dr. Thomas Gambke, Britta Haßelmann, Lisa Paus, weiterer Abgeordneter
Anhang zum Altersübergangs-Report 2012-01
 Anhang 2012-01 Anhang zum Altersübergangs-Report 2012-01 Alterserwerbsbeteiligung in Europa Deutschland im internationalen Vergleich Tabellen und Abbildungen Tabelle Anhang 1: Gesetzliche Rentenaltersgrenzen
Anhang 2012-01 Anhang zum Altersübergangs-Report 2012-01 Alterserwerbsbeteiligung in Europa Deutschland im internationalen Vergleich Tabellen und Abbildungen Tabelle Anhang 1: Gesetzliche Rentenaltersgrenzen
wennsiealsgemeinschaftsschule,alsbekenntnis-oderweltanschauungsschuleerrichtetwerdensollundeineöffentlichevolksschuledieserartinder
 Deutscher Bundestag Drucksache 16/7659 16. Wahlperiode 27. 12. 2007 Antwort der Bundesregierung auf die Kleine Anfrage der Abgeordneten Patrick Meinhardt, Uwe Barth, Cornelia Pieper, weiterer Abgeordneter
Deutscher Bundestag Drucksache 16/7659 16. Wahlperiode 27. 12. 2007 Antwort der Bundesregierung auf die Kleine Anfrage der Abgeordneten Patrick Meinhardt, Uwe Barth, Cornelia Pieper, weiterer Abgeordneter
Gesetzliche Grundlagen der Arzneimittelentwicklung national/ international
 Gesetzliche Grundlagen der Arzneimittelentwicklung national/ international Dr. med. Dirk Mentzer Referatsleiter Arzneimittelsicherheit Facharzt für Kinder- und Jugendmedizin Paul-Ehrlich-Institut Bundesinstitut
Gesetzliche Grundlagen der Arzneimittelentwicklung national/ international Dr. med. Dirk Mentzer Referatsleiter Arzneimittelsicherheit Facharzt für Kinder- und Jugendmedizin Paul-Ehrlich-Institut Bundesinstitut
Die Bedeutung von business migrants im europäischen Vergleich
 Konfinanziert von der Europäischen Union Die Bedeutung von business migrants im europäischen Vergleich Julia Rutz Nationaler Kontaktpunkt Österreich im Europäischen Migrationsnetzwerk Dialogforum Krems,
Konfinanziert von der Europäischen Union Die Bedeutung von business migrants im europäischen Vergleich Julia Rutz Nationaler Kontaktpunkt Österreich im Europäischen Migrationsnetzwerk Dialogforum Krems,
ÖSTERREICH UND HORIZON 2020 >> FACTS AND FIGURES 13. November 2014
 ÖSTERREICH UND HORIZON 2020 >> FACTS AND FIGURES 13. November 2014 EU-PERFORMANCE MONITORING SEIT 2014 IN DER FFG Inhaltlicher Überblick: - Europäische Initiativen in der FFG - 1. Zwischenergebnisse H2020
ÖSTERREICH UND HORIZON 2020 >> FACTS AND FIGURES 13. November 2014 EU-PERFORMANCE MONITORING SEIT 2014 IN DER FFG Inhaltlicher Überblick: - Europäische Initiativen in der FFG - 1. Zwischenergebnisse H2020
Europäische Strukturpolitik im Spannungsfeld von Ist und Soll
 Europäische Strukturpolitik im Spannungsfeld von Ist und Soll WSI Herbstforum Dr. Ines Hartwig, Europäische Kommission 27. November 2008, Berlin Fakten & Zahlen Fonds Anteil am EU-Haushalt (2007-13) ESF
Europäische Strukturpolitik im Spannungsfeld von Ist und Soll WSI Herbstforum Dr. Ines Hartwig, Europäische Kommission 27. November 2008, Berlin Fakten & Zahlen Fonds Anteil am EU-Haushalt (2007-13) ESF
Import und Export von Gebrauchtfahrzeugen in Europa
 Cornelia Merz, Dr.-Ing. Georg Mehlhart 27.03.2012, Berlin Gliederung Rahmen und Motivation Bilanzierung der Entwicklung der Fahrzeugflotte Abschätzung des Altfahrzeugaufkommens Zusammenfassung 2 Rahmen
Cornelia Merz, Dr.-Ing. Georg Mehlhart 27.03.2012, Berlin Gliederung Rahmen und Motivation Bilanzierung der Entwicklung der Fahrzeugflotte Abschätzung des Altfahrzeugaufkommens Zusammenfassung 2 Rahmen
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen
 Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Diabetes. Zulassungserweiterung: Levemir (Insulin detemir) als Add-on Therapie zu Victoza (Liraglutid) bei Mens
 Zulassungserweiterung Levemir (Insulin detemir) als Add-on Therapie zu Victoza (Liraglutid) bei Menschen mit Typ 2 Diabetes Mainz (16. November 2011) Die Europäische Kommission hat die Zulassung des modernen
Zulassungserweiterung Levemir (Insulin detemir) als Add-on Therapie zu Victoza (Liraglutid) bei Menschen mit Typ 2 Diabetes Mainz (16. November 2011) Die Europäische Kommission hat die Zulassung des modernen
FRAGEBOGEN FÜR KINDER UND JUGENDLICHE
 Meinung in Bezug auf die Anwendung von Medikamenten Warum fragen wir? Der Pädiatrische Ausschuss (Paediatric Committee (PDCO)) arbeitet zusammen mit der Europäischen Arzneimittelagentur. Dieser Ausschuss
Meinung in Bezug auf die Anwendung von Medikamenten Warum fragen wir? Der Pädiatrische Ausschuss (Paediatric Committee (PDCO)) arbeitet zusammen mit der Europäischen Arzneimittelagentur. Dieser Ausschuss
Befunde auf der Basis von CVTS
 Betriebliche Weiterbildung in Europa: Befunde auf der Basis von CVTS Wirtschaftsdienst-Konferenz Qualifikation und Arbeitsmarkt: ungenutzte Potentiale 25.11.2010, BIBB Arbeitsbereich Kosten, Nutzen, Finanzierung
Betriebliche Weiterbildung in Europa: Befunde auf der Basis von CVTS Wirtschaftsdienst-Konferenz Qualifikation und Arbeitsmarkt: ungenutzte Potentiale 25.11.2010, BIBB Arbeitsbereich Kosten, Nutzen, Finanzierung
Der Anspruch an eine ethische Nutzen- und Kostenbewertung
 Der Anspruch an eine ethische Nutzen- und Kostenbewertung 20.09.2008 Dr. Katrin Grüber, Institut Mensch, Ethik und Wissenschaft Berlin Das Institut Mensch, Ethik und Wissenschaft wurde 2001 als ggmbh gegründet
Der Anspruch an eine ethische Nutzen- und Kostenbewertung 20.09.2008 Dr. Katrin Grüber, Institut Mensch, Ethik und Wissenschaft Berlin Das Institut Mensch, Ethik und Wissenschaft wurde 2001 als ggmbh gegründet
Pädiatrisches Prüfkonzept (PIP) - Dos and Don ts anhand regulatorischer Erfahrung
 Pädiatrisches Prüfkonzept (PIP) - Dos and Don ts anhand regulatorischer Erfahrung Reinhard Hiersemenzel Senior Medical Expert Global Clinical R&D CNS Merz Pharmaceuticals GmbH - Nicht befugt, für und im
Pädiatrisches Prüfkonzept (PIP) - Dos and Don ts anhand regulatorischer Erfahrung Reinhard Hiersemenzel Senior Medical Expert Global Clinical R&D CNS Merz Pharmaceuticals GmbH - Nicht befugt, für und im
Der neue lohnpolitische Interventionismus in Europa Auswirkungen auf die Lohn- und Tarifpolitik
 Der neue lohnpolitische Interventionismus in Europa Auswirkungen auf die Lohn- und Tarifpolitik Thorsten Schulten WSI/ver.di, 9. Workshop Europäische Tarifpolitik Krise der Europäischen Union. Wo bleibt
Der neue lohnpolitische Interventionismus in Europa Auswirkungen auf die Lohn- und Tarifpolitik Thorsten Schulten WSI/ver.di, 9. Workshop Europäische Tarifpolitik Krise der Europäischen Union. Wo bleibt
Neue Gemeinsame Agrarpolitik ab 20134. Statement
 Bündnis 90 / Die Grünen Neue Gemeinsame Agrarpolitik ab 20134 / Agrarpolitik Landwirtschaft nach 2013 11. Februar 2011 Statement [HAL-080508.PPT] Dr. Hans H. Harpain Hessischer Bauernverband e.v. Leistungen
Bündnis 90 / Die Grünen Neue Gemeinsame Agrarpolitik ab 20134 / Agrarpolitik Landwirtschaft nach 2013 11. Februar 2011 Statement [HAL-080508.PPT] Dr. Hans H. Harpain Hessischer Bauernverband e.v. Leistungen
Güterverkehr in Österreich
 Güterverkehr in Österreich Transportaufkommen (Millionen Tonnen) 1999 (1) Schiff Pipeline (2) Summe Binnen 243 18 0,8 1 263 Import / Export 51 34 6 12 103 Transit 38 18 3 44 103 Gesamt 331 70 10 57 469
Güterverkehr in Österreich Transportaufkommen (Millionen Tonnen) 1999 (1) Schiff Pipeline (2) Summe Binnen 243 18 0,8 1 263 Import / Export 51 34 6 12 103 Transit 38 18 3 44 103 Gesamt 331 70 10 57 469
Risk Management Plans & PSURs. Was könnte die Zukunft bringen?
 Risk Management Plans & PSURs Was könnte die Zukunft bringen? 1 Strategy to better protect public health by strengthening and rationalising EU pharmacovigilance There is an established link between pharmacovigilance
Risk Management Plans & PSURs Was könnte die Zukunft bringen? 1 Strategy to better protect public health by strengthening and rationalising EU pharmacovigilance There is an established link between pharmacovigilance
Europäische Arzneimittelbehörde empfiehlt Aussetzung der Marktzulassung für Raptiva
 Europäische Arzneimittelbehörde empfiehlt Aussetzung der Marktzulassung für Raptiva Darmstadt (19. Februar 2009) Die Merck KGaA hat heute bekannt gegeben, dass die europäische Arzneimittelbehörde EMEA
Europäische Arzneimittelbehörde empfiehlt Aussetzung der Marktzulassung für Raptiva Darmstadt (19. Februar 2009) Die Merck KGaA hat heute bekannt gegeben, dass die europäische Arzneimittelbehörde EMEA
More Medicines for Minors
 More Medicines for Minors Arzneimittelzulassung für Kinder und Jugendliche verbessern Birka Lehmann More Medicines for Minors! Kinder sind keine kleinen Erwachsenen! Ziel der Verodnung (EG) Nr 1901/2006
More Medicines for Minors Arzneimittelzulassung für Kinder und Jugendliche verbessern Birka Lehmann More Medicines for Minors! Kinder sind keine kleinen Erwachsenen! Ziel der Verodnung (EG) Nr 1901/2006
Intelligente Energie Europa 2007-2013
 PTJ Intelligente Energie Europa 2007-2013 Ergebnisse der Projektförderung Ute Roewer Mai 2015 Beteiligung deutscher Partner an IEE An den Aufrufen des Programms Intelligente Energie Europa (IEE) einem
PTJ Intelligente Energie Europa 2007-2013 Ergebnisse der Projektförderung Ute Roewer Mai 2015 Beteiligung deutscher Partner an IEE An den Aufrufen des Programms Intelligente Energie Europa (IEE) einem
New Member and Market Maker of CEGH Gas Exchange Spot & Futures Market:
 New Member and Market Maker of CEGH Gas Exchange Spot & Futures Market: MET International AG, Zug (Switzerland) On the 21 st January 2016 the management of Wiener Börse has decided to approve MET International
New Member and Market Maker of CEGH Gas Exchange Spot & Futures Market: MET International AG, Zug (Switzerland) On the 21 st January 2016 the management of Wiener Börse has decided to approve MET International
(51) Int Cl.: B23K 26/28 (2014.01) B23K 26/32 (2014.01) B23K 26/30 (2014.01) B23K 33/00 (2006.01)
 (19) TEPZZ 87_Z ZA_T (11) EP 2 871 0 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 13.0.1 Patentblatt 1/ (21) Anmeldenummer: 13192326.0 (1) Int Cl.: B23K 26/28 (14.01) B23K 26/32 (14.01)
(19) TEPZZ 87_Z ZA_T (11) EP 2 871 0 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 13.0.1 Patentblatt 1/ (21) Anmeldenummer: 13192326.0 (1) Int Cl.: B23K 26/28 (14.01) B23K 26/32 (14.01)
FORMBLATT für die BESCHREIBUNG GUTER PRAXIS
 FORMBLATT für die BESCHREIBUNG GUTER PRAXIS zur Förderung von Lese- und Schreibkompetenzen von benachteiligten Kindern, Jugendlichen und Erwachsenen in Europa Mithilfe dieses Formblatts soll ein möglichst
FORMBLATT für die BESCHREIBUNG GUTER PRAXIS zur Förderung von Lese- und Schreibkompetenzen von benachteiligten Kindern, Jugendlichen und Erwachsenen in Europa Mithilfe dieses Formblatts soll ein möglichst
(51) Int Cl. 7 : G06K 7/00, G06K 13/08. (72) Erfinder: Baitz, Günter 13629 Berlin (DE) Kamin, Hartmut 10585 Berlin (DE)
 (19) Europäisches Patentamt European Patent Office Office européen des brevets *EP001347405A1* (11) EP 1 347 405 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 24.09.2003 Patentblatt 2003/39
(19) Europäisches Patentamt European Patent Office Office européen des brevets *EP001347405A1* (11) EP 1 347 405 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 24.09.2003 Patentblatt 2003/39
Klinische Forschung. Klinische Forschung. Effectiveness Gap. Versorgungsforschung und evidenzbasierte Medizin. Conclusion
 Versorgungsforschung und evidenzbasierte Medizin Klinische Forschung 00qm\univkli\klifo2a.cdr DFG Denkschrift 1999 Aktuelles Konzept 2006 Workshop der PaulMartiniStiftung Methoden der Versorgungsforschung
Versorgungsforschung und evidenzbasierte Medizin Klinische Forschung 00qm\univkli\klifo2a.cdr DFG Denkschrift 1999 Aktuelles Konzept 2006 Workshop der PaulMartiniStiftung Methoden der Versorgungsforschung
Doro PhoneEasy 331ph
 Doro PhoneEasy 331ph 1 2 6 3 4 5 Deutsch 1 Rufanzeige 2 Höreraufhängung 3 Wahlwiederholung 4 Lautstärke 5 R-Taste/Programmierung 6 Direktwahl Dieses Telefon ist für den Betrieb an einem analogen Telefonanschluss
Doro PhoneEasy 331ph 1 2 6 3 4 5 Deutsch 1 Rufanzeige 2 Höreraufhängung 3 Wahlwiederholung 4 Lautstärke 5 R-Taste/Programmierung 6 Direktwahl Dieses Telefon ist für den Betrieb an einem analogen Telefonanschluss
Herbst Frühjahr 2004
 DIE MITGLIEDSCHAFT IN DER 1. Das Image der : a. Welches Bild ruft die bei Ihnen hervor? (in %, 27) 2007 AT BE BG CY CZ DE DK EE EL ES FI FR HU IE IT LT LU LV MT NL PL PT RO SE SI SK UK 27 ein positives
DIE MITGLIEDSCHAFT IN DER 1. Das Image der : a. Welches Bild ruft die bei Ihnen hervor? (in %, 27) 2007 AT BE BG CY CZ DE DK EE EL ES FI FR HU IE IT LT LU LV MT NL PL PT RO SE SI SK UK 27 ein positives
The Cochrane Library
 The Cochrane Library Was ist die Cochrane Library? Die Cochrane Library bietet hochwertige, evidenzbasierte medizinische Fachinformation zur fundierten Unterstützung bei Diagnose und Behandlung. http://www.cochranelibrary.com/
The Cochrane Library Was ist die Cochrane Library? Die Cochrane Library bietet hochwertige, evidenzbasierte medizinische Fachinformation zur fundierten Unterstützung bei Diagnose und Behandlung. http://www.cochranelibrary.com/
Die volkswirtschaftlichen Impulse des Internets für Österreich
 Die volkswirtschaftlichen Impulse des Internets für Österreich Prof. Dr. Bernhard Felderer Institut für Höhere Studien 21. Juli 2011 Internet IHS-Studie 1 Verschiedene Ansätze bei Internetstudien a) Sektorale
Die volkswirtschaftlichen Impulse des Internets für Österreich Prof. Dr. Bernhard Felderer Institut für Höhere Studien 21. Juli 2011 Internet IHS-Studie 1 Verschiedene Ansätze bei Internetstudien a) Sektorale
Textiltechnologische Innovationen im Bereich adaptierter Kleidung für Menschen mit Handicap
 Textiltechnologische Innovationen im Bereich adaptierter Kleidung für Menschen mit Handicap Ausgangssituation: Laut Statistischem Bundesamt in Wiesbaden, lebten Ende des Jahres 2011 in Deutschland 7,3
Textiltechnologische Innovationen im Bereich adaptierter Kleidung für Menschen mit Handicap Ausgangssituation: Laut Statistischem Bundesamt in Wiesbaden, lebten Ende des Jahres 2011 in Deutschland 7,3
Medizinische Rehabilitation bei Epilepsie
 Fachkliniken Wangen Medizinische Klinik Thoraxchirurgische Klinik Anästhesie und Intensivmedizin Neurologische Klinik Kinderklinik Rehabilitationskinderklinik www.fachkliniken-wangen.de Medizinische Rehabilitation
Fachkliniken Wangen Medizinische Klinik Thoraxchirurgische Klinik Anästhesie und Intensivmedizin Neurologische Klinik Kinderklinik Rehabilitationskinderklinik www.fachkliniken-wangen.de Medizinische Rehabilitation
Service-Angebote des BPI
 Pharmakovigilanz Service-Angebote des BPI BPI-Pharmakovigilanz Knowledge Base Mit dem EU-Pharmapackage und dem Zweiten Gesetz zur Änderung arzneimittelrechtlicher und anderer Vorschriften vom 19. Oktober
Pharmakovigilanz Service-Angebote des BPI BPI-Pharmakovigilanz Knowledge Base Mit dem EU-Pharmapackage und dem Zweiten Gesetz zur Änderung arzneimittelrechtlicher und anderer Vorschriften vom 19. Oktober
Häufig gestellte Fragen (FAQs)
 Häufig gestellte Fragen (FAQs) EU-Register für klinische Prüfungen (EU-CTR) (Inoffizielle Übersetzung des englischen Originaltextes durch das Paul-Ehrlich-Institut) URL: https://www.clinicaltrialsregister.eu/
Häufig gestellte Fragen (FAQs) EU-Register für klinische Prüfungen (EU-CTR) (Inoffizielle Übersetzung des englischen Originaltextes durch das Paul-Ehrlich-Institut) URL: https://www.clinicaltrialsregister.eu/
Dominik Stockem Datenschutzbeauftragter Microsoft Deutschland GmbH
 Dominik Stockem Datenschutzbeauftragter Microsoft Deutschland GmbH Peter Cullen, Microsoft Corporation Sicherheit - Die Sicherheit der Computer und Netzwerke unserer Kunden hat Top-Priorität und wir haben
Dominik Stockem Datenschutzbeauftragter Microsoft Deutschland GmbH Peter Cullen, Microsoft Corporation Sicherheit - Die Sicherheit der Computer und Netzwerke unserer Kunden hat Top-Priorität und wir haben
Winware Zahlungsverkehr mit Lieferanten
 Winware Zahlungsverkehr mit Lieferanten Inhalt Oranger Einzahlungsschein (TA 826)... 2 Oranger Einzahlungsschein mit indirekt Begünstigter (TA 826)... 3 IPI/IBAN- Beleg (TA 836)... 4 Zahlungen an die Übrigen
Winware Zahlungsverkehr mit Lieferanten Inhalt Oranger Einzahlungsschein (TA 826)... 2 Oranger Einzahlungsschein mit indirekt Begünstigter (TA 826)... 3 IPI/IBAN- Beleg (TA 836)... 4 Zahlungen an die Übrigen
Anforderungen, KEFs und Nutzen der Software- Prozessverbesserung
 Process flow Remarks Role Documents, data, tool input, output Important: Involve as many PZU as possible PZO Start Use appropriate templates for the process documentation Define purpose and scope Define
Process flow Remarks Role Documents, data, tool input, output Important: Involve as many PZU as possible PZO Start Use appropriate templates for the process documentation Define purpose and scope Define
10 Antworten zum Thema Generika
 10 Antworten zum Thema Generika Die mit dem Regenbogen Liebe Leserin, Lieber Leser Immer mehr Schweizerinnen und Schweizer leiden unter den jährlich steigenden Gesundheitskosten und Krankenkassenprämien.
10 Antworten zum Thema Generika Die mit dem Regenbogen Liebe Leserin, Lieber Leser Immer mehr Schweizerinnen und Schweizer leiden unter den jährlich steigenden Gesundheitskosten und Krankenkassenprämien.
Regulatorischer Rahmen. Klassifizierung
 Regulatorischer Rahmen Erkenntnisgewinn zu Regenerations- und Reparaturprozessen des menschlichen Körpers führen zu neuen Arten innovativer und komplexer Produkte. Unter Regenerativer Medizin (kurz: RegMed)
Regulatorischer Rahmen Erkenntnisgewinn zu Regenerations- und Reparaturprozessen des menschlichen Körpers führen zu neuen Arten innovativer und komplexer Produkte. Unter Regenerativer Medizin (kurz: RegMed)
Kostenreduktion durch Prävention?
 Gesundheitsökonomische Aspekte der Prävention: Kostenreduktion durch Prävention? Nadja Chernyak, Andrea Icks Jahrestagung DGSMP September 2012 Agenda Spart Prävention Kosten? Ist Prävention ökonomisch
Gesundheitsökonomische Aspekte der Prävention: Kostenreduktion durch Prävention? Nadja Chernyak, Andrea Icks Jahrestagung DGSMP September 2012 Agenda Spart Prävention Kosten? Ist Prävention ökonomisch
GVP Module V Risk Management Systems
 GVP Module V Risk Management Systems Dr. Susanne Wolf Institut für Pharmakovigilanz AGES Gespräche Wien, 26.04.2012 Österreichische Agentur für Gesundheit und Ernährungssicherheit GmbH Guideline on good
GVP Module V Risk Management Systems Dr. Susanne Wolf Institut für Pharmakovigilanz AGES Gespräche Wien, 26.04.2012 Österreichische Agentur für Gesundheit und Ernährungssicherheit GmbH Guideline on good
Sparkasse. Der Standard in Europa: IBAN und BIC.
 Sparkasse Der Standard in Europa: IBAN und BIC. Sehr geehrte Kundin, sehr geehrter Kunde, im neuen einheitlichen Euro-Zahlungsverkehrsraum (SEPA Single Euro Payments Area) sollen Ihre grenzüberschreitenden
Sparkasse Der Standard in Europa: IBAN und BIC. Sehr geehrte Kundin, sehr geehrter Kunde, im neuen einheitlichen Euro-Zahlungsverkehrsraum (SEPA Single Euro Payments Area) sollen Ihre grenzüberschreitenden
1. Pharmaindustrie allgemein. 2. Das Pharmaunternehmen GlaxoSmithKline. Autoren: Anke Jakubzik Tobias Bräutigam
 Unternehmen als internationale Akteure 1. Pharmaindustrie allgemein 2. Das Pharmaunternehmen GlaxoSmithKline Autoren: Anke Jakubzik Tobias Bräutigam Pharmaindustrie allgemein! ein Teil der chemischen Industrie,
Unternehmen als internationale Akteure 1. Pharmaindustrie allgemein 2. Das Pharmaunternehmen GlaxoSmithKline Autoren: Anke Jakubzik Tobias Bräutigam Pharmaindustrie allgemein! ein Teil der chemischen Industrie,
New Member of CEGH Gas Exchange Spot & Futures Market:
 New Member of CEGH Gas Exchange Spot & Futures Market: Axpo Trading AG On the 2 nd July 2015 the management of Wiener Börse has decided to approve Axpo Trading AG as member of CEGH Gas Exchange Spot and
New Member of CEGH Gas Exchange Spot & Futures Market: Axpo Trading AG On the 2 nd July 2015 the management of Wiener Börse has decided to approve Axpo Trading AG as member of CEGH Gas Exchange Spot and
Beschluss. I. Die Anlage XII wird in alphabetischer Reihenfolge um den Wirkstoff Vortioxetin wie folgt ergänzt:
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Arzneimittelforschung mit Kindern - Ethisch geboten oder bedenklich?
 Arzneimittelforschung mit Kindern - Ethisch geboten oder bedenklich? Von der Forschung an Kindern zur Forschung mit und für Kinder Arzneimittelforschung mit Kindern - Einleitung Forum Bioethik, Deutscher
Arzneimittelforschung mit Kindern - Ethisch geboten oder bedenklich? Von der Forschung an Kindern zur Forschung mit und für Kinder Arzneimittelforschung mit Kindern - Einleitung Forum Bioethik, Deutscher
Innovationszentren in der GKV-Versorgung -
 Innovationszentren in der GKV-Versorgung Patientenwohl als Wettbewerbsvorteil Derzeit wenden Krankenhäuser neue Untersuchungs- und Behandlungsmethoden an, ohne dass vorab Nutzen und Schaden geprüft werden.
Innovationszentren in der GKV-Versorgung Patientenwohl als Wettbewerbsvorteil Derzeit wenden Krankenhäuser neue Untersuchungs- und Behandlungsmethoden an, ohne dass vorab Nutzen und Schaden geprüft werden.
*EP001506783A1* EP 1 506 783 A1 (19) (11) EP 1 506 783 A1 (12) EUROPÄISCHE PATENTANMELDUNG. (43) Veröffentlichungstag: 16.02.2005 Patentblatt 2005/07
 (19) Europäisches Patentamt European Patent Office Office européen des brevets *EP001506783A1* (11) EP 1 506 783 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 16.02.2005 Patentblatt 2005/07
(19) Europäisches Patentamt European Patent Office Office européen des brevets *EP001506783A1* (11) EP 1 506 783 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 16.02.2005 Patentblatt 2005/07
Beteiligung der Beschäftigten an betrieblicher Weiterbildung. und Unternehmensgröße
 Beteiligung der Beschäftigten an betrieblicher Weiterbildung und Unternehmensgröße Befunde auf der Grundlage von CVTS3 Friederike Behringer, Gudrun Schönfeld Bonn, Februar 2011 1 Vorbemerkung Im Folgenden
Beteiligung der Beschäftigten an betrieblicher Weiterbildung und Unternehmensgröße Befunde auf der Grundlage von CVTS3 Friederike Behringer, Gudrun Schönfeld Bonn, Februar 2011 1 Vorbemerkung Im Folgenden
International Society of Drug Bulletins ein weltweiter Zusammenschluss unabhängiger Arzneimittelzeitschriften Erahrungen und Perspektiven
 34. Interdisziplinäres res Forum der Bundesärztekammer Unabhängige ngige Arzneimittelinformation International Society of Drug Bulletins ein weltweiter Zusammenschluss unabhängiger Arzneimittelzeitschriften
34. Interdisziplinäres res Forum der Bundesärztekammer Unabhängige ngige Arzneimittelinformation International Society of Drug Bulletins ein weltweiter Zusammenschluss unabhängiger Arzneimittelzeitschriften
Gründe für fehlende Vorsorgemaßnahmen gegen Krankheit
 Gründe für fehlende Vorsorgemaßnahmen gegen Krankheit politische Lage verlassen sich auf Familie persönliche, finanzielle Lage meinen, sich Vorsorge leisten zu können meinen, sie seien zu alt nicht mit
Gründe für fehlende Vorsorgemaßnahmen gegen Krankheit politische Lage verlassen sich auf Familie persönliche, finanzielle Lage meinen, sich Vorsorge leisten zu können meinen, sie seien zu alt nicht mit
Pflegewissenschaftliche Aspekte bei Familien mit chronisch kranken Kindern
 Pflegewissenschaftliche Aspekte bei Familien mit chronisch kranken Kindern Bernadette Bächle-Helde Pflegeexpertin Kinderkrankenschwester Diplompflegepädagogin (FH) Pflegewissenschaftlerin MScN Überblick
Pflegewissenschaftliche Aspekte bei Familien mit chronisch kranken Kindern Bernadette Bächle-Helde Pflegeexpertin Kinderkrankenschwester Diplompflegepädagogin (FH) Pflegewissenschaftlerin MScN Überblick
Patente und Unterlagenschutz
 Patente und Unterlagenschutz ANWALTSKANZLEI STRÄTER Burkhard Sträter Kronprinzenstraße 20 53173 Bonn Tel.:++49-228-93454-0 Fax.:++49-228-93454-54 Mail@kanzleistraeter.de www.kanzleistraeter.de Protection
Patente und Unterlagenschutz ANWALTSKANZLEI STRÄTER Burkhard Sträter Kronprinzenstraße 20 53173 Bonn Tel.:++49-228-93454-0 Fax.:++49-228-93454-54 Mail@kanzleistraeter.de www.kanzleistraeter.de Protection
Faktenbox Kombinationsbehandlung (Antidepressiva und Psychotherapie) bei schweren Depressionen
 Faktenbox (Antidepressiva und Psychotherapie) bei schweren Depressionen Nutzen und Risiken im Überblick Was ist eine? Was passiert bei einer? Bei einer werden mehrere Therapien miteinander gekoppelt: Antidepressiva
Faktenbox (Antidepressiva und Psychotherapie) bei schweren Depressionen Nutzen und Risiken im Überblick Was ist eine? Was passiert bei einer? Bei einer werden mehrere Therapien miteinander gekoppelt: Antidepressiva
Ein neues System für die Allokation von Spenderlungen. LAS Information für Patienten in Deutschland
 Ein neues System für die Allokation von Spenderlungen LAS Information für Patienten in Deutschland Ein neues System für die Allokation von Spenderlungen Aufgrund des immensen Mangels an Spenderorganen
Ein neues System für die Allokation von Spenderlungen LAS Information für Patienten in Deutschland Ein neues System für die Allokation von Spenderlungen Aufgrund des immensen Mangels an Spenderorganen
EP 1 750 416 A1 (19) (11) EP 1 750 416 A1 (12) EUROPÄISCHE PATENTANMELDUNG. (43) Veröffentlichungstag: 07.02.2007 Patentblatt 2007/06
 (19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 1 750 416 A1 (43) Veröffentlichungstag: 07.02.2007 Patentblatt 2007/06 (51) Int Cl.: H04L 29/12 (2006.01) (21) Anmeldenummer: 05016706.3 (22) Anmeldetag: 01.08.2005
(19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 1 750 416 A1 (43) Veröffentlichungstag: 07.02.2007 Patentblatt 2007/06 (51) Int Cl.: H04L 29/12 (2006.01) (21) Anmeldenummer: 05016706.3 (22) Anmeldetag: 01.08.2005
(51) Int Cl. 7 : G09F 21/12. (72) Erfinder: Schimanz, Gerhard
 (19) Europäisches Patentamt European Patent Office Office européen des brevets *EP001411488A1* (11) EP 1 411 488 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 21.04.2004 Patentblatt 2004/17
(19) Europäisches Patentamt European Patent Office Office européen des brevets *EP001411488A1* (11) EP 1 411 488 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 21.04.2004 Patentblatt 2004/17
Strompreise 2011 Fakten und Zusammenhänge Kurt Rohrbach, Präsident VSE. VSE-Medienkonferenz, Hotel Bern, 26. August 2010
 Strompreise 2011 Fakten und Zusammenhänge Kurt Rohrbach, Präsident VSE VSE-Medienkonferenz, Hotel Bern, 26. August 2010 Inhalt Strompreise im Quervergleich Zusammensetzung Strompreis Einflussfaktoren Fazit
Strompreise 2011 Fakten und Zusammenhänge Kurt Rohrbach, Präsident VSE VSE-Medienkonferenz, Hotel Bern, 26. August 2010 Inhalt Strompreise im Quervergleich Zusammensetzung Strompreis Einflussfaktoren Fazit
Wie soll individualisierte Medizin in evidenzbasierten Leitlinien umgesetzt werden? Eine Analyse von Leitlinienmanualen
 IFOM INSTITUT FÜR FORSCHUNG IN DER OPERATIVEN MEDIZIN Wie soll individualisierte Medizin in evidenzbasierten Leitlinien umgesetzt werden? Eine Analyse von Leitlinienmanualen Michaela Eikermann, Tim Mathes,
IFOM INSTITUT FÜR FORSCHUNG IN DER OPERATIVEN MEDIZIN Wie soll individualisierte Medizin in evidenzbasierten Leitlinien umgesetzt werden? Eine Analyse von Leitlinienmanualen Michaela Eikermann, Tim Mathes,
Konzepte und Erfahrungen zur Bekämpfung von Mobbing in Europa Ergebnisse transnationaler Projekt
 Konzepte und Erfahrungen zur Bekämpfung von Mobbing in Europa Ergebnisse transnationaler Projekt Annett Wiedermann ein Beitrag zur Tagung: Gewalterfahrung und Gewaltprävention bei Kindern und Jugendlichen
Konzepte und Erfahrungen zur Bekämpfung von Mobbing in Europa Ergebnisse transnationaler Projekt Annett Wiedermann ein Beitrag zur Tagung: Gewalterfahrung und Gewaltprävention bei Kindern und Jugendlichen
*EP001363019A2* EP 1 363 019 A2 (19) (11) EP 1 363 019 A2 (12) EUROPÄISCHE PATENTANMELDUNG. (43) Veröffentlichungstag: 19.11.2003 Patentblatt 2003/47
 (19) Europäisches Patentamt European Patent Office Office européen des brevets *EP001363019A2* (11) EP 1 363 019 A2 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 19.11.2003 Patentblatt 2003/47
(19) Europäisches Patentamt European Patent Office Office européen des brevets *EP001363019A2* (11) EP 1 363 019 A2 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 19.11.2003 Patentblatt 2003/47
4.5 Disease-Management-Programme
 4.5 Disease-Management-Programme Das Disease-Management-Programm (DMP) ist ein Organisationsansatz von medizinischer Versorgung, bei dem die Behandlungs- und Betreuungsprozesse von über den gesamten Verlauf
4.5 Disease-Management-Programme Das Disease-Management-Programm (DMP) ist ein Organisationsansatz von medizinischer Versorgung, bei dem die Behandlungs- und Betreuungsprozesse von über den gesamten Verlauf
Die wirtschaftliche Bedeutung des Campingtourismus in Deutschland!
 Die wirtschaftliche Bedeutung des Campingtourismus in Deutschland! 1. Informationsveranstaltung der! Qualitätsoffensive Campingtourismus! 23. November 2010, Oldenburg i. H.! Dirk Dunkelberg! Stellv. Hauptgeschäftsführer!
Die wirtschaftliche Bedeutung des Campingtourismus in Deutschland! 1. Informationsveranstaltung der! Qualitätsoffensive Campingtourismus! 23. November 2010, Oldenburg i. H.! Dirk Dunkelberg! Stellv. Hauptgeschäftsführer!
Patientensicherheit aus Patientensicht
 Patientensicherheit aus Patientensicht 6. MetrikAnwendertag Wir haben 100 Jahre versucht Konzepte zu entwickeln damit Menschen älter werden Jetzt haben wir es geschafft! und die Gesellschaft weiß nicht,
Patientensicherheit aus Patientensicht 6. MetrikAnwendertag Wir haben 100 Jahre versucht Konzepte zu entwickeln damit Menschen älter werden Jetzt haben wir es geschafft! und die Gesellschaft weiß nicht,
Flash Eurobarometer 345 ZUGÄNGLICHKEIT ZUSAMMENFASSUNG
 Flash Eurobarometer 345 ZUGÄNGLICHKEIT ZUSAMMENFASSUNG Befragung: März 2012 Veröffentlichung: Dezember 2012 Diese Umfrage wurde von der Europäischen Kommission, Generaldirektion Justiz in Auftrag gegeben
Flash Eurobarometer 345 ZUGÄNGLICHKEIT ZUSAMMENFASSUNG Befragung: März 2012 Veröffentlichung: Dezember 2012 Diese Umfrage wurde von der Europäischen Kommission, Generaldirektion Justiz in Auftrag gegeben
Indikationserweiterungen für JANUVIA (Sitagliptin, MSD) in der EU - Kombination mit Sulfonylharnstoff n
 Indikationserweiterungen für JANUVIA (Sitagliptin, MSD) in der EU Kombination mit Sulfonylharnstoff nun ebenfalls zugelassen Haar (März 2008) - Die europäische Arzneimittelbehörde EMEA hat JANUVIA für
Indikationserweiterungen für JANUVIA (Sitagliptin, MSD) in der EU Kombination mit Sulfonylharnstoff nun ebenfalls zugelassen Haar (März 2008) - Die europäische Arzneimittelbehörde EMEA hat JANUVIA für
2013 Dr. Dietmar Bayer bayer@burnout-zentrum.at 1
 bayer@burnout-zentrum.at 1 4 bayer@burnout-zentrum.at 2 Datenmaterial im Gesundheitswesen Kein einheitliches Datenmaterial in den Krankenanstalten, Kassen, der PVA etc. etc. Prävalenz von BO in der Normalpopulation
bayer@burnout-zentrum.at 1 4 bayer@burnout-zentrum.at 2 Datenmaterial im Gesundheitswesen Kein einheitliches Datenmaterial in den Krankenanstalten, Kassen, der PVA etc. etc. Prävalenz von BO in der Normalpopulation
Die Mitgliedstaaten der EU
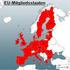 Die Mitgliedstaaten der EU Arbeitsaufträge: 1. Trage in die einzelnen EU-Mitgliedstaaten die jeweilige Abkürzung ein! 2. Schlage in deinem Atlas nach, wo die Hauptstädte der einzelnen Länder liegen und
Die Mitgliedstaaten der EU Arbeitsaufträge: 1. Trage in die einzelnen EU-Mitgliedstaaten die jeweilige Abkürzung ein! 2. Schlage in deinem Atlas nach, wo die Hauptstädte der einzelnen Länder liegen und
3.5 Disease-Management-Programme
 3.5 Disease-Management-Programme Das Disease-Management-Programm (DMP) ist ein Organisationsansatz von medizinischer Versorgung, bei dem die Behandlungs- und Betreuungsprozesse von über den gesamten Verlauf
3.5 Disease-Management-Programme Das Disease-Management-Programm (DMP) ist ein Organisationsansatz von medizinischer Versorgung, bei dem die Behandlungs- und Betreuungsprozesse von über den gesamten Verlauf
Das Boxenmodell des EKO
 Das Boxenmodell des EKO Ernst Agneter 2005 01 14 2005 Dr. Ernst Agneter Inhalt Entstehung (Rückblick 2004) ATC-System Boxensystem Information der Ärzte 2005 01 14 2005 Dr. Ernst Agneter 2 Entstehung (Rückblick
Das Boxenmodell des EKO Ernst Agneter 2005 01 14 2005 Dr. Ernst Agneter Inhalt Entstehung (Rückblick 2004) ATC-System Boxensystem Information der Ärzte 2005 01 14 2005 Dr. Ernst Agneter 2 Entstehung (Rückblick
07.072. Forschung am Menschen. Verfassungsbestimmung ARGUMENTARIEN CONTRA
 07.072 Forschung am Menschen. Verfassungsbestimmung ARGUMENTARIEN CONTRA Verfassungsartikel über die Forschung am Menschen Art. 118b Hauptkritikpunkt: Abs 2,Bst c «Fremdnützige Forschung an urteilsunfähigen
07.072 Forschung am Menschen. Verfassungsbestimmung ARGUMENTARIEN CONTRA Verfassungsartikel über die Forschung am Menschen Art. 118b Hauptkritikpunkt: Abs 2,Bst c «Fremdnützige Forschung an urteilsunfähigen
... Don t be. V. Data Privacy Protection. Jennifer Luxshmy Harikantha, Anna Klein, Gunnar Anderson
 V. Data Privacy Protection Don t be Jennifer Luxshmy Harikantha, Anna Klein, Gunnar Anderson T-Mobile Chair for M-Business & Multilateral Security J.W. Goethe Universität Frankfurt a. M. Agenda Datenschutzdiskussion
V. Data Privacy Protection Don t be Jennifer Luxshmy Harikantha, Anna Klein, Gunnar Anderson T-Mobile Chair for M-Business & Multilateral Security J.W. Goethe Universität Frankfurt a. M. Agenda Datenschutzdiskussion
TMF projects on IT infrastructure for clinical research
 Welcome! TMF projects on IT infrastructure for clinical research R. Speer Telematikplattform für Medizinische Forschungsnetze (TMF) e.v. Berlin Telematikplattform für Medizinische Forschungsnetze (TMF)
Welcome! TMF projects on IT infrastructure for clinical research R. Speer Telematikplattform für Medizinische Forschungsnetze (TMF) e.v. Berlin Telematikplattform für Medizinische Forschungsnetze (TMF)
Methodologie und Instrumentarium des Lead Partner Prinzips
 Interactive knowledge transfer for INTERREG Konferenz: Chancen und Herausforderungen im ETZ Programm 2007 2013 Sopron, 31. Januar 2007 Mauro Novello INTERACT Point Managing Transition and External Cooperation
Interactive knowledge transfer for INTERREG Konferenz: Chancen und Herausforderungen im ETZ Programm 2007 2013 Sopron, 31. Januar 2007 Mauro Novello INTERACT Point Managing Transition and External Cooperation
PSUR Worksharing. Erste Erfahrungen und offene Fragen
 PSUR Worksharing Erste Erfahrungen und offene Fragen 1 Ziel des Projekts Initiative der Heads of Medicines Agencies Working Group on PSUR synchronisation Ziel: EU-weite Synchronisierung der PSUR Vorlage
PSUR Worksharing Erste Erfahrungen und offene Fragen 1 Ziel des Projekts Initiative der Heads of Medicines Agencies Working Group on PSUR synchronisation Ziel: EU-weite Synchronisierung der PSUR Vorlage
Grenzüberschreitungen aus medizinischen Gründen Demografische Aspekte
 Grenzüberschreitungen aus medizinischen Gründen Demografische Aspekte Unionsbürgerschaft, Patientenfreizügigkeit und Begrenzung der Ausgaben für Gesundheit Tagung Max-Planck-Institut Universität Rennes
Grenzüberschreitungen aus medizinischen Gründen Demografische Aspekte Unionsbürgerschaft, Patientenfreizügigkeit und Begrenzung der Ausgaben für Gesundheit Tagung Max-Planck-Institut Universität Rennes
Diese Broschüre fasst die wichtigsten Informationen zusammen, damit Sie einen Entscheid treffen können.
 Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
BAnz AT 11.11.2014 B1. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Theoretische und praktische Auswirkungen altersabhängiger medizinischer Reihenuntersuchungen
 Theoretische und praktische Auswirkungen altersabhängiger medizinischer Reihenuntersuchungen GMTTB, 13.12.2013, Konstanz Uwe Ewert, Dr. phil. MPH, wissenschaftlicher Mitarbeiter u.ewert@bfu.ch www.bfu.ch
Theoretische und praktische Auswirkungen altersabhängiger medizinischer Reihenuntersuchungen GMTTB, 13.12.2013, Konstanz Uwe Ewert, Dr. phil. MPH, wissenschaftlicher Mitarbeiter u.ewert@bfu.ch www.bfu.ch
DAS GRÜNE REZEPT. Für eine sichere Medikation mit rezeptfreien Arzneimitteln
 DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
BAnz AT 20.11.2014 B3. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Was bedeutet die neue Gesetzgebung für mein Forschungsprojekt? Das neue Humanforschungsgesetz
 Was bedeutet die neue Gesetzgebung für mein Forschungsprojekt? Das neue Humanforschungsgesetz 6. Juni 2013 Brigitte Meier Leitung Sektion Forschung am Mensch und Ethik Bundesamt für Gesundheit Inhalt 1.
Was bedeutet die neue Gesetzgebung für mein Forschungsprojekt? Das neue Humanforschungsgesetz 6. Juni 2013 Brigitte Meier Leitung Sektion Forschung am Mensch und Ethik Bundesamt für Gesundheit Inhalt 1.
(Veröffentlichungsbedürftige Rechtsakte)
 27.12.2006 L 378/1 I (Veröffentlichungsbedürftige Rechtsakte) VERORDNUNG (EG) Nr. 1901/2006 S EUROPÄISCHEN PARLAMENTS UND S RATES vom 12. Dezember 2006 über Kinderarzneimittel und zur Änderung der Verordnung
27.12.2006 L 378/1 I (Veröffentlichungsbedürftige Rechtsakte) VERORDNUNG (EG) Nr. 1901/2006 S EUROPÄISCHEN PARLAMENTS UND S RATES vom 12. Dezember 2006 über Kinderarzneimittel und zur Änderung der Verordnung
Information und Beratung des Patienten bei der Abgabe von Arzneimitteln Erst- und Wiederholungsverordnung
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Information und Beratung des Patienten bei der Abgabe von Arzneimitteln Erst- und Stand der Revision: 13.11.2013
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Information und Beratung des Patienten bei der Abgabe von Arzneimitteln Erst- und Stand der Revision: 13.11.2013
Personalisierte Medizin Ende der Solidarität? Heiner Raspe Seniorprofessur für Bevölkerungsmedizin
 Personalisierte Medizin Ende der Solidarität? Heiner Raspe Seniorprofessur für Bevölkerungsmedizin Berlin - Deutscher Ethikrat 24.Mai 2012 Kritische Anmerkungen zur PersoMed Unter falscher Flagge Kritische
Personalisierte Medizin Ende der Solidarität? Heiner Raspe Seniorprofessur für Bevölkerungsmedizin Berlin - Deutscher Ethikrat 24.Mai 2012 Kritische Anmerkungen zur PersoMed Unter falscher Flagge Kritische
Primärer Endpunkt Fallzahlkalkulation...
 Prospective randomized multicentre investigator initiated study: Randomised trial comparing completeness of adjuvant chemotherapy after early versus late diverting stoma closure in low anterior resection
Prospective randomized multicentre investigator initiated study: Randomised trial comparing completeness of adjuvant chemotherapy after early versus late diverting stoma closure in low anterior resection
2. Anzahl der Patienten bzw. Abgrenzung der für die Behandlung infrage kommenden Patientengruppen
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Horizon 2020: Das KMU-Instrument EU-Förderung für marktnahe Innovationen
 Horizon 2020: Das KMU-Instrument EU-Förderung für marktnahe Innovationen Nina Gibbert-Doll Hessen Trade & Invest GmbH Enterprise Europe Network Hessen 3. Juli 2015 Wetzlar Innovationskette KMU-Instrument
Horizon 2020: Das KMU-Instrument EU-Förderung für marktnahe Innovationen Nina Gibbert-Doll Hessen Trade & Invest GmbH Enterprise Europe Network Hessen 3. Juli 2015 Wetzlar Innovationskette KMU-Instrument
gemeinsam Nachbesserungen zum Schutz der Patienten
 EU-Verordnungsentwurf für Medizinprodukte Europaweit fordern Krankenversicherungen gemeinsam Nachbesserungen zum Schutz der Patienten Berlin (2. November 2012) Brustimplantate mit hauchdünnen Hüllen, die
EU-Verordnungsentwurf für Medizinprodukte Europaweit fordern Krankenversicherungen gemeinsam Nachbesserungen zum Schutz der Patienten Berlin (2. November 2012) Brustimplantate mit hauchdünnen Hüllen, die
Klinische Prüfungen Internationale Rahmenbedingungen Ein Überblick 22 Mai 2014. Sabine Atzor, F. Hoffmann-La Roche Ltd
 Klinische Prüfungen Internationale Rahmenbedingungen Ein Überblick 22 Mai 2014 Sabine Atzor, F. Hoffmann-La Roche Ltd Klinische Prüfung/ Klinischer Versuch von Arzneimitteln am Menschen Untersuchung von
Klinische Prüfungen Internationale Rahmenbedingungen Ein Überblick 22 Mai 2014 Sabine Atzor, F. Hoffmann-La Roche Ltd Klinische Prüfung/ Klinischer Versuch von Arzneimitteln am Menschen Untersuchung von
Gliederung. Gliederung. Stellenwert der Versorgungsforschung in der Onkologie und praktische Beispiele
 art\vorveran\dgho10\graphik1.cdr Stellenwert der Versorgungsforschung in der Onkologie und praktische Beispiele Symposium Anforderungen an vorsorgungsrelevante, nichtkommerielle Studien zu Arzneimitteln
art\vorveran\dgho10\graphik1.cdr Stellenwert der Versorgungsforschung in der Onkologie und praktische Beispiele Symposium Anforderungen an vorsorgungsrelevante, nichtkommerielle Studien zu Arzneimitteln
