Gesetzliche Grundlagen der Arzneimittelentwicklung national/ international
|
|
|
- Ralph Pfaff
- vor 6 Jahren
- Abrufe
Transkript
1 Gesetzliche Grundlagen der Arzneimittelentwicklung national/ international Dr. med. Dirk Mentzer Referatsleiter Arzneimittelsicherheit Facharzt für Kinder- und Jugendmedizin Paul-Ehrlich-Institut Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel Langen (Hessen) Inhalt System der Arzneimittel Zulassung in der EU und DE Arzneimitteltherapie Untersuchung zum Nutzen Arzneimitteltherapie Überwachung der Risiken Rolle der Kinderärzte
2
3 aber was genau kann bei der Behandlung von Kindern in diesem Fall zum Zeitpunkt nach der Zulassung geantwortet werden?
4 Wissen Gesetzliche Grundlagen der Arzneimittelentwicklung national/ international Wissen und Feststellung des Nutzen/ Risiko bei Zulassung Wirksamkeit Tolerabilität Qualität? Arzneimittelsicherheit / Risiken?
5 Markt Gesetze Kinderheilkunde Forschung Klinische Studien Zulassung Kostenerstattung Ethik Therapiebedarf Subpopulation Patient/ Eltern Forschung an Kinder ja bitte, aber nicht mit meinem Kind
6 (Paul, S.M., et al.: Nature Reviews Drug Discovery 9, (2010)) Grundlagenforschung Wissenschaftliche Publikation EU Verordnung 1901/2006 Gesetzlicher Rahmen für die Entwicklung neuer Arzneimittel, die ebenfalls in der päd. Population angewendet werden können bzw. den Stand der wissenschaftlichen Kenntnis verbessern sollen. Gesundheit der Kinder
7 Lösungen: Pädiatrische Komitee bei der EMA Zusammensetzung 5 CHMP Mitglieder + 3 Mitglieder - Patientengruppen + 3 Mitglieder der Fachgesellschaft Ein Mitglied/ Vertreter pro Land 12 Meetings pro Jahr
8 Lösungen: Pädiatrischer Prüfplan Die Pädiatrische Arzneimittel Verordnungen (EU 1901/2006) gilt unmittelbar in der EU/EEA. Gilt für Kinder von 0 bis zum 18. Lebensjahr (ohne das 18.) Bei Antragung auf Zulassung oder bei Indikationserweiterung (Arzneimittel unter Patentschutz) muss ein genehmigtes pädiatrisches Prüfkonzept (PIP) vorliegen (Art.7 bzw. 8). Freistellung (Waiver) Zurückstellung (Deferral) PUMA (Paediatric Use Marketing Authorisation) MICE (Medicine in Children)
9 Lösungen: Pädiatrischer Prüfplan PIP ist bindend für Zulassungsinhaber und EMEA Die Entscheidung für eine Freistellung (Waiver) ist abhängig vom 1. Arzneimittel 2. der Erkrankung (Waiver versus PIP und Deferral) 3. dem therapeutischen Effekt (Waiver) 4. den pädiatrischen Therapiebedarf (Paediatric Needs) Ausgenommen von der PIP Pflicht sind 1. Generika, Blutkomponenten 2. Herbals 3. well-established-use medicinal products
10 Bewertung eines Pädiatrischen Prüfplans Tag 30 erste Diskussion im PDCO Rapporteur => 20 Tag Peer Reviewer => 28 Tag Tag 60 zweite Diskussion im PDCO Clock stop Restart Tag 90 dritte Diskussion in PDCO und OE* Beschluss der Opinion durch PDCO 30 Tage 60 Tage 90 Tage 60 Tage Tag -30 PIP Validierung durch EMEA Beschluss der Opinion oder Liste mit offenen Fragen Tag 61 PIP update validiert durch EMEA EMEA Entscheidung an Antragsteller
11 Bewertung eines Pädiatrischen Prüfplans PIP Konzeption schließt das gesamte Unternehmen ein - wann pädiatrische Studien erfolgen sollten - welche Sicherheitsaspekte berücksichtigt werden sollten - Berücksichtigung von ethischen Besonderheiten der Studien Änderung im PIP müssen vom PDCO akzeptiert sein Die Entscheidung über den PIP werden publiziert Class waiver Liste wird vom PDCO regelmäßig aktualisiert
12 Early dialoge project Pilot to start in Q2-2015
13 Möglichkeiten für die Kinderärzte aktiv zu werden Forschung: - Arzneimittel und klinische Forschung - Klinische Studien in Netzwerken - Post-Marketing Studien und Register Patientenversorgung: - Notwendigkeit der klinischen Studien - speziell bei Arzneimittel ohne Patent - Ausbildung Studium und Weiterbildung - Beteiligung der Kinder/ Eltern
14 Ziel einer gesetzlichen Regelung Arzneimitteln Entwicklung für Kinder mit gleichen qualitativen, wissenschaftlichen und ethischen Standards Zeitgleiche Arzneimittel Zulassung für Kinder und Erwachsene Unterstützung von klinischen Prüfungen zur Nutzenanalyse Beteiligung an post-marketing Überwachung Verwendung der altersentsprechenden Formulierung Aufklärung Hinweise in der Fachinformation
15 Child health Research & development Vielen Dank für Ihre Aufmerksamkeit
Die neue Rolle von Kindern im Arzneimittelrecht und ihre praktischen Konsequenzen. Was hat mein Kind von der EU? Prof. Dr. med. Joachim Boos, Münster
 Die neue Rolle von Kindern im Arzneimittelrecht und ihre praktischen Konsequenzen Was hat mein Kind von der EU? Prof. Dr. med. Joachim Boos, Münster Bayer Werbung um 1900: Heroin, das ideale Sedativum
Die neue Rolle von Kindern im Arzneimittelrecht und ihre praktischen Konsequenzen Was hat mein Kind von der EU? Prof. Dr. med. Joachim Boos, Münster Bayer Werbung um 1900: Heroin, das ideale Sedativum
Pädiatrisches Prüfkonzept (PIP) - Dos and Don ts anhand regulatorischer Erfahrung
 Pädiatrisches Prüfkonzept (PIP) - Dos and Don ts anhand regulatorischer Erfahrung Reinhard Hiersemenzel Senior Medical Expert Global Clinical R&D CNS Merz Pharmaceuticals GmbH - Nicht befugt, für und im
Pädiatrisches Prüfkonzept (PIP) - Dos and Don ts anhand regulatorischer Erfahrung Reinhard Hiersemenzel Senior Medical Expert Global Clinical R&D CNS Merz Pharmaceuticals GmbH - Nicht befugt, für und im
Arzneimittelforschung mit Kindern - Ethisch geboten oder bedenklich?
 Arzneimittelforschung mit Kindern - Ethisch geboten oder bedenklich? Von der Forschung an Kindern zur Forschung mit und für Kinder Arzneimittelforschung mit Kindern - Einleitung Forum Bioethik, Deutscher
Arzneimittelforschung mit Kindern - Ethisch geboten oder bedenklich? Von der Forschung an Kindern zur Forschung mit und für Kinder Arzneimittelforschung mit Kindern - Einleitung Forum Bioethik, Deutscher
Gute Klinische Praxis : Prüfungsmaßstäbe für die Ethik-Kommission
 Gute Klinische Praxis : Prüfungsmaßstäbe für die Ethik-Kommission ass. iur. Jan Paus, LL.M. Rechtsreferent Ethik-Kommission der Ärztekammer Westfalen-Lippe und der Medizinischen Fakultät der WWU Münster
Gute Klinische Praxis : Prüfungsmaßstäbe für die Ethik-Kommission ass. iur. Jan Paus, LL.M. Rechtsreferent Ethik-Kommission der Ärztekammer Westfalen-Lippe und der Medizinischen Fakultät der WWU Münster
Prof. Dr. Dr. Martin HärterH
 Effekte von Shared Decision-Making Forschungsstand zur Adherence Prof. Dr. Dr. Martin HärterH Fachtagung Adherence Berlin 11.12.2009 Definition Adherence ist definiert als das Ausmaß, in welchem das Verhalten
Effekte von Shared Decision-Making Forschungsstand zur Adherence Prof. Dr. Dr. Martin HärterH Fachtagung Adherence Berlin 11.12.2009 Definition Adherence ist definiert als das Ausmaß, in welchem das Verhalten
Klinische Prüfungen Internationale Rahmenbedingungen Ein Überblick 22 Mai 2014. Sabine Atzor, F. Hoffmann-La Roche Ltd
 Klinische Prüfungen Internationale Rahmenbedingungen Ein Überblick 22 Mai 2014 Sabine Atzor, F. Hoffmann-La Roche Ltd Klinische Prüfung/ Klinischer Versuch von Arzneimitteln am Menschen Untersuchung von
Klinische Prüfungen Internationale Rahmenbedingungen Ein Überblick 22 Mai 2014 Sabine Atzor, F. Hoffmann-La Roche Ltd Klinische Prüfung/ Klinischer Versuch von Arzneimitteln am Menschen Untersuchung von
Die Sicht der EMEA. für Zulassungs-, Therapie- und. Berlin-Brandenburgische Akademie der
 Lebensqualität und Patientennutzen Die Sicht der EMEA PMS-Workshop: Lebensqualität als Kriterium für Zulassungs-, Therapie- und Erstattungsentscheidungen. Berlin-Brandenburgische Akademie der Wissenschaften
Lebensqualität und Patientennutzen Die Sicht der EMEA PMS-Workshop: Lebensqualität als Kriterium für Zulassungs-, Therapie- und Erstattungsentscheidungen. Berlin-Brandenburgische Akademie der Wissenschaften
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien
 Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
Wie funktioniert eine klinische Studie?
 Wie funktioniert eine klinische Studie? Bernhard Saller 3. Süddeutscher Hypophysen- und Nebennierentag München, 5. Mai 2007 Definitionen Ablauf klinischer Studien Klinische Arzneimittelprüfungen Zulassungsprozess
Wie funktioniert eine klinische Studie? Bernhard Saller 3. Süddeutscher Hypophysen- und Nebennierentag München, 5. Mai 2007 Definitionen Ablauf klinischer Studien Klinische Arzneimittelprüfungen Zulassungsprozess
Gesetzliche Vorgaben für die Aufbereitung von Instrumenten in der Podologie
 Gesetzliche Vorgaben für die Aufbereitung von Instrumenten in der Podologie Rechtliche Abgrenzung zwischen Podologie und Fußpflege Ziele des Medizinprodukterechtes: für die Gesundheit und den erforderlichen
Gesetzliche Vorgaben für die Aufbereitung von Instrumenten in der Podologie Rechtliche Abgrenzung zwischen Podologie und Fußpflege Ziele des Medizinprodukterechtes: für die Gesundheit und den erforderlichen
More Medicines for Minors
 More Medicines for Minors Arzneimittelzulassung für Kinder und Jugendliche verbessern Birka Lehmann More Medicines for Minors! Kinder sind keine kleinen Erwachsenen! Ziel der Verodnung (EG) Nr 1901/2006
More Medicines for Minors Arzneimittelzulassung für Kinder und Jugendliche verbessern Birka Lehmann More Medicines for Minors! Kinder sind keine kleinen Erwachsenen! Ziel der Verodnung (EG) Nr 1901/2006
Versandhandel: Sparen an der Patientensicherheit?
 Versandhandel: Sparen an der Patientensicherheit? Kai Vogel Symposium Fortschritt der Arzneimittelversorgung oder Gesundheitsgefährdung Rheinische Friedrich-Wilhelms-Universität Bonn 11. Oktober 2007 Gliederung
Versandhandel: Sparen an der Patientensicherheit? Kai Vogel Symposium Fortschritt der Arzneimittelversorgung oder Gesundheitsgefährdung Rheinische Friedrich-Wilhelms-Universität Bonn 11. Oktober 2007 Gliederung
Komplementärmedizin nach Transplantation?
 Komplementärmedizin nach Transplantation? Dr.med. Martin Frei-Erb Facharzt FMH Allgemeine Innere Medizin Institut für Komplementärmedizin IKOM Universität Bern 22.3.2014, 10. Symposium für Transplantierte,
Komplementärmedizin nach Transplantation? Dr.med. Martin Frei-Erb Facharzt FMH Allgemeine Innere Medizin Institut für Komplementärmedizin IKOM Universität Bern 22.3.2014, 10. Symposium für Transplantierte,
Die Dokumentation bei Eingriffen an der Wirbelsäule aus ärztlicher Sicht T. Auhuber
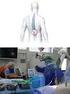 Die Dokumentation bei Eingriffen an der Wirbelsäule aus ärztlicher Sicht T. Auhuber Miljak / Weiß 1053 f&w 12/2015 2 Zeitlicher Dokumentationsaufwand nach Profession und Fachrichtung 03/2015 3 Zeitlicher
Die Dokumentation bei Eingriffen an der Wirbelsäule aus ärztlicher Sicht T. Auhuber Miljak / Weiß 1053 f&w 12/2015 2 Zeitlicher Dokumentationsaufwand nach Profession und Fachrichtung 03/2015 3 Zeitlicher
Bewertung von Kosten und Nutzen in der gesetzlichen Krankenversicherung
 Bewertung von Kosten und Nutzen in der gesetzlichen Krankenversicherung Mathias Kifmann, Universität Augsburg Marlies Ahlert, Universität Halle-Wittenberg Konferenz Kommunales Infrastruktur-Management
Bewertung von Kosten und Nutzen in der gesetzlichen Krankenversicherung Mathias Kifmann, Universität Augsburg Marlies Ahlert, Universität Halle-Wittenberg Konferenz Kommunales Infrastruktur-Management
Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic )
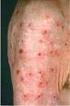 Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic ) Ergebnisse der europäischen Risiko- Bewertungs-Verfahren Anlass für die Risikobewertungsverfahren
Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic ) Ergebnisse der europäischen Risiko- Bewertungs-Verfahren Anlass für die Risikobewertungsverfahren
Better Medicines for Children 2007. Perspektive der EMEA nach 2 Jahren EU-Kinderarzneimittelverordnung
 Better Medicines for Children 2007 Perspektive der EMEA nach 2 Jahren EU-Kinderarzneimittelverordnung Ralph Bax EMEA London Arzneimittelforschung in der Pädiatrie Strategien und Chancen Symposium 1.10.2009
Better Medicines for Children 2007 Perspektive der EMEA nach 2 Jahren EU-Kinderarzneimittelverordnung Ralph Bax EMEA London Arzneimittelforschung in der Pädiatrie Strategien und Chancen Symposium 1.10.2009
Integration der gesetzlich authorisierten Arzneimittelinformation in rechnergestützte klinische Arbeitsplatzsysteme
 Integration der gesetzlich authorisierten Arzneimittelinformation in rechnergestützte klinische Arbeitsplatzsysteme unter Verwendung der ICD und der Alpha-ID Manfred Criegee-Rieck Ein paar Zahlen: Blick
Integration der gesetzlich authorisierten Arzneimittelinformation in rechnergestützte klinische Arbeitsplatzsysteme unter Verwendung der ICD und der Alpha-ID Manfred Criegee-Rieck Ein paar Zahlen: Blick
Paul-Ehrlich-Institut Bundesamt für Sera und Impfstoffe
 Bundesinstitut für Arzneimittel und Medizinprodukte Bundesamt für Sera und Impfstoffe Gemeinsame Empfehlungen des Bundesinstituts für Arzneimittel und Medizinprodukte und des s zur Planung, Durchführung
Bundesinstitut für Arzneimittel und Medizinprodukte Bundesamt für Sera und Impfstoffe Gemeinsame Empfehlungen des Bundesinstituts für Arzneimittel und Medizinprodukte und des s zur Planung, Durchführung
AMNOG: Wenn Innovation aufs System trifft: Ist das AMNOG System fit für Innovation- Beispiel Onkologie
 AMNOG: Wenn Innovation aufs System trifft: Ist das AMNOG System fit für Innovation- Beispiel Onkologie Dr. Jutta Wendel-Schrief Direktor Market Access MSD SHARP & DOHME GMBH Was sind Innovationen? Neue
AMNOG: Wenn Innovation aufs System trifft: Ist das AMNOG System fit für Innovation- Beispiel Onkologie Dr. Jutta Wendel-Schrief Direktor Market Access MSD SHARP & DOHME GMBH Was sind Innovationen? Neue
BAnz AT 20.11.2014 B3. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Nutzen-Schaden-Bewertung von Arzneimitteln nach der Zulassung
 Nutzen-Schaden-Bewertung von Arzneimitteln nach der Zulassung U. Hagemann Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Abteilung Pharmakovigilanz IQWiG im Dialog Köln, 19. Besuchen Sie unsere
Nutzen-Schaden-Bewertung von Arzneimitteln nach der Zulassung U. Hagemann Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Abteilung Pharmakovigilanz IQWiG im Dialog Köln, 19. Besuchen Sie unsere
BAnz AT B3. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung
 Bundesrat Drucksache 768/12 (Beschluss) 01.02.13 Beschluss des Bundesrates Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Der Bundesrat hat in seiner 906. Sitzung am 1. Februar
Bundesrat Drucksache 768/12 (Beschluss) 01.02.13 Beschluss des Bundesrates Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Der Bundesrat hat in seiner 906. Sitzung am 1. Februar
Roche in Deutschland Strategie in der Zusammenarbeit mit Forschern und Kliniken Gerd Maass, Leiter Translational Research Office
 Roche in Deutschland Strategie in der Zusammenarbeit mit Forschern und Kliniken Gerd Maass, Leiter Translational Research Office München, 17. Juni 2013 Roche Ansatz zur Pharma Innovation Diversität in
Roche in Deutschland Strategie in der Zusammenarbeit mit Forschern und Kliniken Gerd Maass, Leiter Translational Research Office München, 17. Juni 2013 Roche Ansatz zur Pharma Innovation Diversität in
Ethik- Grenzen und Möglichkeiten der Autonomie
 Ethik- Grenzen und Möglichkeiten der Autonomie Neonatologische und pädiatrische Intensivpflege Carola Fromm M.A. Angewandte Ethik im Sozial- und Gesundheitswesen Ein Überblick Autonomie in der Pädiatrie
Ethik- Grenzen und Möglichkeiten der Autonomie Neonatologische und pädiatrische Intensivpflege Carola Fromm M.A. Angewandte Ethik im Sozial- und Gesundheitswesen Ein Überblick Autonomie in der Pädiatrie
Service-Angebote des BPI
 Pharmakovigilanz Service-Angebote des BPI BPI-Pharmakovigilanz Knowledge Base Mit dem EU-Pharmapackage und dem Zweiten Gesetz zur Änderung arzneimittelrechtlicher und anderer Vorschriften vom 19. Oktober
Pharmakovigilanz Service-Angebote des BPI BPI-Pharmakovigilanz Knowledge Base Mit dem EU-Pharmapackage und dem Zweiten Gesetz zur Änderung arzneimittelrechtlicher und anderer Vorschriften vom 19. Oktober
Wichtige Änderungen im GKV-WSG für Krebspatienten
 Wichtige Änderungen im GKV-WSG für Krebspatienten Versorgung von Krebspatienten, Qualität quo vadis? Berlin 9./10. März 2007 Dr. Johannes Bruns Kosten Krankheitsklassen in Euro je Einwohner 2002 2004 600
Wichtige Änderungen im GKV-WSG für Krebspatienten Versorgung von Krebspatienten, Qualität quo vadis? Berlin 9./10. März 2007 Dr. Johannes Bruns Kosten Krankheitsklassen in Euro je Einwohner 2002 2004 600
( Arzt/Apotheker-Kooperation )
 ( Arzt/Apotheker-Kooperation ) Vorbemerkung Die Arbeitsgruppe Collaborative Practice der Internationalen Pharmazeutischen Vereinigung (FIP) wurde 2009 vom FIP Board of Pharmaceutical Practice (BPP) zu
( Arzt/Apotheker-Kooperation ) Vorbemerkung Die Arbeitsgruppe Collaborative Practice der Internationalen Pharmazeutischen Vereinigung (FIP) wurde 2009 vom FIP Board of Pharmaceutical Practice (BPP) zu
Ergebnisprotokoll 3. Treffen Swissmedic Arbeitsgruppe Patienten- und Konsumentenorganisationen
 Ergebnisprotokoll 3. Treffen Swissmedic Arbeitsgruppe Patienten- und Konsumentenorganisationen Traktandum Freitag, 21. November 2014, 14.15 bis 17:30 Uhr Swissmedic Hallerstrasse 7, 3000 Bern, Sitzungszimmer
Ergebnisprotokoll 3. Treffen Swissmedic Arbeitsgruppe Patienten- und Konsumentenorganisationen Traktandum Freitag, 21. November 2014, 14.15 bis 17:30 Uhr Swissmedic Hallerstrasse 7, 3000 Bern, Sitzungszimmer
Einstufung von Änderungen
 Einstufung von Änderungen Mag. Caroline Kleber AGES MEA, Wien AGES-Gespräch, 24. Juni 2014 Österreichische Agentur für Gesundheit und Ernährungssicherheit GmbH Aufbau und Zusammenhänge Variation Regulation
Einstufung von Änderungen Mag. Caroline Kleber AGES MEA, Wien AGES-Gespräch, 24. Juni 2014 Österreichische Agentur für Gesundheit und Ernährungssicherheit GmbH Aufbau und Zusammenhänge Variation Regulation
Risk Management Plans & PSURs. Was könnte die Zukunft bringen?
 Risk Management Plans & PSURs Was könnte die Zukunft bringen? 1 Strategy to better protect public health by strengthening and rationalising EU pharmacovigilance There is an established link between pharmacovigilance
Risk Management Plans & PSURs Was könnte die Zukunft bringen? 1 Strategy to better protect public health by strengthening and rationalising EU pharmacovigilance There is an established link between pharmacovigilance
Tragende Gründe. Vom 28. Mai Inhaltsverzeichnis. 1. Rechtsgrundlagen. 2. Eckpunkte der Entscheidung. 3. Beratungsverlauf
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über einen Antrag zur Verordnungsfähigkeit der zulassungsüberschreitenden Anwendung eines Arzneimittels zu Lasten der gesetzlichen Krankenkassen
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über einen Antrag zur Verordnungsfähigkeit der zulassungsüberschreitenden Anwendung eines Arzneimittels zu Lasten der gesetzlichen Krankenkassen
Zulassung von Arzneimitteln in Österreich und EU/EWR
 Zulassung von Arzneimitteln in Österreich und EU/EWR Dr. Gerhard Beck Institute Begutachtung & Analytik AGES Medizinmarkaufsicht UBA 3.12.2015 Österreichische Agentur für Gesundheit und Ernährungssicherheit
Zulassung von Arzneimitteln in Österreich und EU/EWR Dr. Gerhard Beck Institute Begutachtung & Analytik AGES Medizinmarkaufsicht UBA 3.12.2015 Österreichische Agentur für Gesundheit und Ernährungssicherheit
IIT / AWB / NIS. Investigator Initiated Trials. Investigator Initiated Trials (IIT) 11.11.2015. IIT = Investigator Initiated Trials
 IIT / AWB / NIS IIT = Investigator Initiated Trials AWB = Anwendungsbeobachtungen NIS = Nicht-interventionelle Studien Medical-Advisor-IIT-AWB-NIS 11.11.2015 Healthcare Marketing Dr. Umbach & Partner www.umbachpartner.com
IIT / AWB / NIS IIT = Investigator Initiated Trials AWB = Anwendungsbeobachtungen NIS = Nicht-interventionelle Studien Medical-Advisor-IIT-AWB-NIS 11.11.2015 Healthcare Marketing Dr. Umbach & Partner www.umbachpartner.com
Aliskiren-haltige Arzneimittel sind jetzt in Kombination mit ACE-Hemmern oder Angiotensin-Rezeptor-Blockern (ARB) kontraindiziert bei Patienten mit:
 GmbH Novartis Pharma Postfachadresse 90327 Nürnberg Tel 0911/273-0 Fax 0911/273-12653 www.novartis.de 27. Februar 2012 Wichtige Informationen zu neuen Gegenanzeigen und Warnhinweisen bei der Anwendung
GmbH Novartis Pharma Postfachadresse 90327 Nürnberg Tel 0911/273-0 Fax 0911/273-12653 www.novartis.de 27. Februar 2012 Wichtige Informationen zu neuen Gegenanzeigen und Warnhinweisen bei der Anwendung
Die innovative Pharmabranche 2 bekennt sich zur Transparenz bei klinischen Studien, die von ihren Mitgliedsfirmen gesponsert werden.
 Gemeinsame Position zur Offenlegung von Informationen über klinische Studien in Registern und Datenbanken 1 aktualisierte Fassung vom 10. November 2009 Die innovative Pharmabranche 2 bekennt sich zur Transparenz
Gemeinsame Position zur Offenlegung von Informationen über klinische Studien in Registern und Datenbanken 1 aktualisierte Fassung vom 10. November 2009 Die innovative Pharmabranche 2 bekennt sich zur Transparenz
Arzneimittel für seltene Leiden ("Orphan Drugs") im EG- und US-Recht
 Augsburger Schriften zum Arzneimittel- und Medizinprodukterecht herausgegeben von Prof. Dr. iur. Ulrich M. Gassner in Zusammenarbeit mit der Forschungsstelle für Medizinprodukterecht der Universität Augsburg
Augsburger Schriften zum Arzneimittel- und Medizinprodukterecht herausgegeben von Prof. Dr. iur. Ulrich M. Gassner in Zusammenarbeit mit der Forschungsstelle für Medizinprodukterecht der Universität Augsburg
Etablierte therapeutische Präparate
 Etablierte therapeutische Präparate Zusammenfassung der Arbeitsgruppe 3 des DIRECT-Symposiums, Wien, 15.-17. Mai 2008 Prof. A. Biondi, Univ. of Milano-Bicocca, M. Tettamanti Forschungszentrum, Monza, Italien
Etablierte therapeutische Präparate Zusammenfassung der Arbeitsgruppe 3 des DIRECT-Symposiums, Wien, 15.-17. Mai 2008 Prof. A. Biondi, Univ. of Milano-Bicocca, M. Tettamanti Forschungszentrum, Monza, Italien
Unabhängiger Arzneimittelberatungsdienst für Patienten
 Unabhängiger Arzneimittelberatungsdienst für Patienten Uta Heinrich-Gräfe, Apothekerin Projektleitung Arzneimittelberatungsdienst 1. Deutscher Kongress für patientenorientierte Arzneimittelinformation
Unabhängiger Arzneimittelberatungsdienst für Patienten Uta Heinrich-Gräfe, Apothekerin Projektleitung Arzneimittelberatungsdienst 1. Deutscher Kongress für patientenorientierte Arzneimittelinformation
Prof. Dr. Stephan Ludwig. Institut für Molekulare Virologie (IMV)
 Cystus052, ein polyphenolreicher Pflanzenextrakt wirkt gegen Grippeviren durch Blockierung des Viruseintritts in die Wirtszelle Prof. Dr. Stephan Ludwig Institut für Molekulare Virologie (IMV) Die Virusgrippe
Cystus052, ein polyphenolreicher Pflanzenextrakt wirkt gegen Grippeviren durch Blockierung des Viruseintritts in die Wirtszelle Prof. Dr. Stephan Ludwig Institut für Molekulare Virologie (IMV) Die Virusgrippe
AMTS aus der Sicht des Sachverständigenrates zur Begutachtung der Entwicklung im Gesundheitswesen
 SACHVERSTÄNDIGENRAT zur Begutachtung der Entwicklung im Gesundheitswesen AMTS aus der Sicht des Sachverständigenrates zur Begutachtung der Entwicklung im Gesundheitswesen Berlin, 14. Juni 2013 Prof. Dr.
SACHVERSTÄNDIGENRAT zur Begutachtung der Entwicklung im Gesundheitswesen AMTS aus der Sicht des Sachverständigenrates zur Begutachtung der Entwicklung im Gesundheitswesen Berlin, 14. Juni 2013 Prof. Dr.
Braucht jeder Patient eine pharmazeutische Betreuung?
 Braucht jeder Patient eine pharmazeutische Betreuung? Carole Kaufmann, MSc(Pharm) Pharmaceutical Care Research Group & Kantonsspital Baselland, Klinische Pharmazie Das Problem [1] Wiesner C. Dissertation.
Braucht jeder Patient eine pharmazeutische Betreuung? Carole Kaufmann, MSc(Pharm) Pharmaceutical Care Research Group & Kantonsspital Baselland, Klinische Pharmazie Das Problem [1] Wiesner C. Dissertation.
Gesetzliche Betreuungen in Düsseldorf (Stand )
 Gesetzliche Betreuungen in Düsseldorf (Stand 30.06.2013) 6.720; 1,1% Einwohner Betreuungen 592.393; 98,9% 02.12.2013 Amt / 51/6.5 Betreuungsstelle 1 Vorsorgemöglichkeiten zur Wahrung des Selbstbestimmungsrechts
Gesetzliche Betreuungen in Düsseldorf (Stand 30.06.2013) 6.720; 1,1% Einwohner Betreuungen 592.393; 98,9% 02.12.2013 Amt / 51/6.5 Betreuungsstelle 1 Vorsorgemöglichkeiten zur Wahrung des Selbstbestimmungsrechts
Das Zulassungsverfahren für Biozidprodukte. Dr. Jessica Jordan BAuA
 Das Zulassungsverfahren für Biozidprodukte Dr. Jessica Jordan BAuA Biozide - Definition Biozide Biozide Wirkstoffe (WS) Produkte (BP) Definition eines BP Teil 1 dazu bestimmt, Schadorganismen zu bekämpfen
Das Zulassungsverfahren für Biozidprodukte Dr. Jessica Jordan BAuA Biozide - Definition Biozide Biozide Wirkstoffe (WS) Produkte (BP) Definition eines BP Teil 1 dazu bestimmt, Schadorganismen zu bekämpfen
Einwilligungserklärung zur klinischen Prüfung: Teil 2 (vor Studienaufnahme)......
 Einwilligungserklärung zur klinischen Prüfung: Teil 2 (vor Studienaufnahme) Name und Anschrift der Einrichtung, in der die klinische Prüfung durchgeführt wird (Prüfzentrum) Name und Telefon-Nummer des/r
Einwilligungserklärung zur klinischen Prüfung: Teil 2 (vor Studienaufnahme) Name und Anschrift der Einrichtung, in der die klinische Prüfung durchgeführt wird (Prüfzentrum) Name und Telefon-Nummer des/r
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen
 Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Qualitätsmessung: Angemessenheit der Indikationsstellung
 Qualitätsmessung: Angemessenheit der Indikationsstellung 3. Berliner Forum der AWMF Gemeinsam klug entscheiden Initiative der AWMF und ihrer Fachgesellschaften Berlin 15. Oktober 2015 Dr. Regina Klakow-Franck,
Qualitätsmessung: Angemessenheit der Indikationsstellung 3. Berliner Forum der AWMF Gemeinsam klug entscheiden Initiative der AWMF und ihrer Fachgesellschaften Berlin 15. Oktober 2015 Dr. Regina Klakow-Franck,
vfa-positionspapier Orphan Drugs ZUSAMMENFASSUNG
 vfa-positionspapier Orphan Drugs ZUSAMMENFASSUNG Die forschenden Pharma-Unternehmen haben den Patienten und dessen Krankheit in den Mittelpunkt ihrer Aktivitäten gestellt. Das gilt nicht nur für die weit
vfa-positionspapier Orphan Drugs ZUSAMMENFASSUNG Die forschenden Pharma-Unternehmen haben den Patienten und dessen Krankheit in den Mittelpunkt ihrer Aktivitäten gestellt. Das gilt nicht nur für die weit
L o g b u c h. Dokumentation der Weiterbildung gemäß Weiterbildungsordnung (WBO) über die Zusatz-Weiterbildung. Ärztliches Qualitätsmanagement
 L o g b u c h Dokumentation der Weiterbildung gemäß Weiterbildungsordnung (WBO) über die Zusatz-Weiterbildung Ärztliches Qualitätsmanagement Angaben zur Person / Name/Vorname (Rufname bitte unterstreichen)
L o g b u c h Dokumentation der Weiterbildung gemäß Weiterbildungsordnung (WBO) über die Zusatz-Weiterbildung Ärztliches Qualitätsmanagement Angaben zur Person / Name/Vorname (Rufname bitte unterstreichen)
Medizinische Versorgung im Kinder- und Jugendalter: Problematik der Kinderarzneimittel
 Medizinische Versorgung im Kinder- und Jugendalter: Problematik der Kinderarzneimittel Univ. Doz. Dr. Ruth Ladenstein, MBA, cpm Leitung des Koordinierungszentrums für Klinische Studien (S²IRP) St. Anna
Medizinische Versorgung im Kinder- und Jugendalter: Problematik der Kinderarzneimittel Univ. Doz. Dr. Ruth Ladenstein, MBA, cpm Leitung des Koordinierungszentrums für Klinische Studien (S²IRP) St. Anna
Basisstationen und Notwendigkeit epidemiologischer Untersuchungen
 Basisstationen und Notwendigkeit epidemiologischer Untersuchungen Dr. med. Bernhard Aufdereggen, Aertzinnen und Aerzte für Umweltschutz Meine Sicht ist geprägt durch: Meine Erfahrung als Arzt Meine Erfahrung
Basisstationen und Notwendigkeit epidemiologischer Untersuchungen Dr. med. Bernhard Aufdereggen, Aertzinnen und Aerzte für Umweltschutz Meine Sicht ist geprägt durch: Meine Erfahrung als Arzt Meine Erfahrung
Beschluss. I. Die Anlage XII wird in alphabetischer Reihenfolge um den Wirkstoff Vortioxetin wie folgt ergänzt:
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Behandlung der feuchten altersabhängigen Makuladegeneration (feuchte AMD) mit VEGF-Hemmern durch operative Medikamenteneingabe in das Auge
 Augenarztpraxis AltenKirchen Dr. med. Thomas Wehler Facharzt für Augenheilkunde Wilhelmstr. 32 Schlossweg 2 57610 Altenkirchen Tel 02681-1651 Fax 02681-6094 Mail info@ak-augenarzt.de Net www.ak-augenarzt.de
Augenarztpraxis AltenKirchen Dr. med. Thomas Wehler Facharzt für Augenheilkunde Wilhelmstr. 32 Schlossweg 2 57610 Altenkirchen Tel 02681-1651 Fax 02681-6094 Mail info@ak-augenarzt.de Net www.ak-augenarzt.de
Verwendung von Bewertungskriterien in der Evaluationspraxis
 Eidgenössisches Departement des Innern EDI Bundesamt für Gesundheit BAG Direktionsbereich Gesundheitspolitik Verwendung von Bewertungskriterien in der Evaluationspraxis Eine Forschungsstudie anhand von
Eidgenössisches Departement des Innern EDI Bundesamt für Gesundheit BAG Direktionsbereich Gesundheitspolitik Verwendung von Bewertungskriterien in der Evaluationspraxis Eine Forschungsstudie anhand von
Faktenblatt: Traditionelle Chinesische Medizin. (Siehe auch: Mind-Body-Therapien und Medizinische Pilze) Methode/Substanz
 Faktenblatt: Traditionelle Chinesische Medizin Mai 2015 Verantwortlich: PD Dr. J. Hübner, Prof. K. Münstedt, Prof. O. Micke, PD Dr. R. Mücke, Prof. F.J. Prott, Prof. J. Büntzel, Prof. V. Hanf, Dr. C. Stoll
Faktenblatt: Traditionelle Chinesische Medizin Mai 2015 Verantwortlich: PD Dr. J. Hübner, Prof. K. Münstedt, Prof. O. Micke, PD Dr. R. Mücke, Prof. F.J. Prott, Prof. J. Büntzel, Prof. V. Hanf, Dr. C. Stoll
WICHTIG - MITTEILUNG AN DEN KUNDEN FLOWONIX MEDICAL, PROMETRA PROGRAMMIERBARE PUMPE AUFHEBUNG DER CE-KENNZEICHNUNG
 WICHTIG - MITTEILUNG AN DEN KUNDEN FLOWONIX MEDICAL, PROMETRA PROGRAMMIERBARE PUMPE AUFHEBUNG DER CE-KENNZEICHNUNG 558455 Art der Maßnahme: Kundenmitteilung bezüglich der Aufhebung der CE-Kennzeichnung
WICHTIG - MITTEILUNG AN DEN KUNDEN FLOWONIX MEDICAL, PROMETRA PROGRAMMIERBARE PUMPE AUFHEBUNG DER CE-KENNZEICHNUNG 558455 Art der Maßnahme: Kundenmitteilung bezüglich der Aufhebung der CE-Kennzeichnung
Kasper & Kollegen Rechtsanwälte Kassel
 Kasper & Kollegen Rechtsanwälte Kassel Wolfsschlucht 18A 34117 Kassel Telefon: 0561/20865900 Telefax: 0561/20856909 www.rae-med.de und Berufsordnung werden wir Ärzte in die Zange genommen? Kooperation
Kasper & Kollegen Rechtsanwälte Kassel Wolfsschlucht 18A 34117 Kassel Telefon: 0561/20865900 Telefax: 0561/20856909 www.rae-med.de und Berufsordnung werden wir Ärzte in die Zange genommen? Kooperation
Qualitätssicherungsbericht. der IKK classic. für das Behandlungsprogramm. IKK Promed Brustkrebs. in Hamburg
 Qualitätssicherungsbericht der IKK classic für das Behandlungsprogramm IKK Promed Brustkrebs in Hamburg vom 01.01.2013 bis 31.12.2013 Präambel Patienten können in Deutschland auf eine leistungsfähige Medizin
Qualitätssicherungsbericht der IKK classic für das Behandlungsprogramm IKK Promed Brustkrebs in Hamburg vom 01.01.2013 bis 31.12.2013 Präambel Patienten können in Deutschland auf eine leistungsfähige Medizin
Strategien in der Zusammenarbeit. Partnerschaften
 Strategien in der Zusammenarbeit mit Forschern und Kliniken Gerd Maass Leiter Strategische Gerd Maass, Leiter Strategische Partnerschaften Stratifizierende Medizin Welche Verfahren nützen wem und wer soll
Strategien in der Zusammenarbeit mit Forschern und Kliniken Gerd Maass Leiter Strategische Gerd Maass, Leiter Strategische Partnerschaften Stratifizierende Medizin Welche Verfahren nützen wem und wer soll
Wozu ein Gesetz, das Arzneimittel behandelt? Arzneimittelgesetz (AMG)
 Gesetzliche Regelungen für Arzneimittel Wozu ein Gesetz, das Arzneimittel behandelt? Arzneimittelgesetz (AMG) 1 Zweck des Gesetzes Es ist der Zweck dieses Gesetzes, im Interesse einer ordnungsgemäßen Arzneimittelversorgung
Gesetzliche Regelungen für Arzneimittel Wozu ein Gesetz, das Arzneimittel behandelt? Arzneimittelgesetz (AMG) 1 Zweck des Gesetzes Es ist der Zweck dieses Gesetzes, im Interesse einer ordnungsgemäßen Arzneimittelversorgung
RMK - Rehabilitanden Management Kategorien
 RMK - Rehabilitanden Management Kategorien Assessment und Software für die Eingangsdiagnostik 12.03.2014 buss 100. wissenschaftliche Jahrestagung 1 Inhalte RMK Zielsetzung Entwicklung des RMK Assessments
RMK - Rehabilitanden Management Kategorien Assessment und Software für die Eingangsdiagnostik 12.03.2014 buss 100. wissenschaftliche Jahrestagung 1 Inhalte RMK Zielsetzung Entwicklung des RMK Assessments
Politische Balance zwischen Innovationsförderung und Kostenkontrolle 10 Thesen
 Innovationen in in der der Onkologie: Was Was ist ist der der Nutzen wert? wert? BDI BDI initiativ-symposium, Berlin, 07.09.2011 Politische Balance zwischen Innovationsförderung und Kostenkontrolle 10
Innovationen in in der der Onkologie: Was Was ist ist der der Nutzen wert? wert? BDI BDI initiativ-symposium, Berlin, 07.09.2011 Politische Balance zwischen Innovationsförderung und Kostenkontrolle 10
Apotheker als Partner in der Arzneimittelsicherheit Christian Hoffmann Apothekerkammer Hamburg
 Apotheker als Partner in der Arzneimittelsicherheit Christian Hoffmann Apothekerkammer Hamburg Fachtagung Medikamentenabhängigkeit im Alter 21. August 2013 Ein paar Zahlen Patienten über 65 Jahre 48% >
Apotheker als Partner in der Arzneimittelsicherheit Christian Hoffmann Apothekerkammer Hamburg Fachtagung Medikamentenabhängigkeit im Alter 21. August 2013 Ein paar Zahlen Patienten über 65 Jahre 48% >
Erstellung einer Anleitung zur Anwendung von Arzneimitteln im Off-label Use für die ICH
 Erstellung einer Anleitung zur Anwendung von Arzneimitteln im Off-label Use für die ICH Exposé zur Erstellung einer Dissertation am Lehrstuhl für Drug Regulatory Affairs der Rheinischen Friedrich-Wilhelms-Universität
Erstellung einer Anleitung zur Anwendung von Arzneimitteln im Off-label Use für die ICH Exposé zur Erstellung einer Dissertation am Lehrstuhl für Drug Regulatory Affairs der Rheinischen Friedrich-Wilhelms-Universität
QualityRiskManagement
 QualityRiskManagement Workshop Bernd Bödecker GAA Hannover GMP-Gesprächskreis Niedersachsen Abbott Products GmbH, 8. November 2011 Ziele des Workshops (Vorschlag) o Gelegenheit zur allgemeinen Information
QualityRiskManagement Workshop Bernd Bödecker GAA Hannover GMP-Gesprächskreis Niedersachsen Abbott Products GmbH, 8. November 2011 Ziele des Workshops (Vorschlag) o Gelegenheit zur allgemeinen Information
Stellungnahme der Bundesärztekammer
 Stellungnahme der Bundesärztekammer gemäß 91 Abs. 5 SGB V zur Änderung von Anlage I der Richtlinie Methoden vertragsärztliche Versorgung (MVV-RL): Berlin, 27.07.2011 Bundesärztekammer Herbert-Lewin-Platz
Stellungnahme der Bundesärztekammer gemäß 91 Abs. 5 SGB V zur Änderung von Anlage I der Richtlinie Methoden vertragsärztliche Versorgung (MVV-RL): Berlin, 27.07.2011 Bundesärztekammer Herbert-Lewin-Platz
Ausbildung von PJ-Studenten an der DRK-Kinderklinik Siegen ggmbh. Die Lebensqualität für Kinder verbessern. Das ist unser Auftrag.
 Ausbildung von PJ-Studenten an der DRK-Kinderklinik Siegen ggmbh Die Lebensqualität für Kinder verbessern. Das ist unser Auftrag. DRK-Kinderklinik Siegen Das Kind als Patient DRK-Kinderklinik Siegen im
Ausbildung von PJ-Studenten an der DRK-Kinderklinik Siegen ggmbh Die Lebensqualität für Kinder verbessern. Das ist unser Auftrag. DRK-Kinderklinik Siegen Das Kind als Patient DRK-Kinderklinik Siegen im
Risikomanagement bei neuartigen Arzneimitteln
 Risikomanagement bei neuartigen Arzneimitteln IQWiG Herbst - Symposion Köln, 28. November Ulrich Hagemann Abteilung Pharmakovigilanz im BfArM, Bonn Besuchen Sie unsere Webseite: www.bfarm.de/pharmakovigilanz
Risikomanagement bei neuartigen Arzneimitteln IQWiG Herbst - Symposion Köln, 28. November Ulrich Hagemann Abteilung Pharmakovigilanz im BfArM, Bonn Besuchen Sie unsere Webseite: www.bfarm.de/pharmakovigilanz
Fragebogen Weisse Liste-Ärzte
 www.weisse-liste.de Fragebogen Weisse Liste-Ärzte Der Fragebogen ist Teil des Projekts Weisse Liste-Ärzte. DIMENSION: Praxis & Personal voll eher zu eher 1. Das Praxispersonal vermittelt mir das Gefühl,
www.weisse-liste.de Fragebogen Weisse Liste-Ärzte Der Fragebogen ist Teil des Projekts Weisse Liste-Ärzte. DIMENSION: Praxis & Personal voll eher zu eher 1. Das Praxispersonal vermittelt mir das Gefühl,
Klinische Forschung. Klinische Forschung. Effectiveness Gap. Versorgungsforschung und evidenzbasierte Medizin. Conclusion
 Versorgungsforschung und evidenzbasierte Medizin Klinische Forschung 00qm\univkli\klifo2a.cdr DFG Denkschrift 1999 Aktuelles Konzept 2006 Workshop der PaulMartiniStiftung Methoden der Versorgungsforschung
Versorgungsforschung und evidenzbasierte Medizin Klinische Forschung 00qm\univkli\klifo2a.cdr DFG Denkschrift 1999 Aktuelles Konzept 2006 Workshop der PaulMartiniStiftung Methoden der Versorgungsforschung
Tolperison, Nichtigkeitsklage vor dem Gericht der EU gegen den Durchführungsbeschluss der Kommission aus dem Art. 31-Verfahren nach RL 2001/83/EG
 Tolperison, Nichtigkeitsklage vor dem Gericht der EU gegen den Durchführungsbeschluss der Kommission aus dem Art. 31-Verfahren nach RL 2001/83/EG 72. Routinesitzung 29. Mai 2012 Tolperison, Verfahren nach
Tolperison, Nichtigkeitsklage vor dem Gericht der EU gegen den Durchführungsbeschluss der Kommission aus dem Art. 31-Verfahren nach RL 2001/83/EG 72. Routinesitzung 29. Mai 2012 Tolperison, Verfahren nach
The Cochrane Library
 The Cochrane Library Was ist die Cochrane Library? Die Cochrane Library bietet hochwertige, evidenzbasierte medizinische Fachinformation zur fundierten Unterstützung bei Diagnose und Behandlung. http://www.cochranelibrary.com/
The Cochrane Library Was ist die Cochrane Library? Die Cochrane Library bietet hochwertige, evidenzbasierte medizinische Fachinformation zur fundierten Unterstützung bei Diagnose und Behandlung. http://www.cochranelibrary.com/
Tragende Gründe. Therapiehinweis zu Sitagliptin. vom 18. Oktober 2007. Inhaltsverzeichnis. 1. Rechtsgrundlagen 2. 2. Eckpunkte der Entscheidung 2
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses zur Einleitung eines Stellungnahmeverfahrens zur Änderung der Arzneimittel-Richtlinie in Anlage 4: Therapiehinweis zu Sitagliptin vom 18.
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses zur Einleitung eines Stellungnahmeverfahrens zur Änderung der Arzneimittel-Richtlinie in Anlage 4: Therapiehinweis zu Sitagliptin vom 18.
Pharmakotherapie in der Hausarztpraxis
 Pharmakotherapie in der Hausarztpraxis Dr. Andreas Graf Luckner Tengen Lehrbereich Allgemeinmedizin-Universität Freiburg/09-05 1 Lernziele Rahmenbedingungen betr. hausärztlicher Pharmakotherapie kennen
Pharmakotherapie in der Hausarztpraxis Dr. Andreas Graf Luckner Tengen Lehrbereich Allgemeinmedizin-Universität Freiburg/09-05 1 Lernziele Rahmenbedingungen betr. hausärztlicher Pharmakotherapie kennen
Optimierung der Antragstellung Ausgewählte Aspekte aus dem Prüfbereich Wirksamkeit
 Optimierung der Antragstellung Ausgewählte Aspekte aus dem Prüfbereich Wirksamkeit Dr. Thomas Engelke & Karl-Heinz Berendes Julius Kühn-Institut (JKI) Koordinierungsstelle (Schriftgröße mindestens 16,
Optimierung der Antragstellung Ausgewählte Aspekte aus dem Prüfbereich Wirksamkeit Dr. Thomas Engelke & Karl-Heinz Berendes Julius Kühn-Institut (JKI) Koordinierungsstelle (Schriftgröße mindestens 16,
Fachgruppensitzung 21. Jänner Fachgruppensitzung. P. Voitl.
 Fachgruppensitzung P. Voitl Programm Peter Voitl Aktuelles aus der Standespolitik Neue Tarifpositionen für die GKK-Verhandlungen Prim. Univ.-Prof. Dr. Beatrix Volc-Platzer Update AKNE FSME - Preise Honorarverhandlungen
Fachgruppensitzung P. Voitl Programm Peter Voitl Aktuelles aus der Standespolitik Neue Tarifpositionen für die GKK-Verhandlungen Prim. Univ.-Prof. Dr. Beatrix Volc-Platzer Update AKNE FSME - Preise Honorarverhandlungen
Bewertung des neuen Systems aus Sicht der Verbände vfa, BAH und BPI für PEI-Produkte
 Bewertung des neuen Systems aus Sicht der Verbände vfa, BAH und BPI für PEI-Produkte PEI im Dialog Erfahrungen mit der Variation Regulation (EG) Nr. 1234/2008 Allgemeine Erfahrungen der Mitgliedsunternehmen
Bewertung des neuen Systems aus Sicht der Verbände vfa, BAH und BPI für PEI-Produkte PEI im Dialog Erfahrungen mit der Variation Regulation (EG) Nr. 1234/2008 Allgemeine Erfahrungen der Mitgliedsunternehmen
Integrative Kinder- und Jugendmedizin Modeerscheinung oder Notwendigkeit?
 Integrative Kinder- und Jugendmedizin Modeerscheinung oder Notwendigkeit? Alfred Längler Gemeinschaftskrankenhaus, Abteilung für integrative Kinder- und Jugendmedizin, Herdecke Fakultät für Gesundheit,
Integrative Kinder- und Jugendmedizin Modeerscheinung oder Notwendigkeit? Alfred Längler Gemeinschaftskrankenhaus, Abteilung für integrative Kinder- und Jugendmedizin, Herdecke Fakultät für Gesundheit,
Gliederung Vortrag Patientenrechte: 1. Recht auf Aufklärung
 Gliederung Vortrag Patientenrechte: 1. Recht auf Aufklärung 2. Freie Arztwahl 3. Freie Krankenhauswahl 4. Recht auf Zweitmeinung und Arztwechsel 5. Recht auf Behandlungsdokumentation 1 6. Recht auf Einsicht
Gliederung Vortrag Patientenrechte: 1. Recht auf Aufklärung 2. Freie Arztwahl 3. Freie Krankenhauswahl 4. Recht auf Zweitmeinung und Arztwechsel 5. Recht auf Behandlungsdokumentation 1 6. Recht auf Einsicht
Hinweise zum klinischen Nutzen von Xarelto bei Patienten mit Vorhofflimmern und Kardioversion in europäische Produktinformation aufgenommen
 Presse-Information Bayer Pharma AG 13342 Berlin Deutschland Tel. +49 30 468-1111 www.bayerpharma.de Hinweise zum klinischen Nutzen von Xarelto bei Patienten mit Vorhofflimmern und Kardioversion in europäische
Presse-Information Bayer Pharma AG 13342 Berlin Deutschland Tel. +49 30 468-1111 www.bayerpharma.de Hinweise zum klinischen Nutzen von Xarelto bei Patienten mit Vorhofflimmern und Kardioversion in europäische
Der Apothekerberuf Ausbildung und Tätigkeitsfelder
 Der Apothekerberuf Ausbildung und Tätigkeitsfelder 1 Entwicklung der Pharmazie Ausbildung des Apothekers Bundesweit durch Bundes- Apothekerordnung und die Approbationsordnung für Apotheker einheitlich
Der Apothekerberuf Ausbildung und Tätigkeitsfelder 1 Entwicklung der Pharmazie Ausbildung des Apothekers Bundesweit durch Bundes- Apothekerordnung und die Approbationsordnung für Apotheker einheitlich
Forschung transparent, vertrauenswürdig und nachvollziehbar Modell Ethikkommission im nicht-ärztlichen Bereich RCSEQ UMIT und fhg
 Forschung transparent, vertrauenswürdig und nachvollziehbar Modell Ethikkommission im nicht-ärztlichen Bereich RCSEQ UMIT und fhg Forschung soll die Gesundheit der Menschen fördern und erhalten, sowie
Forschung transparent, vertrauenswürdig und nachvollziehbar Modell Ethikkommission im nicht-ärztlichen Bereich RCSEQ UMIT und fhg Forschung soll die Gesundheit der Menschen fördern und erhalten, sowie
Abgrenzung klinischer Prüfungen Phase III und IV gegenüber nichtinterventionellen
 Abgrenzung klinischer Prüfungen Phase III und IV gegenüber nichtinterventionellen Studien Studien PHIII und IV versus Nichtinterventionelle Studien 1 Welche Aussagen sind richtig?? -1- Klinische Studien
Abgrenzung klinischer Prüfungen Phase III und IV gegenüber nichtinterventionellen Studien Studien PHIII und IV versus Nichtinterventionelle Studien 1 Welche Aussagen sind richtig?? -1- Klinische Studien
Das PhD-Studium ein Start ins ForscherInnenleben lb?
 Das PhD-Studium ein Start ins ForscherInnenleben lb? Ao. Univ.-Prof. Dr.med.univ. Wolfgang PRODINGER Sektion Hygiene und Medizinische Mikrobiologie Neues Doktoratsstudium für Medizin wieso denn? Ausgangspunkt:
Das PhD-Studium ein Start ins ForscherInnenleben lb? Ao. Univ.-Prof. Dr.med.univ. Wolfgang PRODINGER Sektion Hygiene und Medizinische Mikrobiologie Neues Doktoratsstudium für Medizin wieso denn? Ausgangspunkt:
Madagaskar die rote Insel im indischen Ozean
 Madagaskar die rote Insel im indischen Ozean Der Reichtum des Landes liegt in seiner einzigartigen Natur und seiner Artenvielfalt. Ein Ferienland für uns doch für die Menschen dort ist das Leben oft nicht
Madagaskar die rote Insel im indischen Ozean Der Reichtum des Landes liegt in seiner einzigartigen Natur und seiner Artenvielfalt. Ein Ferienland für uns doch für die Menschen dort ist das Leben oft nicht
HealtH ClaIms Gesundheitsbezogene Aussagen für Lebensmittel
 HealtH ClaIms Gesundheitsbezogene Aussagen für Lebensmittel Warum gibt es die Health-Claims-Verordnung? Jeder Mensch verzehrt täglich Lebensmittel. Diese müssen grundsätzlich sicher sein, d. h. sie dürfen
HealtH ClaIms Gesundheitsbezogene Aussagen für Lebensmittel Warum gibt es die Health-Claims-Verordnung? Jeder Mensch verzehrt täglich Lebensmittel. Diese müssen grundsätzlich sicher sein, d. h. sie dürfen
Patente und Unterlagenschutz
 Patente und Unterlagenschutz ANWALTSKANZLEI STRÄTER Burkhard Sträter Kronprinzenstraße 20 53173 Bonn Tel.:++49-228-93454-0 Fax.:++49-228-93454-54 Mail@kanzleistraeter.de www.kanzleistraeter.de Protection
Patente und Unterlagenschutz ANWALTSKANZLEI STRÄTER Burkhard Sträter Kronprinzenstraße 20 53173 Bonn Tel.:++49-228-93454-0 Fax.:++49-228-93454-54 Mail@kanzleistraeter.de www.kanzleistraeter.de Protection
POSITIONSPAPIER. Verbesserung der medizinischen Versorgung für Kinder und Jugendliche Problem: Sicherheit der Arzneimitteltherapien
 Verbesserung der medizinischen Versorgung für Kinder und Jugendliche Verbesserung der medizinischen Versorgung für Kinder und Jugendliche POSITIONSPAPIER Verbesserung der medizinischen Versorgung für Kinder
Verbesserung der medizinischen Versorgung für Kinder und Jugendliche Verbesserung der medizinischen Versorgung für Kinder und Jugendliche POSITIONSPAPIER Verbesserung der medizinischen Versorgung für Kinder
Wie wird man PsychotherapeutIn? Gesetzliche Grundlagen. Dipl.-Psych. vor dem PsychThG
 Wie wird man PsychotherapeutIn? Gesetzliche Grundlagen Psychotherapeutengesetz (PTG) vom 16.06.1998 zum Änderung des SGBV Ausbildungs- und Prüfungsverordnung (PsychTh-AprV) vom 18.12.1998 Ausbildungs-
Wie wird man PsychotherapeutIn? Gesetzliche Grundlagen Psychotherapeutengesetz (PTG) vom 16.06.1998 zum Änderung des SGBV Ausbildungs- und Prüfungsverordnung (PsychTh-AprV) vom 18.12.1998 Ausbildungs-
Pharmakovigilanz Basics und Beispiele Gemeinsame Fortbildungs- und Informationsveranstaltung von AkdÄ und AMK am 11.07.
 Pharmakovigilanz Basics und Beispiele Gemeinsame Fortbildungs- und Informationsveranstaltung von AkdÄ und AMK am 11.07.2015 in Berlin Dr. med. Thomas Stammschulte 13. Juli 2015 Interessenkonflikte Referent
Pharmakovigilanz Basics und Beispiele Gemeinsame Fortbildungs- und Informationsveranstaltung von AkdÄ und AMK am 11.07.2015 in Berlin Dr. med. Thomas Stammschulte 13. Juli 2015 Interessenkonflikte Referent
Klinische Studien in Deutschland: Müssen wir mehr tun?
 Klinische Studien in Deutschland: Müssen wir mehr tun? IQWiG-Herbst-Symposium 26.11.2016 Dr. J. Grebe Koordinierungszentrum für Klinische Studien Müssen wir mehr tun? Interessenkonflikt: Nichts zu offenbaren!
Klinische Studien in Deutschland: Müssen wir mehr tun? IQWiG-Herbst-Symposium 26.11.2016 Dr. J. Grebe Koordinierungszentrum für Klinische Studien Müssen wir mehr tun? Interessenkonflikt: Nichts zu offenbaren!
Biosimilars - Die Sicht der Patienten Ulla Ohlms, Vorsitzende der Stiftung PATH Patients Tumorbank of Hope
 Biosimilars - Die Sicht der Patienten Ulla Ohlms, Vorsitzende der Stiftung PATH Patients Tumorbank of Hope Vfa-Tagung Ähnlich, aber eben doch nicht gleich Penzberg, 6. November 2013 März 2000, damals,
Biosimilars - Die Sicht der Patienten Ulla Ohlms, Vorsitzende der Stiftung PATH Patients Tumorbank of Hope Vfa-Tagung Ähnlich, aber eben doch nicht gleich Penzberg, 6. November 2013 März 2000, damals,
Erfahrungen der. DQS GmbH. bei der Zertifizierung von Medizinprodukteherstellern
 Erfahrungen der DQS GmbH bei der Zertifizierung von Medizinprodukteherstellern 2004-11-24, Seite 1 Normensituation Medizinprodukte DIN EN ISO 9001:94 DIN EN ISO 9001:2000 DIN EN 46001/2:1996 DIN EN ISO
Erfahrungen der DQS GmbH bei der Zertifizierung von Medizinprodukteherstellern 2004-11-24, Seite 1 Normensituation Medizinprodukte DIN EN ISO 9001:94 DIN EN ISO 9001:2000 DIN EN 46001/2:1996 DIN EN ISO
WS 2009/2010 Vorlesung - Spezielles Arzneimittelrecht. Mittwoch, 13. Januar 2010. Pandemie - Teil X
 Ministerium für,,, und WS 2009/2010 Vorlesung - Spezielles Arzneimittelrecht Mittwoch, 13. Januar 2010 Pandemie - Teil X -Dr. Michael Cramer-2010-01-13 Folie 1 Ministerium für,,, und Klinische Prüfungen
Ministerium für,,, und WS 2009/2010 Vorlesung - Spezielles Arzneimittelrecht Mittwoch, 13. Januar 2010 Pandemie - Teil X -Dr. Michael Cramer-2010-01-13 Folie 1 Ministerium für,,, und Klinische Prüfungen
Die Laborreform 2014 gefährdet die endokrinologische Patientenversorgung in Deutschland
 Positionspapier Die Laborreform 2014 gefährdet die endokrinologische Patientenversorgung in Deutschland Durch die aktuellen Laborreformen werden endokrinologische Laborleistungen, sofern sie überhaupt
Positionspapier Die Laborreform 2014 gefährdet die endokrinologische Patientenversorgung in Deutschland Durch die aktuellen Laborreformen werden endokrinologische Laborleistungen, sofern sie überhaupt
Heil und Hilfsmittelversorgung
 Heil und Hilfsmittelversorgung Christina Reiß, Sozialberatung, Neuromuskuläres Zentrum der Universitätsmedizin Mannheim, Theodor-Kutzer-Ufer 1-3, 68167 Mannheim, Tel. 0621 / 383-2918, christina.reiss@dgm.org,
Heil und Hilfsmittelversorgung Christina Reiß, Sozialberatung, Neuromuskuläres Zentrum der Universitätsmedizin Mannheim, Theodor-Kutzer-Ufer 1-3, 68167 Mannheim, Tel. 0621 / 383-2918, christina.reiss@dgm.org,
Erfahrungen im Handlungsfeld Gerontopsychiatrie
 Direktion Pflege, Therapien und Soziale Arbeit Klinik für Alterspsychiatrie Erfahrungen im Handlungsfeld Gerontopsychiatrie Workshop ANP Kongress Linz Freyer, Sonja M.Sc. APN Gliederung Vorstellung Begriffsdefinitionen
Direktion Pflege, Therapien und Soziale Arbeit Klinik für Alterspsychiatrie Erfahrungen im Handlungsfeld Gerontopsychiatrie Workshop ANP Kongress Linz Freyer, Sonja M.Sc. APN Gliederung Vorstellung Begriffsdefinitionen
KURZVORSTELLUNG. Ergosign Medical & Pharma Design
 KURZVORSTELLUNG Ergosign Medical & Pharma Design UNSER UNTERNEHMEN Mission & Facts Spezialisierter Anbieter von User Interface Design Services Fokus: B2B Anwendungen, Productivity, Anwendungen für Professionals,
KURZVORSTELLUNG Ergosign Medical & Pharma Design UNSER UNTERNEHMEN Mission & Facts Spezialisierter Anbieter von User Interface Design Services Fokus: B2B Anwendungen, Productivity, Anwendungen für Professionals,
