1 Ionisationsgleichgewicht
|
|
|
- Heike Kruse
- vor 7 Jahren
- Abrufe
Transkript
1 1 Ionisationsgleichgewicht Ein Plasma ist ein Gas aus geladenen Teilchen, in der Regel positiv geladenen Ionen und negativ geladenen Elektronen. Der Plasmazustand entsteht aus einem neutralen Gas, wenn die Energie der Gasteilchen die zur Ionisation notwendige Energie überschreitet. Im thermischen Gleichgewicht stellt sich ein bestimmter Ionisationsgrad ein. Hier soll der Ionisationsgrad eines Plasmas als Funktion von Temperatur und Volumen bzw. Temperatur und Druck bestimmt werden. 1.1 Ionisationsgrad Ein Gas bestehe aus N Atomen einer Sorte A mit der Kernladungszahl Z. Die unterschiedlichen Ladungszustände werden mit A i bezeichnet, wobei der Index i die Werte 0, 1, 2,, Z annimmt. Dabei steht A 0 für das neutrale und A Z für das vollständig ionisierte Atom. Die Zahl der Teilchen im Ladungszustand A i sei N i = α i N, die Zahl der Elektronen, N e = α e N. Aufgrund der Erhaltung der Teilchenzahl und der Ladung gilt Z Z N = N i, N e = in i (1) oder, nach Division durch N, i=0 i=0 Z i=0 α i = 1, Z i=0 iα i = α e. (2) Man bezeichnet α e als den Ionisationsgrad. Der Ionisationsgrad ist ein Mittelwert der Ionisationsstufen i mit den Gewichten α i. Er variiert zwischen 0 und Z. 1.2 Ionisationsgleichgewicht Das Plasma sei im thermischen Gleichgewicht bei der Temperatur T im Volumen V. Die Teilchenzahlen N µ der verschiedenen Teilchensorten µ = i, e stellen sich dann so ein, daß die freie Energie F = F (T, V, N µ ) ein Minimum besitzt, δf = µ F N µ δn µ = 0. (3) Für die Ionisation des Zustandes A i bzw. die Rekombination des Zustandes A i+1 gilt die Reaktionsgleichung A i A i+1 + e. (4) Mit jeder Reaktion ist eine Änderung der Teilchenzahlen δn i = δn e, δn i+1 = +δn e (5) 1
2 verbunden. Das Minimum der freien Energie genügt daher den Z Bedingungen F N i = F + F, i = 0, 1,, Z 1. (6) N i+1 N e Zusammen mit den beiden Nebenbedingungen (1) bestimmen Sie die Teilchenzahlen N i und N e. 1.3 Freie Energie Das Plasma wird nun als ein klassisches ideales Gas aus unterschiedlichen Teilchensorten µ behandelt. Die Energie eines Teilchens der Sorte µ besitzt die allgemeine Form E µ,k (p) = p2 2m µ + ɛ µ,k. (7) wobei ɛ µ,k die innere Energie des Teilchens im Quantenzustand k bezeichnet. Für Elektronen gilt ɛ e,k = 0, da diese keine Änderungen der inneren Energie erfahren. Ebenso gilt für vollständig ionisierte Atome ɛ Z,k =0. Für ein i-fach ionisiertes Atom mit i < Z bezeichnen die Energien ɛ i,k die Energieniveaus des Ions mit Z i Elektronen. Zur Erhöhung der Ionisationsstufe von i 1 nach i im Grundzustand (k = 0) benötigt man die Energie I i = ɛ i,0 ɛ i 1,0. (8) Sie wird als das i-te Ionisationspotential bezeichnet. Die freie Energie kann mit den Methoden der statistischen Physik aus der Zustandssumme des Systems berechnet werden. Die Zustandssumme eines Teilchens ist S µ = V d 3 p e E µ,k(p)/t h 3 k = V h 3 (2πm µt ) 3/2 k e ɛ µ,k/t = V u λ 3 µ exp( ɛ µ,0 µ T ) (9) mit λ µ = h 2 2πm µ T, u µ = k exp( ɛ µ,k ɛ µ,0 ) T Die Zustandssumme für N µ Teilchen ergibt sich daraus zu S µ (N µ, T, V ) = SNµ µ N µ! ( ) Nµ Sµ e (10) N µ 2
3 wobei e = 2, 718 die Eulersche Zahl bezeichnet und im letzten Schritt die Stirlingsche Formel N µ! ( ) Nµ Nµ angewandt wurde. Die freie Energie wird definiert durch e F = µ F µ, (11) mit F µ = T ln S µ (N µ, T, V ) = T N µ [ln(s µ ) + 1 ln(n µ )]. Die Ableitung von F nach der Teilchenzahl N µ bei festem V und T ergibt 1.4 Saha-Gleichung F N µ = T [ln(s µ ) + 1 ln(n µ )] + T = T ln Mit (12) folgt aus der Gleichgewichtsbedingung (6) Unter Verwendung der Zustandssumme (9) erhält man ( Sµ N µ ). (12) ln S i N i = ln S i+1 N i+1 + ln S e N e (13) N i N i+1 N e = = λ3 e V S i S i+1 S e u i exp( I i+1 ). (14) u e u i+1 T Für die Zustandssumme u e der Elektronen gilt u e = 2, da die beiden Spinrichtungen entartet sind. Die Zustandssummen u i werden für i < Z meist durch den Entartungsgrad des Grundzustandes angenähert, u i = g i. Bei vollständiger Ionisation liegt kein elektronischer Zustand vor, so daß u Z = 1 zu setzen ist. Definiert man die Dichte n = N/V so folgt, α i = nk n (i+1) (T ), K n (i+1) (T ) = g i λ 3 e exp( I i+1 ). (15) α i+1 α e 2g i+1 T Diese Gleichung bestimmt den Ionisationsgrad als Funktion von T und n. Ist neben der Temperatur der Druck p vorgegeben, so erhält man aus der Zustandsgleichung für ideale Gase pv = N µ T = (1 + α e )NT (16) µ die zugehörige Gleichgewichtsdichte, n = p (1 + α e )T. (17) 3
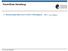
4 Damit folgt : α i (1 + α e ) α i+1 α e = pk (i+1) p (T ), K (i+1) p (T ) = g i 2g i+1 λ 3 e T exp(i i+1 T ). (18) Gleichung (15) oder (18) wird als Saha-Gleichung (M. Saha, 1921) bezeichnet. Sie stellt das Massenwirkungsgesetz für Ionisationsreaktionen dar. Die Massenwirkungskonstanten nk n (i+1) (T ) und pk p (i+1) (T ) sind jeweils proportional zur Zahl der Teilchen im de Broglie-Volumen nλ 3 e. Da diese Zahl für klassische Systeme sehr klein ist, setzt die Ionisation schon bei Temperaturen unterhalb der Ionisationsenergie ein. 1.5 Ionisationsgrad bei einfacher Ionisation Da die höheren Ionisationspotentiale meist sehr viel größer sind als das erste gibt es einen Temperaturbereich, in dem vorwiegend nur neutrale und einfach geladene Ionen vorliegen. Setzt man α i = 0 für i 2, so erhält man aus den Nebenbedingungen (2) Damit lautet die Saha-Gleichung (15) für i = 0, α 0 = 1 α e, α 1 = α e. (19) 1 α e α 2 e = nk (1) n (T ) Die Auflösung nach α e ergibt den Ionisationsgrad bei vorgegebener Dichte ( ) 1 α e = 1 + 4nK 2nK n (1) n (1) (T ) 1. (20) (T ) Entsprechend erhält man aus (18) 1 α 2 e α 2 e = pk (1) p (T ) und damit den Ionisationsgrad bei vorgegebenem Druck 1 α e =. (21) 1+pK p (1) (T ) 2 Übung 1. Bestimmen Sie den Ionisationsgrad von Wasserstoff bei einem Druck von 1 bar als Funktion der Temperatur. Zeichnen Sie einen Graphen α e (T ) wobei die Temperatur in ev angegeben wird. 4
5 2. Z 1-fach ionisierte Ionen werden als wasserstoffähnlich bezeichnet. Sie bestehen aus einem Atomkern mit der Kernladungszahl Z und einem Elektron. Ihre Ionisationsenergie ist I Z = Z 2 I H, wobei I H die Ionisationsenergie von Wasserstoff bezeichnet. Durch einen intensiven Laserpuls werde ein wasserstoffähnliches Plasma bei einem Druck von 1 Mbar erzeugt. Geben Sie als Funktion der Temperatur diejenige Ordnungszahl Z an, bei der der Ionisationsgrad etwa 90% beträgt. Zeichnen Sie einen Graphen Z = Z(T ). 2.1 Hinweise zur Programmierung Konstanten: m e = kg h = Js 1eV = J 1bar = 10 5 N/m 2 I H = eV Drücken Sie die Massenwirkungskonstante in der folgenden Form aus und bestimmen Sie den numerischen Faktor c Saha pk (1) p (T ) = c Saha g 0 g 1 p[bar] (T [ev]) 5/2 exp(i H/T ) Schreiben eine Funktion, die den Ionisationsgrad für einfach ionisierte Atome nach der Saha-Gleichung berechnet: double saha1(double pbar, double tev, double iev, double g0,double g1) \{... \ double pbar: Druck in bar double tev: Temperatur in ev double iev: Erstes Ionisationspotential in ev double g0: Statistisches Gewicht des Grundzustandes des Atoms double g1: Statistisches Gewicht des Grundzustandes des Ions Geben Sie die Temperatur (tev) und den Ionisationsgrad (alpha) zweispaltig in eine Datei aus: FILE *fp; fp=fopen( out.dat, w );... Ausgabe in Datei fprintf(fp,"%15.4e\t%15.4e\n",tev,alpha);... fclose(fp); Dateizeiger Datei {\"offnen Datei schlie{\ssen 5
6 2.2 Header-Datei für alle Aufgaben #ifndef CS_H #define CS_H Numerical constants const double com_pi_c = ; Pi const double com_me_c = 9.109e-28; Electron mass [g] const double com_hp_c = 6.626e-27; Planck constant [gcm^2/s] const double com_c_c = e10; Speed of light [cm/s] const double com_kb_c = e-16; Boltzmann constant [erg/k] const double com_ev_c = 1.602e-12; 1eV [gcm^2/s^2] const double com_bar_c = 1.0e+6; 1bar [g/cm/s] const double com_ionh_c= ; Ionization energy of H [ev] const double com_ionhe_c= 24.59; Ionization energy of He [ev] Function declarations extern double sahac(); extern double saha1(double pbar,double tev,double iev,double g0,double g1,double sahac); extern void drk4(double y[], double dydx[], int n, double x, double h, double yout[], void (*derivs)(double, double [], double [])); #endif CS_H 2.3 Beispielprogramm Aufgabe 1 #include <stdio.h> #include <math.h> #include "cs.h" double sahac() Numerical constant in the Saha equation { double c; c=0.5*pow(com_hp_c/sqrt(2.0*com_pi_c*com_me_c),3.0); c*=(com_bar_c/pow(com_ev_c,2.5)); return c; double saha1 Ionisation degree for single ionization (Saha equation) ( double pbar, pressure [bar] double tev, temperature [ev] double iev, ionization potential [ev] double g0, statistical weight for atom double g1, statistical weight for ion double sahac ){ double pk; constant calculated by sahac.c pk=sahac*g0/g1*pbar/pow(tev,2.5)*exp(iev/tev); return 1.0/sqrt(1.0+pk); Ionisation degree main() { FILE *out; 6
7 double tev,pbar,iev,g0,g1,alpha,c; printf("start\n"); Initialize out=fopen("out1.dat","w"); pbar=1.0; iev=com_ionh_c; g0=2.0; g1=1.0; c=sahac(); Ionization degree for(tev=0.01*iev;tev<=iev;tev+=0.1){ alpha=saha1(pbar,tev,iev,g0,g1,c); fprintf(out,"%15.4e\t%15.4e\n",tev,alpha); fclose(out); printf("end\n"); 2.4 Beispielprogramm Aufgabe 2 #include <stdio.h> #include "cs.h" main() { FILE *out; double tev,dtev,pbar,iev,g0,g1,alpha,c,z; printf("start\n"); Initialize out=fopen("out2.dat","w"); pbar=1.0e6; g0=2.0; g1=1.0; c=sahac(); Ionization degree for(z=1;z<=40;z+=1){ iev=z*z*com_ionh_c; dtev=0.001*iev; for(tev=0.1,alpha=0.0;alpha<=0.9 && tev<iev;tev+=dtev){ alpha=saha1(pbar,tev,iev,g0,g1,c); fprintf(out,"%15.4e\t%15.4e\t%15.4e\n",tev,z,alpha); fclose(out); printf("end\n"); 7
8 1 0.8 α Z= T [ev] Z α=0.9 α=0.8 α= T [ev] Abbildung 1: Ergebnisse zu den Übungen 1 (oben) und 2 (unten). 8
= pkp(t 1 ) und (1) α 1 (1 + α e ) α 2 α e
 Ionisationsgleichgewicht für Helium Da Helium-Atome zwei Elektronen besitzen, wird das Ionisationsgleichgewicht durch zwei Saha-Gleichungen beschrieben. Diese Gleichungen sollen mit dem Newton- Verfahren
Ionisationsgleichgewicht für Helium Da Helium-Atome zwei Elektronen besitzen, wird das Ionisationsgleichgewicht durch zwei Saha-Gleichungen beschrieben. Diese Gleichungen sollen mit dem Newton- Verfahren
Klausur-Musterlösungen
 Klausur-Musterlösungen 9.7.4 Theoretische Physik IV: Statistische Physik Prof. Dr. G. Alber Dr. O. Zobay. Der in Abb. dargestellte Kreisprozess wird mit einem elektromagnetischen Feld ausgeführt. Abb..
Klausur-Musterlösungen 9.7.4 Theoretische Physik IV: Statistische Physik Prof. Dr. G. Alber Dr. O. Zobay. Der in Abb. dargestellte Kreisprozess wird mit einem elektromagnetischen Feld ausgeführt. Abb..
T4p: Thermodynamik und Statistische Physik Prof. Dr. H. Ruhl Übungsblatt 3 Lösungsvorschlag
 T4p: Thermodynamik und Statistische Physik Prof. Dr. H. Ruhl Übungsblatt 3 Lösungsvorschlag 1. Extremwerte unter Nebenbedingungen In der Vorlesung wurden die mittleren Besetzungszahlen für verschiedene
T4p: Thermodynamik und Statistische Physik Prof. Dr. H. Ruhl Übungsblatt 3 Lösungsvorschlag 1. Extremwerte unter Nebenbedingungen In der Vorlesung wurden die mittleren Besetzungszahlen für verschiedene
1 Debye-Abschirmung. 1.1 Grundlagen. Φ = q r exp ( r/λ D), λ D =
 1 Debye-Abschirmung Bringt man eine zusätzliche estladung in ein Plasma ein, so wird deren elektrisches Feld durch die Ladungen des Plasmas mit entgegengesetztem Vorzeichen abgeschirmt. Die charakteristische
1 Debye-Abschirmung Bringt man eine zusätzliche estladung in ein Plasma ein, so wird deren elektrisches Feld durch die Ladungen des Plasmas mit entgegengesetztem Vorzeichen abgeschirmt. Die charakteristische
Nanoplasma. Nano(cluster)plasmen
 Nano(cluster)plasmen Nanoplasma Neben der Rumpfniveauspektroskopie an Clustern bietet FLASH die Möglichkeit Cluster unter extremen Bedingungen im Feld eines intensiven Röntgenpulses zu studieren (Nano)Plasmaphysik
Nano(cluster)plasmen Nanoplasma Neben der Rumpfniveauspektroskopie an Clustern bietet FLASH die Möglichkeit Cluster unter extremen Bedingungen im Feld eines intensiven Röntgenpulses zu studieren (Nano)Plasmaphysik
Erreichte Punktzahlen: Die Bearbeitungszeit beträgt 3 Stunden.
 Fakultät für Physik der LMU München Prof. Ilka Brunner Michael Kay Vorlesung T4, WS11/12 Klausur am 18. Februar 2012 Name: Matrikelnummer: Erreichte Punktzahlen: 1 2 3 4 5 6 Hinweise Die Bearbeitungszeit
Fakultät für Physik der LMU München Prof. Ilka Brunner Michael Kay Vorlesung T4, WS11/12 Klausur am 18. Februar 2012 Name: Matrikelnummer: Erreichte Punktzahlen: 1 2 3 4 5 6 Hinweise Die Bearbeitungszeit
Statistische Physik - Theorie der Wärme (PD Dr. M. Falcke)
 Freie Universität Berlin WS 6/7 Fachbereich Physik 4..6 Statistische Physik - Theorie der Wärme (PD Dr. M. Falcke) Übungsblatt 7: Dichtematrix, Variationsprinzip Aufgabe (5 Punkte) Betrachten Sie ein Gas
Freie Universität Berlin WS 6/7 Fachbereich Physik 4..6 Statistische Physik - Theorie der Wärme (PD Dr. M. Falcke) Übungsblatt 7: Dichtematrix, Variationsprinzip Aufgabe (5 Punkte) Betrachten Sie ein Gas
Physik IV Übung 4
 Physik IV 0 - Übung 4 8. März 0. Fermi-Bose-Boltzmann Verteilung Ein ideales Gas befinde sich in einer Box mit Volumen V = L 3. Das Gas besteht entweder aus Teilchen, die die Bose-Einstein oder Fermi-Dirac
Physik IV 0 - Übung 4 8. März 0. Fermi-Bose-Boltzmann Verteilung Ein ideales Gas befinde sich in einer Box mit Volumen V = L 3. Das Gas besteht entweder aus Teilchen, die die Bose-Einstein oder Fermi-Dirac
Statistische Thermodynamik I Lösungen zur Serie 11
 Statistische Thermodynamik I Lösungen zur Serie Verschiedenes 20 Mai 206 Barometrische Höhenformel: Betrachte die rdatmosphäre im homogenen Gravitationspotential M gz der rde Unter der Annahme, dass sich
Statistische Thermodynamik I Lösungen zur Serie Verschiedenes 20 Mai 206 Barometrische Höhenformel: Betrachte die rdatmosphäre im homogenen Gravitationspotential M gz der rde Unter der Annahme, dass sich
1 Drift in gekreuzten elektrischen und magnetischen
 1 Drift in gekreuzten elektrischen und magnetischen Feldern In einem Magnetfeld wirkt auf eine bewegte Ladung die Lorentzkraft. Aufgrund der Lorentzkraft unterscheidet sich die Bewegung parallel und senkrecht
1 Drift in gekreuzten elektrischen und magnetischen Feldern In einem Magnetfeld wirkt auf eine bewegte Ladung die Lorentzkraft. Aufgrund der Lorentzkraft unterscheidet sich die Bewegung parallel und senkrecht
Stirling sche Näherungsformel
 Stirling sche Näherungsformel ln(n!) N ln(n) N für N 6.5.22 Michael Buballa Stirling sche Näherungsformel ln(n!) = N ln(k) k= N dx ln(x) = (x ln(x) x) N = N ln(n) N 6.5.22 Michael Buballa Stirling sche
Stirling sche Näherungsformel ln(n!) N ln(n) N für N 6.5.22 Michael Buballa Stirling sche Näherungsformel ln(n!) = N ln(k) k= N dx ln(x) = (x ln(x) x) N = N ln(n) N 6.5.22 Michael Buballa Stirling sche
Übungen zur Theoretischen Physik Fa WS 17/18
 Karlsruher Institut für echnologie Institut für heorie der Kondensierten Materie Übungen zur heoretischen Physik Fa WS 17/18 Prof Dr A Shnirman Blatt 1 PD Dr B Narozhny Lösungsvorschlag 1 Landau-Niveaus:
Karlsruher Institut für echnologie Institut für heorie der Kondensierten Materie Übungen zur heoretischen Physik Fa WS 17/18 Prof Dr A Shnirman Blatt 1 PD Dr B Narozhny Lösungsvorschlag 1 Landau-Niveaus:
Vorlesung Statistische Mechanik: N-Teilchensystem
 Virialentwicklung Die Berechnung der Zustandssumme bei realen Gasen ist nicht mehr exakt durchführbar. Eine Möglichkeit, die Wechselwirkung in realen Gasen systematisch mitzunehmen ist, eine Entwicklung
Virialentwicklung Die Berechnung der Zustandssumme bei realen Gasen ist nicht mehr exakt durchführbar. Eine Möglichkeit, die Wechselwirkung in realen Gasen systematisch mitzunehmen ist, eine Entwicklung
Virialentwicklung. Janek Landsberg Fakultät für Physik, LMU München. Janek Landsberg. Die Virialentwicklung. Verschiedene Potentiale
 Die Warum Fakultät für Physik, LMU München 14.06.2006 Die Warum 1 Die Der zweite Virialkoeffizient 2 Hard-Sphere-Potential Lennard-Jones-Potential 3 Warum 4 Bsp. Hard-Sphere-Potential Asakura-Oosawa-Potential
Die Warum Fakultät für Physik, LMU München 14.06.2006 Die Warum 1 Die Der zweite Virialkoeffizient 2 Hard-Sphere-Potential Lennard-Jones-Potential 3 Warum 4 Bsp. Hard-Sphere-Potential Asakura-Oosawa-Potential
Einführung in die Astronomie I
 Einführung in die Astronomie I Teil 6 Peter Hauschildt yeti@hs.uni-hamburg.de Hamburger Sternwarte Gojenbergsweg 112 21029 Hamburg 20. Juni 2017 1 / 30 Übersicht Teil 6 Sternatmosphären Strahlungstransport
Einführung in die Astronomie I Teil 6 Peter Hauschildt yeti@hs.uni-hamburg.de Hamburger Sternwarte Gojenbergsweg 112 21029 Hamburg 20. Juni 2017 1 / 30 Übersicht Teil 6 Sternatmosphären Strahlungstransport
Übungen zu Moderne Theoretischen Physik III SS Maxwell-Boltzmann-Gas: großkanonisches Ensemble (5+5+5=15 Punkte, schriftlich)
 Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Übungen zu Moderne Theoretischen Physik III SS 016 Prof. Dr. A. Shnirman Blatt 6 PD Dr. B. Narozhny, P. Schad Lösungsvorschlag
Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Übungen zu Moderne Theoretischen Physik III SS 016 Prof. Dr. A. Shnirman Blatt 6 PD Dr. B. Narozhny, P. Schad Lösungsvorschlag
Moderne Theoretische Physik III (Theorie F Statistische Mechanik) SS 17
 Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Moderne Theoretische Physik III (Theorie F Statistische Mechanik SS 7 Prof. Dr. Alexander Mirlin Musterlösung: Blatt 6
Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Moderne Theoretische Physik III (Theorie F Statistische Mechanik SS 7 Prof. Dr. Alexander Mirlin Musterlösung: Blatt 6
Kernphysik. Elemententstehung. 2. Kernphysik. Cora Fechner. Universität Potsdam SS 2014
 Elemententstehung 2. Cora Fechner Universität Potsdam SS 2014 alische Grundlagen Kernladungszahl: Z = Anzahl der Protonen Massenzahl: A = Anzahl der Protonen + Anzahl der Neutronen Bindungsenergie: B
Elemententstehung 2. Cora Fechner Universität Potsdam SS 2014 alische Grundlagen Kernladungszahl: Z = Anzahl der Protonen Massenzahl: A = Anzahl der Protonen + Anzahl der Neutronen Bindungsenergie: B
Fermi-Dirac-Verteilung
 Fermi-Dirac-Verteilung Besetzungsfunktion pro innerem Freiheitsgrad: n(ε) = e (ε µ)/k B T + 6.7.23 Michael Buballa Fermi-Dirac-Verteilung Besetzungsfunktion pro innerem Freiheitsgrad: n(ε) = e (ε µ)/k
Fermi-Dirac-Verteilung Besetzungsfunktion pro innerem Freiheitsgrad: n(ε) = e (ε µ)/k B T + 6.7.23 Michael Buballa Fermi-Dirac-Verteilung Besetzungsfunktion pro innerem Freiheitsgrad: n(ε) = e (ε µ)/k
T4p: Thermodynamik und Statistische Physik Prof. Dr. H. Ruhl Übungsblatt 10 Lösungsvorschlag
 4: hermodynamik und Statistische Physik Prof. Dr. H. Ruhl Übungsblatt 10 Lösungsvorschlag 1. Joule-homson-Effekt Ein Gasstrom wird von Bereich 1 (siehe Abbildung) mit einem Kolben durch eine oröse Wand
4: hermodynamik und Statistische Physik Prof. Dr. H. Ruhl Übungsblatt 10 Lösungsvorschlag 1. Joule-homson-Effekt Ein Gasstrom wird von Bereich 1 (siehe Abbildung) mit einem Kolben durch eine oröse Wand
Theoretische Physik F: Zwischenklausur SS 12
 Karlsruher Institut für echnologie Institut für heorie der Kondensierten Materie heoretische Physik F: Zwischenklausur SS 1 Prof. Dr. Jörg Schmalian Lösungen Dr. Igor Gornyi esprechung 18.05.01 1. Quickies:
Karlsruher Institut für echnologie Institut für heorie der Kondensierten Materie heoretische Physik F: Zwischenklausur SS 1 Prof. Dr. Jörg Schmalian Lösungen Dr. Igor Gornyi esprechung 18.05.01 1. Quickies:
Moderne Theoretische Physik III (Theorie F Statistische Mechanik) SS 17
 Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Moderne Theoretische Physik III (Theorie F Statistische Mechanik) SS 7 Prof. Dr. Alexander Mirlin Musterlösung: Blatt
Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Moderne Theoretische Physik III (Theorie F Statistische Mechanik) SS 7 Prof. Dr. Alexander Mirlin Musterlösung: Blatt
Erreichte Punktzahlen: Die Bearbeitungszeit beträgt 3 Stunden.
 Fakultät für Physik der LMU München Prof. Ilka Brunner Vorlesung T4p, WS08/09 Klausur am 11. Februar 2009 Name: Matrikelnummer: Erreichte Punktzahlen: 1.1 1.2 1.3 2.1 2.2 2.3 2.4 Hinweise Die Bearbeitungszeit
Fakultät für Physik der LMU München Prof. Ilka Brunner Vorlesung T4p, WS08/09 Klausur am 11. Februar 2009 Name: Matrikelnummer: Erreichte Punktzahlen: 1.1 1.2 1.3 2.1 2.2 2.3 2.4 Hinweise Die Bearbeitungszeit
Van der Waals-Theorie und Zustandsgleichung
 Van der Waals-Theorie und Zustandsgleichung Eine verbesserte Zustandsgleichung für klassische Gase bei höheren Dichten liefert die Van der Waals-Gleichung. Diese Gleichung beschreibt auch den Phasenübergang
Van der Waals-Theorie und Zustandsgleichung Eine verbesserte Zustandsgleichung für klassische Gase bei höheren Dichten liefert die Van der Waals-Gleichung. Diese Gleichung beschreibt auch den Phasenübergang
Analysis III Gewöhnliche Differentialgleichungen 3. Übungsblatt (mit Lösungshinweisen)
 Analysis III Gewöhnliche Differentialgleichungen 3. Übungsblatt (mit Lösungshinweisen) Fachbereich Mathematik Wintersemester 0/0 Prof. Dr. Burkhard Kümmerer./3. November 0 Andreas Gärtner Walter Reußwig
Analysis III Gewöhnliche Differentialgleichungen 3. Übungsblatt (mit Lösungshinweisen) Fachbereich Mathematik Wintersemester 0/0 Prof. Dr. Burkhard Kümmerer./3. November 0 Andreas Gärtner Walter Reußwig
Moderne Theoretische Physik III (Theorie F Statistische Mechanik) SS 17
 Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Moderne Theoretische Physik III (Theorie F Statistische Mechanik) SS 7 Prof. Dr. Alexander Mirlin Musterlösung: Blatt
Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Moderne Theoretische Physik III (Theorie F Statistische Mechanik) SS 7 Prof. Dr. Alexander Mirlin Musterlösung: Blatt
Moderne Theoretische Physik IIIa WS 18/19
 Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Moderne Theoretische Physik IIIa WS 8/9 Prof. Dr. Alexander Mirlin Lösungen zu Blatt 7 Dr. Stefan Rex Besprechung: 9..9.
Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Moderne Theoretische Physik IIIa WS 8/9 Prof. Dr. Alexander Mirlin Lösungen zu Blatt 7 Dr. Stefan Rex Besprechung: 9..9.
Probeklausur STATISTISCHE PHYSIK PLUS
 DEPARTMENT FÜR PHYSIK, LMU Statistische Physik für Bachelor Plus WS 2011/12 Probeklausur STATISTISCHE PHYSIK PLUS NAME:... MATRIKEL NR.:... Bitte beachten: Schreiben Sie Ihren Namen auf jedes Blatt; Schreiben
DEPARTMENT FÜR PHYSIK, LMU Statistische Physik für Bachelor Plus WS 2011/12 Probeklausur STATISTISCHE PHYSIK PLUS NAME:... MATRIKEL NR.:... Bitte beachten: Schreiben Sie Ihren Namen auf jedes Blatt; Schreiben
Einführung in die Physikalische Chemie Teil 1: Mikrostruktur der Materie
 Einführung in die Physikalische Chemie Teil 1: Mikrostruktur der Materie Kapitel 1: Quantenmechanik Kapitel 2: Atome Kapitel 3: Moleküle Mathematische Grundlagen Schrödingergleichung Einfache Beispiele
Einführung in die Physikalische Chemie Teil 1: Mikrostruktur der Materie Kapitel 1: Quantenmechanik Kapitel 2: Atome Kapitel 3: Moleküle Mathematische Grundlagen Schrödingergleichung Einfache Beispiele
Sterne 16 Sternspektroskopie und Spektralanalyse (Teil 4)
 Sterne 16 Sternspektroskopie und Spektralanalyse (Teil 4) Gesetzmäßigkeiten in der Anordnung der Spektrallinien eines Stoffes? Wasserstoff Johann Jacob Balmer 1825-1898 A=364.4 nm n ganzzahlig > 2 Eine
Sterne 16 Sternspektroskopie und Spektralanalyse (Teil 4) Gesetzmäßigkeiten in der Anordnung der Spektrallinien eines Stoffes? Wasserstoff Johann Jacob Balmer 1825-1898 A=364.4 nm n ganzzahlig > 2 Eine
Elektrodynamik eines Plasmas
 Elektrodynamik eines Plasmas Elektrodynamik eines Plasmas Klassifikation von Plasmen Klassisches Plasma / Quantenplasma nicht-relativistisches / relativistisches Plasma Schwach / stark wechselwirkendes
Elektrodynamik eines Plasmas Elektrodynamik eines Plasmas Klassifikation von Plasmen Klassisches Plasma / Quantenplasma nicht-relativistisches / relativistisches Plasma Schwach / stark wechselwirkendes
Übungsblatt 06. PHYS4100 Grundkurs IV (Physik, Wirtschaftsphysik, Physik Lehramt) Othmar Marti, oder 3. 6.
 Übungsblatt 06 PHYS400 Grundkurs IV (Physik, Wirtschaftsphysik, Physik Lehramt) Othmar Marti, (othmar.marti@uni-ulm.de) 2. 6. 2005 oder 3. 6. 2005 Aufgaben. Schätzen Sie die relativistische Korrektur E
Übungsblatt 06 PHYS400 Grundkurs IV (Physik, Wirtschaftsphysik, Physik Lehramt) Othmar Marti, (othmar.marti@uni-ulm.de) 2. 6. 2005 oder 3. 6. 2005 Aufgaben. Schätzen Sie die relativistische Korrektur E
Ist a > b, dann ist b < a. Ist a < b, dann ist b > a. Ist a > b und b > c, dann ist a > c. Ist a < b und b < c, dann ist a < c.
 Teil Allgemeines zu Ungleichungen Die gebräuchlichsten Symbole für Ungleichungen sind > (ist grösser als), < (ist kleiner als), (ist grösser als oder gleich), (ist kleiner als oder gleich), (ist ungleich)
Teil Allgemeines zu Ungleichungen Die gebräuchlichsten Symbole für Ungleichungen sind > (ist grösser als), < (ist kleiner als), (ist grösser als oder gleich), (ist kleiner als oder gleich), (ist ungleich)
4 Thermodynamik mikroskopisch: kinetische Gastheorie makroskopisch: System:
 Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Physikalische Chemie Physikalische Chemie I SoSe 2009 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas. Thermodynamik
 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
Kapitel 5. Kanonisches Ensemble. 5.1 Herleitung 1; E 1 =? 2; E 2 =?
 Kapitel 5 Kanonisches Ensemble 5.1 Herleitung Abgesehen von der Legendre-Transformation S(E,, N) F (T,, N) besteht noch eine weitere Möglichkeit, die freie Energie zu berechnen, und zwar wiederum mittels
Kapitel 5 Kanonisches Ensemble 5.1 Herleitung Abgesehen von der Legendre-Transformation S(E,, N) F (T,, N) besteht noch eine weitere Möglichkeit, die freie Energie zu berechnen, und zwar wiederum mittels
Statistische Physik I
 Statistische Physik I 136.020 SS 2010 Vortragende: C. Lemell, S. YoshidaS http://dollywood.itp.tuwien.ac.at/~statmech Übersicht (vorläufig) 1) Wiederholung Begriffsbestimmung Eulergleichung 2) Phänomenologische
Statistische Physik I 136.020 SS 2010 Vortragende: C. Lemell, S. YoshidaS http://dollywood.itp.tuwien.ac.at/~statmech Übersicht (vorläufig) 1) Wiederholung Begriffsbestimmung Eulergleichung 2) Phänomenologische
Ruprecht-Karls-Universität Heidelberg Vorbereitung zur Diplomprüfung Theoretische Physik
 Ruprecht-Karls-Universität Heidelberg Vorbereitung zur Diplomprüfung Theoretische Physik begleitend zur Vorlesung Statistische Mechanik und Thermodynamik WS 2006/2007 Prof. Dr. Dieter W. Heermann erstellt
Ruprecht-Karls-Universität Heidelberg Vorbereitung zur Diplomprüfung Theoretische Physik begleitend zur Vorlesung Statistische Mechanik und Thermodynamik WS 2006/2007 Prof. Dr. Dieter W. Heermann erstellt
PCG Grundpraktikum Versuch 5 Lösungswärme Multiple Choice Test
 PCG Grundpraktikum Versuch 5 Lösungswärme Multiple Choice Test 1. Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Lösungswärme wird dieses Vorgespräch durch einen Multiple Choice
PCG Grundpraktikum Versuch 5 Lösungswärme Multiple Choice Test 1. Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Lösungswärme wird dieses Vorgespräch durch einen Multiple Choice
Grundlagen der Physik 3 Lösung zu Übungsblatt 2
 Grundlagen der Physik 3 Lösung zu Übungsblatt 2 Daniel Weiss 17. Oktober 2010 Inhaltsverzeichnis Aufgabe 1 - Zustandsfunktion eines Van-der-Waals-Gases 1 a) Zustandsfunktion.................................
Grundlagen der Physik 3 Lösung zu Übungsblatt 2 Daniel Weiss 17. Oktober 2010 Inhaltsverzeichnis Aufgabe 1 - Zustandsfunktion eines Van-der-Waals-Gases 1 a) Zustandsfunktion.................................
Musterlösung 02/09/2014
 Musterlösung 0/09/014 1 Streuexperimente (a) Betrachten Sie die Streuung von punktförmigen Teilchen an einer harten Kugel vom Radius R. Bestimmen Sie die Ablenkfunktion θ(b) unter der Annahme, dass die
Musterlösung 0/09/014 1 Streuexperimente (a) Betrachten Sie die Streuung von punktförmigen Teilchen an einer harten Kugel vom Radius R. Bestimmen Sie die Ablenkfunktion θ(b) unter der Annahme, dass die
Hochschule Düsseldorf University of Applied Sciences. 13. April 2016 HSD. Energiespeicher. Thermodynamik
 13. April 2016 Energiespeicher Thermodynamik Prof. Dr. Alexander Braun // Energiespeicher // SS 2016 26. April 2017 Thermodynamik Grundbegriffe Prof. Dr. Alexander Braun // Energiespeicher // SS 2017 26.
13. April 2016 Energiespeicher Thermodynamik Prof. Dr. Alexander Braun // Energiespeicher // SS 2016 26. April 2017 Thermodynamik Grundbegriffe Prof. Dr. Alexander Braun // Energiespeicher // SS 2017 26.
(a) Warum spielen die Welleneigenschaften bei einem fahrenden PKW (m = 1t, v = 100km/h) keine Rolle?
 FK Ex 4-07/09/2015 1 Quickies (a) Warum spielen die Welleneigenschaften bei einem fahrenden PKW (m = 1t, v = 100km/h) keine Rolle? (b) Wie groß ist die Energie von Lichtquanten mit einer Wellenlänge von
FK Ex 4-07/09/2015 1 Quickies (a) Warum spielen die Welleneigenschaften bei einem fahrenden PKW (m = 1t, v = 100km/h) keine Rolle? (b) Wie groß ist die Energie von Lichtquanten mit einer Wellenlänge von
(b) Schritt I: freie adiabatische Expansion, also ist δw = 0, δq = 0 und damit T 2 = T 1. Folglich ist nach 1. Hauptsatz auch U = 0.
 3 Lösungen Lösung zu 65. (a) Siehe Abbildung 1. (b) Schritt I: freie adiabatische Expansion, also ist δw 0, δq 0 und damit. Folglich ist nach 1. Hauptsatz auch U 0. Schritt II: isobare Kompression, also
3 Lösungen Lösung zu 65. (a) Siehe Abbildung 1. (b) Schritt I: freie adiabatische Expansion, also ist δw 0, δq 0 und damit. Folglich ist nach 1. Hauptsatz auch U 0. Schritt II: isobare Kompression, also
13.5 Photonen und Phononen
 Woche 11 13.5 Photonen und Phononen Teilchen mit linearem Dispersionsgesetz: E = c p, c - Ausbreitungsgeschwindigkeit (Licht- oder Schallgeschwindigkeit). 13.5.1 Photonen Quantisierung der Eigenschwingungen
Woche 11 13.5 Photonen und Phononen Teilchen mit linearem Dispersionsgesetz: E = c p, c - Ausbreitungsgeschwindigkeit (Licht- oder Schallgeschwindigkeit). 13.5.1 Photonen Quantisierung der Eigenschwingungen
PC-Übung Nr.1 vom
 PC-Übung Nr.1 vom 17.10.08 Sebastian Meiss 25. November 2008 1. Allgemeine Vorbereitung a) Geben Sie die Standardbedingungen in verschiedenen Einheiten an: Druck p in Pa, bar, Torr, atm Temperatur T in
PC-Übung Nr.1 vom 17.10.08 Sebastian Meiss 25. November 2008 1. Allgemeine Vorbereitung a) Geben Sie die Standardbedingungen in verschiedenen Einheiten an: Druck p in Pa, bar, Torr, atm Temperatur T in
Theorie der Wärme Musterlösung 11.
 Theorie der Wärme Musterlösung. FS 05 Prof. Thomas Gehrmann Übung. Edelgas im Schwerefeld Berechne den Erwartungswert der Energie eines monoatomaren idealen Gases z. B. eines Edelgases in einem zylindrischen
Theorie der Wärme Musterlösung. FS 05 Prof. Thomas Gehrmann Übung. Edelgas im Schwerefeld Berechne den Erwartungswert der Energie eines monoatomaren idealen Gases z. B. eines Edelgases in einem zylindrischen
Das Magnetfeld. Das elektrische Feld
 Seite 1 von 5 Magnetisches und elektrisches Feld Das Magnetfeld beschreibt Eigenschaften der Umgebung eines Magneten. Auch bewegte Ladungen rufen Magnetfelder hervor. Mithilfe von Feldlinienbilder können
Seite 1 von 5 Magnetisches und elektrisches Feld Das Magnetfeld beschreibt Eigenschaften der Umgebung eines Magneten. Auch bewegte Ladungen rufen Magnetfelder hervor. Mithilfe von Feldlinienbilder können
Probeklausur: Thermodynamik
 E2-E2p: Experimentalphysik 2 Prof. J. Lipfert SS 2018 Probeklausur: Thermodynamik Probeklausur: Thermodynamik Vorname: Nachname: Matrikelnummer: Studiengang: Fachsemester: Studierende der E2p (6 ECTS)
E2-E2p: Experimentalphysik 2 Prof. J. Lipfert SS 2018 Probeklausur: Thermodynamik Probeklausur: Thermodynamik Vorname: Nachname: Matrikelnummer: Studiengang: Fachsemester: Studierende der E2p (6 ECTS)
Strahlungslose Übergänge. Pumpen Laser
 Prof Ch Berger, Physik f Maschinenbauer, WS 02/03 15 Vorlesung 44 Strahlungsprozesse 441 Das Zerfallsgesetz Elektronen aus energetisch hoher liegenden Zustanden gehen in die tieferen Zustande uber, falls
Prof Ch Berger, Physik f Maschinenbauer, WS 02/03 15 Vorlesung 44 Strahlungsprozesse 441 Das Zerfallsgesetz Elektronen aus energetisch hoher liegenden Zustanden gehen in die tieferen Zustande uber, falls
Übungen zu Moderne Theoretischen Physik III SS Maxwell-Verteilung: (30 Punkte, schriftlich)
 Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Übungen zu Moderne Theoretischen Physik III SS 06 Prof. Dr. A. Shnirman Blatt 4 PD Dr. B. arozhny, P. Schad Lösungsvorschlag.
Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Übungen zu Moderne Theoretischen Physik III SS 06 Prof. Dr. A. Shnirman Blatt 4 PD Dr. B. arozhny, P. Schad Lösungsvorschlag.
Physikdepartment. Ferienkurs zur Experimentalphysik 4. Daniel Jost 10/09/15
 Physikdepartment Ferienkurs zur Experimentalphysik 4 Daniel Jost 10/09/15 Inhaltsverzeichnis Technische Universität München 1 Kurze Einführung in die Thermodynamik 1 1.1 Hauptsätze der Thermodynamik.......................
Physikdepartment Ferienkurs zur Experimentalphysik 4 Daniel Jost 10/09/15 Inhaltsverzeichnis Technische Universität München 1 Kurze Einführung in die Thermodynamik 1 1.1 Hauptsätze der Thermodynamik.......................
Blatt 08: Reihenentwicklung
 Fakultät für Physik Jan von Delft, Katharina Stadler, Frauke Schwarz T0: Rechenmethoden für Physiker, WiSe 203/4 http://homepagesphysikuni-muenchende/~vondelft/lehre/3t0/ Blatt 08: Reihenentwicklung Abgabe:
Fakultät für Physik Jan von Delft, Katharina Stadler, Frauke Schwarz T0: Rechenmethoden für Physiker, WiSe 203/4 http://homepagesphysikuni-muenchende/~vondelft/lehre/3t0/ Blatt 08: Reihenentwicklung Abgabe:
Physik 4, Probeklausur, Prof. Förster
 Physik 4, Probeklausur, Prof. Förster chris@university-material.de Dieser Text ist unter dieser Creative Commons Lizenz veröffentlicht. Ich erhebe keinen Anspruch auf Vollständigkeit oder Richtigkeit.
Physik 4, Probeklausur, Prof. Förster chris@university-material.de Dieser Text ist unter dieser Creative Commons Lizenz veröffentlicht. Ich erhebe keinen Anspruch auf Vollständigkeit oder Richtigkeit.
1 Massenwirkungsgesetz
 1 Massenwirkungsgesetz Zeige: Bei konstantem Druck und konstanter emperatur gilt für chemische Reaktionen der Art a 1 A 1 + a A + : : : a L A L b 1 B 1 + b B + : : : b R B R : K c (A i ) ai c (B j ) bj
1 Massenwirkungsgesetz Zeige: Bei konstantem Druck und konstanter emperatur gilt für chemische Reaktionen der Art a 1 A 1 + a A + : : : a L A L b 1 B 1 + b B + : : : b R B R : K c (A i ) ai c (B j ) bj
Thermodynamische Hauptsätze, Kreisprozesse Übung
 Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 14.09.2010 Inhaltsverzeichnis Inhaltsverzeichnis 1 Thermodynamische Hauptsätze 3 1.1 Aufgabe 1:.................................... 3 1.2 Aufgabe
Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 14.09.2010 Inhaltsverzeichnis Inhaltsverzeichnis 1 Thermodynamische Hauptsätze 3 1.1 Aufgabe 1:.................................... 3 1.2 Aufgabe
Moderne Physik: Elemente der Festkörperphysik Wintersemester 2010/11 Übungsblatt 5 für den
 Moderne Physik: Elemente der Festkörperphysik Wintersemester 21/11 Übungsblatt 5 für den 14.1.211 14. Fermi-Energie von Elektronen in Metallen Bei T = K besitzt ein freies Elektronengas der Ladungsträgerdichte
Moderne Physik: Elemente der Festkörperphysik Wintersemester 21/11 Übungsblatt 5 für den 14.1.211 14. Fermi-Energie von Elektronen in Metallen Bei T = K besitzt ein freies Elektronengas der Ladungsträgerdichte
HAW Hamburg Fachbereich HWI Hamburg, Prof. Dr. Badura B. Hamraz, O. Zarenko, M. Behrens. Chemie Testat 2. Name: Vorname: Matrikelnummer:
 Chemie Testat 2 Name: Vorname: Matrikelnummer: Bearbeitungszeit: 1 Stunde Zugelassene Hilfsmittel: Stifte, unbeschriebenes Papier, ein nichtprogrammierbarer Taschenrechner und ein Periodensystem Bitte
Chemie Testat 2 Name: Vorname: Matrikelnummer: Bearbeitungszeit: 1 Stunde Zugelassene Hilfsmittel: Stifte, unbeschriebenes Papier, ein nichtprogrammierbarer Taschenrechner und ein Periodensystem Bitte
Ferienkurs Experimentalphysik 4
 Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Grundlagen der Physik II
 Grundlagen der Physik II Othmar Marti 12. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 12. 07. 2007 Klausur Die Klausur
Grundlagen der Physik II Othmar Marti 12. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 12. 07. 2007 Klausur Die Klausur
Vorbereitung: Franck-Hertz-Versuch. Christine Dörflinger und Frederik Mayer, Gruppe Do-9 3. Mai 2012
 Vorbereitung: Franck-Hertz-Versuch Christine Dörflinger und Frederik Mayer, Gruppe Do-9 3. Mai 2012 1 Inhaltsverzeichnis 0 Allgemeines 3 1 Aufgabe 1 3 1.1 Versuchsaufbau.............................................
Vorbereitung: Franck-Hertz-Versuch Christine Dörflinger und Frederik Mayer, Gruppe Do-9 3. Mai 2012 1 Inhaltsverzeichnis 0 Allgemeines 3 1 Aufgabe 1 3 1.1 Versuchsaufbau.............................................
Übungen zu Theoretische Physik IV
 Physikalisches Institut Übungsblatt 4 Universität Bonn 02. November 2012 Theoretische Physik WS 12/13 Übungen zu Theoretische Physik IV Priv.-Doz. Dr. Stefan Förste http://www.th.physik.uni-bonn.de/people/forste/exercises/ws1213/tp4
Physikalisches Institut Übungsblatt 4 Universität Bonn 02. November 2012 Theoretische Physik WS 12/13 Übungen zu Theoretische Physik IV Priv.-Doz. Dr. Stefan Förste http://www.th.physik.uni-bonn.de/people/forste/exercises/ws1213/tp4
Die Sonne ein Stern im Detail (2) Die Photosphäre
 Die Sonne ein Stern im Detail (2) Die Photosphäre Plasma der Stoff, aus dem die Sonne ist Ab einer Temperatur von 10000 K liegt die Materie vollständig im Plasmazustand vor. Dieser spezielle 4. Aggregatzustand
Die Sonne ein Stern im Detail (2) Die Photosphäre Plasma der Stoff, aus dem die Sonne ist Ab einer Temperatur von 10000 K liegt die Materie vollständig im Plasmazustand vor. Dieser spezielle 4. Aggregatzustand
A 1. + r 2 ) 2. Stoßquerschnitt und mittlere freie Weglänge
 Stoßquerschnitt und mittlere freie Weglänge Im idealen Gas findet zwischen zwei Teilchen ein Stoß statt, wenn der Abstand der Fluggeraden den beiden Teilchen, der Stoßparameter b, kleiner ist als die Summe
Stoßquerschnitt und mittlere freie Weglänge Im idealen Gas findet zwischen zwei Teilchen ein Stoß statt, wenn der Abstand der Fluggeraden den beiden Teilchen, der Stoßparameter b, kleiner ist als die Summe
Fortgeschrittenen Praktikum I Teil A. Langmuir-Sonde. Nils Thielke und Robert Brauer. 8. November 2012
 Fortgeschrittenen Praktikum I Teil A Langmuir-Sonde Nils Thielke und Robert Brauer 8. November 2012 Wir erklären, dass wir dieses Protokoll eigenhändig anhand des angehängten Messprotokolls und der angegebenen
Fortgeschrittenen Praktikum I Teil A Langmuir-Sonde Nils Thielke und Robert Brauer 8. November 2012 Wir erklären, dass wir dieses Protokoll eigenhändig anhand des angehängten Messprotokolls und der angegebenen
Atomphysik Klasse 9. Aufgabe: Fülle die freien Felder aus!
 1. Was gibt die Massenzahl A eines Atoms an? Die Zahl der Neutronen im Kern. Die Zahl der Protonen im Kern. Die Summe aus Kernneutronen und Kernprotonen. Die Zahl der Elektronen. Die Summe von Elektronen
1. Was gibt die Massenzahl A eines Atoms an? Die Zahl der Neutronen im Kern. Die Zahl der Protonen im Kern. Die Summe aus Kernneutronen und Kernprotonen. Die Zahl der Elektronen. Die Summe von Elektronen
5 Anwendung der Dichtefunktionaltheorie
 5 Anwendung der Dichtefunktionaltheorie Im Rahmen der Born-Oppenheimer-Näherung lässt sich der elektronische Grundzustand E g mithilfe der Dichtefunktionaltheorie berechnen, wobei das Einelektronenpotenzial
5 Anwendung der Dichtefunktionaltheorie Im Rahmen der Born-Oppenheimer-Näherung lässt sich der elektronische Grundzustand E g mithilfe der Dichtefunktionaltheorie berechnen, wobei das Einelektronenpotenzial
Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde. Sommersemester 2007
 Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde Sommersemester 2007 VL #35 am 28.06.2007 Vladimir Dyakonov Leitungsmechanismen Ladungstransport in Festkörpern Ladungsträger
Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde Sommersemester 2007 VL #35 am 28.06.2007 Vladimir Dyakonov Leitungsmechanismen Ladungstransport in Festkörpern Ladungsträger
Moderne Theoretische Physik IIIb 2019
 Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Moderne Theoretische Physik IIIb 09 Prof Dr Alexander Mirlin Lösungen zu Blatt PD Dr Igor Gornyi, Dr Stefan Rex Besprechung:
Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Moderne Theoretische Physik IIIb 09 Prof Dr Alexander Mirlin Lösungen zu Blatt PD Dr Igor Gornyi, Dr Stefan Rex Besprechung:
Aufgabe 1. Lösung nichtlinearer Gleichungen mit einer Variablen
 Aufgabe. Lösung nichtlinearer Gleichungen mit einer Variablen. Teil: Nullstellenbestimmung Aufgabenstellung Es sollten in Fortran verschiedene Verfahren zur iterativen Nullstellenbestimmung von Funktionen
Aufgabe. Lösung nichtlinearer Gleichungen mit einer Variablen. Teil: Nullstellenbestimmung Aufgabenstellung Es sollten in Fortran verschiedene Verfahren zur iterativen Nullstellenbestimmung von Funktionen
Aufbau des Atomkerns a) Gib an, aus wie vielen Protonen und Neutronen die
 Aufbau des Atomkerns a) Gib an, aus wie vielen Protonen und Neutronen die Atomkerne von Cl bestehen. b) Erkläre, was man unter Isotopen versteht. Gib ein Beispiel an. 3, Cl c) Im Periodensystem wird die
Aufbau des Atomkerns a) Gib an, aus wie vielen Protonen und Neutronen die Atomkerne von Cl bestehen. b) Erkläre, was man unter Isotopen versteht. Gib ein Beispiel an. 3, Cl c) Im Periodensystem wird die
Kapitel 3. Statistische Definition der Entropie. 3.1 Ensemble aus vielen Teilchen
 Kapitel 3 Statistische Definition der Entropie 3.1 Ensemble aus vielen Teilchen Die Überlegungen dieses Abschnitts werden für klassische Teilchen formuliert, gelten sinngemäß aber genauso auch für Quantensysteme.
Kapitel 3 Statistische Definition der Entropie 3.1 Ensemble aus vielen Teilchen Die Überlegungen dieses Abschnitts werden für klassische Teilchen formuliert, gelten sinngemäß aber genauso auch für Quantensysteme.
Thermodynamische Hauptsätze, Kreisprozesse Übung
 Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 4.09.00 Inhaltsverzeichnis Inhaltsverzeichnis Thermodynamische Hauptsätze. Aufgabe :..................................... Aufgabe :.....................................
Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 4.09.00 Inhaltsverzeichnis Inhaltsverzeichnis Thermodynamische Hauptsätze. Aufgabe :..................................... Aufgabe :.....................................
Statistische Mechanik
 Kapitel 7 Statistische Mechanik 7.1 Lagrange-Multiplikatoren Fkt fx). Bedingung eines Maximums oder Minimums) df = f x)dx = 0. Fkt von n Variablen: fx 1,x 2,...,x n ). Bedingung des Maximums: Sei df x)
Kapitel 7 Statistische Mechanik 7.1 Lagrange-Multiplikatoren Fkt fx). Bedingung eines Maximums oder Minimums) df = f x)dx = 0. Fkt von n Variablen: fx 1,x 2,...,x n ). Bedingung des Maximums: Sei df x)
Rückblick auf die letzte Vorlesung
 Rückblick auf die letzte Vorlesung 1 Lineare autonome Differentialgleichungen 2 Bestimmung des Fundamentalsystems 3 Jordansche Normalform 4 Reelle Fundamentalsysteme Ausblick auf die heutige Vorlesung
Rückblick auf die letzte Vorlesung 1 Lineare autonome Differentialgleichungen 2 Bestimmung des Fundamentalsystems 3 Jordansche Normalform 4 Reelle Fundamentalsysteme Ausblick auf die heutige Vorlesung
Grundlagen der Physik 3 Lösung zu Übungsblatt 1
 Grundlagen der Physik 3 Lösung zu Übungsblatt Daniel Weiss 0. Oktober 200 Inhaltsverzeichnis Aufgabe - Anzahl von Atomen und Molekülen a) ohlensto..................................... 2 b) Helium.......................................
Grundlagen der Physik 3 Lösung zu Übungsblatt Daniel Weiss 0. Oktober 200 Inhaltsverzeichnis Aufgabe - Anzahl von Atomen und Molekülen a) ohlensto..................................... 2 b) Helium.......................................
Höhere Experimentalphysik 2
 Höhere Experimentalphysik 2 Institut für Angewandte Physik Goethe-Universität Frankfurt am Main 5. Vorlesung 29.05.2015 Ankündigung Übung Die nächste Übung findet am 8.6. statt! Die Übungsblätter und das
Höhere Experimentalphysik 2 Institut für Angewandte Physik Goethe-Universität Frankfurt am Main 5. Vorlesung 29.05.2015 Ankündigung Übung Die nächste Übung findet am 8.6. statt! Die Übungsblätter und das
Experimentalphysik 2
 Repetitorium zu Experimentalphysik 2 Ferienkurs am Physik-Department der Technischen Universität München Gerd Meisl 5. August 2008 Inhaltsverzeichnis 1 Übungsaufgaben 2 1.1 Übungsaufgaben....................................
Repetitorium zu Experimentalphysik 2 Ferienkurs am Physik-Department der Technischen Universität München Gerd Meisl 5. August 2008 Inhaltsverzeichnis 1 Übungsaufgaben 2 1.1 Übungsaufgaben....................................
Theoretische Physik 4 - Blatt 1
 Theoretische Physik 4 - Blatt 1 Christopher Bronner, Frank Essenberger FU Berlin 21.Oktober.2006 Inhaltsverzeichnis 1 Compton-Effekt 1 2 Bohrsches Atommodell 2 2.1 Effektives Potential..........................
Theoretische Physik 4 - Blatt 1 Christopher Bronner, Frank Essenberger FU Berlin 21.Oktober.2006 Inhaltsverzeichnis 1 Compton-Effekt 1 2 Bohrsches Atommodell 2 2.1 Effektives Potential..........................
Alle Atome haben Massen ungefähr einem vielfachen der Masse des Wasserstoff Atoms.
 02. Atom Page 1 2. Das Atom Atom: kleinster unveränderbarer Bestandteil eines chemischen Elements Charakteristische Eigenschaften von Atomen: Masse, Volumen, Ladung 2.1 Bestimmung der Atommasse expt. Befund:
02. Atom Page 1 2. Das Atom Atom: kleinster unveränderbarer Bestandteil eines chemischen Elements Charakteristische Eigenschaften von Atomen: Masse, Volumen, Ladung 2.1 Bestimmung der Atommasse expt. Befund:
Der Gesamtbahndrehimpuls ist eine Erhaltungsgrösse (genau wie in der klassischen Mechanik).
 phys4.017 Page 1 10.4.2 Bahndrehimpuls des Elektrons: Einheit des Drehimpuls: Der Bahndrehimpuls des Elektrons ist quantisiert. Der Gesamtbahndrehimpuls ist eine Erhaltungsgrösse (genau wie in der klassischen
phys4.017 Page 1 10.4.2 Bahndrehimpuls des Elektrons: Einheit des Drehimpuls: Der Bahndrehimpuls des Elektrons ist quantisiert. Der Gesamtbahndrehimpuls ist eine Erhaltungsgrösse (genau wie in der klassischen
4.5 KLASSISCHE FLÜSSIGKEITEN 85
 4.5 KLASSISCHE FLÜSSIGKEITEN 85 σ / 2 σ / 2 Abbildung 4.9: Modell der harten Scheiben Wie wir sehen werden, besitzt dieses Modell mehrere Phasen und ist damit ideal zum Studium gewisser Eigenschaften solcher
4.5 KLASSISCHE FLÜSSIGKEITEN 85 σ / 2 σ / 2 Abbildung 4.9: Modell der harten Scheiben Wie wir sehen werden, besitzt dieses Modell mehrere Phasen und ist damit ideal zum Studium gewisser Eigenschaften solcher
Musterlösung Übung 4
 Musterlösung Übung 4 Aufgabe 1: Radon im Keller a) 222 86Rn hat 86 Protonen, 86 Elektronen und 136 Neutronen. Der Kern hat demnach eine gerade Anzahl Protonen und eine gerade Anzahl Neutronen und gehört
Musterlösung Übung 4 Aufgabe 1: Radon im Keller a) 222 86Rn hat 86 Protonen, 86 Elektronen und 136 Neutronen. Der Kern hat demnach eine gerade Anzahl Protonen und eine gerade Anzahl Neutronen und gehört
Ab-initio Thermodynamik
 Institut für Theoretische Physik Technische Universität Clausthal 4. Dezember 2004 Hintergrund Für kommende Transistorgenerationen ( 2013) müssen Oxide (z.b: Ba x Sr 1 x TiO 3 ) epitaktisch auf Halbleitern
Institut für Theoretische Physik Technische Universität Clausthal 4. Dezember 2004 Hintergrund Für kommende Transistorgenerationen ( 2013) müssen Oxide (z.b: Ba x Sr 1 x TiO 3 ) epitaktisch auf Halbleitern
Übungen zur Theoretischen Physik F SS Ideales Boltzmann-Gas: ( =25 Punkte, schriftlich)
 Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Übungen zur Theoretischen Physik F SS 2016 Prof. Dr. A. Shnirman Blatt 2 Dr. B. Narozhny, Dipl.-Phys. P. Schad Lösungsvorschlag
Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Übungen zur Theoretischen Physik F SS 2016 Prof. Dr. A. Shnirman Blatt 2 Dr. B. Narozhny, Dipl.-Phys. P. Schad Lösungsvorschlag
7. Das Bohrsche Modell des Wasserstoff-Atoms. 7.1 Stabile Elektronbahnen im Atom
 phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
Was haben wir gelernt?
 Was haben wir gelernt? - Gesetze chemischer Reaktionen - Atommodell von Dalton - Elementsymbole - Die atomare Masseneinheit u - Die Avogadro-Zahl und deren Umkehrung - Von Massenverhältnissen zu Teilchenverhältnissen
Was haben wir gelernt? - Gesetze chemischer Reaktionen - Atommodell von Dalton - Elementsymbole - Die atomare Masseneinheit u - Die Avogadro-Zahl und deren Umkehrung - Von Massenverhältnissen zu Teilchenverhältnissen
1. Wärmelehre 1.1. Temperatur. Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités)
 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
Die inhomogene Differentialgleichung höherer Ordnung.
 Die inhomogene Differentialgleichung höherer Ordnung. Ist das Funktionensystem (y 1,..., y n ) ein Fundamentalsystem, so ist die Matrix Y(t) = y (0) 1... y n (0). y (n 1) 1... y n (n 1) eine Fundamentalmatrix
Die inhomogene Differentialgleichung höherer Ordnung. Ist das Funktionensystem (y 1,..., y n ) ein Fundamentalsystem, so ist die Matrix Y(t) = y (0) 1... y n (0). y (n 1) 1... y n (n 1) eine Fundamentalmatrix
6.2 Temperatur und Boltzmann Verteilung
 222 KAPITEL 6. THERMODYNAMIK UND WÄRMELEHRE 6.2 Temperatur und Boltzmann Verteilung Im letzten Abschnitt haben wir gesehen, dass eine statistische Verteilung von Atomen eines idealen Gases in einem Volumen
222 KAPITEL 6. THERMODYNAMIK UND WÄRMELEHRE 6.2 Temperatur und Boltzmann Verteilung Im letzten Abschnitt haben wir gesehen, dass eine statistische Verteilung von Atomen eines idealen Gases in einem Volumen
Theoretische Physik 25. Juli 2013 Thermodynamik und statistische Physik (T4) Prof. Dr. U. Schollwöck Sommersemester 2013
 Theoretische Physik 25. Juli 2013 Thermodynamik und statistische Physik (T4) Klausur Prof. Dr. U. Schollwöck Sommersemester 2013 Matrikelnummer: Aufgabe 1 2 3 4 5 6 Summe Punkte Note: WICHTIG! Schreiben
Theoretische Physik 25. Juli 2013 Thermodynamik und statistische Physik (T4) Klausur Prof. Dr. U. Schollwöck Sommersemester 2013 Matrikelnummer: Aufgabe 1 2 3 4 5 6 Summe Punkte Note: WICHTIG! Schreiben
8 Das klassische ideale Gas
 8 Das klassische ideale Gas 8.1 Unterscheidbare Atome Gleichartige Atome (etwa zwei He-Atome) sind in der Quantenmechanik grundsätzlich nicht unterscheidbar. Wir wollen dies jedoch zunächst ignorieren,
8 Das klassische ideale Gas 8.1 Unterscheidbare Atome Gleichartige Atome (etwa zwei He-Atome) sind in der Quantenmechanik grundsätzlich nicht unterscheidbar. Wir wollen dies jedoch zunächst ignorieren,
2.1 Bestimmung einiger Isothermen von Schwefelhexafluorid SF 6
 Atom- und Kernphysi-Versuch 31 AKP-31-1 Zustandsgrößen realer Gase 1 Vorbereitung Koexistenz von Flüssigeiten und Dampf, Dampfdruc, Verdampfungswärme, Koexistenz von Festörper und Flüssigeit, Koexistenz
Atom- und Kernphysi-Versuch 31 AKP-31-1 Zustandsgrößen realer Gase 1 Vorbereitung Koexistenz von Flüssigeiten und Dampf, Dampfdruc, Verdampfungswärme, Koexistenz von Festörper und Flüssigeit, Koexistenz
Klausur zur Statistischen Physik SS 2013
 Klausur zur Statistischen Physik SS 2013 Prof. Dr. M. Rohlfing Die folgenden Angaben bitte deutlich in Blockschrift ausfüllen: Name, Vorname: geb. am: in: Matrikel-Nr.: Übungsgruppenleiter: Aufgabe maximale
Klausur zur Statistischen Physik SS 2013 Prof. Dr. M. Rohlfing Die folgenden Angaben bitte deutlich in Blockschrift ausfüllen: Name, Vorname: geb. am: in: Matrikel-Nr.: Übungsgruppenleiter: Aufgabe maximale
Die Thermodynamik des Universums
 Die Thermodynamik des Universums Kai Walter Contents 1 Einleitung 2 2 Gleichgewichtsthermodynamik 2 2.1 Quantengas -Einteilchensystem-................... 2 2.2 Quantengase -MehrteilchenSystem.................
Die Thermodynamik des Universums Kai Walter Contents 1 Einleitung 2 2 Gleichgewichtsthermodynamik 2 2.1 Quantengas -Einteilchensystem-................... 2 2.2 Quantengase -MehrteilchenSystem.................
Das Ideale Gas Kinetische Gastheorie (auf atomarer Ebene)
 Das Ideale Gas Kinetische Gastheorie (auf atomarer Ebene) Wir haben gesehen, dass ein sogenanntes 'ideales Gas' durch die Zustandsgleichung pv = νr T [1] beschrieben wird; wir wollen nun verstehen, welchen
Das Ideale Gas Kinetische Gastheorie (auf atomarer Ebene) Wir haben gesehen, dass ein sogenanntes 'ideales Gas' durch die Zustandsgleichung pv = νr T [1] beschrieben wird; wir wollen nun verstehen, welchen
Ferienkurs Experimentalphysik 2
 Ferienkurs Experimentalphysik 2 Vorlesung 1 Thermodynamik Andreas Brenneis, Marcus Jung, Ann-Kathrin Straub 13.09.2010 1 Allgemeines und Grundbegriffe Grundlegend für das nun folgende Kapitel Thermodynamik
Ferienkurs Experimentalphysik 2 Vorlesung 1 Thermodynamik Andreas Brenneis, Marcus Jung, Ann-Kathrin Straub 13.09.2010 1 Allgemeines und Grundbegriffe Grundlegend für das nun folgende Kapitel Thermodynamik
Nachklausur zur Vorlesung Theoretische Physik in zwei Semestern II. Musterlösungen
 UNIVERSITÄT ZU KÖLN Institut für Theoretische Physik Wintersemester 005/006 Nachklausur zur Vorlesung Theoretische Physik in zwei Semestern II Musterlösungen 1. Welche experimentellen Tatsachen weisen
UNIVERSITÄT ZU KÖLN Institut für Theoretische Physik Wintersemester 005/006 Nachklausur zur Vorlesung Theoretische Physik in zwei Semestern II Musterlösungen 1. Welche experimentellen Tatsachen weisen
TU Dresden Fachrichtung Mathematik Institut für Numerische Mathematik 1. Dr. M. Herrich SS 2017
 TU Dresden Fachrichtung Mathematik Institut für Numerische Mathematik 1 Prof. Dr. K. Eppler Institut für Numerische Mathematik Dr. M. Herrich SS 2017 Aufgabe 1 Übungen zur Vorlesung Mathematik II 4. Übung,
TU Dresden Fachrichtung Mathematik Institut für Numerische Mathematik 1 Prof. Dr. K. Eppler Institut für Numerische Mathematik Dr. M. Herrich SS 2017 Aufgabe 1 Übungen zur Vorlesung Mathematik II 4. Übung,
