Inhaltsverzeichnis. Optische Methoden
|
|
|
- Gottlob Wetzel
- vor 7 Jahren
- Abrufe
Transkript
1 Inhaltsverzeichnis Optische Methoden 1. Einführung Elektromagnetische Wellen Lichtabsorption und Farbe Anwendung optischer Verfahren Atomspektroskopie Grundlagen Atomemissionsspektroskopie (AES) Atomabsorptionsspektroskopie (AAS) Flammen-AAS Graphitrohrofen-Technik Hydrid-Technik Kaltdampf-Technik Molekülspektroskopie UV/Vis-Spektroskopie Grundlagen Fluorimetrie IR-Spektrometrie (IR) Nahinfrarot-Spektrometrie (NIR) Polarimetrie H-NMR-Spektroskopie Massenspektrometrie (MS) Prinzip Klassische Ionisationsmethoden Elektronenstoß-Ionisation (EI) Chemische Ionisation (CI) Schonende Ionisation Elektrospray-Ionisation (ESI) Matrix-unterstützte-Laser-Desorption (MALDI) Analysator Quadrupol-Analysator Flugzeit-Analysator
2 1. Einführung 1.1 Elektromagnetische Wellen Ausbreitungsgeschwindigkeit im Vakuum = Lichtgeschwindigkeit Wellen unterscheiden sich in der Wellenlänge λ bzw. in der Frequenz ν [Zahl der Schwingungen pro Sekunde] Ausbreitungsgeschwindigkeit c= c 0 = 0 [c 0: Ausbreitungsgeschwindigkeit im Vakuum; λ 0: Wellenlänge im Vakuum] Wellenzahl ν= 1 [cm -1 ] Anzahl der Wellenlängen pro cm λ proportional zur Frequenz antiproportional zur Wellenlänge elektromagnetische Strahlung besteht aus Teilchen: Lichtquanten bzw. Photonen PLANCK'sche Gleichung: E=h bzw. E= h c [E: Energie eines Lichtquants; h: Proportionalitätsfaktor; ν: Frequenz] Energie der Lichtquanten ist von der Frequenz abhängig; je größer ν, umso größer E je größer λ, umso geringer E 1.2 Lichtabsorption und Farbe Gemisch aller Wellenlängen weiß wird ein Stoff von Licht getroffen, so wird ein Teil absorbiert, der Rest reflektiert; das Auge sieht die Komplementärfarbe des absorbierten Lichts Absorption = Energieaufnahme Emission = Energieabgabe 1.3 Anwendung optischer Verfahren 1. Strukturaufklärung eine vorher noch nie untersuchte Substanz wird analysiert 2. a) Identifizierung Substanz gehört zu den bereits bekannten Substanzen und wird mit diesen verglichen, um eine qualitative Aussage machen zu können b) Wiedererkennung es ist bekannt, welche Substanz vorliegen soll; man überprüft durch Vergleichen, ob es sich auch tatsächlich um die Substanz handelt 3. Quantifizierung 2
3 2. Atomspektroskopie 2.1 Grundlagen durch Einwirken von Strahlungsenergie/Wärme werden die Atome angeregt (Zustand hält ca Sekunden) Rückkehr in den Grundzustand unter Abgabe von Wärmeenergie oder Strahlung qualitative und quantitative Bestimmung von Metallen und Halbmetallen möglich hohe Selektivität bzw. Spezifität E=E B E A =h = h c Atome absorbieren nur Licht, das ihrem Energiezustand entspricht Übergänge des Valenzelektrons verantwortlich für sichtbare Spektrallinien Rotations- und Schwingungszustände für atomspektrometrische Verfahren unwichtig Atomspektren = Linienspektren 2.2 Atomemissionsspektroskopie (AES) Messung der Atomemission die Temperatur der Flamme muss an das Atom angepasst werden Ionsiation ist unerwünscht, da die Ionen auf einer anderen Wellenlänge emittieren als die Atome 2 Atomisierungseinrichtungen: Flammen-AES Bestimmung von hauptsächlich (Erd)alkalimetallen Emissionsspektroskopie mit Plasmaanregung: da die Elektronendichte hier sehr hoch ist, findet keine Ionisation statt, obwohl die verwendete Temperatur so hoch ist, dass sie es könnte Bestimmung von allen Metallen und Halbmetallen; P, S Nachweisgrenze geringer als bei Flammen-AES Intensität des emittierten Lichtes sollte eine lineare Funktion ihrer Konzentration sein, ist es aber auf Grund von Störungen in der Flamme nicht Kalibrierung notwendig 2.3 Atomabsorptionsspektroskopie (AAS) Messung der Atomabsorption Prinzip: 1. Lösungen von Metallsalzen werden in einer Flamme verdampft 2. durch Einstrahlung von Licht werden die gebildeten Atome angeregt 3. man misst die absorbierte Lichtintensität verfügt im Aufbau im Gegensatz zur AES über eine Strahlungsquelle: Hohlkathodenlampe (HKL): Anlegen eines Stroms an die als Strahlungsquelle verwendete Hohlkathodenlampe Ionisation des Füllgases Kationen des Gases schlagen Atome aus der Oberfläche der Kathode heraus teilweise Anregung der ausgeschlagenen Atome Emittierung des Lichts Ne Ne + Pb * Pb Elektrodenlose Entladungslampe (EDL): Bestimmung von leicht verdampfbaren Elementen, z. B. As, Se, Sb, Na, K, Pb als Strahlungsquelle dient das gleiche Element, das man bestimmen möchte 3
4 man verwendet eine Emissionslinie des selben Elements, das man analysieren will, wodurch man den gleichen Elektrodenübergang anregt Resonanzlinie es gilt das LAMBERT-BEER'sche Gesetz (siehe 3.1.1), wobei c nicht aus A errechnet werden kann und b in der Flamme keine konstante Größe ist Analyse sehr kleiner Mengen möglich: ppm- und ppb-bereich hohe Selektivität Flammen-AAS Spektrale Störungen: Untergrundabsorption: Minderung der Strahlungsintensität der Strahlungsquelle durch Nebeneffekte aus Begleitsubstanzen Untergrundkompensation: Methode zur Ausschaltung der Untergrundabsorption abwechselnde elektronische Erfassung der Absorption eines Linienstrahlers (HKL) und der eines Kontinuumstrahlers (D 2 -Lampe) A(HKL) A(D 2 ) = reine Atomabsorption Überlappung von Atomlinien: Emission anderer Elemente auf annähernd gleicher Wellenlänge wie Analysenlinie Abhilfe: Wechsellicht Emission kommt auch in den Lichtpausen beim Detektor an nicht spektrale Störungen: führen generell zu einer Veränderung der Zahl der Atome im Absorptionsvolumen Verdampfungsinterferenzen: Abhilfe: Zusatz von Abfangreagenzien Gasphaseninterferenzen: vor allem Ionisationsstörungen Abhilfe: Zugabe leicht ionisierbarer Verbindungen (Ionisationspuffer) auf Grund erhöhten Elektronendrucks wird die Gleichgewichtsreaktion zwischen Atom und Ion in der Flamme in Richtung Atom verschoben Transportinterferenzen: physikalische Störungen Abhilfe: Standardadditionsmethode zur Kalibrierung Graphitrohrofen-Technik durch ein bestimmtes Temperaturprogramm werden die Begleitsubstanzen von der Probe abgetrennt Bestimmung von allen Metallen (außer Ce, Th) und den Halbmetallen B und Si Hydrid-Technik selektive Abtrennung bestimmter Substanzen durch Bildung gasförmiger Hydride mit naszierendem H Bestimmung von As, Sb, Se, Sn, Bi, Te Kaltdampf-Technik Bestimmung von Hg durch Einleiten von NaBH 4 -Lösung 4
5 3. Molekülspektroskopie 3.1 UV/Vis-Spektroskopie Grundlagen die Energie des sichtbaren und ultravioletten Lichts (Strahlungsenergie) wird von bestimmten organischen Molekülen teilweise absorbiert und regt π- und n-elektronen an man bestimmt in einem Absorptionsspektrophotometer den durch die Moleküle absorbierten Anteil an eingestrahlter Lichtintensität und registriert ihn in Abhängigkeit von der Wellenlänge in Form des Absorptionsspektrums Elektronenanregung: organische Moleküle enthalten drei Arten von Valenzelektronen: σ Elektronen des Molekülgerüsts π Elektronen der Doppel- und Dreifachbindungen nichtbindende n-elektronenpaare von Sauerstoff-, Schwefel- und Stickstoffatomen diese Elektronen können durch die Energie des Lichts angeregt werden σ σ, π π ; n σ oder n π σ σ braucht viel Energie π π ist leichter anzuregen als σ σ, in konjugierten Systemen ist die benötigte Energie sogar noch kleiner n σ oder n π ist leicht anzuregen Absorption: I A=log 0 10 I [I 0: eingestrahlte Lichtintensität; I: Intensität des austretenden Lichts] LAMBERT-BEER'sches Gesetz: A= c b [A: Absorption; ε(λ): molarer Absorptionskoeffizient; c: Konzentration [mol/l]; b: Schichtdicke [cm]] spezifische Absorption: 1 A % 1cm = Absorption einer Lösung mit 1 %Stoff und b=1cm 1 A % 1cm = A [c: Konzentration [g/100 ml]] c b Chromophor: Teil eines Moleküls, der für die Absorption verantwortlich ist Chromophor Übergang λ max ε C H σ σ 122 nm 10 4 C C σ σ 130 nm 10 4 O n σ z.b. 167 nm für H 2O 2000 C=C π π 165 nm C C π π 173 nm 8000 C=O n π Alkene, Polyene: mit zunehmender Zahl von Doppelbindungen verlängert sich die Wellenlänge (Rotverschiebung bzw. bathochrome Verschiebung), da das HOMO in ein immer höheres und das LUMO in ein immer niedrigeres Energieniveau gelangt, wodurch die Energiedifferenz zwischen den beiden kleiner wird 5
6 ist das System konjugierter Doppelbindungen lang genug, so wird das Absorptionsmaximum bis in den sichtbaren Bereich hinein verschoben Substituenten am chromophoren System verschieben das Absorptionsmaximum ebenfalls in den längerwelligen Bereich Polymethinfarbstoffe: an beiden endständigen Kohlenstoffatomen eines konjugierten Polyens mit ungerader C-Zahl befindet sich jeweils ein Stickstoffatom die beiden Stickstoffatome agieren als Elektronendonator bzw. -akzeptor für das π Elektronensystem starke Verringerung der Anregungsenergie Absorptionsmaximum wird in den sichtbaren Bereich verschoben Substanzen sind farbig Gesättigte Carbonylverbindungen: Anregung des π π Übergangs erfordert so viel Energie, dass das Maximum unterhalb von 200 nm liegt über 200 nm zeigt die Verbindung nur ein dem n π Übergang entsprechendes Maximum Ungesättigte Carbonylverbindungen: durch die Erniedrigung von ΔE (siehe 2.2) sowohl für π π als auch für n π Übergänge, verschieben sich die Maxima in den Bereich um 240nm bzw. 320nm mit zunehmender Zahl an Doppelbindungen kann es zu einer Überdeckung der n π Bande durch die π π Bande kommen, da diese sich schneller verschiebt 3.2 Fluorimetrie Methode der Emissionsspektroskopie, bei der Moleküle durch Licht zur Fluoreszenz gebracht werden die Elektronen befinden sich nach der Anregung in verschiedenen Schwingungsniveaus (v = 0, 1, 2 usw.) der Elektronenanregungszustände S 1, S 2 usw.; normalerweise fallen sie strahlungslos direkt wieder zurück in die Schwingungszustände (v = 0, 1, 2 usw.) des Grundzustandes S 0, bei fluoreszierenden Substanzen fallen jedoch alle Elektronen zunächst strahlungslos in den Schwingungszustand v = 0 des Anregungszustandes S 1 und danach unter Fluoreszenz in die verschiedenen Schwingungszustände (v = 0, 1, 2 usw.) des Grundzustandes S 0 3 Möglichkeiten für die Rückkehr eines Elektronensystems aus dem Anregungszustand in den Grundzustand: 1. Strahlungslose Inaktivierung; nicht wirklich strahlungslos, aber da die Energie in Wärmeenergie (IR-Strahlung) umgewandelt wird, ist sie nicht sichtbar 2. Fluoreszenz durch Umwandlung der Elektronenanregungsenergie in Lichtenergie unter Emission von Fluoreszenzlicht; schneller Vorgang 3. Phosphoreszenz durch strahlungslosen Übergang der Elektronen aus dem Singulett-( ) in den Triplett-( )Zustand und danach unter Lichtemission in den Grundzustand; dauert nach der Anregung noch messbar an STOKES'sche Regel: Absorption Anregung Emission die Anregung der Elektronen erfordert mehr Energie als bei der Fluoreszenz in Form von Strahlungsenergie wieder frei wird das LAMBERT-BEER'sche Gesetz gilt nicht! wenn Absorption stattfindet, kommt es auch immer zu einer Fluoreszenz, die allerdings nicht immer zu sehen ist 6
7 Fluoreszenzintensität: I F = k I 0 c b [Φ k:quantenausbeute (Bruchteil an Anregungslichtenergie, der in Fluoreszenzlicht umgewandelt wird), wenn Φ k >0 Fluoreszenz] I F ~ c Konzentrationsbestimmung möglich I F ~ I 0 Erhöhung der Lichtintensität erhöht die Emission und damit die Intensität des messbaren Lichtes geringere Konzentrationen erfassbar (geringere Bestimmungsgrenze, bessere Nachweisgrenze) Fluoreszenzunterdrücker ( Quencher ): Cl -, OH - Blindwert (BL) = Restfluoreszenz, nachdem der Analyt chemisch so verändert worden ist, dass er nicht mehr fluoresziert Fluoreszenz ist häufig bei starren Molekülen vorzufinden, da bei ihnen der angeregte Zustand am kurzweiligsten ist, z. B.: aromatische Systeme Verbindungen mit konjugierten Doppelbindungen Carbonylverbindungen kondensierte Heterocyclen wie Chinolin, Isochinolin, Indol u. a. Fluorophor = der für die Fluoreszenz verantwortliche Teil des Moleküls Lösungsmittel: dürfen keine Eigenabsorption und keine Eigenfluoreszenz aufweisen müssen photostabil sein unpolare LM werden bevorzugt eingesetzt 3.3 IR-Spektrometrie (IR) Prinzip der IR-Spektroskopie: durch Absorption von Strahlung des infraroten Spektralbereichs werden in Molekülen mechanische Schwingungen der Atome erzeugt (Valenz-, Beuge- und Torsionschwingungen) die Molekülschwingungen bestimmter Atomgruppen sind besonders charakteristisch ausgezeichnete Methode zur Prüfung der Identität von Arzneistoffen quantitative Bestimmung durchführbar, aber auf Grund der schwierigen Auswertungen nur zweite Wahl Frequenz der absorbierten Strahlung im wesentlichen abhängig von der Bindungsstärke und der Masse der schwingenden Atome leichte Atome schwingen mit hohen Frequenzen, schwere mit niedrigerer Frequenz einfach gebundene Atome schwingen langsamer als doppelt gebundene, diese langsamer als dreifach gebundene Voraussetzung: Vorhandensein eines Dipols (z. B. H 2 O) oder die Dipolveränderung als Folge der Schwingung (z. B. CO 2 ) Verwendung von Küvetten aus NaCl, da Quarz und Glas im Messbereich ( cm -1 ) eine starke Eigenabsorption haben Aufnahmetechniken: a) Feststoffpräparation: 1 mg Probe mit 300 mg trockenem (!) KBr fein zerreiben und zu einem Pressling formen (lichtdurchlässig) gut aufgelöste Banden keine Störsignale des LMs b) Flüssigkeiten: 1 Tropfen der Flüssigkeit wird zwischen zwei NaCl-Plättchen als dünner Film verteilt echte Lösungen (Konzentration 5-10%) schwieriger zu vermessen, da die 7
8 Eigenabsorption des Lösungsmittels kompensiert werden muss die meisten Lösungsmittel stören in den wichtigen Bereichen a) besser Auswertung: Vergleich des Spektrums des untersuchten Stoffes mit einer Referenzsubstanz (CRS) 2 Substanzen sind identisch, wenn ihre Signale bei der selben Wellenzahl liegen die relative Intensität der Signale übereinstimmt von besonderer Bedeutung ist der Fingerprint -Bereich ( cm -1 ) stimmen die Spektren nicht überein, kann die Identität sicher ausgeschlossen werden cm -1 = Valenzschwingungsbereich cm -1 = einziger Bereich, in dem H erfasst wir, ein in diesem Bereich auftretendes Signal kann nur von H kommen cm.1 = Fingerprint -Bereich; Deformationsschwingungen N N und O=O sind IR-inaktiv, da kein Dipol vorliegt; würden in den Messungen stören, da sie in der Luft enthalten sind OH-Gruppen haben ein breites Erscheinungsbild, da sie Wasserstoffbrückenbindungen ausbilden IR für leicht flüchtige Stoffe ungeeignet 3.4 Nahinfrarot-Spektrometrie (NIR) im NIR-Bereich liegt v zwischen und 4000 cm -1 (entsprechend 800 bis 2500 nm) nahe am sichtbaren Bereich es wirken höhere Energiebeträge auf die Moleküle ein als im MIR-Bereich es werden hauptsächlich schwerer anregbare Oberschwingungen der X H-Valenzgrundschwingungen zwischen cm -1 beobachtet Messung durch diffuse Reflexion (Reflexion in alle Richtungen gleich): R ' = R Probe R Standard Au Lösungsmittel muss H frei sein, z. B. CCl 4, CS 2, C 2 F 6 Vorteil: konkurrenzlos zeitsparende Methode konkurrenzlos günstige Methode Nachteil: relativ hoher Kalibrationsaufwand 4. Polarimetrie Licht ist als elektromagnetische Welle eine Transversalwelle, d. h. der elektrische Feldvektor ( Lichtvektor ) schwingt in einer Ebene senkrecht zur Fortpflanzungsrichtung im Allgemeinen ist keine Richtung bevorzugt nicht polarisiert durch Polarisatoren kann Licht ausgesondert werden, dessen Lichtvektor in nur einer Richtung schwingt linear polarisiert beim Durchgang von linear polarisiertem Licht durch sog. optisch aktive Körper wird die durch den elektrischen Feldvektor und die Ausbreitungsrichtung festgelegte Schwingungsebene des Lichtes gedreht Zuckerlösungen (aus natürlich gewonnenem Zucker) sind optisch aktiv: zeigen Mutarotation (Wert für die optische Drehung stellt sich erst langsam ein), 8
9 NH 3 verhindert dies lineare Polarisation entsteht durch die Überlagerung von rechts und links polarisierten Lichtes verantwortlich für die Drehung ist das asymmetrische Kohlenstoffatom spezifische Drehung: 20 { } D = 100 l c [α: experimentell ermittelter Drehwinkel; c: Konz. in [g/100 ml]; l: Schichtdicke in [dm]] bei Zuckern konzentrationsunabhängig Gehaltsbestimmung möglich bei vielen optisch aktiven Verbindungen ist die spezifische Drehung konzentrationsabhängig, bei einigen tritt sogar Inversion ein der Drehwinkel α ist abhängig von: der Wellenlänge je kürzer λ, desto größer wird α der Konzentration je kleiner c, desto kleiner wird α der Temperatur mit steigender Temperatur sinkt α (Flüssigkeit dehnt sich mit steigender T aus Konzentration sinkt α wird kleiner) dem Lösungsmittel; Messwerte aus Messungen mit unterschiedlichen Lösungsmitteln können nicht verglichen werden NICOL'sches Prisma: ein unpolarisierter Lichtstrahl, der auf das Prisma aus Kalkspat (CaCO 3 ) fällt, wird in zwei Strahlen geteilt, den ordentlichen Strahl, der relativ stark gebrochen wird außerordentlichen Strahl, der schwächer gebrochen wird beide Strahlen sind senkrecht zueinander polarisiert und haben die gleiche Intensität (beide Intensitäten zusammen ergeben die einfallende Intensität) der ordentliche Strahl wird durch die Totalreflexion entfernt der außerordentliche Strahl wird zur Messung verwendet 5. 1 H-NMR-Spektroskopie NMR = nuclear magnetic resonance (Kernresonanz-Spektroskopie) Verhalten von Atomkernen in Magnetfeldern H-Kern dreht sich um seine Längsachse; durch das Einbringen in ein magnetisches Feld erhält er einen Anstoß, der zusätzlich zu einer torkelnden Bewegung (Präzessionsbewegung) führt 2 Arten von H-Kernen im Molekül auf Grund der unterschiedlichen Orientierungen des Spins im magnetischen Feld (Kern-Zeeman-Niveaus): energieärmere (parallele Anordnung) und energiereichere; die energieärmeren H-Kerne können durch Einwirken elektromagnetischer Strahlung in den energiereicheren Zustand gehoben werden, die anschließende Rückkehr in den energieärmeren Zustand geschieht unter Energieabgabe (Relaxation), die messtechnisch ermittelt werden kann die Kerne nehmen die Energie nur auf, wenn diese groß genug ist, um sie in den energiereicheren Zustand zu heben NMR-aktiv sind nur Atome, bei denen Ordnungs- und Massenzahl nicht gleichzeitig gerade sind (g/g), g/u, u/g und u/u sind aktiv günstige Voraussetzungen für NMR: hohe natürliche Häufigkeit Spinquantenzahl = ½ hohes magnetisches Moment 9
10 die relative Entfernung eines Signals der Substanz vom Signal eines Standards bezeichnet man als chemische Verschiebung: Substanz TMS ppm = 10 6 Gerät Beeinflussung der chemischen Verschiebung: links rechts hohe Frequenz entschirmt niedrige e - -Dichte niedrige Feldstärke niedrige Frequenz abgeschirmt hohe e - -Dichte höhere Feldstärke elektronenziehender Rest elektronenschiebender Rest Kopplungskonstante J: Abstand der Aufspaltungslinien eines Signals geräteunabhängig J der Kopplungspartner ist identisch Integrale: die Fläche unter den Signalen ist proportional zu der Anzahl der sie erzeugenden Kerne 6. Massenspektrometrie (MS) 6.1 Prinzip Moleküle werden in positive oder negative Ionen überführt (Ionisation) instabile Moleküle Ionen zerfallen danach in geladene und ungeladene Bruchstücke (Fragmentierung) die geladenen Bruchstücke werden nach ihrer Masse getrennt (Massen-Fokussierung) Darstellung der Massen und relativen Intensitäten in einem Massenspektrum, Auftragen des Masse-Ladungsverhältnis m/z gegen die relative Intensität, das Signal mit der größten Massenzahl entspricht in 80 90% aller Substanzen der relativen Molmasse sehr kleine Mengen bestimmbar: 0,5 mg bis 10 µg, bei Kopplung mit GC oder HPLC sogar nur ca. 1µg bis 0,5 pg hohe Substanzspezifität 6.2 Klassische Ionisationsmethoden Elektronenstoß-Ionisation (EI) Beschuss der Moleküle mit e - : 1. M + e - M + 2e - ein Elektron wird aus dem Molekül herausgeschlagen oder 2. M + e - M - ein Elektron wird aufgenommen die Radikalanionenbildung ist wesentlich seltener Fragmentierungsmechanismus [siehe Rücker S. 307] da Moleküle meist nur an bestimmten Stellen gespalten werden können, erhält man für jede Substanz ein charakteristisches Massenspektrum 10
11 6.2.2 Chemische Ionisation (CI) Probe wird mit einem großen Überschuss eines Reaktand-Gases, z. B. Methan in den EI gebracht zuerst ionisiert das Gas; die Methanionen übertragen dann durch Zusammenstöße mit nicht ionisierten Methanmolekülen Protonen auf selbige die gebildeten CH 5+ -Kationen übertragen Protonen auf die Probemoleküle: + CH 5 + M MH + + CH 4 die MH + fragmentieren und können dann im Spektrum dargestellt werden 6.3 Schonende Ionisation Elektrospray-Ionisation (ESI) Probeaerosol wird mit N 2 begast und in ein Spannungsfeld gebracht durch Verdampfen des LMs schrumpfen die Tröpfchen die Oberfläche wird für die Partialladung zu klein Explosion der Kügelchen Ionen werden freigesetzt Matrix-unterstützte-Laser-Desorption (MALDI) die Probe wird mit einer Matrix im Verhältnis 1: gemischt und auf ein Target gebracht man bestrahlt die Matrix mit Laserstrahlung Matrixsubstanzbestandteile der Oberfläche werden angeregt Übertragung von Protonen auf die Probe oder umgekehrt Ionen werden frei Probe-Matrix-Würfel auf Jahre beständig 6.4 Analysator Quadrupol-Analysator Ionenstrahl der Analysensubstanz wird in Längsrichtung zwischen vier parallel angeordnete Metallstäbe geleitet durch bestimmte Arten der Anlegung von Spannung, können nur Ionen einer bestimmten Masse hindurch Flugzeit-Analysator durch Messung der Flugzeit t eines Teilchens auf einer feldfreien Flugstrecke kann dessen Masse m berechnet werden leichte Teilchen erreichen den Detektor eher als schwere 11
Atomabsorptionsspektroskopie (AAS)
 Atomabsorptionsspektroskopie (AAS) 11.06.2012 1 Übersicht der spektrosk. Methoden Atomspektroskopie Atomemissionsspektroskopie (Flammenphotometrie) Spektralanalyse Emissionsspektroskopie Absorptionsspektroskopie
Atomabsorptionsspektroskopie (AAS) 11.06.2012 1 Übersicht der spektrosk. Methoden Atomspektroskopie Atomemissionsspektroskopie (Flammenphotometrie) Spektralanalyse Emissionsspektroskopie Absorptionsspektroskopie
Wechselwirkung zwischen Licht und chemischen Verbindungen
 Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Spektroskopie-Seminar SS UV-Vis-Spektroskopie. UV-Vis-Spektroskopie
 UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
Polarisationsapparat
 1 Polarisationsapparat Licht ist eine transversale elektromagnetische Welle, d.h. es verändert die Länge der Vektoren des elektrischen und magnetischen Feldes. Das elektrische und magnetische Feld ist
1 Polarisationsapparat Licht ist eine transversale elektromagnetische Welle, d.h. es verändert die Länge der Vektoren des elektrischen und magnetischen Feldes. Das elektrische und magnetische Feld ist
Massenspektrometrie (MS)
 Massenspektrometrie (MS) Die Massenspektrometrie ist unter den heute routinemäßig verwendeten Methoden die jüngste, denn ihre Anwendung begann erst um 1960. Seit den Arbeiten von BIEMANN über Fragmentierungsmuster
Massenspektrometrie (MS) Die Massenspektrometrie ist unter den heute routinemäßig verwendeten Methoden die jüngste, denn ihre Anwendung begann erst um 1960. Seit den Arbeiten von BIEMANN über Fragmentierungsmuster
Strukturaufklärung (BSc-Chemie): Einführung
 Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Lernziele zu Farbigkeit von Stoffen
 Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Massenspektrometrie (MS)
 Massenspektrometrie (MS) Die Massenspektrometrie ist unter den heute routinemäßig verwendeten Methoden die jüngste, denn ihre Anwendung begann erst um 1960. Seit den Arbeiten von BIEMANN über Fragmentierungsmuster
Massenspektrometrie (MS) Die Massenspektrometrie ist unter den heute routinemäßig verwendeten Methoden die jüngste, denn ihre Anwendung begann erst um 1960. Seit den Arbeiten von BIEMANN über Fragmentierungsmuster
Farbstoffe Einleitung
 Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Versuch Fluoreszenz-Quenching
 Versuch Fluoreszenz-Quenching Zielstellung: 1.) Aufnahme des UV-Vis-Spektrums eines Fluoreszenzfarbstoffes 2.) Aufnahme der Kennlinie des verwendeten Photon-Counting-Moduls (PCM) im Bereich von 1,9 2,9
Versuch Fluoreszenz-Quenching Zielstellung: 1.) Aufnahme des UV-Vis-Spektrums eines Fluoreszenzfarbstoffes 2.) Aufnahme der Kennlinie des verwendeten Photon-Counting-Moduls (PCM) im Bereich von 1,9 2,9
Praktikum II PO: Doppelbrechung und eliptisch polatisiertes Licht
 Praktikum II PO: Doppelbrechung und eliptisch polatisiertes Licht Betreuer: Norbert Lages Hanno Rein praktikum2@hanno-rein.de Florian Jessen florian.jessen@student.uni-tuebingen.de 26. April 2004 Made
Praktikum II PO: Doppelbrechung und eliptisch polatisiertes Licht Betreuer: Norbert Lages Hanno Rein praktikum2@hanno-rein.de Florian Jessen florian.jessen@student.uni-tuebingen.de 26. April 2004 Made
Polarisation und optische Aktivität
 Polarisation und optische Aktivität 1 Entstehung polarisiertes Licht Streuung und Brechung einer Lichtwelle Reflexion einer Lichtwelle Emission durch eine polarisierte Quelle z.b. einen schwingenden Dipol
Polarisation und optische Aktivität 1 Entstehung polarisiertes Licht Streuung und Brechung einer Lichtwelle Reflexion einer Lichtwelle Emission durch eine polarisierte Quelle z.b. einen schwingenden Dipol
Physik für Maschinenbau. Prof. Dr. Stefan Schael RWTH Aachen
 Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
Ausbreitung von elektromagnetischer Strahlung
 Ausbreitung von elektromagnetischer Strahlung E! B Der elektrische Feldvektor und der magnetische Feldvektor stehen senkrecht aufeinander Die elektromagentische Welle ist beschrieben durch x x E = E 0
Ausbreitung von elektromagnetischer Strahlung E! B Der elektrische Feldvektor und der magnetische Feldvektor stehen senkrecht aufeinander Die elektromagentische Welle ist beschrieben durch x x E = E 0
NMR Spektroskopie. 1nm Frequenz X-ray UV/VIS Infrared Microwave Radio
 NMR Spektroskopie 1nm 10 10 2 10 3 10 4 10 5 10 6 10 7 Frequenz X-ray UV/VIS Infrared Microwave Radio Anregungsmodus electronic Vibration Rotation Nuclear Spektroskopie X-ray UV/VIS Infrared/Raman NMR
NMR Spektroskopie 1nm 10 10 2 10 3 10 4 10 5 10 6 10 7 Frequenz X-ray UV/VIS Infrared Microwave Radio Anregungsmodus electronic Vibration Rotation Nuclear Spektroskopie X-ray UV/VIS Infrared/Raman NMR
Wie Heavy Metal ist der Boden?
 Wie Heavy Metal ist der Boden? Inhaltsverzeichnis 1. Entstehung und Ausbreitung von Schwermetallen im Boden 2. Analytische Aufschlussverfahren 3. Grundlagen der UV-VIS- und AAS-Spektroskopie 2 Schwermetalle
Wie Heavy Metal ist der Boden? Inhaltsverzeichnis 1. Entstehung und Ausbreitung von Schwermetallen im Boden 2. Analytische Aufschlussverfahren 3. Grundlagen der UV-VIS- und AAS-Spektroskopie 2 Schwermetalle
Atomabsorptionsspektrometrie (AAS)
 Atomabsorptionsspektrometrie (AAS) Zusammenfassung Mit Hilfe eines Atomabsorptionsspektrometers wurden die Konzentrationen von Arsen und Lithium in drei verschieden Mineralwässern bestimmt. Resultate Konzentrationen
Atomabsorptionsspektrometrie (AAS) Zusammenfassung Mit Hilfe eines Atomabsorptionsspektrometers wurden die Konzentrationen von Arsen und Lithium in drei verschieden Mineralwässern bestimmt. Resultate Konzentrationen
5. Elektronen- und Rotations- Spektren von Molekülen
 5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
Grundlagen der Quantentheorie
 Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Protokoll. Kombinierte Anwendung verschiedener Spektroskopischer Methoden
 Protokoll Kombinierte Anwendung verschiedener Spektroskopischer Methoden Zielstellung: Durch die Auswertung von IR-, Raman-, MR-, UV-VIS- und Massenspektren soll die Struktur einer unbekannten Substanz
Protokoll Kombinierte Anwendung verschiedener Spektroskopischer Methoden Zielstellung: Durch die Auswertung von IR-, Raman-, MR-, UV-VIS- und Massenspektren soll die Struktur einer unbekannten Substanz
UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie
 Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Reminder: MO-Diagramm von O 2 2- MdS-1 UV/Vis-Spektroskopie
Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Reminder: MO-Diagramm von O 2 2- MdS-1 UV/Vis-Spektroskopie
Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: Die Essentials der letzten Vorlesung Funktionelle Gruppen
Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: Die Essentials der letzten Vorlesung Funktionelle Gruppen
Spektroskopie-Seminar SS Infrarot-Spektroskopie. Infrarot-Spektroskopie
 Infrarot-Spektroskopie 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden die absorbierten
Infrarot-Spektroskopie 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden die absorbierten
Spektroskopie-Seminar WS 17/18 3 Infrarot-Spektroskopie. Infrarot-Spektroskopie
 WS 17/18 Infrarot-Spektroskopie 1 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden
WS 17/18 Infrarot-Spektroskopie 1 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden
Einführung in die Schwingungsspektroskopie
 Einführung in die Schwingungsspektroskopie Quelle: Frederik Uibel und Andreas Maurer, Uni Tübingen 2004 Molekülbewegungen Translation: Rotation: Die Bewegung des gesamten Moleküls ls in die drei Raumrichtungen.
Einführung in die Schwingungsspektroskopie Quelle: Frederik Uibel und Andreas Maurer, Uni Tübingen 2004 Molekülbewegungen Translation: Rotation: Die Bewegung des gesamten Moleküls ls in die drei Raumrichtungen.
Photom etrieren Photometrie Fraunhofer sche Linien
 17 Photometrieren Die Spektroskopie, auch Spektralphotometrie, Spektrophotometrie oder einfach nur Photometrie genannt, umfasst eine Anzahl experimenteller Messverfahren, die generell die Wechselwirkung
17 Photometrieren Die Spektroskopie, auch Spektralphotometrie, Spektrophotometrie oder einfach nur Photometrie genannt, umfasst eine Anzahl experimenteller Messverfahren, die generell die Wechselwirkung
Zentralabstand b, Spaltbreite a. Dreifachspalt Zentralabstand b, Spaltbreite a. Beugungsgitter (N Spalte, N<10 4, Abstand a)
 Doppelspalt (ideal) Doppelspalt (real) Zentralabstand b, Spaltbreite a Dreifachspalt Zentralabstand b, Spaltbreite a Beugungsgitter (N Spalte, N
Doppelspalt (ideal) Doppelspalt (real) Zentralabstand b, Spaltbreite a Dreifachspalt Zentralabstand b, Spaltbreite a Beugungsgitter (N Spalte, N
9. GV: Atom- und Molekülspektren
 Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG
 ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG Atomabsorptionsspektrometrie (AAS) Chr. Janiak Vorlesung Analytische Chemie I, SS 2004 Prinzip Atomemissionsspektrometrie (AES) Erinnerung: (opt.) AES/OES: Probe Atom*
ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG Atomabsorptionsspektrometrie (AAS) Chr. Janiak Vorlesung Analytische Chemie I, SS 2004 Prinzip Atomemissionsspektrometrie (AES) Erinnerung: (opt.) AES/OES: Probe Atom*
Quantenphysik in der Sekundarstufe I
 Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
Praktikum SC Optische Aktivität und Saccharimetrie
 Praktikum SC Optische Aktivität und Saccharimetrie Hanno Rein, Florian Jessen betreut durch Gunnar Ritt 19. Januar 2004 1 Vorwort In den meiste Fällen setzt man bei verschiedensten Rechnungen stillschweigend
Praktikum SC Optische Aktivität und Saccharimetrie Hanno Rein, Florian Jessen betreut durch Gunnar Ritt 19. Januar 2004 1 Vorwort In den meiste Fällen setzt man bei verschiedensten Rechnungen stillschweigend
Polarisation durch Reflexion
 Version: 27. Juli 2004 Polarisation durch Reflexion Stichworte Erzeugung von polarisiertem Licht, linear, zirkular und elliptisch polarisiertes Licht, Polarisator, Analysator, Polarisationsebene, optische
Version: 27. Juli 2004 Polarisation durch Reflexion Stichworte Erzeugung von polarisiertem Licht, linear, zirkular und elliptisch polarisiertes Licht, Polarisator, Analysator, Polarisationsebene, optische
6.2.2 Mikrowellen. M.Brennscheidt
 6.2.2 Mikrowellen Im vorangegangen Kapitel wurde die Erzeugung von elektromagnetischen Wellen, wie sie im Rundfunk verwendet werden, mit Hilfe eines Hertzschen Dipols erklärt. Da Radiowellen eine relativ
6.2.2 Mikrowellen Im vorangegangen Kapitel wurde die Erzeugung von elektromagnetischen Wellen, wie sie im Rundfunk verwendet werden, mit Hilfe eines Hertzschen Dipols erklärt. Da Radiowellen eine relativ
Radiologie Modul I. Teil 1 Grundlagen Röntgen
 Radiologie Modul I Teil 1 Grundlagen Röntgen Teil 1 Inhalt Physikalische Grundlagen Röntgen Strahlenbiologie Technische Grundlagen Röntgen ROENTGENTECHNIK STRAHLENPHYSIK GRUNDLAGEN RADIOLOGIE STRAHLENBIOLOGIE
Radiologie Modul I Teil 1 Grundlagen Röntgen Teil 1 Inhalt Physikalische Grundlagen Röntgen Strahlenbiologie Technische Grundlagen Röntgen ROENTGENTECHNIK STRAHLENPHYSIK GRUNDLAGEN RADIOLOGIE STRAHLENBIOLOGIE
III. Strukturbestimmung organischer Moleküle
 III. Strukturbestimmung organischer Moleküle Röntgenstrukturbestimmung g Spektroskopie UV-VIS IR NMR Massenspektrometrie (MS) Röntgenstruktur eines bakteriellen Kohlenhydrats O O O O O O O C3 Röntgenstruktur
III. Strukturbestimmung organischer Moleküle Röntgenstrukturbestimmung g Spektroskopie UV-VIS IR NMR Massenspektrometrie (MS) Röntgenstruktur eines bakteriellen Kohlenhydrats O O O O O O O C3 Röntgenstruktur
Kontrollaufgaben zur Optik
 Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Chemisches Grundpraktikum II (270002) Kernresonanzspektroskopie. NMR-Spektroskopie
 hemisches Grundpraktikum II (270002) Kernresonanzspektroskopie NMR-Spektroskopie (Nuclear Magnetic Resonance). Kählig, SS 2010 Von der Substanz zur Struktur Substanz NMR - Spektren Struktur N N 1 Spektroskopie
hemisches Grundpraktikum II (270002) Kernresonanzspektroskopie NMR-Spektroskopie (Nuclear Magnetic Resonance). Kählig, SS 2010 Von der Substanz zur Struktur Substanz NMR - Spektren Struktur N N 1 Spektroskopie
7. Das Bohrsche Modell des Wasserstoff-Atoms. 7.1 Stabile Elektronbahnen im Atom
 phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
SCHWEIZER JUGEND FORSCHT. Chemie und Materialwissenschaften
 SCHWEIZER JUGEND FORSCHT Chemie und Materialwissenschaften Studie einer ultraschnellen Fotochemischen Reaktion mit Laserspektroskopie Gianluca Schmoll Widmer Betreuer: Dr. Sandra Mosquera Vazquez, Dr.
SCHWEIZER JUGEND FORSCHT Chemie und Materialwissenschaften Studie einer ultraschnellen Fotochemischen Reaktion mit Laserspektroskopie Gianluca Schmoll Widmer Betreuer: Dr. Sandra Mosquera Vazquez, Dr.
Atomabsorptionsspektrometrie Atomemissionsspektrometrie. Atomspektrometrie
 Atomabsorptionsspektrometrie Atomemissionsspektrometrie Nachweis-/Bestimmungsgrenze Atomspektrometrie Quantitative und qualitative Methode für die Bestimmung von mehr als 70 Elementen (z.b. Fe, Mn, Zn,
Atomabsorptionsspektrometrie Atomemissionsspektrometrie Nachweis-/Bestimmungsgrenze Atomspektrometrie Quantitative und qualitative Methode für die Bestimmung von mehr als 70 Elementen (z.b. Fe, Mn, Zn,
NG Brechzahl von Glas
 NG Brechzahl von Glas Blockpraktikum Frühjahr 2007 25. April 2007 Inhaltsverzeichnis 1 Einführung 2 2 Theoretische Grundlagen 2 2.1 Geometrische Optik und Wellenoptik.......... 2 2.2 Linear polarisiertes
NG Brechzahl von Glas Blockpraktikum Frühjahr 2007 25. April 2007 Inhaltsverzeichnis 1 Einführung 2 2 Theoretische Grundlagen 2 2.1 Geometrische Optik und Wellenoptik.......... 2 2.2 Linear polarisiertes
 Die Lage der Emissionsbanden der charakteristischen Röntgenstrahlung (anderer Name: Eigenstrahlung) wird bestimmt durch durch das Material der Kathode durch das Material der Anode die Größe der Anodenspannung
Die Lage der Emissionsbanden der charakteristischen Röntgenstrahlung (anderer Name: Eigenstrahlung) wird bestimmt durch durch das Material der Kathode durch das Material der Anode die Größe der Anodenspannung
Spektroskopie. im IR- und UV/VIS-Bereich. Proben, Probengefässe, Probenvorbereitung.
 Spektroskopie im IR- und UV/VIS-Bereich Proben, Probengefässe, Probenvorbereitung Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Allgemeiner Aufbau eines Spektrometers d
Spektroskopie im IR- und UV/VIS-Bereich Proben, Probengefässe, Probenvorbereitung Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Allgemeiner Aufbau eines Spektrometers d
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
Teil 4 Massenspektrometrie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Teil 4 Massenspektrometrie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick auf die letzte Vorlesung Grundprinzip der MS: Trennung nach Ladung und Masse
Teil 4 Massenspektrometrie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick auf die letzte Vorlesung Grundprinzip der MS: Trennung nach Ladung und Masse
Vorlesung Physik für Pharmazeuten PPh Optik
 Vorlesung Physik für Pharmazeuten PPh - 10 Optik 02.07.2007 Wiederholung : Strom und Magnetismus B = µ 0 N I l Ampère'sche Gesetz Uind = d ( BA) dt Faraday'sche Induktionsgesetz v F L = Q v v ( B) Lorentzkraft
Vorlesung Physik für Pharmazeuten PPh - 10 Optik 02.07.2007 Wiederholung : Strom und Magnetismus B = µ 0 N I l Ampère'sche Gesetz Uind = d ( BA) dt Faraday'sche Induktionsgesetz v F L = Q v v ( B) Lorentzkraft
Elektromagnetische Strahlung
 Elektromagnetische Strahlung 1 Absorptionsmethoden - Grundlagen Als Absorptionsmethoden bezeichnet man die Konzentrationsbestimmung einer Substanz, indem gemessen wird, wie sie die Intensität elektromagnetischer
Elektromagnetische Strahlung 1 Absorptionsmethoden - Grundlagen Als Absorptionsmethoden bezeichnet man die Konzentrationsbestimmung einer Substanz, indem gemessen wird, wie sie die Intensität elektromagnetischer
Polarisation des Lichtes
 Polarisation des Lichtes Licht = transversal schwingende el.-magn. Welle Polarisationsrichtung: Richtung des el. Feldvektors Polarisationsarten: unpolarisiert: keine Raumrichtung bevorzugt (z.b. Glühbirne)
Polarisation des Lichtes Licht = transversal schwingende el.-magn. Welle Polarisationsrichtung: Richtung des el. Feldvektors Polarisationsarten: unpolarisiert: keine Raumrichtung bevorzugt (z.b. Glühbirne)
Optische Spektroskopie mit Lasern: Grundlagen und Anwendungen. Wann: Mi Fr Wo: P1 - O1-306
 Laserspektroskopie Was: Optische Spektroskopie mit Lasern: Grundlagen und Anwendungen Wann: Mi 13 15-14 00 Fr 10 15-12 00 Wo: P1 - O1-306 Wer: Dieter Suter Raum P1-O1-216 Tel. 3512 Dieter.Suter@uni-dortmund.de
Laserspektroskopie Was: Optische Spektroskopie mit Lasern: Grundlagen und Anwendungen Wann: Mi 13 15-14 00 Fr 10 15-12 00 Wo: P1 - O1-306 Wer: Dieter Suter Raum P1-O1-216 Tel. 3512 Dieter.Suter@uni-dortmund.de
GRUNDLAGEN DER SPEKTROPHOTOMETRIE
 11 GRUNDLAGEN DER SPEKTROPHOTOMETRE Materie erscheint uns farbig, wenn sie aus dem einfallenden weißen Licht einen bestimmten spektralen Teil absorbiert. Als Farbe nehmen wir den reflektierten Anteil des
11 GRUNDLAGEN DER SPEKTROPHOTOMETRE Materie erscheint uns farbig, wenn sie aus dem einfallenden weißen Licht einen bestimmten spektralen Teil absorbiert. Als Farbe nehmen wir den reflektierten Anteil des
Vorlesung Messtechnik 2. Hälfte des Semesters Dr. H. Chaves
 Vorlesung Messtechnik 2. Hälfte des Semesters Dr. H. Chaves 1. Einleitung 2. Optische Grundbegriffe 3. Optische Meßverfahren 3.1 Grundlagen dρ 3.2 Interferometrie, ρ(x,y), dx (x,y) 3.3 Laser-Doppler-Velozimetrie
Vorlesung Messtechnik 2. Hälfte des Semesters Dr. H. Chaves 1. Einleitung 2. Optische Grundbegriffe 3. Optische Meßverfahren 3.1 Grundlagen dρ 3.2 Interferometrie, ρ(x,y), dx (x,y) 3.3 Laser-Doppler-Velozimetrie
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
Übungen Atom- und Molekülphysik für Physiklehrer (Teil 2)
 Übungen Atom- und Molekülphysik für Physiklehrer (Teil ) Aufgabe 38) Welche J-Werte sind bei den Termen S, P, 4 P und 5 D möglich? Aufgabe 39) Welche Werte kann der Gesamtdrehimpuls eines f-elektrons im
Übungen Atom- und Molekülphysik für Physiklehrer (Teil ) Aufgabe 38) Welche J-Werte sind bei den Termen S, P, 4 P und 5 D möglich? Aufgabe 39) Welche Werte kann der Gesamtdrehimpuls eines f-elektrons im
Ferienkurs Experimentalphysik 3
 Ferienkurs Experimentalphysik 3 Musterlösung Montag 14. März 2011 1 Maxwell Wir bilden die Rotation der Magnetischen Wirbelbleichung mit j = 0: ( B) = +µµ 0 ɛɛ 0 ( E) t und verwenden wieder die Vektoridenditäet
Ferienkurs Experimentalphysik 3 Musterlösung Montag 14. März 2011 1 Maxwell Wir bilden die Rotation der Magnetischen Wirbelbleichung mit j = 0: ( B) = +µµ 0 ɛɛ 0 ( E) t und verwenden wieder die Vektoridenditäet
Primärstruktur Proteinsequenzierung
 Proteinanalytik II Primärstruktur Proteinsequenzierung Hydrolyse der Peptidbindung Aminosäurenachweis Ninhydrin Aminosäurenachweis Fluorescamin Proteinhydrolysat Ionenaustauschchromatographie Polypeptidstruktur
Proteinanalytik II Primärstruktur Proteinsequenzierung Hydrolyse der Peptidbindung Aminosäurenachweis Ninhydrin Aminosäurenachweis Fluorescamin Proteinhydrolysat Ionenaustauschchromatographie Polypeptidstruktur
Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ
 Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ Viele Kerne besitzen einen Spindrehimpuls. Ein Kern mit der Spinquantenzahl I hat einen Drehimpuls (L)
Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ Viele Kerne besitzen einen Spindrehimpuls. Ein Kern mit der Spinquantenzahl I hat einen Drehimpuls (L)
5 Elektronenübergänge im Festkörper
 5 Elektronenübergänge im Festkörper 5.1 Übersicht und Lernziele Übersicht Die Bindung in einem Molekül erfolgt durch gemeinsame Elektronenpaare, die jeweils zwei Atomen angehören (Atombindung, Elektronenpaarbindung).
5 Elektronenübergänge im Festkörper 5.1 Übersicht und Lernziele Übersicht Die Bindung in einem Molekül erfolgt durch gemeinsame Elektronenpaare, die jeweils zwei Atomen angehören (Atombindung, Elektronenpaarbindung).
Protokoll: Infrarotspektroskopie
 Protokoll: Infrarotspektroskopie Durchführung und Beobachtung 1. Backgroundmessung im leeren Gerät Man erkennt, dass das Gerät ausreichend mit getrockneter Luft gespült wurde. Durch die Backgroundmessung
Protokoll: Infrarotspektroskopie Durchführung und Beobachtung 1. Backgroundmessung im leeren Gerät Man erkennt, dass das Gerät ausreichend mit getrockneter Luft gespült wurde. Durch die Backgroundmessung
Optische Eigenschaften fester Stoffe. Licht im neuen Licht Dez 2015
 Licht und Materie Optische Eigenschaften fester Stoffe Matthias Laukenmann Den Lernenden muss bereits bekannt sein: Zahlreiche Phänomene lassen sich erklären, wenn man annimmt, dass die von Atomen quantisiert
Licht und Materie Optische Eigenschaften fester Stoffe Matthias Laukenmann Den Lernenden muss bereits bekannt sein: Zahlreiche Phänomene lassen sich erklären, wenn man annimmt, dass die von Atomen quantisiert
Periodensystem, elektromagnetische Spektren, Atombau, Orbitale
 Periodensystem, elektromagnetische Spektren, Atombau, Orbitale Als Mendelejew sein Periodensystem aufstellte waren die Edelgase sowie einige andere Elemente noch nicht entdeck (gelb unterlegt). Trotzdem
Periodensystem, elektromagnetische Spektren, Atombau, Orbitale Als Mendelejew sein Periodensystem aufstellte waren die Edelgase sowie einige andere Elemente noch nicht entdeck (gelb unterlegt). Trotzdem
SPEKTRALANALYSE. entwickelt um 1860 von: GUSTAV ROBERT KIRCHHOFF ( ; dt. Physiker) + ROBERT WILHELM BUNSEN ( ; dt.
 SPEKTRALANALYSE = Gruppe von Untersuchungsmethoden, bei denen das Energiespektrum einer Probe untersucht wird. Man kann daraus schließen, welche Stoffe am Zustandekommen des Spektrums beteiligt waren.
SPEKTRALANALYSE = Gruppe von Untersuchungsmethoden, bei denen das Energiespektrum einer Probe untersucht wird. Man kann daraus schließen, welche Stoffe am Zustandekommen des Spektrums beteiligt waren.
Zusammenhang zwischen Farbe, Wellenlänge, Frequenz und Energie des sichtbaren Spektrums
 Zusammenhang zwischen Farbe, Wellenlänge, Frequenz und Energie des sichtbaren Spektrums Farbe, die das menschliche Auge empfindet Wellenlänge [10-9 m] Frequenz [10 14 Hz] Energie [kj/ 1 mol Photonen] Rot
Zusammenhang zwischen Farbe, Wellenlänge, Frequenz und Energie des sichtbaren Spektrums Farbe, die das menschliche Auge empfindet Wellenlänge [10-9 m] Frequenz [10 14 Hz] Energie [kj/ 1 mol Photonen] Rot
Methodische Ansätze zur Strukturaufklärung: Rnt. - Kernmagnetische Resonanzspektroskopie (NMR)
 ? Methodische Ansäte ur Strukturaufklärung: - Rastersondenmikroskopie (AFM, SPM) SPM - Röntgenbeugung Rnt. - Elektronenspektroskopie (UV-vis) UV-vis - Schwingungsspektroskopie (IR) IR - Massenspektroskopie
? Methodische Ansäte ur Strukturaufklärung: - Rastersondenmikroskopie (AFM, SPM) SPM - Röntgenbeugung Rnt. - Elektronenspektroskopie (UV-vis) UV-vis - Schwingungsspektroskopie (IR) IR - Massenspektroskopie
Äußerer lichtelektrischer Effekt
 Grundexperiment 1 UV-Licht Video: 301-1 Grundexperiment 2 UV-Licht Grundexperiment 3 Rotes Licht Video: 301-2 Grundexperiment 3 UV-Licht Glasplatte Video: 301-2 Herauslösung von Elektronen aus Metallplatte
Grundexperiment 1 UV-Licht Video: 301-1 Grundexperiment 2 UV-Licht Grundexperiment 3 Rotes Licht Video: 301-2 Grundexperiment 3 UV-Licht Glasplatte Video: 301-2 Herauslösung von Elektronen aus Metallplatte
Die Natriumlinie. und Absorption, Emission, Dispersion, Spektren, Resonanz Fluoreszenz, Lumineszenz
 Die Natriumlinie und Absorption, Emission, Dispersion, Spektren, Resonanz Fluoreszenz, Lumineszenz Absorption & Emissionsarten Absorption (Aufnahme von Energie) Atome absorbieren Energien, z.b. Wellenlängen,
Die Natriumlinie und Absorption, Emission, Dispersion, Spektren, Resonanz Fluoreszenz, Lumineszenz Absorption & Emissionsarten Absorption (Aufnahme von Energie) Atome absorbieren Energien, z.b. Wellenlängen,
2-01. Das Ethen-Molekül. Perspektivische Darstellung des Ethen-Moleküls.
 Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
= 6,63 10 J s 8. (die Plancksche Konstante):
 35 Photonen und Materiefelder 35.1 Das Photon: Teilchen des Lichts Die Quantenphysik: viele Größen treten nur in ganzzahligen Vielfachen von bestimmten kleinsten Beträgen (elementaren Einheiten) auf: diese
35 Photonen und Materiefelder 35.1 Das Photon: Teilchen des Lichts Die Quantenphysik: viele Größen treten nur in ganzzahligen Vielfachen von bestimmten kleinsten Beträgen (elementaren Einheiten) auf: diese
Polarisationstransfer
 Polarisationstransfer Schon früh in der Geschichte der NMR-Spektroskopie hat man Experimente durchgeführt, bei denen auf einzelne Signale, d.h. bestimmte Spinübergänge, selektiv mit einer B 2 -Frequenz
Polarisationstransfer Schon früh in der Geschichte der NMR-Spektroskopie hat man Experimente durchgeführt, bei denen auf einzelne Signale, d.h. bestimmte Spinübergänge, selektiv mit einer B 2 -Frequenz
Elektronenspektroskopie
 Elektronenspektroskopie Die Elektronenspektroskopie befasst sich mit der Wechselwirkung elektromagnetischer Strahlung des Wellenlängenbereichs von etwa 100 bis 800 nm mit Materie. Es werden dabei Elektronen
Elektronenspektroskopie Die Elektronenspektroskopie befasst sich mit der Wechselwirkung elektromagnetischer Strahlung des Wellenlängenbereichs von etwa 100 bis 800 nm mit Materie. Es werden dabei Elektronen
Theoretische Grundlagen Physikalisches Praktikum. Versuch 12: Fotometrie und Polarimetrie
 Theoretische Grundlagen Physikalisches Praktikum Versuch 12: Fotometrie und Polarimetrie Licht als elektromagnetische Welle sichtbares Licht ist eine elektromagnetische Welle andere elektromagnetische
Theoretische Grundlagen Physikalisches Praktikum Versuch 12: Fotometrie und Polarimetrie Licht als elektromagnetische Welle sichtbares Licht ist eine elektromagnetische Welle andere elektromagnetische
Seminar: Photometrie
 Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Physikalisches Praktikum O 1 Polarisation und optische Aktivität
 Versuchsziel Physikalisches Praktikum O 1 Polarisation und optische Aktivität Es soll das Malussche Gesetz überprüft und Wellenlängenabhängigkeit des spezifischen Drehvermögens einer Zuckerlösung untersucht
Versuchsziel Physikalisches Praktikum O 1 Polarisation und optische Aktivität Es soll das Malussche Gesetz überprüft und Wellenlängenabhängigkeit des spezifischen Drehvermögens einer Zuckerlösung untersucht
2 Einführung in Licht und Farbe
 2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
Fortgeschrittenenpraktikum: Ausarbeitung - Versuch 14 Optische Absorption Durchgeführt am 13. Juni 2002
 Fortgeschrittenenpraktikum: Ausarbeitung - Versuch 14 Optische Absorption Durchgeführt am 13. Juni 2002 30. Juli 2002 Gruppe 17 Christoph Moder 2234849 Michael Wack 2234088 Sebastian Mühlbauer 2218723
Fortgeschrittenenpraktikum: Ausarbeitung - Versuch 14 Optische Absorption Durchgeführt am 13. Juni 2002 30. Juli 2002 Gruppe 17 Christoph Moder 2234849 Michael Wack 2234088 Sebastian Mühlbauer 2218723
Kernmagnetismus und Magnetfelder
 Kernmagnetismus und Magnetfelder. Kernspin Die meisten Kerne besitzen einen Eigendrehimpuls oder P ist gequantelt P = h I(I + ) h = h und h: das Plancksche Wirkungsquantum. π I: Kernspinquantenzahl (kurz:
Kernmagnetismus und Magnetfelder. Kernspin Die meisten Kerne besitzen einen Eigendrehimpuls oder P ist gequantelt P = h I(I + ) h = h und h: das Plancksche Wirkungsquantum. π I: Kernspinquantenzahl (kurz:
Spektroskopische Methoden
 Spektroskopische Methoden OCIfolie367 MS - Massenspektroskopie (Bestimmung von Molekulargewichten, charakteristischen Fragmentierungen von Molekülen) Absorptionsspektroskopische Methoden (Absorption =
Spektroskopische Methoden OCIfolie367 MS - Massenspektroskopie (Bestimmung von Molekulargewichten, charakteristischen Fragmentierungen von Molekülen) Absorptionsspektroskopische Methoden (Absorption =
Wärmestrahlung. Einfallende Strahlung = absorbierte Strahlung + reflektierte Strahlung
 Wärmestrahlung Gleichheit von Absorptions- und Emissionsgrad Zwei Flächen auf gleicher Temperatur T 1 stehen sich gegenüber. dunkelgrau hellgrau Der Wärmefluss durch Strahlung muss in beiden Richtungen
Wärmestrahlung Gleichheit von Absorptions- und Emissionsgrad Zwei Flächen auf gleicher Temperatur T 1 stehen sich gegenüber. dunkelgrau hellgrau Der Wärmefluss durch Strahlung muss in beiden Richtungen
Radioaktivität. den 7 Oktober Dr. Emőke Bódis
 Radioaktivität den 7 Oktober 2016 Dr. Emőke Bódis Prüfungsfrage Die Eigenschaften und Entstehung der radioaktiver Strahlungen: Alpha- Beta- und Gamma- Strahlungen. Aktivität. Zerfallgesetz. Halbwertzeit.
Radioaktivität den 7 Oktober 2016 Dr. Emőke Bódis Prüfungsfrage Die Eigenschaften und Entstehung der radioaktiver Strahlungen: Alpha- Beta- und Gamma- Strahlungen. Aktivität. Zerfallgesetz. Halbwertzeit.
27. Wärmestrahlung. rmestrahlung, Quantenmechanik
 24. Vorlesung EP 27. Wärmestrahlung rmestrahlung, Quantenmechanik V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik Photometrie Plancksches Strahlungsgesetz Welle/Teilchen Dualismus für Strahlung
24. Vorlesung EP 27. Wärmestrahlung rmestrahlung, Quantenmechanik V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik Photometrie Plancksches Strahlungsgesetz Welle/Teilchen Dualismus für Strahlung
Die Grundlagen der Spektroskopie: Theorie FÜR EINE BESSERE WISSENSCHAFT AGILENT AND YOU
 Die Grundlagen der Spektroskopie: Theorie FÜR EINE BESSERE WISSENSCHAFT AGILENT AND YOU 1 Agilent engagiert sich für Ausbildung und Lehre und möchte den Zugang zu firmeneigenem Material ermöglichen. Diese
Die Grundlagen der Spektroskopie: Theorie FÜR EINE BESSERE WISSENSCHAFT AGILENT AND YOU 1 Agilent engagiert sich für Ausbildung und Lehre und möchte den Zugang zu firmeneigenem Material ermöglichen. Diese
Physik 2 (GPh2) am
 Name: Matrikelnummer: Studienfach: Physik 2 (GPh2) am 17.09.2013 Fachbereich Elektrotechnik und Informatik, Fachbereich Mechatronik und Maschinenbau Zugelassene Hilfsmittel zu dieser Klausur: Beiblätter
Name: Matrikelnummer: Studienfach: Physik 2 (GPh2) am 17.09.2013 Fachbereich Elektrotechnik und Informatik, Fachbereich Mechatronik und Maschinenbau Zugelassene Hilfsmittel zu dieser Klausur: Beiblätter
Edelgas-polarisierte. NMR- Spektroskopie. Jonas Möllmann Jan Mehlich. SoSe 2005
 Edelgas-polarisierte NMR- Spektroskopie Jonas Möllmann Jan Mehlich SoSe 2005 NMR Prinzip Aufspaltung der Kernspins in verschiedene Niveaus durch angelegtes Magnetfeld Messung des Besetzungs- unterschiedes
Edelgas-polarisierte NMR- Spektroskopie Jonas Möllmann Jan Mehlich SoSe 2005 NMR Prinzip Aufspaltung der Kernspins in verschiedene Niveaus durch angelegtes Magnetfeld Messung des Besetzungs- unterschiedes
Aufgaben zum Wasserstoffatom
 Aufgaben zum Wasserstoffatom Hans M. Strauch Kurfürst-Ruprecht-Gymnasium Neustadt/W. Aufgabenarten Darstellung von Zusammenhängen, Abgrenzung von Unterschieden (können u.u. recht offen sein) Beantwortung
Aufgaben zum Wasserstoffatom Hans M. Strauch Kurfürst-Ruprecht-Gymnasium Neustadt/W. Aufgabenarten Darstellung von Zusammenhängen, Abgrenzung von Unterschieden (können u.u. recht offen sein) Beantwortung
Teil 1 Schwingungsspektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 1 Schwingungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Themenüberblick Schwingungsspektroskopie Physikalische Grundlagen: Mechanisches Bild
Teil 1 Schwingungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Themenüberblick Schwingungsspektroskopie Physikalische Grundlagen: Mechanisches Bild
Die chemische Verschiebung - 1
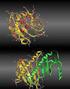 Die chemische Verschiebung - 1 Die Messfrequenz ν einer Kernsorte, hier: 1 H (Protonen), hängt bei einem isolierten Kern ausschließlich vom äußeren Magnetfeld (B 0 ) und ihrem magnetogyrischen Verhältnis
Die chemische Verschiebung - 1 Die Messfrequenz ν einer Kernsorte, hier: 1 H (Protonen), hängt bei einem isolierten Kern ausschließlich vom äußeren Magnetfeld (B 0 ) und ihrem magnetogyrischen Verhältnis
Licht als Teilchenstrahlung
 Der Photoeffekt: die auf die Materie einfallende Strahlung löst ein Elektron aus. Es gibt eine Grenzfrequenz, welche die Strahlung haben muss, um das Atom gerade zu ionisieren. Licht als Teilchenstrahlung
Der Photoeffekt: die auf die Materie einfallende Strahlung löst ein Elektron aus. Es gibt eine Grenzfrequenz, welche die Strahlung haben muss, um das Atom gerade zu ionisieren. Licht als Teilchenstrahlung
Physik III - Anfängerpraktikum- Versuch 601
 Physik III - Anfängerpraktikum- Versuch 601 Sebastian Rollke (103095) und Daniel Brenner (105292) 21. September 2005 Inhaltsverzeichnis 1 Theorie 2 1.1 Grundlagen.......................................
Physik III - Anfängerpraktikum- Versuch 601 Sebastian Rollke (103095) und Daniel Brenner (105292) 21. September 2005 Inhaltsverzeichnis 1 Theorie 2 1.1 Grundlagen.......................................
Fluoreszierende Verbindungen
 Thema: Fluoreszierende Verbindungen Klasse 11 / 12 Schulversuchspraktikum Bastian Hollemann Sommersemester 2015 Klassenstufen 11 & 12 Fluoreszierende Verbindungen Thema: Fluoreszierende Verbindungen Klasse
Thema: Fluoreszierende Verbindungen Klasse 11 / 12 Schulversuchspraktikum Bastian Hollemann Sommersemester 2015 Klassenstufen 11 & 12 Fluoreszierende Verbindungen Thema: Fluoreszierende Verbindungen Klasse
Physikalische. Grundlagen. L. Kölling, Fw Minden
 Physikalische Grundlagen L. Kölling, Fw Minden Radioaktivität kann man weder sehen, hören, fühlen, riechen oder schmecken. Daher muss sie der FA (SB) zumindest verstehen, um im Einsatzfall die erforderlichen
Physikalische Grundlagen L. Kölling, Fw Minden Radioaktivität kann man weder sehen, hören, fühlen, riechen oder schmecken. Daher muss sie der FA (SB) zumindest verstehen, um im Einsatzfall die erforderlichen
K1: Lambert-Beer`sches Gesetz
 K1: Lambert-Beer`sches Gesetz Einleitung In diesem Versuch soll die Entfärbung von Kristallviolett durch atronlauge mittels der Absorptionsspektroskopie untersucht werden. Sowohl die Reaktionskinetik als
K1: Lambert-Beer`sches Gesetz Einleitung In diesem Versuch soll die Entfärbung von Kristallviolett durch atronlauge mittels der Absorptionsspektroskopie untersucht werden. Sowohl die Reaktionskinetik als
Basiskenntnistest - Physik
 Basiskenntnistest - Physik 1.) Welche der folgenden Einheiten ist keine Basiseinheit des Internationalen Einheitensystems? a. ) Kilogramm b. ) Sekunde c. ) Kelvin d. ) Volt e. ) Candela 2.) Die Schallgeschwindigkeit
Basiskenntnistest - Physik 1.) Welche der folgenden Einheiten ist keine Basiseinheit des Internationalen Einheitensystems? a. ) Kilogramm b. ) Sekunde c. ) Kelvin d. ) Volt e. ) Candela 2.) Die Schallgeschwindigkeit
Konzentrationsbestimmung von Zink, Natrium und Calcium in verschiedenen Mineralwassern mittels Atom-Absorptions-Spektroskopie
 Analytisches Physikalisches Praktikum SS 07 AAS Konzentrationsbestimmung von Zink, Natrium und Calcium in verschiedenen Mineralwassern mittels Atom-Absorptions-Spektroskopie Assistent: Markus Wälle, waelle@inorg.chem.ethz.ch
Analytisches Physikalisches Praktikum SS 07 AAS Konzentrationsbestimmung von Zink, Natrium und Calcium in verschiedenen Mineralwassern mittels Atom-Absorptions-Spektroskopie Assistent: Markus Wälle, waelle@inorg.chem.ethz.ch
Fluoreszenz und Excimerenbildung
 Fluoreszenz und Excimerenbildung Fragen und Stichworte zur Vorbereitung: Aufbau und Funktion eines Fluoreszenzspektrometers Spektrale und natürliche Bandbreite Signal-Rausch-Verhältnis Jablonski-Diagramm:
Fluoreszenz und Excimerenbildung Fragen und Stichworte zur Vorbereitung: Aufbau und Funktion eines Fluoreszenzspektrometers Spektrale und natürliche Bandbreite Signal-Rausch-Verhältnis Jablonski-Diagramm:
Grundkurs IIIa für Studierende der Physik, Wirtschaftsphysik und Physik Lehramt
 Grundkurs IIIa für Studierende der Physik, Wirtschaftsphysik und Physik Lehramt Othmar Marti Experimentelle Physik Universität Ulm Othmar.Marti@Physik.Uni-Ulm.de Vorlesung nach Hecht, Perez, Tipler, Gerthsen
Grundkurs IIIa für Studierende der Physik, Wirtschaftsphysik und Physik Lehramt Othmar Marti Experimentelle Physik Universität Ulm Othmar.Marti@Physik.Uni-Ulm.de Vorlesung nach Hecht, Perez, Tipler, Gerthsen
Aufgabe 2.1: Wiederholung: komplexer Brechungsindex
 Übungen zu Materialwissenschaften II Prof. Alexander Holleitner Übungsleiter: Jens Repp / Eric Parzinger Kontakt: jens.repp@wsi.tum.de / eric.parzinger@wsi.tum.de Blatt 2, Besprechung: 23.04.2014 / 30.04.2014
Übungen zu Materialwissenschaften II Prof. Alexander Holleitner Übungsleiter: Jens Repp / Eric Parzinger Kontakt: jens.repp@wsi.tum.de / eric.parzinger@wsi.tum.de Blatt 2, Besprechung: 23.04.2014 / 30.04.2014
Thema heute: Aufbau der Materie: Das Bohr sche Atommodell
 Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Basiskenntnistest - Physik
 Basiskenntnistest - Physik 1.) Welche der folgenden Einheiten ist keine Basiseinheit des Internationalen Einheitensystems? ) Kilogramm ) Sekunde ) Kelvin ) Volt ) Candela 2.) Wenn ein Elektron vom angeregten
Basiskenntnistest - Physik 1.) Welche der folgenden Einheiten ist keine Basiseinheit des Internationalen Einheitensystems? ) Kilogramm ) Sekunde ) Kelvin ) Volt ) Candela 2.) Wenn ein Elektron vom angeregten
Fluoreszenzlampenl. René Riedel. Bettina Haves
 Leuchtstoffe in Fluoreszenzlampenl René Riedel Bettina Haves Inhalt 1) Fluoreszenzlampen 2) Fluoreszenz 3) Geschichte der Leuchtstoffe 4) Leuchtstoffe in Fluoreszenzlampen 5) Weitere Anwendungsbereiche
Leuchtstoffe in Fluoreszenzlampenl René Riedel Bettina Haves Inhalt 1) Fluoreszenzlampen 2) Fluoreszenz 3) Geschichte der Leuchtstoffe 4) Leuchtstoffe in Fluoreszenzlampen 5) Weitere Anwendungsbereiche
Raman- Spektroskopie. Natalia Gneiding. 5. Juni 2007
 Raman- Spektroskopie Natalia Gneiding 5. Juni 2007 Inhalt Einleitung Theoretische Grundlagen Raman-Effekt Experimentelle Aspekte Raman-Spektroskopie Zusammenfassung Nobelpreis für Physik 1930 Sir Chandrasekhara
Raman- Spektroskopie Natalia Gneiding 5. Juni 2007 Inhalt Einleitung Theoretische Grundlagen Raman-Effekt Experimentelle Aspekte Raman-Spektroskopie Zusammenfassung Nobelpreis für Physik 1930 Sir Chandrasekhara
