Kardiovaskuläres Manual
|
|
|
- Adolf Flater
- vor 8 Jahren
- Abrufe
Transkript
1 Kardiovaskuläres Manual 5. Auflage 2017 Endotheliale Dysfunktion Inflammation Oxidation Plaque-Instabilität und Thrombus Nach: Libby P. Circulation 2001;104: ; Ross R. N Engl J Med 1999;340: Eine Dienstleistung des Kantonsspitals St.Gallen Herausgeber: Prof. Dr. Hans Rickli, Chefarzt Klinik für Kardiologie, Kantonsspital St.Gallen Unter Mitarbeit von Dr. Gudrun Haager, Kantonsspital St.Gallen
2 Tipp: Über die verlinkten Titel im Inhaltsverzeichnis (Seite 3) gelangen Sie direkt auf den entsprechenden Inhalt. Mit freundlicher Unterstützung von Inhaltsverzeichnis Ansprechpersonen und Autoren 4 Einleitung 8 Reanimation 9 Globale Risikostratifikation 16 Arterielle Hypertonie 19 Diabetes mellitus 31 Dyslipidämien 41 Rauchstopp 57 Chronische Niereninsuffizienz 63 Schlafassoziierte Atemstörungen 71 Präoperative Abklärung vor nicht-kardialen Operationen 77 Thromboembolieprophylaxe in der Medizin 82 Periinterventionelles Management bei Patienten mit Thrombozytenaggregationshemmern, OAK bzw. NOAKs 85 Nicht-invasive Diagnostik bei koronarer Herzkrankheit (KHK) 91 Stabile Angina pectoris 101 Akutes Koronarsyndrom (ACS) 109 Tiefe Venenthrombose und Lungenembolie 125 Akutes Aortensyndrom 149 Akutbehandlung und Sekundärprävention beim ischämischen Schlaganfall und der Transitorischen Ischämischen Attacke (TIA) 155 Behandlungsstandard intrakranielle Blutung 173 Aortenaneurysma 185 Periphere arterielle Verschlusskrankheit (PAVK) 195 Pulmonale Hypertonie 203 Herzinsuffizienz 217 Vorhofflimmern 237 Supraventrikuläre Rhythmusstörungen 251 Schrittmachertherapie 259 Kammertachykardien 263 ICD und CRT 269 Endokarditis 274 Valvuläre Herzerkrankungen 281 Ambulante kardiale Rehabilitation und Prävention 299 Psychokardiologie 305 Fahrtauglichkeitsbeurteilung bei kardiologischen Patienten 309 Legal Disclaimer/Impressum 313 3
3 Ansprechpersonen und Autoren Ambulante kardiale Rehabilitation und Prävention (AKR), KSSG Tel Dr. Marc Buser Ärztlicher Leiter AKR, OAmbF Kim Denise Gebhardt Leiterin Organisation AKR Sina Rüdt Psychologin FSP, Psychokardiologin Klinik für Anästhesiologie, Intensiv-, Rettungsund Schmerzmedizin, KSSG Tel Prof. Dr. Miodrag Filipovic Stv. Chefarzt Dr. Roland Lenz Ärztlicher Leiter Rettung SG Klinik für Radiologie und Nuklearmedizin, KSSG Tel Prof. Dr. Simon Wildermuth Chefarzt Prof. Dr. Dr. Flavio Forrer Leiter Nuklearmedizin Prof. Dr. Sebastian Leschka Leitender Arzt Dr. Lukas Hechelhammer Leitender Arzt Dr. Johannes Weber Leitender Arzt Dr. Olaf Chan-Hi Kim Leitender Arzt Institut für Rechtsmedizin, KSSG Tel Bruno Liniger Fachbereichsleiter Verkehrsmedizin Klinik für Allgemeine Innere Medizin/Hausarztmedizin, KSSG Tel Prof. Dr. Michael Brändle Chefarzt Dr. Markus Diethelm Stv. Chefarzt Dr. Frédéric Lagger Oberarzt mbf Dr. Monika Fengler Oberärztin Klinik für Angiologie, KSSG Tel Dr. Ulf Benecke Klinikleiter Dr. Alexander Poloczek Oberarzt mbf Klinik für Endokrinologie, Diabetologie, Osteologie und Stoffwechselerkrankungen, KSSG Tel Dr. Stefan Bilz Leitender Arzt Klinik für Gefässchirurgie, KSSG Tel Prof. Dr. Florian Dick Chefarzt PD Dr. Regula von Allmen Stv. Chefärztin Klinik für Herz- und Gefässchirurgie, Universitätsspital Zürich Tel Prof. Dr. Francesco Maisano Klinikdirektor PD Dr. Alberto Weber Leitender Arzt PD Dr. Maurizio Taramasso Oberarzt Dr. Héctor Rodríguez Oberarzt Klinik für Infektiologie /Spitalhygiene, KSSG Tel Dr. Katia Boggian Stv. Chefärztin Klinik für Intensivmedizin, KSSG Tel Dr. Gian-Reto Kleger Klinikleiter Klinik für Kardiologie, KSSG Tel Prof. Dr. Hans Rickli Chefarzt PD Dr. Micha Maeder Stv. Chefarzt Prof. Dr. Peter Ammann Leiter Rhythmologie Dr. Daniel Weilenmann Leiter Interventionelle Kardiologie Dr. Philipp K. Haager Leiter Strukturelle Herzerkrankungen Dr. Lucas Jörg Leitender Arzt Dr. David Altmann Oberarzt mbf Dr. Niklas Ehl Leiter Nicht-invasive Kardiologie Dr. Dr. Roman Brenner Oberarzt mbf Dr. Marc Buser Oberarzt mbf Dr. Giulia Domenichini Oberassistenzärztin Klinik für Nephrologie /Transplantationsmedizin, KSSG Tel Dr. Isabelle Binet Klinikleiterin Dr. Christian Bucher Oberarzt mbf Klinik für Neurochirurgie, KSSG Tel Dr. Jean-Yves Fournier Leitender Arzt Dr. Heiko Richter Oberarzt mbf Dr. Martin Seule Oberarzt Klinik für Neurologie, KSSG Tel Prof. Dr. Barbara Tettenborn Chefärztin Dr. Georg Kägi Leiter Schlaganfallzentrum Dr. Jochen Vehoff Stv. Leiter Schlaganfallzentrum Dr. Monika Kapauer Oberärztin Klinik für Pneumologie und Schlafmedizin, KSSG Tel Prof. Dr. Martin Brutsche Chefarzt Dr. Lukas Kern Stv. Chefarzt Prof. Dr. Otto Schoch Leitender Arzt Dr. Fabian Aigner Oberarzt Dr. Gabriel Benz Oberarzt Dr. Rebekka Kleiner Oberärztin Klinik für Psychosomatik, KSSG Tel Dr. Dagmar Schmid Klinikleiterin Dr. Thorsten Schaffer Stv. Klinikleiter 4 5
4 Klinik für Rheumatologie, KSSG Tel PD Dr. Thomas Neumann Oberarzt mbf Ostschweizer Gefässzentrum Tel Dr. Ulf Benecke Klinikleiter Angiologie Prof. Dr. Florian Dick Chefarzt Gefässchirurgie PD Dr. Regula von Allmen Stv. Chefärztin Gefässchirurgie Dr. Lukas Hechelhammer Leiter Interventionelle Radiologie Zentrum für Labormedizin, KSSG Tel Prof. Dr. Wolfgang Korte Chefarzt Prof. Dr. Dr. h.c. Walter Riesen Emeritierter Institutsvorsteher Dr. Thomas Lehmann Leitender Arzt Dr. Lukas Graf Abteilungsleiter Core Lab REA 2000, KSSG Tel Wolfram Schuhwerk Fachbereichsleiter Zentrale Notfallaufnahme, KSSG Tel Dr. Robert Sieber Chefarzt Dr. Dieter von Ow Stv. Chefarzt 6 7
5 Einleitung Liebe Kolleginnen und Kollegen Die mittlerweile 5. Auflage des altbewährten und beliebten Manuals liegt vor Ihnen, aktualisiert unter Berücksichtigung der zwischenzeitlich publizierten internationalen Richtlinien, praktisch im Format und übersichtlich in der Handhabung. Die Entwicklungen der Neuen Medien gehen auch an uns nicht vor über. Tablets, Apps und e-health haben Einzug gefunden in die Medizin. Diesen Weg wollen auch wir mitgehen. Daher gibt es nun das Kardiovaskuläre Manual auch online unter Registrieren Sie sich gratis und profitieren Sie vom leichten Zugriff jederzeit. Hier erfahren Sie auch, wie Sie einen Patienten für eine kardiologische Abklärung/Behandlung zuweisen können. Die Entwicklung des Manuals wird künftig App-basiert stattfinden damit es stets aktuell und den neusten Richtlinien angepasst ist. Auf der Guidelines-Plattform werden auch Informationsaustausch und Fachdiskussionen ermöglicht. Zudem finden Sie dort relevante Hintergrundinformationen. So schnell geben wir jedoch das handliche Buchformat noch nicht auf. Ich freue mich darüber, Ihnen auch in diesem Jahr wieder ein Medium an die Hand geben zu können, das Ihnen hoffentlich den oftmals hektischen Alltag durch rasche Informationsfindung erleichtert und Ihnen hilfreicher Begleiter sein wird. Im Namen der Autorenschaft Prof. Dr. Hans Rickli Chefarzt Klinik für Kardiologie, Kantonsspital St.Gallen Reanimation bei Personen ab 1 Monat gemäss Richtlinien der American Heart Association (AHA) Grundlagen Die entscheidenden Faktoren für eine erfolgreiche Reanimation sind: Schnellstmögliche und qualitativ hochwertige Thoraxkompressionen ohne unnötige Unterbrechungen Schnellstmögliche Defibrillation Korrekte Ventilation und Oxygenierung bei länger dauerndem Kreislaufstillstand Thoraxkompression Zweck: ATP-Reserven Herzmuskel erhalten oder auffüllen; rechtes Herz leeren, linkes Herz auffüllen; Cerebrum vor anoxischem Schaden bewahren Ziel: ETCO2 > 1.5 kpa Defibrillation Zweck: Beendigung Kammerflimmern oder pulslose Kammertachykardie Kritische Grösse für erfolgreiche Defibrillation: grobschlägiges Kammerflimmern Ventilation Zweck: Oxygenierung und Abtransport von CO2 Ziel: keine Hyperventilation Prognose Es könnten 4- bis 6-mal mehr Personen neurologisch intakt überleben, wenn Ersthelfer schnell und korrekt CPR aufnähmen und ein Defibrillator innerhalb von 4 Min. einsatzbereit wäre. 8 9
6 Klinische Essentials Gute Thoraxkompression Frequenz mind. 100/Min. (nicht mehr als 120/Min.) Bei Erwachsenen: mind. 5 6 cm Kompressionstiefe, bei Kindern und Säuglingen: mind. 1 /3 Brusttiefe (Kinder ca. 5 cm, Säuglinge ca. 4 cm) Vollständige Entlastung des Brustkorbs (100%) Keine unnötigen Unterbrechungen; falls Unterbrechung notwendig: max. 10 Sek. Zweihelfer-Reanimation: alle 2 Min. mit Thoraxkompressionen abwechseln Gute Ventilation 1 Sek. Inspirationsphase; Beatmungsdruck < 30 cm H2O halten, um Mageninsufflationen mit konsekutiver Aspiration zu vermeiden Ventilationsfrequenz 10 pro Min. für Intubierte; Hyperventilation vermeiden, weil das Herzminutenvolumen wegen erhöhtem intrathorakalem Druck reduziert wird Gute Defibrillation Während Aufladen des Defibrillators Thoraxkompression weiterführen Nach Defibrillation kein Rhythmus-/Puls-Check, unverzüglich mit Thoraxkompression weiterfahren Guter iv-zugang und richtiges Timing Medikamente Falls Schwierigkeiten mit iv-zugang, auf intra-ossären Zugang wechseln Bei PEA/Asystolie Adrenalin, sobald iv-/intra-ossärer Zugang In der Regel Applikation von Adrenalin nach Defibrillation, Amiodaron (Cordarone) nach dritter Defibrillation Kein Unterbruch der Thoraxkompression für Legen des iv-zugangs und Medikamentengabe Massnahmen für BLS-AED im Überblick Massnahmen Diagnostik Kompressionen Erwachsene Details Kinder und Säuglinge ab 1 Monat Keine Bewegung/Reaktion Keine Atmung oder Schnappatmung Kein Puls innerhalb von 10 Sek. (nur Professionelle) Frequenz Mind. 100/Min. und 120/Min. Tiefe Mind. 5 6 cm Kinder 1 / 3 AP-Durchmesser/ 5 cm Säuglinge 1 / 3 AP- Durch messer/ 4 cm Entlastung Brustkorb vollständig entlasten Wechsel Falls mehr als 1 Helfer, alle 2 Min. mit Komprimieren wechseln Unterbrechungen Keine unnötigen Unterbrechungen resp. auf < 10 Sek. begrenzen Atemwege Verhältnis Kompression Beatmung (bis Atemhilfe) Beatmung: Ungeschulte oder geschulte, aber nicht erfahrene Rettungskräfte Beatmung bei Intubierten/ Alternativen Defibrillation Kopf überstrecken; Kinn anheben; v.a. Trauma Esmarchscher Handgriff 30:2 (1 oder 2 Helfer) Atemstoss 1 Sek. (bis deutliches Anheben Brustkorb) Nur Thoraxkompressionen 10 Beatmungen/Min. unabhängig von Thoraxkompressionen (1 Atemstoss dauert ungefähr 1 Sek.) 30:2 (1 Helfer) 15:2 (2 prof. Helfer) AED so früh wie möglich einsetzen. Unterbrechungen vor Stromabgabe auf ein Minimum begrenzen. Nach Schock sofort mit Thoraxkompressionen weiterfahren. Modifiziert nach AHA
7 Indikationen für ECMO (ecpr) Herzstillstand ohne ROSC > Minuten mit folgenden Bedingungen: Intoxikationen, Lebenszeichen unter CPR (exkl. Schnappatmung) No-Flow Time < 5 Minuten mit VF, VT (Kammerflimmern, Kammertachykardie oder tachykarder PEA) und Low-Flow Time 60 Minuten mit ETCO kpa Hypothermie, d.h. < 32 Grad C (Kalium 8 mmol/l) Übersetzt nach AHA-Richtlinien 2010/15: Der Swiss Resuscitation Council (SRC) anerkennt die Richtlinien der American Heart Association (AHA) sowie des European Resuscitation Council (ERC). Sie unter scheiden sich in verschiedenen Punkten voneinander. Der BLS-AED- Algorithmus und der ACLS-Algorithmus (siehe nächste Seite) entsprechen den AHA-Richtlinien und fassen die gesamten Reanimationsmassnahmen zusammen. Der SRC verfügt über einen eigenen BLS-AED-Algorithmus für Laien (siehe BLS-AED-Algorithmus für Professionelle Keine Reaktion Keine Atmung oder Schnappatmung Massnahmen nach ROSC (Return of Spontaneous Circulation) Nach Wiedererreichen eines spontanen Kreislaufs folgende Massnahmen ergreifen: Oxygenierung und Ventilation optimieren (SaO2 94%), Intubation, keine Hyperventilation (Normokapnie), Kapnographie-Monitoring Schockbehandlung: iv Flüssigkeits-Bolus, Vasopressoren, Ursachentherapie 12-Ableitungs-EKG (bei STEMI Katheterlabor) Temperatur nicht über 36 Grad C ansteigen lassen Notruf betätigen AED/Defibrillator holen (2. Helfer, falls vorhanden, beauftragen) Puls prüfen < 10 Sek. fehlt 30 Kompressionen: 2 Beatmungen vorhanden 1 Beatmung alle 5 6 Sek. Puls alle 2 Min. prüfen AED/Defibrillator trifft ein Rhythmusanalyse defibrillationswürdig? ja nein 1 Schock Unverzüglich mit CPR weiterfahren (5 Zyklen) Unverzüglich mit CPR weiterfahren (5 Zyklen) Fortfahren, bis Lebenszeichen oder Notarzt eintrifft 12 13
8 Herzstillstand-Algorithmus (Erwachsene) zum Inhaltsverzeichnis Kammerflimmern / pulslose Kammertachykardie CPR 2 Min. iv- / io-zugang Rhythmus defibrillationswürdig? ja 1 Schock 2 Nach Hilfe rufen / Rettungssystem aktivieren CPR 2 Min. Amiodaron 300 mg (Cordarone) Reversible Ursachen behandeln übersetzt nach AHA-Richtlinien 2015 Beginn CPR O2-Gabe Monitor / Defi anschliessen Schock CPR 2 Min. Adrenalin 1 mg alle 3 5 Min. Intubation / Alternative er wägen / Kapnografie Rhythmus defibrillationswürdig? ja ja Schock Rhythmus defibrillationswürdig? nein 3 nein 4 Asystolie/PEA CPR 2 Min. iv- / io-zugang Adrenalin 1 mg alle 3 5 Min. Intubation / Alternative er wägen / Kapnographie CPR 2 Min. Reversible Ursachen behandeln Rhythmus defibrillationswürdig? Reversible Ursachen Hypovolämie, Hypoxie, Hydrogen Ion (Azidose), Hypo-/Hyperkaliämie, Hypothermie Tensions-Pneumothorax, Tamponade kardial, Toxin, Thrombose pulmonal, Thrombose koronar Rhythmus defibrillationswürdig? nein nein nein Zu 1 oder 2 gehen Wenn keine Zeichen von ROSC, zu 3 oder 4 gehen Wenn ROSC, gezielte Post-Herzstillstand- Massnahmen ergreifen ja ja Kriterien für den Abbruch der Reanimation (AND = allowance of natural death) Reagiert der Patient nach korrektem BLS auf ACLS-Massnahmen (Defibrillation und Adrenalin) nicht bzw. liegen keine unmittelbar therapierbaren Ursachen für den Kreislaufstillstand vor, sollte man aktiv folgende Kriterien für den Abbruch prüfen: Suchen und Auffinden einer DNAR-Verfügung (Do not attempt resuscitation) Kontaktaufnahme mit Hausarzt und Angehörigen während laufender Reanimation Konsultation vorbestehender medizinischer Akten Asystolie während 10 Min. trotz lege artis durchgeführtem ACLS und Ausschluss einer zugrunde liegenden Hypothermie, Intoxikation oder Beinahe-Ertrinken Fokussierte Echokardiografie zeigt keine mechanische Aktivität ± Spontankontrast ETCO2 permanent < 1.5 kpa Links Dr. Robert Sieber Wolfram Schuhwerk Dr. Gian-Reto Kleger Dr. Daniel Weilenmann 14 15
9 Globale Risikostratifikation In den folgenden Kapiteln ist die Abklärung und Behandlung der einzelnen kardiovaskulären Risikofaktoren zusammengefasst. Bei der Evaluation der Risikofaktoren ist es von entscheidender Bedeutung, diese im gesamten klinischen Kontext zu beurteilen. Die Präventionsmassnahmen sind abhängig vom berechneten Risiko und sollen helfen, die Atherosklerose und ihre Folgeerkrankungen zu reduzieren. Globale Risikostratifikation Indikation Risikoabschätzung bei 1 Faktor: KHK/Atherosklerose* Diabetes mellitus Typ 2/Typ 1 Hypertonie mit Endorganschäden* Chronische Niereninsuffizienz Männer > 40 J., Frauen > 50 J. oder Mikroalbuminurie post-menopausal Metabolisches Syndrom** Familiäre Hypercholesterinämie Rauchen Prof. Dr. Hans Rickli Prof. Dr. Michael Brändle Notwendige Angaben/Werte Alter Aktives Rauchen Blutdruck MI oder Hirnschlag bei Verwandten 1. Grades LDL-/HDL-Cholesterin, Triglyzeride (nüchtern) Das kardiovaskuläre Gesamtrisiko ist bei einigen Patienten höher als mit diesen Faktoren bestimmt. V.a., wenn weitere Risikofaktoren oder -marker vorhanden sind. Dazu zählen: Schlafapnoe (siehe Seite 71) Entzündliche rheumatische Erkrankungen Autoimmunerkrankungen: Psoriasis, Rheumatoide Arthritis, Lupus erythematosus niedriger sozio-ökonomischer Status; soziale Isolation; psychiatrische Erkrankungen. In Bildgebungsverfahren nachgewiesene klinisch asymptomatische Atherosklerose Erhöhtes Lipoprotein (a) 500 mg/l Erhöhtes hscrp AGLA-Risiko-Score siehe Seite 48 Für prämenopausale : Score durch 4 teilen 16 * Nachgewiesen durch invasive oder nicht-invasive Tests; anamnestisch MI, ACS, koronare/ arterielle Revaskularisationen, ischämischer Hirnschlag, PAVK ** Diagnose Metabolisches Syndrom bei 3 Kriterien: Bauchumfang > 102 cm, > 88 cm; Nüchtern-Triglyzeride 1.7 mmol/l; HDL-Cholesterin < 1.0 mmol/l, < 1.3 mmol/l; Blutdruck systolisch 130 mmhg und/oder diastolisch 85 mmhg; Plasmaglukose 5.6 mmol/l *** Absolutes Risiko in %, innerhalb von 10 Jahren ein tödliches Koronarereignis oder einen nicht-tödlichen Myokardinfarkt zu erleiden. Abkürzungen: KHK = Koronare Herzkrankheit; MI = Myokardinfarkt Wiederholung Risikoabschätzung*** anhand 10-Jahres-Risiko für Myokar d- infarkt/tödliches Koronarereignis: < 10%, d.h. niedrig alle 5 Jahre; Risiko tief halten! 10 20%, d.h. intermediär alle 2 5 Jahre, Risiko senken! > 20%, d.h. hoch, oder sehr hoch 1 folgender Faktoren: KHK, Atherosklerose, Diabetes mellitus Typ 2, BD > 160/100 mmhg, familiäre Hypercholesterinämie individuell Behandlungsstrategien Lebensstil Seite 25 Lipide Seite 41 Diabetes mellitus Seite 31 Hypertonie Seite 19 Rauchen Seite 57 Niereninsuffizienz Seite 63 Schlafapnoe Seite 71 Basierend auf den AGLA-Empfehlungen 2014: AGLA Pocketguide «Prävention der Athero sklerose» und 2016 European Guidelines on cardiovascular disease prevention in clinical practice 17
10 Arterielle Hypertonie Definitionen Blutdruck 140 mmhg systolisch und/oder 90 mmhg diastolisch in wiederholten Praxis-Messungen Weisskittelhypertonie: erhöhter Blutdruck nur in der Praxis Maskierte Hypertonie: erhöhter Blutdruck nur ausserhalb der Praxis Blutdruckklassen 1 (mmhg) systolisch diastolisch Normotonie Optimal Normal Hoch normal Hypertonie 1. Grades (leicht) 2. Grades (mässig) 3. Grades (schwer) Isolierte systolische Hypertonie < < < 90 1 Jeweils drei Messungen an verschiedenen Tagen, Mittelwert der 2. und 3. Messung festhalten. Falls systolischer und diastolischer Wert einen unterschiedlichen Schwere - grad ergeben, so wird der höhere Grad gewählt. Primäre (essentielle) Hypertonie Keine konkrete funktionelle oder morphologische Ursache der Hypertonie fassbar Sekundäre Hypertonie Renale, endokrine, kardiovaskuläre oder andere Ursache der Hypertonie fassbar 18 Primäre (essentielle) Hypertonie 92 96% Sekundäre Hypertonieformen Renal-parenchymatös Renovaskulär Endokrin Alle anderen 4 8% 3 5% 0.5 1% 0.5 1% < 0.5% Heilbare Hypertonieformen 1 2% 19
11 Blutdruckmessung Sitzend (nach 3 Min.) Stehend (nach 1 und 3 Min., orthostatische Hypotonie ausschliessen) An beiden Armen messen (Seitendifferenz ausschliessen) Manschettenbreite an Oberarmumfang anpassen ( 33 cm breite Manschette) Dekompression 2 mmhg/sek. Diastolischer Blutdruck: Phase V (Verschwinden der Töne), Phase IV (Leiserwerden der Töne) in speziellen Fällen (Schwangerschaft) Drei Messungen auf 2 mmhg genau; Mittelwert der 2. und 3. Messung festhalten Messgeräte (klinisch geprüft): Säulen-Manometer (Quecksilber) Aneroid-Manometer Oszillometrische Geräte Messtechnische Prüfung des Messgeräts alle 2 Jahre Normaler Blutdruck (mmhg) In der Praxis Selbstmessung Mittelwert der Langzeitmessung (24h-Messung, ambulante BD-Messung) Tag und Nacht (24 Std.) Tag (wach) Nacht (Schlaf) < 140/90 < 135/85 < 130/80 < 135/85 < 120/70 Anamnese Blutdruck- und Gewichtsverlauf (inkl. Schwangerschaft) Lebensstil (Rauchen, Alkoholkonsum, körperliche Aktivität/Sport, Essgewohnheiten/Salzkonsum, berufliche/private Belastung) Schnarchen, Tagesmüdigkeit (Schlafapnoe-Syndrom) Kardiovaskuläre Risikofaktoren und Komplikationen Nierenkrankheit Antihypertensiva «Pressorische» Medikamente und Substanzen: Ovulationshemmer, NSAR, Steroide, Cyclosporin, Sympathomimetika, Nasentropfen, Erythropoietin, Anabolika, trizyklische Antidepressiva, Onkologika (Tyrosinkinasehemmer, VEGF-Blocker, Aromataseinhibitoren, SERMs, m-tor-inhibitoren), Kokain, Lakritze Familie: Hypertonie, Diabetes mellitus, Hyperlipidämie, Adipositas, Nierenerkrankungen, koronare Herzkrankheit, zerebrovaskuläre Erkrankungen, peripher arterielle Verschlusskrankheit Klinische Untersuchung Grösse, Gewicht, BMI Bauch- und Hüftumfang (stehend) Augenfundus Schilddrüsenpalpation Pulsstatus und Gefässauskultation (Strömungsgeräusche?) Abdominalpalpation (aortale Pulsationen?) Laboruntersuchungen Basisdiagnostik Blut (* nüchtern) Blutbild (Polyzythämia vera?) Kalium (1º / 2º Hyperaldosteronismus, Diuretika?) Kalzium (Hyperparathyreoidismus?) Kreatinin (Niereninsuffizienz?) Glukose* (Metabolisches Syndrom, Diabetes mellitus?) Triglyzeride*, Gesamtcholesterin, LDL- und HDL-Cholesterin Harnsäure Urin Status und Sediment Mikroalbuminurie (2. Morgenurin: mg Albumin/mmol Kreatinin: 3.4) 20 21
12 12-Ableitungs-EKG Hinweise auf linksventrikuläre Hypertrophie (LVH)? Sokolow-Index? Cornell-Produkt? Erweiterte Diagnostik Kreatinin-Clearance HbA1c (Diabetes-Diagnose/-Monitoring) Echokardiografie (Gold-Standard für die Diagnose der LVH) 24h-Blutdruckmessung (V. auf Weisskittelhypertonie, Therapiekontrolle, insgesamt grosszügige Indikationsstellung) Abklärungen bei V. auf sekundäre Hypertonie Nierenerkrankung Serum-Kreatinin, Kreatinin-Clearance resp. egfr Urinsediment, (Mikro-)Albuminurie/Proteinurie 24h-Urin und Nierensonografie in ausgewählten Fällen Renovaskuläre Hypertonie Dopplersonografie Nierenarterien oder andere Bildgebung bei Schwerer oder schwer einstellbarer Hypertonie Kreatinin-Anstieg (> ca. 30%) unter ACE-Hemmern oder AT-II-Antagonisten Abdominellem Strömungsgeräusch, generalisierter Arteriosklerose, akutem Lungenödem Primärer Hyperaldosteronismus* Aldosteron-Renin-Ratio (ARR) bei Schwerer oder schwer einstellbarer Hypertonie oder Kalium < 3.5 mmol/l spontan oder < 3.0 mmol/l unter Diuretika (Cave: falls Bestimmung unter Antihypertensiva Kalziumantagonisten bevorzugen) Phäochromozytom* Bei Kopfschmerzen, Schwitzen und Herzklopfen 24h-Urin auf Metanephrin und Normetanephrin (Urin ansäuern) und/oder Plasma-Metanephrin und -Normetanephrin Hyper-/Hypothyreose TSH Cushing* Bei Mondgesicht, Rubeosis faciei, Striae rubrae, Stammfettsucht, easy bruising usw. Freies Cortisol im 24h-Urin Dexamethason-Hemmtest * Allenfalls spezialärztliche Abklärung Risikostratifizierung Zusätzliche Risikofaktoren für die Bestimmung der Risikogruppe männliches Geschlecht Alter 55 Jahre, 65 Jahre Tabakabusus Dyslipidämie Gesamtcholesterin > 4.9 mmol/l LDL-Cholesterin > 3.0 mmol/l HDL-Cholesterin < 1.0 mmol/l bei, < 1.2 mmol/l bei Triglyzeride > 1.7 mmol/l Erhöhter Nüchtern-Blutzucker mmol/l resp. Prädiabetes HbA1c % Adipositas (BMI 30 kg/m 2 ) Abdominale Adipositas Bauchumfang 102 cm bei, 88 cm bei Familienanamnese mit frühzeitigem kardiovaskulärem Ereignis < 55 Jahre bei, < 65 Jahre bei 22 23
13 Subklinische Endorganschäden Linksventrikuläre Hypertrophie (LVH) im EKG Sokolow-Lyon-Index S in V1 + R in V5 oder V6 > 3.5 mv (Sensitivität ca. 20%, Spezifität ca. 95%) R in avl > 1.1 mv (Sensitivität ca. 10%, Spezifität ca. 95%) Cornell-Produkt (R in avl + S in V3 in mm) x QRS-Dauer in ms (R in avl + S in V3 + 6 mm) x QRS-Dauer in ms falls 244 mv*ms linksventrikuläre Hypertrophie (Sensitivität ca. 50%, Spezifität ca. 95%) Linksventrikuläre Hypertrophie in der Echokardiografie LVM Index: > 115 g/m 2 ; > 95 g/m 2 (BSA) Atherosklerose Intima-Media-Dicke der A. carotis (IMT) > 0.9 mm oder Plaque Pulswellengeschwindigkeit (PWV) A. carotis A. femoralis > 10 m/s Knöchel-Arm-Index < 0.9 (ankle-brachial-index ABI) Hypertensive Nephropathie egfr ml/min/1.73 m 2 Mikroalbuminurie mg/24 Std. resp. Albumin/Kreatinin-Quotient mg/mmol Manifeste kardiovaskuläre/renale Erkrankungen Zerebrovaskulär: ischämischer Insult, hämorrhagischer Insult, TIA Kardial: Angina pectoris, Myokardinfarkt, St. nach koronarer Revaskularisation, Herzinsuffizienz Nephropathie (geschätzte glomeruläre Filtrationsrate egfr < 30 ml/min/1.73 m 2 ), Albuminurie (> 300 mg/24 Std., Albumin/ Kreatinin-Quotient > 34 mg/mmol) Symptomatische periphere arterielle Verschlusskrankheit Hypertensive Retinopathie (Blutungen, Exsudate, Papillenödem) Behandlung Änderung des Lebensstils («life style modifications») Tabakabstinenz Zurückhaltung mit Alkohol ( max. zwei «Einheiten»/Tag, max. eine «Einheit»/Tag; 1 «Einheit» = 13 ml (= 10 g) reiner Alkohol) Ernährung «salzarm», reich an Früchten und Gemüse (< 6 g NaCl/Tag, 24h-Urin-Na + < 100 mmol) Gewichtskontrolle/-reduktion Regelmässiges Training: Marschieren, Joggen, Velofahren, Schwimmen, Langlaufen usw. (mind. 30 Min. an 5 7 Tagen/Woche) Diese Massnahmen begleiten jede Pharmakotherapie. Hypertensive Retinopathie Ab Stadium II (Kaliberschwankungen der Arterien) Diabetes mellitus Nüchtern-Blutzucker 7.0 mmol/l HbA1c 6.5% Postprandialer Blutzucker > 11.0 mmol/l 24 25
14 Pharmakotherapie ACE-Hemmer AT-II-Antagonist Kalziumantagonist Behandlungsziel Generell (inkl. Nierenpatienten): < 140/90 mmhg Diabetiker: < 140/85 mmhg Ältere Menschen*: < 150/90 mmhg * gilt auch für Hochbetagte (> 80-jährig). Bei fitten Älteren < 140/90 erwägen, bei gebrechlichen Älteren individuelle Festlegung der Zielwerte Betablocker Antihypertensiva der 1. Wahl Antihypertensiva für alternative Initialtherapie Diuretikum Keine Kombination von ACE-Hemmern und/oder AT-II-Antagonisten und/oder Reninhemmern Antihypertensiva bei individuellen Zusatzerkrankungen Koronare Herzkrankheit Betablocker, ACE-Hemmer, AT-II-Antagonist, Kalzium antagonist Herzinsuffizienz ACE-Hemmer, Diuretikum, Betablocker, AT-II-Antagonist, Aldosteron-Antagonist Asthma bronchiale Keine Betablocker* Dyslipidämie ACE-Hemmer, AT-II-Antagonist, Kalziumantagonist Mikroalbuminurie, Proteinurie diabetische Nephropathie Gestörte Glukosetoleranz Diabetes mellitus Schwangerschaft Hyperkinetische Zirkulation, Tremor, Migräne ACE-Hemmer, AT-II-Antagonist, bradykardisierender Kalziumantagonist ACE-Hemmer, AT-II-Antagonist, Kalziumantagonist ACE-Hemmer, AT-II-Antagonist, Kalziumantagonist, Betablocker Alpha-Methyldopa, Labetalol, Betablocker, Kalziumantagonist (Dihydropyridin), Dihydralazin Betablocker * Hoch kardioselektive Betablocker können bei stabilen Asthmatikern unter guter Überwachung bei guter Indikation eingesetzt werden. Therapieresistenz Der Zielblutdruck wird trotz einer voll ausgeschöpften, mehrwöchigen antihypertensiven Dreierkombination, die zwingend ein Diuretikum enthalten muss, nicht erreicht
15 Mögliche Ursachen für eine Therapieresistenz Ursache Evaluation Massnahme Fehlmessung Manschette, Messtechnik Messfehler korrigieren Weisskittelhypertonie Schlafapnoe-Syndrom Alkoholabusus, Hormone, NSAR, usw. Lakritze Suboptimale Medikation Malcompliance Adipositas Übermässige Salzzufuhr (> 6 g/tag) Na + - resp. H2O-Retention Sekundäre Hypertonie Selbstmessungen, 24h-Blutdruckmessung Anamnese, Schlafstudie Anamnese Sinnvolle Antihypertensiva-Kombination? Adäquate Dosierung? Anamnese Gewicht, Oberarmumfang messen 24h-Urinsammlung auf Na + (> 100 mmol/24 Std.) Klin. Untersuchung, Na + -retinierende Medi kamente (NSAR), Niereninsuffizienz Gezielte Diagnostik (siehe vorne) Überbehandlung vermeiden Gewichtsreduktion, nächtliche Beatmung Entsprechende Substanzen reduzieren/ absetzen Therapieanpassung Patientenmotivation, häufige Kontrollen, BD-Selbstmessungen, Minidosen-Kombination Manschettengrösse anpassen, Gewichtskontrolle, körperliche Aktivität Salzrestriktion, Diuretika Kontrolle Nierenfunktion, salzretinierende Medikamente absetzen, Diuretika Gezielte Therapie Bei Resistenz unter einer Therapie mit einem Hemmer des Renin- Angiotensin-Systems, einem Diuretikum und einem Kalzium antagonisten muss nach Ausschluss einer «Pseudoresistenz» und von sekundären Hypertonieformen zusätzlich die Gabe von Spironolacton (oder eines Betablockers, eines Alphablockers oder eines zentral wirkenden Sympatholytikums) evaluiert werden. Vorsicht: Kontraindikationen und medikamentöse Interaktionen beachten. Diuretika niedrig dosieren (Cave: Hypokaliämie!). Bei Therapieresistenz kann heute eine kathetertechnische renale Sympathikusdenervation (RSD) oder Baroreflex-Stimulation im Rahmen eines Registers oder einer Studie erwogen werden. Hypertensive Krise Hypertensive Gefahrensituation (urgency) Exzessive BD-Erhöhung mit Epistaxis oder Kopfschmerzen, aber ohne akuten Endorganschaden BD-Senkung innert 24 Std., meist p.o. und ambulant möglich Hypertensiver Notfall (emergency) Exzessive BD-Erhöhung mit Symptomen (z. B. Thoraxschmerzen, Dyspnoe, neurologischem Defizit) und/oder akutem Endorganschaden Zerebraler Infarkt, intrazerebrale oder subarachnoidale Blutung Hypertensive Enzephalopathie Lungenödem Akutes Koronarsyndrom Aortendissektion Fundusblutungen, Papillenödem Präeklampsie, Eklampsie Blutdruck in der Schwangerschaft 160/110 mmhg Notfallmässige Hospitalisation! Cave: zu schnelle oder zu exzessive BD-Senkung mit der Gefahr von Hypoperfusion (zerebral, koronar, renal)! 28 29
16 Links Messgeräte: Schweizerische Hypertonie-Gesellschaft: European Society of Hypertension: British Hypertension Society: Deutsche Hochdruckliga: National Institute for Health and Clinical Excellence (NICE): International Society of Hypertension: American Society of Hypertension: Hypertension CANADA: guidelines.hypertension.ca World Hypertension League: Dr. Markus Diethelm Dr. Dr. Roman Brenner Diabetes mellitus Definition Gruppe von Stoffwechselerkrankungen, die durch eine Hyperglykämie charakterisiert sind Die chronische Hyperglykämie führt zu Langzeitschäden, Funktionsstörungen des Körpers und Versagen von Organen; insbesondere an Augen, Nieren, Füssen, Herz und Gefässen. Diagnose und Klassifikation Diagnostische Richtwerte Nüchtern- Plasmaglukose Oraler Glukosetoleranztest 2-Std.-Wert HbA1c Normal < 5.6 mmol/l < 7.8 mmol/l < 5.7% Gestörte Nüchtern-Glukose 5.6 und < 7.0 mmol/l Verminderte Glukosetoleranz und < 11.1 mmol/l ---- Diabetes mellitus 7.0 mmol/l 11.1 mmol/l 6.5% American Diabetes Association. Diabetes Care. 2011;34:62 69 Kriterien für die Diagnose eines Diabetes mellitus Plasmaglukose zu einem beliebigen Zeitpunkt 11.1 mmol/l und klinische Symptome oder Nüchtern-Plasmaglukose (venös) 7.0 mmol/l oder Plasmaglukose (venös) 2 Std. nach ogtt (75 g Glukose po) 11.1 mmol/l oder HbA1c 6.5% Wichtig Bestätigung des pathologischen Resultates an einem weiteren Tag. Ein erhöhter HbA1c-Wert soll durch die Bestimmung eines Nüchtern- Plasmaglukose-Wertes oder mittels ogtt überprüft werden. Bestim
17 mungen sind mit Laborgeräten auszuführen (in der Regel venöse Blutentnahme). Messungen mit Blutzucker-Selbstmessgeräten sind für die Diagnose unzulässig! Methode zur HbA1c-Bestimmung muss NGSP-zertifiziert und gemäss dem DCCT-Assay standardisiert sein. Klassifikation des Diabetes mellitus Diabetes mellitus Typ 1 (Pathogenese: Beta-Zellzerstörung mit konsekutivem, absolutem Insulinmangel) Diabetes mellitus Typ 2 (Pathogenese: progredienter Insulinsekretionsdefekt und Insulinresistenz) Spezifische Diabetestypen Genetischer Defekt der Beta-Zellfunktion (z. B. Maturity Onset Diabetes of the Young [MODY]; mitochondrialer Diabetes) Genetischer Defekt in der Insulinwirkung (z. B. Typ-A-Insulinresistenz, Insulinrezeptordefekt, lipoatropher Diabetes) Erkrankungen des exokrinen Pankreas (z. B. Pankreatitis, Neoplasmen, zystische Fibrose, Hämochromatose) Endokrinopathien (z. B. Akromegalie, Cushing-Syndrom, Phäochromozytom) Medikamenten-induziert (z. B. Steroide, Immunsuppressiva bei Transplantationen, antiretrovirale Therapie) Infektionen (z. B. kongenitale Röteln, Masern, Coxsackievirus, Cytomegalievirus) Seltene Formen von immunogenem Diabetes (z. B. Stiff-Man-Syndrom, Anti-Insulinrezeptor-Antikörper) Andere genetische Syndrome, die mit Diabetes assoziiert sind (z. B. Trisomie 21, Klinefelter-Syndrom, Turner-Syndrom, myotone Dystrophie) Gestationsdiabetes (Definition: während der Schwangerschaft diagnostizierter Diabetes) Screening nach Diabetes mellitus Typ 2 Risiko-Bestimmung bei asymptomatischen Erwachsenen Zum primären Screening bzw. zur Risiko-Bestimmung für Diabetes mellitus Typ 2 bei asymptomatischen Erwachsenen wird der folgende adaptierte FINDRISC-Fragebogen empfohlen: (Onlineversion abrufbar unter Zählen Sie zu folgenden Angaben Ihres Patienten/ Ihrer Patientin die Punkte zusammen und ermitteln Sie seinen/ihren Risiko-Score. Die weiteren Empfehlungen richten sich nach den jeweiligen Risiko-Kategorien. 1. Alter bis 44 Jahre (0 Punkte) 45 bis 54 Jahre (2 Punkte) 55 bis 64 Jahre (3 Punkte) 65 Jahre und mehr (4 Punkte) 2. Body Mass Index (BMI) 18.5 bis 25 kg/m 2 (Normalgewicht) (0 Punkte) 25.0 bis 29.9 kg/m 2 (Übergewicht) (2 Punkte) über 30.0 kg/m 2 (Adipositas) (3 Punkte) 3. Taillenumfang (Horizontale Messung ausgehend vom Mittelpunkt zwischen unterster Rippe und Beckenkamm) MÄNNER FRAUEN unter 94 cm unter 80 cm (0 Punkte) 94 bis 102 cm 80 bis 88 cm (2 Punkte) über 102 cm über 88 cm (3 Punkte) 4. Täglich mindestens 30 Minuten körperliche Aktivität, sodass er/sie ausser Atem oder ins Schwitzen kommt (bei der Arbeit, im Alltag, in der Freizeit) ja (0 Punkte) nein (2 Punkte) 5. Häufigkeit des Früchte- und Gemüse-Verzehrs täglich (0 Punkte) nicht täglich (1 Punkt) 6. Längerfristig Medikamenteneinnahme gegen Hypertonie (aktuell oder in der Vergangenheit) ja (2 Punkte) nein (0 Punkte) 7. Hohe Blutzuckerwerte in der Vergangenheit (z. B. bei Gesundheits-Checks, während der Schwangerschaft, während Akuterkrankungen) ja (5 Punkte) nein (0 Punkte) 8. Erstgradig Blutverwandte mit einer Diabetes-Diagnose ja (2 Punkte) nein (0 Punkte) Abb. 1: Diabetes Typ 2 Risiko-Test (adaptiert nach FINDRISC) Der Risiko-Test basiert auf dem FINDRISC (Lindstrom J, Tuomilehto J. Diabetes Care 2003; 26(3): ) und wurde für die Schweiz anhand bisher unveröffentlichter Daten der CoLaus-Studie (Firmann M, et al. BMC Cardiovasc Disord 2008;8:6) geringfügig adaptiert
18 Therapieziele Allgemeine Empfehlungen Therapiegrundsätze Eine anhaltend gute Blutzuckerkontrolle verhindert bzw. verzögert das Auftreten oder das Fortschreiten von Diabetes-assoziierten Spätkomplikationen. Die Therapie und die Therapieziele sollten immer individuell mit dem Patienten und dessen Umfeld besprochen und festgelegt werden. Insbesondere folgende Faktoren sollten dabei beachtet werden: Diabetesdauer Alter des Patienten Co-Morbiditäten Lebenserwartung des Patienten Bekannte kardiovaskuläre oder mikrovaskuläre Erkrankung Hypoglykämie-Risiko Schwangerschaft oder Schwangerschaftswunsch Blutzuckersenkende Medikamente und deren Kombinationen sind primär auf der Grundlage des individuellen HbA1c-Wertes, vorhandener Kontraindikationen und Co-Morbiditäten auszuwählen. Ebenfalls sind spezifische Nebenwirkungen und Therapiekosten der blutzuckersenkenden Medikamente zu berücksichtigen. Individuelle Therapieziele Individuelles HbA1c-Ziel Patienten-Einstellung und -Motivation Risiko für Hypoglykämien, andere NW Diabetesdauer Lebenserwartung sehr streng hoch motiviert, adhärent, kümmert sich exzellent um sich tief neu diagnostiziert lang weniger streng weniger motiviert, nicht adhärent, kümmert sich schlecht um sich hoch lange Diabetesdauer kurz Glykämie-Zielwerte Ein HbA1c-Wert > 8% zeigt generell einen Handlungsbedarf an und legt die Einleitung einer Therapie oder einen Therapiewechsel nahe. Bei Patienten mit geringem Hypoglykämie-Risiko und neu bzw. kürzlich diagnostiziertem Diabetes mellitus sollten HbA1c-Werte unter 6.5% angestrebt werden. Bei älteren Patienten (> 70 Jahre) mit mehr als 10-jähriger Diabetesdauer, bekannten makrovaskulären Komplikationen, eingeschränkter Lebenserwartung und/oder vermehrter Hypoglykämie-Neigung sollte ein HbA1c-Wert zwischen 7% bis max. 8% angestrebt werden (vgl. Abb. 2). wichtige Co-Morbiditäten keine bestehende vaskuläre Komplikationen Ressourcen, Unterstützung keine alles vorhanden wenige/mild wenige/mild schwer schwer limitiert 34 Abb. 2: Individuelle Therapieziele adaptiert nach Ismail-Beigi F, et al. Ann Intern Med. 2011;154(8):
19 Therapeutische Richtwerte Nüchtern-Glukose Kapilläres Plasma Einstellung gut mmol/l Einstellung akzeptabel mmol/l bzw mmol/l Einstellung ungenügend** Anpassung der Behandlung nötig < 4.0 mmol/l bzw. > 8.0 mmol/l Postprandiale Glukose (2 Std. nach der < 8.0 mmol/l < 10.0 mmol/l 10.0 mmol/l Mahlzeit) Kapilläres Plasma HbA1c* %** % 8.0%*** Tabelle «Algorithmus Behandlung Diabetes» siehe Seiten 38 und 39 Multifaktorielle Therapie sämtlicher Risikofaktoren Bei Patienten mit einem Typ-2-Diabetes ist das Risiko für kardiovaskuläre Ereignisse im Vergleich zu Nicht-Diabetikern deutlich erhöht. Die aggressive Behandlung sämtlicher kardiovaskulärer Risikofaktoren kann schwere kardiovaskuläre Ereignisse um mehr als 50% reduzieren. Deshalb sollte bei diesen Patienten nicht nur eine optimale Blutzuckerkontrolle angestrebt, sondern es sollten sämtliche kardiovaskulären Risikofaktoren gemäss den unten stehenden Richtwerten behandelt werden: Richtwerte HbA1c < 7.0% Individuelle Therapieziele gemäss Abbildung 2 7.0% 8.0% Blutdruck < 140/90 mmhg Bei Proteinurie/Jugendlichen < 130/80 mmhg Gesamtcholesterin LDL-Cholesterin Bei kardiovaskulärer Erkrankung, chronischer Niereninsuffizienz, bei Proteinurie oder Alter > 40 und 1 kv Risikofaktor Triglyzeride < 5.0 mmol/l < 2.6 mmol/l < 1.8 mmol/l < 1.7 mmol/l Nikotinstopp * Referenzbereich: 4 6.1% (Methode = «NGSP-traceable») ** HbA1c-Zielwerte: Bei neu entdecktem Diabetes ohne Hypoglykämie-Risiko: möglichst normoglykäm (HbA1c < 6.5%) Bei älteren Patienten (> 70 Jahre) oder kurzer Lebenserwartung (< 10 Jahre) HbA1c zwischen 7% bis max 8% Bei längerer Diabetesdauer (> 12 Jahre) und Hypoglykämie-Neigung: HbA1c um 7% *** Ein HbA1c-Wert > 8% zeigt generell einen Handlungsbedarf an und legt die Ein leitung einer Therapie oder einen Therapiewechsel nahe. Prof. Dr. Michael Brändle 36 37
20 Algorithmus für die Behandlung des Diabetes mellitus Typ 2 zum Inhaltsverzeichnis Gesund essen, Gewichtskontrolle, Initiale Medikamenten- Monotherapie Wirksamkeit ( HbA1c) Hypoglykämie Gewicht Nebenwirkungen Kosten Metformin Hoch Tiefes Risiko Neutral/Verlust GI / Laktatazidose Tief Falls individualisiertes HbA1c-Ziel innerhalb von 3 Monaten (angegebene Reihenfolge zeigt keine Präferenz an) vermehrte körperliche Aktivität nicht erreicht wird, Wechsel auf Kombination mit 2 Medikamenten Kombination mit 2 Medikamenten Metformin + Metformin + Metformin + Metformin + Metformin + Sulfonylharnstoff Thiazolidinedione Insulin (meist basal) DPP-4-Inhibitor SGLT2-Inhibitor GLP-1- Rezeptoragonist Wirksamkeit ( HbA1c) Hoch Hoch Am höchsten Mittel Mittel Hoch Hypoglykämie Mittleres Risiko Tiefes Hohes Risiko Tiefes Risiko Tiefes Risiko Tiefes Risiko Gewicht Zunahme Zunahme Neutral Abnahme Abnahme Nebenwirkungen Hypoglykämie Ödem, Hypoglykämie HI, Frakturen Selten Selten GI Kosten Tief Hoch Variabel Hoch Hoch Hoch Falls individualisiertes HbA1c-Ziel innerhalb von 3 Monaten (angegebene Reihenfolge zeigt keine Präferenz an) nicht erreicht wird, Wechsel auf Kombination mit 3 Medikamenten Kombination von 3 Medikamenten Metformin + Sulfonylharnstoff + Metformin + Thiazolidinedione Insulin (meist Basal) + Metformin + DPP-4-Inhibitor + Metformin + SGLT2-Inhibitor + Metformin + GLP-1- Rezeptoragonist + TZD TZD SH * SH * SH * SH * oder DPP-4-I oder DPP-4-I oder TZD oder TZD oder TZD oder SGLT2-I oder SGLT2-I oder SGLT2-I oder DPP-4-I oder Insulin ** oder GLP-1-RA oder GLP-1-RA oder Insulin ** oder Insulin ** oder Insulin ** oder Insulin ** Falls trotz einer Kombinationstherapie, die ein Basisinsulin Wechsel zu einer noch komplexeren Insulin-Strategie, in mit einschliesst, der Ziel-HbA1c nach 3 6 Monaten nicht erreicht wurde, der Regel in Kombination mit 1 2 Nicht-Insulin-Präparaten Kombination von injizierbaren Therapien Basalinsulin + Mahlzeiteninsulin oder GLP-1-RA * SH Sulfonylharnstoff, ** normalerweise Basisinsulin Quelle: angepasst EASD-ADA position paper in Diabetologia 2015;58:
21 Dyslipidämien Einleitung Dyslipidämien stellen einen der wichtigsten kardiovaskulären Risikofaktoren dar. In der INTERHEARTStudie steht das Verhältnis Apo B/Apo A-I (stellvertretend für LDL-C/HDL-C) an erster Stelle der verschiedenen kardiovaskulären Risikofaktoren. In der PROCAM-Studie stehen LDL- Cholesterin nach dem Alter an zweiter, HDL-Cholesterin an vierter und die Triglyzeride an achter Stelle. Durch eine LDL-Cholesterin-Senkung um 1 mmol/l mit einer Statintherapie kann die kardiovaskuläre Mortalität um 16%, die Gesamtmortalität um 10% gesenkt werden. Der Nutzen der Statintherapie ist dabei umso grösser, je höher das absolute kardiovaskuläre Risiko ist. Die Einschätzung des absoluten Risikos ist daher die Grundlage der Indikationsstellung zum Beginn einer lipidsenkenden Therapie. Screening, Abklärung und Einteilung (Tab 1.) der Hyperlipidämien Ein generelles Screening ist ab dem 40. Lebensjahr, früher bei Vorliegen weiterer kardiovaskulärer Risikofaktoren und unmittelbar bei Diagnose einer primärer Hyperlipidämie oder frühzeitigen Arteriosklerose bei erstgradig Verwandten indiziert. Ziel der Abklärung ist eine exakte phänotypische und ätiologische Klassifizierung (Tab. 1 4, Abb. 1). Insbesondere müssen primäre Hyperlipidämien korrekt diagnostiziert und im Falle einer Familiären Hypercholesterinämie oder Familiär kombinierten Hyperlipidämie zwingend eine Familienabklärung eingeleitet werden. Detaillierte persönliche und Familienanamnese bezüglich Dyslipidämien und (frühzeitiger M < 55J, F < 60J) Arteriosklerose; Medikamentenanamese (Tab. 3) einschliesslich Unverträglichkeiten gegenüber Lipidsenkern Ernährungsanamnese, ggf. durch Ernährungsberatung 40 41
22 Klinische Untersuchung: u.a. Blutdruck, Xanthome, Arcus lipoides, Hinweise für Lipodystrophie Fettverteilung Labor: Lipidprofil (ausser bei bekannter Hypertriglyzeridämie Nüchtern-Blutentnahme nicht obligat!), Apolipoprotein B (bei kombinierter Hyperlipidämie und Hypertriglyzeridämie), Lipoprotein (a) (bei FH, frühzeitiger Arteriosklerose, etc.), TSH, Glucose/HbA1c und Urinstatus (Ausschluss sekundäre Hyperlipidämien Tab.2); Kreatinin, egfr und Albumin/Kreatinin-Quotient im Spoturin zur Risikostratifizierung Dutch-Lipid (FH)-Score bei LDL-C > 5 mmol/l / > 3.5 mmol/l unter Statintherapie und/oder Gesamtcholesterin > 8 mmol/l (Abb. 1) Genetische Abklärung: FH-Panel (LDLR-, APOB-,PCSK-9-Gen), ApoE-Genotyp nach Rücksprache Lipidsprechstunde/Endokrinologie Familiäre Hyper cholesterinämie (FH) Familiär kombinierte Hyperlipidämie (FCH) Familiäre Dysbetali poproteinämie Familiäre Chylomikronämie Häufig keit 1:250 1:200 1: : Genetik/ Patho physiologie Autosomal-dominant; LDL-Rezeptor- APOBoder PCSK9-Mutation; polygene Form bei 20% mit klinischer Diagnose Autosomal-dominant VLDL-Überproduktion Autosomal-rezessiv Apo E2/E2 Autosomal-rezessiv Lipoproteinlipasemutation Labor/Klinik LDL-C 5 12 mmol/l (heterozygote), > 13 mmol/l (homozygote) Sehnenscheidenxanthome, Arcus lipoides < 45 Jahre TG > 2.0 mmol/l, Apo B > 1.2 g/l Chylomikronenremnants Chol/Apo B > 6.2 TG/Apo B < 10 Chylomikronensyndrom, akute Pankreatitis (TG > 20 mmol/l) kv- Risiko Gesamt-/LDL-C (mmol/l) Triglyceride (mmol/l) Apo B (g/l) Tab. 2: Wichtige Primäre Hyperlipidämien Hypercholesterinämie > 5.0/3.0 < 2.0 mmol/l > 1.0 Kombinierte Hyperlipidämie > 5.0/3.0 > 2.0 mmol/l > 1.0 Hypertriglyzeridämie < 5.0/3.0 > 2.0 mmol/l < 1.0 Moderate Hypertriglyzeridämie Schwere Hypertriglyzeridämie Tab. 1: Phänotypische Einteilung der Hyperlipidämien mmol/l > 10.0 mmol/l Hypothyreose Diabetes mellitus LDL-C TG, HDL-C Cholestatische Lebererkrankungen Akute intermittierende Porphyrie Chol (LpX) LDL-C Hypercortisolismus Chol, TG Glykogenose Typ 1 TG Lipodystrophien TG, HDL-C Sepsis TG Adipositas Nephrotisches Syndrom TG, HDL-C Monoklonale Gammopathie TG u/o Chol LDL-C, TG Anorexie LDL-C Alkoholabusus TG Schwangerschaft TG Tab. 3: Sekundäre Dyslipidämie-Ursachen 42 43
23 Thiazide (> 25 mg/tag) TG Cyclosporin LDL-C Östrogene TG Sirolimus, Everolimus Chol, TG Tamoxifen, Clomifen TG Olanzapin TG Androgene, Anabolika HDL-C Proteasehemmer Chol, TG, HDL-C Isotretinoin Chol, TG Interferon TG Tab. 4: Häufige medikamenteninduzierte Hyper-/Dyslipidämien Familienanamnese (maximal 2 Punkte) Erstgradig Verwandter mit frühzeitiger KHK (M < 55 Jahre, F < 60 Jahre) 1 Erstgradig Verwandter mit LDL-C > 95. Perzentile (alters- und geschlechstabhängig, CH ~5.5 mmol/l) Erstgradig Verwandter mit Sehnenscheidenxanthomen oder Arcus cornealis 2 Kinder < 18. Lebensjahr LDL-C > 95. Perzentile (alters- und geschlechstabhängig) 2 Punkte Persönliche Anamnese (maximal 2 Punkte) Frühzeitige KHK (M < 55 Jahre, F < 60 Jahre) 2 frühzeitige PAVK oder zerebrovaskuläre Verschlusskrankheit (m < 55 Jahre, f < 60 Jahre) 1 Klinische Untersuchung (maximal 6 Punkte) Sehnenscheidenxanthome 6 Arcus cornealis vor dem 45. Lebensjahr 4 LDL-Cholesterin-Werte > 8.5 mmol/l mmol/l mmol/l mmol/l 1 Molekulargenetische Analyse Nachgewiesene pathogene Mutation im LDL-Rezeptor-, Apo B- oder PCSK-9-Gen 8 > 8 Punkte: definitive Diagnose einer FH; 6 8 Punkte: wahrscheinliche FH; 3 5 Punkte: mögliche FH; 0 2 Punkte: FH unwahrscheinlich Abb. 1: «Dutch Lipid Network Criteria» zur klinischen Diagnosestellung einer autosomaldominant vererbten Familiären Hypercholesterinämie 1 Indikationsstellung zur lipidsenkenden Therapie und Zielwerte (Tab. 5,6, Abb. 2) Bei Hypercholesterinämien, kombinierten Hyperlipidämien und moderaten Hypertriglyzeridämien ist die kardiovaskuläre Risikoreduktion das erste Therapieziel. Bei schwerer Hypertriglyzeridämie steht aufgrund des Pankreatitisrisikos die Triglyzeridsenkung im Vordergrund. Die Indikationsstellung erfolgt aufgrund des absoluten kardiovaskulären Risikos. Falls keine Erkrankung mit einem a priori hohen oder sehr hohen Risiko vorliegt (siehe Tab. 4), wird dieses mit einem Risikokalkulator abgeschätzt. In der Schweiz ist der AGLA-Score empfohlen (AGLA-Score; Abb. 1; alternativ können die Score-Charts für Länder mit tiefem Risiko verwendet werden (SCORE-Charts, Patienten mit Familiärer Hypercholesterinämie und Familiär kombinierter Hyperlipidämie haben a priori ein hohes oder sehr hohes Risiko. Bei diesen Patienten muss bei Diagnosestellung eine primär präventive medikamentöse Therapie evaluiert werden Weitere Risikofaktoren, die nicht in den AGLA-Score eingehen, aber berücksichtigt werden sollen, sind z. B. Lp(a) > 500 mg/l Die Lp(a)-Konzentration wird v.a. über den Längenpolymorphismus des Apolipoprotein (a) bestimmt und ist ein wichtiger unabhängiger kardiovaskulärer Risikofaktor. Indikationen zur Bestimmung des Lp(a) sind frühzeitige KHK oder pos. FA für frühzeitige KHK, Familiäre Hypercholesterinämie, progrediente KHK trotz unter Statin erreichtem LDL-C-Ziel, pos. FA für hohes Lp(a) hscrp > 3 mg/l Bildgebend subklinische Arteriosklerose Metabolisches Syndrom inkl. Schlaf-Apnoe und NAFLD Autoimmunerkrankungen (Psoriasis, SLE, RA) HIV-Infektion 44 45
24 Periodontitis psychosoziale Risikofaktoren, etc. Primär soll zur Risikoreduktion eine Statintherapie eingesetzt werden, um das LDL-Cholesterin zu senken. Das LDL-C-Ziel wird durch das bestehende kardiovaskuläre Risiko bestimmt, je höher das Risiko, desto tiefer der LDL-C-Zielwert. Bei kombinierter Hyperlipidämie/moderater Hypertriglyzeridämie ist die Apo B-Konzentration ein wichtiger sekundärer Zielwert. Die Statintherapie soll so ausgewählt werden, dass mit der ersten gewählten Dosis das LDL-C-Ziel potenziell erreicht wird (Abb. 3). Für Patienten > 75 Jahre gibt es keine zuverlässigen Daten, die den Nutzen/das Risiko einer Statintherapie untersucht haben. In dieser Patientengruppe muss im Einzelfall unter Berücksichtigung der Gesamtsituation gemeinsam mit dem Patienten entschieden werden, ob eine Statintherapie durchgeführt werden soll. Chronische Niereninsuffizienz: Patienten mit dialysepflichtiger Niereninsuffizienz profitieren nicht von einer Statintherapie. Wir empfehlen, die Statintherapie bei für eine Nierentransplantation gelisteten Patienten fortzuführen. Bei einem niedrigen Risiko ist primär eine Lebensstiländerung empfohlen. In der PREDIMED-Studie wurde durch eine mit Olivenöl oder Nüssen angereicherte mediterrane Ernährung das kardiovaskuläre Risiko reduziert. Werden die LDL-C-Zielwerte mit einer Statinmonotherapie nicht erreicht, kommt eine Kombinationstherapie mit Ezetimibe oder einem PCSK-9-Hemmer infrage. In der IMPROVE-IT-Studie wurde bei Patienten nach einem akuten Koronarsyndrom, die zusätzlich zu einer Therapie mit Simvastatin über 7 Jahre Ezetrol erhielten, gegenüber Patienten mit einer Simvastatin-Monotherapie das LDL-C weiter gesenkt (1.4 vs. 1.8 mmol/l) und das kardiovaskuläre Risiko (kardiovaskulärer Tod, Herzinfarkt, Schlaganfall) um 7% gesenkt (absolute Risikoreduktion 2.0%). In der FOURIER-Studie wurde bei Patienten mit einem sehr hohen kardiovaskulären Risiko, die bereits mit einem Statin behandelt waren und zusätzlich über 2.2 Jahre den PSCK-9-Hemmer Evolocumab erhielten, das LDL-C von 2.4 auf 0.8 mmol/l gesenkt und das kardiovaskuläre Risiko (kardiovaskulärer Tod, Herzinfarkt, Schlag anfall) um 20% gesenkt (absolute Risikoreduktion 1.5%). Weder in der IMPROVE-IT noch in der FOURIER-Studie wurde die kardiovaskuläre oder Gesamtmortalität gesenkt. Risikokategorie AGLA 2014 EAS/ESC 2016 Bekannte KHK/Atherosklerose DM Typ 2 oder DM Typ 1 mit Endorganschäden (Mikroalbuminurie) Sehr hohes Risiko Chronische Niereninsuffizienz (egfr < 30 ml/min) 10-Jahres-Risiko 10%** 10-Jahres-Risiko > 20%* 10-Jahres-Risiko 5 und < 10%** Hohes Risiko Stark erhöhte einzelne Risikofaktoren: LDL-C > 4.9 mmol/l, BD > 160/100 mmhg egfr ml/min Stark erhöhte einzelne Risikofaktoren wie familiäre Dyslipidämie und schwere Hypertonie egfr ml/min Intermediäres Risiko 10-Jahres-Risiko 10 20%* 10-Jahres-Risiko 1 und < 5%** Niedriges Risiko 10-Jahres-Risiko < 10%* 10-Jahres-Risiko < 1%** Tab. 5: Risikokategorien modifiziert nach AGLA 2014 ( und ESC 2010 (European Society of Cardiology, * 10-Jahres-Risiko für tödliche und nicht-tödliche koronare Ereignisse ** 10-Jahres-Risiko für tödliche koronare Ereignisse 46 47
25 AGLA-Risiko-Score 1) Punktwerte je Risikofaktor und Ausprägung Zigarettenraucher LDL-Cholesterin Nein 0 (mmol/l) Ja 8 < Alter (Jahre) Systolischer Blutdruck (mmhg) < Triglyzeride (mmol/l) < Positive Familienanamnese HDL-Cholesterin (mmol/l) Nein 0 < Ja 4 AGLA-Risiko-Algorithmus 2) Addition der Punktwerte aller Risikofaktoren 3) Absolutes 10-Jahres-Risiko für ein akutes Koronarereignis nach Gesamtpunktzahl 10-Jahres-Risiko für die Schweiz (in %) P. < P P P P > 58 P. > 20 In Einzelfällen kann das mit dem Score bestimmte Risiko von dem mit dem Algorithmus berechneten abweichen. Wegen der grösseren Zuverlässigkeit soll bei jeder Person mindestens eine Berechnung mit dem Algorithmus durchgeführt werden. Abb. 2: Schätzung des globalen Risikos mithilfe des AGLA-Risiko-Scores bzw. des AGLA-Risiko-Algorithmus, der eine Weiterentwicklung des Scores darstellt und online verfügbar ist. Ernährungstherapie Kardiovaskuläre Prävention: Gesättigte Fette < 10% der Gesamtkalorien, keine Transfette Mit Olivenöl/Nüssen angereicherte mediterrane Ernährung (kv-risikoreduktion in der PREDIMED-Studie) Erreichen eines normalen Körpergewichtes (BMI < 25 kg/m 2 ) Gesteigerte Zufuhr von Nahrungsfasern Hypertriglyzeridämie: Erreichen eines normalen Körpergewichtes (BMI < 25 kg/m 2 ) Reduktion der Alkohohlzufuhr Reduktion der Fettzufuhr und Einsatz mehrfach ungesättigter Fettsäuren Reduktion der Fruktosezufuhr Einsatz von mittelkettigen Triglyzeriden evtl. bei Chylomikronämie Medikamentöse Therapie Medikament Cholesterin LDL-C HDL-C TG Statine 15 40% 20 55% 5 15% 10 30% Ezetimibe 18 20% 15 20% ca. 3% ca. 8% PCSK9-Hemmer 40 50% 50 70% 5 10% 10 20% Fibrate 10 25% 5 20% 10 25% 20 50% Risikokategorie ESC/AGLA Intervention Sehr hoch Hoch Intermediär LDL-C < 1.8 mmol/l oder Reduktion > 50% falls Zielwert nicht erreichbar Apo B < 0.8 g/l* LDLC < 2.6 mmol/l Apo B < 1.0 g/l* LDL-C < 3.0 mmol/l Statin (Ezetimibe, PCSK-9-Hemmer) Statin (Ezetimibe, PCSK-9-Hemmer) Lebensstiländerung (3 Mo), Statin erwägen Niedrig Lebensstiländerung Tab. 6: LDL-C- und Apo B*-Zielwerte, modifiziert gem. AGLA und ESC Guidelines * Bei kombinierter Hyperlipidämie und moderater Hypertriglyzeridämie Tab. 7: Prozentuale Senkung bzw. Erhöhung einzelner Lipide durch verschiedene Lipidsenker Statine Präparate : Simvastatin (10 80 mg)*; 80 mg aufgrund des ungünstigen NW-Profils nicht empfohlen Pravastatin (20 40 mg)* Atorvastatin (10 80 mg)* Rosuvastatin (10 40 mg)* Fluvastatin (Lescol 40 mg u. ret. 80 mg) 48 49
26 Pitavastatin (Livazo 1 4 mg) * Generika Eigenschaften : Gesteigerter LDL-Abbau infolge Cholesterinsynthesehemmung in der Leber LDL-C-Senkung von Präparat/Dosis abhängig, bis 55%, zusätzliche LDL-C-Senkung ca. 6% bei Dosisverdoppelung Reduktion von kardiovaskulärer Morbidität und Mortalität nachgewiesen Bei LDL-C > 3.5 mmol/l und/oder ACS/Stroke primär potentes Statin empfohlen (Simvastatin 40 mg, Atorvastatin 40 mg, Rosuvastatin mg) Kombination mit Ezetimibe, PCSK-9-Hemmern und Fenofibrat möglich T a b e l Lipide Leberenzyme (ALT) CK Vor Therapie Mindestens 2x im Abstand von 1 2 Wochen Ausnahme: bei ACS sofortiger Beginn Statin- Therapie Bestimmen Bestimmen Falls CH > 5x ULN, nicht starten, Test wiederholen Nach Therapiebeginn/ -anpassung 8 (+/ 4) Wochen nach Beginn mit Lipidsenker 8 (plus/minus 4) Wochen nach Therapieanpassung 8 Wochen nach Therapiebeginn 8 Wochen nach Dosis-anpassungen Tab. 8: Labormonitoring bei Statintherapie ( Langzeitverlauf Nach Erreichen der Zielwerte 1x/Jahr, sofern keine besonderen Gründe vorliegen 1x/Jahr, falls Leberenzyme < 3x ULN Keine Routinekontrollen Tests bei Auftreten von Myalgien Cave: ältere Personen, Begleitmedikamente mit Interaktionsrisiko, Polymedikation, Leberoder Nierenkrankheit leezetimibe Präparate: Ezetrol (Ezetimibe) 10 mg/tag Ezetimibe/Simvastatin (Inegy 10/10 mg 10/20 mg, 10/40 mg, 10/80 mg); 10/80 mg aufgrund des ungünstigen Nebenwirkungsprofils nicht empfohlen Ezetimibe/Atorvastatin (Atozet 10/10 mg, 10/20 mg, 10/40 mg, 10/80* mg) Eigenschaften: Hemmung der intestinalen Cholesterinabsorption LDL-C-Senkung ca. 20% Kardiovaskuläre Risikoreduktion in der SHARP- und IMPROVE-IT- Studie in Kombination mit Statinen PCSK-9-Hemmer Präparate: Evolocumab (Repatha 140 mg s.c. alle 2 Wochen) Alirocumab (Praluent 75 oder 150 mg s.c. alle 2 Wochen) Eigenschaften: PCSK9-Hemmer sind humanisierte monoklonale Ak gegen PCSK9, eine Protease, die eine wichtige Rolle im LDL-Rezeptorstoffwechsel spielt. Subkutane Applikation mit Fertigpen alle 2 Wochen LDL-C-Senkung 50 70% Kardiovaskuläre Risikoreduktion in der FOURIER-Studie nachgewiesen Aufgrund der hohen Therapiekosten eingeschränkte Anwendung, v.a. bei klinisch manifester Arteriosklerose und Familiärer Hypercholesterinämie oder Statinintoleranz oder rasch progredienter KHK trotz Statintherapie (Limitatio der Spezialitätenliste des BAG beachten!) 50 51
27 Fibrate Präparate: Fenofibrat (Lipanthyl 200 M, Lipanthyl 267 M, Cholib [Fixkombination mit Simvastatin]) Gemfibrozil (Gevilon Uno) Bezafibrat (Cedur retard) Ciprofibrat (Hyperlipen) Eigenschaften: Gesteigerter Abbau triglyzeridreicher Lipoproteine (v.a. VLDL) Triglyzeridsenkung bis 50%, moderater Anstieg des HDL, z.t. LDL-C-Anstieg infolge beschleunigter Umwandlung VLDL LDL Nur Fenofibrat kann mit Statinen kombiniert werden Einsatz bei moderater und schwerer Hypertriglyzeridämie Kardiovaskuläre Risikoreduktion in einigen Studien nachweisbar (Helskinki Heart-Studie, VA-HIT-Studie, ACCORD-Lipid-Studie bei Kombination mit Simvastatin in Subgruppe mit TG > 2.3 mmol/l und HDL-C < 0.9 mmol/l bei Patienten mit DM Typ 2. Omega-3-Fettsäuren Präparate: Eicosapentaensäure (EPA)/Docosahexaensäure (DHA) (Biorganic Omega-3 Gisand ) Eigenschaften: Hoch dosierte Omega-3-Fettsäuren aus Fischöl (2 3 g gereinigtes EPA/DHA, 6 9 Kapseln Biorganic Omega-3 Gisand) senken die Triglyzeride um ca. 35% und werden bei therapierefraktären Hypertriglyzeridämien empfohlen. Omgea-3-Fettsäuren (ca g EPA/DHA) reduzieren möglicherweise das Risiko kardiovaskulärer Todesfälle bei Patienten mit KHK. Hyper cholesterinämie LDL-C Kombinierte Hyperlipidämie LDL-C TG mmol/l Hypertriglyzeridämie TG > 10.0 mmol/l 1. Wahl Statin Statin Ernährungstherapie 2. Wahl Kombinationstherapie Ezetrol PCSK-9-Hemmer Statin + Ezetrol Statin + PCSK-9- Hemmer Fibrat Statin + Fenofibrat Tab. 9: Auswahl der medikamentösen lipidsenkenden Therapie Fibrat, Fischöl Fibrat + Fischöl Vorgehen bei Nebenwirkungen bzw. Unverträglichkeit der lipidsenkenden Therapie Statin-assoziierte Myopathie Betrifft ca. 10% der mit Statinen behandelten Patienten Myalgien (typischerweise proximal betonte muskelkaterähnliche oder grippale Beschwerden, die oft durch körperliche Aktivität akzen tuiert werden) oder Muskelkrämpfe CK-Erhöhung möglich, nicht obligat, CK-Erhöhung ohne Beschwerden möglich Rhabdomyolyse (CK > U/l): sehr selten, v.a. infolge Medikamenteninteraktionen, die zu erhöhten Plasmakonzentrationen der Statine führen Immunvermittelte nekrotisierende Myopathie: Einzelfälle, Assoziation mit HMGCoA-Reductase-Ak Risikofaktoren genetische Prädisposition, Alter > 80 Jahre, Leberund Niereninsuffizienz, Alkoholabusus, u.a. Dauer bis Auftreten der Beschwerden ca. 6 Monate, bis zum vollständigen Verschwinden nach Absetzen ca. 3 Monate, grosse individuelle Variabilität Systematisches CK-Monitoring bei beschwerdefreien Patienten unter einer Statinmonotherapie nicht gerechtfertigt 52 53
28 Medikament Interaktion mit Fibrate (Ausnahme: Fenofibrat) Allen Statinen Antimykotika (Fluconazol, Ketoconazol) Simvastatin, Atorvastatin HIV-Proteasehemmer Simvastatin, Atorvastatin, Rosuvastatin Verapamil Simvastatin, Atorvastatin Amiodaron Simvastatin, Atorvastatin Cyclosporin Simvastatin, Atorvastatin, Rosuvastatin Makrolide Simvastatin, Atorvastatin Tab. 10: Wichtige Medikamenteninteraktionen mit Statinen Statine und Diabetesrisiko Das Risiko für das Neuauftreten eines DM Typ 2 steigt unter einer Statintherapie um ca. 15%. Betroffen sind v.a. ältere Patienten, die mit potenten Statinen behandelt werden. Das kardiovaskuläre Risiko von Patienten mit DM wird durch Statine erheblich reduziert. Statine führen nicht zu einer Verschlechterung der Diabeteseinstellung. Unveränderte Therapie bei asymptomatischer CK-Erhöhung < U/l, Suche nach alternativen Ursachen (Makro-CK), Verlaufskontrolle Suche nach Medikamenteninteraktionen Suche nach anderen Ursachen einer Myopathie (ibs. Hypothyreose, Polymyalgie, Polymyositis, Medikamente usw.) Wechsel auf ein Statin mit anderen pharmakokinetischen Eigenschaften (Simvastatin, Atorvastatin ersetzen durch Pravastatin, Fluvastatin, Rosuvastatin, Pitavastatin und umgekehrt) Dosisreduktion, ggf. Kombination mit Ezetrol Link: Dr. Stefan Bilz Prof. Dr. Dr. h.c. Walter Riesen Prof. Dr. Hans Rickli Gabe eines Statins mit langer Halbwertszeit (Atorvastatin, Rosuvastatin) jeden 2. Tag Absetzen der Statintherapie. Es gibt Hinweise, dass es nach Absetzen einer Statintherapie im Sinne eines Reboundphänomens vermehrt zu kardiovaskulären Ereignissen kommt, weshalb dieser Schritt bei Patienten mit KHK und tolerablen Symptomen nur gemacht werden soll, wenn die anderen Massnahmen nicht erfolgreich sind. Einsatz alternativer Lipidsenker Tab. 11: Schrittweises Vorgehen bei Statin-assoziierter Myopathie Hepatopathie Hepatopathien sind selten, können unter Statinen und Fibraten auftreten. Eine asymptomatische Transaminasenerhöhung bis zum maximal 3-Fachen der oberen Norm wird als tolerabel betrachtet. Hypertriglyzeridämien sind regelhaft mit einer NAFLD assoziiert, die keine Kontraindikation für den Beginn einer lipidsenkenden Therapie darstellt
29 Rauchstopp Der Tabakkonsum ist ein bekannter Risikofaktor für eine Vielzahl von Erkrankungen und ist mit einer signifikanten Mortalität assoziiert. Die anamnestische Erfassung des Tabakkonsums sowie die klare Aufforderung zum Rauchstopp gehören zu den grundlegenden ärztlichen Pflichten. Der Rauchstopp ist zu jedem Zeitpunkt mit einer Reduktion von Morbidität und Mortalität assoziiert, ungeachtet des Vorliegens einer manifesten Erkrankung. Eine ärztliche «Minimalintervention» von drei Minuten Dauer führt bereits zu einer Verdopplung der Chancen für einen erfolgreichen Rauchstopp! Unterstützende medikamentöse Massnahmen und spezifische Rauchstopp-Interventionen erhöhen die Erfolgsrate zusätzlich. Bei Rauchern, die sich für eine Rauch - entwöhnung entschieden haben, steht bei Bedarf die Rauchstopp- Sprechstunde zur Verfügung. Die zeitaufwendige Betreuung findet dort durch eigens hierfür geschultes Personal statt. Dr. Rebekka Kleiner Prof. Dr. Martin Brutsche 56 57
30 Rauchentwöhnung zum Inhaltsverzeichnis Bereits eine Minimalintervention (Ask + Advise) führt bei 3 5% der Patienten zu einem Rauchstopp! Ask Advise Rauchen Sie? ja Möchten Sie aufhören? ja Brauchen Sie Hilfe? ja nein nein Klar zum Rauchstopp raten Den Entschluss bestärken Assess Nachdenken «Nein, vielleicht später, nach 6 Monaten» Keine Ambivalenz bezüglich Rauchstopp (Erste) Absicht «Ja, nach < 6 Monaten» Ambivalenz bezüglich Rauchstopp Vorbereiten «Ja, in < 1 Monat» Sehr geringe Ambivalenz bezüglich Rauchstopp Überweisung an Rauchstopp- Sprechstunde Assist Sensibilisierende Intervention (~ 5 Min.) Vorteile Rauchstopp Diskutieren Rauchverhalten Hilfe anbieten Motivierende Intervention (~ 10 Min.) Individuelle Vorteile und Risiken Abwägen von Pro/Contra Rauchstopp Hindernisse besprechen (Fehlschlag, Entzugssymptome, Gewicht, Stress, Verlust Genuss) Hilfe anbieten Optionen für Rauchstopp vorstellen Unterstützende Intervention (~ Min.) Entscheid zum Rauchstopp stärken Über Entzugssymptome informieren Stichtag für vollständigen Rauchstopp abmachen Rauchstopp vorbereiten («Raucherarsenal» beseitigen, Umfeld informieren und um Unterstützung bitten) Nikotinabhängigkeit bewerten Nikotinsubstitution oder Vareniclin oder Bupropion bei Nikotinabhängigkeit Rückfall vermeiden Basierend auf Arrange Erneutes Gespräch über Rauchen beim nächsten Termin Termin für erneutes Gespräch abmachen Termine: Wochen ± je nach Bedarf 58 59
31 Rauchentwöhnung: pharmakologische Therapie zum Inhaltsverzeichnis Indikation zur pharmakologischen Unterstützung? = Stadium «Handeln» + Nikotinabhängigkeit Kontraindikation? Nikotinsubstitution: Myokardinfarkt < 2 Wochen, instabile AP, schwere Arrhythmie, evtl. SS/Stillen Vareniclin: absolut SS/Stillen relativ: Psychosen Bupropion: absolut Epilepsie, Anorexie/Bulimie, C2-Entzug, Sedativa, Hirntumor, MAO-Hemmer relativ Epilepsie-Risiko, Leber-/Niereninsuffizienz (hier Risiko bei Überdosierung) Schwache bis mässige Abhängigkeit 1 20 Zigaretten/Tag oder 1. Zigarette > 30 Min. nach Aufwachen ja Starke Abhängigkeit Zigaretten/Tag oder 1. Zigarette 5 30 Min. nach Aufwachen Sehr starke Abhängigkeit > 30 Zigaretten/Tag oder 1. Zigarette < 5 Min. nach Aufwachen Nikotinsubstitution Pflaster 16 Std. Nicorette-Pflaster 25 mg/15 mg/10 mg Pflaster 24 Std. Nicotinell-Pflaster 21 mg/14 mg/7 mg Kaugummi Nicorette/Nicotinell 2 mg/4 mg Starke Dosis: 25 mg x 8 Wochen, dann 15 mg x 2 Wochen, dann 10 mg x 2 Wochen. Dauer: 2 3 Monate bis zu 6 12 Monaten, falls erforderlich. Mittlere Dosis: 15 mg x 4 Wochen, dann 10 mg x 2 (4) Wochen. Dauer: 6 8 Wochen bis zu 6 12 Monaten, falls erforderlich. Niedrige Dosis: 10 mg. Dauer 4 8 Wochen bis zu 6 12 Monaten, falls erforderlich. An eine unbehaarte Stelle des Körpers kleben. Die Stelle jeden Tag wechseln. Starke Dosis: 21 mg x 4 Wochen, hernach 14 mg x 2 (4) Wochen, dann 7 mg x 2 (4) Wochen. Dauer: 2 3 Monate bis zu 6 12 Monaten, falls erforderlich. Mittlere Dosis: 14 mg x 4 Wochen, hernach 7 mg x 2 (4) Wochen. Dauer: 6 8 Wochen bis zu 6 12 Monaten, falls erforderlich. Niedrige Dosis: 7 mg. Dauer 4 8 Wochen bis zu 6 12 Monaten, falls erforderlich. An eine unbehaarte Stelle kleben. Die Stelle jeden Tag wechseln Kaugummis/Tag x 4 Wochen (max. 15/Tag) zu adaptieren. Progressive Reduktion. Dauer: 2 3 Monate bis zu 6 12 Monaten, falls erforderlich. Bei Bitherapie mit Pflaster: max. 6 Kaugummis/ Tag Sekunden kauen, anschliessend den Kaugummi zwischen Zahnfleisch und Wange behalten, auf diese Weise 30 Min. lang mit Pausen kauen. 60 Kaugummi 2 mg Nikotin-Inhalator Nikotintablette (sublingual oder lutschen) Depotpflaster niedrige bis hohe Dosierung ggf. Vareniclin oder Bupropion Nikotinsubstitution: Depotpflaster (hohe Dosierung), Kaugummi 4 mg, Nikotin-Inhalator, Nikotintablette Vareniclin oder Bupropion Entweder alleine oder kombiniert oder 2 verschiedene Nikotinsubstitutionen kombiniert Nikotinsubstitution: Depotpflaster (hohe Dosierung), Kaugummi 4 mg, Nikotintablette Vareniclin oder Bupropion Entweder alleine oder kombiniert oder 2 verschiedene Nikotinsubstitutionen kombiniert (ausser Vareniclin, wofür Kombination mit Nikotinersatz nicht empfohlen) Lutschtablette Nicotinell 1 mg/2 mg Sublingualtablette Nicorette Microtab 2 mg/4 mg Inhalator Nicorette-Inhaler 10 mg 8 12 Tabl./Tag x 4 Wochen (max. 15/Tag) zu adaptieren. Progressive Reduktion. Dauer: 2 3 Monate bis zu 6 12 Monaten, falls erforderlich. Bei Bitherapie mit Pflaster: max. 6 Tabl./Tag Tabl./Tag x 4 Wochen (max. 15/Tag) zu adaptieren. Progressive Reduktion. Dauer: 2 3 Monate, verlängerbar bis zu 6 12 Monaten, falls erforderlich. Bei Bitherapie mit Pflaster: max. 6 Tabl./Tag. Unter der Zunge zergehen lassen Inhalerpatronen/Tag x 4 Wochen (max. 16/Tag) zu adap tieren. Progressive Reduktion. Dauer 2 3 Monate, verlängerbar bis zu 6 12 Monaten, falls erforderlich. Bei Bitherapie mit Pflaster: max. 4 Inhalerpatronen/Tag. Wiederholte Inhalationen von kurzer Dauer während 30 Minuten. 61
32 Vareniclin Champix 0.5 mg/1 mg Bupropion Zyban 150 mg 1x 0.5 mg/tag vom 1. bis 3. Tag, dann 2x 0.5 mg/tag vom 4. bis 7. Tag, schliesslich 2x 1 mg/tag x 11 Wochen ab dem 8. Tag. Rauchstopp normalerweise für den 8. Tag festgelegt, ist aber auch vorher möglich. Raucher informieren über die möglichen Veränderungen des Gemüts und des Verhaltens. Patienten betreuen und bei Auftreten von Verhaltens- oder Gemütsänderungen, Depressionen, suizidalen Ideen oder allergischen Reaktionen Vareniclin sofort absetzen. Bei signifikanten Nebenwirkungen sollte die Dosis auf 2x 0.5 mg/tag vermindert oder ein Absetzen des Präparates erwogen werden. Dauer: 3 Monate bis zu 6 12 Monaten, falls erforderlich. Kosten werden bei Erfüllen der Limitation (hohe Abhängigkeit, Folgeerkrankung) von der KK übernommen. 1x 150 mg/tag vom 1. bis 6. Tag, dann 2x 150 mg/tag x 7 11 Wochen ab dem 7. Tag. Rauchstopp festgelegt zwischen dem 8. und 14. Tag. Bei signifikanten Nebenwirkungen oder bei Sicherheitshinweisen sollte die Dosis auf 1x 150 mg/tag vermindert oder ein Absetzen des Präparates erwogen werden. Dauer: 2 3 Monate bis zu 6 12 Monaten, falls erforderlich. Vorübergehende Nikotinsubstitution: Präparate von kurzer Wirkdauer sind zu bevorzugen (Kaugummi/Tablette/Inhalator); wenn unzureichend: Depotpflaster hinzufügen. Chronische Niereninsuffizienz Einleitung Kardiovaskuläre Erkrankungen sind der Hauptgrund für die sehr hohe Mortalität von Patienten mit dialysepflichtiger Niereninsuffizienz (End Stage Renal Disease, ESRD). Im Vergleich mit der Normalbevölkerung erreicht die kardiovaskuläre Mortalität bei ESRD-Patienten mindestens das 10-fache, bei jungen Erwachsenen sogar mehr als das 100-fache Risiko. Dieses Risiko ist weniger durch vaskulookklusive Ereignisse wie Myokardinfarkte als vielmehr durch plötzlichen Herztod, Arrhythmien und chronische Herzinsuffizienz erklärt. Auch scheinen für dieses spezielle Kollektiv die generell anerkannten Risikofaktoren wie hoher BMI und hoher Cholesterinspiegel eher vor dem Tod zu schützen, weshalb diese Population bezüglich Risikostratifizierung durch den Nephrologen speziell evaluiert und behandelt werden sollte. Patienten mit chronischer Nierenerkrankung (Chronic Kidney Disease, CKD), die keiner Dialysetherapie bedürfen, verhalten sich bezüglich der bekannten kardiovaskulären Risikofaktoren wie die Normalbevölkerung. Neuere Daten zeigen bereits einen Anstieg der kardiovaskulären Mortalität bei einer egfr < 90 ml/min./1.73 m 2 oder einer Albuminurie von 3 30 mg/mmol Creat (entsprechend einer Albuminurie bis 300 mg/tag). Dabei geht die renale Prognose mit dem kardiovaskulären Risiko parallel (siehe Darstellung). Bei schwerer CKD im Stadium 4 ist schliesslich das Risiko abhängig von der Albuminurie 5- bis 10-fach erhöht. Der Gebrauch der MDRD-Formel und v.a. der neueren CKD-EPI- Formel hat die Früherkennung von milden Formen der CKD erleichtert und sollte deshalb zur GFR-Bestimmung konsequent eingesetzt werden. Auch ist das Screening für die Albuminurie (Albumine Creatinine Ratio, ACR) im zweiten Morgenurin einfach und in jeder Sprechstunde durchführbar. Basierend auf und SMW 2011;11(9):
33 Chronische Niereninsuffizienz Laborveränderungen Symptome Persistierende Albuminurie Mortalität der CKD n.s., 1 1.5, 1.5 2, >2 ( 10) (Hazard Ratios) A1 A2 A3 (exemplarisch beginnend, fliessende Übergänge, oft erst spät symptomatisch) Hyperkaliämie, Azidose Hyperpara, Hyperphosphatämie Anämie Abnormale Urinbefunde > 300 mg/ Tag mg/ Tag < 30 mg/ Tag KDIGO 2012 GFR-Stadien G1 5 Albuminurie-Stadien A1 3 Asymptomatisch a s d f G1 90 G Hypertonie Ödeme G3a G3b Müdigkeit, Schlaflosigkeit Gastrointestinale Symptome Juckreiz, Restless legs G G5 < 15 Urämie GFR-Kategorie (ml/min./1.73 m 2 ) Abklärung und Therapie Die Klassifizierung der CKD erfolgt entsprechend der von KDIGO 2012 vorgeschlagenen Einteilung nach Ursache (Cause), GFR-Kategorie und Albuminurie-Kategorie (CGA) oder anhand der KDOQI-Stadien, die nur die GFR berücksichtigt. Ab einer egfr < 45 ml/min./1.73 m 2 oder einer Albuminurie > 300 mg/ Tag respektive Proteinurie > 500 mg/tag sollte die Zuweisung zu einem Nephrologen erfolgen, entsprechend der hellbraun eingefärbten Risiko kategorie. Auch eine anhaltende, nicht anders erklär bare Erythrozyturie, unkontrollierbare Hypertonie in jedem Stadium der CKD oder rezidivierendes Steinleiden sollten fachärztlich beurteilt werden. Komplikationen und Folgeerkrankungen Hypertonie Zielblutdruck bei CKD A1 < 140/90, ab A2 < mmhg Erste Wahl ab Stadium A2: ACE-I oder ARB. Die Wahl des Anti hypertensivums richtet sich ansonsten nach Co-Morbiditäten (siehe ausführliches Kapitel) Eine Kombination von ACE-I und ARB ist nicht mehr empfohlen Bei älteren Patienten und insbesondere beim Einsatz von Vasodilatatoren empfiehlt sich die regelmässige Überprüfung der Orthostase Anämie Diagnostik: Blutbild, Retikulozyten, Eisenstatus (Fe, Ferritin, Transferrin, TSAT) und Vitamine (B12, Folsäure) Kein EPO oder löslichen Transferrinrezeptor messen (nicht relevant) Wenn Hb-Anstieg angestrebt wird: Eisen intravenös, solange TSAT 30% und Ferritin 500 ug/ml ESA-Therapie (Erythropoiesis stimulating Agents): bei Hb < 10 g/l und TSAT > 30% resp. Ferritin > 500 ug/ml Ziel-Hb unter ESA: 110 ± 10 g/l (unter hoch dosiertem ESA Risiko von CV-Ereignissen erhöht) 64 65
34 Prävention der iv-kontrastmittel induzierten Nieren- insuffizienz zum Inhaltsverzeichnis Indikation zur nephrotoxischen KM-Gabe gesichert? ja Nierenfunktion (aktuelle) bekannt? ja nein nein andere Bildgebung prüfen, z. B. US / CEUS, MRI CT ohne Kontrastmittel Serumkreatinin SCr egfr berechnen (Internet) Falls instabile Funktion: Kreatinin-Clearance (Urin 12 Std.) egfr > 60 ml/min? ja Rehydrierung (Ziel: Euvolämie) Allgemeine Massnahmen (siehe Seiten 68 69) egfr > 40 ml/min, < 60 ml/min nein nein egfr < 40 ml/min oder chronische Dialyse? Rücksprache Nephrologie möglich Details siehe Seiten ja ja Möglichst geringe KM-Menge ACE-I, ATII-Blocker, NSAR und Diuretika am Untersuchungstag, Metformin 48 h vor KM weglassen (siehe Seiten 68 69) Elektive Untersuchung: 1 L NaCl 0.9% über 12 h vor, 1 L über 12 Std. nach Untersuchung Notfalluntersuchung: isotone NaBic-Lösung 1.4% 3 ml/kgkg über 1 Std. direkt vor Untersuchung 1 ml/kgkg/h während und nach Untersuchung für insgesamt 6 Std. Alternativ, nur vor CT mit Kontrast: 250 ml isotone NaBic-Lösung 1.4% über 1 Std. Untersuchung durchführen bei egfr > 60 ml/min vor Untersuchung: Kontrolle SCr 48 Std. nach Untersuchung bei egfr < 60 ml/min vor Untersuchung: mindestens 1x Kontrolle SCr, bei baldiger Entlassung oder Intervention 24, sonst 48 Std. nach Untersuchung pausierte Medikamente erst wieder geben, wenn SCr bei Kontrolle nach KM-Exposition stabil bleibt 66 67
35 Weiteres Vorgehen Prävention der iv-kontrastmittel- induzierten Niereninsuffizienz zum Inhaltsverzeichnis Allgemeine Massnahmen Bei peroraler KM-Gabe sind keine nötig Beurteilung Nierenfunktion vor Untersuchung: Kontrolle Serumkreatinin (SCr) in der Regel mittels egfr (bei instabiler Funktion Messung Kreatinin-Clearance im Urin [12 Std.] erwägen) NSAR/COX-Inhibitoren und wenn möglich Diuretika 24 Std. vor Untersuchung pausieren Medikamente erst wieder einsetzen, wenn Serumkreatinin nach 48 Std. nicht ansteigt oder auf den Wert vor der KM-Gabe zurückgegangen ist; Information des Patienten über Dauer der Pause respektive Zeitpunkt des Wiederbeginns egfr < 40 ml/min Rücksprache mit Nephrologie, Tel , vor Untersuchung KM möglichst vermeiden Wenn KM-Gabe nicht vermeidbar, Rehydrierung wie bei egfr > 40 ml/min., < 60 ml/min. (siehe Seiten 66 67) Nächste KM-Gabe erst planen, wenn Kreatinin-Ausgangswert erreicht ACE-I und Angiotensin-Rezeptor-Blocker und Diuretika wenn möglich am Untersuchungstag pausieren (individueller Entscheid: bei Herzinsuffizienz eher belassen) Chronische Dialyse Rücksprache mit Nephrologie, Tel In der Regel Keine Kontraindikation zur iv KM-Gabe Rehydrierung nicht nötig Keine Dialyse unmittelbar nach KM-Gabe (ausser bei Gadolinium-haltigen KM, hier Gefahr nephrogene Fibrose Dialyse planen!) Nota bene: Kreatinin kann nach der Untersuchung stationär, ambulant oder auch beim Hausarzt kontrolliert werden (Absprache!) Nebst Niereninsuffizienz bestehen auch andere Risikofaktoren für eine iv-km-induzierte Niereninsuffizienz (z. B. schwere Proteinurie, Myelom) Bei Hypervolämie oder drohendem Lungenödem Volumen zur Rehydrierung klinisch anpassen Eine Prophylaxe mit N-Acetylcystein wird nicht empfohlen (fehlende Evidenz) CEUS = Kontrastmittelultraschall; egfr = geschätzte glomeruläre Filtrationsrate; iv = intravenös; KG = Körpergewicht; KM = Kontrastmittel; MRI = Magnetresonanztomografie; SCr = Serumkreatinin; US = Ultraschall 68 69
36 Hyperphosphatämie, Hyperparathyreoidismus Serumphosphat mit Phosphatbindern im Normbereich halten 25-OH-Vitamin-D-Mangel korrigieren 1.25-OH-Vitamin-D oder Analoga gemäss Ziel-iPTH erst bei korrigiertem 25-OH-Vitamin-D-Spiegel Ziel-iPTH abhängig von der Nierenfunktion Hyperkaliämie Bei Hyperkaliämie Azidose suchen und korrigieren, RAAS-Blockade reduzieren, Schleifendiuretika einsetzen. Ggf. nephrologische Beurteilung Link: Dr. Christian Bucher Dr. Isabelle Binet Schlafassoziierte Atemstörungen Definition Die Gruppe der schlafassoziierten Atemstörungen umfasst die symptomatische obstruktive Schlafapnoe (obstruktives Schlafapnoe-Syndrom, OSAS), die zentrale Schlafapnoe (ZSA) und die nächtliche alveoläre Hypoventilation. Das schwere OSAS führt primär über nächtliche Arousals mit sympathischer Überaktivierung zu unerholsamem Schlaf, arterieller Hypertonie, verminderter Glukosetoleranz und erhöhter kardiovaskulärer Morbidität und Mortalität sowie häufigeren Verkehrsunfällen aufgrund der Hypersomnie. Diagnose und Klassifikation Atemereignisse von > 10 Sekunden mit Abnahme der Atemzugstiefe um > 80% werden als Apnoen, um > 50% als Hypopnoen bezeichnet, wenn sie mit einem Sauerstoffsättigungsabfall von > 4% einhergehen. Der Index von Apnoen/Hypopnoen (AHI) respektive Sauerstoff- Desaturationen (ODI) pro Schlafstunde ist die Messgrösse für den Schweregrad der nächtlichen Atemstörung, wobei ein AHI von 5 15 als leichtgradige, als mittelschwere und > 30 als schwergradige nächtliche Atemstörung bezeichnet wird. Es wird zwischen obstruktiven Ereignissen mit inspiratorischem Kollaps der oberen Atemwege und zentralen Ereignissen als Folge einer Atemantriebsstörung unterschieden. Die alveoläre Hypoventilation, definiert als pco2 > 6.0 kpa tagsüber, kann Adipositas-assoziiert, als Folge von Thoraxdeformitäten (Kyphoskoliose, schwere restriktive Ventilationsstörung) oder bei neuromuskulären Erkrankungen auftreten
37 Pathophysiologie Risikofaktoren (wichtigste) Klinische Hinweise Obstruktive Schlafapnoe OSA Kollaps der oberen Atemwege Adipositas Retrognathie Zerebrovaskulärer Insult Alkohol, Nikotin, Benzodiazepine Tagesschläfrigkeit, Schnarchen, Retrognathie Zentrale Schlafapnoe ZSA (Cheyne-Stokes-Atmung, Biot'sche Atmung) Atemantriebsstörung Herzinsuffizienz Zerebrovaskulärer Insult Morphine Aufenthalt in grosser Höhe Periodische Atmung (auch tagsüber) Screening nach schlafassoziierter Atemstörung Ein Screening auf OSAS ist bei Populationen mit hoher Prävalenz sinnvoll, da mit einer effizienten Therapie Lebensqualität und Prognose der Patienten effektiv verbessert werden können. Als Trigger für ein Screening gelten Patienten mit Adipositas, Herzinsuffizienz, Vorhofflimmern, therapierefraktärer Hypertonie, Typ-2-Diabetes, nächtlichen Herzrhythmusstörungen, Stroke und pulmonaler Hypertonie. Das Screen - ing besteht in einer gezielten Anamnese bezüglich Schnarchen, Schlafstörung, nächtlicher Atempausen und Tages-Hypersomnie mit Verwendung eines validierten Fragebogens, z. B. mit der Epworth Schläfrigkeitsskala ESS. Patienten mit verdächtigen Symptomen und/ oder einem erhöhten ESS-Score von > 9 Punkten sollen weiter abgeklärt und gegebenenfalls therapiert werden. Die Klinik ist für die Indikation zur Weiterabklärung wichtiger als der Befund einer all fälligen Screening-Pulsoxymetrie. Abklärung und Therapie Bei entsprechendem Verdacht ist eine fachärztliche Weiterabklärung mittels respiratorischer Polygrafie (PG) oder Polysomnografie (PSG) mit Aufzeichnung des nasalen nächtlichen Atemflusses, der Thoraxund Abdomenbewegungen, der Pulsoxymetrie und im Falle der PSG zusätzlich der Schlafstadien und der Infrarot-Videoaufzeichnung Wie leicht fällt es Ihnen, in folgenden Situationen einzuschlafen? Gemeint ist nicht nur das Gefühl, müde zu sein, sondern auch wirklich einzuschlafen. Die Frage bezieht sich auf das übliche tägliche Leben der vergangenen Wochen. Auch wenn Sie einige der beschriebenen Tätigkeiten in letzter Zeit nicht ausgeführt haben, versuchen Sie, sich vorzustellen, welche Wirkung diese auf Sie gehabt hätten. Wählen Sie aus der folgenden Skala die für die entsprechende Frage am besten zutreffende Zahl (Zutreffendes bitte ankreuzen): 0 = würde nie einschlafen; 1 = würde kaum einschlafen; 2 = würde möglicherweise einschlafen; 3 = würde mit grösster Wahrscheinlichkeit einschlafen. Sitzen und lesen Fernsehen Sitzen an einem öffentlichen Ort (z. B. Theater, Sitzung, Vortrag) Als Mitfahrer im Auto während einer Stunde ohne Halt Sich hinlegen, um am Nachmittag auszuruhen, wenn es die Umstände erlauben Sitzen und mit jemandem sprechen Ruhig sitzen nach Mittagessen ohne Alkohol Im Auto beim Stopp an einer Verkehrsampel während einiger Minuten
38 indiziert. Diese Untersuchungen werden in der Regel ambulant durchgeführt. Die Standardtherapie bei leichtem OSAS (AHI 5 15/Std.) besteht in einer Umstellung des Lebensstils mit Gewichtsreduktion, Rauchstopp und Alkoholreduktion. Die CPAP-Therapie ist die Erstlinienbehandlung bei mittelschwerem (AHI 15 30/Std.) und schwerem (AHI > 30/Std.) OSAS. Die CPAP-Geräte werden via Lungenliga instruiert und auf Kosten der Krankenkasse (Pflichtleistung) vermietet. Die Effizienz der CPAP-Therapie zur Normalisierung des AHI liegt bei > 90%, die Akzeptanz nach 12 Monaten bei elektiver Einschulung in unserem Zentrum bei > 80%. Das kardiovaskuläre Risiko nach Therapie der Schlafapnoe und Nutzung von > 4 Std./Nacht entspricht demjenigen der Kontrollpopulation. Therapiealternativen bei OSAS mit CPAP-Unverträglichkeit sind die Unterkiefer-Protrusions-Schiene, eine rigorose Gewichtsreduktion (oft mit Magen-Bypass), selten eine Operation im Hals-Nasen-Ohren- Bereich und noch seltener experimentelle Therapien, wie etwa das Didgeridoo-Spielen oder die Neurostimulation des Nervus Hypoglossus mit einem speziellen Schrittmacher. Auch bei der symptomatischen zentralen Schlafapnoe wird nach Ausschluss einer behandelbaren Ursache (optimale Herzinsuffizienz - behandlung, Absetzen der Morphine) ab mittlerem Schweregrad eine CPAP-Therapie empfohlen. Leider sprechen nur 50% der Patienten auf die Behandlung optimal an (fehlende Unterdrückung der Atempausen und Entsättigungen oder fehlende Verbesserung der Klinik). Dann können die nächtliche Sauerstoffapplikation oder speziellere Beatmungsformen, die adaptive Servoventilation ASV (jedoch nur bei LVEF > 45%) oder die nichtinvasive Ventilation (NIV) versucht werden. Kumulativer %-Anteil von kardiovaskulären Todesfällen (Grafik 1) respektive nicht-tödlichen kardiovaskulären Ereignissen (Grafik 2) bei 1651 Männern in Spanien mit und ohne OSAS Cumulative incidence of fatal CVS events (%) Cumulative incidence of non-fatal CVS events (%) Controls Snorers Mild OSAH Severe OSAH OSAH with CPAP Controls Snorers Mild OSAH Severe OSAH OSAH with CPAP Prof. Dr. Otto Schoch Dr. Gabriel Benz Marin et al, Lancet 2005;365:
39 Präoperative Abklärung vor nicht-kardialen Operationen Ziel: Senkung perioperativer kardialer Komplikationen und Verbesserung der längerfristigen Prognose der Patienten. Festlegung der Abklärungsstrategie aufgrund des Risikos des Eingriffes, der körperlichen Leistungsfähigkeit und des Vorhandenseins klinischer Risikoindikatoren. Abklärungsgang: Zuerst Ausschluss einer akuten oder instabilen Herzkrankheit (Tab. 1) unter Berücksichtigung von kürzlich durchgeführten Koronarinterventionen (können zur Verschiebung eines Wahleingriffs zwingen, Tab. 2). Notfallmässige Operationen kurz nach Koronardilatation mit Stenteinlage beinhalten ein sehr hohes perioperatives Risiko und bedürfen einer intensiven interdisziplinären Betreuung durch Chirurgen, Anästhesisten, Kardiologen und Intensivmediziner. Instabile Koronarsyndrome/akute Koronarsyndrome Instabile Angina pectoris, ausgeprägte Angina pectoris (CCS III oder IV), akuter Myokardinfarkt (< 7 Tage), kürzlich durchgemachte akute Koronarsyndrome/ Myokardinfarkt (8 bis 30 Tage) mit Hinweisen für relevante Restischämie Dekompensierte Herzinsuffizienz Bedeutende (neu aufgetretene oder symptomatische) Rhythmusstörungen, z. B. Höhergradiger AV-Block, symptomatische ventrikuläre Arrhythmie, Rhythmusstörungen mit mangelnder Frequenzkontrolle, symptomatische Bradykardie Schwere Herzklappenerkrankungen Schwere Aortenstenose, symptomatische Mitralstenose CCS = Canadian Cardiovascular Society Tab. 1: Hinweise für das Vorliegen einer akuten/instabilen Herzkrankheit Indikation Art der PCI Minimale Karenzzeit vor nicht-dringlichen Eingriffen Chronische KHK Ballonangioplastie > 1 Woche Chronische KHK Bare Metal Stent (BMS) > 4 bis 6 Wochen Chronische KHK Drug Eluting Stent (DES) > 6 (bis 12) Monate Akutes Koronarsyndrom (ACS) Jede Therapiemodalität 12 Monate Tab. 2: Vorgehen bei Patienten nach PCI 76 77
40 ja hoch Akute/instabile Herzkrankheit? nein PTCA/PCI vor < 12 Monaten? nein vorhanden 3 oder Diabetes mittel/hoch < 4 MET/unbekannt Angina pectoris Nicht-invasive Abklärung Risiko des Eingriffs Körperliche Leistungsfähigkeit Klinische Risikoindikatoren Risiko des Eingriffs mittel Klinische Risikoindikatoren 1 bis 2 erwägen bei neuer Klinik ja niedrig 4 MET ohne Angina pectoris nicht vorhanden Vorgehen Tab. 2 Operationen mit hohem kardialem Risiko (> 5%) Offene gefässchirurgische Eingriffe an der Bauchaorta und der unteren Extremität, ausgedehnte Eingriffe in der Bauchhöhle (Eingriffe an Leber, Pancreas, Oesophagus, Cystektomie), ausgedehnte Eingriffe in der Brusthöhle (Pneumonektomie) Operationen mit mittlerem kardialem Risiko (1 5%) Kleinere und mittlere Eingriffe in der Bauch- oder Brusthöhle, grössere orthopädische Eingriffe, grössere Eingriffe am Hals oder Nacken, endovaskuläre Gefässeingriffe, Eingriffe an den Karotiden (symptomatische Patienten) Operationen mit niedrigem kardialem Risiko (< 1%) Eingriffe an der Körperoberfläche, am Auge, an der Mamma, an der Schilddrüse, transurethrale Eingriffe an der Prostata; kleine orthopädische und gynäkologische Eingriffe, Eingriffe an den Karotiden (asymptomatische Patienten) Die Prozentzahlen geben die durchschnittliche Häufigkeit des perioperativen Auftretens bedeutender kardiovaskulärer Ereignisse an. Tab. 3: Risiko des operativen Eingriffs Verrichtung Körperpflege, leichte Hausarbeiten, langsam geradeaus gehen, 1 Stockwerk steigen Bergaufgehen, kurze Distanzen laufen Schwere Hausarbeiten, Ausdauersport Anzahl MET > 10 Leistungsfähigkeit SCHLECHT MÄSSIG GUT Invasive Abklärung Medikamentöse Therapie Operation Tab. 4: Einschätzung der Leistungsfähigkeit anhand des «metabolic equivalent» (MET), das der Patient leisten kann. Invasive Therapie Reevaluation Therapie der Risikofaktoren Abb. 1: Abklärungsgang bei kardialen Risikopatienten. Weiterführende Erläuterungen siehe Tabellen 1 5. MET = metabolic equivalent Filipovic M. et al. Perioperative kardiale Abklärung und Therapie im Rahmen nicht-herzchirurgischer Eingriffe (Update 2008). Schweiz Med Forum 2008;8(48):
41 Bekannte koronare Herzkrankheit St. n. Myokardinfarkt (vor > 30 Tagen), positiver Ischämienachweis, Q-Welle im 12-Ableitungs-EKG, typische Angina pectoris (CCS I oder II), Nitrattherapie Herzinsuffizienz In der Vorgeschichte dokumentiert, unter medikamentöser Therapie «kompensiert» Zerebrovaskuläre Erkrankungen St. n. zerebrovaskulärem Insult (CVI), St. n. transienter ischämischer Attacke (TIA) Diabetes mellitus, medikamentös behandelt Niereninsuffizienz (Kreatinin > 180 µmol/l oder Clearance < 60 ml/min) CCS = Canadian Cardiovascular Society Tab. 5: Klinische Risikoindikatoren («revised cardiac risk index») Das weitere Vorgehen richtet sich nach dem Risiko des bevorstehenden Eingriffes (Tab. 3), der körperlichen Leistungsfähigkeit des Patienten sowie den Risikoindikatoren (siehe Tab. 5). Wie aus Tab. 4 hervorgeht, brauchen Patienten mit guter Leistungsfähigkeit und/oder fehlenden Risikoindikatoren keine weiteren kardialen Abklärungen. Hingegen müssen Patienten, die nur eingeschränkt leistungsfähig sind und klinische Risikoindikatoren aufweisen (Tab. 5), v.a. im Vorfeld gefässchirurgischer Eingriffe weiter abgeklärt werden. In der Abklärung einer koronaren Herzkrankheit steht die (bildgebende) Ischä miediagnostik, bei einer Herzinsuffizienz oder der Suche nach Klappenvitien die Echokardiographie im Vordergrund. Die Bestimmung eines natriuretischen Peptids (BNP oder NT probnp) ermöglicht v.a. (aber nicht nur) beim Vorliegen einer Herzinsuffizienz eine verbesserte Risikoabschätzung. Wichtig ist der Grundsatz, die Indikationen für invasive Therapien immer auf Basis der allgemein anerkannten kardiologischinternistischen Kriterien zu stellen. Eine invasive Therapie nur um des bevorstehenden Eingriffs willen ist nicht indiziert. Entsprechend muss die Frage nach der therapeutischen Konsequenz allfälliger pathologischer Befunde schon bei der Abklärungsplanung berücksichtigt werden. Perioperative medikamentöse Therapie Die internistisch-kardiologischen Indikationen für den Einsatz von Statinen und Beta-Rezeptoren-Blockern sollen voll ausgeschöpft werden. Die Behandlung sollte mindestens 4 Wochen vor dem Eingriff beginnen. Die Dosierung des Beta-Rezeptoren-Blockers soll schritt weise unter klinischer Kontrolle erhöht werden; Zielherz frequenz < 65/Min. Je nach Indikation bzw. Risiko für das Auftreten von kardiovaskulären Komplikationen und in Abhängigkeit von der Art des Eingriffs sollen Thrombozytenaggregationshemmer über den Eingriff hinaus weitergegeben oder einige Tage vorher abgesetzt werden. Vergleiche hierzu auch Kapitel «Periinterventionelles Management bei Patienten mit Thrombozytenaggregationshemmern bzw. OAK» auf Seite 85. Prof. Dr. Miodrag Filipovic Prof. Dr. Hans Rickli 80 81
42 Thromboembolieprophylaxe in der Medizin zum Inhaltsverzeichnis In der Regel ist bei hospitalisierten Patienten eine Prophylaxe indiziert! Risikofaktoren: Hospitalisation + 1 Risikofaktor: > 60a, BMI > 30 kg/m 2, Malignom, Intensivpatient, Dehydratation, Hormontherapie, Phlebitis, kardiale, metabolische, endokrine, respiratorische, infektiöse oder entzündliche Erkrankung. Signifikant reduzierte Mobilität = Patienten, die bettlägerig sind, die nicht allein gehen können oder einen substanziellen Teil des Tages nur im Bett oder auf einem Stuhl verbringen. J. Thromb Haemost 2008;6: Intervention innerhalb 12 Std.? nein ja Prophylaxe erst 6 Std. nach Intervention beginnen Kontraindikation? Absolut Relevante aktive Blutung Antikoagulantion mit VKA und INR > 2 BD 230/120 mmhg Relativ Thrombozytopenie (< 75 G/l) Erworbene Blutungsneigung (z. B. akute Leberinsuffizienz) Unbehandelte vererbte Blutungsneigung (z. B. Hämophilie, Von-Willebrand-Erkrankung) ja Absolut Relativ Keine Prophylaxe Besprechung Prophylaxe mit Dienstarzt Hämatologie nein Heparin-induzierte Thrombopenie HIT(T) oder Heparinallergie? ja Argatroban (Argatra) iv oder Fondaparinux (Arixtra) sc in Rücksprache mit Dienstarzt Hämatologie nein Niereninsuffizienz egfr ml/min. nein Niereninsuffizienz egfr < 20 ml/min. Indikation für Prophylaxe nein Prof. Dr. Miodrag Filipovic Prof. Dr. Wolfgang Korte Prof. Dr. Hans Rickli Unter Mitarbeit von Dr. Monika Fengler und Dr. Frédéric Lagger VKA= Vitamin-K-Antagonisten 82 ja ja ja Enoxaparin (Clexane) 20 mg sc 1x/Tag um 20 Uhr Cave: Schon eine geringe weitere Verschlechterung der Nierenfunktion geht mit Akkumulationsgefahr einher. Vor Interventionen evtl. Anti-Xa-Aktivität bestimmen. Heparin iv, Richtdosis 200 IE/kg pro 24 Std. oder Heparin 5000 E s.c. 12 stündlich Enoxaparin (Clexane) 40 mg sc 1 x/tag um 20 Uhr Bei < 50 kg Körpergewicht Dosisreduktion auf 20 mg sc 1x/Tag um 20 Uhr Hochrisikosituation*: Enoxaparin (Clexane) 1 mg/kg Körpergewicht sc 1x/Tag um 20 Uhr, max. 100 mg/tag Cave: Die egfr kann sich ändern. Regelmässige Kontrolle der egfr und ggf. Anpassung der Therapie. * Hochrisikosituation: Anamnese von Thromboembolie bei Patient oder Verwandtem 1. Grades oder bei Thrombophilie. 83
43 Periinterventionelles Management bei Patienten mit Thrombozytenaggregationshemmern, OAK bzw. NOAKs Die periinterventionelle Therapie mit gerinnungshemmenden Substanzen kann die Patienten einerseits vor schwerwiegenden Komplikationen schützen (Thromboembolie, Stentthrombose, zerebrale oder myokardiale Ischämie), andererseits aber auch Ursache bedeutender Blutungskomplikationen sein. Der Umgang mit Thrombozytenaggregationshemmern ist in der nachfolgenden Tabelle geregelt: Beibehalten, Absetzen und Wiederbeginnen werden abhängig von der Gefährlichkeit all fälliger Blutungskomplikationen des Eingriffs (von «gering» wie bei gewissen Punktionen bis «sehr hoch» wie bei intrazerebralen Eingriffen) sowie dem zerebro- und kardiovaskulären Risiko (von «tief bis mittel» wie bei Patienten ohne klar dokumentierte arteriosklerotische Gefässerkrankung bis «sehr hoch» wie bei Patienten kurz nach akuten Ereignissen oder Stentimplantationen) gehandhabt. Den Umgang mit oralen Antikoagulantien zeigen die Tabellen auf den Seiten 88/89 und 90. Das Vorgehen hängt ab vom Eingriff und dessen Dringlichkeit sowie vom Aus mass des thromboembolischen Risikos. Hochrisikopatienten bedürfen einer hoch dosierten antithrombotischen «Überbrückungstherapie» (Bridging) mit niedermolekularen Heparinen wie Enoxaparin (Clexane) oder (ausnahmsweise) unfraktioniertem Heparin, bei Patienten ohne hohes Risiko genügt die übliche perinterventionelle Thromboseprophylaxe. Bei Patienten unter direkten bzw. «neuen» oralen Antikoagulantien («DOAK» bzw. «NOAK») erübrigt sich eine überbrückende Therapie: Das Zeitintervall zwischen letzter Einnahme und operativem Eingriff bzw. invasiver Intervention richtet sich nach der Nierenfunktion und Gefährlichkeit allfälliger Blutungskomplikationen (siehe Tabelle Seite 86/87)
44 Periinterventionelles Management bei Patienten mit Thrombozytenaggregationshemmung Zerebro- und kardiovaskuläres Risiko Tief bis mittel Hoch Sehr hoch Gefährlichkeit von Blutungskomplikationen Sehr hoch Hoch Mittel Gering Punktion Pleura/Lunge, Knochenmark, Liquor, epidural, Gelenke, peridural, periphere Nerven, Schilddrüse, Aszites diagnostisch; Mediastinum Endoskopie Pleura/Lunge (exkl. Transbronchiale Biopsie), GIT ± Biopsie, GIT-Endosonografie ohne FNP; TUR-P (Laser), Bülaudrainage OP Augen (ausser Augenlid), Haut, Hand, Gefässshunts Herzschrittmacher, Koronarangiografie, ICD-Implantation Punktion Mamma, Perikard, PEG-Einlage Endoskopie Gynäkologie, Nephrologie, GIT-Polypektomie, Urologie, Transbronchiale Biopsie OP Augenlid, Gefässe, Gynäkologie, HNO, Lunge, Orthopädie, Urologie, Viszeralchirurgie OP Herz Biopsie Leber und Niere perkutan, Schilddrüse OP Leber, Wirbelsäule OP Intrakraniell «Primäre Prävention» Keine manifeste KHK, CVK oder PAVK Pause ASS 5 Tage vor bis 7 Tage nach OP (evtl. Indikation ASS überprüfen) Bei intrakranieller Blutung 6 Wochen Pause ACS > 12 Monate Stabile KHK: St.n. PCI mit BMS > 1 Mt, mit DES > 6 Mte St.n.AKB > 6 Wo St.n.CVI/TIA > 1 Mt, PAVK ASS unverändert weitergeben Indikation Clopidogrel, Prasugrel und/oder Ticagrelor abklären und individuell besprechen Pause ASS 5 Tage vor bis 1./2. Tag nach OP Indikation Clopidogrel, Prasugrel und/oder Ticagrelor abklären und individuell besprechen Pause ASS 5 Tage vor bis 2./3. Tag nach OP Indikation Clopidogrel, Prasugrel und/oder Ticagrelor abklären und individuell besprechen ACS < 12 Monate Stabile KHK: St.n. PCI mit BMS < 1 Mt, mit DES < 6 Mte St.n.AKB < 6 Wo St. n. CVI/TIA < 1 Mt Eingriff verschieben, ansonsten zwingend interdisziplinäre Besprechung mit Operateur, Anästhesist und Kardiologe Bis Entscheid gefällt, ASS, Clopidogrel, Prasugrel und/oder Ticagrelor unverändert weitergeben Eingriff verschieben, ansonsten zwingend interdisziplinäre Besprechung mit Operateur, Anästhesist und Kardiologe 86 AKB = aortokoronare Bypass-Operation; Ap = Angina pectoris; ASS = Acetylsalizylsäure; BMS = Bare Metal Stent (z. B. Prokinetic, Sequent); CVD = Atherosklerose der hirnversorgenden Gefässe («cerebrovascular disease»); CVI = zerebro-vaskulärer Insult; CVK = zerebrale Verschlusskrankheit; DES = Drug-Eluting-Stent (z. B. Onyx, Orsiro, Synergy, Xience); KHK = koronare Herzkrankheit; MI = Myokardinfarkt; OP = Operation; PAVK = periphere arterielle Verschlusskrankheit; PCI = perkutane Coronare Intervention; TIA = transientischämische Attacke; WS = Wirbelsäule; GIT = Gastrointestinaltrakt; FNP = Feinnadelbiopsie; TUR-P = transurethrale Prostataresektion; PEG = perkutane endoskopische Gastrostomie 87
45 Periinterventionelles Management bei Patienten unter Vitamin-K-Antagonisten zum Inhaltsverzeichnis Eingriff unter fortgesetzter OAK möglich? Lokale Hautchirurgie Augen-OP, ausser Lidchirurgie und Hinterkammer Zahnreinigung, Kariessanierung, Zahnextraktion Interventionelle Kardiologie inkl. Rhythmologie GIT-Endoskopie ± Biopsie, EUS ohne FNP, diagnostische Aszitespunktion nein Notfallmässiger Eingriff? nein Patient mit OAK + Tc-Hemmer Schwangere Frau? Antiphospholipidantikörper? ja ja ja INR im Zielbereich halten Keine Heparintherapie PPSB 20 E/kg KG iv, evtl. Vitamin K 2 mg po/iv: Absprache Dosis + Zeit mit OA Anästhesie oder TL ZNA Besprechung mit DA Hämatologie Hochrisikosituation LMWH Enoxaparin (Clexane ) 1 mg/kg (20 mg = 0.2 ml) 12-stdl. max. 2 x 80 mg/d Bei egfr zwischen Reduktion Dosis auf 0.75 mg/kg 12-stdl. Letzte Gabe 36 Std. prä-op Bei egfr < 30ml/min Gabe von unfraktioniertem Heparin (UFH) Bolus 5000 IE Liquemin i.v., gefolgt von 400 E/kg über 24 Std. i.v. Erhaltungsdosis anpassen gemäss PiCT Stopp 4 Std. prä-op Operation Keine Hochrisikosituation übliche präoperative Thromboseprophylaxe Letzte Gabe spätestens > 12 Std. prä-op Operation Sintrom 3 Tage vor Eingriff absetzen nein Marcoumar 5 8 Tage vor Eingriff absetzen Wiederbeginn abhängig von Nach-Blutungsrisiko innerhalb 24 Std. spätestens 48 Std. Übliche postoperative Thromboseprophylaxe INR-Kontrolle 3 4 Tage vor OP INR 2 Erneute INR-Kontrolle 1 2 Tage vor OP Wiederbeginn Vitamin-K-Antagonisten (Marcoumar/Sintrom) frühestens am Abend des OP-Tages (nach Kontrolle Blutungssituation + Rücksprache mit Operateur) Fortführen der LMWH-/UFH-Gabe bis INR an mindestens 2 aufeinander folgenden Tagen > 2 INR < 2 INR < 1.5 INR 1.5 Beginn mit «Bridging»-Therapie Hochrisikosituation für Thromboembolie? Thromboembolie vor < 3 Monaten St. n. Aortenklappenersatz plus 3 Risikofaktoren* St. n. Mitralklappenersatz plus 1 Risikofaktor* Klappenprothese alter Bauart (Björk-Shiley, Starr-Edwards) Vorhofflimmern mit CHA2DS2-VASc** 6 Gabe von 1 2 mg Vita min K (Konakion) po * Risikofaktoren: mechanische Herzklappe, linksventrikuläre Auswurffraktion < 50%, Vorhofflimmern, Hyperkoagulabilität/Thrombophilie, St. n. Thromboembolie ** CHA2DS2-VASc: Punkte addieren für C = Herzinsuffizienz 1, H = Arterielle Hypertonie 1, A = Alter > 75 Jahre 2, D = Diabetes mellitus 1, S = Schlaganfall/TIA 2, V = vaskuläre Erkrankung (z. B. PAVK, St. n. Myokardinfarkt oder schwere Verkalkung der Aorta) 1, A = Alter Jahre 1, S = Frauen, wenn > 65 Jahre 1 DA = Dienstarzt; EUS = Endosonografie; FNP = Feinnadelpunktion; GIT = Gastrointestinaltrakt; INR = International Norm Ratio; LMWH = niedermolekulares Heparin; OAK = orale Antikoagulation; OP = Operation; TL = Teamleader; PPSB = Prothrombinkonzentrat (z. B. Beriplex); St. n. = Status nach; Tc-Hemmer = Thrombozytenaggregationshemmer; UFH = unfraktioniertes Heparin 88 89
46 90 Periinterventionelles Management bei Patienten unter neuen oralen Antikoagulantien (NOAK) Notfallmässiger Eingriff? ja Absprache mit OA Anästhesie und/oder mit DA Hämatologie, Tel. 111 nein nein Pause zwischen letzter Gabe und Intervention Wiederaufnahme nach Intervention Blutungsrisiko hoch* Blutungsrisiko niedrig bis mittel* egfr in ml/min. mit 2.5 mg nach 6 Std. mit 2.5 mg nach 6 Std. AM KSSG NICHT EMPFOHLEN 2 Tage 2 Tage > 24 Std. 2 Tage > Apixaban (Eliquis ) Prof. Dr. Miodrag Filipovic Prof. Dr. Wolfgang Korte Prof. Dr. Hans Rickli Intervention / Operation < 30 Absetzen 1 / Minimale Wartezeit bis Intervention: 3 Tage 3 Tage mit 110 mg nach 12 Std. mit 110 mg nach 12 Std. 3 Tage 4 Tage 36 Std. 2 Tage > Dabigatran (Pradaxa ) KONTRAINDIZIERT < 30 Absetzen 1 / Minimale Wartezeit bis Intervention: 3 Tage 5 Tage mit 15 mg nach 6 Std. mit 15 mg nach 6 Std. AM KSSG NICHT EMPFOHLEN 2 Tage 2 Tage > 24 Std. 2 Tage > Edoxaban (Lixiana ) < 30 Absetzen 1 / Minimale Wartezeit bis Intervention: 3 Tage 3 Tage mit 10 mg nach 6 Std. mit 10 mg nach 6 Std. mit 10 mg nach 6 Std. 2 Tage 2 Tage > 24 Std. 2 Tage > > 10 mg > 10 mg Rivaroxaban (Xarelto ) AM KSSG NICHT EMPFOHLEN < 30 Absetzen 1 / Minimale Wartezeit bis Intervention: 3 Tage 3 Tage Erhöhung auf Dosis vor Intervention* Blutungsrisiko hoch Blutungsrisiko niedrig bis mittel nach 1 2 Tagen nach 3 4 Tagen 1 Bei längerem Zeitintervall zwischen letzter Einnahme und Intervention Substanzwechsel auf Marcoumar (bei sehr langem Intervall) bzw. Heparin erwägen. * Zur Einteilung der Interventionen in niedriges, mittleres respektive hohes Blutungsrisiko siehe Tabelle «Periinterventionlles Management bei Patien ten mit Thrombozytenaggregationshemmung». Gilt auch für interventionelle Kardiologie inkl. Device-Implantationen. Vor Pulmonalvenenisolation bitte Rücksprache mit zuständigem Kardiologen! Nicht-invasive Diagnostik bei koronarer Herzkrankheit (KHK) Einleitung Die Koronarangiografie ist in der Diagnostik der koronaren Herzkrankheit (KHK) Gold-Standard. Daneben gibt es mehrere etablierte, nicht-invasive Untersuchungsmethoden. Dazu gehören die Fahrrad-Ergometrie, die Echokardiografie (Echo), die Myokard-Perfusion-Szintigrafie (MPS) sowie die Computertomografie (CT) und die kar diale Magnetresonanztomografie (MRI). Das Vorgehen in der Dia gnostik der KHK und Indikationen/Möglichkeiten res p. Limiten dieser nicht-invasiven Untersuchungsmethoden werden untenstehend erläutert. Welcher der oben er wähn ten Tests durchgeführt werden soll, muss indi viduell entschieden werden. Diagnostisches Vorgehen Asymptomatische Patienten Ziel der Risikostratifizierung bei asymptomatischen Individuen ist die Abschätzung des Langzeitrisikos für die Manifestation einer KHK und darauf basierend die Anwendung geeigneter primärprophylaktischer Massnahmen. Anhand der Anamnese und des AGLA-Risiko-Score lässt sich das individuelle kardiovaskuläre Gesamtrisiko für die nächsten 10 Jahre berechnen (siehe Seite 48 oder Entsprechend werden Patienten in drei verschiedene Risikogruppen eingeteilt (Tab. 1). Bei asymptomatischen Patienten (Tab. 1) mit niedrigem Risiko (10-Jahres-Risiko < 10%) ist das Ziel, vorhandene kardio vaskuläre Risikofaktoren frühzeitig gemäss den Richtlinien der Primärprophylaxe zu behandeln. Bei Patienten mit intermediärem Risiko (10-Jahres-Risiko unter 10% 20%) kann eine präklinische Atheromatose zusätzlich mithilfe des Atherosclerosis Imaging zur weiteren Risikostratifizierung diagnostiziert werden. 91
47 Asymptomatischer Patient ohne bekannte KHK mit Frage nach präklinischer Atheromatose; Männer > 45 Jahre; Frauen > 55 Jahre Bei Patienten mit hohem Risiko (10-Jahres-Risiko > 20%) sollte neben der Therapie der Risikofaktoren gemäss Kriterien der Sekundärprophylaxe aus prognostischen Gründen eine kardiologische Abklärung durchgeführt werden. Niedriges Risiko Score < 10% Anamnese kardiovaskuläres Risikoprofil: AGLA-Risiko-Score Intermediäres Risiko Score 10 19% Atherosclerosis Imaging Hohes Risiko Score 20% Symptomatische Patienten Bei symptomatischen Patienten mit typischer oder atypischer Angina pectoris ist das Risiko für das Vorliegen einer KHK erhöht (Tab. 2). In dieser Patientenkategorie empfiehlt sich ein nicht-invasiver Test. Die Belastung soll wenn immer möglich physiologisch, am besten mittels Ergometrie, durchgeführt werden. Alternativ dazu können auch bildgebende Untersuchungen mit physiologischer oder pharmakologischer (Adenosin, Dobutamin) Belastung erfolgen (Echo, MPS, cmri). Das Resultat des Belastungstestes erlaubt die Ermittlung der Nachtestwahrscheinlichkeit, und das therapeutische Prozedere konservativ vs. Koronarangiografie (Intervention) kann festgelegt werden (Tab. 4). 92 Konservativ Modifikation der Risikofaktoren gemäss Kriterien der Primärprophylaxe Calcium Score im CT Strahlendosis: 0.2 msv ABI-Index bei PAVK (IMT-Messung an den Karotiden) niedrig intermediär hoch Konservativ Dokumentierte, prognostisch relevante präklinische Atheromatose, somit Modifikation der Risikofaktoren gemäss Kriterien der Sekundärprophylaxe Aus prognostischen Gründen kardiologische Abklärung: Ischämie? Modifikation der Risikofaktoren gemäss Kriterien der Sekundärprophylaxe Tab. 1: National Screening for Heart Attack Prevention and Education (SHAPE) Program, modifiziert; Budoff MJ et al., Circulation 2006;114: Vortestwahrscheinlichkeit (VTW) des Vorliegens einer KHK bei symptomatischen Patienten nach Alter und Geschlecht* Typische Angina Atypische Angina Extrakardiale Thoraxschmerzen Alter Mann Frau Mann Frau Mann Frau > * Alle Werte bezeichnen den Anteil in % einer signifikanten KHK im Herzkatheter < 15% VTW: Management ohne weitere Tests 15 65% VTW: in der Regel Ergometrie 66 85% VTW: Ergometrie oder Belastungstest mit nicht-invasiver Bildgebung > 85% VTW: KHK sehr wahrscheinlich, damit keine Ergometrie aus diagnostischen, aber allenfalls aus prognostischen Gründen Tab. 2: Nicht-invasive Risikostratifizierung, ESC guidelines on the management of stable coronary artery disease
48 Symptomatischer Patient und Frage nach hämodynamisch relevanten Koronarstenosen resp. KHK Anamnese Klinik atypisch/typisch? Alter, Geschlecht, Klinik* Ischämiediagnostik, Ischämielokalisation Ergometrie als Primärdiagnostikum Stress-Echokardiografie Szintigrafie/PET Nachtestwahrscheinlichkeit** Stress-MRI Niedriges Risiko** Konservativ Modifikation der Risikofaktoren gemäss Kriterien der Primär- bzw. Sekundärprophylaxe Intermediäres Risiko** Bei inkonklusivem Ischämietest Entscheid zum konservativen Vorgehen mit konsequenter Behandlung der kardiovaskulären Risikofaktoren +/ invasiver Abklärung oder in selektionierten Fällen Durchführung einer Hochdosis-CT-Angiografie erwägen. CT-Angiographie Strahlendosis: msv Normokarder Rhythmus Ca-Score < 400 (keine schwere Kalzifikation) negativ Tab. 3: Diagnostisches Vorgehen bei symptomatischen Patienten * Vortestwahrscheinlichkeit Tab. 2, siehe vorherige Seite ** Nachtestwahrscheinlichkeit Tab. 4, siehe nächste Seite Hohes Risiko** Koronarangiografie + Intervention Nachtestwahrscheinlichkeit nicht-invasive Risikostratifizierung für das Vorliegen einer KHK Hohes Risiko (> 3% jährliches Mortalitätsrisiko) 1. Schwer eingeschränkte systolische linksventrikuläre Funktion (LVEF < 35%) 2. Hohes Risiko des Treadmill Score* (Score 11) 3. Stress-induzierter, grosser Perfusionsdefekt (v.a. anterior) 4. Grosser, fixierter Perfusionsdefekt mit einer linksventrikulären Dilatation oder erhöhter Lung Heart Ratio (LHR) in der Szintigrafie (als Zeichen der Lungenstauung) 5. Stress-induzierter, moderater Perfusionsdefekt mit einer linksventri kulären Dilatation oder erhöhter Lung Heart Ratio (LHR) in der Szintigrafie 6. Echokardiografisch dokumentierte Wandbewegungsstörung (> 2 Segmente) in der Low-Dose-Dobutamin-Stress-Echokardiografie (< 10 mg/kg/min.) oder bei einer tiefen Herzfrequenz (< 120/Min.) 7. Dokumentation eines grossen Ischämieareals in der ergometrischen und/oder Dobutamin-Stress-Echokardiografie Intermediäres Risiko (1 3% jährliches Mortalitätsrisiko) 1. Leicht bis mittelschwer eingeschränkte systolische linksventrikuläre Funktion (LVEF = 35% bis 49%) 2. Intermediäres Risiko des Treadmill Score* ( 10 bis + 4) 3. Stress-induzierter, moderater Perfusionsdefekt ohne linksventrikuläre Dilatation oder erhöhte Lung Heart Ratio (LHR) in der Szintigrafie 4. Limitierter Nachweis einer Ischämie in der Stress-Echokardiografie mit induzierbaren Wandbewegungsstörungen nur bei hoher ergometrischer Belastung oder Dobutamindosis in zwei oder weniger Wandsegmenten Niedriges Risiko (< 1% jährliches Mortalitätsrisiko) 1. Niedriges Risiko des Treadmill Score* (Score 5) 2. Normale myokardiale Perfusion oder umschriebener myokardialer Perfusionsdefekt in Ruhe oder unter Belastung 3. Normale Stress-Echokardiografie oder nur minimale Wandbewegungsstörungen unter Belastung * Treadmill Score = Ergometriezeit (Min.) 5x ST-Streckensenkung (mm) 4x AP-Index (keine AP = 0; nicht limitierende AP = 1; limitierende AP = 2) Tab. 4: Management vom Patienten mit stabiler koronarer Herzkrankheit (J Am Coll Cardiol 2012;60:e44 164) 94 95
49 Möglichkeiten, Indikationen und Limiten der nicht-invasiven Untersuchungen Fahrrad-Ergometrie Möglichkeiten Ischämienachweis bei einer aussagekräftigen Ergometrie, d.h. bei genügender körperlicher Belastungsfähigkeit, bei Doppelprodukt > (HFmax x BDsystmax) Indikationen Intermediäres Risiko (Klasse I ESC und AHA) Tiefes und hohes kardiovaskuläres Risiko (Klasse IIb) Limiten respektive fehlende Aussagekraft der Ergometrie 1 mm ST-Streckensenkung in Ruhe WPW, Linksschenkelblock (LSB), Schrittmacher-Rhythmus Digoxin-Therapie Stress-Echokardiographie Technik Mittels einer ergometrischen oder pharmakologischen Belastung kann die Kontraktilität des linken Ventrikels visualisiert werden. Nimmt die Kontraktilität in einem oder mehreren koronaren Versorgungsgebieten ab, entspricht dies einem indirekten Ischämienachweis und erlaubt Rückschlüsse auf die Lokalisation der koronaren Herzkrankheit (Stenosen). Indikationen Nicht-konklusive Ergometrie (z. B. geringes Doppelprodukt, vorbestehende EKG-Veränderungen) Ischämienachweis bei limitierter körperlicher Belastbarkeit Präoperative Risikostratifizierung bei nicht-herzchirurgischen Hochrisiko-Operationen Viabilitätsnachweis vor evtl. Revaskularisation Limiten der Stress-Echokardiographie Ungenügende Echoqualität (COPD, adipöser Patient) Kontraindikationen gegen Dobutamin Kardiale Magnetresonanztomografie (MRI) Technik Die kardiale Magnetresonanztomografie generiert Schichtaufnahmen des Herzens mithilfe starker Magnetfelder und Radiowellen. Im Gegensatz zur Computertomografie wird im MRI keine Röntgenstrahlung oder andere ionisierende Strahlung erzeugt oder genutzt. Die MRI eignet sich besonders zur Darstellung von Struktur und Funktion des Herzens und erlaubt nach intravenöser Kontrastmittelapplikation sowohl die Beurteilung der Koronarperfusion (Ruhe/ Belastung) als auch die Identifizierung und Quantifizierung von infarziertem Myokard. Möglichkeiten Links- und rechtsventrikuläre Funktionsdiagnostik (Gold-Standard) Myokard-Diagnostik (Viabilität, Entzündung, Myopathie) Ischämiediagnostik (Regadenoson-/Adenosin-/Dobutaminstress) Darstellung von Klappenfunktion und -morphologie (Flussmessungen) Gefässdarstellung (z. B. vor Pulmonalvenenisolation, fehlmündende Pulmonalvenen, Aortenstenosen) Perikarddiagnostik Indikationen Identifikation des Ausmasses von infarziertem Myokard durch Anreicherung des Kontrastmittels Gadolinium in der Spätphase (Late Gadolinium Enhancement LGE) zur Indikationsstellung einer eventuellen Revaskularisation nach einem Myokardinfarkt (Viabilitätsnachweis). Ischämiediagnostik Vitalitätsdiagnostik vor allfälliger Intervention/Bypass-Operation Komplexe kongenitale Vitien 96 97
50 Entzündliche oder metabolische Herzmuskelerkrankungen Tumore Limite Herzschrittmacher- und ICD-Träger (abhängig vom Modell) Mechanische Herzklappen, die vor 1980 implantiert wurden Herzrhythmusstörungen (Triggerprobleme) Myokardperfusionsszintigrafie (MPS) Technik Die Myokardperfusionsszintigrafie erlaubt die Beurteilung der funktionellen Perfusion in Ruhe und unter Belastung und somit die Diagnose von Ischämien und Mykardnarben. Die Perfusionsdefekte werden semiquantitativ gescored und der summed difference score berechnet, was eine Risikostartifizierung erlaubt. Ausserdem kann mittels EKG-Triggerung eine Aussage zur Motilität sowie zu den Funktionswerten (ESV,EDV und LVEF) genacht werden. Ergänzt wird die Untersuchung durch die Bestimmung der koronaren Kalklast (Agatston-Score), was eine weitere Risikostratifizierung erlaubt. Bei normaler Perfusion unter Belastung sind kardiale Ereignisse wie Myokardinfarkt und Tod selten. Die FDG-PET ermöglicht in ausgewählten Fällen eine validierte Aussage über die Gewebeviabilität vor einer eventuellen Revaskularisation. Indikationen Nicht-konklusive Ergometrie Risikostratifizierung (z. B. präoperativ) Beurteilung der funktionellen Relevanz bei bekannten Koronar stenosen Koronar-CT-Angiografie und Calcium-Scoring Technik Mit EKG-gesteuerter Zeitauflösung erreichen moderne Multislice- Computertomografen eine hohe örtliche Auflösung. Die Strahlenbelastung der Koronar-CT-Angiografie beträgt mit der modernen Technik ca msv. Die Bestimmung der koronaren Kalklast er - folgt in einer nativen Niedrigdosis-CT von 0.2 msv ent sprechend dem Calcium-Score (Agatston-Score). Mit einmaliger Kontrast mittelgabe werden anschliessend der Koronarbaum und die intra-/extrakardiale Morphologie dargestellt sowie die linksventrikuläre Funktion berechnet. Die Untersuchungsdauer beträgt etwa 15 Min. Möglichkeiten der Koronar-CT-Angiografie Ausschluss einer KHK bei tiefer/intermediärer Vortestwahrscheinlichkeit bis circa Prozent gemäss Tabelle 2 Beurteilung von Koronaranomalien Komplexe, angeborene Fehlbildungen Calcium-Scoring zur Bestimmung der koronaren Kalklast Der Calcium-Score quantifiziert die Menge an Verkalkung in den Koronararterien (Agatston-Score) und korreliert mit der Wahrscheinlichkeit des Vorliegens einer KHK (keine Aussage über Schweregrad der KHK, reine Risikostratifizierung/Messung der Kalklast). Das Problem der Messung liegt in der tiefen Spezifität für den Nachweis einer KHK, verglichen mit der Koronarangiografie. Eine in der CT nachgewiesene Verkalkung bei älteren Patienten erlaubt keine Aussage über eine Durchblutungsstörung (verkalktes Gefäss ohne hämodynamisch relevante Stenose. Indikationen für Koronar-CT-Angiografie Bei einem selektionierten Patientengut (entsprechend Tab. 3) Präoperative Bildgebung der Koronarien vor valvulärer oder vitien-korrigierender Herzoperation Verdacht auf Koronaranomalie Nicht indiziert ist die Herzuntersuchung mittels CT Bei Hochrisikopatienten gemäss AGLA-Score und/oder mittlerer bis hoher VTW gemäss Tabelle
51 Zur Verlaufsbeurteilung einer KHK Bei bestehenden komplexen Herzrhythmusstörungen Links Dr. Lucas Jörg Prof. Dr. Hans Rickli Dr. Olaf Chan-Hi Kim Prof. Dr. Sebastian Leschka Prof. Dr. Dr. Flavio Forrer Stabile Angina pectoris Unter dem Begriff «stabile Angina pectoris» wird die chronische koronare Herzkrankheit (KHK) verstanden, d.h. alle Situationen ausserhalb des akuten Koronarsyndroms (ACS). Therapie-Prinzip Es werden zwei Ziele verfolgt: Verbesserung der Prognose durch Prävention von Myokardinfarkt, Herzinsuffizienz und Tod Reduktion der Symptome bzw. Verbesserung der Lebensqualität Diese Ziele werden erreicht durch allgemeine nicht-medikamentöse Massnahmen, eine individualisierte medikamentöse Therapie sowie Revaskularisationseingriffe bei selektionierten Patien ten. Voraussetzungen für eine angemessene Therapie sind eine adäquate Diagnostik und Risikostratifizierung mittels nicht-invasiver Methoden und meist Koronarangiografie (siehe Kapitel Nicht-invasive Diagnostik bei KHK). Die Angriffspunkte der medikamentösen Therapie betreffen: Koronaratherosklerose «Umbauprozesse» des linken Ventrikels nach Infarkt (Remodeling) Myokardiale Ischämie Substanzen, die auf Ebene der Koronaratherosklerose und des Remodelings wirken und somit die Biologie des Krankheitsprozess direkt beeinflussen, haben in der Regel einen prognostischen Nutzen, während dies für die antiischämisch wirksamen Medikamente nicht gilt (Ausnahme: Betablocker bei Postinfarkt-Patienten sowohl mit antiischämischer als auch Anti-Remodeling-Wirkung)
52 102 Die interventionelle (percutaneous coronary intervention; PCI) oder chirurgische (aortokoronarer Bypass) Revaskularisation stellt eine rein mechanische Therapie dar und benötigt ergänzend immer Lebensstilanpassungen (regelmässige körperliche Aktivität, Gewichtsreduktion, gesunde Ernährung, Nikotinabstinenz) und eine medikamentöse Behandlung. Revaskukarisationseingriffe sind sehr effektiv zur Linderung der Symptomatik, haben aber nur in bestimmten Konstellationen einen prognostischen Effekt. Medikamentöse Therapie Substanzen, welche die Koronaratherosklerose beeinflussen Thrombozytenaggregationshemmer und orale Antikoagulation Aspirin 100 mg/tag für alle Patienten mit KHK, bei Aspirin-Allergie Desensibilisierung in Erwägung ziehen Zusätzlich Clopidogrel (Plavix) 75 mg/tag für 6 Monate nach PCI (Dauer in bestimmten Fällen weniger lang, muss in jedem Fall vom Interventionalisten genau festgelegt sein) und eventuell nach aortokoronarer Bypass-Operation Prasugrel (Efient) 10 mg/tag oder Ticagrelor (Brilique) 2x 90 mg/tag für 12 Monate nach PCI im Rahmen eines akuten Ereignisses (STEMI, NSTEMI). Bei stabiler KHK noch nicht genügend Daten zu Prasugrel und Ticagrelor. Deshalb nur bei Kontraindikation für Clopidogrel einsetzen. Bei erhöhtem gastrointestinalem Blutungsrisiko Einsatz eines PPI, in erster Linie Pantoprozol (Pantozol) empfohlen Orale Antikoagulation: Falls eine Indikation für eine orale Antikoa gulation besteht (Vorhofflimmern, mechanische Klappenprothese, St. n. Lungenembolie u.a.), ist die orale Antikoagulation ohne Aspirin oft ausreichend; bei Risiko patienten mit stabiler KHK (insbesondere St. n. Stent) ist die Kombination orale Antikoagulation + Aspirin 100 mg/ Tag zu er wägen. Die Datenlage ist diesbezüglich aber unklar; Vorgehen muss immer individuell (thrombotisches Risiko vs. Blutungs risiko) diskutiert werden. Nach PCI wird die Dauer einer Triple-Therapie (orale Antikoagulation kombiniert mit Aspirin und Clopidogrel) bzw. die Dauer der anschliessenden dualen Therapie (orale Antikoagulation kombiniert mit Clopidogrel) in Abhängigkeit vom Stent-Typ, dem thromboembolischen Risiko und dem Blutungsrisiko individuell festgelegt (Triple-Therapie in der Regel ein Monat, maximal 6 Monate, dies aber nur in Ausnahmefällen). Nicht-Vitamin-K-Antagonisten-orale Antikoagulantien (NOAKs): Triple- Therapie mit Aspirin und Clopidogrel nach PCI möglich (Dauer analog wie bei Vitamin-K-Antagonisten, NOAK jeweils in reduzierter Dosie rung; ebenfalls individuelle Festlegung durch das interventionelle Team). Lipid-modifizierende Therapie Grundsätzlich bei allen Patienten mit KHK, auch bei Cholesterinwerten im Ziel-Bereich ( tiefe Dosis eines gut verträglichen Präparats) Primär Statine mit Ziel-LDL-Cholesterin < 1.8 mmol/l Zusätzlich Ezetimibe (Ezetrol) 10 mg möglich, senkt das LDL-Choleste rin zusätz lich und bringt zusätzlichen prognostischen Nutzen Details zu Substanzen und Dosierungen siehe Kapitel Dyslipidämien Substanzen, die das linksventrikuläre Remodeling beeinflussen Für alle Patienten/-innen mit durchgemachtem Infarkt und eingeschränkter linksventrikulärer Pumpfunktion (left ventricular ejection fraction; LVEF < 40%) Betablocker ACE-Hemmer; bei Unverträglichkeit: Angiotensin-Rezeptor-Blocker Zusätzlich Eplerenon bei Patienten mit LVEF < 40% 3 14 Tage nach Myokardinfarkt und guter Background-Therapie (ACE-Hemmer und Betablocker); später nach Infarkt: LVEF < 35% + NYHA II Eplerenon (Inspra), LVEF < 35% + NYHA III Spironolacton (siehe Kapitel Herzin suffizienz) ACE-Hemmer auch für Patienten ohne früheren Infarkt, falls nicht low risk (siehe Tabelle Seite 104), insbesondere bei arterieller Hypertonie, aber nur lipophile ACE-Hemmer (Perindopril, Ramipril), da in dieser Situa tion primär ein Effekt auf die Athero sklerose vermutet wird. 103
53 104 Medikamente mit günstigem Einfluss auf das linksventrikuläre Remodeling nach Myokardinfarkt Medikament Dosis Indikation Kommentar ACE-Hemmer Enalapril Lisinopril Ramipril Trandolapril ARB Valsartan Losartan Candesartan mg mg 5 10 mg 2 4 mg mg 150 mg 8 16 (32) mg Arterielle Hypertonie Asymptomatische linksventrikuläre Dysfunktion (LVEF < 40%) Herzinsuffizienz Niereninsuffizienz Diabetes Alle anderen Patienten, die nicht low risk sind (low risk = revaskularisiert und gut kontrollierte Risikofaktoren) Alternative zu ACE-Hemmer bei ACE-Hemmer- Intoleranz Eplerenon mg (Früh) nach Myokardinfarkt und alle folgenden Bedingungen: LVEF < 40% Therapie mit ACE-Hemmer und Betablocker Herzinsuffizienz oder Diabetes Keine relevante Niereninsuffizienz, Hyperkaliämie Betablocker Metoprolol Bisoprolol Nebivolol Carvedilol (Kein Atenolol) mg 5 10 mg 5 10 mg mg Nach Myokardinfarkt Asymptomatische linksventrikuläre Dysfunktion Herzinsuffizienz ARB = Angiotensin-Rezeptor-Blocker; UEW = unerwünschte Wirkungen UEW: Reizhusten, Angioödem, Hyper kaliämie, Verschlechterung Nierenfunktion Überwachung Kalium und Nierenfunktion UEW: wie ACE- Hemmer ausser Reizhusten (Cave: Angioödem auch möglich) UEW: erhöhtes Hyperkaliämierisiko Überwachung von Kalium und Nierenfunktion Kontraindiziert bei Asthma, Sick Sinus, höhergradigem AV-Block Vorsicht bei COPD, PAVK, AV-Block I Antiischämische Therapie Prinzip Das Auftreten einer myokardialen Ischämie hängt von der Balance zwischen Sauerstoffzufuhr und -bedarf ab. Im Falle einer signifikanten Stenose ist die Zufuhr bzw. die Zufuhrreserve reduziert, sodass es bei einem Anstieg des Bedarfs im Rahmen körperlicher Belastung zu einer Ischämie kommt. Folgende Faktoren bestimmen den Sauerstoffbedarf des linken Ventrikels: Kontraktilität Herzfrequenz Wandspannung Grundsätze der Behandlung Individualisierte Therapie Verschiedene Kombinationen möglich; Auswahl gemäss Wirkung und Nebenwirkungsprofil (siehe Tabelle Seite 96 97) Die Dosierung der einzelnen antianginösen Substanz sollte vor der Ergänzung durch ein zweites Medikament zuerst nach oben titriert werden. Persistierende Beschwerden trotz antianginöser Zweiertherapie können in der Regel durch den Zusatz einer dritten antianginösen Substanz nur noch wenig beeinflusst werden. Diese Patienten profitieren in der Regel von einer kathetertechnischen oder chirurgischen Revaskularisation, falls eine solche möglich ist. Invasive Therapie Eine invasive Abklärung ist bei den meisten Patienten mit Verdacht auf KHK und unbekanntem Koronarstatus sinnvoll. Eine Revaskularisation muss bei Hinweisen auf eine mittelgrosse oder grosse myokardiale Ischämie (Revaskularisation aus prognostischen Gründen) und/oder bei fehlendem Ansprechen der Symptomatik auf eine medikamentöse antiischämische Therapie (symptomatische Indikation) erwogen werden. Indikationen für eine Koronarangiografie bzw. PCI oder Bypass- 105
54 Operation (falls Koronarstatus schon bekannt) können mit dem Dienstarzt Kardiologie und den interventionell tätigen Kaderärzten intern besprochen werden. Anmeldungen für elektive Untersuchungen von extern sind an die ärztliche Leitung der Klinik für Kardiologie zu richten. Antiischämische Medikamente Medikament Dosis Indikation Kommentar Betablocker Atenolol Metoprolol Bisoprolol Kalziumkanalblocker Amlodipin Nifedipin Verapamil Diltiazem Kurz wirksame Nitrate Glyceroltrinitrat Lang wirksame Nitrate Isosorbidmononitrat Isosorbiddinitrat Glyceroltrinitrat (transdermal) Molsidomin 100 mg mg 5 10 mg 5 10 mg mg 2x 120 mg; 2x 240 mg 2x 90 mg; 1x 240 mg (max. 360 mg) Kapseln 0.8 mg 2 Hübe (0.8 mg) mg 1 2x 100 mg 5 10 mg/24 Std. Retardierte Form, 1 3x 8 mg (meist 2x/d) First-line Antianginosum Alternative zu Betablocker (auch First-line Antianginosum) Kombination von Dihydropyridin* mit Betablocker Kalziumkanalblocker auch bei vermuteter vasospastischer Komponente Behandlung des akuten Anfalls Dauertherapie, Kombination mit anderen Antianginosa Als 24h-Therapie (1 3 Dosen; keine Toleranzentwicklung) Eine Dosis im Nitratfreien Intervall Von ca. 15% aller Patienten nicht toleriert Betablockade anhand Ruhe und Belastungsfrequenz überprüfen UEW: Flüssigkeitsretention (Knöchelödeme), Kopfschmerzen, Obstipation (Verapamil) UEW: Kopfschmerzen, Schwindel, Flush Nitrat-freies Intervall beachten Kontraindiziert bei gleichzeitiger PDEI-Therapie UEW wie Nitrate Nicorandil 2x mg Add-on-Therapie, kann mit Nitraten und Molsidomin kombiniert werden Ranolazin 2x mg Add-on-Therapie zu Betablocker (Cave: Sotalol wegen Interaktion), Amlodipin (Cave: Diltiazem, Verapamil wegen Interaktion), Nitraten Ivabradin 2x mg Patienten im Sinusrhythmus, die Betablocker nicht tolerieren, bei denen Betablocker kontraindiziert sind oder bei denen Betablocker die Herzfrequenz ungenügend senken Vorsicht bei Patienten mit schwerer Angina (CCS 3): in dieser Situation Ausbau Betablockade und/ oder Revaskularsation prüfen * Amlodipin und Nifedipin = Dihydropyridine UEW = unerwünschte Wirkungen; PDEI = Phosphodiesterase-Inhibitoren UEW: gastrointestinale Ulcera, ansonsten wie Nitrate Kontraindiziert mit PDEI UEW: Übelkeit und Schwindel Kontraindiziert bei schwerer Nieren- oder Leberinsuffizienz, gleichzeitiger Gabe von Klasse-III-Antiarrhythmika (ausser Amiodaron) Interaktionspotenzial (CYP3A4) UEW: Phosphene (häufig, aber transient) Kontraindiziert bei Sick-Sinus, akuter KHK Device-Therapie der therapierefraktären Angina bei Patienten ohne Revaskularisationsoptionen Diese Therapien (Rückenmarksstimulation, Koronarsinus-Stent) sind noch in Entwicklung und nur in ausgewählten Einzelfällen eine Option. PD Dr. Micha Maeder Prof. Dr. Hans Rickli
55 Akutes Koronarsyndrom (ACS) Initiales Vorgehen Verdachtsdiagnose Akutes Koronarsyndrom (ACS). Zeit ist Myokard! Wichtigste Massnahme: Verzögerungszeiten minimal halten! Definitionen Leitsymptom Thoraxschmerz Arbeitsdiagnose Akutes Koronarsyndrom EKG Persistierende ST-Hebung* ST/T- Veränderungen Normal oder unspezifisch Labor Troponin Anstieg/Abfall Troponin normal Endgültige Diagnose STEMI NSTEMI Instabile AP * 1 mm in Extremitäten-Ableitungen < 2 mm in Brustwandableitungen 108 Empfehlungen für die initiale Diagnostik Arbeitsdiagnose basiert auf typischem Thoraxschmerz von > 20 Minuten Dauer (trotz Nitroglyzerin) Schmerzbeginn erfragen/erfassen; Blutdruck/Puls erfassen, Fokus auf kardiopulmonalen Status, Herzinsuffizienzzeichen? Frühere Blutungen? 12-Ableitungs-EKG sobald als möglich (< 10 Minuten nach erstem medizinischen Kontakt); evtl. zusätzliche Ableitungen bei hohem V.a. posterioren Infarkt (V7 V9 > 0.05 mv) Kontinuierliche EKG-Überwachung so früh als möglich bei allen Patienten mit V.a. ACS 109
56 Blutentnahme für kardiale biochemische Marker (Troponin, CK- Bestimmung) routinemässig aber Resultate nicht abwarten für Entscheid zur Reperfusionsbehandlung bei STEMI Echokardiografie kann bei unsicheren Fällen helfen zur Diagnosesicherung, soll aber den Transfer zu Angiografie nicht verzögern Diagnose Myokardinfarkt basiert auf Anstieg kardialer Biomarker (vorzugsweise Troponin) mit mindestens einem Wert > 99-ste Perzentile des oberen Referenzwertes + mindestens eines der folgenden Kriterien: Ischämiesymptome, neuer LSB, signifikante ST-T- Veränderungen, Entwicklung einer pathologischen Q-Zacke, neue Wandbewegungsstörung linker (oder rechter) Ventrikel. Initiale Therapie 2 4 l Sauerstoff, falls Sättigung < 95%, bei Atemnot oder akuter Herzinsuffizienz Oberkörper 30 hochlagern Angina pectoris (AP)/Ischämiezeichen: max. 3 Sprühstösse/Kaukapseln Nitroglyzerin, bei persistierenden/rezidivierenden Schmerzen µg/min. iv als Dauerinfusion per Spritzenpumpe, falls BDsys > 100 mmhg Persistierender Schmerz: Morphin 0.1 mg/kg iv, evtl. gleichzeitig Antiemetika zur Reduktion von Nausea Gerinnung: Falls nicht vorbestehend: ASS 250 mg iv oder po Falls keine vorbestehende duale Plättchenhemmung: Ticagrelor (Brilique) 2x 90 mg po Ladedosis, alternativ Prasugrel (Efient) 6 x 10 mg Ladedosis (KI: St. n. CVI/TIA, OAK, Alter > 75 Jahre oder < 60 kg schwer), falls beides nicht verfügbar: Clopidogrel 600 mg po Unfraktioniertes Heparin (UFH) 5000 IE als Bolus, danach gemäss ACS-Schema und Anpassung gemäss Operateur bzw. DA Kardiologie Bei Tachyarrhythmie oder Hypertonie Betablocker iv (Metoprolol 5 mg max. 3x innert 15 Min.), falls hämodynamisch stabil und keine Kontraindikation (u.a. Schock, BD sys < 100 mmhg, Kokain, HF < 45/Min., PQ-Intervall > 0.24 Sek., schweres Asthma) 110 Monitoring EKG, Puls, Blutdruck, SaO2, Schmerzscore. Alle Verzögerungszeiten dokumentieren, Patient in das AMISplus-Register aufnehmen (weitere Informationen auf STEMI (ACS mit persistierender ST-Hebung) Bevorzugte Therapie: primäre perkutane Intervention (PCI) Sofortige Kontaktierung des DA Kardiologie über Tel Für Transfer: Bolus von 5000 IE unfraktioniertes Heparin iv (siehe Abschnitt «Initiale Therapie»), falls noch nicht gegeben GP-IIb/IIIa-Antagonist, nach Rücksprache mit DA Kardiologie: in der Regel Tirofiban, Beginn im HK-Labor bei hoher Thrombus-Last (Dosierung siehe Tabelle Seite 121) Verzögerungen Erster medizinischer Kontakt bis EKG und Diagnose Erster medizinischer Kontakt bis primäre PCI (door to balloon) im KSSG Erster medizinischer Kontakt in auswärtigem Spital/Rettungsdienst bis primäre PCI im KSSG Ziel <_ 10 Minuten <_ 60 Minuten <_ 90 Minuten (akzeptabel bis 120 Minuten) Systemische Thrombolyse nur, wenn Patient < 75 Jahre Schmerzbeginn < 3 Std. Kein kardiogener Schock Tiefes Blutungsrisiko: Rapilysin (Reteplase) 2x 10 IU iv im Abstand von 30 Min. oder Metalyse (Tenecteplase) gewichtsadaptiert 1x iv; Dauerinfusion Heparin für Std., Beginn mit 12 IE/kg, maximal 1000 IE/Std., Ziel PICT 111
57 Vorgehen bei Verdacht auf Akutes Koronarsyndrom zum Inhaltsverzeichnis Zeit ist Myokard Ziel: 10 Min. von Verdacht bis Anmeldung PCI bei STEMI (DA Kardiologie KSSG ) 12-Kanal-EKG STEMI Sofortige PCI: Dienstarzt Kardio via Tel , oder Fax Spital ohne Katheterlabor: Verlegung in Zentrumsspital ja ST-Hebung > 1 mm in Extremitäten- oder > 2 mm in Brustwandableitungen? oder (vermutlich) neu aufgetretener Linksschenkelblock? nein Wiederholung 12-Kanal-EKG nach 10 Min. Monitoring EKG, Blutdruck, Puls, SaO2, Schmerzscore Troponin, Kreatinin, Hb, Tc, PTT, Quick/INR, Lipide* > 1 Kriterium gemäss ESC-Guidelines Myoc. Revasc 2014 ist auch AP > 20 Min., in Ruhe, nachts, wiederholt, nein instabil früh nach Myokardinfarkt Erhöhtes Troponin Dynamische ST-Veränderungen oder ST-Senkung Rhythmogen instabil Diabetes mellitus, Linksherzinsuffizienz (EF 40%) Niereninsuffizienz (GRF < 60 ml/min/1.73 m 2 ) GRACE Score > 140 (siehe Tabelle 7) ja Koro/PCI innert Std.** Instabile Angina pectoris? Weiteres Vorgehen je nach Klinik 112 Atmung O2 bis SaO2 94, Oberkörper 30 hochlagern Kreislauf Bei Tachyarrhythmie oder Hypertonie: Metoprolol 5 mg über 1 Min. iv, max. 3x innert 15 Min. (KI: bei Kokain, Schock, BDsys < 100 mmhg, HF < 45/Min., PQ-Intervall > 0.24 Sek., schweres Asthma) Gerinnung Falls nicht vorbestehend: ASS 250 mg iv/po Brilique (Ticagrelor) 2x 90 mg po 5000 IE Liquemin iv Alternativen siehe Initiale Therapie/Gerinnung (siehe Seite 109) Schmerz Bei AP: max. 3 Sprühstösse/Kaukapseln Nitroglyzerin, dann μg/min. iv falls BDsys > 100 mmhg Morphin 0.1 mg/kg KG iv (Cave bei instabiler AP resp. NSTEMI), evtl. Tropisetron (Navoban) 2 mg in 100 ml NaCl 0.9% über 15 Min. iv Notfall-Koro/PCI (Kontakt s. oben) NSTEMI ja 1 Kriterium Persistierende Sz oder > 20 Min. Hämodynamisch instabil Troponin erhöht? nein nein Rhythmusmonitoring Erneut Troponin + EKG 6 Std. nach Sz- resp. Symptombeginn; bei hochsensitivem Troponin nach 3 Std. EKG unauffällig Troponin negativ Beschwerdefrei ja nein ja Ad MIPS für Std. DA Kardiologie via Tel verbinden lassen Fax oder [email protected] Stationäre Aufnahme Gerinnung ASS 100 mg/tag po NSTEMI: weiter mit Ticagrelor (Brilique) 2x 90 mg/tag po (Dauer: Siehe S. 119) STEMI: Ticagrelor (Brilique ) weiter (KI: (N)OAK) oder Wechsel auf Prasugrel (Efient ) mit einmaliger Ladedosis 6x 10 mg p.o. am Tag nach der Intervention (KI: St.nCVI/TIA, Alter, (N)OAK, Alter > 75 Jahre oder < 60 kg schwer) (Dauer: Siehe S. 119) Plasmatische Gerinnungshemmung: Heparin-Infusion am Abend der PCI stoppen, falls nicht aus anderen Gründen (Vorhofflimmern, mechanische Klappe, sehr grosser Vorderwandinfarkt mit Gefahr von apikalem LV-Thrombus) Thromboseprophylaxe gemäss Thromboembolieprophylaxe in der Medizin Seite 80 Blutdruck Betablocker (z. B. Concor 2.5 mg po, ab 2. Tag falls toleriert 5 mg/tag po); relative KI: HF < 60, BDsys < 90 mmhg, schwere Herzinsuffizienz, PQ-Zeit > 0.24 msek., höhergradiger AV-Block, schwere COPD, Asthma bronchiale ACE-Hemmer (z. B. Zestril 2.5 mg 1x/Tag po) oder AT-Rezeptorblocker (z. B. Valsartan 40 mg 1x/Tag po) Cholesterin Statin-Therapie (z. B. Crestor 10 mg oder Sortis 40 mg 1x/Tag po) innerhalb 24 Std. Frühmobilisation; kardiale Rehabilitation planen (siehe Seite 299) Anmelden AMIS-Register Ischämie in der Ergometrie Hohes kardiovaskuläres Risiko Linksventrikuläre Dysfunktion Alternative Diagnose erwägen nein ja Koro elektiv: Brief, an [email protected] oder Fax * Lipide: Gesamt-, LDL-, HDL-Cholesterin und Triglyzeride ** für Patienten, welche w.mgl. innert 24 Stunden invasiv behandelt werden sollten: Anstieg oder Abfall des kardialen Troponins vereinbar mit Myokardinfarkt, Dynamische ST- oder T-Wellenveränderungen (symptomatisch oder stumm), GRACE-Score > 140 Risikofaktoren: arterielle Hypertonie, Diabetes mellitus, Dyslipidämie, Familienanamnese < 55 J., < 65 J., Nikotin AP = Angina pectoris; ASS = Acetylsalizylsäure; BD = Blutdruck; DA = Dienstarzt; HF = Herz frequenz; KHK = koronare Herzkrankheit; KG = Körpergewicht; KI = Kontraindikation; Koro = Koronarangiographie; LMWH = niedermolekulares Heparin; LVEF = linksventrikuläre Auswurffraktion; MIPS = medizinische Intensivstation; PCI = perkutane Koronarintervention; Sz = Schmerz; Tc = Thrombozyten; UFH = unfraktioniertes Heparin 113
58 Rescue PCI bei erfolgloser Lyse Anhaltende AP Min. nach Lysebeginn < 50% Rückgang der max. ST-Hebung im EKG Hämodynamische Verschlechterung oder Schock Sofortige Rücksprache mit dem DA Kardiologie via NSTEMI (ACS ohne ST-Hebung, Troponin positiv) Patienten mit NSTEMI-ACS stellen ein sehr heterogenes Patientenkollektiv mit einer sehr variablen Prognose dar. Mortalität und Morbidität von Hochrisiko-NSTEMI-ACS-Patienten sind hoch und vergleichbar mit derjenigen von STEMI-Patienten innerhalb der ersten Monate. Eine frühe Risikostratifizierung ist entscheidend für die Wahl der medikamentösen und invasiven Strategie. Hauptziele der Koronarangiografie und Revaskularisation bestehen in der Behandlung von Symptomen und der Verbesserung der Kurz- und Langzeitprognose. Empfehlungen für Diagnose und Risikostratifizierung Rasches «Rule-out»-Protokoll anwenden, falls hochsensitives Troponin verfügbar (siehe Tabelle Seite 115) Echokardiografie mit Frage nach regionaler oder globaler linksventrikulärer Dysfunktion und zur allfälligen Differentialdiagnose Koronar-CT in Betracht ziehen, bei unklaren Thoraxschmerzen, inkonklusivem Troponin und tiefer Wahrscheinlichkeit einer KHK Rasches «Rule-out»-Protokoll bei Verdacht auf NSTEMI hs-troponin nicht erhöht Schmerz > 6 Std. Schmerz < 6 Std. hs-troponin ohne Änderung Schmerzfrei, GRACE-Score < 140, Differentialdiagnose ausgeschlossen Entlassung/ Belastungstest Akuter Thoraxschmerz Erneute Bestimmung hochsensitives (hs) Troponin nach 3 Stunden** hs-troponin Änderung Invasives Management Stark von der Norm abweichendes Tn*** + klinische Präsentation hs-troponin erhöht* hs-troponin ohne Änderung Differentialdiagnose bearbeiten * erhöhtes hs-troponin: Standort St.Gallen: 30 ng/l Standort Flawil / Rorschach: 19 ng/l (POCT-Gerät 23ng/l) ** hs-troponin-änderung nach 3 Stunden: Standort St.Gallen: 10 ng/l (falls 1. Trop < 30ng/l), 20 ng/l (falls 1. Trop 30ng/l) Standort Flawil / Rorschach: 10 ng/l *** stark erhöhtes hs-troponin Standort St.Gallen: 150 ng/l Standort Flawil / Rorschach: 100 ng/l
59 GRACE-Risiko-Nomogramm für akute Koronarereignisse 3. Herzfrequenz 4. Alter 5. Kreatinin-Spiegel 2. Systolischer Blutdruck 1. Killip-Klasse* μmol/l Punkte Jahre Punkte Schläge/Min. Punkte mmhg Punkte Klasse bei Eintritt Punkte sy I 0 II 20 III 39 IV 59 Punkte 6. Herzstillstand bei Eintritt ST-Segment-Veränderung Erhöhte kardiale Marker 14 * Killip-Klasse: I = keine Zeichen Herzinsuffizienz; II = feinblasige Rasselgeräusche oder Jugularvenenstauung; III = Lungenödem; IV = Kardiogener Schock ** Gesamtsterblichkeit im Spital = Sterblichkeit an irgendeiner Ursache während der Hospitalisation Total Punkte für prädiktive Faktoren = Total Punkte Korrespondierende Wahrscheinlichkeit Gesamtsterblichkeit im Krankenhaus**, % Adaptiert nach Arch Intern Med, 2003;163: Empfehlungen für die invasive Abklärung / Revaskularisation Notfallangiografie (< 2 Std.) erwägen (Dienstarzt Kardiologie kontaktieren über ), falls Persistierende Ischämieschmerzen trotz Therapie Hämodynamisch instabil Für Transfer: UFH iv (siehe Abschnitt «Initiale Therapie» Seite 110) Frühe invasive Strategie (innerhalb 24 Std.) empfohlen bei Patienten mit GRACE-Score > 140 (siehe Tab. nebenan) oder Hochrisiko- Kriterien Anstieg oder Abfall des kardialen Troponins vereinbar mit Myokardinfarkt Dynamische ST- oder T-Wellenveränderungen (symptomatisch oder stumm) GRACE-Score > 140 Alle anderen Patienten: PCI innerhalb von Std. Weiterführung UFH resp. Wechsel auf LMWH Dienstarzt Kardiologie kontaktieren (siehe Seite 118) Instabile Angina pectoris (keine ST-Hebung, Troponin negativ, passende Symptomatik) Ggf. Umstellung auf niedermolekulares Heparin Enoxaparin (Clexane) 1 mg/kg sc 2x/Tag, maximal 2x 80 mg/tag für 7 Tage Dalteparin (Fragmin) 120 IE/kg sc 2x/Tag Nadroparin (Fraxiparine) 86 IU/kg sc 2x/Tag Weitere Diagnostik Ergometrie nach Std. Angiografie elektiv anmelden bei: Ischämienachweis, hohem kardiovaskulären Risiko, linksventrikulärer Dysfunktion
60 118 Ansprechpartner für Anmeldung von auswärts für KSSG Notfall-Anmeldung Telefonisch: Dienstarzt Kardiologie via Zentrale KSSG Telefon: Unterlagen inkl. Stammblatt [email protected] oder Fax: Elektive Anmeldung* Schriftlich: Per Post, Fax oder Ärztliche Leitung Kardiologie Rorschacherstr. 95, 9007 St.Gallen Fax: , [email protected] Rückfragen Telefon: Montag Freitag: 8 17 Uhr * mit Versicherungsstatus Übersicht Empfehlungen zur prä-, peri- und postinterventionellen antithrombotischen Therapie Orale Thrombozytenhemmung Aspirin mg po mindestens 2 Std. vor perkutaner Koronarintervention (PCI) oder 250 mg iv direkt im Herzkatheterlabor Keine zusätzliche Aspirin-Gabe bei vorbestehender Aspirin-Therapie von mind. 100 mg pro Tag Wahl des ADP-Rezeptor-Antagonisten für duale Thrombozytenaggregationshemmung in Ergänzung zu Aspirin Erste Wahl bei ACS im akuten Setting: Ticagrelor (Brilique) 2x 90 mg po, als Ladedosis gefolgt von 2x 90 mg pro Tag als Erhaltungsdosis Alternative: Prasugrel (Efient) 60 mg, dann 10 mg pro Tag (KI: St. n.cvi/tia, Dosisreduktion: Alter > 75 J. u/o Gewicht < 60 kg) Clopidogrel 600 mg Ladedosis gefolgt von 75 mg/tag, falls Tica-grelor oder Prasugrel nicht verfügbar oder kontraindiziert (u.a. Notwendigkeit einer OAK) Behandlungsdauer nach ACS: ADP-Rezeptor-Antagonisten- Therapie (duale Thrombozytenaggregationshemmung) nach ACS 12 Monate, dann Entscheid über Weiterführung mit Ticagrelor 2 60 mg/tag po unter Abwägen von Ischämie- und Blutungsrisiko. Behandlungsdauer bei stabiler KHK (elektive Eingriffe): 1 Monat nach einfacher Ballondilatation (inkl. beschichtetem Ballon) und/oder unbeschichtetem Stent 6 Monaten nach medikamentenbeschichtetem Stent (DES und bioresorbierbaren beschichteten Stents) ASS und Clopidogrel (DuoPlavin) Bei Erhaltungstherapie mit ASS 100 mg und Clopidogrel 75 mg Möglichkeit der fixen Kombination in einer Tablette als DuoPlavin Parenterale antithrombotische Therapie Unfraktioniertes Heparin (UFH) iv Die nachfolgenden Dosisempfehlungen gelten nur, wenn keine Vorbehandlung mit UFH erfolgte. Mit GP-IIb/IIIa U/kg mit ACT-Ziel Sek. Ohne GP-IIb/IIIa U/kg mit ACT-Ziel Sek. Bei Vorbehandlung mit UFH erfolgt die Gabe einer reduzierten UFH-Dosis nach Resultat der «Activated Clotting Time» (ACT) Keine Dosisreduktion bei Niereninsuffizienz Heparin-Infusion soll am Abend der PCI gestoppt und durch Thromboseprophylaxe mit Clexane ersetzt werden (falls keine therapeutische plasmatische Gerinnungshemmung aus anderen Gründen [Vorhofflimmern, mechanische Klappe, sehr grosser Vorderwandinfarkt mit Gefahr von apikalem LV-Thrombus]) 119
61 Niedermolekulare Heparine (LMWH) sc und iv (iv nur im Katheterlabor) Die nachfolgenden Dosisempfehlungen gelten nur bei Verabreichung der unten aufgeführten therapeutischen sc-dosis. Bei sc-gabe von prophylaktischer Dosis zu irgendeinem Zeitpunkt (z. B. Enoxaparin [Clexane] mg oder Dalteparin [Fragmin] U) sollte UFH (siehe Seite 119) verwendet werden. Enoxaparin (Clexane) 1 mg/kg 12-stündlich sc Tirofiban (Aggrastat) Dosierung 0.4µg/kgKG über 30 Minuten oder 25 µg/kg iv Ladedosis Initial über 3 Min. Erhaltungsdosis Dosishalbierung bei Kreatinin-Clearance < 30 ml/min µg/kg/min. iv für 18 Stunden post PCI Management von Patienten mit perkutaner koronarer Intervention (PCI) und Notwendigkeit einer oralen Antikoagulation bei nicht-valvulärem Vorhofflimmern Letzte sc Dosis vor Katheter iv Dosierung LMWH im Katheterlabor < 8 Std. keine zusätzliche Dosis iv 8 12 Std. 0.3 mg/kg iv (mit und ohne GP-IIb/IIIa) > 12 Std. UFH oder 0.5 mg/kg iv Dalteparin (Fragmin) 120 U/kg 12-stündlich sc CHA2DS2- V A S c <_ 1 CHA2DS2- V A S c >_ 2 HAS-BLED >_ 3 HAS-BLED <_ 2 Letzte sc Dosis vor Katheter iv Dosierung LMWH im Katheterlabor < 8 Std. keine zusätzliche Dosis iv DAPT SKHK ACS 8 12 Std. 60 U/kg iv (mit und ohne GP-IIb/IIIa) > 12 Std. nur UFH Bei Kreatinin-Clearance < 30 ml/min.: Gabe von UFH Bivalirudin (Angiox) Antithrombotikum der Wahl bei Anamnese einer HIT mg/kg/iv als Bolus, dann 1.75 mg/kg/std. Infusion während und bis zu 4 Stunden nach PCI Bei Upstream-Therapie mit UFH: Stopp der UFH-Infusion mindestens 30 Min. vor Beginn mit Angiox Bei Upstream-Therapie mit LMWH: Letzte LMWH-Injektion muss mindestens 8 Std. zurückliegen Keine Dosisreduktion bei Niereninsuffizienz ohne Dialysepflichtigkeit Dosisreduktion der Infusion bei dialysepflichtiger Niereninsuffizienz von 1.75 mg/kg/std. auf 0.25 mg/kg/std. iv während der PCI (N)OAK* + DAPT für 1 Monat dann (N)OAK + SAPT (6-) 12 Monate (N)OAK* + DAPT für (3-)6 Monate dann (N)OAK + SAPT bis zu 12 Monate (N)OAK* + Clopidogrel bis 12 Monate Legende: DAPT: Duale Anti-Plättchen-Therapie (ASS 100 mg und Clopidogrel) SAPT: Singuläre Anti-Plättchen-Therapie (i.d.regel Clopidogrel) (N)OAK-Dosierung reduzieren bei Triple-Therapie, d.h. 2 x 110 mg Dabigatran/d, 15 mg Rivaroxaban/d, 2 x 2.5 mg Apixaban/d SKHK: stabile koronare Herz-Krankheit HAS-BLED siehe Seite 239 CHA2DS2-VASc siehe Seite 237 Nach: 2014 ESC/EACTS Guidelines on myocardial Revascularization. European Heart Journal (2014) 35,
62 122 Routinemassnahmen akute, subakute und chronische Phase nach STEMI/NSTEMI Routinemässige Echokardiografie bei allen STEMI-Patienten in den ersten Tagen nach STEMI Bei linksventrikulärem Thrombus mindestens 3 Monate OAK mit Marcoumar oder einem NOAK Bei klarer Indikation für OAK (z. B. Vorhofflimmern mit CHA2DS2-VASc > 2, mech. Klappenprothese, St.n.Thrombose/Lungenembolie) Marcoumar (INR , siehe Tabelle Seite 121) Marcoumar vorderhand nicht kombinieren mit Ticagrelor oder Prasugrel Dauer Duale bzw. Triple-Therapie abhängig von CHA2DS2-VASc und HAS-BLED-Score: Tabelle Seite 121 Anschliessend zeitlich unlimitiert Marcoumar oder NOAK in der Regel als Monotherapie (INR ) Protonenpumpeninhibitor: 40 mg Pantozol po Immer während Triple-Therapie Duale Therapie bei Risikofaktoren für GI-Blutung (St. n. GI-Blutung, St. n.ulcus, > 65 J., zusätzliche Einnahme von Steroiden) Orale Betablocker-Th während und nach Hospitalisation bei allen STEMI-Patienten, bei NSTEMI mit Herzinsuffizienz/LV-Dysfunktion Nüchtern-Blutglukose-Profil so früh als möglich während Hospitalisation Statin-Therapie: hohe Dosis (40 80 mg Atorvastatin oder 20 mg Rosuvastatin) so früh als möglich mit Reevaluation 4 6 Wochen nach Infarkt, Ziel-LDL < 1.8 mmol/l (ggf. Dosisanpassung bei Patienten mit erhöhtem NW-Risiko wie ältere Patienten, Nieren- und/oder Lebererkrankung, Statin-NW) ACE-Hemmer bei STEMI innerhalb der ersten 24 Std. bei Hinweisen auf Herzinsuffizienz, erheblicher LV-Dysfunktion (insbesondere Vorderwandinfarkt), Diabetes; bei ACE-Hemmer-Intoleranz Angiotensin-Rezeptorblocker Aldosteron-Antagonist, d.h. Eplerenone oder Spironolactone, falls LV-EF < 40% und Herzinsuffizienz oder Diabetes, vorausgesetzt keine Niereninsuffizienz oder Hyperkaliämie Rauchstopp-Beratung (siehe Seite 57) Prof. Dr. Hans Rickli Dr. Philipp K. Haager Dr. Gian-Reto Kleger Dr. Roland Lenz PD Dr. Micha Maeder Dr. Daniel Weilenmann 123
63 Tiefe Venenthrombose und Lungenembolie Tiefe Venenthrombose (TVT) Epidemiologie und Risikofaktoren Die jährliche TVT-Inzidenz beträgt über alle Altersgruppen hinweg 1 2 pro 1000 Personen. Bei über 70-Jährigen liegt die Inzidenz bei 1 2 pro 100 Personen. Ca. 90% der TVT beginnen im Unterschenkel. Ungefähr 25% der unbehandelten distalen TVT führen zu einer proximalen TVT. Die Ausdehnung einer distalen TVT in eine proximale TVT erfolgt meistens innerhalb einer Woche nach der ersten Präsentation. Der Zusammenhang mit den Lungenembolien wird dort abgehandelt. Die Assoziation des Rauchens mit dem Risiko einer TVT oder LE ist nachgewiesen (Odds Ratio 1.43). Die Risikoerhöhung ist dosisabhängig. Bei Rauchen und Einnahme von oralen Kontrazeptiva (OK) besteht ein ca. 9-fach erhöhtes Risiko (Odds Ratio 8.8). Mit zunehmendem Übergewicht steigt auch das Thromboserisiko ziemlich linear an (Odds Ratio ca. 2.0 bei einem BMI von 30). Adipositas und OK steigern das Risiko massiv (Odds Ratio 23.8 gegenüber Normalgewichtigen ohne OK)
64 Klassische hereditäre und erworbene Thrombophilien Faktor-V-Leiden (APC-Resistenz) Antithrombin-III-Mangel Prothrombin-G20210A-Mutation Antiphospholipid-AK/ Lupus-Antikoagulans Hyperhomozysteinämie Kongenitale Dysfibrinogenämie Protein-C-, Protein-S-Mangel Positive Familienanamnese (erstgradig Verwandte) Risikofaktoren für thromboembolische Ereignisse Trauma/Operation Apoplexie Immobilisation Myokardinfarkt, Herzinsuffizienz Alter Chronisch venöse Insuffizienz Adipositas Rauchen Maligne Erkrankungen/Chemotherapie Schwangerschaft/Wochenbett Nephrotisches Syndrom Orale Kontrazeptiva, Östrogentherapie Liegende zentralvenöse und pulmonal-arterielle Katheter Glukokortikoidtherapie St. nach TVT oder LE Hypervisköse Veränderungen (Polyzythämie, M. Waldenström) Langstreckenflug Medikamente: Tamoxifen, Antipsychotika, Thalidomid u.v.a. Tab. 1: Thrombophilien und Risikofaktoren für tiefe Beinvenenthrombose und Lungenembolien Vortestwahrscheinlichkeit für das Vorliegen einer TVT Das Abschätzen der Vortestwahrscheinlichkeit ist unabdingbar zur Beurteilung der Diagnostik bei der TVT. Der Wells Score (Tab. 2) ist ein gebräuchliches Hilfsmittel dafür. Allerdings darf dieses im Vergleich zur integralen klinischen Beurteilung eines erfahrenen Arztes nicht überschätzt werden. Variable Punkte Aktive Krebserkrankung +1 Lähmung oder kürzliche Immobilisation der Beine +1 Bettruhe (> 3 Tage), grosse Chirurgie in den letzten 12 Wochen +1 Schmerz entlang der tiefen Venen +1 Schwellung ganzes Bein +1 Schwellung des Unterschenkels (> 3 cm Umfangsdifferenz) +1 Eindrückbares Ödem am symptomatischen Bein +1 Prominente Kollateralvenen +1 Frühere, dokumentierte TVT +1 Alternative Diagnose ebenso wahrscheinlich wie TVT 2 2 Punkte hohe Wahrscheinlichkeit für TVT (28%) < 2 Punkte nicht hohe Wahrscheinlichkeit für TVT (6%) Tab. 2: Wells Score zur Abschätzung der Vortestwahrscheinlichkeit einer tiefen Beinvenenthrombose (bei rezidiv. TVT plus 1 Punkt; Wertigkeit des Wells Score mit D-Dimer- Test bei Karzinompatienten umstritten) D-Dimer-Test Die empfindlichen D-Dimer-Tests (ELISA) eignen sich aufgrund ihrer hohen Sensitivität zum Ausschluss von Beinvenenthrombosen. Wegen der geringen Spezifität genügt ein positiver D-Dimer-Test nicht zum Nachweis eines thromboembolischen Geschehens. Der Grenzwert von 500 µg/l kann bei einem Alter über 50 Jahren mit der Formel Alter x 10 µg/l angepasst werden. Ein positiver D-Dimer-Test genügt auch in Kombination mit einer hohen Vortestwahrscheinlichkeit nicht für die Diagnose einer TVT, sondern es muss ein bildgebendes Verfahren angeschlossen werden. Generell wird bei hoher Vortestwahrscheinlichkeit auch ohne vorgängige Bestimmung der D-Dimere direkt eine Bildgebung empfohlen. Ein negativer D-Dimer-Test schliesst bei klinisch nicht hoher Vortestwahrscheinlichkeit eine tiefe Beinvenenthrombose mit hoher Wahrscheinlichkeit aus
65 Kompressionsultraschall der Beinvenen Die Kompressionssonographie in den Händen eines geübten Untersuchers mit einem hochauflösenden Gerät ist heute das diagnostische Mittel der Wahl. Sie hat die Phlebografie als Gold-Standard zum Nachweis einer TVT abgelöst. Vortestwahrscheinlichkeit: hoch Verdacht auf TVT Vortestwahrscheinlichkeit abschätzen Vortestwahrscheinlichkeit: nicht hoch Therapie Oberflächliche Thrombophlebitis, Varikothrombose Bei Befall von V. saphena magna oder parva wird eine Duplexsonografie auch der tiefen Venen empfohlen. Thrombus/Entzündung nahe (< 5 cm) der Mündung von V. saphena in V. femoralis oder V. poplitea (= Crosse) oder Thrombuslänge > 5 cm: volle Antikoagulation für 45 Tage. Bei Kontraindikation für Antikoagulation Venenligatur erwägen. Bei kleinem Befund (< 5 cm) und fern von Crosse/tiefem Venensystem: Kühlung, Kompression, NSAR lokal oder p.o. und klinische Verlaufskontrolle. Wiederholung der klinischen Untersuchung nach 45 Tagen oder bei Symptomverschlimmerung früher zur Beurteilung des Beginns resp. einer Verlängerung der Antikoagulation und allenfalls Suche nach Malignom oder Hyperkoagulabilität. Nachweis einer TVT Behandlung der TVT Kompressionsultraschall Kein Nachweis einer TVT Keine TVT, andere Diagnose suchen Kein eindeutiger Befund Kompressionsultraschall nach 4 7 Tagen oder Phlebografie D-Dimer-Test positiv Abb. 1: Algorithmus zur Diagnose der tiefen Beinvenenthrombose (TVT) D-Dimer-Test D-Dimer-Test negativ Keine TVT, andere Diagnose suchen Isolierte distale Venenthrombose Bei der isolierten distalen (unterhalb V. poplitea) TVT ohne Symptome und ohne Risikofaktoren für eine Ausdehnung (positiver D-Dimer-Test, Nähe zu proximalen Venen, Thrombose > 5 cm lang, mehrere Venen betreffend oder > 7 mm Durchmesser, kein auslösender Risikofaktor, persistierender, irreversibler Risikofaktor, wie z. B. eine aktive Krebserkrankung, Anamnese von TVT oder LE, Hospitalisation oder verlängerte Immobilisation) empfehlen wir serielle sonografische Verlaufskontrollen während 2 Wochen. Bei schweren Symptomen, Risikofaktoren für eine Ausdehnung oder sonographisch nachgewiesener Extension wird analog einer proximalen TVT behandelt. Reine Muskelvenenthrombosen haben ein geringeres Extensionsrisiko. Schwere Symptome sprechen eher für eine Antikoagulation, ein hohes Blutungsrisiko dagegen
66 Proximale tiefe Beinvenenthrombose TVT Bei der proximalen TVT unterscheidet sich die antithrombotische Therapie nicht von der jenigen von Lungen embolien (siehe ab Seite 138). Nur eine Phlegmasia coerulea dolens ist eine absolute Indikation für eine chirurgische oder kathetertechnische Thrombektomie oder eine Thrombolyse. Relative Indikationen können isolierte Beckenvenenthrombosen und 4-Etagen-Thrombosen mit schwerer Symptomatik sein. Es profitieren in solchen Fällen primär jüngere Patienten mit relativ kurz dauernder Symptomatik (< 14 Tage), gutem Allgemeinzustand und tiefem Blutungsrisiko von einer Thrombolyse. Kompressionstherapie Die Kompressionstherapie (initial mit Kurzzugbinden und nach Abschwellung mit Unterschenkel-Kompressionsstrümpfen der Klasse II) wurde traditionell möglichst früh begonnen und im Fall einer proximalen Thrombose (ab V. poplitea) für mind. 2 Jahre weitergeführt. Diese Empfehlung wird durch eine viel diskutierte Studie im Lancet 2014 grundsätzlich infrage gestellt. Aktuelle Richtlinien empfehlen den routinemässigen Einsatz von Kompressionsstrümpfen nicht. Zur Behandlung von akuten oder chronischen Symptomen einer TVT wird die Kompressionstherapie empfohlen. Bei distalen TVT und Muskelvenenthrombosen Dauer der Kompressionstherapie nach Massgabe der Stauungsbeschwerden, da das postthrombotische Syndrom in dieser Situation seltener auftritt. Mobilisation Patienten mit TVT können mit eingebundenen Beinen nach Massgabe der Beschwerden mobilisiert werden, und zwar unabhängig von Ausmass, Lokalisation und Morphologie der TVT. Lungenembolie (LE) Die jährliche Inzidenz liegt bei ca pro Menschen. Die Mortalität liegt ohne Behandlung um 30%, mit Behandlung bei 9 11%. Das Risiko für die Entwicklung einer chronischen thromboembolischen pulmonal-arteriellen Hypertonie (CTEPH) nach unprovozierten Lungenembolien beträgt ca. 1.5%. Zusammenhang zwischen tiefer Beinvenenthrombose und Lungenembolie Ca. 90% der LE sind Folge einer TVT (Autopsiebefunde). Bei akuten, symptomatischen Lungenembolien finden sich mittels Kompres sionsultraschall nur in 30 50% ( 70%) Beinvenenthrombosen. Dieser Nachweis ist aber mit einer erhöhten Mortalität assoziiert. Risikofaktoren für Lungenembolien Die Risikofaktoren entsprechen denjenigen für TVT (siehe Tab. 1). Diagnostik der Lungenembolie Beurteilung der klinischen Stabilität Bei Verdacht auf LE muss als erster Schritt evaluiert werden, ob der Patient im Schock ist und damit gemäss der Abb. 2 vorgegangen werden muss. In solchen Fällen ist die Vortestwahrscheinlichkeit per se schon hoch. Stabile Patienten werden gemäss Abb. 3 abgeklärt. Vortestwahrscheinlichkeit Die Vortestwahrscheinlichkeit ist unabdingbar zur Beurteilung der Diagnostik bei LE. Dafür sind der modifizierte Genfer Score und der Wells Score gebräuchliche Hilfsmittel (Tab. 3). Allerdings dürfen diese im Vergleich zur integralen klinischen Beurteilung eines erfahrenen Arztes nicht überschätzt werden
67 Modifizierter Genfer Score Wells-Score Variable Punkte Variable Punkte Alter > 65 Jahre +1 Frühere TVT oder LE +3 Frühere TVT oder LE +1.5 Operation oder Fraktur im letzten Monat +2 Frische Operation oder Immobilisation Aktive Krebserkrankung +2 Krebserkrankung +1 Einseitige Beinschmerzen +3 Hämoptyse +2 Hämoptyse +1 Herzfrequenz 75 94/Min. 95/Min. Schmerz bei Palpation der tiefen Beinvenen und einseitiges Ödem Herzfrequenz > 100/Min Klinische Zeichen einer TVT Alternative Diagnose unwahrscheinlicher als LE +3 Klinische Wahrscheinlichkeit Klinische Wahrscheinlichkeit Niedrig (8%) 0 3 Niedrig (3%) 0 1 Mittel (28%) 4 10 Mittel (28%) 2 6 Hoch (74%) 11 Hoch (78%) 7 +3 frühes Mortalitätsrisiko Hoch > 15% Intermediärhoch Intermediärtief Tief < 1% PESI- Klasse III V Risikomarker Schock oder Hypotonie Rechtsventrikuläre Dysfunktion (Echo, CT) Kardiale Biomarker (BNP, Troponin) + (+) + (+) Therapie- Implikationen Thrombolyse oder Embolektomie Hospitalisation Hospitalisation Frühe Entlassung oder ambulante Behandlung Tab. 4: Risikostratifizierung bei LE (Bestimmung der kardialen Biomarker bei hohem und tiefem Risiko fakultativ) Rechtsventrikuläre Dysfunktion: im CT erhöhte Ratio end-diastolische RV/LV-Durchmesser (> 0.9 oder 1.0), im Echo erhöhte Ratio end-diastolische RV/LV-Durchmesser (> 0.9 oder 1.0), Hypo kinesie der freien RV-Wand, erhöhte Geschwindigkeit des Tricuspidal regurgitations- Jets oder eine Kombination Tab. 3: Modifizierter Genfer Score und Wells-Score zur Abschätzung der Vortestwahrscheinlichkeit von Lungenembolien
68 Merkmale Alter Männliches Geschlecht +10 Krebs in der persönlichen Anamnese +30 Herzinsuffizienz +10 Chronische Atemwegserkrankung +10 Herzfrequenz 110 pro Min. +20 Systolischer arterieller Blutdruck < 100 mmhg +30 Atemfrequenz 30 pro Min. +20 Temperatur < 36 ºC +20 Punkte +1/Jahr Störung des Bewusstseins (Desorientiertheit, Lethargie, Stupor o. Koma) +60 Arterielle Sauerstoffsättigung < 90% +20 Der Gesamtscore wird durch Addition der Punktezahlen der vorliegenden klinischen Merkmale gebildet. Punkte Klasse 30-Tage-Mortalität 65 Klasse I % Klasse II % Klasse III % Klasse IV % 126 Klasse V % Tab. 5: Pulmonary Embolism Severity Index (PESI) D-Dimer-Test Der D-Dimer-Test eignet sich aufgrund seiner hohen Sensitivität und der geringen Spezifität nur zum Ausschluss von Lungenembolien. Der Grenzwert von 500 μg/l kann bei einem Alter über 50 Jahren mit der Formel Alter x 10 μg/l angepasst werden. Ein negativer D-Dimer-Test schliesst bei tiefer und mittlerer Vortestwahrscheinlichkeit eine LE mit klinisch genügender Sicherheit aus. Eine hohe Vortestwahrscheinlichkeit und ein positiver D-Dimer-Test genügen nicht für die Diagnose einer LE. Bei hoher Vortestwahrscheinlichkeit wird von der Durchführung eines D-Dimer-Tests abgeraten und direkt ein bildgebendes Verfahren empfohlen. Kompressionsultraschall der Beinvenen Der Nachweis einer tiefen Beinvenenthrombose genügt bei entsprechenden Symptomen zum Nachweis von Lungenembolien. Mit Durchführung eines Kompressionsultraschalls vor dem Lungenembolie-CT können ca. 10% der CTs gespart werden. Ventilations- und Perfusionsszintigrafie Diese Untersuchungsmethode kommt nur noch bei unauffälligem konventionellem Röntgenbild der Lunge und bei Kontraindikationen (schwere Nieren insuffizienz, Anaphylaxie auf KM) für ein LE-CT in Frage. Eine normale Perfusionsszintigrafie der Lungen schliesst Lungenembolien mit klinisch genügender Wahrscheinlichkeit aus (negativer Vorhersagewert = negative predictive value 97%) und kann deshalb evtl. in der Schwangerschaft hilfreich sein. Thoraxsonografie Bei schwerer Kontrastmittelallergie, schwerer Niereninsuffizienz oder Schwangerschaft kann eine Thoraxsonografie in geübten Händen diagnostisch hilfreich sein. Pleuranahe dreieckige oder gerundete Defekte sind Zeichen von peripheren Lungenembolien, finden sich aber auch bei zentralen Lungenembolien (sog. «Signalembolien»). Beim Nachweis von mind. zwei subpleuralen Läsionen im Lungenparenchym werden eine gepoolte Sensitivität von 80% und eine Spezifität von 93% angegeben. Lungenembolie-Computertomografie (LE-CT) Heute ist das multislice spiral CT (Mehrzeilen-Spiral-CT) der Gold-Standard zum Nachweis oder Ausschluss von segmentalen oder proximalen Lungenembolien (negativer Vorhersagewert ca. 99%). Der Nachweis von isolierten subsegmentalen Lungenembolien ist mit Mehrzeiler-CTs häufiger
69 Akute rechtsventrikuläre Dysfunktion oder positives LE-CT Thrombolyse oder kathetertechnische Fragmentierung oder Embolektomie Echokardiografie oder LE-CT Abb. 2: Algorithmus LE bei Patienten im Schock Klinische Wahrscheinlichkeit hoch Kompressionsultraschall Negativ Klinische Wahrscheinlichkeit Positiv Keine akute rechtsven trikuläre Dysfunktion oder negatives LE-CT Andere Diagnose suchen D-Dimer-Test positiv Klinische Wahrscheinlichkeit mittel oder tief D-Dimer-Test D-Dimer-Test negativ Therapie Bei hämodynamischer Instabilität ist eine dringende, rasche Wiedereröffnung (mittels Thrombolyse, kathetertechnischer Fragmentierung oder Embolektomie) der Pulmonalarterien die allenfalls lebensrettende Massnahme. Bei weniger schweren Fällen geht es in erster Linie um eine rasch zu beginnende Antikoagulation zur Verhinderung der Progression des thrombotischen Prozesses und zur Verhinderung von Rezidiven. Antithrombotische Therapie bei TVT und LE Bei hoher Vortestwahrscheinlichkeit für eine LE wird die Therapie (Heparin-Bolus, 1. Dosis des NMH oder NOAK (Apixaban, Rivaroxaban)) vor der Vervollständigung der Diagnostik eingeleitet. Bei unfraktioniertem Heparin (UFH) und niedermolekularem Heparin (NMH) ist eine regelmässige Thrombozytenkontrolle (z. B. am Tag 0, 5, 7, 9) notwendig wegen der Möglichkeit einer Heparin-induzierten Thrombopenie (HIT). Bei Niereninsuffizienz (geschätzte, absolute (nicht auf eine Körperoberfläche von 1.73 m 2 normierte) glomeruläre Filtrationsrate egfr < 30 ml/min.), schwerem Übergewicht oder geplanter Reperfusion wird die PiCT-gesteuerte*, kontinuierliche Gabe von unfraktioniertem Heparin empfohlen. LE-CT Andere Diagnose suchen LE-CT negativ Andere Diagnose suchen LE-CT positiv LE behandeln Mit einem voherigen Kom pres sionsultraschall können ca. 10% der LE-CTs eingespart werden. Abb. 3: Algorithmus LE bei hämodynamisch stabilen Patienten * Steuerung der Heparinisierung gemäss hausinternen Richtlinien (im KSSG nach PiCT, in anderen Spitälern nach aptt, Anti-Faktor-Xa-Aktivität etc.)
70 Substanz Intervall Dosis Enoxaparin (Clexane) s.c. 2x/Tag 1 mg/kg oder Enoxaparin (Clexane) s.c. 1x/Tag 1.5 mg/kg Heparin iv Bolus 80 E/kg KG Startgeschwindigkeit Infusion 18 E/kg KG/Std. Weitere Anpassungen nach PiCT* Stopp, wenn INR an zwei Tagen 2.0 Bei Heparin-induzierter Thrombopenie (HIT)** Argatroban (Argatra) iv gemäss Merkblatt «Argatroban (Argatra )» der Gruppe für Arzneimitteltherapiesicherheit oder des KSSG Fondaparinux (Arixtra) s.c. KG < 50 kg 5 mg/tag sc KG kg 7.5 mg/tag sc KG > 100 kg 10 mg/tag sc Phenprocoumon (Marcoumar) Rivaroxaban (Xarelto) Apixaban (Eliquis) Edoxaban (Lixiana) Dabigatran (Pradaxa) Beginn gleichentags, Stunden nach Heparin oder NMH 1x/Tag 2x/Tag für 3 Wochen (kein zusätzliches Heparin oder NMH), dann 1x/Tag 2x/Tag für 7 Tage (kein zusätzliches Heparin oder NMH), dann 2x/Tag Initial mind. 5 Tage Heparin/ NMH, danach 1x/Tag Initial mind. 5 Tage Heparin/ NMH, dann 2x/Tag Ziel-INR 2.5 ( ) gemäss INR 15 mg 20 mg 10 mg 5 mg 60 mg 150 mg * Steuerung der Heparinisierung gemäss hausinternen Richtlinien (im KSSG nach PiCT, in anderen Spitälern nach aptt, Anti-Faktor-Xa-Aktivität etc.) ** Rücksprache mit Hämatologen/Hämostaseologen empfohlen Erstes Ereignis Transienter Risikofaktor (z. B. Operation) Unprovozierte Genese TVT isoliert distal Unprovozierte Genese TVT proximal oder LE danach bei geringem Blutungsrisiko und gutem Monitoring (regelmässige Nutzen-Risiko-Evaluation); andernfalls Apixaban 2x 2.5 mg/d oder Rivaroxaban 1x 10 mg/d oder als weniger wirksame Alternative Aspirin 100 mg/d erwägen Bei aktiver Krebskrankheit: Initial NMH, danach NMH (bei Nichttoleranz oder eingeschränkter Lebensqualität OAK mit Ziel-INR 2.5 oder NOAK) Antiphospholipid-Antikörper-Syndrom Rezidiv (TVT und LE) Unprovozierte Genese Tab. 7: Dauer der Antikoagulation bei TVT oder LE Dauer 3 Monate Sonografisches Follow-up während 2 Wochen oder OAK für 3 Monate (siehe Text) 3 Monate zeitlich unbegrenzt zeitlich unbegrenzt 3 6 Monate zeitlich unbegrenzt Zeitlich unbegrenzt, regelmässige Reevaluation Zeitlich unbegrenzt Das Vorliegen einer laborchemisch charakterisierten Thrombophilie bei einer provozierten Thrombose hat mit Ausnahme des Antiphospholipid-Antikörper-Syndroms in den meisten Fällen keinen Einfluss auf die Dauer der Antikoagulation. Bei einem unprovozierten Zweitereignis ist mit und ohne Nachweis einer laborchemischen Thrombophilie die zeitlich unlimitierte orale Antikoagulation empfohlen (sofern kein hohes Blutungsrisiko vorliegt). Tab. 6: Antithrombotische Therapie bei TVT und LE
71 TVT untere Extremität Unprovoziert Provoziert 2. Ereignis 1. Ereignis 2. Ereignis Proximal/ distal Distal Proximal Proximal/ distal Muskelvenenthrombose Hohes Blutungsrisiko 1. Ereignis Proximal Distal 3 Mte. OAK Tiefes/ moderates Blutungsrisiko Symptome RF für Progression Keine Symptome Keine RF für Progress. 3 Mte. OAK Serielle Sonografie (7 14 Tage) 3 Mte. OAK falls Extension 3 Mte. OAK* Mind. 3 Mte. OAK, dann Risiko-Nutzen- Evaluation Vorgehen wie bei 1. Ereignis Falls frisch/ schmerzhaft: evtl. 4 Wo. OAK, dann Nachkontrolle 3 Mte. OAK* Langfristige OAK mit jährl. Neuevaluation Hohes Blutungsrisiko Tiefes/ moderates Blutungsrisiko OAK-Stopp* * vgl. Text Langfristige OAK mit jährl. Neuevaluation Subsegmentale Lungenembolien: Bei Patienten mit subsegmentalen Lungenembolien (ohne Beteiligung von proximalen Lungenarterien und ohne proximale TVT), die ein tiefes Rezidivrisiko für eine Thromboembolie haben, kann unter gewissen Voraussetzungen auf eine antithrombotische Therapie verzichtet werden. Beim Verzicht auf eine Antikoagulation dürfen folgende Risikofaktoren nicht vorliegen: Hospitalisation oder reduzierte Mobilität, aktives Krebsleiden, nicht reversible Risikofaktoren für Thromboembolie, geringe kardiopulmonale Reserve oder deutliche Symptome, die nicht anders erklärt werden können. Eine serielle Phlebosonografie der Beine ist bei Verzicht auf eine antithrombotische Therapie zu erwägen. Ein hohes Blutungsrisiko spricht eher gegen eine Antikoagulation. Bei allen Patienten ist immer das Risiko einer Blutung unter Antikoagulation gegen das Risiko einer Thromboembolie ohne Antikoagulation abzuwägen. Bei hohem Blutungsrisiko nach einem ersten oder zweiten unprovozierten thromboembolischen Ereignis, das eine Fortführung der Antikoagulation über drei Monate hinaus nicht rechtfertigt, ist Apixaban (2x 2.5 mg/d), Rivaroxaban (1x 10 mg/d) oder Aspirin 100 mg/d (mit geringerem Nutzen als eine OAK) gegenüber keiner antithrombotischen Therapie zu evaluieren
72 Thrombolyse Ein Schock mit nachgewiesener rechtsventrikulärer Dysfunktion ist eine klare Indikation für eine Thrombolyse. Die Thrombolyse bei intermediärhohem Risiko (vgl. Tab. 4) wird diskutiert. Beim Nachweis von mobilen rechtsventrikulären Thromben muss eine Thrombolyse resp. eine kathetertechnische oder chirurgische Embolektomie erwogen werden. Absolute Kontraindikationen Hämorrhagischer Schlaganfall Ischämischer Schlaganfall in den letzten 3 Monaten Hirntumor und Hirnmetastasen Grösseres Trauma, grössere Operation, Schädelhirntrauma in den letzten 3 Wochen Gastrointestinale Blutung im letzten Monat Bekanntes Blutungsrisiko Relative Kontraindikationen TIA in den letzten 6 Monaten Orale Antikoagulation Schwangerschaft (bis 1 Woche postpartal) Nicht komprimierbare Punktionsstellen Traumatische Reanimation Therapierefraktäre Hypertonie (> 180/110 mmhg) Infektiöse Endokarditis Fortgeschrittene Lebererkrankung Aktives peptisches Ulkus Tab. 8: Kontraindikationen für eine Thrombolyse Alteplase (Actilyse) 100 mg über 2 Std. iv oder Akzeleriert 0.6 mg/kg über 15 Min. (max. 50 mg) Tab. 9: Thrombolyseschemata bei Lungenembolie Vorgehen bei Kontraindikationen für eine Thrombolyse Schwere rechtsventrikuläre Dysfunktion Katheterfragmentierung durch die invasiven Radiologen Kardiogener Schock Verlegung auf die MIPS Einbau einer VA-ECMO (veno-arterielle extrakorporale Membranoxygenierung) Katheterfragmentation oder Verlegung zur Embolektomie Bei beobachtetem Herzstillstand und unmittelbar begonnener Reanimation Einbau einer VA-ECMO in der Notfallstation durch ein Team der MIPS Katheterfragmentation oder Verlegung zur Embolektomie Implantation eines Filters in die Vena cava inferior Die Einlage eines Cava-Filters kann indiziert sein bei Kontraindikation für eine Antikoagulation, bei rezidivierenden LE trotz suffizienter OAK, bei einem Polytrauma mit hohem Thromboembolierisiko, ausnahmsweise perioperativ bei frischer TVT und erhöhtem Blutungsrisiko mit passagerer Kontraindikation für eine Antikoagulation. Die Implantation eines Cava-Filters sollte Einzelfällen vorbehalten sein und restriktiv gehandhabt werden. Prinzipiell macht die Einlage eines Cava-Filters die Antikoagulation nicht unnötig (Appositionsthromben auf Filter). Die Antikoagulation soll auch mit einem Cava-Filter so rasch wie möglich begonnen werden. Es sind entfernbare Systeme zu verwenden. Bettruhe Bei hämodynamisch stabilen Patienten ohne rechtsventrikuläre Dysfunktion ist keine Immobilisierung erforderlich. Sobald eine rechtsventrikuläre Dysfunktion vorliegt, soll in den ersten Tagen eine Überwachung unter stationären Bedingungen erfolgen; ggf. bei «gelockerter» Bettruhe
73 144 Die prospektive OTPE-Studie bestätigte, dass Patienten mit einem PESI Klasse II (siehe Tab. 5) auch ambulant behandelt werden können. Weiterführende Diagnostik Malignomsuche Bei einer unprovozierten Thrombose oder Lungenembolie wird bei 3 15% ein Malignom gefunden. Eine beschränkte diesbezügliche Diagnostik (Anamnese, klinische Untersuchung, Routine-Hämatologie und -Chemie) wird empfohlen, wobei jedoch nicht nachgewiesen ist, dass dadurch Morbidität oder Mortalität gesenkt werden kann. Allenfalls Vervollständigung der anerkannten primärpräventiven Untersuchungen (Mammografie, gynäkologische Untersuchung, PAP-Abstrich, Koloskopie usw.). Weiterführende Diagnostik (Thorax-Röntgen, Abdomensonografie, CT, Endoskopien, Tumormarker usw.) nur bei entsprechenden Verdachtsmomenten, insbesondere bei jüngeren Patienten nach Ausschluss einer Thrombophilie. Gerinnungsabklärung/Thrombophilie-Abklärung Akutabklärung Bei familiärer Belastung mit Antithrombin- oder Protein-C-Mangel (hier ist eine Substitution zu erwägen: Beizug eines Spezialisten) Bei einer erneuten Thrombose unter Heparin oder NMH muss sofort ein HIT gesucht werden. Abklärung idealerweise ungefähr 3 Monate nach dem Ereignis, falls Thromboembolie ohne ersichtlichen Grund und Alter < 45 Jahre Rezidivierende Thromboembolien Familiäre Belastung mit Thromboembolien Thrombosen an ungewöhnlichen Orten Neue Thromboembolie unter Antikoagulation Thromboembolie während der Schwangerschaft oder unter oralem Antikonzeptivum Thromboembolie und Abortneigung Generell sollten in der Akutphase einer Thromboembolie keine funktionellen Untersuchungen erfolgen, da die zu untersuchenden Gerinnungsfaktoren durch die Thromboembolie verbraucht werden können und dies dann ohnehin eine zweite Untersuchung notwendig macht (Ausnahme AT-III-Bestimmung bei hohem Heparin-Bedarf). Genetische Tests können unter Heparinisierung, NOAKs und Vitamin-K-Antagonisten durchgeführt werden, jedoch sind diese deutlich teurer als die funktionellen Screening-Methoden. Gerinnungsanalysen nach Beendigung der oralen Antikoagulation APC-Resistenz und/oder Faktor-V-Leiden, Prothrombin-Genmutation G20210A, Protein C-Aktivität, Protein S-Aktivität, Antithrombin-Aktivität, Lupus Antikoagulans, Anticardiolipin-Antikörper, anti-beta-2-glykoprotein-antikörper. Bei einem initial normalen Protein-C-System-Test kann auf die Bestimmung von Protein C und von der APC-Resistenz bzw. die Suche nach einer Faktor-V-Leiden-Mutation verzichtet werden. Bei relevant erhöhtem Risiko für ein Rezidiv (unprovozierte thromboembolische Ereignisse): Vitamin K-Antagonist (Phenprocoumon oder Acenocoumarol) wird abgesetzt und nach Abfall der INR <2 wird eine Thromboseprophylaxe begonnen (z. B. mit 1x täglich Enoxaparin [Clexane] 1 mg/kg KG sc oder allenfalls NOAK). Nach 3 Wochen wird das niedermolekulare Heparin gestoppt, am Tag nach dem Stopp erfolgt die Blutentnahme für die Thrombophilie-Abklärung (bei Niereninsuffizienz muss im Zweifelsfall die Anti-Xa-Aktivität zum Nachweis der fehlenden NMH- Wirkung bestimmt werden). Dann Wiederaufnahme der Prophylaxe bis zum Vorliegen der Laborresultate und Festlegen des weiteren Prozederes. 145
74 NOAK werden Std. vor der Thrombophilieabklärung pausiert und können gleich anschliessend wieder gestartet werden bis zur Festlegung des definitiven Procederes. Bei Unklarheiten Rücksprache mit Hämatologen/Hämostaseologen. Spezielle Situationen Rechtsventrikuläre Thromben Bei echokardiografischem Nachweis von flottierenden Thromben im rechten Ventrikel (mit einer hohen frühen Letalität) wird eine Thrombolyse oder Embolektomie empfohlen. Schwangerschaft Die Inzidenz thromboembolischer Ereignisse beträgt 0.76 bis 1.72 pro 1000 Schwangerschaften. Der D-Dimer-Test ist in der Schwangerschaft physiologisch (leicht) erhöht und hilft deshalb nur weiter, wenn er nicht erhöht ist. Zur Diagnose resp. zum Ausschluss einer TVT oder LE können bei Bedarf und nach Ausschöpfen der sonographischen Möglichkeiten auch radio-diagnostische Untersuchungen ohne signifikantes Risiko für den Fötus durchgeführt werden. Um die Strahlenbelastung für die Mutter zu minimieren, wird eher eine Perfusionsszintigrafie (ohne Ventilations szintigrafie!) als ein LE-CT empfohlen. Während der Schwangerschaft Therapie mit NMH oder Heparin, postpartal mit Phenprocoumon (Marcoumar, auch beim Stillen erlaubt) für mind. 3 Monate. Maligne Erkrankungen Bei Malignomen treten gehäuft thromboembolische Ereignisse auf. Hier wird zuerst eine Therapie mit NMH (in therapeutischer Dosis) für 3 bis 6 Monate empfohlen, danach Weiterführung des NMH oder evtl. Umstellung auf eine orale Antikoagulation mit Vitamin-K-Antagonisten oder NOAKs. Bei Patienten mit eingeschränkter Lebenserwartung (palliative Situation) kann aus Komfort-Gründen auch auf NMH verzichtet und eine orale Antikoagulation in Erwägung gezogen werden. Armvenenthrombose bei Zentralvenenkatheter oder Port-à-Cath Antithrombotische Therapie wie bei TVT. Funktionierende, korrekt liegende, nicht infizierte Katheter können weiter benutzt werden. Weiterführung der antithrombotischen Therapie, solange ZVK oder Port-à- Cath in situ und 6 12 Wochen über die Entfernung derselben hinaus. Dr. Markus Diethelm Dr. Ulf Benecke Dr. Lukas Graf Dr. Lukas Kern Dr. Gian-Reto Kleger Dr. Alexander Poloczek Prof. Dr. Hans Rickli Dr. Robert Sieber Prof. Dr. Simon Wildermuth Auch in der Schwangerschaft soll jeder Verdacht auf Lungenembolie definitiv geklärt werden. Dazu gehört bei Notwendigkeit auch ein Lungenembolie-CT
75 Akutes Aortensyndrom Grundsätzliches Das akute Aortensyndrom umfasst verschiedene, in Beziehung zueinander stehende Aortenpathologien mit ähnlicher klinischer Präsentation und Therapie: die klassische Aortendissektion, das intra murale Hämatom (IMH), das penetrierende Aortenulkus (PAU) und die akute Aortenruptur (iatrogen oder traumatisch). Patho-Mechanismus: Intima-Ruptur mit Bluteintritt in die Media. Sonderform: lokalisiertes IMH bei Ruptur der Vasa vasorum, beim PAU führt eine Plaqueruptur zur Arrosion der Vasa vasorum mit lokalisiertem IMH Risikofaktoren: langjährige arterielle Hypertonie, Bindegewebserkrankungen (Marfan, Ehlers-Danlos, Loeys-Dietz), bikuspide Aortenklappe, Coarctation (Aortenisthmusstenose), entzündliche Gefässerkrankungen, Dezelerationstrauma, schwere Atherosklerose PAU); selten: Kokain, Amphetamin, Schwangerschaft Die Einteilung der Aortendissektion erfolgt bezüglich Symptomdauer in eine akute ( 14 Tage), subakute (14 Tage 6 Wochen) und chronische (> 6 Wochen). Hinsichtlich der Lokalisation des intimalen Einrisses und der Ausdehnung der Dissektion in der Aorta werden Dissektionen unterschieden nach der Stanford Klassifikation: Aortendissektion Typ A mit Befall der Aorta ascendens, Aortendissektion Typ B ohne Befall der Aorta ascendens. IMH analog Dissektion Die Aortendissektion ist selten (Inzidenz: ca. 6/100'000 Personen/ Jahr); v.a. bei Typ A ( 2 /3 der Fälle) treten Komplikationen aber früh und häufig auf. Hauptgefahr der Aortendissektion Typ A: Akute Aortenklappeninsuffizienz, Ruptur/Perikardtamponade, Myokardischämie (Kompression oder Obliteration der Koronargefässe) oder Malperfusion aortaler Äste Letalität bei Aortendissektion Typ A: in den ersten 48 Stunden 1% pro Stunde. 30 Tage Mortalität nach operativer Behandlung liegt bei ca. 30%
76 Akutes Aortensyndrom zum Inhaltsverzeichnis Letalität bei unkomplizierter Aortendissektion Typ B: < 10% in den ersten 30 Tagen (unter maximaler intensivmedizinischer Therapie) Letalität bei komplizierter Aortendissektion Typ B (renale Malperfusion, mesenteriale Ischämie, retrograde Dissektion oder gedeckte Ruptur): bis 25% in den ersten 30 Tagen IMH (10 25% der akuten Aortensyndrome): kann propagieren zu einer Aortenruptur oder einer akuten Dissektion. Regression ebenfalls möglich. Therapie analog Dissektion PAU (2 7% aller akuten Aortensyndrome): kann propagieren zu einem intramuralen Hämatom, Pseudoaneurysma, einer Aortenruptur oder einer akuten Dissektion. Der natürliche Verlauf ist aber gekennzeichnet durch das Grössenwachstum mit Ausbildung eines sakkulären oder fusiformen Aneurysmas. Therapie analog Dissektion, ggf. aggressiver aufgrund der hohen Rupturrate beim symptomatischen PAU Akute Aortendissektion: Befunde Leitsymptom (85%): perakut einsetzender, reissender oder stechender, ggf. von proximal nach distal wandernder Thoraxschmerz. Falls Aorta ascendens betroffen, eher Thoraxschmerzen; falls A. descendens betroffen, eher Rückenschmerzen Hypertonie oder Hypotonie (Pseudohypotonie bei Befall der supraaortalen Äste, A-Dissektion mit Tamponade) BD-Differenz zwischen beiden Armen oder zwischen oberer und unterer Extremität Renale und/oder viszerale Ischämie Zerebrale und/oder spinale Ischämie Uni- oder bilaterale Beinischämie Algorithmus: akutes Aortensyndrom siehe nächste Seite. Breite Differentialdiagnose Akutes Koronarsyndrom (siehe Seite 109), Myo-, Perikarditis, Lungenembolie, Pneumothorax, Pneumonie, Pleuritis, Trauma, Kostovertebralsyndrom, Ulkus, Gastritis, Ösophagusruptur, Cholezystitis, Pankreatitis Bildgebende Diagnosesicherung/Ausschluss 1. Angio-CT Thorax/Abdomen mit KM + ständig verfügbar; Aorteninsuffizienz bei A-Dissektion nur eingeschränkt beurteilbar 2. Alternativ TEE (trans-ösophageales Echo) + Aorteninsuffizienz; Dissektionsende, Viszeralgefässe Typ A Herzchirurgisches Zentrum: Notfall-OP, hohe Letalität, pro Stunde 1% Mortalität 1. Blutdrucksenkung Ziel: < 120 mmhg 1. Betablocker 2. Nitroglyzerin 2. Analgosedation 1. Opioide 2. Benzodiazepine Typ nach Stanford? Typ B Akutphase ggf. Betreuung auf IPS unkompliziert: medikamentöse Therapie kompliziert: primär endovaskulär (Fenestration, Stenting, Stent- Grafting) Nienaber CA, Powell JT; Management of acute aortic syndromes. European Heart Journal
77 Nachsorgeschema: Empfehlung Engmaschige Kontrollen in der frühen Phase wegen erhöhtem Instabilitätsrisiko: Angio-CT bei Eintritt, 3 5 Tage nach Symptombeginn und vor Entlassung Klinisch und CT-angiografische Kontrolle nach 6 Wochen Weitere Kontrollen (immer mit Bildgebung) nach 1/2 Jahr und nach 1 Jahr, danach jährlich Wenn die Aorta über 2 Jahre grössenstabil bleibt, können die Kontroll-Intervalle verlängert werden. Subakute und chronische Aortendissektion Dies schliesst auch Patienten mit ein, die wegen einer Aortendissektion Typ A operiert worden sind, aber auch noch eine Restdissektion der Aorta descendens aufweisen. Subakute Aortendissektion (2 6 Wochen) Unkompliziert Medikamentöse Therapie: Aggressive Blutdrucksenkung (Ziel < 130/80 mmhg; Betablocker, Ca-Antagonisten) Kompliziert Neu aufgetretener hämorrhagischer Pleuraerguss oder periaortales Hämatom; aortaler Durchmesser 55 mm oder Zunahme > 4 mm in den ersten 6 Wochen; erneute Symptome (s.o.), wie persistierende Schmerzen, unkontrollierte arterielle Hypertonie oder Malperfusion sind Zeichen einer Instabilität und damit auch einer drohenden Ruptur Ein interventionelles Vorgehen muss in Erwägung gezogen werden, wenn möglich mit endovaskulärer Behandlung (Stentgraft, TEVAR) oder offenem Aortenersatz (selten nötig, wenn TEVAR kontraindiziert). Chronische Aortendissektion (> 6 Wochen) Unkompliziert Medikamentöse Therapie: Nachhaltige Blutdrucksenkung (Ziel < 130/80 mmhg; Betablocker, Ca-Antagonisten, ggf. ACE-Hemmer, AT2-Antagonist. Ziel: Verlangsamung des Grössenwachstums der Aorta. Kardiovaskuläre Sekundärprophylaxe mit Thrombozytenaggregationshemmer (z. B. Aspirin cardio 100 mg 1-0-0) und Statin (für Letztere bestehen Hinweise auf Reduktion der Grössenprogression von Aneurysmata) ist zu empfehlen, insbesondere bei Vorliegen atherosklerotischer Gefässveränderungen Regelmässige bildgebende Kontrollen wegen Aortendilatation (Aneurysmabildung) und Re-Dissektionen Kompliziert Aortaler Durchmesser > mm oder Zunahme > 10 mm/jahr, erneute Symptome (s.o.), wie Malperfusion oder rezidivierende Schmerzen Evaluation hinsichtlich interventioneller oder chirurgischer Therapie Quellen ESC Guidelines on the diagnosis and treatment of aortic diseases. European Heart Journal 2014 Interdisciplinary Expert Consensus Document on Management of Type B Aortic Dissection. JACC 2013 Dr. Lukas Hechelhammer PD Dr. Regula von Allmen Dr. Alexander Poloczek Prof. Dr. Hans Rickli
78 Akutbehandlung und Sekundärprävention beim ischämischen Schlaganfall und der Transitorischen Ischämischen Attacke (TIA) Prähospitalisationsphase Patienten müssen an Ort und Stelle und ohne Zeitverlust klinisch mithilfe geeigneter Skalen eingeschätzt und im Hinblick auf eine akute Intervention gescreent werden. Am bekanntesten ist die Cincinnati Prehospital Stroke Scale (CPSS), die in Aufklärungskampagnen verbreitet und instruiert werden kann. Eher auf den Notarztdienst zugeschnitten ist die Los Angeles Paramedic Stroke Scale (LAPSS). 1 FAST, Face Arm Speech (Abnormalities) and Telephone Ja Nein 1. Gesichtslähmung 2. Einseitige Armschwäche 3. Abnorme Sprache 4. Telefonische Benachrichtigung Notfalldienst Tab. 1: Die CPSS (aus dem Amerikanischen) Weitere Kriterien, die einen Schlaganfall wahrscheinlicher machen 1. Alter > 45 Jahre 2. Kein Anfallsleiden in der Anamnese 3. Auftreten der neurologischen Symptome in den letzten 24 Stunden Genauer Beginn der Symptomatik (Zeugen?) 4. Patient funktionell körperlich und mental unabhängig vor dem Ereignis 5. Blutglukose zwischen 3.3 und 22 mmol/l 1 Das modifizierte LAPSS-Formular kann von der Homepage des Schlaganfallzentrums heruntergeladen werden:
79 156 Falls alle Kriterien der CPSS erfüllt sind, liegt mit grosser Wahrscheinlichkeit eine Ischämie im vorderen Stromgebiet einer Hemisphäre vor. Dieser «Face/Arm/Speech»-Test hat bei einem positiven Hauptkriterium eine Sensitivität von ca. 90% für das Erkennen einer Ischämie im Mediastromgebiet. Schlechter ist die Sensitivität für das Erkennen einer Ischämie im Posteriorstromgebiet resp. im Hirnstamm (z. B. Basilaristhrombose). Nach der initialen Einschätzung Bei Verdacht auf Schlaganfall niederschwellig zuweisen, Zielspital an - rufen, das einen Akutbehandlungsauftrag im Rahmen eines Schlaganfallnetzwerkes hat (KSSG , diensthabenden Neurologen verlangen, hausinterne Nummer -6459), und als Schlaganfall-Notfall anmelden. Patiententransport via Sanitätsnotruf 144 oder REGA über die Telefonnummer 1414 anfordern. Massnahmen beschränken Sicherung der Vitalfunktionen Glukosegabe bei Hypoglykämie Wenn möglich, grosslumigen venösen Zugang kubital anlegen (weiss, grau oder orange) Unterlassen Keine Aspirin- oder Heparingabe (ischämischer und hämorrhagischer Infarkt können initial klinisch nicht unterschieden werden) In der Regel keine antihypertensive Behandlung Beachten Schlaganfälle können auch im Alter < 45 Jahre auftreten, selbst im Kindesalter. Keine Vorabklärungen in Institutionen durchführen, die keinen Akutbehandlungsauftrag haben. Wenn möglich, Begleitperson aus der Familie für Fremdanamnese und allfällig notwendige Entscheidungsfindung mitschicken oder zumindest eine Telefonnummer für Rückfragen notieren Wenn möglich, den Ereigniszeitpunkt eruieren (oder den zuletzt symptomfreien Zeitpunkt). Akutbehandlung des ischämischen Schlaganfalles Indikationskriterien für eine intravenöse Thrombolyse 2 oder eine endovaskuläre Revaskularisation 3 Klinische Diagnose eines ischämischen Schlaganfalls Behinderndes Defizit zum Zeitpunkt der Untersuchung (NIHSS-Score 4 Punkte) u/o Aphasie u/o Hemianopsie Intervall zwischen Symptom- und Therapiebeginn Stunden für intravenöse und 0 6 Stunden für endovaskuläre Revaskularisation (bei Verschlüssen der A. basilaris möglicherweise auch länger) Ausschluss einer akuten intrakraniellen Blutung im CT oder MRI Kontraindikationen für eine intravenöse oder intraarterielle Thrombolyse oder endovaskuläre Revaskularisation sind zahlreich und Bestandteil des Notfall-Screenings im Stroke Center resp. in der Stroke Unit. Merkpunkte Die systemische Thrombolyse mit rt-pa verbessert das Outcome beim akuten ischämischen Hirninfarkt. Bei proximalen Gefässverschlüssen bringt die endovaskuläre Revaskularisation in Kombination mit der systemischen Thrombolyse (Bridging) einen klaren Zusatznutzen. Ob allein oder in Kombination ist der Nutzen stark zeitabhängig. Zeitvorgaben: «Door to needle»: 30 Minuten «Door to groin puncture»: 60 Minuten 157
80 Die Einnahme von Aspirin und/oder Clopidogrel kontraindizieren nicht für die Thrombolyse. Bei Kombination beider Substanzen muss aber mit einer erhöhten postinterventionellen Blutungsrate gerechnet werden. Patienten unter therapeutischer, oraler Antikoagulation mit einem Vit.-K-Antagonisten (INR > 1.7) oder einem direkten oralen Antikoagulans können bei akutem Verschluss eines proximalen Gefässes mittels endovaskulärer Revaskularisation behandelt werden. Ein fortgeschrittenes Alter (> 80 Jahre) ist kein Ausschlusskriterium. Nach Thrombolyse/endovaskulärer Revaskularisation: keine Antiaggregantien/Antikoagulantien während 24 Std. bis zur Durchführung einer zerebralen Bildgebung zum Ausschluss einer relevanten Einblutung. Ausnahmen bei besonderen Umständen wie einer Dissektion der Karotis (individueller Entscheid) Patienten, bei denen keine Thrombolyse möglich ist (Kontraindikation, Zeitfenster überschritten etc.) sollten 250 mg Aspirin i.v. (alternativ 300 mg p.o.) und Heparin, initial 10'000 E/24 Std., nach der Durchführung einer zerebralen Bildgebung zum Blutungsausschluss erhalten. Bestehen Hinweise auf eine kardiale Embolie, wird 24 Std. postinterventionell mit intravenösem Heparin begonnen, initial mit 10'000 E/ 24 Std. Im Verlauf von 3 14 Tagen, abhängig von der Infarktgrösse, 4 erfolgt dann eine therapeutische Antikoagulation. Bei Wake-up-Stroke oder unklarem zeitlichen Beginn kann aufgrund einer Perfusionsstudie (CT, MRI) mit Mismatch zwischen Perfusionsstörung (dominant resp. gross) und Infarktkern (klein) eine Thrombolyse erwogen werden. Eine signifikante Besserung mit sekundärer Verschlechterung ist in der Akutsituation möglich, weshalb eine kontinuierliche Überwachung über mindestens 24 Std. indiziert ist. Probleme in der akuten und postakuten Phase In der akuten bzw. postakuten Phase können spezifische neurologische und allgemein internistische Probleme zu lebensbedrohlichen Komplikationen führen oder durch Interaktion mit der zerebrovaskulären Reserve das neurologische Outcome beeinträchtigen. Entsprechend ist die Betreuung des akuten Schlaganfallpatienten durch ein erfahrenes Behandlungsteam (Stroke Unit) mit einem besseren Outcome assoziiert. Dysphagie nach Schlaganfall Schluckstörungen nach Schlaganfall sind häufig (bis 50%). Wegen des Aspirationsrisikos und des Risikos der Mangelernährung müssen systematisch nach einer Schluckstörung gesucht (Dysphagiescreening) und allenfalls therapeutische Schritte eingeleitet werden Masseneffekt durch malignes Hirnödem 5 Indikation für frühzeitige (24 48 Std.) parieto-temporale Schädeldekompression bei malignem Mediainfarkt Alter < 60 ( 70) Jahre Symptombeginn vor < 24 Stunden (in Ausnahmefällen auch später) Im CT oder MRI Infarktzeichen, die mindestens die Hälfte des Media stromgebietes umfassen Mutmasslicher Wille des Patienten für ein aktives Vorgehen Keine Kontraindikationen für eine Operation Ein erfolgloser Rekanalisationsversuch bzw. eine erfolglose Thrombolyse ist ein weiteres Argument für eine Hemikraniektomie Indikation für okzipitale Schädeldekompression bei Kleinhirninfarkt, meist ergänzt durch externe Ventrikeldrainage (EVD) Zeichen einer progressiven Druckerhöhung im Hirnstammbereich Radiologisch sichtbare Raumforderung Mutmasslicher Wille des Patienten für ein aktives Vorgehen Keine Kontraindikationen für eine Operation 2 Empfehlungen der Themengruppe «Akuttherapie des Hirnschlags», Schweizerische Hirnschlaggesellschaft, Schweiz Med Forum 2009;9: Berkhemer, et al. A randomized trial of intraarterial treatment for acute ischemic stroke. N Engl J Med 2015;372(1): Zeit bis Beginn OAK: TIA: sofort; kleiner Infarkt: 3 5 Tage; mittelgrosser Infarkt: 5 7 Tage; grosser Infarkt: 14 Tage
81 Probleme, welche die zerebrovaskuläre Reserve beeinträchtigen können Hochgradige Stenose der A. carotis interna Arterielle Hypertonie und Hypotonie Tachyarrhythmie und Bradyarrhythmie, meist im Rahmen eines Vorhofflimmerns (s.u.) Seltene Probleme Zentrale Apnoe und Hypopnoe bei medullären Infarkten Behandlungsbedürftiges obstruktives Schlafapnoesyndrom Allgemein-internistische Probleme in der akuten und postakuten Phase Bei Temp. > 37.5 C (tympanal) antipyretische Therapie (physikalisch, medikamentös (Paracetamol oder Metamizol) einsetzen. Zudem rasche Fokussuche (Anamnese, Abnahme von Blutkulturen, Thorax- Röntgenbild mit Frage nach Aspirationspneumonie, Urinstatus), damit bei bakteriellem Infekt eine gezielte antibiotische Therapie zeitnah begonnen werden kann Infusionen: primär NaCl 0.9% als Grundinfusion. Hypotone Infusionslösungen wie z. B. Glukose 5% vermeiden (Cave: Hirnödem) Thromboembolieprophylaxe: bei eingeschränkter Mobilität (und fehlenden Kontraindikationen) Gabe von niedermolekularem Heparin s.c. in prophylaktischer Dosierung. Bei Kontraindikationen intermittierende pneumatische Kompression der Beine Blutzucker: engmaschige Kontrolle (Blutzuckertagesprofil) und Nüchtern-Werte zwischen 5.5 und 8.5 mmol/l anstreben Rasche Wiederaufnahme der enteralen Ernährung (bei Thrombo lyse frühestens am nächsten Tag), bei Dysphagie mittels nasogastraler Sonde. Parenterale Ernährung nur in Ausnahmefällen Sauerstoffgabe: Es soll bei der Sauerstoffsättigung ein Ziel von > 94% angestrebt werden. Blutdruck: Vor Beginn und innerhalb der ersten 24 Std. nach Thrombolyse sind Werte von < 180/100 mmhg anzustreben, aber schnelle Blutdruckabfälle um > 20% des Ausgangswertes zu vermeiden. Ansonsten wird eine akute Behandlungsbedürftigkeit erst bei persistierenden Werten > 200/110 mmhg angenommen Die Blutdruckuntergrenze richtet sich nach dem klinischen Bild, als Faustregel gilt > 120/80 mmhg. Symptomatische Hypotonien primär mit Volumengabe (NaCl 0.9% i.v.) behandeln Transitorische Ischämische Attacke (TIA) Die transitorische ischämische Attacke wird heute als neurologischer Notfall angesehen, da das Risiko, einen schweren Schlaganfall zu erleiden, innerhalb der ersten 48 Stunden bei bis zu 12% liegt. Deshalb müssen unter den TIA-Patienten die Hochrisiko-Patienten rasch identifiziert werden. Als solche gelten alle mit einem ABCD 3 - resp. ABCD 3 -I- Score von 4 Punkten und mehr. Dabei beinhaltet der bessere und bei uns angewendete ABCD 3 -I-Score zusätzlich den mgl. Nachweis einer ipsilateralen Stenose von mehr als 50% (CTA oder Doppler-/Duplexsonographie) und einer DWI-Läsion. Abhängig von der Einschätzung des Rezidivrisikos und der Latenz nach der TIA, der Risikokonstellation und den lokal verfügbaren Ressourcen soll der Entscheid für eine rasche ambulante oder stationäre Abklärung gefällt werden. Durch eine rasche Abklärung und Behandlung können ca. 80% der Rezidive verhindert werden
82 Schlaganfall therapeutischer Entscheidungsbaum zum Inhaltsverzeichnis Lyse Call Radiologe wird verständigt (Dienstarzt 6622) CCT nativ Lyse Behandlungsoption: Latenz Symptombeginn-Behandlung < 4.5 Std.; ab Std. individueller Entscheid NIHSS 4 od. fkt. sign. Ausfall Keine weiteren Ausschlusskriterien (siehe Kasten unten links) ICB/SDH Tumor Ischämie > 1 / 3 Terr. SAB wenn unklares Ischämieareal Ischämie < 1 / 3 Terr. oder unklar Optional: Unklares Zeitfenster (z. B. «Wake-up-Stroke») Entscheid je nach Mismatch im Perfusions-CT Unklarer Befund Keine weitere akute Bildgebung CT-Angiografie Neurochirurgen verständigen zeitnah MRT ± KM und/oder DSA Überwachung NIPS Neurochirurgen verständigen CT-Perfusion Verschluss A. basilaris ACI M1/M2, A1, P1 Peripherer Ast-Verschluss/ Kein Verschluss > 1/3 = Demarkierung (Infarzierung) von mehr als 1/3 des Territoriums der Arteria cerebri media Ausschlusskriterien für medikamentöse Lyse Intrakranielle Blutung aktuell oder in den letzten 6 Monaten Septische Embolien, Endokarditis, Enzephalitis, Pankreatitis Verlängerte INR (> 1.7; unter Phenprocoumon) oder aptt Einnahme von Dabigatran oder Faktor-Xa-Inhibitoren in den letzten Stunden Aktuelle Einnahme von GPIIbIIIa-Antagonisten Thrombozytopenie < 100 G/l Schweres Trauma Chirurgie an nicht komprimierbaren Organen in den letzten 14 Tagen Geburt vor weniger als 14 Tagen Gastrointestinale oder urogenitale Blutungen vor weniger als 21 Tagen Medikamentös nicht senk- und kontrollierbarer Blutdruck > 180/100 mmhg Rasche und spontane Regredienz der Symptome, sodass der Patient bei Behandlungsbeginn ohne relevante Behinderung ist* Infarktfrühzeichen in > 1 / 3 des Mediastromgebietes* Ischämischer Hirninfarkt in den letzten 3 Monaten* Arteriovenöse Malformation oder Aneurysma* Schädel-Hirntrauma in den letzten 3 Monaten* Hypoglykämie (< 2.7 mmol/l) oder Hyperglykämie (> 22.2 mmol/l)* Epileptischer Anfall zu Symptombeginn (Diskrimination epileptischer Anfall vs. Frühanfall bei Ischämie mittels Perfusions-CT abklären)* Schwangerschaft* Intrakranielle Tumoren* Lumbalpunktion in den letzten 7 Tagen* Traumatische oder > 10 Minuten dauernde Reanimation in den letzten 21 Tagen* Punktion einer nicht-komprimierbaren Arterie in den letzten 7 Tagen* Schwere Komorbidität* Symptombeginn nicht eruierbar, z. B. Auftreten im Schlaf (Entscheid im Zweifelsfall auf Perfusions-CT abstützen)* Überwachung NIPS * relative Kriterien (EVB: alle relativ) Neuroradiologen verständigen i.a./mech. Lyse (EVB) wenn mgl. Bridging (i.v. Lyse mit 0.9 mg/ kg KG rt-pa, EVB) i.v. Lyse Anmerkung: Wenn medikamentöse Lyse nicht möglich, mechanische Rekanalisierung bedenken (Thrombusaspiration, Stent, PTA usw.)
83 Risikoeinschätzung anhand des ABCD 3 - und ABCD 3 -I-Score 5 Empfehlungen der Schweizerischen Arbeitsgruppe: International Journal of Stroke 2009;4: ABCD 3 - Score ABCD 3 -I- Score Alter 60 Jahre 1 1 Blutdruck 140/90 mmhg 1 1 Klinische Faktoren Dauer Sprachstörung ohne halbseitige Schwäche 1 1 Halbseitige Schwäche Minuten Minuten 2 2 Diabetes mellitus 1 1 Vorangegangene TIA in den letzten 7 Tagen 2 2 Ipsilaterale 50%ige Stenose der A. carotis interna NA 2 DWI-Läsion im MRT NA 2 Summe Wenn die Kriterien nicht zutreffen, werden 0 Punkte vergeben. NA = nicht zutreffend; TIA = transitorische ischämische Attacke Sekundärprävention nach Schlaganfall/TIA Pharmakotherapie Antithrombotische Behandlung In der Regel Aspirin, 300 mg/tag in der Akutphase, nach 7 Tagen, 100 mg/tag Extrakranielle Gefässdissektion (3 6 Monate): Aspirin 100 mg/tag oder orale Antikoagulation mit Marcoumar [INR-Ziel: 2 3]) In ausgewählten Fällen mit sehr hohem Schlaganfallrezidivrisiko (hochgradige, unter Aspirin symptomatische intra-/extrakranielle Stenose, ulzerierte Plaque, positives Embolie-Monitoring in der Doppler sonografie unter Aspirin): Aspirin 100 mg/tag + Clopidogrel 75 mg/tag Eine Langzeitdoppeltherapie (> 3 Monate) ist aus rein neurologischer Sicht nicht indiziert, da das Blutungsrisiko den sekundärprophylaktischen Nutzen überwiegt. Bei Therapieversagen Wirksamkeit der Thrombozytenaggregationshemmer durch den Multiplate-Test in vitro prüfen Empfehlungen für die Behandlung der arteriellen Hypertonie Blutdruck-Ziel < 140/90 mmhg ACE-Hemmer in Kombination mit thiazidähnlichen Diuretika sind erste Wahl. Alternativ Kalziumantagonisten und Angiotensin-II- Antagonisten, letztere nicht in Kombination mit ACE-Hemmern. Betablocker gehören in dieser Situation nicht zu den Mitteln der ersten Wahl. Die Auswahl des Medikamentes muss gegebenenfalls den Begleiterkrankungen (KHK, PAVK, Diabetes mellitus, Niereninsuffizienz) angepasst werden. Gewichtsreduktion, körperliches Training, salzarme Ernährung und Einschränkung des Alkoholkonsums helfen bei der Blutdrucksenkung und sollten die medikamentöse Therapie ergänzen. Empfehlungen für die medikamentöse Lipidsenkung Bei Patienten mit ischämischem Hirninfarkt ist eine Therapie mit einem potenten Lipidsenker (Statin) unabhängig von den Ausgangswerten indiziert. Zielwert LDL < 2.6 mmol/l Behandlung mit Antikoagulantien Indikation zur oralen Antikoagulation Kardiale Emboliequelle* (lebenslang) Nicht-valvuläres Vorhofflimmern (CHA2DS2VASc 2 oder CHA2DS2VASc 1 [ausser Frauen < 65 Jahre] mit HAS-BLED < 3)** OAK mit DOAC (Apixaban, Dabigatran, Rivaroxaban oder Edoxaban) unter Beachtung von Nebenwirkungen, Vorsichtsmassnahmen und Kontraindikationen
84 TIA < 7 Tage TIA < 14 Tage TIA < 90 Tage Notfallmässige Zuweisung Klinische Evaluation, CT/ MRI, Bildgebung Karotis 1 u. EKG am gleichen Tag Einleitung Sekundärprophylaxe Hospitalisation Neurologie 4 ja Sofortige Zuweisung (Tel / Fax ) in neurovaskuläre Ambulanz resp. ZNA Klinische Evaluation, CT/ MRI, Bildgebung Karotis 1 u. EKG < 24 Std. Einleitung Sekundärprophylaxe Hohes Rezidivrisiko 2 oder andere Hospitalisationsgründe 3 Sofortige Zuweisung (Fax ) in neurovaskuläre Ambulanz Klinische Evaluation, CT/ MRI, Bildgebung Karotis 1 u. EKG < 3 Tage nein Einleitung Sekundärprophylaxe Ambulante Abklärung und Behandlung 1. CT-Angio (extra- und intrakraniell) oder Duplexsonografie der hirnzuführenden Gefässe (extra- und transkraniell). Notfall-MRI innerhalb von 24 h, nicht zwingend am gleichen Tag und nur, wenn ABCD 3 -I-Score ABCD 3 resp. ABCD 3 -I-Score > 4 Punkte 3. Co-Morbiditäten beachten wie Herzinsuffizienz, instabile Angina pectoris 4. Der Entscheid, ob der Patient auf die NIPS aufgenommen wird, kann der entsprechenden Indikationsliste entnommen werden. Bei TIAs sind dies: ABCD 3 resp. ABCD 3 -I-Score > 4 Punkte, Vorhofflimmern, andere schwere Co-Morbiditäten Falls DOAC ungeeignet: Marcoumar mit INR-Ziel 2.5 (2 3) 6 (Bei zusätzlicher stabiler koronarer Herzkrankheit Zugabe von Thrombozytenaggregationshemmern nicht notwendig) Rheumatische Mitralstenose (je nach Begleitumständen) Mechanische Herzklappe: Marcoumar: INR-Ziel 2.5 (2 3) in aortaler, 3 ( ) in mitraler Position***, DOACs sind hier kontraindiziert Kardiale Emboliequelle* (vorübergehend [3 6 Monate] Marcoumar) Intrakardialer Thrombus; INR-Ziel 2.5 (2 3)**** Akuter Myokardinfarkt mit Herzwandaneurysma mit oder ohne Nachweis eines intrakardialen Thrombus; INR-Ziel 2.5 (2 3)**** Biologische Herzklappen; INR-Ziel 2.5 (2 3), meist nur 3 Monate postoperativ Sinus-/Hirnvenenthrombose (3 6 Monate Marcoumar); INR-Ziel 2.5 (2 3) Hochgradige Karotisstenose Bei hochgradigen, symptomatischen Karotisstenosen (> 70% [distaler Stenosegrad/NASCET]) ist ein Stenting oder eine Endarteriektomie indiziert. Der Nutzen der invasiven Therapie nimmt mit progredientem Stenosegrad zu. Der Nutzen der invasiven Therapie ist geringer bei einem Stenosegrad zwischen 50 und 70%, bei Frauen und wenn der Eingriff jenseits der 12. Woche nach dem Indexereignis durchgeführt wird. Der Zeitraum zwischen Ereignis und invasiver Therapie sollte mit Thrombo zytenaggregationshemmern überbrückt werden (ASS 100 mg). Ist eine Stenose unter einem Thrombozytenaggregationshemmer symptomatisch geworden, empfiehlt sich die Kombination von ASS 100 mg/ Tag mit Clopidogrel 75 mg/tag bis zur Operation. Danach ASS 100 mg/ Tag. Zudem sollte bis zum Eingriff ein hochpotentes und hochdosiertes Statin (z. B. 80 mg Atorvastatin) verabreicht werden. Wird primär 6 Dosierung der NOAK gemäss Präparat, Nierenfunktion und Indikation
85 168 ein Stenting erwogen, soll eine Kombination von ASS 100 mg/tag mit Clopidogrel 75 mg/tag 8 Tage vor Eingriff durchgeführt und eine evtl. Non-Respondance 1 Tag vor dem Eingriff mittels Multiplate-Test überprüft werden. Die Karotisangioplastie mit Stenteinlage hat im Vergleich zur operativen Therapie in Bezug auf das periprozedurale Risiko bei der Behandlung symptomatischer Karotisstenosen ein leicht erhöhtes Kurzzeitrisiko (insbesondere bei Patienten > 70 Jahre). Bei unter 70-Jährigen ist das periprozedurale Risiko des Stentings vergleichbar mit dem der Endarterektomie. Die Langzeitergebnisse (10 Jahre) bezüglich Schlaganfall sind für beide Verfahren vergleichbar. Die Restenoserate ist vergleichbar. Die Karotisendarterektomie ist derzeit die Therapie der ersten Wahl bei Patienten über 70 Jahre. Bis 70 Jahre sind beide Verfahren als gleichwertig einzustufen. Ein Stenting ist Therapie der Wahl bei Patienten mit Rezidivstenose nach TEA, hochgradiger Stenose nach Strahlentherapie oder hoch sitzender und einer chirurgischen Intervention schwer zugänglichen Stenose sowie bei Hochrisikopatienten. Persistierendes Foramen ovale, PFO Sekundärprophylaxe bei PFO 7 Sekundärprophylaxe (Thrombozytenaggregationshemmer /Statin) in der Regel unabhängig vom Entscheid bezüglich PFO-Verschluss beibehalten Ausgenommen sind Patienten mit genereller Empfehlung zu einer OAK (Gerinnungstörung, Lungenembolie, TVT, usw.). Kriterien bezüglich eines Studieneinschlusses prüfen (aktuell laufende Studie Neurologie KSSG: RE-SPECT ESUS (Dabigatran vs. ASS bei kryptogenem Schlaganfall mit embolischem Muster) * Bei akutem Territorialinfarkt volle Antikoagulation nur in Ausnahmefällen (Gefässdissektion, Sinus-/ Hirnvenenthrombose, intrakardialer Thrombus, flottierender Thrombus in der ACI) zu erwägen. Ansonsten in den ersten 7 Tagen keine therapeutische Verlängerung der PTT/PiCT anstreben ** Bei Vorhofflimmern und stabiler Koronarer Herzkrankheit soll Aspirin nicht routinemässig zusätzlich zur oralen Antikoagulation gegeben werden, Ausnahme Patienten mit koronarem Stent für 1 Jahr Vaskuläre Risikofaktoren sind unabhängig davon gemäss der üblichen Risikostratifizierung zu therapieren. Der RoPE-Score erlaubt es, bei Patienten mit kryptogenem (ungeklärtem) Schlaganfall die Prävalenz eines inzidentellen vs. eines pathogenen PFO abzuschätzen. Grundsätzlich gilt, dass ein RoPE-Score von 6 für ein pathogenes PFO hinweisend ist. ASA = Atriales Septumaneurysma TAH = Thrombozytenaggregationshemmer Kryptogener Stroke PFO Medikamentöse TH PFO-Verschluss Erstereignis RoPE-Score 6 Punkte (junges Alter+geringe vrf) Erstereignis und RoPE-Score < 6 Punkte (hohes Alter und viele vrf) Rezidiv-Stroke (erneut kryptogen, Embolic Stroke of Undetermined Source [ESUS]) +/- ASA TAH diskutieren +/- ASA TAH Nein +/- ASA OAK empfehlen 7 Prozedere wird im KSSG im Rahmen des interdisziplinären PFO-Kolloquiums festgelegt * Bei akutem Territorialinfarkt volle Antikoagulation nur in Ausnahmefällen (Gefässdissektion, Sinus-/ Hirnvenenthrombose, intrakardialer Thrombus, flottierender Thrombus in der ACI) zu erwägen. Ansonsten in den ersten 7 Tagen keine therapeutische Verlängerung der PTT/PiCT anstreben ** Bei Vorhofflimmern und stabiler Koronarer Herzkrankheit soll Aspirin nicht routinemässig zusätzlich zur oralen Antikoagulation gegeben werden, Ausnahme Patienten mit koronarem Stent für 1 Jahr *** Je nach Thrombogenität und Lokalisation der Klappe sowie zusätzlichen Risikofaktoren werden auch höhere Ziel-INR empfohlen. Bei ischämischem Insult/TIA trotz adäquater OAK, Zugabe von 100 mg Aspirin/Tag, falls kein hohes Blutungsrisiko vorliegt **** Dauer vom echokardiografischen Verlauf abhängig machen 169
86 RoPE-Score Punkte keine arterielle Hypertonie 1 kein Diabetes 1 kein(e) Stroke/TIA in der Vorgeschichte 1 Nichtraucher 1 kortikaler Infarkt (CT/MRI) 1 Alter Jahre Jahre Jahre Jahre Jahre 1 70 Jahre 0 Total 10 Kent, et al. Trials 2011;12:185. Kent, et al. Neurology 2013;81: Links Dr. Georg Kägi Dr. Jochen Vehoff Dr. Markus Diethelm Dr. Gian-Reto Kleger Mitarbeit von: Dr. Johannes Weber, Dr. Dieter von Ow, Dr. Daniel Weilenmann, Prof. Dr. Wolfgang Korte Medikamentöse Behandlung nach interventionellem, kathetertechnischem PFO-Verschluss Kombination von ASS 100 mg/tag und Clopidogrel 75 mg/tag während 12 Wochen, danach ASS 100 mg/tag für weitere 3 Monate Schliesslich Thrombozytenaggregationshemmung stoppen oder weiterführen gemäss üblichem Indikationsspektrum Periinterventionelles Management bei Patienten nach ischämischem Schlaganfall unter oraler Antikoagulation (OAK) Siehe Kapitel: Periinterventionelles Management bei Patienten mit Thrombozytenaggregationshemmern bzw. OAK
87 Behandlungsstandard intrakranielle Blutung Ätiologie Die häufigsten Ursachen von nicht-traumatischen Hirnblutungen sind die hypertensive (Stammganglien-) Blutung oder Blutungen bedingt durch Aneurysmen (Subarachnoidalblutung) resp. vaskuläre Malformationen. Die Lokalisation der Blutung liefert bereits wichtige Hinweise auf die zugrunde liegende Ätiologie. Ätiologien intrakranieller Blutungen Chronische arterielle Hypertonie (typisch: hypertensive Stammganglienblutung oder Thalamusblutung mit Ventrikeleinbruch) Aneurysmen Vaskuläre Malformationen Gefässwandschäden bei Amyloidangiopathie (v.a. bei älteren Patienten und infektiösen Erkrankungen) Blutungsdiathese Antithrombotika Fibrinolytika Thrombozytopenie/Thrombozytopathie Hämophilie Leukämie Drogen Sinus-/Hirnvenenthrombosen Schädel-Hirn-Trauma Metastase/Tumor Ischämischer Hirninfarkt mit sekundärer Einblutung
88 Diagnostik Da die Hirnblutung klinisch nicht sicher von einem ischämischen Hirninfarkt unterschieden werden kann, weicht die initiale Diagnostik nicht von derjenigen des ischämischen Hirninfarktes ab. Diagnostik: natives CT und CT-Angiografie. Bei atypischer Blutung (thalamisch, lobär) sollte immer auch die Möglichkeit einer Stauungsblutung bei Sinus-/Hirnvenenthrombose in Betracht gezogen werden. Entsprechend sollte die initiale Abklärung durch eine CT-Venografie ergänzt werden. Die CT-Angiografie liefert wertvolle Informationen über die Ursache (Aneurysma, AV-Malformation), aber auch über das weitere Nachblutungsrisiko (Spot-Sign). 1 Da sich die Hirnblutung typischerweise in den ersten 24 Stunden vergrössert, empfiehlt sich eine Verlaufsbildgebung nach diesem Zeitintervall. Bei Lobärblutungen wird im Verlauf der ersten Woche die Abklärung durch eine Schädel-MRI, inkl. Hämosiderin-sensitive Sequenzen und der Frage nach Amyloidangiopathie, ergänzt. Je nach klinischer Fragestellung sollte nach Resorption der Blutung nach 3 Monaten eine Verlaufs-MRI erfolgen, v.a. mit der Frage nach Kavernom oder sonstigen parenchymatösen Blutungsquellen. Allgemeine, konservative Massnahmen Überwachung auf NIPS, CHIPS oder MIPS in Abhängigkeit von der neurologischen Symptomatik und den Vitalparametern; zu beachten ist, dass die Kontrolle der Herz-Kreislauf-Parameter in den ersten 48 bis 72 Std. das Outcome verbessert. Lagerung: 30 Oberkörperhochlagerung Arteriellen Blutdruck senken: Studienlage bezüglich früher intensiver Blutdrucksenkung ist nicht eindeutig, wir empfehlen eine unmittelbare (innerhalb 1 Stunde) Blutdrucksenkung auf < 180 mmhg systolisch, mit einem Zielblutdruck auf < 160 mmhg systolisch Empfohlene Medikamente zur BD-Senkung: Urapidil (Ebrantil ) i.v., Lisinopril (Zestril ) p.o. Das Blutdruckziel im weiteren Verlauf ist jedoch < 140mmHg syst. Prophylaxe tiefer Beinvenenthrombosen/Lungenembolien: Pneumatische Kompressionstherapie Frühzeitige (ab Tag 2) Therapie mit Heparin resp. niedermolekularem Heparin in prophylaktischer Dosierung, Kontrolle der PiCT bzw. des Anti-Xa-Spiegels in Erwägung ziehen (bei prophylaktischer Dosierung macht eine PiCT-Kontrolle keinen Sinn) andere mögliche Ursachen der Blutdrucksteigerung beheben (Schmerzen, Harnverhalt usw.) bewusstseinsgestörte Patienten (GCS < 9) und/oder Schluckstörungen: Intubation, ggf. Hirndrucksonde (MIPS/CHIPS) Medikamentöse/nicht-operative Hirndruckbehandlung bei klinischer Verschlechterung im Zusammenhang mit zunehmendem Hirnödem Nicht-operative Hirndrucktherapie: Mannitol, hypertone NaCl-Lösung und kurzzeitige Hyperventilation Bei Auftreten epileptischer Anfälle medikamentöse antikonvulsive Therapie mind. während 30 Tagen Frühe Mobilisation nach 24 Stunden bei stabiler Blutung und fehlendem Hinweis auf erhöhten intrakraniellen Druck 1 Indikator für Nachblutungsrisiko Lancet Neurol 2012;11:
89 Hämostasiologische Massnahmen Hintergrund: Antikoagulantien-Blutungen sind mit einem grösseren Blutungsvolumen 2 und einem schlechteren Outcome 3 assoziiert: Unklar ist, ob das Outcome relevant durch eine schnelle Antagonisierung verbessert werden kann. 4 Bei spontanen intrazerebralen Blutungen sind keine hämostasiologischen Massnahmen indiziert. Therapie von Hirnblutungen unter oraler Antikoagulation mit Vitamin K- Antagonisten (Marcoumar, Sintrom), INR > 1.4 OAK wird unterbrochen und der INR durch kombinierten Einsatz von Prothrombinkomplex PPSB (PCC) + 10 mg Vitamin K (Konakion) normalisiert (CAVE: Halbwertszeit von Konakion kürzer als von Marcoumar, deshalb kann die INR im Verlauf wieder ansteigen!) Dosierungen siehe Tabelle auf Seite 178. Bei Kontraindikation für PCC (bekannte Unverträglichkeit, Verbrauchskoagulopathie, HIT) Gabe von Frischplasma (FFP) + 10 mg Vitamin K (Konakion), Dosierung s.u. Therapie von Hirnblutungen unter / nach Therapie mit Heparin (UFH/ NMH) mit nachweislicher Anti-Xa-Aktivität: Heparin stoppen Gabe von Protaminsulfat, Dosierungen siehe Tabelle auf Seite 178. Therapie von Hirnblutungen unter direkten oralen Antikoagulantien (Dabigatran, Rivaroxaban, Apixaban, Edoxaban): Stopp des Antikoagulans, Bestimmung der Gerinnungsparameter (Quick, PTT [Thrombinzeit (TT)], Fibrinogen, Faktor XIII, Aktivitätsspiegel der jeweiligen Substanz; Rivaroxaban, Apixaban, Edoxaban Bestimmung über Anti-Xa-Aktivität (wichtig: Substanz angeben!), beeinflussen insbesondere auch Quick; Dabigatran Wirkung auf PTT und insbesondere Thrombinzeit) Aufgrund der kurzen Halbwertszeit (7 14 Std.) der DOACs nimmt der Einfluss auf die Hämostase rasch ab. Im Falle einer eingeschränkten Nierenfunktion muss eine deutlich verlängerte Halbwertszeit berücksichtigt werden. Bei Einnahme eines DOACs innerhalb der letzten 24 Std. sollte unabhängig von den Gerinnungswerten Tranexamsäure 1 g i.v. (8-stündlich, für Std.) verabreicht werden. Die Gabe von Vitamin K, FFP (fresh frozen Plasma) sowie DDAVP (Desmopressin) kann nicht empfohlen werden. intracerebrale Blutungen mit drohender Progression (Beginn <6h, spot sign, therapeutische Thrombinzeit) sollten durch Idarucizumab (Praxbind ) antagonisiert werden. Idarucizumab bindet spezifisch an Dabigatran und hebt dessen gerinnungeshemmende Wirkung auf. Die empfoh lene Dosis von Praxbind beträgt 5 g (2 2.5 g / 50 ml), die intravenös als zwei aufeinanderfolgende Infusionen über je 5 bis 10 Minuten oder als Bolusinjektion verabreicht werden. Bei fehlendem klinischem Effekt und laborchemisch nachweislicher aktiven Substanz eines Faktor-Xa-Inhibitors (Rivaroxaban, Apixaban, Edoxaban) ist nach Rücksprache mit dem Dienstarzt Hämatologie die Gabe von rekombiniertem Faktor VIIa (rfviia) oder Prothrombin complex concentrate (PCC, IU/kg) zu erwägen. Ein Faktorenmangel sollte spezifisch substituiert werden (Vorgehen gemäss perioperativem Procedere KSSG): Fibrinogen < 1.5 g/l, Haemocomplettan 2 g, Faktor XIII < 60, Fibrogammin IE Therapie von Hirnblutungen bei Thrombozytopenie (< ) oder Thrombozytenfunktionsstörung: Plättchenkonzentrat Therapie einer Hirnblutung bei thrombotisch-thrombozytopenischer Purpura: FFP und Kortison, evtl. Plasmapherese 2 Neurology 2008;71: Stroke 2008;39: Stroke 2012;43:
90 Management von Blutungen unter Antikoagulantien Marcoumar (Ziel-INR < 1.5) Heparin (UFH/NMH) Dabigatran Faktor-Xa- Hemmer (Einnahme innerhalb der letzten 24 h) Prothrombin-Komplex (Beriplex P/N 500) Frischplasma Vitamin K (Konakion) Protaminsulfat Idarucizumab Tranexamsäure PCC od. rfviia Bei INR E Beriplex P/N, erneute INR-Messung nach 10 min, wenn INR noch 1.8, erneut 500 E Beriplex 10 ml/kg KG reduzieren die INR von 4.2 auf 2.4, eine INR von 3.0 auf 2.1 oder eine INR von 2.4 auf 1.8 Zur Reduktion der INR von 4.2 auf 1.4 sind 40 ml/kg KG nötig. Bei INR mg i.v., im Verlauf je nach INR-Messung Wirkungseintritt nach ca. 4 6 Std E Protamin i.v. (1 ml) inaktivieren 1'000 E des in den letzten 4 Std. verabreichten Heparins; bei NMH Rücksprache DA Hämatologie 2 x 2.5 g (aufeinanderfolgend als Kl o. Bolus 1 g Bolus i.v., 8-stündlich für Std. Chirurgische Massnahmen Intrazerebrale Blutungen erfordern in Bezug auf die neurochirurgischen Behandlungsoptionen wegen der Vielzahl der potenziell zugrunde liegenden Ursachen eine differenzierte Betrachtung. Die Behandlungsstrategie ist abhängig von der neurologischen Symptomatik und Prognose der Patienten. Bei spontaner, nicht-aneurysmatischer Hirnblutung ist die Prognose im Wesentlichen vom Glasgow Coma Scale, dem Blutvolumen, der intraventrikulären Hämorrhagie, der Blutungs lokalisation und dem Alter des Patienten abhängig. 5 Sekundäre Blutungen im 5 Hemophill et al. Stroke 2001 Ggf. bei instabilen Situationen nach Rücksprache mit DA Hämatologie (KSSG) Rahmen einer Gefässmissbildung (Aneurysma, AV-Malformation) erfordern in der Regel eine neurochirurgische und/oder neuroradiologische Intervention mit kompletter Ausschaltung der Blutungsquelle. Aneurysmatische oder andere Blutungen i.r. einer Gefässmissbildung Die Behandlung und die Festlegung des Prozedere bei Blutungen in der Folge einer Gefässmissbildung (z. B. Aneurysma, AV-Malformation, AV-Fistel) erfolgt durch die Klinik für Neurochirurgie in Kooperation mit der interventionellen Neuroradiologie. Bei entsprechenden Pathologien erfolgt die Behandlung und Überwachung in aller Regel auf der chirurgischen Intensivpflegestation (CHIPS). Supratentorielle, nicht-aneurysmatische Hirnblutungen Die operative Therapie einer supratentoriellen, nicht-aneurysmatischen Hirnblutung bedarf jeweils einer individualisierten Therapieentscheidung. Bei Patienten mit einem kritischen Anstieg des intrakraniellen Drucks und/oder einer signifikanten neurologischen Ausfallsymp tomatik durch den rauforderndem Effekt der Blutung sollte eine operative Therapie in Erwägung gezogen werden. Grundsätzlich wird zwischen der Kraniotomie und minimal-invasiven Operationstechniken zur Hämatomevakuation unterschieden. Die bestmögliche Therapieoption wird interdisziplinär durch die Klinik für Neurologie und Neurochirurgie festgelegt. Bei oberflächlichen Hirnblutungen ( 1 cm von der Kortexoberfläche) ohne Ventrikeleinbruch führt die Kraniotomie mit Hämatomevakuation im Vergleich zur bestmöglichen konservativen Therapie zu einem kleinen Vorteil im Hinblick auf die Sterblichkeit, ohne das Risiko für Langzeit- Behinderung zu erhöhen. 6 Patienten mit tief liegenden Hämatomen (Stammganglien, Hirnstamm) profitieren nicht von einer Hämatomausräumung mittels Kraniotomie. 7 6 Mendelow et al Lancet Mendelow et al., Lancet 2005;365:
91 Minimal-invasive Operationstechniken zur Hämatomevakuation (Endos kopie oder Stereotaxie) zeigen möglicherweise im Vergleich zur bestmöglichen konservativen Therapie und/oder Kraniotomie einen Vorteil im Hinblick auf Langzeit-Behinderung und Sterblichkeit. 8 Dies gilt sowohl für oberflächliche als auch für tief liegende Blutungen. Nicht-aneurysmatische Kleinhirnblutungen Eine operative Therapie bei spontanen, nicht-aneurysmatischen Kleinhirnblutungen soll in Erwägung gezogen werden, wenn der Hämatom- Durchmesser > 3 cm beträgt und/oder eine Hirnstammkompression oder klinisch und bildgebend Hinweise für einen Hydrocephalus be - s tehen. 9 In diesen Fällen ist die Therapie der Wahl die subokzipitale Kraniotomie mit Hämatomevakuation und Anlage einer externen Ventrikeldrainage (EVD). Bei Kleinhirnblutungen handelt es sich immer um einen obstruktiven Hydrozephalus. Die EVD-Anlage ohne Hämatomevakuation wird bei Kleinhirnblutungen > 3 cm in der Regel nicht empfohlen. Bei entsprechender Klinik bzw. bildmorphologischen Befunden (s.o.) sollte tendenziell die operative Therapie zeitnah durchgeführt werden, um eine weitere klinische Zustandsverschlechterung zu verhindern. Erstaunlich gute Resultate können nach chirurgischer Evakuation zerebellärer Hämatome erzielt werden; dies spiegelt sich auch in der deutlichen Empfehlung der AHA/ASA zur operativen Dekompression bei zerebellärer Hämorrhagie wider. 10,11 Intraventrikuläre Blutungen/Hydrocephalus In etwa der Hälfte aller Patienten mit spontaner, nicht-aneurysmatischer Hirnblutung kommt es zu einer intraventrikulären Hämorrhagie mit dem Risiko, einen akuten Hydrocephalus zu entwickeln. Bei klinischen und/oder bildgebenden Hinweisen für einen Hydrocephalus sollte die 8 Vespa et al. Stroke Hanley et al. Lancet Neurol Dunne et al.; Q J Med 1987; 64: Lewis et al. ; Stroke. 2010;41: Anlage einer externen Ventrikeldrainage (EVD) frühzeitig erfolgen. Die Anlage einer lumbalen Liquordrainage bleibt einzelnen Spezialfällen vorbehalten. Eine lumbale Drainage ist bei allen nicht kommunizierenden Formen oder im Zweifelsfall kontraindiziert. 12 Bei Patienten mit schweren Formen der intraventrikulären Hämorrhagie (Tamponade beider Seitenventrikel und/oder des 3. Ventrikels) kommt es oftmals, trotz der EVD-Anlage, zu einem kritischen Anstieg des intra kraniellen Drucks. Diese Patienten werden auf der chirurgischen Intensivpflegestation behandelt und überwacht. Bei therapieresistenten Hirndruckanstiegen erfolgt die intraventrikuläre Lysetherapie über eine liegende EVD. 13 Die endoskopische Reduktion des intraventrikulären Blutvolumens und ggf. auch die endoskopische Ventrikulostomie am Boden des 3. Ventrikels bleibt Spezialfällen vorbehalten. 14 Intrazerebrale Blutung während oder nach Lysetherapie bei ischämischen Hirnfarkten Bei noch laufender Lyse ist diese umgehend zu stoppen. Ist die Lysetherapie bereits abgeschlossen, ist aufgrund der sehr kurzen HWZ von rt-pa ein konservatives, abwartendes Vorgehen gerechtfertigt. Der Patient wird überwacht. Nach der intrakraniellen Blutung Soll die Sekundärprophylaxe mit oralen Antikoagulantien wieder aufgenommen werden und wenn ja, wann? Es handelt sich um eine individuelle Entscheidung in Abhängigkeit des Rezidivblutungsrisikos und des Thromboembolierisikos (Patienten mit mechanischer Herzklappe ohne OAK weisen ein Thromboembolierisiko von % innerhalb von 2 Wochen auf). Bei Patienten mit niedrigem Thromboembolierisiko (z. B. VHF ohne vorhergehenden zerebralen Infarkt, niedrigem CHA2DS2-VASc-Score 12 Steiner et al., 2008; DGN Leitlinie Intrazerebrale Blutungen 13 Ziai et al Int J Stroke 14 S. Obaid, A.G. Weil, R. Rahme, M.W. Bojanowski: J Neurol Surg A 2015;76:
92 (< 2) sollte nach Nutzen-Risiko-Abwägung die Indikation für eine Behandlung mit einem DOAC kritisch gestellt werden. Die Gabe eines Thrombo zytenaggregationshemmers zur Schlaganfallprophylaxe bei Vorhofflimmern kann nicht empfohlen werden. Bei Patienten mit hohem Thromboembolierisiko (CHA2DS2-VASc-Score > 2) und niedrigem Risiko einer Zweitblutung soll die OAK nach ca. 1 Monat wieder begonnen werden. In dieser Situation sind die DOAC aufgrund des niedrigeren Risikos für intrazerebrale Blutungen in Betracht zu ziehen. V.a.Patienten mit schlechter Einstellung profitieren (> 60% der aufgezeichneten INR-Werte nicht im Zielbereich). Aber auch bei den Patienten mit ordentlicher Einstellung ist dieser Vorteil gegeben. Generell: Indikation OAK überprüfen Blutungsrisiko dem prophylaktischen Benefit gegenüberstellen (CHA2DS2-VASc-Score vs. HAS-BLED-Score) Indikation für DOAC prüfen (Zulassung für Vorhofflimmern, tiefe Venenthrombose und Lungenembolie) ggf. OAK mit Vit.-K-Antagonisten mithilfe von CoaguCheck- Kontrolle optimieren (bei kooperativem Patienten mit guter Compliance) Eine schwere Leukenzephalopathie (Grad 2 nach van Swieten 15 ) weist ein erhöhtes Risiko für eine Rezidivhirnblutung auf. Die zerebrale Amyloidangiopathie stellt eine Kontraindikation für die Antikoagulation und die Gabe von Thrombozytenaggregationshemmern dar. Dr. Georg Kägi Dr. Monika Kapauer Dr. Jean-Yves Fournier Dr. Heiko Richter Dr. Martin Seule Dr. Markus Diethelm Dr. Thomas Lehmann Dr. Dieter von Ow Reduktion des Risikos für eine Rezidivblutung Optimale Behandlung der arteriellen Hypertonie Alkoholgenuss vermeiden Nikotin-Stopp Individuelle Entscheidung über den (erneuten) Beginn einer Therapie mit Antikoagulantien oder Thrombozytenaggregationshemmern (in der Regel frühestens erst nach 1 Monat nach Blutungsereignis, in Einzelfällen aufgrund des hohen Thromboembolierisikos ggf. früher) 15 J Neurol Neurosurg Psych 1990;53:
93 Aortenaneurysma Definition Ein Aneurysma ist eine lokalisierte Erweiterung des Gefässdurchmessers auf mindestens das 1.5-Fache der Norm. Bei der Bauchaorta spricht man konventionell ab einem Querdurchmesser von 3 cm von einem Aneurysma (BAA): cm = «kleine BAA»; 5.5 cm = «grosse BAA». Epidemiologie und Ätiologie Die Inzidenz des BAA variiert mit Alter und Geschlecht. Männer sind 3 6 Mal häufiger betroffen. Die geschätzte Prävalenz liegt in der westlichen Welt bei 65-Jährigen bei 2 5% und steigt danach um ca. 6% pro Dekade. BAA sind praktisch immer mit Atherosklerose assoziiert und entstehen primär whs auf dem Boden von Entzündungs-/Proteolyse-Prozessen. Assoziation mit einem BAA ist für folgende Faktoren nachgewiesen (odds ratio): Nikotinkonsum (2.8; 95% CI ); pos. FA (erstgradig Verwandte; 2.0; ); KHK (1.8; ); Dyslipidämie (1.4; ); arterielle Hypertonie (1.4; ); Diabetes (0.7; protektiv!). Abgesehen davon unterhält das Laplace-Gesetz ein initiiertes Aneurysmawachstum quasi «von selbst». Daneben werden inflammatorische (aseptische Wandentzündung) und mykotische (Wandinfekt) BAA unterschieden. Das Rupturrisiko hängt primär von der entstandenen Wandspannung ab und steigt exponentiell mit dem Durchmesser. Weitere Risikofaktoren für Ruptur sind Nikotinkonsum, weibliches Geschlecht, FA für Ruptur, arterielle Hypertonie, exzentrische Form des BAA. Im Gegensatz dazu ist seine Längenausdehnung für die Behandlungsindikation weniger relevant (wohl aber für die Behandlungsplanung). Das rupturierte BAA gehört im Westen bei Männern zu den 15 häufigsten Todesursachen, was Screening-Initiativen in Risikopopulationen rechtfertigt (Halbierung der Ruptur-bedingten Mortalität in MASS, allerdings kein Effekt auf Gesamtüberleben)
94 Morphologie und Lokalisation In unseren Breitengraden betreffen ca. 70% aller AA die Bauchaorta und enden fast immer unterhalb oder an den Nierenarterien. Knapp 25% sind thorakal gelegen (TAA); die restlichen involvieren den thorakoabdominalen Übergang (TAAA). Beim «echten» Aneurysma sind alle Wandschichten des Gefässes betroffen, beim «falschen» Aneurysma (spurium) sind die Innenschichten perforiert und die Ausweitung besteht bloss aus Adventitia (Pseudoaneurysma: z. B. nach Gefässanastomosen, traumatisch, iatrogen [Punktion]). Das Poplitealaneurysma ist bei bis zu 10% der BAA syn- oder metachron assoziiert und muss gesucht werden. Klinische Präsentation Die meisten BAA sind bis zur Ruptur asymptomatisch und wachsen im Verborgenen Pulsierende indolente Masse im Abdomen, verbreiterte Pulse femoral/popliteal Entdeckt als Zufallsbefund bei bildgebender Untersuchung Bekannte Familienanamnese Screening von Risikopopulationen (z. B. 65-jährige, rauchende Männer, UK/USA) Symptomatische BAA Rücken- oder Flankenschmerzen, auch auslösbar durch direkte Palpation Verdrängung der benachbarten Organe: z. B. Wurzelsymptome/Schmerzen bei WK-Arrosion Venöse Abflussstauung, Ureter-Abflussstauung (typisch beim inflammatorischen BAA) Fieber/Sepsis/Entzündungszeichen bei mykotischem BAA Selten: periphere arterio-arterielle Embolie (akute periphere Ischämie) Rupturierte BAA Plötzlich auftretende Flankenschmerzen mit Ausstrahlung inguinal (selten ins Abdomen), evtl. (Prä-)Synkope (vaso vagale Reaktion auf retroperitoneale Blutung: initial praktisch nie Blutungsschock!) Schmerzhafte pulsierende Masse im Abdomen Kreislaufparameter bleiben initial oft im Normbereich (retroperitoneale Tamponade): Cave «pseudo-stabile» Situation: time is life! Freie Ruptur in die Bauchhöhle: rapider Kreislaufzerfall, progredienter Blutungsschock Seltene Rupturformen: intestinale Fistel (1%, gastrointestinale Blutung, meist nach früherer Aortenprothese, immer Infekt); Cava-Fistel (1%, akute [Rechts-]Herzinsuffizienz, Körperstammzyanose/Einflussstauung, auskultierbares Schwirren) Diagnostik Anamnese (inklusive Allergien und Sexualanamnese); klinische Untersuchung (inklusive periphere Ausmessung, Pulsstatus) Duplexsonografie (Sensitivität/Spezifität > 90%): erste Wahl für Screening, Monitoring von kleinen BAA und bei V.a. Ruptur CT-Angiografie: Referenzstandard für Morphometrie. Als Ausgangswert sollte immer die gesamte Aorta/Iliakalachsen ab gebildet werden, im Verlauf (z. B. post EVAR) nur noch das betroffene Gefässsegment. Nativ zur Darstellung von Verkalkungen MR-Angiografie: bei Kontraindikation gegen CT: junge (Strahlenbelastung) oder schwer niereninsuffiziente Patienten Nota bene: konventionelle Angiografie als Diagnostikum irreführend (stellt nur das durchflossene Lumen dar) Untersuchungen zur präoperativen Risikostratifizierung (inklusive Carotis-Duplex, Bestimmung cardio-pulmo-renaler Reserven)
95 188 Natürlicher Verlauf, Monitoring und Behandlungsindikation Primäres Ziel ist die Verhinderung der Aortenruptur; d.h., das elektive Behandlungsrisiko muss kleiner als das Rupturrisiko sein. Kleine BAA (< 4.0 cm): Rupturrisiko vernachlässigbar, Bildgebung alle 1 bis 2 Jahre, kardiovaskuläre Sekundärprophylaxe Kleine BAA ( cm): jährliche Expansion whs ca. 10%, jährliches Rupturrisiko bei knapp 1% (konsistent in mehreren RCT), Bildgebung alle 6 Monate (3 Monate, wenn > 5.0 cm), kardiovaskuläre Sekundärprophylaxe Grosse BAA ( 5.5 cm): deutlicher Anstieg der Expansionsrate und des Rupturrisikos (s.o., bei cm geschätzte 10 20% / Jahr), elektiver Aortenersatz zu erwägen je nach individuellem Nutzen-/ Risiko-Verhältnis Erhöhtes Rupturrisiko: bei Frauen, raschem Wachstum ( 1.0 cm/jahr), aktiven Rauchern mit COPD, unkontrollierter Hypertonie Nota bene: Bei langsamer Progression ist Beobachtung bis zu 5.5 cm Durchmesser (bei Durchschnittspatienten!) gleich sicher wie (aber günstiger als) der offene/endovaskuläre Aortenersatz (konsistente Erkenntnis in 2 grossen RCT: UKSAT und ADAM) Nota bene: Von allen BAA-Patienten stirbt letztlich nur ein Drittel an der Aneurysmaruptur, die meisten sterben vorher an anderer (kardiovaskulärer!) Ursache. Das BAA gilt darum als Risikoäquivalent zur KHK: best medical treatment ist absolut zentral. Folgende akzeptierte Indikationsschwellen für Aneurysmaersatz beruhen auf Inferenz aus diesen Daten und nicht auf direkter Evidenz TAA cm; isoliertes Iliakalaneurysma 3.0 cm; viszerales Aneurysma 2.0 cm Femoralaneurysma cm; Poplitealaneurysma 3.0 ( 2.0 cm bei Thrombussaum) Symptomatisches BAA Nicht-inflammatorisch: dringliche Indikation (24 48 Std.) unabhängig vom Durchmesser, präop. Risikostratifizierung erwägen Inflammatorisch: vorbereitende Steroidtherapie je nach aktuel lem Durch messer manchmal gerechtfertigt Rupturiertes BAA Absolute Notfallindikation (grundsätzlich unabhängig vom Alter) Ausnahmen: ausdrücklicher Patientenwiderspruch/Patienten verfügung, prohibitive gesundheitliche Umstände (wie z. B. Demenz, unkontrolliertes Tumorleiden) OP-Vorbereitung Asymptomatisches BAA: hochelektiver Eingriff Risikostratifizierung internistisch und anästhesiologisch (s.o.), ggf. kardio logisches und pneumologisches Konsil, Bestimmung GFR Dokumentation präoperativer Gefässstatus ASS perioperativ weitergeben, nicht pausieren Symptomatisches BAA: dringlicher Eingriff Grosslumige Zugänge, notfallmässige anästhesiologische Beurteilung Notfallmässige CT-Angiografie (Rupturausschluss, Therapieplanung) Weitere Abklärungen je nach Zustand des Patienten Rupturiertes BAA: absoluter Notfall (time is life) Ständige anästhesiologische Begleitung Hämodynamisches Management: Nur die rasche mechanische Blutungskontrolle rettet den Patienten, zeitraubende hämodynamische «Stabilisation» mittels Volumen/Katecholaminen auf «normale» Blutdruckwerte ist bei ansprechbarem Patienten (oder systolischen Werten > mmhg) kontraproduktiv: verhindert lebensrettende Tampo - nade durch erhöhten Blutungsdruck und führt zu Verdünnungskoagulopathie, Auskühlung und Zeitverlust 189
96 Trotz Zeitdruck: wenn irgend möglich CT-Angiografie (Operationsplanung, Eignung EVAR?) Falls Bildgebung bereits extern: direkte Aufnahme des Patienten in OP-Vorbereitung Nota bene: keine Operation ohne Desinfektion/Abdeckung, keine heroische Laparotomie ausserhalb des OP Erwartete Operationsmortalität bei optimalem Patientenmanagement (unabhängig von Reparaturmethode!): 15 25% Künstlicher Aortenersatz Zurzeit kann nur mit dem künstlichen Aortenersatz die Rupturgefahr dauerhaft ausgeschaltet werden; eine medikamentöse Therapie zur Rever sion des Aneurysmawachstums existiert aktuell nicht. Offener Aortenersatz mittels Dacron-Prothese Mediane (oder quere) Laparotomie, ggf. Lumbotomie für retroperitonealen Zugang (je nach Aneurysmakonfiguration) Bei juxta-/suprarenaler Ausdehnung: suprarenale Aortenklemme nicht länger als 30 min, ggf. Nierenkälteperfusion Falls Iliakalachsen nicht betroffen: Rohrprothese (ca. 30%) Y-Prothese (ca. 70%) mit distalem Anschluss wenn immer möglich im Abdomen (femorale Anastomosen wegen Infektrisiko) zu vermeiden. Revaskularisation beider Aa. iliacae internae (Gesässclaudicatio) Erwartete perioperative Mortalität hängt von der Patientenselektion ab: bei theoretisch EVAR-geeigneten Patienten ca. 1%, bei EVARungeeigneten 2 3%. Permanente Dialysepflicht < 1%. Neue Störung der Sexualfunktion (meist retrograde Ejakulation): 10 20% Endovaskulärer Aortenersatz (EVAR) mittels Stentgraft-Prothese Kollaboration interventionelle Radiologie <=> Gefässchirurgie Gemeinsame Beurteilung der anatomischen Eignung der Zugangsgefässe und Verankerungszonen (gemäss instructions for use [Prothese]: 60 70% aller BAA geeignet, in realiter etwas mehr) Kontrollierter chirurgischer Zugang auf Femoralgefässe («cut down») oder perkutaner Zugang je nach Set-up/Eignung der Gefässe Infrarenales Absetzen der Prothese unter radiologischer Kontrolle und Atemstillstand des Patienten, bei juxta-/suprarenaler BAA-Ausdehnung endovaskuläre Adjuncts (fenestrierte/gebranchte Prothesen, Zusatzleitungen für Chimneys oder Snorkels) Intraoperative Angiografie zum Ausschluss eines relevanten Endoleaks Erwartete perioperative Mortalität bei konventioneller EVAR < 1%, bei komplizierter EVAR 2 3%. Permanente Dialysepflicht ca. 1%. Neue Störung der Sexualfunktion (meist retrograde Ejakulation): 10 20% Nota bene: bei offen-chirurgisch inoperablen Patienten bringt EVAR keinen Überlebensvorteil zur konservativen Therapie (EVAR trial 2) Offen-chirurgische und EVAR-Patientenpopulationen sind meist nicht vergleichbar, da offen-chirurgische Patienten oft eine negativ selektionierte Anatomie repräsentieren und EVAR-Patienten eine negativ selektio nierte Physiologie. Bei vergleichbaren Patienten zeigen praktisch alle RCT konsistent einen perioperativen Überlebensvorteil für EVAR (Operationstrauma), aber eine höhere sekundäre Ruptur- und Reinterventionsrate, sodass spätestens nach 2 Jahren die Behandlungsresultate beider Methoden vergleichbar sind inklusive Lebensqualität und Sexualfunktionsstörun gen (EVAR 1, DREAM, ACE, OVER). Wichtigste Selektionskriterien sind die anatomische Eignung und die lokale Expertise
97 192 Rupturiertes BAA Schockmanagement und Dauer bis zur mechanischen Blutungskontrolle (s.o.) bestimmen die Prognose und nicht die Wahl der Operationsmethode: bei vergleichbaren Patienten sind offener und endovaskulärer Aortenersatz im Notfall äquivalent (IMPROVE). CT-Angiografie, verfügbares Material und verfügbare Expertise sind entscheidend Ist der Patient zu instabil für die Bildgebung, muss meist offen operiert werden (ggf. mit endovaskulärer Aortenokklusion), und die Prognose wird deutlich schlechter Cave: Bei langer Ballonokklusion der Aorta steigt die Gefahr der viszeralen Ischämie, die zu lange unentdeckt bleiben kann EVAR sollte im Notfall nach Möglichkeit in LA durchgeführt werden, um die minimal-invasiven Vorteile voll zu nutzen Cave: Über die unversorgte Rupturstelle können relevante Endoleaks nach EVAR zu abdominalem Compartment-Syndrom führen Die erwartete Operationsmortalität liegt bei optimiertem Management des rupturierten BAA bei 15 25%. Entlassungsmanagement Die kardiovaskuläre Sekundärprophylaxe läuft peri- und postoperativ weiter inklusive ASS. Eine duale Tc-Hemmung ist bei Stentgraftprothesen nicht erforderlich. Der postoperative Gefäss-Status muss inklusive arterieller Ausmessung dokumentiert werden, genauso wie die Nierenfunktion. Offener Aortenersatz Entlassung am 7. bis 10. postoperativen Tag, Bauchgurt nur zu Mobilisation und subjektivem Benefit Entfernung der Hautklammern Tage postoperativ Kuraufenthalt oder Rehabilitation meist nicht erforderlich Bauchdeckenschonung für 6 8 Wochen (Inzidenz der Narbenhernie bei zugrundeliegender Bindegewebserkrankung bei 30%) Chirurgische Kontrolle nach 3 Monaten, anschliessend duplexsonographische Kontrollen der Anastomosenregionen alle 1 2 Jahre Aneurysmacheck weiterer Prädilektionsstellen und bei erstgradig Verwandten Konsequente Eliminierung vaskulärer Risikofaktoren (Rauchstopp, Statin, ACE-Hemmer, Blutdruckkontrolle, ASS) EVAR Entlassung am 3. bis 5. postoperativen Tag, volle Belastung möglich Entfernung der Hautfäden inguinal 12 Tage postoperativ Kuraufenthalt oder Rehabilitation meist nicht erforderlich Erste CT-Angiografie nach 4 6 Wochen zum Ausschluss eines Endoleaks. Bei Endoleckage Monitoring nach Möglichkeit mittels contrast enhanced ultrasound (CEUS). Typ I und III müssen interventionell behoben werden, Typ II kann beobachtet werden, solange es nicht zu einem sekundärem Wachstum des Aneurysmasacks kommt Patientenführung in der chirurgischen oder interventionellen Nachsorgesprechstunde (jährlich) Aneurysmacheck weiterer Prädilektionsstellen und bei erstgradig Verwandten Konsequente Eliminierung vaskulärer Risikofaktoren (Rauchstopp, Statin, ACE-Hemmer, Blutdruckkontrolle, ASS) In Anlehnung an die Treatment Guidelines der European Society for Vascular Surgery und die erwähnten randomisierten Studien Prof. Dr. Florian Dick Dr. Lukas Hechelhammer Dr. Alexander Poloczek 193
98 Periphere arterielle Verschlusskrankheit (PAVK) Allgemeines Zu 90 95% arteriosklerotischer Genese (5 10% entzündlich, traumatisch, embolisch, u.a. Seltenes ) Betrifft zu > 90% die unteren Extremitäten Ist überwiegend eine Erkrankung des alten Menschen (ca. 20% im Rentenalter betroffen) Risikofaktoren analog KHK; am wichtigsten: Rauchen und Diabetes mellitus Primär klinische (Verdachts-)Diagnose, Diagnosesicherung mittels ABI (Ankle-Brachial-Index, Definition siehe Diagnostik) Ca. 75% der Patienten sind asymptomatisch! Prognose bezüglich betroffener Extremität gut (75% stabiler Verlauf) Prognose quoad vitam schlecht (Mortalität ca. 30% / 5 Jahre, v.a. wegen koronarer Ereignisse) Ca. 61% der Patienten mit kardialer und/oder zerebraler atherosklerotischer Erkrankung Einteilung, Definitionen Definition der PAVK ABI 0.9 (Werte von gelten als «grenzwertig patho logisch») oder relevante Plaques/Strombahnhindernisse von Aorta bis Peripherie oder Zustand nach Revaskularisation oder klinisch Pulsdefizit Einteilung der PAVK Es empfiehlt sich eine Unterscheidung in akute und chronische Formen: Akute Verschlusskrankheit Häufigste Ursachen: Kardiale Embolie, arterioarterielle Embolisation aus Plaque/Aneurysma, thrombosiertes Poplitealaneurysma
99 Wegen fehlender Zeit zur Kollateralenbildung oft schwere Klinik («6 x P») und rascher Handlungsbedarf «6 x P»: Pulselessness (Pulslosigkeit), Pallor (Blässe), Pain (Schmerz), Paresthesia (Sensibilitätsstörung/-verlust), Paralysis (motorische Störung/Lähmung), Prostration (Erschöpfung mit lebensgefährdender nekrosebedingter Toxinausschüttung) Stadium IV Kritische Ischämie, Ruhesymptome, ischämisch bedingte trophische Läsion Im Fall vorhandener trophischer Läsionen, die begleitend zur PAVK und nicht auf dem Boden der Perfusionsstörung entstanden sind, werden die Stadien I und II mit dem Zusatz «kompliziert» bezeichnet. Das akut kalte Bein Akut wenige Stunden Kritische, komplette Ischämie Sensibilität, Motorik Knöchelverschlussdruck < 50 mmhg, meist nicht messbar Ziel: Revaskularisation innerhalb von 6 Std. ab Symptombeginn Ambulant: Unverzüglich Zuweisung auf ZNA Stationär: Unverzügliche Information DA Gefässchirurgie oder DA Angiologie Kritische, inkomplette Ischämie Sensibilität, Motorik erhalten Knöchelverschlussdruck < 50 mmhg Ambulant: Rasche Zuweisung auf ZNA Stationär: Rasche Information DA Gefässchirurgie oder Angiologie Bei jeglicher Form der akuten kritischen Ischämie soll ein Heparin-Bolus von E i.v. noch auf der ZNA verabreicht werden. Anschliessend Beginn einer Heparin-Infusion nach hausinternem «TVT»-Infusion-Schema. Chronische Verschlusskrankheit Einteilung adaptiert nach Fontaine: Stadium I Asymptomatisch (= «schweigende Mehrheit») Stadium IIa Claudicatio, Leidensdruck akzeptabel (Gehstrecke > 200 m) Stadium IIb Claudicatio, Leidensdruck belastend (Gehstrecke < 200 m) Stadium III Kritische Ischämie, Ruhesymptome, keine trophische Läsion Im Stadium III und IV: Knöcheldrücke < 50 mmhg; rasche Zuweisung ins Ostschweizer Gefässzentrum oder ggf. ZNA Stufendiagnostik Typische Beschwerden FKDS Anamnese; Klinik; 65 Jahre; 50 Jahre + Raucher od. Diabetes; AGLA-Risk-Score 10 20%; trophische Läsionen mit Wundheilungsstörungen <1.0 Atypische Beschwerden positiv ABI-Messung Ziel: Revaskularisation beschleunigt, aber nicht notfallmässig (auch in Abhängigkeit von der Schmerzsymptomatik und vom Ausmass der Sensibilitätsstörung) Laufbandergometrie Typische Beschwerden negativ Im Fall von Unklarheiten und speziellen Fragestellungen ggf. DSA, CT-Angiographie, MR-Angiographie 1.0 Atypische Beschwerden Weitere Diagnostik (neurogen, vertebrogen, arthrogen ) DSA = konventionelle digitale Subtraktionsangiografie = «konventionelle Angiografie»; FKDS = farbkodierte Duplexsonografie
100 198 Anamnese Prädisponierende Faktoren: Vaskuläre Risikofaktoren Alter, Rauchen, Diabetes mellitus, arterielle Hypertonie, Hypercholesterin - ämie, Kreatinin-Clearance < 60 ml/min., männliches Geschlecht Manifeste Atherosklerose Koronar, zerebrovaskulär je gut 30% Risiko für PAVK Pro «vaskuläre Beschwerdeätiologie» Beschwerden zuverlässig reproduzierbar bei Belastung (langsam zunehmend); Lokalisation in Muskelgruppen (Gesäss, Oberschenkel, Wade usw.); Beschwerderückgang wenige Minuten nach Belastungsstopp; bei St. n. PTA: wie vor Intervention; Charakter: krampfartig/ Müdigkeit Kontra «vaskuläre Beschwerdeätiologie» Beschwerden auch beim Stehen; Anlaufschmerz; Bergabgehen schlimmer als Bergaufgehen; Besserung betont nach Absitzen und/ oder Vornüberbeugen des Oberkörpers ( Claudicatio spinalis); Charakter brennend/stechend/elektrisierend; inkonstantes Auftreten Lokalisation der Beschwerden erlaubt Rückschluss auf erkranktes Gefässsegment: Gesäss A. iliaca communis/interna + kranke Gegenseite Oberschenkel A. iliaca communis/externa, A. profunda femoris Wade A. femoralis superficialis, A. poplitea Wade distal evtl. Truncus tibiofibularis Fuss (fortgeschrittene) Unterschenkelarteriopathie Klinik Inspektion Hautfarbe blass, ggf. bei chronischer kritischer Ischämie (Stadium III und IV) düsterrotlivide insbesondere bei Tieflagerung der Extremität, Abblassung bei Elevation; Onychodystrophie, Alopezie (Cave bei Diabetes mellitus: trockene, warme, rosige Haut trotz reduzierter arterieller Perfusion bei Neuropathie möglich) Temperaturprüfung mit Handrücken Rekapillarisation Prüfung mit Fusselevation (normal 3 5 Sek.) Puls Inguinal, popliteal, A. dorsalis pedis, A. tibialis post., im Zweifel Vergleich mit eigenem Puls; Arrhythmie? ( Hinweis auf mögliche kardiale Embolie) Auskultation Über Arterienverlauf; Sensitivität durch Belastung Je höhergradig die Stenose, desto höher-frequent (nicht lauter) das Geräusch Cave: Spezifität Strömungsgeräusch ca. 40% 60% falsch positive Untersuchungen; Sensitivität 75% 25% falsch negative Untersuchungen Ankle-Brachial-Index (ABI) = pro Bein höherer Knöcheldruck über A. dorsalis pedis oder A. tibialis posterior im Verhältnis zu höherem systolischem Oberarmblutdruck Sensitivität 95%, Spezifität 100% Normwert , Borderline , eindeutig pathologisch 0.9 ABI > 1.4: Nicht verwertbar für PAVK-Diagnostik, da Mediasklerose wahrscheinlich (v.a. bei Diabetes mellitus, chronischer Niereninsuffizienz, chronischer Steroidmedikation) ABI-Messung empfohlen: Bei allen Menschen ab 65 Jahren Bei Menschen mit Risikofaktoren (v.a. Rauchern und Diabetikern) bereits ab 50 Jahren Bei allen Patienten mit belastungsabhängigen Beinbeschwerden Bei Menschen mit intermediärem kardiovasku lären Risiko (AGLA-Score 10 20% 10-Jahres-Risiko für kardiovaskuläres Ereignis) 199
101 Die bildgebenden Verfahren Stärken Bei Patienten mit trophischen Läsionen und Wundheilungsstörung FKDS DSA CTA MRA nicht-invasiv keine Strahlenbelastung funktionelle Messung und Bildgebung kombiniert zuverlässige Stenosegradierung Gefässwandstruktur und Umgebung darstellbar mobiles Gerät Schwächen Arztpersonalintensiv fehlende Übersicht in einem Bild Hürden: Meteorismus, Kalk mit Schallschatten Limitationen Peripherie/Akren (Fuss distal, evtl. crural); keine transthorakale Gefäss - darstellung Übersichtlichkeit Auflösung dynamisch funktionelle Komponente Interventionsbereitschaft invasiv Strahlenbelastung Kontrastmittel nur Gefässlumen dar stellbar grosse Übersichtlichkeit (inklusive nichtvaskulärer Strukturen) wenig invasiv rasch Kontrastmittel Strahlenbelastung Peripherie FKDS = farbkodierte Duplexsonografie; DSA = digitale Subtraktionsangiografie; CTA = Computertomografie-Angiografie; MRA = Magnetresonanz-Angiografie grosse Übersichtlichkeit (inklusive nichtvaskulärer Strukturen, insb. Weichteile) wenig invasiv (Kontrastmittel) bei Pacemaker bei Klaus trophobie Tendenz zu Überschätzung Stenosegrad Peripherie, Stent, Metallprothesen ( Artefakte, scheinbare Perfusionsausfälle) Therapie Sekundärprävention Gehtraining PAVK-Patient = vaskulärer Hochrisikopatient (nach IAS, ESC/EAS innerhalb höchster Risikogruppe) Thrombozytenfunktionshemmer: Aspirin cardio 100 mg/d im Stadium I und II der PAVK (Clopidogrel 75 mg/d bei Unverträglichkeit von Aspirin); Clopidogrel 75 mg/d im Stadium III und IV der PAVK sowie bei Diabetikern mit PAVK Statin unabhängig vom Cholesterinausgangswert; Ziel-LDL < 1.8 mmol/l oder Reduktion > 50% des Ausgangswertes, wenn Zielwert nicht erreicht werden kann Rauchstopp Kontrolle von Blutdruck (Ziel < 140/90 mmhg; bei älteren Patienten mit Ausgangswerten 160 mmhg evtl. Reduktion auf mmhg) Kontrolle von Blutzucker (Ziel HbA1c < 7.0%) Erste therapeutische Option im Stadium IIa Ziel: 3x 30 Min. pro Woche, Effekt ab 3 Monaten abschätzbar Nach Möglichkeit strukturiert im Rahmen eines ambulanten vaskulären Rehabilitationsprogramms (im KSSG verfügbar)
102 202 Revaskularisation Optional ab Stadium IIb der PAVK (individu ell je nach Leidensdruck, Co-Morbi ditäten usw. zu entscheiden) Je nach Befund erfolgt die Revasku larisation entweder mittels interventionell-radiologischer Katheterintervention (Ballon-Angioplastie +/ Stentimplantation), operativ (i.r. eines gefässchirurgischen Eingriffs) oder im Hybrid-Verfahren (Kombination Katheterintervention und gefässchirurgischer Eingriff) Prostaglandine (Ilomedin) bei kritischer Ischämie (v.a. bei distalen/ akralen Gefässverschlüssen) ohne Möglichkeit einer interventionellen oder operativen Verbesserung der arteriellen Perfusion erwägen Dr. Alexander Poloczek Dr. Lukas Hechelhammer Prof. Dr. Florian Dick Pulmonale Hypertonie Definition Die pulmonale Hypertonie (PH) ist definiert als Erhöhung des mittleren pulmonal-arteriellen Drucks (mpap) 25 mmhg im Rechtsherzkatheter in Ruhe. Die hämodynamische Messung im Rechtsherzkatheter ist der Gold-Standard. An der Definition einer pulmonalen Hypertonie unter Belastung (Anstieg des mittleren pulmonal-arteriellen Druckes unter Belastung) wird nicht mehr festgehalten, da dessen Bedeutung heute noch unklar bleibt (Gesunde können ebenfalls einen Anstieg unter Belastung aufweisen). Hämodynamische Klassifikation der pulmonalen Hypertonie im Rechtsherzkatheter Definition Hämodynamische Kriterien* Klinische Gruppe Pulmonale Hypertonie (PH) Präkapilläre PH Postkapilläre PH Isolierte postkapilläre PH (Ipc-PH) Kombinierte postund präkapilläre PH (Cpc-PH) mpap 25 mmhg mpap 25 mmhg PAWP 15 mmhg mpap 25 mmhg PAWP > 15 mmhg DPG < 7 mmhg und/oder PVR 3 WU DPG 7 mmhg und/oder PVR > 3 WU * Alle Drucke in Ruhe gemessen; # siehe Klassifikation der pulmonalen Hypertonie. Abkürzungen: PH = pulmonale Hypertonie, mpap = mittlerer pulmonal-arterieller Druck, PAWP= pulmonal-arterieller Verschlussdruck, DPG= diastolischer Druckgradient (diastolischer PAP - mittlerer PAWP), PVR= pulmonal vaskularer Widerstand, WU = Wood Units (= 80 x dyn sec/cm 5 ) 203 Alle 1. Pulmonal-arterielle Hypertonie (PAH) 3. Pulmonale Hypertonie im Rahmen von Lungenerkrankungen/Hypoxie 4. Chronisch thromboembolische pulmonale Hypertonie (CTEPH) 5. Pulmonale Hypertonie mit unklarem Mechanismus oder mit multifaktorieller Genese 2. PH bei Linksherzkrankheit 5. PH mit unklarem oder multifaktoriellem Mechanismus
103 Klassifikation der pulmonalen Hypertonie* 1. Pulmonal-arterielle Hypertonie (PAH) ~ 4% 1 Pulmonale venookklusive Krankheit und/oder pulmonale kapillare Hamangiomatose 1 Persistierende pulmonale Hypertonie der Neugeborenen 2. Pulmonale Hypertonie infolge Linksherzkrankheit ~ 79% 1.1 Idiopathisch (IPAH) 1.2 Hereditär Genetisch (z. B. BMPR2-Mutation) 1.3 Arzneimittel- oder Toxin-induziert 1.4 Assoziiert mit: Kollagenosen HIV-Infektion Portale Hypertension Kongenitale Herzkrankheiten Schistosomiasis 2.1 Systolische Dysfunktion 2.2 Diastolische Dysfunktion 2.3 Klappenerkrankung Häufigkeit Die postkapilläre pulmonale Hypertonie ist mit knapp 80% weitaus die häufigste Form einer pulmonalen Hypertonie (Häufigkeit: siehe Tabelle der Klassifikation der PH). Die Inzidenz der hereditären pulmonalarteriellen Hypertonie (PAH) beträgt etwa 1 2 auf und die Prävalenz etwa 15 auf (entspricht etwa 300 neuen Patienten pro Jahr in den USA). Frauen sind 3x häufiger betroffen. Die PAH gilt deshalb als «orphan disease». Die Prävalenz anderer Formen der PAH ist etwas häufiger: 8 12% bei systemischer Sklerose (SSc), 22% bei rheumatoider Arthritis (RA), % bei systemischem Lupus erythematodes (SLE), 2 5% bei portopulmonaler Hypertonie, 0.5% bei HIV. Im weiteren Verlauf des Kapitels wird nur noch auf die pulmonalarterielle Hypertonie eingegangen. 3 Pulmonale Hypertonie bei Lungenkrankheit oder bei Hypoxie ~ 10% 3.1 Chronisch obstruktive Lungenkrankheit (COPD) 3.2 Interstitielle Lungenerkrankung 3.3 Andere Lungenerkrankung mit gemischtem obstruktiven und restriktiven Muster 3.4 Schlafassoziierte Atemstörungen 3.5 Alveoläre Hypoventilation 3.6 Chronische Höhenexposition 3.7 Entwicklungsassoziierte Lungenkrankheiten 4. Chronisch-thromboembolische pulmonale Hypertonie und andere Pulmonalarterien- Obstruktionen (CTEPH) 5. Pulmonale Hypertonie mit unklarem oder multifaktoriellem Mechanismus ~ 7% 4.1 Chronisch thromboembolische pulmonale Hypertonie 4.2 Andere Pulmonalarterienobstruktionen Angiosarkome Andere intravaskulare Tumoren Arteriitiden Kongenitale Pulmonalarterienstenose Parasiten (Hydatidosis 5.1 Hämatologische Krankheiten: chronisch hämolytische Anämie, myeloproliferative Krankheiten, Splenektomie 5.2 Systemische Krankheiten: Sarkoidose, pulmonale Histiozytose, Lymphangioleiomyomatose 5.3 Metabolische Krankheiten: Glykogen-Speicherkrankheiten, Gaucher-Krankheit, Schilddrusenkrankheiten 5.4 Andere: pulmonale tumorose thrombotische Mikroangiopathie, fibrosierende Mediastinitis, chronische Niereninsuffizienz (mit- oder ohne Dialyse), segmentale pulmonale Hypertonie 204 * 2015 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension 205
104 Prognose der pulmonal-arteriellen Hypertonie nach Klasse Proportion Surviving Risikofaktoren für eine PAH Gesichert Aminorex Fenfluramin Dexfenfluramin Toxisches Rapsöl Möglich Survival in PAH CHD CVD HIV Portopulm Amphetamine L-Tryptophan Methamphetamine Wahrscheinlich Kokain Phenylpropanolamin Hypericum perforatum (echtes Johanniskraut) Chemotherapeutika Selektive Serotonin re-uptake Inhibitoren Unwahrscheinlich Years Orale Kontrazeptiva Östrogene Zigarettenrauchen Anamnese Hereditäre PAH bekannt? Rheumatologische Erkrankung (systemische Sklerose, SLE, rheumatoide Arthritis [RA]?) Lebererkrankungen, HIV? Medikamente (siehe Risikofaktoren für eine PAH) Symptome der PAH Die Symptome der pulmonalen Hypertonie sind unspezifisch. Die Diagnose wird aus diesem Grund leider oft spät gestellt. Man muss daran denken, v.a. wenn keine anderen Ursachen der Beschwerden des Patienten gefunden werden. Klassische Trias der PAH: Zunehmende Dyspnoe unter Belastung Keine groben Veränderungen im Thorax-Rx Keine groben Veränderungen im Lungenfunktionstest (ausser einer verminderten Diffusionskapazität) Initial allenfalls vorhanden: Müdigkeit Depression Gewichtszunahme 30% beklagen: Brustschmerzen (ähnlich wie Angina pectoris) Palpitationen Synkope (unter Belastung) Periphere Ödeme Weniger häufige Symptome: Husten Hämoptyse Heiserkeit (Dilatation des Truncus pulmonaris) Klinische Zeichen der PAH Klinische Zeichen der pulmonal-arteriellen Hypertonie: Links parasternaler Herzanschlag Akzentuierte pulmonale Komponente des 2. Herztones Systolikum über der Trikuspidalklappe (Trikuspidalinsuffizienz) 3. Herzton
105 Erst im fortgeschrittenen Stadium: Positiver hepatojugulärer Reflux Halsvenenstauung Hepatosplenomegalie Periphere Ödeme Aszites Weitere initiale Untersuchungen Röntgen-Untersuchung des Thorax Ist zum Zeitpunkt der Diagnosestellung meist nicht mehr normal. Das Ausmass der pulmonalen Hypertonie korreliert aber nicht mit dem Ausmass der radiologischen Veränderungen. Bei 90% der Patienten zeigen sich erweiterte Pulmonalarterien oder dilatierte hiläre Gefässe. EKG Nicht diagnostisch, aber evtl. hinweisend. Pulmonale Zeichen der rechtsventrikulären Hypertrophie: R, ST-Senkungen und T-Negativierung in V1 Rechtstyp oder überdrehter Rechtstyp RS-Ratio in V6 < 1 SIQIII-Typ RSB Echokardiografie Screening-Methode der Wahl bei Verdacht auf eine pulmonale Hypertonie. Erfasst eine Linksherzinsuffizienz oder Klappenpathologien als Ursache der pulmonalen Hypertonie (postkapilläre Hypertonie viel häufiger als pulmonal-arterielle Hypertonie!). Suche nach pulmonal-arterieller Hypertonie: Rechtsventrikuläre Grösse und Funktion in der Echokardiografie oder im MRI (u.a. TAPSE, MPI, LVEI*) Abschätzen des Druckes im rechten Ventrikel (RVSP*) aus der Geschwindigkeit der Trikuspidalinsuffizienz (peak tricuspid regurgitant velocity, peak TRV) Ausmass der Trikuspidalinsuffizienz Grösse des rechten Vorhofes Breite und Atemvariabilität der Vena cava inferior Dilatation des Truncus pulmonalis * LVEI = left ventricular eccentricity index; MPI = myocardial performance index; RVSP = rechtsventrikulärer systolischer Druck; TAPSE = tricuspid annular plane systolic excursion Wahrscheinlichkeit für das Vorliegen einer PAH aufgrund der Echokardiografie PH unwahrscheinlich PH möglich PH wahrscheinlich Geschätzter RVSP 36 mmhg (peak TRV 2.8 m/s, was nach Addition von ca. 5 mmhg für den ZVD einem RVSP von ca. 36 mmhg entspricht) Keine indirekten Zeichen für eine pulmonale Hypertonie und normale systolische RV-Funktion Geschätzter RVSP 36 mmhg (peak TRV 2.8 m/s), aber indirekte Zeichen für eine PH oder abnormale RV- Funktion Geschätzter RVSP mmhg Geschätzter RVSP > 50 mmhg (peak TRV > 3.4 m/s) Geschätzer RVSP mmhg mit indirekten Zeichen für eine PH Geschätzer RVSP >50 mmhg (mit oder ohne indirekte Zeichen) Lungenfunktionstest (mit CO-Diffusionskapazität) und 6-Minuten-Gehtest Der Lungenfunktionstest kann obstruktive und restriktive Lungenerkrankungen erfassen
106 Zudem muss bei Verdacht auf eine pulmonale Hypertonie die Diffusionskapazität der Lungen bestimmt werden. Bei pulmonaler Hypertonie ist die Diffusionskapazität häufig vermindert. Der 6-Minuten-Gehtest muss standardisiert nach ATS-Kriterien durchgeführt werden und dient zur Bestimmung der Leistungsfähigkeit, der Prognose und der Verlaufskontrolle. Eine wichtige Rolle kommt auch der Spiroergometrie zu. Diese hilft, alternative Diagnosen abzuklären und das Ausmass der funktionellen Einschränkung, speziell auch im Hinblick auf eine mögliche Lungentransplantation, zu erheben. CT-Thorax mit Kontrastmittel (Lungenembolie-Protokoll) und Ventilations-/Perfusionsszintigrafie der Lunge Diese Untersuchungen sind zur Diagnosestellung von interstitiellen Lungenerkrankungen, Lungenemphysem, Lungenembolien und anderen Pathologien hilfreich. Bei chronischen Lungenembolien ist heute die Lungenszintigrafie wegen der gegenüber der CT höheren Sensitivität diagnostischer Standard. Rechtsherzkatheter-Untersuchung Diese Untersuchung gilt als Gold-Standard in der definitiven Diagnosestellung. Sie dient auch dazu, den Mechanimus der pulmonalen Hypertonie zu definieren (postkapillär bei Linksherzinsuffizienz oder präkapillär bei pulmonal-arterieller Hypertonie) und die pulmonale Hypertonie zu klassifizieren. Dies ist schliesslich für die Therapie wegweisend. Eine spezifische Therapie mit pulmonalen Vasodilatatoren darf nur nach vorgängiger Rechtsherzkatheter-Untersuchung durchgeführt werden. Basis-Laboruntersuchungen Bei der Abklärung hinsichtlich der Genese einer PAH gehört eine Basis- Laborabklärung dazu. Je nach klinischem Befund und allfälliger Verdachtsdiagnose wird die unten angeführte Liste allenfalls noch ergänzt werden müssen. In der Regel aber sollten die meisten der angeführten Bestimmungen durchgeführt werden (ausser die Ätiologie steht schon fest). Leberwerte Nierenwerte Hämatologie Gerinnungsabklärung (gemäss Vorgaben Zentrum für Labormedizin des KSSG) «Rheumatologie-Screening» (Rheumafaktoren und antinukleäre Antikörper, CRP und bei Verdacht auf Kollagenosen auch BSR) HIV-Test BNP/pro-BNP Arterielle Blutgasanalyse Screening von Risikogruppen für eine PAH Risikogruppen für eine PAH sollten mittels Echokardiografie gescreent werden. Patienten mit Sklerodermie oder anderen rheumatologischen Erkrankungen (SLE, RA) Genetisch bedingte PAH (bei direkten Familienangehörigen) Kongenitale Shunt-Vitien Therapie der PAH Vermeiden von Belastungen Rauchen Respiratorische Infekte (Grippe- und Pneumokokken-Impfung) Übermässige körperliche Belastung Höhenexposition Schwangerschaft NSAR Betablocker Sauna, Hamam oder andere heisse Duschprozeduren
107 212 Diagnostischer Ansatz Pulmonale Hypertonie Keine Zeichen einer schweren PH/RV-Dysfunktion Grundkrankheit behandeln Medikamente/ Toxine Symptome und klinische Befunde suggestiv für PH Wahrscheinlichkeit PH gemäss Echokardiografie (Seite 213) Hoch oder intermediär Linksherzerkrankung oder Lungenerkrankung erwägen (Symptome, Risikofaktoren, klinische Befunde, EKG, Thorax, Lungenfunktion, DLCO, HRCT, Blutgase) JA CTD HIV JA CTEPH möglich Angio-CT, RHC, Pulmonalis-Angiografie Hereditäre PVOD/PCH Idiopathische PVOD/PCH Diagnose Linksherzerkrankung oder Lungenerkrankung bestätigt? V/Q Szintigrafie Mismatch? PAH wahrscheinlich Spezifische Tests NEIN PH-Expertenzentrum Idiopathische PAH Andere Gründe für Symptome erwägen, Follow-up JA CHD RHC mpap 25 mmhg, PAWP 15 mmhg, PVR > 3 Wood units Portopulmonale pulmonale Hypertonie Schistosomasis Hereditäre PAH JA Zeichen einer schweren PH/ RV-Dysfunktion PH-Expertenzentrum NEIN tief NEIN andere Ursachen suchen Gruppe 5 CHD: angeborene Herzfehler, CT: Computertomografie, CTD: Bindegewebserkrankungen, CTEPH: chronische thromboembolische pulmonale Hypertonie, DLCO: CO-Diffusionskapazität, PAH: pulmonalarterielle Hypertonie, PAWP: pulmonary artery wedge pressure, PH: pulmonale Hypertonie, PVOD/PCH: pulmonary veno-occlusive disease/pulmonary capillary hemangiomatosis, PVR: pulmonalvaskulärer Widerstand, RHC: Rechtsherzkatheter, RV: rechtsventrikulär, V/Q: Ventilation/Perfusion Basistherapie Sauerstoff, falls Hypoxämie in Ruhe (< 8 kpa) Orale Antikoagulation bei idiopathischer/hereditärer PAH und CTEPH Diuretika bei rechtsventrikulärer Dysfunktion/Hypervolämie Behandlung einer Anämie und/oder eines Eisenmangels Betablocker bei schwererer pulmonal-arterieller Hypertonie nicht geben oder absetzen! Falls möglich, Therapie der Grunderkrankung (Shunt-Vitien, HIV, Sklerodermie, SLE usw.) Psychosoziale Betreuung Therapie mit Vasodilatatoren Die Prognose der PAH ist auch heute noch ungünstig, vergleichbar mit gewissen neoplastischen Erkrankungen. Die heute verfügbare spezifische Therapie zielt darauf hin, den Prozess des vaskulären Remodeling zu bremsen. Damit kann der Verlauf der Krankheit stabilisiert oder im besten Fall verbessert werden. Idealerweise sollte diese spezifische Therapie zur Verbesserung der Prognose früh im Krankheitsverlauf begonnen werden (frühe Diagnosestellung wichtig). Operative Therapieverfahren Bei NYHA-Klasse III oder IV unter Ausbau der medikamentösen Therapie und/oder bei parenteraler PH-spezifischer Therapie sollten Patienten frühzeitig über die Möglichkeit einer Lungentransplantation informiert werden und für drei informative Gespräche dem Lungentransplantationszentrum am Universitätspital in Zürich zugewiesen werden. Bei der CTEPH ist die pulmonale Thrombendarteriektomie (PEA) die Therapie der Wahl bei operablen Patienten. In der Schweiz wird die PEA nur in Zürich am Universitätsspital durchgeführt. Als Basis für die Operabilität muss eine standardisiert durchgeführte Pulmonalis- Angiografie erfolgen. 213
108 Risikostratifikation der PAH Prognostische Faktoren (geschätzte 1-Jahres-Mortalität) Klinische Zeichen der Rechtsherzinsuffizienz Progression der Symptome Tiefes Risiko < 5% Intermediäres Risiko 5 10% Hohes Risiko > 10% Nicht vorhanden Nicht vorhanden Vorhanden Nein Langsam Schnell Synkope Nie Ja Rezidivierend WHO funktionelle Klasse I, II III IV 6MWD > 440 m m <165 m Spiroergometrie Natriuretische Peptide Imaging (Echo, MRI) Hämodynamik Peak VO2 > 15 ml/min/ kg (> 65% Soll) VE/VCO2 slope < 36 BNP < 50 ng/l NT-proBNP < 300 ng/l RA-Fläche < 18 cm 2 Kein Perikarderguss RAP < 8 mmhg CI 2.5 l/min/m 2 SvO2 > 65% Peak VO ml/min/kg (35 65% Soll) VE/ VCO2 slope BNP ng/l NT-proBNP ng/l RA-Fläche cm 2 Keiner/minimaler Perikarderguss RAP 8 14 mmhg CI l/min/m 2 SvO % Peak VO2 < 11 ml/min/ kg (< 35% Soll) VE/VCO2 slope 45 BNP > 300 ng/l NT-proBNP > ng/l RA-Fläche > 26 cm 2 Perikarderguss RAP > 14 mmhg CI < 2.0 l/min/m 2 SvO2 < 60% 6MWD: 6-Minuten-Gehstrecke, BNP: B-type natriuretic peptide, CI: cardiac index, NT-proB- NP: N-terminales probnp, RA: rechter Vorhof, RAP: Druck im rechten Vorhof (zentralvenöser Druck), SvO2: gemischtvenöse Sättigung, peak VO2: maximale Sauerstoffaufnahme, VE/ VCO2 slope: ventilatorische Effizienz, WHO: World Health Organization. Follow-up der PAH Unter Therapie ist in Abhängigkeit des Schweregrades und des Verlaufes ein regelmässiger Follow-up aller Patienten mit PAH wichtig (alle 3 6 Monate, je nach Verlauf). Folgende Parameter werden dabei erhoben: Funktionelle Klasse (NYHA-Klasse) Klinische Zeichen der Rechtsherzinsuffizienz Erfassen der Medikamente inkl. allfälliger Nebenwirkungen Lungenfunktionstest bei hypoxisch bedingten Lungenerkrankungen (Gruppe 3) Messung der O2-Sättigung in Ruhe und während des 6-Minuten- Gehtests Echokardiografie einmal jährlich oder bei Verschlechterung Rechtsherzkatheter bei klinischer Verschlechterung und vor Therapieeskalation BNP Board für pulmonale Hypertonie am KSSG Am KSSG findet alle 4 Wochen, jeweils am ersten Mittwoch des Monats, das PH-Board zur Besprechung von Patienten mit pulmonaler Hypertonie statt. Die Anmeldung für ambulant und stationär betreute Patienten am KSSG erfolgt elektronisch im Boards-Tool (Fachanwendungen -> Bords C57). Die Anmeldung erfolgt durch den Arzt, welcher den Fall vorstellt. Externe Ärzte sind am Board willkommen. Dafür ist eine Anmeldung des Patienten an das Ambulatorium Pneumologie (Karin Sonam, Telefon / [email protected]) mit entsprechenden Unterlagen (Echobefunde, Labor, Lungenfunktion, CT-Thorax etc., falls vorhanden) im Voraus notwendig
109 Weitere Information findet man auf den Homepages des KSSG: Dr. Daniel Weilenmann PD Dr. Micha Maeder Prof. Dr. Otto Schoch Dr. Rebekka Kleiner Dr. Fabian Aigner Herzinsuffizienz Klassifikationen Stadien A D: klinisch von beschränkter Relevanz. A: mit Herzinsuffizienz assoziierte Risikofaktoren (z. B. Diabetes, Hypertonie). B: strukturelle Herzkrankheit ohne Symptome (z. B. asymptomatische linksventrikuläre systolische Dysfunktion nach Infarkt). C: strukturelle Herzkrankheit mit Symptomen (eigentliche Herzinsuffizienz). D: therapierefraktäres Stadium Akut vs. chronisch: Unterscheidung wichtig aufgrund des therapeutischen Ansatzes in der Akutphase. Die meisten Patienten mit akuter Herzinsuffizienz haben aber eine akute Dekompensation einer chronischen Herzinsuffizienz, deren Mechanismus die langfristige Therapie determiniert Herzinsuffizienz mit eingeschränkter vs. erhaltener Auswurffraktion: aus therapeutischen Gründen essenziell. Neu gibt es die intermediäre Klasse der Herzinsuffizienz mit leicht eingeschränkter («midrange») Auswurffraktion, die bis jetzt noch nicht gut charakterisiert ist (Tabelle)
110 Klassifikation der Herzinsuffizienz (heart failure, HF) nach linksventrikulärer Auswurffraktion (left ventricular ejection fraction, LVEF) HF with reduced LVEF (HFrEF): LVEF < 40% HF with midrange LVEF (HFmrEF) LVEF 40 49% Demografie jünger intermediär älter Ätiologie Mechanismus Diagnose Therapie Tabelle 1 v.a. koronare Herzkrankheit (grosser Infarkt), Kardiomyopathien Primär systolische LV-Dysfunktion Symptome±klinische Zeichen plus Echokardiografie: LVEF < 40% ausreichend Gut definiert, verbessert Prognose Koronare Herzkrankheit (kleinerer Infarkt) und andere Variabel Symptome±klinische Zeichen plus Echokardiografie: LVEF (vgl. Definition) + zusätzlich Parameter + erhöhtes BNP/ NT-proBNP Unklar, ws. ähnlich wie HFrEF HF with preserved LVEF (HFpEF) LVEF 50% v.a. hypertensive Herzkrankheit Primär diastolische LV-Dysfunktion Symptome±klinische Zeichen plus Echokardiografie: LVEF (vgl. Definition) + zusätzlich Parameter + erhöhtes BNP/ NT-proBNP Schlecht definiert; keine Massnahme bekannt, die das Überleben verlängert Diagnose Diagnose der Herzinsuffizienz beruht auf folgenden Kriterien: Typische Symptome (Dyspnoe unter Belastung oder in Ruhe, Leistungsintoleranz, Orthopnoe, paroxysmale nächtliche Dyspnoe, Ödeme) Fakultativ (im chronischen Zustand nicht immer vorhanden): klinische Zeichen, die entweder die Stauung (3. Herzton, pulmonale Rasselgeräusche, Halsvenenstauung, Ödeme) oder das verminderte Herzminutenvolumen (kühle Extremitäten) reflektieren Obligat objektiver Nachweis einer kardialen Dysfunktion (z. B. linksventrikuläre Dysfunktion, Klappenvitium) mittels Echokardiografie Das klinische Ansprechen auf eine Therapie unterstützt die Diagnose, ist aber allein nicht ausreichend für die Diagnose. 218 BNP/NT-proBNP erhöht, ohne dass Linksherzinsuffizienz vorliegt Niereninsuffizienz Schwerer Infekt/schwere Entzündung Lungenembolie/pulmonalarterielle Hypertonie (d.h. isolierte Rechtsherzinsuffizienz) Anämie Stroke/Hirnblutung Hohes Alter Hyperdyname Kreislaufzustände (Leberzirrhose, Hyperthyreose) BNP/NT-proBNP tief, obschon Linksherzinsuffizienz vorliegt Perakuter Prozess (BNP/NT-proBNP noch nicht erhöht) Mitralstenose (Obstruktion vor dem linken Ventrikel) Ausgeprägte Adipositas Tabelle 2 219
111 Mögliche Herzinsuffizienz Anamnese (Symptome, prädisponierende Faktoren, z. B. früherer Infarkt, Vorhofflimmern) Klinische Untersuchung EKG Abbildung 1 1 Punkt suggestiv/ abnorm Natriuretische Peptide BNP 35 ng/l NT-proBNP 125 ng/l Ja Echokardiografie Diagnose Herzinsuffizienz Nein Alle Punkte unauffällig/normal Herzinsuffizienz unwahrscheinlich: erwäge alternative Ursachen für Symptome bzw. erhöhte natriuretische Peptide unaufällig Definition des Mechanismus (evtl. weitere Tests) Der Algorithmus (gemäss 2016 ESC Guidelines) gilt grundsätzlich für das akute wie das nicht-akute bzw. chronische Setting. Die hier dargestellte Version gilt für Patienten mit chronischen Symptomen. Die Unterscheidung ist wichtig, da unterschiedliche Cut-offs für B-type natriuretic peptide (BNP) und N-terminal-proBNP (NT-proBNP) gelten. Die für das nicht-akute Setting vorgeschlagenen Cut-offs von 35 bzw. 125 ng/l sind sehr tief und haben einen hohen negativen prädiktiven Wert (Ausschluss). Es gibt verschiedene nicht-kardiale Ursachen für erhöhte BNP- und NT-proBNP-Werte (Tabelle 2). Zu beachten ist im Weiteren, dass BNP und NT-proBNP unspezifische, quantitative Marker eines kardialen (vor allem linksventrikulären) Stresses sind und keine Aussage über den Mechanismus machen können. Eine Echokardiografie wird daher zur Diagnosesicherung und zur Darstellung des Mechanismus der Herzinsuffizienz immer notwendig sein. In Settings mit leichtem Zugang zur Echokardiografie (wie in der Schweiz) kann ohne BNP-/NT-pro-Bestimmung direkt zur Echokardiografie geschritten werden (gestrichelte Linie). Im akuten Setting betragen die Cut-offs für BNP und NT-proBNP 100 bzw. 300 ng/l. Diese Cut-offs haben einen hohen negativen prädiktiven Wert zum Ausschluss einer Herzinsuffizienz bei Patienten mit akuter Dyspnoe. Werte über dem Cut-off sind auch im akuten Setting nicht beweisend für Herzinsuffizienz und müssen zu weiteren Tests führen (primär Echokardiografie). Für weitere Information zum diagnostischen Vorgehen im akuten Setting siehe «akute Herzinsuffizienz». Akute Herzinsuffizienz meist akute Dekompensation eines chronischen Prozesses Dekompensation einer chronischen Herzinsuffizienz mit eingeschränkter Pumpfunktion aufgrund eines Triggers (siehe unten) Dekompensation bei Herzinsuffizienz mit erhaltener Pumpfunktion, in der Regel infolge hypertensiver Entgleisung und/oder Volumen überladung («akute kardiovaskuläre Insuffizienz») seltener akuter Prozess (Myokardinfarkt, Rhythmusstörung, Myokarditis, akute Klappeninsuffizienz usw.)
112 222 Diagnose Akute Herzinsuffizienz = potenziell lebensbedrohlicher Zustand, der ein schnelles und systematisches Vorgehen erfordert. Diagnostischer und therapeutischer Ansatz gemäss Abbildung 2 (ESC Guidelines 2016). Die Idee dieses Ansatzes ist es, differentialdiagnostisch vorzugehen und lebensrettende Massnahmen parallel sofort einzuleiten. Kardiogener Schock = Hypotonie (systolischer Blutdruck < 90 mmhg) PLUS Zeichen der Hypoperfusion (klinisch: kalte Extremitäten, Oligurie, abnormer mentaler Zustand; labor chemisch: erhöhtes Laktat, meta bolische Azidose, erhöhtes Kreatinin bzw. Transaminasen) trotz adäquater Füllung. Die grosse Mehrheit der Patienten mit akuter Herzinsuffizienz ist aber normotensiv. Für alle Patienten mit vermuteter akuter Herzinsuffizienz empfohlene Tests: BNP oder NT-proBNP: Ausschluss Herzinsuffizienz bei Werten > 100 ng/l bzw. 300 ng/l (vgl. oben) bzw. Quantifizierung des «kardialen Stress» (prognostische Aussage). 12-Ableitungs-EKG: ein völlig normales EKG macht eine akute Herzinsuffizienz unwahrscheinlich. Das EKG kann andererseits Hinweise auf den Mechanismus der Herzinsuffizienz geben (akuter Infarkt, Bradykardie, Tachykardie) Thorax-Röntgen-Bild: Nachweis der pulmonalvenösen Hypertonie einerseits und Suche nach Differentialdiagnosen andererseits komplettes Set an Laborparametern zur Suche nach Mechanismen/ Co-Faktoren (Hämoglobin, TSH, CRP) und Effekten (Kreatinin, Transaminasen) der akuten Herzinsuffizienz. Dazu gehört auch das kardiale Troponin, welches als quantitativer unspezifischer Marker der myokardialen Schädigung und nicht immer als akuter Infarkt betrachtet werden muss. Echokardiografie: für alle Patienten innert 48 Stunden, wenn die kardiale Pathologie nicht oder nicht ausreichend bekannt ist. Patienten im kardiogenen Schock benötigen sofort eine Echo- kardiografie unter anderem mit der Frage nach mechanischen, akut zu behandelnden Problemen (mechanische Infarktkomplikationen, Perikardtamponade, akutes Klappenvitium). Patient mit vermuteter AHF Kardiogener Schock? Nein Akute respiratorische Insuffizienz? Nein Suche nach Ätiologie C Akutes K(C)oronarsyndrom H Hypertensiver Notfall A Arrhythmie M Akute Mechanische Ursache P Lungen (Pulmonal)embolie Nein Weiterer diagnostischer Work-up Optimale Therapie Kreislauf-Support medikamentös mechanisch Respiratorischer Support Sauerstoff Nicht-invasive Ventilation* Intubation/Ventilation Ursachen/Trigger für akute Dekompensation Myokardiale Ischämie/Infarkt Inadäquate Therapie/Malcompliance Begleitmedikation (NSAR inkl. COX-2-Inhibitoren, Steroide, trizyklische Antidepressiva, Lithium, Kalziumkanalblocker) Niereninsuffizienz Inadäquate Wasser-/Salzzufuhr Arrhythmien (v.a. tachykardes Vorhofflimmern) Progression eines Klappenvitiums Infektion Ja Ja Ja Kausale Therapie z. B. PCI, Perikarddrainage, Klappenersatz Abbildung 2 *Bei Patienten mit akuter respiratorischer Insuffizienz im Rahmen eines akuten Koronarsyndroms: keine nicht-invasive Ventilation, sondern Intubation. 223
113 Lungenembolie Hyperthyreose, Anämie Toxine, kardiodepressive Substanzen Therapie Kausale Therapie wenn immer möglich und so früh als möglich (vgl. Abbildung 2), ansonsten/zusätzlich allgemeine supportive Therapie gemäss dem klinischen und hämodynamischen Profil. Diese Therapie ist im Wesentlichen empirisch (prognostischer Effekt dieser Massnahmen nicht bewiesen). Ziel ist eine rasche Verbesserung der Symptomatik und eine klinischen Stabilisierung, sodass die Therapie der chronischen Herzinsuffizienz etabliert werden kann. Da die optimale Therapiestrategie bei akuter Herzinsuffizienz unbekannt ist, ist es wichtig, dass trotz Notfallsituation möglichst viele Patienten in entsprechende Studien eingeschlossen werden. Je nach Schweregrad erfolgt die Behandlung auf Notfallstation/ Normalstation oder Notfallstation/MIPS, ggf. mit invasivem Monitoring. Gemäss Hydratationszustand («wet or dry») und Gewebeperfusion («warm or cold», nicht immer, aber oft gleichbedeutend mit normoton vs. hypoton) können vier hämodynamische Profile unterschieden werden, welche die grobe Therapie-Richtung vorgeben «wet and warm» (Mehrheit der Patienten): normo- oder hyperton und gestaut: Therapie mit Vasodilatatoren und Diuretika «wet and cold»: ungünstig, hypoton und gestaut: Therapie mit Inotropika, Vasopressoren, Diuretika, mechanischem Support «dry and warm»: relativ günstige Situation, Anpassung der peroralen Therapie «dry and cold»: primär Volumensubstitution; die Reaktion darauf determiniert das weitere Vorgehen Medikamentöse Therapie Evtl. Analgosedation (Morphin) bei Schmerzen/Agitation Nitrate Bei allen Patienten mit erhöhtem Blutdruck. Kann mit Diuretika kombiniert werden. Falls systolischer Blutdruck > 90 mmhg (Vorsicht bei systolischem Blutdruck mmhg, kontraindiziert, falls < 90 mmhg) Spray: 2 Hübe à 0.4 mg, 1 Kapsel à 0.8 mg, kann nach 5 10 Min. wiederholt werden, ggf. mehrfach, dabei Blutdruckkontrolle; später Nitropflaster. Ggf. iv-verabreichung auf MIPS. Cave: Toleranzentwicklung Ggf. Nitroprussid (MIPS) Schleifendiuretika Die aktuellen Richtlinien sehen das Diuretikum als primäres Medikament der Behandlung der akuten Herzinsuffizienz. Dies trifft nur für Patienten mit Volumenüberladung zu. Falls primär eine hypertensive Entgleisung zur linkskardialen Dekompensation geführt hat, soll das Diuretikum nach Möglichkeit zugunsten des Nitrats zurückgestellt werden. Initial Furosemid (Lasix) als intravenöser Bolus von mg, je nach Schweregrad wiederholen (in den ersten 6 Stunden Totaldosis < 100 mg), je nach Verlauf Umstellung auf orale Therapie Die bolusweise Verabreichung (2 3x/Tag) und die kontinuierliche Infusion sind gleichwertig. Wenn immer möglich in Kombination mit Nitraten (besser hoch dosiert Nitrate und niedrig dosiert Diuretika als umgekehrt) Allgemeine Massnahmen Ruhigstellung Sauerstoff, falls Hypoxämie SaO2 < 90% Nicht-invasive Beatmung, ggf. Intubation; bei akutem Koronarsyndrom: Intubation 224 Inotropika/Vasopressoren (gemäss Intensivmediziner auf MIPS) Bei ungenügender Gewebeperfusion trotz adäquatem Füllungszustand 225
114 226 Manchmal unverzichtbar, generell aber sehr zurückhaltender Einsatz (erhöhtes Arrhythmie-Risiko, Provokation von Ischämie), ggf. Levosimendan anstelle von Inotropika. Betablocker Im Akutstadium nur in Ausnahmefällen indiziert (z. B. intraventrikuläre dynamische Obstruktion) Cave: Gabe eines Betablockers zur Kontrolle der Herzfrequenz (v.a. IV) ohne Kenntnis der LV-Funktion kann kardiogenen Schock präzipitieren Vorbestehende Betablocker-Therapie wenn immer möglich nicht vollständig absetzen, evtl. temporäre Dosisreduktion Kardioversion/Antiarrhythmika Kardioversion/Antiarrhythmika (siehe entsprechende spezifische Kapitel) Elektrische Kardioversion bei Patienten mit atrialen oder ventrikulären Rhythmusstörungen, die als ursächlich für die akute Herzinsuffizienz angesehen werden Antiarrhythmika: neben Betablocker nur Amiodaron (Cordarone) Klasse-IB/C-Antiarrhythmika bei LV-Dysfunktion kontraindiziert Antikoagulation/Thrombozytenaggregationshemmung Akutes Koronarsyndrom: gemäss Standard (siehe spezifisches Kapitel) Vorhofflimmern/-flattern: orale Antikoagulation, Heparin (siehe spezifisches Kapitel) Mechanische Therapieoptionen Koronarangiografie/PCI: bei vermuteter ursächlicher grosser myokar-dialer Ischämie Notfallmässige ACBP-Operation (selten) Notfallmässige Operation von mechanischen Infarktkomplikationen (Papillarmuskelruptur, Ventrikelseptumdefekt, Ruptur der freien Wand) Notfallmässige Operation bei Endokarditis-Komplikationen IABP (kontraindiziert bei Aortendissektion, signifikanter Aorteninsuffizienz): kommt typischerweise im Herzkatheterlabor vor/nach PCI bei selektionierten Patienten zum Einsatz Perkutanes linksventrikuläres Assist Device (LVAD): Impella, kommt typischerweise im Herzkatheterlabor vor/nach PCI bei selektionierten Patienten zum Einsatz VA-ECMO: für Patienten im kardiogenen Schock, auch nach Reanimation mit relativ kurzer «no-flow-time». Indikationsstellung primär durch MIPS-Team, frühzeitige Diskussion der Indikation anstreben (vgl. Abschnitt Reanimation) Chirurgisches linksventrikuläres Assist Device: Diskussion mit Herzchirurgie Chronische Herzinsuffizienz Diagnostik Diagnose-Prinzip und -Algorithmus siehe oben Echokardiografie ist das primäre Imaging-Tool; kardiales MRI bei Erstdiagnostik oft auch sinnvoll (ätiologische Abklärung Kardiomyopathie, Bestimmung Viabilität bei chronischer KHK) Koronarangiografie: nicht zwingend indiziert bei jeder neu diagnostizierten Herzinsuffizienz; bei unklarer Ätiologie im Verlauf (nicht akut) aber meist sinnvoll Therapie Wenn immer möglich kausale Therapie (Ischämie-Behandlung etc.). Ansonsten allgemeine nicht-medikamentöse Massnahmen und medikamentöse Therapie, welche für Patienten mit HFrEF gut, für Patienten mit HFpEF schlecht definiert ist. 227
115 Nicht-medikamentöse Massnahmen (nach Möglichkeit Schulung durch heart failure nurses) Allgemeine Massnahmen (Aufklärung von Patient und Angehörigen, Arzneimittelberatung, Diät, Bewegung und soziale Gewohnheiten)* Gewichtsnormalisierung Begrenzte Kochsalzzufuhr Höchstens begrenzter Alkoholkonsum (max. 30 g/tag beim Mann und 20 g bei der Frau); bei alkoholtoxischer Kardiomyopathie Alkoholkarenz Prinzipiell kein Alkohol (Toxin) Regelmässige körperliche Bewegung bei stabiler Herzinsuffizienz Suche nach optimierbaren Co-Morbiditäten Nicht-kardiovaskulär: Anämie, Lungenerkrankung, renale Dysfunktion, Schilddrüsen-Dysfunktion Medikamentöse Therapie der HFrEF Die Therapie der chronischen HFrEF folgt einem gut definierten Stufenschema. Neben der symptomatischen Behandlung mit Schleifendiuretika müssen die drei Grundpfeiler der Therapie etabliert werden: ACE-Hemmer (oder Angiotensin-Rezeptor-Antagonist, ARB), Betablocker und Mineralokortikoidrezeptor-Blocker (MRA), dann gibt es drei weitere etablierte, individualisiert einsetzbare Optionen (Sacubitril/ Valsartan, Ivabradin, kardiale Resynchronisation), anschliessend Optionen für therapierefraktäre Situationen (Abbildung 3) Diuretika Primär Schleifendiuretika (Furosemid, Torasemid) Effektiv als symptomatische Therapie bei Flüssigkeitsretention Optimierung der Dosis durch Festlegung und Kontrolle des «Trockengewichts», d.h. individuelle Dosierung Wichtigste unerwünschte Nebenwirkungen: Hypokaliämie, Hypomagnesiämie, Hyponatriämie, Störungen des Säure-Basen- Haushaltes, Hyperurikämie Patient kann ACEI oder ARB in mässiger/hoher Dosierung tolerieren (äquivalent zu Enalapril 2x10 mg/d) Wechsel von ACEI/ARB auf ARNI evaluieren HFrEF (LVEF <40%, NYHA II-IVH ACEI (oder ARB) und Betablocker (Reihenfolge des Einsatz unwichtig) Noch NYHA II-IV und LVEF 35%? Ja Zusätzlich MRA (NYHA II: Eplerenon, NYHA III/IV: Spironolacton) Noch NYHA II-IV und LVEF 35%? Ja Sinusrhythmus und QRS-Dauer 130 ms CRT evaluieren Nein Nein Sinusrhythmus und HF 70/min trotz maximaler tolerierter Betablocker-Dosis Ivabradin evaluieren Kombination der 3 Optionen, falls möglich Ja Therapie-refraktäre Symptome? Nein Optionen evaluieren (Digoxin, HTPL, Assist Device) Keine weitere Therapie-Eskalation * Siehe Broschüre: Herzinsuffizienz, Stark für ein schwaches Herz, Schweizerische Herzstiftung, Abbildung
116 230 Nach Erreichen der Euvolämie müssen die Diuretika zugunsten der prognostisch wichtigen Medikamente (ACE-Hemmer, ARB, ARNI, Betablocker, Mineralokortikoidrezeptorblocker) auf die notwendige Minimaldosis zu reduziert werden (Diuretika verbessern die Prognose nicht). Wenn egfr < 30 ml/min/1.73 m 2, keine Thiaziddiuretika verwenden, ausser synergistisch mit Schleifendiuretika eingesetzt Begrenzte Kochsalzzufuhr Ungenügendes Ansprechen: Diuretika-Dosis erhöhen, evtl. mehrfach täglich verordnen, Schleifendiuretika und Metolazon (2.5 5 mg/tag) kombinieren (sequenzielle Nephronblockade), Intravenöse Schleifendiuretika (Furosemid) bei intestinaler Stauung und verminderter Resorption (siehe akute Herzinsuffizienz) ACE-Hemmer Primär Basistherapie bei allen Patienten mit HFrEF (LVEF < 40%) und asymptomatischer linksventrikulärer Dysfunktion (LVEF < 40%) Hypotonie-Risiko minimieren: exzessive Diurese vor Therapiebeginn vermeiden, Diuretika-Therapie für 24 Std. reduzieren oder absetzen, ACE-Hemmer-Therapie evtl. am Abend beginnen Niedrig dosiert beginnen, zu Erhaltungsdosis steigern (Verdopplung der Dosis alle 14 Tage unter Kontrolle von Kalium und Kreatinin, Zieldosis gemäss Studien), schnelleres Auftitrieren im Spital möglich Niereninsuffizienz: Therapie nicht abbrechen, solange Anstieg des Kreatinins 50% Kontrollen im Verlauf: BD, Nierenfunktion und Elektrolyte 1 2 Wochen nach Therapiebeginn bzw. bei jeder Dosiserhöhung, nach 3 Monaten und dann alle 6 Monate Angiotensin-Rezeptorblocker Bei Patienten mit LVEF < 40% und ACE-Hemmer-Unverträglichkeit/ Nebenwirkungen Eintitrierung wie bei ACE-Hemmer Betablocker Behandlung aller Patienten mit stabiler HFrEF (NYHA II IV, LVEF < 40%) unter Beachtung der Kontraindikationen (Bestandteil der Basistherapie neben ACE-Hemmer, siehe Abbildung) Bei Herzinsuffizienz etablierte Betablocker verwenden: Carvedilol, Bisoprolol, Metoprolol-Succinat, Nebivolol Behandlung von Patienten mit linksventrikulärer systolischer Dysfunktion (LVEF < 40%) nach Myokardinfarkt auch ohne Symptome einer Herzinsuffizienz In der Regel zuerst Basisbehandlung mit ACE-Hemmer (Strategie «Betablocker [Bisoprolol] zuerst» ist aber gleichwertig mit der Strategie «ACE-Hemmer [Enalapril] zuerst») Es gilt das Prinzip «start low, go slow, aim high»: Beginn mit sehr niedriger Dosis, Dosissteigerung in Intervallen von 2 4 Wochen, klinische Verschlechterung möglich (Schwäche, Müdigkeit) Bei transienter Verschlechterung der Herzinsuffizienz, v.a. in Frühphase: Dosis der Diuretika evtl. erhöhen, Betablocker-Dosis nicht weiter steigern, evtl. temporär reduzieren Bei Hypotonie zuerst Reduktion der Dosis von Vasodilatatoren, die nicht zwingend notwendig sind (Nitrate), und Diuretika Kombination mit Amiodaron (Cordarone) oder Digoxin möglich; bei exzessiver Bradykardie zunächst Digoxin und andere bradykardisierende Medikamente stoppen Kontraindikationen beachten (Asthma bronchiale, bradykarde Arrhythmien); COPD und PAVK sind keine Kontraindikationen Mineralokortikoidrezeptor-Antagonist, MRA Neben ACE-Hemmer und Betablocker dritter Grundpfeiler der HFrEF-Therapie (vgl. Abbildung) Spironolacton: bei NYHA III/IV unter ACE-Hemmer und Betablocker in den höchsten tolerierten Dosierungen. Dosis 12.5 bis 25 mg/tag (in Ausnahmefällen 50 mg/tag) Eplerenon: für Patienten mit NYHA II (sonst Spironolacton). Dosis mg 231
117 Erhöhtes Risiko von Hyperkaliämien, daher initial engmaschige Kontrolle von Kreatinin und Kalium (in Abhängigkeit von Ausgangswerten und Nierenfunktion) Weitere Optionen für Patienten, die unter ACE-Hemmer (oder ARB), Betablocker und MRA noch symptomatisch sind und eine LVEF < 35% aufweisen Gemäss ESC Guidelines 2016 müssen für all diese Patienten (auch wenn «nur» NYHA II) primär drei Optionen geprüft werden: Sacubitril/ Valsartan, Ivabradin und kardiale Resynchronisation (vgl. Abbildung 3, nachfolgend ausgeführt). Diese Optionen können und sollen bei geeigneten Patienten kombiniert werden. Ivabradin senkt Herzfrequenz via selektivem Effekt auf den Sinusknoten, kein Effekt bei Vorhofflimmern Option bei Patienten mit LVEF 35%, Sinusrhythmus, NYHA II und Therapie mit ACE-Hemmer, die Betablocker nicht tolerieren (es muss versucht worden sein!) und eine Herzfrequenz 70/Min. oder trotz Betablocker eine Herzfrequenz 70/Min. aufweisen (Reduktion des kombinierten Endpunkts kardiovaskulärer Tod und Rehospitalisationen wegen Herzinsuffizienz) Dosis 2x 5 mg/tag, maximal 2x 7.5 mg (in Abhängigkeit von Herzfrequenz), bei Bradykardie Reduktion auf 2x 2.5 mg/tag Unerwünschte Effekte: Bradykardie, Phosphene Angiotensin-Rezeptor-Neprilysin-Inhibitoren (ARNI): verfügbar bisher nur Sacutril/Valsartan Kombination eines ARB mit einem Neprilysin-Inhibitor (hemmt Abbau von BNP und erhöht somit die Verfügbarkeit von biologisch wirksamem BNP) Sacubitril/Valsartan ist dem ACE-Hemmer Enalapril überlegen bezüglich Mortalitätsreduktion bei Patienten, die unter chronischer Therapie mit ACE-Hemmer oder ARB standen Umstellung von Patienten, die unter ACE-Hemmer (oder ARB) und Betablocker in optimalen Dosierungen und in der Regel Mineralokortikoidrezeptor-Blocker noch eine LVEF < 35% aufweisen und noch symptomatisch sind (mindestens NYHA II) Bei Umstellung von ACE-Hemmer auf ARNI muss ein 36-stündiges, ACE-Hemmer-freies Intervall beachtet werden (Gefahr des Angioödems), gilt nicht für Umstellung von ARB auf ARNI Aufgrund des relativ stark blutdrucksenkenden Effekts Beginn mit 2x 50 mg (selten gerade 2x 100 mg), Ziel-Dosis 2x 200 mg. Kontrolle Nierenfunktion und Kalium analog ACE-Hemmer/ARB Kombination mit MRA erlaubt und erwünscht Zur Verlaufskontrolle NT-proBNP messen (BNP-Werte nicht verwertbar als Mass der Herzinsuffizienz) 232 ICD/CRT Die kardiale Resynchronisation (CRT) ist eine wichtige Therapie- Option, die gemäss Algorithmus geprüft werden muss. Details/spezielle Situationen siehe Seite 269. Digoxin Reservemedikament, keine Daten für Verbesserung der Prognose Frequenzkontrolle bei Patienten mit HFrEF und Vorhofflimmern Symptomatische Patienten (NYHA II IV) mit HFrEF im Sinusrhythmus trotz optimaler Therapie (gemäss Algorithmus) Dosierung je nach Alter und Nierenfunktion: mg/tag, manchmal nur 3x/Woche initial Spiegelkontrolle (maximal 0.8 ng/ml, bei höheren Spiegeln nicht wirksamer, aber toxisch) Weitere Optionen Eisen: intravenöses Eisen (Fe-Carbomaltose) ist eine Option zur Verbesserung der Symptomatik bei Patienten HFrEF, NYHA II/III, Hb 9.5 bis 13.5 g und Eisenmangel (Ferritin < 100 µg/l oder Ferritin µg/l und Transferrin-Sättigung < 20%) 233
118 Nicht empfohlene bzw. kontraindizierte Massnahmen bei Patienten mit HFrEF Darbepoetin und andere Erythropoese-stimulierende Substanzen: nicht indiziert Statine: nicht indiziert zur Behandlung der Herzinsuffizienz per se; indiziert bei zugrunde liegender Koronarer Herzkrankheit Orale Antikoagulation: indiziert bei Vorhofflimmern, Klappenprothese etc., aber nicht wegen Herzinsuffizienz per se Renin-Inhibitoren: keine Indikation Diltiazem und Verapamil kontraindiziert bei HFrEF (negativ inotrop); Amlodipin kommt infrage falls Blutdruck mit Standard-Therapie nicht aussreichend behandelt werden kann Zentrale Schlafapnoe: BIPAP-Therapie kontraindiziert (gilt nicht für CPAP, weder für die Therapie von obstruktiver noch zentraler Schlafapnoe) NSAR und Coxibe kontraindiziert Herzinsuffizienz mit erhaltener Pumpfunktion (HFpEF) Pathophysiologie und Diagnose Siehe Tabelle 1 (für Details Spezialliteratur) Therapie Prinzip Es gibt keine Therapie, welche das Überleben dieser Patienten verbessert. Die Therapie zielt darauf ab, Symptome zu verbessern und Hospitalisation zu verhindern, dies durch optimale Behandlung der kardiovaskulären Grundkrankheit (Hypertonie, Diabetes, Koronare Herzkrankheit) und von Co-Morbiditäten (Übergewicht, Schlafapnoe, Niereninsuffizienz) sowie Medikamente, die in der klinischen Erfahrung wirksam sind und/oder in Studien gewisse Effekte gezeigt haben. In der Praxis muss ausprobiert werden, von welchen Medikamenten ein Patient symptomatisch am besten profitiert. Wichtig: Vermeiden/Behandlung von Tachyarrhythmien (Vorhofflimmern) Vermeiden von Volumendepletion und Volumenüberlastung Diuretika Symptomatisch oft wirksam. Cave: schmale therapeutische Breite aufgrund einer steilen end-diastolischen Druck-Volumen-Beziehung des linken Ventrikels bei HFpEF Stauung (Cave: Volumendepletion) Digoxin Option bei tachykardem Vorhofflimmern zur Frequenzkontrolle, im Sinusrhythmus Nutzen unklar ACE-Hemmer und ARB Theoretisch sinnvoll (Verbesserung der Relaxation, Verminderung der Hypertrophie), Nutzen bei Patienten mit etablierter Krankheit (d.h
119 nicht Prävention) nicht bewiesen bzw. mehrere grosse Studien negativ: bei hypertensiven Patienten wahrscheinlich trotzdem sinnvoll. Spironolacton Kein Effekt auf Mortalität, aber Reduktion des Risikos von Re-Hospitalisationen, zudem Verbesserung der Leistungsfähigkeit, allerdings erhöhtes Risiko von Niereninsuffizienz und Hyperkaliämie; somit Einsatz sinnvoll unter engmaschiger Kontrolle von Nierenfunktion und Kalium Betablocker theoretisch sinnvoll (Reduktion der Herzfrequenz, Verlängerung der Diastole), aber Datenlage unklar (Nutzen nicht bewiesen) Ivabradine Theoretisch sinnvoll (Reduktion Herzfrequenz, Verlängerung Diastolendauer). Datenlage bezüglich Effekt auf Leistungsfähigkeit kontrovers; Einsatz möglich. Kalziumkanalblocker (Dihydropyridine) Theoretisch sinnvoll (Verlangsamung der Herzfrequenz [Isoptin, Dilzem], Verbesserung der Relaxation), aber keine Daten hinsichtlich Prognose. Einsatz aber möglich (nicht kontraindiziert im Gegensatz zur HFrEF) Vorhofflimmern Definition Unkoordinierte Vorhofserregungen mit einer Vorhoffrequenz von /min. Das Oberflächen-EKG zeigt eine absolute Arrhythmie und keine eindeutigen P-Wellen. P-Wellen können allerdings, z. B. bei fibrotisch verändertem linken Vorhof oder unter antiarrhythmischer Therapie (Amiodarone), erkennbar sein. Diese weisen dann eine andere Morphologie als z. B. bei typischem Vorhofflattern auf. Epidemiologie 1 2% der Gesamtbevölkerung sind von Vorhofflimmern (VHF) be troffen. Die Prävalenz steigt mit dem Alter (< 0.5% bei 40- bis 50-Jährigen, 5 15% bei über 80-Jährigen). Ursachen Akut (meist reversibel): Hyperthyreose, Alkohol, Drogen (Kokain), akute Lungenembolie, Katecholamin getriggert (nach Operationen, bei Infekten), bei Myokardinfarkten Chronisch (häufig irreversibel): langjährige arterielle Hypertonie oder Diabetes, Klappenvitien (z. B. Mitralvitien) Genetisch bedingt (derzeit noch Forschungsgegenstand) Amiodarone Rhythmuskontrolle bei Episoden von Vorhofflimmern mit konsekutiven Dekompensationen PD Dr. Micha Maeder Prof. Dr. Hans Rickli Dr. Gian-Reto Kleger Dr. Robert Sieber Dr. Marc Buser
120 Klassifizierung Nicht-valvulär Valvulär: Mitralklappenvitium Erstmanifestation jeder Patient mit erstmals festgestelltem VHF Paroxysmal selbstlimitierend < 7 Tage Persistierend anhaltend > 7 Tage oder Kardioversion < 7 Tage durchgeführt: Rhythmuskontrolle noch möglich Lang anhaltend persistierend anhaltend > 1 Jahr Permanent chronisch: Rhythmuskontrolle nicht mehr möglich oder erwünscht (z. B. Aufwand zur Erhaltung des Sinusrhythmus zu gross) Klinische Graduierung EHRA I Keine Symptome EHRA II Milde Symptome (Alltagsaktivität nicht beeinträchtigt) EHRA III Schwere Symptome (Alltagsaktivität beeinträchtigt) EHRA IV Körperlich behindernde Symptome (Alltagsaktivität nicht mehr möglich) Die wichtigsten Fragen Frequenz- oder Rhythmuskontrolle? Thromboseprophylaxe? Orale Antikoagulation (neue Antikoagulantien [NOAK] oder Marcoumar) nötig? (siehe Tabelle Indikation zur oralen Antikoagulation) Dauer des VHF? < 48 Std.: Konversion ohne antithrombotische Therapie möglich; > 48 Std. oder unbekannt: keine Konversion ohne vorhergehende antithrombotische Therapie (INR 2.0 bis 3.0 über mindestens 3 Wochen, alternativ neue Antikoagulantien [NOAK] oder LMW-Heparin) oder TEE zum Ausschluss intrakavitärer Thromben Unabhängig vom Thromboembolierisiko (CHA2DS2-VASc-Score) ist nach einer Konversion im Sinusrhythmus eine Thromboseprophylaxe für 4 Wochen und nach einer Pulmonalvenenisolation für 3 Monate zwingend. Frequenz- oder Rhythmuskontrolle Alle grossen klinischen Studien zeigen bisher keinen Überlebensvorteil einer Rhythmuskontrolle gegenüber einer Frequenzkontrolle! Aber: Jüngere, symptomatische Patienten waren in allen Studien unterrepräsentiert! Eine Rhythmuskontrolle ist für jüngere oder symptomatische Patienten sinnvoll. Probleme: Wenn Beginn des VHF > 48 Std. (Anam nese oft schwierig), muss vorgängig über 3 Wochen eine OAK (NOAK oder Marcoumar, Ziel-INR 2 3) durchgeführt oder mittels TEE ein Vorhofthrombus ausgeschlossen werden. Bei diffusem Beschwerdebild/Unklarheit, ob Vorhofflimmern für Symptome verantwortlich ist Vorhofflimmern-Ferien durch Kardioversion ± Antiarrhythmikum, um Rezidivwahrscheinlichkeit zu reduzieren und Reevaluation der Symptome im Sinusrhythmus. Klinische Probleme Symptomkorrelation: Bei paroxysmalem VHF werden häufig Palpitationen bemerkt. Bei persistierendem VHF eher unspezifische Symptome (Leistungsintoleranz, Müdigkeit). Patienten mit persistierendem VHF haben jedoch auch häufiger extrakardiale (Hypertonie, OSAS) und kardiale Erkrankungen (KHK, hypertensive Herzkrankheit usw.), sodass die klinische Relevanz von insbesondere normokardem VHF unklar ist. In dieser Situation empfehlen sich «Vorhofflimmer-Ferien»: Elektrokonversion, ggf. vorgängig Amiodaron- Therapie (Reduktion Rezidivwahrscheinlichkeit) und Reevaluation der Symptome im Sinusrhythmus (evtl. Ergometrie vor/nach EKV). Tachykardes VHF: kann zu einer links ventrikulären Dysfunktion führen
121 Tachykardes VHF mit hypertensiven BD-Werten: im Alter sehr schlecht vertragen; oft Ursache einer akuten Herzinsuffizienz (auch ohne relevante strukturelle Herzerkrankung; diastolische Dysfunktion!) Bradykardes VHF: oft von Schwindel und Synkopen begleitet; Cave: Sonderform des Sick-Sinus-Syndroms: «Brady-Tachy-Syndrom» bei medikamentöser Therapie des vermeintlich nur tachykarden VHF (Cave: auch Betablocker-Augentropfen wirken systemisch) Postoperativ erstmalig aufgetretenes VHF (v.a. nach Herzchirur gie): Wertigkeit einer langfristigen antithrombotischen und/ oder antiarrhythmischen Therapie unklar. Sinnvoll sind eine Kardioversion und eine zeitlich limitierte antithrombotische (z. B. 4 Wochen) und evtl. antiarrhythmische Therapie. Anschliessend aktive Suche nach VHF mit Langzeit-EKGs. Asymptomatisches VHF: relativ häufig von TIA und ischämischem Hirnschlag begleitet. Cave: häufig nach Pulmonalvenenisolation (auch bei vormals symptomatischen Patienten) Thromboseprophylaxe nach Pulmonalvenenisolation in Abhängigkeit des CHA2DS2-VASc-Scores weiterführen. Behandlungsstrategien Antithrombotische Therapie? (NOAK oder Marcoumar); Thromboembolie- vs. Blutungsrisiko abwägen Frequenz- oder Rhythmuskontrolle? Indikation zur oralen Antikoagulation (NOAK oder Marcoumar) Risikofaktoren für Stroke und Thromboembolien bei nicht-valvulärem Vorhofflimmern «Major»-Risikofaktoren Klinisch relevante «Non-major»- Risikofaktoren Anamnese für Stroke/TIA oder Thromboembolie Alter 75 Jahre Herzinsuffizienz oder LVEF 40% Art. Hypertonie Diabetes mellitus Weibliches Geschlecht Alter Jahre Gefässerkrankung Risikofaktoren-basierter Approach CHA2DS2-VASc-Score (maximal 9 Punkte, Alter gibt 0, 1 oder 2 Punkte) Risikofaktor Herzinsuffizienz/LV-Dysfunktion 1 Art. Hypertonie 1 Alter 75 Jahre 2 Diabetes mellitus 1 Stroke/TIA/andere Thromboembolie 2 Gefässerkrankung (KHK, PAVK) 1 Alter Jahre 1 Weibliches Geschlecht* 1 Maximaler Score 9 Score Risikokategorie intermediär (CHA2DS2-VASc 1) hoch CHA2DS2-VASc- Score 1** niedrig 0 gar nichts Empfohlene antithrombotische Therapie OAK (NOAK oder Vitamin-K-Antagonist) 240 * Unter 65 Jahren gilt das weibliche Geschlecht nicht als Risikofaktor! ** CHA2DS2-VASc-Score = 1: individuelle Entscheidung, da Embolie- und Blutungsrisiko ähnlich hoch. Bei Entscheid für OAK eher NOAK, da intrakranielles Blutungsrisiko geringer als unter Vitamin-K-Antagonist. Aspirin hat in der Strokeprävention bei Vorhofflimmern keinen Stellenwert mehr. 241
122 Neue Antikoagulantien (NOAK) Gleichwertige Indikation (Class I Level A) zur Thromboembolieprophylaxe bei VHF-Patienten wie Marcoumar. Unterschiede zu Marcoumar Fixe Dosierung, keine Überprüfung des Gerinnungsstatus (INR-Messung) notwendig Rascher Wirkungseintritt Weniger hämorrhagische Strokes Vergleichbare Strokeprävention: Dabigatran 2x 110 mg, Rivaroxaban, Apixaban Signifikante Verringerung ischämischer Strokes: Dabigatran 2x 150 mg, Apixaban Mortalitätsbenefit gegenüber Marcoumar: Apixaban Nachteil Einfluss auf Gerinnungsparameter substanzabhängig und komplex Kein Antidot (kurze HWZ führt rasch zur Rückgewinnung der Hämostase. Hämodialyse bei Dabigatran möglich) «Monitoring» des Patienten nicht möglich Bemerkungen Gerinnung im Notfall: Spiegelbestimmung, Gerinnungsspezialist Tablette vergessen: gleichentags 1 Dosis nachholen, dann wie gewohnt weiter Rivaroxaban: Einnahme nach dem Essen Dosisreduktion (Dabigatran 2x 110 mg oder Rivaroxaban 15 mg/tag) bei: > 80 Jahre Zu erwartende Medikamentenwechselwirkung (z. B. Verapamil) HAS-BLED-Score 3 Niereninsuffizienz 1 CrCl ml/min., NOAK kontraindiziert ab CrCl < 30 ml/min. 2 Protonenpumpen-Inhibitoren (reduzieren Absorption) 3 z. B. Azol-Antimykotika, HIV-Protease-Inhibitoren, 4 Rifampicin 5 Gewicht 60 kg 6 z. B. Dronedaron, Verapamil NI = Niereninsuffizienz Blutungsrisiko: HAS-BLED-Score (untersucht für Blutungsrisiko unter Warfarin!) HAS-BLED-Score 3 = Blutungsrisiko erhöht. Patienten sollen, wenn indiziert, trotzdem antikoaguliert werden (BD-Einstellung optimieren, OAK besser monitorisieren oder auf NOAK wechseln, Alkohol reduzieren etc.). 242 Dosierung NI 1 Dabigatran (Thrombin- Inhibitor) 2x 150 mg 2x 110 mg Rivaroxaban (F. Xa- Inhibitor) 1x 20 mg/tag 1x 15 mg/tag Apixaban (F. Xa- Inhibitor) 2x 5 mg 2x 2.5 mg Edoxaban (F. Xa- Inhibitor) 1x 60 mg 1x 30 mg 5 t1/ Std. 18 Std Std. Elimination renal (80%) hepatisch (2/3) renal (1/3) Interaktionen PPI 2 P-gp-Inhibitoren Periinterven tionelles Mana gement Unterbruch (2 bis 5 d) in Abhängigkeit der Nierenfunktion renal (25%) faecal (75%) starke CYP450-3A4-Inhibitoren 3 oder -Induktoren 4 faecal (60%) renal (35%) P-gp- Inhibitoren 6 Stop and go schneller Wirkungseintritt und kurze HWZ macht Bridging mit LMW-Heparinen unnötig Wie umstellen? Marcoumar auf NOAK: Beginn NOAK, wenn INR 2 Buchstabe Klinisches Charakteristikum Punkte H Art. Hypertonie 1 A Abnorme Nieren*- und Leberfunktion** 1 oder 2 (je ein Punkt) S Schlaganfall 1 B Blutung 1 L Labiler INR 1 E Alter > 65 Jahre 1 D Drogen oder Alkohol (je ein Punkt) 1 oder 2 Max. 9 Punkte * Chronische Dialyse oder Nierentransplantation oder Serumkreatinin 200 µmol/l ** Chronische hepatische Erkrankung oder biochemische Evidenz einer signifikanten hepatischen Störung (z. B. Bilirubin > 2x und ASAT/ALAT > 3x Normwert) 243
123 Vorgehen bei Indikation für Thrombozytenaggregationshemmung und oraler Antikoagulation Bei stabiler KHK (keine Angina pectoris, keine akute Ischämie und/oder Stentimplantation < 12 Monate): OAK (Marcoumar, NOAK), Monotherapie (für NOAK sind prospektive Studien ausstehend) Medikamente zur Frequenzkontrolle Betablocker po, z. B. Bisoprolol (Concor) 5 10 mg iv, z. B. Metoprolol (Beloc) langsam 1-mg-weise iv, Zieldosis 5 mg iv, dann auf po wechseln Ca-Antagonisten (Wenn möglich immer po, da iv negativ inotrop) Cave: schlechte LVEF po, Diltiazem (Dilzem) po 3x 60 mg/tag, später bis 2x 120 mg/tag iv, falls nötig 0.25 mg/kg Bolus iv, evtl. wiederholen, Dauerinfusion 5 15 mg/std (Cave: Herzinsuffizienz). Isoptin immer po geben, max. Dosis 480 mg/tag Kardioversion Elektrisch (EKV) Schnellste und effektivste Konversion des VHF Indiziert bei symptomatischen Patienten mit Symptombeginn < 48 Std. oder suffizienter Antikoagulation 3 Wochen oder hämodynamischer Instabilität EKV (synchronisiert!) in Kurznarkose mit 200 J (biphasisch) Medikamentös Primär oder wenn mit EKV kein Erfolg Alle unten angeführten Antiarrhythmika können bei nicht erfolgreicher EKV angewendet werden. EKV nach Medikamentengabe wiederholen Digoxin (bei Herzinsuffizienz) 0.25 mg Bolus iv, evtl. wiederholen, maximal 1 mg (in 3 Dosen), dann po weiter (Cave: Hypokaliämie, Niereninsuffizienz)
124 Medikamente (Klasse) Ibutilid (Corvert) (III) Amiodaron (Cordarone) (III) Flecainid (Tambocor) (Ic) Vernakalant (Brinavess) Dosis Erfolg Kontraindikationen/Warnhinweise 0.87 mg (1 Amp.) über 10 min. iv Infusion mit gleicher Dosis 10 min. nach Erst infusion möglich mg über 15 min. iv maximal 1'200 mg/24 Std. Langsamer Wirkungseintritt, sicher bei eingeschränkter LV-Funktion 300 mg po (1x) 2 mg/kg über 10 min., maximal 150 mg peroral nach circa 4 Std. wirksam 3 mg/kg iv über 10 min. (2. Dosis nach 15 min.; 2 mg/kg) max. 5 mg/kg/24 Std. ca. 60% ca. 70% ca. 80% QT-Intervall Verlängerung möglich, insbes. bei Hypoka liämie. Proar rhythmierisiko bei Hypokaliämie und -magnesiämie erhöht, deshalb vor Therapie mit Ibutilid Elektro lytkorrektur Keine Dosisanpassung bei Niereninsuffizienz Gabe bei Leberinsuffizienz nicht empfohlen Rhythmusüberwachung über mind. 4 Std. oder bis zum Erreichen des initialen QTc-Intervalls wegen möglicher Torsadesde-pointes-Arrhythmie nötig KI: SA Block, AV-Block II Mobitz Bei Dauertherapie initial INR engmaschig kontrollieren (Interaktion) TSH-Kontrollen KI: KHK, Herzinsuffizienz Bei Dauertherapie immer mit Betablocker kombinieren, da im Falle von Konversion in Flattern 1:1-Überleitung möglich KI: hämodynamische Instabilität, NYHA III/IV, ACS, schwere Aorten stenose, BDsys < 100 mmhg, QT > 440 ms, AV-Block II (Mobitz) Blutdruck und Herzfrequenzabfall, v.a. während/bis 15 min. nach Infusionsende möglich (häufiges BD-Monitoring!): Therapieabbruch unabhängig von Symptomen Mögliche EKG-Veränderungen: Sinusbradykardie/-Pausen, SA-/AV-/Schenkelblockierungen, QRS-, QT-Intervall Verlängerungen Keine Dosisanpassung bei Nieren-/Leberdysfunktion, ältere Patienten Rhythmusüberwachung über 2 Std. Medikamente zur Rhythmuskontrolle Keine strukturelle Herzerkrankung Betablocker Antiarrhythmika: Flecainid (Tambocor) 2x mg po immer mit Betablocker kombinieren 2 Sotalol (Sotalex) 2x mg po (Cave: Torsaden bei Hypokaliämie und QTc-Verlängerung, Niereninsuffizienz) Dronedarone (Multaq) 2x 400 mg po. Nur bei paroxysmalem VHF (Cave: Lebertoxizität, Kontrolle der Transaminasen erforderlich, KI bei linksventrikulärer Dysfunktion, NYHA III/IV und instabilen Patienten) Strukturelle Herzerkrankung Antiarrhythmika: Amiodaron (Cordarone) Sotalol (Sotalex) 2x mg po (falls keine Herzinsuffizienz und keine Niereninsuffizienz vorhanden; Cave: erhöhtes Risiko von Torsades de pointes bei Hypokaliämie und QTc-Verlängerung) Dronedaron (Multaq) 2x 400 mg po (siehe oben) Ablationsbehandlung bei Vorhofflimmern (mit Rhythmologen besprechen) Pulmonalvenenisolation (PVI) Symptomatisches Vorhofflimmern oder NW der Antiarrhythmika- Therapie Grundsätzlich bessere Erfolgsrate bei paroxysmalem VHF und je weniger strukturelle Herzerkrankung vorhanden 2 Vorhofflimmern kann durch Flecainid in Vorhofflattern organisieren und 1:1 auf die Ventrikel übergeleitet werden, was hämodynamisch häufig schlecht vertragen wird bzw. Kammerflimmern induzieren kann
125 Langzeiterfolg etwa 70%; ca. 20% der Patienten benötigen aber Zweit- oder Drittinterventionen; Komplikationsrate: insgesamt 2 3%; Leistenkomplikationen (Hämatom, AV-Fistel, Pseudoaneurysma) 1 2%; TIA/Insultrate 1%, Perikardtamponade < 1%, Oesophagusverletzung < 0.25% 3, Pulmonalvenenstenose < 0.5% (Symptome oft Monate nach PVI: Dyspnoe, Husten, Hämoptysen, rez. Pulmonale Infekte) Vorteil: wenn erfolgreich, im Verlauf keine Antiarrhythmika mehr notwendig; OAK jedoch in Abhängigkeit des CHA2DS2-VASC-Scores trotzdem notwendig Erhaltung des Sinusrhythmus bei Vorhofflimmern Relevante Herzkrankheit vorhanden Herzinsuffizienz KHK art. HT mit Hypertrophie Keine oder minimale Herzerkrankung (inkl. art. HT ohne Hypertrophie) VHF paroxysmal VHF persistierend AV-Knoten-Ablation nach vorgängiger Schrittmacherimplantation Nach Implantation eines Schrittmachers wird der AV-Knoten abladiert. Geeignet für ältere Patienten mit Nebenwirkungen der Antiarrhythmika-Therapie oder Tachykardie-Bradykardie-Syndrom (frequenzsenkende Medikamente sollen tachykarde Episoden verhindern, führen aber zu Bradykardien und AV-Über leitungsstörungen) Vorteil: Effektive Frequenzkontrolle; Antiarrhythmika können abgesetzt werden Nachteil: Schrittmacherabhängigkeit, dyssynchrones Pacing im RV, deshalb bei EF < 40% vor Knoten-Ablation CRT-Implantation nötig Sotalol Dronedaron Dronedaron AF-Katheterablation Dronedaron Flecainide Propafenon Sotalol Hybridtherapie Darunter versteht man eine rechtsatriale Isthmusablation bei Vorhofflattern, wenn Vorhofflimmern unter medikamentöser Therapie zu einem Vorhofflattern organisiert 3 Symptome Tage bis Wochen nach PVI, bedingt durch Luftembolie, Bakterämie: Fieber/ Sepsis, Insult, Schluckbeschwerden Computertomografie. KEINE Gastroskopie (Luftembolie)! Hohe Letalität. Rasches Handeln, Antibiose inkl. Abdeckung Gram-Keime. Rhythmologen involvieren. Amiodaron Prof. Dr. Peter Ammann Dr. David Altmann Dr. Dr. Roman Brenner Dr. Giulia Domenichini AF-Katheterablation Amiodaron
126 Supraventrikuläre Rhythmusstörungen Reentry-Tachykardien AV-Knoten-Reentry (AVNRT) Schmalkomplextachykardie, Schenkelblockaberranz möglich AV-Reentrytachy (AVRT) WPW: antegrad leitende akzessorische Bahn (Delta-Welle im Sinusrhythmus (evtl. erst bei höheren Herzfrequenzen sichtbar!) Orthodrome Tachykardie möglich (antegrad über AV-Knoten): Schmalkomplextachykardie, Schenkelblockaberranz Antidrome Tachykardie (antegrad über akzessorische Bahn): Breitkomplextachykardie Concealed WPW: nur retrograd leitende akzessorische Bahn (keine Delta-Welle im Sinusrhythmus) Nur orthodrome Tachykardie möglich: Schmalkomplextachykardie Vorhofflattern Typisch = cavotrikuspidal-gängig (rechtsatrial): meist counterclockwise (negative P-Wellen i.d. inferioren Ableitungen) Atypisch = nicht cavotrikuspidal-gängig (rechts- oder linksatrial). Häufig nach linksatrialer Intervention (Katheter oder chirurgisch), operativ korrigierte kard. Vitien Atriale Tachykardie (fokal, multifokal, mikroreentry): P-Wellenmorphologie anders als im Sinusrhythmus (z. B. negativ in den inferioren Ableitungen): Schmalkomplextachykardie, Schenkelblockaberranz möglich AVNRT, atriale Tachykardie, Vorhofflimmern, Vorhofflattern bei akzessorischer Bahn: Tachykardie wird antegrad über akzessorische Bahn geleitet: Breitkomplextachykardie
127 Klinische Präsentation Palpitationen, Panikattacke, Schwindel, Angina pectoris, Synkope Differentialdiagnostik supraventrikuläre Tachykardie (SVT) und Therapiemassnahmen Anamnese Seit wann, wie oft, Start/Ende, Dauer: plötzlicher Beginn und Ende (On-/Off-Phänomen), Klopfen im Hals («frog sign»: atriale Kontraktion gegen geschlossene AV-Klappen), Terminierung durch vagale Manöver bei Reentry-Tachykardien. Atriale Tachykardie: plötzlicher oder allmählicher Start/Ende. Adenosin unterbricht Reentry-Tachykardie, selten auch atriale Tachykardie Immer Dokumentation der Tachykardie mit 12-Ableitungs-EKG anstreben. EKG-Dokumentation aller Massnahmen während Tachykardie: vagale Manöver, bei Auftreten/Verschwinden von Schenkelblöcken oder der Injektion von Antiarrhythmika SV-Tachykardie ja Regelmässig? ja Sichtbare P? ja Mehr P als R? ja Vorhofflattern oder atriale Tachykardie nein nein nein RP-Intervall AVNRT Vorhofflimmern, atriale Tc oder Vorhofflattern mit unregelmässiger Überleitung, multifokale atriale Tachykardie RP-Intervall kurz RP-Intervall AVRT, atyp. AVNRT, atriale Tc Therapie allgemein Kreislaufmässig instabil: Elektrokonversion J Stabil Vagale Manöver Adenosin 6 12 mg iv schnell in herznahe Vene und Nachspülen mit ml NaCl (KI Asthma) Isoptin 2 ml (5 mg) verdünnt auf 10 ml NaCl langsam iv (Cave: WPW-Syndrom) Breitkomplextachykardie: im Zweifel Cordarone ( mg über Min. iv) oder EKV. Keine AV-Knoten bremsenden Medikamente bei SVT mit antegrader Leitung über akzessorische Bahn (siehe nächste Seite)
128 AV-Knoten-Reentry-Tachykardie Häufigste paroxysmale SV-Tachykardie. Plötzlicher Beginn/Ende, meist belas tungsunabhängig. Im EKG kein oder retrogrades P im Endteil des QRS-Komplex (dadurch in inferioren Ableitungen negatives P und in V1 r «pseudo-inkompletter RSB»). Nach Konversion in SR (kein «inkompletter RSB» mehr nachweisbar) Orthodrome AV-Reentry-Tachykardie Schmalkomplextachykardie: WPW-Syndrom, wenn Delta-Welle im Sinusrhythmus AVNRT mit retrogradem P in V1 («pseudo RSB»), sehr kurze RP-Zeit < 70 ms Akute Therapie: vagale Manöver, Krenosin 6 12 mg iv (zentrale Vene, rasch NaCl nachspritzen), Verapamil, Diltiazem Chronische Therapie: Katheterablation (Erfolgsrate > 95%, Risiko (kompletter AV-Block) < 1%, Betablocker, Ca-Antagonisten, IC oder Klasse III Antiarrhythmika 254 Orthodrome AVRT mit RP > 70 ms 255
129 Plötzlicher Beginn, nicht selten bei körperlicher Belastung. EKG: retrogrades P, abgesetzt vom QRS-Komplex, RP > 70 ms (RP länger als bei AVNRT, deshalb P im 12-Kanal-EKG häufiger erkennbar) Akute Therapie: vagale Manöver, Krenosin 6 12 mg iv (zentrale Vene, rasch NaCl nachspritzen), Verapamil, Diltiazem Chronische Therapie: Katheterablation (Erfolgsrate > 95%, Risiko kompletter AV-Block bei parahissärer Bahn), Betablocker, Klasse 1C oder III AA Vorhofflimmern, das über die akzessorische Bahn übergeleitet wird (FBI fast broad irregular) Antidrome AV-Reentry-Tachykardie (Breitkomplextachykardie, da volle Präexzitation = ventrikuläre Erregung über akzessorische Bahn, kein typischer Schenkelblock) WPW mit schnell übergeleitetem Vorhofflimmern Hämodynamisch stabil: Amiodaron (Cordarone) 150 mg iv Keine AV-Knoten bremsenden Medikamente, da dann mehr Impulse über die akzessorische Bahn geleitet werden, was zu Kammerflimmern führen kann (Bahn hat keine bremsenden [decrementalen] Eigenschaften wie der AV-Knoten) instabil: EKV 200 J Atriale Tachykardie Antidrome AVRT mit RP > 70 ms Plötzlicher Beginn. EKG: immer Breitkomplextachykardie retrogrades P, abgesetzt vom QRS-Komplex, RP > 70 ms Akute Therapie: vagale Manöver, Amiodaron (Cordarone) 150 mg iv, Elektrokonversion Chronische Therapie: Katheterablation, Klasse IC oder III AA 256 Vorhoftachykardie mit wechselnder Überleitung 257
130 Schrittmachertherapie Gleiche atriale Tachykardie nun mit 1:1-Überleitung, z. B. bei körperlicher Belastung Häufig kein klarer Beginn, meist lang dauernde Tachykardien, die medikamentös schwer therapierbar sind EKG: RP variabel (P meist gut sichtbar, andere Morphologie als im Sinusrhythmus) Akute Therapie: vagale Manöver, Adenosin, Verapamil, Diltiazem, IC oder III AA Chronische Therapie: Katheterablation, Betablocker, Verapamil, IC oder III AA Prof. Dr. Peter Ammann Dr. David Altmann Dr. Dr. Roman Brenner Dr. Giulia Domenichini Indikationen zur Schrittmachertherapie (ESC-Guidelines 2007, Auswahl) AV-Blockierungen (erworben) Klasse I asymptomatischer AV-Block III oder AV-Block II Typ Mobitz 2 Chronisch symptomatischer AV-Block II (Typ I + II) oder III AV-Block II oder III bei neuromuskulären Erkrankungen wie Kearns-Sayre-Syndrom, muskulären Dystrophien usw. Bifaszikulärer Block mit intermittierendem AV-Block III oder AV-Block II Typ Mobitz II (2:1-Block oder höhergradig) Wechselnde Schenkelblockbilder Klasse IIa AV-Block II Typ Wenckebach mit Symptomen oder infrahisärer Blockierung Asymptomatischer AV-Block II (Typ I und II) oder III Synkope bei bifaszikulärem Block ohne Nachweis eines AV-Blocks und Ausschluss anderer Ursachen wie Kammertachykardie AV-Blockierung jeden Grades bei neuromuskulären Erkrankungen AV-Block I (PQ>300 ms) mit Symptomen eines Schrittmachersyndroms Sinusknoten-Erkrankung Klasse I Symptomatische Bradykardie mit oder ohne Tachykardie, spontan oder unter notwendiger Therapie (dokumentiert z. B. mit 24h-EKG) Synkope ohne andere Erklärung und verlängerte Sinusknoten-Erholungszeit (> 800 ms) in einer elektrophysiologischen Untersuchung 258 Karotissinus-Syndrom Klasse I Rezidivierende Synkopen durch unbeabsichtigte Stimulation des Karotissinus (z. B. Kopfbewegungen, Rasieren), reproduzierbar durch 259
131 Karotis-Massage mit konsekutiver Asystolie von > 3 Sek. ohne Medikation mit möglicher Beeinflussung des Sinusknotens Klasse IIa Rezidivierende, nicht erklärbare Synkopen ohne unbeabsichtigte Stimulation des Karotissinus, aber reproduzierbar durch Karotis- Massage, verbunden mit Asystolie von > 3 Sek. Vasovagale Synkope Klasse I Keine Klasse IIa Patienten > 40 Jahre mit häufigen (> 5 / Jahr), schweren vasovagalen Synkopen mit Verletzungsfolgen bei nachgewiesener längerer Asystolie und Unwirksamkeit anderer Therapiemassnahmen Patienten mit Synkope und asymptomatischer Pause > 6 Sek. Klassifizierung der Indikationen Klasse I Evidenz und allgemeiner Konsens, dass eine Massnahme nützlich und effizient ist Klasse IIa Überwiegende Evidenz für Nutzen und Effizienz Klasse IIb Fragliche Evidenz für Nutzen und Effizienz Differenzierte Schrittmachertherapie AV-Block zweiten und dritten Grades Sinusknoten normal: VDD, DDD Sinusknotendysfunktion: DDDR Bei seltener Blockierung: DDD-AV, VDD-AV (VVI mit tiefer Hysterese) Sinusknoten-Erkrankung Normale AV-Leitung: AAI(R) Bei AV- oder intraventrikulärer Leitungsstörung: DDD(R)-AV Bei seltenen Pausen: (VVI mit tiefer Hysterese) 260 Bradykardes Vorhofflimmern: VVIR Karotissinus-Syndrom: DDI (VVI) Berücksichtigen: biologisches Alter, Lebensumstände Andere Indikationen Neurogene kardiale Synkope (kontrovers) (DDI) Herzschrittmachercode (ICHD) «Inter-Society Commission for Heart Disease Resources» 1. Stelle Ort der Stimulation 2. Stelle Ort der Wahrnehmung 3. Stelle Betriebsart V = Ventrikel V I = inhibiert A = Atrium D = dual (V+A) S = single A D S T = getriggert D = inhibiert oder getriggert 4. Stelle Programmierbarkeit M = > 3 Funktionen programmierbar R = Frequenzadaptation O = nicht programmierbar 5. Stelle Antitachykardiefunktion VVIR = Ventrikelschrittmacher, frequenzadaptiert; DDM = Zweikammerschrittmacher ohne Frequenzadaptation; DDD-AV = Programmierung zur Erhaltung der AV-Überleitung (z. B. AV-Hysterese, DDD-AAI-Moduswechsel), um rechtsventrikuläre Stimulation zu minimieren Prof. Dr. Peter Ammann Dr. David Altmann Dr. Dr. Roman Brenner Dr. Giulia Domenichini 261
132 Kammertachykardien Einteilung der Kammertachykardien Idiopathisch: keine strukturelle Herzkrankheit Ausflusstrakttachykardie, faszikuläre Kammertachykardie I.R. struktureller Herzkrankheiten: KHK, dilatative Kadiomyopathie (häufig Bundle-Branch-Reentry-Tachykardie), ARVC, HOCM Ionenkanalstörung: Long-QT-, Brugada-Syndrom (i.r. Torsadesde-pointes-Tachykardien) Klinisch: stabil, instabil Zeitlich: anhaltend (> 30 Sek.), nicht anhaltend (Definition mindestens 3 VES > 100 bpm und < 30 Sek.) Morphologisch: monomorph, polymorph Pathophysiologisch: Reentry (KHK), getriggerte Automatizität (Intoxikationen, kongenitale Vitien) Merke Bei bekannter KHK oder Kardiomyopathie ist eine Breitkomplextachykardie mit > 80% Vortestwahrscheinlichkeit eine Kammertachykardie Unregelmässige Breitkomplextachykardien sind immer verdächtig auf Vorhofflimmern mit Schenkelblock oder Schenkelblockaberration Ausflusstrakttachykardien (oder ventrikuläre Extrasystolen) betreffen typischerweise «herzgesunde» junge Patienten und zeigen eine typische Morphologie im EKG: LSB mit inferiorer Achse, R/S-Umschlag bei V3 oder später bei rechtsventrikulärem Fokus bzw. bei linksventrikulärem Fokus besteht häufig ein früherer R/S-Umschlag (V1/V2). Das Ruhe-EKG ist normal. Es sollte eine Bildgebung mit Frage nach arrhythmogener rechtsventrikulärer Kardiomyopathie (ARVC) erfolgen (Echokardiografie oder MRI), da ventrikuläre Tachy kardien i.r. dieser Erkrankung eine ähnliche Morphologie aufweisen können Häufige Extrasystolen aus dem Ausflusstrakt können zu einer linksventrikulären Dysfunktion führen
133 VT Algorithmus nach Vereckei et al EHJ 2007 Morphologie-Kriterien RSB: KT Schritt 1: AV Dissoziation ja KT nein V1 V6 Schritt 2: R Zacke in avr ja KT VT nein Monophasisches V1 Tiefes S in V6: Ratio R/S < 1 Schritt 3: QRS Morphologie (nicht RSB,LSB) ja KT nein Schritt 4: vi/vt 1 ja KT LSB: KT nein SVT > 300 ms VT V1 2 Kleines R V6 nach Kerbe in S-Zacke vi = 0.8 vt = 0.2 vi > vt SVT vi = initiale ventrikuläre Aktivierungsgeschwindigkeit (in den ersten 40 ms). Vi wird in einem bi- oder multiphasischen QRS-Komplex gemessen und zwar in dem Komplex, wo die initiale ventrikuläre Aktivierung am schnellsten ist. vt = terminale ventrikuläre Aktivierungsgeschwindigkeit (in den letzten 40 ms). Kerbe > 100 ms, wenn keine Antiarrhythmika Jedes Q in V
134 RSB: SVT Bazett-Formel RR = 0.83 Sek. V1 V6 SVT RSB QT = 0.52 Sek. LSB: SVT QTc = unkorr. QT = 0.52 = 0.57 RR 0.83 Normal: Sek. Pathologisch: > 0.46 Sek. (Frauen) Kleines R SVT Steile S-Zacke V1 2 V6 LSB Kleines Q Ursache Pathologische QT-Verlängerung (Bild vorherige Seite) durch Häufig: medikamentös bedingt (z. B. Sotalol, Makrolide, Methadon, Antihistaminika usw., verstärkt durch Hypokaliämie und Hypomagnesiämie) Selten: genetisch bedingte, familiäre Formen der QT-Verlängerung (Familienanamnese?) 266 Therapie der Kammertachykardie Instabil: Elektrokonversion (EKV) 150 oder 200 J Stabil: Amiodaron (Cordarone) 150 mg langsam iv (Cave: bei schlechter Pumpfunktion EKV sicherer!) Reservemedikation: Procainamid (Pronestyl) Ladedosis mg (langsam über min i.v.) (Cave: Niereninsuffizienz, schlechte Pumpfunktion oder Hypotonie) 267
135 Idiopathische Kammertachykardie: vagale Manöver, Adenosin oder Verapamil, wenn hämodynamisch stabil. Sonst EKV und/oder Amiodaron. Rezidivprophylaxe mit Verapamil oder Betablocker. Radiofrequenzablation hat gute Langzeiterfolgsrate (> 90%) Therapie der Torsades-de-pointes-Tachykardie Instabil: Elektrokonversion J Stabil: Verursachende Medikamente stoppen Magnesium (2 g langsam iv) und gegebenenfalls Kalium substituieren (Ziel: Serumkalium > 4.0 mmol/l) Gegebenenfalls Überstimulation mit provisorischem PM Familiäre Formen: Betablocker und gegebenenfalls ICD-Implantation Rezidivprophylaxe akut: Provisorischer PM mit tachykarder Stimulation (verkürzt QT-Zeit) Rezidivprophylaxe chronisch: Vermeidung QT-verlängernde Medikamente Rigorose Fiebersenkung Familiäre Formen: Betablocker und gegebenenfalls ICD-Implantation Prof. Dr. Peter Ammann Dr. David Altmann Dr. Dr. Roman Brenner Dr. Giulia Domenichini ICD und CRT ICD (implantable cardioverter defibrillator) Allgemeine Bemerkungen Wird meist pectoral links implantiert (selten rechts oder abdominal) Soll bei operativen Eingriffen in Nähe des Devices abgeschaltet werden Kontraindikation für MR-Untersuchungen Die Tachy-Funktion des ICD kann mit einem Magneten, der auf das ICD-Aggregat gelegt wird, unterdrückt werden (z. B. beim elek - trischen Sturm). Die Defibrillationsenergie liegt zwischen 30 und 40 Joules und kann wegen des Hautwiderstandes des Patienten andere Personen nicht elektrisieren. Indikation Defibrillator meist links pectoral implantiert
136 Primärprophylaxe St. n. Myokardinfarkt (> 40 Tage nach Infarkt) und EF 35% oder 40% mit anhaltender KT in elektrophysiologischer Untersuchung Dilatative Kardiomyopathie ohne reversible Ursache mit EF 35% Sekundärprophylaxe Überlebter Herzstillstand nach Kammertachykardie oder Kammerflimmern ohne reversible Ursache Anhaltende Kammertachykardie (> 30 Sek.) ohne reversible Ursache Synkopen oder anhaltende KT in elektrophysiologischer Untersuchung Spezielle Indikationen: in gewissen Fällen bei rechtsventrikulärer Dysplasie, Ionenkanalmutationen (Long-QT-Syndrom, Brugada), hypertropher Kardiomyopathie oder Sarkoidose. Kardiale Resynchronisation (CRT cardiac resynchronization therapy) Behandlung der Herzinsuffizienz mittels Herzschrittmachertherapie. Prinzip: Der aufgrund eines Linksschenkelblocks dyssynchrone linke Ventrikel wird durch linkslaterale epikardiale Stimulation (über Sinus coronarius) «resynchronisiert». Indikationen Klasse I Sinusrhythmus, LVEF 35%, Linksschenkelblock > 130ms unter ausgebauter medikamentöser HI-Therapie, (oder 150 ms bei anderen Blockbildern mit echokardiografisch nachgewiesener Dyssynchronie) Indikation für RV-pacing (z. B. AV-Block III) und LVEF 40% Problemfall «Elektrischer Sturm» Definition Mehrere Schockabgaben wegen anhaltender oder rezidivierender Kammertachykardie/Flimmer-Episoden. Therapie Am wichtigsten ist die sofortige, sehr starke Sedation; Elektrolyte auf hochnormale Werte (Serumkalium > 4 mmol/l, evtl. Magnesium iv). Antiarrhythmikum Amiodaron (Cordarone) 150 mg langsam iv, Betablocker. Evtl. Anheben der Grundfrequenz mittels PM (Überstimulation des Triggers, z. B. VES), intra-aortale Ballonpumpe, Intubation. Behebung der Ursache: myokardiale Ischämie: Revaskularisation; getriggerte/fokale Arrhythmie (z. B. ventrikuläre Extrasystole, Narben- Reentry): elektrophysiologische Untersuchung/Ablationstherapie. ECG: lead V1? R-S ratio 1 nein ECG: lead I R-S ratio 1 nein Right ventricular pacing = loss of left ventricular pacing Sensitivität 94% (CI ) Spezifität 93% (CI ) ja ja Left ventricular capture Left ventricular capture Der Algorithmus gilt nur bei vorbestehendem LSB und fixem biventrikulärem pacing (nicht bei Algorithmen, welche intrinsische Überleitungen [Fusion pacing)] zulassen)
137 Klasse IIa Sinusrhythmus, LVEF 35%, Nicht-Linksschenkelblock > 150 ms unter ausgebauter medikamentöser HI-Therapie Vorhofflimmern, LVEF 35%, NYHA III, QRS > 130 ms Geplante AV-Knotenablation und linksventrikuläre Funktion 35% Management von ICD-/CRT-D-Geräten vor Operationen/Interventionen mit elektromagnetischer Interferenz Defibrillator (ICD oder CRT-D) ja Magnetauflage während OP möglich (PM zugänglich)? ja CRT-System? nein Eigenrhythmus vorhanden? ja Magnet auf ICD legen und fixieren nein nein ja nein Siehe flowchart PM Umprogrammieren (Ausschalten Antitachyfunktion, evtl. asynchroner Modus) Eigenrhythmus vorhanden? à siehe Prämedikationsvisite oder Rhythmus-Ambi Evtl. umprogrammieren auf DOO, wenn verfügbar, ansonsten Monopolar Kautern verboten Nur für einige Sek. Kautern (z. B. 5 Sek.), dann einige Herzschläge abwarten (ca. 10 Sek.) Biventrikulärer Schrittmacher mit ICD-Elektroden im rechten Atrium, im rechten Ventrikel und in der posterolateralen Vene des Sinus coronarius (für LV-Stimulation) EKG sorgfältig beobachten, bei Problemen frühzeitig DA Kardiologie involvieren Prof. Dr. Peter Ammann Dr. David Altmann Dr. Dr. Roman Brenner Dr. Giulia Domenichini
138 Endokarditis zum Inhaltsverzeichnis Endokarditis-Prophylaxe Patient mit höchstem Endokarditis-Risiko, d.h. mit Klappenersatz (mechanische / biologische Prothese oder Homograft) und -rekonstruktion mit Fremdmaterial St. n. Endokarditis kongenitale Herzerkrankungen zyanotische Vitien korrigierte Vitien mit implantiertem Fremdmaterial während der ersten 6 Monate sowie dauerhaft bei Residualdefekten an oder nahe bei prothetischen Patches oder Prothesen (Verhinderung der Endothelialisierung) Ventrikelseptumdefekt und persistierender Ductus arteriosus Eingriff Zähne, Kiefer, Respirationstrakt? Manipulation gingivaler Sulcus/ periapikale Region** Perforation der oralen Schleimhaut** Tonsillektomie, Adenektomie Inzision der Mucosa Biopsieentnahme Eingriff Gastrointestinal-/ Urogenitaltrakt und Gynäkologie Elektiver Abdominal-Eingriff (Ersatz der bei fehlendem Endokarditisrisiko üblichen Prophylaxe) Bei Urogenitaleingriffen nur, wenn eine Infektion vorliegt Bei endoskopischen Eingriffen ebenfalls nur, falls eine Infektion vorliegt Eingriff Haut An infizierten Gewebeteilen (z. B. Abszess) Dosierungen für normale Nieren- und Leberfunktion! 60 Min. vor Eingriff als Einzeldosis Amoxicillin 2 g po oder iv Alternativ: Cefuroxim-Axetil 1 g po oder Clindamycin 600 mg po/iv oder Cefazolin 1 g iv oder Vancomycin gewichts adaptiert 20 mg/kg KG iv 60 Min. vor Eingriff als Einzeldosis (Enterokokken!) Amoxicillin/Clavulansäure 2.2 g iv oder Piperacillin/Tazobactam 4.5 g iv Alternativ: Vancocin gewichtsadaptiert 20 mg/kgkg iv + Aminoglykosid (Tobramycin 4 mg/kgkg) oder Ciprofloxacin (400 mg iv) (abhängig von Nierenfunktion), und bei Abdominal-OP/Gynäkologie allenfalls zusätzlich Metronidazol 500 mg 60 Min. vor Eingriff (S. aureus + Streptokokken) Amoxicillin/Clavulansäure 2 g po oder 2.2 g iv Alternativ: Cefuroxim-Axetil 1 g po oder Clindamycin 600 mg po/iv oder Cefazolin 1 g iv oder Vancomycin gewichts adaptiert 20 mg/kg KG iv Weitere Therapie abhängig von Infektion nach Eingriff fortführen! Basierend auf den schweizerischen Richtlinien für die Endokarditis-Prophylaxe ** z. B. Extraktion, intraligamentäre Anästhesie, paradontale Therapie, Zahnsteinentfernung
139 276 Wann muss man an eine Endokarditis denken? Grundsätzlich bei Fieber/Sepsis ohne Fokus, speziell bei positiven Blutkulturen und folgenden Zusatzkriterien: Neues Herzgeräusch (Cave: ältere Berichte bezüglich vorbeschriebener Geräusche durchsehen: wirklich «neu»?) Embolische Ereignisse B-Symptomatik über Wochen (Biologische und mechanische) Klappenprothesen, schwer verkalkte native Klappen Endovaskuläre Fremdkörper Mindestens 3 Blutkulturen sollten bei akuter Klinik mit Abstand von 30 Minuten erfolgen (bei schleichender Klinik und stabilem AZ allenfalls sogar mit Abstand von 12 Std.); zudem bei bestehendem Fieber VOR Beginn einer Antibiotikatherapie. Modifizierte Duke-Kriterien für die Diagnose einer infektiösen Endokarditis 2 MAJOR-Kriterien Blutkulturen typische Erreger für eine IE in 2 getrennten Blutkulturen: S. viridans, S. gallolyticus (früher bovis), Bakterien der HACEK-Gruppe, S. aureus oder mit einer IE vereinbare Erreger: mindestens zwei positiven Blutkulturen im Abstand von 12 Std. (oder 3 bzw. die Mehrheit von 4 Blutkulturen positiv) oder eine positive Blutkultur für Coxiella burnetii oder Phase-I-igG-Antikörper-Titer von > 1:800 Bildgebung für IE positive Echokardiografie (Vegetation, Abszess/ Pseudoaneurysma, neue Dehiszenz einer Klappenprothese) pathologische Aktivität um eine Klappenprothese in 18F-FDG PET/ CT oder mit radioaktiv markierten Leukozyten SPECT/CT paravalvuläre Läsion im Herz-CT MINOR-Kriterien Prädisposition: kardial (z. B. Klappenprothese), intravenöser Drogenkonsum Fieber (> 38.0 ºC) Vaskuläre Phänomene: arterielle Embolien, septische Lungeninfarkte, mykotische Aneurysmata, intrakranielle Blutungen, konjunktivale Blutungen, Janeway-Läsionen Immunologische Phänomene: Glomerulonephritis, Osler-Knötchen, Roth-Flecken, positiver Rheumafaktor Mikrobiologie: positive Blutkultur, die kein Major-Kriterium erfüllt, oder serologischer Hinweis auf aktive Infektion mit einem möglichen Erreger für eine IE Definitive Diagnose einer IE 2 Major-Kriterien oder 1 Major- und 3 Minor-Kriterien oder 5 Minor-Kriterien Diagnose einer IE möglich 1 Major- und 1 Minor-Kriterium oder 3 Minor-Kriterien Echokardiografie Indikation für eine transthorakale Echokardiografie (TTE) bei Verdacht auf eine infektiöse Endokarditis (IE) 2,3 Klinischer Verdacht auf IE (insbesondere mit positiven Blutkulturen oder bei neuem Herzgeräusch) (IB) Bakteriämie mit Staphylococcus aureus (IIaB) (wegen hoher Virulenz Häufung von IE) oder persistierende Bakteriämie mit Endokarditistypischen Erregern 277
140 Keine Indikation: Transientes Fieber ohne Nachweis einer Bakteriämie oder eines neuen Herzgeräusches Transiente Bakteriämie mit einem für eine IE atypischen Keim (typische Keime s.o.: Duke-Kriterien) und/oder bei nachgewiesener nicht-endo vaskulärer Infektionsquelle Indikation für eine transösophageale Echokardiografie (TEE) bei Verdacht auf IE 2,3 Persistierend hoher V.a. eine IE trotz negativem TTE (IB) I.d.R. bei positivem TTE-Befund zum Ausschluss lokaler Komplikationen (IIaC) Indikation für eine Wiederholung des TTE/ TEE im Verlauf einer IE 2,3 Neue Komplikationen (z. B. neues Geräusch, Embolie, persistierendes Fieber, Herzinsuffizienz, Abszess, AV-Block) (IB) Bei Abschluss der antibiotischen Therapie (IC) Im Verlauf zur Detektion stummer Komplikationen in Abhängigkeit von Vorbefunden, Keim und klinischem Ansprechen (IIaB) Grundlegende Indikationen für einen chirurgischen Eingriff bei linksseitiger IE 2 1. Herzinsuffizienz schwere akute Klappeninsuffizienz, -obstruktion oder -fistel mit refraktärem Lungenödem oder kardiogenem Schock (IB) schwere Klappeninsuffizienz oder -obstruktion mit Herzinsuffizienz oder echokardiografisch hämodynamischer Relevanz (IB) 2. Unkontrollierte Infektion Lokal unkontrollierte Infektion (Abszess, falsches Aneurysma, Fistel, grössenprogrediente Vegetation: IB) Infektion durch Pilze oder multiresistente Keime (IC) Positive Blutkulturen trotz adäquater antibiotischer Therapie (IIaB) Prothesen-assoziierte IE durch Staphylokokken oder nicht-hacek gramnegative Bakterien (IIaC) 3. Vermeiden von Embolisation Persistierende Vegetation > 10 mm mit mindestens einer Embolie trotz adäquater antibiotischer Therapie (IB) Vegetation > 10 mm und assoziiert mit schwerer Klappeninsuffizienz oder -stenose, niedriges OP-Risiko (IIaB) Vegetation > 30 mm (IIaB) Vegetation > 15 mm und keine andere OP-Indikation (IIbC) Generell grosszügige und frühzeitige Diskussion im «Heart Team» (unter Einbezug von Infektiologie, Herzchirurgie und Kardiologie, bei Bedarf auch anderen Subdisziplinen)! Dr. Katia Boggian Dr. Niklas Ehl PD Dr. Alberto Weber 1 Flückiger U et al. Kardiovaskuläre Medizin 2008;11(12): Habib G et al ESC Guidelines for the management of infective endocarditis. Eur Heart J Nov 21;36(44): Douglas PS et al. Appropriate Use Criteria of Echocardiography. J. Am Soc Echocardiogr Mar;24(3):
141 Valvuläre Herzerkrankungen Aortenklappenstenose (AS) Degenerative, rheumatische oder kongenitale Verengungen der Aortenklappe mit Obstruktion des Blutflusses aus dem linken Ventrikel in die Aorta. Prävalenz steigt mit Alter (2 7% bei Bevölkerung > 65a; 12% > 75a) Ätiologisch v.a. Degeneration (80%), insbesondere bei bikuspiden Klappen (1 2% der Bevölkerung) Prognose Asymptomatisch (bei älteren Patienten schwierig zu erfassen, siehe Diagnostik): jährliche Inzidenz des plötzlichen Herztodes < 1%. Ereignisfreies Überleben innert 2 Jahren jedoch nur 20 50%! Sobald symptomatisch (s. Diagnostik): jährliche Inzidenz des plötzlichen Herztodes 8 34%. 5-Jahres-Überleben 15 50%. Mortalität unter medikamentöser Therapie bei inoperabler, symptomatischer, schwerer Aortenstenose im PARTNER Trial 50% in einem Jahr. Diagnostik Anamnese: belastungsinduzierte Symptome wie Dyspnoe (NYHA I-IV), Angina Pectoris (CCS I-IV), aber auch Schwindel und Synkopen unter Belastung. Im Alter oft unspezifische Symptome wie Ermüdbarkeit und Zeichen der Herzinsuffizienz. Schwierig ist die Situation bei Patienten mit geringer körperlicher Aktivität (s.u.). Klinische Befunde: raues mid- bis spätsystolisches crescendo-decrescendo-geräusch mit p.m. im 2. ICR rechts, fortleitend in die Carotiden (Lautstärke des Geräusches korreliert nicht mit dem Stenosegrad). 2. Herzton bei schwerer AS oft fehlend (oft in Kombination mit einem pulsus parvus et tardus)
142 282 Apparative Untersuchungen EKG: in > 80% unspezifisch, linksventrikuläre Hypertrophie Transthorakale Echokardiografie (TTE): beim erfahrenen Untersucher ausreichend zur Erfassung des Schweregrades der AS (Beurteilung der linksventrikulären Funktion, Aorta, andere Vitien) Echokardiographische Kriterien für eine schwere Aortenklappenstenose Bei diskrepanten Befunden oder nicht optimaler Untersuchungsqualität bei V.a. eine schwere AS weitergehende Diagnostik: Ergometrie oder Laufbandbelastung: bei asymptomatischen Patienten zur Objektivierung der Belastbarkeit. Blutdruckanstieg? Dobutamin Stress-Echokardiografie: bei eingeschränkter linksventrikulärer Funktion mit niedrigen Gradienten zum Unterscheiden zwischen «low-flow, low-gradient»- und «paradoxe low-flow, lowgradient»-aortenstenose (chirurgische Mortalität bei ersterer 5%, bei letzterer ca. 32%) Transösophageale Echokardiografie (TEE) ergänzend zur TTE bei inkonklusiven Befunden. Klappenmorphologie und Planimetrie. Planung vor perkutaner Aortenklappenimplantation (TAVI): 3D bei Niereninsuffizienz alternativ zur CT-Diagnostik (Annulusgrösse). Koronarangiografie: Präoperativ Ausschluss / Nachweis einer relevanten koronaren Herzerkrankung. Mittels simultaner Druckmessung im linken Ventrikel und Aorta Quantifizierung der Aortenstenose. Darstellung der Aorta und der Beckenstrombahn vor perkutanem Klappenersatz. Multislice Angio CT: Methode der Wahl präoperativ vor TAVI/ minimal invasivem Klappenersatz (exakte Morphologie, Verkalkung der Klappe, Abstandmessung Annulus-Koronarostien, Annulus- Klappenöffnungsfläche (KÖF) Indexierte KÖF Mittlerer Druckgradient Maximale Spitzengeschwindigkeit Verhältnis Geschwindigkeitsintegral (AK/LVOT) < 1.0 cm² < 0.6 cm²/m² > 40 mmhg > 4 m/s < 0.25 grösse) und Darstellung Aorta, arterielle Zugangswege (subclavia, femoral, aortal), Kannülierungsstellen. Wie häufig kontrollieren? Welche Parameter zur Verlaufskontrolle? Leichte AS: bei jüngeren Patienten mit leichter Stenose ohne wesentliche Verkalkung 3 5-jährlich Echokardiografie und Ergometrie Mittelschwere AS: alle 1 2 Jahre Schwere AS, asymptomatisch: alle 6 Monate jährlich mit Frage nach Neu-Auftreten von Symptomen, Ergometrie und Echokardiografie mit Frage nach Befundänderung. Evtl. BNP zur Verlaufskontrolle. Bei Risikofaktoren (Verkalkung) oder Malcompliance Intervalle individuell verkürzen. Therapie Die schwere AS ist kausal medikamentös nicht therapierbar! Medikamentöse Therapie Nur Palliation oder kurzfristige Behandlung der Herzinsuffizienz vor AKE oder TAVI: Diuretika, (CAVE: Vermeidung von Hypotonien: ACE- Hemmer oder ATII-Antagonisten, Spironolacton). Keine negativ inotropen Substanzen verwenden. Chirurgischer Aortenklappenersatz (AKE) Konventioneller Standard unter Verwendung der Herz-Lungen- Maschine. Der minimal invasive Zugangsweg ist von rechts parasternal oder mittels Mini-Sternotomie möglich. Resektion und Ersatz der nativen Klappe durch eine mechanische (jüngere Patienten < 50 J; IIaB) oder biologische (ältere Patienten > 70 J; IIaB) Prothese. Bei J individuelle Entscheidung (IIaB): Die Wahl der Prothese basiert auf der Einnahme lebenslanger oraler Antikoagulation (OAK) versus Degeneration der implantierten Klappe (biologisch). Die Entscheidung basiert auf dem Wunsch des aufgeklärten Patienten. 283
143 Perkutane Aortenklappenimplantation (TAVI, Katheterbasiert) Für inoperable Patienten Bei hohem operativem Risiko für AKE (s.u.; Entscheidung im Herzteam) Bei intermediärem Risiko und gutem femoralem Zugangsweg (Entscheidung im Herzteam) Die Diskussion im «HeartTeam» ist obligatorisch für die Therapieentscheidung (Ic, europäische Guidelines). In Lokalanästhesie ohne Herz-Lungen-Maschine mit arteriellen Zugangsmöglichkeiten femoral und via A. subclavia In Narkose auch transapical oder direkt aortal Praktisches Vorgehen bei schwerer Aortenklappenstenose (angepasst aus ESC Guidelines 2012) Nein Nein LVEF < w 50% Schwere Aortenklappenstenose Symptome Ja Nein Ja Kontraindikation für AKE Ja Ballonvalvuloplastie Nur noch bei Hochrisikopatienten mit akuter hämodynamischer Instabilität als Überbrückung vor AKE oder TAVI (IIbC). Nein Körperlich aktiv Ja intermediärhohes Risiko 2) für AKE Lebenserwartung < 1a 284 Präoperative Risikostratifizierung Zwei Score-Systeme: der US-amerikanische STS Score ( sts.org/stswebriskcalc) und der Europäische Euroscore II (www. euroscore.org/calc) werden zur Einschätzung der perioperativen Morbidität und Mortalität herangezogen (STS = Society of Thoracic Surgeons). Hohes operatives Risiko bei einem STS-Score 10% oder EuroSCORE II 10%. Individuelle Faktoren wie «Gebrechlichkeit» («Frailty»), Porzellanaorta, intakte Bypässe nach ACVB-OP, thorakale Bestrahlung etc. müssen bei der Diskussion im Herzteam berücksichtigt werden. Die Scores sind abgeleitet aus Datenbanken des chirurgischen Klappenersatzes (AKE) und ungeeignet, um das individuelle Risiko eines perkutanen Klappeneingriffes (TAVI) zu beurteilen. Belastungstest Symptome, Blutdruckabfall Nein Risikofaktoren 1) und niedriges / mittleres OP-Risiko Nein Ja Ja AKE 2) Nein TAVI konservativ Re-Evaluation in 6 Monaten AKE oder TAVI 2) AS Aortenstenose, AKE Aortenklappenersatz, LVEF linksventrikuläre Auswurfsfraktion, TAVI Transkatheter Klappenimplantation 1) OP sollte bei folgenden Risikofaktoren (IIaC) bedacht werden: Spitzengeschwindigkeit > 5.5 m/s, Schwere Verkalkung und Progression der Spitzengeschwindigkeit > 0.3 m/s/jahr. Kann diskutiert werden (IIbC) bei signifikant erhöhtem BNP, Zunahme des mittleren Gradienten unter Belastung > 20 mmhg, exzessive LV-Hypertrophie. 2) Die Entscheidung soll im «Herzteam» aufgrund individueller klinischer Charakteristika und Anatomie getroffen werden. ESC Guidelines valvuläre Herzkrankheit European Heart Journal (2012) 33, Ja Nein Ja 285
144 286 Aortenklappeninsuffizienz (AI) Ist entweder Folge einer Läsion der Klappentasche oder eine Erkrankung der Aortenwurzel/bzw. des Aortenklappenannulus Akut: bei Endokarditis, Typ A Dissektion der Aorta oder traumatisch. Chronisch: bei bikuspiden Aortenklappen, Dilatation des Aortenklappenannulus oder des Aortensinus (z. B. Marfan-Syndrom) Prognose Leichte bis mittelschwere asymptomatische AI: gute Prognose, d.h. jährliche Mortalität ca. 1%. Schwere asymptomatische AI: niedrige Mortalität, jedoch bei schwerer LV Dilatation (LVESD > 50 mm) beträgt die Wahrscheinlichkeit für Herzinsuffizienz und Tod 19% pro Jahr. Schwere symptomatische AI: jährliche Mortaliät ca %. Akute AI: hohe Mortalität Diagnostik Anamnese: Belastungsdyspnoe und/oder Angina pectoris, Palpitationen und Synkopen. Klinische Befunde: Hohe Blutdruckamplitude, arterielle Pulsationen. Auskultatorisch diastolisches Geräusch mit Decrescendo-Charakteristik (vorgebeugt im Sitzen auskultieren). Meist auch systolisches Austreibungsgeräusch (Pendelvolumen). Bei akuter AI ist das Geräusch kurz und v.a. bei Lungenödem schwierig zu diskriminieren! Apparative Untersuchungen Echokardiografie: Semiquantitative Erfassung des Schweregrades der AI, (OP-relevante) zusätzlicher Befunde: LV Auswurfsfraktion EF und Grösse (Volumen multiplanar oder 3D), aortale Dimensionen und begleitende Vitien. Transösophageale Echo (TEE) insbesondere zur exakten morphologischen Beurteilung der Klappe angezeigt. Zusätzlich kann die Aorta beurteilt werden. Alternative zum CT und MRI bei Niereninsuffizienz. Koronarangiografie/Rechtsherzkatheter: präoperativ bei Patienten > 40 a mit mittlerem-hohen kardiovaskulärem Risiko zum Ausschluss/Nachweis einer relevanten KHK. Semiquantitative Graduierung der AI, Abklärung Druckbelastung des Lungenkreislaufes CT und MRI: Beurteilung des gesamten aortalen Gefässbaumes, insbesondere bei seltenen Ursachen (Marfan, Vaskulitiden unterschiedlicher Genese, Lues). CT als Alternative zur Koronarangiografie bei jungen Patienten bei niedrigem kardiovaskulärem Risiko ausreichend. Therapie/Follow-up Asymptomatische Patienten mit leichter AI sollten alle 5 a, mit mittelschwerer AI alle 2 a klinisch als auch echokardiografisch zur Erfassung einer Progression kardiologisch gesehen werden. Bei Progredienz des Schweregrades oder bei linksventrikulären Dimensionen nahe an den Entscheidungskriterien 6-monatliche Kontrollen. Bei stabilen Messwerten alle 12 Monate. Konservativ Leichtgradige, chronische AI: keine Therapie. Jährliche klinische Beurteilung hinsichtlich der Symptomatik (Hausarzt) und 2 5-jährliche echokardiografische Kontrolle. Behandlung einer evtl. arteriellen Hypertonie primär mit Vasodilatatoren, nach Möglichkeit kein Betablocker. Keine Aktivitätseinschränkungen. Bei Progression oder Dilatationen der Aorta/des linken Ventrikels im Bereich der Grenzwerte: 6-monatige Kontrollen mittels Echo. Vasodilatatoren (ACE-Hemmer; AT-II Antagonisten) kurzfristig bei Patienten mit Herzinsuffizienz vor OP. Bei Patienten mit Marfan-Syndrom (bzw. generell aortaler Dilatation) sind Betablocker prä- und postoperativ angezeigt; AT-II-Antagonisten scheinen günstig zu sein (Daten v.a. für Losartan). Bei schwerer AI oder grenzwertigen aortalen Durchmessern keine isometrischen Übungen, Kontaktsportarten, Wettbewerbe oder hohe körperliche Anstrengungen. 287
145 OP-Indikationen für chirurgischen Aortenklappenersatz (AKE) Symptomatische, akute schwere AI: sofortige/dringliche Operation. Chronische, schwere AI: Bei Auftreten von Symptomen Bei Verschlechterung der linksventrikulären Funktion (EF < 50%) oder Grössenzunahme in seriellen, vergleichbaren Messungen (LVEDD > 65 mm oder LVESD > 50 mm oder > 25 mm/m 2 BSA). Perkutane Aortenklappenimplantation (TAVI) Bei der AI ist TAVI nicht indiziert Indikationsstellung in spezifischen Fällen im Herzteam Praktisches Vorgehen: Schwere Aortenklappeninsuffizienz Nein Aortenklappeninsuffizienz (AI) mit erweiterter aorta ascendens 1) Ja AI schwer Ja Symptome Nein Nein Ja LVEF 50% oder LVEDD > 65 mm oder LVESD > 50mm (oder > 25 mm/m² BSA) Follow-up Nein Ja OP 2) 1) 45 mm Marfan-Syndrom mit Risikofaktor 50 mm Marfan oder bikuspide Klappe mit Risikofaktor; 55 mm für alle übrigen. 2) Diskussion der OP auch bei signifikanten Änderungen der linksventrikulären oder Aortendimension während Follow-up. ESC Guidelines valvuläre Herzkrankheit European Heart Journal (2012) 33,
146 Mitralklappeninsuffizienz (MI) Zweithäufigste Klappenerkrankung in der Allgemeinbevölkerung, die zur OP führt. Prävalenz von mittelschwerer oder schwerer MI: 1.7% in der Normalbevölkerung und 9.3% bei über 75-Jährigen. Ätiologisch: Primär organische MI mit strukturellen/degenerativen Veränderungen der Klappe selbst (Prolaps, «Flail leaflet» bei Sehnenfadenabriss, myxomatöse Veränderungen, rheumatische Erkrankung, Endokarditis, Cleft, Papillarmuskelruptur nach Myokardinfarkt). Funktionelle MI bei strukturell normaler Klappe (Annulusdilatation mit «Tethering» der Klappensegel, ischämisch bei Papillarmuskeldysfunktion). Prognose Leichte MI: Keine Einschränkung der Lebenserwartung. Die chronische MI wird gut toleriert, bleibt lange asymptomatisch. Bei zunehmender linksventrikulärer Leistungseinschränkung klinische Symptome: Dyspnoe, Herzklopfen (Vorhofflimmern bei Vorhofdilatation), Orthopnoe, nächtliche Hustenanfälle. Die Wahrscheinlichkeit für Tod bzw. kardiale Ereignisse ist abhängig von der Ätiologie der valvulären Dysfunktion. Die asymptomatische schwere MI hat eine 5-Jahres- Wahrscheinlichkeit für Tod, kardiale Ereignisse (Tod, Herzinsuffizienz, VHF) von 14 33%. Die schwere symptomatische funktionelle MI (mit oder ohne KHK) sowie die akute schwere MI (Papillarmuskelabriss nach Myokardinfarkt; Sehnenfadenabriss) haben ohne medikamentöse und chirurgische Therapie eine sehr schlechte Prognose. Diagnostik Anamnese: Dyspnoe (NYHA I-IV), Orthopnoe, Palpitationen (Vorhofflimmern). Jedoch: oft jahrelanger, asymptomatischer Verlauf bei chronischer MI! Klinische Befunde: Auskultation in Linksseitenlage: unmittelbar nach dem eher leisen ersten Herzton hochfrequentes, bandförmiges Systolikum mit p.m. über der Herzspitze mit Fortleitung in die Axilla Apparative Untersuchungen EKG: p-mitrale. (paroxysmales) Vorhofflimmern? Echokardiografie: Schweregrad der MI durch Messung des Regurgitationsvolumens, Volumetrie des linken Ventrikels TEE bei diskrepanten Befunden oder nicht optimaler Untersuchungsqualität insbesondere bei V.a. schwere MI, exakte Regurgitationsvolumina mittels 3D-Volumetrie. Präoperativ (vor chirurgischer oder perkutaner Rekonstruktion/Klappeneratz): zur exakten Erfassung der Morphologie (3D-Darstellung der Mitralklappe) Physikalische Belastung mit zusätzlicher Echokardiografie auf dem Liegevelo: in unklaren Fällen oder bei dynamischer (ischämischer) MI Koronarangiografie/Herzkatheter: präoperativ zum Ausschluss/ Nachweis einer relevanten KHK. Ergänzende Beurteilung des Schweregrades der Mitralinsuffizienz und der Abklärung einer allfälligen begleitenden pulmonalen Hypertonie Therapie Die medikamentöse Therapie der degenerativen MI ist indiziert bei der Entwicklung einer systolischen Disfunktion. Im Gegensatz dazu ist bei der funktionellen MI die medikamentöse Therapie der erste Schritt der Behandlung. Die Therapie ist gleich bei beiden Pathologien und beiinhaltet eine Nachlastsenkung mit ACE-Hemmern oder AT-II- Antagonisten, Betablockern (zu starke Bradykardisierung vermeiden), Diuretika und Aldosteron-Antagonisten
147 Chirurgische Therapie für funktionelle und degenerative MI Mitralklappenrekonstruktion (MKR, konventionell oder minimalinvasiv): bei passender Klappenmorphologie Methode der Wahl. Implantation eines Mitralringes, Segelresektion und Einsatz künstlicher Sehnenfäden. Mitralklappenersatz (MKE, biologisch oder mechanisch): Alternative bei schwer vorgeschädigter nativer Herzklappe. Mechanische (jüngere Patienten < 65a; IIaC) oder biologische (ältere Patienten > 70a; IIaC) Prothese. Die Wahl der Prothese ist immer eine individuelle Entscheidung basierend auf der Einnahme lebenslanger oraler Antikoagulation (mechanisch) versus Degeneration der implantierten Klappe (biologisch). Im Alter 65 70a sind beide Prothesen möglich. Die Entscheidung basiert auf dem Wunsch des aufgeklärten Patienten (Ic). Management der schweren Mitralklappeninsuffizienz Nein LVEF 60% oder LVESD 40 mm Nein Nein Neues VHF oder spap > 50 mmhg Ja Ja Symptome Ja Ja LVEF > 30% Nein Kein Ansprechen auf medikamentöse Therapie Ja Nein Perkutane Behandlungsmöglichkeiten Katheterbasierte «MitraClip» bei Hochrisiko-Patienten (Herzteam- Diskussion) mit schwerer, vorwiegend funktioneller oder degenerativer MI. Nicht anwendbar bei Endokarditis, rheumatisch veränderten oder stark verkalkten Klappen. Mittels Implantation eines «Cardiobands» ist eine perkutane Ringannuloplastie bei vorwiegend funktioneller Mitralinsuffizienz möglich. Aktuell sind noch weitere, innovative Verfahren in der Entwicklung. Klappenreparatur möglich; niedriges OP Risiko; Risikofaktoren vorhanden 1) Nein Ja Klappenreparatur möglich; niedriges Risiko Ja Nein Follow-up Klappenreparatur Erweiterte Herzinsuffizienz- Therapie 2) Konservativ medikamentös BSA=Körperoberfläche; LA=linker Vorhof; LV= linker Ventrikel; LV EF linksventrikuläre Auswurffraktion; spap systolischer pulmonal-arterieller Blutdruck; VHF= Vorhofflimmern 1) Bei hoher Repararaturwahrscheinlichkeit > 95% bei niedrigem Risiko < 1% soll eine Reparatur im center of excellence diskutiert werden (IIaC) bei Patienten mit flail leaflet und LVESD 40 mm; diskutabel (IIaB) bei Patienten mit LA-Volumen 60 ml/m² BSA und Sinusrhythmus oder pulmonaler Blutdruck bei Belastung 60 mmhg oder progressive Zunahme der LV Grösse oder EF Abnahme in seriellen Untersuchungen (IIaC). 2) Erweiterte Herzinsuffizienztherapie beinhaltet kardiale Resynchronisationstherapie (CRT), Mitraclip, ventrikuläre Assist Devices, kardiale Restraint Devices, Herztransplantation. ESC Guidelines valvuläre Herzkrankheit European Heart Journal (2012) 33, AHA/ACC Focused Update Incorporated Into the 2014 AHA/ACC Guideline for the Management of Patients With Valvular Heart Disease. March 15, Journal of the American College of Cardiology
148 294 Mitralklappenstenose (MS) Insgesamt selten: degenerativ (Einschränkung der Segelbeweglichkeit über eine Annulusverkalkung). Auch kongenitale Formen. Prognose/Verlauf Der Krankheitsverlauf ist schleichend. Im Mittel vergehen 16 Jahre zwischen dem rheumatischen Fieber und dem Vorliegen einer relevanten Mitralstenose. Diagnostik Anamnese: eingeschränkte Leistungsfähigkeit, Dyspnoe (NYHA I-IV), Müdigkeit. Hämoptysen, Palpitationen, systemische Embolien bei Vorhofflimmern. Klinische Befunde/Auskultation in Linksseitenlage: «paukender» 1. Herzton, gefolgt von normalem 2. Herzton. Niederfrequentes Decre- scendo-geräusch in der Diastole. P.M. über Herzsspitze. Bei Sinusrhythmus präsystolischer Klick. Apparative Untersuchungen EKG: p-mitrale, Vorhofflimmern? Echokardiografie: Beurteilung des Schweregrades, Verkalkung, andere morphologische Veränderungen zur Klassifizierung nach Wilkins vor evt. Ballonvalvuloplastie. Planimetrie der Öffnungsfläche im 3D- Datensatz. Transösophageale Echokardiografie: präoperativ/präinterventionell zur genauen morphologischen Beurteilung der Klappe und des subvalvulären Apparates; Nachweis/Ausschluss linksatrialer Thromben; 3D-Darstellung: zur Beurteilung der Klappenöffnungsfläche. Stressecho (Dobutamin, idealerweise auch physikalisch): bei leichter/ mittelschwerer Mitralstenose und ungeklärter Dyspnoe. Koronarangiografie / Rechtsherzkatheteruntersuchung: präoperativ/präinterventionell zum Ausschluss/Nachweis einer KHK. Simultane Messung PCWP/LV-Druck zur Gradientenbestimmung. Therapie Allgemeines: OAC bei allen Patienten mit Vorhofflimmern oder nach arterieller Embolie (INR 2 3). Bereits bei mittelschwerer Mitralstenose ist eine OAC zur Verhinderung thromboembolischer Ereignisse auch bei Sinusrhythmus angezeigt bei Vorliegen eines schwer vergrösserten linken Vorhofs (> 60 ml/m² oder > 50 mm Mode Diameter). Patienten mit relevanter (d.h. mittelschwerer bis schwerer) Mitralstenose benötigen für eine ausreichende Ventrikelfüllung eine lange Diastole daher muss (v.a. bei Vorhofflimmern) auf eine gute Frequenzkontrolle geachtet werden. Katheterbasierte oder chirurgische Intervention bei symptomatischen Patienten mit schwerer (< 1.5 cm²) sehr schwerer (< 1.0 cm²) Mitralstenose: A) Perkutane Mitralklappenkommissurotomie (PMC): Klasse 1A-Empfehlung bei geeigneter Anatomie bei Kontraindikation oder hohem OP-Risiko auch bei anderen Patienten (1C). Die PMC erfolgt mithilfe eines Ballonkatheters bei geeigneten Patienten (Echo-Score nach Wilkins). Gutes Primärergebnis in > 80% der Patienten, ereignisfreies Überleben beträgt 30 70% in Jahren. Entscheidung über PMC nach klinischen Daten und Echo-Score. Beste Resultate bei jungen Patienten mit niedrigen Score-Werten, Sinusrhythmus, minimalen Verkalkungen und ohne begleitende Mitralklappeninsuffizienz. B) Chirurgische Therapie Meist Mitralklappenersatz (MKE) aufgrund der Klappendestruktion. In sehr spezifischen Fällen kann die Klappe rekonstruiert werden. 295
149 Klappenerkrankungen und perioperatives Management bei «non-cardiac surgery» Nicht-kardiale Eingriffe sind mit vertretbarem Risiko möglich bei Patienten mit relevanter AI und MI (auch schwer), wenn die linksventrikuläre Funktion normal ist. Ebenso bei asymptomatischen Patienten mit MS ohne relevante pulmonale Hypertonie (spap < 50 mmhg). AS: Patienten mit symptomatischer AS und niedrigem OP-Risiko für den Klappenersatz primär Klappenoperation/-eingriff. Bei asymptomatischen Patienten für OP mit niedrigem oder intermediärem Risiko primär OP unter gutem Monitoring. Bei hohem OP-Risiko bei gleichzeitig niedrigem Risiko für die Klappenoperation sollte primär der Klappenersatz durchgeführt werden. Diskussion individuell im gesamten Behandlungsteam: Chirurg, Anästhesist und Kardiologe. Biologische Klappen INR 2.5 für 3 6 Monate (IIaB) bei niedrigem Blutungsrisiko TAVI INR 2.5 für >3Monate (IIbB) oder unbefristet ASS 100 mg und Clopidogrel 75 mg für 6 Monate (IIbC) Dr. Philipp K. Haager Prof. Dr. Francesco Maisano PD Dr. Maurizio Taramasso Dr. Héctor Rodríguez Dr. Niklas Ehl Follow-up bei Klappenerkrankungen postoperativ/ postinterventionell Endokarditisprophylaxe siehe entsprechendes Kapitel bei allen implantierten Fremdmaterialien (auch Ringe und Neochords) sowie TAVI Regelmässige Zahnreinigungen und Kontrollen 3 Monate postoperativ Standortbestimmung mit Röntgen-Thorax, Labor, Echokardiografie. Anschliessend zeitlebens jährliche klinische Verlaufskontrollen mit Labor und Echokardiografie (v.a. bei biolog. Prothesen: Degeneration? Gradienten? Paravalvuläre Leckage? Zusatzstrukturen?) Mechanische Klappen: Hämolyse? INR-Werte? Bei schwieriger Beurteilung/ Gradientenzunahme im Echo ggf. TEE und Klappendurchleuchtung. INR-Zielwerte nach Massgabe des Chirurgen/Klappentyp/Risikofaktoren (üblicherweise moderner AKE 2.5 (+Risikofaktor 3.0); MKE/ TKE 3.0 INR-Selbstmonitoring bei mechanischen Klappen bei geeigneten Patienten empfohlen
150 Ambulante kardiale Rehabilitation (AKR) und Prävention Indikationen Eine kardiovaskuläre Rehabilitation ist indiziert gemäss SAKR Nach einer akuten Herzerkrankung: nach Herzinfarkt oder akutem Koronarsyndrom mit oder ohne kathetertechnischen Eingriff Bei stabiler KHK mit oder ohne St. n. Katheterintervention Nach Operationen am Herzen und an den Gefässen Beim Vorhandensein multipler Risikofaktoren (z. B. metabolisches Syndrom mit oder ohne chronische Herzkrankheit) Bei anderen Herz-Kreislauf-Krankheiten, deren Verlauf durch Rehabilitation günstig beeinflusst wird (z. B. Herzinsuffizienz, Rhythmusstörungen, ICD) ( Ziele Risikostratifizierung für Rezidive im weiteren Verlauf Umsetzung einer adäquaten medikamentösen Sekundärprophylaxe Information über Krankheit (Diagnostik und Therapie) und Risikofaktoren Rekonditionierung nach Immobilisierung Korrektur eines vorbestehenden Bewegungsmangels Bewegungsprogramm als Vehikel für Lebensstilveränderungen Aneignung eines gesunden Lebensstils Ernährungsberatung Stressbewältigung Raucherentwöhnung (
151 Ambulant/stationär Für eine ambulante Rehabilitation sprechen gemäss SAKR Wohnortnähe Möglicher Einbezug von Angehörigen Durchführung abgestuft über längere Zeit Teilzeit-Berufstätigkeit möglich Für eine stationäre Rehabilitation sprechen Komplikationsreicher Verlauf Ausgeprägte Co-Morbiditäten (Begleiterkrankungen) Frühpostoperativer Eintritt erwünscht Erhöhter Pflegebedarf Intensive medizinische Überwachung und Kontrollen nötig Milieuwechsel angezeigt Fehlende Betreuung zu Hause ( Organisatorisches Vor Antritt einer AKR sind sowohl eine Ergometrie als auch eine Kostengutsprache nötig. Die Kostengutsprache wird seitens des Sekretariats KSSG nach Anmeldung parallel zum Aufgebot des Patienten eingeholt. Von stationär KSSG: Wenn AKR geplant, zwingend vor Austritt eine Ergometrie mit dem Auftragsplugin «Ergo vor AKR (stationär)» bei medfolio anmelden. Anmeldung bitte schon während Hospitalisation, damit die Kostengutsprache erfolgen kann. Von extern Adressat für sämtliche Patientenunterlagen ist stationär/ambulant: ausschliesslich das Sekretariat Kardiologie/AKR: (Betreff: AKR) Vorhandenen, aktuellen Ergometriebericht senden oder auf der Anmeldung vermerken, dass die Ergometrie am KSSG durchgeführt werden soll. Wenn ein Patient für eine AKR evaluiert wurde, dann muss eine Kopie des Austrittsberichtes (sowohl Kurzbericht als auch definitiver Bericht) an: (Betreff: AKR) geschickt werden. Der Auftrag bzgl. einer AKR muss im Austrittsbericht klar ersichtlich sein (z. B. Vermerk: «Bitte aufbieten für AKR, Eintrittsuntersuchung [EU] bereits im KSSG erfolgt»/«bitte aufbieten für AKR, Eintrittsuntersuchung konnte noch nicht durchgeführt werden» usw.). Inhalt des Therapieprogrammes 36 nichtärztliche Sitzungen (entspricht 72 Einheiten) 64 Einheiten Physiotherapie (Ausdauer, Kraft, Koordination/Gleichgewicht, Aussenaktivität ) davon 1 Einheit Entspannungstraining pro Woche 6 Einheiten Ernährungsberatung 4 Einheiten psychologische Gruppenberatung Raucherberatung individuell und 2 Einheiten Raucherberatung in der Gruppe Quelle:
152 Ablauf Ambulante Kardiale Rehabilitation und Prävention (AKR) Patient stationär und benötigt AKR Anmeldung Ergometrie mit Medfolio Auftrags-Plug-in «Ergo vor AKR (stationär)» Sekretariat ZEP nimmt Patienten in die Liste auf sendet die Unterlagen an Patienten Ergometrie durch Kardiologie AKR-AA/FAA/Rot-AA Einbindung in Reha-Programm AKR/ADR 36x AVR 48x Patient nimmt Termin E1 wahr Terminanfrage Zentrum für Ergo- und Physiotherapie (ZEP) A) Per Telefon Angabe Name, Geb.datum Einführungstermin AKR wird direkt vereinbart und AKR- AA/FAA/Rot-AA mitgeteilt Betriebszeiten ZEP-Sekretariat: Mo Fr 07:30 11:45 und 13:00 16:00 Termin E1 Patientenaufklärung AKR Abgabe Infomaterial Abgabe Termin E1 Befund Ergo an AKR-AA Innerhalb 48 Std.: Eintrittsempfehlung für Gruppeneinteilung (A/B) Durchführung bis Ende Programm? Nein Ja Verrechnung: Drop out vorzeitiges Beenden der AKR à Brief an Hausarzt Verrechnung und Anmeldung zur AU B) Per Mail: Angabe Name, Geb.datum, Tel. des Pat. Sekretariat ZEP bietet Patienten telefonisch auf Einführungstermin in gleicher Woche Spätestens innerhalb der nächsten 7 Tage Reha beginnt spätestens eine Woche nach Termin E1 Zuständige Physiotherapeuten Ergänzung Teilnehmerliste Sekretariat AKR Einholen Kostengutsprache Ablage Ergo- Bericht in KG Ablage KG in Ambi Kardiologie Abschluss (Listenabschluss, Abschlussgespräch) Dr. Marc Buser Kim Denise Gebhardt
153 Psychokardiologie Die Psychokardiologie ist eine Spezialdisziplin, die sich mit den wechselseitigen Zusammenhängen von psychischen Aspekten und Herzerkrankungen beschäftigt. Psychosoziale Variablen haben einen evidenzbasierten modulierenden Einfluss auf den weiteren Krankheitsverlauf koronarer Herzerkrankungen (Lebensqualität, Morbidität, Mortalität etc.) Praxisrelevante Hinweise für den kardiologischen Alltag: Wer braucht psychokardiologische Unterstützung Angst, Depressivität, negative Affekte: Besteht eine erhöhte, subjektiv berichtet oder objektiv wahrnehmbare Ängstlichkeit? Kam der Patient mehrfach schon auf den Notfall ohne neuen Befund? Ist eine vorbestehende Depression diagnostiziert oder können depressive Symptome wahrgenommen werden? Bestehen Suizidgedanken, ein negativer Blick in die Zukunft? Ist der Patient weinerlich, lustlos, mutlos, pessimistisch und/oder besteht eine erhöhte Reizbarkeit? Insbesondere Depressivität kann nach Beginn einer koronaren Herz erkrankung häufig auftreten und ohne spezifische Behandlung persistieren. Dabei ist nicht nur die Lebensqualität beeinträchtigt, sondern es resultiert auch eine schlechte Prognose. Stress und Belastung: Berichtet der Patient von einer subjektiv wahrgenommenen, meist chronisch dauerhaften beruflichen oder/ und privaten meist konfliktbehafteten Höchstbelastung? Wichtig: Speziell gefährdet sind Patienten mit mehreren Risikofaktoren und fehlenden protektiven Faktoren (Freizeit, Sport, glückliche Paar beziehung, Hobbys etc.)
154 Vitale Erschöpfung: Berichtet der Patient oder Hausarzt von vorbestehenden (meist 6 Monate vor Eintritt eines Infarkts) Symptomen einer schweren Erschöpfung und / oder depressiven Episoden, die die Betroffenen zu ihrem Arzt führten? Krankheitsverarbeitung (Coping-Mechanismen): Ist der Patient gegenüber Veränderungen negativ eingestellt? Kann eine pessimistische Haltung gegenüber der Zukunft und der Einnahme möglicher Medikamente wahrgenommen werden? Entsteht subjektiv und / oder auch objektiv berichtet der Eindruck, der Patient wird die Empfehlungen der Ärzte nicht umsetzen? Möchte der Patient zu viel auf einmal verändern und besteht die Gefahr der Überbelastung? Fehlen dem Patienten realistische, gestaffelte Ziele zur Verarbeitung? Sind allgemein mangelnde Ressourcen wahrnehmbar? Eine optimistische und aktiv gestaltende Haltung hat günstige Effekte, wobei diese abhängig ist von einer guten Informiertheit über die Krankheit und die erforderlichen Lebensstilveränderungen. Eine negative Haltung mit einem pessimistischen Blick in die Zukunft resultiert dafür oft in einer mangelnden compliance. Schichtzugehörigkeit: Kommt der Patient aus einer niedrigen sozialen Schicht? Besteht eine schlechte Schulbildung, keine / schlechte Berufsausbildung, wenig Einkommen oder soziale Unterstützung? Je niedriger die soziale Schicht, desto grösser ist die Wahrscheinlichkeit einer koronaren Herzerkrankung. Diese Aussage gilt nicht allein deshalb, weil man in dieser Schicht mehr raucht, sich ungesünder ernährt, sich weniger bewegt etc. Der inverse Zusammenhang bleibt gültig auch bei Kontrolle all dieser Variablen. Da ärztliches Handeln keinen Einfluss auf diese Lebensbereiche hat, kann nur die vorsorgende Betreuung und Achtsamkeit verstärkt werden. Aufgrund dieser multiplen Einflussfaktoren muss es das Ziel einer optimalen interdisziplinären Zusammenarbeit sein, dass ein niederschwelliger Einbezug der Psychokardiologie (am besten schon stationär) stattfindet, um Risikofaktoren schnell und effektiv behandeln und so einen langfristig erfolgreichen Krankheitsverlauf gewährleisten zu können. Sina Rüdt Dr. Dagmar Schmid Prof. Dr. Hans Rickli Familiärer und sozialer Rückhalt: Fehlt ein gutes soziales Netzwerk? Hat der Patient keine Angehörigen, die für ihn sorgen und ihn besuchen kommen? Droht der Verlust des Arbeitsplatzes und / oder der sozialen Unterbringung? Gute familiäre Unterstützung und Rückhalt in einem grossen sozialen Netzwerk beeinflussen die Krankheitsverarbeitung, die Affektlage und den Krankheitsverlauf günstig. Umgekehrt ist nachgewiesen, dass mangelnder Rückhalt und ein Rückzug aus sozialen Beziehungen (soziale Inhibition) spürbar negative Folgen haben
155 Fahrtauglichkeitsbeurteilung bei kardiologischen Patienten Die Beurteilung der Fahrtauglichkeit bei kardiologischen Patienten stellt den behandelnden Arzt im Alltag immer wieder vor Probleme. Einerseits muss das Risiko für das Auftreten eines potenziell gefährlichen Ereignisses beim Fahren abgeschätzt werden, andererseits kann das Aussprechen eines Fahrverbotes aus medizinischen Gründen das Patienten-Arzt-Verhältnis stark beeinträchtigen. Grundsätzlich existiert eine mathematische Formel, mithilfe derer eine Schädigungswahrscheinlichkeit berechnet werden kann. Dabei spielten unter anderem die Art des Fahrzeuges (Lkw, Bus, Pkw), die verbrachte Zeit beim Fahren, das Risiko eines kardiovaskulär bedingten Kontrollverlustes sowie die Wahrscheinlichkeit, dass ein solches Ereignis tödlich oder mit schwerwiegenden Verletzungsfolgen für andere Verkehrsteilnehmer einhergeht, eine Rolle. Wegen der deutlich verschiedenen Schädigungswahrscheinlichkeiten zwischen Berufs- und Privatfahrern müssen diese bei der Fahrtauglichkeitsbeurteilung separat betrachtet werden. Zu den Berufsfahrern gehören üblicherweise Taxi-, Bus- und Lkw-Fahrer (ab 3.5 Tonnen), aber auch Fahrlehrer. Allgemein existiert wenig Literatur bezüglich Fahrtauglichkeitsbeurteilung kardiologischer Patienten. In der Schweiz sind letztmalig Richtlinien zur verkehrsmedizinischen Begutachtung 2005 erschienen, wobei diese in kardialen Situationen nicht sehr ausführlich/detailliert gehalten sind und aktuell unter Überarbeitung stehen. Zwischenzeitlich sind jedoch per die neuen Medizinischen Mindestanforderungen gemäss Anhang 1 Verkehrszulassungsverordnung (VZV) in Kraft getreten (Kapitel 7 Herz-/Kreislauferkrankungen). Ansonsten gibt es keine explizit für die Schweiz geltenden Richtlinien. Die nachfolgend aufgeführte Zusammenstellung der Fahrtauglichkeiten basiert dementsprechend sowohl auf schweizerischen wie auch auf europäischen und deutschen Richtlinien. Sie sollen bei der Beurteilung als grobe Leitlinien beigezogen werden können, müssen jedoch bei jedem Patienten individuell angeschaut werden. Zudem sollte in Zweifelsfällen und bei Berufsfahrern in jedem Fall eine verkehrsmedizinische Abklärung erfolgen
156 ICD Private Fahrzeuglenker Berufsfahrer (Fahrlehrer, Taxi, Bus, Lkw) Herzinsuffizienz Generell individuelle Abklärung nötig Generell individuelle Abklärung nötig Primärprophylaktische ICD-Implantation Sekundärprophylaktische ICD-Implantation Nach adäquatem ICD-Schock Keine Restriktion nach Erholung vom Eingriff 5 Fahruntauglich 1,5 6 Monate untauglich 5, nachher bei Symptomfreiheit tauglich 1,5 6 Monate untauglich 5, nachher bei Symptomfreiheit tauglich 1,5 Fahruntauglich 1,5 Fahruntauglich 1,5 Synkopen Häufig tauglich, wenn 2,5 : Symptomfrei in Ruhe und beim Lenken (NYHA I III) Keine höhergradigen Rhythmusstörungen Bei ICD s.da Fahruntauglich bei LVEF < 40% 2,4,5 ggf. tauglich bei LVEF > 40%, symptomfrei, keine Arrhythmien 2,5 Nach inadäquatem ICD-Schock Ablehnung primärprophylaktischer ICD Ablehnung sekundärprophylaktischer ICD Koronare Herzkrankheit Stabile Angina pectoris Bis Problem behoben ist 1 Tauglich 1, s. auch Abschnitt Herzinsuffizienz Mind. 6 Monate untauglich Keine Restriktion, sofern keine Ruhebeschwerden 2,5 Fahruntauglich 1,5 Fahruntauglich 1,5 Tauglich, wenn 2 : Asymptomatisch Keine antianginöse Akut-Therapie nötig Regelmässige Belastungstests unauffällig Vasovagale Synkope Einmalig, nicht im Sitzen/beim Fahren Rezidivierend oder einmalig im Sitzen/ beim Fahren Synkope bei Arrhythmie Medikamentöse Behandlung Mit PM-Implantation Mit ICD-Implantation Keine Restriktion 3,5 Keine Restriktion, nachdem Symptome kontrolliert sind (Wartezeit nicht klar definiert) 3 Nach erfolgreicher Etablierung der Medikation 3 max. 1 Woche Wartefrist 3 s. dort Verkehrsmedizinische Abklärung Oft tauglich nach erfolgreicher Etablierung der Medikation 3 Tauglich nach Dokumentation des Langzeiterfolges (6 Monate?) 3 Untauglich Nach Myokardinfarkt Keine Restriktion nach Erholung vom Akutereignis und asymptomatisch (ca. 2 4 Wochen) 2, Wochen untauglich 2,4,5 Nachher tauglich, wenn: Vollständige Erholung vom Akutereignis Beschwerdefrei ohne antianginöse Akut-Therapie Regelmässige Belastungstests unauffällig LVEF >50% Bei LVEF 40 50% Wartezeit 6 Monate 4 Bei LVEF <40% in der Regel untauglich 2,4 Ungeklärte Synkope/ Bewusstseinsverlust Art. Hypertonie Bei erster Synkope 6 Monate untauglich 5 Bei rezidivierenden Synkopen 12 Monate untauglich 5 Fahrtauglich, wenn diastolischer Blutdruck < 130 mmhg 5 Verkehrsmedizinische Abklärung Fahruntauglich wenn 2,5 Syst. Blutdruck > 180 mmhg Diast. Blutdruck > 100 mmhg
157 Literatur: 1. Vijgen J et al. Consensus statement of the European Heart Rhythm Association: updated recommendations for driving by patients with implantable cardioverter defibrillators. Europace (2009) 11, Petch M.C. Driving and heart disease. Eur Heart J (1998) 19, Moya A. et al. Guidelines for the diagnosis and management of syncope (version 2009). Eur Heart J (2009) 30, Klein H. H. et al. Fahreignung bei kardiovaskulären Erkrankungen. Positionspapier der deutschen Gesellschaft für Kardiologie. Der Kardiologe 12/2010; 4(6): Arbeitsgruppe Verkehrsmedizin der Schweizerischen Gesellschaft für Rechtsmedizin. Handbuch der verkehrsmedizinischen Begutachtung. Hans Huber Verlag 2005 Dr. Marc Buser Dr. Bruno Liniger Prof. Dr. Peter Ammann Prof. Dr. Hans Rickli Legal Disclaimer Das Kardiovaskuläre Manual 2017 wurde von den Autoren des Kantons spitals St.Gallen völlig unabhängig erarbeitet. Astra Zeneca, Bayer (Schweiz) AG, B. Braun AG, Biotronik AG, Boston Scientific, Daiichi Sankyo, GE Healthcare, Menarini AG, MSD, Novartis, Sanofi- Aventis AG und St.Jude Medical haben keinerlei Einfluss auf den Inhalt genommen. Die Empfehlungen können inhaltlich von den Informationen in den behördlich genehmigten Fachinformationen der erwähnten Arzneimittel abweichen. Astra Zeneca, Bayer (Schweiz) AG, B. Braun AG, Biotronik AG, Boston Scientific, Daiichi Sankyo, GE Healthcare, Menarini AG, MSD, Novartis, Sanofi-Aventis AG und St.Jude Medical empfehlen keine Anwendung ihrer Arzneimittel bzw. Geräte ausserhalb der zugelassenen Indikationen und Dosierungen. Das Kardiovaskuläre Manual 2017 wird den Ärzten und weiteren interes sierten Fachpersonen auf spezifischen Wunsch und zur eigenverantwortlichen Verwendung überlassen. Die Abgabe wird von Astra Zeneca, Bayer (Schweiz) AG, B. Braun AG, Biotronik AG, Boston Scientific, Daiichi Sankyo, GE Healthcare, Menarini AG, MSD, Novartis, Sanofi-Aventis AG und St.Jude Medical nicht mit promotionellen Aussagen zu Arzneimitteln bzw. Indikationen verbunden. Impressum Herausgeber Prof. Dr. Hans Rickli, Chefarzt Klinik für Kardiologie, Kantonsspital St.Gallen, Rorschacher Strasse 95, 9007 St.Gallen Unter Mitarbeit von Dr. Gudrun Haager, Kantonsspital St.Gallen Konzept/Layout STO Pharmawerbung AG, Wil Druck galledia ag, Flawil
158 Notizen Notizen
159 316 Notizen
160
Arterielle Hypertonie
 Arterielle Hypertonie META... 1 Definitionen... 1 Primäre (essentielle) Hypertonie... 1 Sekundäre Hypertonie... 1 Blutdruckmessung... 2 Anamnese... 2 Klinische Untersuchung... 3 Laboruntersuchungen...
Arterielle Hypertonie META... 1 Definitionen... 1 Primäre (essentielle) Hypertonie... 1 Sekundäre Hypertonie... 1 Blutdruckmessung... 2 Anamnese... 2 Klinische Untersuchung... 3 Laboruntersuchungen...
Check-up 2012 Aus der Sicht des Kardiologen
 Check-up 2012 Aus der Sicht des Kardiologen - Fallbeispiele - Aktive Diskussion Fallbeispiel 1: Mann, 51 j., Gesund, wünscht Check up PA «bland» FA: Vater 79j. (behandelte Hypertonie, Dyslipidämie),
Check-up 2012 Aus der Sicht des Kardiologen - Fallbeispiele - Aktive Diskussion Fallbeispiel 1: Mann, 51 j., Gesund, wünscht Check up PA «bland» FA: Vater 79j. (behandelte Hypertonie, Dyslipidämie),
Innovative und multifaktorielle Therapie des Diabetes mellitus Typ 2
 Innovative und multifaktorielle Therapie des Diabetes mellitus Typ 2 Prim. Dr. Edwin Halmschlager Stoffwechsel-Rehabilitation Lebens.Resort Ottenschlag Zahl der Diabetiker weltweit nach Daten der WHO 1980
Innovative und multifaktorielle Therapie des Diabetes mellitus Typ 2 Prim. Dr. Edwin Halmschlager Stoffwechsel-Rehabilitation Lebens.Resort Ottenschlag Zahl der Diabetiker weltweit nach Daten der WHO 1980
Was kann ich gegen das Auftreten von Spätkomplikationen tun?
 Interdisziplinäres Stoffwechsel-Centrum Charité Campus Virchow Klinikum Was kann ich gegen das Auftreten von Spätkomplikationen tun? Bettina Otte Assistenzärztin Blutzuckereinstellung Ursache aller Spätkomplikationen
Interdisziplinäres Stoffwechsel-Centrum Charité Campus Virchow Klinikum Was kann ich gegen das Auftreten von Spätkomplikationen tun? Bettina Otte Assistenzärztin Blutzuckereinstellung Ursache aller Spätkomplikationen
Kardiovaskuläres Manual
 Kardiovaskuläres Manual 4. Auflage 2015 Endotheliale Dysfunktion Inflammation Oxidation zum Inhaltsverzeichnis Plaque-Instabilität und Thrombus Nach: Libby P. Circulation 2001;104:365 372; Ross R. N Engl
Kardiovaskuläres Manual 4. Auflage 2015 Endotheliale Dysfunktion Inflammation Oxidation zum Inhaltsverzeichnis Plaque-Instabilität und Thrombus Nach: Libby P. Circulation 2001;104:365 372; Ross R. N Engl
Arterielle Hypertonie Update 2012
 18. Engadiner Fortbildungstage Scuol / 09.09.2012 Arterielle Hypertonie Update 2012 Prof. P. Greminger Allgemeine Innere Medizin Kantonsspital St.Gallen BLUTDRUCKMESSUNG Bestätigung erhöhter Blutdruckwerte
18. Engadiner Fortbildungstage Scuol / 09.09.2012 Arterielle Hypertonie Update 2012 Prof. P. Greminger Allgemeine Innere Medizin Kantonsspital St.Gallen BLUTDRUCKMESSUNG Bestätigung erhöhter Blutdruckwerte
Risikofaktor Cholesterin Gute und schlechte Blutfette? Was ist dran an der Cholesterinlüge?
 Medizinische Klinik und Poliklinik II Kardiologie / Pneumologie / Angiologie Risikofaktor Cholesterin Gute und schlechte Blutfette? Was ist dran an der Cholesterinlüge? Dr. med. M. Vasa-Nicotera Oberärztin
Medizinische Klinik und Poliklinik II Kardiologie / Pneumologie / Angiologie Risikofaktor Cholesterin Gute und schlechte Blutfette? Was ist dran an der Cholesterinlüge? Dr. med. M. Vasa-Nicotera Oberärztin
Herzinsuffizienz wie kann das Pumpversagen vermieden (und behandelt) werden?
 Nottwil, 13. April 2013 Herzinsuffizienz wie kann das Pumpversagen vermieden (und behandelt) werden? René Lerch, Genève Spätkomplikationen des Herzinfarkts Erneuter Infarkt Plötzlicher Herztod 10 30 %
Nottwil, 13. April 2013 Herzinsuffizienz wie kann das Pumpversagen vermieden (und behandelt) werden? René Lerch, Genève Spätkomplikationen des Herzinfarkts Erneuter Infarkt Plötzlicher Herztod 10 30 %
Hochdruck Mikrozirkulation
 Hochdruck Mikrozirkulation Teil I C.M. Schannwell Häufigkeit von Bluthochdruck in Deutschland ca. 16 Millionen insgesamt (20%) 11 Millionen bekannt 5 Millionen unbekannt 9 Millionen therapiert 2 Millionen
Hochdruck Mikrozirkulation Teil I C.M. Schannwell Häufigkeit von Bluthochdruck in Deutschland ca. 16 Millionen insgesamt (20%) 11 Millionen bekannt 5 Millionen unbekannt 9 Millionen therapiert 2 Millionen
Update Antihypertensiva
 Update Antihypertensiva Dr. med. Markus Diethelm 26.11.2015 Blutdruck-Zielwerte für Europa ESC/ESH 2004 2007 2013 < 140/90 < 140/90 < 140/90 Vaskuläre Erkrankung* < 130/80 < 130/80 < 140/90 Diabetes mellitus
Update Antihypertensiva Dr. med. Markus Diethelm 26.11.2015 Blutdruck-Zielwerte für Europa ESC/ESH 2004 2007 2013 < 140/90 < 140/90 < 140/90 Vaskuläre Erkrankung* < 130/80 < 130/80 < 140/90 Diabetes mellitus
C Calcium-Antagonisten 60 ff Nebenwirkungen 61 Captopril 46, 50 Prevention Project 51 Carvedilol 59 Claudicatio intermittens 48
 Sachverzeichnis Sachverzeichnis 87 A Abdomen-Sonographie 38 ACE-Hemmer s. Angiotensin- Converting-Enzym-Hemmer Adipositas 5 Adressen 81 Aktivität, körperliche 44 Albuminurie Definition 37 Rückgang unter
Sachverzeichnis Sachverzeichnis 87 A Abdomen-Sonographie 38 ACE-Hemmer s. Angiotensin- Converting-Enzym-Hemmer Adipositas 5 Adressen 81 Aktivität, körperliche 44 Albuminurie Definition 37 Rückgang unter
Wenn der Druck zunimmt - Bluthochdruck und Übergewicht
 Wenn der Druck zunimmt - Bluthochdruck und Übergewicht Dr. med. Arnd J. Busmann Dobbenweg 12, 28203 Bremen praxis-dobbenweg.de Themen des Vortrags Ursachen und Folgen von Übergewicht und Bluthochdruck
Wenn der Druck zunimmt - Bluthochdruck und Übergewicht Dr. med. Arnd J. Busmann Dobbenweg 12, 28203 Bremen praxis-dobbenweg.de Themen des Vortrags Ursachen und Folgen von Übergewicht und Bluthochdruck
Kardiovaskuläres Manual
 Kardiovaskuläres Manual 2011 Endotheliale Dysfunktion Inflammation Oxidation Plaque-Instabilität und Thrombus Nach: Libby P. Circulation. 2001;104:365 372; Ross R. N Engl J Med. 1999;340:115 126. Tipp:
Kardiovaskuläres Manual 2011 Endotheliale Dysfunktion Inflammation Oxidation Plaque-Instabilität und Thrombus Nach: Libby P. Circulation. 2001;104:365 372; Ross R. N Engl J Med. 1999;340:115 126. Tipp:
Der hypertensive Notfall
 Der hypertensive Notfall Update Kardiologie 2013 Stefan Brunner Medizinische Klinik und Poliklinik I Stefan Brunner Anamnese 62 jähriger Patient Angestellter Kreisverwaltungsreferat Anamnese Akut aufgetretene
Der hypertensive Notfall Update Kardiologie 2013 Stefan Brunner Medizinische Klinik und Poliklinik I Stefan Brunner Anamnese 62 jähriger Patient Angestellter Kreisverwaltungsreferat Anamnese Akut aufgetretene
Fortbildung First-Responder
 Puls tasten- WO? Säuglinge Kinder > 1 Jahr A. brachialis A. carotis communis Herzdruckmassage Frequenz: zwischen 100 und 120 Mindestens 1/3 des Thoraxdurchmessers Säuglinge: 4cm Kinder > 1 Jahr: 5cm Herzdruckmassage
Puls tasten- WO? Säuglinge Kinder > 1 Jahr A. brachialis A. carotis communis Herzdruckmassage Frequenz: zwischen 100 und 120 Mindestens 1/3 des Thoraxdurchmessers Säuglinge: 4cm Kinder > 1 Jahr: 5cm Herzdruckmassage
ALS- Advanced Life Support
 ALS- Advanced Life Support - Update der ERC-Leitlinien 2010 - Anne Osmers Klinik für Anästhesiologie und Intensivtherapie Universitätsklinikum Dresden ALS - Themen Minimale Unterbrechungen einer effektiven
ALS- Advanced Life Support - Update der ERC-Leitlinien 2010 - Anne Osmers Klinik für Anästhesiologie und Intensivtherapie Universitätsklinikum Dresden ALS - Themen Minimale Unterbrechungen einer effektiven
Grundlagen der Medizinischen Klinik I + II. Dr. Friedrich Mittermayer Dr. Katharina Krzyzanowska
 Grundlagen der Medizinischen Klinik I + II Dr. Friedrich Mittermayer Dr. Katharina Krzyzanowska 1 Was ist Bluthochdruck? Der ideale Blutdruck liegt bei 120/80 mmhg. Bluthochdruck (Hypertonie) ist eine
Grundlagen der Medizinischen Klinik I + II Dr. Friedrich Mittermayer Dr. Katharina Krzyzanowska 1 Was ist Bluthochdruck? Der ideale Blutdruck liegt bei 120/80 mmhg. Bluthochdruck (Hypertonie) ist eine
Voruntersuchungen. Klinik für Anästhesiologie und Intensivmedizin
 Voruntersuchungen ASA Klassifikation Grundlagen für apparative, technische Untersuchungen entscheidende Grundlagen zur Indikation jeder präoperativen technischen Untersuchung: - Erhebung einer sorgfältigen
Voruntersuchungen ASA Klassifikation Grundlagen für apparative, technische Untersuchungen entscheidende Grundlagen zur Indikation jeder präoperativen technischen Untersuchung: - Erhebung einer sorgfältigen
Das metabolische Syndrom
 Das metabolische Syndrom IDF = International Diabetes Foundation Voraussetzung für das metabolische Syndrom: zentrale Adipositas (bauchbetonte Fettleibigkeit Taillenumfang >94 cm bei Männern, >80 cm bei
Das metabolische Syndrom IDF = International Diabetes Foundation Voraussetzung für das metabolische Syndrom: zentrale Adipositas (bauchbetonte Fettleibigkeit Taillenumfang >94 cm bei Männern, >80 cm bei
Der Akute Herzinfarkt. R. Urbien, Arzt in Weiterbildung, Medizinische Klinik II, Katholisches Klinikum Essen, Philippusstift
 Der Akute Herzinfarkt R. Urbien, Arzt in Weiterbildung, Medizinische Klinik II, Katholisches Klinikum Essen, Philippusstift Koronare Herzerkrankung (KHK) Manifestation der Atherosklerose an den Herzkranzarterien
Der Akute Herzinfarkt R. Urbien, Arzt in Weiterbildung, Medizinische Klinik II, Katholisches Klinikum Essen, Philippusstift Koronare Herzerkrankung (KHK) Manifestation der Atherosklerose an den Herzkranzarterien
Stufendiagnostik der KHK. Anamnese
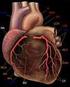 Risikofaktoren für KHK Westfälische Wilhelms- Universität Münster Diagnostik der KHK Anamnese Ischämie-Nachweis Hyperlipoproteinämie LDL-Cholesterin Lp(a) nicht modifizierbar Nikotinabusus Prof. Dr. med.
Risikofaktoren für KHK Westfälische Wilhelms- Universität Münster Diagnostik der KHK Anamnese Ischämie-Nachweis Hyperlipoproteinämie LDL-Cholesterin Lp(a) nicht modifizierbar Nikotinabusus Prof. Dr. med.
Swiss Adopted International (IAS-AGLA) and European Atherosclerosis Society (EAS- SCORE) Guidelines for LDL Lowering Therapy in Primary Care:
 Swiss Adopted International (IAS-AGLA) and European Atherosclerosis Society (EAS- SCORE) Guidelines for LDL Lowering Therapy in Primary Care: Initial Experience of Cordicare I: a Population Based Sample
Swiss Adopted International (IAS-AGLA) and European Atherosclerosis Society (EAS- SCORE) Guidelines for LDL Lowering Therapy in Primary Care: Initial Experience of Cordicare I: a Population Based Sample
Diabetes mellitus Spätschäden früh erkennen und richtig behandeln
 Diabetes mellitus Spätschäden früh erkennen und richtig behandeln Dr. Roman Iakoubov - Diabetesambulanz - II. Medizinische Klinik Klinikum rechts der Isar Diabetes und Spätfolgen Diabetes mellitus Überblick
Diabetes mellitus Spätschäden früh erkennen und richtig behandeln Dr. Roman Iakoubov - Diabetesambulanz - II. Medizinische Klinik Klinikum rechts der Isar Diabetes und Spätfolgen Diabetes mellitus Überblick
Diabetes mellitus Typ 2 Erstdokumentation
 Diabetes mellitus Typ 2 Ziffer 5 Dokumentation 1 DMP-Fallnummer vom Arzt zu vergeben Administrative Daten 2 Krankenkasse bzw. Kostenträger Name der Kasse Name der Kasse 3 Name, Vorname des Versicherten
Diabetes mellitus Typ 2 Ziffer 5 Dokumentation 1 DMP-Fallnummer vom Arzt zu vergeben Administrative Daten 2 Krankenkasse bzw. Kostenträger Name der Kasse Name der Kasse 3 Name, Vorname des Versicherten
Der Bundesausschuß der Ärzte und Krankenkassen hat am 8. Januar 1999 die Neufassung
 Medikamentöse Therapie von Fettstoffwechselstörungen Die Arzneimittelrichtlinien des Bundesausschusses der Ärzte und Krankenkassen Der Bundesausschuß der Ärzte und Krankenkassen hat am 8. Januar 1999 die
Medikamentöse Therapie von Fettstoffwechselstörungen Die Arzneimittelrichtlinien des Bundesausschusses der Ärzte und Krankenkassen Der Bundesausschuß der Ärzte und Krankenkassen hat am 8. Januar 1999 die
Hypertonie. Prof. Dr. David Conen MPH Innere Medizin
 Hypertonie Prof. Dr. David Conen MPH Innere Medizin Erstkonsultation eines 65-jährigen Mannes, ohne relevante Vorerkrankungen, keine Medikamente, klinischer Blutdruck 170/100 mmhg, EKG mit LVH. Welches
Hypertonie Prof. Dr. David Conen MPH Innere Medizin Erstkonsultation eines 65-jährigen Mannes, ohne relevante Vorerkrankungen, keine Medikamente, klinischer Blutdruck 170/100 mmhg, EKG mit LVH. Welches
Reanimation: Advanced Life Support (ERC 2015)
 Reanimation: Advanced Life Support (ERC 2015) Keine Reaktion? keine normale Atmung? Notarzt alarmieren Kardiopulmonale Reanimation (CPR) 30:2 Defibrillator / EKG - Monitor anschließen EKG - Rhythmus beurteilen
Reanimation: Advanced Life Support (ERC 2015) Keine Reaktion? keine normale Atmung? Notarzt alarmieren Kardiopulmonale Reanimation (CPR) 30:2 Defibrillator / EKG - Monitor anschließen EKG - Rhythmus beurteilen
Medikamentengabe zur. Reanimation von Säuglingen & Kindern
 SOP Standardanweisung für alle Rettungsassistenten in RLP schnell kompetent mitmenschlich Gültig ab 2014-10-01 Medikamentengabe zur erweiterten Versorgung während der Reanimation von Säuglingen & Kindern
SOP Standardanweisung für alle Rettungsassistenten in RLP schnell kompetent mitmenschlich Gültig ab 2014-10-01 Medikamentengabe zur erweiterten Versorgung während der Reanimation von Säuglingen & Kindern
Niereninsuffizienz als kardiovaskulärer Risikofaktor
 Bayerischer Internistenkongress München, 07.-08.11.2009 Niereninsuffizienz als kardiovaskulärer Risikofaktor Ulf Schönermarck Schwerpunkt Nephrologie Medizinische Klinik I Klinikum der Universität München
Bayerischer Internistenkongress München, 07.-08.11.2009 Niereninsuffizienz als kardiovaskulärer Risikofaktor Ulf Schönermarck Schwerpunkt Nephrologie Medizinische Klinik I Klinikum der Universität München
Kardiologische Notfälle. Micha T. Maeder Kardiologie KSSG
 Kardiologische Notfälle Micha T. Maeder Kardiologie KSSG Akutes Koronarsyndrom Schmerz 12-Ableitungs-EKG ST-Hebung >1 mm in 2 benachbarten Extremitätenableitungen oder >2 mm in zwei benachbarten Brustwandableitungen
Kardiologische Notfälle Micha T. Maeder Kardiologie KSSG Akutes Koronarsyndrom Schmerz 12-Ableitungs-EKG ST-Hebung >1 mm in 2 benachbarten Extremitätenableitungen oder >2 mm in zwei benachbarten Brustwandableitungen
Zusammenhänge zwischen Übergewicht / Gewichtszunahme und Stoffwechselerkrankungen
 Zusammenhänge zwischen Übergewicht / Gewichtszunahme und Stoffwechselerkrankungen Robert A. Ritzel Klinik für Endokrinologie, Diabetologie und Suchtmedizin Nuklearmedizin Klinikum Schwabing Städtisches
Zusammenhänge zwischen Übergewicht / Gewichtszunahme und Stoffwechselerkrankungen Robert A. Ritzel Klinik für Endokrinologie, Diabetologie und Suchtmedizin Nuklearmedizin Klinikum Schwabing Städtisches
Bluthochdruck und das metabolische Syndrom bei Kindern wer wird behandelt und wie?
 Bluthochdruck und das metabolische Syndrom bei Kindern wer wird behandelt und wie? Andreas Hanslik Abteilung für Pädiatrische Kardiologie, Medizinische Universität Wien Metabolisches Syndrom Definition
Bluthochdruck und das metabolische Syndrom bei Kindern wer wird behandelt und wie? Andreas Hanslik Abteilung für Pädiatrische Kardiologie, Medizinische Universität Wien Metabolisches Syndrom Definition
Arterielle Hypertonie im Kindes- und Jugendalter. W. Siekmeyer Universitätsklinik für Kinder und Jugendliche Leipzig
 W. Siekmeyer Universitätsklinik für Kinder und Jugendliche Leipzig Definition: RR > P 95: Hypertonie RR > P 90 und < P 95: prähypertensiver Wert Werte ab 120/80 mmhg sollten immer mindestens als prähypertensiv
W. Siekmeyer Universitätsklinik für Kinder und Jugendliche Leipzig Definition: RR > P 95: Hypertonie RR > P 90 und < P 95: prähypertensiver Wert Werte ab 120/80 mmhg sollten immer mindestens als prähypertensiv
Behandlung der arteriellen Hypertonie - Wie lautet der Zielwert 2016?
 Behandlung der arteriellen Hypertonie - Wie lautet der Zielwert 2016? Hannes Reuter Klinik III für Innere Medizin Herzzentrum der Universität zu Köln Patient 1 Risikofaktoren: Blutdruck 167/96 mmhg Typ
Behandlung der arteriellen Hypertonie - Wie lautet der Zielwert 2016? Hannes Reuter Klinik III für Innere Medizin Herzzentrum der Universität zu Köln Patient 1 Risikofaktoren: Blutdruck 167/96 mmhg Typ
Der Patient mit Hypercholesterinämie
 Der Patient mit Hypercholesterinämie Cholesterintherapie Ja/Nein - wie - Zielwert Fall 1: 51 j. Mann, St. n. STEMI 10/2015, DES RIVA 10/2015, EF 40%, LDL 3.5 mmol/l Fall 2: 49 j. Mann, art. Hypertonie,
Der Patient mit Hypercholesterinämie Cholesterintherapie Ja/Nein - wie - Zielwert Fall 1: 51 j. Mann, St. n. STEMI 10/2015, DES RIVA 10/2015, EF 40%, LDL 3.5 mmol/l Fall 2: 49 j. Mann, art. Hypertonie,
Leitlinien Reanimation 2015
 Leitlinien Reanimation 2015 Basismaßnahmen Überlebenskette Leitstelle Die neuen Leitlinien 2015 betonen die Interaktion zwischen Leitstelle, dem Wiederbelebung durchführenden Zeugen und der zeitnahen Verfügbarkeit
Leitlinien Reanimation 2015 Basismaßnahmen Überlebenskette Leitstelle Die neuen Leitlinien 2015 betonen die Interaktion zwischen Leitstelle, dem Wiederbelebung durchführenden Zeugen und der zeitnahen Verfügbarkeit
Unverändert höheres Risikoprofil von Frauen in der Sekundärprävention der KHK Sechs-Jahres-Verlauf an Patienten
 Deutsche Gesellschaft für Kardiologie Herz- und Kreislaufforschung e.v. (DGK) Achenbachstr. 43, 40237 Düsseldorf Geschäftsstelle: Tel: 0211 6006920 Fax: 0211 60069267 mail : [email protected] Pressestelle:
Deutsche Gesellschaft für Kardiologie Herz- und Kreislaufforschung e.v. (DGK) Achenbachstr. 43, 40237 Düsseldorf Geschäftsstelle: Tel: 0211 6006920 Fax: 0211 60069267 mail : [email protected] Pressestelle:
Update Reanimationsrichtlinien Nayan Paul, Kardiologie & Angiologie / BLS Tutor
 Update Reanimationsrichtlinien 2015, Kardiologie & Angiologie / BLS Tutor Übersicht Wichtigste Änderungen der BLS-AED - Leitlinien vom 15.10.2015 Neuer Universal-Algorithmus des SRC In der Präsentation
Update Reanimationsrichtlinien 2015, Kardiologie & Angiologie / BLS Tutor Übersicht Wichtigste Änderungen der BLS-AED - Leitlinien vom 15.10.2015 Neuer Universal-Algorithmus des SRC In der Präsentation
Diabetiker mit häufigen Stürzen und Schwindel
 diabetes - sprechstunde Prof. Dr. med. Roger Lehmann Zürich Prof. Dr. med. Jaques Philippe Genf Vignette 1 : Diabetiker mit häufigen Stürzen und Schwindel Ausgangssituation : Ein 73-jähriger Mann, seit
diabetes - sprechstunde Prof. Dr. med. Roger Lehmann Zürich Prof. Dr. med. Jaques Philippe Genf Vignette 1 : Diabetiker mit häufigen Stürzen und Schwindel Ausgangssituation : Ein 73-jähriger Mann, seit
DIE HYPERTENSIVE KRISE. Prim. Univ.Prof. Dr. Michael M. Hirschl. Vorstand der Abteilung für Innere Medizin. Landesklinikum Zwettl
 DIE HYPERTENSIVE KRISE Prim. Univ.Prof. Dr. Michael M. Hirschl Vorstand der Abteilung für Innere Medizin Landesklinikum Zwettl ALLGEMEIN Patienten mit einem hypertensiven Notfall stellen einen erheblichen
DIE HYPERTENSIVE KRISE Prim. Univ.Prof. Dr. Michael M. Hirschl Vorstand der Abteilung für Innere Medizin Landesklinikum Zwettl ALLGEMEIN Patienten mit einem hypertensiven Notfall stellen einen erheblichen
Bluthochdruck. (Hypertonie)
 (Hypertonie) Copyright by HEXAL AG 2008 Was ist der Blutdruck? Damit das Blut alle Organe und auch die kleinsten Kapillargefäße erreichen kann, muss es mit einem gewissen Druck aus dem Herzen gepumpt werden.
(Hypertonie) Copyright by HEXAL AG 2008 Was ist der Blutdruck? Damit das Blut alle Organe und auch die kleinsten Kapillargefäße erreichen kann, muss es mit einem gewissen Druck aus dem Herzen gepumpt werden.
Geschlechtsperspektiven in der Medizin - Gesundheits- und fachpolitische Herausforderungen nach Erkenntnissen bei Diabetes
 fröhlich aber auch gesund? Geschlechtsperspektiven in der Medizin - Gesundheits- und fachpolitische Herausforderungen nach Erkenntnissen bei Diabetes Petra-Maria Schumm-Draeger Städtisches Klinikum München
fröhlich aber auch gesund? Geschlechtsperspektiven in der Medizin - Gesundheits- und fachpolitische Herausforderungen nach Erkenntnissen bei Diabetes Petra-Maria Schumm-Draeger Städtisches Klinikum München
Diabetes mellitus und Niereninsuffizienz: Ein Überblick
 Diabetes mellitus und Niereninsuffizienz: Ein Überblick Folgekrankheiten in den USA Diabetiker mit Visusstörung: Diabetiker neu an HD ab 1980 Folgeerkrankungen beim Diabetes NEJM 2014; 1514 Anteil Diabetiker
Diabetes mellitus und Niereninsuffizienz: Ein Überblick Folgekrankheiten in den USA Diabetiker mit Visusstörung: Diabetiker neu an HD ab 1980 Folgeerkrankungen beim Diabetes NEJM 2014; 1514 Anteil Diabetiker
Sind dicke Kinder auch kranke Kinder? Gesundheitsrisiken und Folgeerkrankungen des Uebergewichtes im Kindes- und Jugendalter
 Sind dicke Kinder auch kranke Kinder? Gesundheitsrisiken und Folgeerkrankungen des Uebergewichtes im Kindes- und Jugendalter Dr. Gabor Szinnai Abteilung Endokrinologie und Diabetologie Universitäts-Kinderspital
Sind dicke Kinder auch kranke Kinder? Gesundheitsrisiken und Folgeerkrankungen des Uebergewichtes im Kindes- und Jugendalter Dr. Gabor Szinnai Abteilung Endokrinologie und Diabetologie Universitäts-Kinderspital
Atemnot Herzinsuffizienz oder ACS?
 Atemnot Herzinsuffizienz oder ACS? Michael J. Zellweger Kardiologische Klinik Universitätsspital Basel Breite DD Brainstorming Ruhedyspnoe Husten Schwäche Miktionsprobleme HIV unbehandelt CDC B3 Adipositas
Atemnot Herzinsuffizienz oder ACS? Michael J. Zellweger Kardiologische Klinik Universitätsspital Basel Breite DD Brainstorming Ruhedyspnoe Husten Schwäche Miktionsprobleme HIV unbehandelt CDC B3 Adipositas
1 Symptome und Krankheitsbilder des Diabetes mellitus 1
 VII Inhaltsverzeichnis 1 Symptome und Krankheitsbilder des Diabetes mellitus 1 1.1 Diabetisches Koma 3 1.2 Folgeerkrankungen bei Diabetes mellitus 3 1.3 Typ-1 - versus Typ-2-Diabetes 4 2 Labordiagnostik
VII Inhaltsverzeichnis 1 Symptome und Krankheitsbilder des Diabetes mellitus 1 1.1 Diabetisches Koma 3 1.2 Folgeerkrankungen bei Diabetes mellitus 3 1.3 Typ-1 - versus Typ-2-Diabetes 4 2 Labordiagnostik
Nierenerkrankung - Welchen Einfluss hat der Bluthochdruck?
 Nierenerkrankung - Welchen Einfluss hat der Bluthochdruck? Dr. med. Arnd J. Busmann Dobbenweg 12, 28203 Bremen praxis-dobbenweg.de Chronische Niereninsuffizienz = Nierenschwäche Ursachen: Diabetes mellitus,
Nierenerkrankung - Welchen Einfluss hat der Bluthochdruck? Dr. med. Arnd J. Busmann Dobbenweg 12, 28203 Bremen praxis-dobbenweg.de Chronische Niereninsuffizienz = Nierenschwäche Ursachen: Diabetes mellitus,
European Resuscitation Council
 European Resuscitation Council Generelle Überlegungen Bei Kindern sind Arrhythmien meistens Folgen von Hypoxien, Azidosen und Hypotension Primär kardiologische Erkrankungen sind eher selten Das Monitoring
European Resuscitation Council Generelle Überlegungen Bei Kindern sind Arrhythmien meistens Folgen von Hypoxien, Azidosen und Hypotension Primär kardiologische Erkrankungen sind eher selten Das Monitoring
Anhang III. Änderungen der entsprechenden Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilagen
 Anhang III Änderungen der entsprechenden Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilagen Anmerkung: Diese Änderungen der entsprechenden Abschnitte der Zusammenfassung
Anhang III Änderungen der entsprechenden Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilagen Anmerkung: Diese Änderungen der entsprechenden Abschnitte der Zusammenfassung
Study Guide Klinik für Kardiologie, Pneumologie und Angiologie
 Study Guide Klinik für Kardiologie, Pneumologie und Angiologie Task: Schwindel [75] Autoren: Dr. med. S. Keymel/Univ.-Prof. Dr. med. T. Rassaf unter Mitarbeit von Dr. med. V.T. Schulze Version 02.10.2013
Study Guide Klinik für Kardiologie, Pneumologie und Angiologie Task: Schwindel [75] Autoren: Dr. med. S. Keymel/Univ.-Prof. Dr. med. T. Rassaf unter Mitarbeit von Dr. med. V.T. Schulze Version 02.10.2013
Der Diabetes liegt mir am Herzen
 Der Diabetes liegt mir am Herzen Priv.Doz. Dr. med. Frank Muders Fachärztliche Gemeinschaftspraxis für Innere Medizin und Kardiologie, Ärztehaus Weiden Diabetikeradern altern schneller Gefäßwandveränderungen
Der Diabetes liegt mir am Herzen Priv.Doz. Dr. med. Frank Muders Fachärztliche Gemeinschaftspraxis für Innere Medizin und Kardiologie, Ärztehaus Weiden Diabetikeradern altern schneller Gefäßwandveränderungen
Man ist so alt wie seine Gefäße Koronare Herzkrankheit Schlaganfall Prävention Diagnostik - Therapie
 Man ist so alt wie seine Gefäße Koronare Herzkrankheit Schlaganfall Prävention Diagnostik - Therapie Priv.-Doz.Dr.L.Pizzulli Innere Medizin Kardiologie Herz-und Gefäßzentrum Rhein-Ahr Gemeinschaftskrankenhaus
Man ist so alt wie seine Gefäße Koronare Herzkrankheit Schlaganfall Prävention Diagnostik - Therapie Priv.-Doz.Dr.L.Pizzulli Innere Medizin Kardiologie Herz-und Gefäßzentrum Rhein-Ahr Gemeinschaftskrankenhaus
Prähospital-Phase: Time is Brain Erkennen des cerebrovaskulären Ereignisses und schnelle Zuweisung an eine Stroke Unit
 1 Prähospital-Phase: Time is Brain Erkennen des cerebrovaskulären Ereignisses und schnelle Zuweisung an eine Stroke Unit Interdisziplinäre Fortbildung für niedergelassene Ärzte und Spezialisten Donnerstag,
1 Prähospital-Phase: Time is Brain Erkennen des cerebrovaskulären Ereignisses und schnelle Zuweisung an eine Stroke Unit Interdisziplinäre Fortbildung für niedergelassene Ärzte und Spezialisten Donnerstag,
Diabetes mellitus Typ 2 kardiovaskuläre Risikofaktoren
 Diabetes mellitus Typ 2 kardiovaskuläre Risikofaktoren nicht-medikamentöse Ansätze Dr. Claudine Falconnier Bendik Take Home Messages Früh übt sich, was ein Meister werden will Was Hänschen nicht lernt,
Diabetes mellitus Typ 2 kardiovaskuläre Risikofaktoren nicht-medikamentöse Ansätze Dr. Claudine Falconnier Bendik Take Home Messages Früh übt sich, was ein Meister werden will Was Hänschen nicht lernt,
Obstruktive Schlafapnoe: Risikofaktoren, Therapie und kardiovaskuläre Konsequenzen
 Obstruktive Schlafapnoe: Risikofaktoren, Therapie und kardiovaskuläre Konsequenzen Bernd Sanner Agaplesion Bethesda Krankenhaus Wuppertal Schlafapnoe - Epidemiologie 2-4% der erwachsenen Bevölkerung sind
Obstruktive Schlafapnoe: Risikofaktoren, Therapie und kardiovaskuläre Konsequenzen Bernd Sanner Agaplesion Bethesda Krankenhaus Wuppertal Schlafapnoe - Epidemiologie 2-4% der erwachsenen Bevölkerung sind
Mittwoch, 14 bis 18 Uhr: für Praxispersonal Lehrverhaltenstraining. Donnerstag, 9 bis 17 Uhr: für Praxispersonal Lehrverhaltenstraining
 Behandlungs- und Schulungsprogramm für Patienten mit Hypertonie Mittwoch, 14 bis 18 Uhr: für Ärzte und Praxispersonal Vorstellung des Behandlungs- und Schulungsprogramms, Diskussion über Therapie und Praxisorganisation
Behandlungs- und Schulungsprogramm für Patienten mit Hypertonie Mittwoch, 14 bis 18 Uhr: für Ärzte und Praxispersonal Vorstellung des Behandlungs- und Schulungsprogramms, Diskussion über Therapie und Praxisorganisation
Vorwort zur 2. Auflage... Abkürzungsverzeichnis...
 IX Vorwort zur 2. Auflage......................................... Abkürzungsverzeichnis......................................... VII XV 1 Situation der Diabetes betreuung................... 1 1.1 Epidemiologie.......................................
IX Vorwort zur 2. Auflage......................................... Abkürzungsverzeichnis......................................... VII XV 1 Situation der Diabetes betreuung................... 1 1.1 Epidemiologie.......................................
Naim Abujarour Facharzt für Innere Medizin und Kardiologie
 Herz und Diabetes Naim Abujarour Facharzt für Innere Medizin und Kardiologie Inhalt Definition Diabetes Zahlen und Fakten Diabetestherapie Folgen von Diabetes KHK (Definition, Symptome, Folgen, Diagnostik,
Herz und Diabetes Naim Abujarour Facharzt für Innere Medizin und Kardiologie Inhalt Definition Diabetes Zahlen und Fakten Diabetestherapie Folgen von Diabetes KHK (Definition, Symptome, Folgen, Diagnostik,
Metabolisches Syndrom was ist das eigentlich?
 Metabolisches Syndrom, Diabetes und KHK Volkskrankheiten auf dem Vormarsch Dr. med. Axel Preßler Lehrstuhl und Poliklinik für Präventive und Rehabilitative Sportmedizin Klinikum rechts der Isar TU München
Metabolisches Syndrom, Diabetes und KHK Volkskrankheiten auf dem Vormarsch Dr. med. Axel Preßler Lehrstuhl und Poliklinik für Präventive und Rehabilitative Sportmedizin Klinikum rechts der Isar TU München
Beratungskommission für Apherese-Behandlungen
 Beratungskommission für Apherese-Behandlungen Fragebogen zur Indikationsbeurteilung der LDL-Apherese entsprechend der Anlage I Ziffer 1 zu den Richtlinien Methoden vertragsärztliche Versorgung gemäß 135
Beratungskommission für Apherese-Behandlungen Fragebogen zur Indikationsbeurteilung der LDL-Apherese entsprechend der Anlage I Ziffer 1 zu den Richtlinien Methoden vertragsärztliche Versorgung gemäß 135
Koronare Herzkrankheit Ziffer 5 Dokumentation
 Koronare Herzkrankheit Ziffer 5 Dokumentation 1 DMP-Fallnummer vom Arzt zu vergeben Administrative Daten 2 Krankenkasse bzw. Kostenträger Name der Kasse Name der Kasse 3 Name, Vorname des Versicherten
Koronare Herzkrankheit Ziffer 5 Dokumentation 1 DMP-Fallnummer vom Arzt zu vergeben Administrative Daten 2 Krankenkasse bzw. Kostenträger Name der Kasse Name der Kasse 3 Name, Vorname des Versicherten
Koronare Herzerkrankung Diagnostik nicht-invasiv
 nicht-invasiv 25. November 2014 Univ.-Prof. Dr. med. Johannes Waltenberger Professor für Innere Medizin, Kardiologie und Angiologie Direktor der Klinik für Kardiologie Leiter des Departments für Kardiologie
nicht-invasiv 25. November 2014 Univ.-Prof. Dr. med. Johannes Waltenberger Professor für Innere Medizin, Kardiologie und Angiologie Direktor der Klinik für Kardiologie Leiter des Departments für Kardiologie
Leitliniengerechte Gerinnungshemmung bei Vorhofflimmern und KHK
 Leitliniengerechte Gerinnungshemmung bei Vorhofflimmern und KHK Dr. med. Murat Nar Ambulantes Herz-Kreislaufzentrum Wolfsburg Vorhofflimmern - Inzidenz Vorhofflimmern ist die häufigste anhaltende Herzrhythmusstörung.
Leitliniengerechte Gerinnungshemmung bei Vorhofflimmern und KHK Dr. med. Murat Nar Ambulantes Herz-Kreislaufzentrum Wolfsburg Vorhofflimmern - Inzidenz Vorhofflimmern ist die häufigste anhaltende Herzrhythmusstörung.
Risikofaktoren und Krankheitsentstehung
 Risikofaktoren und Krankheitsentstehung Dr.med.Bernhard Spoendlin Herzpraxis am Rhein Was ist der Unterschied zwischen einer Reparatur und der Prävention? ? Was ist der Unterschied zwischen einer Reparatur
Risikofaktoren und Krankheitsentstehung Dr.med.Bernhard Spoendlin Herzpraxis am Rhein Was ist der Unterschied zwischen einer Reparatur und der Prävention? ? Was ist der Unterschied zwischen einer Reparatur
Arterielle Hypertonie
 Herz und Kreislauf Arterielle Hypertonie M. Fluri Pulse Classic of Wang 280 v.chr. "Leeches and venesection when the puls hardens" Cornelius Celsus 25 v.chr. "erhöhten und härteren Puls bei Sport, Leidenschaft
Herz und Kreislauf Arterielle Hypertonie M. Fluri Pulse Classic of Wang 280 v.chr. "Leeches and venesection when the puls hardens" Cornelius Celsus 25 v.chr. "erhöhten und härteren Puls bei Sport, Leidenschaft
Welches ANTIHYPERTENSIVUM ist wann indiziert? Blutdruck + Lebensalter. Agenda. Bevölkerungspyramiden - Österreich.
 Welches ANTIHYPERTENSIVUM ist wann indiziert? Martin Schumacher Abteilung für Innere Medizin Barmherzige Brüder Marschallgasse 12, 8020 Graz [email protected] Agenda Bedeutung der Hypertonie
Welches ANTIHYPERTENSIVUM ist wann indiziert? Martin Schumacher Abteilung für Innere Medizin Barmherzige Brüder Marschallgasse 12, 8020 Graz [email protected] Agenda Bedeutung der Hypertonie
Adipositas, Diabetes und Schlaganfall Prof. Dr. Joachim Spranger
 Adipositas, Diabetes und Schlaganfall Prof. Dr. Joachim Spranger Charité-Universitätsmedizin Berlin Adipositas- und Stoffwechselzentrum Campus Benjamin Franklin Hindenburgdamm 30 12200 Berlin The New Yorker
Adipositas, Diabetes und Schlaganfall Prof. Dr. Joachim Spranger Charité-Universitätsmedizin Berlin Adipositas- und Stoffwechselzentrum Campus Benjamin Franklin Hindenburgdamm 30 12200 Berlin The New Yorker
T ransiente I schämische A ttacke
 T ransiente I schämische A ttacke Definition: TIA Eine TIA ist ein plötzlich auftretendes fokales neurologisches Defizit,
T ransiente I schämische A ttacke Definition: TIA Eine TIA ist ein plötzlich auftretendes fokales neurologisches Defizit,
Neue Grenzwerte zur Hypertoniebehandlung Prof. N. Rodondi, Leiter MedPol & Chefarzt
 Neue Grenzwerte zur Hypertoniebehandlung, Leiter MedPol & Chefarzt Universitätsklinik und Poliklinik für Allgemeine Innere Medizin Inselspital, Bern Seekongress 2015, Luzern, 10.09.2015 MC Welche Antworten
Neue Grenzwerte zur Hypertoniebehandlung, Leiter MedPol & Chefarzt Universitätsklinik und Poliklinik für Allgemeine Innere Medizin Inselspital, Bern Seekongress 2015, Luzern, 10.09.2015 MC Welche Antworten
Bewertung relevanter pharmakodynamischer Interaktionen von Antidiabetika
 46. Jahrestagung Deutsche-Diabetes Diabetes- Gesellschaft 01.- 04. Juni 2011, Leipzig Bewertung relevanter pharmakodynamischer Interaktionen von Antidiabetika Dr. Nina Griese Zentrum für Arzneimittelinformation
46. Jahrestagung Deutsche-Diabetes Diabetes- Gesellschaft 01.- 04. Juni 2011, Leipzig Bewertung relevanter pharmakodynamischer Interaktionen von Antidiabetika Dr. Nina Griese Zentrum für Arzneimittelinformation
Katholisches Klinikum Essen. Herzinfarkt wie kann man sich schützen? Prof. Dr. med. Birgit Hailer
 Katholisches Klinikum Essen Herzinfarkt wie kann man sich schützen? 11.04.2016 Datum Mitarbeitereinführungstag 1 Prof. Dr. med. Birgit Hailer Akutes Koronarsyndrom Libby P. N Engl J Med 2013;368:2004-2013
Katholisches Klinikum Essen Herzinfarkt wie kann man sich schützen? 11.04.2016 Datum Mitarbeitereinführungstag 1 Prof. Dr. med. Birgit Hailer Akutes Koronarsyndrom Libby P. N Engl J Med 2013;368:2004-2013
Medizin im Vortrag. Herausgeber: Prof. Dr. med. Christoph Frank Dietrich. Koronare Herzkrankheit
 Medizin im Vortrag Herausgeber: Prof. Dr. med. Christoph Frank Dietrich Koronare Herzkrankheit Autoren: Priv.-Doz. Dr. med. Christoph Frank Dietrich Priv.-Doz. Dr. med. Claudius Teupe Text- und Grafikbausteine
Medizin im Vortrag Herausgeber: Prof. Dr. med. Christoph Frank Dietrich Koronare Herzkrankheit Autoren: Priv.-Doz. Dr. med. Christoph Frank Dietrich Priv.-Doz. Dr. med. Claudius Teupe Text- und Grafikbausteine
HERZLICH WILLKOMMEN ST. GALLER DIABETES SYMPOSIUM.
 HERZLICH WILLKOMMEN ST. GALLER DIABETES SYMPOSIUM eswiss Medical & Surgical Center REFERATE REFERATE GRUSS VON Dr. med. Karl Scheidegger Facharzt für Innere Medizin Facharzt Endokrinologie / Diabetologie
HERZLICH WILLKOMMEN ST. GALLER DIABETES SYMPOSIUM eswiss Medical & Surgical Center REFERATE REFERATE GRUSS VON Dr. med. Karl Scheidegger Facharzt für Innere Medizin Facharzt Endokrinologie / Diabetologie
BAnz AT B3. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneitel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneiteln neuen Wirkstoffen nach 35a SGB V Alirocumab
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneitel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneiteln neuen Wirkstoffen nach 35a SGB V Alirocumab
Diabetes mellitus und kardiovaskuläres Risiko: Welches ist die optimale Therapie?
 Diabetes mellitus und kardiovaskuläres Risiko: Welches ist die optimale Therapie? Hannes Reuter Herzzentrum, Klinik III für Innere Medizin Seite 1 Patienten mit Typ 2-Diabetes haben gehäuft ischämische
Diabetes mellitus und kardiovaskuläres Risiko: Welches ist die optimale Therapie? Hannes Reuter Herzzentrum, Klinik III für Innere Medizin Seite 1 Patienten mit Typ 2-Diabetes haben gehäuft ischämische
Reanimation. Stephan Marsch Intensivmedizin
 Reanimation Stephan Marsch Intensivmedizin Die aktuellen Richtlinien für die Kardiopulmonale Reanimation on 2010 empfehlen folgende Massnahmen ausser? A) Beginn der Reanimation mit 2 Atemstössen B) Herzmassage
Reanimation Stephan Marsch Intensivmedizin Die aktuellen Richtlinien für die Kardiopulmonale Reanimation on 2010 empfehlen folgende Massnahmen ausser? A) Beginn der Reanimation mit 2 Atemstössen B) Herzmassage
S3-LEITLINIE ZUR DIAGNOSTIK, THERAPIE UND NACHSORGE DER PERIPHEREN ARTERIELLEN VERSCHLUSSKRANKHEIT
 S3-LEITLINIE ZUR DIAGNOSTIK, THERAPIE UND NACHSORGE DER PERIPHEREN ARTERIELLEN VERSCHLUSSKRANKHEIT Stand: 30. September 2015 95% der Fälle durch Arteriosklerose Herzinfarkt, Schlaganfall und PAVK In ungefähr
S3-LEITLINIE ZUR DIAGNOSTIK, THERAPIE UND NACHSORGE DER PERIPHEREN ARTERIELLEN VERSCHLUSSKRANKHEIT Stand: 30. September 2015 95% der Fälle durch Arteriosklerose Herzinfarkt, Schlaganfall und PAVK In ungefähr
PALS Basic Life Support
 PALS Basic Life Support Bewusstloser Patient keine Atmung, Schnappatmung Alarmieren: 144 Puls Check max. 10 sec kein Puls Puls 1 Beatmung alle 3s Reevaluation nach jeweils 2 min CPR bei Puls
PALS Basic Life Support Bewusstloser Patient keine Atmung, Schnappatmung Alarmieren: 144 Puls Check max. 10 sec kein Puls Puls 1 Beatmung alle 3s Reevaluation nach jeweils 2 min CPR bei Puls
Alte und neue Antidiabetika - Was ist belegt, was ist bewährt, was ist bezahlbar? Dr. Andreas Klinge Hamburg
 Alte und neue Antidiabetika - Was ist belegt, was ist bewährt, was ist bezahlbar? Dr. Andreas Klinge Hamburg Keine Interessenkonflikte Was ist belegt? Menschen mit Typ 2-Diabetes 1. Stufe Basistherapie:
Alte und neue Antidiabetika - Was ist belegt, was ist bewährt, was ist bezahlbar? Dr. Andreas Klinge Hamburg Keine Interessenkonflikte Was ist belegt? Menschen mit Typ 2-Diabetes 1. Stufe Basistherapie:
Sport bei Herzerkrankungen: additiv oder alternativ zu Medikamenten?
 Sport bei Herzerkrankungen: additiv oder alternativ zu Medikamenten? Martin Halle Klinikum rechts der Isar Prävention und Sportmedizin Technische Universität München www.sport.med.tum.de Sport bei Herzerkrankungen:
Sport bei Herzerkrankungen: additiv oder alternativ zu Medikamenten? Martin Halle Klinikum rechts der Isar Prävention und Sportmedizin Technische Universität München www.sport.med.tum.de Sport bei Herzerkrankungen:
 Begleitmedikation bei gefäßkranken Patienten Was ist evidenzbasiert? N. Attigah Klinischer Abend 27.07.2007 Therapieerfolg -Strenge Indikation -Akkurate OP-Technik -Konsequente Nachsorge -(Best Medical
Begleitmedikation bei gefäßkranken Patienten Was ist evidenzbasiert? N. Attigah Klinischer Abend 27.07.2007 Therapieerfolg -Strenge Indikation -Akkurate OP-Technik -Konsequente Nachsorge -(Best Medical
Mukherjee. EKG Fälle. pocket. Börm Bruckmeier Verlag
 Mukherjee EKG Fälle pocket Börm Bruckmeier Verlag Fall 34 151 Fall 34 Klinische Fallbeschreibung Ein 67 Jahre alter Mann erscheint in der Notaufnahme und klagt über Schmerzen im linken Arm während der
Mukherjee EKG Fälle pocket Börm Bruckmeier Verlag Fall 34 151 Fall 34 Klinische Fallbeschreibung Ein 67 Jahre alter Mann erscheint in der Notaufnahme und klagt über Schmerzen im linken Arm während der
Mittwoch, 14 bis 18 Uhr: für Praxispersonal Wissensvertiefung und Lehrverhaltenstraining im Rollenspiel
 Behandlungs- und Schulungsprogramm für Patienten mit Hypertonie Mittwoch, 14 bis 18 Uhr: für Ärzte und Praxispersonal Vorstellung des Behandlungs- und Schulungsprogramms im Rollenspiel, Diskussion über
Behandlungs- und Schulungsprogramm für Patienten mit Hypertonie Mittwoch, 14 bis 18 Uhr: für Ärzte und Praxispersonal Vorstellung des Behandlungs- und Schulungsprogramms im Rollenspiel, Diskussion über
KHK mit Angina pectoris: Ivabradin reduziert kardiale Ereignisse
 Neue Ergebnisse aus der BEAUTIfUL-Studie KHK mit Angina pectoris: Ivabradin reduziert kardiale Ereignisse Barcelona, Spanien, 31. August 2009 Aktuelle Daten einer auf dem Kongress der European Society
Neue Ergebnisse aus der BEAUTIfUL-Studie KHK mit Angina pectoris: Ivabradin reduziert kardiale Ereignisse Barcelona, Spanien, 31. August 2009 Aktuelle Daten einer auf dem Kongress der European Society
Basic Life Support bei Erwachsenen modifiziert für Professionals. Nach den SRC- Richtlinien (Swiss Resuscitation Council)
 Basic Life Support bei Erwachsenen modifiziert für Professionals Nach den SRC- Richtlinien (Swiss Resuscitation Council) Ziele des BLS Sicherstellung von: Atemwegsoffenheit Atemunterstützung Kreislaufunterstützung
Basic Life Support bei Erwachsenen modifiziert für Professionals Nach den SRC- Richtlinien (Swiss Resuscitation Council) Ziele des BLS Sicherstellung von: Atemwegsoffenheit Atemunterstützung Kreislaufunterstützung
PROTOKOLLE KINDERINTENSIVSTATION SMZO. Inhaltsverzeichnis
 Inhaltsverzeichnis Seite High Quality 2-3 Kinder Algorithmus BLS (ILCOR/AHA) 4 Kinder Algorithmus ALS (ILCOR/AHA) 5 Kinder Algorithmus BLS (ERC) 6 Kinder Algorithmus ALS (ERC) 7 Asystolie Algorithmus (ERC)
Inhaltsverzeichnis Seite High Quality 2-3 Kinder Algorithmus BLS (ILCOR/AHA) 4 Kinder Algorithmus ALS (ILCOR/AHA) 5 Kinder Algorithmus BLS (ERC) 6 Kinder Algorithmus ALS (ERC) 7 Asystolie Algorithmus (ERC)
OP-FREIGABE Operations-Freigabe. Gernot PAUL Ärztlicher Leiter Dialysezentrum Frauenkirchen
 OP-FREIGABE Operations-Freigabe Gernot PAUL Ärztlicher Leiter Dialysezentrum Frauenkirchen Blutbild, Thoraxröntgen EKG vielleicht auch noch eine Überprüfung der Lungenfunktion das gehört heute für viele
OP-FREIGABE Operations-Freigabe Gernot PAUL Ärztlicher Leiter Dialysezentrum Frauenkirchen Blutbild, Thoraxröntgen EKG vielleicht auch noch eine Überprüfung der Lungenfunktion das gehört heute für viele
Middeke TherapieKompass Bluthochdruck endlich wieder gute Werte. Für. Renate Hauff
 Middeke TherapieKompass Bluthochdruck endlich wieder gute Werte Für Renate Hauff mit der ich 1989 meinen ersten Patienten-Ratgeber Bluthochdruck senken ohne Medikamente bei TRIAS veröffentlicht habe. Prof.
Middeke TherapieKompass Bluthochdruck endlich wieder gute Werte Für Renate Hauff mit der ich 1989 meinen ersten Patienten-Ratgeber Bluthochdruck senken ohne Medikamente bei TRIAS veröffentlicht habe. Prof.
Der Typ 2 Diabetiker mit arterieller Hypertonie. 1. zu spät gehandelt. 2. zu spät behandelt. 3. zu ineffektiv therapiert.
 1. zu spät gehandelt 2. zu spät behandelt 3. zu ineffektiv therapiert Torsten Schwalm Häufige Koinzidenz, Problemstellung - gemeinsame pathogenetische Grundlagen - Diabetiker sind 3 x häufiger hyperton
1. zu spät gehandelt 2. zu spät behandelt 3. zu ineffektiv therapiert Torsten Schwalm Häufige Koinzidenz, Problemstellung - gemeinsame pathogenetische Grundlagen - Diabetiker sind 3 x häufiger hyperton
Inhaltsverzeichnis. 1.1 Epidemiologie koronarer Ereignisse bei Diabetes mellitus... 3
 Inhaltsverzeichnis 1 Epidemiologie, Risikofaktoren, Genetik Editoren: D. Tschöpe, P. Rösen 1.1 Epidemiologie koronarer Ereignisse bei Diabetes mellitus... 3 W. Koenig, C. Meisinger, H. Löwel 1.1.1 Prävalenz
Inhaltsverzeichnis 1 Epidemiologie, Risikofaktoren, Genetik Editoren: D. Tschöpe, P. Rösen 1.1 Epidemiologie koronarer Ereignisse bei Diabetes mellitus... 3 W. Koenig, C. Meisinger, H. Löwel 1.1.1 Prävalenz
Checken Sie Ihre Werte. lyondellbasell.com
 Checken Sie Ihre Werte 1 Verantwortung für die eigene Gesundheit übernehmen heißt Werte checken! Im Alltag haben wir viele wichtige Zahlen im Kopf Aber kennen Sie auch Ihre Werte für Blutdruck Cholesterinwert
Checken Sie Ihre Werte 1 Verantwortung für die eigene Gesundheit übernehmen heißt Werte checken! Im Alltag haben wir viele wichtige Zahlen im Kopf Aber kennen Sie auch Ihre Werte für Blutdruck Cholesterinwert
