Woche 1: Grundlagen - Spezialfall Hämoglobin Woche 2: Proteinanalytik - Enzymregulation
|
|
|
- Gerhardt Schuler
- vor 5 Jahren
- Abrufe
Transkript
1 Woche 1: Grundlagen - Spezialfall Hämoglobin Woche 2: Proteinanalytik - Enzymregulation
2 Vorlesung Medizinische Biochemie ( ) Hauptakteure der Sauerstoffversorgung: Hämoglobin und Myoglobin für den Transport und die Speicherung von O 2 Sven Lang, Universität des Saarlandes Medizinische Biochemie und Molekularbiologie sven.lang@uni-saarland.de
3 Schwerpunkte: Das kleine 4 x 4 der Sauerstoffakteure Die Häm-Gruppe Vertreter der Globinfamilie Synthesereaktionen Myoglobin Syntheseregulation Hämoglobin Funktion Sauerstoffbindung Abbau Kooperativität Allosterische Effektoren 2,3-Bisphosphoglycerat Protonenkonzentration Kohlendioxid Bohr-/Haldane-Effekt Assoziierte Krankheitsbilder Diabetes Mellitus Sichelzellanämie Thalassämie Kohlenmonoxidvergiftung 3
4 MIND-BLOWING Millionen Billionen Trilliarden (Hämoglobin pro Erythrozyt) (750 g) (Menge an Erythrozyten pro Person) (O 2 -bindestellen im Hb pro Person) (Sterne in Milchstraße) 7,5 µm ø Haar: 70 µm 4
5 Warum aber benötigt man Sauerstoffakteure? Aerobe Oxidation von Glucose (Nahrung) liefert 15x mehr Energie als anaerobe Version => Glykolyse: 2 ATP/Glc => OXPHOS: 30 ATP/Glc Sauerstoff ist ein recht unpolares Molekül => geringe physikalische Wasserlöslichkeit im polaren (extra-) zellulären Milieu => Blutplasma (3 ml O 2 /l); Vollblut (200 ml O 2 /l) O O Reversibilität der Sauerstoffkoordination => Der wahre Star: Metallionen => Fe 2+ (Hb, Mb), Cu 2+ (Hämocyanin) Fe 2+ HEAVY METAL 5
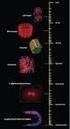
6 Produktion des Metallchelators: Hämbiosynthese Isotopenmarkierungsexperimente im Jahr 1945 durch David Shemin => 14 C-Glycin, 14 C-Acetat (Methyl/Carboxyl) Hämaufbau aus 34 C-Atomen => 8 C-Atome von α-c-glycin => restliche 26 C-Atome von Acetat Hämcharakteristika => Vier Pyrrolringe (Tetrapyrrolring) => Methinbrücken verbinden Pyrrole => Methyl-, Vinyl-, Propionatreste => N-Atome koordinieren Eisen-Ion => Konjugierte Doppelbindungen Rotfärbung Muskel, Blut 6
7 Hämbiosynthese: committed step Schritt 1: Bildung von δ-aminolävulinat => Geschwindigkeitsbestimmender Schritt => Kondensation Glycin mit Succinyl-CoA => Katalysiert durch δ-ala-synthase δ-ala-synthase Coenzym A (CoA, Vit. B5) Pyridoxalphosphat (PLP, Vit. B6) 7
8 Hämbiosynthese Bildung von linearem Tetrapyrrol => Kondensation zweier δ-aminolävulinat zu Porphobilinogen => Vier Porphobilinogen kondensieren zu linearem Tetrapyrrol (Kopf-Schwanz-Reaktion) Porphobilinogen Desaminase 8
9 Hämsynthese: Zyklisierung, Modifikation, Eisen Synthase + Cosynthase Chelatierung durch Ferrochelatase Seitenkettenmodifikaton Zyklisierung 9
10 Hämbiosynthese erfolgt in zwei Kompartimenten Mito Zyto Gewebespezifische Regulation der Hämbiosynthese => Zwei δ-ala-synthase Paraloge (ALAS1 und ALAS2) => ALAS2 (Nicht-Erythrozyten-Zellen) EPO + Fe 2+ => ALAS1 (Erythrozyten-Vorläufer) Häm 10
11 Häm ist eine prosthetische Gruppe in Enzymen Hämhaltige Enzymsysteme => Cytochrome (P450, Atmungskette) => Monooxygenasen, Peroxidasen => Katalase, enos => Chlorophylle => Hämoglobin, Myoglobin Globinpolypeptid (His F8) Prosthetische Gruppe: Ein nicht-proteinöser Kofaktor der kovalent (hoher Affinität) an ein Enzym gebunden ist und dessen katalytische Funktion definiert. (Apo-Enzym + Kofaktor = Holo-Enzym) O 2 Häm 11
12 Ein kleiner Schritt für einen Sauerstoff, ein großer Schritt für die Menschheit Deoxy-Häm Paramagnetischer high spin Zustand Gekrümmter Porphyrinring (tensed) Fe 2+ (größer) außerhalb Ringsystem Oxy-Häm Diamagnetischer low spin Zustand Flacher Porphyrinring (relaxed) Fe 2+ (kleiner) im Ringsystem Proximales Histidin der Globinkette Fe 2+ (Oxygenierung) Sich fortpflanzende Änderung der Tertiärstruktur 12
13 Ein kleiner Schritt für einen Sauerstoff, ein großer Schritt für die Menschheit Deoxy-Häm Paramagnetischer high spin Zustand Gekrümmter Porphyrinring (tensed) Fe 2+ (größer) außerhalb Ringsystem Oxy-Häm Diamagnetischer low spin Zustand Flacher Porphyrinring (relaxed) Fe 2+ (kleiner) im Ringsystem α-helix mit proximalem Histidin Porphyrinring Hebelwirkung des proximalen Histidins (= 5. Koordinationsstelle des Fe 2+ ) bei Oxygenierung vermittelt die Konformationsänderung der Globinkette 13
14 Ein distales Histidin zur Stabilisierung des O 2 Funktion des distalen Histidins => strukturell konserviertes His => Schutz vor Fe 2+ Oxidation => unterbindet Superoxidanion Mesomerie Probleme bei Fe 2+ Oxidation => Fe 2+ (Ferro) Fe 3+ (Ferri) => O 2 Superoxid (Radikal) => Häm Hämatin (MetMb/MetHb) => KEINE O 2 Bindung mehr 14
15 Proteine der Globinfamilie: Myo- & Hämoglobin Myoglobin (Mb) Hämoglobin (Hb) Myo- (von griech. müs ) Muskel Hämo- (von griech. haima ) Blut Roter Farbstoff der Muskulatur Roter Blutfarbstoff der Erythrozyten 1 Polypeptidkette (8 α-helices A-H) 4 Polypeptide (2 identische Dimere) 1 Hämgruppe pro Polypeptidkette eine Hämgruppe O 2 -Speicher in Muskelzellen (Zytosol) O 2 -Transporter des Blutes 1959 durch John Kendrew: 1960 durch Max Perutz: 3D-Struktur Myoglobin (Pottwal) 3D-Struktur Hämoglobin (Pferdeherz) 15
16 Tertiärstruktur (Faltung) ist stärker konserviert als Primärstruktur (Aminosäureabfolge): 3 > 1 16
17 Y (Fraktionelle Sättigung in %) Sauerstoffbindungskurve: Y vs. po 2 Myoglobin (Mb) Monomer 1 Polypeptidkette mit 153 aa Bindet O 2 durch Hämgruppe Hämoglobin A (HbA) Tetramer 2α (je 141 aa) + 2β (je 146 aa) Ketten Bindet O 2 durch Hämgruppe(n)? Wie effizient binden beide den Sauerstoff? Fraktionelle Sättigung (Y): Einheitsloser Zahlenwert der den Anteil aller möglichen Bindungsstellen angibt, welche gebundenen Sauerstoff enthalten. Sauerstoffpartialdruck (po 2 ): Gemessen in Torr, der Maßeinheit für den Druck einer Quecksilbersäule (1 mm Hg). Benannt nach Evangelista Torricello (Erfinder des Quecksilberbarometers) po 2 (Torr) 17
18 Hyperbolische Sauerstoffbindungskurve des Mb Myoglobin (Mb) Monomer, 1 Polypeptidkette mit 153 aa, Hämgruppe bindet O 2 Hyerbolische Bindungskurve (= einfaches chemisches Gleichgewicht) Halbsättigung (P 50 ) bei 2 Torr O 2 18
19 Sigmoidale Sauerstoffbindungskurve des Hb Hämoglobin (Hb) Tetramer, 4 Polypeptidketten, 4 Hämgruppen binden O 2 Sigmoidale Bindungskurve (= komplexes Gleichgewicht durch Kooperativität) Halbsättigung (P 50 ) bei 26 Torr O 2 O 2 O 2 O 2 19
20 Kooperativität basiert auf struktureller Änderung T (tensed) R (relaxed) + O 2 - O 2 Molekulare Lunge (Max Perutz) 20
21 Modellvorstellung der Kooperativität Sequenzielles Modell Ligandbindung (O 2 ) ändert Konformation der Untereinheit Konformationsänderung bewirkt Änderung anderer Untereinheit ( O 2 -Affinität) Übergang T R-Form (intramolekulare Kommunikation) => mit steigendem po 2 steigt O 2 -Affinität des Hämoglobins Puzzle-Analogie Je mehr Teile bereits vorgelegt sind, desto leichter lassen sich fehlende Teile anfügen, quasi freie Stellen besetzen. 21
22 Vergleich der Sauerstofffreigabe von Mb und Hb Nichts in der Biologie macht Sinn außer im Licht der Evolution. T. Dobzhansky ( ) Vorteil der Kooperativität Effiziente O 2 -Freigabe im aktiven Gewebe Scheitelpunkt liegt nahe dem P 50 nahe dem po 2 von Gewebe bei Anstrengung bei Ruhe 22
23 Allosterischer Effektor: 2,3-Bisphosphoglycerat Allosterischer Effektor: Ein direkt bindender Ligand der die Enzymaktivität fernab des aktiven Zentrums beeinflusst. Von griech. allos für andere und stereos für Struktur. 23
24 Allosterischer Effektor #1: 2,3-Bisphosphoglycerat 2,3-Bisphosphoglycerat (2,3-BPG) R-Form des Hb unter physiologischen Bed. begünstigt (wenig O 2 -Freisetzung) 2,3-BPG stabilisiert T-Form => reduziert Sauerstoffaffinität Ein 2,3-BPG bindet im zentralen Kanal des deoxyhb Verschiebt die O 2 -Bindungskurve nach rechts Übergang T R-Form verdrängt 2,3-BPG 2,3- BPG + O 2, - BPG - O 2, + BPG 24
25 Allosterischer Effektor #2 und #3: H + und CO 2 ph Wert (H + ) Aktive Gewebe erzeugen H + ( ph) Protonierung des β C-Terminus (His 146 ) Stabilisierung der T-Form (O 2 -Abgabe) Rechtsverschiebung O 2 -Bindungskurve Kohlendioxid (CO 2 ) Aktive Gewebe erzeugen CO 2 1) CO 2 + H 2 O HCO H + ( ph) 2) Carbamatbildung an den N-Termini T-Form, Rechtsverschiebung (O 2 -Abgabe) (ph 7,2) (ph 7,4) 25
26 Allosterischer Effektor #2 und #3: H + und CO 2 ph Wert (H + ) Aktive Gewebe erzeugen H + ( ph) Protonierung des β C-Terminus (His 146 ) Stabilisierung der T-Form (O 2 -Abgabe) Rechtsverschiebung O 2 -Bindungskurve Bohr- Effekt (Christian Bohr, 1904) Kohlendioxid (CO 2 ) Aktive Gewebe erzeugen CO 2 1) CO 2 + H 2 O HCO H + ( ph) 2) Carbamatbildung an den N-Termini T-Form, Rechtsverschiebung (O 2 -Abgabe) Haldane- Effekt (John Haldane, ~1916) Die allosterischen Effektoren 2,3-BPG, H + und CO 2 wirken synergistisch. Alle drei verschieben die O 2 -Bindungskurve des Hb weiter nach rechts. 26
27 Hämoglobin als Protonen- und CO 2 -Puffer Hämoglobin O 2 Histidinreich (38 His-Reste) R-His + R-His ph Histidinreste (pk s = 6) puffern H + ¼ der H + -Pufferkapazität des Blutes Carbamatbildung als CO 2 Puffer Carboanhydrase ( /sec) 15 % 5 % 80 % 27
28 Nicht-allosterische Änderung der Hb O 2 -Affinität Mögliche Ursachen und Optionen Glykierung (posttranslationale Modifikation) Mutationen (Hämoglobinopathien: Sichelzellanämie, Thalassämie) Isoformen (Schwangerschaft) Kompetitive Strukturanaloga (Kohlenmonoxid) Oxidation (MetHb) 28
29 Glykierung und Diabetes Mellitus Glykierung ( Glycosylierung) Kovalente, posttranslationale Modifikation Amadori-Umlagerung Nicht-enzymatische Anbindung von Hexose an die β-untereinheit HbA mit Glykierung => HbA 1 (i.d.r. < 6% des Hb-Pools) Untertyp HbA 1C (Glykierung mit Glucose an Val1 der β-untereinheit) Glykierung ist proportional der Blutzuckerkonzentration => HbA 1C gibt retrospektive Auskunft über Ausmaß und Dauer einer Hyperglykämie bei Diabetes mellitus 29
30 Hb Mutation #1: Sichelzellanämie Sichezellhämoglobin Punktmutation (1956: Vernon Ingram) In β-untereinheit: E6V (Glutamat Valin) Sichezellhämoglobin (HbS = 2α + 2β S ) Aggregationsproblematik des deoxyhbs Sticky patch => Faserbildung => Deformation Ischämie (Kapillarverschluss) Anämie (kürzere Lebensdauer der Sichelzellen) β S α Val 6 (sticky patch) Phe 85, Leu 88 (complementary patch) 30 HbS Fasern Aggregat aus zwei deoxyhbs Molekülen
31 Sichelzellmerkmal bewirkt Malariaresistenz Malaria Plasmodium falciparum Entwicklungsstadium in Erythrozyten Resistenz der HbS-Träger (Heterozygote; HbS +/- ) Survival of the fittest - C. Darwin 31
32 Hb Mutation #2: Thalassämien α-thalassämie (griech. thalassa Meer) Verminderte/fehlende Expression der α-kette Ohne Synthese der α-kette => Tod in utero Reduzierte Synthese der α-kette => HbH (β-tetramer) HbH mit hoher O 2 -Affinität => wenig O 2 -Freisetzung HbH instabil => Kurze Lebensdauer der Erythrozyten (Anämie) β-thalassämie Verminderte/fehlende Expression der β-kette Ohne Synthese der β-kette => β-thalassaemia major α-kette bilden Aggregate => Kurze Lebensdauer der Erythrozyten (Anämie) Kompensation durch Expression der Globingene γ (=> HbF) und δ (=> HbA 2 ) Bluttransfusion 32
33 Unser Genom kodiert weitere Globingene Hämoglobin-Isoformen Differenzielle Genaktivität Ontogenese (Embryonalentwicklung) Übersicht: Menschlicher Hämoglobine vom Embryo bis zum Erwachsenen HbF HbA HbA 2 (98 %) (Monate) (2 %) α 2 δ 2 33
34 Isoformen zeigen unterschiedliche O 2 -Affinität Besonderheiten des fetalen HbF O 2 -Affinität HbF > HbA Reduzierte 2,3-BPG Bindungsaffinität γ-globinkette trägt Serin anstelle His 143 O 2 -Bindungskurve nach links verschoben Serin (HbF) (HbF) Serin HbA 34
35 Kompetitive Analoga reduzieren O 2 -Affinität Kohlenmonoxid (CO) Farb- und geruchsloses Gas C O Kompetititves Strukturanalogon des O 2 Konkurriert mit O 2 um Bindungsstelle am Häm Bindet 200x affiner an HbA (20.000x affiner an freies Häm) Hyperbare Sauerstofftherapie zur Verdrängung O O 35
36 Oxidation des Häm erzeugt MetHb Methämoglobin (MetHb) Distales Histidin schützt vor Fe 2+ Oxidation Fe 2+ (Ferro) Fe 3+ (Ferri) [durch O 2 und Nitrit] O 2 Superoxid (Radikal) Häm Hämatin (Hb MetHb) KEINE O 2 Bindung mehr Reduktion durch a) Methämoglobin-Reduktase Distales His Mesomerie 36
37 Das Farbspiel des Häm-Abbaus: der Bluterguß Häm-Abbau durch Makrophagen in Milz, Leber und Knochenmark Blut Leber Kolon 37
38 Y (Fraktionelle Sättigung) Quick recap Sauerstoffakteure Die Häm-Gruppe Vertreter der Globinfamilie Proximales His hyperbolisch sigmoidal, kooperativ Fe 2+ Protoporphyrin IX Distales His Allosterische Effektoren Assoziierte Krankheitsbilder Thalassämie po 2 (Torr) Bohr- und Haldane- Effekt, Synergismus HbS Fibrille ( sticky patch ) α: HbH (β-ketten Tetramer) β: HbA 2 Kompensation 38
39 Quellenangaben Löffler/Petrides Biochemie und Pathobiochemie, 9. Auflage Duale Reihe Biochemie, 4. Auflage Stryer Biochemie, 8. Auflage Biologie für Mediziner, 13. Auflage Internet 39
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9)
 Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 1. Funktion des Hämoglobins Sauerstoff
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 1. Funktion des Hämoglobins Sauerstoff
Allgemeines: Konzentration des Hämoglobins im Blut: 160 g/l Verpackung im Erythrocyten -> kolloidosmotisch unwirksam -> beeinträchtigt nicht den Wasse
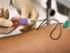 Hämoglobin Allgemeines: Konzentration des Hämoglobins im Blut: 160 g/l Verpackung im Erythrocyten -> kolloidosmotisch unwirksam -> beeinträchtigt nicht den Wasseraustausch im Kapillarbereich Durch die
Hämoglobin Allgemeines: Konzentration des Hämoglobins im Blut: 160 g/l Verpackung im Erythrocyten -> kolloidosmotisch unwirksam -> beeinträchtigt nicht den Wasseraustausch im Kapillarbereich Durch die
Häm. Biosynthese Pathophysiologie der Biosynthese
 Häm Biosynthese Pathophysiologie der Biosynthese Häm = Porphyrin farbige Verbindung, konjugiertes Ringsystem 4 Pyrrolringe ubiquitär in Tier- und Pflanzenreich prosthetische Gruppe von Hämoproteinen Mensch
Häm Biosynthese Pathophysiologie der Biosynthese Häm = Porphyrin farbige Verbindung, konjugiertes Ringsystem 4 Pyrrolringe ubiquitär in Tier- und Pflanzenreich prosthetische Gruppe von Hämoproteinen Mensch
Atmung II Atemgastransport Pathophysiologie
 Atmung II Atemgastransport Pathophysiologie Einführung Äußere und Innere Atmung Atemgastransport Normwerte Atemgastransport Das Blut Eine wesentliche Aufgabe des Blutes ist der Atemgastransport : Das Blut
Atmung II Atemgastransport Pathophysiologie Einführung Äußere und Innere Atmung Atemgastransport Normwerte Atemgastransport Das Blut Eine wesentliche Aufgabe des Blutes ist der Atemgastransport : Das Blut
Funktion von Proteinen:
 Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
Hemmung der Enzym-Aktivität
 Hemmung der Enzym-Aktivität Substrat Kompetitiver Inhibitor Enzym Enzym Substrat Nichtkompetitiver Inhibitor Irreversibler Inhibitor Enzym Enzym Enzym - Kinetik Michaelis Menten Gleichung Lineweaver -
Hemmung der Enzym-Aktivität Substrat Kompetitiver Inhibitor Enzym Enzym Substrat Nichtkompetitiver Inhibitor Irreversibler Inhibitor Enzym Enzym Enzym - Kinetik Michaelis Menten Gleichung Lineweaver -
Fundamentals of Biochemistry
 Donald Voet Judith G. Voet Charlotte W. Pratt Fundamentals of Biochemistry Second Edition Chapter 7: Protein Function: Myoglobin and Hemoglobin Copyright 2006 by John Wiley & Sons, Inc. Proteinfunktion:
Donald Voet Judith G. Voet Charlotte W. Pratt Fundamentals of Biochemistry Second Edition Chapter 7: Protein Function: Myoglobin and Hemoglobin Copyright 2006 by John Wiley & Sons, Inc. Proteinfunktion:
Mechanismus der Enzymkatalyse
 Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
Kapitel: Häm 35. Hämsynthese COOH. Porphobilinogen- Synthase NH 2 H. 5-Aminolävulinsäure (ALA) HOOC CH 2. Uroporphyrinogen- HN Decarboxylase CH 3
 Kapitel: Häm 35 Häm Biosynthese Häm ist, wie wir bereits gesehen haben, eine Fe-haltige prosthetische Gruppe, die ein essentieller Bestandteil vieler Proteine ist, wie z. B. Hämoglobin, Myoglobin und der
Kapitel: Häm 35 Häm Biosynthese Häm ist, wie wir bereits gesehen haben, eine Fe-haltige prosthetische Gruppe, die ein essentieller Bestandteil vieler Proteine ist, wie z. B. Hämoglobin, Myoglobin und der
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase
 Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Gliederung. Puffersysteme. Wofür Puffersysteme? Wofür Puffersysteme? Wofür Puffersysteme? ph-verhältnisse im Körper. Puffersysteme
 Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
- der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen
 Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Enzyme SPF BCH am
 Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Biologie. Anorganische Chemie. Bioanorganische Chemie
 Eine kleine Einführung in die Bioanorganische Chemie illustriert am Sauerstofftransport Jorge Ferreiro Montag, 8.12.2008 OACP II, ETH Zürich Wie lässt sich die Anorganische Chemie mit der Biologie verbinden,
Eine kleine Einführung in die Bioanorganische Chemie illustriert am Sauerstofftransport Jorge Ferreiro Montag, 8.12.2008 OACP II, ETH Zürich Wie lässt sich die Anorganische Chemie mit der Biologie verbinden,
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Hemmung der Enzym-Aktivität
 Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
Kardiopulmonale Homöostase
 Kapitel 2 Kardiopulmonale Homöostase Primäre Funktion des Blutes im Rahmen der Atmung Transport von O 2 aus der Lunge zum peripheren Gewebe, CO 2 aus der Peripherie zu den Lungen, H + vom Gewebe zu den
Kapitel 2 Kardiopulmonale Homöostase Primäre Funktion des Blutes im Rahmen der Atmung Transport von O 2 aus der Lunge zum peripheren Gewebe, CO 2 aus der Peripherie zu den Lungen, H + vom Gewebe zu den
Aminosäuren 1. Aufbau der Aminosäuren
 Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
BLUUUUT!!!!! Und wo und wie wird das HÄM synthetisiert?
 Und wo und wie wird das HÄM synthetisiert? Und wo und wie wird das HÄM synthetisiert? In den Erythroblasten des Knochenmarks Den Ausgang der Synthese stellen die AS Glycin und das Succinyl-CoA (wer liefert
Und wo und wie wird das HÄM synthetisiert? Und wo und wie wird das HÄM synthetisiert? In den Erythroblasten des Knochenmarks Den Ausgang der Synthese stellen die AS Glycin und das Succinyl-CoA (wer liefert
Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!!
 Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!! Indirekte ATP synthese! Protonen können in wässriger Lösung sehr! schnell transportiert werden.! Ionen können biologische Membranen nicht spontan
Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!! Indirekte ATP synthese! Protonen können in wässriger Lösung sehr! schnell transportiert werden.! Ionen können biologische Membranen nicht spontan
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+
![Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ Elektronenspektrum von [Ti(H 2 O) 6 ] 3+](/thumbs/66/55543366.jpg) Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
und Reinstruktur Die Sekundärstruktur ist die Anordnung der Aminosäurenkette, wobei man in zwei Arten unterscheidet: o Faltblatt- oder β- Struktur
 Aufbau von Proteinen insbesondere unter Betrachtung der Primär-,, Sekundär-,, Tertiär-,, Quartär-,, Supersekundär- und Reinstruktur Primärstruktur Unter Primärstruktur versteht man in der Biochemie die
Aufbau von Proteinen insbesondere unter Betrachtung der Primär-,, Sekundär-,, Tertiär-,, Quartär-,, Supersekundär- und Reinstruktur Primärstruktur Unter Primärstruktur versteht man in der Biochemie die
Biochemische UE Alkaline Phosphatase.
 Biochemische UE Alkaline Phosphatase peter.hammerl@sbg.ac.at Alkaline Phosphatase: Katalysiert die Hydrolyse von Phosphorsäure-Estern: O - O - Ser-102 R O P==O O - H 2 O R OH + HO P==O O - ph-optimum im
Biochemische UE Alkaline Phosphatase peter.hammerl@sbg.ac.at Alkaline Phosphatase: Katalysiert die Hydrolyse von Phosphorsäure-Estern: O - O - Ser-102 R O P==O O - H 2 O R OH + HO P==O O - ph-optimum im
BLUUUUT!!!!! Das Blut ist ein Organ!! Es hat wichtige Funktionen: - O2/ CO2+Vitamine+ Nahrung Stoffwechselendprodukt-Transport - Wärmeabtransport!
 BLUUUUUUT!!!!! Das Blut ist ein Organ!! Es hat wichtige Funktionen: - O2/ COVitamine+ Nahrung Stoffwechselendprodukt-Transport - Wärmeabtransport! - Elektrolyttransport -Osmoregulation - Hormontransport
BLUUUUUUT!!!!! Das Blut ist ein Organ!! Es hat wichtige Funktionen: - O2/ COVitamine+ Nahrung Stoffwechselendprodukt-Transport - Wärmeabtransport! - Elektrolyttransport -Osmoregulation - Hormontransport
Bachelorstudiengang Biologie. Vorlesung Biochemie I Klausur am 11. Oktober 2012, 9:00 11:00, H18
 Bachelorstudiengang Biologie Vorlesung Biochemie I Klausur am 11. Oktober 2012, 9:00 11:00, H18 1. (a) Welche Aminosäuren mit positiv geladenen Seitenketten kennen Sie? Bitte geben Sie die Strukturformel
Bachelorstudiengang Biologie Vorlesung Biochemie I Klausur am 11. Oktober 2012, 9:00 11:00, H18 1. (a) Welche Aminosäuren mit positiv geladenen Seitenketten kennen Sie? Bitte geben Sie die Strukturformel
Die α (alpha)-thalassämien- Informationen für Patienten
 Die Alpha Thalassämien Seite 1 von 1 Die α (alpha)-thalassämien- Informationen für Patienten Erstellung Prüfung Prof. Dr. med. Roswitha Dickerhoff Prof. Dr. med. R. Dickerhoff Gültigkeitsbeginn 01.05.2013
Die Alpha Thalassämien Seite 1 von 1 Die α (alpha)-thalassämien- Informationen für Patienten Erstellung Prüfung Prof. Dr. med. Roswitha Dickerhoff Prof. Dr. med. R. Dickerhoff Gültigkeitsbeginn 01.05.2013
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Fettsäurebiosynthese
 Fettsäurebiosynthese Inhalt Fettsäuren Triacylglyceride FS-Biosynthese und einzelne Schritte Fettsäuren Lange CH-Ketten mit einer endständigen Carboxylgruppe 3 Gruppen: -> gesättigte FS -> einfach ungesättigte
Fettsäurebiosynthese Inhalt Fettsäuren Triacylglyceride FS-Biosynthese und einzelne Schritte Fettsäuren Lange CH-Ketten mit einer endständigen Carboxylgruppe 3 Gruppen: -> gesättigte FS -> einfach ungesättigte
1. Die Bildung von Methan durch Mikroorganismen erfolgt (2 Punkte)
 Modul: Einführung in die Biochemie und Genetik Prüfungsleistung: Einführung in die Biochemie Welches Enzym katalysiert die dargestellte Reaktion? (2 Punkte) a) Hexokinase b) Glyceratkinase c) Mitogen-aktivierte
Modul: Einführung in die Biochemie und Genetik Prüfungsleistung: Einführung in die Biochemie Welches Enzym katalysiert die dargestellte Reaktion? (2 Punkte) a) Hexokinase b) Glyceratkinase c) Mitogen-aktivierte
2. Tertiärstruktur. Lernziele: 1) Verstehen wie Röntgenstrukturanalyse und NMR Spektroskopie gebraucht werden um Proteinstrukturen zu bestimmen.
 2. Tertiärstruktur Lernziele: 1) Verstehen wie Röntgenstrukturanalyse und NMR Spektroskopie gebraucht werden um Proteinstrukturen zu bestimmen. 2) Verstehen warum nicht polare Reste im inneren eines Proteins
2. Tertiärstruktur Lernziele: 1) Verstehen wie Röntgenstrukturanalyse und NMR Spektroskopie gebraucht werden um Proteinstrukturen zu bestimmen. 2) Verstehen warum nicht polare Reste im inneren eines Proteins
Wirkungsmechanismen regulatorischer Enzyme
 Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
- Biochemieklausur Name: Matrikelnr.:
 07.02.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
07.02.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Praktikum Biochemie B.Sc. Water Science WS Enzymregulation. Marinja Niggemann, Denise Schäfer
 Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Aminosäuren. Seitenkette. -Kohlenstoffatom. Karboxilgruppe. Aminogruppe
 Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine 18 Primär Struktur Aminosäuer
Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine 18 Primär Struktur Aminosäuer
Atemgastransport im Blut
 Atemgastransport im Blut Institut für MTA-Ausbildung am Klinikum Osnabrück Fachgebiet Anatomie/Physiologie/Krankheitslehre - Dr. U. Krämer 1. Physikalische Löslichkeit der Atemgase Sauerstoff und Kohlendioxid
Atemgastransport im Blut Institut für MTA-Ausbildung am Klinikum Osnabrück Fachgebiet Anatomie/Physiologie/Krankheitslehre - Dr. U. Krämer 1. Physikalische Löslichkeit der Atemgase Sauerstoff und Kohlendioxid
Schweizerische Maturitätsprüfung Gruppe / Kandidat/in Nr:... Fächerübergreifender Teil Biologie
 Gruppe / Kandidat/in Nr:... Name/Vorname:... Schwerpunktfach Teil BIOLOGIE UND CHEMIE Fächerübergreifender Teil Biologie Verfasser: Richtzeit: Hilfsmittel: Hinweise: G. Rutz, M. Lüscher 30 Minuten (von
Gruppe / Kandidat/in Nr:... Name/Vorname:... Schwerpunktfach Teil BIOLOGIE UND CHEMIE Fächerübergreifender Teil Biologie Verfasser: Richtzeit: Hilfsmittel: Hinweise: G. Rutz, M. Lüscher 30 Minuten (von
Tyrosinkinase- Rezeptoren
 Tyrosinkinase- Rezeptoren für bestimmte Hormone gibt es integrale Membranproteine als Rezeptoren Aufbau und Signaltransduktionsweg unterscheiden sich von denen der G- Protein- gekoppelten Rezeptoren Polypeptide
Tyrosinkinase- Rezeptoren für bestimmte Hormone gibt es integrale Membranproteine als Rezeptoren Aufbau und Signaltransduktionsweg unterscheiden sich von denen der G- Protein- gekoppelten Rezeptoren Polypeptide
Präsentation STOFFWECHSEL STOFFWECHSEL. Fettstoffwechsel im Sport. Biologische Oxidation Zitratzyklus und Atmungskette
 STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
Das Hämoglobin des Menschen
 Falko H. Herrmann Martina eh. Herrmann Das Hämoglobin des Menschen Struktur, Funktion, Genetik Die REIHE WISSENSCHAFT ist die wissenschaftliche Handbibliothek des Naturwissenschaftlers und Ingenieurs und
Falko H. Herrmann Martina eh. Herrmann Das Hämoglobin des Menschen Struktur, Funktion, Genetik Die REIHE WISSENSCHAFT ist die wissenschaftliche Handbibliothek des Naturwissenschaftlers und Ingenieurs und
Regulation der Glykolyse: Phosphofructokinase
 Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
0.1 Eiweißstoffe (Proteine)
 1 22.06.2006 0.1 Eiweißstoffe (Proteine) 0.1.1 Die Aminosäuren Bausteine der Proteine Proteine sind aus einer Vielzahl (bis Tausende) von Baueinheiten zusammengesetzte Makromoleküle. Die einzelnen Bausteine,
1 22.06.2006 0.1 Eiweißstoffe (Proteine) 0.1.1 Die Aminosäuren Bausteine der Proteine Proteine sind aus einer Vielzahl (bis Tausende) von Baueinheiten zusammengesetzte Makromoleküle. Die einzelnen Bausteine,
Grundlagen der β-thalassämia major. Stefan Balzer
 Grundlagen der β-thalassämia major Stefan Balzer Universitätsklinikum Düsseldorf Zentrum für Kinder- und Jugendmedizin Klinik für Kinder-Onkologie, -Hämatologie und klinische Immunologie Thalassämie Cooley
Grundlagen der β-thalassämia major Stefan Balzer Universitätsklinikum Düsseldorf Zentrum für Kinder- und Jugendmedizin Klinik für Kinder-Onkologie, -Hämatologie und klinische Immunologie Thalassämie Cooley
Mathematik und Naturwissenschaften, Biologie, Biochemie. Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 20.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 20.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Aminosäuren. Seitenkette. -Kohlenstoffatom. Karboxilgruppe. Aminogruppe
 Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine Bildung der Disulfidbrücke
Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine Bildung der Disulfidbrücke
Sauerstofftransport im Blut. von Ralph Althoff Christoph Mittmann
 Sauerstofftransport im Blut von Ralph Althoff Christoph Mittmann Gliederung des Vortrags 1.) Geschichtliches 2.) Eigenschaften des Blutes 3.) Aufbau des Blutes 4.) Der Sauerstofftransporter 5.) Die Chemie
Sauerstofftransport im Blut von Ralph Althoff Christoph Mittmann Gliederung des Vortrags 1.) Geschichtliches 2.) Eigenschaften des Blutes 3.) Aufbau des Blutes 4.) Der Sauerstofftransporter 5.) Die Chemie
Einführung in die Biochemie Wirkungsweise von Enzymen
 Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
Chemie für Biologen WS 2005/6 Arne Lützen Institut für Organische Chemie der Universität Duisburg-Essen (Teil 5: )
 Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
Grundlagen der Biochemie (BCh 5.3) Prof. Dr. Christoph Thiele WS 2014/15 1. Klausur ( )
 Grundlagen der Biochemie (BCh 5.3) Prof. Dr. Christoph Thiele WS 2014/15 1. Klausur (6.2.2015) Aufgabe 1: Erläutern Sie die Primär-, Sekundär- und die Tertiärstruktur von Proteinen. [3 P] Aufgabe 2: Erklären
Grundlagen der Biochemie (BCh 5.3) Prof. Dr. Christoph Thiele WS 2014/15 1. Klausur (6.2.2015) Aufgabe 1: Erläutern Sie die Primär-, Sekundär- und die Tertiärstruktur von Proteinen. [3 P] Aufgabe 2: Erklären
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion. Mag. Gerald Trutschl
 Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Gluconeognese Neusynthese von Glucose aus Pyruvat
 Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9)
 Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation A. Struktur von Myoglobin Strukturaufklärung
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation A. Struktur von Myoglobin Strukturaufklärung
Intensivkurs Biologie
 Intensivkurs 2016 - Biologie 1. Makromoleküle Lektüre im Cornelsen, Biologie Oberstufe : Chemische Grundlagen: Lipide (S. 40), Proteine (S. 41-42), Kohlenhydrate (S. 92-93) 1.1. Kohlenstoff-Verbindungen
Intensivkurs 2016 - Biologie 1. Makromoleküle Lektüre im Cornelsen, Biologie Oberstufe : Chemische Grundlagen: Lipide (S. 40), Proteine (S. 41-42), Kohlenhydrate (S. 92-93) 1.1. Kohlenstoff-Verbindungen
Sauerstoff und ROS. ROS und Altern
 Molekularer Sauerstoff (O 2 ) ist eine chemisch sehr reaktive und aggressive Substanz. Das erste Auftreten freien Sauerstoffs durch photosynthetische Bakterien dürfte eine der größten ökologischen Katastrophen
Molekularer Sauerstoff (O 2 ) ist eine chemisch sehr reaktive und aggressive Substanz. Das erste Auftreten freien Sauerstoffs durch photosynthetische Bakterien dürfte eine der größten ökologischen Katastrophen
Sauerstoffbindung im Blut
 Sauerstoffbindung im Blut Die Fähigkeit uns zu wundern, ist das Einzige, was wir brauchen, um gute Philosophen zu werden. Gaarder Jostein, Sofies Welt 1 Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung...
Sauerstoffbindung im Blut Die Fähigkeit uns zu wundern, ist das Einzige, was wir brauchen, um gute Philosophen zu werden. Gaarder Jostein, Sofies Welt 1 Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung...
Biologie für Mediziner
 Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/ CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/ CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
-Klausur Biochemie Name: Matrikelnr.: 1. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist.
 4.07.205 Name: Matrikelnr.:. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist. 2. Was bedeutet es, wenn eine schwache Säure einen pks von 5 hat? 3. Nennen Sie
4.07.205 Name: Matrikelnr.:. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist. 2. Was bedeutet es, wenn eine schwache Säure einen pks von 5 hat? 3. Nennen Sie
pk S der α-carbonsäure = 1,88; pk S der β-carbonsäure = 3,65 Die beiden Carbonsäuregruppen unterscheiden sich auch in ihrer chemischen Reaktivität
 Aminosäuren mit sauren Seitengruppen Asparaginsäure (Asp,D) pk S der α-carbonsäure = 1,88; pk S der β-carbonsäure = 3,65 Die beiden Carbonsäuregruppen unterscheiden sich auch in ihrer chemischen Reaktivität
Aminosäuren mit sauren Seitengruppen Asparaginsäure (Asp,D) pk S der α-carbonsäure = 1,88; pk S der β-carbonsäure = 3,65 Die beiden Carbonsäuregruppen unterscheiden sich auch in ihrer chemischen Reaktivität
Lebewesen enthalten weitaus mehr Molekülarten und beherbergen weitaus mehr chemische Reaktionsarten als die ganze anorganische Welt.
 Lebewesen enthalten weitaus mehr Molekülarten und beherbergen weitaus mehr chemische Reaktionsarten als die ganze anorganische Welt. Die aus Biomolekülen aufgebauten biologischen Strukturen sind äußerst
Lebewesen enthalten weitaus mehr Molekülarten und beherbergen weitaus mehr chemische Reaktionsarten als die ganze anorganische Welt. Die aus Biomolekülen aufgebauten biologischen Strukturen sind äußerst
30 Das Blut Das Hämoglobin. Was kann man transfundieren? Notwendige Voruntersuchungen
 498 30 Das Blut Auf dem gleichen Effekt beruht im Übrigen die Tatsache, dass die Gefahr einer Sensibilisierung größer ist, wenn Mutter und erstes Kind AB0-kompatibel sind. Sind sie es nämlich nicht, so
498 30 Das Blut Auf dem gleichen Effekt beruht im Übrigen die Tatsache, dass die Gefahr einer Sensibilisierung größer ist, wenn Mutter und erstes Kind AB0-kompatibel sind. Sind sie es nämlich nicht, so
Km: Michaelis-Konstante: Entspricht der Substratkonzentration, bei der die Hälfte der maximalen Gescwindigkeit (vmax) erreicht wird
 BioMol II Klausur 1. Kinetik 1.1 Michaelis-Menten Michaelis-Menten-Gleichung stellt einen Zusammenhang her zwischen der Konzentration des Substrates und der entsprechenden Geschwindigkeit der Reaktion.
BioMol II Klausur 1. Kinetik 1.1 Michaelis-Menten Michaelis-Menten-Gleichung stellt einen Zusammenhang her zwischen der Konzentration des Substrates und der entsprechenden Geschwindigkeit der Reaktion.
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Musterlösung. Frage Summe Note Punkte 1, ,5 1,0
 Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Die Bindung in Übergangsmetallkomplexenn. Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth
 Die Bindung in Übergangsmetallkomplexenn Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth heorie) Ligandenfeld-Theorie H 3 3+ H 3 H 3 Cr H 3 H 3 H 3 Molekülorbital-Theorie
Die Bindung in Übergangsmetallkomplexenn Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth heorie) Ligandenfeld-Theorie H 3 3+ H 3 H 3 Cr H 3 H 3 H 3 Molekülorbital-Theorie
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus)
 Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit
 In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit in der Nucleotidsequenz der DNA verschlüsselt (codiert)
In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit in der Nucleotidsequenz der DNA verschlüsselt (codiert)
-Klausur Biochemie Name:
 -Klausur Biochemie -03.02.5 Name: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
-Klausur Biochemie -03.02.5 Name: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Der Energiestoffwechsel eukaryotischer Zellen
 Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
-Übersicht. 2. G-Protein-gekoppelte Rezeptoren. 5. Na + -K + -Pumpe REZEPTOREN. 1. Allgemeine Definition: Rezeptoren. 3. Tyrosin-Kinase Rezeptoren
 REZEPTOREN -Übersicht 1. Allgemeine Definition: Rezeptoren 2. G-Protein-gekoppelte Rezeptoren 3. Tyrosin-Kinase Rezeptoren Beispiel: Insulin 4. Steroidhormone 5. Na + -K + -Pumpe EINFÜHRUNG Definition
REZEPTOREN -Übersicht 1. Allgemeine Definition: Rezeptoren 2. G-Protein-gekoppelte Rezeptoren 3. Tyrosin-Kinase Rezeptoren Beispiel: Insulin 4. Steroidhormone 5. Na + -K + -Pumpe EINFÜHRUNG Definition
Proteinogene Aminosäuren. Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren
 Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
ENZYME. Teil 1: Grundlagen und Substratbestimmungen
 ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
Stoffwechsel der essentiellen Aminosäuren
 Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Aufgabe 5 (Supersekundärstruktur)
 Aufgabe 5 (Supersekundärstruktur) Fragestellung Bei der Untereinheit des Arthropodenhämocyanins aus Limulus polyphemus werden folgende Fragestellungen untersucht: - Welche Supersekundärstrukturen gibt
Aufgabe 5 (Supersekundärstruktur) Fragestellung Bei der Untereinheit des Arthropodenhämocyanins aus Limulus polyphemus werden folgende Fragestellungen untersucht: - Welche Supersekundärstrukturen gibt
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine
 4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
Blutzellen: Übersicht. Erythrozyten: Zahl und Form. Erythropoiese. Erythrozyten: Verformbarkeit
 Blutzellen: Übersicht Erythrozyten: Zahl und Form >99% der Blutzellen :4.8*10 12 ; : 5.3*10 12 /Liter Hauptinhaltsstoff: H 2 O und Hämoglobin Form: kernlos bikonkav Oberflächenvergrößerung Erythropoiese
Blutzellen: Übersicht Erythrozyten: Zahl und Form >99% der Blutzellen :4.8*10 12 ; : 5.3*10 12 /Liter Hauptinhaltsstoff: H 2 O und Hämoglobin Form: kernlos bikonkav Oberflächenvergrößerung Erythropoiese
Physiologische Grundlagen der Ausdauer
 Lisa Maria Hirschfelder Aus der Reihe: e-fellows.net stipendiaten-wissen e-fellows.net (Hrsg.) Band 340 Physiologische Grundlagen der Ausdauer Leistungssport - Ausdauer-Grundlagen Skript Physiologische
Lisa Maria Hirschfelder Aus der Reihe: e-fellows.net stipendiaten-wissen e-fellows.net (Hrsg.) Band 340 Physiologische Grundlagen der Ausdauer Leistungssport - Ausdauer-Grundlagen Skript Physiologische
LIPIDE. Periphere Gruppe mit Cysteinylrest. FS-Synthase. Zentrale Gruppe Phosphopanthetinarm kovalente Bindung
 Periphere Gruppe mit Cysteinylrest FS-Synthase Zentrale Gruppe Phosphopanthetinarm kovalente Bindung Die FS-Biosynthse aus Acetyl-CoA und Malonyl-CoA, wird komplett an dem dimeren Multienzymkomplex FETTSÄURESYNTHETASE
Periphere Gruppe mit Cysteinylrest FS-Synthase Zentrale Gruppe Phosphopanthetinarm kovalente Bindung Die FS-Biosynthse aus Acetyl-CoA und Malonyl-CoA, wird komplett an dem dimeren Multienzymkomplex FETTSÄURESYNTHETASE
1 Vom Organismus zum Molekül... 3
 I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
Oxidativer Stress Vitamine
 1 Oxidativer Stress Vitamine 2 Reaktive Sauerstoffspezies (ROS) Reaktive Sauerstoffspezies (ROS) Ein-Elektronenreduktion von Sauerstoff durch Strahlung oder Autooxidation von reduzierten Stoffwechselzwischenprodukten
1 Oxidativer Stress Vitamine 2 Reaktive Sauerstoffspezies (ROS) Reaktive Sauerstoffspezies (ROS) Ein-Elektronenreduktion von Sauerstoff durch Strahlung oder Autooxidation von reduzierten Stoffwechselzwischenprodukten
Schrittweise Oxidation und Decarboxylierung von Glucose-6-phosphat zu Ribulose-5- phosphat
 1. Der plastidäre oxidative Pentosephosphatweg Abbau von Hexose unter NADPH+H + -Synthese Schlüsselenzym=Glucose-6-phosphat-Dehydrogenase Glucose-6-phosphat-Dehydrogenase wird durch Thioredoxin im reduzierten
1. Der plastidäre oxidative Pentosephosphatweg Abbau von Hexose unter NADPH+H + -Synthese Schlüsselenzym=Glucose-6-phosphat-Dehydrogenase Glucose-6-phosphat-Dehydrogenase wird durch Thioredoxin im reduzierten
MGZ. Medizinisch Genetisches Zentrum DIE GENETIK DER THALASSÄMIEN
 MGZ Medizinisch Genetisches Zentrum 1 DIE GENETIK DER THALASSÄMIEN < 0,1 0,1-0,19 0,2-0,99 1,0-4,9 5,0-9,9 10,0-18,9 19,0 Neugeborene mit einer krankhaften Hämoglobinstörung, pro 1000 Lebendgeburten www.ironhealthalliance.com
MGZ Medizinisch Genetisches Zentrum 1 DIE GENETIK DER THALASSÄMIEN < 0,1 0,1-0,19 0,2-0,99 1,0-4,9 5,0-9,9 10,0-18,9 19,0 Neugeborene mit einer krankhaften Hämoglobinstörung, pro 1000 Lebendgeburten www.ironhealthalliance.com
Chemie für Biologen SS Georg Jansen AG Theoretische Organische Chemie Universität Duisburg Essen. (Teil 3: Kovalente Bindungen)
 Chemie für Biologen SS 2007 Georg Jansen AG Theoretische rganische Chemie Universität Duisburg Essen (Teil 3: Kovalente Bindungen) (3) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung
Chemie für Biologen SS 2007 Georg Jansen AG Theoretische rganische Chemie Universität Duisburg Essen (Teil 3: Kovalente Bindungen) (3) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung
Abschlussklausur zur Vorlesung Biomoleküle II WS 2004/05
 16.02.2005 Abschlussklausur zur Vorlesung Biomoleküle II WS 2004/05 Name: Studienfach: Matrikelnummer: Fachsemester: Hinweise: 1. Bitte tragen Sie Ihren Namen, Matrikelnummer, Studienfach und Semesterzahl
16.02.2005 Abschlussklausur zur Vorlesung Biomoleküle II WS 2004/05 Name: Studienfach: Matrikelnummer: Fachsemester: Hinweise: 1. Bitte tragen Sie Ihren Namen, Matrikelnummer, Studienfach und Semesterzahl
Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016
 Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016 Fragen für die Übungsstunde 4 (20.06. 24.06.) Regulation der Transkription II, Translation
Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016 Fragen für die Übungsstunde 4 (20.06. 24.06.) Regulation der Transkription II, Translation
Stoffklasse: LIPIDE Funktionen in der Zelle
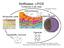 Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
Kapitel 2.2 Kardiopulmonale Homöostase. Kohlendioxid
 Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Vorname: Frage 1. Nennen Sie drei Metalle, die :für den Menschen essentiell sind und als Mengenelemente Körper vorkommen (3 P) Frage 2
 1\.1 Matrikelnummer: Name: Vorname: Bitte eintragen Bitte ankreuzen: Fachsemester: Fachrichtung: Chemie Sonstige Bitte prüfen Sie Ihre Klausur sofort auf Vollständigkeit (Seiten fortlaufend nummeriert
1\.1 Matrikelnummer: Name: Vorname: Bitte eintragen Bitte ankreuzen: Fachsemester: Fachrichtung: Chemie Sonstige Bitte prüfen Sie Ihre Klausur sofort auf Vollständigkeit (Seiten fortlaufend nummeriert
Bioorganische Chemie Enzymatische Katalyse 2011
 Ringvorlesung Chemie B - Studiengang Molekulare Biotechnologie Bioorganische Chemie Enzymatische Katalyse 2011 Prof. Dr. A. Jäschke INF 364, Zi. 308, Tel. 54 48 51 jaeschke@uni-hd.de Lehrziele I Kenntnis
Ringvorlesung Chemie B - Studiengang Molekulare Biotechnologie Bioorganische Chemie Enzymatische Katalyse 2011 Prof. Dr. A. Jäschke INF 364, Zi. 308, Tel. 54 48 51 jaeschke@uni-hd.de Lehrziele I Kenntnis
1) Erklären sie die Begriffe Primär Sekundär und Tertiärstruktur von Proteinen. Nennen Sie drei typische Sekundärstrukturelemente (6P)
 1. Klausur zum Modul 5.3 Biochemie WS 09/10 12.2.2010 1) Erklären sie die Begriffe Primär Sekundär und Tertiärstruktur von Proteinen. Nennen Sie drei typische Sekundärstrukturelemente (6P) 2) Welche Funktion
1. Klausur zum Modul 5.3 Biochemie WS 09/10 12.2.2010 1) Erklären sie die Begriffe Primär Sekundär und Tertiärstruktur von Proteinen. Nennen Sie drei typische Sekundärstrukturelemente (6P) 2) Welche Funktion
Elektronenmikroskopie zeigte die Existenz der A-, P- und E- trna-bindungsstellen. Abb. aus Stryer (5th Ed.)
 Elektronenmikroskopie zeigte die Existenz der A-, P- und E- trna-bindungsstellen Die verschiedenen Ribosomen-Komplexe können im Elektronenmikroskop beobachtet werden Durch Röntgenkristallographie wurden
Elektronenmikroskopie zeigte die Existenz der A-, P- und E- trna-bindungsstellen Die verschiedenen Ribosomen-Komplexe können im Elektronenmikroskop beobachtet werden Durch Röntgenkristallographie wurden
Enzyme als Biokatalysatoren
 1 Enzymwirkung Enzyme als Biokatalysatoren Versuch: Wasserstoffperoxid wird bei RT mit a) Mn(IV)-oxid und b) Katalase versetzt. Beobachtung: a) Gasentwicklung Glimmspanprobe positiv b) Gasentwicklung Glimmspanprobe
1 Enzymwirkung Enzyme als Biokatalysatoren Versuch: Wasserstoffperoxid wird bei RT mit a) Mn(IV)-oxid und b) Katalase versetzt. Beobachtung: a) Gasentwicklung Glimmspanprobe positiv b) Gasentwicklung Glimmspanprobe
 hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
Kapitel 5: 1. Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D.
 Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
Atmung Übersicht. Atmung der Mitochondrien
 Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail. Mag. Gerald Trutschl
 Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail Mag. Gerald Trutschl 1 Inhalt 1. Enzym Reaktion im Detail 2. Thermodynamische Reaktion 3. Katalysemechanismen 4. Michaelis-Menten-Konstante
Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail Mag. Gerald Trutschl 1 Inhalt 1. Enzym Reaktion im Detail 2. Thermodynamische Reaktion 3. Katalysemechanismen 4. Michaelis-Menten-Konstante
Citratzyklus. Citratzyklus
 Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
-, ßa 66, 104, 117 -, aß GG, 104. Sachregister
 10. Addition -intragenische 46, 61, 64 - in der!x-kette 61, 64 -in der ß-Kette 61, 64 Allel 45, 119 Allelie, multiple 70-72!X-Amino-ß-Ketoadipinat 17 J-Aminolävulinat 17 J-Aminolä vulina t-dehydratase.17
10. Addition -intragenische 46, 61, 64 - in der!x-kette 61, 64 -in der ß-Kette 61, 64 Allel 45, 119 Allelie, multiple 70-72!X-Amino-ß-Ketoadipinat 17 J-Aminolävulinat 17 J-Aminolä vulina t-dehydratase.17
