Arbeitsgruppe Regulierung von Arzneimitteln und Prüfungen. Endfassung von Anhang 15 zum EU-Leitfaden einer. guten Herstellungspraxis
|
|
|
- Timo Dunkle
- vor 8 Jahren
- Abrufe
Transkript
1 EUROPÄISCHE KOMMISSION GENERALDIREKTION UNTERNEHMEN Binnenmarkt : Durchführung und Rechtsvorschriften für Verbrauchsgüter Arzneimittel : Rechtsrahment und Genehmigungen für die Markteinführung Arbeitsgruppe Regulierung von Arzneimitteln und Prüfungen Endfassung von Anhang 15 zum EU-Leitfaden einer guten Herstellungspraxis Titel: Qualifizierung und Validierung Erste Erörterung in Redaktionsgruppe Erörterung in der Arbeitsgruppe Regulierung von Arzneimitteln und Prüfungen für die Freigabe zur Beratung 16. September 1999 Pharmazeutischer Ausschuss 28. September 1999 Zur Beratung freigegeben 30. Oktober 1999 Frist für Anmerkungen 28. Februar 2000 Abschließende Genehmigung durch Arbeitsgruppe des Prüfers Dezember 2000 Pharmazeutischer Ausschuss (zur Unterrichtung) April 2001 Datum des Anwendungsbeginns September 2001 Hinweis: Dieses Dokument basiert auf dem Empfehlungen von PICS/S
2 Inhalt Seite 1. Zulassungsprüfung und Validierung 3 2. Planung der Validierung 4 3. Dokumentation 4 4. Qualifizierung 5 5. Prozessvalidierung 6 6. Reinigungsvalidierung 8 7. Änderungskontrolle 8 8. Revalidierung 9 9. Glossar 10 2
3 PRINZIPIEN 1. Der vorliegende Anhang beschreibt die auf die Herstellung von Arzneimittel anzuwendenden Prinzipien der Qualifizierung und Validierung. Es ist eine GMP- Anforderung, dass der Hersteller feststellt, welche Validierungsarbeiten für den Nachweis notwendig sind, dass die kritischen Aspekte der von ihm vorgenommenen Aktivitäten unter Kontrolle stehen. Größere Änderungen an Einrichtungen, Ausrüstung und Prozessen, die die Produktqualität beeinflussen können, sollten validiert werden. Weiterhin sollte eine Risikobewertung vorgenommen werden, um Validierungsumfang und -tiefe bestimmen zu können. 3
4 PLANUNG EINER VALIDIERUNG 2. Alle Validierungsaktivitäten sollten geplant werden. Die Schlüsselelemente eines Validierungsprogramms sollten in einem Validierungsmasterplan (VMP) oder gleichartigen Dokumenten klar definiert und dokumentiert werden. 3. Der VMP sollte eine kurze, präzise und deutliche Zusammenfassung sein. 4. Der VMP sollte mindestens Informationen zu folgenden Punkten enthalten: (a) Validierungspolitik; (b) organisatorische Struktur der Validierungsaktivitäten; (c) zusammenfassende Darstellung der zu validierenden Einrichtungen, Anlagen, Ausrüstung und Prozesse; (d) Dokumentationsformat: das für Anweisungen und Berichte zu verwendende Format; (e) Planung und Zeiteinteilung; (f) Änderungskontrolle; (g) Verweise auf bestehende Dokumente. 5. Im Falle größerer Projekte kann es erforderlich sein, separate Validierungsmasterpläne zu erstellen. DOKUMENTATION 6. Eine schriftliche Anweisung, aus der hervorgeht, wie die Qualifizierung und Validierung durchzuführen ist, ist zu erstellen. Die Anweisung sollte überprüft und genehmigt werden. Aus ihr sollten die kritischen Schritte und die Akzeptanzkriterien hervorgehen. 7. Ein mit Querverweisen auf die Qualifizierungs- und/oder Validierungsanweisungen versehener Bericht sollte erstellt werden, der die Ergebnisse zusammenfasst, festgestellte Abweichungen kommentiert und die notwendigen Schlussfolgerungen zieht. Letzteres schließt Empfehlungen zur Mängelbeseitigung ein. Änderungen des Plans, so wie er in der Anweisung beschrieben ist, sollten zusammen mit einer angemessenen Begründung dokumentiert werden. 8. Im Anschluss an eine zufriedenstellende Qualifizierung sollte in Form einer schriftlichen Genehmigung eine formale Freigabe für den nächsten Schritt der Qualifizierung und Validierung erfolgen. 4
5 QUALIFIZIERUNG Designqualifizierung 9. Der erste Schritt einer Validierung neuer Einrichtungen, Anlagen oder Ausrüstungsgegenstände sollte die Designqualifizierung (DQ) sein. 10. Die Übereinstimmung des Designs mit den GMP-Anforderungen sollte demonstriert und dokumentiert werden. Installationsqualifizierung 11. Bei neuen oder veränderten Einrichtungen, Anlagen oder Ausrüstungsgegenständen ist eine Installationsqualifizierung (IQ) vorzunehmen. 12. Die IQ sollte mindestens umfassen: (a) Installation von Ausrüstung, Rohrleistungen, Versorgungseinrichtungen und Instrumenten nach Abgleich mit aktuellen technischen Zeichnungen und Spezifikationen; (b) Zusammentragen und Vergleich von Betriebs- und Arbeitsanweisungen sowie Wartungsanforderungen des Lieferanten; (c) Anforderungen an die Kalibrierung; (d) Verifizierung der Konstruktionsmaterialien. Funktionsqualifizierung 13. Die Funktionsqualifizierung (OQ) sollte im Anschluss an die Installationsqualifizierung stattfinden. 14. Die OQ sollte mindestens umfassen: (a) Tests, die auf der Grundlage von aus den Prozessen, Anlagen und Ausrüstungsgegenständen gewonnenem Wissen entwickelt wurden; (b) Tests, die obere und untere Betriebsgrenzen mit einschließen, zuweilen als worst case -Bedingungen bezeichnet. 15. Der Abschluß der erfolgreichen Funktionsqualifizierung sollte die Fertigstellung von Kalibrierungs-, Betriebs- und Reinigungsverfahren, Schulung des Bedienpersonals und vorbeugende Wartungsanforderungen erlauben. Er sollte die formale Freigabe der Einrichtungen, Anlagen und Ausrüstung ermöglichen. Leistungsqualifizierung 16. Die Leistungsqualifizierung (PQ) sollte im Anschluss an die erfolgreiche Durchführung einer Installations- und Funktionsqualifizierung vorgenommen werden. 17. Die PQ sollte mindestens umfassen: (a) Tests mit Produktionsmaterialien, geeigneten Ersatzmaterialien oder simulierten Produkten, die auf der Grundlage von aus dem Prozess sowie den Einrichtungen, Anlagen oder Ausrüstungsgegenständen gewonnenem Wissen entwickelt wurden; (b) Tests, die obere und untere Betriebsgrenzen mit einschließen. 5
6 18. Obwohl die Leistungsqualifizierung als eine eigenständige Aktivität dargestellt wird, kann es in einigen Fällen sinnvoll sein, sie zusammen mit der Funktionsqualifizierung durchzuführen. Qualifizierung bestehender (in Gebrauch befindlicher) Einrichtungen, Anlagen und Ausrüstung 19. Es sollten Daten verfügbar sein, die die Betriebsparameter und Grenzwerte für die kritischen Variablen der Betriebsausrüstung stützen und verifizieren. Weiterhin sollten die Verfahren und Aufzeichnungen für Kalibrierung, Reinigung, vorbeugende Wartung, Betriebsvorgänge und Schulungen des Bedienpersonals dokumentiert werden. PROZESSVALIDIERUNG Allgemeine Hinweise 20. Die in diesem Kapitel dargelegten Anforderungen und Prinzipien gelten für die Herstellung pharmazeutischer Darreichungsformen. Abgedeckt werden die anfängliche Validierung neuer Prozesse, die anschließende Validierung veränderter Prozesse und Revalidierungen. 21. Die Prozessvalidierung sollte im Regelfall vor dem Vertrieb eines Arzneimittels abgeschlossen werden (prospektive Validierung). In Ausnahmefällen, wenn dies nicht möglich ist, kann es notwendig sein, Prozesse während der routinemäßigen Produktion zu validieren (begleitende Validierung). Prozesse, die sich bereits seit einiger Zeit im Einsatz befinden, sollten ebenfalls validiert werden (retrospektive Validierung). 22. Die zu verwendenden Einrichtungen Anlagen und Ausrüstungsgegenstände sollten qualifiziert und die analytischen Prüfmethoden validiert worden sein. Die an der Validierung beteiligten Mitarbeiter sollten angemessen geschult worden sein. 23. Einrichtungen, Anlagen, Ausrüstung und Prozesse sollten in bestimmten Zeitabständen bewertet werden, um sicherzustellen, dass sie sich weiterhin in einem validierten Zustand befinden. Prospektive Validierung 24. Eine prospektive Validierung soltel mindestens umfassen: (a) kurze Beschreibung des Prozesses; (b) zusammenfassende Darlegung der zu untersuchenden kritischen Prozessschritte; (c) Auflistung der zu verwendenden Ausrüstung/Einrichtungen (einschließlich Mess- / Überwachungs-/Protokollierausrüstung) zusammen mit ihrem jeweiligen Kalibrierstatus (d) Spezifikationen des Fertigproduktes für die Freigabe; (e) gegebenenfalls eine Auflistung der Prüfmethoden; (f) die vorgeschlagenen Inprozesskontrollen einschließlich Akzeptanzkriterien; (g) gegebenenfalls zusätzlich durchzuführende Prüfungen einschließlich Akzeptanzkriterien und Validierung der Methoden; (h) Probenahmeplan; 6
7 (i) (j) (k) Methoden für die Aufzeichnung und Bewertung von Ergebnissen Funktionen und Verantwortlichkeiten; vorgesehener Zeitplan. 25. Mit Hilfe eines solchen definierten Prozesses (einschließlich spezifizierter Bestandteile) kann eine bestimmte Anzahl von Chargen des Endprodukt unter routinemäßigen Bedingungen hergestellt werden. Theoretisch sollten die Zahl der durchgeführten Prozessläufe und die entsprechenden Beobachtungen ausreichen, um das normale Ausmaß an Variationen und Trends feststellen zu können und ausreichend Daten für eine Bewertung zu erhalten. Allgemein wird es als zulässig angesehen, dass drei aufeinanderfolgende Chargen/Läufe innerhalb der endgültig festgelegten Parameter die Validierung des Prozesses darstellen. 26. Die für die Prozessvalidierung hergestellten Chargen sollten die gleiche Größe wie die für den Handel vorgesehen haben. 27. Sollten Validierungschargen verkauft oder vertrieben werden, sollten die Bedingungen, unter denen sie hergestellt werden, vollständig mit den GMP- Anforderungen, inklusive zufriedenstellender Ergebnisse der Validierungsläufe, und mit der Zulassung übereinstimmen. Begleitende Validierung 28. In Ausnahmefällen kann es zulässig sein, vor dem Beginn der routinemäßigen Produktion das Validierungsprogramm noch nicht abgeschlossen zu haben. 29. Die Entscheidung, eine begleitende Validierung durchzuführen, muss begründet, dokumentiert und von befugtem Personal genehmigt werden. 30. Die für eine begleitende Validierung notwendige Dokumentation entspricht der für die prospektive Validierung. Retrospektive Validierung 31. Eine retrospektive Validierung ist nur bei gut etablierten Prozessen zulässig und gilt dann als ungeeignet, wenn vor Kurzem Änderungen an der Zusammensetzung des Produkts, den Betriebsverfahren oder der Ausrüstung vorgenommen wurden. 32. Die Validierung derartiger Prozesse sollte sich auf historische Daten stützen. Die hierbei zu durchlaufenden Schritte erfordern die Erstellung einer spezifischen Anweisung sowie eine Darlegung der Ergebnisse der Datenüberprüfung, die zu einer Schlussfolgerung und einer Empfehlung führen soll. 33. Die Datenquellen für eine solche Validierung sollten mindestens Chargenherstellungs- und Verpackungsprotokolle, Prozesskontrolldiagramme, Wartungslogbücher, Aufzeichnungen zu Personalwechseln, Prozessfähigkeitsuntersuchungen sowie Daten zum Fertigprodukt einschließlich Trendkarten und Stabilitätsergebnisse aus der Lagerung umfassen. 34. Die für die retrospektive Validierung gewählten Chargen sollten repräsentativ für alle während des Überprüfungszeitraums hergestellten Chargen, einschließlich derjenigen, die außerhalb der Spezifikationen lagen, sein und ausreichend in der Anzahl sein, um die Beständigkeit des Prozesses nachweisen zu können. Eine zusätzliche Überprüfung von Rückstellmustern kann erforderlich sein, um die für eine retrospektive Validierung notwendige Menge an oder Art von Daten zu erhalten. 7
8 35. Bei der retrospektiven Validierung sollten grundsätzlich Daten von zehn bis dreißig aufeinanderfolgenden Chargen untersucht werden, um die Beständigkeit des Prozesses zu bewerten. Bei entsprechender Begründung können weniger Chargen untersucht werden. REINIGUNGSVALIDIERUNG 36. Eine Reinigungsvalidierung ist durchzuführen, um die Wirksamkeit eines Reinigungsverfahren zu belegen. Die Begründung für die Festlegung von Grenzwerten für die Übertragung von Produktrückständen, Reinigungsmitteln und mikrobieller Kontamination sollte logisch auf der Basis der beteiligten Materialien erfolgen. Die Grenzwerte sollten erreichbar und verifizierbar sein. 37. Es sollten validierte Prüfmethoden, die empfindlich genug sind, Rückstände oder Kontaminanten nachzuweisen, verwendet werden. Die jeweilige Prüfmethode sollte eine ausreichend empfindliche Nachweisgrenze aufweisen, um das festgelegte akzeptable Maß der Rückstände oder Kontaminenten bestimmen zu können. 38. Im Regelfall müssen nur Reinigungsverfahren für produktberührende Ausrüstungsoberflächen validiert werden. Gegebenenfalls sollten auch Teile, die keinen Kontakt mit dem Produkt haben, berücksichtigt werden. Die Zeitabstände zwischen der Verwendung und der Reinigung sowie der Reinigung und der Wiederverwendung sollten validiert werden. Reinigungsintervalle und -methoden sind festzulegen. 39. Bei Reinigungsverfahren für einander ähnliche Produkte und Prozesse gilt es als zulässig, eine repräsentative Auswahl der ähnlichen Produkte und Prozesse zu treffen. Zu diesem Zweck kann eine einzelne Validierungsuntersuchung, der ein worst case -Vorgehen zugrundeliegt und die alle kritischen Aspekte berücksichtigt, vorgenommen werden. 40. Normalerweise sollte ein Reinigungsverfahren dreimal hintereinander vollzogen und als erfolgreich eingestuft worden sein, um zu beweisen, dass die entsprechende Methode validiert ist. 41. Ein Reinigen bis zur Sauberkeit ( test until clean ) gilt nicht als geeignete Alternative zur Reinigungsvalidierung. 42. Ausnahmsweise können Produkte, die die physikochemischen Eigenschaften der zu beseitigenden Substanzen simulieren, statt der Substanzen selbst verwendet werden, wenn diese entweder toxisch oder gefährlich sind. ÄNDERUNGSKONTROLLE 43. Für den Fall der beabsichtigen Änderung an einem Ausgangsstoff, einem Produktbestandteil, einem Ausrüstungsgegenstand, der Prozessumgebung (oder der Anlage), der Produktions- oder Testmethode oder jeder anderen Änderung, 8
9 die die Produktqualität oder Reproduzierbarkeit des Prozesses beeinflussen könnte, sollte es schriftliche Verfahren geben, die die dann zu ergreifenden Maßnahmen darlegen. Änderungskontrollverfahren sollten sicherstellen, dass ausreichend stützende Daten erzeugt werden, um beweisen zu können, dass mit Hilfe des überarbeiteten Prozesses ein der gewünschten Qualität und den genehmigten Spezifikationen entsprechendes Produkt hergestellt werden kann. 44. Alle Änderungen, die die Produktqualität oder die Reproduzierbarkeit des Prozesses beeinflussen könnten, sollten formal beantragt, dokumentiert und genehmigt werden. Die wahrscheinlichen Auswirkungen der Änderung der Einrichtungen, Anlagen und Ausrüstung auf das Produkt sollten bewertet werden. Dies schließt eine Risikoanalyse ein. Der Bedarf und das Ausmaß einer Requalifizierung oder Revalidierung sollten bestimmt werden. REVALIDIERUNG 45. Einrichtungen, Anlagen, Ausrüstung und Prozesse einschließlich der Reinigung sollten in bestimmten Zeitabständen bewertet werden, um zu gewährleisten, dass sie sich weiterhin in einem validierten Zustand befinden. Wurden am Validierungsstatus keine bedeutenden Änderungen vorgenommen, erfüllt eine Überprüfung, die den Nachweis erbringt, dass die Einrichtungen, Systeme, Ausrüstung und Prozesse den vorgeschriebenen Anforderungen entsprechen, die Notwendigkeit einer Revalidierung. 9
10 GLOSSAR Es folgen Definitionen von mit Qualifizierung und Validierung in Zusammenhang stehenden Begriffen, die nicht im Glossar des aktuellen GMP-Leitfadens der EG enthalten sind, aber im vorliegenden Anhang verwendet werden. Änderungskontrolle Ein formales System, durch das qualifizierte Vertreter entsprechender Fachbereiche beabsichtigte oder tatsächliche Änderungen, die den validierten Zustand von Einrichtungen, Anlagen, Ausrüstung oder Prozessen beeinflussen könnten, überprüfen. Ziel ist es, die Vorkehrungen festzulegen, die für den Nachweis und die Dokumentation der Einhaltung des validierten Zustands erforderlich sind. Anlage Summe miteinander verbundener Geräte mit gemeinsamer Zweckbestimmung. Begleitende Validierung Validierung, die während der routinemäßigen Herstellung von für den Verkauf bestimmten Produkten durchgeführt wird. Designqualifizierung (DQ) Eine dokumentierte Verifizierung, dass das für Einrichtungen, Anlagen und Ausrüstung vorgesehene Design für den entsprechenden Verwendungszweck geeignet ist. Funktionsqualifizierung (OQ) Eine dokumentierte Verifizierung, dass Einrichtungen, Anlagen und Ausrüstung, so wie sie installiert oder modifiziert wurden, im Rahmen der vorgesehenen Betriebsbereiche den Erwartungen gemäß funktionieren. Installationsqualifizierung (IQ) Eine dokumentiere Verifizierung, dass Einrichtungen, Anlagen und Ausrüstung, so wie sie installiert oder modifiziert wurden, mit dem genehmigten Design und den Empfehlungen des Herstellers übereinstimmen. Leistungsqualifizierung (PQ) Eine dokumentierte Verifizierung, dass Einrichtungen, Anlagen und Ausrüstung, so wie sie miteinander verbunden wurden, auf der Grundlage der genehmigten Prozessmethode und Produktspezifikation effektiv und reproduzierbar funktionieren. Prospektive Validierung Eine vor der routinemäßigen Produktion von für den Verkauf bestimmten Produkten durchgeführte Validierung. Prozessvalidierung Dokumentierte Beweisführung, dass der Prozess innerhalb bestimmter Parameter auf effektive und reproduzierbare Art ein Arzneimittel hervorbringt, dass im voraus festgelegte Spezifikationen und Qualitätsattribute erfüllt. Reinigungsvalidierung 10
11 Bei der Reinigungsvalidierung handelt es sich um eine dokumentierte Beweisführung, dass ein genehmigtes Reinigungsverfahren die Ausrüstung in einen Zustand versetzt, in dem sie für die Herstellung von Arzneimitteln geeignet ist. Retrospektive Validierung Prozessvalidierung für ein Produkt, dass auf der Grundlage von zusammengetragenen Herstellungs-, Test- und Kontrollchargendaten auf den Markt gebracht wurde. Revalidierung Eine Wiederholung der Prozessvalidierung, um zu gewährleisten, dass Änderungen am Prozess oder der Ausrüstung, die gemäß bestimmter Änderungskontrollverfahren vorgenommen wurden, die Prozesseigenschaften und die Produktqualität nicht beeinträchtigen. Risikoanalyse Methode, die für das Funktionieren von Ausrüstung oder Prozess kritischen Parameter zu bewerten und zu definieren. Simuliertes Produkt Ein Material, das den physikalischen und, wenn möglich, den chemischen Eigenschaften (z.b. Viskosität, Korngröße, ph, etc.) des zu validierenden Produkts sehr ähnlich ist. In vielen Fällen können diese Eigenschaften mit Hilfe einer Placebocharge erreicht werden. Worst Case Eine oder mehrere Bedingungen, die obere und untere Betriebsgrenzen und die Umstände in den zugrundeliegenden Standardverfahrensanweisungen einschließen, bei denen, verglichen mit den Idealbedingungen, fehlerhafte Prozesse oder Produkte mit der größten Wahrscheinlichkeit auftreten. Diese Bedingungen führen nicht zwangsläufig zu einem Produkt- oder Prozessversagen. 11
Abweichungen. Anforderungen / Zitate aus den Rechtsvorschriften
 Abweichungen Anforderungen / Zitate aus den Rechtsvorschriften AMWHV [...] Alle Abweichungen im Prozess und von der Festlegung der Spezifikation sind zu dokumentieren und gründlich zu untersuchen. [...]
Abweichungen Anforderungen / Zitate aus den Rechtsvorschriften AMWHV [...] Alle Abweichungen im Prozess und von der Festlegung der Spezifikation sind zu dokumentieren und gründlich zu untersuchen. [...]
Ein Weg zu einem qualifizierten Zustand. Der vorliegende Text und dass Prüfprozedere ist praxisnahe es wird kein Anspruch auf vollstädigkeit gegeben.
 Ein Weg zu einem qualifizierten Zustand Der vorliegende Text und dass Prüfprozedere ist praxisnahe es wird kein Anspruch auf vollstädigkeit gegeben. VMP VMP = Validierungs Master Plan Im VMP muss die detaillierte
Ein Weg zu einem qualifizierten Zustand Der vorliegende Text und dass Prüfprozedere ist praxisnahe es wird kein Anspruch auf vollstädigkeit gegeben. VMP VMP = Validierungs Master Plan Im VMP muss die detaillierte
Dok.-Nr.: Seite 1 von 6
 Logo Apotheke Planung, Durchführung und Dokumentation von QM-Audits Standardarbeitsanweisung (SOP) Standort des Originals: Dok.-Nr.: Seite 1 von 6 Nummer der vorliegenden Verfaßt durch Freigabe durch Apothekenleitung
Logo Apotheke Planung, Durchführung und Dokumentation von QM-Audits Standardarbeitsanweisung (SOP) Standort des Originals: Dok.-Nr.: Seite 1 von 6 Nummer der vorliegenden Verfaßt durch Freigabe durch Apothekenleitung
PRÜFMODUL D UND CD. 1 Zweck. 2 Durchführung. 2.1 Allgemeines. 2.2 Antrag
 1 Zweck PRÜFMODUL D UND CD Diese Anweisung dient als Basis für unsere Kunden zur Information des Ablaufes der folgenden EG-Prüfung nach folgenden Prüfmodulen: D CD Es beschreibt die Aufgabe der benannten
1 Zweck PRÜFMODUL D UND CD Diese Anweisung dient als Basis für unsere Kunden zur Information des Ablaufes der folgenden EG-Prüfung nach folgenden Prüfmodulen: D CD Es beschreibt die Aufgabe der benannten
WS 2011 / 2012 Spezielles Arzneimittelrecht Industrielle Arzneimittelherstellung versus Individualherstellung Teil II 2. November 2011 in Mainz
 WS 2011 / 2012 Spezielles Arzneimittelrecht Industrielle Arzneimittelherstellung versus Individualherstellung Teil II in Mainz Folie 1 2 Begriffsbestimmungen 3. ist der EG-GMP Leitfaden (BAnz. S. 6887)
WS 2011 / 2012 Spezielles Arzneimittelrecht Industrielle Arzneimittelherstellung versus Individualherstellung Teil II in Mainz Folie 1 2 Begriffsbestimmungen 3. ist der EG-GMP Leitfaden (BAnz. S. 6887)
Prof. Dr. Werner Fresenius / Vorsitzender AG AAMP. Tierarzneimittelbereich: Dr. Heinrich Bottermann / Vorsitzender AG AfAM. <Oberste Landesbehörde>
 Dokumenten-Nr.: 07110702 Verfahrensanweisung Gültig ab: Zentralstelle der Länder für Gesundheitsschutz bei Arzneimiteln und Medizinprodukten 1/5 Titel: Site Master File (SMF) Geltungsbereich: Inspektorat
Dokumenten-Nr.: 07110702 Verfahrensanweisung Gültig ab: Zentralstelle der Länder für Gesundheitsschutz bei Arzneimiteln und Medizinprodukten 1/5 Titel: Site Master File (SMF) Geltungsbereich: Inspektorat
Abschnitt 2 Vier Fragen, jeweils 5 Punkte pro Frage erreichbar (Maximal 20 Punkte)
 Abschnitt 1 2. Listen Sie zwei Abschnitte von ISO 9001 (Nummer und Titel) auf. die das Qualitätsmanagementprinzip Systemorientierter Ansatz unterstützen. (2 Punkte) Abschnitt 2 Vier Fragen, jeweils 5 Punkte
Abschnitt 1 2. Listen Sie zwei Abschnitte von ISO 9001 (Nummer und Titel) auf. die das Qualitätsmanagementprinzip Systemorientierter Ansatz unterstützen. (2 Punkte) Abschnitt 2 Vier Fragen, jeweils 5 Punkte
Managementbewertung Managementbewertung
 Managementbewertung Grundlagen für die Erarbeitung eines Verfahrens nach DIN EN ISO 9001:2000 Inhalte des Workshops 1. Die Anforderungen der ISO 9001:2000 und ihre Interpretation 2. Die Umsetzung der Normanforderungen
Managementbewertung Grundlagen für die Erarbeitung eines Verfahrens nach DIN EN ISO 9001:2000 Inhalte des Workshops 1. Die Anforderungen der ISO 9001:2000 und ihre Interpretation 2. Die Umsetzung der Normanforderungen
Automatisierte Fertigungsprozesse. Umbruch in der Medizintechnik. Medizintechnisches Kolloquium 06.11.2012
 Automatisierte Fertigungsprozesse Umbruch in der Medizintechnik Medizintechnisches Kolloquium 06.11.2012 Rolf Andrasi Unit Manager Plates Stryker Leibinger GmbH & Co.KG Agenda Unternehmensvorstellung Stryker
Automatisierte Fertigungsprozesse Umbruch in der Medizintechnik Medizintechnisches Kolloquium 06.11.2012 Rolf Andrasi Unit Manager Plates Stryker Leibinger GmbH & Co.KG Agenda Unternehmensvorstellung Stryker
SAQ FG Medizinprodukte Hersteller. Validierung
 SAQ FG Medizinprodukte Hersteller Validierung Die Forderungen der ISO 13485:2003 und EU Richtlinien aus der Sicht einer Zertifizierungsstelle 1 Was heisst Verifizierung / Validierung? Gemäss EN ISO 9000:2000:
SAQ FG Medizinprodukte Hersteller Validierung Die Forderungen der ISO 13485:2003 und EU Richtlinien aus der Sicht einer Zertifizierungsstelle 1 Was heisst Verifizierung / Validierung? Gemäss EN ISO 9000:2000:
Qualitätsmanagement-Handbuch. 1.7 Projektmanagement
 Seite 1 von 5 Erstellt: Geprüft: Freigegeben: Dr. Christine Reimann Datum: Datum: Datum: Inhaltsverzeichnis Nr. Element-Abschnitt Seite 1 Ziel und Zweck 2 2 Geltungsbereich / Verantwortung 2 3 Vorgehen
Seite 1 von 5 Erstellt: Geprüft: Freigegeben: Dr. Christine Reimann Datum: Datum: Datum: Inhaltsverzeichnis Nr. Element-Abschnitt Seite 1 Ziel und Zweck 2 2 Geltungsbereich / Verantwortung 2 3 Vorgehen
Wann ist eine Software in Medizinprodukte- Aufbereitungsabteilungen ein Medizinprodukt?
 DGSV-Kongress 2009 Wann ist eine Software in Medizinprodukte- Aufbereitungsabteilungen ein Medizinprodukt? Sybille Andrée Betriebswirtin für und Sozialmanagement (FH-SRH) Prokuristin HSD Händschke Software
DGSV-Kongress 2009 Wann ist eine Software in Medizinprodukte- Aufbereitungsabteilungen ein Medizinprodukt? Sybille Andrée Betriebswirtin für und Sozialmanagement (FH-SRH) Prokuristin HSD Händschke Software
Referent: Mathias Notheis Kontakt: Mathias.Notheis@dqs.de
 ISO/IEC 62304 Medizingeräte-Software Referent: Mathias Notheis Kontakt: Mathias.Notheis@dqs.de DQS Medizin nprodukte GmbH Übersicht Basics Wann ist ein MP Software? Markteinführung vor der 62304 alles
ISO/IEC 62304 Medizingeräte-Software Referent: Mathias Notheis Kontakt: Mathias.Notheis@dqs.de DQS Medizin nprodukte GmbH Übersicht Basics Wann ist ein MP Software? Markteinführung vor der 62304 alles
Validierung von Heißsiegelprozessen nach DIN EN ISO 11607-2
 Validierung von Heißsiegelprozessen nach DIN EN ISO 11607-2 Ralph Ebersbach Vortrag auf dem 3. Berlin/Brandenburger Steritreff am 15. September 2012 in Berlin Mehr wissen. Weiter denken. Über HYBETA HYBETA
Validierung von Heißsiegelprozessen nach DIN EN ISO 11607-2 Ralph Ebersbach Vortrag auf dem 3. Berlin/Brandenburger Steritreff am 15. September 2012 in Berlin Mehr wissen. Weiter denken. Über HYBETA HYBETA
1 Allgemeine Angaben Angaben zum Lieferanten: Firma Anschrift
 1 Allgemeine Angaben Angaben zum Lieferanten: Firma Anschrift Straße PLZ und Ort Telefon Fax Ansprechpartner Vor-, Nachname Funktion Abteilung E-Mail Qualitätsmanagement Qualitätsmanager Vor-, Nachname
1 Allgemeine Angaben Angaben zum Lieferanten: Firma Anschrift Straße PLZ und Ort Telefon Fax Ansprechpartner Vor-, Nachname Funktion Abteilung E-Mail Qualitätsmanagement Qualitätsmanager Vor-, Nachname
Schweizer Verordnung über Bedarfsgegenstände in Kontakt mit Lebensmitteln (SR 817.023.21) Zugelassene Stoffe für Verpackungstinten
 Schweizer Verordnung über Bedarfsgegenstände in Kontakt mit Lebensmitteln (SR 817.023.21) Zugelassene Stoffe für Verpackungstinten Fragen und Antworten Seite 1 von 6 Das Eidgenössische Department des Innern
Schweizer Verordnung über Bedarfsgegenstände in Kontakt mit Lebensmitteln (SR 817.023.21) Zugelassene Stoffe für Verpackungstinten Fragen und Antworten Seite 1 von 6 Das Eidgenössische Department des Innern
Rückverfolgbarkeit ISO 13485
 ISO 13485 Normforderung Rückverfolgbarkeit Stolpersteine aus Sicht einer Zertifizierungsstelle ISO 13485 Die Norm ISO 13485: Zweck: Zur Unterstützung der Erfüllung der grundlegenden Anforderungen der europäischen
ISO 13485 Normforderung Rückverfolgbarkeit Stolpersteine aus Sicht einer Zertifizierungsstelle ISO 13485 Die Norm ISO 13485: Zweck: Zur Unterstützung der Erfüllung der grundlegenden Anforderungen der europäischen
6 Informationsermittlung und Gefährdungsbeurteilung
 Verordnung zum Schutz vor Gefahrstoffen TK Lexikon Arbeitsrecht 6 Informationsermittlung und Gefährdungsbeurteilung HI2516431 (1) 1 Im Rahmen einer Gefährdungsbeurteilung als Bestandteil der Beurteilung
Verordnung zum Schutz vor Gefahrstoffen TK Lexikon Arbeitsrecht 6 Informationsermittlung und Gefährdungsbeurteilung HI2516431 (1) 1 Im Rahmen einer Gefährdungsbeurteilung als Bestandteil der Beurteilung
Name Funktion Datum Unterschrift
 Bericht über die Kassenprüfung der Teilgliederung Kreisverband Mittelhaardt der Piratenpartei Deutschland für das laufende Geschäftsjahr 2010 (12.12.2009 01.11.2010) Name Funktion Datum Unterschrift Markus
Bericht über die Kassenprüfung der Teilgliederung Kreisverband Mittelhaardt der Piratenpartei Deutschland für das laufende Geschäftsjahr 2010 (12.12.2009 01.11.2010) Name Funktion Datum Unterschrift Markus
Erlaubnisscheine bei der Instandhaltung
 Erlaubnisscheine bei der Instandhaltung Werner Weiß BASF SE Standort Ludwigshafen 22.09.2010 Werner Weiß, BASF SE 1 BASF SE Standort Ludwigshafen Stammwerk Fläche ca 10 km² Mitarbeiter ~ 32 500 Kontraktorenmitarbeiter
Erlaubnisscheine bei der Instandhaltung Werner Weiß BASF SE Standort Ludwigshafen 22.09.2010 Werner Weiß, BASF SE 1 BASF SE Standort Ludwigshafen Stammwerk Fläche ca 10 km² Mitarbeiter ~ 32 500 Kontraktorenmitarbeiter
Rückverfolgbarkeit von Lebensmitteln Erfahrungen aus den Ländern
 Rückverfolgbarkeit von Lebensmitteln Erfahrungen aus den Ländern Untersuchung und Erfassung lebensmittelbedingter Ausbrüche Informationsveranstaltung des Bundesinstituts für Risikobewertung am 25. Januar
Rückverfolgbarkeit von Lebensmitteln Erfahrungen aus den Ländern Untersuchung und Erfassung lebensmittelbedingter Ausbrüche Informationsveranstaltung des Bundesinstituts für Risikobewertung am 25. Januar
Änderungskontrolle. Anforderungen / Zitate aus den Rechtsvorschriften
 Änderungskontrolle Anforderungen / Zitate aus den Rechtsvorschriften Definition im Glossar zum Annex 15 (Qualifizierung und Validierung) des EU-GMP-Leitfadens: Die Änderungskontrolle ist ein formales System,
Änderungskontrolle Anforderungen / Zitate aus den Rechtsvorschriften Definition im Glossar zum Annex 15 (Qualifizierung und Validierung) des EU-GMP-Leitfadens: Die Änderungskontrolle ist ein formales System,
Richtlinie für den Zeitpunkt der Erstkontrolle
 Seite: 1 von 6 EUREPGAP Richtlinie für den Zeitpunkt der Erstkontrolle Obst und Gemüse Version 1.5-Sep05 Veröffentlicht am 30. September 2005 Änderungen seit der letzten Version sind rot markiert. Seite:
Seite: 1 von 6 EUREPGAP Richtlinie für den Zeitpunkt der Erstkontrolle Obst und Gemüse Version 1.5-Sep05 Veröffentlicht am 30. September 2005 Änderungen seit der letzten Version sind rot markiert. Seite:
Hilfe zur Urlaubsplanung und Zeiterfassung
 Hilfe zur Urlaubsplanung und Zeiterfassung Urlaubs- und Arbeitsplanung: Mit der Urlaubs- und Arbeitsplanung kann jeder Mitarbeiter in Coffee seine Zeiten eintragen. Die Eintragung kann mit dem Status anfragen,
Hilfe zur Urlaubsplanung und Zeiterfassung Urlaubs- und Arbeitsplanung: Mit der Urlaubs- und Arbeitsplanung kann jeder Mitarbeiter in Coffee seine Zeiten eintragen. Die Eintragung kann mit dem Status anfragen,
Regulatorische Anforderungen an die Entwicklung von Medizinprodukten
 Regulatorische Anforderungen an die Entwicklung von Medizinprodukten Alexander Fink, Metecon GmbH Institut für Medizintechnik Reutlingen University Alteburgstraße 150 D-72762 Reutlingen Reutlingen, 04.03.2015
Regulatorische Anforderungen an die Entwicklung von Medizinprodukten Alexander Fink, Metecon GmbH Institut für Medizintechnik Reutlingen University Alteburgstraße 150 D-72762 Reutlingen Reutlingen, 04.03.2015
Qualitätsmanagement. Audit-Fragebogen. für Lieferanten der. x-y GmbH QUALITÄTS- MANAGEMENT. Fragebogen für externes Lieferantenaudit SYSTEM.
 von 4 Qualitätsmanagement Audit-Fragebogen für Lieferanten der x-y GmbH QM 05-09/ 2 von 4 auditiertes Unternehmen: QM 05-09/ 3 von 4 INHALTSVERZEICHNIS. Vorwort 2. Fragen zur Unternehmens- bzw. Betriebsorganisation
von 4 Qualitätsmanagement Audit-Fragebogen für Lieferanten der x-y GmbH QM 05-09/ 2 von 4 auditiertes Unternehmen: QM 05-09/ 3 von 4 INHALTSVERZEICHNIS. Vorwort 2. Fragen zur Unternehmens- bzw. Betriebsorganisation
Häufig wiederkehrende Fragen zur mündlichen Ergänzungsprüfung im Einzelnen:
 Mündliche Ergänzungsprüfung bei gewerblich-technischen und kaufmännischen Ausbildungsordnungen bis zum 31.12.2006 und für alle Ausbildungsordnungen ab 01.01.2007 Am 13. Dezember 2006 verabschiedete der
Mündliche Ergänzungsprüfung bei gewerblich-technischen und kaufmännischen Ausbildungsordnungen bis zum 31.12.2006 und für alle Ausbildungsordnungen ab 01.01.2007 Am 13. Dezember 2006 verabschiedete der
Erstellung eines QM-Handbuches nach DIN. EN ISO 9001:2008 - Teil 1 -
 Erstellung eines QM-Handbuches nach DIN Klaus Seiler, MSc. managementsysteme Seiler Zum Salm 27 D-88662 Überlingen / See EN ISO 9001:2008 - Teil 1 - www.erfolgsdorf.de Tel: 0800 430 5700 1 Der Aufbau eines
Erstellung eines QM-Handbuches nach DIN Klaus Seiler, MSc. managementsysteme Seiler Zum Salm 27 D-88662 Überlingen / See EN ISO 9001:2008 - Teil 1 - www.erfolgsdorf.de Tel: 0800 430 5700 1 Der Aufbau eines
Zwischen Deutschland, Liechtenstein, Österreich und der Schweiz abgestimmte deutsche Übersetzung
 Zwischen Deutschland, Liechtenstein, Österreich und der Schweiz abgestimmte deutsche Übersetzung ÄNDERUNG DES ÜBEREINKOMMENS ÜBER DEN ZUGANG ZU INFORMATIONEN, DIE ÖFFENTLICHKEITSBETEILIGUNG AN ENTSCHEIDUNGSVERFAHREN
Zwischen Deutschland, Liechtenstein, Österreich und der Schweiz abgestimmte deutsche Übersetzung ÄNDERUNG DES ÜBEREINKOMMENS ÜBER DEN ZUGANG ZU INFORMATIONEN, DIE ÖFFENTLICHKEITSBETEILIGUNG AN ENTSCHEIDUNGSVERFAHREN
Beispielfragen L4(3) Systemauditor nach AS/EN9100 (1st,2nd party)
 Allgemeine Hinweise: Es wird von den Teilnehmern erwartet, dass ausreichende Kenntnisse vorhanden sind, um die Fragen 1.1 bis 1.10 unter Verwendung der EN 9100 und ISO 19011 innerhalb von 20 Minuten zu
Allgemeine Hinweise: Es wird von den Teilnehmern erwartet, dass ausreichende Kenntnisse vorhanden sind, um die Fragen 1.1 bis 1.10 unter Verwendung der EN 9100 und ISO 19011 innerhalb von 20 Minuten zu
Lenkung der QM-Dokumentation
 Datum des LAV-Beschlusses: 08.05.2007 Seite1 von 5 Inhalt 1 Zweck, Ziel... 1 2 Geltungsbereich... 1 3 Begriffe, Definitionen... 1 4 Beschreibung... 2 4.1 Struktur der QM-Dokumentation... 2 4.2 Aufbau der
Datum des LAV-Beschlusses: 08.05.2007 Seite1 von 5 Inhalt 1 Zweck, Ziel... 1 2 Geltungsbereich... 1 3 Begriffe, Definitionen... 1 4 Beschreibung... 2 4.1 Struktur der QM-Dokumentation... 2 4.2 Aufbau der
teischl.com Software Design & Services e.u. office@teischl.com www.teischl.com/booknkeep www.facebook.com/booknkeep
 teischl.com Software Design & Services e.u. office@teischl.com www.teischl.com/booknkeep www.facebook.com/booknkeep 1. Erstellen Sie ein neues Rechnungsformular Mit book n keep können Sie nun Ihre eigenen
teischl.com Software Design & Services e.u. office@teischl.com www.teischl.com/booknkeep www.facebook.com/booknkeep 1. Erstellen Sie ein neues Rechnungsformular Mit book n keep können Sie nun Ihre eigenen
Charakteristika: VO (EG) 852/2004
 VO (EG) 852/2004 Charakteristika: Ziel: ein hohes Maß an Schutz für Leben und Gesundheit ist Basis des Lebensmittelrechts. HACCP bildet das Herzstück der Steuerung der Lebensmittelsicherheit (ausgenommen
VO (EG) 852/2004 Charakteristika: Ziel: ein hohes Maß an Schutz für Leben und Gesundheit ist Basis des Lebensmittelrechts. HACCP bildet das Herzstück der Steuerung der Lebensmittelsicherheit (ausgenommen
AUF LETZTER SEITE DIESER ANLEITUNG!!!
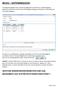 BELEG DATENABGLEICH: Der Beleg-Datenabgleich wird innerhalb des geöffneten Steuerfalls über ELSTER-Belegdaten abgleichen gestartet. Es werden Ihnen alle verfügbaren Belege zum Steuerfall im ersten Bildschirm
BELEG DATENABGLEICH: Der Beleg-Datenabgleich wird innerhalb des geöffneten Steuerfalls über ELSTER-Belegdaten abgleichen gestartet. Es werden Ihnen alle verfügbaren Belege zum Steuerfall im ersten Bildschirm
Entwurf. Anwendungsbeginn E DIN EN 62304 (VDE 0750-101):2013-10. Anwendungsbeginn dieser Norm ist...
 Anwendungsbeginn Anwendungsbeginn dieser Norm ist.... Inhalt Einführung... 13 1 Anwendungsbereich... 16 1.1 *Zweck... 16 1.2 *Anwendungsbereich... 16 1.3 Beziehung zu anderen Normen... 16 1.4 Einhaltung...
Anwendungsbeginn Anwendungsbeginn dieser Norm ist.... Inhalt Einführung... 13 1 Anwendungsbereich... 16 1.1 *Zweck... 16 1.2 *Anwendungsbereich... 16 1.3 Beziehung zu anderen Normen... 16 1.4 Einhaltung...
Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV)
 Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV) Vom 20. Dezember 2001, BGBl. I S. 3854 geändert am 4. Dezember 2002, BGBl I S. 4456 zuletzt geändert am 13. Februar 2004, BGBl I S. 216
Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV) Vom 20. Dezember 2001, BGBl. I S. 3854 geändert am 4. Dezember 2002, BGBl I S. 4456 zuletzt geändert am 13. Februar 2004, BGBl I S. 216
Weisung 2: Technische Anbindung
 Weisung : Technische Anbindung vom 07.09.00 Datum des Inkrafttretens: 0..00 Weisung : Technische Anbindung 0..00 Inhalt. Zweck und Grundlage.... Allgemeines.... Definitionen und Abkürzungen... 4. Anbindungsarten
Weisung : Technische Anbindung vom 07.09.00 Datum des Inkrafttretens: 0..00 Weisung : Technische Anbindung 0..00 Inhalt. Zweck und Grundlage.... Allgemeines.... Definitionen und Abkürzungen... 4. Anbindungsarten
Fachanforderungen für die Abiturprüfung im Fach Elektrotechnik
 Fachanforderungen für die Abiturprüfung im Fach Elektrotechnik auf der Basis der FgVO 1999/03 FG-Handreichung 2004 FgPVO 2001 EPA 1989 Lehrpläne 2002 Stand 07.12.2004 1. Fachliche Qualifikationen Die Schülerinnen
Fachanforderungen für die Abiturprüfung im Fach Elektrotechnik auf der Basis der FgVO 1999/03 FG-Handreichung 2004 FgPVO 2001 EPA 1989 Lehrpläne 2002 Stand 07.12.2004 1. Fachliche Qualifikationen Die Schülerinnen
Sanktionsreglement zu den Richtlinien für Regionalmarken. Eigentümer: IG Regionalprodukte Letzte Aktualisierung: 20.11.2014 Version: 4.
 Sanktionsreglement zu den Richtlinien für Regionalmarken Eigentümer: IG Regionalprodukte Letzte Aktualisierung: 20.11.2014 Version: 4.00 INHALT 1 Zielsetzung / Geltungsbereich... 3 2 Erläuterungen und
Sanktionsreglement zu den Richtlinien für Regionalmarken Eigentümer: IG Regionalprodukte Letzte Aktualisierung: 20.11.2014 Version: 4.00 INHALT 1 Zielsetzung / Geltungsbereich... 3 2 Erläuterungen und
DAkkS Anwendungshinweise DIN EN ISO 50001 Erfassung wesentlicher Energieverbräuche und Überwachung. Stand 05/2014
 DAkkS Anwendungshinweise DIN EN ISO 50001 Erfassung wesentlicher Energieverbräuche und Überwachung Stand 05/2014 Inhalt 1 Vorwort... 3 2 Wesentlichkeitskriterium DIN EN ISO 50001 Kap. 4.4.3 b... 4 2.1
DAkkS Anwendungshinweise DIN EN ISO 50001 Erfassung wesentlicher Energieverbräuche und Überwachung Stand 05/2014 Inhalt 1 Vorwort... 3 2 Wesentlichkeitskriterium DIN EN ISO 50001 Kap. 4.4.3 b... 4 2.1
Kostenstellen verwalten. Tipps & Tricks
 Tipps & Tricks INHALT SEITE 1.1 Kostenstellen erstellen 3 13 1.3 Zugriffsberechtigungen überprüfen 30 2 1.1 Kostenstellen erstellen Mein Profil 3 1.1 Kostenstellen erstellen Kostenstelle(n) verwalten 4
Tipps & Tricks INHALT SEITE 1.1 Kostenstellen erstellen 3 13 1.3 Zugriffsberechtigungen überprüfen 30 2 1.1 Kostenstellen erstellen Mein Profil 3 1.1 Kostenstellen erstellen Kostenstelle(n) verwalten 4
Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV)
 05.07.2005 Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV) vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 13. Februar 2004 (BGBl. I S. 216)
05.07.2005 Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV) vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 13. Februar 2004 (BGBl. I S. 216)
Fachbereich Wirtschaftswissenschaften Die Vorsitzenden der Prüfungsausschüsse
 Fachbereich Wirtschaftswissenschaften Die Vorsitzenden der Prüfungsausschüsse Hinweise für Studierende in den Bachelorstudiengängen Business Administration (B.A.; Rheinbach) Betriebswirtschaft (B.Sc.;
Fachbereich Wirtschaftswissenschaften Die Vorsitzenden der Prüfungsausschüsse Hinweise für Studierende in den Bachelorstudiengängen Business Administration (B.A.; Rheinbach) Betriebswirtschaft (B.Sc.;
Einen Wiederherstellungspunktes erstellen & Rechner mit Hilfe eines Wiederherstellungspunktes zu einem früheren Zeitpunkt wieder herstellen
 Einen Wiederherstellungspunktes erstellen & Rechner mit Hilfe eines Wiederherstellungspunktes zu einem früheren Zeitpunkt wieder herstellen 1 Hier einige Links zu Dokumentationen im WEB Windows XP: http://www.verbraucher-sicher-online.de/node/18
Einen Wiederherstellungspunktes erstellen & Rechner mit Hilfe eines Wiederherstellungspunktes zu einem früheren Zeitpunkt wieder herstellen 1 Hier einige Links zu Dokumentationen im WEB Windows XP: http://www.verbraucher-sicher-online.de/node/18
Maintenance & Re-Zertifizierung
 Zertifizierung nach Technischen Richtlinien Maintenance & Re-Zertifizierung Version 1.2 vom 15.06.2009 Bundesamt für Sicherheit in der Informationstechnik Postfach 20 03 63 53133 Bonn Tel.: +49 22899 9582-0
Zertifizierung nach Technischen Richtlinien Maintenance & Re-Zertifizierung Version 1.2 vom 15.06.2009 Bundesamt für Sicherheit in der Informationstechnik Postfach 20 03 63 53133 Bonn Tel.: +49 22899 9582-0
Fragebogen: Abschlussbefragung
 Fragebogen: Abschlussbefragung Vielen Dank, dass Sie die Ameise - Schulung durchgeführt haben. Abschließend möchten wir Ihnen noch einige Fragen zu Ihrer subjektiven Einschätzung unseres Simulationssystems,
Fragebogen: Abschlussbefragung Vielen Dank, dass Sie die Ameise - Schulung durchgeführt haben. Abschließend möchten wir Ihnen noch einige Fragen zu Ihrer subjektiven Einschätzung unseres Simulationssystems,
Wir beraten Sie. Wir unterstützen Sie. Wir schaffen Lösungen. Wir bringen Qualität. Wir beraten Sie. Wir unterstützen Sie. Wir schaffen Lösungen
 Was bedeutet es, ein Redaktionssystem einzuführen? Vorgehensmodell für die Einführung eines Redaktionssystems Die Bedeutung Fast alle Arbeitsabläufe in der Abteilung werden sich verändern Die inhaltliche
Was bedeutet es, ein Redaktionssystem einzuführen? Vorgehensmodell für die Einführung eines Redaktionssystems Die Bedeutung Fast alle Arbeitsabläufe in der Abteilung werden sich verändern Die inhaltliche
Welche Unterschiede gibt es zwischen einem CAPAund einem Audiometrie- Test?
 Welche Unterschiede gibt es zwischen einem CAPAund einem Audiometrie- Test? Auch wenn die Messungsmethoden ähnlich sind, ist das Ziel beider Systeme jedoch ein anderes. Gwenolé NEXER g.nexer@hearin gp
Welche Unterschiede gibt es zwischen einem CAPAund einem Audiometrie- Test? Auch wenn die Messungsmethoden ähnlich sind, ist das Ziel beider Systeme jedoch ein anderes. Gwenolé NEXER g.nexer@hearin gp
Änderung des EG-GMP Leitfadens, Kapitel 1 u. 6 PQR und Stabilitätsstudien
 Änderung des EG-GMP Leitfadens, Kapitel 1 u. 6 PQR und Stabilitätsstudien Dr. A. Terhechte, BR-Münster Status Quo Kapitel 1 Juli 2003 Entwurf Oktober 2005 Endversion gültig ab 01. Januar 2006 der erste
Änderung des EG-GMP Leitfadens, Kapitel 1 u. 6 PQR und Stabilitätsstudien Dr. A. Terhechte, BR-Münster Status Quo Kapitel 1 Juli 2003 Entwurf Oktober 2005 Endversion gültig ab 01. Januar 2006 der erste
Weisung 2: Technische Anbindung
 SIX Structured Products Exchange AG Weisung : Technische Anbindung vom.04.05 Datum des Inkrafttretens: 0.07.05 Weisung : Technische Anbindung 0.07.05 Inhalt. Zweck und Grundlage.... Allgemeines.... Definitionen
SIX Structured Products Exchange AG Weisung : Technische Anbindung vom.04.05 Datum des Inkrafttretens: 0.07.05 Weisung : Technische Anbindung 0.07.05 Inhalt. Zweck und Grundlage.... Allgemeines.... Definitionen
9001 weitere (kleinere) Änderungen
 6.2 Ziele: SMARTE Ziele: was, Ressorucen, Verantwortung, Termin, Bewertung der Ergebnisse (für ecco nicht nue, wurde aber betont) 6.3 Änderungen: Der Einfluss von Änderungen am QMS uss bewertet werden
6.2 Ziele: SMARTE Ziele: was, Ressorucen, Verantwortung, Termin, Bewertung der Ergebnisse (für ecco nicht nue, wurde aber betont) 6.3 Änderungen: Der Einfluss von Änderungen am QMS uss bewertet werden
ÜBER DIE ROLLE DER NATIONALEN PARLAMENTE IN DER EUROPÄISCHEN UNION
 PROTOKOLL (Nr. 1) zum Vertrag von Lissabon ÜBER DIE ROLLE DER NATIONALEN PARLAMENTE IN DER EUROPÄISCHEN UNION DIE HOHEN VERTRAGSPARTEIEN EINGEDENK dessen, dass die Art der Kontrolle der Regierungen durch
PROTOKOLL (Nr. 1) zum Vertrag von Lissabon ÜBER DIE ROLLE DER NATIONALEN PARLAMENTE IN DER EUROPÄISCHEN UNION DIE HOHEN VERTRAGSPARTEIEN EINGEDENK dessen, dass die Art der Kontrolle der Regierungen durch
ÜBER DIE ANWENDUNG DER GRUNDSÄTZE DER SUBSIDIARITÄT UND DER VERHÄLTNISMÄSSIGKEIT
 PROTOKOLL (Nr. 2) ÜBER DIE ANWENDUNG DER GRUNDSÄTZE DER SUBSIDIARITÄT UND DER VERHÄLTNISMÄSSIGKEIT DIE HOHEN VERTRAGSPARTEIEN IN DEM WUNSCH sicherzustellen, dass die Entscheidungen in der Union so bürgernah
PROTOKOLL (Nr. 2) ÜBER DIE ANWENDUNG DER GRUNDSÄTZE DER SUBSIDIARITÄT UND DER VERHÄLTNISMÄSSIGKEIT DIE HOHEN VERTRAGSPARTEIEN IN DEM WUNSCH sicherzustellen, dass die Entscheidungen in der Union so bürgernah
Übungsbeispiele für die mündliche Prüfung
 Übungsbeispiele für die mündliche Prüfung Nr. Frage: 71-02m Welche Verantwortung und Befugnis hat der Beauftragte der Leitung? 5.5.2 Leitungsmitglied; sicherstellen, dass die für das Qualitätsmanagementsystem
Übungsbeispiele für die mündliche Prüfung Nr. Frage: 71-02m Welche Verantwortung und Befugnis hat der Beauftragte der Leitung? 5.5.2 Leitungsmitglied; sicherstellen, dass die für das Qualitätsmanagementsystem
Kapitel 10: Dokumentation
 Kapitel 10: Dokumentation Inhalt 10.1 Stellenwert der Dokumentation 10.2 Dokumentenlenkung 10.3 Dokumentation des Qualitätsmanagementsystems Schlüsselbegriffe Dokument, Dokumentenlenkung, Qualitätshandbuch
Kapitel 10: Dokumentation Inhalt 10.1 Stellenwert der Dokumentation 10.2 Dokumentenlenkung 10.3 Dokumentation des Qualitätsmanagementsystems Schlüsselbegriffe Dokument, Dokumentenlenkung, Qualitätshandbuch
Sicherheitsbewertungsbericht
 Sicherheitsbewertungsbericht auf Basis der "Verordnung (EG) Nr. 352/2009 der Kommission vom 24. April 2009 über die Festlegung einer gemeinsamen Sicherheitsmethode für die Evaluierung und Bewertung von
Sicherheitsbewertungsbericht auf Basis der "Verordnung (EG) Nr. 352/2009 der Kommission vom 24. April 2009 über die Festlegung einer gemeinsamen Sicherheitsmethode für die Evaluierung und Bewertung von
Delta Audit - Fragenkatalog ISO 9001:2014 DIS
 QUMedia GbR Eisenbahnstraße 41 79098 Freiburg Tel. 07 61 / 29286-50 Fax 07 61 / 29286-77 E-mail info@qumedia.de www.qumedia.de Delta Audit - Fragenkatalog ISO 9001:2014 DIS Zur Handhabung des Audit - Fragenkatalogs
QUMedia GbR Eisenbahnstraße 41 79098 Freiburg Tel. 07 61 / 29286-50 Fax 07 61 / 29286-77 E-mail info@qumedia.de www.qumedia.de Delta Audit - Fragenkatalog ISO 9001:2014 DIS Zur Handhabung des Audit - Fragenkatalogs
Internet Explorer Version 6
 Internet Explorer Version 6 Java Runtime Ist Java Runtime nicht installiert, öffnet sich ein PopUp-Fenster, welches auf das benötigte Plugin aufmerksam macht. Nach Klicken auf die OK-Taste im PopUp-Fenster
Internet Explorer Version 6 Java Runtime Ist Java Runtime nicht installiert, öffnet sich ein PopUp-Fenster, welches auf das benötigte Plugin aufmerksam macht. Nach Klicken auf die OK-Taste im PopUp-Fenster
GPP Projekte gemeinsam zum Erfolg führen
 GPP Projekte gemeinsam zum Erfolg führen IT-Sicherheit Schaffen Sie dauerhaft wirksame IT-Sicherheit nach zivilen oder militärischen Standards wie der ISO 27001, dem BSI Grundschutz oder der ZDv 54/100.
GPP Projekte gemeinsam zum Erfolg führen IT-Sicherheit Schaffen Sie dauerhaft wirksame IT-Sicherheit nach zivilen oder militärischen Standards wie der ISO 27001, dem BSI Grundschutz oder der ZDv 54/100.
Ihr Mandant möchte einen neuen Gesellschafter aufnehmen. In welcher Höhe wäre eine Vergütung inklusive Tantieme steuerrechtlich zulässig?
 Ihr Mandant möchte einen neuen Gesellschafter aufnehmen. In welcher Höhe wäre eine Vergütung inklusive Tantieme steuerrechtlich zulässig? Oft wirft die Aufnahme neuer Gesellschafter oder auch die Einstellung
Ihr Mandant möchte einen neuen Gesellschafter aufnehmen. In welcher Höhe wäre eine Vergütung inklusive Tantieme steuerrechtlich zulässig? Oft wirft die Aufnahme neuer Gesellschafter oder auch die Einstellung
Datenübernahme easyjob 3.0 zu easyjob 4.0
 Datenübernahme easyjob 3.0 zu easyjob 4.0 Einführung...3 Systemanforderung easyjob 4.0...3 Vorgehensweise zur Umstellung zu easyjob 4.0...4 Installation easyjob 4.0 auf dem Server und Arbeitsstationen...4
Datenübernahme easyjob 3.0 zu easyjob 4.0 Einführung...3 Systemanforderung easyjob 4.0...3 Vorgehensweise zur Umstellung zu easyjob 4.0...4 Installation easyjob 4.0 auf dem Server und Arbeitsstationen...4
Qualitätsstandards für Betriebliche Aufträge. Eine Handreichung der IHK-Organisation
 Qualitätsstandards für Betriebliche Aufträge Eine Handreichung der IHK-Organisation Vorwort Für die industriellen Metall- und Elektroberufe wurde vor einigen Jahren das Variantenmodell eingeführt. Der
Qualitätsstandards für Betriebliche Aufträge Eine Handreichung der IHK-Organisation Vorwort Für die industriellen Metall- und Elektroberufe wurde vor einigen Jahren das Variantenmodell eingeführt. Der
Lexware eservice personal - Nutzung ab Januar 2014
 Lexware eservice personal - Nutzung ab Januar 2014 Sie möchten sich von den vielen Vorteilen überzeugen und Lexware eservice personal ab 2014 nutzen. Wie können Sie sich registrieren und welche Funktionen
Lexware eservice personal - Nutzung ab Januar 2014 Sie möchten sich von den vielen Vorteilen überzeugen und Lexware eservice personal ab 2014 nutzen. Wie können Sie sich registrieren und welche Funktionen
Die Beschreibung bezieht sich auf die Version Dreamweaver 4.0. In der Version MX ist die Sitedefinition leicht geändert worden.
 In einer Website haben Seiten oft das gleiche Layout. Speziell beim Einsatz von Tabellen, in denen die Navigation auf der linken oder rechten Seite, oben oder unten eingesetzt wird. Diese Anteile der Website
In einer Website haben Seiten oft das gleiche Layout. Speziell beim Einsatz von Tabellen, in denen die Navigation auf der linken oder rechten Seite, oben oder unten eingesetzt wird. Diese Anteile der Website
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Hygienemanagement. Stand der Revision: 13.11.
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 13.11.2013 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 13.11.2013 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische
Kapitalerhöhung - Verbuchung
 Kapitalerhöhung - Verbuchung Beschreibung Eine Kapitalerhöhung ist eine Erhöhung des Aktienkapitals einer Aktiengesellschaft durch Emission von en Aktien. Es gibt unterschiedliche Formen von Kapitalerhöhung.
Kapitalerhöhung - Verbuchung Beschreibung Eine Kapitalerhöhung ist eine Erhöhung des Aktienkapitals einer Aktiengesellschaft durch Emission von en Aktien. Es gibt unterschiedliche Formen von Kapitalerhöhung.
Der Datenschutzbeauftragte
 Die Zulässigkeit von Videoüberwachungsmaßnahmen am Arbeitsplatz unterliegt sehr strengen gesetzlichen Anforderungen und erfordert immer eine ausführliche Abwägung der betroffenen Interessen des Kameraverwenders
Die Zulässigkeit von Videoüberwachungsmaßnahmen am Arbeitsplatz unterliegt sehr strengen gesetzlichen Anforderungen und erfordert immer eine ausführliche Abwägung der betroffenen Interessen des Kameraverwenders
Anhang V EG-Konformitätserklärung (Qualitätssicherung Produktion)
 Dieses Werk, einschließlich aller seiner Teile, ist urheberrechtlich geschützt. Jede Verwertung außerhalb der engen Grenzen des Urheberrechtsgesetzes ist ohne Zustimmung des Verlages unzulässig und strafbar.
Dieses Werk, einschließlich aller seiner Teile, ist urheberrechtlich geschützt. Jede Verwertung außerhalb der engen Grenzen des Urheberrechtsgesetzes ist ohne Zustimmung des Verlages unzulässig und strafbar.
Für Lieferanten mit zertifiziertem Qualitätsmanagement
 Für Lieferanten mit zertifiziertem Qualitätsmanagement Bitte füllen Sie diesen Fragebogen nur aus, wenn Ihr Unternehmen über ein zertifiziertes Qualitätsmanagement verfügt. Lieferant/Dienstleister der
Für Lieferanten mit zertifiziertem Qualitätsmanagement Bitte füllen Sie diesen Fragebogen nur aus, wenn Ihr Unternehmen über ein zertifiziertes Qualitätsmanagement verfügt. Lieferant/Dienstleister der
Datensicherung. Beschreibung der Datensicherung
 Datensicherung Mit dem Datensicherungsprogramm können Sie Ihre persönlichen Daten problemlos Sichern. Es ist möglich eine komplette Datensicherung durchzuführen, aber auch nur die neuen und geänderten
Datensicherung Mit dem Datensicherungsprogramm können Sie Ihre persönlichen Daten problemlos Sichern. Es ist möglich eine komplette Datensicherung durchzuführen, aber auch nur die neuen und geänderten
Datenübernahme von HKO 5.9 zur. Advolux Kanzleisoftware
 Datenübernahme von HKO 5.9 zur Advolux Kanzleisoftware Die Datenübernahme (DÜ) von HKO 5.9 zu Advolux Kanzleisoftware ist aufgrund der von Update zu Update veränderten Datenbank (DB)-Strukturen in HKO
Datenübernahme von HKO 5.9 zur Advolux Kanzleisoftware Die Datenübernahme (DÜ) von HKO 5.9 zu Advolux Kanzleisoftware ist aufgrund der von Update zu Update veränderten Datenbank (DB)-Strukturen in HKO
Wissenswertes über die Bewertung. Arbeitshilfe
 Wissenswertes über die Bewertung Arbeitshilfe Grundlagen 02 Der Zweck der Archivierung ist es, Rechtssicherheit und Rechtsstaatlichkeit zu gewährleisten, eine kontinuierliche und rationelle Aktenführung
Wissenswertes über die Bewertung Arbeitshilfe Grundlagen 02 Der Zweck der Archivierung ist es, Rechtssicherheit und Rechtsstaatlichkeit zu gewährleisten, eine kontinuierliche und rationelle Aktenführung
InVo. Information zu Verordnungen in der GKV. Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen. Stand: Februar 2010
 Nr. 1 2010 InVo Information zu Verordnungen in der GKV Stand: Februar 2010 Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen Bisher konnten Sie als Arzt Arzneimittel (z. B.
Nr. 1 2010 InVo Information zu Verordnungen in der GKV Stand: Februar 2010 Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen Bisher konnten Sie als Arzt Arzneimittel (z. B.
PowerPoint 2010 Mit Folienmastern arbeiten
 PP.002, Version 1.1 07.04.2015 Kurzanleitung PowerPoint 2010 Mit Folienmastern arbeiten Der Folienmaster ist die Vorlage für sämtliche Folien einer Präsentation. Er bestimmt das Design, die Farben, die
PP.002, Version 1.1 07.04.2015 Kurzanleitung PowerPoint 2010 Mit Folienmastern arbeiten Der Folienmaster ist die Vorlage für sämtliche Folien einer Präsentation. Er bestimmt das Design, die Farben, die
Die Betriebssicherheitsverordnung (BetrSichV) TRBS 1111 TRBS 2121 TRBS 1203
 Die Betriebssicherheitsverordnung (BetrSichV) TRBS 1111 TRBS 2121 TRBS 1203 Achim Eckert 1/12 Am 3. Oktober 2002 ist die Betriebssicherheitsverordnung in Kraft getreten. Auch für den Gerüstbauer und den
Die Betriebssicherheitsverordnung (BetrSichV) TRBS 1111 TRBS 2121 TRBS 1203 Achim Eckert 1/12 Am 3. Oktober 2002 ist die Betriebssicherheitsverordnung in Kraft getreten. Auch für den Gerüstbauer und den
Ordner Berechtigung vergeben Zugriffsrechte unter Windows einrichten
 Ordner Berechtigung vergeben Zugriffsrechte unter Windows einrichten Was sind Berechtigungen? Unter Berechtigungen werden ganz allgemein die Zugriffsrechte auf Dateien und Verzeichnisse (Ordner) verstanden.
Ordner Berechtigung vergeben Zugriffsrechte unter Windows einrichten Was sind Berechtigungen? Unter Berechtigungen werden ganz allgemein die Zugriffsrechte auf Dateien und Verzeichnisse (Ordner) verstanden.
Qualitätsmanagement in Gesundheitstelematik und Telemedizin: Sind ISO 9001 basierte Managementsysteme geeignet?
 DGG e.v. PRE-WORKSHOP TELEMED BERLIN 2009 Qualitätsmanagement in Gesundheitstelematik und Telemedizin: Sind ISO 9001 basierte Managementsysteme geeignet? Dr. med. Markus Lindlar Deutsches Zentrum für Luft-
DGG e.v. PRE-WORKSHOP TELEMED BERLIN 2009 Qualitätsmanagement in Gesundheitstelematik und Telemedizin: Sind ISO 9001 basierte Managementsysteme geeignet? Dr. med. Markus Lindlar Deutsches Zentrum für Luft-
BGI 5190 Wiederkehrende Prüfungen ortsveränderlicher elektrischer Arbeitsmittel - Organisation durch den Unternehmer
 BGI 5190 Wiederkehrende Prüfungen ortsveränderlicher elektrischer Arbeitsmittel - Organisation durch den Unternehmer DGUV Information 5190 (Fassung April 2010) Standort Dresden Dr. Jelena Nagel Gr. 2.4
BGI 5190 Wiederkehrende Prüfungen ortsveränderlicher elektrischer Arbeitsmittel - Organisation durch den Unternehmer DGUV Information 5190 (Fassung April 2010) Standort Dresden Dr. Jelena Nagel Gr. 2.4
Podiumsdiskussion DGSV Kongress 2014 zur KRINKO-BfArM-Empfehlung Validierung Leitung: Dr. M.-Th.Linner, Dr. W. Michels
 Professionelle Aufbereitung von Medizinprodukten Podiumsdiskussion DGSV Kongress 2014 zur KRINKO-BfArM-Empfehlung Validierung Leitung: Dr. M.-Th.Linner, Dr. W. Michels Grundaussagen zur Validierung (1)
Professionelle Aufbereitung von Medizinprodukten Podiumsdiskussion DGSV Kongress 2014 zur KRINKO-BfArM-Empfehlung Validierung Leitung: Dr. M.-Th.Linner, Dr. W. Michels Grundaussagen zur Validierung (1)
KOMMISSION DER EUROPÄISCHEN GEMEINSCHAFTEN. Vorschlag für GEMEINSAME REGELUNG
 KOMMISSION DER EUROPÄISCHEN GEMEINSCHAFTEN Brüssel, den 15.4.2004 SEK(2004) 411 endgültig Vorschlag für GEMEINSAME REGELUNG zur Festlegung der Modalitäten für die Überweisung eines Teils der Dienstbezüge
KOMMISSION DER EUROPÄISCHEN GEMEINSCHAFTEN Brüssel, den 15.4.2004 SEK(2004) 411 endgültig Vorschlag für GEMEINSAME REGELUNG zur Festlegung der Modalitäten für die Überweisung eines Teils der Dienstbezüge
Topo Deutschland 2010 Freischaltung der Karten-Software. Anleitung
 4 8 0 7 2 3 N 1 1 2 7 0 8 E Topo Deutschland 2010 Freischaltung der Karten-Software Anleitung Warum muss ich die Topo Deutschland 2010 freischalten? Für die Nutzung der Karten auf einem PC ist eine Freischaltung
4 8 0 7 2 3 N 1 1 2 7 0 8 E Topo Deutschland 2010 Freischaltung der Karten-Software Anleitung Warum muss ich die Topo Deutschland 2010 freischalten? Für die Nutzung der Karten auf einem PC ist eine Freischaltung
Die vorliegende Arbeitshilfe befasst sich mit den Anforderungen an qualitätsrelevante
 ISO 9001:2015 Die vorliegende Arbeitshilfe befasst sich mit den Anforderungen an qualitätsrelevante Prozesse. Die ISO 9001 wurde grundlegend überarbeitet und modernisiert. Die neue Fassung ist seit dem
ISO 9001:2015 Die vorliegende Arbeitshilfe befasst sich mit den Anforderungen an qualitätsrelevante Prozesse. Die ISO 9001 wurde grundlegend überarbeitet und modernisiert. Die neue Fassung ist seit dem
Installationsanleitung dateiagent Pro
 Installationsanleitung dateiagent Pro Sehr geehrter Kunde, mit dieser Anleitung möchten wir Ihnen die Installation des dateiagent Pro so einfach wie möglich gestalten. Es ist jedoch eine Softwareinstallation
Installationsanleitung dateiagent Pro Sehr geehrter Kunde, mit dieser Anleitung möchten wir Ihnen die Installation des dateiagent Pro so einfach wie möglich gestalten. Es ist jedoch eine Softwareinstallation
Wie erfasse ich die Arzneimittelqualität nach Software-Änderungen sinnvoll?
 Wie erfasse ich die Arzneimittelqualität nach Software-Änderungen sinnvoll? Paul-Ehrlich-Institut M. Doll Paul-Ehrlich-Straße 51-59 63225 Langen GERMANY +49 (0) 6013 77-0 +49 (0) 6013 77-1234 Email: pei@pei.de
Wie erfasse ich die Arzneimittelqualität nach Software-Änderungen sinnvoll? Paul-Ehrlich-Institut M. Doll Paul-Ehrlich-Straße 51-59 63225 Langen GERMANY +49 (0) 6013 77-0 +49 (0) 6013 77-1234 Email: pei@pei.de
Fragebogen zur Anforderungsanalyse
 Fragebogen zur Anforderungsanalyse Geschäftsprozess Datum Mitarbeiter www.seikumu.de Fragebogen zur Anforderungsanalyse Seite 6 Hinweise zur Durchführung der Anforderungsanalyse Bevor Sie beginnen, hier
Fragebogen zur Anforderungsanalyse Geschäftsprozess Datum Mitarbeiter www.seikumu.de Fragebogen zur Anforderungsanalyse Seite 6 Hinweise zur Durchführung der Anforderungsanalyse Bevor Sie beginnen, hier
kundenbezogene Prozesse Produktion und Dienstleistung Lenkung von Überwachungs- und Messmitteln
 Planung Produktrealisierung - Überblick - DIN EN ISO 9001 kundenbezogene Prozesse Entwicklung Beschaffung Produktion und Dienstleistung Lenkung von Überwachungs- und Messmitteln Abb. 1 Qualitätswirksame
Planung Produktrealisierung - Überblick - DIN EN ISO 9001 kundenbezogene Prozesse Entwicklung Beschaffung Produktion und Dienstleistung Lenkung von Überwachungs- und Messmitteln Abb. 1 Qualitätswirksame
DIN EN 1090 Aktuelle Anforderungen an den Korrosionsschutz kennen RA Lars Walther Geschäftsführer QIB e.v.
 DIN EN 1090 Aktuelle Anforderungen an den Korrosionsschutz kennen RA Lars Walther Geschäftsführer QIB e.v. Einführung EN 1090 und was geht mich das als Korrosionsschutzunternehmen eigentlich an? Vermehrte
DIN EN 1090 Aktuelle Anforderungen an den Korrosionsschutz kennen RA Lars Walther Geschäftsführer QIB e.v. Einführung EN 1090 und was geht mich das als Korrosionsschutzunternehmen eigentlich an? Vermehrte
das usa team Ziegenberger Weg 9 61239 Ober-Mörlen Tel. 06002 1559 Fax: 06002 460 mail: lohoff@dasusateam.de web: www.dasusateam.de
 Kommunikation mit Kunden das usa team Ziegenberger Weg 9 61239 Ober-Mörlen Tel. 06002 1559 Fax: 06002 460 mail: lohoff@dasusateam.de web: www.dasusateam.de 1 Wie Sie überzeugend argumentieren Viele Verkäufer
Kommunikation mit Kunden das usa team Ziegenberger Weg 9 61239 Ober-Mörlen Tel. 06002 1559 Fax: 06002 460 mail: lohoff@dasusateam.de web: www.dasusateam.de 1 Wie Sie überzeugend argumentieren Viele Verkäufer
Termin-Umfragen mit Doodle
 Termin-Umfragen mit Doodle Mit Doodle können Sie schnell und einfach Umfragen erstellen, um gemeinsam mit Ihren Kollegen oder Geschäftspartnern einen Termin für eine Konferenz, Sitzung oder sonstige Veranstaltungen
Termin-Umfragen mit Doodle Mit Doodle können Sie schnell und einfach Umfragen erstellen, um gemeinsam mit Ihren Kollegen oder Geschäftspartnern einen Termin für eine Konferenz, Sitzung oder sonstige Veranstaltungen
Informationen zur Erstellung des Projektantrags in den IT-Berufen und zum AbschlussPrüfungOnlineSystem (CIC-APrOS)
 Informationen zur Erstellung des Projektantrags in den IT-Berufen und zum AbschlussPrüfungOnlineSystem (CIC-APrOS) Allgemeine Hinweise zum Projektantrag Den Prüferinnen und Prüfern der Industrie- und Handelskammer
Informationen zur Erstellung des Projektantrags in den IT-Berufen und zum AbschlussPrüfungOnlineSystem (CIC-APrOS) Allgemeine Hinweise zum Projektantrag Den Prüferinnen und Prüfern der Industrie- und Handelskammer
Ohne Fehler geht es nicht Doch wie viele Fehler sind erlaubt?
 Ohne Fehler geht es nicht Doch wie viele Fehler sind erlaubt? Behandelte Fragestellungen Was besagt eine Fehlerquote? Welche Bezugsgröße ist geeignet? Welche Fehlerquote ist gerade noch zulässig? Wie stellt
Ohne Fehler geht es nicht Doch wie viele Fehler sind erlaubt? Behandelte Fragestellungen Was besagt eine Fehlerquote? Welche Bezugsgröße ist geeignet? Welche Fehlerquote ist gerade noch zulässig? Wie stellt
Muster Nachweisdokumentation und Sicherheitsbewertungsbericht
 Muster Nachweisdokumentation und Sicherheitsbewertungsbericht auf Basis der "Verordnung (EG) Nr. 352/2009 der Kommission vom 24. April 2009 über die Festlegung einer gemeinsamen Sicherheitsmethode für
Muster Nachweisdokumentation und Sicherheitsbewertungsbericht auf Basis der "Verordnung (EG) Nr. 352/2009 der Kommission vom 24. April 2009 über die Festlegung einer gemeinsamen Sicherheitsmethode für
D.3.3. Betriebsleitfaden zur Zuweisung/Vergabe von ECVET Krediten. EUCoopC. PROJEKT Nr.: 527301-LLP-1-2012-1-IT-LEONARDO-LMP
 EUCoopC PROJEKT Nr.: 527301-LLP-1-2012-1-IT-LEONARDO-LMP MULTILATERALE PROJEKTE ZUR INNOVATIONSENTWICKLUNG D.3.3. Betriebsleitfaden zur Zuweisung/Vergabe von ECVET Krediten Arbeitspaket 3 Entwurfsverfahren
EUCoopC PROJEKT Nr.: 527301-LLP-1-2012-1-IT-LEONARDO-LMP MULTILATERALE PROJEKTE ZUR INNOVATIONSENTWICKLUNG D.3.3. Betriebsleitfaden zur Zuweisung/Vergabe von ECVET Krediten Arbeitspaket 3 Entwurfsverfahren
Abschnitt 1 Anwendungsbereich und Allgemeine Anforderungen an die Konformitätsbewertung 1 Anwendungsbereich
 13.06.2007 Verordnung über Medizinprodukte - (Medizinprodukte-Verordnung - MPV)* vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 16. Februar 2007 (BGBl. I S.
13.06.2007 Verordnung über Medizinprodukte - (Medizinprodukte-Verordnung - MPV)* vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 16. Februar 2007 (BGBl. I S.
Überprüfung der digital signierten E-Rechnung
 Überprüfung der digital signierten E-Rechnung Aufgrund des BMF-Erlasses vom Juli 2005 (BMF-010219/0183-IV/9/2005) gelten ab 01.01.2006 nur noch jene elektronischen Rechnungen als vorsteuerabzugspflichtig,
Überprüfung der digital signierten E-Rechnung Aufgrund des BMF-Erlasses vom Juli 2005 (BMF-010219/0183-IV/9/2005) gelten ab 01.01.2006 nur noch jene elektronischen Rechnungen als vorsteuerabzugspflichtig,
Würfelt man dabei je genau 10 - mal eine 1, 2, 3, 4, 5 und 6, so beträgt die Anzahl. der verschiedenen Reihenfolgen, in denen man dies tun kann, 60!.
 040304 Übung 9a Analysis, Abschnitt 4, Folie 8 Die Wahrscheinlichkeit, dass bei n - maliger Durchführung eines Zufallexperiments ein Ereignis A ( mit Wahrscheinlichkeit p p ( A ) ) für eine beliebige Anzahl
040304 Übung 9a Analysis, Abschnitt 4, Folie 8 Die Wahrscheinlichkeit, dass bei n - maliger Durchführung eines Zufallexperiments ein Ereignis A ( mit Wahrscheinlichkeit p p ( A ) ) für eine beliebige Anzahl
DAUERHAFTE ÄNDERUNG VON SCHRIFTART, SCHRIFTGRÖßE
 DAUERHAFTE ÄNDERUNG VON SCHRIFTART, SCHRIFTGRÖßE UND ZEILENABSTAND Word 2010 und 2007 Jedes neue leere Dokument, das mit Word 2010 erstellt wird, basiert auf einer Dokumentvorlage mit dem Namen Normal.dotx.
DAUERHAFTE ÄNDERUNG VON SCHRIFTART, SCHRIFTGRÖßE UND ZEILENABSTAND Word 2010 und 2007 Jedes neue leere Dokument, das mit Word 2010 erstellt wird, basiert auf einer Dokumentvorlage mit dem Namen Normal.dotx.
Anleitung über den Umgang mit Schildern
 Anleitung über den Umgang mit Schildern -Vorwort -Wo bekommt man Schilder? -Wo und wie speichert man die Schilder? -Wie füge ich die Schilder in meinen Track ein? -Welche Bauteile kann man noch für Schilder
Anleitung über den Umgang mit Schildern -Vorwort -Wo bekommt man Schilder? -Wo und wie speichert man die Schilder? -Wie füge ich die Schilder in meinen Track ein? -Welche Bauteile kann man noch für Schilder
INTERNET SERVICES ONLINE
 VERTRAG ZUR UNTERSTÜTZUNG BEI DER ERSTELLUNG EINES PFLICHTENHEFTES f INTERNET SERVICES ONLINE VERTRAG ZUR UNTERSTÜTZUNG BEI DER ERSTELLUNG EINES PFLICHTENHEFTES... nachfolgend Kunde genannt und Internet
VERTRAG ZUR UNTERSTÜTZUNG BEI DER ERSTELLUNG EINES PFLICHTENHEFTES f INTERNET SERVICES ONLINE VERTRAG ZUR UNTERSTÜTZUNG BEI DER ERSTELLUNG EINES PFLICHTENHEFTES... nachfolgend Kunde genannt und Internet
Pensionskasse der Burkhalter Gruppe Zürich. Bericht der Revisionsstelle an den Stiftungsrat zur Jahresrechnung 2013
 Pensionskasse der Burkhalter Gruppe Zürich Bericht der Revisionsstelle an den Stiftungsrat zur Jahresrechnung 2013 Bericht der Revisionsstelle an den Stiftungsrat der Pensionskasse der Burkhalter Gruppe
Pensionskasse der Burkhalter Gruppe Zürich Bericht der Revisionsstelle an den Stiftungsrat zur Jahresrechnung 2013 Bericht der Revisionsstelle an den Stiftungsrat der Pensionskasse der Burkhalter Gruppe
