Kurstag 8. Synthese eines Arzneimittels Acetylsalicylsäure (ASS, Aspirin )
|
|
|
- Maximilian Fischer
- vor 7 Jahren
- Abrufe
Transkript
1 Kurstag 8 Synthese eines Arzneimittels Acetylsalicylsäure (ASS, Aspirin ) Stichworte zur Vorbereitung Partialladung, Mesomerie, Grundlagen der Nomenklatur organischer Verbindungen, funktionelle Gruppen, Phenole, Ester (Synthese und ydrolyse), Aufbau von Lipiden, Aspirin Ziel des Versuchstags Einführung in die Grundlagen der organischen Chemie, insbesondere die Eigenschaften und eaktionen der Carbonsäureester.
2 Theorie Bisher haben wir uns in der anorganischen Chemie damit beschäftigt, wie Ionen also Teilchen mit realer Ladung miteinander reagieren. Diese Ionenreaktionen laufen sehr rasch mit hoher Geschwindigkeit ab, der Gleichgewichtszustand stellt sich praktisch momentan ein. Anders liegen die Verhältnisse bei organischen eaktionen. Auch in der organischen Chemie laufen die meisten eaktionen über Ionen. Diese Ionen sind aber in den reagierenden Molekülen nicht vorgebildet, sondern entstehen erst während der eaktion unter dem Einfluss eines geeigneten eaktionspartners. Diese Bildung von Ionen verläuft in der egel relativ langsam. Daher verlaufen organische eaktionen oft langsam und setzen sich häufig aus mehreren Teilreaktionen zusammen. Verbindungen, die organische eaktionen eingehen, bestehen im einfachsten Fall aus kovalent verbundenen - und C-Atomen, zwischen denen die Bindungselektronen auf Grund ähnlicher Elektronegativität gleichmäßig verteilt sind. Ist ein C-Atom jedoch mit einem anderem Element wie N,, verbunden, so zieht dieses Atom die Bindungselektronen näher zu seinem Kern oder schiebt diese zum Kern des C-Atoms je nach Elektronegativitätsverhältnis. Die Ungleichverteilung von Elektronen führt zur Ausbildung von Partialladungen. Diese Partialladungen sind für das Zustandekommen von organischen eaktionen verantwortlich. Ganz allgemein verlaufen organische eaktionen an einem durch entsprechende benachbarte Gruppen aktivierten C-Atom: δ+ δ- δ- δ+ Abb.: Partialladungen Zieht der Substituent X Elektronen vom C-Atom ab, erhält das C-Atom eine partiell positive Ladung und wird dadurch zugänglich für eine eaktion mit einem elektronenreichen Teilchen, z. B. einem Anion ( - ). Das angreifende elektronenreiche Teilchen bezeichnet man als Nucleophil (kernliebendes Teilchen), die eaktion als nucleophilen Angriff. Solche eaktionen sind relativ häufig. Schiebt der Substituent X Elektronen zum C-Atom hin, erhält das C-Atom eine partiell negative Ladung und wird dadurch zugänglich für eine eaktion mit einem elektronenarmen Teilchen z.b. einem Kation (Br+). Das elektronenarme Teilchen 1
3 bezeichnet man als Elektrophil (elektronenliebendes Teilchen), die eaktion als einen elektrophilen Angriff. Funktionelle Gruppen Die Chemie organischer Verbindungen wird maßgeblich durch funktionelle Gruppen bestimmt. Je nach atomarer Zusammensetzung und Struktur der funktionellen Gruppe unterscheiden sich die Art und Lage der resultierenden Partialladungen und damit das eaktionsverhalten der Verbindung. Da die funktionellen Gruppen einen sehr großen Einfluss auf das eaktionsverhalten organischer Verbindungen haben, werden sie zur Klassifizierung der Verbindungen herangezogen. Beispiele einiger einfacher funktioneller Gruppen: Verbindungsklasse Funktionelle Gruppe Struktur Alkohol ydroxygruppe Ether Ethergruppe ' Aldehyd Carbonylgruppe Keton Carbonylgruppe ' Carbonsäure Carboxylgruppe Carbonsäureanhydrid ' Carbonsäurehalogenid Cl 2
4 Carbonsäureester ' Carbonsäureamid Säureamidgruppe N 2 Amin Aminogruppe N 2 Thiol Thiolgruppe S Funktionelle Gruppen sind keine unveränderlichen Charakteristika von organischen Verbindungen, sondern können durch bestimmte eaktionen in andere umgewandelt werden. Ein klassisches Beispiel für eine eihe von Umwandlungen ist die xidation von Alkoholen: zunehmende xidation primärer Alkohol sekundärer Alkohol tertiärer Alkohol Aldehyd Keton keine weitere Carbonsäure keine weitere xidation möglich xidation möglich Die Chemie der funktionellen Gruppen hängt also auch von der Struktur des restlichen Molekülkörpers ab! Primär, sekundär bzw. tertiär beschreibt im Fall der Alkohole, wie viele weitere C- Atome mit dem C-Atom, das die funktionelle Gruppe trägt, verbunden sind. Wie man sieht kann nur ein weiteres C-Atom ( primärer Alkohol) oder mehrere C-Atome ( sekundär, tertiär) an das C-Atom mit der funktionellen Gruppe gebunden sein. Carbonsäuren Zum Verständnis dieses Versuchstages spielen die Carbonsäuren als Ausgangsverbindungen der Estersynthese eine besondere olle. Generell haben Carbonsäuren folgende eaktionsmöglichkeiten mit anderen funktionellen Gruppen: 3
5 Achtung: Diese Abbildung ist nicht vollständig! Es sind weitere eaktionswege möglich, zudem treten immer Nebenprodukte auf. Allgemein werden zur Estersynthese Carbonsäuren und Alkohole benötigt. Je nach eingesetzter Carbonsäure und eingesetztem Alkohol erhält man Produkte mit unterschiedlichen Eigenschaften, z.b. Geruch. saure Estersynthese Die eaktionsgleichung der Estersynthese sollte also folgendermaßen aussehen: Gibt man jedoch im Versuch eine Carbonsäure und einen Alkohol zusammen, so entsteht nur sehr langsam Produkt, d.h. die Gleichgewichtseinstellung zwischen Edukten und Produkten dauert lange. Gibt man jedoch eine katalytische Menge mineralische Säure wie Salz- oder Schwefelsäure hinzu, so erhält man schneller messbare Mengen an Produkt. Diese Beobachtung lässt sich durch den genauen eaktionsmechanismus erklären: 1. Schritt: Das C-Atom in einer Carboxylgruppe ist auf Grund des doppelt gebundenen - Atoms und der ydroxygruppe schon stark positiv polarisiert, d.h. es trägt eine große positive Partialladung und ist ein Elektrophil. Dennoch läuft die eaktion nur sehr langsam ab. Durch Protonierung der Carboxylgruppe wird eine reale positive Ladung erzeugt. Diese kann entweder am - oder C-Atom lokalisiert sein und führt zu einer 4
6 drastischen Erhöhung der Elektrophilie des C-Atoms und daraus resultierenden Erhöhung der Geschwindigkeit der Gleichgewichtseinstellung. Dieser Schritt ist der entscheidende zur Erhöhung der Geschwindigkeit! 2. Schritt: Die reale positive Ladung am C-Atom führt dazu, dass es sehr leicht von einem Nucleophil in diesem Fall dem -Atom des Alkohols angegriffen werden kann. Das tetraedrische Zwischenprodukt ist nicht stabil. 3. Schritt: Es kommt zu einer intramolekularen Protonenumlagerung. Dabei wird eine ydroxylgruppe protoniert, was die Abspaltung von Wasser und Stabilisierung des Produkts erleichtert. 4. Schritt: Abspaltung von Wasser: Dehydratisierung. 5.Schritt: Deprotonierung d.h. Freisetzung des Katalysators + und Entstehung des Esters. 5
7 Wie durch die Gleichgewichtspfeile schon angedeutet, ist jede Einzelreaktion reversibel. D.h. eine Esterverbindung lässt sich in wässriger Lösung durch Zugabe von +, also Säuren, wieder in Carbonsäure und Alkohol spalten. Diesen Vorgang bezeichnet man als saure ydrolyse, da wieder ein Proton zur eaktivitätssteigerung führt und ein Wassermolekül als Nucleophil das positiv geladene C-Atom angreift. An dieser eaktion zeigt sich beispielhaft, dass man organische eaktionen anders als anorganische in mehrere Einzelschritte zerlegen kann, um den eaktionsmechanismus zu verdeutlichen. Die dabei auftretenden Zwischenprodukte ( Intermediate ) können häufig anders als bei anorganischen eaktionen, bei denen die Zwischenprodukte zu instabil und damit kurzlebig, isoliert und untersucht werden, um so den eaktionsmechanismus aufzuklären. alkalische Esterhydrolyse (basische Verseifung) Ester lassen sich nicht nur im Sauren hydrolysieren. Gibt man zu einer wässrigen Esterlösung eine Base hinzu, so wird der Ester wie auch im Sauren in eine Carbonsäure und einen Alkohol gespalten. Auch diese eaktion lässt sich in Einzelschritte aufteilen: 1. Schritt: Das Carbonyl-C-Atom des Esters trägt wegen der beiden daran gebundenen - Atome eine starke positive Partialladung. Das Nucleophil ist in dieser eaktion ein negativ geladenes ydroxid-ion, das das Carbonyl-C-Atom mit einem freien Elektronenpaar direkt angreift. Man beachte den Unterschied zur sauren ydrolyse (Schritt 4 von rechts nach links gelesen)! In dieser eaktion trägt das Nucleophil 2 keine Ladung und kann deshalb das Carbonyl-C-Atom des Esters in neutraler Lösung nicht ohne weiteres angreifen. Damit die eaktion dennoch ablaufen kann, wird Säure zugegeben, sodass am Carbonyl-C-Atom durch Protonierung des doppelt gebundenen -Atoms eine positive Ladung entsteht. 6
8 2. Schritt: Das entstandene tetraedrische, negativ geladene Zwischenprodukt ist äußerst instabil, da die negative Ladung nicht durch Mesomerie stabilisiert werden kann. Es zerfällt in die freie Carbonsäure und das Alkoholat-Ion. 3. Schritt: Da das Alkoholat-Ion eine sehr viel stärkere Base als das Carboxylat-Ion (deprotonierte Säure) ist, findet ein Protonentransfer von der Säure zum Alkoholat- Ion statt. Die negative Ladung des Carboxylat-Ions ist im Gegensatz zum tetraedrischen Zwischenprodukt mesomeriestabilisiert: Das entstandene Carboxylat-Ion kann auf Grund der über die gesamte funktionelle Gruppe verteilten negativen Ladung (siehe Mesomeriestrukturen) nicht mehr von einem Nucleophil angegriffen werden. Dieser eaktionsschritt macht die gesamte eaktion irreversibel. Ein weiterer Unterschied zur sauren ydrolyse besteht darin, dass die ydroxid- Ionen im Gegensatz zu den Protonen verbraucht werden, d.h. sie sind keine Katalysatorteilchen. 7
9 Synthese von Acetylsalicylsäure Salicylsäure reagiert mit Essigsäureanhydrid in einer säurekatalysierten eaktion zu Acetylsalicylsäure nach folgender Gleichung: Die eaktion läuft analog zur oben beschriebenen sauren Estersynthese ab, mit dem Unterschied, dass statt eines Moleküls Wasser ein Molekül Essigsäure entsteht. Essigsäureanhydrid ist ein sehr gutes Acetylierungsmittel und überträgt den C 3 C- est auf -Gruppen oder auch auf N 2 -Gruppen. Als Essigsäureester ist Acetylsalicylsäure natürlich sowohl gegen Lauge als auch gegen wässrige Säure empfindlich (Esterhydrolyse). Die (saure) ydrolyse an der Luft kann u.u. durch Essigsäuregeruch nachgewiesen werden. Andererseits kann Acetylsalicylsäure noch mit Alkoholen zum Ester umgesetzt werden. Beispielsweise entsteht aus der Umsetzung mit Ethanol der Ethylester (sog. Wintergrünöl, enthalten in der amerikanischen Teebeere, ebenfalls fiebersenkend). eaktion von Salicylsäure mit Fe 3+ -Ionen Alkohole mit der Gruppierung -C=C reagieren mit Fe³+ zu einer blauvioletten Verbindung. Fe³ + ist also auch ein empfindlicher Nachweis für Phenole. Salicylsäure (nicht die acetylierte Form, warum?) reagiert mit Fe 3+ in einer Komplexbildungsreaktion zwischen Fe 3+ und dem Salicylsäure-Anion, wobei die Fe 3+ -Ionen über die Koordinationszahl 6 mit drei Salicylsäure-Anionen als zweizähnige Liganden rot-violette Chelatkomlexe ausbilden. Fe Salicylat-Anionen Tris-salicylat-eisen(III)-Komplex gelb blauviolett Der Komplex ist ein oktaedrisch aufgebauter Chelatkomplex, der in neutraler, wässriger Lösung außerordentlich stabil ist, in stark saurer Lösung und alkalischer Lösung zerfällt. 8
10 Vorfragen 1. Woher kommt der Ausdruck basische Verseifung? 2. Sie haben einen Ester alkalisch hydrolysiert. Können Sie den Ester durch Ansäuern der Lösung wieder synthetisieren? 3. Wie wirkt Aspirin? (freiwillig, Biochemiestoff!) 4. Erklären Sie mit eigenen Worten den Unterschied zwischen Partialladung und Ionenladung. 5. Ermitteln Sie die Eigenschaften der verwendeten Chemikalien (Strukturformeln, Schmelzpunkt, Löslichkeit etc.). 6. Schreiben Sie die einfachen Monocarbonsäuren von C1 bis C4 auf. 7. Was versteht man unter einem Carbonsäureamid? Schreiben Sie folgende Amide: a) Essigsäureamid b) Benzoesäureamid 8. Versuchen Sie, möglichst alle Alkohole von C1 bis C4 zu formulieren. Benennen Sie diese Alkohole und geben Sie an, ob es sich um einen primären, sekundären oder tertiären Alkohol handelt. 9. Was versteht man unter einem Triglycerid? Um was handelt es sich bei diesen Verbindungen chemisch betrachtet? Zeichnen Sie die Alkoholkomponente eines Triglycerids. Finden Sie heraus, ob es sich um einen primären, sekundären oder tertiären Alkohol handelt. Übungsaufgaben 1. Woher kommt der Ausdruck basische Verseifung? 2. Formulieren Sie die eaktion der Acetyl-Salicylsäure-Synthese. 3. Wie reagiert ASS mit Ethanol? 4. Formulieren Sie die eaktion von Acetanhydrid (Essigsäureanhydrid) mit Ammoniak. Welche Verbindung entsteht dabei? 5. Paracetamol ist ebenfalls ein sehr häufig verwendetes fiebersenkendes und schmerzstillendes Arzneimittel. Es enthält ebenfalls eine Acetylgruppe (Name!). Geben Sie die Strukturformel an. Welche Gruppe ist hier acetyliert? Wie nennt man die so entstandende chemische Bindung? 9
11 Neue Geräte und Arbeitsweisen Schmelzpunktbestimmung Die fein pulverisierte, gut getrocknete Substanz wird in einer 2 bis 4 mm hohen Schicht in ein etwa 1 mm weites, einseitig zugeschmolzenes Kapillarröhrchen gebracht. Dazu taucht man die Kapillare in die Substanzprobe und klopft das Pulver vorsichtig auf den Kapillarboden. Das Schmelzpunktsröhrchen wird nun mit der zugeschmolzenen Seite nach unten in den Schmelzpunktbestimmungsapparat gestellt und der eizblock langsam aufgeheizt. Da jedes Thermometer eine gewisse Anzeigeverzögerung aufweist, wird der eizblock nur so schnell erhitzt, dass in der Nähe des Schmelzpunktes der Temperaturbereich etwa 1-2 C/min beträgt. Vorher, d.h. bis etwa 10 C unterhalb des Schmelzpunktes kan n selbstverständlich schneller erhitzt werden. Ist der Schmelzpunkt einer unbekannten Substanz zu ermitteln, ist es zweckmäßig, zwei Kapillaren zu füllen und den Schmelzpunkt zunächst mit einer Probe grob zu bestimmen, dann das Bad etwas abkühlen lassen, um anschließend eine exakte Schmelzpunktsbestimmung mit der zweiten Probe durchzuführen. Kurz vor Erreichen des Schmelzpunktes stellt man ein plötzliches Erweichen der Kristalle fest, wobei die Kristalle häufig zusammenfallen. Kurz darauf erfolgt völliges Aufschmelzen zu einer klaren Flüssigkeit. Voraussetzung dafür ist, dass sich die Substanz nicht vor Erreichen des Schmelzpunktes oder beim Schmelzen zersetzt. 10
12 Durchführung Versuch 1: Vorversuche zur Esterverseifung 1ml livenöl (ca. 1cm Füllhöhe im eagenzglas werden mit 2ml Ethanol gelöst, mit 2 Stückchen K und 1-2 Siedesteine versetzt und vorsichtig zum schwachen Sieden erhitzt. Vorsicht Siedverzug möglich. Die Lösung wird heiß auf zwei eagenzgläser verteilt. Nach Abkühlen scheiden sich die Kaliumsalze der ab. Zum zweiten eagenzglas wird dasselbe Volumen an Wasser gegeben und danach mit verd. Schwefelsäure angesäuert. Beobachtung? Fragen: a) Woraus besteht der Niederschlag im zweiten eagenzglas? b) Was ist eine Seife? c) Warum wird die basische Esterhydrolyse auch als Verseifung bezeichnet? d) Wie könnte man das Vorhandensein einer ungesättigten Fettsäure nachweisen? e) Welche Fettsäure überwiegt mengenmäßig in natürlichen Fetten. 11
13 Versuch 2: Vorversuche zur Versterung /Verseifung Man vermischt in einem eagenzglas ca. 1 ml Ethanol und 2 Tropfen wasserfreier Essigsäure (Eisessig) und fügt dann vorsichtig 1 Tropfen Schwefelsäure (Vorsicht stark ätzend!!) zu und kocht kurz vorsichtig aus. Geruch? Versuch 3: Vorversuche zur Versterung a) Mischen Sie ca. 1ml Isobutanol (Formel?) mit der gleichen Menge konz. Essigsäure und erwärmen die Mischung vorsichtig. Prüfen Sie vorsichtig dengeruch. b) Kühlen Sie nun die Lösung durch Eintauchen in Eiswasser ab und geben 1-2 Tropfen konz. Schwefelsäure dazu und erwärmen wieder. Geruch? Worin besteht der Unterschied zu Versuch 3a? Welchen Mechanismus nimmt man für diese Veresterung an. Welche Funktion hat die Schwefelsäure? Wie könnte man die Ausbeute an Ester erhöhen? (MWG!) Versuch 4: Vorversuche Versterung 1 ml Isoamylalkohol und 1 ml konz. Essigsäure werden mit 2 Tropfen konz. Schwefelsäure vorsichtig erwärmt. Geruchsprobe. An was erinnert Sie der Geruch? Versuch 5: Synthese von Acetylsalicylsäure (Aspirin, ASS) Chemikalien: Salicylsäure, Essigsäureanhydrid (Acetanhydrid), Phosphorsäure (85%) ACTUNG!!!, Ethanol (vergällt) zum Umkristallisieren. 1g Salicylsäure wird in ein eagenzglas eingewogen und vorsichtig mit 2,5ml Essigsäureanhydrid versetzt. Leicht umschütteln. Danach gibt man ca. 4 Tropfen (ca. 120µl) Phosphorsäure dazu und erhitzt auf einem Wasserbad (250ml Becherglas ca. 1/3 füllen) bis auf 75 C. Immer wieder vorsichtig umschütteln bis sich alles klar gelöst hat. Man hält nun die Temperatur für ca. 15 min bei C. 12
14 Man nimmt nun das eagenzglas heraus, lässt leicht abkühlen und gibt in die noch warme Lösung ca. 1ml Wasser (warum?). Achtung äußerste Vorsicht, Spritzgefahr, eagenzglas vom Gesicht und Nachbarn weg halten!!! Bei vorsichtigem iechen kann man Essigsäuregeruch wahrnehmen. Nach weiteren 5 min gibt man 10ml Wasser dazu, schüttelt gut durch und stellt das eagenzglas in Eiswasser. Nach ca. 5 min beginnt die Acetylsalicylsäure auszufallen. Nun wird mit einer Nutsche abfiltriert und mit Eiswasser gut nachgewaschen (warum?). Das Produkt riecht immer noch stark nach Essigsäure und muss daher nochmals umkristallisiert werden. Das eaktionsprodukt wird wiederum in das eagenzglas überführt (vorher einen kleinen Teil davon für die Dünnschichtchromatographie bzw. als Impfkristall abnehmen) und mit 1,0 ml Ethanol und 6 ml Wasser versetzt und wiederum durch Erhitzen auf ca. 60 C weitestgehend gelöst. (Wesha lb nicht zu lange und zu hoch erhitzen?) Nun kann man abkühlen lassen. a) durch Abkühlen am Wasserhahn b) Stehen lassen bei aumtemperatur c) Stehen lassen auf Eis. Langsames Abkühlen gibt sehr schöne, lange Kristallnadeln. Sie können an einem Mikroskop genauer betrachtet werden (steht am Tisch 16, Mikroskop sauber halten!). Auch hier gilt: Geduld bringt oft die besten Ergebnisse. Die Kristalle werden nun wieder abgesaugt und zwischen 2 Papierfiltern getrocknet. Anschließend wird der Schmelzpunkt bestimmt. einheitskontrolle A) Mit ilfe der Dünnschichtchromatographie Zur einheitskontrolle wird eine Dünnschichtchromatographie auf einer Kieselgelfolie (mit Fluoreszenzindikator) durchgeführt. Weiterhin werden zwei weitere Analgetika: Ibuprofen und Paracetamol aufgetragen Dafür wird je eine kleine Menge Salicylsäure, oh-acetylsalicylsäure und die gereinigte Acetylsalicylsäure sowie Ibiprofen und Paracetamol in Ethanol/Wasser 13
15 gelöst und mittels Kapillare aufgetragen und im Laufmittel entwickelt. Nach dem Trocknen wird die DC-Platte mit UV-Licht bei 254 nm bestrahlt (Assistent, nicht direkt in die Lampe sehen!) und die nun sichtbaren Flecken mit einem Bleistift vorsichtig markiert. Enthält die Acetylsalicylsäure noch freie Salicylsäure? Formeln von Ibuprofen und Paracetamol? Können Sie die Grundkörper angeben? ptional: Schließlich wird die Folie mit einem Sprühreagenz (1% FeCl3) besprüht. Was können Sie damit nachweisen? B) eaktion mit Eisen(III)Chlorid War die Synthese nicht vollständig, ist noch freie Salicylsäure vorhanden. Diese bildet mit Fe3+-Ionen einen dunkelblauen Komplex. Das Synthesepodukt Acetylsalicylsäure bildet hingegen keinen blauen Komplex mit den Eisenionen aus. Daher kann die Menge an nicht reagiertem Ausgangsprodukt anhand der Blaufärbung bestimmt werden. Folgende Lösungen/Chemikalien stehen aus: 0.1% (w/v) Salicylsäure 0.1% (w/v) Acetylsalicylsäure 1% (w/v) FeCl 3 -Lösung (Eisen(III)chloridlösung) 50 % (v/v) Ethanol) ASS-Tablette der Fa. atiopharm (muss im Mörser zuvor zerrieben werden) Folgende Ansätze werden in einem eagenzglas hergestellt. Sie dienen als Positiv- bzw. als Negativkontrolle sowie zur Abschätzung der Verunreinigung der Probe mit Salicylsäure. Nr µl 0.1% Salicylsäurelösung 3 Tropfen FeCl 3 Nr µl 0.1% ASS-Lösung 3 Tropfen FeCl 3 14
16 Nr.3 Spatelspitze Tablette in 1000 µl Ethanol/Wasser (1:1) Nr.4 Spatelspitze eigenes Produkt in 1000 µl Ethanol/Wasser (1:1) Nr.5 Wie Nr.4, Lsg. aber vorher ca. 5min im Wasserbad auf 70 o C erhitzen 3 Tropfen FeCl 3 3 Tropfen FeCl 3 3 Tropfen FeCl 3 Der Versuch Nr.5 soll zeigen, dass Arzneimittel eine begrenzte Stabilität ( altbarkeit ) aufweisen und oft temperaturempfindlich sind. Weshalb kann man bei sehr alten, schlecht gelagerten ASS-Tabletten einen schwachen Essigsäuregeruch wahrnehmen? Auf der Fensterbank stehen bereits 4 Lösungen zum Abschätzen Ihrer Verunreinigungen (müssen nicht selbst hergestellt werden) 1% 1000 µl 0.1% ASS-Lösung + 1% Verunreinigung an Salicylsäure 2.5% 1000 µl 0.1% ASS-Lösung + 2.5% Verunreinigung an Salicylsäure 5% 1000 µl 0.1% ASS-Lösung + 5% Verunreinigung an Salicylsäure 10% 1000 µl 0.1% ASS-Lösung + 10% Verunreinigung an Salicylsäure 3 Tropfen FeCl 3 3 Tropfen FeCl 3 3 Tropfen FeCl 3 3 Tropfen FeCl 3 Ergebnis: Die von mir hergestellte Acetylsalicylsäure hat eine Verunreinigung von ca..%. Evt. gibt es einen kleinen Wettbewerb. Je 2 Proben eines Tisches werden in unserem Labor mittels einer modernen Trenntechnik (PLC, high performance liquid chromatography) untersucht. ier kann die einheit ganz genau bestimmt werden. Die Ergebnisse werden am nächsten Donnerstag gezeigt. 15
17 16
Kurstag 8. Estersynthese
 Kurstag 8 Estersynthese Stichworte zur Vorbereitung: Partialladung, Mesomerie, Grundlagen der Nomenklatur organischer Verbindungen, funktionelle Gruppen, Phenole, Ester (Synthese und ydrolyse), Aufbau
Kurstag 8 Estersynthese Stichworte zur Vorbereitung: Partialladung, Mesomerie, Grundlagen der Nomenklatur organischer Verbindungen, funktionelle Gruppen, Phenole, Ester (Synthese und ydrolyse), Aufbau
Kurstag 8. Synthese eines Arzneimittels Acetylsalicylsäure (ASS, Aspirin )
 Kurstag 8 Synthese eines Arzneimittels Acetylsalicylsäure (ASS, Aspirin ) Stichworte zur Vorbereitung Partialladung, Mesomerie, Grundlagen der Nomenklatur organischer Verbindungen, funktionelle Gruppen,
Kurstag 8 Synthese eines Arzneimittels Acetylsalicylsäure (ASS, Aspirin ) Stichworte zur Vorbereitung Partialladung, Mesomerie, Grundlagen der Nomenklatur organischer Verbindungen, funktionelle Gruppen,
Organische Chemie für Mediziner WS 2016/2017. Übungsblatt 3: Ausgewählte Substanzklassen
 1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Reak%onen an der Carbonylgruppe
 Reak%onen an der Carbonylgruppe H. Wünsch 2013 1.1 Struktur der Carbonylgruppe Die Carbonylgruppe entsteht bei der OxidaBon primärer und sekundärer Alkohole. Kohlenstoff und Sauerstoff sind doppelt gebunden,
Reak%onen an der Carbonylgruppe H. Wünsch 2013 1.1 Struktur der Carbonylgruppe Die Carbonylgruppe entsteht bei der OxidaBon primärer und sekundärer Alkohole. Kohlenstoff und Sauerstoff sind doppelt gebunden,
8 Carbonsäuren und Derivate
 8 arbonsäuren und Derivate 8.1 Allgemeine Darstellungsverfahren xidation primärer Alkohole und Aldehyde (s. Kap. 6) 2 2 xidation durch r 3 /, KMn 4 /, N 3 aloform-eaktion (s. Kap. 9) 3 Br 2 xidation von
8 arbonsäuren und Derivate 8.1 Allgemeine Darstellungsverfahren xidation primärer Alkohole und Aldehyde (s. Kap. 6) 2 2 xidation durch r 3 /, KMn 4 /, N 3 aloform-eaktion (s. Kap. 9) 3 Br 2 xidation von
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) OH H + - H 2 O. (aus H 3 PO 4 H 2 SO 4 ) - H + Stichpunkte zum E1-Mechanismus:
 Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Claisen-Kondensation
 Quelle: gerlicher.de In dieser Datei soll der Mechanismus der Biosynthese wichtiger Bausteine von Ölen und festen Fetten näher betrachtet werden, nämlich die Biosynthese der Fettsäuren. Quelle: gerlicher.de
Quelle: gerlicher.de In dieser Datei soll der Mechanismus der Biosynthese wichtiger Bausteine von Ölen und festen Fetten näher betrachtet werden, nämlich die Biosynthese der Fettsäuren. Quelle: gerlicher.de
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid
 NP 5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Klassifizierung
NP 5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Klassifizierung
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
Chemie für Biologen, Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema ) iii) Carbonsäure iv) Dicarbonsäure
 Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Definiere den Begriff Orbital. Erkläre den ph-wert! Erkläre die Autoprotolyse des Wassers mit Hilfe der Reaktionsgleichung.
 Definiere den Begriff rbital. Das rbital ist ein Bereich, in dem sich ein Elektron mit großer Wahrscheinlichkeit befindet. In jedem rbital befinden sich maximal zwei Elektronen. Erkläre den pwert! Der
Definiere den Begriff rbital. Das rbital ist ein Bereich, in dem sich ein Elektron mit großer Wahrscheinlichkeit befindet. In jedem rbital befinden sich maximal zwei Elektronen. Erkläre den pwert! Der
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Orbital. Atombindung, Bindung. Elektronegativität. Dipol
 GW Chemie 10. SG GA rbital aum, in dem sich Elektronen mit 99%iger Wahrscheinlichkeit aufhalten; in einem rbital halten sich maximal 2 Elektronen auf; man unterscheidet Atom- und Molekülorbitale Atombindung,
GW Chemie 10. SG GA rbital aum, in dem sich Elektronen mit 99%iger Wahrscheinlichkeit aufhalten; in einem rbital halten sich maximal 2 Elektronen auf; man unterscheidet Atom- und Molekülorbitale Atombindung,
im Molekül eine Dreifachbindung (eine σ-bindung,
 1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1. Bei den folgenden Stoffumwandlungen handelt es sich um typische Reaktionen der organischen Chemie.
 rganische hemie E 102 Aufgaben 7 1. Bei den folgenden Stoffumwandlungen handelt es sich um typische Reaktionen der organischen hemie. 2 /Na Na + Et Et / KN N 2 Um welche Reaktionen handelt es sich? 1.
rganische hemie E 102 Aufgaben 7 1. Bei den folgenden Stoffumwandlungen handelt es sich um typische Reaktionen der organischen hemie. 2 /Na Na + Et Et / KN N 2 Um welche Reaktionen handelt es sich? 1.
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 13.02.2017 Die Klausur besteht aus 10 Seiten. Bitte zu den folgenden Aufgaben die jeweils richtige Antwort (A, B, C, D) bzw. den berechneten Wert (ohne Maßeinheit)
Chemisches Praktikum für Biologen Klausur am 13.02.2017 Die Klausur besteht aus 10 Seiten. Bitte zu den folgenden Aufgaben die jeweils richtige Antwort (A, B, C, D) bzw. den berechneten Wert (ohne Maßeinheit)
Bist Du nicht "FIT", dann musst Du nacharbeiten.
 Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
Synthese von Acetylsalicylsäure (Aspirin)
 1 Grundlagen 1.1 Einleitung Synthese von Acetylsalicylsäure (Aspirin) von HRISTPH KÖLBL Acetylsalicylsäure, ist eines der weit verbreiteten Schmerz- und Entzündungshemmenden Mittel. Bekannt wurde Acetylsalicylsäure
1 Grundlagen 1.1 Einleitung Synthese von Acetylsalicylsäure (Aspirin) von HRISTPH KÖLBL Acetylsalicylsäure, ist eines der weit verbreiteten Schmerz- und Entzündungshemmenden Mittel. Bekannt wurde Acetylsalicylsäure
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2018
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Carbonsäuren und Derivate Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser/Dr. Martin Sumser September
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Carbonsäuren und Derivate Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser/Dr. Martin Sumser September
Alkohole Brüder des Wassers
 6. Alkohole Brüder des Wassers 6.1 Alkohole Brüder des Wassers entsteht aus Zucker durch die alkoholische Gärung. Dabei werden Glucosemoleküle mit ilfe von efezellen in und Kohlendioxid umgewandelt. NS29
6. Alkohole Brüder des Wassers 6.1 Alkohole Brüder des Wassers entsteht aus Zucker durch die alkoholische Gärung. Dabei werden Glucosemoleküle mit ilfe von efezellen in und Kohlendioxid umgewandelt. NS29
a81 a Carbonylverbindungen (I)
 Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
a81 a Carbonylverbindungen (I)
 Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
Herstellung und Oxidation von 2,4,6-Tri-tert-butylphenol
 2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
Aspirin und Paracetamol im chemischen Vergleich
 Aspirin und Paracetamol im chemischen Vergleich Achtung Aspirin und Paracetamol sind geschützte Namen und dürfen nicht ohne weiteres verwendet werden. Strukturformeln Aus den Strukturformeln leiten wir
Aspirin und Paracetamol im chemischen Vergleich Achtung Aspirin und Paracetamol sind geschützte Namen und dürfen nicht ohne weiteres verwendet werden. Strukturformeln Aus den Strukturformeln leiten wir
Versuch: Seifenherstellung aus Kokosfett
 Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
9 Aromaten. 1 Elemente Chemie Oberstufe NRW Ernst Klett Verlag GmbH, Stuttgart Lösungen zu den Durchblick-Seiten
 Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
Organostickstoff- Verbindungen
 rganostickstoff- Verbindungen [1] Chiralität von Aminen [2] -Enantiomere Isomerisieren sehr schnell -E A 20-30 KJ/mol [2] Alkylierung von Ammoniak [2] [2] [2] -geringe Selektivität aufgrund von Mehrfachalkylierung
rganostickstoff- Verbindungen [1] Chiralität von Aminen [2] -Enantiomere Isomerisieren sehr schnell -E A 20-30 KJ/mol [2] Alkylierung von Ammoniak [2] [2] [2] -geringe Selektivität aufgrund von Mehrfachalkylierung
Die Basis der Biochemie ist Wasser! eine Kartoffel besteht zu 80 % aus Wasser. eine Tomate ist mit 95 % eigentlich kaum etwas anderes als Wasser
 Die Basis der Biochemie ist Wasser! Wasser ist überall: eine Kartoffel besteht zu 80 % aus Wasser eine Tomate ist mit 95 % eigentlich kaum etwas anderes als Wasser ein Bakterium besteht zu 75 % aus Wasser
Die Basis der Biochemie ist Wasser! Wasser ist überall: eine Kartoffel besteht zu 80 % aus Wasser eine Tomate ist mit 95 % eigentlich kaum etwas anderes als Wasser ein Bakterium besteht zu 75 % aus Wasser
+ MnO MnO 3. Oxidierbarkeit primärer, sekundärer und tertiärer Alkohole. Chemikalien. Materialien
 DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
Kohlenwasserstoffe. Homologe Reihe. Alkane. Alkene. HGA-Grundwissen Chemie-10. Klasse NTG
 GA-Grundwissen Chemie-10. Klasse NTG Kohlenwasserstoffe Sind eine Stoffgruppe von chemischen Verbindungen, die nur aus C- und - Atomen bestehen. Aufgrund des unpolaren Molekülbaus sind sie lipophil und
GA-Grundwissen Chemie-10. Klasse NTG Kohlenwasserstoffe Sind eine Stoffgruppe von chemischen Verbindungen, die nur aus C- und - Atomen bestehen. Aufgrund des unpolaren Molekülbaus sind sie lipophil und
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Additionen an Carbonylverbindungen
 Beispielaufgaben Ih. unde 018 Additionen an arbonylverbindungen Additionen an arbonylverbindungen Beispiel 1: Aldolreaktionen finden zwischen zwei arbonylverbindungen statt. Ein Beispiel dafür ist die
Beispielaufgaben Ih. unde 018 Additionen an arbonylverbindungen Additionen an arbonylverbindungen Beispiel 1: Aldolreaktionen finden zwischen zwei arbonylverbindungen statt. Ein Beispiel dafür ist die
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 17.11.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 17.11.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Die Verknüpfung zweier kleinerer Bausteine zu einem größeren läuft in diesem Fall über eine sogenannte Aldoladdition.
 Quelle: www.helpster.de Quelle: www.fotocommunity.de Quelle: www.hobbybrauer.de Das Gehirn benötigt ständig Traubenzucker als Energieträger. Im Fall von Traubenzuckermangel kann der Körper über die Gluconeogenese
Quelle: www.helpster.de Quelle: www.fotocommunity.de Quelle: www.hobbybrauer.de Das Gehirn benötigt ständig Traubenzucker als Energieträger. Im Fall von Traubenzuckermangel kann der Körper über die Gluconeogenese
Seminar zum Organisch-Chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016. Carbonsäuren und Derivate. Dr. Florian Achrainer AK Zipse
 Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Carbonsäuren und Derivate Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Carbonsäuren und Derivate Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
6. Rechenübung Organik (27.01./ )
 1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
ALDEHYDE & KETONE. Referat über die Carbonylverbindungen: Aldehyde und Ketone Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium
 ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
Seminarplan zum. Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie. (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE
 Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Darstellung von Phenolphthalein und Fluorescein
 Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Summenformel. Strukturformel. Halbstrukturformel. Fossile Energieträger. ( 10. Klasse NTG 1 / 47 ) ( 10. Klasse NTG 2 / 47 ) ( 10. Klasse NTG 3 / 47 )
 Summenformel ( 10. Klasse NTG 1 / 47 ) Angabe der Atomsorten und deren Anzahl innerhalb eines Moleküls z.b. Ethanol C 2 6 O Strukturformel ( 10. Klasse NTG 2 / 47 ) Darstellung der bindenden und freien
Summenformel ( 10. Klasse NTG 1 / 47 ) Angabe der Atomsorten und deren Anzahl innerhalb eines Moleküls z.b. Ethanol C 2 6 O Strukturformel ( 10. Klasse NTG 2 / 47 ) Darstellung der bindenden und freien
Chemie Alkohole, Aldehyde & Ketone, Carbonsäuren
 Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Lösung 5 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Falls Sie Fragen zur Vorlesung/Übung/generellen Konzepten haben schreiben
1 Lösung 5 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Falls Sie Fragen zur Vorlesung/Übung/generellen Konzepten haben schreiben
Organische Chemie 10C1. Funktionelle Gruppen 10C2. Homologe Reihe der Alkane 10C3. Nomenklatur der Alkane (gesättigte Kohlenwasserstoffe) 10C4
 Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Philipps-Universität Marburg Organisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß Assistentin: Beate Abé
 Philipps-Universität Marburg 14.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 4/Assistentenversuch):
Philipps-Universität Marburg 14.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 4/Assistentenversuch):
1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie
 1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie Name: Vorname: Matrikel Nr.: 15.12.2010 Die Durchführung und Auswertung der 12 Aufgaben im zweiten Teil dieser Klausur mit je vier Aussagen (a-d)
1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie Name: Vorname: Matrikel Nr.: 15.12.2010 Die Durchführung und Auswertung der 12 Aufgaben im zweiten Teil dieser Klausur mit je vier Aussagen (a-d)
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Elektrophile Additionen von HX an die CC-Doppelbindung (Vollhardt, 3. Aufl., S , 4. Aufl., S ; Hart, S ; Buddrus, S.
 Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!)
 . Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
. Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1. Grundwissen 10.Klasse NTG 2 Grundwissen 10.Klasse NTG 2
 Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Beispielaufgaben IChO 2. Runde 2019 Säurederivate. H2, Pd/C
 Beispielaufgaben Ih 2. Runde 2019 Säurederivate Beispiel 1 ligocarbonsäuren Gegeben sei folgendes Reaktionsschema: A H2, Pd/ H 2, Lindlar Na/NH 3(l) B D Base E A hat eine molare Masse von 118,09 g mol
Beispielaufgaben Ih 2. Runde 2019 Säurederivate Beispiel 1 ligocarbonsäuren Gegeben sei folgendes Reaktionsschema: A H2, Pd/ H 2, Lindlar Na/NH 3(l) B D Base E A hat eine molare Masse von 118,09 g mol
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
113 Estersynthese GEFAHRENSYMBOLE SICHERHEITSRATSCHLÄGE
 113 Estersynthese GUT ZU WISSEN Die Ester sind eine große Stoffgruppe in der organischen Chemie und auch im Alltag finden haben wir häufig mit ihnen zu tun. Bekannteste Vertreter dürften wohl die Polyester
113 Estersynthese GUT ZU WISSEN Die Ester sind eine große Stoffgruppe in der organischen Chemie und auch im Alltag finden haben wir häufig mit ihnen zu tun. Bekannteste Vertreter dürften wohl die Polyester
Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 )
![Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 ) Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 )](/thumbs/74/69784240.jpg) 1 25.01.2006 0.1 Alkohole Alkohole enthalten neben den Elementen C und H auch O. Sie leiten sich aber dennoch von den Kohlenwasserstoffen ab. Beispiel: C 2 H 6 O als Summenformel Strukturformel: C C O
1 25.01.2006 0.1 Alkohole Alkohole enthalten neben den Elementen C und H auch O. Sie leiten sich aber dennoch von den Kohlenwasserstoffen ab. Beispiel: C 2 H 6 O als Summenformel Strukturformel: C C O
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt: Organische Chemie II. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
1. Qualitativer Nachweis von Anionen und Sodaauszug
 Anionennachweis 1 1. Qualitativer Nachweis von Anionen und Sodaauszug Die moderne Analytische Chemie unterscheidet zwischen den Bereichen der qualitativen und quantitativen Analyse sowie der Strukturanalyse.
Anionennachweis 1 1. Qualitativer Nachweis von Anionen und Sodaauszug Die moderne Analytische Chemie unterscheidet zwischen den Bereichen der qualitativen und quantitativen Analyse sowie der Strukturanalyse.
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09. Name: Sarah Henkel Datum:
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 5: alogenalkane Versuch: Reaktivität von
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 5: alogenalkane Versuch: Reaktivität von
Synthese eines Fruchtesters
 Synthese eines Fruchtesters 1/5 Synthese eines Fruchtesters Theorie arbonsäuren können mit Alkoholen unter Abspaltung eines Wasser-Moleküls zu arbonsäure-estern reagieren: ' ' Die Einstellung der Gleichgewichts-Lage
Synthese eines Fruchtesters 1/5 Synthese eines Fruchtesters Theorie arbonsäuren können mit Alkoholen unter Abspaltung eines Wasser-Moleküls zu arbonsäure-estern reagieren: ' ' Die Einstellung der Gleichgewichts-Lage
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 03.02.2016 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 03.02.2016 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Aufgaben zur Chemie der Alkohole und Ether (incl. deren Herstellung)
 Aufgaben zur Chemie der Alkohole und Ether (incl. deren erstellung) TGJ Nucleophile Substitution 1.1. Warum verlaufen nucleophile Substitutionen an Alkoholen leicht in saurer, nicht aber in basischer Lösung?
Aufgaben zur Chemie der Alkohole und Ether (incl. deren erstellung) TGJ Nucleophile Substitution 1.1. Warum verlaufen nucleophile Substitutionen an Alkoholen leicht in saurer, nicht aber in basischer Lösung?
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
KW Alkene. Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1
 KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
Säure-Base-Reaktionen L20. A. Soi
 Säure-Base-Reaktionen L20 244 X Bindungstyp und EN Polarität der Elektronenpaarbindung DEN = 0 X DEN N Cl DEN > 0 d+ d- Z X X + - Na Cl DEN > 1.7 + - Z Elektronenpaarbindung (Kovalente Bindung) => Molekulare
Säure-Base-Reaktionen L20 244 X Bindungstyp und EN Polarität der Elektronenpaarbindung DEN = 0 X DEN N Cl DEN > 0 d+ d- Z X X + - Na Cl DEN > 1.7 + - Z Elektronenpaarbindung (Kovalente Bindung) => Molekulare
Kunststoffe (Polykondensation)
 Kunststoffe (Polykondensation) Herstellung eines Phenoplasts 7. Stunde (13 15 14 00 Uhr) am Donnerstag, den 27. Januar 2011 Ein Chemieprotokoll von Sebastian Huber, Maximilian Mayer, Robert Bozsak und
Kunststoffe (Polykondensation) Herstellung eines Phenoplasts 7. Stunde (13 15 14 00 Uhr) am Donnerstag, den 27. Januar 2011 Ein Chemieprotokoll von Sebastian Huber, Maximilian Mayer, Robert Bozsak und
Funktionelle Gruppen Alkohol
 Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
13. Amine und ihre Derivate
 Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
Präparat 3: Isolierung und Verseifung von Trimyristin aus Muskatnuss - Naturstoff -
 hristina Sauermann 1 - A- Praktikum Präparat 3: Isolierung und Verseifung von Trimyristin aus Muskatnuss - Naturstoff - Teil I: Isolierung von Trimyristin aus Muskatnuss 1. Prinzip Gepulverte Muskatnüsse
hristina Sauermann 1 - A- Praktikum Präparat 3: Isolierung und Verseifung von Trimyristin aus Muskatnuss - Naturstoff - Teil I: Isolierung von Trimyristin aus Muskatnuss 1. Prinzip Gepulverte Muskatnüsse
Organische Chemie 1 Teil 2 2. Vorlesung, Freitag
 Inhalte der 2. Vorlesung: Wdh. 1. Vorlesung 1. Die eaktivität organischer Moleküle 1.4 Der Einfluss von Ladungen 1.5 Der Einfluss von rbitalen 1.6 Das ukleophil-elektrophil-modell 1.7 Die Verwendung von
Inhalte der 2. Vorlesung: Wdh. 1. Vorlesung 1. Die eaktivität organischer Moleküle 1.4 Der Einfluss von Ladungen 1.5 Der Einfluss von rbitalen 1.6 Das ukleophil-elektrophil-modell 1.7 Die Verwendung von
Eine Auswahl typischer Carbonylreaktionen
 Eine Auswahl typischer Carbonylreaktionen Aldol-eaktion ( anschließende Aldol-Kondensation) Kondensation = Abspaltung von Wasser Aldol-eaktion kann basenkatalysiert oder säurekatalysiert durchgeführt werden.
Eine Auswahl typischer Carbonylreaktionen Aldol-eaktion ( anschließende Aldol-Kondensation) Kondensation = Abspaltung von Wasser Aldol-eaktion kann basenkatalysiert oder säurekatalysiert durchgeführt werden.
Halogenalkane. Radikalische Halogenierung von Alkanen. Addition von Halogenwasserstoffen an Alkene. H 3 C + HBr H C C C H.
 alogenalkane erstellung: adikalische alogenierung von Alkanen + l + l + l l l + l Addition von alogenwasserstoffen an Alkene 3 Br + Br 3 Nucleophile Substitution an Alkylhalogeniden Nucleophil Elektrophil
alogenalkane erstellung: adikalische alogenierung von Alkanen + l + l + l l l + l Addition von alogenwasserstoffen an Alkene 3 Br + Br 3 Nucleophile Substitution an Alkylhalogeniden Nucleophil Elektrophil
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan
 Endersch, Jonas 16.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan Reaktionsgleichung:
Endersch, Jonas 16.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan Reaktionsgleichung:
Lösungsblatt 11: Carbonsäuren und Aromaten
 1 Lösungsblatt 11: Carbonsäuren und Aromaten Warm Up Benennen Sie die folgenden Verbindungen nach IUPAC. Finden Sie gegebenenfalls die Trivialnamen: Aufgaben 1) Carbonsäuren i. Begründen Sie aufgrund der
1 Lösungsblatt 11: Carbonsäuren und Aromaten Warm Up Benennen Sie die folgenden Verbindungen nach IUPAC. Finden Sie gegebenenfalls die Trivialnamen: Aufgaben 1) Carbonsäuren i. Begründen Sie aufgrund der
Darstellung von Malachitgrün Präparat 5
 Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
Seminar zum Organisch-Chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016. Oxidation und Reduktion. Dr. Florian Achrainer AK Zipse
 Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 xidation und eduktion Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse März
Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 xidation und eduktion Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse März
Chemie für Biologen WS 2005/6 Arne Lützen Institut für Organische Chemie der Universität Duisburg-Essen (Teil 5: )
 Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
2.Präparat: 1,2 Dibrom -1-phenylethan
 Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Fette, Öle und Tenside
 Schulversuchspraktikum Thomas Polle Sommersemester 2015 Klassenstufen 11 & 12 Fette, Öle und Tenside Kurzprotokoll Inhalt Inhaltsverzeichnis 1Weitere Lehrerversuche... 3 V1 Verseifungszahl... 3 2Weitere
Schulversuchspraktikum Thomas Polle Sommersemester 2015 Klassenstufen 11 & 12 Fette, Öle und Tenside Kurzprotokoll Inhalt Inhaltsverzeichnis 1Weitere Lehrerversuche... 3 V1 Verseifungszahl... 3 2Weitere
Von Arrhenius zu Brönsted
 Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
GK Chemie Carbonsaeuren Ester 1975//II 1. Wie kann man Essigsäure (Ethansäure) aus anorganischen Grundstoffen hergestellt werden? Beschreiben Sie die
 GK Chemie Carbonsaeuren Ester 1975//II 1. Wie kann man Essigsäure (Ethansäure) aus anorganischen Grundstoffen hergestellt werden? Beschreiben Sie die Reaktionsschritte mit Hilfe von Gleichungen! 2. Welche
GK Chemie Carbonsaeuren Ester 1975//II 1. Wie kann man Essigsäure (Ethansäure) aus anorganischen Grundstoffen hergestellt werden? Beschreiben Sie die Reaktionsschritte mit Hilfe von Gleichungen! 2. Welche
Organische Chemie für Biologen und Nebenfächler Übungsaufgaben für die Klausur
 rganische Chemie für Biologen und Nebenfächler Übungsaufgaben für die Klausur Aufgabe 1: Sie wollen Fettflecken von ihrem Kleidungsstück entfernen. Man gibt Ihnen als Fleckenentferner folgende Chemikalien
rganische Chemie für Biologen und Nebenfächler Übungsaufgaben für die Klausur Aufgabe 1: Sie wollen Fettflecken von ihrem Kleidungsstück entfernen. Man gibt Ihnen als Fleckenentferner folgende Chemikalien
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung bildet mit einem primären Amin ein Imin.
Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung bildet mit einem primären Amin ein Imin.
Schulversuch (Gruppe 6/Assistentenversuch): Vergleich aliphatischer Alkohole und Phenole
 Philipps-Universität Marburg 26.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 6/Assistentenversuch):
Philipps-Universität Marburg 26.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 6/Assistentenversuch):
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
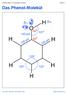 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Synthese von Essigsäureisopropylester (1) Präparat 1
 Synthese von Essigsäureisopropylester (1) Präparat 1 1. Reaktionstyp: Azeotrope Veresterung 2. Reaktionsgleichung: 3 3 3 3 2 3 3 Essigsäure Isopropanol Essigsäureisopropylester Wasser 60,05 g/mol 60,1
Synthese von Essigsäureisopropylester (1) Präparat 1 1. Reaktionstyp: Azeotrope Veresterung 2. Reaktionsgleichung: 3 3 3 3 2 3 3 Essigsäure Isopropanol Essigsäureisopropylester Wasser 60,05 g/mol 60,1
Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag)
 Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
b) Zeichnen Sie die beiden möglichen Isomere der Aldol-Kondensation und bezeichnen Sie die Stereochemie der Produkte.
 1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Zeichnen Sie die beiden
1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Zeichnen Sie die beiden
A) Bei zweiprotonigen Säuren wird zur vollständigen Neutralisation exakt ein
 1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist richtig? A) Bei zweiprotonigen Säuren wird zur vollständigen Neutralisation exakt ein Äquivalent an Natronlauge
1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist richtig? A) Bei zweiprotonigen Säuren wird zur vollständigen Neutralisation exakt ein Äquivalent an Natronlauge
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2017
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2017 xidation und eduktion Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser September 2017 Die Übungsfragen
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2017 xidation und eduktion Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser September 2017 Die Übungsfragen
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der umanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Klausur zum 2. Praktikumsteil (C) vom 25.07.17 NAME;
Chemisches Praktikum für Studierende der umanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Klausur zum 2. Praktikumsteil (C) vom 25.07.17 NAME;
Klausur. Abschluss-Klausur Teil 2 (Praktikumabschluss-Klausur) zum chemischen Praktikum
 Klausur Abschluss-Klausur Teil 2 (Praktikumabschluss-Klausur) zum chemischen Praktikum für Studierende der Physik (Diplom, BSc), Geologie und Geophysik (Diplom), Geowissenschaften (BSc), Landschaftsökologie
Klausur Abschluss-Klausur Teil 2 (Praktikumabschluss-Klausur) zum chemischen Praktikum für Studierende der Physik (Diplom, BSc), Geologie und Geophysik (Diplom), Geowissenschaften (BSc), Landschaftsökologie
Organische Chemie 1 Teil 2 3. Vorlesung Dienstag
 Inhalte der 3. Vorlesung: 2. Carbonylchemie 2.1.2 -Nukleophile 2.1.2.1 eaktivitäten unterschiedlicher Carbonylderivate 2.1.2.2 eduktionen mit NaB4 2.1.2.3 Lithiumaluminiumhydrid (LiAl4) als eduktionsmittel
Inhalte der 3. Vorlesung: 2. Carbonylchemie 2.1.2 -Nukleophile 2.1.2.1 eaktivitäten unterschiedlicher Carbonylderivate 2.1.2.2 eduktionen mit NaB4 2.1.2.3 Lithiumaluminiumhydrid (LiAl4) als eduktionsmittel
Homologe Reihe. Alkane. Alkene. Alkine
 GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
Analytische Chemie. B. Sc. Chemieingenieurwesen. 6. Juli 2016, Uhr. Prof. Dr. T. Jüstel & Stephanie Möller M.Sc.
 Analytische Chemie B. Sc. Chemieingenieurwesen 6. Juli 2016, 10.30 13.30 Uhr Prof. Dr. T. Jüstel & Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Analytische Chemie B. Sc. Chemieingenieurwesen 6. Juli 2016, 10.30 13.30 Uhr Prof. Dr. T. Jüstel & Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Synthese von E,E-dibenzylidenaceton
 Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von E,Edibenzylidenaceton Dietikon, 9. März 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung Der E,E dibenzylidenaceton
Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von E,Edibenzylidenaceton Dietikon, 9. März 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung Der E,E dibenzylidenaceton
