Anhang 1: PATIENTENINFORMATION, ALLGEMEINE INFORMATION
|
|
|
- Berthold Jaeger
- vor 7 Jahren
- Abrufe
Transkript
1 Anhang 1: PATIENTENINFORMATION, ALLGEMEINE INFORMATION Myeloablative Konditionierung von Patienten mit Myelofibrose mit myeloischer Metaplasie (MMM) bzw. Osteomyelofibrose mittels i.v. Treosulfan und autologer peripherer Blutvorläuferzelltransplantation (PBPCT) mit hohen Dosen an CD34+ Zellen Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen wurde eine Erkrankung des Knochenmarks diagnostiziert, die zu den sogenannten chronischen myeloproliferativen Erkrankungen gerechnet wird. Die genaue Diagnose bei Ihnen kann Polycythaemia vera, essentielle Thrombozythämie oder idiopathische Myelofibrose lauten. Bei allen diesen Erkrankungen kann es im Krankheitsverlauf zu einer fortschreitenden Verfaserung (Fibrosierung) des Knochenmarks kommen. Diese Diagnose ist bei Ihnen bereits durch eine Knochenmarkentnahme (Biopsie) gesichert worden. Die Ursache dieser Erkrankung wird in einer Störung der Blutstammzellen vermutet, die falsche Botenstoffe an die Umgebung abgeben und Bindegewebszellen zu einer vermehrten Faserbildung anregen. Durch die Verfaserung ist im Knochenmark nicht mehr ausreichend Platz für die Blutbildung vorhanden, und es kann in der Folge zu einer Abnahme der Blutbildung kommen. Dies kann sich in einer Abnahme des roten Blutfarbstoffs (Hämoglobin) und der Blutplättchen (Thrombozyten) bemerkbar machen, weshalb sie eventuell bereits Bluttransfusionen benötigen oder in absehbarer Zeit benötigen werden. Außerdem kann es zu einer Vergrößerung der inneren Organe Milz und Leber kommen. An Allgemeinsymptomen bemerken Sie vielleicht Nachtschweiß, Fieber und Gewichtsverlust. Liegen mehrere dieser Befunde vor, so ist die Krankheit bereits relativ weit fortgeschritten, und es ist mit einer weiteren Verschlechterung zu rechnen. Die vorliegende Studie hat das Ziel, das Voranschreiten der Erkrankung aufzuhalten. Insbesondere geht es darum zu erreichen, dass sie für einige Zeit weniger oder keine Bluttransfusionen benötigen, bzw. darum, den Zeitpunkt der erstmaligen Transfusionsbedürftigkeit deutlich herauszuschieben. BESCHREIBUNG DES STUDIENABLAUFS: Vor Beginn der Studie werden Sie gründlich untersucht. Hierzu gehören Blutabnahmen, Ultraschall und Röntgenuntersuchungen und eine Knochenmarkbiopsie und eine Knochenmarkaspiration. Wir werden Ihre Herz- und Lungenfunktion prüfen und Blutuntersuchungen durchführen, um auszuschließen, daß Sie an HIV erkrankt sind. Die Medikamente, die bei der Therapie zum Einsatz kommen, haben erbgutverändernde Nebenwirkungen. Daher muß vor Beginn der Therapie gewährleistet sein, daß bei Ihnen ein sichere Empfängnisverhütung vorliegt. Fragen einer eventuellen Familienplanung sollten im Vorfeld mit Ihrem behandelnden Arzt geklärt werden. Sind die Voraussetzungen gegeben und haben Sie sich bereit erklärt, sich an der Untersuchung zu beteiligen, wird ambulant eine Behandlung mit G-CSF (Handelsname Neupogen) begonnen. Dies ist ein sogenannter Blutzell-Wachstumsfaktor, der dazu dient, Blutstammzellen aus dem Knochenmark in das Blut freizusetzen. Das G-CSF wird täglich für zunächst vier Tage unter die Haut gespritzt, so daß die weißen Blutkörperchen und die
2 Blutstammzellen aus dem Knochenmark ins Blut geschwemmt werden. Wenn die Leukozytenzahl deutlich ansteigt, beginnt man, die Stammzellen zu sammeln. Dabei werden Sie, wie bei einer Art Blutwäsche, an einen Blutseparator angeschlossen. Das Blut läuft aus einer Vene in diesen Blutseparator und wird Ihnen nach entsprechender Aufarbeitung im Separator zurückgeführt. Eine solche Prozedur dauert ca. 3-4 Stunden und muß, falls nicht genügend Blutstammzellen gewonnen werden können, nach fortgesetzter Gabe von G-CSF an den folgenden Tagen fortgesetzt werden. Im Anschluss an die Sammlung werden die gesammelten Zellen eingefroren. Zu Kontrolluntersuchungen der Transplantatfunktion können Zellen, die nicht für die Transplantation benötigt werden bzw. bis zu 5% der Transplantatzellen verwendet werden. Im Abstand von einigen Tagen bis Monaten wird dann mit einer sogenannten Hochdosischemotherapie begonnen. Diese beinhaltet die Gabe eines chemotherapeutischen Medikamentes über drei Tage. Dies führt zu einer Zerstörung der blutbildenden Funktion des Knochenmarks, zusammen mit den kranken Blutstammzellen. Nach einem Tag Pause, die der Körper benötigt, um sich von den Resten der giftigen Chemotherapie zu befreien, werden die zuvor gesammelten, eingefrorenen Blutstammzellen direkt ins Blut zurückgegeben. Sie siedeln sich von dort aus wieder im Knochenmark an und beginnen eine neue Blutbildung. Da durch die Hochdosischemotherapie die zahl der kranken Stammzellen deutlich vermindert wurde, kommt die Fibrosierung für einige Zeit zum Stillstand und bildet sich voraussichtlich auch in einigen Fällen zurück. Nachdem man genügend Blutstammzellen gesammelt hat, werden Sie zur Hochdosis- Therapie mit Treosulfan stationär aufgenommen. Der stationäre Aufenthalt wird etwa fünf Wochen betragen. Sie werden mit einem zentralen Venenkatheter versorgt werden, damit gewährleistet ist, daß die unterstützende Therapie problemlos durchgeführt werden kann. Diese kann u.a. die Gabe von Blutprodukten und Antibiotika beinhalten. Die Hochdosis- Therapie besteht aus einer Gabe von Treosulfan an drei aufeinander folgenden Tagen. Die Infusionsdauer beträgt jeweils zwei Stunden. Treosulfan zerstört im wesentlichen das blutbildende Knochenmark. Nach einem Tag Pause, die der Körper benötigt, um sich von den Resten der giftigen Chemotherapie zu befreien, werden die zuvor gesammelten, eingefrorenen Blutstammzellen direkt ins Blut zurückgegeben. Sie siedeln sich von dort aus wieder im Knochenmark an und beginnen eine neue Blutbildung. Da durch die Hochdosischemotherapie die zahl der kranken Stammzellen deutlich vermindert wurde, kommt die Fibrosierung für einige Zeit zum Stillstand und bildet sich voraussichtlich auch in einigen Fällen zurück. Um die Stammzellen bei der Rückgabe nicht zu schädigen, müssen diese relativ kalt zurückgegeben werden, so daß es bei der Rückgabe zu Herzrhythmusstörungen und Kreislaufnebenwirkungen kommen kann. Des weiteren wird zur Haltbarmachung der Stammzellen eine Substanz zugesetzt, die nach Rückgabe zu einem unangenehmen Geruch und Geschmack und eventuell Übelkeit führt. In den darauffolgenden Tagen werden die Blutwerte sehr niedrig sein, wobei die roten Blutkörperchen und die Blutplättchen Ihnen gegebenenfalls durch Transfusionen ersetzt werden. Die fehlenden weißen Blutkörperchen können nicht ersetzt werden und bedingen die erhöhte Infektionsbereitschaft, so daß prophylaktisch bereits Antibiotika verabreicht werden. In dieser Phase müssen Sie also mit Fieber und Entzündungen der Mundschleimhaut rechnen. Es werden strenge hygienische Maßnahmen, wie häufige Händedesinfektion, keimarme Kost u.a. eingesetzt. Diese sogenannte Aplasiephase ist bei Ihrer Erkrankung voraussichtlich deutlich länger als bei anderen Erkrankungen, die ebenfalls mit autologer Blutstammzelltransplantation behandelt werden.
3 Da sowohl die Stammzellsammlung als auch die Hochdosistherapie und Stammzellrückgabe, zusammen wird dies autologe Blutstammzelltransplantation genannt, für sich genommen etablierte Verfahren sind, gibt es dafür bereits anerkannte Aufklärungen. Wir möchten Sie bitten, sich auch diese in Ruhe durchzulesen. NUTZEN/RISIKO Die vorgeschlagene Therapie bietet die Möglichkeit, das Voranschreiten der Erkrankung aufzuhalten, zu erwarten ist eine Verzögerung um ca. ein Jahr. Für ungefähr diese Zeitspanne kann auch mit einer Abnahme der Transfusionsbedürftigkeit gerechnet werden. Wir hoffen, insgesamt mit dieser Therapie auch eine Lebensverlängerung zu erreichen. Dem gegenüber steht das Risiko, in der Folge der autologen Blutstammzelltransplantation zu versterben, was auf weniger als 10% im ersten Jahr geschätzt wird. UNTERSUCHUNGEN WÄHREND DER STUDIE, AUTOPSIE Für die Studie müssen Blutabnahmen in regelmäßigen Zeitabständen, sowie insgesamt drei Knochenmarkentnahmen (Biopsien) aus dem beckenknochen durchgeführt werden. Die Ergebnisse dieser Untersuchungen fliessen in Ihre Behandlung ein, im Einzelfall kann es aber sein, dass insgesamt mehr Proben entnommen werden, als alleine klinisch erforderlich wären. Sollten Sie nach Beginn der Teilnahme an der Studie zu irgendeinem Zeitpunkt versterben, bitten wir Sie bereits jetzt, vor Beginn, einer Autopsie zustimmen. Dies ist notwendig, da wir in jedem Fall herausfinden wollen, ob Ihr Tod in irgendeinem Zusammenhang mit dieser Studie steht. Die Zustimmung zur Autopsie ist in der Zustimmung zur Studie (s.u.) enthalten. ALTERNATIVE BEHANDLUNGEN Die Möglichkeiten einer weniger aggressiven Behandlung bei dieser Erkrankung sind begrenzt, in Frage kommen Behandlungen mit Cortisonpräparaten und Interferon. Diese lassen keine derart günstige Beeinflussung der Transfusionsnotwendigkeit erwarten. Es gibt für die vorliegende Erkrankung eine wesentlich riskantere Behandlung mittels einer Fremdspende von Blutstammzellen von verwandten oder fremden Spendern (allogene Blutstammzelltransplantation). Diese bietet die Chance einer kompletten Heilung, allerdings ist die Behandlung wesentlich belastender als eine autologe Transplantation und die Sterblichkeit liegt im ersten Jahr bei ca. 30%. Eine allogene Blutstammzelltransplantation ist auch nach einer autologen Blutstammzelltransplantation noch möglich. DATENSCHUTZ Während der Teilnahme an der Studie werden medizinische Befunde und persönliche Informationen von Ihnen erhoben und niedergeschrieben. Die Aufzeichnung der im Rahmen dieser Studie erhobenen Daten erfolgt zunächst in Originalunterlagen bzw. Ihrer Krankenakte, in der Ihr Arzt auch bisher alle Befunde eingetragen hat. Die für die Studie wichtigen Daten werden zusätzlich in einem gesonderten Dokumentationsbogen eingetragen. Diese werden der Studienzentrale in der Medizinischen Klinik und Poliklinik V der Universität Heidelberg übermittelt. Mit dem Unterzeichnen der Einverständniserklärung geben Sie Ihre Einwilligung zur Weitergabe ihrer Daten als auch zur Einsichtnahme durch autorisierte Dritte. Die Belange der ärztlichen Schweigepflicht und des Datenschutzes werden voll gewahrt. Ihr Name wird zu keiner Zeit öffentlich gemacht. Anonymisierten Daten können auch an ausländische Gesundheitsbehörden weitergegeben werden. Im Rahmen der Überwachung von klinischen
4 Studien können unabhängige Personen von autorisierter Seite Einsicht in ihre Krankenakte nehmen, um sicherzustellen, dass die Daten in dieser Studie korrekt erhoben wurden. Diese Personen sind jedoch von Amts wegen zur Verschwiegenheit verpflichtet. Um sicherzustellen, daß alle Daten korrekt aus den Originalunterlagen/Ihrer Krankenakte in die Dokumentationsbögen übertragen wurden, können die Eintragungen in die Dokumentationsbögen durch besonders geschulte und zur Verschwiegenheit verpflichtete Mitarbeiter, sog. Monitore, mit den Originaldaten verglichen werden. Mit Ihrem Einverständnis zur Teilnahme an dieser klinischen Studie entbinden Sie den Prüfarzt gegenüber den staatlichen Gesundheitsbehörden und gegenüber den Monitoren von seiner Schweigepflicht insofern, als Gesundheitsbehörden und Monitor, soweit zur Überprüfung der korrekten Datenübertragung notwendig, Einsicht in die im Rahmen dieser klinischen Studie erfolgten Originalaufzeichnungen nehmen können. Bei Rücktritt von der Studie ist aus gesetzlichen Gründen für eine bestimmte Zeit keine Löschung der Daten möglich. MÖGLICHE RISIKEN UND NEBENWIRKUNGEN G-CSF: Knochenschmerzen, Muskelschmerzen, Kopfschmerzen, Veränderungen der Leberwerte, Anstieg der Harnsäure, Zunahme der Milzgröße. Verschlechterung von präexistierenden entzündlichen Erkrankungen wie Psoriasis oder einer Vaskulitis. Allergische Reaktionen einschl. Schmerzen in der Brust und ein Blutdruckabfall sind in Einzelfällen in Zusammenhang mit der Erstgabe beschrieben worden. Treosulfan: Übelkeit und Erbrechen, Durchfall, veränderte Pigmentierung der Haut mit Bronzefärbung, Hautausschlag, Schuppenflechte, Sklerodermie, allergische Lungenentzündung und Lungenfibrose, Haarausfall, Sterilität, Störung des blutbildenden Systems, Herzstörungen, Schleimhautentzündungen, Parästhesien, hämorrhagische Zystitis, Morbus Addison, und Hypoglykämie. Schmerzhafte Entzündungen bei Extravasation. Transfusionen: Bis zu dem Anwachsen und der vollständigen Funktionstüchtigkeit der übertragenen Stammzellen sind zudem Übertragungen von roten Blutkörperchen und Blutplättchen notwendig und mit den entsprechenden Risiken (wie z.b. der Übertragung von Infektionen) verbunden. Die unerwünschten Wirkungen bilden sich glücklicherweise bei den meisten Patienten von alleine wiederzurück. Allerdings können Nebenwirkungen welche die Lebensqualität deutlich vermindern, wie z. B. Einschränkung von wichtigen Körperorganen (Herz, Niere, Leber und andere) oder Nebenwirkungen, welche kosmetisch störend sind, wie z. B. Dunkelfärbungen der Haut oder fehlender Haarwuchs lebenslang vorhanden bleiben. Auch kann durch die Chemotherapien die Entstehung von anderen bösartigen Erkrankungen (wie z. B. Blutkrebs) zu einem späteren Zeitpunkt begünstigen. Über mögliche nach Jahren auftretende Spätfolgen ist bis heute wenig bekannt. Die Wahrscheinlichkeit, akut an den Nebenwirkungen dieser Therapie zu versterben, beträgt etwa 5%.
5 NACHSORGEUNTERSUCHUNGEN Falls Sie an dieser Untersuchung teilnehmen, ist es notwendig, daß Sie regelmäßig (zunächst in kürzeren, später in längeren Abständen) und langfristig (mindestens 10 Jahre nach Transplantation, ab dem dritten Jahr nach Transplantation mindestens einmal jährlich) an Nachsorgeuntersuchungen teilnehmen. PROBANDENVERSICHERUNG Gegen eine körperliche Schädigung, die ursächlich mit dieser Therapie zusammenhängt, wird für Sie entsprechend den Vorschriften des Deutschen Arzneimittelgesetzes eine Patientenversicherung bei der: Westfälische Provinzial-Versicherung, Provinzial-Allee-1, Münster Unter folgender Policen-Nr.: LS-Nr.089/ abgeschlossen. Obliegenheiten der Patienten/Probanden: Um den Versicherungsschutz nicht zu gefährden, dürfen Sie sich einer medizinischen Behandlung nur im Einvernehmen mit dem Prüfarzt unterziehen (Notfälle ausgenommen) und müssen jede Änderung, insbesondere aber eine Verschlechterung Ihres Gesundheitszustandes, die als Folge der klinischen Prüfung aufgetreten sein könnte, unverzüglich dem Versicherer mitteilen. Dabei sollten Sie die Hilfe des Prüfarztes in Anspruch nehmen. Abschließend möchten wir Sie darauf hinweisen, daß Ihre Teilnahme an dieser Studie freiwillig ist. Sie können Ihre Einverständnis jederzeit und ohne Angaben von Gründen und ohne Nachteile für Ihre weitere medizinische Versorgung zurückziehen. Wir möchten Sie darauf hinweisen, dass der erwartete therapeutische Nutzen Ihrer Teilnahme an dieser Untersuchung für Sie möglicherweise gering sein wird, daß jedoch neue Erkenntnisse gewonnen werden können, von denen eventuell andere Patienten/innen zu einem späteren Zeitpunkt profitieren können. Wir möchten Sie außerdem bitten, alle Fragen, die Sie im Zusammenhang mit dieser Untersuchung haben, offen mit uns zu diskutieren. Für eventuelle weitergehende Fragen können Sie sich an die Studienzentrale unter der Telefonnummer +49 (0)6221 / wenden. Wir danken für Ihre Mitarbeit Name des Arztes: Telefon:......
6 Anhang 2: Einverständniserklärung zur Teilnahme an der klinischen Studie: Myeloablative Konditionierung von Patienten mit Myelofibrose mit myeloischer Metaplasie (MMM) bzw. Osteomyelofibrose mittels i.v. Treosulfan und autologer peripherer Blutvorläuferzelltransplantation (PBPCT) mit hohen Dosen an CD34+ Zellen Herr/Frau hat mit mir, (Name des aufklärenden Arztes) (Vorname/Name der/s Patientin/en) heute ein ausführliches abschließendes Aufklärungsgespräch geführt. Ich bin über Sinn, Bedeutung und Verlauf der Studie sowie über mögliche Belastungen und Risiken anhand der schriftlichen Patienten-/Probanden-Information, die ich erhalten habe, aufgeklärt worden. In diesem Zusammenhang sind mir alle meine Fragen vollständig beantwortet worden. Das Aufklärungsgespräch erstreckte sich im einzelnen über 1. die Art der Erkrankung, ihre Behandlungsmöglichkeiten und die Prognose 2. das Ziel der Untersuchung 3. die Gabe der Blutzell-Wachstumsfaktoren, ihre Nebenwirkungen und Risiken 4. die Art der Stammzellgewinnung und -reinfusion sowie dabei auftretende Risiken 5. die Art und Durchführung der geplanten Chemotherapie, ihre Nebenwirkungen und Risiken 6. die Notwendigkeit sicherer empfängnisverhütender Maßnahmen 7. die Zustimmung zu einer Autopsie 8. die Notwendigkeit therapiebegleitender Diagnostik einschl. Röntgenuntersuchungen und häufiger Blutuntersuchungen 9. die Notwendigkeit und die Art der die Chemotherapie begleitenden Behandlung einschl. der eventuellen Gabe von Blutprodukten (rote Blutzellen oder Blutplättchen) und Antibiotika 10. Weitergabe und Nutzung von Daten zur wissenschaftlichen Auswertung 11. Entscheidungsfreiheit der/s Patientin/en
7 Ich wurde darüber aufgeklärt und stimme zu, daß die im Rahmen dieser klinischen Studie erhobenen Daten in anonymisierter Form an die zuständigen Gesundheitsbehörden (örtliche Überwachungsbehörde, Bundesoberbehörden) weitergegeben werden können. Ich entbinde den Prüfarzt gegenüber den staatlichen Gesundheitsbehörden insofern, als Gesundheitsbehörden und Monitor, soweit zur Überprüfung der korrekten Datenübertragung erforderlich, Einsicht in die im Rahmen dieser klinischen Studie erfolgten Originalaufzeichnungen nehmen können. Ein Exemplar dieses Merkblattes ist mir zum Verbleib ausgehändigt worden. Mir ist klar, daß die o.g. Methode bislang noch nicht bei einer größeren Patientenzahl zur Anwendung gekommen ist. Ich stimme der Teilnahme an der oben genannten Studie freiwillig zu. Ich weiß, daß ich meine Zustimmung jederzeit und ohne Begründung und ohne Nachteile für meine weitere medizinische Versorgung widerrufen kann. Falls ich teilnehme, bin ich bereit, langfristig an Nachsorgeuntersuchungen teilzunehmen. Ort, Datum Ort, Datum Ort Datum Unterschrift Unterschrift Unterschrift der/s Patientin/en der/s Ärztin/Arztes Zeuge der/s Patientin/en
Einverständniserklärung:
 Zum Verbleib beim Patienten Einverständniserklärung: Name, Vorname...geb. am... wohnhaft in... Ich wurde ausreichend in mündlicher und schriftlicher Form über die klinische Studie Phase II Studie zur Therapie
Zum Verbleib beim Patienten Einverständniserklärung: Name, Vorname...geb. am... wohnhaft in... Ich wurde ausreichend in mündlicher und schriftlicher Form über die klinische Studie Phase II Studie zur Therapie
Patienteninformation und Einwilligungserklärung. zur Teilnahme am Nephronophthise-Register
 Patienteninformation und Einwilligungserklärung zur Teilnahme am Nephronophthise-Register Auftraggeber der Studie: Prof. Dr. med. Heymut Omran Direktor der Klinik und Poliklinik für Kinder- und Jugendmedizin
Patienteninformation und Einwilligungserklärung zur Teilnahme am Nephronophthise-Register Auftraggeber der Studie: Prof. Dr. med. Heymut Omran Direktor der Klinik und Poliklinik für Kinder- und Jugendmedizin
Patienteninformation:
 Patienteninformation: Synthetisches Netz versus kein Netz bei Nabelbrüchen: eine prospektive, doppelblinde, randomisierte, kontrollierte Studie Synthetic mesh versus no mesh for umbilical hernias: a prospective
Patienteninformation: Synthetisches Netz versus kein Netz bei Nabelbrüchen: eine prospektive, doppelblinde, randomisierte, kontrollierte Studie Synthetic mesh versus no mesh for umbilical hernias: a prospective
Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
 Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
 Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Therapie mit Cyclophosphamid
 PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Therapie mit Cyclophosphamid Sehr geehrte Patientin! Sehr geehrter Patient! Sie leiden unter einer schwerwiegenden entzündlichen Erkrankung des rheumatischen
PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Therapie mit Cyclophosphamid Sehr geehrte Patientin! Sehr geehrter Patient! Sie leiden unter einer schwerwiegenden entzündlichen Erkrankung des rheumatischen
PATIENTENINFORMATION. Nationales Klinisches Amyloidose-Register
 UniversitätsKlinikum Heidelberg Medizinische Klinik Universitätsklinikum Heidelberg Im Neuenheimer Feld 410 69120 Heidelberg Medizinische Klinik (Krehl-Klinik) Abteilung Innere Medizin V Hämatologie, Onkologie
UniversitätsKlinikum Heidelberg Medizinische Klinik Universitätsklinikum Heidelberg Im Neuenheimer Feld 410 69120 Heidelberg Medizinische Klinik (Krehl-Klinik) Abteilung Innere Medizin V Hämatologie, Onkologie
Myelofibrose: Krankheit, Diagnose, Beschwerden
 Myelofibrose: Krankheit, Diagnose, Beschwerden Wissenswertes über Myelofibrose Was ist eine Myelofibrose? Wie entsteht Myelofibrose? Welche Beschwerden verursacht die Erkrankung? Wie erkennt man die Myelofibrose?
Myelofibrose: Krankheit, Diagnose, Beschwerden Wissenswertes über Myelofibrose Was ist eine Myelofibrose? Wie entsteht Myelofibrose? Welche Beschwerden verursacht die Erkrankung? Wie erkennt man die Myelofibrose?
Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
 Universitätsmedizin Göttingen, 37099 Göttingen Institut für Neuropathologie, Robert-Koch-Str. 40, D-37075 Göttingen Institut für Neuropathologie Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472
Universitätsmedizin Göttingen, 37099 Göttingen Institut für Neuropathologie, Robert-Koch-Str. 40, D-37075 Göttingen Institut für Neuropathologie Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472
Schriftliche Einwilligung und datenschutzrechtliche Erklärung zur Teilnahme an der Studie mit dem Namen
 Prüfstelle: Schriftliche Einwilligung und datenschutzrechtliche Erklärung zur Teilnahme an der Studie mit dem Namen Simultaneous Study of Docetaxel Based Anthracycline Free Adjuvant Treatment Evaluation,
Prüfstelle: Schriftliche Einwilligung und datenschutzrechtliche Erklärung zur Teilnahme an der Studie mit dem Namen Simultaneous Study of Docetaxel Based Anthracycline Free Adjuvant Treatment Evaluation,
Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
 Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des ZNS im Rahmen des MS-Spenderprogramms Universitätsmedizin Göttingen, 37099 Göttingen Institut für Neuropathologie,
Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des ZNS im Rahmen des MS-Spenderprogramms Universitätsmedizin Göttingen, 37099 Göttingen Institut für Neuropathologie,
Patienten-Information und Einwilligung zur Durchführung einer klinischen Untersuchung mit volljährigen einwilligungsfähigen Patienten 1
 Patienten-Information und Einwilligung zur Durchführung einer klinischen Untersuchung mit volljährigen einwilligungsfähigen Patienten 1 Prüfstelle: Prüfarzt: Petrus-Krankenhaus Wuppertal Prof. Dr. med.
Patienten-Information und Einwilligung zur Durchführung einer klinischen Untersuchung mit volljährigen einwilligungsfähigen Patienten 1 Prüfstelle: Prüfarzt: Petrus-Krankenhaus Wuppertal Prof. Dr. med.
Patientenaufklärungs- und Informationshinweise
 Patientenaufklärungs- und Informationshinweise ZIELSETZUNG DER STUDIE Ihnen wird hiermit die Teilnahme an einer klinischen Studie angeboten. Ziel dieser Studie ist der klinische Ausgang und der Wirksamkeitsnachweis
Patientenaufklärungs- und Informationshinweise ZIELSETZUNG DER STUDIE Ihnen wird hiermit die Teilnahme an einer klinischen Studie angeboten. Ziel dieser Studie ist der klinische Ausgang und der Wirksamkeitsnachweis
Patienteninformation zur Teilnahme an der Registerstudie NEOCYST Netzwerk zur Erforschung zystischer Nierenerkrankungen im Kindesalter
 Patienteninformation und Einwilligungserklärung zur Teilnahme an der Registerstudie NEOCYST Patienten von 6 17 Jahren Registerleitung: Univ.-Prof. Dr. med. Martin Konrad Klinik und Poliklinik für Kinder-
Patienteninformation und Einwilligungserklärung zur Teilnahme an der Registerstudie NEOCYST Patienten von 6 17 Jahren Registerleitung: Univ.-Prof. Dr. med. Martin Konrad Klinik und Poliklinik für Kinder-
PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Basistherapie mit Abatacept
 PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Basistherapie mit Abatacept Sehr geehrte Patientin! Sehr geehrter Patient! Sie leiden an einer chronischen Polyarthritis (Rheumatoiden Arthritis). Ihr
PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Basistherapie mit Abatacept Sehr geehrte Patientin! Sehr geehrter Patient! Sie leiden an einer chronischen Polyarthritis (Rheumatoiden Arthritis). Ihr
PATIENTENINFORMATION. Caregiver Burden bei betreuenden Angehörigen schwer betroffener Parkinsonpatienten
 Version 1.2 Neurologische Klinik mit Klinischer Neurophysiologie Kommissarischer Direktor: Prof. Dr. med. M. Stangel PD Dr. med. F. Wegner Telefon: (0511) 532-3110 Fax: (0511) 532-3115 Carl-Neuberg-Straße
Version 1.2 Neurologische Klinik mit Klinischer Neurophysiologie Kommissarischer Direktor: Prof. Dr. med. M. Stangel PD Dr. med. F. Wegner Telefon: (0511) 532-3110 Fax: (0511) 532-3115 Carl-Neuberg-Straße
Studie zur Sicherheit von Flugreisen bei Patienten mit Pulmonaler Hypertonie (jeglicher Genese)
 Prüfstelle: Abteilung Pneumologie und Intensivmedizin der Medizinischen Klinik II Uniklinik Gießen und Marburg Standort Gießen Klinikstr. 33, 35392 Gießen Telefon: 0641 985 42352 Prüfärzte: Prof. Dr. A.
Prüfstelle: Abteilung Pneumologie und Intensivmedizin der Medizinischen Klinik II Uniklinik Gießen und Marburg Standort Gießen Klinikstr. 33, 35392 Gießen Telefon: 0641 985 42352 Prüfärzte: Prof. Dr. A.
Patienteninformation. Sehr geehrte Patientin, sehr geehrter Patient,
 und Biomaterialbank Biomaterialsammlung und prospektive Datenerfassung zu Diagnostik, Behandlung und Krankheitsverlauf der ALL des Erwachsenen Patienteninformation Sehr geehrte Patientin, sehr geehrter
und Biomaterialbank Biomaterialsammlung und prospektive Datenerfassung zu Diagnostik, Behandlung und Krankheitsverlauf der ALL des Erwachsenen Patienteninformation Sehr geehrte Patientin, sehr geehrter
PATIENTENAUFKLÄRUNG ZWECK DER ZUSATZUNTERSUCHUNG
 Immunologische und molekularbiologische Untersuchungen im Blut und im Gewebe zur Verbesserung der Diagnostik als PATIENTENAUFKLÄRUNG Sie werden gebeten, an einer Zusatzuntersuchung zur Bestimmung Ihres
Immunologische und molekularbiologische Untersuchungen im Blut und im Gewebe zur Verbesserung der Diagnostik als PATIENTENAUFKLÄRUNG Sie werden gebeten, an einer Zusatzuntersuchung zur Bestimmung Ihres
Sehr geehrte Patientin! Sehr geehrter Patient!
 Univ. Klinik f. Innere Medizin LKH Graz Klinische Abteilung für Rheumatologie und Immunologie Univ. Prof. Dr. W. Graninger Auenbruggerplatz 15, A-8036 Graz Tel 0 316-385-12645 PATIENTENAUFKLÄRUNG ZUR THERAPIE
Univ. Klinik f. Innere Medizin LKH Graz Klinische Abteilung für Rheumatologie und Immunologie Univ. Prof. Dr. W. Graninger Auenbruggerplatz 15, A-8036 Graz Tel 0 316-385-12645 PATIENTENAUFKLÄRUNG ZUR THERAPIE
Information und Einverständniserklärung für Patienten und Patientinnen, die an der Schweizerischen HIV-Kohortenstudie teilnehmen
 Information und Einverständniserklärung für Patienten und Patientinnen, die an der Schweizerischen HIV-Kohortenstudie teilnehmen Sehr geehrte Patientin, sehr geehrter Patient Wir laden Sie ein, an der
Information und Einverständniserklärung für Patienten und Patientinnen, die an der Schweizerischen HIV-Kohortenstudie teilnehmen Sehr geehrte Patientin, sehr geehrter Patient Wir laden Sie ein, an der
Patienten-/Patientinneninformation und Einwilligungserklärung zur Teilnahme an der Beobachtungsstudie
 Patienten-/Patientinneninformation und Einwilligungserklärung zur Teilnahme an der Beobachtungsstudie APRES: Angemessenheit der Antibiotika -Verschreibungen in der hausärztlichen Praxis in Europa im Hinblick
Patienten-/Patientinneninformation und Einwilligungserklärung zur Teilnahme an der Beobachtungsstudie APRES: Angemessenheit der Antibiotika -Verschreibungen in der hausärztlichen Praxis in Europa im Hinblick
Diese Broschüre fasst die wichtigsten Informationen zusammen, damit Sie einen Entscheid treffen können.
 Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Erläuterungen zur Einwilligungserklärung
 Erläuterungen zur Einwilligungserklärung Leisten Sie einen Beitrag zur medizinischen Forschung Liebe Patientin, Lieber Patient Dank der medizinischen Forschung leisten die Ärzte und Wissenschaftler der
Erläuterungen zur Einwilligungserklärung Leisten Sie einen Beitrag zur medizinischen Forschung Liebe Patientin, Lieber Patient Dank der medizinischen Forschung leisten die Ärzte und Wissenschaftler der
Patienteninformation und Einverständniserklärung zur Biobank des Universitätsklinikums Düsseldorf
 Patienteninformation und Einverständniserklärung zur Biobank des Universitätsklinikums Düsseldorf Sehr geehrte Patientin, sehr geehrter Patient, im Folgenden möchten wir Sie um Ihr Einverständnis bitten,
Patienteninformation und Einverständniserklärung zur Biobank des Universitätsklinikums Düsseldorf Sehr geehrte Patientin, sehr geehrter Patient, im Folgenden möchten wir Sie um Ihr Einverständnis bitten,
Biologicaregister für entzündliche rheumatische Erkrankungen e.v. BioReg. ZVR-Zahl Zahl p.a. Schloßhoferstrasse 4/4/12, 1210 Wien
 Biologicaregister für entzündliche rheumatische Erkrankungen e.v. BioReg ZVR-Zahl Zahl 295050213 p.a. Schloßhoferstrasse 4/4/12, 1210 Wien Patientenaufklärung und Patientendatenschutzrechtliche Zustimmungserklärung
Biologicaregister für entzündliche rheumatische Erkrankungen e.v. BioReg ZVR-Zahl Zahl 295050213 p.a. Schloßhoferstrasse 4/4/12, 1210 Wien Patientenaufklärung und Patientendatenschutzrechtliche Zustimmungserklärung
Patienteninformation. zur Teilnahme an
 Prüfstelle: Patienteninformation zur Teilnahme an Randomisierte endokrine Therapieintervention bei postmenopausalen, hormonrezeptorpositiven Patientinnen mit dem Nachweis zirkulierender Tumorzellen im
Prüfstelle: Patienteninformation zur Teilnahme an Randomisierte endokrine Therapieintervention bei postmenopausalen, hormonrezeptorpositiven Patientinnen mit dem Nachweis zirkulierender Tumorzellen im
Kymriah (tisagenlecleucel)
 Um die Wirkungen des Arzneimittels Kymriah für Ihre Gesundheit optimal nutzen zu können, seine ordnungsgemäße Anwendung sicherzustellen und seine Nebenwirkungen zu begrenzen, sind bestimmte Maßnahmen/Sicherheitsvorkehrungen
Um die Wirkungen des Arzneimittels Kymriah für Ihre Gesundheit optimal nutzen zu können, seine ordnungsgemäße Anwendung sicherzustellen und seine Nebenwirkungen zu begrenzen, sind bestimmte Maßnahmen/Sicherheitsvorkehrungen
für die Patienten-Information und -Einwilligung zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Patienten
 PROSTATITIS, ENTZÜNDUNG UND FRUCHTBARKEIT für die zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Patienten Prüfstelle: Klinik für Urologie, Kinderurologie und Andrologie,
PROSTATITIS, ENTZÜNDUNG UND FRUCHTBARKEIT für die zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Patienten Prüfstelle: Klinik für Urologie, Kinderurologie und Andrologie,
Klinisch wissenschaftliches Begleitprogramm
 Version 3.0; Köln, den 26.07.2010 Sponsor Code: Uni-Koeln-1167 Sponsor: Universität zu Köln Leiter der Klinischen Prüfung: Prof. Dr. A. Engert Patienteninformation Phase I Studie mit AVD plus Lenalidomid
Version 3.0; Köln, den 26.07.2010 Sponsor Code: Uni-Koeln-1167 Sponsor: Universität zu Köln Leiter der Klinischen Prüfung: Prof. Dr. A. Engert Patienteninformation Phase I Studie mit AVD plus Lenalidomid
Patienteninformation
 Patienteninformation zum MS-Register der DMSG, Bundesverband e.v. Sehr geehrte Patientin, sehr geehrter Patient, wir möchten Sie um Ihre Einwilligung zur Teilnahme an dem MS-Register der DMSG, Bundesverband
Patienteninformation zum MS-Register der DMSG, Bundesverband e.v. Sehr geehrte Patientin, sehr geehrter Patient, wir möchten Sie um Ihre Einwilligung zur Teilnahme an dem MS-Register der DMSG, Bundesverband
Patienteninformation und Einverständniserklärung zur Knochenschmerztherapie mit Samarium-153-EDTMP (Quadramet )
 Kopie erhalten Patient: geb. Adresse: Sehr geehrte(r) Patient(in), aufgrund Ihrer Knochenschmerzen durch Skelettmetastasen wurde Ihnen eine Therapie mit Samarium-153-EDTMP (Quadramet ) vorgeschlagen. Was
Kopie erhalten Patient: geb. Adresse: Sehr geehrte(r) Patient(in), aufgrund Ihrer Knochenschmerzen durch Skelettmetastasen wurde Ihnen eine Therapie mit Samarium-153-EDTMP (Quadramet ) vorgeschlagen. Was
Diskussionsleitfaden für Studienteilnehmer von klinischen Studien
 Diskussionsleitfaden für Studienteilnehmer von klinischen Studien Sehr geehrte Frau [last name], / Sehr geehrter Herr [last name], vielen Dank, dass Sie sich Zeit nehmen, um über eine Teilnahme an einer
Diskussionsleitfaden für Studienteilnehmer von klinischen Studien Sehr geehrte Frau [last name], / Sehr geehrter Herr [last name], vielen Dank, dass Sie sich Zeit nehmen, um über eine Teilnahme an einer
Behandlungsprotokoll für Kinder und Jugendliche mit akuter lymphoblastischer Leukämie (ALL) nach der Therapiestudie AIEOP-BFM ALL 2009
 Behandlungsprotokoll für Kinder und Jugendliche mit akuter lymphoblastischer Leukämie (ALL) nach der Therapiestudie AIEOP-BFM ALL 2009 Liebe(r), bei Dir wurde festgestellt, dass Du eine schwere Krankheit
Behandlungsprotokoll für Kinder und Jugendliche mit akuter lymphoblastischer Leukämie (ALL) nach der Therapiestudie AIEOP-BFM ALL 2009 Liebe(r), bei Dir wurde festgestellt, dass Du eine schwere Krankheit
Patienteninformation zur klinischen Studie:
 UniversitätsKlinikum Heidelberg Universitätsklinikum Heidelberg INF 400 69120 Heidelberg Radiologische Klinik Abteilung RadioOnkologie und Strahlentherapie -Czernyklinik- Patienteninformation zur klinischen
UniversitätsKlinikum Heidelberg Universitätsklinikum Heidelberg INF 400 69120 Heidelberg Radiologische Klinik Abteilung RadioOnkologie und Strahlentherapie -Czernyklinik- Patienteninformation zur klinischen
Patienteninformation / Merkblatt
 Patienteninformation / Merkblatt Pankreaslinksresektion eine randomisierte kontrollierte Studie zum Vergleich von zwei chirugischen Techniken Distal Pancreatectomy A randomised controlled Trial to compare
Patienteninformation / Merkblatt Pankreaslinksresektion eine randomisierte kontrollierte Studie zum Vergleich von zwei chirugischen Techniken Distal Pancreatectomy A randomised controlled Trial to compare
Patienteninformation. Behandlung der akuten Promyelozytenleukämie mit Arsentrioxid (TRISENOX)
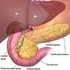 Anlage 11 Patienteninformation Behandlung der akuten Promyelozytenleukämie mit Arsentrioxid (TRISENOX) Eine Phase-IV Studie mit Arsentrioxid (ATO) zur Erfassung der Wirksamkeit und Toxizität sowie des
Anlage 11 Patienteninformation Behandlung der akuten Promyelozytenleukämie mit Arsentrioxid (TRISENOX) Eine Phase-IV Studie mit Arsentrioxid (ATO) zur Erfassung der Wirksamkeit und Toxizität sowie des
PATIENTENINFORMATION UND EINVERSTÄNDNISERKLÄRUNG für die klinische Prüfung
 PATIENTENINFORMATION UND EINVERSTÄNDNISERKLÄRUNG für die klinische Prüfung Eine historisch-kontrollierte, einarmige, multizentrische, prospektive Studie zur Untersuchung der Sicherheit und Wirksamkeit
PATIENTENINFORMATION UND EINVERSTÄNDNISERKLÄRUNG für die klinische Prüfung Eine historisch-kontrollierte, einarmige, multizentrische, prospektive Studie zur Untersuchung der Sicherheit und Wirksamkeit
PED-PTLD-Pilot 2005 Patienten-Einverständnis zur Behandlung Supplement II.5.2
 PED-PTLD-Pilot 2005 Patienten-Einverständnis zur Behandlung Supplement II.5.2 PATIENTENINFORMATION und EINVERSTÄNDNISERKLÄRUNG zur Behandlung einer Transplantations-assoziierten lymphoproliferativen Erkrankung
PED-PTLD-Pilot 2005 Patienten-Einverständnis zur Behandlung Supplement II.5.2 PATIENTENINFORMATION und EINVERSTÄNDNISERKLÄRUNG zur Behandlung einer Transplantations-assoziierten lymphoproliferativen Erkrankung
Informationsbroschüre für Patienten
 Haben Sie Gedächtnisprobleme? Schwierigkeiten, klar zu denken? Wenn das auf Sie oder auf jemanden in Ihrem Bekanntenkreis zutrifft, dann ziehen Sie bitte eine Teilnahme an der EMERGE- Studie in Betracht
Haben Sie Gedächtnisprobleme? Schwierigkeiten, klar zu denken? Wenn das auf Sie oder auf jemanden in Ihrem Bekanntenkreis zutrifft, dann ziehen Sie bitte eine Teilnahme an der EMERGE- Studie in Betracht
WICHTIGE INFORMATIONEN FÜR PATIENTEN
 WICHTIGE INFORMATIONEN FÜR PATIENTEN denen STELARA zur Behandlung der mittelschweren bis schweren Plaque-Psoriasis bzw. aktiven psoriatischen Arthritis verschrieben wurde 2 Version 5 (Stand: Februar 2017)
WICHTIGE INFORMATIONEN FÜR PATIENTEN denen STELARA zur Behandlung der mittelschweren bis schweren Plaque-Psoriasis bzw. aktiven psoriatischen Arthritis verschrieben wurde 2 Version 5 (Stand: Februar 2017)
MPN PATIENTENTAG AM KLINIKUM RECHTS DER ISAR
 MPN PATIENTENTAG AM KLINIKUM RECHTS DER ISAR PATIENTENINFORMATION IM FOKUS: - DIE MPN ERKRANKUNGEN - VERSORGUNGSSTRUKTUREN AM KLINIKUM RD ISAR GLIEDERUNG Was sind Myeloproliferative Neoplasien (MPN)? Wie
MPN PATIENTENTAG AM KLINIKUM RECHTS DER ISAR PATIENTENINFORMATION IM FOKUS: - DIE MPN ERKRANKUNGEN - VERSORGUNGSSTRUKTUREN AM KLINIKUM RD ISAR GLIEDERUNG Was sind Myeloproliferative Neoplasien (MPN)? Wie
Erläuterungen zur Einwilligungserklärung mit zusätzlicher Blutentnahme
 Erläuterungen zur Einwilligungserklärung mit zusätzlicher Blutentnahme Leisten Sie einen Beitrag zur medizinischen Forschung Liebe Patientin, Lieber Patient Dank der medizinischen Forschung leisten die
Erläuterungen zur Einwilligungserklärung mit zusätzlicher Blutentnahme Leisten Sie einen Beitrag zur medizinischen Forschung Liebe Patientin, Lieber Patient Dank der medizinischen Forschung leisten die
Sie stehen nun vor der Entscheidung, an einer weiteren Studie teilzunehmen, die begleitend zu den o.g. Studien durchgeführt wird.
 Patienteninformation 1 PATIENTENINFORMATION Multizentrische randomisierte Phase-III-Studie zur Bestimmung von Effektivität und Sicherheit von Rasburicase (Fasturtec ) im Vergleich zu Allopurinol zur Behandlung
Patienteninformation 1 PATIENTENINFORMATION Multizentrische randomisierte Phase-III-Studie zur Bestimmung von Effektivität und Sicherheit von Rasburicase (Fasturtec ) im Vergleich zu Allopurinol zur Behandlung
Herkunft Blutstammzellen Arbeitsblatt
 Lehrerinformation 1/5 Arbeitsauftrag Die Sch erfahren, auf welche Art man Menschen helfen kann (Transplantation). Die Sch lösen das, welches die Abläufe beschreibt und visuell darstellt. Ziel Die Sch erklären
Lehrerinformation 1/5 Arbeitsauftrag Die Sch erfahren, auf welche Art man Menschen helfen kann (Transplantation). Die Sch lösen das, welches die Abläufe beschreibt und visuell darstellt. Ziel Die Sch erklären
WICHTIGE INFORMATIONEN FÜR PATIENTEN. denen STELARA zur Behandlung des mittelschweren bis schweren aktiven Morbus Crohn verschrieben wurde
 WICHTIGE INFORMATIONEN FÜR PATIENTEN denen STELARA zur Behandlung des mittelschweren bis schweren aktiven Morbus Crohn verschrieben wurde 2 Version 2 (Stand: Februar 2017) Erstellt in Abstimmung mit dem
WICHTIGE INFORMATIONEN FÜR PATIENTEN denen STELARA zur Behandlung des mittelschweren bis schweren aktiven Morbus Crohn verschrieben wurde 2 Version 2 (Stand: Februar 2017) Erstellt in Abstimmung mit dem
Autoimmun-Lymphoproliferatives Syndrom (ALPS)
 CC CI C Centrum für Chronische Immundefizienz Autoimmun-Lymphoproliferatives Syndrom (ALPS) 1. ALPS - was ist das? 2. Wie häufig ist die Erkrankung? 3. Was sind die Ursachen der Erkrankung? 4. Ist es eine
CC CI C Centrum für Chronische Immundefizienz Autoimmun-Lymphoproliferatives Syndrom (ALPS) 1. ALPS - was ist das? 2. Wie häufig ist die Erkrankung? 3. Was sind die Ursachen der Erkrankung? 4. Ist es eine
Offene (konventionelle) versus laparoskopische Magenresektion beim Magenkarzinom
 Patienteninformation Offene (konventionelle) versus laparoskopische Magenresektion beim Magenkarzinom Sehr geehrte, liebe Patientin, sehr geehrter, lieber Patient, ihr behandelnder Chirurg hat Sie bereits
Patienteninformation Offene (konventionelle) versus laparoskopische Magenresektion beim Magenkarzinom Sehr geehrte, liebe Patientin, sehr geehrter, lieber Patient, ihr behandelnder Chirurg hat Sie bereits
Patienteninformation und Einverständniserklärung zur Teilnahme an der ARPKD Registerstudie ARegPKD
 Patienteninformation und Einverständniserklärung zur Teilnahme an der ARPKD Registerstudie ARegPKD Registerleitung: Stellvertreter: Dr. med. Max C. Liebau Dr. med. Markus Feldkötter Kinderklinik Zentrum
Patienteninformation und Einverständniserklärung zur Teilnahme an der ARPKD Registerstudie ARegPKD Registerleitung: Stellvertreter: Dr. med. Max C. Liebau Dr. med. Markus Feldkötter Kinderklinik Zentrum
Weiterverwendung von Patientendaten und biologischen Proben für die Forschung
 Forschungskommission KSW Weiterverwendung von Patientendaten und biologischen Proben für die Forschung Sehr geehrte Patientin Sehr geehrter Patient Die Erkennung und Behandlung von Krankheiten hat in den
Forschungskommission KSW Weiterverwendung von Patientendaten und biologischen Proben für die Forschung Sehr geehrte Patientin Sehr geehrter Patient Die Erkennung und Behandlung von Krankheiten hat in den
Einwilligungserklärung zur Teilnahme an der Studie. Intelligenzminderung und syndromale Krankheitsbilder mit Mutationen im SWI/SNF-Komplex"
 Institut für Humangenetik Universitätsklinikum Düsseldorf Universitätsstr. 1, Gebäue 23.12.03, 40225 Düsseldorf Prof. Dr. med. Dagmar Wieczorek Telefon: +49 211 81 12350 Telefax: +49 211 81 12538 E-Mail:
Institut für Humangenetik Universitätsklinikum Düsseldorf Universitätsstr. 1, Gebäue 23.12.03, 40225 Düsseldorf Prof. Dr. med. Dagmar Wieczorek Telefon: +49 211 81 12350 Telefax: +49 211 81 12538 E-Mail:
Die neue Chance auf Leben. DKMS Deutsche Knochenmarkspenderdatei
 Gegen leukämie brauchen wir sie! Die neue Chance auf Leben. www.dkms.de DKMS Deutsche Knochenmarkspenderdatei kämpfen sie mit gegen Leukämie Ich stelle mir vor ich bin krank. Ein Spender wäre meine Rettung.
Gegen leukämie brauchen wir sie! Die neue Chance auf Leben. www.dkms.de DKMS Deutsche Knochenmarkspenderdatei kämpfen sie mit gegen Leukämie Ich stelle mir vor ich bin krank. Ein Spender wäre meine Rettung.
Patienteninformation Teil 2 Untersuchung der Erbsubstanz (genetische und epigenetische Untersuchung) der Blutproben für das
 Technische Universität München Leiter des Forschungsvorhaben Univ.-Prof. Dr. Wolfgang Dott Direktor des Instituts für Hygiene und Umweltmedizin Pauwelsstr. 30 D 52074 Aachen Telefon (+49) 0241 80 88 385
Technische Universität München Leiter des Forschungsvorhaben Univ.-Prof. Dr. Wolfgang Dott Direktor des Instituts für Hygiene und Umweltmedizin Pauwelsstr. 30 D 52074 Aachen Telefon (+49) 0241 80 88 385
und mehr und mehr
 Modul 2 Aufgabe 1: Blutstammzellen 1. Todesursachen in der Schweiz (2010) In der folgenden Abbildung sind die häufigsten Todesursachen in der Schweiz für das Jahr 2010 aufgeführt, wie sie vom Bundesamt
Modul 2 Aufgabe 1: Blutstammzellen 1. Todesursachen in der Schweiz (2010) In der folgenden Abbildung sind die häufigsten Todesursachen in der Schweiz für das Jahr 2010 aufgeführt, wie sie vom Bundesamt
Mustertext. (Studienteilnehmer und schwangere Partnerin des Studienteilnehmers)
 Mustertext Klinische Prüfung von Arzneimitteln: Information und Einwilligungserklärung zur Nachverfolgung einer Schwangerschaft der Partnerin eines Studienteilnehmers und zur Gesundheit des Kindes (Studienteilnehmer
Mustertext Klinische Prüfung von Arzneimitteln: Information und Einwilligungserklärung zur Nachverfolgung einer Schwangerschaft der Partnerin eines Studienteilnehmers und zur Gesundheit des Kindes (Studienteilnehmer
Publikumsvortrag an der AndreasKlinik Cham Zug vom 30. Mai 2006 Leukämien bei älteren Patienten: Neue diagnostische und therapeutische Möglichkeiten
 Publikumsvortrag an der AndreasKlinik Cham Zug vom 30. Mai 2006 Leukämien bei älteren Patienten: Neue diagnostische und therapeutische Möglichkeiten PD Dr.med. Andreas Himmelmann PD Dr.med. Andreas Himmelmann
Publikumsvortrag an der AndreasKlinik Cham Zug vom 30. Mai 2006 Leukämien bei älteren Patienten: Neue diagnostische und therapeutische Möglichkeiten PD Dr.med. Andreas Himmelmann PD Dr.med. Andreas Himmelmann
Information und Einwilligung für Eltern / Erziehungsberechtige zur Durchführung genetischer Analysen bei Kindern und Jugendlichen
 Information und Einwilligung für Eltern / Erziehungsberechtige zur Durchführung genetischer Analysen bei Kindern und Jugendlichen Studienstelle: Klinik für Nephrologie Universitätsklinikum Düsseldorf Moorenstr.
Information und Einwilligung für Eltern / Erziehungsberechtige zur Durchführung genetischer Analysen bei Kindern und Jugendlichen Studienstelle: Klinik für Nephrologie Universitätsklinikum Düsseldorf Moorenstr.
Sehr geehrte Patientin! Sehr geehrter Patient!
 Univ. Klinik f. Innere Medizin LKH Graz Klinische Abteilung für Rheumatologie und Immunologie Univ. Prof. Dr. W. Graninger Auenbruggerplatz 15, A-8036 Graz Tel 0 316-385-12645 PATIENTENAUFKLÄRUNG ZUR THERAPIE
Univ. Klinik f. Innere Medizin LKH Graz Klinische Abteilung für Rheumatologie und Immunologie Univ. Prof. Dr. W. Graninger Auenbruggerplatz 15, A-8036 Graz Tel 0 316-385-12645 PATIENTENAUFKLÄRUNG ZUR THERAPIE
Einfluss der Lymphombehandlung auf das Blut. Michael Gregor Abteilung für Hämatologie Kantonsspital Luzern
 Einfluss der Lymphombehandlung auf das Blut Michael Gregor Abteilung für Hämatologie Kantonsspital Luzern Zusammensetzung des Blutes Blutgefäss Erythrozyten Blutkörperchen (Zellen) Blutflüssigkeit (Plasma)
Einfluss der Lymphombehandlung auf das Blut Michael Gregor Abteilung für Hämatologie Kantonsspital Luzern Zusammensetzung des Blutes Blutgefäss Erythrozyten Blutkörperchen (Zellen) Blutflüssigkeit (Plasma)
AMGEVITA (Adalimumab)
 AMGEVITA (Adalimumab) Patientenpass für Ihr Kind behördlich genehmigtes Schulungsmaterial Dieser Pass enthält wichtige Sicherheitsinformationen über AMGEVITA. Alle, die an der medizinischen Versorgung
AMGEVITA (Adalimumab) Patientenpass für Ihr Kind behördlich genehmigtes Schulungsmaterial Dieser Pass enthält wichtige Sicherheitsinformationen über AMGEVITA. Alle, die an der medizinischen Versorgung
Patienteninformation zur Behandlung der Psoriasis mit Methotrexat
 Praxis Dr. Ralph von Kiedrowski Patienteninformation zur Behandlung der Psoriasis mit Methotrexat Liebe Patientin, lieber Patient, dieses Informationsblatt soll Ihnen die vorgesehene Behandlung mit Methotrexat
Praxis Dr. Ralph von Kiedrowski Patienteninformation zur Behandlung der Psoriasis mit Methotrexat Liebe Patientin, lieber Patient, dieses Informationsblatt soll Ihnen die vorgesehene Behandlung mit Methotrexat
RoACTEMRA (Tocilizumab) Patientenpass
 RoACTEMRA (Tocilizumab) Patientenpass Dieser Patientenpass ist eine Auflage im Rahmen der Zulassung von RoACTEMRA und enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/gesetzliche
RoACTEMRA (Tocilizumab) Patientenpass Dieser Patientenpass ist eine Auflage im Rahmen der Zulassung von RoACTEMRA und enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/gesetzliche
Bitte ergänzen Sie diese Seite mit Ihrem zentrumsspezifischen Briefbogen und füllen Sie alle Leerstellen im Dokument mit den entsprechenden Angaben
 Information und Einwilligung für die Einlagerung von Blutproben für die Zentrallabore und deren weitere Verwendung (CLLR3-Studie der DCLLSG, Sponsor ist das Städtische Klinikum München GmbH) Version 2.0
Information und Einwilligung für die Einlagerung von Blutproben für die Zentrallabore und deren weitere Verwendung (CLLR3-Studie der DCLLSG, Sponsor ist das Städtische Klinikum München GmbH) Version 2.0
Leukämie. weißes Blut, Blutkrebs. bösartige Erkrankung der weißen Blutkörperchen
 Leukämie weißes Blut, Blutkrebs bösartige Erkrankung der weißen Blutkörperchen Genetische Veränderungen der Stammzellen durch folgende Risikofaktoren: radioaktive Strahlung (Hiroshima und Nagasaki) Röntgenstrahlung
Leukämie weißes Blut, Blutkrebs bösartige Erkrankung der weißen Blutkörperchen Genetische Veränderungen der Stammzellen durch folgende Risikofaktoren: radioaktive Strahlung (Hiroshima und Nagasaki) Röntgenstrahlung
RoACTEMRA (Tocilizumab) i.v. und s.c. Patientenpass
 RoACTEMRA (Tocilizumab) i.v. und s.c. Patientenpass Dieser Patientenpass enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/ Erziehungsberechtigte Bescheid wissen müssen, bevor,
RoACTEMRA (Tocilizumab) i.v. und s.c. Patientenpass Dieser Patientenpass enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/ Erziehungsberechtigte Bescheid wissen müssen, bevor,
- Patienteninformation / Merkblatt. Sehr geehrte Patientin, sehr geehrter Patient,
 Universitätsklinikum Chirurgische Klinik SDGC Im Neuenheimer Feld 110 69120 Heidelberg PORTAS-3: Multizentrische, randomisierte, kontrollierte Studie (RCT) zum Vergleich der Komplikationsraten der offenen
Universitätsklinikum Chirurgische Klinik SDGC Im Neuenheimer Feld 110 69120 Heidelberg PORTAS-3: Multizentrische, randomisierte, kontrollierte Studie (RCT) zum Vergleich der Komplikationsraten der offenen
AMLSG Amendment Nr. 3 vom zur Version der Protokollanhänge vom
 Studie: Randomisierte Phase II-Studie zu All-trans-Retinsäure bei der Induktions- und Konsolidierungstherapie sowie Pegfilgrastim in der Konsolidierungstherapie bei jüngeren Patienten mit neu diagnostizierter
Studie: Randomisierte Phase II-Studie zu All-trans-Retinsäure bei der Induktions- und Konsolidierungstherapie sowie Pegfilgrastim in der Konsolidierungstherapie bei jüngeren Patienten mit neu diagnostizierter
Elterninformation zum Pulsoxymetrie- Screening bei Neugeborenen Warum wird für Neugeborene eine Untersuchung auf schwere Herzfehler angeboten?
 Elterninformation zum Pulsoxymetrie- Screening bei Neugeborenen Warum wird für Neugeborene eine Untersuchung auf schwere Herzfehler angeboten? Liebe Eltern, im Verlauf der Schwangerschaft und in den ersten
Elterninformation zum Pulsoxymetrie- Screening bei Neugeborenen Warum wird für Neugeborene eine Untersuchung auf schwere Herzfehler angeboten? Liebe Eltern, im Verlauf der Schwangerschaft und in den ersten
Patienteninformation
 Patienteninformation Bitte lesen Sie den folgenden Text sorgfältig, bevor Sie eine Entscheidung treffen. Wenn Sie etwas nicht verstehen, fragen Sie bitte den für Sie zuständigen Prüfarzt. Sehr geehrte
Patienteninformation Bitte lesen Sie den folgenden Text sorgfältig, bevor Sie eine Entscheidung treffen. Wenn Sie etwas nicht verstehen, fragen Sie bitte den für Sie zuständigen Prüfarzt. Sehr geehrte
Blutstammzell-Transplantation
 Informationen zusammengestellt in Anstimmung mit Frau Dr. Johanna Tischer, Oberärztin an der Medizinischen Klinik und Poliklinik III, Klinikum der Universität München, Campus Großhadern Blutstammzell-Transplantation
Informationen zusammengestellt in Anstimmung mit Frau Dr. Johanna Tischer, Oberärztin an der Medizinischen Klinik und Poliklinik III, Klinikum der Universität München, Campus Großhadern Blutstammzell-Transplantation
Typisierungsaktion Ablauf und Information für die Mitarbeiterinnen und Mitarbeiter der Firma
 Typisierungsaktion Ablauf und Information für die Mitarbeiterinnen und Mitarbeiter der Firma Mittwoch, 09.11.2016 von 09.00 16.00 Uhr beim Betriebsärztlichen Dienst Für eine möglichst rasche und fehlerfreie
Typisierungsaktion Ablauf und Information für die Mitarbeiterinnen und Mitarbeiter der Firma Mittwoch, 09.11.2016 von 09.00 16.00 Uhr beim Betriebsärztlichen Dienst Für eine möglichst rasche und fehlerfreie
Wie sich die schleichende Autoimmunerkrankung kontrollieren lässt
 Vaskulitiden wenn Blutgefäße sich entzünden Wie sich die schleichende Autoimmunerkrankung kontrollieren lässt Hamburg (24. August 2010) - Fieber, Nachtschweiß und Gewichtsverlust, rheumatische Beschwerden
Vaskulitiden wenn Blutgefäße sich entzünden Wie sich die schleichende Autoimmunerkrankung kontrollieren lässt Hamburg (24. August 2010) - Fieber, Nachtschweiß und Gewichtsverlust, rheumatische Beschwerden
Das beste Mittel gegen Blutkrebs sind Sie.
 Information zur Stammzellspende. Das beste Mittel gegen Blutkrebs sind Sie. Martin Q., registrierter Stammzellspender Ein Menschenleben zu retten ist so einfach. Friederike K., Stammzellspenderin Als registrierter
Information zur Stammzellspende. Das beste Mittel gegen Blutkrebs sind Sie. Martin Q., registrierter Stammzellspender Ein Menschenleben zu retten ist so einfach. Friederike K., Stammzellspenderin Als registrierter
AMGEVITA (Adalimumab)
 AMGEVITA (Adalimumab) Patientenpass behördlich genehmigtes Schulungsmaterial Dieser Pass enthält wichtige Sicherheitsinformationen über AMGEVITA. Alle, die an Ihrer medizinischen Versorgung beteiligt sind,
AMGEVITA (Adalimumab) Patientenpass behördlich genehmigtes Schulungsmaterial Dieser Pass enthält wichtige Sicherheitsinformationen über AMGEVITA. Alle, die an Ihrer medizinischen Versorgung beteiligt sind,
SPENDE VON HÄMATOPOETISCHEN STAMMZELLEN (HSZ) EINE HOFFNUNG AUF LEBEN
 IN IHRER NÄHE SIE? SPENDE VON HÄMATOPOETISCHEN STAMMZELLEN (HSZ) EINE HOFFNUNG AUF LEBEN SIND SIE KOMPATIBEL? WER KANN SICH ALS POTENTIELLER SPENDER EINTRAGEN LASSEN? Jede Person zwischen 18 und 40 Jahren,
IN IHRER NÄHE SIE? SPENDE VON HÄMATOPOETISCHEN STAMMZELLEN (HSZ) EINE HOFFNUNG AUF LEBEN SIND SIE KOMPATIBEL? WER KANN SICH ALS POTENTIELLER SPENDER EINTRAGEN LASSEN? Jede Person zwischen 18 und 40 Jahren,
Sehr geehrte Patientin! Sehr geehrter Patient!
 Univ. Klinik f. Innere Medizin LKH Graz Klinische Abteilung für Rheumatologie und Immunologie Univ. Prof. Dr. W. Graninger Auenbruggerplatz 15, A-8036 Graz Tel 0 316-385-12645 PATIENTENAUFKLÄRUNG ZUR THERAPIE
Univ. Klinik f. Innere Medizin LKH Graz Klinische Abteilung für Rheumatologie und Immunologie Univ. Prof. Dr. W. Graninger Auenbruggerplatz 15, A-8036 Graz Tel 0 316-385-12645 PATIENTENAUFKLÄRUNG ZUR THERAPIE
PTT2.0 INFORMATIONSBROSCHÜRE FÜR KINDER (6-12 JAHRE)
 UniversitätsKlinikum Heidelberg Universitätsklinik für Kinder- und Jugendmedizin Abt. III Im Neuenheimer Feld 430 69120 Heidelberg PTT2.0 INFORMATIONSBROSCHÜRE FÜR KINDER (6-12 JAHRE) - Personalisierte
UniversitätsKlinikum Heidelberg Universitätsklinik für Kinder- und Jugendmedizin Abt. III Im Neuenheimer Feld 430 69120 Heidelberg PTT2.0 INFORMATIONSBROSCHÜRE FÜR KINDER (6-12 JAHRE) - Personalisierte
Informationen für Betroffene LEBEN MIT MORBUS FABRY
 Informationen für Betroffene LEBEN MIT MORBUS FABRY Morbus Fabry Bei Ihnen wurde Morbus Fabry diagnostiziert, und Sie machen sich jetzt vielleicht Gedanken, was das für Sie und Ihre Familie bedeuten mag.
Informationen für Betroffene LEBEN MIT MORBUS FABRY Morbus Fabry Bei Ihnen wurde Morbus Fabry diagnostiziert, und Sie machen sich jetzt vielleicht Gedanken, was das für Sie und Ihre Familie bedeuten mag.
Liebe Patientin, lieber Patient,
 30.8/066-09/14 Liebe Patientin, lieber Patient, wir freuen uns, dass Sie sich für das TK-Angebot Besondere ambulante ärztliche Versorgung interessieren. Hier erfahren Sie mehr darüber und wie Sie daran
30.8/066-09/14 Liebe Patientin, lieber Patient, wir freuen uns, dass Sie sich für das TK-Angebot Besondere ambulante ärztliche Versorgung interessieren. Hier erfahren Sie mehr darüber und wie Sie daran
Leukämie (CML) Was ist Chronische Myeloische Leukämie? Download. Published on Novartis Austria (https://www.novartis.at)
 Published on Novartis Austria (https://www.novartis.at) Home > Printer-friendly PDF > Leukämie (CML) Leukämie (CML) Was ist Chronische Myeloische Leukämie? Die chronische myeloische Leukämie (CML) ist
Published on Novartis Austria (https://www.novartis.at) Home > Printer-friendly PDF > Leukämie (CML) Leukämie (CML) Was ist Chronische Myeloische Leukämie? Die chronische myeloische Leukämie (CML) ist
Was wird in diesem Register untersucht? Im Rahmen des Registers Sichelzellkrankheit werden folgende Fragen zur Sichelzellkrankheit untersucht:
 Liebe Sorgeberechtigte, Ihr Kind ist von der Sichelzellkrankheit betroffen. Der Verlauf dieser angeborenen Bluterkrankung ist schwer vorherzusagen. Grundsätzlich können aber alle Organe durch diese Krankheit
Liebe Sorgeberechtigte, Ihr Kind ist von der Sichelzellkrankheit betroffen. Der Verlauf dieser angeborenen Bluterkrankung ist schwer vorherzusagen. Grundsätzlich können aber alle Organe durch diese Krankheit
Patienteninformation zur Behandlung der Psoriasis mit Ustekinumab
 Praxis Dr. Ralph von Kiedrowski Patienteninformation zur Behandlung der Psoriasis mit Ustekinumab Liebe Patientin, lieber Patient, dieses Informationsblatt soll Ihnen die vorgesehene Behandlung mit Ustekinumab
Praxis Dr. Ralph von Kiedrowski Patienteninformation zur Behandlung der Psoriasis mit Ustekinumab Liebe Patientin, lieber Patient, dieses Informationsblatt soll Ihnen die vorgesehene Behandlung mit Ustekinumab
Patienteninformation. Blutserum IR-Spektroskopie zur Diagnose der Hereditären Hämorrhagischen Teleangiektasie
 PD Dr. rer. nat. Andreas Lux Institut für Molekular- und Zellbiologie Hochschule Mannheim, Paul-Wittsackstr. 10, 68163 Mannheim fon 0621-2926537 fax 0621-2926420 mobil 0157-74233028 e-mail: A.Lux@hs-mannheim.de
PD Dr. rer. nat. Andreas Lux Institut für Molekular- und Zellbiologie Hochschule Mannheim, Paul-Wittsackstr. 10, 68163 Mannheim fon 0621-2926537 fax 0621-2926420 mobil 0157-74233028 e-mail: A.Lux@hs-mannheim.de
Was wird in diesem Register untersucht? Im Rahmen des Registers Sichelzellkrankheit werden folgende Fragen zur Sichelzellkrankheit untersucht:
 Liebe Patientin, lieber Patient, Du bist von der Sichelzellkrankheit betroffen. Der Verlauf dieser angeborenen Bluterkrankung ist schwer vorherzusagen. Grundsätzlich können aber alle Organe durch diese
Liebe Patientin, lieber Patient, Du bist von der Sichelzellkrankheit betroffen. Der Verlauf dieser angeborenen Bluterkrankung ist schwer vorherzusagen. Grundsätzlich können aber alle Organe durch diese
PATIENTENINFORMATION. Nationales Klinisches Amyloidose-Register
 UniversitätsKlinikum Heidelberg Medizinische Klinik Universitätsklinikum Heidelberg Im Neuenheimer Feld 410 69120 Heidelberg Medizinische Klinik (Krehl-Klinik) Abteilung Innere Medizin V Hämatologie, Onkologie
UniversitätsKlinikum Heidelberg Medizinische Klinik Universitätsklinikum Heidelberg Im Neuenheimer Feld 410 69120 Heidelberg Medizinische Klinik (Krehl-Klinik) Abteilung Innere Medizin V Hämatologie, Onkologie
PatientInneninformation 1 und Einwilligungserklärung zur Teilnahme an der klinischen Studie
 PatientInneninformation 1 und Einwilligungserklärung zur Teilnahme an der klinischen Studie Der Einfluss von kontrollierter Bewegung und balneologischer Therapie bei PatientInnen mit chronischen unspezifischen
PatientInneninformation 1 und Einwilligungserklärung zur Teilnahme an der klinischen Studie Der Einfluss von kontrollierter Bewegung und balneologischer Therapie bei PatientInnen mit chronischen unspezifischen
PatientInneninformation zum Projekt
 PatientInneninformation zum Projekt Erstellung eines gesamtösterreichischen Registers zur Erfassung der Familiären Hypercholesterinämie Pilotprojekt Wien, Graz und Innsbruck 1 von5 Lieber Patient, liebe
PatientInneninformation zum Projekt Erstellung eines gesamtösterreichischen Registers zur Erfassung der Familiären Hypercholesterinämie Pilotprojekt Wien, Graz und Innsbruck 1 von5 Lieber Patient, liebe
Information für die Eltern (Personensorgeberechtigte) zur Vorbereitung der mündlichen Aufklärung für die Reihenuntersuchung.
 Information für die Eltern (Personensorgeberechtigte) zur Vorbereitung der mündlichen Aufklärung für die Reihenuntersuchung auf Mukoviszidose Liebe Eltern, zeitgleich mit dem erweiterten Neugeborenen-
Information für die Eltern (Personensorgeberechtigte) zur Vorbereitung der mündlichen Aufklärung für die Reihenuntersuchung auf Mukoviszidose Liebe Eltern, zeitgleich mit dem erweiterten Neugeborenen-
Behandlung mit. was Sie darüber wissen müssen
 Information für Patienten, denen Volibris verschrieben wurde Behandlung mit was Sie darüber wissen müssen Diese Informationsbroschüre ist verpflichtender Teil der Zulassung um sicherzustellen, dass Angehörige
Information für Patienten, denen Volibris verschrieben wurde Behandlung mit was Sie darüber wissen müssen Diese Informationsbroschüre ist verpflichtender Teil der Zulassung um sicherzustellen, dass Angehörige
Weiterverwendung von Patientendaten
 FORSCHUNGSKOMMISSION KSW KANTONSSPITAL WINTERTHUR Brauerstrasse 15 Postfach 834 8401 Winterthur Tel. 052 266 21 21 info@ksw.ch www.ksw.ch Weiterverwendung von Patientendaten Kontakt Zentrale Studienkoordination
FORSCHUNGSKOMMISSION KSW KANTONSSPITAL WINTERTHUR Brauerstrasse 15 Postfach 834 8401 Winterthur Tel. 052 266 21 21 info@ksw.ch www.ksw.ch Weiterverwendung von Patientendaten Kontakt Zentrale Studienkoordination
Patienteninformation und Einwilligungserklärung zur Teilnahme an der klinischen Prüfung
 Patienteninformation und Einwilligungserklärung zur Teilnahme an der klinischen Prüfung EINE RANDOMISIERTE, MULTIZENTRISCHE, PROSPEKTIVE, BEOBACHTER UND PATIENTEN VERBLINDETE STUDIE ZUR BEURTEILUNG VON
Patienteninformation und Einwilligungserklärung zur Teilnahme an der klinischen Prüfung EINE RANDOMISIERTE, MULTIZENTRISCHE, PROSPEKTIVE, BEOBACHTER UND PATIENTEN VERBLINDETE STUDIE ZUR BEURTEILUNG VON
in vivo -- Das Magazin der Deutschen Krebshilfe vom
 Seite 1/5 in vivo -- Das Magazin der Deutschen Krebshilfe vom 15.12.2009 Expertengespräch zum Thema Leukämie Dr. Karl-Anton Kreuzer ist heute bei uns. Schön, dass Sie zu uns gekommen sind. Schönen guten
Seite 1/5 in vivo -- Das Magazin der Deutschen Krebshilfe vom 15.12.2009 Expertengespräch zum Thema Leukämie Dr. Karl-Anton Kreuzer ist heute bei uns. Schön, dass Sie zu uns gekommen sind. Schönen guten
Prospektive Phase-I/II-Studie zur Therapie mit Capecitabin, Mitomycin C und Oxaliplatin beim fortgeschrittenen Ösophaguskarzinom (CAMOXA-Studie)
 Prospektive Phase-I/II-Studie zur Therapie mit Capecitabin, Mitomycin C und Oxaliplatin beim fortgeschrittenen Ösophaguskarzinom (CAMOXA-Studie) Patienteninformation Prüfzentrum (Name, Anschrift): Prüfarzt
Prospektive Phase-I/II-Studie zur Therapie mit Capecitabin, Mitomycin C und Oxaliplatin beim fortgeschrittenen Ösophaguskarzinom (CAMOXA-Studie) Patienteninformation Prüfzentrum (Name, Anschrift): Prüfarzt
Patienteninformation
 Patienteninformation Prüfzentrum (Name, Anschrift): Prüfarzt (Name/Telefon): Studienzentrale (Anschrift/Telefon): Studienleiter: Prof. Dr. med. M. Gregor, Universitätsklinikum Tübingen Dokumentationsassistentin:
Patienteninformation Prüfzentrum (Name, Anschrift): Prüfarzt (Name/Telefon): Studienzentrale (Anschrift/Telefon): Studienleiter: Prof. Dr. med. M. Gregor, Universitätsklinikum Tübingen Dokumentationsassistentin:
in vivo -- Das Magazin der Deutschen Krebshilfe vom
 Seite 1/5 in vivo -- Das Magazin der Deutschen Krebshilfe vom 10.03.2009 Expertengespräch zum Thema Plasmozytom Wir haben ihn eben schon im Film gesehen zusammen mit Wolfgang S., heute ist er hier: Prof.
Seite 1/5 in vivo -- Das Magazin der Deutschen Krebshilfe vom 10.03.2009 Expertengespräch zum Thema Plasmozytom Wir haben ihn eben schon im Film gesehen zusammen mit Wolfgang S., heute ist er hier: Prof.
ChroPacStudie. zum Vergleich von zwei chirurgischen Techniken bei chronischer Bauchspeicheldrüsenentzündung
 ChroPac- eine randomisierte, kontrollierte multizentrische Studie zum Vergleich von zwei chirurgischen Techniken bei chronischer Bauchspeicheldrüsenentzündung ChroPac-Duodenum preserving head resection
ChroPac- eine randomisierte, kontrollierte multizentrische Studie zum Vergleich von zwei chirurgischen Techniken bei chronischer Bauchspeicheldrüsenentzündung ChroPac-Duodenum preserving head resection
Klinikum der Universität München
 Patienteninformation Patienten-Aufklärungsbogen zur Studie Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen wurde eine bösartige Erkrankung des Lymphsystems ein sogenanntes Non- Hodgkin-Lymphom
Patienteninformation Patienten-Aufklärungsbogen zur Studie Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen wurde eine bösartige Erkrankung des Lymphsystems ein sogenanntes Non- Hodgkin-Lymphom
Informationsbroschüre HLA-Typisierung
 Informationsbroschüre HLA-Typisierung Stammzellspender oder Spender von Blutplättchen Informationsbroschüre HLA-Typisierung Einleitung 3 Warum eine Stammzelltransplantation? 3 Warum Blutplättchenspender?
Informationsbroschüre HLA-Typisierung Stammzellspender oder Spender von Blutplättchen Informationsbroschüre HLA-Typisierung Einleitung 3 Warum eine Stammzelltransplantation? 3 Warum Blutplättchenspender?
