Zusammenfassung der Merkmale des Arzneimittels 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
|
|
|
- Frida Wagner
- vor 6 Jahren
- Abrufe
Transkript
1 Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Hydal 2 mg/ml Injektionslösung Hydal 10 mg/ml Injektionslösung Hydal 20 mg/ml Injektionslösung Hydal 50 mg/ml Injektionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Hydal 2 mg/ml Injektionslösung: 1 Ampulle enthält 2 mg Hydromorphonhydrochlorid (entsprechend 1,77 mg Hydromorphon) in 1 ml Injektionslösung. Hilfsstoff: 1 ml enthält 0,153 mmol Natrium (3,52 mg/ml Natrium) Hydal 10 mg/ml Injektionslösung: 1 Ampulle enthält 10 mg Hydromorphonhydrochlorid (entsprechend 8,87 mg Hydromorphon) in 1 ml Injektionslösung. Hilfsstoff: 1 ml enthält 0,128 mmol Natrium (2,94 mg/ml Natrium) Hydal 20 mg/ml Injektionslösung: 1 Ampulle enthält 20 mg Hydromorphonhydrochlorid (entsprechend 17,73 mg Hydromorphon) in 1 ml Injektionslösung. Hilfsstoff: 1 ml enthält 0,105 mmol Natrium (2,41 mg/ml Natrium) Hydal 50 mg/ml Injektionslösung: 1 Ampulle enthält 50 mg Hydromorphonhydrochlorid (entsprechend 44,33 mg Hydromorphon) in 1 ml Injektionslösung. Hilfsstoff: 1 ml enthält 0,040 mmol Natrium (0,92 mg/ml Natrium) Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt DARREICHUNGSFORM Lösung zur Injektion oder Infusion. Klare, farblose bis leicht gelbliche Lösung, ph-wert 4.0
2 4. KLINISCHE ANGABEN 4.1 Anwendungsgebiete Behandlung von starken Schmerzen. 4.2 Dosierung, Art und Dauer der Anwendung Art der Anwendung: Zur subkutanen Injektion oder Infusion bzw. zur intravenösen Injektion oder Infusion. Optische Kontrollen sollen vor der Anwendung und nach der Verdünnung durchgeführt werden. Es dürfen ausschließlich klare, annähernd partikelfreie Lösungen verwendet werden. Die Injektionslösung soll sofort nach dem Öffnen verabreicht werden. Unverbrauchte Reste müssen verworfen werden. Dosierung: Die Dosis von Hydal ist abhängig von der Stärke der Schmerzen und dem individuellen Ansprechen des Patienten auf die Schmerztherapie. Die Dosis sollte bis zur optimalen analgetischen Wirkung titriert werden. Grundsätzlich sollte eine ausreichend hohe Dosis gegeben werden. Im Einzelfall sollte die niedrigste analgetisch wirksame Dosis angestrebt werden. Hydal 10 mg/ml, 20 mg/ml und 50 mg/ml sind für die initiale Opioidtherapie nicht geeignet. Diese stärkeren Arzneiformen dürfen nur zur individuellen Dosierung bei Patienten, für die niedrigere Stärken von Hydromorphon-Zubereitungen wie etwa Hydal 2 mg/ml oder vergleichbar starke Analgetika aus dem Bereich der chronischen Schmerztherapie nicht ausreichen, angewendet werden. Das Reservoir einer Schmerzpumpe kann auch mit individuellen Dosierungen von 10 mg/ml, 20 mg/ml oder 50 mg/ml befüllt werden, da die Kalibrierung der Schmerzpumpe die Kontrolle der Dosierung sicher stellt. Hydal sollte nicht länger als unbedingt notwendig verabreicht werden. Wenn eine Langzeitbehandlung erforderlich ist, sollte durch eine sorgfältige und regelmäßige Überprüfung sichergestellt werden, ob und in welchem Ausmaß eine Weiterbehandlung notwendig ist. Falls eine Opioid-Therapie nicht länger angezeigt ist, kann es ratsam sein, die Tagesdosis allmählich zu reduzieren, um das Auftreten von Entzugssymptomen zu vermeiden.
3 Alter Bolus Infusion Erwachsene und Jugendliche (> 12 Jahre) Subkutane Anwendung (s.c.) 1-2 mg s.c. alle 3-4 Stunden 0,15-0,45 mg/stunde bzw. 0,004 mg/kg Intravenöse Anwendung (i.v.) PCA (s.c. und i.v.) 1-1,5 mg i.v. alle 3-4 Stunden, langsam über mindestens 2-3 Minuten injizieren Kinder (<12 Jahre) Nicht empfohlen 0,2 mg Bolus bei einem Sperrintervall von 5-10 min Körpergewicht/Stunde 0,15-0,45 mg/stunde bzw. 0,004 mg/kg Körpergewicht/Stunde Umstellung von oraler Einnahme auf parenterale Anwendung von Hydromorphon: Die Tagesdosis soll wie folgt berechnet werden: 3 mg Hydromorphon oral entspricht 1 mg Hydromorphon intravenös. Es wird betont, dass es sich dabei um eine Empfehlung zur Dosiseinstellung handelt. Aufgrund individuellen Ansprechens wird bei jedem Patienten eine sorgfältige Dosistitration empfohlen. Kinder unter 12 Jahre: Hydal Injektionslösung wird nicht empfohlen für die Anwendung bei Kindern unter 12 Jahren aufgrund nicht ausreichender Daten zur Unbedenklichkeit und Wirksamkeit. Ältere Patienten: Bei älteren Patienten (im Regelfall über 75 Jahre) kann eventuell mit einer geringeren Dosierung eine ausreichende Analgesie erzielt werden. Patienten mit Einschränkung der Nieren- und/oder Leberfunktion: Bei diesen Patienten kann eine geringere Dosis zur adäquaten Schmerzlinderung ausreichend sein. Deshalb sollte bei diesen Patienten die Dosierung anfänglich vorsichtig erfolgen (siehe Abschnitt 5.2). 4.3 Gegenanzeigen Überempfindlichkeit gegenüber Hydromorphon oder einem der Hilfsstoffe Schwere Atemdepression mit Hypoxie oder Hyperkapnie schwere chronische obstruktive Atemwegserkrankung Cor pulmonale Koma akutes Abdomen paralytischer Ileus gleichzeitige Therapie mit Monoaminoxidase-Hemmern oder innerhalb von 2 Wochen nach deren Absetzen 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung Das Hauptrisiko der Opioid-Überdosierung ist eine Atemdepression. Vorsicht ist geboten bei opiatabhängigen Patienten, bei Patienten mit Kopfverletzungen (da ein Risiko eines erhöhten Hirndruckes besteht), konvulsiven Erkrankungen, Alkoholismus, Delirium tremens, bei Patienten mit toxischer
4 Psychose, Hypotonie mit Hypovolämie, Bewusstseinsstörungen, Gallenwegserkrankungen, Gallen- oder Harnleiterkoliken, Pankreatitis, obstruktiven und entzündlichen Darmerkrankungen, Prostatahyperplasie, Nebennierenrindeninsuffizienz (z.b. Addison Syndrom), Hypothyreose, chronisch obstruktiven Atemwegserkrankungen, verminderter Atemreserve, bei Kindern unter 12 Jahren, bei geschwächten älteren oder gebrechlichen Patienten und bei Patienten mit chronischer Nieren- und Lebererkrankung (siehe Abschnitt 4.2). Bei diesen Patienten, kann eine Dosisreduktion ratsam sein. Bei Langzeitanwendung von Hydal kann sich Toleranz entwickeln, die immer höhere Dosen zur Schmerzkontrolle erfordert. Es kann auch Kreuztoleranz mit anderen Opioiden bestehen. Physische Abhängigkeit kann unter längerer Einnahme von Hydromorphon auftreten und abruptes Absetzen möglicherweise ein Entzugssyndrom hervorrufen. Langsames Ausschleichen zur Vermeidung von Entzugssymptomen kann angezeigt sein. Hydromorphon hat ein ähnliches Missbrauchprofil wie andere starke Opioidagonisten und kann von latent oder manifest Suchterkrankten bewusst missbraucht werden. Eine psychische Abhängigkeit (Arzneimittelsucht) kann sich nach Gabe opioidhaltiger Analgetika wie Hydal Injektionslösung entwickeln. Besondere Sorgfalt sollte daher bei der Behandlung von Patienten mit Alkohol- oder Drogenproblemen in der Anamnese angewendet werden. Hyperalgesie, die auf eine weitere Dosiserhöhung nicht anspricht, kann sehr selten insbesondere bei hoher Dosierung auftreten. Eine Dosisreduktion oder Opioid- Wechsel kann erforderlich sein. Bei Gefahr eines paralytischen Ileus, sollte Hydal Injektionslösung nicht angewendet werden. Sollte ein paralytischer Ileus vermutet werden oder während der Behandlung auftreten, muss die Behandlung mit Hydromorphon sofort abgebrochen werden. Hydal ist prä- und intraoperativ sowie in den ersten 24 Stunden postoperativ mit Vorsicht anzuwenden. Patienten, die einer anderen zusätzlichen Schmerztherapie (z.b. Operation, Plexusblockade) unterzogen werden, sollten 4 Stunden vor dem Eingriff kein Hydromorphon mehr erhalten. Wenn eine Weiterbehandlung mit Hydal indiziert ist, muss die Dosis nach dem Eingriff neu eingestellt werden. Es muss betont werden, dass Patienten, deren wirksame Dosis eines bestimmten Opioids durch Titration bestimmt worden ist, nicht ohne erneute sorgfältige Dosistitration und klinische Untersuchung auf andere Opioid-Analgetika umgestellt werden dürfen, da sonst eine durchgehende Analgesie nicht gewährleistet ist. Die Anwendung von Hydromorphon kann bei Dopingkontrollen zu positiven Ergebnissen führen. Dieses Arzneimittel enthält weniger als 1 mmol Natrium (23 mg) pro 1 ml, das heißt es ist nahezu natriumfrei.
5 4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen Zentralwirksame Arzneimittel wie Tranquilizer, Anästhetika (wie z.b. Barbiturate), Hypnotika und Sedativa, Neuroleptika, Antidepressiva, Antiemetika, Antihistaminika und andere Opioide oder Alkohol können die Wirkung beider Arzneimittel, beispielsweise Sedierung, Atemdepression verstärken. Arzneimittel mit anticholinerger Wirkung (z.b. Psychopharmaka, Antiemetika, Antihistaminika, Antiparkinsonmittel) können anticholinerge Nebenwirkungen von Opioiden verstärken (z.b. Obstipation, Mundtrockenheit oder Harnretention). Die gleichzeitige Verabreichung von Monoaminooxidase-Hemmern oder innerhalb von 2 Wochen nach deren Absetzen ist kontraindiziert (siehe Abschnitt 4.3). Es wurden keine Wechselwirkungsstudien durchgeführt. 4.6 Schwangerschaft und Stillzeit Schwangerschaft Es liegen keine klinischen Daten bezüglich Exposition in der Schwangerschaft vor. Tierstudien wiesen reproduktionstoxische Wirkungen auf (siehe Abschnitt 5.3). Das potenzielle Risiko für Menschen ist nicht bekannt. Hydromorphon sollte während der Schwangerschaft nur bei eindeutiger Indikation verwendet werden. Hydal sollte nicht in der Schwangerschaft und nicht während der Geburt verwendet werden, da es die Kontraktilität des Uterus beeinträchtigt und das Risiko einer neonatalen Atemdepression erhöht. Bei Neugeborenen von Müttern unter Langzeitbehandlung können Entzugserscheinungen auftreten. Stillzeit Hydromorphon geht in kleinen Mengen in die Muttermilch über. Hydal sollte daher nicht an stillende Mütter verabreicht werden. 4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen Hydromorphon kann die Verkehrstüchtigkeit und die Fähigkeit, Maschinen zu bedienen, beeinträchtigen. Dies ist insbesondere zu Beginn einer Therapie mit Hydromorphon, nach Dosiserhöhung oder Präparatewechsel sowie beim Zusammenwirken von Hydromorphon mit Alkohol oder anderen ZNS-dämpfenden Substanzen zu erwarten. Bei einer stabilen Therapie sind Beschränkungen nicht zwangsläufig erforderlich. Deshalb sollten Patienten mit ihrem behandelnden Arzt besprechen, ob sie ein Fahrzeug lenken oder Maschinen bedienen dürfen. 4.8 Nebenwirkungen Bei der Bewertung von Nebenwirkungen werden folgende Häufigkeiten zugrunde gelegt: Sehr häufig (>1/10) Häufig (>1/100, <1/10) Gelegentlich (>1/1 000, <1/100) Selten (>1/10 000, <1/1 000) Sehr selten (<1/10 000)
6 Nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar) Erkrankungen des Immunsystems Sehr selten: Überempfindlichkeitsreaktionen (einschließlich Schwellungen im Bereich des Oropharynx) Nicht bekannt: Anaphylaktische Reaktionen Stoffwechsel- und Ernährungsstörungen Häufig: Anorexie Psychiatrische Erkrankungen Häufig: Angst, Verwirrtheit, Schlaflosigkeit Gelegentlich: Depression, Dysphorie, Euphorie, Halluzinationen, Albträume Selten: Abhängigkeit, Agitiertheit Erkrankungen des Nervensystems Häufig: Schwindel, Somnolenz Gelegentlich: Kopfschmerzen, Tremor, Myoklonus, Parästhesien Selten: Konvulsionen, Sedierung Sehr selten: Hyperalgesie (siehe Abschnitt 4.4) Augenerkrankungen Gelegentlich: Miosis, Verschwommensehen Herzerkrankungen Gelegentlich: Tachykardie Selten: Bradykardie, Palpitationen Gefäßerkrankungen Häufig: Hypotonie Erkrankungen der Atemwege, des Brustkorbs und des Mediastinums Gelegentlich: Dyspnoe Selten: Atemdepression, Bronchospasmus Erkrankungen des Gastrointestinaltrakts Häufig: Obstipation, abdominale Beschwerden, Mundtrockenheit, Nausea, Erbrechen Gelegentlich: Dyspepsie, Diarrhoe, Geschmacksstörungen Sehr selten: paralytischer Ileus Leber- und Gallenerkrankungen Selten: Gallenkoliken, Erhöhung der Pankreasenzyme Sehr selten: Erhöhung hepatischer Enzyme
7 Erkrankungen der Haut und des Unterhautzellgewebes Häufig: Pruritus, Schwitzen Gelegentlich: Hautausschlag, Urtikaria Selten: Rötung des Gesichtes Erkrankungen der Nieren und Harnwege Häufig: Harnverhalten, Harndrang Erkrankungen der Geschlechtsorgane und der Brustdrüse Gelegentlich: Libido erniedrigt, erektile Dysfunktion Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Häufig: Schwächezustände, Lokalreaktionen an der Injektionsstelle Gelegentlich: Toleranz, Entzugssyndrom* Sehr selten: periphere Ödeme, Verhärtungen an der Injektionsstelle (insbesondere nach wiederholter s.c. Gabe) * Entzugssymptome wie Reizbarkeit, Angst, Nervosität, Schlaflosigkeit, Hyperkinesien, Tremor und gastrointestinale Beschwerden können auftreten. 4.9 Überdosierung Symptome einer Hydromorphonintoxikation und Überdosierung können sich durch Miosis, Bradykardie, Atemdepression, Hypotonie, fortschreitende Somnolenz bis hin zu Stupor und Koma manifestieren. Bei massiver Überdosierung können Kreislaufversagen und vertieftes Koma unter Umständen mit letalem Ausgang auftreten. Bei bewusstlosen Patienten mit Atemstillstand sind Intubation und künstliche Beatmung erforderlich. Es sollte ein Opiatantagonist (z.b. 0,4 mg Naloxon; bei Kindern 0,01 mg Naloxon/kg KG) intravenös verabreicht werden. In 2- bis 3- minütigen Abständen muss diese Einzeldosis solange wie nötig wiederholt werden. Strenge Überwachung (über mindestens 24 Stunden) ist notwendig, da die Wirkung des Opiatantagonisten kürzer als die des Hydromorphons ist und mit einem erneuten Auftreten der Überdosierungssymptome wie z. B. Ateminsuffizienz gerechnet werden muss. 5. PHARMAKOLOGISCHE EIGENSCHAFTEN 5.1 Pharmakodynamische Eigenschaften Pharmakotherapeutische Gruppe: Opioidanalgetikum, natürliche Opiumalkaloide ATC Code N02A A 03. Hydromorphon ist ein µ-selektiver, reiner Opioid-Agonist. Hydromorphon und verwandte Opioide wirken hauptsächlich auf das zentrale Nervensystem und den Darm.
8 Die therapeutische Wirkung ist hauptsächlich analgetisch, anxiolytisch, antitussiv und sedierend. Es können auch Stimmungsveränderungen, Atemdepression, verminderte gastrointestinale Motilität, Übelkeit, Erbrechen und Veränderungen des endokrinen und autonomen Nervensystems auftreten. Opioide können die Hypothalamus-Hypophysen-Nebennieren- oder Gonaden- Achsen beeinflussen. Zu den Veränderungen, die beobachtet werden können, zählen ein Anstieg des Prolaktins im Serum und eine Abnahme von Kortisol und Testosteron im Plasma. Eine Manifestation klinischer Symptome aufgrund dieser Hormonveränderungen kann möglich sein. Präklinische Studien zeigen unterschiedliche Effekte von Opioiden auf die Komponenten des Immunsystems. Die klinische Bedeutung dieser Befunde ist nicht bekannt. 5.2 Pharmakokinetische Eigenschaften Der Wirkungseintritt erfolgt nach intravenöser Verabreichung meist innerhalb der ersten 5 Minuten und nach subkutaner Verabreichung innerhalb der ersten 5-10 Minuten. Die Wirkungsdauer nach intravenöser und subkutaner Verabreichung beträgt 3-4 Stunden. Nach epiduraler Verabreichung von 1 mg Hydromorphon beobachtete man bis zur vollständigen analgetischen Wirkung eine Latenzzeit von 22,5 ± 6 Minuten. Die Wirkung hielt 9,8 ± 5,5 Stunden an (n = 84 Patienten im Alter von 22 bis 84 Jahren). Hydromorphon passiert die Plazentaschranke. Angaben über die Ausscheidung in die Muttermilch liegen nicht vor. Die Plasmaproteinbindung ist gering (< 10 %), wobei dieser Prozentsatz von 2,46 ng/ml bis zu sehr hohen Plasmaspiegeln von 81,99 ng/ml, die nur durch sehr hohe Hydromorphon-Dosen erreicht werden können, konstant bleibt. Hydromorphon weist ein relativ hohes Verteilungsvolumen von 1,22 ± 0,23 l/kg (C.I.: 90 % : 0,97 1,60 l/kg) auf (n = 6 männliche Probanden). Dies weist auf eine deutliche Gewebeaufnahme hin. Aus dem Verlauf der Plasmakonzentrations-Zeit-Kurven nach einmaliger Gabe von Hydromorphonhydrochlorid 2 mg i.v. oder 4 mg oral an 6 gesunden Probanden im randomisierten Cross-over-Versuch ergab sich eine relativ kurze Eliminationshalbwertszeit von 2,64 ± 0,88 Stunden (1,68 3,87 Stunden). Hydromorphon wird durch direkte Konjugation oder durch Reduktion der Ketogruppe mit nachfolgender Konjugation metabolisiert. Nach Resorption wird Hydromorphon hauptsächlich zu Hydromorphon-3-Glukuronid, Hydromorphon-3-Glukosid und Dihydroisomorphin-6-Glukuronid, Hydromorphon-3-Glukosid und Dihydroisomorphin- 6-Glukuronid metabolisiert. Zu einem kleineren Anteil wurden auch die Metabolite Dihydroisomorphin-6-Glykosid, Dihydromorphin und Dihydroisomorphin beobachtet. Hydromorphon wird in der Leber metabolisiert und zu einem geringen Anteil unverändert hauptsächlich renal ausgeschieden.
9 Hydromorphonmetaboliten wurden im Plasma, Urin und in humanen Hepatozyten- Test-Systemen festgestellt. Es gibt keine Hinweise darauf, dass Hydromorphon invivo durch das Cytochrom P 450-Enzymsystem metabolisiert wird. In-vitro hemmt Hydromorphon mit einer IC50>50 µm nur geringfügig die rekombinanten CYP- Isoformen, einschließlich CYP1A2, 2A6, 2C8, 2D6 und 3A4. Es ist deshalb nicht zu erwarten, dass Hydromorphon den Metabolismus von anderen Arzneistoffen, die durch diese CYP-Isoformen metabolisiert werden, inhibiert. 5.3 Präklinische Daten zur Sicherheit Nichtklinische Studienergebnisse zeigen kein spezielles Risiko für den Menschen basierend auf konventionellen Studien zur pharmakologischen Sicherheit, zur Toxizität bei wiederholter Gabe und zur Genotoxizität. Es wurde auf die männliche oder weibliche Fertilität bzw. auf die Spermien bei Ratten selbst nach 5 mg/kg/tag (30 mg/m²/tag oder das 1,4fache der erwarteten Humandosis auf die Oberfläche bezogen) von oralem Hydromorphon keine Wirkung beobachtet. Hydromorphon war bei Ratten und Kaninchen in Dosen, die im Muttertier toxisch waren, nicht teratogen. Eine verzögerte fötale Entwicklung wurde bei Ratten bei Dosen von 50 mg/kg festgestellt, die no-observed-effect-level-dosis betrug 25 mg/kg oder 380 mg/m 2 mit einer Exposition (AUC), die annähernd das 4-fache der erwarteten Humandosis ist. Es gab keinen Nachweis einer fötalen Toxizität bei Ratten, auch nicht bei Dosen von 10 mg/kg oralem Hydromorphon-Hydrochlorid (308 mg/m 2 mit einer AUC, die etwa das 1,8-fache der erwarteten Humandosis ist) zeigten die behandelten Ratten fötale Schädigungen. Die Peripartum/Postpartum-Mortalität von Rattenjungen (F1) war bei 2 und 5 mg/kg/tag erhöht und die Körpergewichte waren geringer während der Stillzeit. Langzeitstudien zur Kanzerogenität wurden nicht durchgeführt. 6. PHARMAZEUTISCHE ANGABEN 6.1 Liste der sonstigen Bestandteile Wasserfreie Citronensäure, Natriumcitrat, Natriumchlorid, Natriumhydroxid-Lösung (4 %) (zur ph-werteinstellung), Salzsäure 3,6 % (zur ph-werteinstellung) und Wasser für Injektionszwecke. 6.2 Inkompatibilitäten Dieses Arzneimittel darf nicht mit anderen Arzneimitteln vermischt werden, außer jenen, die unter Abschnitt 6.6 genannt werden. 6.3 Dauer der Haltbarkeit 3 Jahre. Nach dem Öffnen muss die Lösung sofort verwendet werden.
10 Hydal Injektionslösung, unverdünnt oder verdünnt mit 0.9 % Kochsalzlösung zur Infusion, 50 mg/ml (5 %) Dextroselösung zur Infusion oder Wasser für Injektionszwecke, ist über einen Zeitraum von 24 Stunden bei Raumtemperatur (25 C) im Kontakt mit den gebräuchlichen Markenprodukten von Polypropylen- oder Polycarbonatspritzen, Polyethylen- oder PVC-Schlauchmaterialien und PVC- oder EVA (Ethylenvinylacetat)- Infusionsbeuteln physikalisch und chemisch stabil. Aus mikrobiologischer Sicht muss Hydal Injektionslösung sofort nach dem Öffnen verabreicht werden. Bei nicht sofortiger Verabreichung obliegt die Verantwortung über die Lagerungsdauer und die Lagerungsbedingungen nach dem Öffnen dem Anwender. Im Allgemeinen sollte die Lagerungsdauer der geöffneten Ampulle nicht länger als 24 Stunden bei Raumtemperatur (25 C) erfolgen, sofern die Lösung nicht unter kontrollierten, validierten, aseptischen Bedingungen hergestellt bzw. verdünnt wurde. 6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung Die Ampullen im Umkarton aufbewahren, um sie vor Licht zu schützen. Für weitere Informationen zur Handhabung nach dem Öffnen siehe Abschnitt Art und Inhalt des Behältnisses Klare Typ 1 neutral Glasampulle zu 1 ml. Packungsgröße: je 5 Ampullen 6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise zur Handhabung Es zeigten sich keine Inkompatibilitäten bei der Aufbewahrung von Hydal Injektionslösung unverdünnt oder verdünnt mit 0.9 % Kochsalzlösung zur Infusion, 50 mg/ml (5 %) Dextroselösung zur Infusion oder Wasser für Injektionszwecke in Kombination mit den gebräuchlichen Markenprodukten parenteraler Formen der unten genannten Arzneimittel mit hoher oder niedriger Dosis, über einen Zeitraum von 24 Stunden bei Raumtemperatur in Polypropylenspritzen. Butylscopolaminbromid Scopolaminhydrobromid Dexamethasonnatriumphosphat Haloperidol Midazolamhydrochlorid Metoclopramidhydrochlorid Levomepromazinhydrochlorid Glycopyrroniumbromid Ketaminhydrochlorid Unsachgemäßer Gebrauch der unverdünnten Injektionslösung nach dem erstmaligen Öffnen der Ampulle oder der verdünnten Injektionslösung kann die Sterilität des Produktes beeinträchtigen. Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu entsorgen.
11 7. INHABER DER ZULASSUNG Mundipharma Ges.m.b.H., Wien 8. ZULASSUNGSNUMMER Hydal 2 mg/ml Injektionslösung: Hydal 10 mg/ml Injektionslösung: Hydal 20 mg/ml Injektionslösung: Hydal 50 mg/ml Injektionslösung: DATUM DER ERTEILUNG DER ZULASSUNG/VERLÄNGERUNG DER ZULASSUNG STAND DER INFORMATION 11/2010 VERSCHREIBUNGSPFLICHT/APOTHEKENPFLICHT Suchtgift, Abgabe nur auf Suchtgiftrezept, apothekenpflichtig
20 27 ½ Tablette 3mal täglich (entsprechend 15 mg Dihydrocodeinhydrogentartrat pro Tag) Kinder 9 12
 Paracodin-Tabletten 2. Qualitative und quantitative Zusammensetzung 1 Tablette enthält 10 mg Dihydrocodeinhydrogentartrat, entsprechend 6,7 mg Dihydrocodein. Die vollständige Auflistung der sonstigen Bestandteile
Paracodin-Tabletten 2. Qualitative und quantitative Zusammensetzung 1 Tablette enthält 10 mg Dihydrocodeinhydrogentartrat, entsprechend 6,7 mg Dihydrocodein. Die vollständige Auflistung der sonstigen Bestandteile
Substitol retard 120 mg-kapseln 2. Qualitative und quantitative Zusammensetzung Je 1 Kapsel enthält: Darreichungsform 120 mg: 200 mg:
 Substitol retard 120 mg-kapseln 2. Qualitative und quantitative Zusammensetzung Je 1 Kapsel enthält: 120 mg Morphinsulfat, entsprechend 90 mg Morphin. Vollständige Auflistung der sonstigen Bestandteile
Substitol retard 120 mg-kapseln 2. Qualitative und quantitative Zusammensetzung Je 1 Kapsel enthält: 120 mg Morphinsulfat, entsprechend 90 mg Morphin. Vollständige Auflistung der sonstigen Bestandteile
1. WAS IST DAFALGAN Zäpfchen UND WOFÜR WIRD ES ANGEWENDET?
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER DAFALGAN Säuglinge 80 mg Zäpfchen DAFALGAN Kleinkinder 150 mg Zäpfchen DAFALGAN große Kinder 300 mg Zäpfchen Paracetamol Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER DAFALGAN Säuglinge 80 mg Zäpfchen DAFALGAN Kleinkinder 150 mg Zäpfchen DAFALGAN große Kinder 300 mg Zäpfchen Paracetamol Lesen Sie die gesamte Packungsbeilage
Betreff: Citalopram hältige Arzneispezialitäten Änderungen der Fach- und Gebrauchsinformationen
 Datum: 15.11.2011 Kontakt: Mag. pharm. Dr. Ulrike Rehberger Abteilung: Tel. / Fax: +43(0)505 55 36258, DW.Fax-36207 E-Mail: ulrike.rehberger@ages.at Unser Zeichen: 16c-111114-23425-A-PHV Ihr Zeichen: Betreff:
Datum: 15.11.2011 Kontakt: Mag. pharm. Dr. Ulrike Rehberger Abteilung: Tel. / Fax: +43(0)505 55 36258, DW.Fax-36207 E-Mail: ulrike.rehberger@ages.at Unser Zeichen: 16c-111114-23425-A-PHV Ihr Zeichen: Betreff:
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Magnevist 2 mmol/l Injektionslösung. Gadopentetsäure, Dimeglumin
 1 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Magnevist 2 mmol/l Injektionslösung Gadopentetsäure, Dimeglumin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor dieses Arzneimittel bei
1 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Magnevist 2 mmol/l Injektionslösung Gadopentetsäure, Dimeglumin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor dieses Arzneimittel bei
Eine vollständige Auflistung der sonstigen Bestandteile finden Sie unter Abschnitt 6.1.
 1. BEZEICHNUNG DES TIERARZNEIMITTELS Butomidor 10 mg/ml Injektionslösung für Pferde, Hunde und Katzen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml enthält: Wirkstoff: Butorphanol als Tartrat Sonstige
1. BEZEICHNUNG DES TIERARZNEIMITTELS Butomidor 10 mg/ml Injektionslösung für Pferde, Hunde und Katzen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml enthält: Wirkstoff: Butorphanol als Tartrat Sonstige
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Tilidin N Lichtenstein Wirkstoffe: Tilidinhydrochlorid 50 mg in 20 Tropfen Naloxonhydrochlorid 4 mg in 20 Tropfen Für Erwachsene, Kinder ab 2 Jahre Lösung
Gebrauchsinformation: Information für Anwender Tilidin N Lichtenstein Wirkstoffe: Tilidinhydrochlorid 50 mg in 20 Tropfen Naloxonhydrochlorid 4 mg in 20 Tropfen Für Erwachsene, Kinder ab 2 Jahre Lösung
GEBRAUCHSINFORMATION
 GEBRAUCHSINFORMATION Bezeichnung Tramadol Sandoz 100 mg, Tabletten mit langfristiger Wirkung Tramadol Sandoz 150 mg, Tabletten mit langfristiger Wirkung Tramadol Sandoz 200 mg, Tabletten mit langfristiger
GEBRAUCHSINFORMATION Bezeichnung Tramadol Sandoz 100 mg, Tabletten mit langfristiger Wirkung Tramadol Sandoz 150 mg, Tabletten mit langfristiger Wirkung Tramadol Sandoz 200 mg, Tabletten mit langfristiger
Erratum Benkert, Pocket Guide, Psychopharmaka von A bis Z. 3.Aufl. ISBN (print): 978-3-642-54766-9/ DOI 10.1007/978-3-642-54767-6
 Erratum Benkert, Pocket Guide, Psychopharmaka von A bis Z. 3.Aufl. ISBN (print): 978-3-642-54766-9/ DOI 10.1007/978-3-642-54767-6 Trotz sorgfältiger Erstellung des Buchs Benkert, Pocket Guide, Psychopharmaka
Erratum Benkert, Pocket Guide, Psychopharmaka von A bis Z. 3.Aufl. ISBN (print): 978-3-642-54766-9/ DOI 10.1007/978-3-642-54767-6 Trotz sorgfältiger Erstellung des Buchs Benkert, Pocket Guide, Psychopharmaka
Kinder erhalten ca. 1/8 der Erwachsenenäquivalenzdosen. Schulkinder > Kleinkinder > Säuglinge
 Opioidanalgetika Morphinmythos das macht abhängig ist es schon so weit? viel zu gefährlich für Kinder massive Nebenwirkungen??? (schwere NW sehr selten z.b. im Vergleich zum gastrointestinalen Blutungsrisiko
Opioidanalgetika Morphinmythos das macht abhängig ist es schon so weit? viel zu gefährlich für Kinder massive Nebenwirkungen??? (schwere NW sehr selten z.b. im Vergleich zum gastrointestinalen Blutungsrisiko
PHV-issue: Naltrexon hältige Arzneispezialitäten Änderungen der Fach- und Gebrauchsinformationen aufgrund des HBD PSUR Worksharing Projektes
 Datum: 10.01.2014 Kontakt: Mag. pharm. Dr. Ulrike Rehberger Abteilung: Tel. / Fax: +43 (0) 505 55 36258, DW.Fax-36207 E-Mail: ulrike.rehberger@ages.at Unser Zeichen: 16c-140110-00003-A-PHV Ihr Zeichen:
Datum: 10.01.2014 Kontakt: Mag. pharm. Dr. Ulrike Rehberger Abteilung: Tel. / Fax: +43 (0) 505 55 36258, DW.Fax-36207 E-Mail: ulrike.rehberger@ages.at Unser Zeichen: 16c-140110-00003-A-PHV Ihr Zeichen:
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 563-TG10/5,20/10,-11/08-FI / 1 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Targin 10 mg/5 mg Retardtabletten Targin 20 mg/10 mg Retardtabletten 2. QUALITATIVE UND QUANTITATIVE
563-TG10/5,20/10,-11/08-FI / 1 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Targin 10 mg/5 mg Retardtabletten Targin 20 mg/10 mg Retardtabletten 2. QUALITATIVE UND QUANTITATIVE
FACHINFORMATION ELUDRIL N
 FACHINFORMATION ELUDRIL N ZUSAMMENSETZUNG Wirkstoffe: Chlorhexidini Digluconas. Hilfsstoffe: Propylenglycolum, Aromatica Vanillinum et alia, Color: E 124, Conserv.: Alcohol benzylicus, Excipiens ad solutionem
FACHINFORMATION ELUDRIL N ZUSAMMENSETZUNG Wirkstoffe: Chlorhexidini Digluconas. Hilfsstoffe: Propylenglycolum, Aromatica Vanillinum et alia, Color: E 124, Conserv.: Alcohol benzylicus, Excipiens ad solutionem
Atronase 0,3 mg/ml Nasenspray, Lösung (Ipratropiumbromid)
 GEBRAUCHSINFORMATION ATRONASE 0,3 MG/ML NASENSPRAY, LÖSUNG Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel ist auch ohne Verschreibung
GEBRAUCHSINFORMATION ATRONASE 0,3 MG/ML NASENSPRAY, LÖSUNG Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel ist auch ohne Verschreibung
Handelsregister: Amtsgericht Freiburg i. Br. HRB 2137
 Alcon Pharma GmbH Blankreutestraße 1 79108 Freiburg i. Br. Deutschland Telefon: 0761 1304-0 Telefax: 0761 1304-200 www.alcon.com Bankverbindung: Deutsche Bank, Freiburg i. Br. 2626588 (BLZ 68070030) IBAN:
Alcon Pharma GmbH Blankreutestraße 1 79108 Freiburg i. Br. Deutschland Telefon: 0761 1304-0 Telefax: 0761 1304-200 www.alcon.com Bankverbindung: Deutsche Bank, Freiburg i. Br. 2626588 (BLZ 68070030) IBAN:
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Legalon SIL - Trockensubstanz zur Infusionsbereitung
 PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Legalon SIL - Trockensubstanz zur Infusionsbereitung Wirkstoff: Silibinin-C-2,3-bis(hydrogensuccinat), Dinatriumsalz Lesen Sie die gesamte
PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Legalon SIL - Trockensubstanz zur Infusionsbereitung Wirkstoff: Silibinin-C-2,3-bis(hydrogensuccinat), Dinatriumsalz Lesen Sie die gesamte
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER SINUTAB 500/30 mg Tabletten SINUTAB FORTE 500/60 mg Tabletten Paracetamol und Pseudoephedrinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER SINUTAB 500/30 mg Tabletten SINUTAB FORTE 500/60 mg Tabletten Paracetamol und Pseudoephedrinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender. APOZEMA Bluthochdruck Crataegus complex Nr.10-Tropfen
 Gebrauchsinformation: Information für Anwender APOZEMA Bluthochdruck Crataegus complex Nr.10-Tropfen Wirkstoffe: Crataegus Dil. D4, Arnica Dil. D4, Aurum chloratum natronatum Dil. D5, Barium jodatum Dil.
Gebrauchsinformation: Information für Anwender APOZEMA Bluthochdruck Crataegus complex Nr.10-Tropfen Wirkstoffe: Crataegus Dil. D4, Arnica Dil. D4, Aurum chloratum natronatum Dil. D5, Barium jodatum Dil.
Pulver zur Herstellung einer Lösung zum Einnehmen, verpackt in Beuteln.
 Fachinformation 1. BEZEICHNUNG DES ARZNEIMITTELS Dulcolax M Balance 10 g Pulver zur Herstellung einer Lösung zum Einnehmen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Jeder Beutel enthält 10 g Macrogol
Fachinformation 1. BEZEICHNUNG DES ARZNEIMITTELS Dulcolax M Balance 10 g Pulver zur Herstellung einer Lösung zum Einnehmen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Jeder Beutel enthält 10 g Macrogol
Betreff: Finasterid hältige Arzneispezialitäten Änderungen der Fachund Gebrauchsinformationen aufgrund des HBD PSUR Worksharing Projektes
 Datum: 03. Februar 2011 Kontakt: Mag. pharm. Dr. Ulrike Rehberger Abteilung: Tel. / Fax: +43 (0) 505 55 36258, DW.Fax-36207 E-Mail: ulrike.rehberger@ages.at Unser Zeichen: 16c-110202-21500-A-PHV Ihr Zeichen:
Datum: 03. Februar 2011 Kontakt: Mag. pharm. Dr. Ulrike Rehberger Abteilung: Tel. / Fax: +43 (0) 505 55 36258, DW.Fax-36207 E-Mail: ulrike.rehberger@ages.at Unser Zeichen: 16c-110202-21500-A-PHV Ihr Zeichen:
Nasa Rhinathiol 0,1 %ige Nasenspray, Lösung Xylometazolinhydrochlorid
 Seite 1/5 Packungsbeilage Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mir der Anwendung dieses Arzneimittels beginnen. Sie enthält wichtige Informationen für Ihre Behandlung. Wenn
Seite 1/5 Packungsbeilage Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mir der Anwendung dieses Arzneimittels beginnen. Sie enthält wichtige Informationen für Ihre Behandlung. Wenn
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Androfin 5 mg - Filmtabletten Wirkstoff: Finasterid
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Androfin 5 mg - Filmtabletten Wirkstoff: Finasterid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Androfin 5 mg - Filmtabletten Wirkstoff: Finasterid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Heumann s Blasen- und Nierentee Solubitrat Wirkstoffe: Dickextrakt aus Birkenblättern, Dickextrakt aus Riesengoldrutenkraut Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Heumann s Blasen- und Nierentee Solubitrat Wirkstoffe: Dickextrakt aus Birkenblättern, Dickextrakt aus Riesengoldrutenkraut Lesen Sie die gesamte Packungsbeilage
Fachinformation. (Zusammenfassung der Merkmale des Arzneimittels)
 (Zusammenfassung der Merkmale des Arzneimittels) 1. Bezeichnung des Arzneimittels PROSCAR-Filmtabletten 2. Qualitative und quantitative Zusammensetzung 1 Filmtablette enthält 5 mg Finasterid. Die vollständige
(Zusammenfassung der Merkmale des Arzneimittels) 1. Bezeichnung des Arzneimittels PROSCAR-Filmtabletten 2. Qualitative und quantitative Zusammensetzung 1 Filmtablette enthält 5 mg Finasterid. Die vollständige
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Kamillosan -Mundspray. Kamillenblütenauszug Pfefferminzöl Anisöl
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Kamillosan -Mundspray Kamillenblütenauszug Pfefferminzöl Anisöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Kamillosan -Mundspray Kamillenblütenauszug Pfefferminzöl Anisöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Vitagutt Vitamin E 670 mg, Weichkapsel Zur Anwendung bei Erwachsenen Wirkstoff: 1000 mg all-rac-alpha-tocopherolacetat (entsprechend 670 mg RRR-alpha- Tocopherol-Äquivalente).
Gebrauchsinformation: Information für Anwender Vitagutt Vitamin E 670 mg, Weichkapsel Zur Anwendung bei Erwachsenen Wirkstoff: 1000 mg all-rac-alpha-tocopherolacetat (entsprechend 670 mg RRR-alpha- Tocopherol-Äquivalente).
Gebrauchsinformation: Information für Patienten. Urgenin Tropfen Tinktur aus Serenoa repens (Bartram Small) ; Saft aus Echinacea purpurea (Moench)
 Gebrauchsinformation: Information für Patienten Urgenin Tropfen Tinktur aus Serenoa repens (Bartram Small) ; Saft aus Echinacea purpurea (Moench) Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für Patienten Urgenin Tropfen Tinktur aus Serenoa repens (Bartram Small) ; Saft aus Echinacea purpurea (Moench) Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
1. Was sind Dorithricin Halstabletten und wofür werden sie angewendet?
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Dorithricin - Halstabletten Wirkstoffe: Tyrothricin, Benzalkoniumchlorid, Benzocain Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Dorithricin - Halstabletten Wirkstoffe: Tyrothricin, Benzalkoniumchlorid, Benzocain Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
Gebrauchsinformation: Information für Patienten
 Gebrauchsinformation: Information für Patienten MINIRIN 0,1 mg/ml - Nasenspray Wirkstoff: Desmopressinacetat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Gebrauchsinformation: Information für Patienten MINIRIN 0,1 mg/ml - Nasenspray Wirkstoff: Desmopressinacetat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Sonstige Bestandteile mit bekannter Wirkung: Jede Retardtablette enthält 103,55 mg wasserfreie Lactose.
 Targin 40 mg/20 mg Retardtabletten 2. Qualitative und quantitative Zusammensetzung Jede Targin 40 mg/20 mg Retardtablette enthält 40 mg Oxycodonhydrochlorid entsprechend 36 mg Oxycodon und 21,8 mg Naloxonhydrochlorid-Dihydrat
Targin 40 mg/20 mg Retardtabletten 2. Qualitative und quantitative Zusammensetzung Jede Targin 40 mg/20 mg Retardtablette enthält 40 mg Oxycodonhydrochlorid entsprechend 36 mg Oxycodon und 21,8 mg Naloxonhydrochlorid-Dihydrat
Zusammenfassung der Merkmale des Arzneimittels. Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Virupos 30 mg/g Augensalbe 2. Qualitative und quantitative Zusammensetzung Wirkstoff: 1 g Salbe enthält Aciclovir 30 mg Die
Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Virupos 30 mg/g Augensalbe 2. Qualitative und quantitative Zusammensetzung Wirkstoff: 1 g Salbe enthält Aciclovir 30 mg Die
PACKUNGSBEILAGE. Bisolvon Hustenlöser - Saft Version 4.1 1
 PACKUNGSBEILAGE Bisolvon Hustenlöser - Saft Version 4.1 1 Gebrauchsinformation: Information für Patienten Bisolvon Hustenlöser - Saft Wirkstoff: Bromhexinhydrochlorid Lesen Sie die gesamte Packungsbeilage
PACKUNGSBEILAGE Bisolvon Hustenlöser - Saft Version 4.1 1 Gebrauchsinformation: Information für Patienten Bisolvon Hustenlöser - Saft Wirkstoff: Bromhexinhydrochlorid Lesen Sie die gesamte Packungsbeilage
Isotonische Kochsalzlösung 0,9% Infusionslösung
 Gebrauchsinformation und Fachinformation SERAG-WIESSNER GmbH & Co. KG Zum Kugelfang 8-12 95119 Naila Isotonische Kochsalzlösung 0,9% Infusionslösung Diese Packungsbeilage beinhaltet: 1. Was ist Isotonische
Gebrauchsinformation und Fachinformation SERAG-WIESSNER GmbH & Co. KG Zum Kugelfang 8-12 95119 Naila Isotonische Kochsalzlösung 0,9% Infusionslösung Diese Packungsbeilage beinhaltet: 1. Was ist Isotonische
Intoxikationen Seite - 1 - Intoxikationen
 Intoxikationen Seite - 1 - Intoxikationen Häu Ca. 10.000 Vergiftungen im Jahr in Deutschland, davon 80% durch orale Aufnahme, 6% durch Hautkontakt und 5% durch Inhalation. Überwiegend betroffen sind Jugendliche
Intoxikationen Seite - 1 - Intoxikationen Häu Ca. 10.000 Vergiftungen im Jahr in Deutschland, davon 80% durch orale Aufnahme, 6% durch Hautkontakt und 5% durch Inhalation. Überwiegend betroffen sind Jugendliche
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Vibrocil Nasenspray. Phenylephrin, Dimetindenmaleat
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Vibrocil Nasenspray Phenylephrin, Dimetindenmaleat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Vibrocil Nasenspray Phenylephrin, Dimetindenmaleat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Tantum Verde 3 mg Pastillen mit Minzgeschmack Wirkstoff: Benzydaminhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tantum Verde 3 mg Pastillen mit Minzgeschmack Wirkstoff: Benzydaminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tantum Verde 3 mg Pastillen mit Minzgeschmack Wirkstoff: Benzydaminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Wirkstoff: Pilocarpinhydrochlorid (5 mg/ml)
 Spersacarpin 0,5% (5 mg/ml) Augentropfen Wirkstoff: Pilocarpinhydrochlorid (5 mg/ml) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. -
Spersacarpin 0,5% (5 mg/ml) Augentropfen Wirkstoff: Pilocarpinhydrochlorid (5 mg/ml) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. -
GfKT-Fachtagung 13.11.2015. Antagonisierung und Substitution von Opioiden: Fallstricke bzw. ausgewählte Besonderheiten
 GfKT-Fachtagung 13.11.2015 Antagonisierung und Substitution von Opioiden: Fallstricke bzw. ausgewählte Besonderheiten Dr. med. Andreas U N I V E Vagt, R S I T Ä Giftnotruf T S M E D I Z I N Berlin, B E
GfKT-Fachtagung 13.11.2015 Antagonisierung und Substitution von Opioiden: Fallstricke bzw. ausgewählte Besonderheiten Dr. med. Andreas U N I V E Vagt, R S I T Ä Giftnotruf T S M E D I Z I N Berlin, B E
1. WAS IST RHINATHIOL ANTIRHINITIS UND WOFÜR WIRD ES ANGEWENDET?
 GEBRAUCHSINFROMATION: INFORMATION FÜR PATIENTEN Rhinathiol Antirhinitis 10 mg / 4 mgtabletten Rhinathiol Antirhinitis 10 mg + 4 mg / 10 ml Sirup (Phenylephrinhydrochlorid Chlorphenamin) Lesen Sie die gesamte
GEBRAUCHSINFROMATION: INFORMATION FÜR PATIENTEN Rhinathiol Antirhinitis 10 mg / 4 mgtabletten Rhinathiol Antirhinitis 10 mg + 4 mg / 10 ml Sirup (Phenylephrinhydrochlorid Chlorphenamin) Lesen Sie die gesamte
Gebrauchsinformation: Information für den Anwender
 Wortlaut der für die Gebrauchsinformation vorgesehenen Angaben Stand: Mai 2008 1 Gebrauchsinformation: Information für den Anwender Harntee-Steiner, Teeaufgusspulver Zur Anwendung bei Heranwachsenden ab
Wortlaut der für die Gebrauchsinformation vorgesehenen Angaben Stand: Mai 2008 1 Gebrauchsinformation: Information für den Anwender Harntee-Steiner, Teeaufgusspulver Zur Anwendung bei Heranwachsenden ab
Gebrauchsinformation: Information für Patienten. Desloratadin Genericon 5 mg Filmtabletten. Wirkstoff: Desloratadin
 Gebrauchsinformation: Information für Patienten Desloratadin Genericon 5 mg Filmtabletten Wirkstoff: Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Patienten Desloratadin Genericon 5 mg Filmtabletten Wirkstoff: Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
1. NAME UND ANSCHRIFT DES PHARMAZEUTISCHEN UNTERNEHMERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS
 Gebrauchsinformation Eurican SHPPi2 Staupe-Adenovirusinfektion-Parvovirose-Parainfluenza Typ 2-Lebendimpfstoff, Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension, für Hunde 1. NAME
Gebrauchsinformation Eurican SHPPi2 Staupe-Adenovirusinfektion-Parvovirose-Parainfluenza Typ 2-Lebendimpfstoff, Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension, für Hunde 1. NAME
Gebrauchsinformation: Information für Anwender. Cevitol 500 mg-kautabletten Wirkstoff: Ascorbinsäure (Vitamin C)
 Gebrauchsinformation: Information für Anwender Cevitol 500 mg-kautabletten Wirkstoff: Ascorbinsäure (Vitamin C) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender Cevitol 500 mg-kautabletten Wirkstoff: Ascorbinsäure (Vitamin C) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Wirkstoffe: Trockenextrakt aus Birkenblättern, Trockenextrakt aus Goldrutenkraut
 Gebrauchsinformation: Information für Anwender HEUMANN Blasen- und Nierentee SOLUBITRAT uro Teeaufgusspulver Wirkstoffe: Trockenextrakt aus Birkenblättern, Trockenextrakt aus Goldrutenkraut Lesen Sie die
Gebrauchsinformation: Information für Anwender HEUMANN Blasen- und Nierentee SOLUBITRAT uro Teeaufgusspulver Wirkstoffe: Trockenextrakt aus Birkenblättern, Trockenextrakt aus Goldrutenkraut Lesen Sie die
- wenn Sie Asthma haben. Chronischer Husten kann ein Warnzeichen für einbeginnendes Asthma bronchiale sein. Darauf ist insbesondere bei Kindern
 1Was ist "Codeinum phosphoricum Tabletten" und wofür wird es angewendet? 1.1"Codeinum phosphoricum Tabletten" enthält den Wirkstoff Codein, ein Arzneimittel aus der Gruppe dersogenannten Opium-Alkaloide.
1Was ist "Codeinum phosphoricum Tabletten" und wofür wird es angewendet? 1.1"Codeinum phosphoricum Tabletten" enthält den Wirkstoff Codein, ein Arzneimittel aus der Gruppe dersogenannten Opium-Alkaloide.
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Otrivin 0,05 % - Nasenspray ohne Konservierungsmittel. Xylometazolinhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Otrivin 0,05 % - Nasenspray ohne Konservierungsmittel Xylometazolinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Otrivin 0,05 % - Nasenspray ohne Konservierungsmittel Xylometazolinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Pulver und Lösungsmittel zur Herstellung einer Injektions- oder Infusionslösung
 Fachinformation Berinert P 500 Einheiten Pulver und Lösungsmittel zur Herstellung einer Injektions- oder Infusionslösung 1. BEZEICHNUNG DES ARZNEIMITTELS Berinert P 500 Einheiten Pulver und Lösungsmittel
Fachinformation Berinert P 500 Einheiten Pulver und Lösungsmittel zur Herstellung einer Injektions- oder Infusionslösung 1. BEZEICHNUNG DES ARZNEIMITTELS Berinert P 500 Einheiten Pulver und Lösungsmittel
LANSOYL Paraffine Gel zum Einnehmenv3.0_B2.0 1/5
 PIL September 2015 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER LANSOYL PARAFFINE 78,230 g/100 g Gel zum Einnehmen Paraffinöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
PIL September 2015 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER LANSOYL PARAFFINE 78,230 g/100 g Gel zum Einnehmen Paraffinöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. AERIUS 5 mg Filmtabletten Desloratadin
 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN AERIUS 5 mg Filmtabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN AERIUS 5 mg Filmtabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Boehringer Ingelheim RCV GmbH & Co KG 28.10.2014 / Mes GI Rhinospray plus Version 2.4 C 1 PACKUNGSBEILAGE
 Rhinospray plus Version 2.4 C 1 PACKUNGSBEILAGE Rhinospray plus Version 2.4 C 2 Gebrauchsinformation: Information für Anwender Rhinospray plus ätherische Öle - Nasenspray Wirkstoff: Tramazolinhydrochlorid
Rhinospray plus Version 2.4 C 1 PACKUNGSBEILAGE Rhinospray plus Version 2.4 C 2 Gebrauchsinformation: Information für Anwender Rhinospray plus ätherische Öle - Nasenspray Wirkstoff: Tramazolinhydrochlorid
XANOR 0,5 mg-tabletten 2. Qualitative und quantitative Zusammensetzung Sonstiger Bestandteil mit bekannter Wirkung: Darreichungsform
 XANOR 0,5 mg-tabletten 2. Qualitative und quantitative Zusammensetzung Jede Tablette enthält 0,5 mg Alprazolam. Sonstiger Bestandteil mit bekannter Wirkung: Jede Tablette enthält 96 mg Lactose. Vollständige
XANOR 0,5 mg-tabletten 2. Qualitative und quantitative Zusammensetzung Jede Tablette enthält 0,5 mg Alprazolam. Sonstiger Bestandteil mit bekannter Wirkung: Jede Tablette enthält 96 mg Lactose. Vollständige
FACHINFORMATION. Es sollte darauf geachtet werden, dass das Verstopfen oder Abtrennen der Infusionsschläuche
 CARINOPHARM FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Remimed 1 mg Pulver für ein Konzentrat zur Herstellung einer Injektions-/Infusionslösung Remimed 2 mg Pulver für ein Konzentrat zur Herstellung
CARINOPHARM FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Remimed 1 mg Pulver für ein Konzentrat zur Herstellung einer Injektions-/Infusionslösung Remimed 2 mg Pulver für ein Konzentrat zur Herstellung
Boehringer Ingelheim RCV GmbH & Co KG 06.10.2010 / Mac GI Mucosolvan 15 mg - Lutschpastillen Version 2.0 C 1 PACKUNGSBEILAGE
 Mucosolvan 15 mg - Lutschpastillen Version 2.0 C 1 PACKUNGSBEILAGE Mucosolvan 15 mg - Lutschpastillen Version 2.0 C 2 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Mucosolvan 15 mg - Lutschpastillen
Mucosolvan 15 mg - Lutschpastillen Version 2.0 C 1 PACKUNGSBEILAGE Mucosolvan 15 mg - Lutschpastillen Version 2.0 C 2 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Mucosolvan 15 mg - Lutschpastillen
Sonstiger Bestandteil: Natrium 6,3-10,5 mmol (bzw. 144,9-241,5 mg) pro Dosis (30-50 IE/kg)
 FACHINFORMATION (Zusammenfassung der Merkmales des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Atenativ SD 500 IE Trockenstechampulle mit Lösungsmittel 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
FACHINFORMATION (Zusammenfassung der Merkmales des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Atenativ SD 500 IE Trockenstechampulle mit Lösungsmittel 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Boehringer Ingelheim RCV GmbH & Co KG 28.05.2013 / DrMü GI Rhinospray plus Version 2.3 C 1 PACKUNGSBEILAGE
 Rhinospray plus Version 2.3 C 1 PACKUNGSBEILAGE Rhinospray plus Version 2.3 C 2 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Rhinospray plus ätherische Öle - Nasenspray Wirkstoff: Tramazolinhydrochlorid
Rhinospray plus Version 2.3 C 1 PACKUNGSBEILAGE Rhinospray plus Version 2.3 C 2 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Rhinospray plus ätherische Öle - Nasenspray Wirkstoff: Tramazolinhydrochlorid
Packungsbeilage GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. NUSO-SAN Menthol 1mg/ml Nasenspray, Lösung. Xylometazolinhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER NUSO-SAN Menthol 1mg/ml Nasenspray, Lösung Xylometazolinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER NUSO-SAN Menthol 1mg/ml Nasenspray, Lösung Xylometazolinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
UND WOFÜR WIRD ES ANGEWENDET?
 Gebrauchsinformation: Information für den Anwender Quadronal comp. gegen Kopfschmerzen 400 mg Paracetamol und 50 mg Coffein, Tablette Zur Anwendung bei Erwachsenen und Jugendlichen ab 12 Jahren Wirkstoffe:
Gebrauchsinformation: Information für den Anwender Quadronal comp. gegen Kopfschmerzen 400 mg Paracetamol und 50 mg Coffein, Tablette Zur Anwendung bei Erwachsenen und Jugendlichen ab 12 Jahren Wirkstoffe:
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. AERIUS 5 mg Schmelztabletten Desloratadin
 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN AERIUS 5 mg Schmelztabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN AERIUS 5 mg Schmelztabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Tramadolhydrochlorid Actavis 100 mg Retardtabletten Tramadolhydrochlorid Actavis 150 mg Retardtabletten Tramadolhydrochlorid
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Tramadolhydrochlorid Actavis 100 mg Retardtabletten Tramadolhydrochlorid Actavis 150 mg Retardtabletten Tramadolhydrochlorid
ARBEIT MIT DER ARZNEIMITTELKOMMISSION DER DEUTSCHEN ÄRZTESCHAFT ONLINE UNTER: HTTP://AIS.KBV.DE. Tapentadol
 Ausgabe 3/2012 Wirkstoff AKTUELL ARBEIT MIT DER ARZNEIMITTELKOMMISSION DER DEUTSCHEN ÄRZTESCHAFT ONLINE UNTER: HTTP://AIS.KBV.DE Tapentadol Tapentadol sollte nur bei Patienten mit schweren nicht Tumor-bedingten
Ausgabe 3/2012 Wirkstoff AKTUELL ARBEIT MIT DER ARZNEIMITTELKOMMISSION DER DEUTSCHEN ÄRZTESCHAFT ONLINE UNTER: HTTP://AIS.KBV.DE Tapentadol Tapentadol sollte nur bei Patienten mit schweren nicht Tumor-bedingten
Alizaprid ist ein Wirkstoff zur Behandlung von Erbrechen (Antiemetikum).
 Gebrauchsinformation: Information für Anwender Vergentan 50 mg/2 ml Injektionslösung Wirkstoff: Alizapridhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
Gebrauchsinformation: Information für Anwender Vergentan 50 mg/2 ml Injektionslösung Wirkstoff: Alizapridhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
OPIOID-THERAPIE. 10-30mg Gtt 2%- 1gtt=1mg. 4h 1. 5+325 6h. 4mg 12h-24h 7,5 12,5 72 70-100
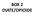 BOX 2 OIATE/OPIOIDE OPIOID-THERAPIE Freinamen Handelsnamen Initiale Dosis Zeitintervall Analgetische Anmerkungen Potenz Morphin Oramorph Verfügbarkeit verschieden wegen first pass. Wgg nach 15-60 Minuten.
BOX 2 OIATE/OPIOIDE OPIOID-THERAPIE Freinamen Handelsnamen Initiale Dosis Zeitintervall Analgetische Anmerkungen Potenz Morphin Oramorph Verfügbarkeit verschieden wegen first pass. Wgg nach 15-60 Minuten.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Noctamid - Tabletten. Wirkstoff: Lormetazepam
 1 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Noctamid - Tabletten Wirkstoff: Lormetazepam Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
1 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Noctamid - Tabletten Wirkstoff: Lormetazepam Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Anwender. Zoledronsäure-ratiopharm 5 mg Infusionslösung in Beuteln Zoledronsäure
 Gebrauchsinformation: Information für Anwender Zoledronsäure-ratiopharm 5 mg Infusionslösung in Beuteln Zoledronsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor dieses Arzneimittel bei
Gebrauchsinformation: Information für Anwender Zoledronsäure-ratiopharm 5 mg Infusionslösung in Beuteln Zoledronsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor dieses Arzneimittel bei
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Humanalbumin 20 % Biotest elektrolytarm 200 g/l, Infusionslösung
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Humanalbumin 20 % Biotest elektrolytarm 200 g/l, Infusionslösung Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Humanalbumin 20 % Biotest elektrolytarm 200 g/l, Infusionslösung Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. PROGESTOGEL 1 % Gel. Progesteron
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER PROGESTOGEL 1 % Gel Progesteron Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. Heben
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER PROGESTOGEL 1 % Gel Progesteron Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. Heben
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Lexotanil 6 mg Tabletten Bromazepam Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Anwender Lexotanil 6 mg Tabletten Bromazepam Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Fachinformation. (Zusammenfassung der Merkmale des Arzneimittels)
 Fachinformation (Zusammenfassung der Merkmale des Arzneimittels) 1. Bezeichnung des Arzneimittels Rhophylac 300 Mikrogramm / 2 ml Injektionslösung in einer Fertigspritze 2. Qualitative und quantitative
Fachinformation (Zusammenfassung der Merkmale des Arzneimittels) 1. Bezeichnung des Arzneimittels Rhophylac 300 Mikrogramm / 2 ml Injektionslösung in einer Fertigspritze 2. Qualitative und quantitative
GEBRAUCHSINFORMATION. Wirkstoff: Acetylsalicylsäure. Z.Nr.: 3155
 Liebe Patientin, lieber Patient! Bitte lesen Sie diese Gebrauchsinformation aufmerksam, weil sie wichtige Informationen darüber enthält, was Sie bei der Einnahme dieses Arzneimittels beachten sollen. Wenden
Liebe Patientin, lieber Patient! Bitte lesen Sie diese Gebrauchsinformation aufmerksam, weil sie wichtige Informationen darüber enthält, was Sie bei der Einnahme dieses Arzneimittels beachten sollen. Wenden
PARABIO 500 mg Tabletten Wirkstoff: Paracetamol
 Eine fiktive Packungsbeilage: Das Medikament PARABIO ist erfunden. In der Apotheke kann man jedoch mehrere Medikamente kaufen, die den gleichen Wirkstoff enthalten und die für die gleiche Anwendung bestimmt
Eine fiktive Packungsbeilage: Das Medikament PARABIO ist erfunden. In der Apotheke kann man jedoch mehrere Medikamente kaufen, die den gleichen Wirkstoff enthalten und die für die gleiche Anwendung bestimmt
GEBRAUCHSINFORMATION UND FACHINFORMATION
 GEBRAUCHSINFORMATION UND FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Grippe-Impfstoff CSL, Suspension zur Injektion in Fertigspritzen Influenza-Impfstoff (Spaltvirus, inaktiviert) 2. QUALITATIVE UND
GEBRAUCHSINFORMATION UND FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Grippe-Impfstoff CSL, Suspension zur Injektion in Fertigspritzen Influenza-Impfstoff (Spaltvirus, inaktiviert) 2. QUALITATIVE UND
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1/52
 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1/52 1. BEZEICHNUNG DES ARZNEIMITTELS Suboxone 2 mg/0,5 mg Sublingualtabletten 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Sublingualtablette
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1/52 1. BEZEICHNUNG DES ARZNEIMITTELS Suboxone 2 mg/0,5 mg Sublingualtabletten 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Sublingualtablette
AUFKLÄRUNGSBLATT* ZUR IMPFUNG GEGEN DIE FSME (Frühsommer-Meningoenzephalitis) *(Auszug aus den jeweiligen Packungsinformationen)
 AUFKLÄRUNGSBLATT* ZUR IMPFUNG GEGEN DIE FSME (Frühsommer-Meningoenzephalitis) *(Auszug aus den jeweiligen Packungsinformationen) Lesen Sie die gesamte Information sorgfältig durch, bevor Sie sich bzw.
AUFKLÄRUNGSBLATT* ZUR IMPFUNG GEGEN DIE FSME (Frühsommer-Meningoenzephalitis) *(Auszug aus den jeweiligen Packungsinformationen) Lesen Sie die gesamte Information sorgfältig durch, bevor Sie sich bzw.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER duraultra N sine 1 mg/ml Augentropfen
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER duraultra N sine 1 mg/ml Augentropfen 1 ml Augentropfen enthält 1 mg Naphazolinhydrochlorid Zur Anwendung bei Kindern ab 2 Jahren und bei Erwachsenen
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER duraultra N sine 1 mg/ml Augentropfen 1 ml Augentropfen enthält 1 mg Naphazolinhydrochlorid Zur Anwendung bei Kindern ab 2 Jahren und bei Erwachsenen
Demetrin /Mono Demetrin
 1. BEZEICHNUNG DER ARZNEIMITTEL 10 mg Tabletten Mono 20 mg Tabletten Prazepam 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Tablette enthält 10 mg Prazepam. Mono 1 Tablette enthält 20 mg Prazepam.
1. BEZEICHNUNG DER ARZNEIMITTEL 10 mg Tabletten Mono 20 mg Tabletten Prazepam 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Tablette enthält 10 mg Prazepam. Mono 1 Tablette enthält 20 mg Prazepam.
Boehringer Ingelheim RCV GmbH & Co KG Mucosolvan 15 mg / 5 ml - Saft GI 1. 24.01.2014 / DrMü Version 4.2 C PACKUNGSBEILAGE
 1 PACKUNGSBEILAGE 2 Gebrauchsinformation: Information für Anwender Mucosolvan 15 mg / 5 ml - Saft für Kinder Wirkstoff: Ambroxolhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
1 PACKUNGSBEILAGE 2 Gebrauchsinformation: Information für Anwender Mucosolvan 15 mg / 5 ml - Saft für Kinder Wirkstoff: Ambroxolhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Name und Anschrift des Zulassungsinhabers und, wenn unterschiedlich, des Herstellers, der für die Chargenfreigabe verantwortlich ist
 GEBRAUCHSINFORMATION Narcoren, 16 g/100 ml Injektionslösung für Pferd, Hund, Katze, Nerz, Iltis, Huhn, Taube, Ziervögel, Hase, Kaninchen, Meerschweinchen, Hamster, Ratte, Maus, Schlangen, Schildkröten,
GEBRAUCHSINFORMATION Narcoren, 16 g/100 ml Injektionslösung für Pferd, Hund, Katze, Nerz, Iltis, Huhn, Taube, Ziervögel, Hase, Kaninchen, Meerschweinchen, Hamster, Ratte, Maus, Schlangen, Schildkröten,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER ISOPTO CARPINE 1% Augentropfen ISOPTO CARPINE 2% Augentropfen ISOPTO CARPINE 3% Augentropfen ISOPTO CARPINE 4% Augentropfen Pilocarpinhydrochlorid Lesen
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER ISOPTO CARPINE 1% Augentropfen ISOPTO CARPINE 2% Augentropfen ISOPTO CARPINE 3% Augentropfen ISOPTO CARPINE 4% Augentropfen Pilocarpinhydrochlorid Lesen
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Tebofortan 40 mg - Filmtabletten. Wirkstoff: Trockenextrakt aus Ginkgo-biloba-Blättern
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tebofortan 40 mg - Filmtabletten Wirkstoff: Trockenextrakt aus Ginkgo-biloba-Blättern Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tebofortan 40 mg - Filmtabletten Wirkstoff: Trockenextrakt aus Ginkgo-biloba-Blättern Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
ANWEISUNGSKARTE FÜR DEN PATIENTEN
 Der Plan zur Risikobegrenzung in Belgien, zu dem diese Information gehört, ist eine Maßnahme, die ergriffen wurde, um eine sichere und wirksame Anwendung fon ZypAdhera TM zu garantieren. (RMA modifizierte
Der Plan zur Risikobegrenzung in Belgien, zu dem diese Information gehört, ist eine Maßnahme, die ergriffen wurde, um eine sichere und wirksame Anwendung fon ZypAdhera TM zu garantieren. (RMA modifizierte
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Clarityn 10 mg - Brausetabletten Wirkstoff: Loratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Clarityn 10 mg - Brausetabletten Wirkstoff: Loratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
FluxoMed Fluoxetinhydrochlorid
 Liebe Patientin, lieber Patient! Ihr Arzt hat Ihnen zur Behandlung Ihrer Erkrankung FluxoMed 20 mg Kapseln verordnet. Um eine baldmögliche Besserung Ihrer Beschwerden zu erzielen, richten Sie sich bei
Liebe Patientin, lieber Patient! Ihr Arzt hat Ihnen zur Behandlung Ihrer Erkrankung FluxoMed 20 mg Kapseln verordnet. Um eine baldmögliche Besserung Ihrer Beschwerden zu erzielen, richten Sie sich bei
Sonstige Bestandteile: Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 1. BEZEICHNUNG DES ARZNEIMITTELS MUTAGRIP Kinder 2014/2015 Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Impfdosis
1. BEZEICHNUNG DES ARZNEIMITTELS MUTAGRIP Kinder 2014/2015 Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Impfdosis
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Prosta Albin. Wirkstoffe: Pareira brava Dil. D2, Populus tremuloides Ø, Sabal serrulatum Ø
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Prosta Albin 50 ml Mischung zum Einnehmen Wirkstoffe: Pareira brava Dil. D2, Populus tremuloides Ø, Sabal serrulatum Ø Lesen Sie bitte die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Prosta Albin 50 ml Mischung zum Einnehmen Wirkstoffe: Pareira brava Dil. D2, Populus tremuloides Ø, Sabal serrulatum Ø Lesen Sie bitte die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Ibuprofen Sandoz 200 mg Filmtabletten Ibuprofen Sandoz 400 mg Filmtabletten Ibuprofen
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Ibuprofen Sandoz 200 mg Filmtabletten Ibuprofen Sandoz 400 mg Filmtabletten Ibuprofen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Ibuprofen Sandoz 200 mg Filmtabletten Ibuprofen Sandoz 400 mg Filmtabletten Ibuprofen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie
Kompendium der medikamentösen Schmerztherapie
 Eckhard Beubler Kompendium der medikamentösen Schmerztherapie Wirkungen, Nebenwirkungen und Kombinationsmöglichkeiten Unter Mitarbeit von Roland Kunz und Jürgen Sorge 5. Auflage ^ Springer IX Inhaltsverzeichnis
Eckhard Beubler Kompendium der medikamentösen Schmerztherapie Wirkungen, Nebenwirkungen und Kombinationsmöglichkeiten Unter Mitarbeit von Roland Kunz und Jürgen Sorge 5. Auflage ^ Springer IX Inhaltsverzeichnis
Gebrauchsinformation: Information für den Anwender. Thyrogen 0,9 mg Pulver zur Herstellung einer Injektionslösung Thyrotropin alfa
 Gebrauchsinformation: Information für den Anwender Thyrogen 0,9 mg Pulver zur Herstellung einer Injektionslösung Thyrotropin alfa Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Gebrauchsinformation: Information für den Anwender Thyrogen 0,9 mg Pulver zur Herstellung einer Injektionslösung Thyrotropin alfa Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Tumorschmerzen im Alter
 Tumorschmerzen im Alter Eine vielschichtige Herausforderung Dr. med. Roland Kunz, Chefarzt Geriatrie + Palliative Care 1 Was ist anders in der Schmerztherapie beim alten Menschen? Multimorbidität Komplexität
Tumorschmerzen im Alter Eine vielschichtige Herausforderung Dr. med. Roland Kunz, Chefarzt Geriatrie + Palliative Care 1 Was ist anders in der Schmerztherapie beim alten Menschen? Multimorbidität Komplexität
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. IBUMED 200mg Tabletten Ibuprofen
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER IBUMED 200mg Tabletten Ibuprofen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER IBUMED 200mg Tabletten Ibuprofen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel
PHV-issue: Codein for the treatment of cough or cold in paediatric patients
 BASG / AGES Institut LCM Traisengasse 5, A-1200 Wien Datum: Kontakt: Abteilung: Tel. / Fax: E-Mail: Unser Zeichen: Ihr Zeichen: 27.05.2015 Mag. pharm. Dr. Ulrike Rehberger REGA +43 (0) 505 55 36258 pv-implementation@ages.at
BASG / AGES Institut LCM Traisengasse 5, A-1200 Wien Datum: Kontakt: Abteilung: Tel. / Fax: E-Mail: Unser Zeichen: Ihr Zeichen: 27.05.2015 Mag. pharm. Dr. Ulrike Rehberger REGA +43 (0) 505 55 36258 pv-implementation@ages.at
Influbene Erkältungsgetränk Pulver zur Herstellung einer Lösung zum Einnehmen 2. Qualitative und quantitative Zusammensetzung Ein Beutel enthält: 500
 Influbene Erkältungsgetränk Pulver zur Herstellung einer Lösung zum Einnehmen 2. Qualitative und quantitative Zusammensetzung Ein Beutel enthält: 500 mg Paracetamol 200 mg Guaifenesin 10 mg Phenylephrinhydrochlorid
Influbene Erkältungsgetränk Pulver zur Herstellung einer Lösung zum Einnehmen 2. Qualitative und quantitative Zusammensetzung Ein Beutel enthält: 500 mg Paracetamol 200 mg Guaifenesin 10 mg Phenylephrinhydrochlorid
Hepatyrix Injektionssuspension Hepatitis-A-(inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert) ab dem vollendeten 15.
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER 22.07.2009 Hepatyrix Injektionssuspension Hepatitis-A-(inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert) ab dem vollendeten 15. Lebensjahr
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER 22.07.2009 Hepatyrix Injektionssuspension Hepatitis-A-(inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert) ab dem vollendeten 15. Lebensjahr
Datum: Kontakt: Abteilung: Tel. / Fax: E-Mail: Unser Zeichen: Ihr Zeichen:
 BASG / AGES Institut LCM Traisengasse 5, A-1200 Wien Datum: Kontakt: Abteilung: Tel. / Fax: E-Mail: Unser Zeichen: Ihr Zeichen: 06.11.2014 Veronika Iro REGA +43 (0) 505 55 36247 pv-implementation@ages.at
BASG / AGES Institut LCM Traisengasse 5, A-1200 Wien Datum: Kontakt: Abteilung: Tel. / Fax: E-Mail: Unser Zeichen: Ihr Zeichen: 06.11.2014 Veronika Iro REGA +43 (0) 505 55 36247 pv-implementation@ages.at
Gebrauchsinformation: Information für Anwender. Cyprostol - Tabletten Wirkstoff: Misoprostol
 1 Gebrauchsinformation: Information für Anwender Cyprostol - Tabletten Wirkstoff: Misoprostol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
1 Gebrauchsinformation: Information für Anwender Cyprostol - Tabletten Wirkstoff: Misoprostol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Normhydral - lösliches Pulver
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Normhydral - lösliches Pulver p 1/5 Wirkstoffe: Wasserfreie Glucose, Natriumchlorid, Natriumcitrat, Kaliumchlorid Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Normhydral - lösliches Pulver p 1/5 Wirkstoffe: Wasserfreie Glucose, Natriumchlorid, Natriumcitrat, Kaliumchlorid Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Patienten
 Gebrauchsinformation: Information für Patienten Esberitox -Tabletten Trockenextrakt aus einer Mischung von Lebensbaumspitzen und -blättern, Purpursonnenhutwurzel, Blassfarbener Sonnenhutwurzel und Färberhülsenwurzel
Gebrauchsinformation: Information für Patienten Esberitox -Tabletten Trockenextrakt aus einer Mischung von Lebensbaumspitzen und -blättern, Purpursonnenhutwurzel, Blassfarbener Sonnenhutwurzel und Färberhülsenwurzel
Gebrauchsinformation: Information für Patienten. Petinimid-Kapseln Wirkstoff: Ethosuximid
 Gebrauchsinformation: Information für Patienten Petinimid-Kapseln Wirkstoff: Ethosuximid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Patienten Petinimid-Kapseln Wirkstoff: Ethosuximid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
