Werkstoffwissenschaften
|
|
|
- Kirsten Waldfogel
- vor 6 Jahren
- Abrufe
Transkript
1 Werkstoffwissenschaften Struktur und Eigenschaften von Werkstoffen Aufbau kristalliner Werkstoffe Atomaufbau Quantenzahlen: Hauptquantenzahlen: Energieniveau n = 1,, Nebenquantenzahlen: Bahndrehniveau, Energieunterniveau l = 0, 1,, n-1 Magnetquantelzahlen: Ausrichtung im Magnetfeld / Orbital m = -l,, l Spinquantenzahlen: Rotationsmöglichkeiten s = 1, + 1 Pauli-Prinzip: Von den Elektronen eines Atoms stimmen niemals zwei in allen 4 Quantenzahlen überein. Hund sche Regel: Von den Orbitalen, die zum gleichen Nebenenergieniveau gehören, erhält zunächst jedes Orbital ein Elektron, bevor mit der vollen Besetzung dieser Orbitale durch ein zweites Elektron begonnen wird. Atomanordnung: Gasförmig (geringe Teilchendichte) Flüssig (Nahordnung [1- Atomdurchmesser] danach statistische Verteilung) Amorph (keine zeitl. Änderung, beschränkte Beweglichkeit) Kristallin (homogen verteilt, energieärmster stabiler Zustand, Fernordnung) Bindungskraft / -energie: Bindungskraft Bindungsenergie Seite 1 von 1
2 Bindungstypen Ionenbindung: Bsple.: MgO, NaCl Schlechter Leiter für Elektrizität und Wärme Heteropolare, ungerichtete Bindung Diamagnetisch Im sichtbaren Licht durchsichtig Kovalente Bindung (Atombindung): Bsple.: H, CH 4 Überlappen von Atomorbitalen => energetisch günstigerer Zustand Starke, gerichtete Bindung Wichtige Begriffe: Valenzwinkel, Hybridisierung z.b.: Diamant: sp³, guter Isolator für Elektrizität, Durchsichtigkeit, Diamagnetismus, hoher Schmelzpunkt Graphit: sp² Metallbindung: Bsple.: Fe Gute elektrische und thermische Leitfähigkeit Ungerichtete Bindung Möglichst dichte Raumfüllung (Kugelpackung: kfz, hdp, (krz)) Gute plastische Verformbarkeit Neben- / Restvalenzbindung: Bsple.: O, CO, H Van-der-Waals-Kräfte (Vor.: Bindungsenergie bei Raumtemp. sehr niedrig) Vor allem bei Makromolekülen der Polymere H-Brücken-Bindung, Dispersionskräfte, Orientierungskräfte (Dipol-Dipol / Dipol-Ion / Induktion) Stoff Bindungsart Beispiel Metall metallisch Fe Glas & Keramik Kovalent, ionisch SiO Polymere Kovalent, van-der-waals PET Halbleiter Kovalent, kovalentionisch Si, Ge Seite von 1
3 Elementstrukturen Kubischraumzentriert (krz): Bsple.: W, Mo, Ta, α-fe (Schwermetalle) Enthält Atome ( ) 4 r 4 Πr KZ = 8, akrz =, PDkrz = = 0,68 a ( PD : Packungsdichte, r : Atomradius, a : Gitterkonstante ) Gleitsystem: {111} < 110 > Burgersvektor: a < 110 > Kubischflächenzentriert (kfz): Bsple.: Ag, Cu, Al, γ-fe (hohe elektrische Leitfähigkeit) Enthält 4 Atome ( ) 8 4 r 44 Πr KZ = 1, akfz =, PDkfz = = 0,74 a Eigenschaften : gut verformbar Gleitsystem: {110} < 111 > Burgersvektor: a < 111 > a < 100 > Hexagonaldichteste Kugelpackung (hdp): Bsple.: Mg, Ba, α-ti (Leichtmetalle) Enthält Atome ( ) Πr KZ = 1, PDhdp = = 0,74 a Schlagwort : Schichtfolge Gleitsystem: {0001} < 110 > Burgersvektor: a < 110 > c < 0001 > Werkstoffarten: Eisen-WS: Stahl, Gusseisen Nichteisen-WS: Be, Al, Mg, Ag, Au, W, Ta Halbleiter: Ge, Si, GaAs, InP Anorg.Nichtmet.-WS: Glas, Keramik Kunststoffe: PP, PE, PET, PVC Mineralische Naturstoffe: Asbest, Marmor, Rubin Organische Naturstoffe: Holz, Kautschuk Seite von 1
4 Bravais-Gitter: Indizierung von Ebenen und Richtungen Punkt [[x,y,z]] Richtung / Vektor [x,y,z] Ebene (x,y,z) Gruppe von Gitterpunkten <x,y,z> Gruppe von Ebenen {x,y,z} z.b. : <1,0,0> = [100],[010],[001],[-100],[0-10],[00-1] (a,b,c) ist senkrecht zu [a,b,c] Bestimmung einer Ebene: Schnittpunkt mit Koordinatenachsen: m*a, n*b, p*c (h,k,l) = Hauptnenner * ( 1 m, 1 n, 1 p ) Seite 4 von 1
5 Defekte: 0-dimensional: Leerstellen, Zwischengitteratome, Substitutionsatome 1-dimensional: Versetzungen ( Stufen~, Schrauben~ ) -dimensional: Stapelfehler, Grenzflächen -dimensional: Cluster von Punktfehlern, Poren, Ausscheidungen Kristallbaufehler: Im thermodynamischen Gleichgewicht nur Leerstellen, alles andere durch Störung des Gleichgewichts Leerstellen: n U = cl = exp N R T ( U: Energie bei Bildung einer Leerstelle; n: # Leerstellen; N: # Gitterplätze; R: Gaskonstante; c L : Gleichgewichtskonzentration der Leerstellen) J Metalle: U = mol, c L(T Schmelz ) = 10-4 Leerstellen durch: plast. Verformung, Bestrahlung mit energiereichen Teilchen (Vorsicht: Versprödung)! Überschussleerstellen (beschleunigen Ausscheidungsvorgänge, beeinflussen Verformung) cz DZ! cl DL (c: Gleichgewichtskonzentration; D: Diffusionskoeffizient; L: Leerstellen; Z: Zwischengitteratome) F = U T S (F: freie Energie, U: innere Energie, S: Entropie; T: thermodynamische Gleichgewichtskonstante) 1 Verzerrungsfeld ~ (r: Abstand von Defekt) r 5 Fehlordnungstypen bei Ionengitter: Schottky~ : gleiche Konzentration von Leerstellen im Kationen- und Anionenteilgitter Anti-Schottky~ : gleiche Konzentration von Kationen und Anionen auf Zwischengitterplätzen Frenkel~ : gleiche Konzentration von Leerstellen im Kationenteilgitter und Kationen auf Zwischengitterplätzen Anti-Frenkel~ : gleiche Konzentration von Leerstellen im Anionenteilgitter und Anionen auf Zwischengitterplätzen Antistrukturelle ~ : gleiche Konzentration von Kationen im Anionenteilgitter und Anionen im Kationenteilgitter 1-dimensionale Defekte:! Spannungsfeld ( Energie EV G b (b: Burgersvektor; V: Versetzungslinie)) Stufenversetzung: eingeschobene Halbebene, b v, Verzerrung ~ 1, Klettern (Verlassen der Gleitebene) nur r durch Anlagern von Punktdefekten Schraubenversetzung: verschobene Ebene, b# v, keine definierte Gleitebene, Quergleiten (Wechseln der Gleitebenen) 1 Versetzungsdichte ρ /V, [ ρ /V ] =, ρ : Gesamtlänge der Versetzungslinie cm Einkristall: ρ /V = 1 cm gegossenes Metall: ρ /V =10 8 cm verformte Metalle: ρ /V =10 1 cm Seite 5 von 1
6 Defekte: -dimensionale Defekte: Stapelfehler (kfz) o Extrinsisch: A B C A BAC A B C o Intrinsisch: A B C B C A B C Entstehung: Kristallwachstum, plast. Verformung, Phasenumwandlung Energie: mj Cu: 60 m, Al: 00 mj m, Ag: 0 mj m (alle kfz, AG kann auch hdp) Innere Grenzfläche: Einphasig Korngrenze Vielkristall Mehrphasig Phasengrenze Korngrenze Korngrenze: trennt Bereiche verschiedener Kristallstruktur aber unterschiedlicher Orientierung - Kleinwinkel~ : Orientierungsunterschiede < 15 vollständig aus Versetzungen aufgebaut - Großwinkel~ : Orientierungsunterschiede > 15 Phasengrenze: trennt verschiedenphasige Kristallite Zwillingsgrenzen: Großwinkelkorngrenzen mit ungestörtem Gitteraufbau, Spiegelebene Bragg sche Gleichung: n λ = d sin( θ ) (n: Ordnung; λ: Wellenlänge; d: Netzebenenabstand; θ: Einfalls-/Reflektionswinkel) (Grundlage zur Untersuchung von Kristallen mit Röntgen-, Neutronen-, Elektronen-Strahlen) Netzebenenabstand d unabhängig von Kristallstruktur und Millerindizes von {h,k,l} a kubisch: d = h + k + l a hexagonal: d =, a,c: Gitterparameter 4 ( h + k + l ) + l ( c ) a Seite 6 von 1
7 Gefüge: Als ~ bezeichnet man die mit dem Mikroskop sichtbare Struktur eines Werkstoffes. Das ~ wird bestimmt von der chemischen / strukturellen Beschaffenheit innerhalb eines Feststoffes (Phasen/Defekte). Das ~ beschreibt die Gesamtheit aller am Aufbau beteiligten Phasen und Defekte Gefügebildende Prozesse: - Erstarrung: flüssig fest ( Metalle, Halbleiter ) - Sublimation: gasförmig fest - Kristallisation aus Lösung : elektrolytische Ausscheidung ( hochreines Cu ) Gibbs che Phasenregel: F = N P + F: # Freiheitsgrade; N: # Komponenten; P: # Phasen Abkühlkurven: Kristallisation, Keimbildung, Keimwachstum - Bei gegebener Temperatur und festem Druck ist immer derjenige Zustand stabil, der die geringste freie Enthalpie besitzt. - Ein fester Zustand stellt sich nicht spontan ein, erst muss sich ein fester Keim bilden durch Fluktuationen, die in jeder Schmelze vorkommen. - Ein Keim ist bei T<T Schmelz nur dann stabil, wenn er eine kritische Größe überschreitet γ TS ( rc = ; γ : Oberflächenspannung, H S : Umwandlungsenthalpie ). Je größer T, T H S r c desto kleiner wird, d.h. größere Anzahl von wachstumsfähigen Keimen, d.h. feinkristallines Gefüge. - Die Gestalt eines Kristalls bei der Entstehung ist durch die Wachstumsanisotropie bestimmt. Nur wenn der Kristall in alle Richtungen gleich schnell wächst, entsteht eine Kugel, ansonsten ein Polyeder. - Der Wachstumsprozess läuft so lange ab, bis sich Kristalle berühren und Korngrenzen bilden. - Umwandlung im festen Zustand Verschiedene Kristallstrukturen eines Elementes im festen Zustand bezeichnet man als allotrope Modifikationen, z.b. bei Fe α < 911 C krz 911 C < γ < 19 C kfz 19 C < δ < 156 C krz Seite 7 von 1
8 Gefüge Mischkristalle - Substitutions-Mkr: Hume-Rothery: kristallisieren im gleichen Gittertyp, Atomradienunterschied < 15%, geringe chemische Affinität Vegard: Gitterkonstante ändert sich etwa linear mit Konzentration, Gitterkonst. des Mkr ist gleich Summe aus Gitterkonst. der reinen Kristalle (±1%). - Einlagerungs-Mkr: Einlagerung von H, B, C, N nur sehr geringe Löslichkeit (wenige %) in Oktaeder-/Tetraederlücken die Einlagerungsatome dürfen nicht zu viel Spiel haben (=> Mindestgröße) Intermetallische Phasen - Laves-Phasen: Strukturtyp AB ( Mittelwertcharakter ), sehr dicht gepackt, z.b. AlFe, FeTi - Hume-Rothery-Phasen: Stabilitätsgrenzen gegeben durch Valenzelektronenkonz. VEK = V G (V: # ans Gitter abgeg. Elektronen; G: # einbezogene Gitteratome) z.b. Cu-Zn (Messing) Thermisch aktivierbare Prozesse Zustandsänderungen laufen nur dann ab, wenn die freie Energie dabei herabgesetzt wird. z.b. Diffusion Unter ~ versteht man die Fähigkeit von Atomen in Festkörpern, ihren Gitterplatz durch thermische Anregung zu verlassen und sich über andere geeignete Plätze durch den Kristall zu bewegen. Handelt es sich dabei um gittereigene Atome, so spricht man von Selbstdiffusion, bei gitterfremden Atomen von Fremdatomen. Grundlage dafür sind Platzwechselvorgänge: Leerstellen-, Zwischengitter-, Ring-, Austausch-Mechanismus. $ 1. Fick sches Gesetz: j = D $$% c mit j:diffusionsstrom; D:Diffusionskonst. D D0 e = [m²/s]; c:konzentration Das Minuszeichen besagt, dass der Strom von hoher zu niedriger Konzentration geht:! Der Konzentrationsunterschied gleicht sich aus. Parabolisches Zeitgesetz: x = D t mit x: Weg den Diffusionsfront zurücklegt Festigkeitsverlust metallischer Werkstoffe Ursache: Beseitigung und Umordnung von Versetzungen (Klettern, Quergleiten) Erholung: Vorgänge, bei denen lediglich Auslöschung (Annihilation) und Umordnung von Versetzungen stattfinden. Diese Umordnungen finden allerdings erst bei einer höheren Verformungstemperatur statt, ab welcher die mechanische Stabilität überwunden werden kann. Dies führt zu einer Abnahme der Versetzungsdichte und außerdem zu ganz speziellen Versetzungsmustern, nämlich einen räumlichen Verbund von Kleinwinkelkorngrenzen, was man als Polygonisation bezeichnet. Ursache für die Erholung ist die Wechselwirkung der Versetzungen durch ihr langreichweitiges Spannungsfeld. Q RT Seite 8 von 1
9 Gefüge Annihilation: Zwei Versetzungen auf gleicher Ebene löschen sich aus. Liegen sie nicht auf einer Ebene, kommt es zur Bildung eines Versetzungsdipols (Kette von Leerstellen). Rekristallisation: Unter ~ versteht man die Gefügeneubildung bei Wärmebehandlung. Kristallographisch gesehen vollzieht sie sich durch die Entstehung und Bewegung von Großwinkelkorngrenzen unter Beseitigung der Verformungsstruktur. Das ist der zur Erholung, wo nur die Auslöschung und Umordnung von Versetzungen geschieht. Man beobachtet die Entstehung sehr kleiner Körner, die dann wachsen, bis sie zusammenstoßen bzw. das verformte Gewebe vollständig aufgezehrt haben. Sie ist somit charakterisiert durch Keimbildung und Keimwachstum und wird als primäre Rekristallisation bezeichnet. Ursachen: treibende Kraft auf Korngrenzen, durch welche die freie Enthalpie des Kristalls vermindert wird. Bei der primären ~ entspricht die treibende Kraft der in der Versetzung gespeicherten Verformungsenergie( E 1 V = G b ). => treibende Kraft: P = E ρ ( ρ : Versetzungsdichte) V V V Kriterien: - thermodynamische Instabilität (krit. Keimgröße, präexist. Keime) - mechanische Instabilität (Inhomogenität der Treibkraft) - kinetische Instabilität (bewegliche Grenzflächen) Härtung: Dispersions~ : Verfahren bei Metallen mit nichtmetallischen Einschlüssen, Versetzungen können nicht hindurchschneiden (ähnlich Frank-Read), sonder müssen sich zwischen den Teilchen auswölben. G b Krit. Spannung: τ = l r Ausscheidungs~ : Ausscheiden eines übersättigten Mischkristalls (z.b. Fe C), Ausscheidungen sind durch Phasengrenzen getrennt, inkohärente PhGr Korngrenze, kohärnete PhGr => Kräfte auf Versetzungen => Hindernis für Bewegung Mischkristall~ : Mkre stellen Hindernisse für Versetzungen dar Frank-Read : Ein Versetzungsstück der Länge l 0 in einer Gleitebene wird durch Anlegen G b einer Schubspannung τ = gekrümmt, dabei vergrößert sich der Radius von selbst, und l0 es bildet sich ein geschlossener Ring. Unter der anliegenden Spannung breitet sich der Ring aus und weitere entstehen. Korngrenzen : Versetzungen können Korngrenzen nicht überwinden (Hall-Petch) Hebelgesetz: m m m Mkr S Mkr c c'' = c' c ' c' c = c' c ' + m = 1 S Seite 9 von 1
10 Plastizität und Elastizität Plastizität: Umformvermögen Während plastische Werkstoffe auf Überbeanspruchung mit bleibender Formänderung reagieren, reagieren nichtplastische mit Versagen durch Trennbruch. Die Sicherheit einer Konstruktion hängt somit von der Plastizität ab. Mechanismus der plastischen Verformung: Plastische Deformation geschieht durch Abgleiten größerer Gitterbereiche ( Gitterpakete ) parallel zu best. Kristallebenen in best. Kristallrichtungen. Die Kristallebenen werden also gegeneinander verschoben. Diese Ebenen und Richtungen (zusammen als Gleitsystem bezeichnet) sind für die verschiedenen Gittertypen unterschiedlich. σ-ε-diagramm: Materialversagen: Bruch: o Spröd~: Der Rissausbreitung geht keine irreversible Verformung voraus. o Duktil~: Stärkere irreversible Verformung ging voraus. Ebenfalls unterscheidet man zwischen interkristallinem und transkristallinem Bruch. Riss: o ~Bildung: Ursache sind Eigenspannungen (innere Spannungen in einem Werkstoff ohne Einwirken von äußeren Kräften, die in der Fertigung entstehen). Häufig entstehen Risse aber erst infolge lokalisierter Verformungen beim Einwirken äußerer Beanspruchungen. o ~Ausbreitung: Die Rissbildung führt nur dann zum Bruch, wenn der Riss ausbreitungsfähig ist. Die Rissausbreitung kann entweder stabil (unter Energiefreisetzung) oder instabil (unter ständiger Energiezufuhr) verlaufen. Die instabile Rissbildung erfolgt nur, wenn die Griffith-Bedingung erfüllt ist: σ π a > k Jc ( k J :Bruchzähigkeit) c Rissausbreitungskraft: Rissausbreitungsenergie: W E π a σ G = E π a σ = E Seite 10 von 1
11 Elektrizität: Halbleiter: z.b.: Ge, Si Eigenleitung: ValenzBand - LeitungsBand e- aus VB angehoben in LB bei Raumtemperatur ( E = 1,1 Si / 0,7 Ge ev)! Löcher/Defektelektronen im VB => ebenfalls elektrische Leitfähigkeit! Ebenfalls Ladungstransport ohne Massetransport Volumenkonzentration der e - : bei HL niedriger als bei Me Elektronenbeweglichkeit: bei HL höher als bei Me Dotierung: p-~ : Elektronen-Akzeptor (. Hauptgruppe) => Loch n-~ : Elektronen-Donator (5. Hauptgruppe) => freies Elektron Elektrischer Widerstand: Ursachen: 1.) Temperatur: Wärmeschwingungen der Atomrümpfe.) Gitterbaufehler: Leerstellen, Fremdatome, Versetzungen Regel von Matthiesen: Sei ρ G der aus der Wärmeschwingung und ρ Z der aus Gitterbaufehlern oder Fremdatomen resultierende spezifische Widerstand, dann ergibt sich der gesamte spezifische Widerstand additiv: ρ = ρ + ρ G Z Supraleitung: z.b.: Nb, V, Pb Widerstand 0 bei T < TSprung(Stoff) (Metallische Materialien: T Sprung K Spezielle oxidische Keramik: T Sprung 90 K) Kann durch Magnetfeld aufgehoben werden, kritische Feldstärke H für T ' T H H0 1 T Sprung kritische Größen: - Sprungtemperatur - Feldstärke - Stromdichte 1.Art: supraleitende reine Materialien{Nb,V,Te}, magnetischer Fluß nur in Randschicht (Meißner- Ochsenfeld-Effekt), weiche Supraleiter, Diamagnetismus.Art: normalleitende Flussschläuche, dazwischen supraleitend keramische Supraleiter: spröde, brüchig Ba, Bi, Y, Sr, Tl, Ca, CuO (immer) O-Konzentration entscheidenden Einfluss auf Sprungtemperatur Herstellung: Pulver pressen, anschließend sintern Seite 11 von 1
12 Elektrizität: Piezoelektrischer Effekt: Magnetismus: Dia~: Magnetische Kraftliniendichte wird durch Stoff geschwächt, entgegengesetztes induziertes Moment, abgeschlossene Elektronenschalen, z.b.: Edelgase, Salze, organische Verbindungen Para~: Mindestens eine der Elektronenschalen nicht voll besetzt, in allen Aggregatszuständen Ferro~: Vgl. Para~, starke Wechselwirkung zwischen benachbarten Atomen, parallel ausgerichtet, nur bei Festkörpern, Dauermagnet,!!!! Antiferro~: Antiparallelstellung benachbarter Atome (z.b.: Cr)! keine Bereiche mit magnetischem Moment, aber weißsche Bezirke, da Antiparallelstellung nur über kleine Bereiche,!"!" Ferri~: Vgl. Antiferro~, Untergitter mit entgegengesetzten Magneten, nur teilweise Kompensation,!"!" => restliches magnetisches Moment Weißsche Bezirke : magnetische Bezirke mit resultierendem Moment Seite 1 von 1
3. Struktur des Festkörpers
 3. Struktur des Festkörpers 3.1 Kristalline und amorphe Strukturen Amorphe Struktur - Atombindung ist gerichtet - unregelmäßige Anordnung der Atome - keinen exakten Schmelzpunkt, sondern langsames Erweichen,
3. Struktur des Festkörpers 3.1 Kristalline und amorphe Strukturen Amorphe Struktur - Atombindung ist gerichtet - unregelmäßige Anordnung der Atome - keinen exakten Schmelzpunkt, sondern langsames Erweichen,
Typische Eigenschaften von Metallen
 Typische Eigenschaften von Metallen hohe elektrische Leitfähigkeit (nimmt mit steigender Temperatur ab) hohe Wärmeleitfähigkeit leichte Verformbarkeit metallischer Glanz Elektronengas-Modell eines Metalls
Typische Eigenschaften von Metallen hohe elektrische Leitfähigkeit (nimmt mit steigender Temperatur ab) hohe Wärmeleitfähigkeit leichte Verformbarkeit metallischer Glanz Elektronengas-Modell eines Metalls
Institut für Eisen- und Stahl Technologie. Seminar 2 Binäre Systeme Fe-C-Diagramm. www.stahltechnologie.de. Dipl.-Ing. Ch.
 Institut für Eisen- und Stahl Technologie Seminar 2 Binäre Systeme Fe-C-Diagramm Dipl.-Ing. Ch. Schröder 1 Literatur V. Läpple, Wärmebehandlung des Stahls, 2003, ISBN 3-8085-1308-X H. Klemm, Die Gefüge
Institut für Eisen- und Stahl Technologie Seminar 2 Binäre Systeme Fe-C-Diagramm Dipl.-Ing. Ch. Schröder 1 Literatur V. Läpple, Wärmebehandlung des Stahls, 2003, ISBN 3-8085-1308-X H. Klemm, Die Gefüge
Grundlagen der Chemie Metalle
 Metalle Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Metalle 75% aller chemischen Elemente sind Metalle. Typische
Metalle Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Metalle 75% aller chemischen Elemente sind Metalle. Typische
Grundlagen der Chemie
 1 Die Metallbindung Hartstoffe 75% aller chemischen Elemente sind. Typische Eigenschaften: 1. Die Absorption für sichtbares Licht ist hoch. Hieraus folgt das große Spiegelreflexionsvermögen. Das ist die
1 Die Metallbindung Hartstoffe 75% aller chemischen Elemente sind. Typische Eigenschaften: 1. Die Absorption für sichtbares Licht ist hoch. Hieraus folgt das große Spiegelreflexionsvermögen. Das ist die
Wiederholung der letzten Vorlesungsstunde:
 Wiederholung der letzten Vorlesungsstunde: Ionenbindung, Koordinationspolyeder, ionische Strukturen, NaCl, CsCl, ZnS, Elementarzelle, Gitter, Gitterkonstanten, 7 Kristallsysteme, Ionenradien, Gitterenergie
Wiederholung der letzten Vorlesungsstunde: Ionenbindung, Koordinationspolyeder, ionische Strukturen, NaCl, CsCl, ZnS, Elementarzelle, Gitter, Gitterkonstanten, 7 Kristallsysteme, Ionenradien, Gitterenergie
A. N. Danilewsky 77. Inhalt von Kapitel 4
 A. N. Danilewsky 77 Inhalt von Kapitel 4 4 Kristallchemie... 78 4.1 Chemische Bindung und Koordination... 79 4.2 Konzept der dichtesten Kugelpackungen... 81 4.3 Strukturtypen... 84 4.3.1 Metalle... 84
A. N. Danilewsky 77 Inhalt von Kapitel 4 4 Kristallchemie... 78 4.1 Chemische Bindung und Koordination... 79 4.2 Konzept der dichtesten Kugelpackungen... 81 4.3 Strukturtypen... 84 4.3.1 Metalle... 84
Werkstoffe der Elektrotechnik im Studiengang Elektrotechnik
 Werkstoffe der Elektrotechnik im Studiengang Elektrotechnik - Stoffgemische - Prof. Dr. Ulrich Hahn WS 2008/2009 welche Stoffgemische gibt es? technisch relevante Stoffgemische: Lösung Suspension Legierung
Werkstoffe der Elektrotechnik im Studiengang Elektrotechnik - Stoffgemische - Prof. Dr. Ulrich Hahn WS 2008/2009 welche Stoffgemische gibt es? technisch relevante Stoffgemische: Lösung Suspension Legierung
Chemische Bindung. Wie halten Atome zusammen? Welche Atome können sich verbinden? Febr 02
 Chemische Bindung locker bleiben Wie halten Atome zusammen? positiv Welche Atome können sich verbinden? power keep smiling Chemische Bindung Die chemischen Reaktionen spielen sich zwischen den Hüllen der
Chemische Bindung locker bleiben Wie halten Atome zusammen? positiv Welche Atome können sich verbinden? power keep smiling Chemische Bindung Die chemischen Reaktionen spielen sich zwischen den Hüllen der
4.2 Metallkristalle. 4.2.1 Bindungsverhältnisse
 4.2 Metallkristalle - 75 % aller Elemente sind Metalle - hohe thermische und elektrische Leitfähigkeit - metallischer Glanz - Duktilität (Zähigkeit, Verformungsvermögen): Fähigkeit eines Werkstoffs, sich
4.2 Metallkristalle - 75 % aller Elemente sind Metalle - hohe thermische und elektrische Leitfähigkeit - metallischer Glanz - Duktilität (Zähigkeit, Verformungsvermögen): Fähigkeit eines Werkstoffs, sich
Einführung in Werkstoffkunde Zustandsdiagramme
 Einführung in Werkstoffkunde Dr.-Ing. Norbert Hort norbert.hort@gkss.de Magnesium Innovations Center (MagIC) GKSS Forschungszentrum Geesthacht GmbH Inhalte Über mich Einführung Aufbau von Werkstoffen Physikalische
Einführung in Werkstoffkunde Dr.-Ing. Norbert Hort norbert.hort@gkss.de Magnesium Innovations Center (MagIC) GKSS Forschungszentrum Geesthacht GmbH Inhalte Über mich Einführung Aufbau von Werkstoffen Physikalische
Inhalt der VL: 1. Metallbindung 2. Kristalliner Aufbau 3. Kristallbaufehler 4. Schmelzen und Erstarren 5. Isotropie und Anisotropie
 Inhalt der VL: 1. Metallbindung 2. Kristalliner Aufbau 3. Kristallbaufehler 4. Schmelzen und Erstarren 5. Isotropie und Anisotropie 1 Eisenwerkstoffe NE- Stähle Eisengusswerkstoffe Aluminium und -legierungen
Inhalt der VL: 1. Metallbindung 2. Kristalliner Aufbau 3. Kristallbaufehler 4. Schmelzen und Erstarren 5. Isotropie und Anisotropie 1 Eisenwerkstoffe NE- Stähle Eisengusswerkstoffe Aluminium und -legierungen
Magische Kristalle Prof. Dr. R. Glaum
 Magische Kristalle Prof. Dr. R. Glaum Institut für Anorganische Chemie Universität Bonn http://www.glaum.chemie.uni-bonn.de email: rglaum@uni-bonn.de Dank Herr Michael Kortmann Herr Andreas Valder Deutsche
Magische Kristalle Prof. Dr. R. Glaum Institut für Anorganische Chemie Universität Bonn http://www.glaum.chemie.uni-bonn.de email: rglaum@uni-bonn.de Dank Herr Michael Kortmann Herr Andreas Valder Deutsche
Kristallstruktur der Metalle
 Bedeutung Metallische Werkstoffe sind in der Regel kristallin aufgebaut. Die vorliegende Kristallstruktur hat einen erheblichen Einfluss auf die Eigenschaften des Werkstoffs, wie z.b. die Festigkeit, Verformbarkeit,
Bedeutung Metallische Werkstoffe sind in der Regel kristallin aufgebaut. Die vorliegende Kristallstruktur hat einen erheblichen Einfluss auf die Eigenschaften des Werkstoffs, wie z.b. die Festigkeit, Verformbarkeit,
Anorganische Chemie III
 Seminar zu Vorlesung Anorganische Chemie III Wintersemester 01/13 Christoph Wölper Universität Duisburg-Essen Koordinationszahlen Ionenradien # dichteste Packung mit 1 Nachbarn -> in Ionengittern weniger
Seminar zu Vorlesung Anorganische Chemie III Wintersemester 01/13 Christoph Wölper Universität Duisburg-Essen Koordinationszahlen Ionenradien # dichteste Packung mit 1 Nachbarn -> in Ionengittern weniger
Element. Verbindung. Reinstoff. Gemisch
 Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Grundlagen der Festkörperchemie
 Grundlagen der Festkörpercheie 1. Der feste Aggregatzustand Aggregatzustand Beständigkeit Ordnung Voluen For gas (g) - - - flüssig (l) + - Teilordnung fest (s) + + + akroskopisch subikrokopisch - ideales
Grundlagen der Festkörpercheie 1. Der feste Aggregatzustand Aggregatzustand Beständigkeit Ordnung Voluen For gas (g) - - - flüssig (l) + - Teilordnung fest (s) + + + akroskopisch subikrokopisch - ideales
Erläutere den CO 2 -Nachweis. Definiere den Begriff exotherme Reaktion und zeichne ein passendes Energiediagramm. Grundwissenskatalog Chemie 8 NTG
 Erläutere den CO 2 -Nachweis. Wird das Gas in Kalkwasser (Ca(OH) 2 ) eingeleitet bildet sich ein schwerlöslicher Niederschlag von Calciumcarbonat (CaCO 3 ). Abgabe von innerer Energie (Wärme, Knall,...)
Erläutere den CO 2 -Nachweis. Wird das Gas in Kalkwasser (Ca(OH) 2 ) eingeleitet bildet sich ein schwerlöslicher Niederschlag von Calciumcarbonat (CaCO 3 ). Abgabe von innerer Energie (Wärme, Knall,...)
Elektrische Leitung. Strom
 lektrische Leitung 1. Leitungsmechanismen Bändermodell 2. Ladungstransport in Festkörpern i) Temperaturabhängigkeit Leiter ii) igen- und Fremdleitung in Halbleitern iii) Stromtransport in Isolatoren iv)
lektrische Leitung 1. Leitungsmechanismen Bändermodell 2. Ladungstransport in Festkörpern i) Temperaturabhängigkeit Leiter ii) igen- und Fremdleitung in Halbleitern iii) Stromtransport in Isolatoren iv)
Elektrischer Strom S.Alexandrova 1
 Elektrischer Strom S.Alexandrova 1 Elektrischer Strom Wichtiger Begriff: Strom als Ladungs Transport Jeder Art: - in ioniziertem Gas - in Elektrolytlösung - im Metall - im Festkörper Enstehet wenn elektrisches
Elektrischer Strom S.Alexandrova 1 Elektrischer Strom Wichtiger Begriff: Strom als Ladungs Transport Jeder Art: - in ioniziertem Gas - in Elektrolytlösung - im Metall - im Festkörper Enstehet wenn elektrisches
Kleines Repetitorium zur Vorlesung Werkstoffkunde für E-Techniker (Prof. Dr. A. Winnacker)
 Kleines Repetitorium zur Vorlesung Werkstoffkunde für E-Techniker (Prof. Dr. A. Winnacker) WET Kapitel 1 - Mechanische Eigenschaften von Festkörpern Skizzieren Sie ein Spannungs-Dehnungs-Diagramm (Bezeichnungen
Kleines Repetitorium zur Vorlesung Werkstoffkunde für E-Techniker (Prof. Dr. A. Winnacker) WET Kapitel 1 - Mechanische Eigenschaften von Festkörpern Skizzieren Sie ein Spannungs-Dehnungs-Diagramm (Bezeichnungen
Stufe. Schraube. Materialphysik II Prof. Dr. Guido Schmitz 05.07.2013. 12.4 Versetzungen
 12.4 Versetzungen Versetzungen sind linienhafte Störungen des Kristallgitters, die den abgeglittenen Teil eines Kristalls von dem noch nicht abgeglittenen Teil auf einer Gleitebene voneinander trennen.
12.4 Versetzungen Versetzungen sind linienhafte Störungen des Kristallgitters, die den abgeglittenen Teil eines Kristalls von dem noch nicht abgeglittenen Teil auf einer Gleitebene voneinander trennen.
Thema heute: Aufbau fester Stoffe - Kristallographie
 Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung Ionenbindung, Kationen, Anionen, Coulomb-Kräfte Thema heute: Aufbau fester Stoffe - Kristallographie 244 Aufbau fester Materie Im Gegensatz
Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung Ionenbindung, Kationen, Anionen, Coulomb-Kräfte Thema heute: Aufbau fester Stoffe - Kristallographie 244 Aufbau fester Materie Im Gegensatz
Einführung in Werkstoffkunde Aufbau von Werkstoffen
 Einführung in Werkstoffkunde Aufbau von Werkstoffen Dr.-Ing. Norbert Hort norbert.hort@gkss.de Magnesium Innovations Center (MagIC) GKSS Forschungszentrum Geesthacht GmbH Inhalte Über mich Herstellung,
Einführung in Werkstoffkunde Aufbau von Werkstoffen Dr.-Ing. Norbert Hort norbert.hort@gkss.de Magnesium Innovations Center (MagIC) GKSS Forschungszentrum Geesthacht GmbH Inhalte Über mich Herstellung,
1. Stoffe und Eigenschaften
 1. Stoffe und Eigenschaften Chemischer Vorgang Stoffänderung, keine Zustandsänderung Physikalischer Vorgang Lösung Zustandsänderung, keine Stoffänderung (z.b. Lösen, Aggregatzustände,...) Homogenes Gemisch
1. Stoffe und Eigenschaften Chemischer Vorgang Stoffänderung, keine Zustandsänderung Physikalischer Vorgang Lösung Zustandsänderung, keine Stoffänderung (z.b. Lösen, Aggregatzustände,...) Homogenes Gemisch
Chemische Bindung. Ue Mol 1. fh-pw
 Ue Mol 1 Chemische Bindung Periodensystem - Atome - Moleküle Periodensystem(e) 3 Nichtmetalle - Metalloide 5 Eigenschaften der Elemente 6 Bindungstypen 7 Ionenbindung 8 Kovalente, homöopolare Bindung 10
Ue Mol 1 Chemische Bindung Periodensystem - Atome - Moleküle Periodensystem(e) 3 Nichtmetalle - Metalloide 5 Eigenschaften der Elemente 6 Bindungstypen 7 Ionenbindung 8 Kovalente, homöopolare Bindung 10
Christian-Ernst-Gymnasium
 Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 9 - MuG erstellt von der Fachschaft Chemie C 9.1 Stoffe und en Element kann chemisch nicht mehr zerlegt werden Teilchen
Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 9 - MuG erstellt von der Fachschaft Chemie C 9.1 Stoffe und en Element kann chemisch nicht mehr zerlegt werden Teilchen
Konzepte der anorganischen und analytischen Chemie II II
 Konzepte der anorganischen und analytischen Chemie II II Marc H. Prosenc Inst. für Anorganische und Angewandte Chemie Tel: 42838-3102 prosenc@chemie.uni-hamburg.de Outline Einführung in die Chemie fester
Konzepte der anorganischen und analytischen Chemie II II Marc H. Prosenc Inst. für Anorganische und Angewandte Chemie Tel: 42838-3102 prosenc@chemie.uni-hamburg.de Outline Einführung in die Chemie fester
1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig?
 1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig? 1) Es sind alles Metalle. 2) In der äußeren Elektronenschale werden s- bzw. s- und p-orbitale aufgefüllt. 3) Sie stimmen
1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig? 1) Es sind alles Metalle. 2) In der äußeren Elektronenschale werden s- bzw. s- und p-orbitale aufgefüllt. 3) Sie stimmen
VI Aufbau mehrphasiger Werkstoffe
 VI Aufbau mehrphasiger Werkstoffe 1. Grundbegriffe A.Phasen eines Werkstoffes Definition: Eine Phase ist ein Bereich konstanter Struktur (Atomanordnung) und chemischer Zusammensetzung (d.h. keine sprunghafte
VI Aufbau mehrphasiger Werkstoffe 1. Grundbegriffe A.Phasen eines Werkstoffes Definition: Eine Phase ist ein Bereich konstanter Struktur (Atomanordnung) und chemischer Zusammensetzung (d.h. keine sprunghafte
Inhaltsverzeichnis. 1 Einleitung 1
 nhaltsverzeichnis Vorwort zur 9. Auflage V 1 Einleitung 1 Zustände des festen Körpers 4 Kristalliner Zustand 6 Raumgitter und Kristallsysteme 7 Bravais-Gitter und Kristallstruktur 8 Analytische Beschreibung
nhaltsverzeichnis Vorwort zur 9. Auflage V 1 Einleitung 1 Zustände des festen Körpers 4 Kristalliner Zustand 6 Raumgitter und Kristallsysteme 7 Bravais-Gitter und Kristallstruktur 8 Analytische Beschreibung
Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung
 Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung Elementarzelle, Symmetrie, 7 Kristallsysteme, Zentrierte Elementarzellen, Salzstrukturen, NaCl-Struktur, AB-Strukturen, ZnS, CsCl, AB 2 -Strukturen,
Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung Elementarzelle, Symmetrie, 7 Kristallsysteme, Zentrierte Elementarzellen, Salzstrukturen, NaCl-Struktur, AB-Strukturen, ZnS, CsCl, AB 2 -Strukturen,
Werkstoffkunde Chemische Bindungsarten
 Folie 1/27 Die Elektronen auf der äußersten Schale eines Atoms (Außenelektronen oder Valenzelektronen genannt) bestimmen maßgeblich die chemischen Eigenschaften. Jedes Atom hat dabei das Bestreben die
Folie 1/27 Die Elektronen auf der äußersten Schale eines Atoms (Außenelektronen oder Valenzelektronen genannt) bestimmen maßgeblich die chemischen Eigenschaften. Jedes Atom hat dabei das Bestreben die
Einheiten und Einheitenrechnungen
 Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen
Einführung in Werkstoffkunde
 Einführung in Werkstoffkunde Magnesium Innovations Center (MagIC) GKSS Forschungszentrum Geesthacht GmbH Dr.-Ing. Norbert Hort norbert.hort@gkss.de Inhalte Über mich Einführung Aufbau von Werkstoffen Physikalische
Einführung in Werkstoffkunde Magnesium Innovations Center (MagIC) GKSS Forschungszentrum Geesthacht GmbH Dr.-Ing. Norbert Hort norbert.hort@gkss.de Inhalte Über mich Einführung Aufbau von Werkstoffen Physikalische
Begriffe zur Elektrik und Elektrochemie
 Staatsinstitut für Schulqualität und Bildungsforschung Begriffe zur Elektrik und Elektrochemie Akkumulator Atom Atomkern Batterie Ein Akkumulator ist eine Energiequelle, die wie eine Batterie Gleichstrom
Staatsinstitut für Schulqualität und Bildungsforschung Begriffe zur Elektrik und Elektrochemie Akkumulator Atom Atomkern Batterie Ein Akkumulator ist eine Energiequelle, die wie eine Batterie Gleichstrom
GRUNDWISSEN CHEMIE 9 - MuG erstellt von der Fachschaft Chemie
 Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 9 - MuG erstellt von der Fachschaft Chemie C 9.1 Stoffe und Reaktionen Reinstoff Element Kann chemisch nicht mehr zerlegt
Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 9 - MuG erstellt von der Fachschaft Chemie C 9.1 Stoffe und Reaktionen Reinstoff Element Kann chemisch nicht mehr zerlegt
Element. Verbindung. Reinstoff. homogenes Gemisch
 Element Reinstoff, der chemisch nicht mehr zersetzt werden kann und dessen Teilchen(Atome oder Moleküle) aus einer einzigen Atomart (d.h. Teilchen mit gleicher Ordnungszahl) besteht. Verbindung Reinstoff,
Element Reinstoff, der chemisch nicht mehr zersetzt werden kann und dessen Teilchen(Atome oder Moleküle) aus einer einzigen Atomart (d.h. Teilchen mit gleicher Ordnungszahl) besteht. Verbindung Reinstoff,
22. Chemische Bindungen
 .05.03. Chemische Bindungen Molekül: System aus zwei oder mehr Atomen Kleinste Einheit einer Substanz, die deren chemische Eigenschaften ausweist Quantenmechanisches Vielteilchensystem: Exakte explizite
.05.03. Chemische Bindungen Molekül: System aus zwei oder mehr Atomen Kleinste Einheit einer Substanz, die deren chemische Eigenschaften ausweist Quantenmechanisches Vielteilchensystem: Exakte explizite
Übung Grundlagen der Werkstoffe. Thema: Das Eisen-Kohlenstoffdiagramm
 Übung Grundlagen der Werkstoffe Thema: Das Eisen-Kohlenstoffdiagramm Einstiegsgehälter als Motivation für das Studium Übungsaufgaben 7. Skizzieren Sie eine Volumen/Temperatur-Kurve von Eisen. Begründen
Übung Grundlagen der Werkstoffe Thema: Das Eisen-Kohlenstoffdiagramm Einstiegsgehälter als Motivation für das Studium Übungsaufgaben 7. Skizzieren Sie eine Volumen/Temperatur-Kurve von Eisen. Begründen
Präparation. 1) Spaltung: Materialien: Alkalihalogenide (NaCl, KBr) Erdalkali (CaF 2. ) Oxide (MgO) Halbleiter (GaAs) Brechen Glas Bruchflächen amorph
 Oberflächenphysik 19.2. Vacuum technique [vapour pressure, Langmuir, pumps] 26.2. Structure, relaxations and reconstructions 4. 3. Diffractionsmethods: LEED, He atom scattering, grazing X-ray, ions 11.
Oberflächenphysik 19.2. Vacuum technique [vapour pressure, Langmuir, pumps] 26.2. Structure, relaxations and reconstructions 4. 3. Diffractionsmethods: LEED, He atom scattering, grazing X-ray, ions 11.
Grundlagen der Chemie Polare Bindungen
 Polare Bindungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Elektronegativität Unter der Elektronegativität
Polare Bindungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Elektronegativität Unter der Elektronegativität
Atombau, Periodensystem der Elemente
 Seminar zum Brückenkurs Chemie 2015 Atombau, Periodensystem der Elemente Dr. Jürgen Getzschmann Dresden, 21.09.2015 1. Aufbau des Atomkerns und radioaktiver Zerfall - Erläutern Sie den Aufbau der Atomkerne
Seminar zum Brückenkurs Chemie 2015 Atombau, Periodensystem der Elemente Dr. Jürgen Getzschmann Dresden, 21.09.2015 1. Aufbau des Atomkerns und radioaktiver Zerfall - Erläutern Sie den Aufbau der Atomkerne
Vorlesung Anorganische Chemie
 Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 6 Entropie und Gibbs Enthalpie Gibbs-elmholtz-Gleichung Absolute Entropien Gibbs Standardbildungsenthalpien Kinetik
Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 6 Entropie und Gibbs Enthalpie Gibbs-elmholtz-Gleichung Absolute Entropien Gibbs Standardbildungsenthalpien Kinetik
Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung / Salzstrukturen
 Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung / Salzstrukturen Der metallische Zustand, Dichtestpackung von Kugeln, hexagonal-, kubischdichte Packung, Oktaeder-, Tetraederlücken, kubisch-innenzentrierte
Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung / Salzstrukturen Der metallische Zustand, Dichtestpackung von Kugeln, hexagonal-, kubischdichte Packung, Oktaeder-, Tetraederlücken, kubisch-innenzentrierte
3.4. Leitungsmechanismen
 a) Metalle 3.4. Leitungsmechanismen - Metall besteht aus positiv geladenen Metallionen und frei beweglichen Leitungselektronen (freie Elektronengas), Bsp.: Cu 2+ + 2e - - elektrische Leitung durch freie
a) Metalle 3.4. Leitungsmechanismen - Metall besteht aus positiv geladenen Metallionen und frei beweglichen Leitungselektronen (freie Elektronengas), Bsp.: Cu 2+ + 2e - - elektrische Leitung durch freie
Chemische Bindung. Ionenbindung (heteropolare Bindung) kovalente Bindung van-der-waals-bindung Metallbindung
 Chemische Bindung Ionenbindung (heteropolare Bindung) kovalente Bindung van-der-waals-bindung Metallbindung 1 Was sind Ionen? Ein Ion besteht aus einem oder mehreren Atomen und hat elektrische Ladung Kationen
Chemische Bindung Ionenbindung (heteropolare Bindung) kovalente Bindung van-der-waals-bindung Metallbindung 1 Was sind Ionen? Ein Ion besteht aus einem oder mehreren Atomen und hat elektrische Ladung Kationen
Grundwissen Chemie 8. Jahrgangsstufe G8
 Grundwissen Chemie 8. Jahrgangsstufe G8 1. Stoffeigenschaften und Teilchenmodell - Teilchenmodell: Alle Stoffe bestehen aus kleinsten Teilchen, am einfachsten aus Kugeln (Kugelteilchenmodell). Die Teilchen
Grundwissen Chemie 8. Jahrgangsstufe G8 1. Stoffeigenschaften und Teilchenmodell - Teilchenmodell: Alle Stoffe bestehen aus kleinsten Teilchen, am einfachsten aus Kugeln (Kugelteilchenmodell). Die Teilchen
GDOES-Treffen Berlin 2008. Sputterprozess und Kristallorientierung
 GDOES-Treffen Berlin 2008 Sputterprozess und Kristallorientierung Die folgenden drei Folien zeigen, daß bei polykristallinen Materialien kein mehr oder weniger gleichmäßiger Sputterangriff beobachtet werden
GDOES-Treffen Berlin 2008 Sputterprozess und Kristallorientierung Die folgenden drei Folien zeigen, daß bei polykristallinen Materialien kein mehr oder weniger gleichmäßiger Sputterangriff beobachtet werden
HÜTTE - Das Ingenieurwissen
 HÜTTE - Das Ingenieurwissen von Horst Czichos, Manfred Hennecke, Akademischer Verein Hütte e.v. Neuausgabe Springer 2007 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 540 71851 2 Zu Inhaltsverzeichnis
HÜTTE - Das Ingenieurwissen von Horst Czichos, Manfred Hennecke, Akademischer Verein Hütte e.v. Neuausgabe Springer 2007 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 540 71851 2 Zu Inhaltsverzeichnis
Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch. Reinstoff, Element, Verbindung. Zweiatomige Elemente.
 1 1 Einteilung der Stoffe: Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Stoff Reinstoff Mischen Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b.
1 1 Einteilung der Stoffe: Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Stoff Reinstoff Mischen Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b.
Grundwissen Chemie 9. Jahrgangsstufe Sprachlicher Zweig
 Grundwissen Chemie 9. Jahrgangsstufe Sprachlicher Zweig 1. Stoffeigenschaften und modell a) modell Alle Stoffe bestehen aus kleinsten Die eines Stoffes sind untereinander gleich. Die verschiedener Stoffe
Grundwissen Chemie 9. Jahrgangsstufe Sprachlicher Zweig 1. Stoffeigenschaften und modell a) modell Alle Stoffe bestehen aus kleinsten Die eines Stoffes sind untereinander gleich. Die verschiedener Stoffe
Auswirkungen von Wärmebehandlungen
 14 Auswirkungen von Wärmebehandlungen Mit der plastischen Verformung eines Werkstoffs wird die Anzahl und die Dichte von Gitterfehlern, insbesondere der Versetzungen, erhöht. Damit wird auch die innere
14 Auswirkungen von Wärmebehandlungen Mit der plastischen Verformung eines Werkstoffs wird die Anzahl und die Dichte von Gitterfehlern, insbesondere der Versetzungen, erhöht. Damit wird auch die innere
Übungsaufgaben zur Vorlesung Chemie der Materialien
 Übungsaufgaben zur Vorlesung Chemie der Materialien Aufgabe 1: a) Was ist die Referenz für die Mohs Härteskala? b) Ordnen Sie die folgenden Festkörper nach ihrer Härte auf der Skala: Korund, Graphit, CaF
Übungsaufgaben zur Vorlesung Chemie der Materialien Aufgabe 1: a) Was ist die Referenz für die Mohs Härteskala? b) Ordnen Sie die folgenden Festkörper nach ihrer Härte auf der Skala: Korund, Graphit, CaF
Metallbindung und Metalle Ionenbindung und Salze
 Metallbindung und Metalle Ionenbindung und Salze Patrick Bucher 18. Juli 2011 Inhaltsverzeichnis 1 Metalle 1 1.1 Metallgitter und metallische Bindung...................... 2 1.2 Chemische Eigenschaften
Metallbindung und Metalle Ionenbindung und Salze Patrick Bucher 18. Juli 2011 Inhaltsverzeichnis 1 Metalle 1 1.1 Metallgitter und metallische Bindung...................... 2 1.2 Chemische Eigenschaften
Zustände der Elektronen sind Orbitale, die durch 4 Quantenzahlen
 Wiederholung der letzten Vorlesungsstunde: Thema: Das wellenmechanische h Atommodell (Orbitalmodell) ll) Zustände der Elektronen sind Orbitale, die durch 4 Quantenzahlen beschrieben werden, Hauptquantenzahl
Wiederholung der letzten Vorlesungsstunde: Thema: Das wellenmechanische h Atommodell (Orbitalmodell) ll) Zustände der Elektronen sind Orbitale, die durch 4 Quantenzahlen beschrieben werden, Hauptquantenzahl
Informationen zur Feststellungsprüfung im Fach Chemie (T-Kurs)
 Informationen zur Feststellungsprüfung im Fach Chemie (T-Kurs) Stoffgebiete GRUNDBEGRIFFE Teilchen; Stoffsysteme, Mehrstoffsysteme; Elemente, Metalle; Verbindungen; Molekülverbindungen, Säuren; Ionenverbindungen,
Informationen zur Feststellungsprüfung im Fach Chemie (T-Kurs) Stoffgebiete GRUNDBEGRIFFE Teilchen; Stoffsysteme, Mehrstoffsysteme; Elemente, Metalle; Verbindungen; Molekülverbindungen, Säuren; Ionenverbindungen,
2. Chemische Bindungen 2.1
 2. Chemische Bindungen 2.1 Chemische Bindungen Deutung von Mischungsversuchen Benzin und Wasser mischen sich nicht. Benzin ist somit eine hydrophobe Flüssigkeit. Auch die Siedepunkte der beiden Substanzen
2. Chemische Bindungen 2.1 Chemische Bindungen Deutung von Mischungsversuchen Benzin und Wasser mischen sich nicht. Benzin ist somit eine hydrophobe Flüssigkeit. Auch die Siedepunkte der beiden Substanzen
Wiederholung: Duktilität
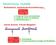 Wiederholung: Duktilität Bulkmaterial: prozentuale Bruchdehnung ε b lz l0 εb = l Dünne Schicht: 3-Punkt-Biegetest 0 l Z = Länge der Probe nach dem Bruch l 0 = Länge der Probe vor dem Bruch ε B = Bruchdehnung
Wiederholung: Duktilität Bulkmaterial: prozentuale Bruchdehnung ε b lz l0 εb = l Dünne Schicht: 3-Punkt-Biegetest 0 l Z = Länge der Probe nach dem Bruch l 0 = Länge der Probe vor dem Bruch ε B = Bruchdehnung
Eigenleitung von Germanium
 Eigenleitung von Germanium Fortgeschrittenen Praktikum I Zusammenfassung In diesem Versuch wird an einem undotierten Halbleiter die Temperaturabhängigkeit der elektrischen Leitfähigkeit bestimmt. Im Gegensatz
Eigenleitung von Germanium Fortgeschrittenen Praktikum I Zusammenfassung In diesem Versuch wird an einem undotierten Halbleiter die Temperaturabhängigkeit der elektrischen Leitfähigkeit bestimmt. Im Gegensatz
Elektrischer Widerstand als Funktion der Temperatur
 V10 Elektrischer Widerstand als Funktion der Temperatur 1. Aufgabenstellung 1.1 Messung Sie den elektrischen Widerstand vorgegebener Materialien als Funktion der Temperatur bei tiefen Temperaturen. 1.2
V10 Elektrischer Widerstand als Funktion der Temperatur 1. Aufgabenstellung 1.1 Messung Sie den elektrischen Widerstand vorgegebener Materialien als Funktion der Temperatur bei tiefen Temperaturen. 1.2
GMB 11.11.02. >5g/cm 3 <5g/cm 3. Gusseisen mit Lamellengraphit Gusseisen mit Kugelgraphit (Sphäroguss) (Magensiumbeisatz)
 GMB 11.11.02 1. Wie werden Metallische Werkstoffe eingeteilt? METALLE EISENWERKSTOFFE NICHTEISENWERKSTOFFE STÄHLE EISENGUSS- WERKSTOFFE SCHWERMETALLE LEICHTMETALLE >5g/cm 3
GMB 11.11.02 1. Wie werden Metallische Werkstoffe eingeteilt? METALLE EISENWERKSTOFFE NICHTEISENWERKSTOFFE STÄHLE EISENGUSS- WERKSTOFFE SCHWERMETALLE LEICHTMETALLE >5g/cm 3
Chemische Bindung. Chemische Bindung
 Chemische Bindung Atome verbinden sich zu Molekülen oder Gittern, um eine Edelgaskonfiguration zu erreichen. Es gibt drei verschiedene Arten der chemischen Bindung: Atombindung Chemische Bindung Gesetz
Chemische Bindung Atome verbinden sich zu Molekülen oder Gittern, um eine Edelgaskonfiguration zu erreichen. Es gibt drei verschiedene Arten der chemischen Bindung: Atombindung Chemische Bindung Gesetz
Die chemische Reaktion
 Die chemische Reaktion Die Chemie beschäftigt sich mit Stoffen und ihren Eigenschaften. Die Dinge in unserer Umwelt bestehen aus vielen verschiedenen Stoffen, die häufig miteinander vermischt sind. Mit
Die chemische Reaktion Die Chemie beschäftigt sich mit Stoffen und ihren Eigenschaften. Die Dinge in unserer Umwelt bestehen aus vielen verschiedenen Stoffen, die häufig miteinander vermischt sind. Mit
Phasendiagramme. Seminar zum Praktikum Modul ACIII
 Phasendiagramme Seminar zum Praktikum Modul ACIII Definition Phase Eine Phase ist ein Zustand der Materie, in dem sie bezüglich ihrer chemischen Zusammensetzung und bezüglich ihres physikalischen Zustandes
Phasendiagramme Seminar zum Praktikum Modul ACIII Definition Phase Eine Phase ist ein Zustand der Materie, in dem sie bezüglich ihrer chemischen Zusammensetzung und bezüglich ihres physikalischen Zustandes
Stoffeigenschaften und Teilchenmodell
 Stoffeigenschaften und Teilchenmodell Teilchenmodell (1) Alle Stoffe bestehen aus kleinsten Teilchen. (2) Zwischen den Teilchen wirken Anziehungskräfte. (3) Alle Teilchen befinden sich in ständiger, regelloser
Stoffeigenschaften und Teilchenmodell Teilchenmodell (1) Alle Stoffe bestehen aus kleinsten Teilchen. (2) Zwischen den Teilchen wirken Anziehungskräfte. (3) Alle Teilchen befinden sich in ständiger, regelloser
Thema heute: Grundlegende Ionenstrukturen
 Wiederholung der letzten Vorlesungsstunde Einfache Metallstrukturen, Dichtestpackung von "Atomkugeln", N Oktaeder-, 2N Tetraederlücken, Hexagonal-dichte Packung, Schichtfolge ABAB, hexagonale Elementarzelle,
Wiederholung der letzten Vorlesungsstunde Einfache Metallstrukturen, Dichtestpackung von "Atomkugeln", N Oktaeder-, 2N Tetraederlücken, Hexagonal-dichte Packung, Schichtfolge ABAB, hexagonale Elementarzelle,
Intermetallische Systeme, ( Legierungen ) Metalle
 Eigenschaften Metalle plastisch verformbar meist hohe Dichte ( Ausnahme: Leichtmetalle ) gute elektrische Leitfähigkeit gute Wärmeleitung optisch nicht transparent metallischer Glanz Intermetallische Systeme,
Eigenschaften Metalle plastisch verformbar meist hohe Dichte ( Ausnahme: Leichtmetalle ) gute elektrische Leitfähigkeit gute Wärmeleitung optisch nicht transparent metallischer Glanz Intermetallische Systeme,
Arten chemischer Bindungen
 Arten chemischer Bindungen Bindungsarten Atombindung (Kovalenzbindung) Ionenbindung Metallbindung Bindung in Komplexen Intermolekulare Wechselwirkungen polar unpolar Wasserstoffbrückenbindung Van-der-Waals-
Arten chemischer Bindungen Bindungsarten Atombindung (Kovalenzbindung) Ionenbindung Metallbindung Bindung in Komplexen Intermolekulare Wechselwirkungen polar unpolar Wasserstoffbrückenbindung Van-der-Waals-
Untersuchung von Einzelausscheidungen in Aluminiumlegierungen mit einem Positronenstrahl
 Untersuchung von Einzelausscheidungen in Aluminiumlegierungen mit einem Positronenstrahl von Osman Balarisi Diplomarbeit in Physik angefertigt am Helmholtz-Institut für Strahlen- und Kernphysik vorgelegt
Untersuchung von Einzelausscheidungen in Aluminiumlegierungen mit einem Positronenstrahl von Osman Balarisi Diplomarbeit in Physik angefertigt am Helmholtz-Institut für Strahlen- und Kernphysik vorgelegt
Fällungsreaktion. Flammenfärbung. Fällungsreaktion:
 2 Fällungsreaktion: 2 Fällungsreaktion Entsteht beim Zusammengießen zweier Salzlösungen ein Niederschlag eines schwer löslichen Salzes, so spricht man von einer Fällungsreaktion. Bsp: Na + (aq) + Cl -
2 Fällungsreaktion: 2 Fällungsreaktion Entsteht beim Zusammengießen zweier Salzlösungen ein Niederschlag eines schwer löslichen Salzes, so spricht man von einer Fällungsreaktion. Bsp: Na + (aq) + Cl -
2 Gleichgewichtssysteme
 Studieneinheit III Gleichgewichtssysteme. Einstoff-Systeme. Binäre (Zweistoff-) Systeme.. Grundlagen.. Systeme mit vollständiger Mischbarkeit.. Systeme mit unvollständiger Mischbarkeit..4 Systeme mit Dreiphasenreaktionen..4.
Studieneinheit III Gleichgewichtssysteme. Einstoff-Systeme. Binäre (Zweistoff-) Systeme.. Grundlagen.. Systeme mit vollständiger Mischbarkeit.. Systeme mit unvollständiger Mischbarkeit..4 Systeme mit Dreiphasenreaktionen..4.
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 Chemie für Biologen Vorlesung im WS 200/05 V2, Mi 10-12, S0 T01 A02 Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen (Teil : 03.11.200) MILESS: Chemie für Biologen 66 Chemische
Chemie für Biologen Vorlesung im WS 200/05 V2, Mi 10-12, S0 T01 A02 Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen (Teil : 03.11.200) MILESS: Chemie für Biologen 66 Chemische
Einfache Kristallstrukturen
 Einfache Kristallstrukturen Konstruktion von Kristallen: Kugelpackungen - hexagonal und kubisch dichteste Packungen - kubisch einfache Packung - kubisch innenzentrierte Packung Kristallstrukturen der Metalle
Einfache Kristallstrukturen Konstruktion von Kristallen: Kugelpackungen - hexagonal und kubisch dichteste Packungen - kubisch einfache Packung - kubisch innenzentrierte Packung Kristallstrukturen der Metalle
B II 7 Leitfähigkeit in lonenkristallen
 B II 7 Leitfähigkeit in lonenkristallen Die elektrische Leitfähigkeit von festen Stoffen ist von den Metallen (1 6 Ohm -1 cm -1 ) bis zum Quarz (1-18 Ohm -1 cm -1 ) bei Zimmertemperatur über 24 bis 25
B II 7 Leitfähigkeit in lonenkristallen Die elektrische Leitfähigkeit von festen Stoffen ist von den Metallen (1 6 Ohm -1 cm -1 ) bis zum Quarz (1-18 Ohm -1 cm -1 ) bei Zimmertemperatur über 24 bis 25
3 Elektrische Leitung
 3.1 Strom und Ladungserhaltung 3 Elektrische Leitung 3.1 Strom und Ladungserhaltung Elektrischer Strom wird durch die Bewegung von Ladungsträgern hervorgerufen. Er ist definiert über die Änderung der Ladung
3.1 Strom und Ladungserhaltung 3 Elektrische Leitung 3.1 Strom und Ladungserhaltung Elektrischer Strom wird durch die Bewegung von Ladungsträgern hervorgerufen. Er ist definiert über die Änderung der Ladung
Bindungsarten und ihre Eigenschaften
 Bindungsarten und ihre Eigenschaften Atome sowohl desselben als auch verschiedener chemischer Elemente können sich miteinander verbinden. Dabei entstehen neue Stoffe, die im Allgemeinen völlig andere Eigenschaften
Bindungsarten und ihre Eigenschaften Atome sowohl desselben als auch verschiedener chemischer Elemente können sich miteinander verbinden. Dabei entstehen neue Stoffe, die im Allgemeinen völlig andere Eigenschaften
Grundwissenskatalog Chemie G8 8. Klasse nt
 Grundwissenskatalog Chemie G8 8. Klasse nt 1. Wissenschaft Chemie: Chemie ist die Lehre von den Stoffen. Chemischer Vorgang: Stoffänderung Physikalischer Vorgang: Zustandsänderung 2. Unterteilung Stoffe:
Grundwissenskatalog Chemie G8 8. Klasse nt 1. Wissenschaft Chemie: Chemie ist die Lehre von den Stoffen. Chemischer Vorgang: Stoffänderung Physikalischer Vorgang: Zustandsänderung 2. Unterteilung Stoffe:
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg
 TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg PROTOKOLL Modul: Versuch: Physikalische Eigenschaften I. VERSUCHSZIEL Die
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg PROTOKOLL Modul: Versuch: Physikalische Eigenschaften I. VERSUCHSZIEL Die
4.4 Induktion. Bisher: Strom durch einen Draht Magnetfeld Jetzt: zeitlich veränderliches Magnetfeld Strom
 Bisher: Strom durch einen Draht Magnetfeld Jetzt: zeitlich veränderliches Magnetfeld Strom 4.4 Induktion Spannungen und Ströme, die durch Veränderungen von Magnetfeldern entstehen, bezeichnet man als Induktionsspannungen,
Bisher: Strom durch einen Draht Magnetfeld Jetzt: zeitlich veränderliches Magnetfeld Strom 4.4 Induktion Spannungen und Ströme, die durch Veränderungen von Magnetfeldern entstehen, bezeichnet man als Induktionsspannungen,
Der Schmelzpunkt von Salzen
 Der Schmelzpunkt von Salzen Vergleich die Smp. der Salze (links). Welche Rolle könnten die Ionenradien bzw. die Ladung der enthaltenen Ionen spielen? Der Schmelzpunkt von Salzen ist i.d.r. sehr hoch. Er
Der Schmelzpunkt von Salzen Vergleich die Smp. der Salze (links). Welche Rolle könnten die Ionenradien bzw. die Ladung der enthaltenen Ionen spielen? Der Schmelzpunkt von Salzen ist i.d.r. sehr hoch. Er
18. Magnetismus in Materie
 18. Magnetismus in Materie Wir haben den elektrischen Strom als Quelle für Magnetfelder kennen gelernt. Auch das magnetische Verhalten von Materie wird durch elektrische Ströme bestimmt. Die Bewegung der
18. Magnetismus in Materie Wir haben den elektrischen Strom als Quelle für Magnetfelder kennen gelernt. Auch das magnetische Verhalten von Materie wird durch elektrische Ströme bestimmt. Die Bewegung der
Einführung in die Kristallographie
 Einführung in die Kristallographie Gerhard Heide Institut für Mineralogie Professur für Allgemeine und Angewandte Mineralogie Brennhausgasse 14 03731-39-2665 oder -2628 gerhard.heide@mineral.tu-freiberg.de
Einführung in die Kristallographie Gerhard Heide Institut für Mineralogie Professur für Allgemeine und Angewandte Mineralogie Brennhausgasse 14 03731-39-2665 oder -2628 gerhard.heide@mineral.tu-freiberg.de
Schulversuchspraktikum WS2000/2001 Redl Günther 9655337. Elektromagnet. 7.Klasse
 Schulversuchspraktikum WS2000/2001 Redl Günther 9655337 Elektromagnet 7.Klasse Inhaltsverzeichnis: 1) Lernziele 2) Verwendete Quellen 3) Versuch nach Oersted 4) Magnetfeld eines stromdurchflossenen Leiter
Schulversuchspraktikum WS2000/2001 Redl Günther 9655337 Elektromagnet 7.Klasse Inhaltsverzeichnis: 1) Lernziele 2) Verwendete Quellen 3) Versuch nach Oersted 4) Magnetfeld eines stromdurchflossenen Leiter
= 8.28 10 23 g = 50u. n = 1 a 3 = = 2.02 10 8 = 2.02Å. 2 a. k G = Die Dispersionsfunktion hat an der Brillouinzonengrenze ein Maximum; dort gilt also
 Aufgabe 1 Ein reines Material habe sc-struktur und eine Dichte von 10 g/cm ; in (1,1,1) Richtung messen Sie eine Schallgeschwindigkeit (für große Wellenlängen) von 000 m/s. Außerdem messen Sie bei nicht
Aufgabe 1 Ein reines Material habe sc-struktur und eine Dichte von 10 g/cm ; in (1,1,1) Richtung messen Sie eine Schallgeschwindigkeit (für große Wellenlängen) von 000 m/s. Außerdem messen Sie bei nicht
1.6. Die Ionenbindung
 1.6. Die Ionenbindung 1.6.1. Die Edelgasregel Die Edelgase gehen kaum Verbindungen ein und zeigen in ihrer Periode jeweils die höchsten Ionisierungsenergien. Ihre Elektronenkonfiguration mit jeweils Außenelektronen
1.6. Die Ionenbindung 1.6.1. Die Edelgasregel Die Edelgase gehen kaum Verbindungen ein und zeigen in ihrer Periode jeweils die höchsten Ionisierungsenergien. Ihre Elektronenkonfiguration mit jeweils Außenelektronen
Halbleitergrundlagen
 Halbleitergrundlagen Energie W Leiter Halbleiter Isolator Leitungsband Verbotenes Band bzw. Bandlücke VB und LB überlappen sich oder LB nur teilweise mit Elektronen gefüllt Anzahl der Elektronen im LB
Halbleitergrundlagen Energie W Leiter Halbleiter Isolator Leitungsband Verbotenes Band bzw. Bandlücke VB und LB überlappen sich oder LB nur teilweise mit Elektronen gefüllt Anzahl der Elektronen im LB
Polymorphie Festkörperpraktikum Modul AC III 23.04.2014
 Polymorphie 1. Definitionen - Polymorphie Isotyp: Verbindungen mit gleicher Kristallstruktur aber unterschiedlichem Bindungstyp Isomorph: Verbindungen mit gleicher Kristallstruktur und gleichem Bindungstyp
Polymorphie 1. Definitionen - Polymorphie Isotyp: Verbindungen mit gleicher Kristallstruktur aber unterschiedlichem Bindungstyp Isomorph: Verbindungen mit gleicher Kristallstruktur und gleichem Bindungstyp
Die Companion Website (CWS) zum Buch... 16. Kapitel 1 Einleitung und chemische Begriffsbestimmung 17
 Vorwort 15 Die Companion Website (CWS) zum Buch......................... 16 Kapitel 1 Einleitung und chemische Begriffsbestimmung 17 1.1 Was ist Chemie und warum ist sie wichtig?.........................
Vorwort 15 Die Companion Website (CWS) zum Buch......................... 16 Kapitel 1 Einleitung und chemische Begriffsbestimmung 17 1.1 Was ist Chemie und warum ist sie wichtig?.........................
Stoffeigenschaften und Teilchenmodell
 Stoffeigenschaften und Teilchenmodell Teilchenmodell (1) Alle Stoffe bestehen aus kleinsten Teilchen. (2) Zwischen den Teilchen wirken Anziehungskräfte. (3) Alle Teilchen befinden sich in ständiger, regelloser
Stoffeigenschaften und Teilchenmodell Teilchenmodell (1) Alle Stoffe bestehen aus kleinsten Teilchen. (2) Zwischen den Teilchen wirken Anziehungskräfte. (3) Alle Teilchen befinden sich in ständiger, regelloser
Verbindungen zwischen Nichtmetallatomen. Verbindungen zwischen Metallen und Nichtmetallen (in Form ihrer Ionen)
 Grundwissen Chemie 1. Stoffe 1.1. Reinstoffe können durch physikalische Trennverfahren nicht zerlegt werden. Sie sind gekennzeichnet durch charakteristische Kenneigenschaften (Siedepunkt, Schmelzpunkt,
Grundwissen Chemie 1. Stoffe 1.1. Reinstoffe können durch physikalische Trennverfahren nicht zerlegt werden. Sie sind gekennzeichnet durch charakteristische Kenneigenschaften (Siedepunkt, Schmelzpunkt,
Der Einfluß der Gitterfehler auf die mechanischen Eigenschaften der Metalle
 Der Einfluß der Gitterfehler auf die mechanischen Eigenschaften der Metalle Einführung Das gewählte Thema ist ein gutes Beispiel zur Verdeutlichung dessen, was man unter Werkstoffwissenschaften (Werkstofftechnik)
Der Einfluß der Gitterfehler auf die mechanischen Eigenschaften der Metalle Einführung Das gewählte Thema ist ein gutes Beispiel zur Verdeutlichung dessen, was man unter Werkstoffwissenschaften (Werkstofftechnik)
Allotrope Kohlenstoffmodifikationen. Ein Vortrag von Patrick Knicknie. Datum: 04.05.06 Raum:112
 Allotrope Kohlenstoffmodifikationen Ein Vortrag von Patrick Knicknie Datum: 04.05.06 Raum:112 Themen: 1. Was ist Allotrop? 2. Unterschiedliche Kohlenstoffmodifikationen 3. Der Graphit 4. Der Diamant 5.
Allotrope Kohlenstoffmodifikationen Ein Vortrag von Patrick Knicknie Datum: 04.05.06 Raum:112 Themen: 1. Was ist Allotrop? 2. Unterschiedliche Kohlenstoffmodifikationen 3. Der Graphit 4. Der Diamant 5.
Allgemeine Chemie. SS 2014 Thomas Loerting. Thomas Loerting Allgemeine Chemie
 Allgemeine Chemie SS 2014 Thomas Loerting 1 Inhalt 1 Der Aufbau der Materie (Teil 1) 2 Die chemische Bindung (Teil 2) 3 Die chemische Reaktion (Teil 3) 2 Definitionen von den an einer chemischen Reaktion
Allgemeine Chemie SS 2014 Thomas Loerting 1 Inhalt 1 Der Aufbau der Materie (Teil 1) 2 Die chemische Bindung (Teil 2) 3 Die chemische Reaktion (Teil 3) 2 Definitionen von den an einer chemischen Reaktion
Welche Eigenschaften haben Werkstoffe? --> alle Werkstoffe sind fest. 1) Festkörperphysik 2) physikalische Chemie 3) Festkörperchemie
 Welche Eigenschaften haben Werkstoffe? --> alle Werkstoffe sind fest 1) Festkörperphysik 2) physikalische Chemie 3) Festkörperchemie --> beschäftigen sich mit Bildung/Aufbau/Eigenschaften fester Stoffe
Welche Eigenschaften haben Werkstoffe? --> alle Werkstoffe sind fest 1) Festkörperphysik 2) physikalische Chemie 3) Festkörperchemie --> beschäftigen sich mit Bildung/Aufbau/Eigenschaften fester Stoffe
Naturwissenschaft Vermutungswissen Alles ist Chemie!!! Analyse Synthese
 SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
Klausur Vertiefungsfach 2: Master
 I E H K Institut für Eisenhüttenkunde Rheinisch-Westfälische Technische Hochschule Aachen Klausur Vertiefungsfach 2: Master Stahlmetallurgie Univ.-Prof. Dr.-Ing. D. Senk 10.09.2012 Nachname, Vorname: Matrikel-Nr.:
I E H K Institut für Eisenhüttenkunde Rheinisch-Westfälische Technische Hochschule Aachen Klausur Vertiefungsfach 2: Master Stahlmetallurgie Univ.-Prof. Dr.-Ing. D. Senk 10.09.2012 Nachname, Vorname: Matrikel-Nr.:
Packung, Oktaeder-, Tetraederlücken, kubisch-innenzentrierte Packung, Raumausfüllung, Ionenstrukturen - abgeleitet von Ionendichtestpackungen,
 Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung / Salzstrukturen Der metallische Zustand, Dichtestpackung von Kugeln, hexagonal-, kubischdichte Packung, Oktaeder-, Tetraederlücken, kubisch-innenzentrierte
Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung / Salzstrukturen Der metallische Zustand, Dichtestpackung von Kugeln, hexagonal-, kubischdichte Packung, Oktaeder-, Tetraederlücken, kubisch-innenzentrierte
Empfohlene Hilfsmittel zum Lösen der Arbeitsaufträge: Arbeitsblätter, Theorieblätter, Fachbuch, Tabellenbuch und Ihr Wissen aus dem Praxisalltag
 2.1.1 Aufbau der Materie (Arbeitsaufträge) Empfohlene Hilfsmittel zum Lösen der Arbeitsaufträge: Arbeitsblätter, Theorieblätter, Fachbuch, Tabellenbuch und Ihr Wissen aus dem Praxisalltag 1. Beim Bearbeiten
2.1.1 Aufbau der Materie (Arbeitsaufträge) Empfohlene Hilfsmittel zum Lösen der Arbeitsaufträge: Arbeitsblätter, Theorieblätter, Fachbuch, Tabellenbuch und Ihr Wissen aus dem Praxisalltag 1. Beim Bearbeiten
Vorbereitung: Eigenschaften elektrischer Bauelemente
 Vorbereitung: Eigenschaften elektrischer Bauelemente Marcel Köpke & Axel Müller 15.06.2012 Inhaltsverzeichnis 1 Grundlagen 3 2 Aufgaben 7 2.1 Temperaturabhängigkeit............................ 7 2.2 Kennlinien....................................
Vorbereitung: Eigenschaften elektrischer Bauelemente Marcel Köpke & Axel Müller 15.06.2012 Inhaltsverzeichnis 1 Grundlagen 3 2 Aufgaben 7 2.1 Temperaturabhängigkeit............................ 7 2.2 Kennlinien....................................
