Lösungshinweise zu alten Prüfungsaufgaben. = c 2 V 1 V 2. =1nM 1000 ml nm V 1
|
|
|
- Susanne Bayer
- vor 6 Jahren
- Abrufe
Transkript
1 Lösungshinweise zu alten Prüfungsaufgaben Die Lösungshinweise sind ohne Gewähr! Das Dokument wurde in erster Linie erstellt, damit Sie prüfen können, ob Sie die alten Prüfungsaufgaben richtig gerechnet haben. Entsprechend findet sich i.d.r. nur das Endergebnis der rechnerisch zu lösenden Teilaufgaben. Bei anderen Teilaufgaben finden sich, wenn überhaupt, nur einzelne Schlüsselworte um Ihnen eine Hilfestellung für die grobe Richtung der Antwort zu geben. Die Hinweise sind also keinesfalls vollständig. Die Lösen sind umgekehrt chronologisch sortiert. AW1 Sommer 2014 Cadmium im Boden m(cd(no 3) 2) = 147,8 mg Beispiel. Es gibt mehrere Lösungswege! Am genauesten sind solche Lösungswege, bei denen die pipettierenden Volumina möglichst groß ausfallen, da kleinere Pipettiervolumina zu größeren Fehlern führen. Hier wird deshalb ein Weg vorgestellt der nur 1000mLMesskolben nutzt und deshalb Pipettiervolumina unter 400 µl meidet. Zwischenverdünnung: 1000 µl Stammlsg. ad 1000 ml verdünnen. result. c: 2,5 µm = 2500 nm Verdünnungsformel: z.b. c 1 V 1 Zwischenverdünnung 2500 nm V 1 Zwischenverdünnung Wunschlösung = c 2 V 2 =1nM 1000 ml Wunschlösung V 1 =0,4 ml(400μ L) c 1 = 2500 nm c 2: Wunschgehalt in nm V 1: zu Pipettierendes Volumen an Zwischenverdünnung V 2: Wunschvolumen. hier gewählt: 1000 ml Gehalt der Wunschlösung Zu pipettierendes Volumen an Zwischenverdünnung (V2) in µl 1 nm nm nm nm nm β = 407,8 ng/l jeweils ad 1000 µl verdünnen AW2 Sommer 2014 Prolin im OSaft β = 593,0 mg/l AW3 Sommer 2014 FTIR Paracetamol
2 AW4 Sommer 2014 Lebensmittelfarbstoffe AW5 Sommer 2014 Grignard AW6 Sommer 2014 Alu AW7 Sommer 2014 Nickel t = 7,6 h c = 0,25 mol/l AW8 Sommer 2014 Potentiometrie Ammoniak 8.2 ÄP = 12,5 ml, ph = 5,8 8.5 m(nh 3) = 30,2 mg AW9 Sommer 2014 Iodometrie 9.3 t = 1, β(so 3 2 ) = 85,7 mg/l AW1 Winter 2013/2014 AW2 Winter 2013/ w(myr.säure.ester) = 16,5% ; w(palm.säure.ester) = 39,0% ; wstear.säure.ester) = 44,5% AW3 Winter 2013/2014 AW4 Winter 2013/ A = 0, β(cu 2+ ) = 33,4 mg/l
3 AW4 Winter 2013/ c(mno 4 ) = 0,54 mmol/l L 5.5 ε 460 mol cm (aus Geradensteigung) AW6 Winter 2013/2014 Ammoniaksynthese 6.2 K c 0,0024 L2 mol φ =28% AW7 Winter 2013/2014 Abflussreiniger w(naoh) = 0, w(naoh) = 0,275 AW8 Winter 2013/2014 Lakritz 8.2 C = 0,788 cm w(nh 4Cl) = 2,0% Grenzwert ist gerade erreicht AW9 Winter 2013/2014 Phosphat in Düngmittel w(po 4 3 ) = 15,0% AW1 Sommer R = 1,14 Da R < 1,5 : Trennung ist unvollständig AW2 Sommer 2013) c(ca 2+ ) 11,4 mg/l AW3 Sommer β(cof) = 138 mg/ml AW4 Sommer β(aspartam) = 0,5 g/l W(Cola) = 935 kj W(Cola light) = 4,3 kj AW5 Sommer 2013
4 AW6 Sommer 2013 AW7 Sommer t = 1, m(mgco 3) = 208,53 mgm(caco 3) = 247,54 mg w(caco 3+MgCO3) = 91,58% AW8 Sommer t = 0, c(nh 3)= 14,80 mol/l 8.5 ph 5,6 AW9 Sommer w(ag) = 98,49% 9.3 c(ag + ) = 1, mol/l m(ag + ) = 0,27 mg AW1 Winter 2012/ m(phenol) = 29 g AW2 Winter 2012/2013 AW3 Winter 2012/ w 4,08% AW4 Winter 2012/2013 AW5 Winter 2012/2013 AW6 Winter 2012/2013) 6.5 w(al 2O 3) 13,81% AW7 Winter 2012/ m(kio 3) = 89 mg
5 7.4 IZ 84,9 AW8 Winter 2012/2013 AW9 Winter 2012/ G = 1347 μs AW1 Sommer Innerhalb von 24 h werden 60,4% Toluen abgebaut. AW2 Sommer 2012 AW3 Sommer 2012 AW4 Sommer β(lyc) = 4,14 mg/l Es müssen 64 ml Lösungsmittel dazu gegeben werden. AW5 Sommer 2012 AW6 Sommer ph(hclo 4) 1,3 ph(hclo) 4, ph 10,0 AW7 Sommer ph 5,1 AW8 Sommer w(fe 3+ ) = 16,9% AW9 Sommer w(n) = 0,26%
6 AC1 Winter 2011/ m³ AC2 Winter 2011/ ,64 t t c = 1,55 mmol/l AC3 Winter 2011/2012) 3.1 w = 48,61% 3.2 c = 0,00001 mol/l 3.3 0,233 mg AC4 Winter 2011/ ,38% n(fe 2+ ) : n(mno 4 ) = 5 : w = 1,14% WQ1 Winter 2011/2012 WQ2 Winter 2011/ m(hbr) rein = 28,86 g m(hbr) techn = 30,4 g WQ3 Winter 2011/ ΔU = 0,601 V WQ4 Winter 2011/ η(mg) = 82,1% 4.3 R = 0, Ω kwh WQ5 Winter 2011/ Wert X = 9 mg/l Wert Y = 0,338
7 mg/l AC1 Sommer ,6 mg 1.2 t = 0, ,1% AC2 Sommer ,527% 2.3 ΔU = 1,6 V AC3 Sommer t(hcl)= 1,0062 t(naoh) = 1, w(mgcl 2) = 74,7% AC4 Sommer p = 1,102 bar Zunahme um 10,2% AC5 Sommer β = 6,05 µg/ml WQ1 Sommer ΔU = 0,03 V 1.3 ΔU 0 = 0,03 V 1.4 ΔU = 0,0 V => System im Gleichgewicht 1.5 ΔU = 0,03 V WQ2 Sommer p = 7500 bar WQ3 Sommer ,7 mg V(1) = 0,25 ml V(2) = 0,75 ml V(3) = 1,25 ml V(4) = 1,75 ml ε mittel = 0,514 L mg 1 cm 1
8 3.3.3 β = 4,11 mg/l WQ4 Sommer 2011 AC1 Winter 2010/ w(fe 3+ ) = 99%, Δm = 0,4 mg, liegt im Toleranzbereich ,6% AC2 Winter 2010/ ph =2,6 2.3 HÄP bei ph = 4,9 = pk s(propansäure) ph = 9, ,94 g AC3 Winter 2010/ σ(etoh) = 0,85% kann nicht verwendet werden AC4 Winter 2010/2011) 4.2 m(li) = 13 kg m(cl 2) = 66,5 kg AC5 Winter 2010/ ,0253 mol/l WQ1 Winter 2010/2011 WQ2 Winter 2010/2011 WQ3 Winter 2010/2011 WQ4 Winter 2010/ ε mittel = L mol 1 cm , mol/l
9 WQ5 Winter 2010/ h 34 min AC1 Sommer 2010 AC2 Sommer w(nh 3) = 91,5% ,3 g AC3 Sommer f = 0, Messkolben: 500 ml, Vollpipette: 20 ml AC4 Sommer Valin: Rf = 0,7 Serin: Rf = 0,35Asparaginsäure: Rf = 0,15 AC5 Sommer Nr. Probe (µl) Standard (µl) Hexan (µl) βstandard) (ng/ml) WQ1 Sommer 2010) WQ2 Sommer 2010) WQ3 Sommer 2010) 3.3 W = kwh, 1654 WQ4 Sommer 2010) ε mittel = L mol 1 cm 1 : Ausreißer werden nicht berücksichtigt!
10 ,43 g/l: Ausreißer/Extreme nicht berücksichtigt WQ5 Sommer 2010) 5.4 6,4 mg/l AC1 Winter 2009/2010) 1.3 damit sich kein explosives H 2/Cl 2Gesmich ( Chlorknallgas ) bildet. 1.4 ph = 13, m 3 AC2 Winter 2009/2010) g ,4% AC3 Winter 2009/2010) 3.3 t = 0, w = 88,6% AC4 Winter 2009/2010) 4.6 5,72% AC5 Winter 2009/2010) WQ 1 Winter 2009/2010) 1.1 bei 340 nm absorbiert nur NADH und kann dort ohne NAD erfasst werden. 1.2 Veränderung des pielektronensystems. 1.3 β = 1,43 g/l, w = 1,43 WQ2 Winter 2009/2010) 2.6 Probe: β(cu) = 19 mg/l 2.7. Steigung wird kleiner. LBGesetz nicht mehr anwendbar. WQ3 Winter 2009/2010)
11 WQ4 Winter 2009/2010) WQ5 Winter 2009/2010) 5.1 Pb/Pb 2+ Anode, Minuspol H 3O +, H 2 Kathode, Pluspol 5.2 Ox: Pb wird zu Pb 2+ Red: Teilgleichung mit H 3O + /H c(pb 2+ ) = 8, mol/l 5.4 Pb 2+ Konz. nimmt ab, Potential der Halbzelle sinkt, Spannung (Potentialdifferenz) steigt U(Pb/Pb 2+ ) = 0,89 V AC1 Sommer 2009 Düngemittel 1.3 w(nh 4NO 3) = 27,0% w(n) = 9,44% AC2 Sommer 2009 Drogenanalyse AC3 Sommer 2009 Schwermetallentsorgung 3.2 β(pb 2+ ) = 3, g/l σ(h 2S) = 5,09% AC4 Sommer 2009 Silbermünzen 4.4 w(ag) = 90% AC5 Sommer 2009 SäureBaseTitration 5.5 Kurve 1: c 0(HAc) = 0,14 mol/l Kurve 2: c 0(HCl) = 0,1 mol/l WQ1 Sommer 2009 Carbonylverbindungen 1.4 η = 76,8% WQ2 Sommer 2009 IRSpektrometrie WQ 3 Sommer 2009 Fotometrie 3.1 β = 24,3 mg/l
12 3.2 ε spez = 23,1 L g 1 cm 1 ε molar = 7392 L mol 1 cm τ = 0,8 E = 0,097 WQ4 Sommer 2009 Atomabsorptionsspektrometrie 4.4 Probenr. Probevolumen in Standardvolumen Standardkonz. Absorbanz ml in ml β(ni 2+ ) in mg/l , , , ,338 β(ni 2+ ) = 270 mg/l WQ5 Sommer 2009 Elektrolyse 5.6 W el = kwh AC1 Winter 2008/2009 Gravimetrie 1.2 w(al) = 43,7% AC2 Winter 2008/2009 Volumetrie 2.2 t(h2so4) = 1,045 c(h2so4) = 0,0523 mol/l AC3 Winter 2008/2009 Manganometrie 3.2 m(kmno 4) = 1,5803 g 3.4 w = 9,17% AC4 Winter 2008/2009 Atombau/Periodensystem V(H 2) = 3,08 m³ AC5 Winter 2008/2009 Gaschromatographie WQ1 Winter 2008/2009 Farbstoffe
13 WQ2 Winter 2008/2009 Dicarbonsäuren ph = 3,0 WQ3 Winter 2008/2009 Konduktometrie 3.2 G = 11,7 ms κ = 9,91 ms/cm WQ4 Winter 2008/2009 Atomabsorptionsspektrometrie 4.3 ε 0,2007 L mmol cm WQ5 Winter 2008/2009 Infrarotspektrometrie AC1 Sommer w = 90,06% ,5418 mol/l AC2 Sommer 2008 AC3 Sommer cs 2 ) = mol/l 3.2 m(ni 2+ ) = 1, mg AC4 Sommer 2008 AC4 Sommer 2008
Standardadditionsverfahren (Eichzusatzverfahren)
 Standardadditionsverfahren (Eichzusatzverfahren) C3CL 1. Eine Farbstofflösung besitzt bei einer Messung in einem Fotometer (Schichtdicke und Wellenlänge unbekannt) die Absorbanz von A= 0,393. Berechnen
Standardadditionsverfahren (Eichzusatzverfahren) C3CL 1. Eine Farbstofflösung besitzt bei einer Messung in einem Fotometer (Schichtdicke und Wellenlänge unbekannt) die Absorbanz von A= 0,393. Berechnen
Übungsaufgabe 1. Photometrische Bestimmung von Chrom als Chromat Chemikalien: H 2 O 2, Natronlauge, Chrom-(III)-salz
 Übungsaufgabe 1 Photometrische Bestimmung von Chrom als Chromat Chemikalien: H 2 O 2, Natronlauge, Chrom-(III)-salz Versuchsbeschreibung: 20 ml der erhaltenen Probelösung werden in ein 150 ml Becherglas
Übungsaufgabe 1 Photometrische Bestimmung von Chrom als Chromat Chemikalien: H 2 O 2, Natronlauge, Chrom-(III)-salz Versuchsbeschreibung: 20 ml der erhaltenen Probelösung werden in ein 150 ml Becherglas
Verdünnungsaufgaben aus dem Laboralltag
 Verdünnungsaufgaben aus dem Laboralltag Biolaboranten 1. Aus einer lösung mit β 0 = 50 mg/l soll eine Verdünnungsreihe mit 4 Verdünnungen hergestellt werden. Zusammen sollen die 5 Lösungen den Konzentrationsbereich
Verdünnungsaufgaben aus dem Laboralltag Biolaboranten 1. Aus einer lösung mit β 0 = 50 mg/l soll eine Verdünnungsreihe mit 4 Verdünnungen hergestellt werden. Zusammen sollen die 5 Lösungen den Konzentrationsbereich
Übung 10 (Redox-Gleichgewichte und Elektrochemie)
 Übung 10 (Redox-Gleichgewichte und Elektrochemie) Verwenden Sie neben den in der Aufgabenstellung gegebenen Potenzialen auch die Werte aus der Potenzial-Tabelle im Mortimer. 1. Ammoniak kann als Oxidationsmittel
Übung 10 (Redox-Gleichgewichte und Elektrochemie) Verwenden Sie neben den in der Aufgabenstellung gegebenen Potenzialen auch die Werte aus der Potenzial-Tabelle im Mortimer. 1. Ammoniak kann als Oxidationsmittel
Chemisches Rechnen. Diese Lerneinheit befasst sich mit verschiedenen chemisch relevanten Größen Konzentrationsangaben mit den folgenden Lehrzielen:
 Chemisches Rechnen Diese Lerneinheit befasst sich mit verschiedenen chemisch relevanten Größen Konzentrationsangaben mit den folgenden Lehrzielen: Verständnis der unterschiedlichen Größen Sichere Anwendung
Chemisches Rechnen Diese Lerneinheit befasst sich mit verschiedenen chemisch relevanten Größen Konzentrationsangaben mit den folgenden Lehrzielen: Verständnis der unterschiedlichen Größen Sichere Anwendung
Für enzymkinetische Untersuchungen legen Sie 0.2 ml einer 5 mm Substratlösung vor. Der fertige Inkubationsansatz hat ein Volumen von 2 ml.
 Die Gehschule ist ein Teil der Biochemischen Übungen für das Bakkalaureat LMBT. Der Test wird im Anschluss an die Prüfung aus Grundlagen der Biochemie angeboten, welche 90 min dauert (also bei der Türe
Die Gehschule ist ein Teil der Biochemischen Übungen für das Bakkalaureat LMBT. Der Test wird im Anschluss an die Prüfung aus Grundlagen der Biochemie angeboten, welche 90 min dauert (also bei der Türe
LF - Leitfähigkeit / Überführung
 Verfasser: Matthias Ernst, Tobias Schabel Gruppe: A 11 Betreuer: G. Heusel Datum: 18.11.2005 Aufgabenstellung LF - Leitfähigkeit / Überführung 1) Es sind die Leitfähigkeiten von zwei unbekanten Elektrolyten
Verfasser: Matthias Ernst, Tobias Schabel Gruppe: A 11 Betreuer: G. Heusel Datum: 18.11.2005 Aufgabenstellung LF - Leitfähigkeit / Überführung 1) Es sind die Leitfähigkeiten von zwei unbekanten Elektrolyten
Experimentelle Durchführung u. Eingabe der Ergebnisse Gruppen-Nr C2
 7-Eisen_Komplex_pH-08.xls Fe_Phe_pH 2.08.2007 ph-abhängige Bildung eines gefärbten Eisen-Chelat-Komplexes. Photometrische Bestimmung der Gesamt-Komplexbildungskonstanten. Datum 01.05.2006 Experimentelle
7-Eisen_Komplex_pH-08.xls Fe_Phe_pH 2.08.2007 ph-abhängige Bildung eines gefärbten Eisen-Chelat-Komplexes. Photometrische Bestimmung der Gesamt-Komplexbildungskonstanten. Datum 01.05.2006 Experimentelle
Redoxreaktionen. Mg + ½ O 2. MgO. 3 Mg + N 2 Mg 3 N 2. Mg ½ O + 2 e O 2. 3 Mg 3 Mg e
 Redoxreaktionen Mg + ½ O 2 MgO 3 Mg + N 2 Mg 3 N 2 2 Mg ½ O + 2 e 2+ Mg + 2 e O 2 3 Mg 3 Mg 2+ + 6 e N + 6 e 2 N 3 2 1 Redoxreaktionen 2 Oxidation und Reduktion Eine Oxidation ist ein Elektronenverlust
Redoxreaktionen Mg + ½ O 2 MgO 3 Mg + N 2 Mg 3 N 2 2 Mg ½ O + 2 e 2+ Mg + 2 e O 2 3 Mg 3 Mg 2+ + 6 e N + 6 e 2 N 3 2 1 Redoxreaktionen 2 Oxidation und Reduktion Eine Oxidation ist ein Elektronenverlust
Das Potenzial einer Halbzelle lässt sich mittels der Nernstschen Gleichung berechnen. oder
 Zusammenfassung Redoxreaktionen Oxidation entspricht einer Elektronenabgabe Reduktion entspricht einer Elektronenaufnahme Oxidation und Reduktion treten immer gemeinsam auf Oxidationszahlen sind ein Hilfsmittel
Zusammenfassung Redoxreaktionen Oxidation entspricht einer Elektronenabgabe Reduktion entspricht einer Elektronenaufnahme Oxidation und Reduktion treten immer gemeinsam auf Oxidationszahlen sind ein Hilfsmittel
Redoxtitrationen. Redox-Reaktionen Oxidation und Reduktion
 RedoxReaktionen Oxidation und Reduktion Redoxtitrationen Beschreibung der Lage von Redoxgleichgewichten Standardpotentiale, Spannungsreihe Nernst sche Gleichung Berechnung von Titrationskurven Indikationen
RedoxReaktionen Oxidation und Reduktion Redoxtitrationen Beschreibung der Lage von Redoxgleichgewichten Standardpotentiale, Spannungsreihe Nernst sche Gleichung Berechnung von Titrationskurven Indikationen
Elektrizität. = C J m. Das Coulomb Potential φ ist dabei:
 Elektrizität Die Coulombsche potentielle Energie V einer Ladung q im Abstand r von einer anderen Ladung q ist die Arbeit, die aufgewendet werden muss um die zwei Ladungen aus dem Unendlichen auf den Abstand
Elektrizität Die Coulombsche potentielle Energie V einer Ladung q im Abstand r von einer anderen Ladung q ist die Arbeit, die aufgewendet werden muss um die zwei Ladungen aus dem Unendlichen auf den Abstand
SwissChO 2016 Erste Runde
 Erste Runde Information Die Prüfung sollte innerhalb von einer Stunde gelöst werden. Die einzigen erlaubten Hilfsmittel sind Bücher und ein Taschenrechner. Übertrage die Antworten auf das separate Antwortblatt.
Erste Runde Information Die Prüfung sollte innerhalb von einer Stunde gelöst werden. Die einzigen erlaubten Hilfsmittel sind Bücher und ein Taschenrechner. Übertrage die Antworten auf das separate Antwortblatt.
SS Thomas Schrader. der Universität Duisburg-Essen. (Teil 8: Redoxprozesse, Elektrochemie)
 Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 8: Redoxprozesse, Elektrochemie) Oxidation und Reduktion Redoxreaktionen: Ein Atom oder
Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 8: Redoxprozesse, Elektrochemie) Oxidation und Reduktion Redoxreaktionen: Ein Atom oder
A. Wieviel molar ist eine 30 % Wasserstoffperoxidlösung (d = 1.11, M = 34)
 Grundlagen der Biochemie 29. 2. 2008 Einfache Rechenfragen: A. Wieviel molar ist eine 30 % Wasserstoffperoxidlösung (d = 1.11, M = 34) B. Welche Stoffmenge enthalten 2 µl einer 5 µm Lösung? Richtige Einheit
Grundlagen der Biochemie 29. 2. 2008 Einfache Rechenfragen: A. Wieviel molar ist eine 30 % Wasserstoffperoxidlösung (d = 1.11, M = 34) B. Welche Stoffmenge enthalten 2 µl einer 5 µm Lösung? Richtige Einheit
Seminar zum Quantitativen Anorganischen Praktikum WS 2011/12
 Seminar zum Quantitativen Anorganischen Praktikum WS 211/12 Teil des Moduls MN-C-AlC Dr. Matthias Brühmann Dr. Christian Rustige Inhalt Montag, 9.1.212, 8-1 Uhr, HS III Allgemeine Einführung in die Quantitative
Seminar zum Quantitativen Anorganischen Praktikum WS 211/12 Teil des Moduls MN-C-AlC Dr. Matthias Brühmann Dr. Christian Rustige Inhalt Montag, 9.1.212, 8-1 Uhr, HS III Allgemeine Einführung in die Quantitative
Lösungen zu den Übungen zur Experimentalvorlesung AC
 Lösungen zu den Übungen zur Experimentalvorlesung AC 1. Stöchiometrisches Rechnen 1.1. n (S = mol n (S 8 = 0,5 mol 1.. n (P = 8 mol n (P = mol 1.3. m (P =,8 g m (P =,8 g m (P = 1, g 1.. m (1/3 As 3+ =
Lösungen zu den Übungen zur Experimentalvorlesung AC 1. Stöchiometrisches Rechnen 1.1. n (S = mol n (S 8 = 0,5 mol 1.. n (P = 8 mol n (P = mol 1.3. m (P =,8 g m (P =,8 g m (P = 1, g 1.. m (1/3 As 3+ =
Allgemeine Chemie I (AC) HS 2011 Übungen Serie 6
 Prof. A. Togni, D-CHAB, HCI H 239 Allgemeine Chemie I (AC) HS 2011 Übungen Serie 6 Säure-Base-Gleichgewichte E 1. Sie möchten 200 ml einer Pufferlösung mit ph = 5.00 mit dem Säure-Base-Paar Essigsäure
Prof. A. Togni, D-CHAB, HCI H 239 Allgemeine Chemie I (AC) HS 2011 Übungen Serie 6 Säure-Base-Gleichgewichte E 1. Sie möchten 200 ml einer Pufferlösung mit ph = 5.00 mit dem Säure-Base-Paar Essigsäure
Grundlagen der Chemie für Nichtchemiker AUFGABENSAMMLUNG
 AUFGABENSAMMLUNG 1. Chemische Grundlagen: Masse -Berechnungen 1-1. Berechnen Sie die molaren Massen folgender Stoffe: a)caco 3 ; b)caso 4 2H 2 O; c)agcl; d)al 2 O 3 ; e)phenol C 6 H 5 OH; f)magnesiumammoniumphosphat-
AUFGABENSAMMLUNG 1. Chemische Grundlagen: Masse -Berechnungen 1-1. Berechnen Sie die molaren Massen folgender Stoffe: a)caco 3 ; b)caso 4 2H 2 O; c)agcl; d)al 2 O 3 ; e)phenol C 6 H 5 OH; f)magnesiumammoniumphosphat-
Stöchiometrie-Seminar April 2019 Moritz Helmstädter 1
 Stöchiometrie-Seminar 4 1 Themen des heutigen Seminars 1) Zusammenfassung des letzten Seminars 2) Besprechung der Hausaufgaben 3) Theorie 4) Übungsaufgaben 2 Themen des heutigen Seminars 1) Zusammenfassung
Stöchiometrie-Seminar 4 1 Themen des heutigen Seminars 1) Zusammenfassung des letzten Seminars 2) Besprechung der Hausaufgaben 3) Theorie 4) Übungsaufgaben 2 Themen des heutigen Seminars 1) Zusammenfassung
Das Chemische Gleichgewicht
 Das Chemische Gleichgewicht Geschwindigkeit der Hinreaktion: v hin = k hin c(a 2 ) c(x 2 ) Geschwindigkeit der Rückreaktion: v rück = k rück c 2 (AX) Gleichgewicht: v hin = v rück k hin c(a 2 ) c(x 2 )
Das Chemische Gleichgewicht Geschwindigkeit der Hinreaktion: v hin = k hin c(a 2 ) c(x 2 ) Geschwindigkeit der Rückreaktion: v rück = k rück c 2 (AX) Gleichgewicht: v hin = v rück k hin c(a 2 ) c(x 2 )
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2009/10 vom
 Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2009/10 vom 18.09.2009 A1 A2 A3 A4 A5 Σ Note 10 10 10 10 10 NAME:... VORNAME:...MUSTERLÖSUNG... Pseudonym für Ergebnisveröffentlichung:... Schreiben
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2009/10 vom 18.09.2009 A1 A2 A3 A4 A5 Σ Note 10 10 10 10 10 NAME:... VORNAME:...MUSTERLÖSUNG... Pseudonym für Ergebnisveröffentlichung:... Schreiben
2. Klausur zum Chemischen Grundpraktikum im WS 2010/11 vom ( Wiederholungsklausur )
 2. Klausur zum Chemischen Grundpraktikum im WS 2010/11 vom 08.04.2011 ( Wiederholungsklausur ) A1 A2 A3 A4 A5 A6 A7 PC1 PC2 PC3 PC4 PC5 Σ Note 10 10 10 10 10 10 10 6 5 3 9 7 NAME:... VORNAME:... IMMATRIKULATIONSNUMMER:...
2. Klausur zum Chemischen Grundpraktikum im WS 2010/11 vom 08.04.2011 ( Wiederholungsklausur ) A1 A2 A3 A4 A5 A6 A7 PC1 PC2 PC3 PC4 PC5 Σ Note 10 10 10 10 10 10 10 6 5 3 9 7 NAME:... VORNAME:... IMMATRIKULATIONSNUMMER:...
Typische Fragen für den Gehschul-Teil: Typ 1: Mengen und Konzentrationen:
 Die Gehschule ist ein Teil der Biochemischen Übungen für das Bakkalaureat LMBT. Aus organisatorischen Gründen wird dieser Test gleichzeitig mit der Prüfung aus Grundlagen der Biochemie angeboten. Das Abschneiden
Die Gehschule ist ein Teil der Biochemischen Übungen für das Bakkalaureat LMBT. Aus organisatorischen Gründen wird dieser Test gleichzeitig mit der Prüfung aus Grundlagen der Biochemie angeboten. Das Abschneiden
Übungsaufgaben zu Ionenreaktionen in wässriger Lösung
 Übungsaufgaben zu Ionenreaktionen in wässriger Lösung 1) Berechnen Sie den phwert von folgenden Lösungen: a) 0.01 M HCl b) 3 10 4 M KOH c) 0.1 M NaOH d) 0.1 M CH 3 COOH (*) e) 0.3 M NH 3 f) 10 8 M HCl
Übungsaufgaben zu Ionenreaktionen in wässriger Lösung 1) Berechnen Sie den phwert von folgenden Lösungen: a) 0.01 M HCl b) 3 10 4 M KOH c) 0.1 M NaOH d) 0.1 M CH 3 COOH (*) e) 0.3 M NH 3 f) 10 8 M HCl
NADUF: Methoden der chemischen Analysen (EAWAG) Parameter Jahr Methode Prinzip Bestimmungsgrenze Angewandte Methode korrespondiert mit
 Gesamthärte (Ca 2+ + Mg 2+) bis 1974 Manuelle Nach Alkalinitätsbest. mit Komplexon III (0.05 M) bei ph 10 (Ammoniak-Puffer) und visuelle Endpunktsanzeige 0.05 mmol/l ISO 6059:1984 1975-1976 Autom. 1977-2006
Gesamthärte (Ca 2+ + Mg 2+) bis 1974 Manuelle Nach Alkalinitätsbest. mit Komplexon III (0.05 M) bei ph 10 (Ammoniak-Puffer) und visuelle Endpunktsanzeige 0.05 mmol/l ISO 6059:1984 1975-1976 Autom. 1977-2006
Einteilung der Maßanalyse
 Einteilung der Maßanalyse Neutralisation (Säure-Base-Titration Acidimetrie Alkalimetrie Fällungstitration Redoxtitration Iodometrie Dichromatometrie Manganometrie etc. Komplexometrie Säure/Basen Theorien
Einteilung der Maßanalyse Neutralisation (Säure-Base-Titration Acidimetrie Alkalimetrie Fällungstitration Redoxtitration Iodometrie Dichromatometrie Manganometrie etc. Komplexometrie Säure/Basen Theorien
3 Mg 3 Mg e N e 2 N 3
 Redoxreaktionen Mg + ½ O 2 MgO 3 Mg + N 2 Mg 3 N 2 Mg Mg 2+ + 2 e ½ O 2 + 2 e O 2 3 Mg 3 Mg 2+ + 6 e N 2 + 6 e 2 N 3 1 Redoxreaktionen 2 Oxidation und Reduktion Eine Oxidation ist ein Elektronenverlust
Redoxreaktionen Mg + ½ O 2 MgO 3 Mg + N 2 Mg 3 N 2 Mg Mg 2+ + 2 e ½ O 2 + 2 e O 2 3 Mg 3 Mg 2+ + 6 e N 2 + 6 e 2 N 3 1 Redoxreaktionen 2 Oxidation und Reduktion Eine Oxidation ist ein Elektronenverlust
Reduktion und Oxidation. Oxidationszahlen (OZ)
 Redox-Reaktionen Reduktion und Oxidation Oxidationszahlen (OZ) REDOX Reaktionen / - Gleichungen Das elektrochemische Potential Die Spannungsreihe der Chemischen Elemente Die Nernstsche Gleichung Definitionen
Redox-Reaktionen Reduktion und Oxidation Oxidationszahlen (OZ) REDOX Reaktionen / - Gleichungen Das elektrochemische Potential Die Spannungsreihe der Chemischen Elemente Die Nernstsche Gleichung Definitionen
MgO. Mg Mg e ½ O e O 2. 3 Mg 3 Mg e N e 2 N 3
 Redox-Reaktionen Mg + ½ O 2 MgO 3 Mg + N 2 Mg 3 N 2 Mg Mg 2+ + 2 e ½ O 2 + 2 e O 2 3 Mg 3 Mg 2+ + 6 e N 2 + 6 e 2 N 3 Redox-Reaktionen Oxidation und Reduktion Eine Oxidation ist ein Elektronenverlust Na
Redox-Reaktionen Mg + ½ O 2 MgO 3 Mg + N 2 Mg 3 N 2 Mg Mg 2+ + 2 e ½ O 2 + 2 e O 2 3 Mg 3 Mg 2+ + 6 e N 2 + 6 e 2 N 3 Redox-Reaktionen Oxidation und Reduktion Eine Oxidation ist ein Elektronenverlust Na
Maßanalyse. Bestimmung einer Schwefelsäure mit einer NaOH Maßlösung: bzw. n(naoh * 1 = n(h 2 SO 4 ) * 2 V [ml] * * t * 1 = n(h 2 SO 4 ) * 2
![Maßanalyse. Bestimmung einer Schwefelsäure mit einer NaOH Maßlösung: bzw. n(naoh * 1 = n(h 2 SO 4 ) * 2 V [ml] * * t * 1 = n(h 2 SO 4 ) * 2 Maßanalyse. Bestimmung einer Schwefelsäure mit einer NaOH Maßlösung: bzw. n(naoh * 1 = n(h 2 SO 4 ) * 2 V [ml] * * t * 1 = n(h 2 SO 4 ) * 2](/thumbs/79/78929570.jpg) Maßanalyse Bei der Maßanalyse (Volumetrie) wird zu der zu analysierenden Lösung unbekannten Gehaltes soviel einer Lösung bekannter Konzentration der Maßlösung zugegeben, bis ein Indikationssystem den Endpunkt
Maßanalyse Bei der Maßanalyse (Volumetrie) wird zu der zu analysierenden Lösung unbekannten Gehaltes soviel einer Lösung bekannter Konzentration der Maßlösung zugegeben, bis ein Indikationssystem den Endpunkt
Analytische Chemie. B. Sc. Chemieingenieurwesen. 11. Februar Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 11. Februar 2014 Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der
Analytische Chemie B. Sc. Chemieingenieurwesen 11. Februar 2014 Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der
1.3. Fragen zu chemischen Reaktionen
 1.3. Fragen zu chemischen Reaktionen Reaktionsgleichungen Ergänze die fehlenden Koeffizienten: a) PbI 4 PbI 2 + I 2 b) PbO 2 PbO + O 2 c) CO + O 2 CO 2 d) SO 2 + O 2 SO 3 e) N 2 + H 2 NH 3 f) N 2 + O 2
1.3. Fragen zu chemischen Reaktionen Reaktionsgleichungen Ergänze die fehlenden Koeffizienten: a) PbI 4 PbI 2 + I 2 b) PbO 2 PbO + O 2 c) CO + O 2 CO 2 d) SO 2 + O 2 SO 3 e) N 2 + H 2 NH 3 f) N 2 + O 2
Seminar zum Quantitativen Anorganischen Praktikum WS 2012/13
 Seminar zum Quantitativen Anorganischen Praktikum WS 2012/13 Teil des Moduls MN-C-AlC Dipl.-Chem. Corinna Hegemann Dipl.-Chem. Eva Rüttgers Inhalt Freitag, 11.01.2013, 8-10 Uhr, HS II Allgemeine Einführung
Seminar zum Quantitativen Anorganischen Praktikum WS 2012/13 Teil des Moduls MN-C-AlC Dipl.-Chem. Corinna Hegemann Dipl.-Chem. Eva Rüttgers Inhalt Freitag, 11.01.2013, 8-10 Uhr, HS II Allgemeine Einführung
Quantitativen Anorganischen Praktikum
 Seminar zum Quantitativen Anorganischen Praktikum WS 2011/12 Teil des Moduls MN-C-AlC Dr. Matthias Brühmann Dr. Christian Rustige Inhalt Montag, 09.01.2012, 8-10 Uhr, HS III Allgemeine Einführung in die
Seminar zum Quantitativen Anorganischen Praktikum WS 2011/12 Teil des Moduls MN-C-AlC Dr. Matthias Brühmann Dr. Christian Rustige Inhalt Montag, 09.01.2012, 8-10 Uhr, HS III Allgemeine Einführung in die
Wasserchemie und Wasseranalytik SS 2015
 Wasserchemie und Wasseranalytik SS 015 Übung zum Vorlesungsblock II Wasserchemie Dr.-Ing. Katrin Bauerfeld 5,5 6,5 7,5 8,5 9,5 10,5 11,5 1,5 13,5 Anteile [%] Übungsaufgaben zu Block II Wasserchemie 1.
Wasserchemie und Wasseranalytik SS 015 Übung zum Vorlesungsblock II Wasserchemie Dr.-Ing. Katrin Bauerfeld 5,5 6,5 7,5 8,5 9,5 10,5 11,5 1,5 13,5 Anteile [%] Übungsaufgaben zu Block II Wasserchemie 1.
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2011/12 vom
 Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2011/12 vom 23.09.2011 A1 A2 A3 A4 A5 Σ Note 8 8 10 10 14 50 NAME/VORNAME:... Matrikelnummer: STICHPUNKTE ZU DEN LÖSUNGEN Pseudonym für Ergebnisveröffentlichung:...
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2011/12 vom 23.09.2011 A1 A2 A3 A4 A5 Σ Note 8 8 10 10 14 50 NAME/VORNAME:... Matrikelnummer: STICHPUNKTE ZU DEN LÖSUNGEN Pseudonym für Ergebnisveröffentlichung:...
Klausur zur Vorlesung AC1 (Anorganische Experimentalchemie) am Klausur B
 1 2 3 4 5 6 7 8 9 10 B* 10 10 10 10 10 10 10 10 10 10 100 Note: (*nur für Biologie, Lehramt) 1 Vorname: Matr.-Nr.: Nachname: Studiengang: Chemie und Biochemie Lehramt Chemie vertieft Musterlösung! Bitte
1 2 3 4 5 6 7 8 9 10 B* 10 10 10 10 10 10 10 10 10 10 100 Note: (*nur für Biologie, Lehramt) 1 Vorname: Matr.-Nr.: Nachname: Studiengang: Chemie und Biochemie Lehramt Chemie vertieft Musterlösung! Bitte
Abschlussprüfung 2004 an den vierstufigen Realschulen in Bayern
 Abschlussprüfung 00 an den vierstufigen Realschulen in Bayern Mathematik II Aufgabengruppe C Aufgabe C Lösungsmuster und Bewertung C. x 0 5 6 7 8 9 0 0, 5x + x -,75 5,75 7 7,75 8 7,75 7 5,75,75 - y C p
Abschlussprüfung 00 an den vierstufigen Realschulen in Bayern Mathematik II Aufgabengruppe C Aufgabe C Lösungsmuster und Bewertung C. x 0 5 6 7 8 9 0 0, 5x + x -,75 5,75 7 7,75 8 7,75 7 5,75,75 - y C p
Zentralprüfung SwissChO 2016
 PROBLEM 1 - VERSCHIEDENE FRAGEN 9.5 PUNKTE a 6 N A = 3.61 10 4 mol 1 Punkt b Aufgrund der Verdünnung hat man 0.05M Br Ionen, 0.05M I Ionen und 0.1M Br + Ionen. 1/ Punkt wenn Br und I richtig, 1/ Punkt
PROBLEM 1 - VERSCHIEDENE FRAGEN 9.5 PUNKTE a 6 N A = 3.61 10 4 mol 1 Punkt b Aufgrund der Verdünnung hat man 0.05M Br Ionen, 0.05M I Ionen und 0.1M Br + Ionen. 1/ Punkt wenn Br und I richtig, 1/ Punkt
2. Klausur zum Chemischen Grundpraktikum im WS 2010/11 vom ( Wiederholungsklausur ) LÖSUNGEN
 2. Klausur zum Chemischen Grundpraktikum im WS 2010/11 vom 08.04.2011 ( Wiederholungsklausur ) A1 A2 A3 A4 A5 A6 A7 PC1 PC2 PC3 PC4 PC5 Σ Note 10 10 10 10 10 10 10 6 5 3 9 7 NAME:... LÖSUNGEN IMMATRIKULATIONSNUMMER:...
2. Klausur zum Chemischen Grundpraktikum im WS 2010/11 vom 08.04.2011 ( Wiederholungsklausur ) A1 A2 A3 A4 A5 A6 A7 PC1 PC2 PC3 PC4 PC5 Σ Note 10 10 10 10 10 10 10 6 5 3 9 7 NAME:... LÖSUNGEN IMMATRIKULATIONSNUMMER:...
NADUF: Methoden der chemischen Analysen (EAWAG)
 Gesamthärte (Ca 2+ + Mg 2+) bis 1974 Manuelle Komplexon III (0.05 M) bei ph 10 (Ammoniak-Puffer) und visuelle Endpunktsanzeige 0.05 mmol/l ISO 6059:1984 1975-1976 Autom. 1977-2006 Autom. seit 2007 Autom.
Gesamthärte (Ca 2+ + Mg 2+) bis 1974 Manuelle Komplexon III (0.05 M) bei ph 10 (Ammoniak-Puffer) und visuelle Endpunktsanzeige 0.05 mmol/l ISO 6059:1984 1975-1976 Autom. 1977-2006 Autom. seit 2007 Autom.
Übungsklausur Sommer 2007
 AC 2, Anorganische Chemie in Lösung Übungsklausur Sommer 2007 1) In einem Becherglas befinden sich 100 ml einer 1 M a 4 EDTA Lösung (a). Zu dieser Lösung gibt man festes Radiumsulfat bis zur Sättigung,
AC 2, Anorganische Chemie in Lösung Übungsklausur Sommer 2007 1) In einem Becherglas befinden sich 100 ml einer 1 M a 4 EDTA Lösung (a). Zu dieser Lösung gibt man festes Radiumsulfat bis zur Sättigung,
2. Teilklausur zum Chemischen Grundpraktikum im WS 2011/12 vom
 2. Teilklausur zum Chemischen Grundpraktikum im WS 2011/12 vom 01.02.2012 A1 A2 A3 R4 F5 E6 Σ Note 8 11 6 10 10 5 50 NAME/VORNAME:... STICHPUNKTE ZU DEN LÖSUNGEN Matrikelnummer:... Pseudonym für Ergebnisveröffentlichung
2. Teilklausur zum Chemischen Grundpraktikum im WS 2011/12 vom 01.02.2012 A1 A2 A3 R4 F5 E6 Σ Note 8 11 6 10 10 5 50 NAME/VORNAME:... STICHPUNKTE ZU DEN LÖSUNGEN Matrikelnummer:... Pseudonym für Ergebnisveröffentlichung
Weiterführendes Rechnen mit Löslichkeitsprodukten
 Weiterführendes Rechnen mit öslichkeitsprodukten Fachschule für Technik In der online-version dieses Arbeitsblattes gibt es u.u. noch Bonusaufgaben. Immer auch Nummerierung und genaue Aufgabenstellung
Weiterführendes Rechnen mit öslichkeitsprodukten Fachschule für Technik In der online-version dieses Arbeitsblattes gibt es u.u. noch Bonusaufgaben. Immer auch Nummerierung und genaue Aufgabenstellung
4. Wie viele Liter Gas von 35 C und 995 mbar entstehen bei der thermischen Zersetzung von 15,50 g Ammoniumcarbamat? 2 NH 3 (g) + CO 2 (g)
 LAP 2010 Teil 1 Alle 6 Aufgaben sind zu lösen 1. Zur Bestimmung des Wassergehaltes wurden 0,1693 g Honig mit 5,005 ml Titriermittel titriert. 7,533 ml dieses Titriermittels titrierte zuvor 36,46 mg Wasser.
LAP 2010 Teil 1 Alle 6 Aufgaben sind zu lösen 1. Zur Bestimmung des Wassergehaltes wurden 0,1693 g Honig mit 5,005 ml Titriermittel titriert. 7,533 ml dieses Titriermittels titrierte zuvor 36,46 mg Wasser.
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2012/13 vom
 Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2012/13 vom 21.09.2012 A1 A2 A3 A4 A5 Σ Note 14 10 9 8 9 50 NAME/VORNAME:... Lösungsstichpunkte Pseudonym für Ergebnisveröffentlichung:... Schreiben
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2012/13 vom 21.09.2012 A1 A2 A3 A4 A5 Σ Note 14 10 9 8 9 50 NAME/VORNAME:... Lösungsstichpunkte Pseudonym für Ergebnisveröffentlichung:... Schreiben
Erste Runde SwissChO 2018
 Erste Runde SwissChO 2018 Informationen Die Prüfung sollte innerhalb von einer Stunde gelöst werden. Die einzigen erlaubten Hilfsmittel sind Bücher und ein Taschenrechner. Übertrage die Antworten auf das
Erste Runde SwissChO 2018 Informationen Die Prüfung sollte innerhalb von einer Stunde gelöst werden. Die einzigen erlaubten Hilfsmittel sind Bücher und ein Taschenrechner. Übertrage die Antworten auf das
Seminar zum Quantitativen Anorganischen Praktikum WS 2012/13
 Seminar zum Quantitativen Anorganischen Praktikum WS 2012/13 Teil des Moduls MN-C-AlC Dipl.-Chem. Corinna Hegemann Dipl.-Chem. Eva Rüttgers Inhalt Freitag, 11.01.2013, 8-10 Uhr, HS II Allgemeine Einführung
Seminar zum Quantitativen Anorganischen Praktikum WS 2012/13 Teil des Moduls MN-C-AlC Dipl.-Chem. Corinna Hegemann Dipl.-Chem. Eva Rüttgers Inhalt Freitag, 11.01.2013, 8-10 Uhr, HS II Allgemeine Einführung
2. Teilklausur zum Chemischen Grundpraktikum im WS 2011/12 vom
 2. Teilklausur zum Chemischen Grundpraktikum im WS 2011/12 vom 01.02.2012 A1 A2 A3 R4 F5 E6 Σ Note 8 11 6 10 10 5 50 NAME/VORNAME:... Matrikelnummer:... Pseudonym für Ergebnisveröffentlichung Schreiben
2. Teilklausur zum Chemischen Grundpraktikum im WS 2011/12 vom 01.02.2012 A1 A2 A3 R4 F5 E6 Σ Note 8 11 6 10 10 5 50 NAME/VORNAME:... Matrikelnummer:... Pseudonym für Ergebnisveröffentlichung Schreiben
E3 Aktivitätskoeffizient
 Physikalisch-Chemische Praktika E3 Aktivitätskoeffizient Stichworte zur Vorbereitung: Den Kontext der folgenden Stichworte sollten Sie zur Vorbesprechung und während der Durchführung des Praktikumstermins
Physikalisch-Chemische Praktika E3 Aktivitätskoeffizient Stichworte zur Vorbereitung: Den Kontext der folgenden Stichworte sollten Sie zur Vorbesprechung und während der Durchführung des Praktikumstermins
Beispielaufgaben IChO 2. Runde 2019 Grundlagen der Thermodynamik, Lösungen. = -0,900 kj/k (21,84 22,15) K / 13,16 g = 0,279 kj / 13,16 g
 Lösung Beispiel 1 Erhaltung der Energie a) ZnSO 4(s) ZnSO 4(aq): Lösungsenthalpie Lsg (ZnSO 4) = -0,900 kj/k (23,52 22,55) K / 1,565 g = -0,873 kj / 1,565 g mit (ZnSO 4) = 161,48 g/mol: Lsg (ZnSO 4) =
Lösung Beispiel 1 Erhaltung der Energie a) ZnSO 4(s) ZnSO 4(aq): Lösungsenthalpie Lsg (ZnSO 4) = -0,900 kj/k (23,52 22,55) K / 1,565 g = -0,873 kj / 1,565 g mit (ZnSO 4) = 161,48 g/mol: Lsg (ZnSO 4) =
Puffer-Lösungen COOH / CH 3. COO - Na + Acetat-Puffer Essigsäure / Natriumacetat. Beispiele: CH 3 / NH NH 3. Ammonium-Puffer
 Puffer-Lösungen Folie156 Beispiel: Der ph-wert des Blutes (ph = 7.4) darf nicht schwanken, da sonst die Funktionen von ph-abhängigen Enzymen gestört wird. Der ph-wert lässt sich mit einem Puffersystem
Puffer-Lösungen Folie156 Beispiel: Der ph-wert des Blutes (ph = 7.4) darf nicht schwanken, da sonst die Funktionen von ph-abhängigen Enzymen gestört wird. Der ph-wert lässt sich mit einem Puffersystem
Seminar Stöchiometrie. Stöchiometrieseminar Wintersemester 2016 Leonie Gellrich
 Seminar Stöchiometrie Stöchiometrieseminar Wintersemester 2016 Leonie Gellrich Preis: 19,90 2 Leonie Gellrich Johann Wolfgang Goethe -Universität Frankfurt am Main Themen/Inhalte der Zwischenklausur Seminar
Seminar Stöchiometrie Stöchiometrieseminar Wintersemester 2016 Leonie Gellrich Preis: 19,90 2 Leonie Gellrich Johann Wolfgang Goethe -Universität Frankfurt am Main Themen/Inhalte der Zwischenklausur Seminar
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 Chemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul Rademacher Institut für rganische Chemie der Universität Duisburg-Essen (Teil 6: 17.11.2004) MILESS: Chemie für Biologen 102 Reduktion
Chemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul Rademacher Institut für rganische Chemie der Universität Duisburg-Essen (Teil 6: 17.11.2004) MILESS: Chemie für Biologen 102 Reduktion
Stöchiometrie Seminar Sommersemester 2019 Leonie Gellrich
 Stöchiometrie Seminar Sommersemester 2019 Leonie Gellrich Taschenrechner Zugelassen für das erste Semester sind Modelle der TI-30 Serie der Casio FX-82/85/87/991-Reihe oder Vorgänger-Modelle davon, die
Stöchiometrie Seminar Sommersemester 2019 Leonie Gellrich Taschenrechner Zugelassen für das erste Semester sind Modelle der TI-30 Serie der Casio FX-82/85/87/991-Reihe oder Vorgänger-Modelle davon, die
Name: Punktzahl: von 57 Note:
 Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
Das Potenzial einer Halbzelle lässt sich mittels der Nernstschen Gleichung berechnen. oder
 Zusammenfassung Redoxreaktionen Oxidation entspricht einer Elektronenabgabe Reduktion entspricht einer Elektronenaufnahme Oxidation und Reduktion treten immer gemeinsam auf Oxidationszahlen sind ein Hilfsmittel
Zusammenfassung Redoxreaktionen Oxidation entspricht einer Elektronenabgabe Reduktion entspricht einer Elektronenaufnahme Oxidation und Reduktion treten immer gemeinsam auf Oxidationszahlen sind ein Hilfsmittel
Stöchiometrieseminar Wintersemester 2017 Leonie Gellrich
 Stöchiometrieseminar Wintersemester 2017 Leonie Gellrich Taschenrechner und: Casio fx-991de Casio fx-991de X TI-30Xa TI 30 ECO RS TI 30 PRO Multiview Casio FX-991DE Plus 2 Leonie Gellrich Johann Wolfgang
Stöchiometrieseminar Wintersemester 2017 Leonie Gellrich Taschenrechner und: Casio fx-991de Casio fx-991de X TI-30Xa TI 30 ECO RS TI 30 PRO Multiview Casio FX-991DE Plus 2 Leonie Gellrich Johann Wolfgang
Analytische Chemie. B. Sc. Chemieingenieurwesen. 23. März Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 23. März 2009 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 23. März 2009 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Chemie Klausur SS Aminosäuren (11.5 Punkte) a) Benennen Sie die unten stehenden Aminosäuren:
 Chemie Klausur SS14 1. Aminosäuren (11.5 Punkte) a) Benennen Sie die unten stehenden Aminosäuren: b) Bestimmen Sie den isoelektrischen Punkt der Aminosäure Lysin (unterer Graph)! pks1 = 2,0 pks2 = 9,1
Chemie Klausur SS14 1. Aminosäuren (11.5 Punkte) a) Benennen Sie die unten stehenden Aminosäuren: b) Bestimmen Sie den isoelektrischen Punkt der Aminosäure Lysin (unterer Graph)! pks1 = 2,0 pks2 = 9,1
[H3O+] [A-] [M+] - [Y-] >> [HA] [OH-] [Y - ] = Menge an M + (Base) welche zur Neutralisation der starkesäure gebraucht wurde!
![[H3O+] [A-] [M+] - [Y-] >> [HA] [OH-] [Y - ] = Menge an M + (Base) welche zur Neutralisation der starkesäure gebraucht wurde! [H3O+] [A-] [M+] - [Y-] >> [HA] [OH-] [Y - ] = Menge an M + (Base) welche zur Neutralisation der starkesäure gebraucht wurde!](/thumbs/55/37326984.jpg) Analytik 4.29 Einige wichtige Punkte der Titrationskurve: A: Beginn der Titration. Da starke Säure zur Essigsäure gegeben wurde ist f < 1. B,E: f = 0; Die starke Säure wurde titriert. Essigsäure in einer
Analytik 4.29 Einige wichtige Punkte der Titrationskurve: A: Beginn der Titration. Da starke Säure zur Essigsäure gegeben wurde ist f < 1. B,E: f = 0; Die starke Säure wurde titriert. Essigsäure in einer
6,
 ph-wert 10,00 9,50 9,00 8,50 8,00 7,50 7,00 6,50 U:\13h\U135009_DGW_Änderung_Planfeststellung\02_Daten\Chemie\Wasser\Analyseberichte_neu\Sickerwasse_v03.xls Seite 1/18 Leitfähigkeit µs/cm 20000 15000 10000
ph-wert 10,00 9,50 9,00 8,50 8,00 7,50 7,00 6,50 U:\13h\U135009_DGW_Änderung_Planfeststellung\02_Daten\Chemie\Wasser\Analyseberichte_neu\Sickerwasse_v03.xls Seite 1/18 Leitfähigkeit µs/cm 20000 15000 10000
Titrationskurve einer starken Säure (HCl) mit einer starken Base (NaOH)
 Titrationskurve einer starken Säure (HCl) mit einer starken Base (NaOH) Material 250 mlbecherglas 100 ml Messzylinder 50 mlbürette, Magnetrührer, Magnetfisch, Stativmaterial phmeter Chemikalien Natronlauge
Titrationskurve einer starken Säure (HCl) mit einer starken Base (NaOH) Material 250 mlbecherglas 100 ml Messzylinder 50 mlbürette, Magnetrührer, Magnetfisch, Stativmaterial phmeter Chemikalien Natronlauge
Die spezifische Leitfähigkeit κ ist umgekehrt proportional zum Widerstand R:
 Institut für Physikalische Chemie Lösungen zu den Übungen zur Vorlesung Physikalische Chemie II im WS 206/207 Prof. Dr. Eckhard Bartsch / M. Werner M.Sc. Aufgabenblatt 3 vom..6 Aufgabe 3 (L) Leitfähigkeiten
Institut für Physikalische Chemie Lösungen zu den Übungen zur Vorlesung Physikalische Chemie II im WS 206/207 Prof. Dr. Eckhard Bartsch / M. Werner M.Sc. Aufgabenblatt 3 vom..6 Aufgabe 3 (L) Leitfähigkeiten
A 2.6 Wie ist die Zusammensetzung der Flüssigkeit und des Dampfes eines Stickstoff-Sauerstoff-Gemischs
 A 2.1 Bei - 10 o C beträgt der Dampfdruck des Kohlendioxids 26,47 bar, die Dichte der Flüssigkeit 980,8 kg/m 3 und die Dichte des Dampfes 70,5 kg/m 3. Bei - 7,5 o C beträgt der Dampfdruck 28,44 bar. Man
A 2.1 Bei - 10 o C beträgt der Dampfdruck des Kohlendioxids 26,47 bar, die Dichte der Flüssigkeit 980,8 kg/m 3 und die Dichte des Dampfes 70,5 kg/m 3. Bei - 7,5 o C beträgt der Dampfdruck 28,44 bar. Man
NAD+/NADH ADH CH 3 CH 2 OH + NAD + CH 3 CHO + NADH + H + Hier unterscheiden sich Ethanol und NAD + in der Tat funktionell nicht.
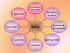 NAD+/NADH NAD + (Nicotinamid-adenin-dinukleotid) ist das häufigste "Coenzym" enzymatischer Redox-reaktionen. Von den Lehrbüchern wird es teils als Coenzym, teils als Cosubstrat eingeordnet. Das erstere
NAD+/NADH NAD + (Nicotinamid-adenin-dinukleotid) ist das häufigste "Coenzym" enzymatischer Redox-reaktionen. Von den Lehrbüchern wird es teils als Coenzym, teils als Cosubstrat eingeordnet. Das erstere
H 2 N OH H. Nipecotinsäure. homo-β-prolin. Guvacin GABA H 3 C. HCl. HCl O CH 3. Tiagabin GABITRIL (5 mg, 10 mg, 15 mg) SKF 89976A. E.
 E. Urban 1 H 2 H H H H H H H GABA ipecotinsäure Guvacin homo-β-prolin H 3 C S H S H HCl HCl CH 3 SKF 89976A Tiagabin GABITRIL (5 mg, 10 mg, 15 mg) E. Urban 2 H 3 C S H S H HCl HCl CH 3 SKF 89976A IC 50
E. Urban 1 H 2 H H H H H H H GABA ipecotinsäure Guvacin homo-β-prolin H 3 C S H S H HCl HCl CH 3 SKF 89976A Tiagabin GABITRIL (5 mg, 10 mg, 15 mg) E. Urban 2 H 3 C S H S H HCl HCl CH 3 SKF 89976A IC 50
Coffein-Natriumbenzoat Coffeinum-natrii benzoas Synonym: Coffeinum-Natrium benzoicum
 !!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmenf sind bis zum 15.September 2008 an folgende Adresse
!!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmenf sind bis zum 15.September 2008 an folgende Adresse
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Versuchsprotokoll. Konduktometrie
 Versuchsprotokoll Versuchsdatum: 19.10.04 Protokolldatum: Sttempell Durchgeführt von: Konduktometrie 1. Inhaltsangabe: 1..Inhaltsangabe:--------------------------------------------------------------------------------
Versuchsprotokoll Versuchsdatum: 19.10.04 Protokolldatum: Sttempell Durchgeführt von: Konduktometrie 1. Inhaltsangabe: 1..Inhaltsangabe:--------------------------------------------------------------------------------
Multiple Choice Fragen zur Physikalischen Chemie für Pharmazeuten: Klausur vom : /*max.100 Punkte */
 Mutipe Choice Fragen zur Physikaischen Chemie für Pharmazeuten: Kausur vom 02.03.2018: /*max.100 Punkte */ Name: Matrike-Nr.: Punkte: Markieren Sie jeweis die korrekte Antwort: (1) Mathematische Grundagen:
Mutipe Choice Fragen zur Physikaischen Chemie für Pharmazeuten: Kausur vom 02.03.2018: /*max.100 Punkte */ Name: Matrike-Nr.: Punkte: Markieren Sie jeweis die korrekte Antwort: (1) Mathematische Grundagen:
Anorganisch-Chemisches Praktikum für Physiker und Geoökologen: Quantitative Analyse (Teil 2)
 Anorganisch-Chemisches Praktikum für Physiker und Geoökologen: Quantitative Analyse (Teil 2) Dr. Christopher Anson INSTITUT FÜR ANRGANISCHE CHEMIE KIT Universität des Landes Baden-Württemberg und nationales
Anorganisch-Chemisches Praktikum für Physiker und Geoökologen: Quantitative Analyse (Teil 2) Dr. Christopher Anson INSTITUT FÜR ANRGANISCHE CHEMIE KIT Universität des Landes Baden-Württemberg und nationales
Versuch EM: Elektromotorische
 Versuch EM: Elektromotorische Kraft Seite 1 Einleitung Der Begriff Elektromotorische Kraft (EMK), auch als Urspannung bezeichnet, beschreibt trotz seiner Bezeichnung keine Kraft im physikalischen Sinn,
Versuch EM: Elektromotorische Kraft Seite 1 Einleitung Der Begriff Elektromotorische Kraft (EMK), auch als Urspannung bezeichnet, beschreibt trotz seiner Bezeichnung keine Kraft im physikalischen Sinn,
Universität des Saarlandes - Fachrichtung Anorganische Chemie Chemisches Einführungspraktikum. Elektrochemie
 Universität des Saarlandes Fachrichtung Anorganische Chemie Chemisches Einführungspraktikum Elektrochemie Elektrochemie bezeichnet mehrere verschiedene Teilgebiete innerhalb der Chemie. Sie ist zum einen
Universität des Saarlandes Fachrichtung Anorganische Chemie Chemisches Einführungspraktikum Elektrochemie Elektrochemie bezeichnet mehrere verschiedene Teilgebiete innerhalb der Chemie. Sie ist zum einen
Studienbegleitende Prüfung Modul 12 Anorganisch-Chemisches Grundpraktikum WS 2002/
 Studienbegleitende Prüfung Modul 12 Anorganisch-Chemisches Grundpraktikum WS 2002/2003 22.04.2003 Name: Vorname: Matrikelnummer: Fachsemester: Punkte: Note: Frage 1 Welche Flammenfärbung zeigen folgende
Studienbegleitende Prüfung Modul 12 Anorganisch-Chemisches Grundpraktikum WS 2002/2003 22.04.2003 Name: Vorname: Matrikelnummer: Fachsemester: Punkte: Note: Frage 1 Welche Flammenfärbung zeigen folgende
Stöchiometrie-Seminar November 2017 Pascal Heitel 1
 Stöchiometrie-Seminar 4 Pascal Heitel 1 Themen des heutigen Seminars 1) Zusammenfassung des letzten Seminars 2) Besprechung der Hausaufgaben 3) Theorie 4) Übungsaufgaben Pascal Heitel 2 1) Zusammenfassung
Stöchiometrie-Seminar 4 Pascal Heitel 1 Themen des heutigen Seminars 1) Zusammenfassung des letzten Seminars 2) Besprechung der Hausaufgaben 3) Theorie 4) Übungsaufgaben Pascal Heitel 2 1) Zusammenfassung
Übung zu den Vorlesungen Organische und Anorganische Chemie
 Übung zu den Vorlesungen Organische und Anorganische Chemie für Biologen und Humanbiologen 07.11.08 - Lösungen - 1. Vervollständigen Sie die Reaktionsgleichungen und benennen Sie alle Verbindungen und
Übung zu den Vorlesungen Organische und Anorganische Chemie für Biologen und Humanbiologen 07.11.08 - Lösungen - 1. Vervollständigen Sie die Reaktionsgleichungen und benennen Sie alle Verbindungen und
3.2. Aufgaben zu Säure-Base-Gleichgewichten
 .. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
.. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
2. Teilklausur zum Chemischen Grundpraktikum im WS 2010/11 vom
 2. Teilklausur zum Chemischen Grundpraktikum im WS 2010/11 vom 02.02.2011 A1 A2 A3 F1 F2 R1 R2 E1 Σ Note 8 7 10 4 5 3 6 7 NAME/VORNAME:... LÖSUNGEN Matrikelnummer:... Schreiben Sie bitte gut leserlich:
2. Teilklausur zum Chemischen Grundpraktikum im WS 2010/11 vom 02.02.2011 A1 A2 A3 F1 F2 R1 R2 E1 Σ Note 8 7 10 4 5 3 6 7 NAME/VORNAME:... LÖSUNGEN Matrikelnummer:... Schreiben Sie bitte gut leserlich:
wird titriert mit Salzsäure der Konzentration c(hcl) = 1 mol/l.
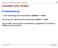 1 Problemstellung 1 Liter Natronlauge der Konzentration c(naoh) = 1 mol/l wird titriert mit Salzsäure der Konzentration c(hcl) = 1 mol/l. Der ph-wert Lösung soll für verschiedene zugegebene HCl-Volumina
1 Problemstellung 1 Liter Natronlauge der Konzentration c(naoh) = 1 mol/l wird titriert mit Salzsäure der Konzentration c(hcl) = 1 mol/l. Der ph-wert Lösung soll für verschiedene zugegebene HCl-Volumina
2. Teilklausur zum Chemischen Grundpraktikum im WS 2009/10 vom (Liebig-Laboratorium)
 2. Teilklausur zum Chemischen Grundpraktikum im WS 2009/10 vom 27.01.2010 (Liebig-Laboratorium) A1 A2 A3 A4 A5 A6 A 7 Σ Note 10 9 6 5 5 9 6 NAME:... VORNAME:... IMMATRIKULATIONSNUMMER:... Schreiben Sie
2. Teilklausur zum Chemischen Grundpraktikum im WS 2009/10 vom 27.01.2010 (Liebig-Laboratorium) A1 A2 A3 A4 A5 A6 A 7 Σ Note 10 9 6 5 5 9 6 NAME:... VORNAME:... IMMATRIKULATIONSNUMMER:... Schreiben Sie
κ Κα π Κ α α Κ Α
 κ Κα π Κ α α Κ Α Ζ Μ Κ κ Ε Φ π Α Γ Κ Μ Ν Ξ λ Γ Ξ Ν Μ Ν Ξ Ξ Τ κ ζ Ν Ν ψ Υ α α α Κ α π α ψ Κ α α α α α Α Κ Ε α α α α α α α Α α α α α η Ε α α α Ξ α α Γ Α Κ Κ Κ Ε λ Ε Ν Ε θ Ξ κ Ε Ν Κ Μ Ν Τ μ Υ Γ φ Ε Κ Τ θ
κ Κα π Κ α α Κ Α Ζ Μ Κ κ Ε Φ π Α Γ Κ Μ Ν Ξ λ Γ Ξ Ν Μ Ν Ξ Ξ Τ κ ζ Ν Ν ψ Υ α α α Κ α π α ψ Κ α α α α α Α Κ Ε α α α α α α α Α α α α α η Ε α α α Ξ α α Γ Α Κ Κ Κ Ε λ Ε Ν Ε θ Ξ κ Ε Ν Κ Μ Ν Τ μ Υ Γ φ Ε Κ Τ θ
Übungsklausur zum chemischen Praktikum für Studierende mit Chemie als Nebenfach
 Übungsklausur zum chemischen Praktikum für Studierende mit Chemie als Nebenfach 1. (10P) Was ist richtig (mehrere Richtige sind möglich)? a) Fructose besitzt 5 Kohlenstoffatome. FALSCH, Fructose besitzt
Übungsklausur zum chemischen Praktikum für Studierende mit Chemie als Nebenfach 1. (10P) Was ist richtig (mehrere Richtige sind möglich)? a) Fructose besitzt 5 Kohlenstoffatome. FALSCH, Fructose besitzt
Seminar zum Praktikum Quantitative Analyse
 Seminar zum Praktikum Quantitative Analyse Dr. Dietmar Stephan Tel.: 089-289-13167 Raum: CH 57105 E-Mail: dietmar.stephan@bauchemie-tum.de Stärke von Säuren und Basen Stärke von Säuren und Basen Dissoziationskonstanten
Seminar zum Praktikum Quantitative Analyse Dr. Dietmar Stephan Tel.: 089-289-13167 Raum: CH 57105 E-Mail: dietmar.stephan@bauchemie-tum.de Stärke von Säuren und Basen Stärke von Säuren und Basen Dissoziationskonstanten
Stöchiometrie-Seminar November 2016 Pascal Heitel 1
 Stöchiometrie-Seminar 4 Pascal Heitel 1 Themen des heutigen Seminars 1) Zusammenfassung des letzten Seminars 2) Besprechung der Hausaufgaben 3) Theorie 4) Übungsaufgaben Pascal Heitel 2 Themen des heutigen
Stöchiometrie-Seminar 4 Pascal Heitel 1 Themen des heutigen Seminars 1) Zusammenfassung des letzten Seminars 2) Besprechung der Hausaufgaben 3) Theorie 4) Übungsaufgaben Pascal Heitel 2 Themen des heutigen
(a) [4] Um welches Element handelt es sich? (Lösungsweg angeben)
![(a) [4] Um welches Element handelt es sich? (Lösungsweg angeben) (a) [4] Um welches Element handelt es sich? (Lösungsweg angeben)](/thumbs/88/117474080.jpg) Klausur zur Vorlesung LV 18000, AC1 (Anorganische Experimentalchemie) am 03.09.2007 1 1 2 3 4 5 6 7 8 9 10 Σ Note: Vorname: Matr.-Nr.: Nachname: Chemie und Biochemie Lehramt Chemie vertieft Lehramt Chemie
Klausur zur Vorlesung LV 18000, AC1 (Anorganische Experimentalchemie) am 03.09.2007 1 1 2 3 4 5 6 7 8 9 10 Σ Note: Vorname: Matr.-Nr.: Nachname: Chemie und Biochemie Lehramt Chemie vertieft Lehramt Chemie
7. Chemische Reaktionen
 7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte 7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte 7.3 Redox - Reaktionen
7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte 7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte 7.3 Redox - Reaktionen
Anorganisch-Chemisches Praktikum für Physiker:
 Anorganisch-Chemisches Praktikum für Physiker: Quantitative Analyse (Teil 1) Dr. Christopher Anson INSTITUT FÜR ANORGANISCHE CHEMIE KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum
Anorganisch-Chemisches Praktikum für Physiker: Quantitative Analyse (Teil 1) Dr. Christopher Anson INSTITUT FÜR ANORGANISCHE CHEMIE KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2016/17 vom
 Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2016/17 vom 23.09.2016 A1 A2 A3 A4 A5 Note 12 12 8 10 8 NAME:... VORNAME:... Stichpunkte zu den Lösungen Pseudonym für Ergebnisveröffentlichung:...
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2016/17 vom 23.09.2016 A1 A2 A3 A4 A5 Note 12 12 8 10 8 NAME:... VORNAME:... Stichpunkte zu den Lösungen Pseudonym für Ergebnisveröffentlichung:...
Seminar zum Quantitativen Anorganischen Praktikum WS 2011/12
 Seminar zum Quantitativen Anorganischen Praktikum WS 2011/12 Teil des Moduls MN-C-AlC Dr. Matthias Brühmann Dr. Christian Rustige Inhalt Montag, 09.01.2012, 8-10 Uhr, HS III Allgemeine Einführung in die
Seminar zum Quantitativen Anorganischen Praktikum WS 2011/12 Teil des Moduls MN-C-AlC Dr. Matthias Brühmann Dr. Christian Rustige Inhalt Montag, 09.01.2012, 8-10 Uhr, HS III Allgemeine Einführung in die
Abschlussprüfung Analytische Chemie 2: Musterprüfung
 Abschlussprüfung Analytische Chemie 2: Musterprüfung Dauer : 2 Stunden; keine Pause Erlaubte Hilfsmittel : Skript AChe2 Kunze U.R.: "Grundlagen der quantitativen Analyse", WileyVCH, Berlin (22) Schwedt
Abschlussprüfung Analytische Chemie 2: Musterprüfung Dauer : 2 Stunden; keine Pause Erlaubte Hilfsmittel : Skript AChe2 Kunze U.R.: "Grundlagen der quantitativen Analyse", WileyVCH, Berlin (22) Schwedt
Das Chemische Gleichgewicht
 Das Chemische Gleichgewicht a A + b B c C + d D r r r r Für r G = 0 gilt: Q = K r G G E D r G = dg dx
Das Chemische Gleichgewicht a A + b B c C + d D r r r r Für r G = 0 gilt: Q = K r G G E D r G = dg dx
4. Redox- und Elektrochemie
 4. Redox und Elektrochemie 4. Redox und Elektrochemie 4.1 Oxidationszahlen Eine Oxidation ist ein Vorgang, wo ein Teilchen Elektronen abgibt. Eine Reduktion ist ein Vorgang, wo ein Teilchen ein Elektron
4. Redox und Elektrochemie 4. Redox und Elektrochemie 4.1 Oxidationszahlen Eine Oxidation ist ein Vorgang, wo ein Teilchen Elektronen abgibt. Eine Reduktion ist ein Vorgang, wo ein Teilchen ein Elektron
