(no title) Ingo Blechschmidt. 4. März 2007
|
|
|
- Guido Busch
- vor 5 Jahren
- Abrufe
Transkript
1 (no title) Ingo Blechschmidt 4. März 2007 Inhaltsverzeichnis 0.1 Alkohole Alkohole im Überblick Eigenschaften der Alkohole xidierbarkeit von Alkoholen xidationsprodulte der Alkohole [Physikalische] Eigenschaften der xidationsprodukte der Alkohole (im Vergleich) hemische Eigenschaften der xidationsprodukte der Alkohole [Übersicht] Phenol ein besonderer Alkohol arbonylverbindungen arbonsäuren Ester Sauerstoffhaltige Verbindungen im Überblick Alkohole Alkohole enthalten neben den Elementen und auch. Sie leiten sich aber dennoch von den Kohlenwasserstoffen ab. 1
2 INALTSVEZEINIS 2 Beispiel: 2 6 als Summenformel Strukturformel: oder Versuch [Zugabe von Natrium zu Wasser und 2 6 ]? Beobachtung [Jeweils] exotherme eaktion unter Gasentwicklung ( 2 ) Folgerung Na Na + Na Na Da vergleichbares eaktionsprinzip, muss auch die Verbindung vergleichbar zu Wasser sein. Abspaltung von als (leichte Abspaltung, da Bindung bereits polar!) 2 Abspaltung von als Keine polare [-]Bindung; unwahrscheinlich als Struktur Alkohole im Überblick Alkohole leiten sich formal von den einfachen Kohlenwasserstoffen ab. Es existiert ebenfalls eine homologe eihe.
3 INALTSVEZEINIS 3 Formel Formel: Bezeichnung Methanol Ethanol Propanol Butanol : ydroxiegruppe [ist eine] funktionelle Gruppe, ändert die Eigenschaften Mehrwertige Alkohole [besitzen] mehr als eine -Funktion im Molekül. Beispiele: Ethandiol (1,2,3-)Propantriol Primäre Alkohole [-Atom mit -Gruppe bindet genau ein -Atom] [prim-ethanol ] prim-propanol Sekundäre Alkohole [-Atom mit -Gruppe bindet genau zwei -Atome]
4 INALTSVEZEINIS 4 [sek-propanol ] sek-butanol, 2-Butanol, Butan-2-ol Tertiäre Alkohole [-Atom mit -Gruppe bindet genau drei -Atome] tet-butanol, 2-Methylpropan-2-ol Die -Funktion ändert (je nach Lage im Molekül) die Eigenschaften eines Moleküls [Zwei -Gruppen an einem -Atom sind normalerweise nicht stabil, weil wegen der Elektronegativität des Sauerstoffs zu wenig Elektronen verfügbar wären (es findet eine zu starke Polarisierung statt)] Eigenschaften der Alkohole Die Eigenschaften der Alkohole sind durch das Vorhandensein einer -Funktion bestimmt. Löslichkeit Ethanol ist im Vergleich zu Ethan in Wasser löslich (hydrophil). Erklärung: Ethanol ist ein polares Molekül:
5 INALTSVEZEINIS 5 Ethan Keine e -Verschiebung; keine Polarität Ethanol e -Verschiebung; Polarität Lösbarkeit im polaren Lösungsmittel 2 (Umhüllung des [gesamten] Moleküls mit Wasserteilchen möglich) 2Achtung: Je länger die -Kette, desto mehr dominiert der unpolare Teil Löslichkeit sinkt [ab 10 überhaupt keine Löslichkeit mehr] Siedepunkt/Schmelzpunkt Im Vergleich zu Alkanen sind Siedepunkt/Schmelzpunkt deutlich erhöht. Es wird folglich mehr Energie benötigt, um Moleküle voneinander zu trennen. δ δ + δ + δ [Voraussetzung für Wasserstoffbrückenbindung: stark negativ polarisiertes Atom mit freien Elektronenpaaren und -Atom] Wasserstoffbrücken als sehr starke Wechselwirkung zwischen Molekülen sorgen für hohe Siedepunkte/Schmelzpunkte. [Die Wasserstoffbrückenbindung ist deshalb so stark, weil sie a) deutlich lokalisiert und b) permanent ist.] Viskosität Durch Wasserstoffbrücken werden Alkohole viskoser als vergleichbare Alkane. Brennbarkeit Ethanol brennt mit nicht rußender blauer Flamme. : -Anteil; schon teilweise oxidiert!
6 INALTSVEZEINIS xidierbarkeit von Alkoholen Grundlage: xidationszahl (gedachte Ladungszahl e an Atom) Beispiel: 2 S ( S ) Vorstellung als Ionen : + S S Für Kohlenstoffverbindungen gilt: ( ) Primärer Alkohol +1 ( ( 1 +1 Sekundärer Alkohol +1 ±0 1{ 2 +1 } 1
7 INALTSVEZEINIS 7 Tertiärer Alkohol +1 1{ Versuch Primärer Alkohol + u u +? Sekundärer Alkohol + u u +? Tertiärer Alkohol + u u 0 3 u Primäre Alkohole sind bereit, e abzugeben. Sie werden dabei zu sog. Aldehyden Exkurs: Aufstellen von edoxgleichungen 1. Teilgleichungen mit xidationszahlen 2. e -Ausgleich Bestimmung, ob xidation oder eduktion 3. Ladungsausgleich 4. Stoffausgleich 5. e -Bilanzausgleich edoxgleichung [Gesamtgleichung] eduktion +2 u + 2 e u ± xidation e
8 INALTSVEZEINIS 8 Gesamtgleichung +2 u + 1 u eduktion +7 Mn e Mn xidation e Gesamtgleichung Mn e 2 Mn e eduktion +6 r e r xidation ± / e Gesamtgleichung / 3 ± r r
9 INALTSVEZEINIS 9 ± u 0 / u + Sekundäre Alkohole sind bereit, e abzugeben. Sie werden dabei zu sog. Ketonen xidationsprodulte der Alkohole Primärer Alkohol x. Aldehyd Mit funktioneller Gruppe: δ δ + Name: Stammname al Sekundärer Alkohol x. Keton Mit funktioneller Gruppe (arbonylgruppe [auch Ketofunktion]): / Name: Stammname on [Physikalische] Eigenschaften der xidationsprodukte der Alkohole (im Vergleich) Siedepunkt/Schmelzpunkt Siedepunkt/Schmelzpunkt bei Aldehyden und Ketonen vergleichbar (durch ähnliche Polarität der funktionellen Gruppe). Im Vergleich zu Alkoholen niedrigerer Siedepunkt/Schmelzpunkt, da nur Polarität, aber keine Wasserstoffbrücken. [Je länger die Kette, desto mehr V.d.W.-Kräfte, desto höhere Siedepunkte/Schmelzpunkte]
10 INALTSVEZEINIS 10 Löslichkeit Niedrigere Vertreter sind aufgrund der polaren Gruppen in Wasser löslich; durch längere Kohlenstoffketten sinkt die Löslichkeit in Wasser, während sie in Benzin zunimmt. Viskosität Die Viskosität nimmt mit steigender Kettenlänge zu [V.d.W.- Kräfte!], ist aber nicht so stark wie bei den Alkoholen hemische Eigenschaften der xidationsprodukte der Alkohole Aldehyde a) mit ammoniakalischer Silbernitratlösung eduktion Ag + + e Ag xidation + 2 b) mit Fehling I- und II-Lösung + 2 e + 2 eduktion 2 u e + 2 u xidation e + 2 Aldehyde lassen sich oxidieren! Ketone Ketone lassen sich weder durch die sog. Fehlingprobe noch durch eine Silberspiegelprobe weiter oxidieren.
11 INALTSVEZEINIS 11 Damit gilt: Die Fehlingprobe und die Silberspiegelprobe sind spezifische Nachweisreaktionen für Aldehydfunktionen. [Die Fehlingprobe ist bei ziegelrotem Ausschlag (u 2 ) positiv. Die Silberspiegelprobe ist bei silbernem Niederschlag (Ag) positiv.] [Übersicht] Primäre Alkohole x. x. Aldehyde x. x. arbonsäuren (arboxylgruppe) [Wenn man Aldehyde haben will, darf man primäre Alkohole nur mäßig oxidieren oxidiert man zu stark, erhält man arbonsäuren.] Sekundäre Alkohole x. Ketone x. / Tertiäre Alkohole [xidiert man teritäre Alkohole (mit einem sehr starken xidationsmittel), so zerfällt das Ding.] Unterscheidungsmöglichkeit von Alkoholen und deren xidationsprodukten! Phenol ein besonderer Alkohol Aromatisierter Alkohol Mesomeriestabilisierung
12 INALTSVEZEINIS 12 Funktion Benzolring Aromatischer Alkohol mit mesomeren Grenzformeln nicht oxidierbar! reagiert sauer Protonendonator Erklärung: Phenolation (Ethanoation) Warum gibt Phenol leichter ein Proton ab als andere Alkohole? [Beim Ethanoation ist die] negative Ladung lokalisiert [ungut]: [Beim Phenolation dagegen ist die] negative Ladung über das gesamte Molekül delokalisiert [und] damit energetisch günstiger:
13 INALTSVEZEINIS 13 Es reagiert leicht sauer (gibt Proton nicht sehr leicht ab) Mesomeriestabilisierung von Phenol Mesomeriestabilisierung von 1,2-Dihydroxybenzol
14 INALTSVEZEINIS 14 [Man kann beim Aufstellen mesomerer Grenzformeln eine negative Ladung nur an Substituenten setzen, welche sind (Platzgründe: ansonsten zu große este)] arbonylverbindungen Funktionelle Gruppe: / / Alkanale (Aldehyde) / / 2
15 INALTSVEZEINIS 15 a) Beispiele Name Strukturformel Siedepunkt ( ) Wasserlöslichkeit Methanal = (Formaldehyd) / / Ethanal (Acetaldehyd) Benzaldehyd exanal (apronaldehyd) / / / 5 11 [Benzolgruppe mit dran] b) hemische Eigenschaften xidierbar zu arbonsäure 1 = + 2 / / 1 Bedeutung und Verwendung Konservation organischer Stoffe, Desinfektionsmittel 21 + Zwischenprodukt beim Alkoholabbau Propanal (Propionaldehyd) 48 - Kunst- und Duftstoffe, Arzneimittel (XXX) Anstrichmittel (XXX) Nachweis: Silberspiegel- oder Fehlingprobe 2. Ketone (Alkanone) / / 1 2 1, 2 a) Beispiele Duft- und Aromastoffe e
16 INALTSVEZEINIS 16 Propanon (Aceton) / / 3 3 Siedepunkt: 56 [Verwendung:] Lösungsmittel, Tränengas Butanon / / b) hemische Eigenschaften nicht weiter oxidierbar Unterscheidung von den Alkanalen Nucleophile Addition an die arbonylgruppe Versuch Trichlorethanal + Wasser Beobachtung Feststoff entsteht. Erklärung l l + l l / l l (hloralhydrat) Die Addition[sbereitschaft] von Wassermolekülen an die arbonylgruppe ist eine chemische Eigenschaft der Alkanale und Alkanone. Es bilden sich ydrate Typische gemeinsame eaktion der Alkanale und Alkanone Starke Polarität der arbonylgruppe aufgrund der hohen Elektronegativität des Sauerstoffatoms δ + = /δ
17 INALTSVEZEINIS 17 Allgemein: 1 = + Nu / / / / Nu Nucleophile: Wasser, Ammoniak, ydrogenchlorid, Blausäure (N), alle Alkanole ( ) Säurekatalysierter Mechanismus arboxoniumion [stabil wg. Mesomerie stabilisierung] Basenkatalysierter Mechanismus Beispiele: Nucleophile Addition von N 3 an Propanal: / N N
18 INALTSVEZEINIS 18 Nucleophile Addition von N an Propanal: N / 3 2 N [zuvor: N + + N, da Blausäure ja eine Säure ist] Addition von Alkanalen (a) albacetalbildung (b) Vollacetalbildung Weitere Nachweise der Aldehydgruppe Aldehyd + KMn 4 [Aldehyde werden oxidiert, andere Moleküle z.b. KMn 4 reduziert.]
19 INALTSVEZEINIS 19 Aldehyd + SIFFsches eagenz Farbvertiefung [Addition von Blausäure zur Kettenverlängerung] [Wenn ein oder ein N eines N potentiell angreifen könnte, greift bei uns immer das an.] [Wichtig: Mesomeriestabiliserung der positiven Ladung des - Atoms (Überklappen eines Elektronenpaars des zum damit trägt das die positive Ladung.] arbonsäuren Funktionelle Gruppe: arboxygruppe } } arbonylgruppe } } ydroxygruppe Einteilung der arbonsäuren Eine -Gruppe Monocarbonsäure Zwei -Gruppen Dicarbonsäure [Beispiel:] xalsäure / / [Mehr als zwei -Gruppen pro -Atom gibt s nicht (XXX).] [ist] aliphatisch [kettenförmig, II] Alkan-, Alken-, Alkinsäure [ist] aromatisch aromatische arbonsäure [Andere Möglichkeiten auch zulässig, aber keine spezielle Benennung (zumindest für uns)]
20 INALTSVEZEINIS 20 Vertreter Methansäure (Ameisensäure): a) Vorkommen Ameisen, Brennnessel b) Eigenschaften Farblose Flüssigkeit Stechender Geruch Sauer Versuch: Ameisensäure + KMn 4 Beobachtung: Braunfärbung und Gasentwicklung Erklärung: e (xidation) +7 Mn e Mn (eduktion) Mn Mn (Gesamtgleichung) Die Ameisensäure nimmt aufgrund ihrer reduzierenden Wirkung eine Sonderstellung bei den arbonsäuren ein. [arbonylgruppe mit statt -est = Aldehyd (oxidierbar) statt Keton (nicht oxidierbar)] Löslich in Wasser Siedepunkt 100,7 c) Darstellung [Einschub:] Versuch: Zerlegung der Armeisensäure:
21 INALTSVEZEINIS Na + Na (Natriumformiat) 2. Na + 2 S 4 + Na 2 S 4 d) [Verwendung einigungsmittel Zigarettenrauch Schädlingsbekämpfungsmittel] Ethansäure (Essigsäure): Propansäure (Propionsäure): 2 5 Butansäure (Buttersäure): 3 7 exadecansäure (Palmitinsäure): Benzolcarbonsäure (Benzoesäure): ctadecansäure (Stearinsäure): Eigenschaften der arbonsäuren a) Physikalische Eigenschaften
22 INALTSVEZEINIS 22 Siedepunkt: öher als bei Alkanen und Alkanalen durch Wasserstoffbrückenbindungen. Dimerisation [Zwei Brücken Molekül bestehend aus zwei Submolekülen ; sehr starker Zusammenhalt] [Bei Alkanalen könnte es mit der Argumentation auch zur Dimerisation kommen kommt es aber nicht (hemie ist wie backen etc.).] Löslichkeit: In Wasser nimmt die Löslichkeit mit zunehmender Anzahl der Wasserstoffatome ab, in unpolaren Lösungsmitteln zu. b) hemische Eigenschaften Säurewirkung: Versuch 1: Konzentrierte Essigsäure mit Magnesiumband [ keine eaktion] Versuch 2: Konzentrierte Essigsäure mit Magnesiumband und Wasser Gasentwicklung/Mg-Band löst sich auf [Konzentrierte Säuren können ganz allgemein niemals Metalle angreifen; Protonen alleine können das nicht. Nur wenn Wasser dazu kommt geht s: In diesem Fall kann das Proton, welches von der Säure abgegeben wird, mit dem Wasser zu 3 + -Ionen reagieren, welche dann Metalle angreifen können.] Erklärung: 3 Protonendonator Mg 2 + Mg Protonenakzeptor 3 Ethanoation
23 INALTSVEZEINIS 23 Mg Ester 3 Mg 3 2 [Magnesiumethanoat] [XXX eigentlich fehlt doch noch das 2 als Produkt, oder?] [Allgemeines] arboxylation [mesomeriestabilisiert]: / Versuch: Ethanol + Essigsäure + 2 S 4 Beobachtung: Lösungsmittelgeruch, nicht mischbar mit Wasser Erklärung: / Kondensation / Ethanol Ethylethanoat Ethansäure [Das -Atom mit den Verbindungen zu den zwei -Atomen kann bei anorganischen Estern auch beispielsweise ein N sein.] [Funktionelle Gruppe:] / ]Estergruppe Versuch: Ethylethanoat Na + Phenolphthalein Beobachtung: Entfärbung der roten [basischen] Lösung [zum Neutralen]
24 INALTSVEZEINIS 24 Erklärung: / + Na ydrolyse + + Na Ethanol Allgemein: Alkohol arbonsäure Kondensation ydrolyse / Wasser Ester [Gleichgewichtsverschiebung um gewünschte Stauffausbeite zu erhöhen] [Siedepunkt von Ester ungefähr genauso groß wie der von Alkanalen (XXX evtl. falsch!); keine Wasserstoffbrückenbindungen, aber Polarität] Verwendung Aromastoff Lösungsmittel Fette und Öle (Glycerinester mit höheren arbonsäuren) Nitroglycerin Glycerin +3 N 3 N 2 N N 2 Nitroglycerin [Das nennt man Etherbrücke.]
25 INALTSVEZEINIS 25 [Nitroglycerin ist in Wasser gelöst ok; es geht erst bei Erschütterungen hoch. Lagerung bei ca. -10.] Kunststoffe n / / n 2 + / Terephtalsäure / / / 2 2 Polyethylenterephtalat n Estergleichgewicht A + B < 0 v = v [vhin = v rück Gleichgewicht] Beeinflussung [der] eaktionsgeschwindigkeit: c T [Temperaturerniedrigung bevorzugt exotherme eaktion] P [Druckerhöhung bevorzugt eaktionsergebnis mit geringerer Teilchenzahl] Katalysator Beispiel: / > 0
26 INALTSVEZEINIS 26 Das Gleichgewicht kann nach dem Prinzip von Le hatelier beeinflusst werden (Prinzip des kleinsten Zwanges). a) Konzentrationsänderung [Ziel: größere Esterausbeute] 2 -Entzug Erhöhung [der] Alkanol[-Konzentration] b) Temperaturerniedrigung Multifunktionelle Verbindungen Versuch: Salicylsäure + Methanol Beobachtung: Typischer Estergeruch Erklärung: / / [2-ydroxybenzolcarbonsäure] + 3 / / + 2 Mehrfunktionelle Verbindungen besitzen mehrere verschiedene funktionelle Gruppen. [Eigentlich kann man das verschieden im vorherigen Satz streichen aber blablabla] Biologisch bedeutsame Verbindungen a) Glycerinaldehyd (2,3-Dihydroxypropanal) [immer das höchstoxidierteste ist Nummer 1!!] Vorkommen: Als Glycerinaldehydphosphat im Zuckerstoffwechsel (Glycolyse)
27 INALTSVEZEINIS 27 b) Brenztraubensäure (2-Ketopropansäure) / Vorkommen: Entsteht im Körper beim Zuckerstoffwechsel Alkoholische Gährung: (anaerob) Atmung: (aerob) Milchsäuregärung: [ Muskelkater zu wenig Sauerstoff vorhanden] c) Milchsäure (2-ydroxypropansäure) [Milchsäure] entsteht bei der Vergärung von Zucker durch bestimmte Bakterien. Vorkommen: Schweiß, Blut, Muskel (Muskelkater) Verwendung: Säuerungsmittel d) Zitronensäure (3-ydroxy-3-carboxy-1,5-dipentansäure) / [Zitronensäure] entsteht im Körper beim aeroben Abbau von Brenztraubensäure (Zitratzyklus). Vorkommen: Früchte, Tabak, Wein Verwendung: einigungs-, Säuerungsmittel
28 INALTSVEZEINIS 28 e) Ascorbinsäure (Vitamin ) Versuch: Ascorbinsäure + Fehling-Lösung Beobachtung: otfärbung Erklärung: e Ascorbinsäure reduzierte Form oxidierte Form Funktionelle Gruppen: ydroxy, Ester Eigenschaften: eduzierende Wirkung, Säurewirkung Nachweise: Fehlingprobe Tillmans eagenz Asc 2 + DPIP Asc x. + DPIP 2 [Bei vielen Lebensmitteln als Antioxidans unter der Nummer E 300.] f) Acetylsalicylsäure (ASS) Darstellung: / / 3 3 / + = = / / } / {{ } Essigsäurehydrid 2 S 4 / / / Acetylsalicylsäure
29 INALTSVEZEINIS Sauerstoffhaltige Verbindungen im Überblick Verbindungsklasse Allgemeine Struktur Funktionelle Gruppe Alkanole (ydroxygruppe) Ether 1 (Etherbrücke) Alkanale Alkanone arbonsäuren Ester = / / 1 1 (arbonyl- /Aldehydgruppe) / = / / / (arbonyl- /Ketogruppe) (arboxygruppe) (Estergruppe) Beispiel 3 (Methanol) 3 3 (Dimethylether) (Methanal) / (Propanon) (Methansäure) / (Methylmethanoat)
Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 )
![Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 ) Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 )](/thumbs/74/69784240.jpg) 1 25.01.2006 0.1 Alkohole Alkohole enthalten neben den Elementen C und H auch O. Sie leiten sich aber dennoch von den Kohlenwasserstoffen ab. Beispiel: C 2 H 6 O als Summenformel Strukturformel: C C O
1 25.01.2006 0.1 Alkohole Alkohole enthalten neben den Elementen C und H auch O. Sie leiten sich aber dennoch von den Kohlenwasserstoffen ab. Beispiel: C 2 H 6 O als Summenformel Strukturformel: C C O
Aldehyde und Ketone. Aldehyde C 2 H 5 H 3 C. H Propanal Propionaldehyd. H Ethanal Acetaldehyd. H Methanal Formaldehyd. Benzaldehyd.
 Aldehyde und Ketone Aldehyde Methanal Formaldehyd 3 Ethanal Acetaldehyd 2 5 Propanal Propionaldehyd Benzaldehyd Ketone 3 3 2 5 Propanon Aceton 3 2 5 2-Butanon 2 5 3-Pentanon Acetophenon 3 Natürliche Aldehyde
Aldehyde und Ketone Aldehyde Methanal Formaldehyd 3 Ethanal Acetaldehyd 2 5 Propanal Propionaldehyd Benzaldehyd Ketone 3 3 2 5 Propanon Aceton 3 2 5 2-Butanon 2 5 3-Pentanon Acetophenon 3 Natürliche Aldehyde
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Chemie Alkohole, Aldehyde & Ketone, Carbonsäuren
 Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
GRUNDWISSEN CHEMIE 10. KLASSE
 Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Organische Chemie für Mediziner WS 2016/2017. Übungsblatt 3: Ausgewählte Substanzklassen
 1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
a81 a Carbonylverbindungen (I)
 Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
a81 a Carbonylverbindungen (I)
 Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
1 Stoffklasse Alkane : C n H 2n+2 Namensendung an
 rganische hemie LÖSUNGEN Seite 1 von 11 1 Stoffklasse Alkane : n 2n+2 Namensendung an Zahl der -Atome Name Molekülformel Lewisformel Keilstrichformel Skelettformel 1 Methan 4 Sinnlos 2 Ethan 2 6 3 Propan
rganische hemie LÖSUNGEN Seite 1 von 11 1 Stoffklasse Alkane : n 2n+2 Namensendung an Zahl der -Atome Name Molekülformel Lewisformel Keilstrichformel Skelettformel 1 Methan 4 Sinnlos 2 Ethan 2 6 3 Propan
Summenformel. Strukturformel. Halbstrukturformel. Fossile Energieträger. ( 10. Klasse NTG 1 / 47 ) ( 10. Klasse NTG 2 / 47 ) ( 10. Klasse NTG 3 / 47 )
 Summenformel ( 10. Klasse NTG 1 / 47 ) Angabe der Atomsorten und deren Anzahl innerhalb eines Moleküls z.b. Ethanol C 2 6 O Strukturformel ( 10. Klasse NTG 2 / 47 ) Darstellung der bindenden und freien
Summenformel ( 10. Klasse NTG 1 / 47 ) Angabe der Atomsorten und deren Anzahl innerhalb eines Moleküls z.b. Ethanol C 2 6 O Strukturformel ( 10. Klasse NTG 2 / 47 ) Darstellung der bindenden und freien
IUPAC-Nomenklaturregeln als Grundlage für Q11 Chemie
 Nomenklatur 1 IUPA-Nomenklaturregeln als Grundlage für Q11 hemie 1 Kohlenwasserstoffe und Derivate 1.1 Regeln zur Benennung von unverzweigten Alkanen (n-alkane) Der Name der n-alkane enthält die folgenden
Nomenklatur 1 IUPA-Nomenklaturregeln als Grundlage für Q11 hemie 1 Kohlenwasserstoffe und Derivate 1.1 Regeln zur Benennung von unverzweigten Alkanen (n-alkane) Der Name der n-alkane enthält die folgenden
Kohlenwasserstoffe. Homologe Reihe. Alkane. Alkene. HGA-Grundwissen Chemie-10. Klasse NTG
 GA-Grundwissen Chemie-10. Klasse NTG Kohlenwasserstoffe Sind eine Stoffgruppe von chemischen Verbindungen, die nur aus C- und - Atomen bestehen. Aufgrund des unpolaren Molekülbaus sind sie lipophil und
GA-Grundwissen Chemie-10. Klasse NTG Kohlenwasserstoffe Sind eine Stoffgruppe von chemischen Verbindungen, die nur aus C- und - Atomen bestehen. Aufgrund des unpolaren Molekülbaus sind sie lipophil und
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
Chemie der Kohlenwasserstoffe
 hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt: Organische Chemie II. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Grundwissen Chemie Mittelstufe (10 MNG)
 Grundwissen hemie Mittelstufe (10 MNG) Marie-Therese-Gymnasium Erlangen Einzeldateien: GW8 Grundwissen für die 8. Jahrgangsstufe GW9 Grundwissen für die 9. Jahrgangsstufe (MNG) GW9a Grundwissen für die
Grundwissen hemie Mittelstufe (10 MNG) Marie-Therese-Gymnasium Erlangen Einzeldateien: GW8 Grundwissen für die 8. Jahrgangsstufe GW9 Grundwissen für die 9. Jahrgangsstufe (MNG) GW9a Grundwissen für die
Alkohole Brüder des Wassers
 6. Alkohole Brüder des Wassers 6.1 Alkohole Brüder des Wassers entsteht aus Zucker durch die alkoholische Gärung. Dabei werden Glucosemoleküle mit ilfe von efezellen in und Kohlendioxid umgewandelt. NS29
6. Alkohole Brüder des Wassers 6.1 Alkohole Brüder des Wassers entsteht aus Zucker durch die alkoholische Gärung. Dabei werden Glucosemoleküle mit ilfe von efezellen in und Kohlendioxid umgewandelt. NS29
Halogenalkane. Radikalische Halogenierung von Alkanen. Addition von Halogenwasserstoffen an Alkene. H 3 C + HBr H C C C H.
 alogenalkane erstellung: adikalische alogenierung von Alkanen + l + l + l l l + l Addition von alogenwasserstoffen an Alkene 3 Br + Br 3 Nucleophile Substitution an Alkylhalogeniden Nucleophil Elektrophil
alogenalkane erstellung: adikalische alogenierung von Alkanen + l + l + l l l + l Addition von alogenwasserstoffen an Alkene 3 Br + Br 3 Nucleophile Substitution an Alkylhalogeniden Nucleophil Elektrophil
im Molekül eine Dreifachbindung (eine σ-bindung,
 1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
Aufgaben zu Aldehyden und Ketonen
 Aufgaben zu Aldehyden und Ketonen 1. Formulieren Sie jeweils die Reaktionsgleichungen! a) erstellung von Ethanal aus einem Alkanol mit Sauerstoff (mit Ag als Katalysator) b) erstellung von yclohexanon
Aufgaben zu Aldehyden und Ketonen 1. Formulieren Sie jeweils die Reaktionsgleichungen! a) erstellung von Ethanal aus einem Alkanol mit Sauerstoff (mit Ag als Katalysator) b) erstellung von yclohexanon
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissenkarten Hans-Carossa- Gymnasium
 Grundwissenkarten Hans-Carossa- Gymnasium 10. Klasse Chemie SG Es sind insgesamt 20 Karten für die 10. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundwissenkarten Hans-Carossa- Gymnasium 10. Klasse Chemie SG Es sind insgesamt 20 Karten für die 10. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
1. Homologe Reihe der Alkansäuren
 1. omologe Reihe der Alkansäuren 2 Mit Zunahme der Kettenlänge verlängern sich die unpolaren Teile (Alkylgruppen) der Alkansäuremoleküle, dadurch steigen die van-der-waals-kräfte zwischen den Molekülen
1. omologe Reihe der Alkansäuren 2 Mit Zunahme der Kettenlänge verlängern sich die unpolaren Teile (Alkylgruppen) der Alkansäuremoleküle, dadurch steigen die van-der-waals-kräfte zwischen den Molekülen
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Funktionelle Gruppen Alkohol
 Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Orbital. Atombindung, Bindung. Elektronegativität. Dipol
 GW Chemie 10. SG GA rbital aum, in dem sich Elektronen mit 99%iger Wahrscheinlichkeit aufhalten; in einem rbital halten sich maximal 2 Elektronen auf; man unterscheidet Atom- und Molekülorbitale Atombindung,
GW Chemie 10. SG GA rbital aum, in dem sich Elektronen mit 99%iger Wahrscheinlichkeit aufhalten; in einem rbital halten sich maximal 2 Elektronen auf; man unterscheidet Atom- und Molekülorbitale Atombindung,
Vom Alkohol zum Oxidationsprodukte der Alkohole
 Vom Alkohol zum xidationsprodukte der Alkohole Wiederholung: Alkohole und Aldehyde sind wichtige organische Stoffklassen. Sie spielen sowohl in der organischen hemie, als auch im Alltag eine wichtige Rolle.
Vom Alkohol zum xidationsprodukte der Alkohole Wiederholung: Alkohole und Aldehyde sind wichtige organische Stoffklassen. Sie spielen sowohl in der organischen hemie, als auch im Alltag eine wichtige Rolle.
III. Saure, basische und neutrale Lösungen
 III. Saure, basische und neutrale Lösungen Säure/Base-Reaktionen sind Reaktionen bei denen Protonen ausgetauscht werden. Säuren sind immer Protonendonatoren, d.h. sie geben Protonen ab. So bilden sich
III. Saure, basische und neutrale Lösungen Säure/Base-Reaktionen sind Reaktionen bei denen Protonen ausgetauscht werden. Säuren sind immer Protonendonatoren, d.h. sie geben Protonen ab. So bilden sich
Organische Chemie 10C1. Funktionelle Gruppen 10C2. Homologe Reihe der Alkane 10C3. Nomenklatur der Alkane (gesättigte Kohlenwasserstoffe) 10C4
 Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Grundwissen Chemie 10. Jahrgangsstufe NTG
 Grundwissen hemie 10. Jahrgangsstufe NTG 1. rganische hemie Definition: Die organische hemie ist die hemie der Kohlenstoffverbindungen mit Ausnahme von, 2, Kohlensäure und ihren Salzen 2. Kohlenwasserstoffe
Grundwissen hemie 10. Jahrgangsstufe NTG 1. rganische hemie Definition: Die organische hemie ist die hemie der Kohlenstoffverbindungen mit Ausnahme von, 2, Kohlensäure und ihren Salzen 2. Kohlenwasserstoffe
Polare Atombindung. Elektronegativität (EN) Elektronenpaarabstoßungsmodell. Dipolmoleküle. ( 10. Klasse SG - WSG 01 / 69 )
 Polare Atombindung ( 10. Klasse SG - WSG 01 / 69 ) ierbei ist das bindende Elektronenpaar zum Atom mit der höheren Elektronegativität (EN) verschoben. Dabei entstehen Teilladungen: + δ δ Elektronegativität
Polare Atombindung ( 10. Klasse SG - WSG 01 / 69 ) ierbei ist das bindende Elektronenpaar zum Atom mit der höheren Elektronegativität (EN) verschoben. Dabei entstehen Teilladungen: + δ δ Elektronegativität
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
Carbonylgruppe Aldehyd Keton. Nomenklatur (Vollhardt, 3. Aufl., S , 4. Aufl., S ; Hart S ; Buddrus, S.
 Vorlesung 35 Aldehyde und Ketone Beiden Substanzklassen gemeinsam ist die arbonylgruppe.. arbonylgruppe Aldehyd Keton Nomenklatur (Vollhardt, 3. Aufl., S. 782783, 4. Aufl., S. 857859; art S. 304305; Buddrus,
Vorlesung 35 Aldehyde und Ketone Beiden Substanzklassen gemeinsam ist die arbonylgruppe.. arbonylgruppe Aldehyd Keton Nomenklatur (Vollhardt, 3. Aufl., S. 782783, 4. Aufl., S. 857859; art S. 304305; Buddrus,
Homologe Reihe der Alkane. Benennung der Alkane. Konstitutionsisomerie. Isomerie. Was versteht man unter der Homologen Reihe der Alkane?
 Grundwissen hemie: NTG 10 1/24 omologe eihe der Alkane Was versteht man unter der omologen eihe der Alkane? Grundwissen hemie: NTG 10 2/24 Benennung der Alkane Benenne die ersten zwölf Vertreter aus der
Grundwissen hemie: NTG 10 1/24 omologe eihe der Alkane Was versteht man unter der omologen eihe der Alkane? Grundwissen hemie: NTG 10 2/24 Benennung der Alkane Benenne die ersten zwölf Vertreter aus der
Grundwissen Chemie 10. Klasse NTG
 Grundwissen Chemie 10. Klasse NTG Homologe Reihe der Alkane Methan, Ethan, Propan, Butan, Pentan, Hexan, Heptan, Octan, Nonan, Decan 10.1 C NTG Allg. Summenformel Alkane C n H 2n+2 (gesättigte Kohlenwasserstoffe,
Grundwissen Chemie 10. Klasse NTG Homologe Reihe der Alkane Methan, Ethan, Propan, Butan, Pentan, Hexan, Heptan, Octan, Nonan, Decan 10.1 C NTG Allg. Summenformel Alkane C n H 2n+2 (gesättigte Kohlenwasserstoffe,
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) OH H + - H 2 O. (aus H 3 PO 4 H 2 SO 4 ) - H + Stichpunkte zum E1-Mechanismus:
 Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
1.9. Aldehyde und Ketone (Carbonylverbindungen)
 1.9. Aldehyde und Ketone (arbonylverbindungen) omenklatur: achsilbe al on Funktionelle Gruppe arbonylgruppe xogruppe Aldehyd Alkohol dehydrogenatus Keton xidationsstufe II 3 3 3 2 3 3 Methanal Formaldehyd
1.9. Aldehyde und Ketone (arbonylverbindungen) omenklatur: achsilbe al on Funktionelle Gruppe arbonylgruppe xogruppe Aldehyd Alkohol dehydrogenatus Keton xidationsstufe II 3 3 3 2 3 3 Methanal Formaldehyd
Grundwissen der 10.Klasse NTG
 Grundwissen der 10.Klasse NTG 1. Kohlenwasserstoffe 1.1 Alkane 1.1.1 Organische Stoffe = Verbindungen, die Kohlenstoffatome enthalten Ausnahme: Kohlenstoffoxide, Kohlensäure, Carbonate 1.1.2 Kohlenwasserstoffe
Grundwissen der 10.Klasse NTG 1. Kohlenwasserstoffe 1.1 Alkane 1.1.1 Organische Stoffe = Verbindungen, die Kohlenstoffatome enthalten Ausnahme: Kohlenstoffoxide, Kohlensäure, Carbonate 1.1.2 Kohlenwasserstoffe
Grundwissen 10. Klasse NTG 1
 Grundwissen 10. Klasse NTG 1 1. rganische hemie = Kohlenstoffchemie rganische Verbindungen sind Kohlenstoffverbindungen. Ausnahmen:, 2, Kohlensäure, arbonate; 2. Eigenschaften organischer Verbindungen
Grundwissen 10. Klasse NTG 1 1. rganische hemie = Kohlenstoffchemie rganische Verbindungen sind Kohlenstoffverbindungen. Ausnahmen:, 2, Kohlensäure, arbonate; 2. Eigenschaften organischer Verbindungen
Essigsäure und Co Stationenlernen Carbonsäuren
 8. arbonsäuren 8.1 Essigsäure und o Stationenlernen arbonsäuren arbonsäuren Der erste Vertreter der arbonsäuren, den wir im Unterricht hergestellt haben ist die Benzoesäure. Strukturell einfachere Vertreter
8. arbonsäuren 8.1 Essigsäure und o Stationenlernen arbonsäuren arbonsäuren Der erste Vertreter der arbonsäuren, den wir im Unterricht hergestellt haben ist die Benzoesäure. Strukturell einfachere Vertreter
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul ademacher Institut für rganische hemie der Universität Duisburg-Essen (Teil 11: 22.12.2004) MILESS: hemie für Biologen 198 Beispiele
hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul ademacher Institut für rganische hemie der Universität Duisburg-Essen (Teil 11: 22.12.2004) MILESS: hemie für Biologen 198 Beispiele
c) Gleichzeitiger Bruch der C-X-Bindung und der C-H-Bindung
 Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
Organik KOMPAKT Organik Blatt 1/5
 rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
Carbonsäuren (Vollhardt, 3. Aufl., S. 893 ff, 4. Aufl., S. 967 ff; Hart, S. 345 ff; Buddrus, S. 501 ff)
 Vorlesung 39 arbonsäuren (Vollhardt, 3 Aufl, S 893 ff, 4 Aufl, S 967 ff; art, S 345 ff; Buddrus, S 501 ff) Die funktionelle Gruppe der arbonsäuren (= Fettsäuren) ist die arboxyl- (bzw arboxy-) Gruppe In
Vorlesung 39 arbonsäuren (Vollhardt, 3 Aufl, S 893 ff, 4 Aufl, S 967 ff; art, S 345 ff; Buddrus, S 501 ff) Die funktionelle Gruppe der arbonsäuren (= Fettsäuren) ist die arboxyl- (bzw arboxy-) Gruppe In
Christian-Ernst-Gymnasium
 Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 10 - MuG erstellt von der Fachschaft Chemie C 10.1 Molekülstruktur und Stoffeigenschaften Atombindung Die chemische Bindung,
Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 10 - MuG erstellt von der Fachschaft Chemie C 10.1 Molekülstruktur und Stoffeigenschaften Atombindung Die chemische Bindung,
1. Bei den folgenden Stoffumwandlungen handelt es sich um typische Reaktionen der organischen Chemie.
 rganische hemie E 102 Aufgaben 7 1. Bei den folgenden Stoffumwandlungen handelt es sich um typische Reaktionen der organischen hemie. 2 /Na Na + Et Et / KN N 2 Um welche Reaktionen handelt es sich? 1.
rganische hemie E 102 Aufgaben 7 1. Bei den folgenden Stoffumwandlungen handelt es sich um typische Reaktionen der organischen hemie. 2 /Na Na + Et Et / KN N 2 Um welche Reaktionen handelt es sich? 1.
Inhaltsverzeichnis zu Kapitel 10. Aldehyde und Ketone
 Inhaltsverzeichnis zu Kapitel 10. Aldehyde und Ketone 10. Aldehyde und Ketone 106 10.1 Nomenklatur 106 10.2 Die arbonylgruppe 106 10.3 Darstellung 107 10.3.1 xidation von Alkoholen 107 10.3.2 eduktion
Inhaltsverzeichnis zu Kapitel 10. Aldehyde und Ketone 10. Aldehyde und Ketone 106 10.1 Nomenklatur 106 10.2 Die arbonylgruppe 106 10.3 Darstellung 107 10.3.1 xidation von Alkoholen 107 10.3.2 eduktion
ALDEHYDE & KETONE. Referat über die Carbonylverbindungen: Aldehyde und Ketone Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium
 ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
10. Jahrgangsstufe Organische Chemie Skript Einführungsklasse
 4. Die Eigenschaften von Alkanen 4.1 Der Aggregatszustand bzw. die Siedetemperatur Der Aggregatszustand von Alkanen bei Raumtemperatur ist von der Siedetemperatur abhängig und steht in Zusammenhang mit
4. Die Eigenschaften von Alkanen 4.1 Der Aggregatszustand bzw. die Siedetemperatur Der Aggregatszustand von Alkanen bei Raumtemperatur ist von der Siedetemperatur abhängig und steht in Zusammenhang mit
Zur Benennung organischer Moleküle
 Zur Benennung organischer Moleküle Beispiele und Übungen Funktionelle Gruppen Es sind Atomgruppen in organischen Verbindungen. Sie verändern die Stoffeigenschaften und das Reaktionsverhalten des Ausgangskohlenwasserstoffs.
Zur Benennung organischer Moleküle Beispiele und Übungen Funktionelle Gruppen Es sind Atomgruppen in organischen Verbindungen. Sie verändern die Stoffeigenschaften und das Reaktionsverhalten des Ausgangskohlenwasserstoffs.
Wo wird am meisten Alkohol abgebaut in unserem Körper? Antworten: a) Ausscheidung durch Schweiss (=> Posten 12d) b) Abbau in Leber (=> Posten 7t)
 Posten 1a Wo wird am meisten Alkohol abgebaut in unserem Körper? a) Ausscheidung durch Schweiss (=> Posten 12d) b) Abbau in Leber (=> Posten 7t) c) Ausscheidung durch Lunge (=> Posten 16n) d) Kann nicht
Posten 1a Wo wird am meisten Alkohol abgebaut in unserem Körper? a) Ausscheidung durch Schweiss (=> Posten 12d) b) Abbau in Leber (=> Posten 7t) c) Ausscheidung durch Lunge (=> Posten 16n) d) Kann nicht
Organische Chemie. Kohlenstoff. Kohlenstoffkreislauf. Erdölverarbeitung. Kohlenwasserstoffe
 rganische hemie Teilgebiet der hemie, welches sich mit Aufbau, erstellung und Eigenschaften der Verbindungen des Kohlenstoffs beschäftigt. NTG 10.1 Kohlenstoff - 4. auptgruppe 4 Valenzelektronen 4 Bindungen
rganische hemie Teilgebiet der hemie, welches sich mit Aufbau, erstellung und Eigenschaften der Verbindungen des Kohlenstoffs beschäftigt. NTG 10.1 Kohlenstoff - 4. auptgruppe 4 Valenzelektronen 4 Bindungen
c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
 Carbonsäuren schriftliche Ausarbeitungen zu folgenden Themen: a) Eigenschaften von organischen Säuren b) Begriff der homologen Reihe der Carbonsäuren c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
Carbonsäuren schriftliche Ausarbeitungen zu folgenden Themen: a) Eigenschaften von organischen Säuren b) Begriff der homologen Reihe der Carbonsäuren c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
O H H 3 C. Methanol. Molekulargewicht Siedepunkt Löslichkeit in Wasser H 3 C-OH. unbegrenzt H 3 C-Cl. 7.4 g/l H 3 C-CH 3 -24/C -88/C
 Struktur und Eigenschaften 3 C 3 C C 3 105 109 112 Wasser Methanol Dimethylether Vektoraddition der einzelnen Dipolmomente eines Moleküls zum Gesamtdipolmoment Anmerkung zu aktuellen Ereignissen: itrofen
Struktur und Eigenschaften 3 C 3 C C 3 105 109 112 Wasser Methanol Dimethylether Vektoraddition der einzelnen Dipolmomente eines Moleküls zum Gesamtdipolmoment Anmerkung zu aktuellen Ereignissen: itrofen
Prof. Christoffers, Vorlesung Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler
 Prof. hristoffers, Vorlesung rganische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 10. Aldehyde und Ketone 10.1 Nomenklatur ' Aldehyd Keton thanal "Formaldehyd" hanal
Prof. hristoffers, Vorlesung rganische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 10. Aldehyde und Ketone 10.1 Nomenklatur ' Aldehyd Keton thanal "Formaldehyd" hanal
13.1. Struktur der Carbonyl-Gruppe, Prinzipielle Reaktivität
 13. arbonyl -Verbindungen 13.1. Struktur der arbonyl-gruppe, Prinzipielle Reaktivität 13.2. Aldehyde & Ketone 13.2.1 Nomenklatur 13.2.2 Darstellungen xidationen 13.2.3 Reaktionen Additionen an der = Acetale
13. arbonyl -Verbindungen 13.1. Struktur der arbonyl-gruppe, Prinzipielle Reaktivität 13.2. Aldehyde & Ketone 13.2.1 Nomenklatur 13.2.2 Darstellungen xidationen 13.2.3 Reaktionen Additionen an der = Acetale
Organische Chemie. Maximilian Ernestus
 rganische hemie Maximilian Ernestus Inhaltsverzeichnis 1 rganische hemie 2 1.1 Wichtige Eigenschaften von Kohlenstoff..................... 2 1.2 Alkane....................................... 3 1.2.1 Isomere..................................
rganische hemie Maximilian Ernestus Inhaltsverzeichnis 1 rganische hemie 2 1.1 Wichtige Eigenschaften von Kohlenstoff..................... 2 1.2 Alkane....................................... 3 1.2.1 Isomere..................................
Chemie für Biologen, Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema ) iii) Carbonsäure iv) Dicarbonsäure
 Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
9 Aromaten. 1 Elemente Chemie Oberstufe NRW Ernst Klett Verlag GmbH, Stuttgart Lösungen zu den Durchblick-Seiten
 Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
chulportfolio 3. Schulkonzept 3.7 Kern- und Schulcurricula G9 (Klasse 5 11) Chemie Chemie Klasse 11
 Bildungsstandards Kerncurriculum Schulcurriculum Empfohlener Stundenumfang Die SuS können Stoffe beschreiben (Alkane, Alkene ); - die Verwendung Stoffe in Alltag und Technik (Methan, Ethen, ); - den Informationsgehalt
Bildungsstandards Kerncurriculum Schulcurriculum Empfohlener Stundenumfang Die SuS können Stoffe beschreiben (Alkane, Alkene ); - die Verwendung Stoffe in Alltag und Technik (Methan, Ethen, ); - den Informationsgehalt
Grundwissen Chemie Jahrgangsstufe 10 (NTG)
 Grundwissen Chemie Jahrgangsstufe 10 (NTG) Die organische Chemie ist die Chemie des Kohlenstoffs und seiner Verbindungen. Kohlenstoffkreislauf ATMSPHÄE (C 2 ) BISPHÄE (Lebewesen) LITHSPHÄE HYDSPHÄE (Gesteine)
Grundwissen Chemie Jahrgangsstufe 10 (NTG) Die organische Chemie ist die Chemie des Kohlenstoffs und seiner Verbindungen. Kohlenstoffkreislauf ATMSPHÄE (C 2 ) BISPHÄE (Lebewesen) LITHSPHÄE HYDSPHÄE (Gesteine)
+ MnO MnO 3. Oxidierbarkeit primärer, sekundärer und tertiärer Alkohole. Chemikalien. Materialien
 DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
Carbonylverbindungen (Carbonsäuren, Aldehyde)
 Kapitel 9 arbonylverbindungen (arbonsäuren, Aldehyde) ' Aldehyde Ketone arbonsäuren Kohlensäuren Nomenklatur Aldehyde: NAME = KW-Stamm + al - als Substituent: Formyl- Beispiel: Pentanal S 3 2-Formyl-butansulfonsäure
Kapitel 9 arbonylverbindungen (arbonsäuren, Aldehyde) ' Aldehyde Ketone arbonsäuren Kohlensäuren Nomenklatur Aldehyde: NAME = KW-Stamm + al - als Substituent: Formyl- Beispiel: Pentanal S 3 2-Formyl-butansulfonsäure
Beispiel für eine Anionenaustausch-Matrix. Als funktionelle Gruppe dient hier eine Diethylaminoethylgruppe.
 Aufgabe 1 Essigsäure exansäure Der Laugenverbrauch ist im Falle der Essigsäure höher. Essigsäure verteilt sich besser in die Wasserphase, exansäure aufgrund der höheren Anzahl unpolarer Alkylreste besser
Aufgabe 1 Essigsäure exansäure Der Laugenverbrauch ist im Falle der Essigsäure höher. Essigsäure verteilt sich besser in die Wasserphase, exansäure aufgrund der höheren Anzahl unpolarer Alkylreste besser
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
GK Chemie Carbonsaeuren Ester 1975//II 1. Wie kann man Essigsäure (Ethansäure) aus anorganischen Grundstoffen hergestellt werden? Beschreiben Sie die
 GK Chemie Carbonsaeuren Ester 1975//II 1. Wie kann man Essigsäure (Ethansäure) aus anorganischen Grundstoffen hergestellt werden? Beschreiben Sie die Reaktionsschritte mit Hilfe von Gleichungen! 2. Welche
GK Chemie Carbonsaeuren Ester 1975//II 1. Wie kann man Essigsäure (Ethansäure) aus anorganischen Grundstoffen hergestellt werden? Beschreiben Sie die Reaktionsschritte mit Hilfe von Gleichungen! 2. Welche
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1. Grundwissen 10.Klasse NTG 2 Grundwissen 10.Klasse NTG 2
 Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
2.7. Fragen zu Carbonsäuren und Estern
 Benennung Wie heißen die folgenden Verbindungen? 2.7. Fragen zu arbonsäuren und Estern NH 2 H H a) N b) H 2 a) R-2,4-Diaminobutansäure (D-Form) b) 2-Hydroxypropensäure H Struktur und Benennung Erkläre
Benennung Wie heißen die folgenden Verbindungen? 2.7. Fragen zu arbonsäuren und Estern NH 2 H H a) N b) H 2 a) R-2,4-Diaminobutansäure (D-Form) b) 2-Hydroxypropensäure H Struktur und Benennung Erkläre
Carbonylverbindungen
 δ + polarisierte -Doppelbindung: δ- arbonylverbindungen Folie293 sp 2 (planar) Aldehyde: Aldehydfunktion 3 3 2 3 Formaldehyd Methanal Acetaldehyd Ethanal Propionaldehyd Propanal rotonaldehyd E-2-Butenal
δ + polarisierte -Doppelbindung: δ- arbonylverbindungen Folie293 sp 2 (planar) Aldehyde: Aldehydfunktion 3 3 2 3 Formaldehyd Methanal Acetaldehyd Ethanal Propionaldehyd Propanal rotonaldehyd E-2-Butenal
Fachcurriculum Chemie Jahrgang 11 / Einführungsphase ab 2018/19
 Fachcurriculum Chemie Jahrgang 11 / Einführungsphase ab 2018/19 Ganzjähriger Unterricht 2-stündig Unterthemen Kohlenwasserstoffe Kraftstoffe und mehr Organische Chemie organische Verbindungen Definition
Fachcurriculum Chemie Jahrgang 11 / Einführungsphase ab 2018/19 Ganzjähriger Unterricht 2-stündig Unterthemen Kohlenwasserstoffe Kraftstoffe und mehr Organische Chemie organische Verbindungen Definition
Robert-Koch-Gymnasium Deggendorf. Grundwissen Chemie. 10. Jahrgangsstufe (WSG)
 obertkochgymnasium Deggendorf Grundwissen Chemie 10. Jahrgangsstufe (WSG) Molekülstruktur und Stoffeigenschaften rbitalmodell: Die Elektronen in der Atomhülle befinden sich in rbitalen (rt mit der höchsten
obertkochgymnasium Deggendorf Grundwissen Chemie 10. Jahrgangsstufe (WSG) Molekülstruktur und Stoffeigenschaften rbitalmodell: Die Elektronen in der Atomhülle befinden sich in rbitalen (rt mit der höchsten
Oxidationsversuche an allen C 1 -C 4 -Alkanolen
 Oxidationsversuche an allen C 1 -C 4 -Alkanolen Chemikalien: Geräte: Methanol, Ethanol, 1-Propanol, 2-Propanol, 1-Butanol, 2-Butanol, 2-Methyl-1-propanol, 2-Methyl-2-propanol, Kupfer-Blech, Wasser, Indikatorpapier,
Oxidationsversuche an allen C 1 -C 4 -Alkanolen Chemikalien: Geräte: Methanol, Ethanol, 1-Propanol, 2-Propanol, 1-Butanol, 2-Butanol, 2-Methyl-1-propanol, 2-Methyl-2-propanol, Kupfer-Blech, Wasser, Indikatorpapier,
Weiterentwicklung des Atommodells
 Weiterentwicklung des Atommodells Rutherfordsches Atommodell (1911) Ein Atom besteht aus * dem Kern, der positiv geladen ist und fast die gesamte Masse des Atoms ausmacht * der Atomhülle, in der sich die
Weiterentwicklung des Atommodells Rutherfordsches Atommodell (1911) Ein Atom besteht aus * dem Kern, der positiv geladen ist und fast die gesamte Masse des Atoms ausmacht * der Atomhülle, in der sich die
Stoffverteilungsplan
 Stoffverteilungsplan für Chemie Klasse 10 in Bayern für sprachliche, humanistische, musische, Wirtschafts- und sozialwissenschaftliche Gymnasien 934.339 für das 8-jährige Gymnasium C 10.1 Molekülstruktur
Stoffverteilungsplan für Chemie Klasse 10 in Bayern für sprachliche, humanistische, musische, Wirtschafts- und sozialwissenschaftliche Gymnasien 934.339 für das 8-jährige Gymnasium C 10.1 Molekülstruktur
Versuchsprotokoll. Synthese von Aromastoffen. Gruppe 7, Typ: Pflichtversuch O OH H 3 C C C C C CH 3 H H 3 C C C C C O C C OH
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 26.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Synthese von Aromastoffen Gruppe
Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 26.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Synthese von Aromastoffen Gruppe
Schulcurriculum für die Einführungsphase Chemie Jahrgang 11
 Helene-Lange-Schule Hannover Schulcurriculum für die Einführungsphase Chemie Jahrgang 11 ganzjähriger Unterricht: ca. 64 Unterrichtsstd. Hinweis: Folgende grundlegende Kompetenzen aus dem Bereich Kommunikation
Helene-Lange-Schule Hannover Schulcurriculum für die Einführungsphase Chemie Jahrgang 11 ganzjähriger Unterricht: ca. 64 Unterrichtsstd. Hinweis: Folgende grundlegende Kompetenzen aus dem Bereich Kommunikation
C H. Grundwissen Chemie Jahrgangsstufe 10, sprachlicher Zweig
 Grundwissen Chemie Jahrgangsstufe 10, Räumlicher Bau von Molekülen ier eignet sich das VSEPR-Modell (valence shell electron pair repulsion) gut zur Erklärung fast aller Strukturen. Dabei positionieren
Grundwissen Chemie Jahrgangsstufe 10, Räumlicher Bau von Molekülen ier eignet sich das VSEPR-Modell (valence shell electron pair repulsion) gut zur Erklärung fast aller Strukturen. Dabei positionieren
GRUNDWISSEN CHEMIE 10 - MuG erstellt von der Fachschaft Chemie
 Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 10 - MuG erstellt von der Fachschaft Chemie C 10.1 Molekülstruktur und Stoffeigenschaften Atombindung Die chemische Bindung,
Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 10 - MuG erstellt von der Fachschaft Chemie C 10.1 Molekülstruktur und Stoffeigenschaften Atombindung Die chemische Bindung,
Schuleigenes Curriculum für das Fach Chemie in der Einführungsphase
 Schuleigenes Curriculum für das Fach Chemie in der Einführungsphase Inhalte Homologe Reihe der Alkane Fachwissen und Fachkenntnisse beschreiben, dass ausgewählte organische Verbindungen Kohlenstoff- und
Schuleigenes Curriculum für das Fach Chemie in der Einführungsphase Inhalte Homologe Reihe der Alkane Fachwissen und Fachkenntnisse beschreiben, dass ausgewählte organische Verbindungen Kohlenstoff- und
wir-sind-klasse.jimdo.com
 Alkohole Alkohole sind Kohlenwasserstoffverbindungen mit einer Hydroxylgruppe (funktionelle Gruppe). Ihre allgemeine Summenformel ist C n H 2n+n OH Alkohole können mit ihrer funktionellen Gruppe Wasserstoffbrückenbindungen
Alkohole Alkohole sind Kohlenwasserstoffverbindungen mit einer Hydroxylgruppe (funktionelle Gruppe). Ihre allgemeine Summenformel ist C n H 2n+n OH Alkohole können mit ihrer funktionellen Gruppe Wasserstoffbrückenbindungen
Homologe Reihe. Alkane. Alkene. Alkine
 GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
Stoffklasse Alkane Alkene/Alkine Aromaten
 Stoffklasse Alkane Alkene/Alkine Aromaten funktionelle Gruppe Bezeichnung Einfachbindung Doppel-/Dreifachbindung aromatisches System Präfix Alkyl- Alkenyl/Alkinyl- Phenyl- Suffix -alkan -en/-in -Benzol
Stoffklasse Alkane Alkene/Alkine Aromaten funktionelle Gruppe Bezeichnung Einfachbindung Doppel-/Dreifachbindung aromatisches System Präfix Alkyl- Alkenyl/Alkinyl- Phenyl- Suffix -alkan -en/-in -Benzol
ORGANISCHE CHEMIE TEIL 2 ORGANISCHE SAUERSTOFFVERBINDUNGEN
 KS RGANISCE CEMIE TEIL 2 RGANISCE SAUERSTFFVERBINDUNGEN Skript rganische Chemie 2 (GF) V2.0 02/14 Marc Borer 1 INALTSVERZEICNIS "RGANISCE SAUERSTFFVERBINDUNGEN" 1. Die Stoffgruppe der Alkohole... 02 1.1
KS RGANISCE CEMIE TEIL 2 RGANISCE SAUERSTFFVERBINDUNGEN Skript rganische Chemie 2 (GF) V2.0 02/14 Marc Borer 1 INALTSVERZEICNIS "RGANISCE SAUERSTFFVERBINDUNGEN" 1. Die Stoffgruppe der Alkohole... 02 1.1
Grundwissen Chemie Klasse
 Grundwissen Chemie 8. 10. Klasse Grundwissen Chemie 8I Chemie Reinstoff und Gemisch Atome und Moleküle Chemische Reaktionen Analyse und Synthese Katalysatoren Luft Sauerstoff und Wasserstoff Redoxreaktionen
Grundwissen Chemie 8. 10. Klasse Grundwissen Chemie 8I Chemie Reinstoff und Gemisch Atome und Moleküle Chemische Reaktionen Analyse und Synthese Katalysatoren Luft Sauerstoff und Wasserstoff Redoxreaktionen
6. Rechenübung Organik (27.01./ )
 1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
Orbital. Elektronenpaarabstoßungsmodell. räumliche Grundstrukturen 1. räumliche Grundstrukturen 2
 Orbital Der Raum, in dem sich ein Elektron mit größtmöglicher Wahrscheinlichkeit aufhält. Dieses Modell ermöglicht eine Vorhersage der räumlichen Struktur eines Moleküls. Elektronenpaarabstoßungsmodell
Orbital Der Raum, in dem sich ein Elektron mit größtmöglicher Wahrscheinlichkeit aufhält. Dieses Modell ermöglicht eine Vorhersage der räumlichen Struktur eines Moleküls. Elektronenpaarabstoßungsmodell
10.1. Was versteht man unter einem Orbital? 10.2
 10.1 Was versteht man unter einem Orbital? Ein Orbital ist ein dreidimensionaler Aufenthaltsraum für maximal 2 Elektronen, in dem diese sich mit 99% Wahrscheinlichkeit aufhalten. Je nach Energiestufe ist
10.1 Was versteht man unter einem Orbital? Ein Orbital ist ein dreidimensionaler Aufenthaltsraum für maximal 2 Elektronen, in dem diese sich mit 99% Wahrscheinlichkeit aufhalten. Je nach Energiestufe ist
Viel Spaß und Erfolg!!!
 In der Jahrgangsstufe 10 erwerben die Schüler folgendes : o Sie sind in der Lage, den räumlichen Bau einfacher Moleküle zu beschreiben, daraus die zwischen den Molekülen herrschenden Kräfte abzuleiten
In der Jahrgangsstufe 10 erwerben die Schüler folgendes : o Sie sind in der Lage, den räumlichen Bau einfacher Moleküle zu beschreiben, daraus die zwischen den Molekülen herrschenden Kräfte abzuleiten
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Stationenlernen Chemie im Paket. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Stationenlernen Chemie im Paket Das komplette Material finden Sie hier: School-Scout.de Titel: Bestellnummer: 59149 Stationenlernen:
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Stationenlernen Chemie im Paket Das komplette Material finden Sie hier: School-Scout.de Titel: Bestellnummer: 59149 Stationenlernen:
Versuchsprotokoll. Mischbarkeit von Alkoholen
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Mischbarkeit von Alkoholen Gruppe
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Mischbarkeit von Alkoholen Gruppe
P Station 1: Darstellung der Carbonsäuren
 P Station 1: Darstellung der Carbonsäuren Carbonsäuren lassen sich durch Oxidation der entsprechenden Aldehyde darstellen. Die Oxidation der Aldehyde kann in einem Versuch mit heißem Kupferoxid im Abzug
P Station 1: Darstellung der Carbonsäuren Carbonsäuren lassen sich durch Oxidation der entsprechenden Aldehyde darstellen. Die Oxidation der Aldehyde kann in einem Versuch mit heißem Kupferoxid im Abzug
8 Carbonsäuren und Derivate
 8 arbonsäuren und Derivate 8.1 Allgemeine Darstellungsverfahren xidation primärer Alkohole und Aldehyde (s. Kap. 6) 2 2 xidation durch r 3 /, KMn 4 /, N 3 aloform-eaktion (s. Kap. 9) 3 Br 2 xidation von
8 arbonsäuren und Derivate 8.1 Allgemeine Darstellungsverfahren xidation primärer Alkohole und Aldehyde (s. Kap. 6) 2 2 xidation durch r 3 /, KMn 4 /, N 3 aloform-eaktion (s. Kap. 9) 3 Br 2 xidation von
O + I +I I + III 0. P Station 1: Darstellung der Carbonsäuren. Lernzirkel: Carbonsäuren und Carbonsäure-Ester, Lösung
 P Station 1: Darstellung der Carbonsäuren Ergebnis: Das schwarze Kupferblech wird nach dem Eintauchen wieder blank. Kupferoxid wurde zu metallischem Kupfer reduziert. Ergänzen Sie in folgender Tabelle
P Station 1: Darstellung der Carbonsäuren Ergebnis: Das schwarze Kupferblech wird nach dem Eintauchen wieder blank. Kupferoxid wurde zu metallischem Kupfer reduziert. Ergänzen Sie in folgender Tabelle
Definiere den Begriff Orbital. Leiten Sie die räumliche Struktur des Wassers her, zeichnen und benennen Sie sie.
 Definiere den Begriff rbital. Das rbital ist ein Bereich, in dem sich ein Elektron mit großer Wahrscheinlichkeit befindet. In jedem rbital befinden sich maximal zwei Elektronen. Leiten Sie die räumliche
Definiere den Begriff rbital. Das rbital ist ein Bereich, in dem sich ein Elektron mit großer Wahrscheinlichkeit befindet. In jedem rbital befinden sich maximal zwei Elektronen. Leiten Sie die räumliche
Molekülstruktur und Stoffeigenschaften
 Molekülstruktur und Stoffeigenschaften rbital Der aum, in dem sich ein Elektron mit größtmöglicher Wahrscheinlichkeit aufhält. Elektronenpaarabstoßungsmodell Dieses Modell ermöglicht eine Vorhersage der
Molekülstruktur und Stoffeigenschaften rbital Der aum, in dem sich ein Elektron mit größtmöglicher Wahrscheinlichkeit aufhält. Elektronenpaarabstoßungsmodell Dieses Modell ermöglicht eine Vorhersage der
Carbonylverbindungen
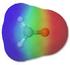 arbonylverbindungen Aliphatische arbonylverbindungen Ableitung Alkan Aldehyd Alkan Keton Funktionelle Gruppe * Formyl-Gruppe * arbonyl-gruppe * * xo-gruppe 2 Aldehyde Nomenklatur Alkan + al 2 Methanal
arbonylverbindungen Aliphatische arbonylverbindungen Ableitung Alkan Aldehyd Alkan Keton Funktionelle Gruppe * Formyl-Gruppe * arbonyl-gruppe * * xo-gruppe 2 Aldehyde Nomenklatur Alkan + al 2 Methanal
