Aufgabensammlung. Grundlagen der Verfahrenstechnik und Naturstofftechnik
|
|
|
- Etta Förstner
- vor 7 Jahren
- Abrufe
Transkript
1 Fakultät ashinenwesen Institut für Verfahrenstehnik und Uwelttehnik Professur für heishe Verfahrens- und Anlagentehnik Aufgabensalung zu Gebrauh in der Lehrveranstaltung Grundlagen der Verfahrenstehnik und Naturstofftehnik Prof. Dr.-Ing. habil. R. Lange Stand: (nur zu persönlihen Gebrauh) 1
2 Fakultät ashinenwesen Institut für Verfahrenstehnik und Uwelttehnik Professur für heishe Verfahrens- und Anlagentehnik Aufgabe Stöhioetrie 1, Aoniaksynthese - Das Haber-Bosh-Verfahren Der Grundstoff Aoniak wird nah de Haber-Bosh-Verfahren in eine Ströungsrohr katalytish produziert (500 und 450 bar). Aoni ak ist ein wihtiges Zwishenprodukt z. B. für die Herstellung von Düngeitteln und Salpetersäure. Aoniak wird bei diese Verfahren aus Stikstoff und Wasserstoff it eine stöhioetrishen engenverhältnis von 3:1 hergestellt. Der Eintrittsvoluenstro beträgt N³/h it folgenden olenbrühen: Anfangsolenbruh Aoniak 0,029 Stikstoff 0,205 Wasserstoff 0,676 Der olenbruh von Aoniak a Reaktorausgang ist 0,12. a) Welher Usatz an Wasserstoff und Stikstoff wird erreiht? Lösung: U H2 =0,18, U N2 =0,20 b) Wie viele Tonnen Aoniak werden pro Jahr produziert? Lösung: t/a ) Berehnen Sie den Aoniakvoluenstro! Lösung: 7168 N³/h Aufgabe Stöhioetrie 2, Synthese von Arolin (aus J. Hagen: he. Reaktionstehnik) Bei der katalytishen Synthese von Arolin (Propenal) aus Foraldehyd (ethanal, Einsatz als 30 %ige wässrige Lösung) und Aetaldehyd (Ethanal) geäß folgender Reaktionsgleihung: werden folgende Stoffe zu- bzw. abgeführt: H HO + H 3 HO H 2 =H HO + H 2 O (A) (B) (P) + W Zufuhr (kg/h) Abfuhr (kg/h) H HO (A) H 3 HO (B) H 2 O (W) H 2 =H HO (P) 224 Abgase und Nebenprodukte 86 Bestien Sie die Usätze von Foraldehyd und Aetaldehyd sowie die Ausbeute und Selektivität von Arolin bezogen auf die beiden Edukte! Lösung: U A =60%, U B =44%, A P,A =40%, A P,B =35,2%, S P,A =66,7%, S P,B =80% 2
3 Fakultät ashinenwesen Institut für Verfahrenstehnik und Uwelttehnik Professur für heishe Verfahrens- und Anlagentehnik Aufgabe Stöhioetrie 3, Glykol-Herstellung Zur Herstellung von Glykol (Frostshutzittel) werden die Einsatzstoffe Ethylenoxid, das aus der katalytishen Oxidation von Ethylen gewonnen wird, und Wasser verwendet: 2 H4O + H 2O 2H 4(OH) 2 E + W G Diese Reaktion läuft als Flüssigphasenreaktion ab und kann als voluenbeständig angenoen werden. Das gesate aus de Reaktor ausströende Voluen beträgt 0,75 3 /h. Die Analysen a Reaktorausgang ergaben folgende olkonzentrationen: ol G = 1,8 l ol E,12 und Wasser. l Stoffwerte: Dihte (g/l) olasse (kg/kol) 2 H 4 O (E) H 2 O (W) H 4 (OH) 2 (G) a) Wieviel ol Glykol werden stündlih erzeugt? Lösung: 1,35 kol/h b) Wieviel Wasser verlässt unverbrauht den Reaktor? Lösung: 0,665 ³/h ) Wie groß ist die ittlere Dihte des edius? Lösung: 959,2 kg/³ d) In welhe Voluenverhältnis üssen Ethylenoxid und Wasser dosiert werden, wenn das olverhältnis 1:20 betragen soll? Lösung: E/W=0,156 e) Wieviel Voluen an Wasser wird jährlih benötigt, wenn 2500 t Ethylenoxid verarbeitet werden? Lösung: a ³/a 3
4 Fakultät ashinenwesen Institut für Verfahrenstehnik und Uwelttehnik Professur für heishe Verfahrens- und Anlagentehnik Aufgabe DRK 1, Reaktion A P Eine voluenbeständige Reaktion erster Ordnung A P wird in eine diskontinuierlih betriebenen Rührkessel bei 50 durhgeführt. Der Usatz soll 0,85 betragen. Die Geshwindigkeitskonstante beträgt k,225 exp (-2570 K / T) s -1. Welhe Reaktionszeit ist erforderlih? Lösung: t R =6,69 h Aufgabe DRK 2, A + 2B 3 Die voluenbeständige Flüssigphasenreaktion A + 2 B 3 it de Reaktionsgeshwindigkeitsansatz r = k A B wird in eine diskontinuierlihen Rührkesselreaktor durhgeführt. Pro Jahr sollen Tonnen an Produkt hergestellt werden. Es sind weiterhin bekannt: A = 200 kg/kol B,0 = 2 A,0 B = 160 kg/kol B,0 = 4 ol l -1 = 120 kg/kol k,583 l/(ol. h) t Rüst = 1,5 t R a) Welher Usatz an B kann erreiht werden, wenn die Reaktionszeit eine Stunde beträgt? Lösung: U B =70% b) Welhes Reaktorvoluen ist dazu erforderlih (V R,8V DRK )? Lösung: V DRK =11,6 ³ ) Welhe asse an A, B und sind nah der Reaktion (ein Zyklus) vorhanden? Lösung: A =1116 kg, B =1785,6 kg, =4687,2 kg d) Welhe Leistungssteigerung ist in Bezug auf die produzierte enge öglih, wenn: 1.) das Reaktorvoluen verdoppelt wird, oder Lösung: 100% 2.) die Rüstzeit halbiert werden kann, oder Lösung: 42,8% 3.) die Reaktionsgeshwindigkeitskonstante verdoppelt werden kann? Lösung: 25% Definition Leistungssteigerung:, neu = 4
5 Fakultät ashinenwesen Institut für Verfahrenstehnik und Uwelttehnik Professur für heishe Verfahrens- und Anlagentehnik Aufgabe, DRK 3, A + B + D (nah Hertwig K., artens L., heishe Verfahrenstehnik Berehnung, Auslegung und Betrieb heisher Reaktoren) In eine idealen isotheren diskontinuierlihen Rührkesselreaktor findet die einfahe voluenbeständige Flüssigphasenreaktion A + B + D statt. Die Reaktion ist zweiter Ordnung (r = k A B ) und weiterhin sind gegeben: 5 k = 5,5 10 ³ kol s E A = 68400J t Rüst = 1, 5h A B D = 60g = 46g = 88g = 18g A,0 B,0,0 D,0 = 3,5kol = 4,8kol a) Berehnen Sie die notwendige ittlere Reaktionszeit, u einen Usatz der Koponente A von 97 % zu erreihen, wenn die Reaktionsteperatur 363 K beträgt! Lösung: t R =6,16 h b) Bestien Sie die Konzentrationen aller Koponenten des Reaktionsgeishes bei der erittelten Reaktionszeit! Lösung: A =0,105 ol/l, B =1,405 ol/l, =3,395 ol/l, D =3,395 ol/l ) Wie groß ist das benötigte Reaktionsvoluen, wenn jährlih 5000 t des Produktes bei einer Gesatbetriebszeit von 8000 h/a produziert werden? Lösung: V R =16,03 ³ d) Berehnen Sie die Kapazitätserhöhung für die jährlih produzierte enge an in Tonnen je Jahr, wenn it de Reaktor der gleihe Endusatz erreiht werden soll und die Reaktion bei einer u 10 K erhöhten Teperatur ablaufen würde! Lösung: =7897 t/a, Steigerung u a. 57% Aufgabe KRK 1, A + B + R In eine kontinuierlih betriebenen Rührkesselreaktor wird eine voluenbeständige Flüssigphasenreaktion it folgender Kinetik durhgeführt: A + B + R r = k A it k,6 in -1 Der Reaktorzulaufstro für die Koponente A beträgt n& A, 0 = 9ol Eintrittskonzentration A,0,5 ol. l -1. Der Usatz an A soll 60 % betragen. a) Berehnen Sie das Reaktionsvoluen! Lösung: V R = 45l / in und die b) Wie groß ist die ittlere Verweilzeit der Reaktion? Lösung: t = 2,5 in 5
6 Fakultät ashinenwesen Institut für Verfahrenstehnik und Uwelttehnik Professur für heishe Verfahrens- und Anlagentehnik Aufgabe KRK-Shaltung, A + B + D Zur Projektierung einer Versuhsanlage soll ein idealer kontinuierliher Rührkesselreaktor it einer Reihenshaltung von vier idealen Rührkesseln für eine voluenbeständige Flüssigphasenreaktion A + B + D verglihen werden. Der kontinuierlihe Rührkessel hat ein Reaktionsvoluen von 10 ³. Der Durhsatz beträgt 0,9 ³/h und für die Reaktionsgeshwindigkeit gilt r = ka it 1 k,04 in. a) Welher axiale Usatz wird für die Koponente A in de kontinuierlihen U Rührkessel erreiht? Lösung: A = 96,4% b) Wie groß uss das Reaktionsvoluen eines Rührkessel der Kaskade sein, u V l l gleihe Usätze zu erzielen? Lösung: R, Kakskade = = 1940 Aufgabe KRK 2, Reaktion zweiter Ordnung (nah Hertwig K., artens L., heishe Verfahrenstehnik Berehnung, Auslegung und Betrieb heisher Reaktoren) In eine idealen, isother und stationär betriebenen Kontinuierlihen Rührkesselreaktor findet die einfahe voluenbeständige Flüssigphasenreaktion A + B + D statt. Die Reaktion ist zweiter Ordnung (r = k A B ) und weiterhin sind gegeben: k V 5 ³ kol E A 68,4kJ = 5,5 10 s R = A B D 16³ = 60g = 46g = 88g = 18g A,0 B,0,0 D,0 = T = 363K = 3,5kol = 4,8kol a) Leiten Sie die Gleihungen für die Konzentrationen der Stoffe A und B in Abhängigkeit der Verweilzeit her! Zeihnen Sie den Verlauf für 0 < t < 100 h! b) Berehnen Sie die jährlih produzierte asse an bei einer Gesatbetriebszeit von 8000 h/a und eine Usatz an A von 97 %. Lösung: =473 t/a 6
7 Fakultät ashinenwesen Institut für Verfahrenstehnik und Uwelttehnik Professur für heishe Verfahrens- und Anlagentehnik Aufgabe RR, A + B + D (nah Hertwig K., artens L., heishe Verfahrenstehnik Berehnung, Auslegung und Betrieb heisher Reaktoren) In eine idealen isotheren Rohrreaktor findet die einfahe voluenbeständige Reaktion A + B + D statt. Die Reaktion ist zweiter Ordnung r = k A B und weiterhin sind gegeben: V = R 16³ T = 363K k 5 ³ kol E A = 68400J = 5,5 10 s A B D = 60g = 46g = 88g = 18g A,0 B,0,0 D,0 = 3,5kol = 4,8kol a) Berehnen Sie die notwendige ittlere Verweilzeit und den Voluenstro, u einen Usatz der Koponente A von 97 % zu erreihen! Lösung: t = 6, 16h V & = 2,597³ / h b) Bestien Sie die Jahresproduktion des Stoffes bei einer Gesatbetriebszeit von 8000 h/a und eine Usatz der Koponente A von 97 %. Lösung: & = 6207t / a Hinweis: dx 1 Ax + B = ln x( Ax + B) B x Aufgabe RR-DRK, A + B + D In eine diskontinuierlih betriebenen Rührkessel soll bei 100 das Produkt nah der Reaktionsgleihung A + B + D hergestellt werden. Die olaren assen der Koponenten betragen: A = 60 g/ol, B = 46 g/ol, = 88 g/ol, D = 18 g/ol Die voluenbeständige Reaktion ist in 2. Ordnung von der Konzentration an A abhängig 2 ( r = k A, k = 2,90 10 kol s ). Das Stoffengenverhältnis A/B zu Reaktionsbeginn beträgt 1:3, die Dihte der Reaktionsishung wird it 0,76 kg l -1 angegeben. 7
8 Fakultät ashinenwesen Institut für Verfahrenstehnik und Uwelttehnik Professur für heishe Verfahrens- und Anlagentehnik a) Welher Usatz an A wird bei einer Reaktionszeit von 35 inuten erreiht? Lösung: U = 70 A % b) Berehnen sie die Rüstzeit für eine Produktionsleistung von 200 kg/h an, wenn das Reaktionsvoluen des Reaktors 0,9 ³ beträgt. Lösung: t = 28,9 in ) Vergleihen sie die jährlih produzierte enge an (in t/a ) des diskontinuierlihen Rührkesselreaktors it der produzierten enge an, die in eine Rohrreaktor it gleihe Reaktionsvoluen erhalten wird der ebenso bei 70 % Usatz arbeitet! Lösung: & = 2919,6t / a Rüst d) Wie groß ist die Aktivierungsenergie, wenn der Stoßfaktor beträgt? Lösung: kj E A = 40 ol k = kol s - Aufgabe Reaktorvergleih, A + B + D Die voluenbeständige Flüssigphasenreaktion A + B + D soll in den Reaktorgrundtypen, sowie Reaktorshaltungen realisiert werden. Alle Reaktoren werden isother betrieben. Folgende Daten sind bekannt: Kinetik: Anfangskonzentrationen: r = k -4-1 A B k = 2 10 l ol s A, 0 = B, 0 = 3, 5 ol l, 0 = D, 0 a) Berehnen Sie den Endusatz nah einer Reaktionszeit von t R = 2 h, wenn die Reaktion i idealen diskontinuierlihen Rührkesselreaktor durhgeführt wird! Lösung: U A =0,83 Berehnen Sie den Endusatz, wenn die Reaktion unter den Bedingungen Voluenstro: 3 V& 3 = 2, 5 und Gesatreaktionsvoluen V 5 h R = b) i ströungstehnish idealen KRK, Lösung: U A =0,64 ) i ströungstehnish idealen RR, Lösung: U A =0,83 d) in einer Reihenshaltung aus gleihgroßen ströungstehnish idealen KRK und RR, Lösung: U A =0,79 e) in einer Reihenshaltung aus gleihgroßen ströungstehnish idealen RR und KRK durhgeführt wird! Lösung: U A =0,81 8
Institut für Technische Chemie Technische Universität Clausthal
 Institut für Tehnishe Chemie Tehnishe Universität Clausthal Tehnish-hemishes Praktikum M Versuh: Praktikumsversuh Reaktoren - Verweilzeitverteilungen Einleitung Aufgrund der Vielfalt und Komplexität hemisher
Institut für Tehnishe Chemie Tehnishe Universität Clausthal Tehnish-hemishes Praktikum M Versuh: Praktikumsversuh Reaktoren - Verweilzeitverteilungen Einleitung Aufgrund der Vielfalt und Komplexität hemisher
Strömungsrohr(reaktor)
 Strömungsrohr(reaktor) Labor für Thermishe Verfahrenstehnik bearbeitet von Prof. Dr.-Ing. habil. R. Geike 1. Aufgabenstellung Untersuht wird die hemishe Umsetzung von Essigsäureethylester (Ethylaetat)
Strömungsrohr(reaktor) Labor für Thermishe Verfahrenstehnik bearbeitet von Prof. Dr.-Ing. habil. R. Geike 1. Aufgabenstellung Untersuht wird die hemishe Umsetzung von Essigsäureethylester (Ethylaetat)
Klausur Technische Chemie SS 2007 Prof. M. Schönhoff // PD Dr. C. Cramer-Kellers Klausur zur Vorlesung
 Klausur zur Vorlesung Technische Chemie: Reaktionstechnik 9.7.2007 9:00 Uhr bis 11.00 Uhr Name, Vorname Geburtsdatum Studiengang/Semester Matrikelnummer Hinweis: Alle Ansätze und Rechenwege sind mit Worten
Klausur zur Vorlesung Technische Chemie: Reaktionstechnik 9.7.2007 9:00 Uhr bis 11.00 Uhr Name, Vorname Geburtsdatum Studiengang/Semester Matrikelnummer Hinweis: Alle Ansätze und Rechenwege sind mit Worten
Versuch 12: Wärmeflusskalorimetrie - Bestimmung der Molwärme verschiedener Stoffe
 1 Versuh 12: Wäreflusskalorietrie - Bestiung der Molwäre vershiedener Stoffe 1. Theorie und ufgabenstellung Theorie und Methode Wäreübertragungen, die it physikalishen oder heishen Reaktionen i Zusaenhang
1 Versuh 12: Wäreflusskalorietrie - Bestiung der Molwäre vershiedener Stoffe 1. Theorie und ufgabenstellung Theorie und Methode Wäreübertragungen, die it physikalishen oder heishen Reaktionen i Zusaenhang
Umsatzgrad (USG) Technische Reaktionsführung EINLEITUNG VERSUCHSZIEL. INW - Ingenieur- und NaturWissenschaften
 Umsatzgrad (USG) EINLEITUNG Die Hauptaufgabe des Reaktionstechnikers besteht darin, chemische Produktionen in geeigneten Reaktoren mit optimierter Wertschöpfung auszulegen. Wichtige Parameter auf die Wertschöpfung
Umsatzgrad (USG) EINLEITUNG Die Hauptaufgabe des Reaktionstechnikers besteht darin, chemische Produktionen in geeigneten Reaktoren mit optimierter Wertschöpfung auszulegen. Wichtige Parameter auf die Wertschöpfung
12 Enzymatische Prozesse *
 12 Enzyatishe Prozesse * Nahde in apitel 3 bereits die Grundlagen der Enzykinetik erläutert wurden, beshäftigt sih dieses apitel it der tehnishen Nutzung von Enzyen. Die Geshihte enzyatisher Prozesse beginnt
12 Enzyatishe Prozesse * Nahde in apitel 3 bereits die Grundlagen der Enzykinetik erläutert wurden, beshäftigt sih dieses apitel it der tehnishen Nutzung von Enzyen. Die Geshihte enzyatisher Prozesse beginnt
Das Chemische Gleichgewicht Massenwirkungsgesetz
 Das Chemishe Gleihgewiht Massenwirkungsgesetz Reversible Reaktionen: Beisiel : (Bodenstein 899 Edukt (Reaktanden Produkt H + I HIH Beobahtung: Die Reaktion verläuft unvollständig! ndig! D.h. niht alle
Das Chemishe Gleihgewiht Massenwirkungsgesetz Reversible Reaktionen: Beisiel : (Bodenstein 899 Edukt (Reaktanden Produkt H + I HIH Beobahtung: Die Reaktion verläuft unvollständig! ndig! D.h. niht alle
Chemische Grundgesetze
 Björn Schulz Berlin,.10.001 p.1 Cheische Grundgesetze Gesetz von der Erhaltung der Masse (Lavoisier 1785) Abbrennen einer Kerze Massenverlust geschlossenes Syste Eisennagel rostet Massenzunahe konstante
Björn Schulz Berlin,.10.001 p.1 Cheische Grundgesetze Gesetz von der Erhaltung der Masse (Lavoisier 1785) Abbrennen einer Kerze Massenverlust geschlossenes Syste Eisennagel rostet Massenzunahe konstante
Versuch 1 Bestimmung der Dichte einer Flüssigkeit
 Versuh 1 Bestiung der Dihte einer Flüssigkeit Versuh 1 Bestiung der Dihte einer Flüssigkeit Dihteessung it de digitalen Dihteeßgerät nah DIN 51757 ( Verfahren D ) Die Dihte ρ ist eine wihtige und vielfah
Versuh 1 Bestiung der Dihte einer Flüssigkeit Versuh 1 Bestiung der Dihte einer Flüssigkeit Dihteessung it de digitalen Dihteeßgerät nah DIN 51757 ( Verfahren D ) Die Dihte ρ ist eine wihtige und vielfah
Berufliches Gymnasium (WG, EG, AG, SG) Hauptprüfung 2009 Teil 4, Wirtschaftliche Anwendungen, Aufgabe 1 Baden-Württemberg
 Beruflihes Gymnasium (WG, EG, AG, SG) Hauptprüfung 9 eil, Wirtshaftlihe Anwendungen, Aufgabe Baden-Württemberg In einem Betrieb werden aus den Rohstoffen R, R, R und R die Bauteile B, B und B und aus diesen
Beruflihes Gymnasium (WG, EG, AG, SG) Hauptprüfung 9 eil, Wirtshaftlihe Anwendungen, Aufgabe Baden-Württemberg In einem Betrieb werden aus den Rohstoffen R, R, R und R die Bauteile B, B und B und aus diesen
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für hysikalische Cheie Albert-Ludwigs-Universität Freiburg hysikalische Cheie für Studierende der Mikrosystetechnik Lösungen zu 10. Übungsblatt i WS 010/11 rof. Dr. Gräber 10.1 L (8 unkte) Skizzieren
Institut für hysikalische Cheie Albert-Ludwigs-Universität Freiburg hysikalische Cheie für Studierende der Mikrosystetechnik Lösungen zu 10. Übungsblatt i WS 010/11 rof. Dr. Gräber 10.1 L (8 unkte) Skizzieren
Klausur Technische Chemie SS 2008 Prof. M. Schönhoff // PD Dr. C. Cramer-Kellers Klausur zur Vorlesung
 Klausur zur Vorlesung Technische Chemie: Reaktionstechnik 14.7.2008 10.00 Uhr bis 12.00 Uhr Name, Vorname Geburtsdatum Studiengang/Semester Matrikelnummer Hinweis: Alle Ansätze und Rechenwege sind mit
Klausur zur Vorlesung Technische Chemie: Reaktionstechnik 14.7.2008 10.00 Uhr bis 12.00 Uhr Name, Vorname Geburtsdatum Studiengang/Semester Matrikelnummer Hinweis: Alle Ansätze und Rechenwege sind mit
TU Ilmenau Chemisches Praktikum Versuch Photometrische Bestimmung der Fachgebiet Chemie. Komplexzusammensetzung
 TU Ilmenau Chemishes Praktikum Versuh Photometrishe Bestimmung der Fahgebiet Chemie Komplexzusammensetzung V20 1 Aufgabenstellung Bestimmen Sie von der folgenden Kombination CuSO 4 5 H 2 O und Ethylendiamin
TU Ilmenau Chemishes Praktikum Versuh Photometrishe Bestimmung der Fahgebiet Chemie Komplexzusammensetzung V20 1 Aufgabenstellung Bestimmen Sie von der folgenden Kombination CuSO 4 5 H 2 O und Ethylendiamin
Weiterführende Aufgaben zu chemischen Gleichgewichten
 Weiterführende Aufgaben zu hemishen Gleihgewihten Fahshule für Tehnik Suhe nah Ruhe, aber durh das Gleihgewiht, niht durh den Stillstand deiner Tätigkeiten. Friedrih Shiller Der Shlüssel zur Gelassenheit
Weiterführende Aufgaben zu hemishen Gleihgewihten Fahshule für Tehnik Suhe nah Ruhe, aber durh das Gleihgewiht, niht durh den Stillstand deiner Tätigkeiten. Friedrih Shiller Der Shlüssel zur Gelassenheit
Kinetik: a) Reaktionsgeschwindigkeit (zeitlicher Verlauf) b) Reaktionsweg (Mechanismus)
 Kinetik Kinetik: a) Reaktionsgeschwindigkeit (zeitlicher Verlauf) b) Reaktionsweg (Mechanismus) Klassifizierung chem. Reaktionen nach kinetischen Aspekten a) Reaktionsmolekularität: wie viele Teilchen
Kinetik Kinetik: a) Reaktionsgeschwindigkeit (zeitlicher Verlauf) b) Reaktionsweg (Mechanismus) Klassifizierung chem. Reaktionen nach kinetischen Aspekten a) Reaktionsmolekularität: wie viele Teilchen
Das Chemische Gleichgewicht
 Das Chemische Gleichgewicht a A + b B c C + d D r r r r Für r G = 0 gilt: Q = K r G G E D r G = dg dx
Das Chemische Gleichgewicht a A + b B c C + d D r r r r Für r G = 0 gilt: Q = K r G G E D r G = dg dx
Lösung der Zusatzaufgabe von Blatt 13
 Lösung der Zusatzaufgabe von Blatt 13 (1) Freier Fall (Fall eines Körpers i Vakuu, d.h. ohne Reibungswiderstand): (i) s = g. (a) Lösung von (i) it den Anfangsbedingungen s(0) = h und v(0) = ṡ(0) = 0: Integrieren
Lösung der Zusatzaufgabe von Blatt 13 (1) Freier Fall (Fall eines Körpers i Vakuu, d.h. ohne Reibungswiderstand): (i) s = g. (a) Lösung von (i) it den Anfangsbedingungen s(0) = h und v(0) = ṡ(0) = 0: Integrieren
Vorlesung Reaktionstechnik SS 09 Prof. M. Schönhoff/ PD Dr. Cramer
 Vorlesung Reaktonstehnk SS 9 Prof. M. Shönhoff/ PD Dr. Cramer 2.7.29 Musterlösungen zu Übungsaufgaben 2 vorzurehnen am Mo, 2.7.9 Aufgabe 5.) En Rohrbündelreaktor soll für de Durhführung ener Gasreakton
Vorlesung Reaktonstehnk SS 9 Prof. M. Shönhoff/ PD Dr. Cramer 2.7.29 Musterlösungen zu Übungsaufgaben 2 vorzurehnen am Mo, 2.7.9 Aufgabe 5.) En Rohrbündelreaktor soll für de Durhführung ener Gasreakton
Welcher Bewegungsspielraum ist für die beweglichen Auflager der Brücke zu berücksichtigen?
 Ü 4. Längendehnung einer Autobahnbrücke Bei 0 beträgt die Länge einer Autobahnbrücke 60. Die eperaturschwankung beträgt -0 i Winter bis zu +4 i Soer. Der Wäredehnungskoeffizient des bei der Brückenkonstruktion
Ü 4. Längendehnung einer Autobahnbrücke Bei 0 beträgt die Länge einer Autobahnbrücke 60. Die eperaturschwankung beträgt -0 i Winter bis zu +4 i Soer. Der Wäredehnungskoeffizient des bei der Brückenkonstruktion
Rechnungen zu Wärme und Temperatur
 Rehnunen zu Wäre und Teperatur. Welhes Voluen besitzt Propanon bei 40 C, wenn das Voluen bei 22 C 250 L beträt? kubisher Ausdehnunskoeffizient: γ(propanon) =,4 0. 2. Queksilber besitzt i Norzustand (T
Rehnunen zu Wäre und Teperatur. Welhes Voluen besitzt Propanon bei 40 C, wenn das Voluen bei 22 C 250 L beträt? kubisher Ausdehnunskoeffizient: γ(propanon) =,4 0. 2. Queksilber besitzt i Norzustand (T
Vorwort. Gernot Wilhelms. Übungsaufgaben Technische Thermodynamik ISBN: Weitere Informationen oder Bestellungen unter
 Vorwort Gernot Wilhels Übungsaufgaben Technische Therodynaik ISBN: 978-3-446-42514-9 Weitere Inforationen oder Bestellungen unter http://www.hanser.de/978-3-446-42514-9 sowie i Buchhandel. Carl Hanser
Vorwort Gernot Wilhels Übungsaufgaben Technische Therodynaik ISBN: 978-3-446-42514-9 Weitere Inforationen oder Bestellungen unter http://www.hanser.de/978-3-446-42514-9 sowie i Buchhandel. Carl Hanser
Leibniz Universität Hannover Institut für Turbomaschinen und Fluid-Dynamik Prof. Dr.-Ing. J. Seume. Klausur Herbst Strömungsmechanik I
 Leibniz Univerität Hannover Intitut für urboahinen und Fluid-Dynaik Prof. Dr.-Ing. J. Seue lauur Herbt 7 Ströungehanik I Bearbeitungdauer 9 in zugelaene Hilfittel: - ahenrehner (niht rograierbar) - FD-Forelalung
Leibniz Univerität Hannover Intitut für urboahinen und Fluid-Dynaik Prof. Dr.-Ing. J. Seue lauur Herbt 7 Ströungehanik I Bearbeitungdauer 9 in zugelaene Hilfittel: - ahenrehner (niht rograierbar) - FD-Forelalung
K4: Alkalische Esterhydrolyse
 K4: Alkalishe Esterhydrolyse Theoretishe Grundlagen: Die Konzentrationsbestimmung eines Stoffes während einer hemishen Reaktion kann auf hemishem Wege, aber auh über physikalishe Methoden vorgenommen werden.
K4: Alkalishe Esterhydrolyse Theoretishe Grundlagen: Die Konzentrationsbestimmung eines Stoffes während einer hemishen Reaktion kann auf hemishem Wege, aber auh über physikalishe Methoden vorgenommen werden.
Grundoperationen der Verfahrenstechnik. Berechnung idealer Reaktoren II
 Grundoperationen der Verfahrenstechnik 9. Übung, WS 2016/2017 Betreuer: Maik Tepper M.Sc., Maik.Tepper@avt.rwth-aachen.de Morten Logemann M.Sc., Morten.Logemann@avt.rwth-aachen.de Johannes Lohaus M.Sc.,
Grundoperationen der Verfahrenstechnik 9. Übung, WS 2016/2017 Betreuer: Maik Tepper M.Sc., Maik.Tepper@avt.rwth-aachen.de Morten Logemann M.Sc., Morten.Logemann@avt.rwth-aachen.de Johannes Lohaus M.Sc.,
Bestimmung von Reaktionsordnung und Geschwindigkeitskonstante der Hydrolyse von tertiärem Butylchlorid mit Hilfe der Leitfähigkeitsmessung
 Übungen in physialisher Chemie für B. S.-Studierende Versuh Nr.: W 14 Version 018 (13018) Kurzbezeihnung: t-butylhlorid Bestimmung von Reationsordnung und Geshwindigeitsonstante der Hydrolyse von tertiärem
Übungen in physialisher Chemie für B. S.-Studierende Versuh Nr.: W 14 Version 018 (13018) Kurzbezeihnung: t-butylhlorid Bestimmung von Reationsordnung und Geshwindigeitsonstante der Hydrolyse von tertiärem
Einführung. Versuchsaufbau, untersuchte Substrate. Ergebnisse. Bemessungsmodell. Fazit
 Einfluss der Faulraubelastung auf die Gasausbeute von Gülle und nahwahsenden Rohstoffen Forshungsprojekt gefördert von Fahagentur Nahwahsende Rohstoffe e.v. Bernd Linke und Pia Mähnert Institut für Agrartehnik
Einfluss der Faulraubelastung auf die Gasausbeute von Gülle und nahwahsenden Rohstoffen Forshungsprojekt gefördert von Fahagentur Nahwahsende Rohstoffe e.v. Bernd Linke und Pia Mähnert Institut für Agrartehnik
Absenkung des Messgastaupunktes
 72 Absenkung des Messgastaupunktes Konzentrationsänderungen und Auswashung von Shadgasen und eruhsstoffen Peter Boeker Institut für Landtehnik, Universität Bonn Zur Konditionierung von feuhten Messgasströen
72 Absenkung des Messgastaupunktes Konzentrationsänderungen und Auswashung von Shadgasen und eruhsstoffen Peter Boeker Institut für Landtehnik, Universität Bonn Zur Konditionierung von feuhten Messgasströen
Karlsruher Institut für Technologie (KIT) Institut für Technische Chemie und Polymerchemie Prof. Dr. O. Deutschmann Prof. Dr. J.-D.
 Karlsruher Institut für Tehnologie (KIT) Institut für Tehnishe Chemie und Polymerhemie Prof. Dr. O. Deutshmann Prof. Dr. J.-D. Grunwaldt Versuhsbeshreibung zum Chemish-Tehnishen Grundpraktikum Verweilzeitspektren
Karlsruher Institut für Tehnologie (KIT) Institut für Tehnishe Chemie und Polymerhemie Prof. Dr. O. Deutshmann Prof. Dr. J.-D. Grunwaldt Versuhsbeshreibung zum Chemish-Tehnishen Grundpraktikum Verweilzeitspektren
Reissen Sie das hinterste Blatt der Aufgabenstellung ab und verwenden Sie es als Deckblatt Ihrer Lösungen beim Abgeben.
 Institut für Chemie und Bioingenieurwissenshaften Chemieingenieurwissenshaften I Prof. W. J. Stark Prüfung SS 2007 Chemieingenieurwissenshaften, 4. Semester Bitte nehmen Sie sih Zeit, die Prüfung VRHER
Institut für Chemie und Bioingenieurwissenshaften Chemieingenieurwissenshaften I Prof. W. J. Stark Prüfung SS 2007 Chemieingenieurwissenshaften, 4. Semester Bitte nehmen Sie sih Zeit, die Prüfung VRHER
Übung 4. SS 2013 Übung - Einführung in die Verbrennung - Methling, Özuylasi 1
 Ziel: Grundlagen der chemischen Reaktionskinetik verstehen Verstehen qualitativer Reaktionsverläufe Aufstellung des Zeitgesetzes Umgang mit nicht reagierenden Stoßpartner (M) Berechnung Geschwindigkeitskoeffizient
Ziel: Grundlagen der chemischen Reaktionskinetik verstehen Verstehen qualitativer Reaktionsverläufe Aufstellung des Zeitgesetzes Umgang mit nicht reagierenden Stoßpartner (M) Berechnung Geschwindigkeitskoeffizient
Rechnen mit dem Mischungskreuz und der Mischungsgleichung
 Rehnen it de ishunskreuz und der ishunsleihun 1. Welhe Voluina einer 0,15-NaCl-ösun und einer 0,5-NaCl-ösun üssen eisht werden, u 50 einer 0,4-ösun herzustellen?. Aus 0,7 Ca(NO 3 ) -Stalösun und H O sollen
Rehnen it de ishunskreuz und der ishunsleihun 1. Welhe Voluina einer 0,15-NaCl-ösun und einer 0,5-NaCl-ösun üssen eisht werden, u 50 einer 0,4-ösun herzustellen?. Aus 0,7 Ca(NO 3 ) -Stalösun und H O sollen
PRAKTIKUM DER TECHNISCHEN CHEMIE I PRAKTIKUMSPROTOKOLL. WiSe 2015/2016. Versuch 6. Adiabatischer Batch-Reaktor
 PRAKTIKUM DER TECHNISCHEN CHEMIE I PRAKTIKUMSPROTOKOLL WiSe 2015/2016 Versuch 6 Adiabatischer Batch-Reaktor Rami Saoudi (356563) Guido Petri (364477) Gruppe 29 1. EINFÜHRUNG Es wurde der Temperaturverlauf
PRAKTIKUM DER TECHNISCHEN CHEMIE I PRAKTIKUMSPROTOKOLL WiSe 2015/2016 Versuch 6 Adiabatischer Batch-Reaktor Rami Saoudi (356563) Guido Petri (364477) Gruppe 29 1. EINFÜHRUNG Es wurde der Temperaturverlauf
2. Klausur zur Vorlesung Einführung in die physikalische Chemie für Lehramtskandidaten Modul 4, Wintersemester 05/06
 . Klausur zur Vorlesung Einführung in die hysikalische Cheie für Lehratskandidaten Modul 4, Winterseester 5/6 3. März 6, 9 5 45 Uhr Nae, Vornae:... Geburtsdatu, -ort:... Matrikelnuer:... Fachseester,.
. Klausur zur Vorlesung Einführung in die hysikalische Cheie für Lehratskandidaten Modul 4, Winterseester 5/6 3. März 6, 9 5 45 Uhr Nae, Vornae:... Geburtsdatu, -ort:... Matrikelnuer:... Fachseester,.
Grundpraktikum Technische Chemie. Reaktionstechnik
 Grundpraktikum Tehnishe Chemie Reaktionstehnik Inhaltsverzeihnis 1.... Übersiht 2 1.1. Versuh 2 1.2. Literatur 2 1.2.1. Grundlagen 2 1.2.2. Weiterführende Literatur 2 1.3. Zwek des Versuhs 2 1.4. Theoretishe
Grundpraktikum Tehnishe Chemie Reaktionstehnik Inhaltsverzeihnis 1.... Übersiht 2 1.1. Versuh 2 1.2. Literatur 2 1.2.1. Grundlagen 2 1.2.2. Weiterführende Literatur 2 1.3. Zwek des Versuhs 2 1.4. Theoretishe
Lehrveranstaltung: Chemische Prozesstechnik (CPT)
 Lehrveranstaltung: Chemische Prozesstechnik (CPT) Semester: Projektkurs: 1. Semester (Sommersemester) CEN Vorlesung: 3h ECTS: 5 Dozenten: Unterrichtssprache: Voraussetzungen: 2h Prof. Dr. A. König, Prof.
Lehrveranstaltung: Chemische Prozesstechnik (CPT) Semester: Projektkurs: 1. Semester (Sommersemester) CEN Vorlesung: 3h ECTS: 5 Dozenten: Unterrichtssprache: Voraussetzungen: 2h Prof. Dr. A. König, Prof.
Verweilzeitmodellierung
 Otto-von-Guerike-Universität Magdeburg Fakultät für Verfahrens- und Systemtehnik Institut für Verfahrenstehnik Versuh im Rahmen des verfahrenstehnishen Praktikums Verweilzeitmodellierung Praktikumsversuh:
Otto-von-Guerike-Universität Magdeburg Fakultät für Verfahrens- und Systemtehnik Institut für Verfahrenstehnik Versuh im Rahmen des verfahrenstehnishen Praktikums Verweilzeitmodellierung Praktikumsversuh:
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für hysikalische Cheie lbert-ludwigs-universität Freiburg Lösungen zu 9. Übungsblatt zur Vorlesung hysikalische Cheie I SS 2014 rof. Dr. artsch 9.1 L/M Hean (C 6 H 14 ) und Heptan (C 7 H 16 )
Institut für hysikalische Cheie lbert-ludwigs-universität Freiburg Lösungen zu 9. Übungsblatt zur Vorlesung hysikalische Cheie I SS 2014 rof. Dr. artsch 9.1 L/M Hean (C 6 H 14 ) und Heptan (C 7 H 16 )
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für hysikalische Cheie lbert-ludwigs-universität Freiburg Lösungen zu 8. Übungsblatt zur Vorlesung hysikalische Cheie I SS 00 rof. Dr. Bartsch 8. (5 unkte) Benzol erstarrt unter at bei 5,5 C;
Institut für hysikalische Cheie lbert-ludwigs-universität Freiburg Lösungen zu 8. Übungsblatt zur Vorlesung hysikalische Cheie I SS 00 rof. Dr. Bartsch 8. (5 unkte) Benzol erstarrt unter at bei 5,5 C;
Klausur Chemie für Verfahrenstechniker III
 Name: Matr.-Nr.: Klausur Chemie für Verfahrenstehniker III 6. 1. 26 Aufgabe 1 (2.5 Punkte) 1.1 Die Reaktion: C (s) + CO 2 (g) 2 CO (g) ist endotherm. Wie wird das Gleihgewiht beeinflusst, wenn a) CO 2
Name: Matr.-Nr.: Klausur Chemie für Verfahrenstehniker III 6. 1. 26 Aufgabe 1 (2.5 Punkte) 1.1 Die Reaktion: C (s) + CO 2 (g) 2 CO (g) ist endotherm. Wie wird das Gleihgewiht beeinflusst, wenn a) CO 2
Studienbegleitende Prüfung Modul 12 Anorganisch-Chemisches Grundpraktikum SS
 Studienbegleitende Prüfung Modul 12 Anorganish-Chemishes Grundpraktikum SS 2004 03.09.2004 ame: Vorname: Matrikelnummer: Fahsemester: Punkte: ote: Frage 1 Welhe Oxidationsstufen besitzt Chlor in: ClO -
Studienbegleitende Prüfung Modul 12 Anorganish-Chemishes Grundpraktikum SS 2004 03.09.2004 ame: Vorname: Matrikelnummer: Fahsemester: Punkte: ote: Frage 1 Welhe Oxidationsstufen besitzt Chlor in: ClO -
Besprechung der thermodynamischen Grundlagen von Wärmekraftmaschinen und Wärmepumpen
 3.5 Zustandsänderung nderung von Gasen Ziel: Besrehung der thermodynamishen Grundlagen von Wärmekraftmashinen und Wärmeumen Zustand von Gasen wird durh Druk, olumen, und emeratur beshrieben thermodyn.
3.5 Zustandsänderung nderung von Gasen Ziel: Besrehung der thermodynamishen Grundlagen von Wärmekraftmashinen und Wärmeumen Zustand von Gasen wird durh Druk, olumen, und emeratur beshrieben thermodyn.
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Isttut für Physkalshe Chee lbert-ludwgs-uverstät Freburg Lösuge zu 1. Übugsblatt zur orlesug Physkalshe Chee I SS 2014 Prof. Dr. Bartsh 1.1 L We groß st de olasse vo Dethylether (CH CH 2 OCH 2 CH )? We
Isttut für Physkalshe Chee lbert-ludwgs-uverstät Freburg Lösuge zu 1. Übugsblatt zur orlesug Physkalshe Chee I SS 2014 Prof. Dr. Bartsh 1.1 L We groß st de olasse vo Dethylether (CH CH 2 OCH 2 CH )? We
Allgemeine Chemie 3.6 KINETIK
 Allgemeine Chemie. CEMISCE REAKTINEN.6 KINETIK 1 Kinetik hemisher Reaktionen Die Kinetik befasst sih mit den Geshwindigkeiten und Mehanismen hemisher Reaktionen. Sie beshreibt zeitabhängige Konzentrationsänderungen
Allgemeine Chemie. CEMISCE REAKTINEN.6 KINETIK 1 Kinetik hemisher Reaktionen Die Kinetik befasst sih mit den Geshwindigkeiten und Mehanismen hemisher Reaktionen. Sie beshreibt zeitabhängige Konzentrationsänderungen
Die Maxwell-Boltzmann-Verteilung
 Die Maxwell-Boltzann-Verteilung Sebastian Meiss 5. Oktober 8 Mit der Maxwell-Boltzann-Verteilung kann an Aussagen über die Energie- bzw. Geschwindigkeitsverteilung von Teilchen in eine Syste beschreiben.
Die Maxwell-Boltzann-Verteilung Sebastian Meiss 5. Oktober 8 Mit der Maxwell-Boltzann-Verteilung kann an Aussagen über die Energie- bzw. Geschwindigkeitsverteilung von Teilchen in eine Syste beschreiben.
Studienbegleitende Prüfung Modul 12 Anorganisch-Chemisches Grundpraktikum SS Niederschlag von CuS Niederschlag von PbS
 Studienbegleitende Prüfung Modul 1 Anorganish-Chemishes Grundpraktikum SS 003.09.003 Name: Vorname: Matrikelnummer: Fahsemester: Punkte: Note: Frage 1 Was geshieht, wenn Sie Lösungen folgender Kationen
Studienbegleitende Prüfung Modul 1 Anorganish-Chemishes Grundpraktikum SS 003.09.003 Name: Vorname: Matrikelnummer: Fahsemester: Punkte: Note: Frage 1 Was geshieht, wenn Sie Lösungen folgender Kationen
Verbrennungsprozess: Mischung, Erwärmung, Reaktion und Energieabgabe Brennstoffe und Verbrennungsgleichungen
 11 Verbreug M45 11 Verbreug 11.1 Der Verbreugsprozess Verbreugsprozess: Mischug, Erwärug, Reaktio ud Eergieabgabe ild 11-1 Schea des Verbreugsprozesses 11.2 restoffe ud Verbreugsgleichuge Erste restoffgruppe:
11 Verbreug M45 11 Verbreug 11.1 Der Verbreugsprozess Verbreugsprozess: Mischug, Erwärug, Reaktio ud Eergieabgabe ild 11-1 Schea des Verbreugsprozesses 11.2 restoffe ud Verbreugsgleichuge Erste restoffgruppe:
Labor Messtechnik Versuch 3 Wärmetauscher
 FR Mashinenbau Labor Messtehni Versuh 3 Wäretausher Seite von 8 Versuh 3: Wäreaustausher. Versuhsaufbau.. fang es Versuhes I Versuh weren folgene Theenreise behanelt: - Gleihstro - Gegenstro - Wäreurhgangszahl..
FR Mashinenbau Labor Messtehni Versuh 3 Wäretausher Seite von 8 Versuh 3: Wäreaustausher. Versuhsaufbau.. fang es Versuhes I Versuh weren folgene Theenreise behanelt: - Gleihstro - Gegenstro - Wäreurhgangszahl..
Versuch 5: Adsorption von Essigsäure an Aktivkohle
 Versuch 5: Adsorption von Essigsäure an Aktivkohle Aufgabenstellung Es ist die Adsorption von Essigsäure an Aktivkohle quantitativ zu untersuchen und 1) der Verlauf der Adsorptionsisotheren nach Freundlich
Versuch 5: Adsorption von Essigsäure an Aktivkohle Aufgabenstellung Es ist die Adsorption von Essigsäure an Aktivkohle quantitativ zu untersuchen und 1) der Verlauf der Adsorptionsisotheren nach Freundlich
Lösungen 10 (Kinetik)
 Chemie I WS 2003/2004 Lösungen 10 (Kinetik) Aufgabe 1 Verschiedenes 1.1 Als Reaktionsgeschwindigkeit v c wird die Ableitung der Konzentration eines Reaktanden A nach der Zeit t, dividiert durch dessen
Chemie I WS 2003/2004 Lösungen 10 (Kinetik) Aufgabe 1 Verschiedenes 1.1 Als Reaktionsgeschwindigkeit v c wird die Ableitung der Konzentration eines Reaktanden A nach der Zeit t, dividiert durch dessen
Übungen PC - Kinetik - Seite 1 (von 5)
 Übungsaufgaben PC: Kinetik 1) Für die Umlagerung von cis- in trans-dichlorethylen wurde die Halbwertszeit 245 min gefunden; die Reaktion gehorcht einem Geschwindigkeitsgesetz erster Ordnung. Wie viel g
Übungsaufgaben PC: Kinetik 1) Für die Umlagerung von cis- in trans-dichlorethylen wurde die Halbwertszeit 245 min gefunden; die Reaktion gehorcht einem Geschwindigkeitsgesetz erster Ordnung. Wie viel g
Rechnung wurde das gerundete Ergebnis verwendet. Abhängig vom Rechenweg kann es aber dennoch zu leicht abweichenden Ergebnissen kommen!
 Löungen zur chriftlichen Prüfung au VO Kraftwerke a 28.04.205 Hinwei: Bei den Berechnungen wurden alle Zwichenergebnie in der technichen Notation (Forat ENG) dargetellt und auf drei Nachkoatellen gerundet.
Löungen zur chriftlichen Prüfung au VO Kraftwerke a 28.04.205 Hinwei: Bei den Berechnungen wurden alle Zwichenergebnie in der technichen Notation (Forat ENG) dargetellt und auf drei Nachkoatellen gerundet.
Leibniz Universität Hannover Institut für Turbomaschinen und Fluid-Dynamik Prof. Dr.-Ing. J. Seume. Klausur Frühjahr Strömungsmechanik I
 Leibniz Univerität Hannover Intitut für Turboahinen und luid-dynaik rof. Dr.-Ing. J. Seue Klauur rühjahr 9 Ströungehanik I Bearbeitungdauer: 9 in zugelaene Hilfittel: - Tahenrehner (niht rograierbar) -
Leibniz Univerität Hannover Intitut für Turboahinen und luid-dynaik rof. Dr.-Ing. J. Seue Klauur rühjahr 9 Ströungehanik I Bearbeitungdauer: 9 in zugelaene Hilfittel: - Tahenrehner (niht rograierbar) -
1. Geschwindigkeit von Elektronen in Drähten (2+2+2)
 Lösungen zur Übungen zur Physik (Elektrodynaik) SS 5 6 Übungsblatt 955 Bearbeitung bis Mi 555 Geschwindigkeit on Elektronen in Drähten (++) Ein Kupferdraht it de Durchesse durchflossen Berechnen Sie a)
Lösungen zur Übungen zur Physik (Elektrodynaik) SS 5 6 Übungsblatt 955 Bearbeitung bis Mi 555 Geschwindigkeit on Elektronen in Drähten (++) Ein Kupferdraht it de Durchesse durchflossen Berechnen Sie a)
Laborpraktikum Grundlagen der Umwelttechnik II
 Hochschule für Technik, Wirtschaft und Kultur Leipzig Maschinenbau und Energietechnik Versuchstag: Brennstoff- und Umweltlabor Bearbeiter: Prof. Dr.-Ing. J. Schenk Dipl.- Chem. Dorn Namen: Seminargruppe:
Hochschule für Technik, Wirtschaft und Kultur Leipzig Maschinenbau und Energietechnik Versuchstag: Brennstoff- und Umweltlabor Bearbeiter: Prof. Dr.-Ing. J. Schenk Dipl.- Chem. Dorn Namen: Seminargruppe:
. V2. = p 2 T 1 T 2. Normbedingungen Das Volumen von 1 Mol eines idealen Gases beträgt bei Normbedingungen (1.013 bar, 0 C) Liter.
 Wäreausdehnung der Gase LMPG_GASE LABA/B Während bei Flüssigkeiten und Festkörpern die Wäreausdehnung auch von der Art des Stoffes abhängt, ist dies bei Gasen nicht der Fall. Bei konstante Druck und einer
Wäreausdehnung der Gase LMPG_GASE LABA/B Während bei Flüssigkeiten und Festkörpern die Wäreausdehnung auch von der Art des Stoffes abhängt, ist dies bei Gasen nicht der Fall. Bei konstante Druck und einer
PC I Thermodynamik G. Jeschke FS Lösung zur Übung 12
 PC I Thermodynamik G. Jeschke FS 2015 Lösung zur Übung 12 12.1 Die Hydrierung von Ethen zu Ethan a) Die Reaktionsenthalpie ist direkt aus den in der Aufgabenstellung tabellierten Standardbildungsenthalpien
PC I Thermodynamik G. Jeschke FS 2015 Lösung zur Übung 12 12.1 Die Hydrierung von Ethen zu Ethan a) Die Reaktionsenthalpie ist direkt aus den in der Aufgabenstellung tabellierten Standardbildungsenthalpien
Verweilzeitverteilung
 Verweilzeitverteilung (VWZ) EINLEITUNG Die Hauptaufgabe des Reaktionstechnikers besteht darin, chemische Produktionen in geeigneten Reaktoren mit optimierter Wertschöpfung auszulegen. Wichtige Parameter
Verweilzeitverteilung (VWZ) EINLEITUNG Die Hauptaufgabe des Reaktionstechnikers besteht darin, chemische Produktionen in geeigneten Reaktoren mit optimierter Wertschöpfung auszulegen. Wichtige Parameter
Mikroplasmareaktoren für den Umweltschutz und chemischer Synthese
 Mikroplasmareaktoren für den Umweltschutz und chemischer Synthese Norbert Steinfeldt Leibniz-Institut für Katalyse e.v. an der Universität Rostock Inhalt Vorteile der Mikroverfahrenstechnik Beispiele Kombination
Mikroplasmareaktoren für den Umweltschutz und chemischer Synthese Norbert Steinfeldt Leibniz-Institut für Katalyse e.v. an der Universität Rostock Inhalt Vorteile der Mikroverfahrenstechnik Beispiele Kombination
MWG. 1. Massenwirkungsgesetz
 MWG 1. Massenwirkungsgesetz Betrahten wir den Ablauf einer hemishen Reaktion, so stellen wir fest, dass bestimmte Reaktionsgeshwindigkeiten den Vorgang beeinflussen. Wir wissen, dass formal ähnlihe Umsetzungen
MWG 1. Massenwirkungsgesetz Betrahten wir den Ablauf einer hemishen Reaktion, so stellen wir fest, dass bestimmte Reaktionsgeshwindigkeiten den Vorgang beeinflussen. Wir wissen, dass formal ähnlihe Umsetzungen
Lösungen zum Übungsblatt 6 zur Vorlesung Physikalische Chemie WS 2009/2010 Prof. Dr. Bartsch
 Lösungen zu Übungsblatt 6 zur orlesung hysikalische heie WS 9/ rof. r. artsch 6. L (6 unkte) erechnen Sie ie Stanarverbrennungsenthalpie von thylbenzol ( 8 H, aus seiner Stanarbilungsenthalpie von H -.
Lösungen zu Übungsblatt 6 zur orlesung hysikalische heie WS 9/ rof. r. artsch 6. L (6 unkte) erechnen Sie ie Stanarverbrennungsenthalpie von thylbenzol ( 8 H, aus seiner Stanarbilungsenthalpie von H -.
Verweilzeitverhalten im Rührkessel / Kaskade und Verweilzeitverhalten im Strömungsrohr
 Protokoll Verweilzeitverhalten im Rührkessel / Kaskade und Verweilzeitverhalten im Strömungsrohr Von Christian Terhorst 716822-1- Inhaltsverzeichnis 1 Aufgabenstellung 2 Rührkessel ( -kaskade ) 2.1 Versuchsaufbau
Protokoll Verweilzeitverhalten im Rührkessel / Kaskade und Verweilzeitverhalten im Strömungsrohr Von Christian Terhorst 716822-1- Inhaltsverzeichnis 1 Aufgabenstellung 2 Rührkessel ( -kaskade ) 2.1 Versuchsaufbau
2.1 Stopfgrenze. w = 1 s m o, 067. Darin bedeuten: 3,2 2,4 "' -E GI OI. e 1, ,8
 Wahl des Rohrdurhessers für pneuatishe Flugförderanlagen i Drukbetrieb on Hinrih Petersen, Braunshweig*) DK 62.867.82 Für die Berehnung von pneuatishen Förderanlagen gibt es eine ielzahl von Methoden,
Wahl des Rohrdurhessers für pneuatishe Flugförderanlagen i Drukbetrieb on Hinrih Petersen, Braunshweig*) DK 62.867.82 Für die Berehnung von pneuatishen Förderanlagen gibt es eine ielzahl von Methoden,
Institut für Abfallwirtschaft und Altlasten, TU-Dresden Seminar Thermische Abfallbehandlung - Veranstaltung 4 - Dampfkraftprozesse
 Institut für Abfallwirtschaft und Altlasten, TU-Dresden Seinar Therische Abfallbehandlung - Veranstaltung 4 - Dapfkraftprozesse Dresden, 09. Juni 2008 Dipl.- Ing. Christoph Wünsch, Prof. Dr.- Ing. habil.
Institut für Abfallwirtschaft und Altlasten, TU-Dresden Seinar Therische Abfallbehandlung - Veranstaltung 4 - Dapfkraftprozesse Dresden, 09. Juni 2008 Dipl.- Ing. Christoph Wünsch, Prof. Dr.- Ing. habil.
Mathematik-Aufgabenpool > Geraden (Haupt-/Normalform)
 Mihael Buhlann Matheatik-Aufgabenpool > Geraden (Haupt-/Noralfor) Einleitung: Geraden sind (als ganz rationale Funktionen Grades, lineare Funktionen) von der For: = x + it Geradensteigung und -Ahsenabshnitt,,
Mihael Buhlann Matheatik-Aufgabenpool > Geraden (Haupt-/Noralfor) Einleitung: Geraden sind (als ganz rationale Funktionen Grades, lineare Funktionen) von der For: = x + it Geradensteigung und -Ahsenabshnitt,,
Übungsaufgabe. Bestimmen Sie das molare Volumen für Ammoniak bei einem Druck von 1 MPa und einer Temperatur von 100 C nach
 Übungsaufgabe Bestien Sie das olare Voluen für Aoniak bei eine Druck von 1 MPa und einer Teperatur von 100 C nach a) de idealen Gasgesetz b) der Van der Waals-Gleichung c) der Redlich-Kwong- Gleichung
Übungsaufgabe Bestien Sie das olare Voluen für Aoniak bei eine Druck von 1 MPa und einer Teperatur von 100 C nach a) de idealen Gasgesetz b) der Van der Waals-Gleichung c) der Redlich-Kwong- Gleichung
Aufgabe, Bedeutung und Definition der chemischen Reaktionstechnik... 1
 Kapitel 1 Aufgabe, Bedeutung und Definition der chemischen Reaktionstechnik... 1 1. Klassifizierung chemischer Reaktionen 2 2. Grundbegriffe der Reaktionstechnik 3 Kapitel 2 Stöchiometrie chemischer Reaktionen
Kapitel 1 Aufgabe, Bedeutung und Definition der chemischen Reaktionstechnik... 1 1. Klassifizierung chemischer Reaktionen 2 2. Grundbegriffe der Reaktionstechnik 3 Kapitel 2 Stöchiometrie chemischer Reaktionen
Richtung von spontanem Prozeßablauf und Veränderung der G in Abhängigkeit vom Vorzeichen der Enthalpie und der Entropie
 Richtung von spontanem Prozeßablauf und Veränderung der G in Abhängigkeit vom Vorzeichen der Enthalpie und der Entropie H S G= H-T S Prozeß 1. (-) (+) (-) immer exergonisch, erfolgt spontan bei allen Temperaturen
Richtung von spontanem Prozeßablauf und Veränderung der G in Abhängigkeit vom Vorzeichen der Enthalpie und der Entropie H S G= H-T S Prozeß 1. (-) (+) (-) immer exergonisch, erfolgt spontan bei allen Temperaturen
Polarimetrie 1. Polarimetrie
 Polarimetrie 1 Polarimetrie Bei Reaktionen mit optish aktiven Reaktanten kann die Konzentration der an der Reaktion beteiligten toffe gut polarimetrish gemessen werden, indem für das Gemish der Drehwinkel
Polarimetrie 1 Polarimetrie Bei Reaktionen mit optish aktiven Reaktanten kann die Konzentration der an der Reaktion beteiligten toffe gut polarimetrish gemessen werden, indem für das Gemish der Drehwinkel
PRAKTIKUM DER TECHNISCHEN CHEMIE I PRAKTIKUMSPROTOKOLL. WiSe 2015/2016. Versuch 4. Betriebspunkte des indirekt gekühlten CSTR
 PRAKTIKUM DER TECHNISCHEN CHEMIE I PRAKTIKUMSPROTOKOLL WiSe 2015/2016 Versuch 4 Betriebspunkte des indirekt gekühlten CSTR Rami Saoudi (356563) Guido Petri (364477) Gruppe 29 1. EINFÜHRUNG Ziel ist es,
PRAKTIKUM DER TECHNISCHEN CHEMIE I PRAKTIKUMSPROTOKOLL WiSe 2015/2016 Versuch 4 Betriebspunkte des indirekt gekühlten CSTR Rami Saoudi (356563) Guido Petri (364477) Gruppe 29 1. EINFÜHRUNG Ziel ist es,
Das Chemische Gleichgewicht
 Das Chemische Gleichgewicht Geschwindigkeit der Hinreaktion: v hin = k hin c(a 2 ) c(x 2 ) Geschwindigkeit der Rückreaktion: v rück = k rück c 2 (AX) Gleichgewicht: v hin = v rück k hin c(a 2 ) c(x 2 )
Das Chemische Gleichgewicht Geschwindigkeit der Hinreaktion: v hin = k hin c(a 2 ) c(x 2 ) Geschwindigkeit der Rückreaktion: v rück = k rück c 2 (AX) Gleichgewicht: v hin = v rück k hin c(a 2 ) c(x 2 )
NAME, Vorname Matr.-Nr. Studiengang. Prüfung am im Fach Thermodynamik II
 NAME, Vornae Matr.-Nr. Studiengang Prof. Dr.-Ing. G. Schitz Prüfung a 03. 0. 2013 i Fach Therodynaik II Fragenteil ohne Hilfsittel erreichbare Punktzahl: 20 Dauer: 20 Minuten 1. ( Punkte) Skizzieren Sie
NAME, Vornae Matr.-Nr. Studiengang Prof. Dr.-Ing. G. Schitz Prüfung a 03. 0. 2013 i Fach Therodynaik II Fragenteil ohne Hilfsittel erreichbare Punktzahl: 20 Dauer: 20 Minuten 1. ( Punkte) Skizzieren Sie
Reaktionstechnik I. Lehrbuch. Autoren:
 Reaktionstechnik I Lehrbuch Autoren: Prof. Dr. sc. techn. K. Budde, Merseburg (federführender Autor) Prof. Dr. sc. techn. K. Hertwig, Köthen Doz. Dr. sc. techn. R. Köpsel, Freiberg Dr. rer. nat. H. Rückauf,
Reaktionstechnik I Lehrbuch Autoren: Prof. Dr. sc. techn. K. Budde, Merseburg (federführender Autor) Prof. Dr. sc. techn. K. Hertwig, Köthen Doz. Dr. sc. techn. R. Köpsel, Freiberg Dr. rer. nat. H. Rückauf,
Die Innere Energie U
 Die Innere Energie U U ist die Summe aller einem System innewohnenden Energien. Es ist unmöglich, diese zu berechnen. U kann nicht absolut angegeben werden! Differenzen in U ( U) können gemessen werden.
Die Innere Energie U U ist die Summe aller einem System innewohnenden Energien. Es ist unmöglich, diese zu berechnen. U kann nicht absolut angegeben werden! Differenzen in U ( U) können gemessen werden.
Übung 2. Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen
 Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen Wärmekapazitäten isochore/isobare Zustandsänderungen Standardbildungsenthalpien Heizwert/Brennwert adiabatische Flammentemperatur WS 2013/14
Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen Wärmekapazitäten isochore/isobare Zustandsänderungen Standardbildungsenthalpien Heizwert/Brennwert adiabatische Flammentemperatur WS 2013/14
ph-wert Berechnung starke Säuren z.b. HCl, HNO 3, H 2 SO 4 vollständige Dissoziation c(h 3 O + ) = c(säure)
 ph-wert Berehnung starke Säuren z.b. HCl, HNO 3, H 2 SO 4 vollständige Dissoziation (H 3 O + ) = (Säure) ph lg H 3 O Beispiel H 2 SO 4 (H 2 SO 4 ) = 0,1 mol/l (H 3 O + ) = 0,2 mol/l ph = -lg 0,2 = -(-0,699)
ph-wert Berehnung starke Säuren z.b. HCl, HNO 3, H 2 SO 4 vollständige Dissoziation (H 3 O + ) = (Säure) ph lg H 3 O Beispiel H 2 SO 4 (H 2 SO 4 ) = 0,1 mol/l (H 3 O + ) = 0,2 mol/l ph = -lg 0,2 = -(-0,699)
1 Aufwärmen nach den Ferien
 Physikalische Chemie II Lösung 23. September 206 Aufwärmen nach den Ferien. Ermitteln Sie die folgenden Integrale. Partielle Integration mit der Anwendung der generellen Regel f g = fg fg (in diesem Fall
Physikalische Chemie II Lösung 23. September 206 Aufwärmen nach den Ferien. Ermitteln Sie die folgenden Integrale. Partielle Integration mit der Anwendung der generellen Regel f g = fg fg (in diesem Fall
Fragen zum Versuch Kinetik:
 Fragen zum Versuch Kinetik: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen von Rohrzucker im Wasser
Fragen zum Versuch Kinetik: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen von Rohrzucker im Wasser
1 EMK-Messung thermodynamischer Aktivitäten mit einer Konzentrationszelle
 EMK 1.1 1 EMK-Messung therodynaischer ktivitäten it einer Konzentrationszelle 1.1 Grundlagen Je nachde, ob in einer binären flüssigen oder festen Lösung -B die nziehungskräfte zwischen den - und B-eilchen
EMK 1.1 1 EMK-Messung therodynaischer ktivitäten it einer Konzentrationszelle 1.1 Grundlagen Je nachde, ob in einer binären flüssigen oder festen Lösung -B die nziehungskräfte zwischen den - und B-eilchen
Versuchsprotokoll. Esterverseifung
 Versuhsprotokoll Versuhsdatum:09.11.2004 Protokolldatum: Sttempell Durhgeführt von: Esterverseifung 1. Inhaltsangabe 1..Inhaltsangabe---------------------------------------------------------------------------------
Versuhsprotokoll Versuhsdatum:09.11.2004 Protokolldatum: Sttempell Durhgeführt von: Esterverseifung 1. Inhaltsangabe 1..Inhaltsangabe---------------------------------------------------------------------------------
Übung 3. Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen (Teil 2) Verständnis des thermodynamischen Gleichgewichts
 Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen (Teil 2) adiabatische Flammentemperatur Verständnis des thermodynamischen Gleichgewichts Definition von K X, K c, K p Berechnung von K
Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen (Teil 2) adiabatische Flammentemperatur Verständnis des thermodynamischen Gleichgewichts Definition von K X, K c, K p Berechnung von K
Ferienkurs Experimentalphysik 2
 Ferienkurs Experimentalphysik 2 Sommersemester 25 Gabriele Semino, Alexander Wolf, Thomas Maier sblatt 4 Elektromagnetishe Wellen und spezielle Relativitätstheorie Aufgabe : Leistung eines Herzshen Dipols
Ferienkurs Experimentalphysik 2 Sommersemester 25 Gabriele Semino, Alexander Wolf, Thomas Maier sblatt 4 Elektromagnetishe Wellen und spezielle Relativitätstheorie Aufgabe : Leistung eines Herzshen Dipols
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für hysikalische heie lbert-ludwigs-universität Freiburg Lösungen zu 7. Übungsblatt zur orlesung hysikalische heie I SS 04 rof. Dr. Bartsch 7. L Berechnen Sie aus der olaren Standardentropie des
Institut für hysikalische heie lbert-ludwigs-universität Freiburg Lösungen zu 7. Übungsblatt zur orlesung hysikalische heie I SS 04 rof. Dr. Bartsch 7. L Berechnen Sie aus der olaren Standardentropie des
Die Theorie des aktivierten Komplexes
 Die Theorie des aktiierten Komplexes Theorie kommt aus der statistishen Thermodynamik! (wird in höheren Semestern behandelt) Streke über die der aktiierten Komplex existiert A+BC AB+C A+BC A..B. C AB+C
Die Theorie des aktiierten Komplexes Theorie kommt aus der statistishen Thermodynamik! (wird in höheren Semestern behandelt) Streke über die der aktiierten Komplex existiert A+BC AB+C A+BC A..B. C AB+C
Die Reflexion von Elektronen an einem Potentialsprung nach der relativistischen Dynamik von Dirac.
 Die Reflexion von Elektronen an einem Potentialsprung nah der relativistishen Dynamik von Dira. Von 0. Klein in Kopenhagen. (Eingegangen am 24. Dezember 1928.) Es wird die Reflexion von Elektronen an einem
Die Reflexion von Elektronen an einem Potentialsprung nah der relativistishen Dynamik von Dira. Von 0. Klein in Kopenhagen. (Eingegangen am 24. Dezember 1928.) Es wird die Reflexion von Elektronen an einem
Tabellen und Formelsammlung Chemie
 Tabellen und Forelsalung Cheie Fakultät Maschinenbau Stand SS 2015 Nachfolgende Tabellen und Inforationen staen aus de Lehrbuch G. Kickelbick, Cheie für Ingenieure, Pearson-Verlag, 2008 soweit nicht anderweitig
Tabellen und Forelsalung Cheie Fakultät Maschinenbau Stand SS 2015 Nachfolgende Tabellen und Inforationen staen aus de Lehrbuch G. Kickelbick, Cheie für Ingenieure, Pearson-Verlag, 2008 soweit nicht anderweitig
Chemie Protokoll. Versuch 2 3 (RKV) Reaktionskinetik Esterverseifung. Stuttgart, Sommersemester 2012
 Chemie Protokoll Versuch 2 3 (RKV) Reaktionskinetik Esterverseifung Stuttgart, Sommersemester 202 Gruppe 0 Jan Schnabel Maximilian Möckel Henri Menke Assistent: Durmus 20. Mai 202 Inhaltsverzeichnis Theorie
Chemie Protokoll Versuch 2 3 (RKV) Reaktionskinetik Esterverseifung Stuttgart, Sommersemester 202 Gruppe 0 Jan Schnabel Maximilian Möckel Henri Menke Assistent: Durmus 20. Mai 202 Inhaltsverzeichnis Theorie
Versuch LF: Leitfähigkeit
 Versuhsdatum: 8.9.9 Versuh LF: Versuhsdatum: 8.9.9 Seite -- Versuhsdatum: 8.9.9 Einleitung bedeutet, dass ein hemisher Stoff oder ein Stoffgemish in der Lage ist, Energie oder Ionen zu transportieren und
Versuhsdatum: 8.9.9 Versuh LF: Versuhsdatum: 8.9.9 Seite -- Versuhsdatum: 8.9.9 Einleitung bedeutet, dass ein hemisher Stoff oder ein Stoffgemish in der Lage ist, Energie oder Ionen zu transportieren und
Lösungsvorschlag Übung 2
 Lösungsvorschlag Übung Aufgabe : Dichte von Gasen a) Die Dichte ρ eines Gases ist definiert als der Quotient aus Masse m und Volumen V ρ = m V..) Die Masse eines Gases erhält man aus dem Produkt seiner
Lösungsvorschlag Übung Aufgabe : Dichte von Gasen a) Die Dichte ρ eines Gases ist definiert als der Quotient aus Masse m und Volumen V ρ = m V..) Die Masse eines Gases erhält man aus dem Produkt seiner
Wieviel Gramm eines technischen Kaliumbromids mit einer Reinheit von 98,1 % müssen eingewogen werden, um 1 kg einer 8%igen KBr-Lösung herzustellen?
 Beispielaufgabe 1 Wieviel Gra eines technischen Kaliubroids it einer Reinheit von 98,1 % üssen eingeogen erden, u 1 kg einer 8%igen -Lösung herzustellen? Zuerst acht an sich klar, as da eigentlich passiert.
Beispielaufgabe 1 Wieviel Gra eines technischen Kaliubroids it einer Reinheit von 98,1 % üssen eingeogen erden, u 1 kg einer 8%igen -Lösung herzustellen? Zuerst acht an sich klar, as da eigentlich passiert.
Beziehungen zwischen Umsatz und Konzentrationen bei sich ändernder Dichte ρ der Reaktionsmasse (M) infolge chemischer Reaktion c(t)/c (t)/ (1
 7..00 Tehnishe Chemie - 87 4.0 Berehnung isothermer dealreaktoren 4.0. Eführung differentielle Stoffmengenbilanzen jeder Spezies i der Reaktionsmasse differentielle Wärmebilanz ( Kap. TC - ) differentielle
7..00 Tehnishe Chemie - 87 4.0 Berehnung isothermer dealreaktoren 4.0. Eführung differentielle Stoffmengenbilanzen jeder Spezies i der Reaktionsmasse differentielle Wärmebilanz ( Kap. TC - ) differentielle
Chemische Verfahrenstechnik
 Chemische Verfahrenstechnik Berechnung, Auslegung und Betrieb chemischer Reaktoren von Prof. Dr.-lng. habil. Klaus Hertwig und Prof. Dr.-lng. Lothar Martens Olden bourg Verlag Munchen Wien Vorwort Symbolverzeichnis
Chemische Verfahrenstechnik Berechnung, Auslegung und Betrieb chemischer Reaktoren von Prof. Dr.-lng. habil. Klaus Hertwig und Prof. Dr.-lng. Lothar Martens Olden bourg Verlag Munchen Wien Vorwort Symbolverzeichnis
Versuch MG: Molmassenbestimmung eines Gases nach der Methode von Dumas
 Dies ist ein Beispielprotokoll zu fiktiven Versuch Molassenbestiung, das Ihnen insbesondere für die physikalischcheischen Versuche (GMS, ABS, BSP, MWG, LFG) aufzeigt, wie Ihr Protokoll auszusehen hat.
Dies ist ein Beispielprotokoll zu fiktiven Versuch Molassenbestiung, das Ihnen insbesondere für die physikalischcheischen Versuche (GMS, ABS, BSP, MWG, LFG) aufzeigt, wie Ihr Protokoll auszusehen hat.
Theoretische Prozessanalyse Übungsaufgaben
 TU Dresden Institut für Verfahrenstechnik und Umwelttechnik Prof. Dr.-Ing. habil. W. Klöden Theoretische Prozessanalyse Übungsaufgaben 1. Übung Für die im folgenden Bild dargestellte Schaltung zweier Wärmeübertrager
TU Dresden Institut für Verfahrenstechnik und Umwelttechnik Prof. Dr.-Ing. habil. W. Klöden Theoretische Prozessanalyse Übungsaufgaben 1. Übung Für die im folgenden Bild dargestellte Schaltung zweier Wärmeübertrager
Begriffe und Definitionen der Chemischen Reaktionstechnik
 Begriffe und Definitionen der Chemischen Reaktionstechnik 2 In Kap. 1 wurden die übergeordneten Ziele und die Lehrinhalte der Chemischen Reaktionstechnik erläutert. Kap. 2 beruht auf der Tatsache, dass
Begriffe und Definitionen der Chemischen Reaktionstechnik 2 In Kap. 1 wurden die übergeordneten Ziele und die Lehrinhalte der Chemischen Reaktionstechnik erläutert. Kap. 2 beruht auf der Tatsache, dass
Grundlagen der Kinetik
 Kapitel 1 Grundlagen der Kinetik In diesem Kapitel werden die folgenden Themen kurz wiederholt: Die differenziellen und integralen Geschwindigkeitsgesetze von irreversiblen Reaktionen., 1., und. Ordnung
Kapitel 1 Grundlagen der Kinetik In diesem Kapitel werden die folgenden Themen kurz wiederholt: Die differenziellen und integralen Geschwindigkeitsgesetze von irreversiblen Reaktionen., 1., und. Ordnung
5.1 Gas-Flüssig-Extraktion mit der Chromatomembran-Methode 73
 5.1 Gas-Flüssig-Extraktion mit der Chromatomembran-Methode 7 5.1.2 Bestimmung von Shwefeldioxid 5.1.2.1 Einführung Shwefeldioxid ist ein farbloses, stehend riehendes Gas, das unter anderem bei Vulkanausbrühen
5.1 Gas-Flüssig-Extraktion mit der Chromatomembran-Methode 7 5.1.2 Bestimmung von Shwefeldioxid 5.1.2.1 Einführung Shwefeldioxid ist ein farbloses, stehend riehendes Gas, das unter anderem bei Vulkanausbrühen
Institut für Technische Chemie und Polymerchemie Chemisch-Technisches Grundpraktikum Prof. Dr.-Ing. H. Bockhorn
 Universität Karlsruhe Institut für Chemische Technik Prof. Dr. H. Bockhorn Versuchsbeschreibung zum Chemisch-Technischen Grundpraktikum Verweilzeitspektren 1. Literatur - J. Hagen, Chemische Reaktionstechnik,
Universität Karlsruhe Institut für Chemische Technik Prof. Dr. H. Bockhorn Versuchsbeschreibung zum Chemisch-Technischen Grundpraktikum Verweilzeitspektren 1. Literatur - J. Hagen, Chemische Reaktionstechnik,
INVERSION DES ROHRZUCKERS
 INVERSION DES ROHRZUCKERS 1. Versuhsplatz Komponenten: - Thermostat - Polarimeter - zerlegbare Küvette - Thermometer 2. Allgemeines zum Versuh Im Rahmen der Reaktionskinetik wird der zeitlihe Ablauf von
INVERSION DES ROHRZUCKERS 1. Versuhsplatz Komponenten: - Thermostat - Polarimeter - zerlegbare Küvette - Thermometer 2. Allgemeines zum Versuh Im Rahmen der Reaktionskinetik wird der zeitlihe Ablauf von
Klausur Strömungsmaschinen I WiSe 2012/2013
 Klausur Ströungsaschinen I WiSe 2012/2013 5. März 2013, Beginn 14:00 Uhr Prüfungszeit: 90 Minutenn Zugelassene Hilfsittel sind: Taschenrechner, Geodreieck, Zeichenaterial Andere Hilfsittel, insbesondere:
Klausur Ströungsaschinen I WiSe 2012/2013 5. März 2013, Beginn 14:00 Uhr Prüfungszeit: 90 Minutenn Zugelassene Hilfsittel sind: Taschenrechner, Geodreieck, Zeichenaterial Andere Hilfsittel, insbesondere:
2.2 Arbeit und Energie. Aufgaben
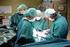 Technische Mechanik 3 2.2-1 Prof. Dr. Wandinger Aufgabe 1 Auf eine Katapult befindet sich eine Kugel der Masse, die durch eine Feder beschleunigt wird. Die Feder ist a Anfang u die Strecke s 0 zusaengedrückt.
Technische Mechanik 3 2.2-1 Prof. Dr. Wandinger Aufgabe 1 Auf eine Katapult befindet sich eine Kugel der Masse, die durch eine Feder beschleunigt wird. Die Feder ist a Anfang u die Strecke s 0 zusaengedrückt.
