Moderne Konzepte der phosphororganischen Chemie
|
|
|
- Harry Meinhardt
- vor 7 Jahren
- Abrufe
Transkript
1 Moderne Konzepte der phosphororganischen Chemie Wahlpflichtvorlesung für Studierende des Studiengangs Chemie-Diplom R. Streubel Institut für Anorganische Chemie
2 Gliederung 1. Phosphinidene 2. Phosphiniden-Komplexe 3. Phosphaalkine 4. Phosphaalkene 5. Iminophosphane 6. Phosphenium-Ionen und Phosphaallyl-Systeme 7. Phosphinine und Phosphinin-Komplexe 8. Amphipolare P-Heterocyclen 9. Radikalische und Carben-haltige P-Heterocyclen
3 Literatur zum Thema Phosphinidene 1)* U. Schmidt, Angew. Chem. 1975, 87, )* F. Mathey, Angew. Chem. 1987, 99, )* F. Mathey in Multiple Bonds and Low Coordination in Phosphorus Chemistry (Hrsg: M. Regitz, O. J. Scherer), G. Thieme, 1990, S. 33 ff. 4)* R. Streubel, Dissertation, Universität Bonn ) F. Mathey, N. H. Tran Huy, A. Marinetti, Helv. Chim. Acta 2001, 84, ) K. Lammertsma, Top. Curr. Chem. 2003, 229, 95. 7) F. Mathey, Angew. Chem. 2003, 115, Folie 1
4 1. Phosphinidene (IUPAC-Nomenklatur: Phosphandiyl) 1877, H. Köhler, A. Michaelis berichten über Phosphobenzol (Diphosphenyl) (Ber. dtsch. chem. Ges. 1877, 10, 807) Ph-PCl 2 + PhPH 2 Ph-P. P-Ph + 2 HCl? 1958, W. Kuchen, H. Buchwald, zeigen das hier (Ph-P) n vorliegt mit n > 2! (Chem. Ber. 1958, 91, 2296) 1965, J.J. Daly, L. Maier bestimmen die Festkörperstruktur des Hauptproduktes (Ph-P) 5 (Nature (London) 1965, 208, 383) 1966, E. Fluck, K. Issleib glauben 31 P-NMR-spektroskopisch Ph-P in der Schmelze von (Ph-P) 5 nachgewiesen zu haben (δ = ± 3.5 ppm) (Z. Naturforschg. 1966, 21 b, 736) 1969, H.F. Grützmacher weist Ph-P mittels Massenspektrometrie nach (Chem. Ber. 1969, 102, 3230) Folie 2
5 Theoretische Vorhersage der Bindungssituation in RP Rechnungen zu E (T-S) [kcal/mol] von R P R E [a] E [b] p x p y p x p y H H P sp H P sp Ph OH Triplettgrundzustand (T) (open-shell-system) ( 3 Σ ) niedrigster Singulettzustand (S) (closed-shell-system) ( 1 ) NH PH ([a] M.T. Nguyen et al., J. Org. Chem. 1996, 61, 7077; CISD(Q)/6-311G(d,p)) ([b] M.T. Nguyen et al., Eur. J. Inorg. Chem. 1999, 107; B3LYP/6-31G(d,p)) Neue Berechnungen weisen auf mögliche stabile Derivate mit einem Singulett- Grundzustand hin: W.W. Schoeller, Eur. J. Inorg. Chem. 2000, 369. Folie 3
6 Theoretische Vorhersage der Bindungssituation in RP Mikrowellenspektroskopische Befunde zeigen eine X-P-Bindungsverkürzung: E (kcal/mol) H-P: vs N-P: vs H P Singulett H H N P 1.637: schwach gedehnte N-P-Doppelbindung E = 33.3 Singulett Triplett E = 3.1 Triplett H Relative Energien P H H N P 1.711: schwach gedehnte N-P-Einfachbindung (M. T. Nguyen et al., J. Org. Chem. 1996, 61, 7077) Folie 4
7 Denkbare Generierungsmethoden für R-P I: Kathodische Dissoziation von PH 3 zu HP und H 2 II: Elektrochemische Reduktion von RPX - zu RP und 2X- 2 (?) III: Reduktion von RPX 2 mittels unedlen Metallen zu (RP) n (!) IVa: 1,1-Eliminierung von RP(H)X zu RP und HX (?) IVb: 1,1-Eliminierung von RP(SiMe 3 )X zu RP und Me 3 SiX (?) V: Zersetzung von (RP) n zu n RP (?) VI: Zersetzung von 5-Ring-P-Heterocyclen zu RP und 4π-Systemen VII: Zersetzung von 3-Ring-P-Heterocyclen zu RP und 2π-Systemen VIII: P=X-Spaltung unter Bildung von RP und X Folie 5
8 Erwartungen: Diradikalische Reaktivität (im Triplett-Grundzustand), z.b. Dimerisierung Gering ausgeprägte Elektrophilie für RP (Ausnahmen: RO-P und F-P) (aus Lit. 3) IIa: Elektrochemische Reduktion von RPX 2 Falls PhP hier gebildet wird, sollte man dann nicht auch PhP=PPh finden? Folie 6
9 IIa: Vorschlag zur Erklärung des Auftretens von PhPH 2 nach Lit. 3 (aus Lit. 3) Einwand: Andere Untersuchungen zeigen, dass ArPCl-Radikale dimerisieren! III: Der Mechanismus der (PhP) n -Bildung ist (noch) nicht genau bekannt! Neueste Untersuchungen zeigen einen ersten Zusammenhang zwischen R 4 P 4 -Dianionen und RP=PR-Radikalanionen! J. Geier, J. Harmer, H. J. Grützmacher, Angew. Chem. Int. Ed. 2004, 43, Folie 7
10 Zu III: Nachweis der RP=PR-Radikalanionen durch ESR a) g = , b) g = mit a) a iso [P] = 115 MHz, b) a iso [P] = 127 MHz Folie 8
11 IVa: 1,1-Eliminierung von RP(H)X zu RP und HX (?) (aus Lit. 3) Zu alternativen Folgereaktionen siehe auch IIa; im Falle sperriger Substituenten dominieren Kondensationsreaktionen unter HX-Eliminierung! IVb: 1,1-Eliminierung von RP(SiMe 3 )X zu RP und Me 3 SiX (?) 1. Darstellung von RP(SiMe 3 )X aus RP(SiMe 3 ) 2 durch SiMe 3 /Cl-Austausch: R. Appel, W. Paulen, Angew. Chem. 1981, 93, Einsatz von RP(SiMe 3 )X in der P-Heterocyclensynthese: E. Niecke, R. Streubel, M. Nieger, D. Stalke, Angew. Chem. 1989, 101, Folie 9
12 IVb: Zweistufiger Mechanismus der HMPT-induzierten Me 3 SiCl-Eliminierung (zur weiteren Diskussion s Lit. 4) Aktuelles Beispiel für eine thermisch induzierte 1,1-Eliminierung: J. Geier, J. Harmer, H. J. Grützmacher, Angew. Chem. Int. Ed. 2003, 42, Bindungswinkelsumme an P ca. 220 ( 4, Theorie) und 228 ( Komplex) Folie 10
13 V: Zersetzung von (RP) n zu n RP (?) W. Mahler, J. Am. Chem. Soc. 1964, 86, (aus Lit. 3) Erst später gelang der Nachweis des Phosphols! C. Charrier, J. Guilhem, F. Mathey, J. Org. Chem. 1981, 46, 3. Butadiene und Heterobutadiene reagieren mit (PhP) 5 zu [4+1]-Cycloaddukten Mechanistisch sind Zwischenstufen des fünffach-koordinierten Phosphors plausibel Folie 11
14 VI: Zersetzung von 5-Ring-P-Heterocyclen zu RP und 4π-Systemen K. C. Kaster, L. D. Quin, Tetrahedron Lett. 1983, 24, Hierbei treten jedoch keine freien Phosphinidene auf! VII: Zersetzung von 3-Ring-P-Heterocyclen zu RP und 2π-Systemen 1. Beispiel im Jahr 1981 E. Niecke, A. Nickloweit-Rüger, B. Krebs, M. Dartmann, Z. Naturforsch. 1981, 36B, Folie 12
15 VII: Zersetzung von 3-Ring-P-Heterocyclen zu RP und 2π-Systemen Nach E. Niecke et al. Nach dem CGMT-Modell kann vorhergesagt werden, welche Fragmentierung erfolgt, d.h. es bildet sich das Fragment mit der größten Singulett-Triplett-Differenz CGMT-Modell: M. Driess, H. J. Grützmacher, Angew. Chem. Int. Ed. 1996, 35, 828. Die Methode von Niecke et al. wurde bislang präparativ nicht genutzt! Folie 13
16 VII: Zersetzung von 3-Ring-P-Heterocyclen zu RP und 2π-Systemen 1994, P.P. Gaspar weist Mesityl-P in der Matrix bei 4 K mittels ESR nach (J. Am. Chem. Soc. 1994, 116, 7899) Die Abfangreaktionen mit Alkinen und Alkenen legen einen elektrophilen Phosphor nahe! (aus Lit. 6) Folie 14
17 VIII: P=X-Spaltung unter Bildung von RP und X; X = PR 3 (aus Lit. 6) G. Fritz, T. Vaahs, H. Fleischer, E. Matern, Angew. Chem. 1989, 101, 324. Überraschend wenig Folgechemie! 1. Verbindung dieses Typs: F 3 C-P=PMe 3 A.B. Burg, W. Mahler, J. Am. Chem. Soc. 1961, 83, (aus Lit. 6) Folie 15
18 VIII: P=X-Spaltung unter Bildung von RP und X; X = PR 3 (aus Lit. 6) Hier ist die C-C- und die C-H-Insertion besonders interessant! S. Shah, M.C. Simpson, R.C. Smith, J.D. Protasiewicz, J.Am.Chem.Soc. 2001, 123, Folie 16
Moderne Konzepte der phosphororganischen Chemie
 Moderne Konzepte der phosphororganischen Chemie Wahlpflichtvorlesung für Studierende des Studiengangs Chemie-Diplom. Streubel Institut für Anorganische Chemie http://anorganik.chemie.uni-bonn.de/akstreubel/streubel_home.html
Moderne Konzepte der phosphororganischen Chemie Wahlpflichtvorlesung für Studierende des Studiengangs Chemie-Diplom. Streubel Institut für Anorganische Chemie http://anorganik.chemie.uni-bonn.de/akstreubel/streubel_home.html
Moderne Konzepte der phosphororganischen Chemie
 Moderne Konzepte der phosphororganischen Chemie Wahlpflichtvorlesung für Studierende des Studiengangs Chemie-Diplom R. Streubel Institut für Anorganische Chemie http://anorganik.chemie.uni-bonn.de/akstreubel/streubel_home.html
Moderne Konzepte der phosphororganischen Chemie Wahlpflichtvorlesung für Studierende des Studiengangs Chemie-Diplom R. Streubel Institut für Anorganische Chemie http://anorganik.chemie.uni-bonn.de/akstreubel/streubel_home.html
Moderne Konzepte der phosphororganischen Chemie
 Moderne Konzepte der phosphororganischen Chemie Wahlpflichtvorlesung für Studierende des Studiengangs Chemie-Diplom R. Streubel Institut für Anorganische Chemie http://anorganik.chemie.uni-bonn.de/akstreubel/streubel_home.html
Moderne Konzepte der phosphororganischen Chemie Wahlpflichtvorlesung für Studierende des Studiengangs Chemie-Diplom R. Streubel Institut für Anorganische Chemie http://anorganik.chemie.uni-bonn.de/akstreubel/streubel_home.html
Moderne Konzepte der phosphororganischen Chemie
 Moderne Konzepte der phosphororganischen Chemie Wahlpflichtvorlesung für Studierende des Studiengangs Chemie-Diplom R. Streubel Institut für Anorganische Chemie http://anorganik.chemie.uni-bonn.de/akstreubel/streubel_home.html
Moderne Konzepte der phosphororganischen Chemie Wahlpflichtvorlesung für Studierende des Studiengangs Chemie-Diplom R. Streubel Institut für Anorganische Chemie http://anorganik.chemie.uni-bonn.de/akstreubel/streubel_home.html
Von Fendt Franziska und Mädl Eric. Phosphinidene
 Von Fendt Franziska und Mädl Eric Phosphinidene Synthese elektrophiler Phosphiniden-Komplexe (I) Elektrophile Phosphinidene 1.Ringspaltungsmethode: a. aus 7-Phosphanorbornadien Marinetti A, Methey F, Fischer
Von Fendt Franziska und Mädl Eric Phosphinidene Synthese elektrophiler Phosphiniden-Komplexe (I) Elektrophile Phosphinidene 1.Ringspaltungsmethode: a. aus 7-Phosphanorbornadien Marinetti A, Methey F, Fischer
Moderne Konzepte der phosphororganischen Chemie
 Moderne Konzepte der phosphororganischen Chemie Wahlpflichtvorlesung für Studierende des Studiengangs Chemie-Diplom R. Streubel Institut für Anorganische Chemie http://anorganik.chemie.uni-bonn.de/akstreubel/streubel_home.html
Moderne Konzepte der phosphororganischen Chemie Wahlpflichtvorlesung für Studierende des Studiengangs Chemie-Diplom R. Streubel Institut für Anorganische Chemie http://anorganik.chemie.uni-bonn.de/akstreubel/streubel_home.html
Organokatalyse durch N-Heterocyclische Carbene
 Organokatalyse durch N-Heterocyclische Carbene Lena Hahn und Daniel Hack 13.11.2008 Dieter Enders, Oliver Niemeier, and Alexander Henseler Chem. Rev. 2007, 107, 5606-5655 Übersicht Organokatalyse Carbene
Organokatalyse durch N-Heterocyclische Carbene Lena Hahn und Daniel Hack 13.11.2008 Dieter Enders, Oliver Niemeier, and Alexander Henseler Chem. Rev. 2007, 107, 5606-5655 Übersicht Organokatalyse Carbene
Homoaromatizität. Charlotte Over Lara Schultes
 Homoaromatizität Charlotte Over Lara Schultes 02.12.2010 Übersicht 1. Einführung 2. Aromatizität 3. Homoaromatizität 4. Beispiele 4.1 Kationische Homoaromaten 4.2 Neutrale Homoaromaten 4.3 Anionische Homoaromaten
Homoaromatizität Charlotte Over Lara Schultes 02.12.2010 Übersicht 1. Einführung 2. Aromatizität 3. Homoaromatizität 4. Beispiele 4.1 Kationische Homoaromaten 4.2 Neutrale Homoaromaten 4.3 Anionische Homoaromaten
 INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
VII INHALTSVERZEICHNIS
 VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
KW Alkene. Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1
 KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
OC07 Seminar WS15/16
 OC07 Seminar WS15/16 Chemie Frustrierter Lewis-Paare Bastian Oberhausen und Stephan Muth Betreuer: Lukas Junk D. W. Stephan und G. Erker, Angew. Chem. 2015, 127, 6498 6541. D. W. Stephan und G. Erker,
OC07 Seminar WS15/16 Chemie Frustrierter Lewis-Paare Bastian Oberhausen und Stephan Muth Betreuer: Lukas Junk D. W. Stephan und G. Erker, Angew. Chem. 2015, 127, 6498 6541. D. W. Stephan und G. Erker,
CH-Aktivierung. MCII - Seminar Christoph Sonnenschein und David Schrempp
 C-Aktivierung MCII - Seminar 17.12.09 Christoph Sonnenschein und David Schrempp 1 Inhalt 1. Einleitung 2. Aktivierung über σ-komplexe 3. Intramolekularer Verlauf 4. Murai-Reaktion 5. Intermolekularer Verlauf
C-Aktivierung MCII - Seminar 17.12.09 Christoph Sonnenschein und David Schrempp 1 Inhalt 1. Einleitung 2. Aktivierung über σ-komplexe 3. Intramolekularer Verlauf 4. Murai-Reaktion 5. Intermolekularer Verlauf
Vorlesung OC-V. Carbeniumionen
 Carbeniumionen Woher kennen wir bereits Carbeniumionen? 1. Triphenylmethanfarbstoffe Adolf von Bayer erzeugte 1902 die ersten stabilen intensiv farbigen Triarylmethylkationen Lebensdauer in Wasser > 1h
Carbeniumionen Woher kennen wir bereits Carbeniumionen? 1. Triphenylmethanfarbstoffe Adolf von Bayer erzeugte 1902 die ersten stabilen intensiv farbigen Triarylmethylkationen Lebensdauer in Wasser > 1h
Stoff der Vorlesung 3
 Stoff der Vorlesung 3 Übungen zur Oxida0on von Alkoholen und Aldehyden unter dem Gesichtspunkt formaler β- Eliminierungen: Anwendung in der Synthese der Prostaglandine Thermisch induzierte syn- β- Eliminierungen
Stoff der Vorlesung 3 Übungen zur Oxida0on von Alkoholen und Aldehyden unter dem Gesichtspunkt formaler β- Eliminierungen: Anwendung in der Synthese der Prostaglandine Thermisch induzierte syn- β- Eliminierungen
D D. D endo-cis exo-cis trans p = 1 bar: 58.4 : 38.6 : 3.0 cis- stereoselectivity: 97% p = 6.8 kbar: 72.0 : 27.0 : <1.0 cis-stereoselectivity: >99%
 4_folie100 [4 + 2] endo-cis exo-cis trans p = 1 bar: 58.4 : 38.6 : 3.0 cis- stereoselectivity: 97% + 120 p = 6.8 kbar: 72.0 : 27.0 : 99% V (endo-exo) -2.5 cm 3 /mol [2 + 2]
4_folie100 [4 + 2] endo-cis exo-cis trans p = 1 bar: 58.4 : 38.6 : 3.0 cis- stereoselectivity: 97% + 120 p = 6.8 kbar: 72.0 : 27.0 : 99% V (endo-exo) -2.5 cm 3 /mol [2 + 2]
Triquinacen Gruppe E: Miriam Liebeck, Tobias Montag, Stefan Reese, Silke Steiger
 Triquinacen Gruppe E: Miriam Liebeck, Tobias Montag, Stefan Reese, Silke Steiger Triquinacen kann systematisch als Tricyclo(5.2.10 4,10)deca-2,5,8 Trien benannt werden. Physikalische Daten: Summenformel:
Triquinacen Gruppe E: Miriam Liebeck, Tobias Montag, Stefan Reese, Silke Steiger Triquinacen kann systematisch als Tricyclo(5.2.10 4,10)deca-2,5,8 Trien benannt werden. Physikalische Daten: Summenformel:
4. Zusammenfassung 116
 4. Zusammenfassung 116 =XVDPPHQIDVVXQJ Die vorliegende Arbeit beschreibt die Synthese homoleptischer E(PH 2 ) 4 -Verbindungen (E = Si (), Ge ()). Es konnten außerdem neue Beiträge zur Chemie von Al-P-Verbindungen
4. Zusammenfassung 116 =XVDPPHQIDVVXQJ Die vorliegende Arbeit beschreibt die Synthese homoleptischer E(PH 2 ) 4 -Verbindungen (E = Si (), Ge ()). Es konnten außerdem neue Beiträge zur Chemie von Al-P-Verbindungen
Shvo s Katalysator. Von Michaela Märken und Matthias Hussong
 Shvo s Katalysator Von Michaela Märken und Inhalt Allgemeines und Struktur Entdeckung Synthese Anwendung Mechanismen analoge Systeme Y.Shvo et al. J. Am. Chem. Soc. 1986, 108,7400 Allgemeine Daten kristalliner
Shvo s Katalysator Von Michaela Märken und Inhalt Allgemeines und Struktur Entdeckung Synthese Anwendung Mechanismen analoge Systeme Y.Shvo et al. J. Am. Chem. Soc. 1986, 108,7400 Allgemeine Daten kristalliner
Vorlesung OC-V. Carbeniumionen
 Carbeniumionen Woher kennen wir bereits Carbeniumionen? 1. Triphenylmethanfarbstoffe Adolf von Bayer erzeugte 1902 die ersten stabilen intensiv farbigen Triarylmethylkationen Lebensdauer in Wasser > 1h
Carbeniumionen Woher kennen wir bereits Carbeniumionen? 1. Triphenylmethanfarbstoffe Adolf von Bayer erzeugte 1902 die ersten stabilen intensiv farbigen Triarylmethylkationen Lebensdauer in Wasser > 1h
π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!)
 . Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
. Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
E. Zusammenfassung. E. Zusammenfassung
 E. Zusammenfassung Seit den 1960er Jahren wird die Frage untersucht, ob elektronenreiche (insbesondere tetraaminosubstituierte) Alkene, an ihrer Doppelbindung dissoziieren können [99][100]. Spaltungsprodukte
E. Zusammenfassung Seit den 1960er Jahren wird die Frage untersucht, ob elektronenreiche (insbesondere tetraaminosubstituierte) Alkene, an ihrer Doppelbindung dissoziieren können [99][100]. Spaltungsprodukte
Komplexe mit einfachen Hydroxo-, Alkoxo- und Amidliganden
 Seminar Anorganische Chemie Komplexe mit einfachen ydroxo-, Alkoxo- und Amidliganden Boris Kosog 07. Dezember 2006 R. G. Bergman, Acc. Chem. Res. 2002, 35, 44-56 Komplexe mit einfachen ydroxo-, Alkoxo-
Seminar Anorganische Chemie Komplexe mit einfachen ydroxo-, Alkoxo- und Amidliganden Boris Kosog 07. Dezember 2006 R. G. Bergman, Acc. Chem. Res. 2002, 35, 44-56 Komplexe mit einfachen ydroxo-, Alkoxo-
Die Baldwin-Regeln. Ringschluss oder nicht?
 Die Baldwin-Regeln Ringschluss oder nicht? Inhalt Sir Jack E. Baldwin Die originalen Regeln Suche nach der 5-endo-trig-Reaktion Sauerstoff-Nukleophile Enolendo- & Enolexo-exo-Reaktionen Ausnahmen & Enzymkatalyse
Die Baldwin-Regeln Ringschluss oder nicht? Inhalt Sir Jack E. Baldwin Die originalen Regeln Suche nach der 5-endo-trig-Reaktion Sauerstoff-Nukleophile Enolendo- & Enolexo-exo-Reaktionen Ausnahmen & Enzymkatalyse
Strukturchemie von Iodverbindungen in den Oxidationsstufen + 1 / 7 bis +5
 Strukturchemie von Iodverbindungen in den Oxidationsstufen + 1 / 7 bis +5 Inaugural-Dissertation Zur Erlangung der Doktorwürde dem Fachbereich Biologie, Chemie und Pharmazie der Freien Universität Berlin
Strukturchemie von Iodverbindungen in den Oxidationsstufen + 1 / 7 bis +5 Inaugural-Dissertation Zur Erlangung der Doktorwürde dem Fachbereich Biologie, Chemie und Pharmazie der Freien Universität Berlin
4. Alkene und Alkine : Reaktionen und Darstellung
 Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
Vorlesung Chemie für Biologen: Klausur 1 WS Sa
 1 Vorlesung Chemie für Biologen: Klausur 1 WS 02-03 Sa 07.12.02 Name:... Ihre Unterschrift:... Vorname:... Matrikel-Nr.:... Studienbeginn: SS: WS:...... Tutor der Übungen: (Dort Klausureinsicht.) Punkteschlüssel
1 Vorlesung Chemie für Biologen: Klausur 1 WS 02-03 Sa 07.12.02 Name:... Ihre Unterschrift:... Vorname:... Matrikel-Nr.:... Studienbeginn: SS: WS:...... Tutor der Übungen: (Dort Klausureinsicht.) Punkteschlüssel
Carbenkomplexe. Vortrag von Marcel Lang und Malin Reller. Institut für Anorganische Chemie, Fakulät Chemie- und Biowissenschaften
 Carbenkomplexe Vortrag von Marcel Lang und Malin Reller Institut für Anorganische Chemie, Fakulät Chemie- und Biowissenschaften KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum
Carbenkomplexe Vortrag von Marcel Lang und Malin Reller Institut für Anorganische Chemie, Fakulät Chemie- und Biowissenschaften KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum
Vortag OC07 Moderne Synthesemethoden Jessica Hilschmann
 Vortag OC07 Moderne Synthesemethoden Jessica Hilschmann 26.10.2011 1. Definition 2. Was macht ein stabiles Radikal stabil? 3. Kohlenstoffradikale - Gomberg 3.1. Entdeckung 3.2. Stabilisierung 3.3. Verwendung
Vortag OC07 Moderne Synthesemethoden Jessica Hilschmann 26.10.2011 1. Definition 2. Was macht ein stabiles Radikal stabil? 3. Kohlenstoffradikale - Gomberg 3.1. Entdeckung 3.2. Stabilisierung 3.3. Verwendung
Prof. Dr. P. Rademacher Organische Chemie IV OCIV-SS2005-Teil7
 Prof. r. P. ademacher rganische Chemie IV CIV-SS2005-Teil7 Arine C. Grundmann, Arine, Methoden der rganischen Chemie (ouben-weyl), Bd. 5/2b, Georg Thieme Verlag, Stuttgart, 1981, S. 613-648... Wenk, M.
Prof. r. P. ademacher rganische Chemie IV CIV-SS2005-Teil7 Arine C. Grundmann, Arine, Methoden der rganischen Chemie (ouben-weyl), Bd. 5/2b, Georg Thieme Verlag, Stuttgart, 1981, S. 613-648... Wenk, M.
Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I
 Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
Olefinierungen. H. Fricke, S. Gocke
 Olefinierungen H. Fricke, S. Gocke 29.11.2004 Inhalt Wittig-Reaktion Klassische Wittig-Reaktion, Schlosser-Variante Wittig-Horner-Reaktion Horner-Wadsworth-Emmons-Reaktion (HWE) Klassische HWE, Still-Gennari-Variante
Olefinierungen H. Fricke, S. Gocke 29.11.2004 Inhalt Wittig-Reaktion Klassische Wittig-Reaktion, Schlosser-Variante Wittig-Horner-Reaktion Horner-Wadsworth-Emmons-Reaktion (HWE) Klassische HWE, Still-Gennari-Variante
4. Alkene und Alkine : Reaktionen und Darstellung
 Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
Reaktionstypen der Aliphate
 Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
4 Addition an Kohlenstoff-Mehrfachbindungen
 Übung zur Vorlesung rganische Chemie Reaktivität (Dr. St. Kirsch, Dr. A. Bauer) 4 Addition an Kohlenstoff-Mehrfachbindungen 4.1 Grundsätzliche Unterscheidung 4.1-39 Elektrophile Additionsreaktionen (A
Übung zur Vorlesung rganische Chemie Reaktivität (Dr. St. Kirsch, Dr. A. Bauer) 4 Addition an Kohlenstoff-Mehrfachbindungen 4.1 Grundsätzliche Unterscheidung 4.1-39 Elektrophile Additionsreaktionen (A
Kapitel 3. Nucleophile Substitution
 Kapitel 3. Nucleophile Substitution Reaktionsmechanismen - S N 1-Reaktion: Reaktionskoordinate-Energie-Diagramm; Kinetik, Struktur-Reaktivitätsbeziehungen (stabiles Carbokation, schwaches Nucleophil, gute
Kapitel 3. Nucleophile Substitution Reaktionsmechanismen - S N 1-Reaktion: Reaktionskoordinate-Energie-Diagramm; Kinetik, Struktur-Reaktivitätsbeziehungen (stabiles Carbokation, schwaches Nucleophil, gute
 I. II. I. II. III. IV. I. II. III. I. II. III. IV. I. II. III. IV. V. I. II. III. IV. V. VI. I. II. I. II. III. I. II. I. II. I. II. I. II. III. I. II. III. IV. V. VI. VII. VIII.
I. II. I. II. III. IV. I. II. III. I. II. III. IV. I. II. III. IV. V. I. II. III. IV. V. VI. I. II. I. II. III. I. II. I. II. I. II. I. II. III. I. II. III. IV. V. VI. VII. VIII.
Fragmentierung geradelektronischer Ionen
 Fragmentierung geradelektronischer Ionen Problem: unterschiedliche Fragmentierungswege für geradelektronische Ionen [M+H] +, [M-H] - und Radikalionen [M] + umfangreiche Kenntnisse über die Fragmentierung
Fragmentierung geradelektronischer Ionen Problem: unterschiedliche Fragmentierungswege für geradelektronische Ionen [M+H] +, [M-H] - und Radikalionen [M] + umfangreiche Kenntnisse über die Fragmentierung
D 2. Elektronische Struktur von E 2 H 4. in C 2 8 in b MO, 4 in ab MO. 12e N = 2. 10e. in B 2. N = 1 höhere Bindungsordnung durch Reduktion.
 Elektronische Struktur von E 2 H 4 D 2 h: σ π H π ^= H E π σ π σ σ in C 2 H 4 8 in b MO, 4 in ab MO in B 2 H 4 12e N = 2 10e N = 1 höhere Bindungsordnung durch Reduktion Folie 1 Elektronische Struktur
Elektronische Struktur von E 2 H 4 D 2 h: σ π H π ^= H E π σ π σ σ in C 2 H 4 8 in b MO, 4 in ab MO in B 2 H 4 12e N = 2 10e N = 1 höhere Bindungsordnung durch Reduktion Folie 1 Elektronische Struktur
Functionalization of Organic Molecules by Transition-Metal-Catalyzed C(sp 3 )-H Activation
 Functionalization of Organic Molecules by Transition-Metal-Catalyzed C(sp 3 )- Activation Rodolphe Jazzar, Julien itce, Alice Renaudat, Julien Sofack-Kreutzer, and Olivier Baudoin Chem. Eur. J. 2010, 16,
Functionalization of Organic Molecules by Transition-Metal-Catalyzed C(sp 3 )- Activation Rodolphe Jazzar, Julien itce, Alice Renaudat, Julien Sofack-Kreutzer, and Olivier Baudoin Chem. Eur. J. 2010, 16,
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Grundlagen der Organischen Chemie
 Grundlagen der Organischen Chemie Vorlesung im WS 2010/2011 1. Einführung 1 1.1 Die wunderbare Welt der Organischen Chemie 1.2 Kohlenstoff ein ganz besonderes Element 4 2. Die kovalente Bindung 5 2.1 Atomorbitale
Grundlagen der Organischen Chemie Vorlesung im WS 2010/2011 1. Einführung 1 1.1 Die wunderbare Welt der Organischen Chemie 1.2 Kohlenstoff ein ganz besonderes Element 4 2. Die kovalente Bindung 5 2.1 Atomorbitale
Aromaten und Annulene
 OC 8 Struktur, Eigenschaften und Reaktivität organischer Moleküle Aromaten und Annulene Corannulen im 1 H-NMR Synthese von Kohlenwasserstoffen Pericyclische Reaktionen Reaktivkonformation: Bullvalen Armin
OC 8 Struktur, Eigenschaften und Reaktivität organischer Moleküle Aromaten und Annulene Corannulen im 1 H-NMR Synthese von Kohlenwasserstoffen Pericyclische Reaktionen Reaktivkonformation: Bullvalen Armin
Organokatalytische Transferhydrierung. Von Mathias Ronellenfitsch und Christoph Krämer
 rganokatalytische Transferhydrierung Von Mathias Ronellenfitsch und Christoph Krämer 03.12.2009 Gliederung 1. Metallkatalysierte ydrierung von Doppelbindungen 2. Enantioselektive ydrierung in der atur
rganokatalytische Transferhydrierung Von Mathias Ronellenfitsch und Christoph Krämer 03.12.2009 Gliederung 1. Metallkatalysierte ydrierung von Doppelbindungen 2. Enantioselektive ydrierung in der atur
Exotische organische. Alexander Zech Tobias Setzer. 5. November 2009
 Exotische organische Verbindungen Alexander Zech Tobias Setzer 5. November 2009 Abb1: http://upload.wikimedia.org/wikipedia/en/1/13/catenane_crystal_structure_chemcomm_page634_1991.jpg (Stand: 04.11.2009)
Exotische organische Verbindungen Alexander Zech Tobias Setzer 5. November 2009 Abb1: http://upload.wikimedia.org/wikipedia/en/1/13/catenane_crystal_structure_chemcomm_page634_1991.jpg (Stand: 04.11.2009)
Vorschreiber: Teilnahme OC/I bzw. Modul OC/I im WiSe 2014/ / /2017
 Name: Matrikelnummer: Fachsemester Studienfach: LC Chemie-Bachelor Lehramt-Staatsex. Lehramt-Master Praktikumsteilnehmer und Nachschreiber Praktikumsteilnahme (bitte deutlich lesbar ausfüllen) SoSe 017
Name: Matrikelnummer: Fachsemester Studienfach: LC Chemie-Bachelor Lehramt-Staatsex. Lehramt-Master Praktikumsteilnehmer und Nachschreiber Praktikumsteilnahme (bitte deutlich lesbar ausfüllen) SoSe 017
Alkene / Additions-, Eliminierungsreaktionen
 2.2.2. Alkene / Additions-, Eliminierungsreaktionen 64 65 Struktur und Bindung in Ethen Ethen ist planar 2 trigonale C-Atome Bindungswinkel annähernd 120 o C ist sp2-hybridisiert Einfachbindung durch Überlapp
2.2.2. Alkene / Additions-, Eliminierungsreaktionen 64 65 Struktur und Bindung in Ethen Ethen ist planar 2 trigonale C-Atome Bindungswinkel annähernd 120 o C ist sp2-hybridisiert Einfachbindung durch Überlapp
Verzeichnis der Wortabkürzungen... Verzeichnis der Zeichen und Symbole...XVII
 VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
Übungen Kapitel 1 Alkane- Radikalische Substitution
 Übungen Kapitel 1 Alkane- Radikalische Substitution 1. Ein Gemisch aus Halogen und Alkan reagiert bei Bestrahlung mit UV- Licht oder höheren Temperaturen (Bsp. die Gase Methan und Chlor erst bei 250-400
Übungen Kapitel 1 Alkane- Radikalische Substitution 1. Ein Gemisch aus Halogen und Alkan reagiert bei Bestrahlung mit UV- Licht oder höheren Temperaturen (Bsp. die Gase Methan und Chlor erst bei 250-400
Die 18 Valenzelektronen-Regel
 Die 18 Valenzelektronen-Regel 18 VE-Regel basiert auf VB-Betrachtung lokalisierter Bindungen und besagt: Stabile ÜM-Komplexe liegen vor wenn die Summe der Metall-d-Elektronen und der Elektronen, die von
Die 18 Valenzelektronen-Regel 18 VE-Regel basiert auf VB-Betrachtung lokalisierter Bindungen und besagt: Stabile ÜM-Komplexe liegen vor wenn die Summe der Metall-d-Elektronen und der Elektronen, die von
Kapitel 5: Additionen an C-C- Mehrfachbindungen
 Kapitel 5: Additionen an C-C- hrfachbindungen» Theorie, Konzepte, chanismus - MO Theorie: elektrophile Addition (Brom/Olefin) und [2+4]- Cycloaddition (Diels-Alder-Reaktion) - Bromierung der Doppelbindung:
Kapitel 5: Additionen an C-C- hrfachbindungen» Theorie, Konzepte, chanismus - MO Theorie: elektrophile Addition (Brom/Olefin) und [2+4]- Cycloaddition (Diels-Alder-Reaktion) - Bromierung der Doppelbindung:
Inhaltsverzeichnis. 3 Organische Chemie. Vorwort Chemische Bindung Chemische Reaktionstypen Bindungen...
 VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I
 Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
Übungen zur Vorlesung Chemie der Hauptgruppenelemente. im WS 2010/11
 Übungen zur Vorlesung Chemie der Hauptgruppenelemente im WS 2010/11 Aufgabe 1 Geben Sie Reaktionsgleichungen an für die heute praktizierte technische Herstellung von H 2. Für die photolytische H 2 O-Spaltung
Übungen zur Vorlesung Chemie der Hauptgruppenelemente im WS 2010/11 Aufgabe 1 Geben Sie Reaktionsgleichungen an für die heute praktizierte technische Herstellung von H 2. Für die photolytische H 2 O-Spaltung
Aldehyde und Ketone Carbonylverbindungen
 Aldehyde und Ketone Carbonylverbindungen Prof. Dr. Ivo C. Ivanov 1 Prof. Dr. Ivo C. Ivanov 2 Die Siedepunkte liegen höher als bei den jeweils zugrundeliegenden Alkanen, eine Folge des polaren Charakters
Aldehyde und Ketone Carbonylverbindungen Prof. Dr. Ivo C. Ivanov 1 Prof. Dr. Ivo C. Ivanov 2 Die Siedepunkte liegen höher als bei den jeweils zugrundeliegenden Alkanen, eine Folge des polaren Charakters
OC07: Click -Reaktionen: Ein vielseitiges Werkzeug zur Synthese
 OC07: Click -Reaktionen: Ein vielseitiges Werkzeug zur Synthese 06.01.2016 Von Christian Rohrbacher & Marc Schneider Inhalt 1. Einleitung 1.1 Was sind Click -Reaktionen? 1.2 Anwendungsbeispiel: Peptid-Konjugate
OC07: Click -Reaktionen: Ein vielseitiges Werkzeug zur Synthese 06.01.2016 Von Christian Rohrbacher & Marc Schneider Inhalt 1. Einleitung 1.1 Was sind Click -Reaktionen? 1.2 Anwendungsbeispiel: Peptid-Konjugate
Chemie der Inamide und Inamine
 Chemie der Inamide und Inamine Ruprecht-Karls-Universität Heidelberg MCII-Seminar Referenten: Friedrich Baumgärtel und Max Joost Betreuender Assistent: R. Döpp WS 2008/2009 Übersicht 1. Einleitung 1.1.
Chemie der Inamide und Inamine Ruprecht-Karls-Universität Heidelberg MCII-Seminar Referenten: Friedrich Baumgärtel und Max Joost Betreuender Assistent: R. Döpp WS 2008/2009 Übersicht 1. Einleitung 1.1.
A6. METALLORGANISCHE CHEMIE Masterstudiengang Chemie
 A6. METALLORGANISCHE CHEMIE Masterstudiengang Chemie Kapitel 9 + 10 Metallcluster Prof. Dr. David Scheschkewitz Lehrstuhl für Allgemeine und Anorganische Chemie Universität des Saarlandes Tel. 0681/302-71641
A6. METALLORGANISCHE CHEMIE Masterstudiengang Chemie Kapitel 9 + 10 Metallcluster Prof. Dr. David Scheschkewitz Lehrstuhl für Allgemeine und Anorganische Chemie Universität des Saarlandes Tel. 0681/302-71641
Ligandbeiträge g zum VE-Zählen
 Die 18 Valenzelektronen-Regel 18 VE-Regel basiert auf VB-Betrachtung lokalisierter Bindungen und besagt: Stabile ÜM-Komplexe liegen vor, wenn die Summe der Metall-d-Elektronen und der Elektronen, die von
Die 18 Valenzelektronen-Regel 18 VE-Regel basiert auf VB-Betrachtung lokalisierter Bindungen und besagt: Stabile ÜM-Komplexe liegen vor, wenn die Summe der Metall-d-Elektronen und der Elektronen, die von
D 2. Elektronische Struktur von E 2 H 4. in C 2 8 in b MO, 4 in ab MO. 12e N = 2. 10e. in B 2. N = 1 höhere Bindungsordnung durch Reduktion.
 Elektronische Struktur von E 2 H 4 D 2 h: σ π H π ^= H E π σ π σ σ in C 2 H 4 8 in b MO, 4 in ab MO in B 2 H 4 12e N = 2 10e N = 1 höhere Bindungsordnung durch Reduktion Folie 1 Elektronische Struktur
Elektronische Struktur von E 2 H 4 D 2 h: σ π H π ^= H E π σ π σ σ in C 2 H 4 8 in b MO, 4 in ab MO in B 2 H 4 12e N = 2 10e N = 1 höhere Bindungsordnung durch Reduktion Folie 1 Elektronische Struktur
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
Fluorierungsreaktionen. Seminarvortrag am 20.11.2008 im MCII-Seminar von Reida Rutte und Joachim Moser v. Filseck
 Fluorierungsreaktionen Seminarvortrag am 20.11.2008 im MCII-Seminar von Reida Rutte und Joachim Moser v. Filseck 1 Gliederung Einleitung Reaktionen Nucleophile Fluorierung Elektrophile Fluorierung Radikalische
Fluorierungsreaktionen Seminarvortrag am 20.11.2008 im MCII-Seminar von Reida Rutte und Joachim Moser v. Filseck 1 Gliederung Einleitung Reaktionen Nucleophile Fluorierung Elektrophile Fluorierung Radikalische
2. Übungsblatt. Organische Chemie für Studierende mit Nebenfach Chemie
 Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Prof. Dr. P. Rademacher Organische Chemie IV
 Prof. Dr. P. Rademacher Organische hemie IV arbokationen 1. Nomenklatur arbokationen = alle kationischen -Verbindungen Beispiele:,, 2, 3, 4, 5. Im Massenspektrum von than bei hohem Druck findet man Peaks
Prof. Dr. P. Rademacher Organische hemie IV arbokationen 1. Nomenklatur arbokationen = alle kationischen -Verbindungen Beispiele:,, 2, 3, 4, 5. Im Massenspektrum von than bei hohem Druck findet man Peaks
Vorlesung Organische Chemie II Reaktionsmechanismen (3. Sem.)
 Vorlesung Organische Chemie II Reaktionsmechanismen (3. Sem.) Gliederung Grundlagen der physikalisch-organischen Chemie Radikalreaktionen Nukleophile und elektrophile Substitution am gesättigten C-Atom
Vorlesung Organische Chemie II Reaktionsmechanismen (3. Sem.) Gliederung Grundlagen der physikalisch-organischen Chemie Radikalreaktionen Nukleophile und elektrophile Substitution am gesättigten C-Atom
2. Übungsblatt. Organische Chemie für Studierende mit Nebenfach Chemie
 Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
2.Präparat: 1,2 Dibrom -1-phenylethan
 Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Vorlesung Anorganische Chemie I: Pentele
 Gruppentendenzen: Nichtmetall-Metall-Übergang, Stabilität von Oxidationsstufen, Sonderstellung Stickstoff: Stärke von σ- und π-bindungen bei Stickstoff bzw. Phosphor lemente: Phosphor: llotrope (Strukturen,
Gruppentendenzen: Nichtmetall-Metall-Übergang, Stabilität von Oxidationsstufen, Sonderstellung Stickstoff: Stärke von σ- und π-bindungen bei Stickstoff bzw. Phosphor lemente: Phosphor: llotrope (Strukturen,
The Nature of Hydrogen Bonds in Cytidine-H + -Cytidine DNA Base Pairs
 The ature of Hydrogen Bonds in Cytidine-H + -Cytidine DA Base Pairs A. L. Lieblein, M. Krämer, A. Dreuw, B. Fürtig, H. Schwalbe, Angew. Chem. Int. Ed. 2012, 51, 4067 4070. Seminar Moderne Anwendungen der
The ature of Hydrogen Bonds in Cytidine-H + -Cytidine DA Base Pairs A. L. Lieblein, M. Krämer, A. Dreuw, B. Fürtig, H. Schwalbe, Angew. Chem. Int. Ed. 2012, 51, 4067 4070. Seminar Moderne Anwendungen der
Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag)
 Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Graphisches Inhaltsverzeichnis
 Kapitel I Graphisches Inhaltsverzeichnis Einübung von ausgewählten Reinigungs- und Trennverfahren............ 65 R C 2 S Ph 2 R C 2 Ph 3 S R C 2 Ph R 3 R C 2 Ph R 2 R C 2 R C 2 Trennung dieser Diastereomere
Kapitel I Graphisches Inhaltsverzeichnis Einübung von ausgewählten Reinigungs- und Trennverfahren............ 65 R C 2 S Ph 2 R C 2 Ph 3 S R C 2 Ph R 3 R C 2 Ph R 2 R C 2 R C 2 Trennung dieser Diastereomere
Inorganic Chemistry at FU Berlin. Fabeckstr. 34/36, Berlin
 Inorganic Chemistry at FU Berlin Fabeckstr. 34/36, 14195 Berlin Inorganic Chemistry at FU Berlin Prof. Dr. Sebastian Hasenstab-Riedel Chemistry of the Halogens Matrix-Isolation- Spectroscopy Prof. Dr.
Inorganic Chemistry at FU Berlin Fabeckstr. 34/36, 14195 Berlin Inorganic Chemistry at FU Berlin Prof. Dr. Sebastian Hasenstab-Riedel Chemistry of the Halogens Matrix-Isolation- Spectroscopy Prof. Dr.
Vertiefte Organische Chemie der Aromaten und Heterocyclen
 Prof. Dr. J. Christoffers Institut für Organische Chemie Universität Stuttgart 01.07.2004 Vertiefte Organische Chemie der Aromaten und Heterocyclen 1. Aromaten 1.1 Aromatizität 1.1.1 Hückel-Regel 1.1.2
Prof. Dr. J. Christoffers Institut für Organische Chemie Universität Stuttgart 01.07.2004 Vertiefte Organische Chemie der Aromaten und Heterocyclen 1. Aromaten 1.1 Aromatizität 1.1.1 Hückel-Regel 1.1.2
M U S T E R L Ö S U N G
 Prof. Dr. B. König Prof. Dr.. Geyer 3. Klausur zum Praktikum rganische hemie I für Studierende der hemie und der Biochemie im SS 2001 am Donnerstag, dem 26. Juli 2001 M U S T E R L Ö S U G ame:...vorname:...
Prof. Dr. B. König Prof. Dr.. Geyer 3. Klausur zum Praktikum rganische hemie I für Studierende der hemie und der Biochemie im SS 2001 am Donnerstag, dem 26. Juli 2001 M U S T E R L Ö S U G ame:...vorname:...
M U S T E R L Ö S U N G
 Prof. Dr.. Reiser Prof. Dr. A. Geyer 3. Klausur zum Praktikum rganische hemie I für Studierende der hemie und der Biochemie im SS 2002 am Dienstag, dem 16. Juli 2002 ame:... Vorname:... Matrikelnummer:...
Prof. Dr.. Reiser Prof. Dr. A. Geyer 3. Klausur zum Praktikum rganische hemie I für Studierende der hemie und der Biochemie im SS 2002 am Dienstag, dem 16. Juli 2002 ame:... Vorname:... Matrikelnummer:...
Name: Matrikelnummer: Studienfach (bitte ankreuzen): LC Chemie-Bachelor Chemie-Diplom
 Fachrichtung Chemie Professur für rganische Chemie II rganisch-chemisches Praktikum zum Modul C II http://www.chm.tu-dresden.de/oc2/modul_c_ii.shtml ame: Matrikelnummer: Studienfach (bitte ankreuzen):
Fachrichtung Chemie Professur für rganische Chemie II rganisch-chemisches Praktikum zum Modul C II http://www.chm.tu-dresden.de/oc2/modul_c_ii.shtml ame: Matrikelnummer: Studienfach (bitte ankreuzen):
Totalsynthese von Citrafungin A
 Totalsynthese von Citrafungin A HC HC R S HC R HC H H R R Fanny Epperlein, Michael Hans, Anja Hartmann, René Jatzke, Marco Kunaschk, Christian Pätzold, Anne-Kathrin Weniger Quelle: TU Dresden, 17.12.2009
Totalsynthese von Citrafungin A HC HC R S HC R HC H H R R Fanny Epperlein, Michael Hans, Anja Hartmann, René Jatzke, Marco Kunaschk, Christian Pätzold, Anne-Kathrin Weniger Quelle: TU Dresden, 17.12.2009
Ausgewählte wichtige Reaktionen (Transformationen) für die Syntheseplanung
 Ausgewählte wichtige Reaktionen (Transformationen) für die Syntheseplanung folie267 TGT Structure Retron Transform Precursor(s) (1) C 2 t-bu C C C (E)-Enolate Aldol C + C 2 t-bu (2) C C C C C Michael +
Ausgewählte wichtige Reaktionen (Transformationen) für die Syntheseplanung folie267 TGT Structure Retron Transform Precursor(s) (1) C 2 t-bu C C C (E)-Enolate Aldol C + C 2 t-bu (2) C C C C C Michael +
Aktuelle Chemie der Nichtmetalle Moderne Stickstoffchemie
 Aktuelle Chemie der Nichtmetalle Moderne Stickstoffchemie N 2 Wintersemester 2015 Jörg Stierstorfer (jstch@cup.uni-muenchen.de) Stickstoffreiche 5-Ring Heterocyclen: Stickstoffreiche 6-Ring Heterocyclen:
Aktuelle Chemie der Nichtmetalle Moderne Stickstoffchemie N 2 Wintersemester 2015 Jörg Stierstorfer (jstch@cup.uni-muenchen.de) Stickstoffreiche 5-Ring Heterocyclen: Stickstoffreiche 6-Ring Heterocyclen:
Im Wasser sind ph-werte von ca bis 15 möglich.
 8 Superbasen 8.1 Basizität im System Wasser 2 H 2 O H 3 O + + OH pk =14 Säurestärken (pk S ): pk S HClO 4 10 saurer als H 3 O + HCl 7 H 2 SO 4 3 H 3 O + 0 H 3 PO 4 2.2 H 3.2 HCN 9.2 H 2 O 2 11.6 H 2 O
8 Superbasen 8.1 Basizität im System Wasser 2 H 2 O H 3 O + + OH pk =14 Säurestärken (pk S ): pk S HClO 4 10 saurer als H 3 O + HCl 7 H 2 SO 4 3 H 3 O + 0 H 3 PO 4 2.2 H 3.2 HCN 9.2 H 2 O 2 11.6 H 2 O
Zweite Klausur zum Organisch-Chemischen Grundpraktikum
 Prof. Dr. Jens Christoffers 12. Juni 2006 Universität ldenburg Zweite Klausur zum rganisch-chemischen Grundpraktikum Vorname: Name: Matrikelnummer: Studiengang: Falls Sie zusätzliche Seiten verwenden,
Prof. Dr. Jens Christoffers 12. Juni 2006 Universität ldenburg Zweite Klausur zum rganisch-chemischen Grundpraktikum Vorname: Name: Matrikelnummer: Studiengang: Falls Sie zusätzliche Seiten verwenden,
Inhaltsverzeichnis Phosphor- und Schwefel-Yliden
 Inhaltsverzeichnis 3.6 Enolate von Carbonylverbindungen als Nukleophile 3.6.1 Allgemeines 3.6.2 Zur Darstellung von Enolaten und verwandten Spezies 3.6.3 Zur Spaltung von β-dicarbonylverbindungen 3.6.4
Inhaltsverzeichnis 3.6 Enolate von Carbonylverbindungen als Nukleophile 3.6.1 Allgemeines 3.6.2 Zur Darstellung von Enolaten und verwandten Spezies 3.6.3 Zur Spaltung von β-dicarbonylverbindungen 3.6.4
Übung 11 (Chemie der Elemente der Gruppen 17 und 18)
 Übung 11 (Chemie der Elemente der Gruppen 17 und 18) Literatur: Housecroft Chemistry, Kap. 22.12-13 1. Prüfungsaufgabe W2013 a) Vergleichen Sie die Eigenschaften des Chlors mit folgenden Elementen. Setzen
Übung 11 (Chemie der Elemente der Gruppen 17 und 18) Literatur: Housecroft Chemistry, Kap. 22.12-13 1. Prüfungsaufgabe W2013 a) Vergleichen Sie die Eigenschaften des Chlors mit folgenden Elementen. Setzen
CHEMIE. Campher IN UNSERER ZEIT. Supporting Information zu DOI: /ciuz
 CHEMIE IN UNSERER ZEIT Supporting Information zu DOI:.0/ciuz.0130064 Campher KATRIN STEINKE ELENA JOSE HANS-ULLRICH SIEHL KLAUS-PETER ZELLER STEFAN BERGER 013 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim
CHEMIE IN UNSERER ZEIT Supporting Information zu DOI:.0/ciuz.0130064 Campher KATRIN STEINKE ELENA JOSE HANS-ULLRICH SIEHL KLAUS-PETER ZELLER STEFAN BERGER 013 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim
3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen.
 Inhalt Index 3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der Alkene Eine C=C Doppelbindung ist die funktionelle Gruppe, die
Inhalt Index 3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der Alkene Eine C=C Doppelbindung ist die funktionelle Gruppe, die
Spektroskopiemodul II. H-NMR und 13 C-NMR
 Spektroskopiemodul II 1 H-NMR und 13 C-NMR 1 1. Was gehört zu einer vollständigen Spektreninterpretation zur Strukturaufklärung? 1.1. 1 H-NMR-Spektren Man muss die chemische Verschiebung jedes einzelnen
Spektroskopiemodul II 1 H-NMR und 13 C-NMR 1 1. Was gehört zu einer vollständigen Spektreninterpretation zur Strukturaufklärung? 1.1. 1 H-NMR-Spektren Man muss die chemische Verschiebung jedes einzelnen
Übungen zur VL Chemie für Biologen und Humanbiologen
 Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Analytische Chemie. B. Sc. Chemieingenieurwesen. 11. September Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 11. September 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 11. September 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I
 Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
Deutsche Biographie Onlinefassung. 1) 1957 Mechthild Maier ( 1978), 2) 1983 Gerda Deutskens;
 Deutsche Biographie Onlinefassung NDB-Artikel Neumann, Wilhelm Paul Chemiker, * 29.10.1926 Würzburg, 1.8.1993 Dortmund. Genealogie V Wilhelm (1898 1965) aus Berlin, Dr. med. Dr. phil., o. Prof. f. Pharmakol.
Deutsche Biographie Onlinefassung NDB-Artikel Neumann, Wilhelm Paul Chemiker, * 29.10.1926 Würzburg, 1.8.1993 Dortmund. Genealogie V Wilhelm (1898 1965) aus Berlin, Dr. med. Dr. phil., o. Prof. f. Pharmakol.
Moderne Methoden in der Organischen Chemie
 oderne ethoden in der rganischen Chemie 0 Allgemeines: Wichtig für alle chemischen eaktionen: elektivität Chemoselektivität: egioselektivität: + tereoselektivät: - nantioselektivität: -Diastereosektivität:
oderne ethoden in der rganischen Chemie 0 Allgemeines: Wichtig für alle chemischen eaktionen: elektivität Chemoselektivität: egioselektivität: + tereoselektivät: - nantioselektivität: -Diastereosektivität:
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Klausur OC1 (BA-Studiengang) PIN: :00 16:00 Uhr N10. Name: Punkte: Matrikel Nr. Note:
 Klausur OC1 (BA-Studiengang) PIN: 10.02.2011 13:00 16:00 Uhr N10 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0 49-48=3.3
Klausur OC1 (BA-Studiengang) PIN: 10.02.2011 13:00 16:00 Uhr N10 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0 49-48=3.3
Zweite Klausur zur Vorlesung Grundlagen der Organischen Chemie
 Prof. Dr. Jens Christoffers 28. Februar 2011 Universität ldenburg Zweite Klausur zur Vorlesung Grundlagen der rganischen Chemie für Studierende der Chemie (Fach-Bachelor und Zwei-Fächer-Bachelor, Wert:
Prof. Dr. Jens Christoffers 28. Februar 2011 Universität ldenburg Zweite Klausur zur Vorlesung Grundlagen der rganischen Chemie für Studierende der Chemie (Fach-Bachelor und Zwei-Fächer-Bachelor, Wert:
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
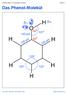 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
