Versorgungslücken in der Kinder- und Jugendmedizin schließen - Arzneimittelzulassung mit bewährten Wirkstoffen stärken
|
|
|
- Peter Dressler
- vor 7 Jahren
- Abrufe
Transkript
1 Versorgungslücken in der Kinder- und Jugendmedizin schließen - Arzneimittelzulassung mit bewährten Wirkstoffen stärken More Medicines for Minors - Arzneimittelzulassung für Kinder und Jugendliche verbessern BfArM - Bonn, Wolfgang Rascher Kinder- und Jugendklinik
2 Aufgaben der KAKJ Mitwirkung bei der Entscheidung zur Zulassung vom Arzneimitteln, die zur Anwendung bei Kindern oder Jugendlichen bestimmt sind. an der Beratung bei Arzneimitteln, die nicht für die Anwendung bei Kindern oder Jugendlichen zugelassen sind, die aber nach dem anerkannten Stand der Wissenschaft angewendet werden (off-label-problematik). an der Erstellung des Therapiebedarfsinventars in der pädiatrischen Bevölkerungsgruppe der Europäischen Gemeinschaft gemäß Artikel 42 und 43 der EU- Kinderarzneimittelverordnung
3 Arbeitswelt der KAKJ Beratung des Amtes durch die Pädiatrische Kommission sehr gut (gegenseitiges Lernen). Durch Verlagerung der Zulassung von Deutschland nach Europa (EMA) Rückgang der interessanten Aufgaben Keine Einbindung bei europäischer Zulassung, aber bei Artikel 45 Verfahren (Paediatric Worksharing Project) Kaum Fragen zur Off-label Anwendung rechtlich schwieriges Feld Selten Fragen zum Therapiebedarfsinventar (Artikel 42 und 43)
4 5 Jahre Pädiatrieausschuss der EMA (PCDO) Neue Medikamente werden für Kinder gut entwickelt. Generika in der off-label Anwendung bleiben problematisch bzw. orphan Das PUMA-Konzept ist in der aktuellen Umsetzung gescheitert Es wird immer eine off-label Anwendung geben. Bei diesen Medikamenten müssen wir eine validierte Dosis einsetzen. Die richtige Dosis ist so wichtig wie das richtige Medikament
5 1. PUMA-Zulassungen Buccolam - Buccales Midazolam zur Behandlung prolongierter Krampfanfällen bei Kindern - Kann gut von Eltern oder Personal in Kindergärten und Schulen gegeben werden Kosten Diazepam rectal 5 Tuben ca. 25 Buccolam 4 Tuben ca PUMA-Zulassungen Hemangiol - Propranolol zur Behandlung proliferierender infantiler Hämangiome (Dosisfindung) - Schon off-label Anwendung zeigt erheblichen Zusatznutzen Kosten Propranolol-Lsg 5 mg/ml 50 ml Flasche ca. 7 Hemangiol 3,75mg/ml 120 ml Flasche ca. 230
6 Dosisfindung bei Kindern Teilmengen Erwachsener (1793): 1-Jährige ein Zwölftel 2-Jährige ein Achtel 3-Jährige ein Sechstel 4-Jährige ein Viertel 4-7-Jährige ein Drittel 7-14-Jährige die Hälfte Jährige zwei Drittel Seit 220 Jahren wird so dosiert, aber Vorsicht! Hackel JC: Vollständige und practische Abhandlung von den Arzeneymitteln [.] Bd. 1 Wien : Wappler; S. 503 (zitiert nach Ritzmann I: Medikamentöse Therapie von Kindern im 18. Jahrhundert. Arzneimittel-, Therapie-Kritik & Medizin und Umwelt 2009; Hans Marseille Verlag GmbH, München
7 Zulassung vs off-label Anwendung Stationäre Versorgung (Knöppel et al. 2000) Off label 60 % Nur 12 % der Patienten Unlicenced 9 % erhielten ausschließlich Approved 31 % zugelassene Medikamente Ambulanten Versorgung (Bücheler et al, 2002) 13,2 % off-label Gebrauch AOK Verordnungsdaten 1 Quartal 1999; 3/4 aufgrund von fehlenden Daten bei Kindern oder in speziellen Altersgruppen Ambulanten Versorgung (Mühlbauer 2009) 15,7 % off-label Gebrauch (Wirkstoffe) GEK Versicherte, 726 Wirkstoffe, Packungen 7
8 Off-Label in der pädiatrischen Bevölkerungsgruppe (ambulant) In den letzten 7 Tagen erhielten von Kindern und Jugendlichen: (50,9%) Medikamente (1,62 pro Pat.), (38,8% Selbstmed.) Off-label: Kinder: 40,2%, Medikamente: 30,0% H. Knopf, I.-K. Wolf, G. Sarganas, W. Zhuang, W. Rascher, A. Neubert BMC Public Health. 2013; 13:631
9 Off label-anwendung in den Ambulanzen der Kinder- und Jugendklinik, FAU Erlangen-Nürnberg off-label Anwendung Medikamente Patienten Allgemeine Hochschulambulanz 17,0% 25,0% Daten: Wochenprävalenz Onkologische Ambulanz 28,8% 76,2% Rheumatologische Ambulanz 21,4% 28,6% Nephologische Ambulanz 38,7% 86,1% Endokrinologische Ambulanz 16,0% 22,6% Stoffwechselambulanz 52,4% 50,0% Neuropädiatrische Ambulanz 33,6% 63,3% Cystische Fibrose 30,8% 66,7% Gastroenterologische Ambulanz 28,6% 33,3% Pneumologische Ambulanz 20,7% 31,3% Kardiologische Ambulanz 38,2% 31,6% Summe Ambulanzen 28,2% 41,7% Orth H, Neubert A, Rascher W.
10 EU Therapiebedarfsinventar EU Off-patent list
11 List of paediatric needs (Therapiebedarfsinventar) Erarbeitung/Bewertung eines Therapiebedarfsinventars ( List of paediatric needs ) Paediatric Working Party (PEG) between 2001 and Therapieklassen Kontinuierlicher Prozess 11
12 Therapiebedarfsinventar (paediatric needs) 15 Klassen Therapeutic area active substances Cardiovascular 61 15,8% Chemotherapy I (Cytotoxic) 40 10,4% Anaesthesiology 38 9,9% Nephrology 35 9,1% Psychiatry 31 8,1% Gastroenterology 29 7,5% Epilepsy 25 6,5% Anti-infectious therapy 23 6,0% Rheumatology 20 5,2% Immunology 17 4,4% Chemotherapy II (Support) 16 4,2% Pain 14 3,6% Migraine 14 3,6% Obstructive lung diseases 13 3,4% Diabetes (Types I and II) 9 2,3% Total ,0%
13 Off-patent list der EMA Prioritätsliste für klinische Studien mit Medikamenten im off-label Status 1. Veröffentlichung im Jahre 2004 basierend auf dem Therapiebedarfsinventar Höchster Bedarf an off-label Medikamenten Periodisches Update durch das Paediatric Committee (PDCO) Basis für Forschungsförderung durch die European Commission 152 aktive Substanzen seit
14 Therapiebedarfsinventar & off-patent Liste Paediatric Therapeutic Needs Off-patent priority list ( ) Nur 4 Substanzen (Amiodaron, Clonidin, Cyclophosphamid, Ibuprofen) sind in der Original off-patent priority list und in jeder Revision genannt. PIPs gibt es für Clonidin und Cyclophosphamid Analyse: Neubert A. et al. 14
15 PIP and paediatric needs (Juni 2013) 45 active substances with PIP List of Paediatric Needs 45 active substances with PIP Therapeutic area active substances 5 7,6% 10 19,6% Cardiovascular 61 15,8% 7 10,6% 5 9,8% Chemotherapy I (Cytotoxic) 40 10,4% 7 10,6% 6 11,8% Anaesthesiology 38 9,9% 8 12,1% 4 7,8% Nephrology 35 9,1% 9 13,6% 3 5,9% Psychiatry 31 8,1% 1 1,5% 3 5,9% Gastroenterology 29 7,5% 0 0,0% 1 2,0% Epilepsy 25 6,5% 2 3,0% 5 9,8% Anti-infectious therapy 23 6,0% 2 3,0% 2 3,9% Rheumatology 20 5,2% 3 4,5% 2 3,9% Immunology 17 4,4% 6 9,1% 1 2,0% Chemotherapy II (Support) 16 4,2% 0 0,0% 4 7,8% Pain 14 3,6% 3 4,5% 1 2,0% Migraine 14 3,6% 4 6,1% 2 3,9% Obstructive lung diseases 13 3,4% 0 0,0% 2 3,9% Diabetes (Types I and II) 9 2,3% 3 4,5% ,0% Total ,0% 51 von 511 PIPs (9.9 %) beinhalten aktive Substanzen, die im Therapiebedarfsinventar erwähnt werden. 14.3% der genehmigten PIPs sind im Therapiebedarfsinventar enthalten (51/357) Wimmer S, Rascher W, McCarthy S, Neubert A: Pediatr Drugs 2014;16:
16 Off-Label Medikamente Paediatric Use Marketing Authorisation (PUMA) Anreiz: 10 Jahre Datenschutz 152 aktive Substanzen 17 (19) PIPs angenommen 14 Projekte im FP7 Forschungs- projekten 5 andere PIPs für off-label Medikamente Midazolam, Furosemide, rekombiniert L-Asparaginase, Paracetamol, Melatonin 2 PUMAs Active substance Cyclophosphamide Dobutamine Dopamine Fentanyl Mercaptopurine Morphine Risperidone Clonidine Gabapentin Meropenem Azithromycin Deferiprone Hydrocortisone Vancomycin FP7 project 03K Neo-CIRC THE HIP TRIAL NeoOpioid LOULLA&PHIL LA NeoOpioid PERS CloSed GAPP Neomero TINN2 DEEP TAIN Neo-Vanc
17 Dosisfindung am Beispiel von Clonidin zur Sedierung auf der pädiatrischen und neonatologischen Intensivstation BMBF-Studie , publiziert 2014 EU-Studie Ambrose C et al. Intravenous clonidine infusion in critically ill children: dose-dependent sedative effects and cardiovascular stability. Br J Anaesth. 2000; 84: background infusion of midazolam 50 mg/kg per h combined with a variable clonidine infusion (0.1-2 mg/kg per h) to maintain optimal sedation. Halbwertszeit (t 1/2) Clonidin: Neugeborene (10 Tage): Säugling (100 Tage): Kind (425 Tage): 16,9 h 11,4 h 7,4 h
18 Multicenterstudie mit Clonidin zur Sedierung von Kindern auf einer neonatologisch-pädiatrischen Intensivstationen (Ziel: Pediatric Use Marketing Authorisation (PUMA)). WP2 Scientific Coordination and Clinical Study Management Antje Neubert WP4 PK-PD Modelling and Statistics - Joe Standing Entwicklung eines PK-PD Modells für Clonidin Startdosis von intravenös verabreichtem Clonidin für die Sedierung und klinisch sinnvolle Dosierungen für die Dauerinfusion
19 Hünseler et al Clonidine Study Group: Continuous Infusion of Clonidine in Ventilated Newborns and Infants: A Randomized Controlled Trial. Pediatr Crit Care Med 2014 BMBF PaedNet Förderung (2002) Demonstrationsstudie Ventilated newborns and infants: stratum I: 1 28 d; stratum II: d; stratum III: 121 d to 2 yr Clonidine 1 μg/kg per h in ventilated newborns reduced fentanyl and midazolam demand with deeper levels of analgesia and sedation without substantial side effects. This was not demonstrated in older infants, possibly due to lower clonidine serum levels.
20 Sheng Y, Standing JF: Pharmacokinetic Reason for Negative Results of Clonidine Sedation in Long-Term-Ventilated Neonates and Infants, Pediatr Crit care 2015; 16: Simulation der Clonidinkinetik nach Hünseler et al. Schwarze Linie: mittlere Konzentration, grau 95% CI. Die gestrichelte Linie ist die mittlere Konzentration über die 72-Stunden-Studie Zeitraum.
21 PK von Clonidin Lipophil: Hohes Verteilungsvolumen. 2-Kompartmodell-Elimination 1. Ordnung Clearance: Zentrales Verteilungsvolumen: Clearance zwischen den Kompartimenten: Peripheres Verteilungsvolumen: 180 l/kg 14,6 l/h/70kg 62,5 l/kg 157 l/h/70kg 119 l/kg Modellrechnung: Zielkonzentration von Clonidin: 1 µg/l (1-6 Jahre): Loading dose 1 µg/kg Infusion: 2 µg/kg/h für 30 min, 1 µg/kg/h für 0,5 1 h, 0,5 µg/kg/h für 1 3 h, 0,3 µg/kg/h ab 4 h Potts AL1, Larsson P, Eksborg S, Warman G, Lönnqvist PA, Anderson BJ. Clonidine disposition in children; a population analysis. Paediatr Anaesth. 2007;17:924-33
22 1. Sättigungsdosis 2 µg/kg pro 15 Min., dann 1 µg/kg pro Std. Wenn Sedierung nicht ausreichend: 2. Sättigungsdosis 2 µg/kg pro 15 Min., dann 1,5 µg/kg pro Std. Wenn Sedierung nicht ausreichend: 3. Sättigungsdosis 2 µg/kg pro 15 Min., dann 2 µg/kg pro Std. Wenn Sedierung nicht ausreichend: 3. Sättigungsdosis 2 µg/kg pro 15 Min., dann 2 µg/kg pro Std. Wenn Sedierung nicht ausreichend: 4. Sättigungsdosis 2 µg/kg pro 15 Min., dann 2 µg/kg pro Std.
23 Fazit, um Versorgungslücken zu schließen: Gute Dosisfindung (PK-PD-Studien) Pädiatrische klinische Pharmakologie Öffentliche Förderung der Dosisfindungsstudien (PK-PD-Studien) Analyse der wissenschaftlichen Basis der off-label Anwendung (Literaturrecherche und Bewertung) Dosishandbuch für Deutschland Kindermedikamente fallen unter Festbetragsregelung. Soll sich das ändern?
24
25 Aktionsplan des Bundesministeriums für Gesundheit zur Verbesserung der Arzneimitteltherapiesicherheit in Deutschland 2.2 Handlungsempfehlungen für relevante Arzneimittel und Arzneimittelgruppen mit hohen Anwendungsrisiken (16) Erarbeitung von Handlungsempfehlungen für den Einsatz von Arzneimitteln bei Kindern insbesondere im stationären Bereich Termin: ab 2013 Verantwortlich: AkdÄ, APS, BOB, DKG AkdÄ in der AG Arzneimitteltherapie bei Kindern (Pädiatrie) Päd-Dos-Team der Kinder- und Jugendklinik Erlangen Pädiatrische Fachgesellschaften
26 Auswahl klinisch relevanter Wirkstoffe (PädDos-Team, AkdÄ) Abfrage gängiger Dosierinformationen (Fachgesellschaften ) Rückmeldung mit Dosierinformationen Abgleichen/ Verifizieren/ Ergänzen der Dosierinformationen Strukturierte Eingabe in die Datenbank Vorlage zur Diskussion und gemeinsamer Konsens (PädDos-Team, AkdÄ und Fachgesellschaften) Eine Orginator- Fachinformation Zwei Generika- Fachinformationen Lexicomp Pediatric & Neonatal Dosage Handbook British National Formulary for Children (BNFC) Leitlinien und Standardlehrbücher
27 Vorlage zur Diskussion und gemeinsamer Konsens (PädDos-Team, AkdÄ und Fachgesellschaften) Validierung der Daten in der Datenbank durch Reviewer (PädDos-Team, AkdÄ) Freigabe der Dosierinformation in der Datenbank (PädDos-Team, AkdÄ) Datenbank PädDos-Team, AkdÄ Dosierinformation für AV23 (23. Auflage Arzneimittelinformationen)
Besonderheiten der Arzneimitteltherapiesicherheit
 Besonderheiten der Arzneimitteltherapiesicherheit in der Pädiatrie 4. Deutscher Kongress für Patientensicherheit bei medikamentöser Therapie, Berlin 13.06.-14.06.2013 W. Rascher Kinder- und Jugendklinik
Besonderheiten der Arzneimitteltherapiesicherheit in der Pädiatrie 4. Deutscher Kongress für Patientensicherheit bei medikamentöser Therapie, Berlin 13.06.-14.06.2013 W. Rascher Kinder- und Jugendklinik
Pressegespräch der ABDA- Bundesvereinigung Deutscher Apothekerverbände
 Off-label-Anwendung bei Kindern Pressegespräch der ABDA- Bundesvereinigung Deutscher Apothekerverbände 17.06.2009, Berlin Tag der Apotheke - Von klein auf in besten Händen Prof. Dr. Dr. h.c. Wolfgang Rascher
Off-label-Anwendung bei Kindern Pressegespräch der ABDA- Bundesvereinigung Deutscher Apothekerverbände 17.06.2009, Berlin Tag der Apotheke - Von klein auf in besten Händen Prof. Dr. Dr. h.c. Wolfgang Rascher
Praktische Beispiele verbesserter AMTS auf einer neonatologischen Intensivstation
 Praktische Beispiele verbesserter AMTS auf einer neonatologischen Intensivstation Workshop zur Arzneimitteltherapiesicherheit APS - Jahrestagung in Berlin 27. April 2012 Michael Welsch Checkliste Arzneitherapiesicherheit
Praktische Beispiele verbesserter AMTS auf einer neonatologischen Intensivstation Workshop zur Arzneimitteltherapiesicherheit APS - Jahrestagung in Berlin 27. April 2012 Michael Welsch Checkliste Arzneitherapiesicherheit
Ambulante Notfalltherapie cerebraler Krampfanfälle. Siegener Pädiatrietag 2013
 Ambulante Notfalltherapie cerebraler Krampfanfälle Siegener Pädiatrietag 2013 Philipp Wolf Oberarzt Neuropädiatrie DRK-Kinderklinik Siegen Die Lebensqualität für Kinder verbessern. Das ist unser Auftrag.
Ambulante Notfalltherapie cerebraler Krampfanfälle Siegener Pädiatrietag 2013 Philipp Wolf Oberarzt Neuropädiatrie DRK-Kinderklinik Siegen Die Lebensqualität für Kinder verbessern. Das ist unser Auftrag.
AMNOG-Fachtagung des G-BA Besondere Therapiesituationen Bedingte Zulassung, Kinderarzneimittel und Orphan Drugs
 AMNOG-Fachtagung des G-BA Besondere Therapiesituationen Bedingte Zulassung, Kinderarzneimittel und Orphan Drugs Martin Völkl, Director Market Access & Public Affairs, Celgene GmbH Warum forschen Pharmaunternehmen?
AMNOG-Fachtagung des G-BA Besondere Therapiesituationen Bedingte Zulassung, Kinderarzneimittel und Orphan Drugs Martin Völkl, Director Market Access & Public Affairs, Celgene GmbH Warum forschen Pharmaunternehmen?
Label und Off-Label Use von Medikamenten bei Kindern und Jugendlichen in Österreich
 Label und Off-Label Use von Medikamenten bei Kindern und Jugendlichen in Österreich AGES Gespräch 04.10.2007 Dr. Doris Tschabitscher AGES PharmMed, National Contact Point Paediatrics Erkenntnis Kinder
Label und Off-Label Use von Medikamenten bei Kindern und Jugendlichen in Österreich AGES Gespräch 04.10.2007 Dr. Doris Tschabitscher AGES PharmMed, National Contact Point Paediatrics Erkenntnis Kinder
Problematik des off-label use von Medikamenten für Kinder - was darf ich verordnen, wo liegen die Probleme?
 Problematik des off-label use von Medikamenten für Kinder - was darf ich verordnen, wo liegen die Probleme? IQN Fortbildungsveranstaltung für niedergelassene und Krankenhausärzte Düsseldorf am 13. Mai
Problematik des off-label use von Medikamenten für Kinder - was darf ich verordnen, wo liegen die Probleme? IQN Fortbildungsveranstaltung für niedergelassene und Krankenhausärzte Düsseldorf am 13. Mai
Therapeutische Indikationen. Anwendungsfälle in europäischen Bereichen
 Therapeutische Indikationen Anwendungsfälle in europäischen Bereichen Dr. med. Hans-Peter Dauben Mannheim, 09.Sep 2010 Inhalt Therapeutische Indikationen - die medizinische und die autorisierte Indikation
Therapeutische Indikationen Anwendungsfälle in europäischen Bereichen Dr. med. Hans-Peter Dauben Mannheim, 09.Sep 2010 Inhalt Therapeutische Indikationen - die medizinische und die autorisierte Indikation
Dosierung parenteraler ß-Laktame: Welche klinischen Vorteile bieten höhere Dosen und die kontinuierliche Infusion?
 Dosierung parenteraler ß-Laktame: Welche klinischen Vorteile bieten höhere Dosen und die kontinuierliche Infusion? Katja de With Medizinische Universitätsklinik Freiburg Entwicklung antibiotikaresistenter
Dosierung parenteraler ß-Laktame: Welche klinischen Vorteile bieten höhere Dosen und die kontinuierliche Infusion? Katja de With Medizinische Universitätsklinik Freiburg Entwicklung antibiotikaresistenter
Wirksame und sichere Arzneimittelbehandlung: Gesundheit für unsere Kinder
 Wirksame und sichere Arzneimittelbehandlung: Gesundheit für unsere Kinder Prof. Dr. Fred Zepp, PAED-Net Direktor des Zentrums für Kinder- und Jugendmedizin, 16 Millionen Kinder und Jugendliche unter 18
Wirksame und sichere Arzneimittelbehandlung: Gesundheit für unsere Kinder Prof. Dr. Fred Zepp, PAED-Net Direktor des Zentrums für Kinder- und Jugendmedizin, 16 Millionen Kinder und Jugendliche unter 18
Beteiligung von Patienten an der Bewertung von Arzneimitteln bei der Zulassung und der Nutzen-Schaden- Bewertung
 Beteiligung von Patienten an der Bewertung von Arzneimitteln bei der Zulassung und der Nutzen-Schaden- Bewertung U. Hagemann Bundesinstitut für Arzneimittel und Medizinprodukte, Bonn Gesundheit e.v. 10.
Beteiligung von Patienten an der Bewertung von Arzneimitteln bei der Zulassung und der Nutzen-Schaden- Bewertung U. Hagemann Bundesinstitut für Arzneimittel und Medizinprodukte, Bonn Gesundheit e.v. 10.
Beschluss. I. Die Anlage XII wird in alphabetischer Reihenfolge um die Wirkstoffkombination Insulin degludec/liraglutid wie folgt ergänzt:
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
 Arzneimittel für Kinder Stand November 2009 Viele neue Kindermedikamente in Entwicklung In den letzten vier Jahren wurde viel zugunsten einer besser ausgestatteten Kinderapotheke bewegt. Forschende Pharma-Unternehmen
Arzneimittel für Kinder Stand November 2009 Viele neue Kindermedikamente in Entwicklung In den letzten vier Jahren wurde viel zugunsten einer besser ausgestatteten Kinderapotheke bewegt. Forschende Pharma-Unternehmen
Curriculum Entwicklungspsychopharmakologie: Arzneimittel in der Kinder- und Jugendpsychiatrie, Ulm 2017
 Curriculum Entwicklungspsychopharmakologie: Arzneimittel in der Kinder- und Jugendpsychiatrie, Ulm 2017 Welche Nebenwirkungen sollten gemeldet werden? Erläuterung und Diskussion anhand von Fallbeispielen
Curriculum Entwicklungspsychopharmakologie: Arzneimittel in der Kinder- und Jugendpsychiatrie, Ulm 2017 Welche Nebenwirkungen sollten gemeldet werden? Erläuterung und Diskussion anhand von Fallbeispielen
CHRONISCHE ERKRANKUNGEN GESUNDHEITSVERSORGUNG UND SOZIALE TEILHABE. Dr. Katja Renner, Wassenberg Apothekerverband Nordrhein
 CHRONISCHE ERKRANKUNGEN GESUNDHEITSVERSORGUNG UND SOZIALE TEILHABE Dr. Katja Renner, Wassenberg Apothekerverband Nordrhein Gesundheit bedeutet Chancengleichheit Um allen Kindern und Jugendlichen die gleichen
CHRONISCHE ERKRANKUNGEN GESUNDHEITSVERSORGUNG UND SOZIALE TEILHABE Dr. Katja Renner, Wassenberg Apothekerverband Nordrhein Gesundheit bedeutet Chancengleichheit Um allen Kindern und Jugendlichen die gleichen
Die neue Rolle von Kindern im Arzneimittelrecht und ihre praktischen Konsequenzen. Was hat mein Kind von der EU? Prof. Dr. med. Joachim Boos, Münster
 Die neue Rolle von Kindern im Arzneimittelrecht und ihre praktischen Konsequenzen Was hat mein Kind von der EU? Prof. Dr. med. Joachim Boos, Münster Bayer Werbung um 1900: Heroin, das ideale Sedativum
Die neue Rolle von Kindern im Arzneimittelrecht und ihre praktischen Konsequenzen Was hat mein Kind von der EU? Prof. Dr. med. Joachim Boos, Münster Bayer Werbung um 1900: Heroin, das ideale Sedativum
1. Zusatznutzen des Arzneimittels im Verhältnis zur zweckmäßigen Vergleichstherapie
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss. I. Die Anlage XII wird in alphabetischer Reihenfolge um die Wirkstoffkombination Dapagliflozin/Metformin wie folgt ergänzt:
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Europäische Kommission erteilt Zulassung für neue intravenöse Formulierung von Revatio (Sildenafil) d
 Europäische Kommission erteilt Zulassung für neue intravenöse Formulierung von Revatio (Sildenafil) der Firma Pfizer zur Behandlung der pulmonal-arteriellen Hypertonie (PAH) - Revatio ist die einzige PAH-Behandlung
Europäische Kommission erteilt Zulassung für neue intravenöse Formulierung von Revatio (Sildenafil) der Firma Pfizer zur Behandlung der pulmonal-arteriellen Hypertonie (PAH) - Revatio ist die einzige PAH-Behandlung
Pflanzliche Arzneimittel Tradition und Zukunft aus regulatorischer Sicht Prof. Dr. Werner Knöss
 Pflanzliche Arzneimittel Tradition und Zukunft aus regulatorischer Sicht Prof. Dr. Werner Knöss Bundesinstitut für Arzneimittel, Bonn Das BfArM ist ein Bundesinstitut im Geschäftsbereich des Bundesministeriums
Pflanzliche Arzneimittel Tradition und Zukunft aus regulatorischer Sicht Prof. Dr. Werner Knöss Bundesinstitut für Arzneimittel, Bonn Das BfArM ist ein Bundesinstitut im Geschäftsbereich des Bundesministeriums
Europäische Verfahren
 Europäische Verfahren Zur Zeit existieren 3 verschieden Zulassungsverfahren in der EU: Verfahren der gegenseitigen Anerkennung (MRP) dezentrales Verfahren (DCP) zentrales Verfahren Alle Biotech Produkte
Europäische Verfahren Zur Zeit existieren 3 verschieden Zulassungsverfahren in der EU: Verfahren der gegenseitigen Anerkennung (MRP) dezentrales Verfahren (DCP) zentrales Verfahren Alle Biotech Produkte
Neue Lungenfunktionstechniken vom Labor in die Klinik Philipp Latzin 24. Januar 2013
 Neue Lungenfunktionstechniken vom Labor in die Klinik Philipp Latzin 24. Januar 2013 PD Dr. med. Dr. phil. nat. Philipp Latzin Universitätskinderklinik Bern Abteilung für Pädiatrische Pneumologie Neue
Neue Lungenfunktionstechniken vom Labor in die Klinik Philipp Latzin 24. Januar 2013 PD Dr. med. Dr. phil. nat. Philipp Latzin Universitätskinderklinik Bern Abteilung für Pädiatrische Pneumologie Neue
Evidenztransfer bei Kindern: Konsequenzen für die frühe Nutzenbewertung
 Evidenztransfer bei Kindern: Konsequenzen für die frühe Nutzenbewertung 19. DGRA Jahreskongress Bonn, 23. Mai 2017 Thomas Müller Arzt und Apotheker, Leiter Abteilung Arzneimittel des Gemeinsamen Bundesausschusses
Evidenztransfer bei Kindern: Konsequenzen für die frühe Nutzenbewertung 19. DGRA Jahreskongress Bonn, 23. Mai 2017 Thomas Müller Arzt und Apotheker, Leiter Abteilung Arzneimittel des Gemeinsamen Bundesausschusses
1. Die Angaben zu Perampanel in der Fassung des Beschlusses vom 7. März 2013 (BAnz AT B4) werden aufgehoben.
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Erstmals Zahlen zu jährlichen Neuerkrankungen
 BEST-Studie: Neueste Daten zur Volkskrankheit Osteoporose Erstmals Zahlen zu jährlichen Neuerkrankungen - Jedes Jahr erleidet mehr als jeder zehnte Osteoporose-Patient eine Fraktur - Tendenz zu Verbesserungen
BEST-Studie: Neueste Daten zur Volkskrankheit Osteoporose Erstmals Zahlen zu jährlichen Neuerkrankungen - Jedes Jahr erleidet mehr als jeder zehnte Osteoporose-Patient eine Fraktur - Tendenz zu Verbesserungen
Macht HES Nierenversagen? Eine Analyse von VISEP
 Macht HES Nierenversagen? Eine Analyse von VISEP Christian Madl Universitätsklinik für Innere Medizin III Intensivstation 13H1 AKH Wien christian.madl@meduniwien.ac.at Financial Disclosure Information
Macht HES Nierenversagen? Eine Analyse von VISEP Christian Madl Universitätsklinik für Innere Medizin III Intensivstation 13H1 AKH Wien christian.madl@meduniwien.ac.at Financial Disclosure Information
BAnz AT B5. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Ekzemschübe bei atopischer Dermatitis vermeiden Protopic Salbe jetzt zur proaktiven Therapie zugelassen
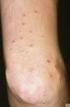 Ekzemschübe bei atopischer Dermatitis vermeiden Protopic Salbe jetzt zur proaktiven Therapie zugelassen München (1. Mai 2009) Die europäische Arzneimittelagentur EMEA hat mit Wirkung zum 1. Mai 2009 Protopic
Ekzemschübe bei atopischer Dermatitis vermeiden Protopic Salbe jetzt zur proaktiven Therapie zugelassen München (1. Mai 2009) Die europäische Arzneimittelagentur EMEA hat mit Wirkung zum 1. Mai 2009 Protopic
Kinder mit seltenen Erkrankungen in klinischen Prüfungen-was gibt es aus ärztlicher Sicht zu beachten
 Kinder mit seltenen Erkrankungen in klinischen Prüfungen-was gibt es aus ärztlicher Sicht zu beachten Dr. med. Christina Lampe Zentrum für seltene Erkrankungen Helios Horst Schmidt Kliniken, (HSK) Wiesbaden,
Kinder mit seltenen Erkrankungen in klinischen Prüfungen-was gibt es aus ärztlicher Sicht zu beachten Dr. med. Christina Lampe Zentrum für seltene Erkrankungen Helios Horst Schmidt Kliniken, (HSK) Wiesbaden,
Klassifikation. Dauer (Lothman, 1990): initialer CSE (< min) definitiver CSE (30-60 min) refraktärer CSE (> 60 min)
 Klassifikation Dauer (Lothman, 1990): initialer CSE (< 20-30 min) definitiver CSE (30-60 min) refraktärer CSE (> 60 min) Epilepsia, 54(Suppl. 7):23 34, 2013 generalisiert fokal sekundär generalisiert Klassifikation
Klassifikation Dauer (Lothman, 1990): initialer CSE (< 20-30 min) definitiver CSE (30-60 min) refraktärer CSE (> 60 min) Epilepsia, 54(Suppl. 7):23 34, 2013 generalisiert fokal sekundär generalisiert Klassifikation
Immunsuppression in der Organtransplantation. Diagnostik schnell gehört, schnell gewusst
 Immunsuppression in der Organtransplantation Diagnostik schnell gehört, schnell gewusst Einsatzgebiete und Verabreichung Immunsuppressiva (ISD) sind Medikamente, welche die Funktionen des Immunsystems
Immunsuppression in der Organtransplantation Diagnostik schnell gehört, schnell gewusst Einsatzgebiete und Verabreichung Immunsuppressiva (ISD) sind Medikamente, welche die Funktionen des Immunsystems
Bedeutung von MAO-B-Hemmern
 DGN-Kongress 2014: Rasagilin verlässlicher Therapiepartner im Krankheitsverlauf Individuelle Konzepte in der Parkinson-Therapie: Bedeutung von MAO-B-Hemmern München (17. September 2014) - Wie kann der
DGN-Kongress 2014: Rasagilin verlässlicher Therapiepartner im Krankheitsverlauf Individuelle Konzepte in der Parkinson-Therapie: Bedeutung von MAO-B-Hemmern München (17. September 2014) - Wie kann der
Projekte: Erkrankungen der Haut und des Unterhautzellgewebes
 Monitoring services for one country for a multi-country registry in chronic urticaria Preparation of a CRF for a registry in chronic urticaria Development of a Clinical Study Protocol, Master PIC and CRF
Monitoring services for one country for a multi-country registry in chronic urticaria Preparation of a CRF for a registry in chronic urticaria Development of a Clinical Study Protocol, Master PIC and CRF
Bundesgremienbesetzungsgesetz BGremBG- Aufsichts-Gremien Ressort: Bundesministerium für Gesundheit
 Bundesgremienbesetzungsgesetz BGremBG- Aufsichts-Gremien Ressort: Bundesministerium für Gesundheit Stand: 30.06.205 Aufsichts-Gremien Name Aufsichtsgremium Ministerium Verwaltungsrat des Europäischen Zentrums
Bundesgremienbesetzungsgesetz BGremBG- Aufsichts-Gremien Ressort: Bundesministerium für Gesundheit Stand: 30.06.205 Aufsichts-Gremien Name Aufsichtsgremium Ministerium Verwaltungsrat des Europäischen Zentrums
Schwerpunkte zur Verbesserung der Arzneimittelsicherheit im Versorgungsprozess
 Schwerpunkte zur Verbesserung der Arzneimittelsicherheit im Versorgungsprozess Ministerialrat a. D. Dr. Horst Möller, ehem. Leiter des Referates Arzneimittelsicherheit des BMG, Außerordentliches Mitglied
Schwerpunkte zur Verbesserung der Arzneimittelsicherheit im Versorgungsprozess Ministerialrat a. D. Dr. Horst Möller, ehem. Leiter des Referates Arzneimittelsicherheit des BMG, Außerordentliches Mitglied
Kinderarzneimittel im deutschen Gesundheitssystem
 Kinderarzneimittel im deutschen Gesundheitssystem Die Initiative Arzneimittel für Kinder ist ein gemeinnütziger Verein, der von Mitgliedern aus der Arzneimittelindustrie, der Apothekerschaft und der Forschung
Kinderarzneimittel im deutschen Gesundheitssystem Die Initiative Arzneimittel für Kinder ist ein gemeinnütziger Verein, der von Mitgliedern aus der Arzneimittelindustrie, der Apothekerschaft und der Forschung
Umsetzung der Handlungsempfehlung Arzneimitteltherapiesicherheit im Krankenhaus Welchen Beitrag leistet closed-loop medication?
 Umsetzung der Handlungsempfehlung Arzneimitteltherapiesicherheit im Krankenhaus Welchen Beitrag leistet closed-loop medication? Dr. Juliane Eidenschink, Apothekerin Was ist Arzneimitteltherapiesicherheit?
Umsetzung der Handlungsempfehlung Arzneimitteltherapiesicherheit im Krankenhaus Welchen Beitrag leistet closed-loop medication? Dr. Juliane Eidenschink, Apothekerin Was ist Arzneimitteltherapiesicherheit?
Pharmakogenomik und companion diagnostics aus Sicht der Regulierungsbehörde. Prof. Dr. Julia Stingl, Forschungsdirektorin BfArM, Bonn
 Pharmakogenomik und companion diagnostics aus Sicht der Regulierungsbehörde Prof. Dr. Julia Stingl, Forschungsdirektorin BfArM, Bonn Aufgaben des BfArM Zulassung von Fertigarzneimitteln Pharmakovigilanz
Pharmakogenomik und companion diagnostics aus Sicht der Regulierungsbehörde Prof. Dr. Julia Stingl, Forschungsdirektorin BfArM, Bonn Aufgaben des BfArM Zulassung von Fertigarzneimitteln Pharmakovigilanz
Arzneimittel als Proxy für eine Diagnose: Methodisch sinnvoll? - Das Beispiel Asthma
 Arzneimittel als Proxy für eine Diagnose: Methodisch sinnvoll? - Das Beispiel Asthma AGENS-Methodenworkshop am 12. und 13. März 2009 im Universitätsklinikum Magdeburg Dr. Falk Hoffmann, MPH Hintergrund
Arzneimittel als Proxy für eine Diagnose: Methodisch sinnvoll? - Das Beispiel Asthma AGENS-Methodenworkshop am 12. und 13. März 2009 im Universitätsklinikum Magdeburg Dr. Falk Hoffmann, MPH Hintergrund
Neues in der Diagnose der Tuberkulose
 Neues in der Diagnose der Tuberkulose Klinische Diagnose Dr. med. Alexander Turk Zürcher Höhenklinik Wald alexander.turk@zhw.ch Tuberkulose in Homo erectus vor 500 000 Jahren? AMERICAN JOURNAL OF PHYSICAL
Neues in der Diagnose der Tuberkulose Klinische Diagnose Dr. med. Alexander Turk Zürcher Höhenklinik Wald alexander.turk@zhw.ch Tuberkulose in Homo erectus vor 500 000 Jahren? AMERICAN JOURNAL OF PHYSICAL
PK/PD Anforderungen für die Zulassung neuer Substanzen
 PK/PD Anforderungen für die Zulassung neuer Substanzen PD Dr. Norbert Schnitzler, Bundesinstitut für Arzneimittel und Medizinprodukte, Bonn Inhalt Kurze Erläuterung der Rahmenbedingungen Bedeutung der
PK/PD Anforderungen für die Zulassung neuer Substanzen PD Dr. Norbert Schnitzler, Bundesinstitut für Arzneimittel und Medizinprodukte, Bonn Inhalt Kurze Erläuterung der Rahmenbedingungen Bedeutung der
Eine neue Zukunft in der Epilepsie-Behandlung Wirksamkeit und Sicherheit. Von Anfang an mit KetoCal!
 Eine neue Zukunft in der Epilepsie-Behandlung Wirksamkeit und Sicherheit Von Anfang an mit KetoCal! Fol_effektivitaet_12-08.indd 1 17.12.2008 15:55:30 Uhr Ketogene Therapie bietet eine sichere Alternative
Eine neue Zukunft in der Epilepsie-Behandlung Wirksamkeit und Sicherheit Von Anfang an mit KetoCal! Fol_effektivitaet_12-08.indd 1 17.12.2008 15:55:30 Uhr Ketogene Therapie bietet eine sichere Alternative
10 Superlativ Begriffe Google s news search. Artikel N=94
 Status quo und zukünftige Anforderungen an wissenschaftliche Erkenntnisse zu Wirksamkeit und Sicherheit bei der Zulassung onkologischer Wirkstoffe im Zeitalter der Präzisionsmedizin Wolf-Dieter Ludwig
Status quo und zukünftige Anforderungen an wissenschaftliche Erkenntnisse zu Wirksamkeit und Sicherheit bei der Zulassung onkologischer Wirkstoffe im Zeitalter der Präzisionsmedizin Wolf-Dieter Ludwig
Umgang mit Medikationsfehlern - Ein Bericht der AG AMTS des BfArM - Dr. rer. nat. Claudia Kayser BfArM
 Umgang mit Medikationsfehlern - Ein Bericht der AG AMTS des BfArM - Dr. rer. nat. Claudia Kayser BfArM Zielsetzung Klare, eindeutige und allgemein verständliche Durch regulatorische Maßnahmen Medikationsfehler
Umgang mit Medikationsfehlern - Ein Bericht der AG AMTS des BfArM - Dr. rer. nat. Claudia Kayser BfArM Zielsetzung Klare, eindeutige und allgemein verständliche Durch regulatorische Maßnahmen Medikationsfehler
BAnz AT B2. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Nutzenbewertung und unabhängige Arzneimittelinformationen
 Gemeinsame Fortbildungs- und Informationsveranstaltung der AkdÄ und der AMK Berlin, 11. Juli 2015 Nutzenbewertung und unabhängige Arzneimittelinformationen Dr. med. Katrin Bräutigam Geschäftsführerin der
Gemeinsame Fortbildungs- und Informationsveranstaltung der AkdÄ und der AMK Berlin, 11. Juli 2015 Nutzenbewertung und unabhängige Arzneimittelinformationen Dr. med. Katrin Bräutigam Geschäftsführerin der
Integrative Medizin in der Onkologie
 Integrative Medizin in der Onkologie Integrative Medizin in der Onkologie Dr med Marc Schlaeppi MSc Zentrumsleiter Zentrum für Integrative Medizin Kantonsspital St. Gallen 1 Integrative Medizin in der
Integrative Medizin in der Onkologie Integrative Medizin in der Onkologie Dr med Marc Schlaeppi MSc Zentrumsleiter Zentrum für Integrative Medizin Kantonsspital St. Gallen 1 Integrative Medizin in der
Arzneimitteltherapiesicherheit in der Kindermedizin
 Arzneimitteltherapiesicherheit in der Kindermedizin 4. ATMS-Expertenworkshop in Erlangen 9./10.11.2012 W. Rascher, A. Neubert Kinder- und Jugendklinik Medikamentöse Therapie als Hochrisikoprozess Besonderheiten
Arzneimitteltherapiesicherheit in der Kindermedizin 4. ATMS-Expertenworkshop in Erlangen 9./10.11.2012 W. Rascher, A. Neubert Kinder- und Jugendklinik Medikamentöse Therapie als Hochrisikoprozess Besonderheiten
POSITIONSPAPIER. Verbesserung der medizinischen Versorgung für Kinder und Jugendliche Problem: Sicherheit der Arzneimitteltherapien
 Verbesserung der medizinischen Versorgung für Kinder und Jugendliche Verbesserung der medizinischen Versorgung für Kinder und Jugendliche POSITIONSPAPIER Verbesserung der medizinischen Versorgung für Kinder
Verbesserung der medizinischen Versorgung für Kinder und Jugendliche Verbesserung der medizinischen Versorgung für Kinder und Jugendliche POSITIONSPAPIER Verbesserung der medizinischen Versorgung für Kinder
Doxylamin zur Behandlung von Schlafstörungen bei Kindern
 Doxylamin zur Behandlung von Schlafstörungen bei Kindern Sachverständigen-Ausschuss für Verschreibungspflicht 27. Juni 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Juni 2017 Seite 1 BfArM
Doxylamin zur Behandlung von Schlafstörungen bei Kindern Sachverständigen-Ausschuss für Verschreibungspflicht 27. Juni 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Juni 2017 Seite 1 BfArM
BAnz AT B3. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Nutzen-Bewertung und Zweitmeinung Neue Instrumente für f r eine wirtschaftliche und sichere Arzneimitteltherapie
 Kosten-Nutzen Nutzen-Bewertung und Zweitmeinung Neue Instrumente für f r eine wirtschaftliche und sichere Arzneimitteltherapie 24. Oktober 2007 Presseseminar des Gemeinsamen Bundesausschuss Thomas Müller
Kosten-Nutzen Nutzen-Bewertung und Zweitmeinung Neue Instrumente für f r eine wirtschaftliche und sichere Arzneimitteltherapie 24. Oktober 2007 Presseseminar des Gemeinsamen Bundesausschuss Thomas Müller
Beschluss. I. Die Anlage XII wird in alphabetischer Reihenfolge um die Wirkstoffkombination Netupitant/Palonosetron wie folgt ergänzt:
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Heroin Pharmakologie Struktur von Heroin 1
 Heroin Pharmakologie Struktur von Heroin 1 Heroin = 3,6-Diacetylmorphin = Diamorphin = DAM Acetylgruppe 3 Synthetische Herstellung aus Morphin Diacetyliert mit Essigsäurechlorid N Morphin 6 Acetylgruppe
Heroin Pharmakologie Struktur von Heroin 1 Heroin = 3,6-Diacetylmorphin = Diamorphin = DAM Acetylgruppe 3 Synthetische Herstellung aus Morphin Diacetyliert mit Essigsäurechlorid N Morphin 6 Acetylgruppe
BAnz AT B4. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Tragende Gründe. Therapiehinweis zu Sitagliptin. vom 18. Oktober 2007. Inhaltsverzeichnis. 1. Rechtsgrundlagen 2. 2. Eckpunkte der Entscheidung 2
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses zur Einleitung eines Stellungnahmeverfahrens zur Änderung der Arzneimittel-Richtlinie in Anlage 4: Therapiehinweis zu Sitagliptin vom 18.
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses zur Einleitung eines Stellungnahmeverfahrens zur Änderung der Arzneimittel-Richtlinie in Anlage 4: Therapiehinweis zu Sitagliptin vom 18.
Arzneimittelforschung mit Kindern: Ethische Herausforderungen
 Georg Marckmann Institut für Ethik, Geschichte und Theorie der Medizin Arzneimittelforschung mit Kindern: Ethische Herausforderungen Forum Bioethik des Deutschen Ethikrats Arzneimittelforschung mit Kindern:
Georg Marckmann Institut für Ethik, Geschichte und Theorie der Medizin Arzneimittelforschung mit Kindern: Ethische Herausforderungen Forum Bioethik des Deutschen Ethikrats Arzneimittelforschung mit Kindern:
Stufenschema der Schmerztherapie für alle Schmerzen?
 Stufenschema der Schmerztherapie für alle Schmerzen? M. Zenz Ruhr-Universität Bochum 200102-003-1 200102-003-2 Prävalenz chronischer Schmerzen Breivik et al 2006 200102-003-3 Deutschland 2003 5-8 Millionen
Stufenschema der Schmerztherapie für alle Schmerzen? M. Zenz Ruhr-Universität Bochum 200102-003-1 200102-003-2 Prävalenz chronischer Schmerzen Breivik et al 2006 200102-003-3 Deutschland 2003 5-8 Millionen
Schmerzdurchbruch: Schnelles Handeln ist gefragt
 Schmerzdurchbruch: Schnelles Handeln ist gefragt Wie schnell? Wer soll handeln? Was ist gefragt? 21.11.2015 Wolfgang M. Stangl 1 OA.Dr.Wolfgang Stangl Tumorboard KRAGES Vernetzung Mobiles Palliativteam
Schmerzdurchbruch: Schnelles Handeln ist gefragt Wie schnell? Wer soll handeln? Was ist gefragt? 21.11.2015 Wolfgang M. Stangl 1 OA.Dr.Wolfgang Stangl Tumorboard KRAGES Vernetzung Mobiles Palliativteam
Periphere neuropathische Schmerzen: Topische Therapie mit QutenzaTM gewinnt weiter an Bedeutung
 Periphere neuropathische Schmerzen Topische Therapie mit Qutenza TM gewinnt weiter an Bedeutung Mannheim (16. Oktober 2015) - Auf einer Pressekonferenz im Rahmen des deutschen Schmerzkongresses referierten
Periphere neuropathische Schmerzen Topische Therapie mit Qutenza TM gewinnt weiter an Bedeutung Mannheim (16. Oktober 2015) - Auf einer Pressekonferenz im Rahmen des deutschen Schmerzkongresses referierten
Translationale Zentren Ein Weg für Innovationen? Brennpunkt Onkologie. Berlin, Bernhard Egger GKV-Spitzenverband
 Translationale Zentren Ein Weg für Innovationen? Brennpunkt Onkologie Berlin, 30.11.2016 Bernhard Egger GKV-Spitzenverband 2 Abs. (1) Satz 3 SGB V Qualität und Wirksamkeit der Leistungen haben dem anerkannten
Translationale Zentren Ein Weg für Innovationen? Brennpunkt Onkologie Berlin, 30.11.2016 Bernhard Egger GKV-Spitzenverband 2 Abs. (1) Satz 3 SGB V Qualität und Wirksamkeit der Leistungen haben dem anerkannten
More Medicines for Minors
 More Medicines for Minors Arzneimittelzulassung für Kinder und Jugendliche verbessern Birka Lehmann More Medicines for Minors! Kinder sind keine kleinen Erwachsenen! Ziel der Verodnung (EG) Nr 1901/2006
More Medicines for Minors Arzneimittelzulassung für Kinder und Jugendliche verbessern Birka Lehmann More Medicines for Minors! Kinder sind keine kleinen Erwachsenen! Ziel der Verodnung (EG) Nr 1901/2006
Was ist eine klinische Studie? Was bringt sie Patienten und Wissenschaftlern? Tobias Welte Klinik für Pneumologie und Infektionsmedizin
 Was ist eine klinische Studie? Was bringt sie Patienten und Wissenschaftlern? Tobias Welte Klinik für Pneumologie und Infektionsmedizin Was gibt es überhaupt für klinische Studien? Medikamenten und Device
Was ist eine klinische Studie? Was bringt sie Patienten und Wissenschaftlern? Tobias Welte Klinik für Pneumologie und Infektionsmedizin Was gibt es überhaupt für klinische Studien? Medikamenten und Device
Übung 6 im Fach "Biometrie / Q1"
 Universität Ulm, Institut für Epidemiologie und Medizinische Biometrie, D-89070 Ulm Institut für Epidemiologie und Medizinische Biometrie Leiter: Prof. Dr. D. Rothenbacher Schwabstr. 13, 89075 Ulm Tel.
Universität Ulm, Institut für Epidemiologie und Medizinische Biometrie, D-89070 Ulm Institut für Epidemiologie und Medizinische Biometrie Leiter: Prof. Dr. D. Rothenbacher Schwabstr. 13, 89075 Ulm Tel.
Medikamentenverordnung Daten und Fakten
 Fachtagung BKK Bundesverband, Deutsche Hauptstelle gegen Suchtgefahren, Kassenärztliche Bundesvereinigung Medikamentenabhängigkeit: ngigkeit: Gemeinsam handeln Berlin, 23. April 2007 Medikamentenverordnung
Fachtagung BKK Bundesverband, Deutsche Hauptstelle gegen Suchtgefahren, Kassenärztliche Bundesvereinigung Medikamentenabhängigkeit: ngigkeit: Gemeinsam handeln Berlin, 23. April 2007 Medikamentenverordnung
Nutzenbewertung durch G-BA nach 35a SGB V
 Nutzenbewertung durch G-BA nach 35a SGB V 15. DGRA Jahreskongress 20. Juni 2013 in Bonn Dr. Antje Behring Referentin, Abteilung Arzneimittel des Gemeinsamen Bundesausschusses Vor Markteintritt - Möglichkeit
Nutzenbewertung durch G-BA nach 35a SGB V 15. DGRA Jahreskongress 20. Juni 2013 in Bonn Dr. Antje Behring Referentin, Abteilung Arzneimittel des Gemeinsamen Bundesausschusses Vor Markteintritt - Möglichkeit
Objektive Forschung der Pharmaindustrie ist nicht möglich
 a-t im Internet: http://www.arznei-telegramm.de Objektive Forschung der Pharmaindustrie ist nicht möglich Wolfgang BECKER-BRÜSER IQWiG Interessenkonflikt keiner Überblick Strategien der Beeinflussung Folgen
a-t im Internet: http://www.arznei-telegramm.de Objektive Forschung der Pharmaindustrie ist nicht möglich Wolfgang BECKER-BRÜSER IQWiG Interessenkonflikt keiner Überblick Strategien der Beeinflussung Folgen
Preise für innovative Arzneimittel Kommt das System an seine Grenzen?
 AOK-Forum live Potsdam, 28. April 2015 Preise für innovative Arzneimittel Kommt das System an seine Grenzen? Wolf-Dieter Ludwig Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ); HELIOS Klinikum
AOK-Forum live Potsdam, 28. April 2015 Preise für innovative Arzneimittel Kommt das System an seine Grenzen? Wolf-Dieter Ludwig Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ); HELIOS Klinikum
Mukoviszidose-Register, Software Muko.dok. aus Recherche und Antworten befragter Projektträger
 Quellen Informationsgrundlage für diesen Datensatz Name der Qualitätsinitiative Alias Literatur aus Recherche und Antworten befragter Projektträger Mukoviszidose-Register, Software Muko.dok CF-Register,
Quellen Informationsgrundlage für diesen Datensatz Name der Qualitätsinitiative Alias Literatur aus Recherche und Antworten befragter Projektträger Mukoviszidose-Register, Software Muko.dok CF-Register,
Sektorenübergreifendes. Arzneimitteltherapie-Management
 Sektorenübergreifendes Arzneimitteltherapie-Management Aktionsbündnis Patientensicherheit, 12. APS Jahrestagung am 4.5. 5.5.2017 in Berlin Petra Kellermann-Mühlhoff 15.05.2017 Seite 1 ebi und AdAM Versorgungssituation
Sektorenübergreifendes Arzneimitteltherapie-Management Aktionsbündnis Patientensicherheit, 12. APS Jahrestagung am 4.5. 5.5.2017 in Berlin Petra Kellermann-Mühlhoff 15.05.2017 Seite 1 ebi und AdAM Versorgungssituation
Symposium Anforderungen an neue Rezepturbestandteile für Dermatika und Kosmetika
 Symposium Anforderungen an neue Rezepturbestandteile für Dermatika und Kosmetika - Unterlagenschutz bei topisch angewendeten Produkten und Hilfsstoffen Markus Ambrosius ANWALTSKANZLEI STRÄTER Kronprinzenstraße
Symposium Anforderungen an neue Rezepturbestandteile für Dermatika und Kosmetika - Unterlagenschutz bei topisch angewendeten Produkten und Hilfsstoffen Markus Ambrosius ANWALTSKANZLEI STRÄTER Kronprinzenstraße
Orphan Drugs. Arzneimitteltherapie seltener Krankheiten
 Orphan Drugs Arzneimitteltherapie seltener Krankheiten Seltene Krankheiten 30 Millionen Europäer, davon etwa 4 Millionen Deutsche, leiden an seltenen Krankheiten. Als selten gilt hier eine Krankheit, wenn
Orphan Drugs Arzneimitteltherapie seltener Krankheiten Seltene Krankheiten 30 Millionen Europäer, davon etwa 4 Millionen Deutsche, leiden an seltenen Krankheiten. Als selten gilt hier eine Krankheit, wenn
Therapeutisches Drug Monitoring bei Antiepileptika
 Therapeutisches Drug Monitoring bei Antiepileptika Prof. Dr. med. Gerd Mikus Abteilung Innere Medizin VI Klinische Pharmakologie und Pharmakoepidemiologie Universitätsklinikum Heidelberg gerd.mikus@med.uni-heidelberg.de
Therapeutisches Drug Monitoring bei Antiepileptika Prof. Dr. med. Gerd Mikus Abteilung Innere Medizin VI Klinische Pharmakologie und Pharmakoepidemiologie Universitätsklinikum Heidelberg gerd.mikus@med.uni-heidelberg.de
ONKOLOGIE C. Düsseldorf
 MDS MDK GKV ONKOLOGIE C Düsseldorf Wiesbaden 09. April 2013 Relevanz klinischer Studien für die Versorgung onkologischer Patienten Sicht des MDK Prof. Dr. med. Axel Heyll Kompetenz Centrum Onkologie der
MDS MDK GKV ONKOLOGIE C Düsseldorf Wiesbaden 09. April 2013 Relevanz klinischer Studien für die Versorgung onkologischer Patienten Sicht des MDK Prof. Dr. med. Axel Heyll Kompetenz Centrum Onkologie der
BAnz AT B7. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Projekte: Gutartige, boesartige und unspezifische Neubildungen (einschl. Zysten und Polypen)
 Erstellung einer Stellungnahme für den G-BA zur Nutzenbewertung eines VEGF-Rezeptor Hemmers Andere Erstellung einer Stellungnahme für den G-BA zur Nutzenbewertung Erstellung eines Dossiers für eine Nutzenbewertung
Erstellung einer Stellungnahme für den G-BA zur Nutzenbewertung eines VEGF-Rezeptor Hemmers Andere Erstellung einer Stellungnahme für den G-BA zur Nutzenbewertung Erstellung eines Dossiers für eine Nutzenbewertung
Gelius Heidelberg 12/2014
 Europäische Bewegungsstrategie Entwurf des WHO Regionalbüros für Europa Dr. Peter Gelius Institut für Sportwissenschaft und Sport WHO-Kooperationszentrum für Bewegung und Gesundheit Friedrich-Alexander-Universität
Europäische Bewegungsstrategie Entwurf des WHO Regionalbüros für Europa Dr. Peter Gelius Institut für Sportwissenschaft und Sport WHO-Kooperationszentrum für Bewegung und Gesundheit Friedrich-Alexander-Universität
Disease-Management-Programme (DMP)
 Management im Gesundheitswesen Krankenversicherung und Leistungsanbieter Disease-Management-Programme (DMP) Reinhard Busse, Prof. Dr. med. MPH FFPH FG Management im Gesundheitswesen, Technische Universität
Management im Gesundheitswesen Krankenversicherung und Leistungsanbieter Disease-Management-Programme (DMP) Reinhard Busse, Prof. Dr. med. MPH FFPH FG Management im Gesundheitswesen, Technische Universität
Stammzellforschung in Deutschland unter dem Blickwinkel europäischer Förderung
 Bürgerbefragung zur Stammzellforschung Berlin, 13. März 2004 Technische Universität Berlin Stammzellforschung in Deutschland unter dem Blickwinkel europäischer Förderung Christian Gericke, Dr. med., M.Sc.
Bürgerbefragung zur Stammzellforschung Berlin, 13. März 2004 Technische Universität Berlin Stammzellforschung in Deutschland unter dem Blickwinkel europäischer Förderung Christian Gericke, Dr. med., M.Sc.
Die EU zum Thema Kräuter
 Die EU zum Thema Kräuter Herbert DORFMANN Mitglied des Europäischen Parlaments AGENDA Die Herausforderungen Nationale Agenturen Europäische Arzneimittelagentur Der Gesetzesrahmen Richtlinie zu pflanzlichen
Die EU zum Thema Kräuter Herbert DORFMANN Mitglied des Europäischen Parlaments AGENDA Die Herausforderungen Nationale Agenturen Europäische Arzneimittelagentur Der Gesetzesrahmen Richtlinie zu pflanzlichen
Zulassung von Arzneimitteln. Klinische Untersuchungen. Katalin Müllner
 Zulassung von Arzneimitteln. Klinische Untersuchungen Katalin Müllner Arzneimittel In gesetzlicher Definition sind Arzneimittel Stoffe oder Zubereitungen aus Stoffen, die vom Hersteller, der sie in den
Zulassung von Arzneimitteln. Klinische Untersuchungen Katalin Müllner Arzneimittel In gesetzlicher Definition sind Arzneimittel Stoffe oder Zubereitungen aus Stoffen, die vom Hersteller, der sie in den
BAnz AT B5. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V Opicapon
Beschluss des Gemeinsamen Bundesausschusses über eine der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V Opicapon
Pädiatrische Hämatologie und Onkologie
 Pädiatrische Hämatologie und Onkologie Infos für Eltern & Patienten Liebe Eltern, liebe Patienten, unser Team ist spezialisiert auf die Betreuung von Kindern, Jugendlichen und auch jungen Erwachsenen mit
Pädiatrische Hämatologie und Onkologie Infos für Eltern & Patienten Liebe Eltern, liebe Patienten, unser Team ist spezialisiert auf die Betreuung von Kindern, Jugendlichen und auch jungen Erwachsenen mit
Zu Therapie und Prophylaxe des paroxysmalen Vorhofflimmerns
 AMB 2000, 34, 92 Zu Therapie und Prophylaxe des paroxysmalen Vorhofflimmerns In einer Untersuchung von G. Cotter et al. aus Israel (1) wurden 100 Patienten (Durchschnittsalter 68 Jahre) mit seit weniger
AMB 2000, 34, 92 Zu Therapie und Prophylaxe des paroxysmalen Vorhofflimmerns In einer Untersuchung von G. Cotter et al. aus Israel (1) wurden 100 Patienten (Durchschnittsalter 68 Jahre) mit seit weniger
28. Oktober 2015 I Seite 1. Der Vertragsarzt im Spannungsfeld zwischen Verordnungsfähigkeit und Regressgefahr
 28. Oktober 2015 I Seite 1 Der Vertragsarzt im Spannungsfeld zwischen Verordnungsfähigkeit und Regressgefahr Dipl.-Med. Jutta Eckert Forum Ambulant-stationärer Dialog, 21. Oktober 2015 DEGAM Leitlinie
28. Oktober 2015 I Seite 1 Der Vertragsarzt im Spannungsfeld zwischen Verordnungsfähigkeit und Regressgefahr Dipl.-Med. Jutta Eckert Forum Ambulant-stationärer Dialog, 21. Oktober 2015 DEGAM Leitlinie
Hämodynamische Stabilisierung praxisnah umgesetzt
 DAC 2006 Leipzig, 17. bis 20. Mai 2006 Hämodynamische Stabilisierung praxisnah umgesetzt Andreas Meier-Hellmann Hämodynamische Stabilisierung praxisnah umgesetzt Welche Werkzeuge haben wir? Volumen zur
DAC 2006 Leipzig, 17. bis 20. Mai 2006 Hämodynamische Stabilisierung praxisnah umgesetzt Andreas Meier-Hellmann Hämodynamische Stabilisierung praxisnah umgesetzt Welche Werkzeuge haben wir? Volumen zur
Arzneimittelinformation mit dem Handheld - Einsatzmöglichkeiten für Personal Digital Assistants (PDA)
 Arzneimittelinformation mit dem Handheld - Einsatzmöglichkeiten für Personal Digital Assistants (PDA) Erlangen 17. Januar 2009 1. Deutscher Kongress für patientenorientierte Arzneimittelinformation Köln
Arzneimittelinformation mit dem Handheld - Einsatzmöglichkeiten für Personal Digital Assistants (PDA) Erlangen 17. Januar 2009 1. Deutscher Kongress für patientenorientierte Arzneimittelinformation Köln
Klinische Prüfung von Arzneimitteln: Öffentliche Informationen in PharmNet.Bund Clinical Trials (CT)
 Klinische Prüfung von Arzneimitteln: Öffentliche Informationen in PharmNet.Bund Clinical Trials (CT) Nutzertreffen, Köln 8. November 2011 Dr. Barbara Höfgen, Dr. Irina Bosman PharmNet.Bund-CT Gesetzliche
Klinische Prüfung von Arzneimitteln: Öffentliche Informationen in PharmNet.Bund Clinical Trials (CT) Nutzertreffen, Köln 8. November 2011 Dr. Barbara Höfgen, Dr. Irina Bosman PharmNet.Bund-CT Gesetzliche
Frühe Nutzenbewertung von Arzneimitteln: Ergebnisse und Wirkung
 Frühe Nutzenbewertung von Arzneimitteln: Ergebnisse und Wirkung 53. Wirtschaftsforum des Deutschen Apothekerverbandes (DAV) am 28. April 2016 in Berlin Georg Wager, General Manager Inhaltsübersicht Ziele
Frühe Nutzenbewertung von Arzneimitteln: Ergebnisse und Wirkung 53. Wirtschaftsforum des Deutschen Apothekerverbandes (DAV) am 28. April 2016 in Berlin Georg Wager, General Manager Inhaltsübersicht Ziele
Analgesie bei Kindernotfällen
 Analgesie na klar! Wo liegen die Probleme? Analgesie bei Kindernotfällen Unterzeile zum Titel Uwe Trieschmann 19.06.2010 DAK 2010 Umgang und Erfahrung des Notfallteams mit Kindern Wie bekommen wir bei
Analgesie na klar! Wo liegen die Probleme? Analgesie bei Kindernotfällen Unterzeile zum Titel Uwe Trieschmann 19.06.2010 DAK 2010 Umgang und Erfahrung des Notfallteams mit Kindern Wie bekommen wir bei
KHK mit Angina pectoris: Ivabradin reduziert kardiale Ereignisse
 Neue Ergebnisse aus der BEAUTIfUL-Studie KHK mit Angina pectoris: Ivabradin reduziert kardiale Ereignisse Barcelona, Spanien, 31. August 2009 Aktuelle Daten einer auf dem Kongress der European Society
Neue Ergebnisse aus der BEAUTIfUL-Studie KHK mit Angina pectoris: Ivabradin reduziert kardiale Ereignisse Barcelona, Spanien, 31. August 2009 Aktuelle Daten einer auf dem Kongress der European Society
TOP-PAPER ARZNEIMITTELINFORMATION
 CAMPUS GROSSHADERN CAMPUS INNENSTADT TOP-PAPER ARZNEIMITTELINFORMATION Dr. Dorothea Strobach, München THE STEPPER 2 THERE ARE WORLDS WAITING. ALL IT TAKES IS ONE SMALL STEP. Terry Pratchett, Stephen Baxter.
CAMPUS GROSSHADERN CAMPUS INNENSTADT TOP-PAPER ARZNEIMITTELINFORMATION Dr. Dorothea Strobach, München THE STEPPER 2 THERE ARE WORLDS WAITING. ALL IT TAKES IS ONE SMALL STEP. Terry Pratchett, Stephen Baxter.
Kongress der European Respiratory Society 2012: Neues Positionspapier zum Paradigmen wechsel in de. in der COPD-Therapie
 Kongress der European Respiratory Society 2012 Neues Positionspapier zum Paradigmen wechsel in der COPD-Therapie Wien, Österreich (2. September 2012) Internationale Experten auf dem Gebiet der Pneumologie
Kongress der European Respiratory Society 2012 Neues Positionspapier zum Paradigmen wechsel in der COPD-Therapie Wien, Österreich (2. September 2012) Internationale Experten auf dem Gebiet der Pneumologie
AktuellerZulassungsstatusvon HAES-Produkten
 AktuellerZulassungsstatusvon HAES-Produkten Dr. Frank Dalbeck Fresenius Kabi Deutschland Frankfurt, den 21.11.2013 As the CMDh position has been adopted by majority vote, it will now be sent to the European
AktuellerZulassungsstatusvon HAES-Produkten Dr. Frank Dalbeck Fresenius Kabi Deutschland Frankfurt, den 21.11.2013 As the CMDh position has been adopted by majority vote, it will now be sent to the European
Der Erhalt der Kinder-Grundversorgung in Europa muss eine Herausforderung der Zukunft sein
 Der Erhalt der Kinder-Grundversorgung in Europa muss eine Herausforderung der Zukunft sein Elke Jäger-Roman, ECPCP European Confederation of Primary Care Paediatricians In Europa gibt es derzeit: 91 Mill
Der Erhalt der Kinder-Grundversorgung in Europa muss eine Herausforderung der Zukunft sein Elke Jäger-Roman, ECPCP European Confederation of Primary Care Paediatricians In Europa gibt es derzeit: 91 Mill
Behandlung von Kindern, Jugendlichen und Erwachsenen am ImmunDefektCentrum Leipzig Probleme mit der Transition gelöst?
 dsai - Ärztefortbildung und Patiententreffen 05. November 2016, The Westin Hotel Leipzig Behandlung von Kindern, Jugendlichen und Erwachsenen am ImmunDefektCentrum Leipzig Probleme mit der Transition gelöst?
dsai - Ärztefortbildung und Patiententreffen 05. November 2016, The Westin Hotel Leipzig Behandlung von Kindern, Jugendlichen und Erwachsenen am ImmunDefektCentrum Leipzig Probleme mit der Transition gelöst?
