Farbigkeit und Theorien
|
|
|
- Dieter Becke
- vor 8 Jahren
- Abrufe
Transkript
1 Farbigkeit und Theorien Farbigkeit von Dinah Shafry Licht ist elektromagnetische Strahlung, bei der jede Farbe eine einzelne Wellenlänge besitzt, die als unterschiedliche Farben vom Menschen wahrgenommen wird, sobald diese von einem Gegenstand reflektiert wird. Weißes Licht enthält alle Farben und, wenn dieses auf eine Oberfläche trifft, wird ein Teil der Farben reflektiert, andere können absorbiert werden. Bei Schwarz hingegen werden alle Lichtstrahlen absorbiert. Wenn Farben absorbiert werden, erscheint die Oberfläche in der Farbe der jeweiligen Komplementärfarbe. Nimmt ein Stoff beispielsweise blaues Licht auf, so hat der Stoff für das menschliche Auge eine gelbe Farbe. Durch die Energie der absorbierten Farben wird das Schwingen der Moleküle angeregt: Es entsteht Wärme. Umso kürzer die Wellenlängen sind, desto mehr Energie wird umgesetzt und die Strahlen werden gefährlicher. Das menschliche Auge vermischt Farbeindrücke, wenn mehrere Wellenlängen reflektiert werden. Der Mensch kann ein Farbspektrum von nm wahrnehmen. In einem Farbspektrum sind alle Spektralfarben enthalten, d.h. alle Farben eines Regenbogens. Spektralfarben des Regenbogens für das Auge sichtbare Wellenlängen des Lichts Einordnung des sichtbaren Farbspektrums in das Gesamtspektrum der elektromagnetischen Strahlung
2 Entstehung eines Farbspektrum durch die Lichtbrechung eines Prismas Ein Farbspektrum kann auch durch die Lichtbrechung eines Prismas entstehen. Dieser Vorgang funktioniert folgendermaßen: Wenn ein Lichtstrahl durch ein Prisma (Glasprisma) fällt, wird dieser zweimal gebrochen. Erstens beim Übergang vom optisch dünneren zum optisch dichteren Medium, d.h. von der Luft zum Glas hin, und zweitens beim Übergang vom optisch dichteren zum optisch dünneren Medium. D.h. der Lichtstrahl wird gebrochen, sobald er auf das Glas des Prismas trifft, scheint dann auf dieser Bahn durch das Glas hindurch und wird ein zweites Mal an der Stelle gebrochen, wo der Lichtstrahl das Glas wieder verlässt. Allgemein gilt, dass verschiedene Wellenlängen auch unterschiedlich gebrochen werden. Bei theoretischen Erklärungen bzw. Berechnungen geht man von Sonnenlicht aus, welches dann oft auch als weißes Licht bezeichnet wird. Die Brechung des Sonnenlichts durch ein Prisma lässt ein kontinuierliches Spektrum entstehen, welches ungefähr 300 unterschiedliche Farbnuancen beinhaltet. Diese lassen sich jedoch optisch nicht weiter aufspalten, deshalb nennt man sie spektralrein. Wie diese Spektralfarben entstehen, lässt sich anhand folgender Abbildung verdeutlichen: Entstehung der Spektralfarben Entstehung der Spektralfarben Wittsche Farbstofftheorie Nach der Wittschen Farbstofftheorie werden Farbstoffmoleküle in verschiedene funktionelle Bereiche eingeteilt: Chromophore Teile (Teile, die den Farbstoff tragen) und auxchrome Gruppen (farbhelfende Gruppen). Bei dieser Theorie unterscheidet man zwischen Hypsochromen und Bathochromen Effekten. Der hypsochrome Effekt bezeichnet die Verschiebung der Absorption in den kurzwelligeren, energiereicheren Bereich des elektromagnetischen Spektrums. Der bathochrome Effekt beschreibt die Verschiebung eines Absorptionsspektrums in Richtung größerer Wellenlängen und somit in den energieärmeren Bereich des Lichtspektrums. kurzer Abstand = geringe Anhebung des Elektrons = energiearmes Licht mit langer Wellenlänge wird absorbiert (800 nm) größerer Abstand = stärkere Anhebung des Elektrons = energiereicheres Licht mit kürzerer Wellenlänge wird absorbiert (600 nm) 2
3 Die auxochromen Gruppen sind an den Phenylringen hängende Reste, die die Farbgebung beeinflussen. Die auxochrome Gruppe kann einen +M-Effekt auf die aromatischen Ringe ausbilden. Wenn sich jedoch ein Substituent an der auxochromen Gruppe anlagert, wird der +M-Effekt verhindert. Es nimmt am konjugierten Doppelsystem teil und vergrößert das π Elektronensystem, das heißt, es findet ein bathochromer Effekt statt. Ihre Wirkung beruht auf ihrer Elektronendonatoreigenschaft, die die Delokalisierung im Chromophor erhöht und unterstützt die Farbigkeit. Je wirksamer ein auxchromer Rest ist, desto weiter verschiebt er die Lichtaufnahme in den längeren Wellenbereich. Eine weitere Möglichkeit zur Steigerung der Delokalisierung von π - Elektronen im Chromophor ist zusätzlich zur auxochromen Gruppe eine anti-auxochrome Gruppe. Diese kann einen M-Effekt auf das π Elektronensystem ausbilden und kann freie Elektronenpaare aufnehmen, die durch den +M-Effekt der auxochromen Gruppe in das System gegeben werden. Weil das zentrale π - Elektronensystem immer gleich ist, kommt den auxochromen und anti-auxochromen hier eine entschiedene Bedeutung zu: Sie können in der richtigen Stellung zueinander einen Push and Pull- Mechanismus entwickeln und damit zu einer Bathochromie führen. Einteilung von Methylorange nach der Wittschen Farbstofftheorie Das Chromophor ist der Teil eines Farbstoffes, der für das Vorhandensein der Farbe sorgt, da er das zentrale Bindungsatom darstellt. Man versteht darunter im Allgemeinen ungesättigte Verbindungen, welche leicht bewegliche π - Elektronen enthalten. Das Chromophor enthält delokalisierte Elektronen und kann Farbton und Farbtiefe eines Farbstoffes beeinflussen. Er muss allerdings sp² hybridisiert sein, um Farbe zu ermöglichen. Durch die Mesomerie sind die Elektronen sogar noch weiter delokalisiert, wodurch der chromophore Charakter noch weiter verstärkt wird, da sich HOMO (highest occupied molecular orbital) und LUMO (lowest unoccupied molecual orbital) Orbital noch weiter annähern. (MO-Theorie, s.u.) Das Chromogen verlängert das π Elektronensystem oder ermöglicht die Mesomerie, wodurch die Farbigkeit entsteht. 3
4 Valenzbindungstheorie Die Valenzbindungstheorie (VB-Theorie) erklärt den Aufbau und die Geometrie von Molekülen anhand der Bindungen zwischen den in ihnen enthaltenen Atomen. Die VB-Theorie ist die in der Schule am intensivsten unterrichtete Theorie. Man unterscheidet 1-fach, 2-fach und in manchen Fällen auch 3-fach Bindungen. Am Beispiel des Kohlenstoffs soll dies kurz erklärt werden: Kohlenstoff (Formelzeichen C) besitzt vier "eigene" Elektronen in seiner äußeren Schale. Im Zustand größter Stabilität befindet es sich allerdings nur, wenn es sich Elektronen mit einem anderen Atom "teilt", also eine Bindung eingeht, da es danach strebt, nicht nur seine vier freien Elektronen zur Verfügung zu haben, sondern diese zu einer vollen äußere Schale mit insgesamt acht Elektronen zu ergänzen (Oktett- bzw. Edelgas-Regel). Bei einer solchen sogenannten Valenzbindung, die aus jeweils (mindestens) einem Elektron jedes Bindungspartners besteht, werden die Elektronen also quasi "doppelt genutzt": Jedes der beiden Atome erreicht dadurch einen Zustand größerer Stabilität (acht Außenelektronen). Zusätzlich zu diesen sogenannten Einfach-Bindungen, bei denen sich nur zwei Elektronen pro Bindung kombinieren, gibt es auch noch sogenannte Zweifach-Bindungen bzw Doppelbindungen. Diese kommen zum Beispiel sehr häufig bei Kohlenstoff vor. Bei einer Doppelbindung steuert jeder Bindungspartner 2 Elektronen zur Bindung bei, wodurch diese also aus insgesamt 4 Elektronen besteht. Sie sind dadurch in ihrer "Bewegungsfreiheit" weniger stark eingeschränkt und können deshalb angeregt werden. Dies ist der entscheidende Punkt beim Thema Farbigkeit. Wird einem Molekül mit einer Doppelbindung Energie (z. B. durch Absorption von Licht) Energie hinzugefügt, so können ein oder auch mehrere Elektronen angeregt werden, wodurch sie in eine höhere Schale springen. Fallen sie in ihre ursprüngliche Schale zurück, so geben sie dabei genau die Energiemenge in Form von Licht (Photonen) ab, die jeweils nötig war, um sie anzuregen. Da diese Energie je Molekül und Atom unterschiedlich ist, emittieren sie auch unterschiedliches Licht, da die Wellenlänge des Lichts nach Heisenberg direkt von der Energie des emittierten Photons abhängig ist. Mithilfe der Valenzbindungstheorie kann man anhand des Wissens um die Bindungen zwischen den Atomen in einem Molekül zwar relativ einfach Schlüsse auf die Geometrie des Moleküls ziehen, für die Erklärung der Farbigkeit ist sie jedoch etwas ungenau, weswegen man besser auf die Molekülorbitaltheorie zurückgreift. Man geht davon aus, dass die Doppelbindungelektronen sich in konjugierten Doppelbindungen, also jeweils übernächste Doppelbindungen, durch Mesomerie beliebig frei bewegen können. Je größer das Doppelbindungssystem ist, desto länger sind die Wellen, die zur Resonanz des schwingenden Elektrons passen und von diesem absorbiert werden: Je länger das Doppelbindungssystem ist, desto länger ist auch die Wellenlänge des absorbierten Lichts. sp 2 -hybridisierte C-Atome einer C=C-Doppelbindung Konjugierte Doppelbindungen 4
5 Molekülorbitaltheorie Neben der Valenzbindungstheorie ist die Molekülorbitaltheorie (MO-Theorie) ein wichtiges Hilfsmittel zur Beschreibung der chemischen Bindung. Die bindenden Elektronenpaare werden hierbei nicht als lokalisiert betrachtet, sondern man stellt sich die Bindungselektronen als auf verschiedene Molekülorbitale diskreter Energie verteilt vor. Diese Orbitale können sich über das gesamte Molekül erstrecken. Die Grundlage der MO- Theorie ist die Schrödinger-Gleichung. Die Wellenfunktion beschreibt die Wechselwirkung des Elektrons mit den anderen Elektronen und Atomkernen im Molekül. Die MO-Theorie beschreibt mit Hilfe von komplementären Möglichkeiten den Aufbau von Atombindungen. Die Struktur des Moleküls nach dem MO-Modell ist ausschlaggebend für die Farbigkeit. Bei dieser Theorie hängt es von den Symmetrieeigenschaften der Einzelorbitale ab, welche Kombinationen bindende bzw. antibindende oder nichtbindende Molekülorbitale bilden. Je größer die Moleküle sind, desto mehr Energie wird für die Hybridisierung der π Elektronenwolke benötigt. Die Energie die im Licht enthalten ist, bringt die Elektronen in dem π Molekülorbital dazu, in das nächst höhere Energielevel, dem π* - Molekülorbital aufzusteigen. Das heißt von dem HOMO (highest occupied molecular orbital) zu dem LUMO (lowest unoccupied molecual orbital). Dabei muss die Energie des Lichts genau mit der Energie übereinstimmen, die benötigt wird, damit die Elektronen aufsteigen können. Anschließend fallen die Elektronen wieder runter und die Energie wird als Wärmeenergie freigesetzt. 5
6 Anwendung und Vergleich der Theorien anhand des Farbstoffes Kristallviolett Kristallviolett zeigt bei einer Titration mit Natronlauge (NaOH, Base) eine Entfärbung von gelb zu farblos, es geht also in den UV-Bereich. Dieser Vorgang kann auch nicht mehr umgekehrt werden: Ist der Stoff einmal farblos, bleibt er dauerhaft in diesem Zustand. Bei der Zugabe von Salzsäure (HCl, Säure) nimmt der Stoff Farbe an: Er wechselt von blau zu gründ und gelb. Durch zusätzliche Zugabe von Natronlauge kann der Stoff anders als bei der ersten Reaktion farblos gemacht werden. Entfärbung bei Kristallviolett: Farbstofftheorie Base (NaOH) Säure (HCl) Wittsche Farbstofftheorie Molekülorbitaltheorie Valenzbindungstheorie Das OH-Anion lagert sich an dem zentralen Chromophor an, wodurch sich die Farbigkeit auflöst bzw. in einen kürzerwelligen UV-Bereich verschoben wird: Hypsochromie. Durch die Anlagerung des OH-Anions (Nucleophil) an zentralen Kohlenstoff verändert sich die sp²-hybridisierung zu sp 3 und das π Elektronensystem verkürzt sich zu drei kleineren, isolierten Systemen. Alleine absorbieren sie nur noch das Licht im UV-Bereich, da der Abstand zwischen HOMO und LUMO durch weniger p-orbitale größer und damit energiereicher wird. Der zentrale Kohlenstoffs ist durch die zusätzliche OH-Gruppe nicht mehr in der Lage, ein chinoides Doppelbindungssystem zu bilden. Der Kohlenstoff kann nicht mehr an einer Mesomerie teilnehmen und das konjugierte Doppelbindungssystem verkürzt sich. Durch die Zugabe von Salzsäure entsteht ein hypsochromer Effekt. Der +M-Effekt der auxochromen Gruppen wird durch Anlagerung des Protons verhindert und die Wellenlänge verkürzt sich. Durch die Anlagerung des Protons an den sp 2 - hybridirsierten Stickstoff wird dieser sp3- hybridisiert und besitzt keine p-orbitale mehr. Das π Elektronensystem verkürzt sich und die Absorption erfolgt in einem energiereicheren kürzerwelligen Bereich. Die Säure bindet das freie Elektronenpaar der Amino-Gruppe durch die Bindung zum Proton, wodurch die Mesomerie nicht mehr möglich ist. Das konjugierte Doppelbindungssystem wird verkleinert und damit verkürzt sich die absorbierte Wellenlänge. Literaturverzeichnis Material aus dem Unterricht 6
1 mm 20mm ) =2.86 Damit ist NA = sin α = 0.05. α=arctan ( 1.22 633 nm 0.05. 1) Berechnung eines beugungslimitierten Flecks
 1) Berechnung eines beugungslimitierten Flecks a) Berechnen Sie die Größe eines beugungslimitierten Flecks, der durch Fokussieren des Strahls eines He-Ne Lasers (633 nm) mit 2 mm Durchmesser entsteht.
1) Berechnung eines beugungslimitierten Flecks a) Berechnen Sie die Größe eines beugungslimitierten Flecks, der durch Fokussieren des Strahls eines He-Ne Lasers (633 nm) mit 2 mm Durchmesser entsteht.
UV/VIS-Spektroskopie
 UV/VIS-Spektroskopie Dies ist die älteste spektroskopische Methode, die aber wegen begrenzter Aussagekraft heute in der Praxis keine allzu große Rolle mehr spielt. Es werden elektronische Übergänge angeregt,
UV/VIS-Spektroskopie Dies ist die älteste spektroskopische Methode, die aber wegen begrenzter Aussagekraft heute in der Praxis keine allzu große Rolle mehr spielt. Es werden elektronische Übergänge angeregt,
2-01. Das Ethen-Molekül. Perspektivische Darstellung des Ethen-Moleküls.
 Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Übungen zur VL Chemie für Biologen und Humanbiologen 18.11.2011 Lösung Übung 3
 Übungen zur VL Chemie für Biologen und Humanbiologen 18.11.2011 Lösung Übung 3 Teil 1: Die Geometrie organischer Verbindungen 1. Welche Form hat ein s-orbital? Welche Form haben p-orbitale? Skizzieren
Übungen zur VL Chemie für Biologen und Humanbiologen 18.11.2011 Lösung Übung 3 Teil 1: Die Geometrie organischer Verbindungen 1. Welche Form hat ein s-orbital? Welche Form haben p-orbitale? Skizzieren
Lichtbrechung an Linsen
 Sammellinsen Lichtbrechung an Linsen Fällt ein paralleles Lichtbündel auf eine Sammellinse, so werden die Lichtstrahlen so gebrochen, dass sie durch einen Brennpunkt der Linse verlaufen. Der Abstand zwischen
Sammellinsen Lichtbrechung an Linsen Fällt ein paralleles Lichtbündel auf eine Sammellinse, so werden die Lichtstrahlen so gebrochen, dass sie durch einen Brennpunkt der Linse verlaufen. Der Abstand zwischen
Optik. Optik. Optik. Optik. Optik
 Nenne das Brechungsgesetz! Beim Übergang von Luft in Glas (Wasser, Kunststoff) wird der Lichtstrahl zum Lot hin gebrochen. Beim Übergang von Glas (Wasser...) in Luft wird der Lichtstrahl vom Lot weg gebrochen.
Nenne das Brechungsgesetz! Beim Übergang von Luft in Glas (Wasser, Kunststoff) wird der Lichtstrahl zum Lot hin gebrochen. Beim Übergang von Glas (Wasser...) in Luft wird der Lichtstrahl vom Lot weg gebrochen.
Professionelle Seminare im Bereich MS-Office
 Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
Selbst-Test zur Vorab-Einschätzung zum Vorkurs Chemie für Mediziner
 Liebe Studierende der Human- und Zahnmedizin, mithilfe dieses Tests können Sie selbst einschätzen, ob Sie den Vorkurs besuchen sollten. Die kleine Auswahl an Aufgaben spiegelt in etwa das Niveau des Vorkurses
Liebe Studierende der Human- und Zahnmedizin, mithilfe dieses Tests können Sie selbst einschätzen, ob Sie den Vorkurs besuchen sollten. Die kleine Auswahl an Aufgaben spiegelt in etwa das Niveau des Vorkurses
SUPERABSORBER. Eine Präsentation von Johannes Schlüter und Thomas Luckert
 SUPERABSORBER Eine Präsentation von Johannes Schlüter und Thomas Luckert Inhalt: Die Windel Die Technik des Superabsorbers Anwendungsgebiete des Superabsorbers Ein kurzer Abriss aus der Geschichte der
SUPERABSORBER Eine Präsentation von Johannes Schlüter und Thomas Luckert Inhalt: Die Windel Die Technik des Superabsorbers Anwendungsgebiete des Superabsorbers Ein kurzer Abriss aus der Geschichte der
Outlook. sysplus.ch outlook - mail-grundlagen Seite 1/8. Mail-Grundlagen. Posteingang
 sysplus.ch outlook - mail-grundlagen Seite 1/8 Outlook Mail-Grundlagen Posteingang Es gibt verschiedene Möglichkeiten, um zum Posteingang zu gelangen. Man kann links im Outlook-Fenster auf die Schaltfläche
sysplus.ch outlook - mail-grundlagen Seite 1/8 Outlook Mail-Grundlagen Posteingang Es gibt verschiedene Möglichkeiten, um zum Posteingang zu gelangen. Man kann links im Outlook-Fenster auf die Schaltfläche
Das Leitbild vom Verein WIR
 Das Leitbild vom Verein WIR Dieses Zeichen ist ein Gütesiegel. Texte mit diesem Gütesiegel sind leicht verständlich. Leicht Lesen gibt es in drei Stufen. B1: leicht verständlich A2: noch leichter verständlich
Das Leitbild vom Verein WIR Dieses Zeichen ist ein Gütesiegel. Texte mit diesem Gütesiegel sind leicht verständlich. Leicht Lesen gibt es in drei Stufen. B1: leicht verständlich A2: noch leichter verständlich
PCD Europe, Krefeld, Jan 2007. Auswertung von Haemoccult
 Auswertung von Haemoccult Ist das positiv? Nein! Ja! Im deutschen Krebsfrüherkennungsprogramm haben nur etwa 1 % der Frauen und 1,5 % der Männer ein positives Haemoccult -Ergebnis, da dieser Test eine
Auswertung von Haemoccult Ist das positiv? Nein! Ja! Im deutschen Krebsfrüherkennungsprogramm haben nur etwa 1 % der Frauen und 1,5 % der Männer ein positives Haemoccult -Ergebnis, da dieser Test eine
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren
 Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Optik: Teilgebiet der Physik, das sich mit der Untersuchung des Lichtes beschäftigt
 -II.1- Geometrische Optik Optik: Teilgebiet der, das sich mit der Untersuchung des Lichtes beschäftigt 1 Ausbreitung des Lichtes Das sich ausbreitende Licht stellt einen Transport von Energie dar. Man
-II.1- Geometrische Optik Optik: Teilgebiet der, das sich mit der Untersuchung des Lichtes beschäftigt 1 Ausbreitung des Lichtes Das sich ausbreitende Licht stellt einen Transport von Energie dar. Man
1 Zwei Teilchen in einem Kastenpotenzial
 1 Zwei Teilchen in einem Kastenpotenzial Es geht hier darum herauszu nden, welche prinzipiellen Eigenschaften die Wellenfunktion für mehrere Teilchen im gleichen Potenzial aufweisen muss. Wir unterscheiden
1 Zwei Teilchen in einem Kastenpotenzial Es geht hier darum herauszu nden, welche prinzipiellen Eigenschaften die Wellenfunktion für mehrere Teilchen im gleichen Potenzial aufweisen muss. Wir unterscheiden
Würfelt man dabei je genau 10 - mal eine 1, 2, 3, 4, 5 und 6, so beträgt die Anzahl. der verschiedenen Reihenfolgen, in denen man dies tun kann, 60!.
 040304 Übung 9a Analysis, Abschnitt 4, Folie 8 Die Wahrscheinlichkeit, dass bei n - maliger Durchführung eines Zufallexperiments ein Ereignis A ( mit Wahrscheinlichkeit p p ( A ) ) für eine beliebige Anzahl
040304 Übung 9a Analysis, Abschnitt 4, Folie 8 Die Wahrscheinlichkeit, dass bei n - maliger Durchführung eines Zufallexperiments ein Ereignis A ( mit Wahrscheinlichkeit p p ( A ) ) für eine beliebige Anzahl
Das große ElterngeldPlus 1x1. Alles über das ElterngeldPlus. Wer kann ElterngeldPlus beantragen? ElterngeldPlus verstehen ein paar einleitende Fakten
 Das große x -4 Alles über das Wer kann beantragen? Generell kann jeder beantragen! Eltern (Mütter UND Väter), die schon während ihrer Elternzeit wieder in Teilzeit arbeiten möchten. Eltern, die während
Das große x -4 Alles über das Wer kann beantragen? Generell kann jeder beantragen! Eltern (Mütter UND Väter), die schon während ihrer Elternzeit wieder in Teilzeit arbeiten möchten. Eltern, die während
Übungsblatt zu Säuren und Basen
 1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
Organische Chemie I Chemie am 16.11.2012. Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2
 Organische Chemie I Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2 Verstehen was Organische Chemie heisst und die Entstehung von Kohlenstoffverbindungen kennen!... 2
Organische Chemie I Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2 Verstehen was Organische Chemie heisst und die Entstehung von Kohlenstoffverbindungen kennen!... 2
1 Mathematische Grundlagen
 Mathematische Grundlagen - 1-1 Mathematische Grundlagen Der Begriff der Menge ist einer der grundlegenden Begriffe in der Mathematik. Mengen dienen dazu, Dinge oder Objekte zu einer Einheit zusammenzufassen.
Mathematische Grundlagen - 1-1 Mathematische Grundlagen Der Begriff der Menge ist einer der grundlegenden Begriffe in der Mathematik. Mengen dienen dazu, Dinge oder Objekte zu einer Einheit zusammenzufassen.
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt für die Klassen 7 bis 9: Linsen und optische Geräte
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt für die Klassen 7 bis 9: Linsen und optische Geräte Das komplette Material finden Sie hier: Download bei School-Scout.de
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt für die Klassen 7 bis 9: Linsen und optische Geräte Das komplette Material finden Sie hier: Download bei School-Scout.de
h- Bestimmung mit LEDs
 h- Bestimmung mit LEDs GFS im Fach Physik Nicolas Bellm 11. März - 12. März 2006 Der Inhalt dieses Dokuments steht unter der GNU-Lizenz für freie Dokumentation http://www.gnu.org/copyleft/fdl.html Inhaltsverzeichnis
h- Bestimmung mit LEDs GFS im Fach Physik Nicolas Bellm 11. März - 12. März 2006 Der Inhalt dieses Dokuments steht unter der GNU-Lizenz für freie Dokumentation http://www.gnu.org/copyleft/fdl.html Inhaltsverzeichnis
1.1 Auflösungsvermögen von Spektralapparaten
 Physikalisches Praktikum für Anfänger - Teil Gruppe Optik. Auflösungsvermögen von Spektralapparaten Einleitung - Motivation Die Untersuchung der Lichtemission bzw. Lichtabsorption von Molekülen und Atomen
Physikalisches Praktikum für Anfänger - Teil Gruppe Optik. Auflösungsvermögen von Spektralapparaten Einleitung - Motivation Die Untersuchung der Lichtemission bzw. Lichtabsorption von Molekülen und Atomen
Zeichen bei Zahlen entschlüsseln
 Zeichen bei Zahlen entschlüsseln In diesem Kapitel... Verwendung des Zahlenstrahls Absolut richtige Bestimmung von absoluten Werten Operationen bei Zahlen mit Vorzeichen: Addieren, Subtrahieren, Multiplizieren
Zeichen bei Zahlen entschlüsseln In diesem Kapitel... Verwendung des Zahlenstrahls Absolut richtige Bestimmung von absoluten Werten Operationen bei Zahlen mit Vorzeichen: Addieren, Subtrahieren, Multiplizieren
Optik Kontaktlinsen Instrumente Photo
 Stand 09.04.2015 Seite 1 UV-Filter Die ultraviolette Strahlung sind kurzwellige, elektromagnetische Strahlen, welche eine Streuung erzeugen. Mit einem UV-Filter werden gerade diese Streulichter absorbiert.
Stand 09.04.2015 Seite 1 UV-Filter Die ultraviolette Strahlung sind kurzwellige, elektromagnetische Strahlen, welche eine Streuung erzeugen. Mit einem UV-Filter werden gerade diese Streulichter absorbiert.
Die Bundes-Zentrale für politische Bildung stellt sich vor
 Die Bundes-Zentrale für politische Bildung stellt sich vor Die Bundes-Zentrale für politische Bildung stellt sich vor Deutschland ist ein demokratisches Land. Das heißt: Die Menschen in Deutschland können
Die Bundes-Zentrale für politische Bildung stellt sich vor Die Bundes-Zentrale für politische Bildung stellt sich vor Deutschland ist ein demokratisches Land. Das heißt: Die Menschen in Deutschland können
Simulation LIF5000. Abbildung 1
 Simulation LIF5000 Abbildung 1 Zur Simulation von analogen Schaltungen verwende ich Ltspice/SwitcherCAD III. Dieses Programm ist sehr leistungsfähig und wenn man weis wie, dann kann man damit fast alles
Simulation LIF5000 Abbildung 1 Zur Simulation von analogen Schaltungen verwende ich Ltspice/SwitcherCAD III. Dieses Programm ist sehr leistungsfähig und wenn man weis wie, dann kann man damit fast alles
Was meinen die Leute eigentlich mit: Grexit?
 Was meinen die Leute eigentlich mit: Grexit? Grexit sind eigentlich 2 Wörter. 1. Griechenland 2. Exit Exit ist ein englisches Wort. Es bedeutet: Ausgang. Aber was haben diese 2 Sachen mit-einander zu tun?
Was meinen die Leute eigentlich mit: Grexit? Grexit sind eigentlich 2 Wörter. 1. Griechenland 2. Exit Exit ist ein englisches Wort. Es bedeutet: Ausgang. Aber was haben diese 2 Sachen mit-einander zu tun?
Grundlagen der Theoretischen Informatik, SoSe 2008
 1. Aufgabenblatt zur Vorlesung Grundlagen der Theoretischen Informatik, SoSe 2008 (Dr. Frank Hoffmann) Lösung von Manuel Jain und Benjamin Bortfeldt Aufgabe 2 Zustandsdiagramme (6 Punkte, wird korrigiert)
1. Aufgabenblatt zur Vorlesung Grundlagen der Theoretischen Informatik, SoSe 2008 (Dr. Frank Hoffmann) Lösung von Manuel Jain und Benjamin Bortfeldt Aufgabe 2 Zustandsdiagramme (6 Punkte, wird korrigiert)
Die Gesellschaftsformen
 Jede Firma - auch eure Schülerfirma - muss sich an bestimmte Spielregeln halten. Dazu gehört auch, dass eine bestimmte Rechtsform für das Unternehmen gewählt wird. Für eure Schülerfirma könnt ihr zwischen
Jede Firma - auch eure Schülerfirma - muss sich an bestimmte Spielregeln halten. Dazu gehört auch, dass eine bestimmte Rechtsform für das Unternehmen gewählt wird. Für eure Schülerfirma könnt ihr zwischen
Es gilt das gesprochene Wort. Anrede
 Sperrfrist: 28. November 2007, 13.00 Uhr Es gilt das gesprochene Wort Statement des Staatssekretärs im Bayerischen Staatsministerium für Unterricht und Kultus, Karl Freller, anlässlich des Pressegesprächs
Sperrfrist: 28. November 2007, 13.00 Uhr Es gilt das gesprochene Wort Statement des Staatssekretärs im Bayerischen Staatsministerium für Unterricht und Kultus, Karl Freller, anlässlich des Pressegesprächs
Adobe Photoshop. Lightroom 5 für Einsteiger Bilder verwalten und entwickeln. Sam Jost
 Adobe Photoshop Lightroom 5 für Einsteiger Bilder verwalten und entwickeln Sam Jost Kapitel 2 Der erste Start 2.1 Mitmachen beim Lesen....................... 22 2.2 Für Apple-Anwender.........................
Adobe Photoshop Lightroom 5 für Einsteiger Bilder verwalten und entwickeln Sam Jost Kapitel 2 Der erste Start 2.1 Mitmachen beim Lesen....................... 22 2.2 Für Apple-Anwender.........................
Zerlegung der Verbindung Wasser. Weiterbildung für fachfremd unterrichtende Lehrkräfte
 Zerlegung der Verbindung Wasser Weiterbildung für fachfremd unterrichtende Lehrkräfte Chromatografi e von Blattfarbstoffen Destillation von Rotwein Titration Herstellung von Natronlauge Öltröpfchen versuch
Zerlegung der Verbindung Wasser Weiterbildung für fachfremd unterrichtende Lehrkräfte Chromatografi e von Blattfarbstoffen Destillation von Rotwein Titration Herstellung von Natronlauge Öltröpfchen versuch
Anleitung über den Umgang mit Schildern
 Anleitung über den Umgang mit Schildern -Vorwort -Wo bekommt man Schilder? -Wo und wie speichert man die Schilder? -Wie füge ich die Schilder in meinen Track ein? -Welche Bauteile kann man noch für Schilder
Anleitung über den Umgang mit Schildern -Vorwort -Wo bekommt man Schilder? -Wo und wie speichert man die Schilder? -Wie füge ich die Schilder in meinen Track ein? -Welche Bauteile kann man noch für Schilder
DER SELBST-CHECK FÜR IHR PROJEKT
 DER SELBST-CHECK FÜR IHR PROJEKT In 30 Fragen und 5 Tipps zum erfolgreichen Projekt! Beantworten Sie die wichtigsten Fragen rund um Ihr Projekt für Ihren Erfolg und für Ihre Unterstützer. IHR LEITFADEN
DER SELBST-CHECK FÜR IHR PROJEKT In 30 Fragen und 5 Tipps zum erfolgreichen Projekt! Beantworten Sie die wichtigsten Fragen rund um Ihr Projekt für Ihren Erfolg und für Ihre Unterstützer. IHR LEITFADEN
Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010
 1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
Was ist Sozial-Raum-Orientierung?
 Was ist Sozial-Raum-Orientierung? Dr. Wolfgang Hinte Universität Duisburg-Essen Institut für Stadt-Entwicklung und Sozial-Raum-Orientierte Arbeit Das ist eine Zusammen-Fassung des Vortrages: Sozialräume
Was ist Sozial-Raum-Orientierung? Dr. Wolfgang Hinte Universität Duisburg-Essen Institut für Stadt-Entwicklung und Sozial-Raum-Orientierte Arbeit Das ist eine Zusammen-Fassung des Vortrages: Sozialräume
infach Geld FBV Ihr Weg zum finanzellen Erfolg Florian Mock
 infach Ihr Weg zum finanzellen Erfolg Geld Florian Mock FBV Die Grundlagen für finanziellen Erfolg Denn Sie müssten anschließend wieder vom Gehaltskonto Rückzahlungen in Höhe der Entnahmen vornehmen, um
infach Ihr Weg zum finanzellen Erfolg Geld Florian Mock FBV Die Grundlagen für finanziellen Erfolg Denn Sie müssten anschließend wieder vom Gehaltskonto Rückzahlungen in Höhe der Entnahmen vornehmen, um
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Übungsbuch für den Grundkurs mit Tipps und Lösungen: Analysis
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Übungsbuch für den Grundkurs mit Tipps und Lösungen: Analysis Das komplette Material finden Sie hier: Download bei School-Scout.de
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Übungsbuch für den Grundkurs mit Tipps und Lösungen: Analysis Das komplette Material finden Sie hier: Download bei School-Scout.de
Alle gehören dazu. Vorwort
 Alle gehören dazu Alle sollen zusammen Sport machen können. In diesem Text steht: Wie wir dafür sorgen wollen. Wir sind: Der Deutsche Olympische Sport-Bund und die Deutsche Sport-Jugend. Zu uns gehören
Alle gehören dazu Alle sollen zusammen Sport machen können. In diesem Text steht: Wie wir dafür sorgen wollen. Wir sind: Der Deutsche Olympische Sport-Bund und die Deutsche Sport-Jugend. Zu uns gehören
1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig?
 1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig? 1) Es sind alles Metalle. 2) In der äußeren Elektronenschale werden s- bzw. s- und p-orbitale aufgefüllt. 3) Sie stimmen
1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig? 1) Es sind alles Metalle. 2) In der äußeren Elektronenschale werden s- bzw. s- und p-orbitale aufgefüllt. 3) Sie stimmen
Wie Sie mit Mastern arbeiten
 Wie Sie mit Mastern arbeiten Was ist ein Master? Einer der großen Vorteile von EDV besteht darin, dass Ihnen der Rechner Arbeit abnimmt. Diesen Vorteil sollten sie nutzen, wo immer es geht. In PowerPoint
Wie Sie mit Mastern arbeiten Was ist ein Master? Einer der großen Vorteile von EDV besteht darin, dass Ihnen der Rechner Arbeit abnimmt. Diesen Vorteil sollten sie nutzen, wo immer es geht. In PowerPoint
Einführungsexperiment mit Hellraumprojektor. Spiegel zuklappen. Behälter mit Wasser gefüllt. zuklappen. Schwarzes Papier als Abdeckung.
 Einführungsexperiment mit Hellraumprojektor Spiegel zuklappen Behälter mit Wasser gefüllt zuklappen Schwarzes Papier als Abdeckung zuklappen schmaler Lichtstreifen ergibt bessere Ergebnisse Tipps: Je höher
Einführungsexperiment mit Hellraumprojektor Spiegel zuklappen Behälter mit Wasser gefüllt zuklappen Schwarzes Papier als Abdeckung zuklappen schmaler Lichtstreifen ergibt bessere Ergebnisse Tipps: Je höher
Organische Moleküle. Verschiedene Ansichten des Methans
 Organische Räumlicher Bau, Elektronendichteverteilungen Verschiedene Ansichten des Methans Ansicht des Methans mit seiner Elektronenhülle (Solid-Darstellung) Ansicht des Methans mit seiner Elektronenhülle
Organische Räumlicher Bau, Elektronendichteverteilungen Verschiedene Ansichten des Methans Ansicht des Methans mit seiner Elektronenhülle (Solid-Darstellung) Ansicht des Methans mit seiner Elektronenhülle
Zahlenwinkel: Forscherkarte 1. alleine. Zahlenwinkel: Forschertipp 1
 Zahlenwinkel: Forscherkarte 1 alleine Tipp 1 Lege die Ziffern von 1 bis 9 so in den Zahlenwinkel, dass jeder Arm des Zahlenwinkels zusammengezählt das gleiche Ergebnis ergibt! Finde möglichst viele verschiedene
Zahlenwinkel: Forscherkarte 1 alleine Tipp 1 Lege die Ziffern von 1 bis 9 so in den Zahlenwinkel, dass jeder Arm des Zahlenwinkels zusammengezählt das gleiche Ergebnis ergibt! Finde möglichst viele verschiedene
Die chemischen Grundgesetze
 Die chemischen Grundgesetze Ausgangsproblem Beim Verbrennen von Holz im Ofen bleibt Asche übrig, die Masse der Asche ist deutlich geringer als die Masse des ursprünglichen Holzes. Lässt man einen Sack
Die chemischen Grundgesetze Ausgangsproblem Beim Verbrennen von Holz im Ofen bleibt Asche übrig, die Masse der Asche ist deutlich geringer als die Masse des ursprünglichen Holzes. Lässt man einen Sack
Eva Douma: Die Vorteile und Nachteile der Ökonomisierung in der Sozialen Arbeit
 Eva Douma: Die Vorteile und Nachteile der Ökonomisierung in der Sozialen Arbeit Frau Dr. Eva Douma ist Organisations-Beraterin in Frankfurt am Main Das ist eine Zusammen-Fassung des Vortrages: Busines
Eva Douma: Die Vorteile und Nachteile der Ökonomisierung in der Sozialen Arbeit Frau Dr. Eva Douma ist Organisations-Beraterin in Frankfurt am Main Das ist eine Zusammen-Fassung des Vortrages: Busines
40-Tage-Wunder- Kurs. Umarme, was Du nicht ändern kannst.
 40-Tage-Wunder- Kurs Umarme, was Du nicht ändern kannst. Das sagt Wikipedia: Als Wunder (griechisch thauma) gilt umgangssprachlich ein Ereignis, dessen Zustandekommen man sich nicht erklären kann, so dass
40-Tage-Wunder- Kurs Umarme, was Du nicht ändern kannst. Das sagt Wikipedia: Als Wunder (griechisch thauma) gilt umgangssprachlich ein Ereignis, dessen Zustandekommen man sich nicht erklären kann, so dass
Vibono Coaching Brief -No. 39
 Gemüse hat doch auch Kohlenhydrate! Wieso kann man mit Gemüse also überhaupt abnehmen? Vibono GmbH 2011-2012, www.vibono.de Kann man mit Gemüse abnehmen, wenn es doch auch Kohlenhydrate hat? Diese Frage
Gemüse hat doch auch Kohlenhydrate! Wieso kann man mit Gemüse also überhaupt abnehmen? Vibono GmbH 2011-2012, www.vibono.de Kann man mit Gemüse abnehmen, wenn es doch auch Kohlenhydrate hat? Diese Frage
Alles, was Sie über unsere Augenbehandlungen wissen sollten
 Alles, was Sie über unsere Augenbehandlungen wissen sollten Korbinian Kofler hat sich bei Memira behandeln lassen. Jetzt beginnt mein neues Leben ohne Brille und Kontaktlinsen! Der sichere Weg zu einem
Alles, was Sie über unsere Augenbehandlungen wissen sollten Korbinian Kofler hat sich bei Memira behandeln lassen. Jetzt beginnt mein neues Leben ohne Brille und Kontaktlinsen! Der sichere Weg zu einem
Qualitätsbedingungen schulischer Inklusion für Kinder und Jugendliche mit dem Förderschwerpunkt Körperliche und motorische Entwicklung
 Forschungsprojekt: Qualitätsbedingungen schulischer Inklusion für Kinder und Jugendliche mit dem Förderschwerpunkt Körperliche und motorische Entwicklung Leichte Sprache Autoren: Reinhard Lelgemann Jelena
Forschungsprojekt: Qualitätsbedingungen schulischer Inklusion für Kinder und Jugendliche mit dem Förderschwerpunkt Körperliche und motorische Entwicklung Leichte Sprache Autoren: Reinhard Lelgemann Jelena
Professionelle Seminare im Bereich MS-Office
 Gegenüber PowerPoint 2003 hat sich in PowerPoint 2007 gerade im Bereich der Master einiges geändert. Auf Handzettelmaster und Notizenmaster gehe ich in diesen Ausführungen nicht ein, die sind recht einfach
Gegenüber PowerPoint 2003 hat sich in PowerPoint 2007 gerade im Bereich der Master einiges geändert. Auf Handzettelmaster und Notizenmaster gehe ich in diesen Ausführungen nicht ein, die sind recht einfach
Farbtypen. Bedeutung von Farben 1. Drucken. Arbeiten mit Farben. Papierhandhabung. Wartung. Problemlösung. Verwaltung. Index
 Bedeutung von Farben 1 Ihr Drucker bietet Ihnen die Möglichkeit, Farben als Kommunikationsmittel einzusetzen. Farben wecken die Aufmerksamkeit, schaffen Respekt und verleihen Ihren Ausdrucken oder sonstigen
Bedeutung von Farben 1 Ihr Drucker bietet Ihnen die Möglichkeit, Farben als Kommunikationsmittel einzusetzen. Farben wecken die Aufmerksamkeit, schaffen Respekt und verleihen Ihren Ausdrucken oder sonstigen
How to do? Projekte - Zeiterfassung
 How to do? Projekte - Zeiterfassung Stand: Version 4.0.1, 18.03.2009 1. EINLEITUNG...3 2. PROJEKTE UND STAMMDATEN...4 2.1 Projekte... 4 2.2 Projektmitarbeiter... 5 2.3 Tätigkeiten... 6 2.4 Unterprojekte...
How to do? Projekte - Zeiterfassung Stand: Version 4.0.1, 18.03.2009 1. EINLEITUNG...3 2. PROJEKTE UND STAMMDATEN...4 2.1 Projekte... 4 2.2 Projektmitarbeiter... 5 2.3 Tätigkeiten... 6 2.4 Unterprojekte...
Fernseher Bild Bildschirm Computergeräte. Festplatte CD DVD Eingabegerät. Computertasten Mauszeiger Cursor rechten Maustaste
 Lückenfüller Arbeitsblatt 2 - Der Computer Nadine Roth CC BY-NC-SA Der Computer Der Monitor: - Der Monitor ist einem Fernseher ganz ähnlich. - Er zeigt dir als Bild alle Programme, Spiele und andere Dinge,
Lückenfüller Arbeitsblatt 2 - Der Computer Nadine Roth CC BY-NC-SA Der Computer Der Monitor: - Der Monitor ist einem Fernseher ganz ähnlich. - Er zeigt dir als Bild alle Programme, Spiele und andere Dinge,
Umgang mit Schaubildern am Beispiel Deutschland surft
 -1- Umgang mit Schaubildern am Beispiel Deutschland surft Im Folgenden wird am Beispiel des Schaubildes Deutschland surft eine Lesestrategie vorgestellt. Die Checkliste zur Vorgehensweise kann im Unterricht
-1- Umgang mit Schaubildern am Beispiel Deutschland surft Im Folgenden wird am Beispiel des Schaubildes Deutschland surft eine Lesestrategie vorgestellt. Die Checkliste zur Vorgehensweise kann im Unterricht
2.8 Grenzflächeneffekte
 - 86-2.8 Grenzflächeneffekte 2.8.1 Oberflächenspannung An Grenzflächen treten besondere Effekte auf, welche im Volumen nicht beobachtbar sind. Die molekulare Grundlage dafür sind Kohäsionskräfte, d.h.
- 86-2.8 Grenzflächeneffekte 2.8.1 Oberflächenspannung An Grenzflächen treten besondere Effekte auf, welche im Volumen nicht beobachtbar sind. Die molekulare Grundlage dafür sind Kohäsionskräfte, d.h.
Abgestufte Lernhilfen
 Abgestufte Lernhilfen Checkliste für die Beobachtungen: o o o o o Farbe des Indikators bei bei Zugabe zu Natronlauge Temperatur vor Zugabe der Salzsäure Farbveränderungen bei Zugabe der Salzsäure Temperaturveränderungen
Abgestufte Lernhilfen Checkliste für die Beobachtungen: o o o o o Farbe des Indikators bei bei Zugabe zu Natronlauge Temperatur vor Zugabe der Salzsäure Farbveränderungen bei Zugabe der Salzsäure Temperaturveränderungen
3. Beschreibe wie eine Mondfinsternis entstehen kann. + möglichst exakte, beschriftete Skizze
 Probetest 1 1. Wann wird Licht für uns sichtbar? (2 Möglichkeiten) 2. Den Lichtkegel eines Scheinwerfers sieht man besser wenn a) Rauch in der Luft ist b) die Luft völlig klar ist c) Nebeltröpfchen in
Probetest 1 1. Wann wird Licht für uns sichtbar? (2 Möglichkeiten) 2. Den Lichtkegel eines Scheinwerfers sieht man besser wenn a) Rauch in der Luft ist b) die Luft völlig klar ist c) Nebeltröpfchen in
Kurzanleitung. MEYTON Aufbau einer Internetverbindung. 1 Von 11
 Kurzanleitung MEYTON Aufbau einer Internetverbindung 1 Von 11 Inhaltsverzeichnis Installation eines Internetzugangs...3 Ist mein Router bereits im MEYTON Netzwerk?...3 Start des YAST Programms...4 Auswahl
Kurzanleitung MEYTON Aufbau einer Internetverbindung 1 Von 11 Inhaltsverzeichnis Installation eines Internetzugangs...3 Ist mein Router bereits im MEYTON Netzwerk?...3 Start des YAST Programms...4 Auswahl
Diagnostisches Interview zur Bruchrechnung
 Diagnostisches Interview zur Bruchrechnung (1) Tortendiagramm Zeigen Sie der Schülerin/dem Schüler das Tortendiagramm. a) Wie groß ist der Teil B des Kreises? b) Wie groß ist der Teil D des Kreises? (2)
Diagnostisches Interview zur Bruchrechnung (1) Tortendiagramm Zeigen Sie der Schülerin/dem Schüler das Tortendiagramm. a) Wie groß ist der Teil B des Kreises? b) Wie groß ist der Teil D des Kreises? (2)
Oxidation und Reduktion Redoxreaktionen Blatt 1/5
 Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Studieren- Erklärungen und Tipps
 Studieren- Erklärungen und Tipps Es gibt Berufe, die man nicht lernen kann, sondern für die man ein Studium machen muss. Das ist zum Beispiel so wenn man Arzt oder Lehrer werden möchte. Hat ihr Kind das
Studieren- Erklärungen und Tipps Es gibt Berufe, die man nicht lernen kann, sondern für die man ein Studium machen muss. Das ist zum Beispiel so wenn man Arzt oder Lehrer werden möchte. Hat ihr Kind das
Dieser Ablauf soll eine Hilfe für die tägliche Arbeit mit der SMS Bestätigung im Millennium darstellen.
 Millennium SMS Service Schnellübersicht Seite 1 von 6 1. Tägliche Arbeiten mit der SMS Bestätigung Dieser Ablauf soll eine Hilfe für die tägliche Arbeit mit der SMS Bestätigung im Millennium darstellen.
Millennium SMS Service Schnellübersicht Seite 1 von 6 1. Tägliche Arbeiten mit der SMS Bestätigung Dieser Ablauf soll eine Hilfe für die tägliche Arbeit mit der SMS Bestätigung im Millennium darstellen.
Säure-Base Titrationen. (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen)
 Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Kapitel 13: Laugen und Neutralisation
 Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Die Sch. kennen die Zusammensetzung von Luft und können die verschiedenen Gase per Formel benennen.
 Anleitung LP Ziel: Die Sch. kennen die Zusammensetzung von Luft und können die verschiedenen Gase per Formel benennen. Arbeitsauftrag: Textblatt lesen lassen und Lücken ausfüllen mit Hilfe der zur Verfügung
Anleitung LP Ziel: Die Sch. kennen die Zusammensetzung von Luft und können die verschiedenen Gase per Formel benennen. Arbeitsauftrag: Textblatt lesen lassen und Lücken ausfüllen mit Hilfe der zur Verfügung
Erfahrungen mit Hartz IV- Empfängern
 Erfahrungen mit Hartz IV- Empfängern Ausgewählte Ergebnisse einer Befragung von Unternehmen aus den Branchen Gastronomie, Pflege und Handwerk Pressegespräch der Bundesagentur für Arbeit am 12. November
Erfahrungen mit Hartz IV- Empfängern Ausgewählte Ergebnisse einer Befragung von Unternehmen aus den Branchen Gastronomie, Pflege und Handwerk Pressegespräch der Bundesagentur für Arbeit am 12. November
Schritte 4. Lesetexte 13. Kosten für ein Girokonto vergleichen. 1. Was passt? Ordnen Sie zu.
 Kosten für ein Girokonto vergleichen 1. Was passt? Ordnen Sie zu. a. die Buchung, -en b. die Auszahlung, -en c. der Dauerauftrag, - e d. die Überweisung, -en e. die Filiale, -n f. der Kontoauszug, - e
Kosten für ein Girokonto vergleichen 1. Was passt? Ordnen Sie zu. a. die Buchung, -en b. die Auszahlung, -en c. der Dauerauftrag, - e d. die Überweisung, -en e. die Filiale, -n f. der Kontoauszug, - e
SICHERN DER FAVORITEN
 Seite 1 von 7 SICHERN DER FAVORITEN Eine Anleitung zum Sichern der eigenen Favoriten zur Verfügung gestellt durch: ZID Dezentrale Systeme März 2010 Seite 2 von 7 Für die Datensicherheit ist bekanntlich
Seite 1 von 7 SICHERN DER FAVORITEN Eine Anleitung zum Sichern der eigenen Favoriten zur Verfügung gestellt durch: ZID Dezentrale Systeme März 2010 Seite 2 von 7 Für die Datensicherheit ist bekanntlich
Zustände der Elektronen sind Orbitale, die durch 4 Quantenzahlen
 Wiederholung der letzten Vorlesungsstunde: Thema: Das wellenmechanische h Atommodell (Orbitalmodell) ll) Zustände der Elektronen sind Orbitale, die durch 4 Quantenzahlen beschrieben werden, Hauptquantenzahl
Wiederholung der letzten Vorlesungsstunde: Thema: Das wellenmechanische h Atommodell (Orbitalmodell) ll) Zustände der Elektronen sind Orbitale, die durch 4 Quantenzahlen beschrieben werden, Hauptquantenzahl
Inkrementelles Backup
 Inkrementelles Backup Im Gegensatz zu einer kompletten Sicherung aller Daten werden bei einer inkrementellen Sicherung immer nur die Dateien gesichert, die seit der letzten inkrementellen Sicherung neu
Inkrementelles Backup Im Gegensatz zu einer kompletten Sicherung aller Daten werden bei einer inkrementellen Sicherung immer nur die Dateien gesichert, die seit der letzten inkrementellen Sicherung neu
Wichtig ist die Originalsatzung. Nur was in der Originalsatzung steht, gilt. Denn nur die Originalsatzung wurde vom Gericht geprüft.
 Das ist ein Text in leichter Sprache. Hier finden Sie die wichtigsten Regeln für den Verein zur Förderung der Autonomie Behinderter e. V.. Das hier ist die Übersetzung der Originalsatzung. Es wurden nur
Das ist ein Text in leichter Sprache. Hier finden Sie die wichtigsten Regeln für den Verein zur Förderung der Autonomie Behinderter e. V.. Das hier ist die Übersetzung der Originalsatzung. Es wurden nur
Allotrope Kohlenstoffmodifikationen. Ein Vortrag von Patrick Knicknie. Datum: 04.05.06 Raum:112
 Allotrope Kohlenstoffmodifikationen Ein Vortrag von Patrick Knicknie Datum: 04.05.06 Raum:112 Themen: 1. Was ist Allotrop? 2. Unterschiedliche Kohlenstoffmodifikationen 3. Der Graphit 4. Der Diamant 5.
Allotrope Kohlenstoffmodifikationen Ein Vortrag von Patrick Knicknie Datum: 04.05.06 Raum:112 Themen: 1. Was ist Allotrop? 2. Unterschiedliche Kohlenstoffmodifikationen 3. Der Graphit 4. Der Diamant 5.
Stellen Sie bitte den Cursor in die Spalte B2 und rufen die Funktion Sverweis auf. Es öffnet sich folgendes Dialogfenster
 Es gibt in Excel unter anderem die so genannten Suchfunktionen / Matrixfunktionen Damit können Sie Werte innerhalb eines bestimmten Bereichs suchen. Als Beispiel möchte ich die Funktion Sverweis zeigen.
Es gibt in Excel unter anderem die so genannten Suchfunktionen / Matrixfunktionen Damit können Sie Werte innerhalb eines bestimmten Bereichs suchen. Als Beispiel möchte ich die Funktion Sverweis zeigen.
Festigkeit von FDM-3D-Druckteilen
 Festigkeit von FDM-3D-Druckteilen Häufig werden bei 3D-Druck-Filamenten die Kunststoff-Festigkeit und physikalischen Eigenschaften diskutiert ohne die Einflüsse der Geometrie und der Verschweißung der
Festigkeit von FDM-3D-Druckteilen Häufig werden bei 3D-Druck-Filamenten die Kunststoff-Festigkeit und physikalischen Eigenschaften diskutiert ohne die Einflüsse der Geometrie und der Verschweißung der
Mit der Maus im Menü links auf den Menüpunkt 'Seiten' gehen und auf 'Erstellen klicken.
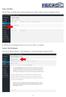 Seite erstellen Mit der Maus im Menü links auf den Menüpunkt 'Seiten' gehen und auf 'Erstellen klicken. Es öffnet sich die Eingabe Seite um eine neue Seite zu erstellen. Seiten Titel festlegen Den neuen
Seite erstellen Mit der Maus im Menü links auf den Menüpunkt 'Seiten' gehen und auf 'Erstellen klicken. Es öffnet sich die Eingabe Seite um eine neue Seite zu erstellen. Seiten Titel festlegen Den neuen
Entwicklung nach der Geburt
 Entwicklung nach der Geburt Entwicklung des Babys nach der Geburt. Wie sich ein Baby in den ersten Monaten entwickelt,verändert und was sich in ihren ersten 12 Monaten so alles tut. Entwicklungsphasen
Entwicklung nach der Geburt Entwicklung des Babys nach der Geburt. Wie sich ein Baby in den ersten Monaten entwickelt,verändert und was sich in ihren ersten 12 Monaten so alles tut. Entwicklungsphasen
PTV VISWALK TIPPS UND TRICKS PTV VISWALK TIPPS UND TRICKS: VERWENDUNG DICHTEBASIERTER TEILROUTEN
 PTV VISWALK TIPPS UND TRICKS PTV VISWALK TIPPS UND TRICKS: VERWENDUNG DICHTEBASIERTER TEILROUTEN Karlsruhe, April 2015 Verwendung dichte-basierter Teilrouten Stellen Sie sich vor, in einem belebten Gebäude,
PTV VISWALK TIPPS UND TRICKS PTV VISWALK TIPPS UND TRICKS: VERWENDUNG DICHTEBASIERTER TEILROUTEN Karlsruhe, April 2015 Verwendung dichte-basierter Teilrouten Stellen Sie sich vor, in einem belebten Gebäude,
Alle Schlüssel-Karten (blaue Rückseite) werden den Schlüssel-Farben nach sortiert und in vier getrennte Stapel mit der Bildseite nach oben gelegt.
 Gentlemen", bitte zur Kasse! Ravensburger Spiele Nr. 01 264 0 Autoren: Wolfgang Kramer und Jürgen P. K. Grunau Grafik: Erhard Dietl Ein Gaunerspiel für 3-6 Gentlemen" ab 10 Jahren Inhalt: 35 Tresor-Karten
Gentlemen", bitte zur Kasse! Ravensburger Spiele Nr. 01 264 0 Autoren: Wolfgang Kramer und Jürgen P. K. Grunau Grafik: Erhard Dietl Ein Gaunerspiel für 3-6 Gentlemen" ab 10 Jahren Inhalt: 35 Tresor-Karten
Lineare Gleichungssysteme
 Lineare Gleichungssysteme 1 Zwei Gleichungen mit zwei Unbekannten Es kommt häufig vor, dass man nicht mit einer Variablen alleine auskommt, um ein Problem zu lösen. Das folgende Beispiel soll dies verdeutlichen
Lineare Gleichungssysteme 1 Zwei Gleichungen mit zwei Unbekannten Es kommt häufig vor, dass man nicht mit einer Variablen alleine auskommt, um ein Problem zu lösen. Das folgende Beispiel soll dies verdeutlichen
Jede Zahl muss dabei einzeln umgerechnet werden. Beginnen wir also ganz am Anfang mit der Zahl,192.
 Binäres und dezimales Zahlensystem Ziel In diesem ersten Schritt geht es darum, die grundlegende Umrechnung aus dem Dezimalsystem in das Binärsystem zu verstehen. Zusätzlich wird auch die andere Richtung,
Binäres und dezimales Zahlensystem Ziel In diesem ersten Schritt geht es darum, die grundlegende Umrechnung aus dem Dezimalsystem in das Binärsystem zu verstehen. Zusätzlich wird auch die andere Richtung,
Der Kalender im ipad
 Der Kalender im ipad Wir haben im ipad, dem ipod Touch und dem iphone, sowie auf dem PC in der Cloud einen Kalender. Die App ist voreingestellt, man braucht sie nicht laden. So macht es das ipad leicht,
Der Kalender im ipad Wir haben im ipad, dem ipod Touch und dem iphone, sowie auf dem PC in der Cloud einen Kalender. Die App ist voreingestellt, man braucht sie nicht laden. So macht es das ipad leicht,
Kreatives Occhi. - V o r s p a n n - Alle Knoten und Knüpfelemente sowie ihre Verwendbarkeit. Die Knoten
 Kreatives Occhi - V o r s p a n n - Alle Knoten und Knüpfelemente sowie ihre Verwendbarkeit Die Knoten Der Doppelknoten: Er wird mit nur 1 Schiffchen gearbeitet (s. page Die Handhabung der Schiffchen )
Kreatives Occhi - V o r s p a n n - Alle Knoten und Knüpfelemente sowie ihre Verwendbarkeit Die Knoten Der Doppelknoten: Er wird mit nur 1 Schiffchen gearbeitet (s. page Die Handhabung der Schiffchen )
Die Post hat eine Umfrage gemacht
 Die Post hat eine Umfrage gemacht Bei der Umfrage ging es um das Thema: Inklusion Die Post hat Menschen mit Behinderung und Menschen ohne Behinderung gefragt: Wie zufrieden sie in dieser Gesellschaft sind.
Die Post hat eine Umfrage gemacht Bei der Umfrage ging es um das Thema: Inklusion Die Post hat Menschen mit Behinderung und Menschen ohne Behinderung gefragt: Wie zufrieden sie in dieser Gesellschaft sind.
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Wortschema Reaktionsschema Beispiel 1: Kupfer und Schwefel Vorzahlen
 6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
Dow Jones am 13.06.08 im 1-min Chat
 Dow Jones am 13.06.08 im 1-min Chat Dieser Ausschnitt ist eine Formation: Wechselstäbe am unteren Bollinger Band mit Punkt d über dem 20-er GD nach 3 tieferen Hoch s. Wenn ich einen Ausbruch aus Wechselstäben
Dow Jones am 13.06.08 im 1-min Chat Dieser Ausschnitt ist eine Formation: Wechselstäbe am unteren Bollinger Band mit Punkt d über dem 20-er GD nach 3 tieferen Hoch s. Wenn ich einen Ausbruch aus Wechselstäben
Häufig wiederkehrende Fragen zur mündlichen Ergänzungsprüfung im Einzelnen:
 Mündliche Ergänzungsprüfung bei gewerblich-technischen und kaufmännischen Ausbildungsordnungen bis zum 31.12.2006 und für alle Ausbildungsordnungen ab 01.01.2007 Am 13. Dezember 2006 verabschiedete der
Mündliche Ergänzungsprüfung bei gewerblich-technischen und kaufmännischen Ausbildungsordnungen bis zum 31.12.2006 und für alle Ausbildungsordnungen ab 01.01.2007 Am 13. Dezember 2006 verabschiedete der
Primzahlen und RSA-Verschlüsselung
 Primzahlen und RSA-Verschlüsselung Michael Fütterer und Jonathan Zachhuber 1 Einiges zu Primzahlen Ein paar Definitionen: Wir bezeichnen mit Z die Menge der positiven und negativen ganzen Zahlen, also
Primzahlen und RSA-Verschlüsselung Michael Fütterer und Jonathan Zachhuber 1 Einiges zu Primzahlen Ein paar Definitionen: Wir bezeichnen mit Z die Menge der positiven und negativen ganzen Zahlen, also
Freitag Version 42. ein Spiel für (2)3-5 SpielerInnen von Friedemann Friese
 Freitag Version 42 ein Spiel für (2)3-5 SpielerInnen von Friedemann Friese Spielmaterial: 5 Aktiensorten mit je 25 Markern (grün, rot, blau, gelb, lila) 5 andere Marker in den gleichen Farben als Aktienpreise.
Freitag Version 42 ein Spiel für (2)3-5 SpielerInnen von Friedemann Friese Spielmaterial: 5 Aktiensorten mit je 25 Markern (grün, rot, blau, gelb, lila) 5 andere Marker in den gleichen Farben als Aktienpreise.
Zwischenablage (Bilder, Texte,...)
 Zwischenablage was ist das? Informationen über. die Bedeutung der Windows-Zwischenablage Kopieren und Einfügen mit der Zwischenablage Vermeiden von Fehlern beim Arbeiten mit der Zwischenablage Bei diesen
Zwischenablage was ist das? Informationen über. die Bedeutung der Windows-Zwischenablage Kopieren und Einfügen mit der Zwischenablage Vermeiden von Fehlern beim Arbeiten mit der Zwischenablage Bei diesen
1. Weniger Steuern zahlen
 1. Weniger Steuern zahlen Wenn man arbeitet, zahlt man Geld an den Staat. Dieses Geld heißt Steuern. Viele Menschen zahlen zu viel Steuern. Sie haben daher wenig Geld für Wohnung, Gewand oder Essen. Wenn
1. Weniger Steuern zahlen Wenn man arbeitet, zahlt man Geld an den Staat. Dieses Geld heißt Steuern. Viele Menschen zahlen zu viel Steuern. Sie haben daher wenig Geld für Wohnung, Gewand oder Essen. Wenn
Was ich als Bürgermeister für Lübbecke tun möchte
 Wahlprogramm in leichter Sprache Was ich als Bürgermeister für Lübbecke tun möchte Hallo, ich bin Dirk Raddy! Ich bin 47 Jahre alt. Ich wohne in Hüllhorst. Ich mache gerne Sport. Ich fahre gerne Ski. Ich
Wahlprogramm in leichter Sprache Was ich als Bürgermeister für Lübbecke tun möchte Hallo, ich bin Dirk Raddy! Ich bin 47 Jahre alt. Ich wohne in Hüllhorst. Ich mache gerne Sport. Ich fahre gerne Ski. Ich
Die Einheit der Atommasse m ist u. Das ist der 12. Teil der Masse eines Kohlenstoffatoms. 1 u = 1,6608 * 10-27 kg m(h) = 1 u
 Analytische Chemie Stöchiometrie Absolute Atommasse Die Einheit der Atommasse m ist u. Das ist der 12. Teil der Masse eines Kohlenstoffatoms. 1 u = 1,6608 * 10-27 kg m() = 1 u Stoffmenge n Die Stoffmenge
Analytische Chemie Stöchiometrie Absolute Atommasse Die Einheit der Atommasse m ist u. Das ist der 12. Teil der Masse eines Kohlenstoffatoms. 1 u = 1,6608 * 10-27 kg m() = 1 u Stoffmenge n Die Stoffmenge
icloud nicht neu, aber doch irgendwie anders
 Kapitel 6 In diesem Kapitel zeigen wir Ihnen, welche Dienste die icloud beim Abgleich von Dateien und Informationen anbietet. Sie lernen icloud Drive kennen, den Fotostream, den icloud-schlüsselbund und
Kapitel 6 In diesem Kapitel zeigen wir Ihnen, welche Dienste die icloud beim Abgleich von Dateien und Informationen anbietet. Sie lernen icloud Drive kennen, den Fotostream, den icloud-schlüsselbund und
3.2 Spiegelungen an zwei Spiegeln
 3 Die Theorie des Spiegelbuches 45 sehen, wenn die Person uns direkt gegenüber steht. Denn dann hat sie eine Drehung um die senkrechte Achse gemacht und dabei links und rechts vertauscht. 3.2 Spiegelungen
3 Die Theorie des Spiegelbuches 45 sehen, wenn die Person uns direkt gegenüber steht. Denn dann hat sie eine Drehung um die senkrechte Achse gemacht und dabei links und rechts vertauscht. 3.2 Spiegelungen
Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch. Reinstoff, Element, Verbindung. Zweiatomige Elemente.
 1 1 Einteilung der Stoffe: Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Stoff Reinstoff Mischen Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b.
1 1 Einteilung der Stoffe: Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Stoff Reinstoff Mischen Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b.
Penelope. Bügel BH und Pant
 Penelope Bügel BH und Pant In der Farbe weiß ist Penelope ein wunderschöner, modischer Klassiker wie er immer wieder gesucht wird. In der Modefarbe atlantic ist die Serie ein absoluter Hingucker. Der Bügel-Bh
Penelope Bügel BH und Pant In der Farbe weiß ist Penelope ein wunderschöner, modischer Klassiker wie er immer wieder gesucht wird. In der Modefarbe atlantic ist die Serie ein absoluter Hingucker. Der Bügel-Bh
Erklärung zum Internet-Bestellschein
 Erklärung zum Internet-Bestellschein Herzlich Willkommen bei Modellbahnbau Reinhardt. Auf den nächsten Seiten wird Ihnen mit hilfreichen Bildern erklärt, wie Sie den Internet-Bestellschein ausfüllen und
Erklärung zum Internet-Bestellschein Herzlich Willkommen bei Modellbahnbau Reinhardt. Auf den nächsten Seiten wird Ihnen mit hilfreichen Bildern erklärt, wie Sie den Internet-Bestellschein ausfüllen und
Wie oft soll ich essen?
 Wie oft soll ich essen? Wie sollen Sie sich als Diabetiker am besten ernähren? Gesunde Ernährung für Menschen mit Diabetes unterscheidet sich nicht von gesunder Ernährung für andere Menschen. Es gibt nichts,
Wie oft soll ich essen? Wie sollen Sie sich als Diabetiker am besten ernähren? Gesunde Ernährung für Menschen mit Diabetes unterscheidet sich nicht von gesunder Ernährung für andere Menschen. Es gibt nichts,
