HTLV BLOT 2.4 WESTERN BLOT ASSAY
|
|
|
- Felix Meinhardt
- vor 8 Jahren
- Abrufe
Transkript
1 BEDEUTUNG DER VERWENDETEN SYMBOLE Bei Produkten und Verpackungen von MP Diagnostics werden die folgenden grafischen Symbole verwendet. Die Symbole entsprechen den bei medizinischen Instrumenten und deren Verpackungen üblicherweise verwendeten Symbolen. Eine umfassende Symbolerklärung enthält die Britische und Europäische Norm BS EN 980: HTLV BLOT 2.4 WESTERN BLOT ASSAY REVISIONSDATUM: 05/05 MAK 0011-GER-0 (Kit für 18 Tests) : (Kit für 36 Tests) : NAME UND VERWENDUNGSZWECK Hinweis: Änderungen hervorgehoben. Der MP Diagnostics (MPD) HTLV BLOT 2.4 ist ein qualitativer Enzym-Immunoassay für den in vitro Nachweis von Antikörpern gegen HTLV-I und HTLV-II in humanem Serum und Plasma. Durch seine höhere Spezifität wird er als Zusatztest eingesetzt, wenn humane Serum- bzw. Plasmaproben bei der Anwendung von Screening-Tests, z.b. ELISA (Enzyme-Linked Immunosorbent Assay) wiederholt positiv getestet wurden. Verwendbar bis Synonym hierfür: Verfalldatum Batch-Nummer Synonyme hierfür: Chargennummer Referenznummer Temperaturbegrenzung Hersteller Ausreichend für <n> Tests Nicht wiederverwenden In vitro - Diagnostikum Katalognummer Achtung. Siehe Anleitung Autorisierte Vertretung in der Europäische Gemeinschaft Gebrauchsanweisung beachten EINFÜHRUNG Kürzlich durchgeführte epidemiologische Studien in den Vereinigten Staaten und Europa haben eine gemischte Prävalenz von HTLV-I und HTLV-II unter verschiedenen risikogefährdeten Populationen, beispielsweise unter Konsumenten intravenöser Drogen, bestätigt. Es stehen eine Reihe von Screening-Tests zum Nachweis von HTLV-I/II zur Verfügung. Wiederholt reaktive Ergebnisse bei Screening-Tests erfordern zusätzliche und noch spezifischere Tests, um die HTLV-I- bzw. HTLV-II-Seropositivität nachzuweisen. Entsprechende Zusatztests dienen zum Nachweis von Antikörpern gegen Core- (gag) und Envelope-Proteine (env) von HTLV-I und HTLV-II. Als Zusatztest werden häufig Western- Blot-Streifen verwendet, welche native virale HTLV-I-Antigene enthalten. Jedoch ist aufgrund des Fehlens nativer Envelope- Antigene beim klassischen HTLV-I Western Blot oft der Einsatz von Methoden der Radioimmun-Präzipitation notwendig, um das Vorliegen von HTLV-I/II-Antikörpern nachzuweisen. Zur Differenzierung zwischen HTLV-I und HTLV-II seropositiven Proben sind zusätzliche Assays (z. B. spezifische Peptide, ELISAs, PCR) erforderlich. Unkomplizierte serologische Zusatztests, die sich durch hohe Spezifität und Sensitivität auszeichnen, sind daher notwendig, um einen schnellen Nachweis und eine Unterscheidung zwischen HTLV-I und HTLV-II seropositiven Proben zu erhalten. Der MP Diagnostics HTLV BLOT 2.4 verfügt über verbesserte Spezifität und Sensitivität beim Nachweis und bei der Differenzierung zwischen HTLV-I- und HTLV-II-Seroreaktivität. Dies wird durch die auf den Streifen enthaltenen rekombinanten Envelope-Proteine MTA-1, spezifisch für HTLV-I (rgp46-l), K55, spezifisch für HTLV-II (rgp46-ii), und GD21, ein für HTLV-I und HTLV-II spezifisches Epitop, erreicht. Außerdem enthält jeder Streifen eine Probenzugabe-Kontrolle, um das durch Handhabungsfehler bedingte Risiko falsch-negativer Testergebnisse zu senken. Der MP Diagnostics HTLV BLOT 2.4 dient als zusätzlicher Antikörper-Test für Proben, die sich bei initialen Screening-Tests zum Nachweis von HTLV-I/II-Antikörpern wiederholt reaktiv gezeigt haben. Folgende serologische Profile lassen sich mit dem MP Diagnostics HTLV BLOT 2.4 bestimmen: HTLVseropositiv, HTLV-I-seropositiv, HTLV-II-seropositiv, Seronegativ und Fraglich. 1 CHEMISCHE UND BIOLOGISCHE GRUNDLAGEN DES VERFAHRENS Die Nitrozellulose-Streifen enthalten HTLV-I-Virusproteine, die aus nativen inaktivierten getrennten Viruspartikeln und gentechnisch hergestellten Proteinen gewonnen werden. Die einzelnen Nitrozellulose-Streifen werden mit verdünnten Humanserum- bzw. -plasmaproben sowie den Kontrollen inkubiert. Liegen spezifische Antikörper gegen HTLV-I/II in den Proben vor, binden diese an die HTLV-I/II-Proteine auf den Streifen. Nichtgebundenes Material wird durch Waschen von den Streifen entfernt, während Antikörper, die sich spezifisch an HTLV-Proteine binden, durch eine Folge von Reaktionen mit Anti-Human-IgG der Ziege, das an alkalische Phosphatase konjugiert ist, und dem Substrat BCIP/NBT sichtbar gemacht werden können. Mit diesem Verfahren lassen sich auch sehr geringe Mengen HTLV-Antikörper im Serum oder Plasma nachweisen.
2 EINZELKOMPONENTEN DES TESTS Komponentenbeschreibung NITROZELLULOSE- STREIFEN Enthält HTLV-I-Viruslysat, rekombinante Envelope- Antigene und einen Probenzugabe-Kontrollbereich (anti-humanes IgG). Trocken lagern und vor Licht schützen. NICHTREAKTIVE KONTROLLE Inaktiviertes normales Humanserum, nichtreaktiv auf Anti-HCV, Anti-HIV-1/2, Anti- HTLV-I/II und HBsAg. Enthält Natriumazid und Thimerosal als Konservierungsstoffe. HOCHREAKTIVE KONTROLLE I Inaktiviertes Humanserum mit einem hohen Antikörpertiter gegen HTLV-I und nichtreaktiv auf Anti-HCV, Anti-HIV-1/2 und HBsAg. Enthält Natriumazid und Thimerosal als Konservierungsstoffe. HOCHREAKTIVE KONTROLLE II Inaktiviertes Humanserum mit einem hohen Antikörpertiter gegen HTLV-II und nichtreaktiv auf Anti-HCV, Anti-HIV-1/2 und HBsAg. Enthält Natriumazid und Thimerosal als Konservierungsstoffe. LYOPHILISIERTER STAMMPUFFER In hochreinem destillierten Wasser aufzulösen. Tris-Puffer mit hitzeinaktivierten tierischen und nichttierischen Proteinen. Enthält Thimerosal als Konservierungsstoff. WASCHPUFFER- KONZENTRAT (20fach) Tris-Puffer mit Tween-20. Enthält Thimerosal als Konservierungsstoff. KONJUGAT Anti-Human-IgG von der Ziege konjugiert an alkalische Phosphatase. Liefermenge Lieferbar mit 18 oder 36 Teststreifen 1 Ampulle (80 Øl) 1 Ampulle (80 Øl) 1 Ampulle (80 Øl) 1 oder 2 Flaschen (auf je 100 ml aufzufüllen) 1 Flasche (70 ml) 1 Ampulle (120 Øl) Hinweis: SUBSTRAT Lösung aus 5-Brom-4-Chlor-3- Indolylphosphat (BCIP) und Nitrotetrazolium-Chloridblau (NBT). BLOTTING-PULVER Fettfreies Milchpulver Inkubationsschalen mit je 9 Vertiefungen (Wells) BEDIENUNGSHANDBUCH Pinzette Die enthaltene Reagenzienmenge ist ausreichend für vier Testläufe. WARNUNGEN UND VORSICHTSMASSNAHMEN 1. Nur für die in vitro Diagnostik. 2. Nur für Fachpersonal. 3. Bitte beachten Sie die Produktkennzeichnung hinsichtlich potenziell gefährlicher Komponenten. HINWEISE ZU GESUNDHEITLICHEN RISIKEN UND SICHERHEIT VORSICHT: Dieser Test enthält Bestandteile aus menschlichem Serum. Bei keiner Testmethode ist ausgeschlossen, dass mögliche Infektionen durch humane Blutprodukte übertragen werden können. BEHANDELN SIE ALLE PROBEN, DIE HOCHREAKTIVEN KONTROLLEN I und II SOWIE DIE NICHTREAKTIVEN KONTROLLEN ALS POTENZIELL INFEKTIÖSES MATERIAL. Es wird empfohlen, beim Umgang mit Bestandteilen und Testproben entsprechend den Grundsätzen der Guten Laborpraxis zu arbeiten. Das Material ist gemäß den vorgeschriebenen Sicherheitsmaßnahmen zu entsorgen. Die hochreaktiven Kontrollen I und II sowie die nichtreaktiven Kontrollen enthalten Thimerosal und Natriumazid, das Stammpuffer- und Waschpuffer-Konzentrat enthalten Thimerosal, während das Konjugat nur Natriumazid enthält. Natriumazid kann mit Kupfer und Blei, die in einigen Abwasserleitungen vorkommen, reagieren und explosive Salze bilden. Die in diesem Test verwendeten Mengen sind zwar gering, doch sollten azidhaltige Stoffe unter Beimengung relativ großer Wassermengen hinweggespült werden, damit sich in der Abwasserleitung keine Metallazide bilden. Folgende Risiko- Hinweise (R) sind entsprechend zu beachten: R20/21/22 1 Flasche (100 ml) 10 Packungen (je 1g) 2 oder 4 Schalen 1 Exemplar 1 Stück Gesundheitsschädlich beim Einatmen, Verschlucken und bei Berührung mit der Haut. Das Substrat enthält 5-Brom-4-Chlor-3-Indolylphosphat und Nitrotetrazolium-Chloridblau. Diese Substanzen werden laut den Direktiven der Europäischen Wirtschaftsgemeinschaft (EWG) als schädlich (Xn) eingestuft. Folgende Risiko-Hinweise (R) sind entsprechend zu beachten: R20/21/22 Gesundheitsschädlich bei Einatmung, Verschlucken und Hautkontakt. 2
3 1. Vermeiden Sie beim Öffnen oder bei der Entnahme aus den Originalampullen und -flaschen die mikrobielle Kontamination der Reagenzien. 2. Nicht mit dem Mund pipettieren. 3. Behandeln Sie alle Untersuchungsproben, Nitrozellulose- Streifen, hochreaktiven Kontrollen I und II und die nichtreaktiven Kontrollen als potenziell infektiöses Material. 4. Einmal-Handschuhe und Laborkittel tragen. Die Handschuhe als biologisch gefährliches (Biohazard-) Material entsorgen. Anschließend gründlich die Hände waschen. 5. Es wird dringend empfohlen, diesen Test nur unter einer Biohazard Schutzhaube durchzuführen. 6. Niemals in die Nähe von Lebensmitteln bringen. 7. Bei Augenkontakt sofort mit reichlich Wasser spülen und in ärztliche Behandlung begeben. 8. Beim Verschlucken kontaminierter Substanzen oder bei Materialkontakt mit offenen Hautstellen ist sofort ein Arzt aufzusuchen. 9. Verschüttete potenziell infektiöse Substanzen mit saugfähigem Papierhandtuch aufnehmen und den kontaminierten Bereich sofort mit 1 %-iger Natriumhypochlorit-Lösung abwischen. Natriumhypochlorit sollte nicht bei verschütteten säurehaltigen Substanzen angewendet werden, sofern der betreffende Bereich vorher nicht gründlich mit einem saugfähigen Papierhandtuch trockengewischt wurde. Verwendete Materialien (einschließlich Einmal-Handschuhe) sind als potenzielles Biohazard-Material zu entsorgen. Natriumhypochlorithaltiges Material nicht autoklavieren. 10. Alle benutzten und kontaminierten Materialien vor der Entsorgung bei 121 C und 103,42 kpa (15 p.s.i.) 30 Minuten autoklavieren. Alternativ können Materialien vor der Entsorgung als Biohazard Minuten in 5 %-iger Natriumhypochlorit-Lösung dekontaminiert werden. 11. Alle verwendeten Chemikalien und Reagenzien in mindestens 1 %-iger Natriumhypochlorit-Lösung dekontaminieren. Zur effektiven Dekontamination 30 Minuten darin ruhen lassen. 12. Es wird empfohlen, die Inkubationskammern nur einmal zu benutzen. HINWEISE ZUM TESTVERFAHREN 1. Optimale Testergebnisse erfordern ein STRENGES EINHALTEN des im Bedienungshandbuch beschriebenen Testverfahrens. Abweichungen vom Verfahren können die Ergebnisse verfälschen. 2. REAGENZIEN NICHT MODIFIZIERN UND KEINESFALLS REAGENZIEN ANDERER CHARGEN VERWENDEN. Zur Erzielung optimaler Ergebnisse sind Kontrollen, Konjugat und Western-Blot-Streifen aufeinander abgestimmt. Nur die mit dem Kit mitgelieferten Reagenzien verwenden. 3. Die Komponenten nicht nach dem Verfalldatum verwenden. 4. Beim Öffnen oder bei der Entnahme aus den Originalampullen und -flaschen die mikrobielle Kontamination der Reagenzien vermeiden. Dies führt ansonsten zu kürzerer Haltbarkeit des Kits und verfälschten Ergebnissen. Bei der Materialentnahme aus Ampullen sind sterile Arbeitsmittel, einschließlich der Pipetten und Pipettenspitzen, zu verwenden. 5. Bei jedem Test sind gleichzeitig mit den Patientenproben auch die Kontrollproben zu bestimmen. 6. Zur Vermeidung einer Kreuzkontamination ist bei der Entnahme aus Ampullen für jede Probe eine neue Pipettenspitze zu nehmen. 7. Die besten Testergebnisse werden erzielt, wenn alle Reagenzien im gekühlten Zustand entnommen und so bald wie möglich wieder bei 2-8 C gelagert werden. 8. Es wird empfohlen, Glasbehälter vor dem Gebrauch mit 2 M Salzsäure zu waschen und mit destilliertem oder entionisiertem Wasser gründlich nachzuspülen. 9. Zur Verdünnung von Reagenzien nur hochreines entionisiertes oder destilliertes Wasser verwenden. 10. Alle Reagenzien vor dem Gebrauch gut mischen. 11. Die Konjugat-Arbeitslösung, der verdünnte Waschpuffer und der Blotting-Puffer sollten erst kurz vor Gebrauch angesetzt werden. 12. Die Konjugat-Arbeitslösung ist in einem Polypropylen- Behälter oder -Becher anzusetzen. 13. Die Reagenzien während der Lagerung, Inkubationsphasen und Testdurchführung keinen konzentrierten Dämpfen chemischer Desinfektionsmittel (z.b. Hypochloritdämpfen) aussetzen. Die Farbreaktion wird durch den Kontakt inhibiert. Eine unnötige Lichtexposition der Reagenzien vermeiden. 14. Der Test ist möglichst bei Raumtemperatur (25 ± 3 C) durchzuführen. 15. Darauf achten, dass die Nummern auf den Streifen stets nach oben zeigen. 16. Bei Western Blot Assays darf kein Rotationsschüttler, sondern nur ein Wippschüttler verwendet werden. Anderenfalls kann die Genauigkeit der Testergebnisse leiden. Es wird eine Wippfrequenz von 12 bis 16 min -1 und ein Neigungswinkel von 5-10 empfohlen. 17. Beim Arbeiten mit Laborautomaten darauf achten, dass diese validiert sind. 18. Die Proben dürfen nicht direkt auf die Streifen gegeben werden. Zur Probenzugabe wird die Schale geneigt und die Proben werden am unteren Ende aufgetragen, wo sich die Pufferlösung sammelt. Dies verhindert das Auftreten dunkler Spots auf dem Streifen überall dort, wo die Probe aufgetragen wurde. 19. Zur Lagerung von Reagenzien und Proben keine Gefrierschänke mit Abtauautomatik verwenden. 3
4 HINWEISE ZUR LAGERUNG 1. Der MPD HTLV BLOT 2.4 Kit und seine Komponenten sind bei 2-8 C zu lagern. 2. Alle Reagenzien und Teststreifen sind bis zu dem auf dem Kit aufgedruckten Verfalldatum haltbar, sofern sie bei 2-8 C gelagert werden. Die Reagenzien nicht einfrieren. a) ANTIGEN-STREIFEN Die Antigen-Streifen soweit wie möglich vor Licht schützen. b) Reagenzien Die Reagenzien in den Originalampullen und -flaschen lagern und stets verschließen. Alle Reagenzien im gekühlten Zustand entnehmen und so bald wie möglich wieder bei 2-8 C lagern. Wird das Substrat bei 2-8 C gelagert, kann es zu Ausfällungen kommen. Die Testergebnisse werden dadurch nicht beeinflusst. Vorsicht: Das Substrat soweit wie möglich vor Licht schützen. PROBENENTNAHME, TRANSPORT UND LAGERUNG Zur Verwendung geeignet sind Serum- oder Plasmaproben, die mit EDTA, Heparin oder Natriumcitrat versetzt wurden. Vor der Lagerung sicherstellen, dass die festen Blutbestandteile abzentrifugiert wurden. Die Proben lassen sich bei 2-8 C lagern, sofern der Test innerhalb von 7 Tagen nach der Entnahme durchgeführt wird. Wird der Test mehr als 7 Tage nach der Probenentnahme durchgeführt, sollten die Proben bei mindestens -20 C eingefroren werden. Vorzugsweise sind klare, nichthämolysierte Proben zu verwenden. Lipämische, ikterische und (mit Partikeln) kontaminierte Proben sind vor dem Test zu filtern (0,45 Øm) oder zentrifugieren. Die Patientenseren können inaktiviert werden, jedoch ist dies nicht notwendig, um optimale Testergebnisse zu erhalten. Die Inaktivierung wird folgendermaßen durchgeführt: 1. Verschlusskappen der Serumbehälter lösen. 2. Das Serum für 30 Minuten in einem Wasserbad bei 56 C erhitzen. 3. Das Serum abkühlen lassen, bevor die Kappen wieder verschlossen werden. 4. Das Serum kann bis zur Analyse eingefroren werden. Es wird empfohlen, Patientenseren nicht mehrfach einzufrieren und aufzutauen. ZUSÄTZLICH ERFORDERLICHE MATERIALIEN (NICHT ENTHALTEN) Entionisiertes oder destilliertes Wasser Einmal-Handschuhe Wippschüttler (mit einer Schüttelfrequenz von 12 bis 16 min -1 und einem Neigungswinkel von 5-10 zum gleichmäßigen Waschen der Streifen) Pipetten und Pipettenspitzen ausreichender Größe. Aspirator mit Natriumhypochlorit-Auffangbehälter 56 C Wasserbad (optional) Natriumhypochlorit zur Dekontamination 1. VERDÜNNTE WASCHPUFFERLÖSUNG (a) Die VERDÜNNTE WASCHPUFFERLÖSUNG erst kurz vor Gebrauch ansetzen. (b) Das WASCHKONZENTRAT (20X) mit hochreinem destillierten Wasser im Verhältnis 1:19 verdünnen und gut mischen. 2. BLOTTING-PUFFER (a) Jede Flasche LYOPHILISIERTES STAMMPUFFER- KONZENTRAT mit 100 ml hochreinem destillierten Wasser auffüllen. Zum Auflösen gut mischen. Dieser REKONSTITUIERTE STAMMPUFFER ist 6 Wochen haltbar, sofern er bei 2-8 C gelagert wird. (b) Die VERDÜNNTE BLOTTINGPUFFERLÖSUNG erst kurz vor Gebrauch ansetzen. (c) Je 1 g BLOTTING-PULVER auf 20 ml REKONSTITUIERTE STAMMPUFFERLÖSUNG hinzugeben, die wie in Schritt 2(a) beschrieben vorbereitet wurde. Die Pufferlösung umrühren, bis sich das Pulver vollständig aufgelöst hat. (d) Vor der Entnahme erneut umrühren. 3. KONJUGAT-ARBEITSLÖSUNG Hinweis: Die Lösung in einem Behälter oder Becher aus Polypropylen ansetzen. (a) Die KONJUGAT-ARBEITSLÖSUNG erst kurz vor Gebrauch ansetzen. (b) Für das Ansetzen der KONJUGAT-ARBEITSLÖSUNG wird das KONJUGAT mit der BLOTTING- PUFFERLÖSUNG im Verhältnis 1:1000 verdünnt, zum Beispiel 10 Øl KONJUGAT auf 10 ml BLOTTING- PUFFER. 4. SUBSTRATLÖSUNG (gebrauchsfertig) (a) Die benötigte Menge direkt aus der Flasche entnehmen. Mit einer sauberen Pipette arbeiten. Nach Gebrauch fest verschließen. Hinweis: a) Alle verwendeten Chemikalien und Reagenzien immer in einen Auffangbehälter mit Natriumhypochlorit aspirieren. Vorsicht: b) Die Inkubation ist stets auf einem Wippschüttler durchzuführen. Bei einigen Proben entstehen dunkle Spots auf den Streifen an den Stellen, wo die Probe hinzugegeben wurde. Dies lässt sich vermeiden, wenn Folgendes beachtet wird: i. Die Probe erst nach Zugabe des BLOTTING-PUFFERS hinzugeben. ii. VORBEREITUNG DER REAGENZIEN TESTDURCHFÜHRUNG iii. Die Schale durch Anheben des oberen bzw. unteren Endes in eine leichte Schräglage bringen. Die Blotting- Pufferlösung strömt zum tieferen Ende der Schale. Die Probe dort hinzugeben, wo sich die Blotting-Pufferlösung angesammelt hat. Nach Zugabe aller Proben die Schale wieder flach abstellen. Die Streifen müssen während des Verfahrens stets feucht gehalten werden. Alternativ lassen sich die Proben auch am oberen oder unteren Ende der Vertiefungen (Wells) hinzugeben, wenn die Lage der Schale nicht verändert werden soll. Entstehen durch diese Vorgehensweise dunkle Spots auf den Streifen, werden die Testergebnisse dadurch nicht verfälscht. 4
5 Durchführung: 1. Die benötigte Anzahl STREIFEN vorsichtig mit der Pinzette dem Vorratsröhrchen entnehmen und mit der nummerierten Seite nach oben in die jeweils vorgesehene Vertiefung legen. Streifen für hochreaktive, schwachreaktive und nichtreaktive Kontrollen einbeziehen ml VERDÜNNTE WASCHPUFFERLÖSUNG in jede Vertiefung geben. 3. Die Streifen für mindestens 5 Minuten bei Raumtemperatur (25 ± 3 C) auf einem Wippschüttler inkubieren (Wippfrequenz von 12 bis 16 min -1 ). Die Waschpufferlösung aspirieren ml BLOTTING-PUFFERLÖSUNG in jede Vertiefung geben. 5. Jeweils 20 Øl Patientenserum oder Kontrolle in die entsprechenden Vertiefungen geben. 6. Die Schalenabdeckung auflegen und für 1 Stunde bei Raumtemperatur (25 ± 3 C) auf dem Wippschüttler inkubieren. 7. Die Abdeckung vorsichtig abnehmen, damit die Proben nicht etwa verspritzt oder vermischt werden. Die Schale leicht schräg stellen und das Reagenziengemisch aspirieren. Zur Vermeidung einer eventuellen Kreuzkontamination für jede Probe eine neue Aspiratorspitze nehmen. 8. Jeden Streifen dreimal mit 2 ml VERDÜNNTER WASCHPUFFERLÖSUNG abspülen und zwischen den Spülvorgängen jeweils 5 Minuten auf dem Wippschüttler einweichen lassen ml KONJUGAT-ARBEITSLÖSUNG in jede Vertiefung geben. 10. Die Schalenabdeckung auflegen und 1 Stunde bei Raumtemperatur (25 ± 3 C) auf dem Wippschüttler inkubieren. 11. KONJUGAT aus den Vertiefungen aspirieren. Abspülen wie in Schritt 8 beschrieben ml SUBSTRATLÖSUNG in jede Vertiefung geben. 13. Die Schalenabdeckung auflegen und für 15 Minuten auf dem Wippschüttler inkubieren. 14. Das SUBSTRAT aspirieren und die Streifen mindestens dreimal mit hochreinem destillierten Wasser abspülen, um die Reaktion zu stoppen. 15. Die Streifen vorsichtig mit der Pinzette entnehmen und auf Papiertücher legen. Mit Papiertüchern bedecken und abtrocknen. Alternativ können die Streifen zum Trocknen in den Vertiefungen belassen werden. 16. Die Streifen auf der Arbeitsfläche (nichtsaugendes weißes Papier) befestigen. Klebeband nicht über sichtbare Banden kleben. Die Banden bewerten (siehe Auswertung der Ergebnisse ). Die Streifen anschließend im Dunkeln lagern. 2 ml 5 Minuten 2 ml 20 Øl 60 Minuten 3 x 2 ml 2 ml 60 Minuten 3 x 2 ml 2 ml 15 Minuten 3 x 2 ml ZUSAMMENFASSUNG DER ARBEITSSCHRITTE Reagenzien Menge Dauer Nitrozellulose-Streifen 1 - Waschpufferlösung 2 ml 5 Minuten Blotting-Pufferlösung 2 ml - Probe 20 Øl 60 Minuten Waschpufferlösung 3 x 2 ml 3 x 5 Minuten Konjugat 2 ml 60 Minuten Waschpufferlösung 3 x 2 ml 3 x 5 Minuten Substratlösung 2 ml 15 Minuten (gebrauchsfertig) Destilliertes Wasser 3 x 2 ml - REAGENZIENVERBRAUCH BEI UNTERSCHIEDLICHER STREIFENANZAHL Reagenzien ANZAHL VERWENDETER STREIFEN x Waschpufferlösung (ml) 1x Blotting Pufferlösung (ml) Konjugat (Øl) Substrat (ml) Blotting-Pulver (g) QUALITÄTSKONTROLLE Es wird empfohlen, unabhängig von der Probenanzahl bei jedem Test die nichtreaktive und beide hochreaktiven Kontrollen durchzuführen. Folgende Kriterien müssen erfüllt sein, damit die Testergebnisse als valide betrachtet werden können. 1. NICHTREAKTIVE KONTROLLE Auf dem Streifen der nichtreaktiven Kontrolle dürfen keine HTLV-I/II-spezifischen Banden, rgp46-i, rgp46-ii oder GD21 erkennbar sein. Die Bande der Probenzugabe- Kontrolle (Anti-Human-IgG) muss vorhanden sein. 2. HOCHREAKTIVE KONTROLLE I Die Bande der Probenzugabe-Kontrolle sowie die Banden aller relevanten HTLV-I/II Molekulargewichte müssen erkennbar sein. Die relevanten HTLV-I-Banden, die vorhanden sein müssen, sind p19, p24, gp46, rgp46-i und GD21. Die gp46-bande ist diffus erkennbar. 3. HOCHREAKTIVE KONTROLLE II Die Bande der Probenzugabe-Kontrolle sowie die Banden aller relevanten HTLV-I/II Molekulargewichte müssen erkennbar sein. Die relevanten HTLV-Banden, die vorhanden sein müssen, sind p24, GD21 und rgp46-ii. 5
6 AUSWERTUNG DER ERGEBNISSE Die Bande der Probenzugabe-Kontrolle dient zur Überprüfung der erfolgten Probenzugabe bei einem Test. Das Fehlen dieser Bande deutet auf nicht erfolgte Proben-, Konjugat- oder Substratzugabe bzw. andere Handhabungsfehler hin. Die Banden auf den Streifen der hochreaktiven Kontrollen bestimmen. Diese Streifen werden danach zur Bestimmung der auf den Testproben-Streifen vorhandenen Banden verwendet. BANDENMUSTER 1. Keine Reaktivität auf HTLVspezifische Proteine. 2. Reaktivität auf GAG (p19 mit oder ohne p24) und zwei ENV (GD21 und rgp46-i) 3. Reaktivität auf GAG (p24 mit oder ohne p19) und zwei ENV (GD21 und rgp46-ii) 4. Reaktivität auf GAG (p19 und p24) und ENV (GD21) - HTLV-I SEROPOSITIV, wenn p19 p24 - HTLV-II SEROPOSITIV, wenn p19 < p24 5. HTLV-spezifische Banden erkennbar, entspricht aber nicht den Kriterien für HTLV-I-, HTLV- II- oder HTLV-seropositiv. Jedoch können folgende fragliche Bandenmuster als SERONEGATIV interpretiert werden: - HTLV-I GAG fragliche Western-Blot-Bandenmuster (HGIP) Erkennbar sind p19, p26, p28, p32, p36, p53, aber p24 und jegliches ENV-Protein fehlen. - Alle Kombinationen von GAG- Proteinen (p19, p26, p28, p32, p36, p53), aber p24 und jegliches ENV-Protein fehlen. - Alle einzelnen GAG-Proteine (p19, p24, p26, p28, p32, p36, p53) INTERPRETATION SERONEGATIV HTLV-I SEROPOSITIV HTLV-II SEROPOSITIV HTLV SEROPOSITIV* FRAGLICH** * Nicht-typisierbare HTLV-seropositive Ergebnisse können mit Hilfe des von Wiktor et al. entwickelten Algorithmus bei Fehlen von rgp46-i und rgp46-ii weiter untersucht werden. Mit diesem Algorithmus, bei dem mit der relativen Reaktivität von p19 und p24 gearbeitet wird, kann die Differenzierung der beiden Serotypen erfolgen. 7,11,12,13,14 ** Die Einstufung eines Testergebnisses als fraglich basiert auf den WHO-Richtlinien von Jedoch haben verschiedene Studien nahe gelegt, dass bestimmte fragliche Bandenmuster (wie aufgeführt), besonders bei gesunden Blutspendern, als seronegativ interpretiert werden können Eine Studie mit gesunden Blutspendern zeigte beispielsweise, dass HGIP sicher als seronegativ eingestuft werden kann. 26 Dennoch sind fragliche Bandenmuster bei Konsumenten intravenöser Drogen oder Blutspendern aus endemischen Gebieten und von Patienten mit neurologischen Krankheiten mit Vorsicht zu bewerten. 26,27 Proben mit Doppelinfektion sind zwar selten, können jedoch auch auftreten und dann entsprechend den obigen Kriterien differenziert werden. Die Bandenmuster dieser Proben zeigen die HTLV-I- und HTLV-II-Positivität. Aus dazu verfügbarem Datenmaterial ergibt sich, dass die Seroreaktivität auf rgp46-i für HTLV-I bzw. auf rgp46-ii für HTLV-II spezifisch ist. Daher sind Proben, die sich als reaktiv auf rgp46-i, rgp46-ii, GD21, p19 und p24 zeigen, als doppelinfiziert einzustufen. EINSCHRÄNKUNGEN FÜR DAS TESTVERFAHREN Optimale Testergebnisse erfordern ein strenges Einhalten des beschriebenen Testverfahrens. Eine abweichende Vorgehensweise kann die Ergebnisse verfälschen. Bei einem NEGATIVEN Ergebnis kann die Möglichkeit eines Kontakts oder einer Infektion mit HTLV-I oder HTLV-II nicht ausgeschlossen werden. FRAGLICHE Blots dürfen nicht als Grundlage für die Diagnose einer HTLV-I/II-Infektion dienen. Außerdem wurde bei nichtinfizierten Populationen mit niedrigem Risiko eine p19- sowie p24-seroreaktivität beobachtet, obwohl fragliche p24-ergebnisse sehr selten sind. Die Sensitivität von rgp46-i wird in Frankreich mit 95%, bei durch PCR bestätigten Proben in Jamaika und den Vereinigten Staaten mit 100% und bei HTLV-I seropositiven Blutspendern mit 98% angegeben. Die ermittelte Sensitivität von rgp46-ii beträgt bei durch PCR bestätigten Proben aus den Vereinigten Staaten 98%. Die Sensitivität wird insgesamt bei rgp46-i und rgp46-ii auf über 97% geschätzt. Der geringe Anteil an HTLV-I- und HTLV-II- Proben, die nicht reaktiv auf rgp46-i bzw. rgp46-ii sind, zeigt sich mindestens mit GD21 und einer weiteren GAG-Bande, p19 oder p24, reaktiv und entspricht somit den Kriterien für eine Einstufung als HTLV-seropositiv (Muster 4) bzw. -fraglich (Muster 5). Es wurden keine falsch-negativen Ergebnisse festgestellt. Zusatztests wie die PCR (HTLV-I und HTLV-II) können zur Unterscheidung zwischen HTLV-seropositiven Proben, die sich mit dem MPD HTLV BLOT 2.4 nicht als HTLV-I- oder HTLV-IIseropositiv bestimmen lassen (z. B. Muster 4), hilfreich sein. SPEZIFISCHE LEISTUNGSMERKMALE Die Leistungsfähigkeit des MPD HTLV BLOT 2.4 zum Nachweis von Antikörpern gegen HTLV-I und HTLV-II wurde mit HTLV-I/ II-seropositiven und -seronegativen Proben beurteilt und mit zwei Line-Immunoassays verglichen, die HTLV-I- und HTLV-II- Antigene (rekombinante Proteine oder Peptide) enthalten. Sensitivität Zur Bestimmung der Sensitivität des MPD HTLV BLOT 2.4 wurden Proben verwendet, die zuvor mit handelsüblichen ELISAs positiv auf HTLV-I- und/oder HTLV-II-Antikörper getestet worden waren. 6
7 A. Vergleich mit Line-Immunoassay 1 Beim Vergleich zwischen MPD HTLV BLOT 2.4 und Line- Immunoassay 1 (LI 1) mit positiven Proben (Quellen: Boston Biomedica, Inc., USA (BBI) und ProMedDx) wurden folgende Blot-Ergebnisse erzielt: Line-Immunoassay 1 Methode Negativ/ Positiv Gesamt Fraglich Negativ/ 3* 0 3 MPD HTLV Fraglich BLOT 2.4 Positiv Gesamt * MPD HTLV BLOT 2.4 lieferte 2 fragliche und 1 negatives Ergebnis (diese Probe wurde auch von Line-Immunoassay 1 negativ getestet). Line-Immunoassay 1 lieferte 3 negative Ergebnisse. Die zwei Blots lieferten für die 102 HTLV-positiven Proben die folgenden Diskriminationen: Interpretation Methode HTLV-I HTLV-II HTLV-I & Nicht Gesamt HTLV-II** typisierbar*** MPD HTLV BLOT 2.4 LI ** Es wurden sowohl HTLV-I- als auch HTLV-II-spezifische Marker festgestellt. Dies deutet auf eine Koinfektion hin. *** Die HTLV-Stämme konnten aufgrund fehlender spezifischer Marker nicht typisiert werden. MPD HTLV BLOT 2.4 und LI 1 lieferten vergleichbare Ergebnisse. Die wenigen diskordanten Ergebnisse gehen auf die verschiedenen auf den Blots immobilisierten Antigene und die unterschiedlichen verwendeten Methoden zurück. MPD HTLV BLOT 2.4 zeigte eine Sensitivität von 97,1 %. Dies entspricht der von Line-Immunoassay 1 erzielten Sensitivität. B. Vergleich mit Line-Immunoassay 2 Untersucht wurde das Anti-HTLV-I/II-Performance-Panel SFTS- 94 (Quelle: Französische Gesellschaft für Bluttransfusion) mit 26 HTLV-I- und 6 HTLV-II-Proben. Der Vergleich zwischen MPD HTLV BLOT 2.4 und Line-Immunoassay 2 (LI 2) lieferte bei diesem Panel folgende Ergebnisse: Interpretation Methode HTLV-I HTLV-II Nicht Falsch- Gesamt typisierbar negativ MPD HTLV BLOT 2.4 LI MPD HTLV BLOT 2.4 kann HTLV-positive Proben korrekt identifizieren und erzielte bei diesem Panel eine Sensitivität > 99,9 %. Line-Immunoassay 2 erreichte bei demselben Panel eine Sensitivität von 96,9 %. Spezifität Bei den insgesamt untersuchten 200 Proben von Blutspendern wurde eine Spezifität von 92,5 % festgestellt.15 Proben waren fraglich; falsch-positive Ergebnisse traten nicht auf. Unter Berücksichtigung von 150 klinischen Proben, 50 Schwangerschaftsproben, 50 potenziell die Testergebnisse beeinträchtigenden Proben (jeweils 10 ikterische, hämolysierte, lipämische, Triglycerid- und Gesamteiweiß-Proben) sowie 73 potenziell kreuzreaktiven Proben (TB, Helicobacter pylori, HEV, Dengue-Fieber, HBV, HCV, HIV-1, HIV-2) ergab sich insgesamt eine Spezifität von 89,2 % (461/517).56 Proben waren fraglich; falsch-positive Ergebnisse traten nicht auf.6 Proben waren echtpositiv. Dies wurde durch einen zusätzlichen Test bestätigt. EINGESCHRÄNKTE GARANTIE Der Hersteller sichert lediglich die Funktionstüchtigkeit des Assays zum Gebrauch für die in vitro Diagnostik innerhalb der Bestimmungen und Einschränkungen zu, die im Bedienungshandbuch des Tests beschrieben sind, sofern der Test unter Beachtung der dortigen Anweisungen durchgeführt wird. Der Hersteller lehnt jegliche - ausdrückliche oder stillschweigende - Gewährleistung ab, einschließlich einer solchen ausdrücklichen oder stillschweigenden Garantie auf Marktgängigkeit, Gebrauchsfähigkeit oder unterstellter Verwendbarkeit für andere Zwecke. Die Haftung des Herstellers beschränkt sich auf entweder Ersatz des Produktes oder Rückerstattung des Kaufpreises für das Produkt. Der Hersteller haftet nicht gegenüber dem Käufer oder gegenüber Dritten für jedwede Schäden, Verletzungen oder wirtschaftliche Verluste, in welcher Form auch immer diese durch den Gebrauch oder in der Anwendung des Produktes hervorgerufen werden mögen. TECHNISCHE PROBLEME / REKLAMATIONEN Bei eventuellen technischen Problemen/Reklamationen bitte folgende Hinweise beachten: 1. Die Chargennummer des Kits und das Verfalldatum notieren. 2. Den Kit und die damit gewonnenen Testergebnisse verwahren. 3. Mit der nächstgelegenen Vertretung von MP Biomedicals oder dem für Sie zuständigen Repräsentanten in Verbindung setzen. LITERATUR 1. Towbin H., Staehlin T. und Gordan J. Electrophoretic transfer of Proteines from polyacrylamide gels to nitrocellulose sheets: procedure and some applications. Proc. Natl. Acad. Sci., U.S.A.1976; 76: Poiesz BJ., Ruscetti FW., Gazdar AF., Bonn PA., Minna JD. und Gallo RC. Detection and Isolation of type C retrovirus particles from fresh and cultured lymphocytes of a patient with cutaneous T-cell lymphoma. Proc. Natl. Acad. Sci., U.S.A.1980; 77(12): Kalyanaraman VS., Sarngadharan MG., Robert-Guroff M., Miyoshi I., Blayney D., Golde und Gallo RC. A new subtype of human T-cell leukemia virus (HTLV-II) associated with a T-cell variant of hairy cell leukemia. Science 1982; 218: , 4. William AE., Fang CT., Slamon DJ. et al. Seroprevalence and epidemiological correlates of HTLV-I infection in U.S. blood donors. Science 1988; 240:
8 5. Lee H., Swanson P., Shorty VS., Zack JA., Roseblatt JD. und Chen ISY. High rate of HTLV-II infection in seropositive IV drug abusers in New Orleans. Science 1989; 244: Lipka JJ., Bui K., Reyes GR, Moeckli R., Wiktor SZ., Blattner WA., Murphy EL., Hanson CV., Shaw GM., Shinsky JJ. und Foung SKH. Determination of a unique immunodominant epitope of HTLV-I. Infect Dis 1990; 162: Wiktor SZ., Alexandra SS., Shaw GM. et al. Distinguishing between HTLV-I and HTLV-II by Western Blot. Lancet 1990; 335: Samuel KP., Lautenberger JA., Jorcyk CL., Josephs S., Wong Staal F. und Papas TS. Diagnostic potential for human malignancies of bacterially produced HTLV-I envelope protein. Science 1984; 226: Hadlock KG., Goh CJ., Bradshaw PA., Perkins S., Lo J., Habbaz RK., Kaplan J. und Foung SKH. Delineation of an immunodominant and highly HTLV specific epitope within the HTLV-I transmembrane glycoprotein. Blood 1995; 68(4): Varma M., Rudolph D., Knuchel M., Switzer W., Hadlock KG., Velligan M., Chan L., Foung SKH., LaI RB. Enhanced specificity of truncated transmembrane protein for serologic confirmation of HTLV-I and HTLV-II infection by Western Blot assay containing recombinant envelope glycoproteins. J. Clin. Micro. 1995; 33(12): Lillehoj EP., Alexander SS., Dubrule CJ., Wiktor S., Adams R., Thi, A. Manns CC., and Blattner WA. Development and evaluation of a human T-Cell leukemia virus type I serologic confirmatory assay incorporating a recombinant envelope polypeptide. J. Clin. Microbiol.1990; 28: Lal RB., Brodine SK., Coligan JE., and Roberts CR. Differential antibody responsiveness to p19 gag results in serological discrimination between human T-lymphotropic virus type I and type II. J. Med. Virol.1991; 1: Hjelle B., Cyrus S., Swenson S. und Mills R. Serologic distinction between human T-lymphotropic virus (HTLV) type I and HTLV type II. Transfusion 1991; 31: Madeleine, MM., Wiktor SZ., Goedert JI., Manns A., Levine PH., Biggar RJ., Blattner WA. HTLV-I and HTLV-II worldwide distribution: reanalysis of immunoblot results. Inte. J. Cancer 1993.; 54(2): World Health Organization s Global Programme on AIDS. WHO Global Programme on AIDS Information Update. Virus Information Exchange Newsletter 1990; 7(2): Lal, RB., Rudolph DL., Coligan JE., Brodine SK. und Roberts CR. Failure to detect evidence of human T- lymphotropic virus (HTLV) type I and type II in blood donors with isolated gag antibodies to HTLV-I/II. Blood 1992; 80: Lipka, JJ., Young KK., Kwok SY., Reyes GR., Sninsky JJ und Foung SK. Significance of human T-lymphotropic virus type I indeterminant serological findings among healthy individuals. Vox Sang.1991; 61: Zrein M., Louwagie J., Boeykens H., Govers L., Hendickx G., Bosman F., Sablon E., Demarquilly C., Boniface M. und Saman E. Assessment of a new immunoassay for serological confirmation and discrimination of human T- cell lymphotropic virus infections. Clin. Diag. Lab. Immunol.1998; 5: Witt DJ., Kuramoto K., Kemper M. und Holland P. Utility of prospective study of donors deferred as HTLV indeterminate. Vox Sang.2000; 78: Hayes C.G., Burans JP. und Oberst RB. Antibodies to Human T Lymphotropic virus Type I in a population from the Philippines: Evidence for cross-reactivity with Plasmodiun falciparum. The J. Infect. Dis.1990; 163: Gallo D., Diggs JL., and Hanson CV. Evaluation of two commercial Human T-Cell Lymphotropic Virus Western blot (Immunoblot) kits with problem specimens. J. Clin. Microbiol. 1994; 32: Garin B., Gosselin S., de The G. und Gessain A. HTLV- I/II infection in a high viral endemic area of Zaire, Central Africa: Comparative evaluation of serology, PCR, and significance of indeterminate Western blot pattern. J. Med. Virol. 1994; 44: Fujiyama C., Fujiyoshi T., Matsumoto D., Yashiki S., Tamashiro H. und Sonoda S. Re-evaluation of anti-htlv- I Western blot assay using HTLV-I and HTLV-II serum panels. Clin. & Diag. Virol. 1995; 4: Rouet F., Meertens L., Courouble G., Herrmann-Storck C., Pabingui R., Chancerel B., Abid A., Strobel M., Mauclere P., und Gessain A. Serological, epidemiological, and molecular differences between human T-cell lymphotropic virus type I - seropositive healthy carriers and persons with HTLV-I gag indeterminate Western blot patterns from the Caribbean. J. Clin. Microbiol. 2001; 39: Cesaire R., Bera O., Maier H., Lezin A., Martial J., Ouka M., Kerob-Bauchet B., Ould Amar AK. und Vernant JC. Seroindeterminate patterns and seroconversions to human T-lymphotropic virus type I positivity in blood donors from Martinique, French West Indies. Transfusion 1999; 39: Soldan SS., Graf MD., Waziri A., Flerlage AN., Robinson SM., Kawaninshi T, Leist TP., Lehky TJ., Levin MC. und Jacobson S. HTLV-I/II seroindeterminate western blot reactivity in a cohort of patients with neurological disease. J. Infect. Dis.1999; 180: Khabbaz, RF., Heneine W., Grindon A., Hartley TM., Shulman G. und Kaplan J. Indeterminate HTLV serologic results in U.S. blood donors: Are they due to HTLV-I or HTLV-II? J. Acquir. Immune Defic. Syndr.1992; 5:
9 MP Biomedicals Asia Pacific Pte Ltd. 85 Science Park Drive #04-01, The Cavendish Singapore Science Park Singapur Tel. No. : Fax. No. : enquiry_ap@mpbio.com Medical Technology Promedt Consulting GmbH Altenhofstrasse 80 D St. Ingbert Deutschland Tel. No. : Fax No. : info@mt-procons.com Regionale Vertretungen: MP Biomedicals Suisse S.A. Halle de Fret/Aeroport P.O. Box Genf 5 Schweiz Tel. : Fax : mpbiosuisse@mpbio.com * US-Patent 5,066,579; 5,614,366; 5,763,572; 5,814,441; 5,871,933; 5,643,714 * Australisches Patent: ; ; * Kanadisches Patent: * Europäisches Patent: * Japanisches Patent: * Schriftzug und Logo von Genelabs sind von Genelabs Technologies, Inc. lizenziert. 9
10 ABBILDUNG 1 Probenzugabe-Kontrolle rgp46-l rgp46-ll p53 gp46 p36 p32 p28 p26 p24 gp21 p19 GD21 a. b. c. d. Virusspezifische Banden: a. HTLV-I/II-doppelinfizierte Probe b. Stark reaktive Kontrolle I (nur reaktiv auf HTLV-I) c. Stark reaktive Kontrolle II (nur reaktiv auf HTLV-II) d. Nichtreaktive Kontrolle 10
HIV BLOT 2.2 WESTERN BLOT ASSAY
 BEDEUTUNG DER VERWENDETEN SYMBOLE Bei Produkten und Verpackungen von MP Diagnostics werden die folgenden grafischen Symbole verwendet. Die Symbole entsprechen den bei medizinischen Instrumenten und deren
BEDEUTUNG DER VERWENDETEN SYMBOLE Bei Produkten und Verpackungen von MP Diagnostics werden die folgenden grafischen Symbole verwendet. Die Symbole entsprechen den bei medizinischen Instrumenten und deren
HTLV I/II ELISA 3.0 0123 REVISIONSDATUM: 11/05 MBN 0011-GER-1 NAME UND VERWENDUNGSZWECK
 BEDEUTUNG DER VERWENDETEN SYMBOLE Bei Produkten und Verpackungen von MP Diagnostics werden die folgenden grafischen Symbole verwendet. Die Symbole entsprechen den bei medizinischen Instrumenten und deren
BEDEUTUNG DER VERWENDETEN SYMBOLE Bei Produkten und Verpackungen von MP Diagnostics werden die folgenden grafischen Symbole verwendet. Die Symbole entsprechen den bei medizinischen Instrumenten und deren
HIV1 /HIV2 Schnelltest In nur 60 Sekunden
 HIV1 /HIV2 Schnelltest In nur 60 Sekunden INSTI TM HIV Antikörper Test Features HIV 1 and HIV 2 Antikörpertest Human IgG Kontrolle Findet alle bekannten HIV 1 und HIV 2 Antikörpersubtypen, einschließlich
HIV1 /HIV2 Schnelltest In nur 60 Sekunden INSTI TM HIV Antikörper Test Features HIV 1 and HIV 2 Antikörpertest Human IgG Kontrolle Findet alle bekannten HIV 1 und HIV 2 Antikörpersubtypen, einschließlich
Pflege und Wartung von Elektroden
 Pflege und Wartung von Elektroden Dipl.-Ing. (FH) Lars Sebralla Ein Meßwert der mit einer Elektrode ermittelt wird ist nur so genau wie die Elektrode selber. Grundlegende Details sollten dabei beachtet
Pflege und Wartung von Elektroden Dipl.-Ing. (FH) Lars Sebralla Ein Meßwert der mit einer Elektrode ermittelt wird ist nur so genau wie die Elektrode selber. Grundlegende Details sollten dabei beachtet
Anleitung zur Handhabung von Durchstechflasche und Einmalspritze (für Patienten, Ärzte, Diabetesberater und Apotheker)
 Anleitung zur Handhabung von Durchstechflasche und Einmalspritze (für Patienten, Ärzte, Diabetesberater und Apotheker) EIN LEITFADEN ZUR ERSTEN VERWENDUNG VON APIDRA in 10ml- DURCHSTECHFLASCHEN Apidra
Anleitung zur Handhabung von Durchstechflasche und Einmalspritze (für Patienten, Ärzte, Diabetesberater und Apotheker) EIN LEITFADEN ZUR ERSTEN VERWENDUNG VON APIDRA in 10ml- DURCHSTECHFLASCHEN Apidra
AUF LETZTER SEITE DIESER ANLEITUNG!!!
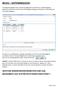 BELEG DATENABGLEICH: Der Beleg-Datenabgleich wird innerhalb des geöffneten Steuerfalls über ELSTER-Belegdaten abgleichen gestartet. Es werden Ihnen alle verfügbaren Belege zum Steuerfall im ersten Bildschirm
BELEG DATENABGLEICH: Der Beleg-Datenabgleich wird innerhalb des geöffneten Steuerfalls über ELSTER-Belegdaten abgleichen gestartet. Es werden Ihnen alle verfügbaren Belege zum Steuerfall im ersten Bildschirm
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren
 Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Der HIV-Antikörper-Schnelltest aus Sicht des Labormediziners. Dr. Thomas Berg, Berlin www.bergdoctor.de
 Der HIV-Antikörper-Schnelltest aus Sicht des Labormediziners Was untersucht der HIV-Antikörper- Schnelltest? (am Beispiel Vitest HIV) Der HIV-Antikörper-Schnelltest ist ein SUCHTEST, der untersucht, ob
Der HIV-Antikörper-Schnelltest aus Sicht des Labormediziners Was untersucht der HIV-Antikörper- Schnelltest? (am Beispiel Vitest HIV) Der HIV-Antikörper-Schnelltest ist ein SUCHTEST, der untersucht, ob
Ihre Protein Analyse
 Ihre Protein Analyse Patient Max Dusan Mustermann Sladek... geboren am 17.10.1986... Gewicht 83 kg... Probennummer P07245... Probenmaterial Plasma... Eingang 18.6.2014... Ausgang 7.7.2014 Sehr geehrter
Ihre Protein Analyse Patient Max Dusan Mustermann Sladek... geboren am 17.10.1986... Gewicht 83 kg... Probennummer P07245... Probenmaterial Plasma... Eingang 18.6.2014... Ausgang 7.7.2014 Sehr geehrter
 Bluetooth Headset Modell Nr. BT-ET007 (Version V2.0+EDR) ANLEITUNG Modell Nr. BT-ET007 1. Einführung Das Bluetooth Headset BT-ET007 kann mit jedem Handy verwendet werden, das über eine Bluetooth-Funktion
Bluetooth Headset Modell Nr. BT-ET007 (Version V2.0+EDR) ANLEITUNG Modell Nr. BT-ET007 1. Einführung Das Bluetooth Headset BT-ET007 kann mit jedem Handy verwendet werden, das über eine Bluetooth-Funktion
Datensicherung. Beschreibung der Datensicherung
 Datensicherung Mit dem Datensicherungsprogramm können Sie Ihre persönlichen Daten problemlos Sichern. Es ist möglich eine komplette Datensicherung durchzuführen, aber auch nur die neuen und geänderten
Datensicherung Mit dem Datensicherungsprogramm können Sie Ihre persönlichen Daten problemlos Sichern. Es ist möglich eine komplette Datensicherung durchzuführen, aber auch nur die neuen und geänderten
PCD Europe, Krefeld, Jan 2007. Auswertung von Haemoccult
 Auswertung von Haemoccult Ist das positiv? Nein! Ja! Im deutschen Krebsfrüherkennungsprogramm haben nur etwa 1 % der Frauen und 1,5 % der Männer ein positives Haemoccult -Ergebnis, da dieser Test eine
Auswertung von Haemoccult Ist das positiv? Nein! Ja! Im deutschen Krebsfrüherkennungsprogramm haben nur etwa 1 % der Frauen und 1,5 % der Männer ein positives Haemoccult -Ergebnis, da dieser Test eine
Ein Blick in die Zukunft, Entwicklung neuer Testverfahren zum Nachweis von Salmonellen und Campylobacter. Dr. Janin Stratmann-Selke
 Ein Blick in die Zukunft, Entwicklung neuer Testverfahren zum Nachweis von Salmonellen und Campylobacter Dr. Janin Stratmann-Selke Salmonellen und Campylobacter als Erreger von Lebensmittelinfektionen
Ein Blick in die Zukunft, Entwicklung neuer Testverfahren zum Nachweis von Salmonellen und Campylobacter Dr. Janin Stratmann-Selke Salmonellen und Campylobacter als Erreger von Lebensmittelinfektionen
Wasserchemie Modul 7
 Wasserchemie Modul 7 Prinzip eines heterogenen Enzyme ELISA Enzyme Linked Immuno Sorbent Assay Was sind Antikörper Antikörper (Immunoglobuline) sind Eiweißstoffe stoffe,, die Tiere und Menschen zur Abwehr
Wasserchemie Modul 7 Prinzip eines heterogenen Enzyme ELISA Enzyme Linked Immuno Sorbent Assay Was sind Antikörper Antikörper (Immunoglobuline) sind Eiweißstoffe stoffe,, die Tiere und Menschen zur Abwehr
Anleitung zum Computercheck Windows Firewall aktivieren oder eine kostenlose Firewall installieren
 Anleitung zum Computercheck Windows Firewall aktivieren oder eine kostenlose Firewall installieren Ziel der Anleitung Sie möchten ein modernes Firewallprogramm für Ihren Computer installieren, um gegen
Anleitung zum Computercheck Windows Firewall aktivieren oder eine kostenlose Firewall installieren Ziel der Anleitung Sie möchten ein modernes Firewallprogramm für Ihren Computer installieren, um gegen
Die Post hat eine Umfrage gemacht
 Die Post hat eine Umfrage gemacht Bei der Umfrage ging es um das Thema: Inklusion Die Post hat Menschen mit Behinderung und Menschen ohne Behinderung gefragt: Wie zufrieden sie in dieser Gesellschaft sind.
Die Post hat eine Umfrage gemacht Bei der Umfrage ging es um das Thema: Inklusion Die Post hat Menschen mit Behinderung und Menschen ohne Behinderung gefragt: Wie zufrieden sie in dieser Gesellschaft sind.
Kapitel 4: Blutspende Bezug Arbeitsauftrag Material Sozialform Zeit Weiterführende Ideen
 Stufe 2 4.1 / Das Blut Lehrerinformation 1/5 Bezug Kapitel 4: Blutspende 4. Die Blutspende / Seite 23 Arbeitsauftrag Die Schüler lösen nach der Lektüre in der Schülerinformation das Arbeitsblatt. Material
Stufe 2 4.1 / Das Blut Lehrerinformation 1/5 Bezug Kapitel 4: Blutspende 4. Die Blutspende / Seite 23 Arbeitsauftrag Die Schüler lösen nach der Lektüre in der Schülerinformation das Arbeitsblatt. Material
Bijsluiter DE versie Imaverol 100 mg (glas) B. PACKUNGSBEILAGE 1
 B. PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION Imaverol 100 mg, Konzentrat zur örtlichen Anwendung 1.NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
B. PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION Imaverol 100 mg, Konzentrat zur örtlichen Anwendung 1.NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
West-Nil-Virus und Hepatitis E-Virus: durch Bluttransfusion übertragbare Viren
 West-Nil-Virus und Hepatitis E-Virus: durch Bluttransfusion übertragbare Viren 100 nm HEV, Abb.: Center of Disease Control and Prevention WNV, Abb.: Dr. H. Gelderblohm, RKI Institut für Transfusionsmedizin
West-Nil-Virus und Hepatitis E-Virus: durch Bluttransfusion übertragbare Viren 100 nm HEV, Abb.: Center of Disease Control and Prevention WNV, Abb.: Dr. H. Gelderblohm, RKI Institut für Transfusionsmedizin
Station 1: Säuren in Lebensmitteln (1)
 Station 1: Säuren in Lebensmitteln (1) An dieser Station testet ihr, welche Lebensmittel Säuren enthalten. Für den Säurenachweis benutzt man im Labor bestimmte chemische Stoffe, die man Indikatoren (Zeigerstoffe)
Station 1: Säuren in Lebensmitteln (1) An dieser Station testet ihr, welche Lebensmittel Säuren enthalten. Für den Säurenachweis benutzt man im Labor bestimmte chemische Stoffe, die man Indikatoren (Zeigerstoffe)
Gebrauchsanweisung Ladebrücke
 BGR 233 GEPRÜFT Gebrauchsanweisung Ladebrücke Beachten Sie den Schulungsfilm auf www.kruizinga.de Bitte vorab lesen! 1Lesen Sie diese Anleitung sorgfältig durch, bevor Sie die Ladebrücke gebrauchen. Die
BGR 233 GEPRÜFT Gebrauchsanweisung Ladebrücke Beachten Sie den Schulungsfilm auf www.kruizinga.de Bitte vorab lesen! 1Lesen Sie diese Anleitung sorgfältig durch, bevor Sie die Ladebrücke gebrauchen. Die
DAS GRÜNE REZEPT. Für eine sichere Medikation mit rezeptfreien Arzneimitteln
 DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
Dieser Ablauf soll eine Hilfe für die tägliche Arbeit mit der SMS Bestätigung im Millennium darstellen.
 Millennium SMS Service Schnellübersicht Seite 1 von 6 1. Tägliche Arbeiten mit der SMS Bestätigung Dieser Ablauf soll eine Hilfe für die tägliche Arbeit mit der SMS Bestätigung im Millennium darstellen.
Millennium SMS Service Schnellübersicht Seite 1 von 6 1. Tägliche Arbeiten mit der SMS Bestätigung Dieser Ablauf soll eine Hilfe für die tägliche Arbeit mit der SMS Bestätigung im Millennium darstellen.
Professionelle Seminare im Bereich MS-Office
 Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
EU-Verordnung Nr. 1907/2006 (REACH)
 Was bedeutet REACH? REACH ist die EG-Verordnung Nr. 1907/2006 zur Registration, Evaluation, Authorization and Restriction of CHemicals (Registrierung, Bewertung und Zulassung von Chemikalien). Mit dieser
Was bedeutet REACH? REACH ist die EG-Verordnung Nr. 1907/2006 zur Registration, Evaluation, Authorization and Restriction of CHemicals (Registrierung, Bewertung und Zulassung von Chemikalien). Mit dieser
Reinigung... 2. Normale Reingung der CheckStab Leitfähigkeitselektrode... 2. Gründliche Reinigung der Leitfähigkeitselektrode... 2
 Diese Anleitung fasst einige Punkte zusammen, die für eine gute Funktion der CheckStab Geräte wichtig sind. Sie ist nicht als Ersatz für das Handbuch, sondern als Ergänzung zum Handbuch gedacht. Bitte
Diese Anleitung fasst einige Punkte zusammen, die für eine gute Funktion der CheckStab Geräte wichtig sind. Sie ist nicht als Ersatz für das Handbuch, sondern als Ergänzung zum Handbuch gedacht. Bitte
FÜR 2 BIS 4 SPIELER AB 8 JAHREN
 FÜR 2 BIS 4 SPIELER AB 8 JAHREN Inhalt 104 Zutatenkarten (11 Sorten: 2, 2, 3, 3, 4, 4, 5, 5, 6, 8, 10) Ziel Ziel des Spieles ist es, drei Zutaten zu komplettieren und so als Erster sein Experiment erfolgreich
FÜR 2 BIS 4 SPIELER AB 8 JAHREN Inhalt 104 Zutatenkarten (11 Sorten: 2, 2, 3, 3, 4, 4, 5, 5, 6, 8, 10) Ziel Ziel des Spieles ist es, drei Zutaten zu komplettieren und so als Erster sein Experiment erfolgreich
Praktikum Biochemie Einführung in die Molekularbiologie. Bettina Siebers
 Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers Rekombinante Expression einer Esterase aus Pseudomonas aeruginosa in E. coli Polyacrylamide Gelelektrophorese (PAGE) Denaturierende
Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers Rekombinante Expression einer Esterase aus Pseudomonas aeruginosa in E. coli Polyacrylamide Gelelektrophorese (PAGE) Denaturierende
Welche Unterschiede gibt es zwischen einem CAPAund einem Audiometrie- Test?
 Welche Unterschiede gibt es zwischen einem CAPAund einem Audiometrie- Test? Auch wenn die Messungsmethoden ähnlich sind, ist das Ziel beider Systeme jedoch ein anderes. Gwenolé NEXER g.nexer@hearin gp
Welche Unterschiede gibt es zwischen einem CAPAund einem Audiometrie- Test? Auch wenn die Messungsmethoden ähnlich sind, ist das Ziel beider Systeme jedoch ein anderes. Gwenolé NEXER g.nexer@hearin gp
Sollten während der Benutzung Probleme auftreten, können Sie die folgende Liste zur Problembehebung benutzen, um eine Lösung zu finden.
 12. Problembehebung Sollten während der Benutzung Probleme auftreten, können Sie die folgende Liste zur Problembehebung benutzen, um eine Lösung zu finden. Sollte Ihr Problem nicht mit Hilfe dieser Liste
12. Problembehebung Sollten während der Benutzung Probleme auftreten, können Sie die folgende Liste zur Problembehebung benutzen, um eine Lösung zu finden. Sollte Ihr Problem nicht mit Hilfe dieser Liste
Video Unlimited -Nutzungsbeschränkungen
 Video Unlimited -Nutzungsbeschränkungen In diesem Dokument werden Beschränkungen erklärt, die für die Verwendung von Videos gelten, die Sie über Video Unlimited -Dienste gekauft oder ausgeliehen haben
Video Unlimited -Nutzungsbeschränkungen In diesem Dokument werden Beschränkungen erklärt, die für die Verwendung von Videos gelten, die Sie über Video Unlimited -Dienste gekauft oder ausgeliehen haben
Weiterleitung einrichten für eine GMX-E-Mail-Adresse
 Weiterleitung einrichten für eine GMX-E-Mail-Adresse Für die Nutzung der E-Mail-Adresse mit den Push-E-Mail-Services BlackBerry und Windows Mobile E-Mail von Vodafone Sämtliche geistigen Eigentumsrechte
Weiterleitung einrichten für eine GMX-E-Mail-Adresse Für die Nutzung der E-Mail-Adresse mit den Push-E-Mail-Services BlackBerry und Windows Mobile E-Mail von Vodafone Sämtliche geistigen Eigentumsrechte
Nachricht der Kundenbetreuung
 Cisco WebEx: Service-Pack vom [[DATE]] für [[WEBEXURL]] Sehr geehrter Cisco WebEx-Kunde, Cisco WebEx sendet diese Mitteilung an wichtige Geschäftskontakte unter https://[[webexurl]]. Ab Samstag, 1. November
Cisco WebEx: Service-Pack vom [[DATE]] für [[WEBEXURL]] Sehr geehrter Cisco WebEx-Kunde, Cisco WebEx sendet diese Mitteilung an wichtige Geschäftskontakte unter https://[[webexurl]]. Ab Samstag, 1. November
Bitte leiten Sie diese Information an die zuständige Fachabteilung, bzw. die Anwender der oben genannten Produkte weiter.
 3. April 2013 cobas Software v1.x und v2.0 auf den Systemen cobas 4800 und cobas z 480: Seltener Channel Shift bei der Fluoreszenzauswertung führt zu invaliden Ergebnissen oder
3. April 2013 cobas Software v1.x und v2.0 auf den Systemen cobas 4800 und cobas z 480: Seltener Channel Shift bei der Fluoreszenzauswertung führt zu invaliden Ergebnissen oder
Anti-Botnet-Beratungszentrum. Windows XP in fünf Schritten absichern
 Windows XP in fünf Schritten absichern Inhalt: 1. Firewall Aktivierung 2. Anwendung eines Anti-Virus Scanner 3. Aktivierung der automatischen Updates 4. Erstellen eines Backup 5. Setzen von sicheren Passwörtern
Windows XP in fünf Schritten absichern Inhalt: 1. Firewall Aktivierung 2. Anwendung eines Anti-Virus Scanner 3. Aktivierung der automatischen Updates 4. Erstellen eines Backup 5. Setzen von sicheren Passwörtern
Outlook. sysplus.ch outlook - mail-grundlagen Seite 1/8. Mail-Grundlagen. Posteingang
 sysplus.ch outlook - mail-grundlagen Seite 1/8 Outlook Mail-Grundlagen Posteingang Es gibt verschiedene Möglichkeiten, um zum Posteingang zu gelangen. Man kann links im Outlook-Fenster auf die Schaltfläche
sysplus.ch outlook - mail-grundlagen Seite 1/8 Outlook Mail-Grundlagen Posteingang Es gibt verschiedene Möglichkeiten, um zum Posteingang zu gelangen. Man kann links im Outlook-Fenster auf die Schaltfläche
6 Schulungsmodul: Probenahme im Betrieb
 6 Schulungsmodul: Probenahme im Betrieb WIEDNER Wie schon im Kapitel VI erwähnt, ist die Probenahme in Betrieben, die Produkte nach dem Lebensmittel- und Futtermittelgesetzbuch herstellen oder in den Verkehr
6 Schulungsmodul: Probenahme im Betrieb WIEDNER Wie schon im Kapitel VI erwähnt, ist die Probenahme in Betrieben, die Produkte nach dem Lebensmittel- und Futtermittelgesetzbuch herstellen oder in den Verkehr
Anleitung zur Installation und Nutzung des Sony PRS-T1 ebook Readers
 Anleitung zur Installation und Nutzung des Sony PRS-T1 ebook Readers Der neue Sony PRS-T1 ebook-reader ist nicht mehr mit dem Programm Adobe Digital Editions zu bedienen. Es sind daher einige Schritte
Anleitung zur Installation und Nutzung des Sony PRS-T1 ebook Readers Der neue Sony PRS-T1 ebook-reader ist nicht mehr mit dem Programm Adobe Digital Editions zu bedienen. Es sind daher einige Schritte
Anleitung zur Installation und Nutzung des Sony PRS-T1 ebook Readers
 Anleitung zur Installation und Nutzung des Sony PRS-T1 ebook Readers Der neue Sony PRS-T1 ebook-reader ist nicht mehr mit dem Programm Adobe Digital Editions zu bedienen. Es sind daher einige Schritte
Anleitung zur Installation und Nutzung des Sony PRS-T1 ebook Readers Der neue Sony PRS-T1 ebook-reader ist nicht mehr mit dem Programm Adobe Digital Editions zu bedienen. Es sind daher einige Schritte
Wann ist eine Software in Medizinprodukte- Aufbereitungsabteilungen ein Medizinprodukt?
 DGSV-Kongress 2009 Wann ist eine Software in Medizinprodukte- Aufbereitungsabteilungen ein Medizinprodukt? Sybille Andrée Betriebswirtin für und Sozialmanagement (FH-SRH) Prokuristin HSD Händschke Software
DGSV-Kongress 2009 Wann ist eine Software in Medizinprodukte- Aufbereitungsabteilungen ein Medizinprodukt? Sybille Andrée Betriebswirtin für und Sozialmanagement (FH-SRH) Prokuristin HSD Händschke Software
Richtlinie zur Feststellung und Überwachung des PRRS-Status von Schweinebeständen (PRRS-Richtlinie) Rd. Erl. des MLU vom 27.
 Richtlinie zur Feststellung und Überwachung des PRRS-Status von Schweinebeständen (PRRS-Richtlinie) Rd. Erl. des MLU vom 27. Februar 2004 Anlagen 1. Einleitung Das PRRS-Virus wurde Anfang der 90-iger Jahre
Richtlinie zur Feststellung und Überwachung des PRRS-Status von Schweinebeständen (PRRS-Richtlinie) Rd. Erl. des MLU vom 27. Februar 2004 Anlagen 1. Einleitung Das PRRS-Virus wurde Anfang der 90-iger Jahre
-------------------------------------------------------------------------------------------
 Sicherheitshinweise im Zusammenhang mit Drahtlosnetzwerken: Hier aufgeführt finden Sie wichtige Informationen. Damit Sie als Käufer von drahtlosen Produkten einfach zu einer bestmöglichen Wireless Netzwerkumgebung
Sicherheitshinweise im Zusammenhang mit Drahtlosnetzwerken: Hier aufgeführt finden Sie wichtige Informationen. Damit Sie als Käufer von drahtlosen Produkten einfach zu einer bestmöglichen Wireless Netzwerkumgebung
Vergleichende Untersuchungen der Sarstedt Blutsenkungssysteme. S-Monovette BSG und S-Sedivette und der Messgeräte Sediplus S 200 und S 2000
 Vergleichende Untersuchungen der Sarstedt Blutsenkungssysteme S-Monovette BSG und S-Sedivette und der Messgeräte Sediplus S 200 und S 2000 Einleitung: Für Blutentnahmen einer BSG Bestimmung bietet Sarstedt
Vergleichende Untersuchungen der Sarstedt Blutsenkungssysteme S-Monovette BSG und S-Sedivette und der Messgeräte Sediplus S 200 und S 2000 Einleitung: Für Blutentnahmen einer BSG Bestimmung bietet Sarstedt
Vergleich Borrelia-ELISA unterschiedlicher Testhersteller mit Immunoblot: Hochspezifische, aber niedrig-sensitive Tesverfahren
 Vergleich Borrelia-ELISA unterschiedlicher Testhersteller mit Immunoblot: Hochspezifische, aber niedrig-sensitive Tesverfahren Dr. med. Armin Schwarzbach Facharzt für Laboratoriumsmedizin Mitglied der
Vergleich Borrelia-ELISA unterschiedlicher Testhersteller mit Immunoblot: Hochspezifische, aber niedrig-sensitive Tesverfahren Dr. med. Armin Schwarzbach Facharzt für Laboratoriumsmedizin Mitglied der
Über den Link https://www.edudip.com/academy/dbv erreichen Sie unsere Einstiegsseite:
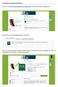 Anmeldung und Zugang zum Webinar Über den Link https://www.edudip.com/academy/dbv erreichen Sie unsere Einstiegsseite: Dort finden Sie die Ankündigung unserer Webinare: Wenn Sie auf den Eintrag zum gewünschten
Anmeldung und Zugang zum Webinar Über den Link https://www.edudip.com/academy/dbv erreichen Sie unsere Einstiegsseite: Dort finden Sie die Ankündigung unserer Webinare: Wenn Sie auf den Eintrag zum gewünschten
GEVITAS Farben-Reaktionstest
 GEVITAS Farben-Reaktionstest GEVITAS Farben-Reaktionstest Inhalt 1. Allgemeines... 1 2. Funktionsweise der Tests... 2 3. Die Ruhetaste und die Auslösetaste... 2 4. Starten der App Hauptmenü... 3 5. Auswahl
GEVITAS Farben-Reaktionstest GEVITAS Farben-Reaktionstest Inhalt 1. Allgemeines... 1 2. Funktionsweise der Tests... 2 3. Die Ruhetaste und die Auslösetaste... 2 4. Starten der App Hauptmenü... 3 5. Auswahl
Transportieren und Verpacken des Druckers
 Transportieren und Verpacken des Druckers Dieses Thema hat folgenden Inhalt: smaßnahmen beim Transportieren des Druckers auf Seite 4-37 Transportieren des Druckers innerhalb des Büros auf Seite 4-38 Vorbereiten
Transportieren und Verpacken des Druckers Dieses Thema hat folgenden Inhalt: smaßnahmen beim Transportieren des Druckers auf Seite 4-37 Transportieren des Druckers innerhalb des Büros auf Seite 4-38 Vorbereiten
WAS finde ich WO im Beipackzettel
 WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
TECHNISCHE INFORMATION LESSOR LOHN/GEHALT BEITRAGSNACHWEIS-AUSGLEICH BUCH.-BLATT MICROSOFT DYNAMICS NAV
 MICROSOFT DYNAMICS NAV Inhaltsverzeichnis TECHNISCHE INFORMATION: Einleitung... 3 LESSOR LOHN/GEHALT Beschreibung... 3 Prüfung der Ausgleichszeilen... 9 Zurücksetzen der Ausgleichsroutine... 12 Vorgehensweise
MICROSOFT DYNAMICS NAV Inhaltsverzeichnis TECHNISCHE INFORMATION: Einleitung... 3 LESSOR LOHN/GEHALT Beschreibung... 3 Prüfung der Ausgleichszeilen... 9 Zurücksetzen der Ausgleichsroutine... 12 Vorgehensweise
Das große ElterngeldPlus 1x1. Alles über das ElterngeldPlus. Wer kann ElterngeldPlus beantragen? ElterngeldPlus verstehen ein paar einleitende Fakten
 Das große x -4 Alles über das Wer kann beantragen? Generell kann jeder beantragen! Eltern (Mütter UND Väter), die schon während ihrer Elternzeit wieder in Teilzeit arbeiten möchten. Eltern, die während
Das große x -4 Alles über das Wer kann beantragen? Generell kann jeder beantragen! Eltern (Mütter UND Väter), die schon während ihrer Elternzeit wieder in Teilzeit arbeiten möchten. Eltern, die während
SCHLÜSSEL: Protokoll für die vorbereitende Desinfizierung/manuelle Reinigung und Sterilisation der Schlüssel von SATELEC
 SCHLÜSSEL: Protokoll für die vorbereitende Desinfizierung/manuelle Reinigung und Sterilisation der Schlüssel von SATELEC Warnhinweise: Keine Stahlwolle oder Scheuermittel verwenden. Die Verwendung von
SCHLÜSSEL: Protokoll für die vorbereitende Desinfizierung/manuelle Reinigung und Sterilisation der Schlüssel von SATELEC Warnhinweise: Keine Stahlwolle oder Scheuermittel verwenden. Die Verwendung von
Systemen im Wandel. Autor: Dr. Gerd Frenzen Coromell GmbH Seite 1 von 5
 Das Management von Informations- Systemen im Wandel Die Informations-Technologie (IT) war lange Zeit ausschließlich ein Hilfsmittel, um Arbeitsabläufe zu vereinfachen und Personal einzusparen. Sie hat
Das Management von Informations- Systemen im Wandel Die Informations-Technologie (IT) war lange Zeit ausschließlich ein Hilfsmittel, um Arbeitsabläufe zu vereinfachen und Personal einzusparen. Sie hat
TESTEN SIE IHR KÖNNEN UND GEWINNEN SIE!
 9 TESTEN SIE IHR KÖNNEN UND GEWINNEN SIE! An den SeniorNETclub 50+ Währinger Str. 57/7 1090 Wien Und zwar gleich in doppelter Hinsicht:!"Beantworten Sie die folgenden Fragen und vertiefen Sie damit Ihr
9 TESTEN SIE IHR KÖNNEN UND GEWINNEN SIE! An den SeniorNETclub 50+ Währinger Str. 57/7 1090 Wien Und zwar gleich in doppelter Hinsicht:!"Beantworten Sie die folgenden Fragen und vertiefen Sie damit Ihr
QUANTA Chek Celiac Panel
 QUANTA Chek Celiac Panel 708113 Verwendungszweck Die QUANTA Chek TM Celiac Probereihe wird für die Qualitätskontrolle bei IFA und ELISA Autoantikörper verfahren verwendet. Jedes Serum dient sowohl als
QUANTA Chek Celiac Panel 708113 Verwendungszweck Die QUANTA Chek TM Celiac Probereihe wird für die Qualitätskontrolle bei IFA und ELISA Autoantikörper verfahren verwendet. Jedes Serum dient sowohl als
Dow Jones am 13.06.08 im 1-min Chat
 Dow Jones am 13.06.08 im 1-min Chat Dieser Ausschnitt ist eine Formation: Wechselstäbe am unteren Bollinger Band mit Punkt d über dem 20-er GD nach 3 tieferen Hoch s. Wenn ich einen Ausbruch aus Wechselstäben
Dow Jones am 13.06.08 im 1-min Chat Dieser Ausschnitt ist eine Formation: Wechselstäbe am unteren Bollinger Band mit Punkt d über dem 20-er GD nach 3 tieferen Hoch s. Wenn ich einen Ausbruch aus Wechselstäben
Dieses erste Kreisdiagramm, bezieht sich auf das gesamte Testergebnis der kompletten 182 getesteten Personen. Ergebnis
 Datenanalyse Auswertung Der Kern unseres Projektes liegt ganz klar bei der Fragestellung, ob es möglich ist, Biere von und geschmacklich auseinander halten zu können. Anhand der folgenden Grafiken, sollte
Datenanalyse Auswertung Der Kern unseres Projektes liegt ganz klar bei der Fragestellung, ob es möglich ist, Biere von und geschmacklich auseinander halten zu können. Anhand der folgenden Grafiken, sollte
Was meinen die Leute eigentlich mit: Grexit?
 Was meinen die Leute eigentlich mit: Grexit? Grexit sind eigentlich 2 Wörter. 1. Griechenland 2. Exit Exit ist ein englisches Wort. Es bedeutet: Ausgang. Aber was haben diese 2 Sachen mit-einander zu tun?
Was meinen die Leute eigentlich mit: Grexit? Grexit sind eigentlich 2 Wörter. 1. Griechenland 2. Exit Exit ist ein englisches Wort. Es bedeutet: Ausgang. Aber was haben diese 2 Sachen mit-einander zu tun?
Installation von Malwarebytes
 Installation von Malwarebytes Ziel der Anleitung Diese Anleitung zeigt Ihnen, wie Sie das Programm Malwarebytes auf Ihrem Computer installieren können. Das kostenlose Programm Malwarebytes findet und entfernt
Installation von Malwarebytes Ziel der Anleitung Diese Anleitung zeigt Ihnen, wie Sie das Programm Malwarebytes auf Ihrem Computer installieren können. Das kostenlose Programm Malwarebytes findet und entfernt
1 P-002-034-B-I-885-DEU-V1.0. 5.2 Drucker-Farbband wechseln. H Bedienung. 5.2.1 Übersicht
 H Bedienung 5.2 Drucker-Farbband wechseln 5.2.1 Übersicht Sie können jederzeit Informationen zum Drucker-Farbband in der Benutzeroberfläche einsehen. Im Menü Dashboard im Bereich Verpackungseinheit wird
H Bedienung 5.2 Drucker-Farbband wechseln 5.2.1 Übersicht Sie können jederzeit Informationen zum Drucker-Farbband in der Benutzeroberfläche einsehen. Im Menü Dashboard im Bereich Verpackungseinheit wird
Diese Broschüre fasst die wichtigsten Informationen zusammen, damit Sie einen Entscheid treffen können.
 Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Die Schul(-landheim)druckerei geht auf die Methode des Reformpädagogen Celestin Freinet (1896-1966) zurück.
 J U G E N D H A U S L E I N A C H Anleitung Druckerei Die Schul(-landheim)druckerei geht auf die Methode des Reformpädagogen Celestin Freinet (1896-1966) zurück. 1. Vorbereitung: Texte überlegen und schreiben,
J U G E N D H A U S L E I N A C H Anleitung Druckerei Die Schul(-landheim)druckerei geht auf die Methode des Reformpädagogen Celestin Freinet (1896-1966) zurück. 1. Vorbereitung: Texte überlegen und schreiben,
«Eine Person ist funktional gesund, wenn sie möglichst kompetent mit einem möglichst gesunden Körper an möglichst normalisierten Lebensbereichen
 18 «Eine Person ist funktional gesund, wenn sie möglichst kompetent mit einem möglichst gesunden Körper an möglichst normalisierten Lebensbereichen teilnimmt und teilhat.» 3Das Konzept der Funktionalen
18 «Eine Person ist funktional gesund, wenn sie möglichst kompetent mit einem möglichst gesunden Körper an möglichst normalisierten Lebensbereichen teilnimmt und teilhat.» 3Das Konzept der Funktionalen
Fragebogen zur Anforderungsanalyse
 Fragebogen zur Anforderungsanalyse Geschäftsprozess Datum Mitarbeiter www.seikumu.de Fragebogen zur Anforderungsanalyse Seite 6 Hinweise zur Durchführung der Anforderungsanalyse Bevor Sie beginnen, hier
Fragebogen zur Anforderungsanalyse Geschäftsprozess Datum Mitarbeiter www.seikumu.de Fragebogen zur Anforderungsanalyse Seite 6 Hinweise zur Durchführung der Anforderungsanalyse Bevor Sie beginnen, hier
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Viscosan - Augentropfen Wirkstoff: Hypromellose
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Viscosan - Augentropfen Wirkstoff: Hypromellose Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Viscosan - Augentropfen Wirkstoff: Hypromellose Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
E S - M P 3 Einbauanleitung. 17 -Monitor-Panel STAND: FEBRUAR 2010
 E S - M P 3 Einbauanleitung 17 -Monitor-Panel STAND: FEBRUAR 2010 Lieferumfang 2x Monitor-Haltebleche (2) 1x Halteblech für die linke Seite des 17 -Monitor-Panels (4) 1x Halteblech für die rechte Seite
E S - M P 3 Einbauanleitung 17 -Monitor-Panel STAND: FEBRUAR 2010 Lieferumfang 2x Monitor-Haltebleche (2) 1x Halteblech für die linke Seite des 17 -Monitor-Panels (4) 1x Halteblech für die rechte Seite
CTI SYSTEMS S.A. CTI SYSTEMS S.A. 12, op der Sang. Fax: +352/2685-3000 L- 9779 Lentzweiler. Email: cti@ctisystems.com G.D.
 Z.I. Eselborn - Lentzweiler Phone: +352/2685-2000 12, op der Sang Fax: +352/2685-3000 L- 9779 Lentzweiler Email: cti@ctisystems.com G.D. Luxembourg URL: www.ctisystems.com Benutzung von Höhensicherungsgeräten
Z.I. Eselborn - Lentzweiler Phone: +352/2685-2000 12, op der Sang Fax: +352/2685-3000 L- 9779 Lentzweiler Email: cti@ctisystems.com G.D. Luxembourg URL: www.ctisystems.com Benutzung von Höhensicherungsgeräten
Anleitung zum DKM-Computercheck Windows Defender aktivieren
 Anleitung zum DKM-Computercheck Windows Defender aktivieren Ziel der Anleitung Sie möchten das Antivirenprogramm Windows Defender auf Ihrem Computer aktivieren, um gegen zukünftige Angriffe besser gewappnet
Anleitung zum DKM-Computercheck Windows Defender aktivieren Ziel der Anleitung Sie möchten das Antivirenprogramm Windows Defender auf Ihrem Computer aktivieren, um gegen zukünftige Angriffe besser gewappnet
Vorlesung - Medizinische Biometrie
 Vorlesung - Medizinische Biometrie Stefan Wagenpfeil Institut für Medizinische Biometrie, Epidemiologie und Medizinische Informatik Universität des Saarlandes, Homburg / Saar Vorlesung - Medizinische Biometrie
Vorlesung - Medizinische Biometrie Stefan Wagenpfeil Institut für Medizinische Biometrie, Epidemiologie und Medizinische Informatik Universität des Saarlandes, Homburg / Saar Vorlesung - Medizinische Biometrie
Anmeldung und Zugang zum Webinar des Deutschen Bibliotheksverbandes e.v. (dbv)
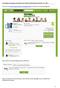 Anmeldung und Zugang zum Webinar des Deutschen Bibliotheksverbandes e.v. (dbv) Über den Link https://www.edudip.com/academy/dbv erreichen Sie unsere Einstiegsseite: Hier finden Sie die Ankündigung unseres
Anmeldung und Zugang zum Webinar des Deutschen Bibliotheksverbandes e.v. (dbv) Über den Link https://www.edudip.com/academy/dbv erreichen Sie unsere Einstiegsseite: Hier finden Sie die Ankündigung unseres
Säuglingsanfangsnahrung und Folgenahrung Was ändert sich? Was bleibt?
 Säuglingsanfangsnahrung und Folgenahrung Was ändert sich? Was bleibt? Begleitinformationen: Handout für das Verkaufspersonal im Handel Bei Rückfragen sprechen Sie uns bitte gerne an: DIÄTVERBAND e. V.
Säuglingsanfangsnahrung und Folgenahrung Was ändert sich? Was bleibt? Begleitinformationen: Handout für das Verkaufspersonal im Handel Bei Rückfragen sprechen Sie uns bitte gerne an: DIÄTVERBAND e. V.
PalmCD2 Programmiergerät
 Stand: Februar 2004 Inhaltsverzeichnis 1.0 Einführung 3 2.0 Inbetriebnahme 3 3.0 Programmieren mit PC oder Laptop 4 4.0 Programmieren mit dem Palm Organizer 4 5.0 PalmCD2 mit Transponder-Funktion einrichten
Stand: Februar 2004 Inhaltsverzeichnis 1.0 Einführung 3 2.0 Inbetriebnahme 3 3.0 Programmieren mit PC oder Laptop 4 4.0 Programmieren mit dem Palm Organizer 4 5.0 PalmCD2 mit Transponder-Funktion einrichten
PFBV - ELISA. Enzyme Linked Immuno Sorbent Assay. zum Nachweis des. Pelargonium flower break virus (PFBV)
 Baumgartenstr. 5 D-79285 Ebringen (FRG) Tel.: +49 7664 600254 Fax: +49 7664 600255 Email: info@steffens-biotec.com PFBV - ELISA Enzyme Linked Immuno Sorbent Assay zum Nachweis des Pelargonium flower break
Baumgartenstr. 5 D-79285 Ebringen (FRG) Tel.: +49 7664 600254 Fax: +49 7664 600255 Email: info@steffens-biotec.com PFBV - ELISA Enzyme Linked Immuno Sorbent Assay zum Nachweis des Pelargonium flower break
Diagnostisches Interview zur Bruchrechnung
 Diagnostisches Interview zur Bruchrechnung (1) Tortendiagramm Zeigen Sie der Schülerin/dem Schüler das Tortendiagramm. a) Wie groß ist der Teil B des Kreises? b) Wie groß ist der Teil D des Kreises? (2)
Diagnostisches Interview zur Bruchrechnung (1) Tortendiagramm Zeigen Sie der Schülerin/dem Schüler das Tortendiagramm. a) Wie groß ist der Teil B des Kreises? b) Wie groß ist der Teil D des Kreises? (2)
Anmeldung und Zugang zum Webinar des Deutschen Bibliotheksverbandes e.v. (dbv)
 Anmeldung und Zugang zum Webinar des Deutschen Bibliotheksverbandes e.v. (dbv) Über den Link https://www.edudip.com/academy/dbv erreichen Sie unsere Einstiegsseite: Hier finden Sie die Ankündigung unseres
Anmeldung und Zugang zum Webinar des Deutschen Bibliotheksverbandes e.v. (dbv) Über den Link https://www.edudip.com/academy/dbv erreichen Sie unsere Einstiegsseite: Hier finden Sie die Ankündigung unseres
Dipl.-Ing. Herbert Schmolke, VdS Schadenverhütung
 1. Problembeschreibung a) Ein Elektromonteur versetzt in einer überwachungsbedürftigen Anlage eine Leuchte von A nach B. b) Ein Elektromonteur verlegt eine zusätzliche Steckdose in einer überwachungsbedürftigen
1. Problembeschreibung a) Ein Elektromonteur versetzt in einer überwachungsbedürftigen Anlage eine Leuchte von A nach B. b) Ein Elektromonteur verlegt eine zusätzliche Steckdose in einer überwachungsbedürftigen
Testosteron ELISA, EIA
 Testosteron ELISA, EIA Enzymimmunoassay für Testosteron in porcinem Serum/Plasma Kurzbeschreibung der Assay-Durchführung 1. Testbestandteile und Lösungen auf Raumtemperatur bringen (Ausnahme: Tracer-Stammlösung
Testosteron ELISA, EIA Enzymimmunoassay für Testosteron in porcinem Serum/Plasma Kurzbeschreibung der Assay-Durchführung 1. Testbestandteile und Lösungen auf Raumtemperatur bringen (Ausnahme: Tracer-Stammlösung
- Zweimal Wöchentlich - Windows Update ausführen - Live Update im Norton Antivirusprogramm ausführen
 walker radio tv + pc GmbH Flüelerstr. 42 6460 Altdorf Tel 041 870 55 77 Fax 041 870 55 83 E-Mail info@walkerpc.ch Wichtige Informationen Hier erhalten sie einige wichtige Informationen wie sie ihren Computer
walker radio tv + pc GmbH Flüelerstr. 42 6460 Altdorf Tel 041 870 55 77 Fax 041 870 55 83 E-Mail info@walkerpc.ch Wichtige Informationen Hier erhalten sie einige wichtige Informationen wie sie ihren Computer
Novell Client. Anleitung. zur Verfügung gestellt durch: ZID Dezentrale Systeme. Februar 2015. ZID Dezentrale Systeme
 Novell Client Anleitung zur Verfügung gestellt durch: ZID Dezentrale Systeme Februar 2015 Seite 2 von 8 Mit der Einführung von Windows 7 hat sich die Novell-Anmeldung sehr stark verändert. Der Novell Client
Novell Client Anleitung zur Verfügung gestellt durch: ZID Dezentrale Systeme Februar 2015 Seite 2 von 8 Mit der Einführung von Windows 7 hat sich die Novell-Anmeldung sehr stark verändert. Der Novell Client
STARSTICK 2 DVB-T Receiver als USB Stick
 STARSTICK 2 DVB-T Receiver als USB Stick Bedienungsanleitung Sehr geehrter Kunde, Vielen Dank, das Sie Sich für dieses hochwertige Produkt entschieden haben. Sollte ihr USB-Stick nicht richtig funktionieren,
STARSTICK 2 DVB-T Receiver als USB Stick Bedienungsanleitung Sehr geehrter Kunde, Vielen Dank, das Sie Sich für dieses hochwertige Produkt entschieden haben. Sollte ihr USB-Stick nicht richtig funktionieren,
Fachbericht zum Thema: Anforderungen an ein Datenbanksystem
 Fachbericht zum Thema: Anforderungen an ein Datenbanksystem von André Franken 1 Inhaltsverzeichnis 1 Inhaltsverzeichnis 1 2 Einführung 2 2.1 Gründe für den Einsatz von DB-Systemen 2 2.2 Definition: Datenbank
Fachbericht zum Thema: Anforderungen an ein Datenbanksystem von André Franken 1 Inhaltsverzeichnis 1 Inhaltsverzeichnis 1 2 Einführung 2 2.1 Gründe für den Einsatz von DB-Systemen 2 2.2 Definition: Datenbank
SafeRun-Modus: Die Sichere Umgebung für die Ausführung von Programmen
 SafeRun-Modus: Die Sichere Umgebung für die Ausführung von Programmen Um die maximale Sicherheit für das Betriebssystem und Ihre persönlichen Daten zu gewährleisten, können Sie Programme von Drittherstellern
SafeRun-Modus: Die Sichere Umgebung für die Ausführung von Programmen Um die maximale Sicherheit für das Betriebssystem und Ihre persönlichen Daten zu gewährleisten, können Sie Programme von Drittherstellern
Abamsoft Finos im Zusammenspiel mit shop to date von DATA BECKER
 Abamsoft Finos im Zusammenspiel mit shop to date von DATA BECKER Abamsoft Finos in Verbindung mit der Webshopanbindung wurde speziell auf die Shop-Software shop to date von DATA BECKER abgestimmt. Mit
Abamsoft Finos im Zusammenspiel mit shop to date von DATA BECKER Abamsoft Finos in Verbindung mit der Webshopanbindung wurde speziell auf die Shop-Software shop to date von DATA BECKER abgestimmt. Mit
FRAGE 39. Gründe, aus denen die Rechte von Patentinhabern beschränkt werden können
 Jahrbuch 1963, Neue Serie Nr. 13, 1. Teil, 66. Jahrgang, Seite 132 25. Kongress von Berlin, 3. - 8. Juni 1963 Der Kongress ist der Auffassung, dass eine Beschränkung der Rechte des Patentinhabers, die
Jahrbuch 1963, Neue Serie Nr. 13, 1. Teil, 66. Jahrgang, Seite 132 25. Kongress von Berlin, 3. - 8. Juni 1963 Der Kongress ist der Auffassung, dass eine Beschränkung der Rechte des Patentinhabers, die
Lizenzierung von System Center 2012
 Lizenzierung von System Center 2012 Mit den Microsoft System Center-Produkten lassen sich Endgeräte wie Server, Clients und mobile Geräte mit unterschiedlichen Betriebssystemen verwalten. Verwalten im
Lizenzierung von System Center 2012 Mit den Microsoft System Center-Produkten lassen sich Endgeräte wie Server, Clients und mobile Geräte mit unterschiedlichen Betriebssystemen verwalten. Verwalten im
www.01805- telefonkonferenz.de für Endanwender
 www.01805- telefonkonferenz.de für Endanwender Sofort-Konferenzen ohne Anmeldung Kurzanleitung Inhaltsverzeichnis 1 Einführung...2 2 Sofort-Konferenz führen...4 3 Konferenz mit Einladung führen...4 4 Impressum...7
www.01805- telefonkonferenz.de für Endanwender Sofort-Konferenzen ohne Anmeldung Kurzanleitung Inhaltsverzeichnis 1 Einführung...2 2 Sofort-Konferenz führen...4 3 Konferenz mit Einladung führen...4 4 Impressum...7
Zahlenwinkel: Forscherkarte 1. alleine. Zahlenwinkel: Forschertipp 1
 Zahlenwinkel: Forscherkarte 1 alleine Tipp 1 Lege die Ziffern von 1 bis 9 so in den Zahlenwinkel, dass jeder Arm des Zahlenwinkels zusammengezählt das gleiche Ergebnis ergibt! Finde möglichst viele verschiedene
Zahlenwinkel: Forscherkarte 1 alleine Tipp 1 Lege die Ziffern von 1 bis 9 so in den Zahlenwinkel, dass jeder Arm des Zahlenwinkels zusammengezählt das gleiche Ergebnis ergibt! Finde möglichst viele verschiedene
InVo. Information zu Verordnungen in der GKV. Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen. Stand: Februar 2010
 Nr. 1 2010 InVo Information zu Verordnungen in der GKV Stand: Februar 2010 Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen Bisher konnten Sie als Arzt Arzneimittel (z. B.
Nr. 1 2010 InVo Information zu Verordnungen in der GKV Stand: Februar 2010 Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen Bisher konnten Sie als Arzt Arzneimittel (z. B.
impact ordering Info Produktkonfigurator
 impact ordering Info Copyright Copyright 2013 veenion GmbH Alle Rechte vorbehalten. Kein Teil der Dokumentation darf in irgendeiner Form ohne schriftliche Genehmigung der veenion GmbH reproduziert, verändert
impact ordering Info Copyright Copyright 2013 veenion GmbH Alle Rechte vorbehalten. Kein Teil der Dokumentation darf in irgendeiner Form ohne schriftliche Genehmigung der veenion GmbH reproduziert, verändert
sm@rt-tan plus Flickerfeld bewegt sich nicht
 Technischer Hintergrund Um die Verwendung des Verfahrens Sm@rt-TAN plus des neuen sicheren TAN- Verfahrens so komfortabel wie möglich zu gestalten, wurde eine Möglichkeit geschaffen, die Angaben einer
Technischer Hintergrund Um die Verwendung des Verfahrens Sm@rt-TAN plus des neuen sicheren TAN- Verfahrens so komfortabel wie möglich zu gestalten, wurde eine Möglichkeit geschaffen, die Angaben einer
IhreInsulinfunktionen
 Insulinfunktionen: Insulinfunktionen: Wichtige Wichtige Informationen BlutzuckerBlutzucker-und undketon-messsystem Keton-Messsystem Ihre IhreInsulinfunktionen Insulinfunktionen Die DieInsulineinstellungen
Insulinfunktionen: Insulinfunktionen: Wichtige Wichtige Informationen BlutzuckerBlutzucker-und undketon-messsystem Keton-Messsystem Ihre IhreInsulinfunktionen Insulinfunktionen Die DieInsulineinstellungen
Immunserologie III. ELISA, Western-blot, Dot-blot
 Immunserologie III. ELISA, Western-blot, Dot-blot Universität ität Pécs, Medizinische Fakul ultät Institut für Immunologie und Biotechnologie ie ELISA 1. - Grundlagen o Enzyme o Linked o Immuno o Sorbent
Immunserologie III. ELISA, Western-blot, Dot-blot Universität ität Pécs, Medizinische Fakul ultät Institut für Immunologie und Biotechnologie ie ELISA 1. - Grundlagen o Enzyme o Linked o Immuno o Sorbent
Garantie und Pflegehinweise für dormabell Bettsysteme
 Garantie und Pflegehinweise für dormabell Bettsysteme Vielen Dank sehr geehrter Kunde, Sie haben sich für ein dormabell Produkt entschieden, das in Material und Verarbeitung unserem hohen Qualitätsverständnis
Garantie und Pflegehinweise für dormabell Bettsysteme Vielen Dank sehr geehrter Kunde, Sie haben sich für ein dormabell Produkt entschieden, das in Material und Verarbeitung unserem hohen Qualitätsverständnis
Die Gesellschaftsformen
 Jede Firma - auch eure Schülerfirma - muss sich an bestimmte Spielregeln halten. Dazu gehört auch, dass eine bestimmte Rechtsform für das Unternehmen gewählt wird. Für eure Schülerfirma könnt ihr zwischen
Jede Firma - auch eure Schülerfirma - muss sich an bestimmte Spielregeln halten. Dazu gehört auch, dass eine bestimmte Rechtsform für das Unternehmen gewählt wird. Für eure Schülerfirma könnt ihr zwischen
4. AUSSAGENLOGIK: SYNTAX. Der Unterschied zwischen Objektsprache und Metasprache lässt sich folgendermaßen charakterisieren:
 4. AUSSAGENLOGIK: SYNTAX 4.1 Objektsprache und Metasprache 4.2 Gebrauch und Erwähnung 4.3 Metavariablen: Verallgemeinerndes Sprechen über Ausdrücke von AL 4.4 Die Sprache der Aussagenlogik 4.5 Terminologie
4. AUSSAGENLOGIK: SYNTAX 4.1 Objektsprache und Metasprache 4.2 Gebrauch und Erwähnung 4.3 Metavariablen: Verallgemeinerndes Sprechen über Ausdrücke von AL 4.4 Die Sprache der Aussagenlogik 4.5 Terminologie
Verband der TÜV e. V. STUDIE ZUM IMAGE DER MPU
 Verband der TÜV e. V. STUDIE ZUM IMAGE DER MPU 2 DIE MEDIZINISCH-PSYCHOLOGISCHE UNTERSUCHUNG (MPU) IST HOCH ANGESEHEN Das Image der Medizinisch-Psychologischen Untersuchung (MPU) ist zwiespältig: Das ist
Verband der TÜV e. V. STUDIE ZUM IMAGE DER MPU 2 DIE MEDIZINISCH-PSYCHOLOGISCHE UNTERSUCHUNG (MPU) IST HOCH ANGESEHEN Das Image der Medizinisch-Psychologischen Untersuchung (MPU) ist zwiespältig: Das ist
Scheper Ziekenhuis Emmen. Tel.: + 31 (0) 591-691 320 Fax: + 31 (0) 591-691 321 Web: www.plastici.nl
 Scheper Ziekenhuis Emmen Tel.: + 31 (0) 591-691 320 Fax: + 31 (0) 591-691 321 Web: www.plastici.nl PREISE Wir bieten Ihnen Brustvergrößerungen von 3000,- bis 5.500,- Euro an. ALLGEMEINE INFORMATIONEN Die
Scheper Ziekenhuis Emmen Tel.: + 31 (0) 591-691 320 Fax: + 31 (0) 591-691 321 Web: www.plastici.nl PREISE Wir bieten Ihnen Brustvergrößerungen von 3000,- bis 5.500,- Euro an. ALLGEMEINE INFORMATIONEN Die
SICHERN DER FAVORITEN
 Seite 1 von 7 SICHERN DER FAVORITEN Eine Anleitung zum Sichern der eigenen Favoriten zur Verfügung gestellt durch: ZID Dezentrale Systeme März 2010 Seite 2 von 7 Für die Datensicherheit ist bekanntlich
Seite 1 von 7 SICHERN DER FAVORITEN Eine Anleitung zum Sichern der eigenen Favoriten zur Verfügung gestellt durch: ZID Dezentrale Systeme März 2010 Seite 2 von 7 Für die Datensicherheit ist bekanntlich
Tevalo Handbuch v 1.1 vom 10.11.2011
 Tevalo Handbuch v 1.1 vom 10.11.2011 Inhalt Registrierung... 3 Kennwort vergessen... 3 Startseite nach dem Login... 4 Umfrage erstellen... 4 Fragebogen Vorschau... 7 Umfrage fertigstellen... 7 Öffentliche
Tevalo Handbuch v 1.1 vom 10.11.2011 Inhalt Registrierung... 3 Kennwort vergessen... 3 Startseite nach dem Login... 4 Umfrage erstellen... 4 Fragebogen Vorschau... 7 Umfrage fertigstellen... 7 Öffentliche
1. Weniger Steuern zahlen
 1. Weniger Steuern zahlen Wenn man arbeitet, zahlt man Geld an den Staat. Dieses Geld heißt Steuern. Viele Menschen zahlen zu viel Steuern. Sie haben daher wenig Geld für Wohnung, Gewand oder Essen. Wenn
1. Weniger Steuern zahlen Wenn man arbeitet, zahlt man Geld an den Staat. Dieses Geld heißt Steuern. Viele Menschen zahlen zu viel Steuern. Sie haben daher wenig Geld für Wohnung, Gewand oder Essen. Wenn
A.u.S. Spielgeräte GmbH A-1210 Wien Scheydgasse 48 Tel.+43-(0)1-271 66 00 Fax. +43-(0)1-271 66 00 75
 Inhaltsverzeichnis Seite 1. Einleitung. 2 2. Vorraussetzung.. 2 2.1 Software 2 2.2 Hardware.. 2 3. Vorbereitung... 3 4. Programmierung 4 5. Ändern des Schlüssels... 6 6. Test 6 7. Informationen.. 7 1.Einleitung
Inhaltsverzeichnis Seite 1. Einleitung. 2 2. Vorraussetzung.. 2 2.1 Software 2 2.2 Hardware.. 2 3. Vorbereitung... 3 4. Programmierung 4 5. Ändern des Schlüssels... 6 6. Test 6 7. Informationen.. 7 1.Einleitung
