HVG-Mitteilung Nr Zur Steuerbarkeit des Redoxzustands mit Sulfat und Kohle
|
|
|
- Mina Sommer
- vor 5 Jahren
- Abrufe
Transkript
1 HVG-Mitteilung Nr Zur Steuerbarkeit des Redoxzustands mit Sulfat und Kohle Hayo Müller-Simon, Hüttentechnische Vereinigung der Deutschen Glasindustrie, Offenbach 1 Einleitung In einem aktuellen Forschungsvorhaben zur Anreicherung störender Komponenten durch Recycling wird ein System von Modellen entwickelt, das die Vorgänge im Schmelzprozess mit den Anreicherungsvorgängen in den Kreisläufen des Produkt- und des Filterstaub- Recycling verknüpft. Diese Modelle sollen zunächst mit vorhandenen Messdaten getestet werden. Dazu werden die Messergebnisse aus früheren Forschungsaktivitäten zur Redoxchemie, Sulfatläuterung, Selenentfärbung und Boremissionen aufbereitet und verfügbar gemacht [5,6]. Durch eine inzwischen effektivere Programmiertechnik lassen sich Zusammenhänge sichtbar machen, die bisher unbeachtet blieben. Im Folgenden sollen solche Zusammenhänge für den Einsatz von Sulfat und Kohle bei der industriellen Glasschmelze dokumentiert werden. 2 Redoxzahlsysteme Die Ergebnisse der Qualitätskontrolle haben den Nachteil, dass die Messergebnisse erst am Ende des Produktionsprozesses zur Verfügung stehen. Geht man aber davon aus, dass der Redoxzustand der Glasschmelze maßgeblich durch das Gemenge bestimmt wird, so stünde durch eine entsprechende Kennzahl die Information schon zu Beginn des Prozesses zur Verfügung. Um den Oxidationszustand eines Gemenges zu kennzeichnen, wurden in der Vergangenheit mehrere Redoxzahlkonzepte entwickelt. Die Basis dieser Konzepte bildet die in den 1950iger Jahren von Manring und Hopkins entwickelte Carbon Number. Dieses Konzept folgt einem einfachen System, das davon ausgeht, dass Natriumsulfat und Kohle im Gemenge entsprechend der Gleichung
2 Zur Steuerbarkeit des Redoxzustands mit Sulfat und Kohle 2Na 2 SO 4 + C Na 2 O + 2SO 2 + CO 2 (1) miteinander reagieren. Dabei wird angenommen, dass die Reaktionsprodukte den Redoxzustand nicht weiter beeinflussen, d. h. neutral sind, wenn die Reaktion 1 stöchiometrisch abläuft. Unter diesen Bedingungen würde ein Mol Kohlenstoff genau durch 2 Mol Natriumsulfat neutralisiert werden. Setzt man die entsprechenden Molgewichte für Kohle (12) und Natriumsulfat (142) ein, so wird eine Gewichtseinheit Kohle durch 23,6 Gewichtseinheiten Natriumsulfat neutralisiert. Um diesen Zusammenhang in der Praxis anwenden zu können, führten Manring und Hopkins relative Faktoren ein, mit denen die Komponenten eines Gemengesatzes bezüglich ihres Redoxpotentials gewichtet werden konnten. Darin erhalten reduzierende Bestandteile negative Faktoren und oxidierende Bestandteile positive Faktoren. Als Bezugspunkt gaben sie einer Gewichtseinheit Kohlenstoff willkürlich den Wert -16. Wenn 1 kg Kohlenstoff den Faktor -16 erhält, so müssen 23,7 kg Natriumsulfat, die diese Menge Kohlenstoff nach Gleichung 1 neutralisieren, den Wert +16 erhalten. Damit erhält 1 kg Natriumsulfat den Redoxfaktor: Redoxfaktor(Na 2 SO 4 ) = 16 23, 6 = +0, 67 (2) Für reduzierende Komponenten zieht man die Reaktion mit Natriumsulfat heran. CaS + 3Na 2 SO 4 3Na 2 O + CaO + 4SO 2 (3) , 67 Redoxfaktor(CaS) = = 4 (4) 72 Auf diese Weise kann für jeden Rohstoff ein theoretischer Redoxfaktor ermittelt werden. Um aus den Redoxfaktoren den Oxidationszustand eines Gemenges zu berechnen, wird der Anteil einer Gemengekomponente mit dem jeweiligen Redoxfaktor gewichtet und über alle Komponenten i summiert: Redoxfaktor(i) Gewichtsanteile(i) (5) i Der Anteil der Gemengekomponenten wird auf eine Charge mit 2000 kg Sand bezogen. Schon die ersten Versuche zeigten, dass diese theoretischen Faktoren nicht dem beobachteten Verhalten entsprechen. Insbesondere die Kohle ist in der Praxis weit weniger wirksam, als der theoretische Faktor der carbon number annehmen lässt. Diese Tatsache trat insbesondere zutage, wenn der Redoxzustand einer Schmelze bei der Umstellung von Kohle/Sulfat auf Calumite konstant bleiben sollte. Simpson und Myers modifizierten deshalb die von Manring und Hopkins angegebenen Faktoren [8]. Dabei beließen sie die Faktoren für die oxidierenden Gemengekomponenten bei den Faktoren der carbon number. Die wesentliche Änderung ist die Absenkung des Faktors für Kohle auf -6,7. Dieser modifizierte Wert wurde empirisch ermittelt und beruht maßgeblich auf den Erfahrungen, die mit der Umstellung von Sulfat/Kohle auf Calumite gemacht wurden. Die
3 HVG-Mitteilung Nr Abbildung 1: Abhängigkeit des Fe 2+ /Fe 3+ -Verhältnis als Funktion der CSB-Redoxzahl berechnet nach Daten aus [2] und [1] Redoxzahl wird heute, wohl hauptsächlich wegen ihrer Einfachheit, in vielen Glashütten benutzt. Alternativ dazu wurde ein Konzept entwickelt, bei dem die reduzierende Wirkung der Rohstoffe experimentell bestimmt wird [4]. Über den chemischen Sauerstoffbedarf (CSB) der Rohstoffe wird eine äquivalente Kohlenstoffmenge ermittelt, die bei der Berechnung der Redoxzahl nach Gleichung 1 eingesetzt wird. Diese CSB-Redoxzahl ist zwar aufwendiger, hat jedoch den Vorteil, experimentell abgesicherte Aussagen über den Redoxzustand des Gemenges machen zu können. Genauere Zusammenhänge sind allenfalls mit der CSB-Redoxzahl zu erarbeiten, weil die oxidierende bzw. reduzierende Wirkung von Filterstäuben und Scherben sehr stark schwanken. In dieser Mitteilung wird die CSB-Redoxzahl verwendet, wobei für den CSB-Wert soweit nicht gemessen Schätzwerte verwendet werden. 3 Befunde 3.1 Literatur In der Literatur befassen sich zwei Arbeiten eingehender mit dem Einfluss der Sulfat- Zugabe zu Glasgemengen [1, 2]. Dabei zeigt sich eine auffällige Nicht-Linearität des Redoxzustands des Eisens von der Kohlezugabe. Eine weitere Abhängigkeit besteht von der Sulfatzugabe. Diese verschiebt den Zusammenhang zwischen der Kohlezugabe und dem Redoxzustand des Eisens in Richtung höherer Kohlezugaben. Dieses Verhalten ähnelt einer Titration, d.h. die Kohle wird durch die direkte Reaktion mit dem Sulfat verbraucht
4 Zur Steuerbarkeit des Redoxzustands mit Sulfat und Kohle Tabelle 1: Hauptkomponenten der Gläser und Schmelzbedingungen bei den Laborversuchen [1] [2] Hauptkomponenten 66.9 % SiO % SiO % B 2 O % Na 2 O 14.8 % Na 2 O 10.8 % CaO 8.3 % CaO Chargengröße ca. 1 kg ca. 200 g Beheizung Gas Gas Sauerstoffüberschuss 1 % 3 % Schmelzdauer 2.5 h 4 h Schmelztemperatur 1470 C 1450 C In Abb. 1 sind diese Abhängigkeiten zusammengefasst. Für die Ausgleichskurven wurde eine tanh-funktion gewählt: log F e2+ A = 0.65 tanhredoxzahl F e3+ B Darin ist A die Verschiebung der Kurven in Abhängigkeit von der Schwefelzugabe und B die Steilheit der Kurven. B muss mit zunehmender Sulfat-Zugabe größer gewählt werden. Da die beiden untersuchten Gläser verschiedene Bereiche für die Sulfat-Zugabe abdecken, lässt sich nicht entscheiden, ob das Verhalten von B eine grundsätzliche Änderung der Kurvenform von der Sulfat-Zugabe darstellt oder sich aus der unterschiedlichen Glaszusammensetzung ergibt. Auch ein Einfluss der Schmelzbedingungen kann nicht ausgeschlossen werden (s. Tab. 1). (6) 3.2 Industrie-Messungen In industriell erschmolzenen Gläsern ist der Nachweis dieser Zusammenhänge schwieriger, weil sowohl die Kohlezugabe als auch die Sulfatzugabe ständigen Variationen unterliegen. Das gilt insbesondere beim Einsatz von Recycling-Scherben oder Filterstaub. Messungen des CSB an Altglasscherben liegen zwischen 500 und 1500 ppm C. Für die Abschätzung der CSB-Werte wurde ein mittlerer Wert von 1000 ppm angesetzt. Filterstäube enthalten zwischen 20 und 45 % SO 3. Für die Berechnungen wurde ein mittlerer SO 3 -Gehalt von 35 % angesetzt. Abb. 2 zeigt analog zu Abb. 1 Ergebnisse von Messungen an 6 weißen, 3 grünen und 7 braunen Gläsern. Dabei handelt es sich um Mittelwerte, die einem stationären Zustand zugeordnet werden können. In Abb. 2 deutet sich sowohl bei den oxidierend geschmolzenen Gläsern als auch bei den reduzierend geschmolzenen Gläsern ein minimales bzw. maximales Fe 2+ /Fe 3+ -Verhältnis in Übereinstimmung mit Abb. 1 an. Bei
5 HVG-Mitteilung Nr Abbildung 2: Fe 2+ /Fe 3+ -Verhältnis als Funktion der CSB-Redoxzahl für 6 weiße, 3 grüne und 7 braune unter annähernd stationären Bedingungen erschmolzene Gläser mittleren Fe 2+ /Fe 3+ -Verhältnissen findet man eine breite Streuung der zugehörigen CSB- Redoxzahlen des eingesetzten Gemenges. Die Variationen bei mittleren Fe 2+ /Fe 3+ -Verhältnissen sollten nach [1] und [2] auf die unterschiedlichen Sulfat-Zugaben zurückgeführt werden können. Um das nachzuweisen, sind in Abb. 3 sechs Industriemessungen detaillierter dargestellt. Die Verschiebung der Kurven nach Gleichung 6 lässt sich für zwei grüne und eine weiße Glasschmelze überprüfen. Die Verschiebung A ist für diese Gläser und die Werte aus Abb. 1 in Abb. 4 zusammengestellt. Eine Erhöhung der Sulfat-Zugabe führt sowohl bei den Labor- als auch bei den Industrieschmelzen zu einer Verschiebung der Kurven in Richtung größerer Kohle-Zugabe. Die beiden Braungläser und ein Weißglas sind in Abb. 3 den Extremwerten des Fe 2+ /Fe 3+ -Verhältnisses zuzuordnen und lassen sich bezüglich Abb. 4 nicht auswerten. Allerdings lassen sich umgekehrt aus Abb. 4 die zu den gegebenen Sulfat- Zugaben gehörigen Verschiebungen A in Gleichung 6 ablesen. Die entsprechenden Kurven sind in Abb. 3 gestrichelt eingezeichnet und spiegeln das Verhalten der Messergebnisse korrekt wider. 4 Diskussion Trotz der sehr groben Bestimmung der CSB-Redoxzahl spiegeln die Abbildungen 2 und 3 gut das Verhalten der Laborschmelzen in Abb. 1 wider. In Abb. 1 lassen sich für eine gegebene Sulfatzugabe drei Bereiche unterscheiden: Unter sehr reduzierenden und sehr oxidie
6 Zur Steuerbarkeit des Redoxzustands mit Sulfat und Kohle Abbildung 3: Fe 2+ /Fe 3+ -Verhältniss als Funktion der CSB-Redoxzahl für 6 industriell erschmolzene Gläser Abbildung 4: Verschiebung der Ausgleichskurven durch die Sulfat-Zugabe
7 HVG-Mitteilung Nr Abbildung 5: Sauerstoffpartialdruck als Funktion der CSB-Redoxzahl für die Gläser in Abb. 2 renden Bedingungen ist das Fe 2+ /Fe 3+ -Verhältnis nahezu unabhängig von Änderungen der Kohle-Zugabe, dazwischen besteht eine näherungsweise lineare Abhängigkeit. Sauerstoffpartialdruck-Messungen (s. Abb. 5) zeigen ein ähnliches Verhalten wie die das Fe 2+ /Fe 3+ -Verhältnis in Abb. 2. Diese Abhängigkeit ergibt sich aus dem thermodynamischen Zusammenhang zwischen Sauerstoffpartialdruck und Fe 2+ /Fe 3+ -Verhältnis [3]. Der theoretische Verlauf ist gemeinsam mit den Messwerten für die untersuchten Gläser in Abb. 6 zu sehen. Die Messwerte folgen näherungsweise dem theoretischen Verlauf. Allerdings führen eine Reihe von Messungenauigkeiten zu der beobachteten Schwankungsbreite: die Fe 2+ /Fe 3+ -Verhältnisse wurden in verschiedenen (Werks-)Laboren mit unterschiedlichen Messverfahren gemessen, die Temperaturen der Sauerstoffpartialdruck-Messungen variieren zwischen 1100 und 1300 C, das Fe 2+ /Fe 3+ -Verhältnis verschiebt sich beim Abkühlen [7]. Trotz der Streubreite der Messdaten darf aus den Abbildungen 2, 5 und 6 geschlossen werden, dass die Extremwerte des Fe 2+ /Fe 3+ -Verhältnisses spezifischen Gleichgewichten zuzuordnen sind. Die Existenz eines Plateaus des Fe 2+ /Fe 3+ -Verhältnis ist in der Literatur dokumentiert [3, 7]. Es liegt je nach Gleichgewichtstemperatur und Glaszusammensetzung bei log Fe 2+ /Fe 3+ = 0,8-1,3. Dieser Wert wird bei Sauerstoffpartialdrücken zwischen 10 8 und bar erreicht. Verursacht wird das Plateau durch die Bildung von
8 Zur Steuerbarkeit des Redoxzustands mit Sulfat und Kohle Abbildung 6: Zusammenhang zwischen Fe 2+ /Fe 3+ -Verhältnis und Sauerstoffpartialdruck für die Gläser in Abb. 2 metallischem Eisen, das sich als eigene Phase ausscheidet. Die zugehörigen Sauerstoffpartialdrücke weichen sowohl in Abb. 5 als auch in Abb. 6 deutlich vom Verlauf der übrigen Messwerte ab. Nach Abb. 5 scheint das zugehörige Gleichgewicht, das den Messergebnissen aus [2] und [1] entspricht, eher bei 10 5 bar zu liegen. Dieser Sauerstoffpartialdruck und das zugehörige Fe 2+ /Fe 3+ -Verhältnis lassen sich mit einem Gleichgewicht, das auf einer CO 2 -Sättigung beruht erklären [3]. Auf der oxidierenden Seite liegt es nah, eine Sättigung mit SO 3 anzunehmen [2]. Der dem entsprechende Sauerstoffpartialdruck von log po 2 = -0,5 und das entsprechende Redoxverhältnis des Eisen von log Fe 2+ /Fe 3+ von -1,4 stimmen allerdings nicht mit den Befunden in Abb. 1, 2 bzw. 5 überein. Abb. 4 zeigt einen vergleichbaren Einfluss der Sulfatzugabe auf die Verschiebung A in Gleichung 6. Allerdings erscheint der Verlauf deutlich steiler. Dieser Unterschied ist möglicherweise eine Folge der Wahl der Steilheit B für die Ausgleichskurven der Industrie-Messungen. Insgesamt stellt die Anpassung mit dem Tangens hyperbolicus eine recht grobe Näherung dar. Hier könnte eine Anpassung über eine Modellierung der Abläufe im Gemenge, wie sie für das laufende Projekt geplant ist, eine Verbesserung bringen. Was bedeuten diese Befunde nun für die Schwefelzugabe unter Industriebedingungen. Die Schwefelzugabe muss drei Randbedingungen genügen: die Glasschmelze muss ausreichend geläutert werden, redoxabhängige Eigenschaften wie die Farbe müssen sicher eingestellt werden und
9 HVG-Mitteilung Nr Abbildung 7: Zusammenfassung die Emissionen müssen die gegebenen Grenzwerte einhalten. Abb. 7 fasst die Möglichkeiten für eine Redoxregelung durch Sulfat- bzw. Kohle- Zugabe zusammen. Redoxabhängige Eigenschaften wie die Farbe lassen sich nur in dem mittleren Bereich durch Variation der Kohle-Zugabe ändern. Umgekehrt ist die Produktion in den Randbereichen von Vorteil beim Einsatz von Rohstoffen mit stark schwankenden Redoxeigenschaften wie Recycling-Scherben. Auch die Variation der Sulfat-Konzentration im Filterstaub hat im Bereich der Sättigung keinen Einfluss, solange der Übergangsbereich ausreichend weit vom aktuellen Arbeitspunkt entfernt ist. Literatur [1] Barton, J.L. ; Chopinet, M.-H.: The problem of predicting the redox state of a glass. In: Proc. 1st Int. Conf. on Adv. Fusion Glass (1988) [2] Bassine, J. F. ; Mestdagh, M. M. ; Rouxhet, P. G. ; Cangh, L. V.: Redox buffering by sulphate and carbonate during the melting of reduced soda-lime-silica glasses. In: Glass Technol. 28 (1987) [3] Johnston, W. D.: Oxidation-Reduction Equilibria in Iron-Containing Glass. In: J. Am. Ceram. Soc. 47 (1964), S [4] Manring, W.H. ; Diken, G.M.: A practical approach to evaluating redox phenomena involved in the melting-fining of soda-lime glasses. In: J. Non-Cryst. Solids (1980)
10 Zur Steuerbarkeit des Redoxzustands mit Sulfat und Kohle [5] Müller-Simon, H.: Schlussbericht zum AiF/IGF-Foraschungsvorhaben Nr N: Messanordnung zur Kontrolle der Farbe und des Läuterzustandes industrieller Glasschmelzen. / Hüttentechnische Vereinigung der Deutschen Glasindustrie e.v Forschungsbericht [6] Müller-Simon, H.: Schlussbericht zum AiF/IGF-Forschungsvorhaben Nr N: Minderung der Schwefelemissionen industrieller Glasschmelzaggregaete durch die Einstellung optimaler Läuterung mit einer Regelstrecke. / Hüttentechnische Vereinigung der Deutschen Glasindustrie e.v Forschungsbericht [7] Müller-Simon, H. ; Hüttentechnische Vereinigung der Deutschen Glasindustrie (Hrsg.): Elektronenaustausch zwischen Paaren polyvalenter Elemente in technischen Gläsern und seine Auswirkungen auf die industrielle Glasherstellung. Verlag der Deutschen Glastechnischen Gesellschaft, 2007 [8] Simpson, W. ; Myers, D. D.: The redox number concept and ist use by the glass technologist. In: Glass Technology 19 (1978), S
HVG-Mitteilung Nr. 2093
 HVG-Mitteilung Nr. 9 Redox-Reaktionen polyvalenter Elemente im Laborversuch und in industriellen Glasschmelzen Hayo Müller-Simon, Hüttentechnische Vereinigung der Deutschen Glasindustrie, Offenbach Vortrag
HVG-Mitteilung Nr. 9 Redox-Reaktionen polyvalenter Elemente im Laborversuch und in industriellen Glasschmelzen Hayo Müller-Simon, Hüttentechnische Vereinigung der Deutschen Glasindustrie, Offenbach Vortrag
HVG-Mitteilung Nr Gasfreisetzung während der Läuterung: Vergleich von Messung und Berechnung
 HVG-Mitteilung Nr. 2071 Gasfreisetzung während der Läuterung: Vergleich von Messung und Berechnung D.Köpsel, O. Claußen, W.Rausch, Schott Glas, Mainz Einleitung Das wichtigste Kriterium bei der Auswahl
HVG-Mitteilung Nr. 2071 Gasfreisetzung während der Läuterung: Vergleich von Messung und Berechnung D.Köpsel, O. Claußen, W.Rausch, Schott Glas, Mainz Einleitung Das wichtigste Kriterium bei der Auswahl
Struktur von Kalk-Natron-Silicatgläsern
 Erfordernisse an silicatische Rohstoffe für die Glasindustrie Priv.-Doz. Dr.-Ing. Hayo Müller-Simon Hüttentechnische Vereinigung g der Deutschen Glasindustrie Offenbach/Main HVG-DGG Struktur von Kalk-Natron-Silicatgläsern
Erfordernisse an silicatische Rohstoffe für die Glasindustrie Priv.-Doz. Dr.-Ing. Hayo Müller-Simon Hüttentechnische Vereinigung g der Deutschen Glasindustrie Offenbach/Main HVG-DGG Struktur von Kalk-Natron-Silicatgläsern
HVG-Mitteilung Nr Modifikation von Glasoberflächen mit Metallhalogeniden und Ammoniumverbindungen
 HVG-Mitteilung Nr. 2136 Modifikation von Glasoberflächen mit Metallhalogeniden und Ammoniumverbindungen A. Nadolny, TU Bergakademie Freiberg Vortrag in der gemeinsamen Sitzung der Fachausschüsse II und
HVG-Mitteilung Nr. 2136 Modifikation von Glasoberflächen mit Metallhalogeniden und Ammoniumverbindungen A. Nadolny, TU Bergakademie Freiberg Vortrag in der gemeinsamen Sitzung der Fachausschüsse II und
7 Gültige und zukünftige Richtlinien auf dem Gebiet der Druckentlastung
 Eine Verbesserung der Übereinstimmung zwischen berechneten und experimentellen Druck- Zeit-Kurven lässt sich sicherlich auch durch Verfeinerung des Reaktionsmodells erzielen. FLUENT bietet diese Möglichkeit.
Eine Verbesserung der Übereinstimmung zwischen berechneten und experimentellen Druck- Zeit-Kurven lässt sich sicherlich auch durch Verfeinerung des Reaktionsmodells erzielen. FLUENT bietet diese Möglichkeit.
5. Statistische Auswertung
 5. Statistische Auswertung 5.1 Varianzanalyse Die Daten der vorliegenden Versuchsreihe zeigen eine links steile, rechts schiefe Verteilung. Es wird untersucht, ob sich die Meßdaten durch Transformation
5. Statistische Auswertung 5.1 Varianzanalyse Die Daten der vorliegenden Versuchsreihe zeigen eine links steile, rechts schiefe Verteilung. Es wird untersucht, ob sich die Meßdaten durch Transformation
HVG-Mitteilung Nr Anwendung statistischer Methoden für die Analyse von Messungen in der Glasproduktion. (IGF/AiF-Forschungsvorhaben Nr.
 HVG-Mitteilung Nr. 2171 Anwendung statistischer Methoden für die Analyse von Messungen in der Glasproduktion. (IGF/AiF-Forschungsvorhaben Nr.18270 N) Hayo Müller-Simon, Hüttentechnische Vereinigung der
HVG-Mitteilung Nr. 2171 Anwendung statistischer Methoden für die Analyse von Messungen in der Glasproduktion. (IGF/AiF-Forschungsvorhaben Nr.18270 N) Hayo Müller-Simon, Hüttentechnische Vereinigung der
Messung der Driftgeschwindigkeit von Elektronen in Gasen
 Messung der Driftgeschwindigkeit von Elektronen in Gasen Versuch Nr. 1 Ausarbeitung -. Oktober 01 Ausgearbeitet von Martin Günther und Nils Braun 1 Durchführung und Rechnung Im Versuch wurde wie in der
Messung der Driftgeschwindigkeit von Elektronen in Gasen Versuch Nr. 1 Ausarbeitung -. Oktober 01 Ausgearbeitet von Martin Günther und Nils Braun 1 Durchführung und Rechnung Im Versuch wurde wie in der
Applikationsfeld / Industriezweig:
 Applikationsfeld / Industriezweig: Chemie / Polymerindustrie Elektronik Energie Ernährung / Landwirtschaft Geologie / Bergbau Halbleiter-Technologie Klinische Chemie / Medizin / Hygiene / Gesundheitswesen
Applikationsfeld / Industriezweig: Chemie / Polymerindustrie Elektronik Energie Ernährung / Landwirtschaft Geologie / Bergbau Halbleiter-Technologie Klinische Chemie / Medizin / Hygiene / Gesundheitswesen
Schmelzdiagramme Kornelia Schmid & Jelena Cikoja Gruppe 150. Schmelzdiagramme
 Schmelzdiagramme 1. Aufgabenstellung: Im Versuch sollen die Schmelzpunkte von 7 Gemischen unterschiedlicher Zusammensetzung aus den Komponenten Biphenyl (A) und Naphthalin (B) bestimmt werden. Anschließend
Schmelzdiagramme 1. Aufgabenstellung: Im Versuch sollen die Schmelzpunkte von 7 Gemischen unterschiedlicher Zusammensetzung aus den Komponenten Biphenyl (A) und Naphthalin (B) bestimmt werden. Anschließend
endotherme Reaktionen
 Exotherme/endotherme endotherme Reaktionen Edukte - H Produkte Exotherme Reaktion Edukte Produkte + H Endotherme Reaktion 101 Das Massenwirkungsgesetz Das Massenwirkungsgesetz Gleichgewicht chemischer
Exotherme/endotherme endotherme Reaktionen Edukte - H Produkte Exotherme Reaktion Edukte Produkte + H Endotherme Reaktion 101 Das Massenwirkungsgesetz Das Massenwirkungsgesetz Gleichgewicht chemischer
Lösung 7. Allgemeine Chemie I Herbstsemester Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf.
 Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan
 Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Zustandsgleichung....... 2 2.2. Koexistenzgebiet........ 3 2.3. Kritischer
Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Zustandsgleichung....... 2 2.2. Koexistenzgebiet........ 3 2.3. Kritischer
Praktikum Physik. Protokoll zum Versuch: Oberflächenspannung. Durchgeführt am Gruppe X
 Praktikum Physik Protokoll zum Versuch: Oberflächenspannung Durchgeführt am 02.02.2012 Gruppe X Name 1 und Name 2 (abc.xyz@uni-ulm.de) (abc.xyz@uni-ulm.de) Betreuer: Wir bestätigen hiermit, dass wir das
Praktikum Physik Protokoll zum Versuch: Oberflächenspannung Durchgeführt am 02.02.2012 Gruppe X Name 1 und Name 2 (abc.xyz@uni-ulm.de) (abc.xyz@uni-ulm.de) Betreuer: Wir bestätigen hiermit, dass wir das
1 Relaxationskinetik der Neutralisationsreaktion in Wasser
 Physikalische Chemie II Lösung 6 28. Oktober 206 Relaxationskinetik der Neutralisationsreaktion in Wasser. Für die Reaktion A + B definiert man die Auslenkungsvariable x so, dass gilt k a kb 2P [A] = [A]
Physikalische Chemie II Lösung 6 28. Oktober 206 Relaxationskinetik der Neutralisationsreaktion in Wasser. Für die Reaktion A + B definiert man die Auslenkungsvariable x so, dass gilt k a kb 2P [A] = [A]
HVG-Mitteilung Nr Optische Emissionsspektroskopie an eisenhaltigen Gläsern (HVG/AiF-Forschungsvorhaben Nr BR)
 HVG-Mitteilung Nr. 294 (HVG/AiF-Forschungsvorhaben Nr. 13653 BR) A. Baum, M. Müller, C. Rüssel, Otto-Schott-Institut für Glaschemie, Jena Vortrag im Fachausschuss III der DGG am 12. Oktober 25 in Würzburg
HVG-Mitteilung Nr. 294 (HVG/AiF-Forschungsvorhaben Nr. 13653 BR) A. Baum, M. Müller, C. Rüssel, Otto-Schott-Institut für Glaschemie, Jena Vortrag im Fachausschuss III der DGG am 12. Oktober 25 in Würzburg
Versuch 1: Herstellung von gefärbten Silikatgläsern
 Versuch 1: Herstellung von gefärbten Silikatgläsern Glas läßt sich sowohl für den Alltagsgebrauch als auch für technische Anwendungen in vielfältiger Weise einfärben. In den meisten Fällen geschieht das
Versuch 1: Herstellung von gefärbten Silikatgläsern Glas läßt sich sowohl für den Alltagsgebrauch als auch für technische Anwendungen in vielfältiger Weise einfärben. In den meisten Fällen geschieht das
HVG-Mitteilung Nr Wie passt der statistische Energieverbrauch der Glasindustrie und der reale Energieverbrauch zum Schmelzen von Glas zusammen?
 Wie passt der statistische Energieverbrauch der Glasindustrie und der reale Energieverbrauch zum Schmelzen von Glas zusammen? B. Fleischmann, Hüttentechnische Vereinigung der Deutschen Glasindustrie e.v.,
Wie passt der statistische Energieverbrauch der Glasindustrie und der reale Energieverbrauch zum Schmelzen von Glas zusammen? B. Fleischmann, Hüttentechnische Vereinigung der Deutschen Glasindustrie e.v.,
VL Limnochemie
 VL Limnochemie Redoxreaktionen und -gleichgewichte WIEDERHOLUNG: SAUERSTOFF 1 Henry-Gesetz Massenwirkungsgesetz für den Fall: gasförmiger Stoff löst sich in Wasser A gas A fl K H = c(a fl ) c(a gas ) Henry-
VL Limnochemie Redoxreaktionen und -gleichgewichte WIEDERHOLUNG: SAUERSTOFF 1 Henry-Gesetz Massenwirkungsgesetz für den Fall: gasförmiger Stoff löst sich in Wasser A gas A fl K H = c(a fl ) c(a gas ) Henry-
Elektrolytische Leitfähigkeit
 Elektrolytische Leitfähigkeit 1 Elektrolytische Leitfähigkeit Gegenstand dieses Versuches ist der Zusammenhang der elektrolytischen Leitfähigkeit starker und schwacher Elektrolyten mit deren Konzentration.
Elektrolytische Leitfähigkeit 1 Elektrolytische Leitfähigkeit Gegenstand dieses Versuches ist der Zusammenhang der elektrolytischen Leitfähigkeit starker und schwacher Elektrolyten mit deren Konzentration.
Versuch 5. Kinetik der Kaliumaufnahme durch Getreidewurzeln
 Versuch Kinetik der Kaliumaufnahme durch Getreidewurzeln Till Biskup Matrikelnummer: 67. Juni Aufgaben. Geben Sie die Kaliumkonzentration an, die am Ende der ersten Meßserie im Medium festgestellt wurde.
Versuch Kinetik der Kaliumaufnahme durch Getreidewurzeln Till Biskup Matrikelnummer: 67. Juni Aufgaben. Geben Sie die Kaliumkonzentration an, die am Ende der ersten Meßserie im Medium festgestellt wurde.
Praktikumsprotokoll Physikalisch-Chemisches Anfängerpraktikum
 Praktikumsprotokoll Physikalisch-Chemisches Anfängerpraktikum Tobias Schabel Datum des Praktikumstags: 02.12.2005 Matthias Ernst Protokoll-Datum: 12/20/2005 Gruppe A-11 11. Versuch: Schmelzdiagramm Assistent:
Praktikumsprotokoll Physikalisch-Chemisches Anfängerpraktikum Tobias Schabel Datum des Praktikumstags: 02.12.2005 Matthias Ernst Protokoll-Datum: 12/20/2005 Gruppe A-11 11. Versuch: Schmelzdiagramm Assistent:
Lebensdauerverlängerung von Feuerfestmaterial für die Glasindustrie
 Institut für Keramik, Glas- und Baustofftechnik Lebensdauerverlängerung von Feuerfestmaterial für die Glasindustrie Verteidigung Diplomarbeit Rolf Weigand Betreuer: Prof. Dr.-Ing. H. Hessenkemper DI H.
Institut für Keramik, Glas- und Baustofftechnik Lebensdauerverlängerung von Feuerfestmaterial für die Glasindustrie Verteidigung Diplomarbeit Rolf Weigand Betreuer: Prof. Dr.-Ing. H. Hessenkemper DI H.
Praktikum - Physikalische Chemie I 14. Januar Reaktion 2. Ordnung. Guido Petri Anastasiya Knoch PC111/112, Gruppe 11
 Praktikum - Physikalische Chemie I 14. Januar 2016 Reaktion 2. Ordnung Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 Aufgabenstellung Die Reaktionsgeschwindigkeit von der Hydrolyse von Essigsäureacetatester
Praktikum - Physikalische Chemie I 14. Januar 2016 Reaktion 2. Ordnung Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 Aufgabenstellung Die Reaktionsgeschwindigkeit von der Hydrolyse von Essigsäureacetatester
Protokoll Grundpraktikum I: M9 - Reversionspendel
 Protokoll Grundpraktikum I: M9 - Reversionspendel Sebastian Pfitzner. Juni 013 Durchführung: Sebastian Pfitzner (553983), Anna Andrle (55077) Arbeitsplatz: Platz Betreuer: Peter Schäfer Versuchsdatum:
Protokoll Grundpraktikum I: M9 - Reversionspendel Sebastian Pfitzner. Juni 013 Durchführung: Sebastian Pfitzner (553983), Anna Andrle (55077) Arbeitsplatz: Platz Betreuer: Peter Schäfer Versuchsdatum:
Laborübungen aus Physikalischer Chemie (Bachelor) Universität Graz
 Arbeitsbericht zum Versuch Temperaturverlauf Durchführung am 9. Nov. 2016, M. Maier und H. Huber (Gruppe 2) In diesem Versuch soll der Temperaturgradient entlang eines organischen Kristalls (Bezeichnung
Arbeitsbericht zum Versuch Temperaturverlauf Durchführung am 9. Nov. 2016, M. Maier und H. Huber (Gruppe 2) In diesem Versuch soll der Temperaturgradient entlang eines organischen Kristalls (Bezeichnung
12GE1 - Wiederholung - Verbesserung Praktikum 01
 12GE1 - Wiederholung - Verbesserung Praktikum 01 Raymond KNEIP, LYCÉE DES ARTS ET MÉTIERS September 2015 1 Die gleichförmige Bewegung Dritte Reihe der Tabelle: s/t (m/s) (F.I.) 0.5 0.5 0.5 0.5 a. Der Quotient
12GE1 - Wiederholung - Verbesserung Praktikum 01 Raymond KNEIP, LYCÉE DES ARTS ET MÉTIERS September 2015 1 Die gleichförmige Bewegung Dritte Reihe der Tabelle: s/t (m/s) (F.I.) 0.5 0.5 0.5 0.5 a. Der Quotient
Praktikum Physikalische Chemie I 30. Januar Aktivierungsenergie. Guido Petri Anastasiya Knoch PC111/112, Gruppe 11
 Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
6. Temperaturbehandlung Ag/Na-ionenausgetauschter Gläser
 Temperaturbehandlung Ag/Na-ionenausgetauschter Gläser 35 6. Temperaturbehandlung Ag/Na-ionenausgetauschter Gläser 6.1. Natriumsilikatglas Nach dem Ionenaustausch folgten Temperaturbehandlungen zwischen
Temperaturbehandlung Ag/Na-ionenausgetauschter Gläser 35 6. Temperaturbehandlung Ag/Na-ionenausgetauschter Gläser 6.1. Natriumsilikatglas Nach dem Ionenaustausch folgten Temperaturbehandlungen zwischen
Mittelwert, Standardabweichung, Median und Bereich für alle durchgeführten Messungen (in Prozent)
 3. Ergebnisse 3.1 Kennwerte, Boxplot Die Kennwerte der deskriptiven Statistik sind in der Tabelle 1 für alle Messungen, in der Tabelle 2 für die Messungen, bei denen mit der Referenzmethode eine festgestellt
3. Ergebnisse 3.1 Kennwerte, Boxplot Die Kennwerte der deskriptiven Statistik sind in der Tabelle 1 für alle Messungen, in der Tabelle 2 für die Messungen, bei denen mit der Referenzmethode eine festgestellt
Zukunft Bau KURZBERICHT. Titel Entwicklung eines Verfahrens zur Bestimmung der Verbrennungseffektivität für Brandlastberechnungen
 Zukunft Bau KURZBERICHT Titel Entwicklung eines Verfahrens zur Bestimmung der für Brandlastberechnungen Anlass/ Ausgangslage Brandlastberechnungen für Industriebauten werden nach DIN 18230 unter Anwendung
Zukunft Bau KURZBERICHT Titel Entwicklung eines Verfahrens zur Bestimmung der für Brandlastberechnungen Anlass/ Ausgangslage Brandlastberechnungen für Industriebauten werden nach DIN 18230 unter Anwendung
HVG-Mitteilung Nr Ergebnisse von Messungen mit dem Spektralradiometer
 HVG-Mitteilung Nr. 257 Spektrale Messung der im Verbrennungsraum von Glasschmelzwannen vorhandenen Strahlung im Rahmen des AiF-Forschungsvorhabens Nr. 8 ZN Spektral Teil 2: Messungen mit dem Spektralradiometer
HVG-Mitteilung Nr. 257 Spektrale Messung der im Verbrennungsraum von Glasschmelzwannen vorhandenen Strahlung im Rahmen des AiF-Forschungsvorhabens Nr. 8 ZN Spektral Teil 2: Messungen mit dem Spektralradiometer
HVG-Mitteilung 2028 Einleitung Experimetelle Methoden Untersuchungen im 200-g-Maßstab
 HVG-Mitteilung 2028 Untersuchungen lokaler und weiträumiger kinetischer Vorgänge beim Einschmelzen von Gemengen mit und ohne Scherben O. Dubois, R. Conradt, Lehrstuhl für Glas und keramische Verbundwerkstoffe,
HVG-Mitteilung 2028 Untersuchungen lokaler und weiträumiger kinetischer Vorgänge beim Einschmelzen von Gemengen mit und ohne Scherben O. Dubois, R. Conradt, Lehrstuhl für Glas und keramische Verbundwerkstoffe,
Bestimmung des Spannungskoeffizienten eines Gases
 Bestimmung des Spannungskoeffizienten eines Gases Einleitung Bei diesem Experiment wollen wir den Spannungskoeffizienten α eines Gases möglichst genau bestimmen und in Folge mit dem Spannungskoeffizienten
Bestimmung des Spannungskoeffizienten eines Gases Einleitung Bei diesem Experiment wollen wir den Spannungskoeffizienten α eines Gases möglichst genau bestimmen und in Folge mit dem Spannungskoeffizienten
Allgemeine Chemie I (AC) HS 2011 Übungen Serie 6
 Prof. A. Togni, D-CHAB, HCI H 239 Allgemeine Chemie I (AC) HS 2011 Übungen Serie 6 Säure-Base-Gleichgewichte E 1. Sie möchten 200 ml einer Pufferlösung mit ph = 5.00 mit dem Säure-Base-Paar Essigsäure
Prof. A. Togni, D-CHAB, HCI H 239 Allgemeine Chemie I (AC) HS 2011 Übungen Serie 6 Säure-Base-Gleichgewichte E 1. Sie möchten 200 ml einer Pufferlösung mit ph = 5.00 mit dem Säure-Base-Paar Essigsäure
Versuch 17: Kennlinie der Vakuum-Diode
 Versuch 17: Kennlinie der Vakuum-Diode Inhaltsverzeichnis 1 Einleitung 3 2 Theorie 3 2.1 Prinzip der Vakuumdiode.......................... 3 2.2 Anlaufstrom.................................. 3 2.3 Raumladungsgebiet..............................
Versuch 17: Kennlinie der Vakuum-Diode Inhaltsverzeichnis 1 Einleitung 3 2 Theorie 3 2.1 Prinzip der Vakuumdiode.......................... 3 2.2 Anlaufstrom.................................. 3 2.3 Raumladungsgebiet..............................
Untersuchung zur Gleichwertigkeit des LOVIBOND CSB vario Küvettentest mit dem Hach * CSB Küvettentest
 Untersuchung zur Gleichwertigkeit des LOVIBOND CSB vario Küvettentest mit dem CSB Küvettentest Inhaltsverzeichnis Seite Einleitung und Zielsetzung 1 Verwendete Methoden, Reagenzien und Geräte 1 Teil I
Untersuchung zur Gleichwertigkeit des LOVIBOND CSB vario Küvettentest mit dem CSB Küvettentest Inhaltsverzeichnis Seite Einleitung und Zielsetzung 1 Verwendete Methoden, Reagenzien und Geräte 1 Teil I
Anwendung der Verdünnte Verbrennung für regenerativ beheizte Glasschmelzwannen Eine Möglichkeit zur NO x -Reduzierung
 Anwendung der Verdünnte Verbrennung für regenerativ beheizte Glasschmelzwannen Eine Möglichkeit zur NO x -Reduzierung Dr.-Ing. Anne Giese, Prof. Dr.-Ing. habil. Klaus Görner 24. Deutscher Flammentag Postersession
Anwendung der Verdünnte Verbrennung für regenerativ beheizte Glasschmelzwannen Eine Möglichkeit zur NO x -Reduzierung Dr.-Ing. Anne Giese, Prof. Dr.-Ing. habil. Klaus Görner 24. Deutscher Flammentag Postersession
ALVA-Ringanalyse. Herbsttagung 2009 der ALVA-Fachgruppe Boden - Pflanzenernährung Linz, 10. November 2009
 ALVA-Ringanalyse Mag. Tanja Strimitzer Bereich DSR Herbsttagung 2009 der ALVA-Fachgruppe Boden - Pflanzenernährung Linz, 10. November 2009 www.ages.at Österreichische Agentur für Gesundheit und Ernährungssicherheit
ALVA-Ringanalyse Mag. Tanja Strimitzer Bereich DSR Herbsttagung 2009 der ALVA-Fachgruppe Boden - Pflanzenernährung Linz, 10. November 2009 www.ages.at Österreichische Agentur für Gesundheit und Ernährungssicherheit
E5: Faraday-Konstante
 E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
Parametrische vs. Non-Parametrische Testverfahren
 Parametrische vs. Non-Parametrische Testverfahren Parametrische Verfahren haben die Besonderheit, dass sie auf Annahmen zur Verteilung der Messwerte in der Population beruhen: die Messwerte sollten einer
Parametrische vs. Non-Parametrische Testverfahren Parametrische Verfahren haben die Besonderheit, dass sie auf Annahmen zur Verteilung der Messwerte in der Population beruhen: die Messwerte sollten einer
HVG-Mitteilung Nr. 2103
 HVG-Mitteilung Nr. 2103 Optische Messung der Temperatur mit Pyrometern bei der Glasherstellung Teil 1: Bestimmung der Temperatur von feuerfesten Bauteilen im Verbrennungsraum von Glasschmelzwannen B. Fleischmann,
HVG-Mitteilung Nr. 2103 Optische Messung der Temperatur mit Pyrometern bei der Glasherstellung Teil 1: Bestimmung der Temperatur von feuerfesten Bauteilen im Verbrennungsraum von Glasschmelzwannen B. Fleischmann,
Abb. 5.10: Funktion und Tangentialebene im Punkt ( ) ( ) ( ) 3.) Die Zahlenwerte und in Gleichung (Def. 5.11) berechnen sich durch ( ) ( )
 Abb. 5.0: Funktion und Tangentialebene im Punkt Aus der totalen Differenzierbarkeit folgt sowohl die partielle Differenzierbarkeit als auch die Stetigkeit von : Satz 5.2: Folgerungen der totalen Differenzierbarkeit
Abb. 5.0: Funktion und Tangentialebene im Punkt Aus der totalen Differenzierbarkeit folgt sowohl die partielle Differenzierbarkeit als auch die Stetigkeit von : Satz 5.2: Folgerungen der totalen Differenzierbarkeit
PHYSIKO CHEMISCHE UNTERSUCHlJNGEN DER ALLYLÄTHOXY.SILANE I
 PHYSKO CHEMSCHE UNTERSUCHlJNGEN DER ALLYLÄTHOXY.SLANE Von J. NAGY und K. BECKER-PALOSSY Lehrstuhl für Anorganische Chemie, Technische Universität, Budapest. (Eingegangen am 14. November 1974) Die theoretische
PHYSKO CHEMSCHE UNTERSUCHlJNGEN DER ALLYLÄTHOXY.SLANE Von J. NAGY und K. BECKER-PALOSSY Lehrstuhl für Anorganische Chemie, Technische Universität, Budapest. (Eingegangen am 14. November 1974) Die theoretische
Gasthermometer. durchgeführt am von Matthias Dräger, Alexander Narweleit und Fabian Pirzer
 Gasthermometer 1 PHYSIKALISCHE GRUNDLAGEN durchgeführt am 21.06.2010 von Matthias Dräger, Alexander Narweleit und Fabian Pirzer 1 Physikalische Grundlagen 1.1 Zustandgleichung des idealen Gases Ein ideales
Gasthermometer 1 PHYSIKALISCHE GRUNDLAGEN durchgeführt am 21.06.2010 von Matthias Dräger, Alexander Narweleit und Fabian Pirzer 1 Physikalische Grundlagen 1.1 Zustandgleichung des idealen Gases Ein ideales
Säure-Base Titrationen
 Chemie Praktikum Säure-Base Titrationen WS 2006/2007 Verfasser: Lorenz Germann, Lukas Bischoff Versuchsteilnehmer: Lorenz Germann, Lukas Bischoff Datum: 29.11.2006 Assistent: Lera Tomasic E-mail: lukas-bischoff@student.ethz.ch
Chemie Praktikum Säure-Base Titrationen WS 2006/2007 Verfasser: Lorenz Germann, Lukas Bischoff Versuchsteilnehmer: Lorenz Germann, Lukas Bischoff Datum: 29.11.2006 Assistent: Lera Tomasic E-mail: lukas-bischoff@student.ethz.ch
Versuchsprotokoll. Mathematisch-Naturwissenschaftliche Fakultät I Institut für Physik. Versuch O10: Linsensysteme Arbeitsplatz Nr.
 Mathematisch-Naturwissenschaftliche Fakultät I Institut für Physik Physikalisches Grundpraktikum I Versuchsprotokoll Versuch O10: Linsensysteme Arbeitsplatz Nr. 1 0. Inhaltsverzeichnis 1. Einleitung 2.
Mathematisch-Naturwissenschaftliche Fakultät I Institut für Physik Physikalisches Grundpraktikum I Versuchsprotokoll Versuch O10: Linsensysteme Arbeitsplatz Nr. 1 0. Inhaltsverzeichnis 1. Einleitung 2.
Messwiederholungen und abhängige Messungen
 Messwiederholungen und abhängige Messungen t Tests und Varianzanalysen für Messwiederholungen Kovarianzanalyse Thomas Schäfer SS 009 1 Messwiederholungen und abhängige Messungen Bei einer Messwiederholung
Messwiederholungen und abhängige Messungen t Tests und Varianzanalysen für Messwiederholungen Kovarianzanalyse Thomas Schäfer SS 009 1 Messwiederholungen und abhängige Messungen Bei einer Messwiederholung
W2 Gasthermometer. 1. Grundlagen: 1.1 Gasthermometer und Temperaturmessung
 W2 Gasthermometer Stoffgebiet: Versuchsziel: Literatur: Temperaturmessung, Gasthermometer, Gasgesetze Mit Hilfe eines Gasthermometers sind der Ausdehnungs- und Druckkoeffizient von Luft zu bestimmen. Beschäftigung
W2 Gasthermometer Stoffgebiet: Versuchsziel: Literatur: Temperaturmessung, Gasthermometer, Gasgesetze Mit Hilfe eines Gasthermometers sind der Ausdehnungs- und Druckkoeffizient von Luft zu bestimmen. Beschäftigung
Tabelle 1: Altersverteilung der Patienten (n = 42) in Jahren
 3. Ergebnisse Die 42 Patienten (w= 16, m= 26) hatten ein Durchschnittsalter von 53,5 Jahren mit einem Minimum von und einem Maximum von 79 Jahren. Die 3 Patientengruppen zeigten hinsichtlich Alters- und
3. Ergebnisse Die 42 Patienten (w= 16, m= 26) hatten ein Durchschnittsalter von 53,5 Jahren mit einem Minimum von und einem Maximum von 79 Jahren. Die 3 Patientengruppen zeigten hinsichtlich Alters- und
Prozesstechnik-Übung Wintersemester Es ist das Phasendiagramm des Systems Naphthalin/Biphenyl durch thermische Analyse zu bestimmen.
 Prozesstechnik-Übung Wintersemester 2008-2009 Thermische Analyse 1 Versuchsziel Es ist das Phasendiagramm des Systems Naphthalin/Biphenyl durch thermische Analyse zu bestimmen. 2 Theoretische Grundlagen
Prozesstechnik-Übung Wintersemester 2008-2009 Thermische Analyse 1 Versuchsziel Es ist das Phasendiagramm des Systems Naphthalin/Biphenyl durch thermische Analyse zu bestimmen. 2 Theoretische Grundlagen
Verseifungsgeschwindigkeit eines Esters
 A 32 Verseifungsgeschwindigkeit eines Esters Aufgabe: Man bestimme die Geschwindigkeitskonstante k der Methylacetatverseifung bei 2 verschiedenen Temperaturen und berechne daraus den Vorfaktor sowie die
A 32 Verseifungsgeschwindigkeit eines Esters Aufgabe: Man bestimme die Geschwindigkeitskonstante k der Methylacetatverseifung bei 2 verschiedenen Temperaturen und berechne daraus den Vorfaktor sowie die
Einführung Fehlerrechnung
 Einführung Fehlerrechnung Bei jeder Messung, ob Einzelmessung oder Messreihe, muss eine Aussage über die Güte ( Wie groß ist der Fehler? ) des Messergebnisses gemacht werden. Mögliche Fehlerarten 1. Systematische
Einführung Fehlerrechnung Bei jeder Messung, ob Einzelmessung oder Messreihe, muss eine Aussage über die Güte ( Wie groß ist der Fehler? ) des Messergebnisses gemacht werden. Mögliche Fehlerarten 1. Systematische
Praktikum Physikalische Chemie I. Versuch 4. p, V, T - Verhalten realer Gase am Beispiel von SF 6
 Praktikum Physikalische Chemie I ersuch 4 p,, T - erhalten realer Gase am Beispiel von SF 6 1. Grundlagen Komprimiert man ein Gas isotherm, so steigt dessen Druck näherungsweise gemäß dem idealen Gasgesetz
Praktikum Physikalische Chemie I ersuch 4 p,, T - erhalten realer Gase am Beispiel von SF 6 1. Grundlagen Komprimiert man ein Gas isotherm, so steigt dessen Druck näherungsweise gemäß dem idealen Gasgesetz
4 Ergebnisse. Ergebnisse
 4 4.1 Entwicklung der Körpertemperatur und der Wärmeproduktion bei Enten- und Hühnerembryonen in Abhängigkeit vom Alter bei normaler Bruttemperatur Im untersuchten Abschnitt der Embryonalentwicklung stieg
4 4.1 Entwicklung der Körpertemperatur und der Wärmeproduktion bei Enten- und Hühnerembryonen in Abhängigkeit vom Alter bei normaler Bruttemperatur Im untersuchten Abschnitt der Embryonalentwicklung stieg
3.11 Einflussgröße: Elementarer Kohlenstoff (EC) und organischer Kohlenstoff
 3.11 Einflussgröße: Elementarer Kohlenstoff (EC) und organischer Kohlenstoff (OC) im PM10 Eine vollständige Minderung von EC (Ruß) und OC würde eine maximale Reduktion der PM10-Feinstaubkonzentration um
3.11 Einflussgröße: Elementarer Kohlenstoff (EC) und organischer Kohlenstoff (OC) im PM10 Eine vollständige Minderung von EC (Ruß) und OC würde eine maximale Reduktion der PM10-Feinstaubkonzentration um
Allgemeine Chemie Computer Praktikum Frühjahrssemester Regressions-Tutorial Lineare und nicht-lineare Regression
 1 Einführung Allgemeine Chemie Computer Praktikum Frühjahrssemester Regressions-Tutorial Lineare und nicht-lineare Regression Datenauswertung In einem naturwissenschaftlichen Experiment werden Sie meist
1 Einführung Allgemeine Chemie Computer Praktikum Frühjahrssemester Regressions-Tutorial Lineare und nicht-lineare Regression Datenauswertung In einem naturwissenschaftlichen Experiment werden Sie meist
Schmelzdiagramm eines binären Stoffgemisches
 Praktikum Physikalische Chemie I 30. Oktober 2015 Schmelzdiagramm eines binären Stoffgemisches Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1. Theorie hinter dem Versuch Ein Schmelzdiagramm zeigt
Praktikum Physikalische Chemie I 30. Oktober 2015 Schmelzdiagramm eines binären Stoffgemisches Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1. Theorie hinter dem Versuch Ein Schmelzdiagramm zeigt
Grundpraktikum A A2 Franck-Hertz-Versuch
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Physik Grundpraktikum A A2 Franck-Hertz-Versuch 30.06.2017 Studenten: Tim Will Betreuer: Raum: J. NEW14-2.01 Messplatz: 2 INHALTSVERZEICHNIS INHALTSVERZEICHNIS
Mathematisch-Naturwissenschaftliche Fakultät Institut für Physik Grundpraktikum A A2 Franck-Hertz-Versuch 30.06.2017 Studenten: Tim Will Betreuer: Raum: J. NEW14-2.01 Messplatz: 2 INHALTSVERZEICHNIS INHALTSVERZEICHNIS
Physikalisches Anfaengerpraktikum. Zustandsgleichung idealer Gase und kritischer Punkt
 Physikalisches Anfaengerpraktikum Zustandsgleichung idealer Gase und kritischer Punkt Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 18. März 005 email: Marcel.Engelhardt@mytum.de
Physikalisches Anfaengerpraktikum Zustandsgleichung idealer Gase und kritischer Punkt Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 18. März 005 email: Marcel.Engelhardt@mytum.de
Abb. 1: Konstruktionsfolge
 Hans Walser, [20180501] DIN-Format, Goldener Schnitt und gleichseitiges Dreieck 1 Worum geht es? Die klassische Konstruktion eines Rechtecks im DIN-Format (Walser 2013b) wird iteriert und führt zum gleichseitigen
Hans Walser, [20180501] DIN-Format, Goldener Schnitt und gleichseitiges Dreieck 1 Worum geht es? Die klassische Konstruktion eines Rechtecks im DIN-Format (Walser 2013b) wird iteriert und führt zum gleichseitigen
Redoxtitrationen. Redox-Reaktionen Oxidation und Reduktion
 RedoxReaktionen Oxidation und Reduktion Redoxtitrationen Beschreibung der Lage von Redoxgleichgewichten Standardpotentiale, Spannungsreihe Nernst sche Gleichung Berechnung von Titrationskurven Indikationen
RedoxReaktionen Oxidation und Reduktion Redoxtitrationen Beschreibung der Lage von Redoxgleichgewichten Standardpotentiale, Spannungsreihe Nernst sche Gleichung Berechnung von Titrationskurven Indikationen
2. Übung Grundlagen der Hauptgruppenchemie AC02
 Allgemeine und Anorganische Chemie 2. Übung Grundlagen der Hauptgruppenchemie AC02 Aufgabe 1: Vervollständigen und gleichen Sie die folgenden Gleichungen aus: a) CaO + H 2 O Ca(OH) 2 b) Al 2 O 3 + 6 H
Allgemeine und Anorganische Chemie 2. Übung Grundlagen der Hauptgruppenchemie AC02 Aufgabe 1: Vervollständigen und gleichen Sie die folgenden Gleichungen aus: a) CaO + H 2 O Ca(OH) 2 b) Al 2 O 3 + 6 H
Brückenschaltung (BRÜ)
 TUM Anfängerpraktikum für Physiker II Wintersemester 2006/2007 Brückenschaltung (BRÜ) Inhaltsverzeichnis 9. Januar 2007 1. Einleitung... 2 2. Messung ohmscher und komplexer Widerstände... 2 3. Versuchsauswertung...
TUM Anfängerpraktikum für Physiker II Wintersemester 2006/2007 Brückenschaltung (BRÜ) Inhaltsverzeichnis 9. Januar 2007 1. Einleitung... 2 2. Messung ohmscher und komplexer Widerstände... 2 3. Versuchsauswertung...
Physikalisches Grundpraktikum I
 INSTITUT FÜR PHYSIK DER HUMBOLDT-UNIVERSITÄT ZU BERLIN Physikalisches Grundpraktikum I Versuchsprotokoll P2 : F7 Statistik und Radioaktivität Versuchsort: Raum 217-2 Versuchsbetreuer: E. von Seggern, D.
INSTITUT FÜR PHYSIK DER HUMBOLDT-UNIVERSITÄT ZU BERLIN Physikalisches Grundpraktikum I Versuchsprotokoll P2 : F7 Statistik und Radioaktivität Versuchsort: Raum 217-2 Versuchsbetreuer: E. von Seggern, D.
Grundpraktikum A T7 Spezifische Wärmekapazität idealer Gase
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Physik Grundpraktikum A T7 Spezifische Wärmekapazität idealer Gase 16.6.217 Studenten: Tim Will Betreuer: Raum: Messplatz: M. NEW14-2.15 Links
Mathematisch-Naturwissenschaftliche Fakultät Institut für Physik Grundpraktikum A T7 Spezifische Wärmekapazität idealer Gase 16.6.217 Studenten: Tim Will Betreuer: Raum: Messplatz: M. NEW14-2.15 Links
Säure-Base-Titrationen
 Martin Raiber Chemie Protokoll Nr.3 19.2.2006 Säure-Base-Titrationen 1. Titration von Salzsäure mit Natronlauge Chemikalien: Salzsäure (100ml; c(hcl)=0,1 mol/l) Natronlauge (c(naoh)=1 mol/l) Bromthymolblau
Martin Raiber Chemie Protokoll Nr.3 19.2.2006 Säure-Base-Titrationen 1. Titration von Salzsäure mit Natronlauge Chemikalien: Salzsäure (100ml; c(hcl)=0,1 mol/l) Natronlauge (c(naoh)=1 mol/l) Bromthymolblau
Übungsaufgabe Parameter und Verteilungsschätzung
 Übungsaufgabe Parameter und Verteilungsschätzung Prof. Dr. rer. nat. Lüders Datum: 21.01.2019 Autor: Marius Schulte Matr.-Nr.: 10049060 FH Südwestfalen Aufgabenstellung Analysiert werden sollen die Verteilungen
Übungsaufgabe Parameter und Verteilungsschätzung Prof. Dr. rer. nat. Lüders Datum: 21.01.2019 Autor: Marius Schulte Matr.-Nr.: 10049060 FH Südwestfalen Aufgabenstellung Analysiert werden sollen die Verteilungen
2 Elektrischer Stromkreis
 2 Elektrischer Stromkreis 2.1 Aufbau des technischen Stromkreises Nach der Durcharbeitung dieses Kapitels haben Sie die Kompetenz... Stromkreise in äußere und innere Abschnitte einzuteilen und die Bedeutung
2 Elektrischer Stromkreis 2.1 Aufbau des technischen Stromkreises Nach der Durcharbeitung dieses Kapitels haben Sie die Kompetenz... Stromkreise in äußere und innere Abschnitte einzuteilen und die Bedeutung
Konzentrationsbestimmung mit Lösungen
 Kapitel 5 Konzentrationsbestimmung mit Lösungen Abb. 5.1: Die Farben von Universalindikatoren sind nützlich für Konzentrationsbestimmungen. Sie lernen auf den folgenden Seiten eine sehr nützliche Methode
Kapitel 5 Konzentrationsbestimmung mit Lösungen Abb. 5.1: Die Farben von Universalindikatoren sind nützlich für Konzentrationsbestimmungen. Sie lernen auf den folgenden Seiten eine sehr nützliche Methode
Einiges zu den Potenzfunktionen. Exponentialfunktionen
 Einiges zu den Potenzfunktionen Es sind zunächst zwei Arten der Potenzfunktionen zu unterscheiden. Erstens die eigentlichen Potenzfunktionen, bei denen die Variable x als Basis von Potenzen vorkommt. Diese
Einiges zu den Potenzfunktionen Es sind zunächst zwei Arten der Potenzfunktionen zu unterscheiden. Erstens die eigentlichen Potenzfunktionen, bei denen die Variable x als Basis von Potenzen vorkommt. Diese
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Kapitel 4: Meßergebnisse Vergleiche der aerodynamischen und akustischen Meßgrößen des Originalstaubsaugers und des modifizierten Staubsaugers
 Kapitel 4: Meßergebnisse 65 4.4 Vergleiche der aerodynamischen und akustischen Meßgrößen des Originalstaubsaugers und des modifizierten Staubsaugers In diesem Abschnitt werden die aerodynamischen und akustischen
Kapitel 4: Meßergebnisse 65 4.4 Vergleiche der aerodynamischen und akustischen Meßgrößen des Originalstaubsaugers und des modifizierten Staubsaugers In diesem Abschnitt werden die aerodynamischen und akustischen
6.2 Zweiter HS der Thermodynamik
 Die Änderung des Energieinhaltes eines Systems ohne Stoffaustausch kann durch Zu-/Abfuhr von Wärme Q bzw. mechanischer Arbeit W erfolgen Wird die Arbeit reversibel geleistet (Volumenarbeit), so gilt W
Die Änderung des Energieinhaltes eines Systems ohne Stoffaustausch kann durch Zu-/Abfuhr von Wärme Q bzw. mechanischer Arbeit W erfolgen Wird die Arbeit reversibel geleistet (Volumenarbeit), so gilt W
+ - H3O(aq) + OH(aq) H2O(l) + H2O(l) 1/19. Autoprotolyse des Wassers
 Autoprotolyse des Wassers 1/19 Autoprotolyse des Wassers 2/19 c(h3o + ) = 10-7 mol/l c(h2o) = 55,4 mol/l c(oh - ) = 10-7 mol/l Autoprotolyse des Wassers 3/19 K = [H 3 O+ ][OH ] [H 2 O][H 2 O] Autoprotolyse
Autoprotolyse des Wassers 1/19 Autoprotolyse des Wassers 2/19 c(h3o + ) = 10-7 mol/l c(h2o) = 55,4 mol/l c(oh - ) = 10-7 mol/l Autoprotolyse des Wassers 3/19 K = [H 3 O+ ][OH ] [H 2 O][H 2 O] Autoprotolyse
Versuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten -
 1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
Messungen zur Abbaukinetik von Einzelsubstraten und Substratmischungen
 Nils Engler, Michael Nelles Messungen zur Abbaukinetik von Einzelsubstraten und Substratmischungen Fachtagung Prozessmesstechnik an Biogasanlagen 25. und 26. März 2014 / Leipzig 27.03.2014 UNIVERSITÄT
Nils Engler, Michael Nelles Messungen zur Abbaukinetik von Einzelsubstraten und Substratmischungen Fachtagung Prozessmesstechnik an Biogasanlagen 25. und 26. März 2014 / Leipzig 27.03.2014 UNIVERSITÄT
Bist Du nicht "FIT", dann musst Du nacharbeiten.
 Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
Übungsaufgaben Chemie Nr. 3
 Übungsaufgaben Chemie Nr. 3 22) Wie hoch ist die Molarität der jeweiligen Lösungen, wenn die angegebene Substanzmenge in Wasser gelöst und auf 200 ml aufgefüllt wurde? a) 58.44g NaCl (Kochsalz) b) 100
Übungsaufgaben Chemie Nr. 3 22) Wie hoch ist die Molarität der jeweiligen Lösungen, wenn die angegebene Substanzmenge in Wasser gelöst und auf 200 ml aufgefüllt wurde? a) 58.44g NaCl (Kochsalz) b) 100
1. Versuchsaufbau 2. Versuchsauswertung a. Diagramme b. Berechnung der Zerfallskonstanten und Halbwertszeit c. Fehlerbetrachtung d.
 Christian Müller Jan Philipp Dietrich K2 Halbwertszeit (Thoron) Protokoll 1. Versuchsaufbau 2. Versuchsauswertung a. Diagramme b. Berechnung der Zerfallskonstanten und Halbwertszeit c. Fehlerbetrachtung
Christian Müller Jan Philipp Dietrich K2 Halbwertszeit (Thoron) Protokoll 1. Versuchsaufbau 2. Versuchsauswertung a. Diagramme b. Berechnung der Zerfallskonstanten und Halbwertszeit c. Fehlerbetrachtung
Merkmale des PVT500 im Vergleich zur Add-on Option* Kapillarrheometer
 RHEO-INFO PVT500 das autarke Prüfsystem für die pvt-messung ein Systemvergleich pvt-messungen dienen zur Ermittlung des thermodynamischen Verhaltens von Kunststoffen, Elastomeren, Duroplasten und Flüssigkeiten.
RHEO-INFO PVT500 das autarke Prüfsystem für die pvt-messung ein Systemvergleich pvt-messungen dienen zur Ermittlung des thermodynamischen Verhaltens von Kunststoffen, Elastomeren, Duroplasten und Flüssigkeiten.
Diskussion der Ergebnisse
 5 Diskussion der Ergebnisse Die Auswertung der Basiseigenschaften der Gläser beider Versuchsreihen lieferte folgende Ergebnisse: Die optische Einteilung der hergestellten Gläser konnte in zwei Gruppen
5 Diskussion der Ergebnisse Die Auswertung der Basiseigenschaften der Gläser beider Versuchsreihen lieferte folgende Ergebnisse: Die optische Einteilung der hergestellten Gläser konnte in zwei Gruppen
2.1 Bestimmung einiger Isothermen von Schwefelhexafluorid SF 6
 Atom- und Kernphysi-Versuch 31 AKP-31-1 Zustandsgrößen realer Gase 1 Vorbereitung Koexistenz von Flüssigeiten und Dampf, Dampfdruc, Verdampfungswärme, Koexistenz von Festörper und Flüssigeit, Koexistenz
Atom- und Kernphysi-Versuch 31 AKP-31-1 Zustandsgrößen realer Gase 1 Vorbereitung Koexistenz von Flüssigeiten und Dampf, Dampfdruc, Verdampfungswärme, Koexistenz von Festörper und Flüssigeit, Koexistenz
Überlegungen zur Leistung und zum Wirkungsgrad von Solarkochern
 Überlegungen zur Leistung und zum Wirkungsgrad von Solarkochern (Dr. Hartmut Ehmler) Einführung Die folgenden Überlegungen gelten ganz allgemein für Solarkocher, unabhängig ob es sich um einen Parabolkocher,
Überlegungen zur Leistung und zum Wirkungsgrad von Solarkochern (Dr. Hartmut Ehmler) Einführung Die folgenden Überlegungen gelten ganz allgemein für Solarkocher, unabhängig ob es sich um einen Parabolkocher,
Grundlagen der Kinetik
 Kapitel 1 Grundlagen der Kinetik In diesem Kapitel werden die folgenden Themen kurz wiederholt: Die differenziellen und integralen Geschwindigkeitsgesetze von irreversiblen Reaktionen., 1., und. Ordnung
Kapitel 1 Grundlagen der Kinetik In diesem Kapitel werden die folgenden Themen kurz wiederholt: Die differenziellen und integralen Geschwindigkeitsgesetze von irreversiblen Reaktionen., 1., und. Ordnung
Sind Sie nun bereit für die Lernkontrolle? Lösen Sie die Aufgaben zu diesem Thema.
 Anwendungen des chemischen Gleichgewichtes 7 Gruppe1: Gruppe 1 Die Konzentration beeinflusst das chemische Gleichgewicht Uebersicht Die Reaktionsteilnehmer einer chemischen Reaktion im Gleichgewicht liegen
Anwendungen des chemischen Gleichgewichtes 7 Gruppe1: Gruppe 1 Die Konzentration beeinflusst das chemische Gleichgewicht Uebersicht Die Reaktionsteilnehmer einer chemischen Reaktion im Gleichgewicht liegen
1) Redoxverhältnisse an einer Sediment-Wasser-Grenzfläche in einem Fluss
 1 Uebungen zur Prüfungsvorbereitung 4.12.14 1) Redoxverhältnisse an einer Sediment-Wasser-Grenzfläche in einem Fluss Die folgenden Tiefenprofile von gelöstem Mangan, Eisen und Sulfid (S 2- ) sowie die
1 Uebungen zur Prüfungsvorbereitung 4.12.14 1) Redoxverhältnisse an einer Sediment-Wasser-Grenzfläche in einem Fluss Die folgenden Tiefenprofile von gelöstem Mangan, Eisen und Sulfid (S 2- ) sowie die
Mathematisch-Naturwissenschaftliche Fakultät I der Humboldt-Universität zu Berlin Institut für Physik Physikalisches Grundpraktikum.
 Mathematisch-Naturwissenschaftliche Fakultät I der Humboldt-Universität zu Berlin Institut für Physik Physikalisches Grundpraktikum Versuchsprotokoll zur Bestimmung der Federkonstante (F4) am Arbeitsplatz
Mathematisch-Naturwissenschaftliche Fakultät I der Humboldt-Universität zu Berlin Institut für Physik Physikalisches Grundpraktikum Versuchsprotokoll zur Bestimmung der Federkonstante (F4) am Arbeitsplatz
Kalibriermaterialien für die Viskositätsmessung an Glasschmelzen
 Arbeitsgruppe 3.32 Flüssigkeitseigenschaften Kalibriermaterialien für die Viskositätsmessung an Glasschmelzen Die PB bietet drei Gläser mit unterschiedlichem Viskositäts-emperatur-Verhalten (V-Verhalten)
Arbeitsgruppe 3.32 Flüssigkeitseigenschaften Kalibriermaterialien für die Viskositätsmessung an Glasschmelzen Die PB bietet drei Gläser mit unterschiedlichem Viskositäts-emperatur-Verhalten (V-Verhalten)
Physikalisches Grundpraktikum Technische Universität Chemnitz
 Physikalisches Grundpraktikum Technische Universität Chemnitz Protokoll «A3 - Atomspektren - BALMER-Serie» Martin Wolf Betreuer: DP Emmrich Mitarbeiter: Martin Helfrich
Physikalisches Grundpraktikum Technische Universität Chemnitz Protokoll «A3 - Atomspektren - BALMER-Serie» Martin Wolf Betreuer: DP Emmrich Mitarbeiter: Martin Helfrich
E 2-24 Setzungsprognosen für nicht bodenähnliche Abfälle
 E 2-24 1 E 2-24 Setzungsprognosen für nicht bodenähnliche Abfälle Stand: GDA 1997 1 Allgemeines Bei bodenähnlichen körnigen Abfällen nach E 1-8 werden die zu erwartenden Setzungen aus Spannungs-Verformungsuntersuchungen
E 2-24 1 E 2-24 Setzungsprognosen für nicht bodenähnliche Abfälle Stand: GDA 1997 1 Allgemeines Bei bodenähnlichen körnigen Abfällen nach E 1-8 werden die zu erwartenden Setzungen aus Spannungs-Verformungsuntersuchungen
Bayern Teil 1. Aufgabe 1. Abitur Mathematik: Musterlösung. Der Term unter der Wurzel darf nicht negativ werden. Es muss also gelten:
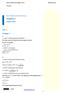 Abitur Mathematik: Bayern 2013 Teil 1 Aufgabe 1 a) 1. SCHRITT: DEFINITIONSMENGE BESTIMMEN Der Term unter der Wurzel darf nicht negativ werden. Es muss also gelten: 3x + 9 0 x 3 2. SCHRITT: NULLSTELLEN
Abitur Mathematik: Bayern 2013 Teil 1 Aufgabe 1 a) 1. SCHRITT: DEFINITIONSMENGE BESTIMMEN Der Term unter der Wurzel darf nicht negativ werden. Es muss also gelten: 3x + 9 0 x 3 2. SCHRITT: NULLSTELLEN
Diplomarbeit Nachbehandlung von Beton durch Zugabe wasserspeichernder Zusätze 3 Versuchsdurchführung und Versuchsauswertung
 2,50 Serie 1, w/z=0,45 Serie 3, w/z=0,45, mit FM Serie 5, w/z=0,60 Serie 7, w/z=0,60, mit FM Serie 2, w/z=0,45, mit Stab. Serie 4, w/z=0,45, mit Stab.+FM Serie 6, w/z=0,60, mit Stab. Serie 8, w/z=0,60,
2,50 Serie 1, w/z=0,45 Serie 3, w/z=0,45, mit FM Serie 5, w/z=0,60 Serie 7, w/z=0,60, mit FM Serie 2, w/z=0,45, mit Stab. Serie 4, w/z=0,45, mit Stab.+FM Serie 6, w/z=0,60, mit Stab. Serie 8, w/z=0,60,
Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 11
 Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 11 Prof. Dr. Norbert Hampp Jens Träger Sommersemester 2007 02. 07. 2007 Aufgabe 1 a) Die Dampfdrücke nach dem Raoult schen
Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 11 Prof. Dr. Norbert Hampp Jens Träger Sommersemester 2007 02. 07. 2007 Aufgabe 1 a) Die Dampfdrücke nach dem Raoult schen
Schnellbericht Elbe. Sächsischer Elbe - Längsschnitt. Dresden
 Abteilung Wasser, Boden, Wertstoffe Zur Wetterwarte 11, 01109 Dresden Internet: http://www.smul.sachsen.de/lfulg Schnellbericht Elbe Sächsischer Elbe - Längsschnitt Zehren/ Dresden Ausgewählte Untersuchungsergebnisse
Abteilung Wasser, Boden, Wertstoffe Zur Wetterwarte 11, 01109 Dresden Internet: http://www.smul.sachsen.de/lfulg Schnellbericht Elbe Sächsischer Elbe - Längsschnitt Zehren/ Dresden Ausgewählte Untersuchungsergebnisse
Nachweis- (NG) und Bestimmungsgrenzen (BG)
 1 Freiheitsgrade Nachweis- (NG) und Bestimmungsgrenzen (BG) - Die Anzahl von Freiheitsgraden hängt vor allem von der Anzahl der verfügbaren Informationen ab (A). (A) f = n-v-m f: Freiheitsgrade n: Anzahl
1 Freiheitsgrade Nachweis- (NG) und Bestimmungsgrenzen (BG) - Die Anzahl von Freiheitsgraden hängt vor allem von der Anzahl der verfügbaren Informationen ab (A). (A) f = n-v-m f: Freiheitsgrade n: Anzahl
Klausur Technische Chemie SS 2008 Prof. M. Schönhoff // PD Dr. C. Cramer-Kellers Klausur zur Vorlesung
 Klausur zur Vorlesung Technische Chemie: Reaktionstechnik 14.7.2008 10.00 Uhr bis 12.00 Uhr Name, Vorname Geburtsdatum Studiengang/Semester Matrikelnummer Hinweis: Alle Ansätze und Rechenwege sind mit
Klausur zur Vorlesung Technische Chemie: Reaktionstechnik 14.7.2008 10.00 Uhr bis 12.00 Uhr Name, Vorname Geburtsdatum Studiengang/Semester Matrikelnummer Hinweis: Alle Ansätze und Rechenwege sind mit
Leitthema: Klima und Wetter, langfristige Trends und kurzzeitige Fluktuationen
 Leitthema: Klima und Wetter, langfristige Trends und kurzzeitige Fluktuationen Physikalische Übung zu: statistische Verteilungen, Mittelwerte, Fluktuationen, Wahrscheinlichkeiten und Signifikanz Fragen:
Leitthema: Klima und Wetter, langfristige Trends und kurzzeitige Fluktuationen Physikalische Übung zu: statistische Verteilungen, Mittelwerte, Fluktuationen, Wahrscheinlichkeiten und Signifikanz Fragen:
Einführung. Ablesen von einander zugeordneten Werten
 Einführung Zusammenhänge zwischen Größen wie Temperatur, Geschwindigkeit, Lautstärke, Fahrstrecke, Preis, Einkommen, Steuer etc. werden mit beschrieben. Eine Zuordnung f, die jedem x A genau ein y B zuweist,
Einführung Zusammenhänge zwischen Größen wie Temperatur, Geschwindigkeit, Lautstärke, Fahrstrecke, Preis, Einkommen, Steuer etc. werden mit beschrieben. Eine Zuordnung f, die jedem x A genau ein y B zuweist,
8.4.5 Wasser sieden bei Zimmertemperatur ******
 8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
