|
|
|
- Johanna Müller
- vor 5 Jahren
- Abrufe
Transkript
1 PC III Aufbau der Materie Kapitel 6 Molekülspektren Vorlesung: Übung: 1
2 Molekülspektren Bei der Atomspektroskopie entsprechen die Übergänge immer Änderungen der Elektronenkonfiguration. Bei Molekülen können zusätzlich noch Schwingungen und Rotationen auftreten, was zur Folge hat, dass die entsprechenden Spektren (noch) komplizierter als bei den Atomen sind, dafür aber auch Informationen über Bindungsstärken und Struktur des Moleküls enthalten. Für isolierte (unabhängige) Bewegungsmodi ist die Gesamtenergie E einfach die Summe der elektronischen E el, der vibronischen E vib, und der rotatorischen Energie E rot des Moleküls: E = E rot + E vib + E el Die Energien der Zustände sind deutlich unterschiedlich: E rot << E vib << E el Entsprechend gilt für die Übergänge innerhalb einer Bewegungsform : hν rot << hν vib << hν el ν rot Übergänge zwischen benachbarten Rotationsniveaus im fernen IR oder Mikrowellen (wenige cm -1) ) ν vib Vibrationsübergänge im IR (um 1000 cm -1 ) ν el elektronische Übergänge im sichtbaren / UV 2
3 Spektralbereiche 3
4 Molekülspektren E rot << E vib << E el 4
5 Molekülspektren E rot << E vib << E el 5
6 Molekülspektren Es sollen zunächst Formeln für die Energieniveaus der Rotation angegeben werden und anhand der Auswahlregeln soll dann das reine Rotationsspektrum analysiert werden. Ist die Energie so hoch, dass auch Schwingungen angeregt werden können, dann werden auch gleichzeitig Rotationen mit angeregt. Ist die Energie noch höher, so dass auch elektronische Zustände angeregt werden können, dann werden i.a. sowohl Schwingungen als auch Rotation angeregt sein. Die Übergangswahrscheinlichkeit von einem Zustand n in einen Zustand m ist allgemein über gegeben (dτ ist das Volumenelement) und kann bei Kenntnis von µ und den beiden Wellenfunktionen leicht ausgerechnet werden. 6
7 Dipolmoment Dipolmoment µ = e r <µ> = ψ*(r) (- e r) ψ(r) dτ ψ(r,t) = 1 / 2 [ϕ n (r ) e ie nt /h + ϕ m (r ) e ie mt /h ] <µ mn > = ( e ϕ m *. r. ϕ n dτ e i ωt + konjugiert komplex ) / 2 R mn = ϕ m * r ϕ n dτ <µ mn > = e R mn e iωt 7
8 Zusammenhang zwischen R mn, Emission A mn, Lebensdauer τ und induzierter Absorption B mn I 0 I [counts] I = I 0 e -t /τ t 0 ln(i) = ln(i 0 ) - t / τ t [ps] A mn / Bmn = 8πhν³ / c³ 1 / τ = A mn = 8π²e² / 3 ħεο c³. ν mn ³ R mn ² 8
9 K.-H. Gericke, Mono exponential FLIM I I [counts] 10 I = I 0 e -t /τ t 0 ln(i) = ln(i 0 ) - t / τ t [ps] Fluorescence lifetime picture (τ-map) Picture of: ph-value n η Ca 2+
10 ph-imaging BCECF: ph-indicator pk S = 6.89 large dynamic ph-range high retention in cell HOOC HO HO O O O COOH COOH τ F [ps] Sigmoidal fit τ min = 2488 ± 19 ps τ max = 3597 ± 15 ps ph K.-H. Gericke,
11 K.-H. Gericke, ph-imaging BCECF τ-pictures in artificial epidermis 50 x 51 µm² Depth = 0 µm 3.37 µm 6.74 µm µm µm µm µm µm µm µm
12 K.-H. Gericke, ph-imaging ph - value 7,4 7,2 7,0 6,8 6,6 6,4 6,2 6,0 5,8 5,6 cell intercellular average Depth z [µm] ph-map Depth z = µm Stratum granulosum
13 K.-H. Gericke, Bi-exponential FLIM I [counts] τ free NAD(P)H 1 τ 2 I = a 1 e -t / τ 1 + a 2 e-t / τ 2 enzyme bound NAD(P)H τ 1 -Map τ 2 -Map t [ps] ratio of one component
14 K.-H. Gericke, Cellular metabolism of fibroblasts % 5 µm Fluorescence intensity 0 Cellular metabolism ps 3000 ps τ -Map of free NAD(P)H 0 τ -Map of enzyme bound NAD(P)H 0
15 K.-H. Gericke, NAD(P)H cellular-metabolism NAD(P)H in a B-Cell of a pankreatic islet 5 µm Fluorescence intensity Cellular metabolism free NAD(P)H Enzyme bound NAD(P)H
16 K.-H. Gericke, Phagocytosis Hypher (fungus) (Aspergillus Fumigatus) free conidia (young fungus) phagocyted conidia cell of immune system (neutrophils)
17 Phagocytosis 2D + spectral discrimination + total real time 60 minutes K.-H. Gericke,
18 Phagocytosis K.-H. Gericke,
19 K.-H. Gericke, Zusammenhang zwischen R mn, Emission A mn, Lebensdauer τ und induzierter Absorption B mn I I [counts] 10 I = I 0 e -t /τ t 0 ln(i) = ln(i 0 ) - t / τ t [ps] A mn / Bmn = 8πhν³ / c³ 1 / τ = A mn = 8π²e² / 3 ħεο c³. ν mn ³ R mn ²
20 Zusammenhang zwischen R mn, integriertem Absorptionsquerschnitt σ 0, induzierter Absorption B mn und Oszillatorstärke f mn 20
21 Rotation Ein Körper, der um drei Achsen (A, B, C), sogenannte Hauptträgheitsachsen, frei rotieren kann, hat die Rotationsenergie (klassisch): E = ½ I A ω A 2 + ½ I B ω B 2 + ½ I C ω C 2 mit J i = I i ω i (J = Drehimpuls) erhalten wir: E = J A2 /(2I A ) + J B2 /(2I B ) + J C2 /(2I C ) Sphärischer Kreisel: Symmetrischer Kreisel: I A = I B = I C = I CH 4, CCl 4, SF 6 I A = I B = I und I C = I I > I oblate I < I prolate Benzol CH 3 I linearer Kreisel: I A = 0, I B = I C (alle zweiatomigen Molek.) NO, C 2 N 2, CO 2 asymmetrischer Kreisel: I A I B I C, I A I C I A < I B < I C H 2 O 21
22 Linearer Kreisel B [cm -1 ] = ħ² / 2Ihc = h / 8π²cI Lineare Moleküle wie z.b. HCCH, NCCN, CO 2 ; alle zweiatomigen Moleküle Lineare Moleküle besitzten aufgrund der geringen Masse der Elektronen ein verschwindend kleines Trägheitsmoment bzgl. der Molekülachse, d.h. wir brauchen nur die Rotation um die beiden Achsen senkrecht zur Molekülachse betrachten: Tabelle einiger Rotationskonstanten Molekül I / kgm 2 B / cm -1 A / cm -1 H 2 0,46 60,85 D 2 0,92 30,44 HCl 2,69 10,59 OH 1,51 18,91 O 2 1,98 1,44 N 2 1,43 1,998 I ,037 NH 3 2,81 4,41 9,98 6,34 oblate CH 3 Cl 63,6 0,18 0,444 5,02 prolate CCl ,24 E J = BJ(J + 1) 22
23 Der symmetrische Kreisel K = 0, ±1, ±2,..., ±J J = 0, 1, 2,... B = ħ/(4πci ) A = ħ /(4πcI ) Extremfälle der Rotation eines symmetrischen Kreisel a) um Molekülachse b) senkrecht zur Molekülachse 23
24 Asymmetrischer Kreisel Beispiel: H 2 O, OClO Die Energien eines asymmetrischen Kreisels mit dem Gesamtdrehimpuls J = 3. Die Hauptträgheitsmomente sind willkürlich auf I A = 1 und I C = 2 gesetzt. Die Figur zeigt die Position der Energieniveaus wenn I B zwischen den oblaten und prolaten Grenzfällen variiert. 24
25 Auswahlregeln für reine Rotationsübergänge Die Erhaltung des Drehimpulses liefert uns sofort die Auswahlregeln für ein lineares Molekül: ΔJ = ± 1 ΔM J = 0, ± 1 Für einen symmetrischen Kreisel liegt das Dipolmoment immer parallel zur Molekülachse, d.h. keine Änderung der Rotation um die Molekülachse ist möglich: ΔK = 0 Für eine Absorption, J + 1 <- J, erwarten wir Signale bei folgenden Wellenzahlen ν [cm -1 ] ν = B(J + 1)(J + 2) -BJ(J + 1) ν = 2B(J + 1) mit J = 0, 1, 2... Der Abstand zwischen zwei Linien ist konstant, Δν = ν(j) -ν(j - 1) = 2B. 25
26 Reine Rotationsspektren - Mikrowellen Das Rotationsspektrum des Orionnebels mit den spektralen Fingerabdrücken zwei- und mehratomiger Moleküle in der Wolke. (Nach G. A. Blake et al., Astrophys. J. <B>315</B> (1987) 621.) 26
27 Molekülschwingungen Harmonische Näherung des Potentials: V(r) = ½ kr² Kraft F = - V / r = - k r Kraft F = m r (für eine Masse) Die Bewegungsgleichung m r = - k r hat die Lösung r = a sin ω t (periodische Schwingung) mit Kreisfrequenz ω = 2πν = k m ω = 2πν = 27 k µ
28 Molekülschwingungen In Molekülen schwingen die Atome gegeneinander, wobei sich der Schwerpunkt nicht verschieben darf. Im einfachsten Fall eines zweiatomigen Moleküls A-B, mit den beiden Massen m A und m B bleibt die Lösung erhalten, nur muss die Masse m durch die reduzierte Masse µ ersetzt werden: µ = m m A A + m m B B ω = 2πν = Die Quantenmechanik zeigt, dass die Energie der Schwingung durch gegeben ist. E = hν = 1 2π k µ k µ 28
29 Molekülschwingungen Die Quantenmechanik zeigt auch, dass die Schwingungsenergie nur ganzzahlige Vielfache von 1 k 2π µ sein kann und dem Molekül nur jeweils dieser Betrag als Schwingungsenergie zugeführt werden kann (für V(r)=-kr²). E = hν = 1 2π k µ 29
30 Typische X-H, X=Y, X=Y Bindungen 30
31 Wieviele unterschiedliche Molekülschwingungen gibt es? Ammoniak N = 4, 3 N-6 = 6 Schwingungen Wasser N = 3, 3 N-6 = 3 Schwingungen Kohlendioxid N = 3, 3 N-5 = 4 Schwingungen Sauerstoff N = 2, 3 N-5 = 1 Schwingung Wie diese Schwingungsmoden aussehen haben wir bereits im Kapitel Symmetrie der PC II Vorlesung gesehen. 31
32 Rotations- Schwingungsspektren E gesamt = E v + E r hν = (E v +E r ) (E v +E r ) Vibrationsniveaus E v = (v + ½) hω 0 Rotationsniveaus E r = B J (J + 1) 32
33 Auswahlregeln für symmetrischen Kreisel Die Auswahlregeln für den symmetrischen Kreisel lauten für die sogenannte Parallelbande (ΔK = 0) für K = 0, ΔJ = ± 1 (wie 2atom. Molek.) für K 0, ΔJ = 0, ± 1 (wie 2atom. mit Elektr.) Senkrechtbande (ΔK = ± 1) ΔJ = 0, ± 1 33
34 Bilanz und Fragen Voraussetzung für die IR-Anregung eines Schwingungsübergangs ist, dass sich das dynamische Dipolmoment während der Anregung ändert. o Für Wasser und Kohlendioxid kann man sich das ja noch zur Not vorstellen, aber bei einem beliebigen Molekül? Gibt es da überhaupt eine Chance zu sagen, welche Schwingungen mit IR-Licht angeregt werden können und welche nicht?? Und kann ich diese letzteren evtl. anders anregen??? Die Antwort kennen wir aus der PC II Vorlesung: Symmetrie 34
35 Elektronische Übergänge Wie bei Atomen gibt es verschiedene Energiezustände aufgrund der unterschiedlichen Elektronenkonfiguration. Die Energiezustände sind charakterisiert durch den Spin (Singulett, Dublett, Triplett,...) und durch die Drehimpulskomponente L Z parallel zur Molekülachse, da diese eine ausgewählte Richtung darstellt. Die entsprechenden Eigenwerte Λ werden durch griechische Buchstaben gekennzeichnet: Λ ±1 ±2 ±3 ±4 ±5... Term Σ Π Δ Φ Γ... E gesamt = E el + E vib + E rot E = T e + ω e (v + ½) + BJ(J+1), ΔE = E el + ΔE vib + ΔE rot ΔE el = E' el - E'' el = T' e - T'' e ΔE vib = ω' e (v'+ ½) - ω'' e (v''+½) ΔE rot = B'J'(J'+1) - B''J''(J''+1) 35
36 Auswahlregeln Welche Übergänge möglich sind, wird über die Auswahlregeln festgelegt. Beispiel erlaubt ΔΛ = 0, ± 1 and ΔS = 0 verboten 1 Π 1 Σ 3 Π 1 Σ, da ΔS = 1 1 Π 1 Π 1 Π 1 Φ, da ΔΛ = 2 3 Δ 3 Δ 3 Δ 1 Σ, da ΔS = 1 und ΔΛ = 2 ΔJ = J' - J'' = +1 R-Zweig Für die Rotation gilt Drehimpuls erhaltung: erlaubt ΔJ = 0, ± 1 = 0 Q-Zweig (nicht Σ <-> Σ und nicht J' = 0 <-> J'' = 0) = - 1 P-Zweig aber J'' = 0 <-> J' = 0 verboten 36
37 Raman-Spektroskopie 37
38 Chandrasekhara Venkata Raman Chandrasekhara Venkata Raman * 7. Nov in Trichinopoly (Indien) Nov Karnataka (Indien) 1930 Nobelpreis für Physik 38
39 Lorentz- und Dopplerprofil Lorentzprofil L(ν,ν o ) = 1 / 2π ν L /(ν νo)²+( ν L /2)² ν D = ν o (1 v /c ) I = I o ( 4 ln 2 / π ) ½. 1 / νd e 4ln2((ν ο ν D) / ν D )² ν D = 2 ν o /c (2 ln2 kt / m ) ½ 39
40 Vergleich der Linienformen von einem Lorentz- und einem Gaußprofil (Doppler) gleicher Breite. Die Fläche unter beiden Profilen ist auf 1 normiert. 40
41 Ende Kapitel 6 41
42 Energieumrechnungen Die IR-Spektroskopie (mittleres Infrarot) von Schwingungen umfasst die Spektralbereiche der elektromagnetischen Strahlung cm -1 Wellenzahlen ,5 µm Mikrometer THz Terahertz mev Millielektronenvolt Alle diese Angaben sind äquivalent und durch folgende Umrechnungen miteinander verknüpft: λ [µm] = / ν ~ [cm -1 ] λ = c / ν ν = c / λ ν [Hz] = ν ~ [cm -1 ] ν ~ = 1 / λ E [ev] = 1/ 8065,5 ν ~ [cm -1 ] E = h ν (E = e U) h : PLANCKsches Wirkungsquantum e : Elementarladung U : Spannung [Volt]; hier 1V 42
43 Absorption: Lambert-Beersches Gesetz I 0 dl l c I trans ) Detektor I(ν) = I 0 (ν) 10 -εcl I(ν) = I 0 (ν) e -σ (ν)n (ν) l ecl = log( I 0/ I ) := optische Dichte σ(ν)n(ν)l = ln( I 0/ I ) := Absorbanz 43
44 Absorptionsspektrometer 44
45 FTIR-Spektroskopie (Interferenz) Abb. rechts: beide Wellen (grau und lila) interferieren (überlagern sich) zu einer resultierenden Welle (rot) [Bemerkung: die graue sieht man nur als Animation] 45
46 FTIR-Spektroskopie (Interferenz) Da Spektrometer Licht vieler Wellenlängen verarbeiten, entsteht die Interferenz für jede Wellenlänge. Entsprechend überlagern sich die Interferenz-Intensitäten der einzelnen Wellenlängen zusätzlich. Überlagert man alle Wellenlängen (Kontinuum) des an der Messung beteiligten Lichts, so ergibt sich die vom Detektor erfasste Intensität; als Integral über die Bandbreite B der Anordnung: 46
47 FTIR-Spektroskopie Nach der Fouriertransformation erhält man die Einstrahlspektren und nach Korrektur über das Referenzspektrum (rot), welches durch die Meßzelle, Detektor, Lichtquelle oder andere Gase beeinflußt ist, das eigentliche Spektrum. 1,0 0,9 0,6 HCl Hintergrund (Referenz) HCl / willkürliche HCl Signal Einheiten 0,8 0,5 0,7 0,6 0,4 0,5 0,3 0,4 0,3 0,2 0,2 0,1 0,1 0, Wellenzahl //cm -1 47
48 Gruppenfrequenzen Schwingungen betreffen streng genommen immer ein Molekül als Ganzes. In guter Näherung lassen sich jedoch viele Schwingungen eines Moleküls isoliert betrachten. Im Methylen-Beispiel rechts bewegt sich das Kohlenstoffatom (fälschlicherweise) nicht. Eigentlich bewegen sich die beiden H-Atome auf das C zu und das C bewegt sich auch ein wenig auf die H-Atome zu. Da diese aber wesentlich leichter sind, als das C-Atom, bewegt sich das C-Atom viel weniger. Es befindet sich annähernd in Ruhe. Schwere Atome schwingen schwächer und langsamer als leichte. Die Frequenz der Schwingungen in z.b. einer Alkankette lassen sich so in verschiedene Bereiche unterteilen: Die H-Atome der einzelnen Methylengruppe schwingen viel schneller, als die Methylengruppen gegeneinander (Deformationsschwingungen im C-C-C Winkel). Man kann diese verschiedene Schwingungen näherungsweise einzeln betrachten. Die Abstraktion auf einzelne Molekülgruppen führt zum Konzept der Gruppenfrequenzen. Vielen funktionelle Gruppen besitzen charakteristische Absorptionsfrequenzen. Diese sind nur wenig von ihrer chemischen Umgebung im Molekül abhängig. Sie verschieben sich in deren Abhängigkeit um einen geringen Wert (Shift). So liegt z.b. die Absorption der C=O Doppelbindung einer Carbonylgruppe (-COOH) bei 1705 cm -1, wobei sie aber je nach Umgebung im Bereich cm -1 liegen kann. 48
49 Gruppenfrequenzen Innerhalb der einzelnen Schwingungsgruppen lassen sich die einzelnen Absorptionsbanden bestimmten Schwingungsübergängen zuordnen. In einem Alkan gibt es die Methylengruppen, die z.b. symmetrische und asymmetrische Streckschwingungen beschreiben. 49
50 50
51 Wellenzahl [cm -1 ] Bandenstärke -form Schwingungstyp Verbindungsklasse ss = sehr stark, s = stark, m = mittel, w = schwach, b = breit, sb = sehr breit b ν(oh) Alkohole, Phenole b ν(nh) Amine (Primäre Amine - 2Banden) m, sb ν(oh) Carbonsäuren m-w ν(=c-h) Aromaten, Olefine s-m ν(-c-h) gesättigte Kohlenwasserstoffe 2960, 2870 s-m ν(ch 3 ) gesättigte Kohlenwasserstoffe 2925, 2850 w ν(ch 2 ) gesättigte Kohlenwasserstoffe w ν(-s-h) Thiole, Thiophenole m-s ν(-c X) Acetylene (X=C), Nitrile (X=N) s ν(-x=c=y) Isocyanate, Isothiocyanate, Nitrile s ν(-c=o) Carbonylverbindungen m ν(-c=c) Olefine s δ(-nh 2 ) primäre Säureamide (Amidbande) m δ(-n-h) primäre und sekundäre Amine m ν(-c=c) Ringschwingung der Aromaten ν Streckschwingung einer X-H-Bindung δ Deformationsschwingung einer X-H-Bindung 51
52 Wellenzahl [cm -1 ] Bandenstärke -form Schwingungstyp Verbindungsklasse ss = sehr stark, s = stark, m = mittel, w = schwach, b = breit, sb = sehr breit m ν(-c=c) Ringschwingung der Aromaten s ν(-no 2 ) Nitroverbindungen m ν(-c=c) Ringschwingung der Aromaten s-m δ(-c-h) gesättigte Kohlenwasserstoffe m ν(-c=c) Ringschwingung der Aromaten s ν(-so 2 Sulfonylverbindungen s δ(-ch 3 ) gesättigte Kohlenwasserstoffe m-s δ(c-n) Amide, Amine s ν(no 2 ) Nitroverbindungen ss-s ν(-c-o-c) Ether, Ester, Anhydride, Acetale m-s ν(-so 2 ) Sulfonylverbindungen s ν(-s=o) Solfoxide s δ(=c-h) Olefine s δ(=c-h)o.o.p. Substituierte Benzole m-w ν(-c-hal) Halogenverbindungen m-w ν(-c-s) Thiole, Thioether ν Streckschwingung einer X-H-Bindung δ Deformationsschwingung einer X-H-Bindung 52
53 Symbol Bezeichnung der Schwingungsform α, β i. p. Deformationsschwingung, allgemein in plane Γ o. o. p. Deformationsschwingung von Gerüstatomen out of plane γ o. o. p. Deformationsschwingung i. p. Deformationsschwingung von Gerüstatomen δ i. p. Deformationsschwingung einer X-H-Bindung δ s symmetrische Deformationsschwingung (bending) δ as asymmetrische Deformationsschwingung (bending) δ' Deformationsschwingung (twisting, rocking) κ o. o. p. wagging Schwingung einer XH 2 -Gruppe (X ¹ C) r rocking Schwingung r β i. p. rocking Schwingung r γ o. o. p. rocking Schwingung ρ i. p. rocking Schwingung einer XH 2 -Gruppe (X ¹ C) ν Streckschwingung einer X-H-Bindung ν s symmetrische Streckschwingung ν as asymmetrische Streckschwingung ν β i. p. Streckschwingung ν γ o. o. p. Streckschwingung t twisting Schwingung τ Torsion, twisting Schwingung einer XH 2 -Gruppe (X ¹ C) Φ o. o. p. Ring-Deformationsschwingung ω wagging Schwingung Streckschwingung von Gerüstatomen ohne H-Bindung ω 53
54 Schwingungen CH 2 -Gruppe, CH 4 ρ t ω 54
55 3 N 5 oder Was schwingt noch? Wasser hat als dreiatomiges nichtlineares Molekül 3 Schwingungsmoden CO 2 soll 4 haben, aber welche? Ok: 1. symmetrische Streckschwingung 2. asymmetrische Streckschwingung 3. Biegeschwingung 4. Eine weitere Biegeschwingung: nach oben und unten + nach vorne und hinten Diese beiden Schwingungen sind energetisch nicht zu unterscheiden, man spricht in diesem Fall von einer zweifach entarteten Schwingung. 55
PC II Kinetik und Struktur. Grundzüge der Spektroskopie
 PC II Kinetik und Struktur Kapitel 4 Grundzüge der Spektroskopie Spektralbereiche, Dipolmoment, Molekülschwingungen, Energie der Schwingungen, IR-Absorptions- und Raman-Spektroskopie 1 2 Elektromagnetisches
PC II Kinetik und Struktur Kapitel 4 Grundzüge der Spektroskopie Spektralbereiche, Dipolmoment, Molekülschwingungen, Energie der Schwingungen, IR-Absorptions- und Raman-Spektroskopie 1 2 Elektromagnetisches
Physik IV Einführung in die Atomistik und die Struktur der Materie
 Physik IV Einführung in die Atomistik und die Struktur der Materie Sommersemester 2011 Vorlesung 20 29.06.2011 Physik IV - Einführung in die Atomistik Vorlesung 20 Prof. Thorsten Kröll 29.06.2011 1 Anmeldung
Physik IV Einführung in die Atomistik und die Struktur der Materie Sommersemester 2011 Vorlesung 20 29.06.2011 Physik IV - Einführung in die Atomistik Vorlesung 20 Prof. Thorsten Kröll 29.06.2011 1 Anmeldung
Dynamik von Molekülen. Rotationen und Schwingungen von Molekülen
 Rotationen und Schwingungen von Molekülen Schwingungen und Rotationen Bis jetzt haben wir immer den Fall betrachtet, daß die Kerne fest sind Was geschieht nun, wenn sich die Kerne bewegen können? Zwei
Rotationen und Schwingungen von Molekülen Schwingungen und Rotationen Bis jetzt haben wir immer den Fall betrachtet, daß die Kerne fest sind Was geschieht nun, wenn sich die Kerne bewegen können? Zwei
5. Elektronen- und Rotations- Spektren von Molekülen
 5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
Einführung in die Schwingungsspektroskopie
 Einführung in die Schwingungsspektroskopie Quelle: Frederik Uibel und Andreas Maurer, Uni Tübingen 2004 Molekülbewegungen Translation: Rotation: Die Bewegung des gesamten Moleküls ls in die drei Raumrichtungen.
Einführung in die Schwingungsspektroskopie Quelle: Frederik Uibel und Andreas Maurer, Uni Tübingen 2004 Molekülbewegungen Translation: Rotation: Die Bewegung des gesamten Moleküls ls in die drei Raumrichtungen.
Molekulare Kerndynamik. Grundlagen
 Grundlagen Bei der Bestimmung der elektronischen Struktur von Molekülen haben wir bis jetzt den Fall betrachtet, daß die Kerne fest sind. Lösung der elektronischen Schrödingergleichung in einem festen
Grundlagen Bei der Bestimmung der elektronischen Struktur von Molekülen haben wir bis jetzt den Fall betrachtet, daß die Kerne fest sind. Lösung der elektronischen Schrödingergleichung in einem festen
Spektroskopie. im IR- und UV/VIS-Bereich. Schwingungen.
 Spektroskopie im IR- und UV/VIS-Bereich Schwingungen Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Resonanzschwingungen http://www.youtube.com/watch?v=eaxva XWZ8 Resonanzschwingungen
Spektroskopie im IR- und UV/VIS-Bereich Schwingungen Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Resonanzschwingungen http://www.youtube.com/watch?v=eaxva XWZ8 Resonanzschwingungen
Spektroskopie-Seminar SS Infrarot-Spektroskopie. Infrarot-Spektroskopie
 Infrarot-Spektroskopie 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden die absorbierten
Infrarot-Spektroskopie 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden die absorbierten
Schwingungsspektroskopie
 Schwingungsspektroskopie In N-atomigen Molekülen haben wir 3N-5 (linear) bzw. 3N-6 (nichtlinear) Freiheitsgrade der Schwingung, welche die Position der Atome relativ zueinander beschreiben. Der Potentialterm
Schwingungsspektroskopie In N-atomigen Molekülen haben wir 3N-5 (linear) bzw. 3N-6 (nichtlinear) Freiheitsgrade der Schwingung, welche die Position der Atome relativ zueinander beschreiben. Der Potentialterm
Spektroskopie-Seminar WS 17/18 3 Infrarot-Spektroskopie. Infrarot-Spektroskopie
 WS 17/18 Infrarot-Spektroskopie 1 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden
WS 17/18 Infrarot-Spektroskopie 1 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden
Schwingungsspektroskopie
 In N atomigen Molekülen haben wir 3N 5 (linear) bzw. 3N 6 (nichtlinear) Freiheitsgrade der Schwingung, welche die Position der Atome relativ zueinander beschreiben. Der Potentialterm wird zu einer komplizierten
In N atomigen Molekülen haben wir 3N 5 (linear) bzw. 3N 6 (nichtlinear) Freiheitsgrade der Schwingung, welche die Position der Atome relativ zueinander beschreiben. Der Potentialterm wird zu einer komplizierten
Infrarot-Spektroskopie
 SoSe 19 Infrarot-Spektroskopie E = h v = h c ሚθ E = Energie; h = Planck sches Wirkungsquantum; v = Frequenz; c = Lichtgeschwindigkeit, ሚθ = Wellenzahl 1 3.1 Schwingungsmodi T / % Moleküle werden mit Licht
SoSe 19 Infrarot-Spektroskopie E = h v = h c ሚθ E = Energie; h = Planck sches Wirkungsquantum; v = Frequenz; c = Lichtgeschwindigkeit, ሚθ = Wellenzahl 1 3.1 Schwingungsmodi T / % Moleküle werden mit Licht
Theoretical Biophysics - Quantum Theory and Molecular Dynamics. 13. Vorlesung. Pawel Romanczuk WS 2016/17
 Theoretical Biophysics - Quantum Theory and Molecular Dynamics 13. Vorlesung Pawel Romanczuk WS 2016/17 http://lab.romanczuk.de/teaching Zusammenfassung letzte VL Variationsrechnung LCAO-Verfahren am Beispiel
Theoretical Biophysics - Quantum Theory and Molecular Dynamics 13. Vorlesung Pawel Romanczuk WS 2016/17 http://lab.romanczuk.de/teaching Zusammenfassung letzte VL Variationsrechnung LCAO-Verfahren am Beispiel
Schwingungen (Vibrationen) zweiatomiger Moleküle
 Schwingungen (Vibrationen) zweiatomiger Moleküle Das Molekülpotential ist die Potentialkurve für die Schwingung H 2 Molekül 0.0 2.5 4 5 6 H( 1s) + H( 3l ) Energie in ev 5.0 7.5 H( 1s) + H( 2l ) H( 1s)
Schwingungen (Vibrationen) zweiatomiger Moleküle Das Molekülpotential ist die Potentialkurve für die Schwingung H 2 Molekül 0.0 2.5 4 5 6 H( 1s) + H( 3l ) Energie in ev 5.0 7.5 H( 1s) + H( 2l ) H( 1s)
VL 24 VL Homonukleare Moleküle VL Heteronukleare Moleküle VL Molekülschwingungen
 VL 24 VL 22 22.1. Homonukleare Moleküle VL 23 23.1. Heteronukleare Moleküle VL 24 24.1. Molekülschwingungen Wim de Boer, Karlsruhe Atome und Moleküle, 17.07.2012 1 Zum Mitnehmen Moleküle: Rotation und
VL 24 VL 22 22.1. Homonukleare Moleküle VL 23 23.1. Heteronukleare Moleküle VL 24 24.1. Molekülschwingungen Wim de Boer, Karlsruhe Atome und Moleküle, 17.07.2012 1 Zum Mitnehmen Moleküle: Rotation und
(2.65 ev), da sich die beiden Elektronen gegenseitig abstossen.
 phys4.026 Page 1 13.8 Das Wasserstoff-Molekül Wie im Fall des H2 + Moleküls führen im H2 Molekül symmetrische Wellenfunktionen zu bindenden Zuständen, wohingegen anti-symmetrische Wellenfunktionen zu anti-bindenden
phys4.026 Page 1 13.8 Das Wasserstoff-Molekül Wie im Fall des H2 + Moleküls führen im H2 Molekül symmetrische Wellenfunktionen zu bindenden Zuständen, wohingegen anti-symmetrische Wellenfunktionen zu anti-bindenden
Spektroskopie OC Grundpraktikum. Wintersemester 2006/2007
 Spetrosopie OC Grundpratium Wintersemester 2006/2007 Werner Schwalbach Erste Fassung 10. Dezember 2006 Werner Schwalbach schwalbach@chemie-mainz.de http://www.chemie-mainz.de Dieses Doument darf ohne das
Spetrosopie OC Grundpratium Wintersemester 2006/2007 Werner Schwalbach Erste Fassung 10. Dezember 2006 Werner Schwalbach schwalbach@chemie-mainz.de http://www.chemie-mainz.de Dieses Doument darf ohne das
Methoden-Kurs - Teil IR-Spektroskopie. Anwendungen der IR-Spektroskopie
 Methoden-Kurs - Teil I-Spektroskopie Dr. Markus berthür Fachbereich Chemie, Uni Marburg aum 6217 oberthuer@chemie.uni-marburg.de Anwendungen der I-Spektroskopie Strukturaufklärung von organischen Molekülen
Methoden-Kurs - Teil I-Spektroskopie Dr. Markus berthür Fachbereich Chemie, Uni Marburg aum 6217 oberthuer@chemie.uni-marburg.de Anwendungen der I-Spektroskopie Strukturaufklärung von organischen Molekülen
Die meisten Elemente liegen in gebundener Form als einzelne Moleküle, in Flüssigkeiten oder in Festkörpern vor.
 phys4.025 Page 1 13. Moleküle Nur eine kleine Anzahl von Elementen kommt natürlich in Form von einzelnen Atomen vor. Die meisten Elemente liegen in gebundener Form als einzelne Moleküle, in Flüssigkeiten
phys4.025 Page 1 13. Moleküle Nur eine kleine Anzahl von Elementen kommt natürlich in Form von einzelnen Atomen vor. Die meisten Elemente liegen in gebundener Form als einzelne Moleküle, in Flüssigkeiten
Moleküle und Wärmestatistik
 Moleküle und Wärmestatistik Musterlösung.08.008 Molekülbindung Ein Molekül bestehe aus zwei Atomkernen A und B und zwei Elektronen. a) Wie lautet der Ansatz für die symmetrische Wellenfunktion in der Molekülorbitalnäherung?
Moleküle und Wärmestatistik Musterlösung.08.008 Molekülbindung Ein Molekül bestehe aus zwei Atomkernen A und B und zwei Elektronen. a) Wie lautet der Ansatz für die symmetrische Wellenfunktion in der Molekülorbitalnäherung?
9. Moleküle. 9.1 Wasserstoff-Molekül Ion H Wasserstoff-Molekül H Schwerere Moleküle 9.4 Angeregte Moleküle. Physik IV SS
 9.1 Wasserstoff-Molekül Ion H + 9. Wasserstoff-Molekül H 9.3 Schwerere Moleküle 9.4 Angeregte Moleküle 9.1 9.1 Wasserstoff-Molekül Ion H + Einfachstes Molekül: H + = p + e p + Coulomb-Potenzial: Schrödinger-Gleichung:
9.1 Wasserstoff-Molekül Ion H + 9. Wasserstoff-Molekül H 9.3 Schwerere Moleküle 9.4 Angeregte Moleküle 9.1 9.1 Wasserstoff-Molekül Ion H + Einfachstes Molekül: H + = p + e p + Coulomb-Potenzial: Schrödinger-Gleichung:
Ferienkurs Experimentalphysik Übung 4 - Musterlösung
 Ferienkurs Experimentalphysik 4 11 Übung 4 - Musterlösung 1. Übergänge im Wasserstoffatom (**) Ein Wasserstoffatom befindet sich im angeregten Zustand p und geht durch spontane Emission eines Photons in
Ferienkurs Experimentalphysik 4 11 Übung 4 - Musterlösung 1. Übergänge im Wasserstoffatom (**) Ein Wasserstoffatom befindet sich im angeregten Zustand p und geht durch spontane Emission eines Photons in
z n z m e 2 WW-Kern-Kern H = H k + H e + H ek
 2 Molekülphysik Moleküle sind Systeme aus mehreren Atomen, die durch Coulomb-Wechselwirkungen Elektronen und Atomkerne ( chemische Bindung ) zusammengehalten werden. 2.1 Born-Oppenheimer Näherung Der nichtrelativistische
2 Molekülphysik Moleküle sind Systeme aus mehreren Atomen, die durch Coulomb-Wechselwirkungen Elektronen und Atomkerne ( chemische Bindung ) zusammengehalten werden. 2.1 Born-Oppenheimer Näherung Der nichtrelativistische
Teil 1 Schwingungsspektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 1 Schwingungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Themenüberblick Schwingungsspektroskopie Physikalische Grundlagen: Mechanisches Bild
Teil 1 Schwingungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Themenüberblick Schwingungsspektroskopie Physikalische Grundlagen: Mechanisches Bild
Übungen Atom- und Molekülphysik für Physiklehrer (Teil 2)
 Übungen Atom- und Molekülphysik für Physiklehrer (Teil ) Aufgabe 38) Welche J-Werte sind bei den Termen S, P, 4 P und 5 D möglich? Aufgabe 39) Welche Werte kann der Gesamtdrehimpuls eines f-elektrons im
Übungen Atom- und Molekülphysik für Physiklehrer (Teil ) Aufgabe 38) Welche J-Werte sind bei den Termen S, P, 4 P und 5 D möglich? Aufgabe 39) Welche Werte kann der Gesamtdrehimpuls eines f-elektrons im
Atom-, Molekül- und Festkörperphysik
 Atom-, Molekül- und Festkörperphysik für LAK, SS 2013 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 6. Vorlesung, 16. 5. 2013 Molekülspektren, Normalkoordinaten, Franck-Condonprinzip,
Atom-, Molekül- und Festkörperphysik für LAK, SS 2013 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 6. Vorlesung, 16. 5. 2013 Molekülspektren, Normalkoordinaten, Franck-Condonprinzip,
Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: Die Essentials der letzten Vorlesung Funktionelle Gruppen
Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: Die Essentials der letzten Vorlesung Funktionelle Gruppen
Strukturaufklärung (BSc-Chemie): Einführung
 Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Short Summary of the Essentials of the PC V Lecture. To be covered by the first excercise of this class
 Short Summary of the Essentials of the PC V Lecture To be covered by the first excercise of this class Das elektromagnetische Spektrum und Spektralbereiche Lineare Polarisation Elektromagnetische Wellen
Short Summary of the Essentials of the PC V Lecture To be covered by the first excercise of this class Das elektromagnetische Spektrum und Spektralbereiche Lineare Polarisation Elektromagnetische Wellen
Grundlagen der Quantentheorie
 Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Seminar WiSe 2015/2016
 IR-Spektroskopie Seminar WiSe 2015/2016 PD Dr. Markus Nett Nachwuchsgruppenleiter Leibniz-Institut für Naturstoff-Forschung und Infektionsbiologie E-mail: markus.nett@hki-jena.de Anwendungsfelder der IR-Spektroskopie
IR-Spektroskopie Seminar WiSe 2015/2016 PD Dr. Markus Nett Nachwuchsgruppenleiter Leibniz-Institut für Naturstoff-Forschung und Infektionsbiologie E-mail: markus.nett@hki-jena.de Anwendungsfelder der IR-Spektroskopie
Ψ = Dexp( k II a) mit k II = [ 2m e (V 0 E)/ 2] 1/2
![Ψ = Dexp( k II a) mit k II = [ 2m e (V 0 E)/ 2] 1/2 Ψ = Dexp( k II a) mit k II = [ 2m e (V 0 E)/ 2] 1/2](/thumbs/97/132117650.jpg) Institut für Physikalische Chemie Lösungen zu den Übungen zur Vorlesung Physikalische Chemie II im WS 015/016 Prof. Dr. Eckhard Bartsch / Marcel Werner M.Sc. Aufgabenblatt 11 vom 9.01.16 Aufgabe 11 1 L
Institut für Physikalische Chemie Lösungen zu den Übungen zur Vorlesung Physikalische Chemie II im WS 015/016 Prof. Dr. Eckhard Bartsch / Marcel Werner M.Sc. Aufgabenblatt 11 vom 9.01.16 Aufgabe 11 1 L
Klausur zum Modul PC-3-P - Matrie und Strahlung
 Klausur zum Modul PC-3-P - Matrie und Strahlung Nils Bartels 8. September 008 Formaldehyd 1 Spektroskopischer Nachweis von Formaldehyd in der Raumluft 1.1 Rotationsspektrum Die übergeordnete Auswahlregel
Klausur zum Modul PC-3-P - Matrie und Strahlung Nils Bartels 8. September 008 Formaldehyd 1 Spektroskopischer Nachweis von Formaldehyd in der Raumluft 1.1 Rotationsspektrum Die übergeordnete Auswahlregel
FK Ex 4 - Musterlösung 08/09/2015
 FK Ex 4 - Musterlösung 08/09/2015 1 Spektrallinien Die Natrium-D-Linien sind emittiertes Licht der Wellenlänge 589.5932 nm (D1) und 588.9965 nm (D2). Diese charakteristischen Spektrallinien entstehen beim
FK Ex 4 - Musterlösung 08/09/2015 1 Spektrallinien Die Natrium-D-Linien sind emittiertes Licht der Wellenlänge 589.5932 nm (D1) und 588.9965 nm (D2). Diese charakteristischen Spektrallinien entstehen beim
Ferienkurs Experimentalphysik 4
 Ferienkurs Experimentalphysik 4 Vorlesung 4 Emission und Absorption elektromagnetischer Strahlung Stephan Huber, Markus Kotulla, Markus Perner 01.09.2011 Inhaltsverzeichnis 1 Emission und Absorption elektromagnetischer
Ferienkurs Experimentalphysik 4 Vorlesung 4 Emission und Absorption elektromagnetischer Strahlung Stephan Huber, Markus Kotulla, Markus Perner 01.09.2011 Inhaltsverzeichnis 1 Emission und Absorption elektromagnetischer
Termschema des neutralen Natriumatoms. Die Zahlen bei den schrägen Strichen sind die Wellenlängen beobachteter Übergänge in nm.
 Termschema des neutralen Natriumatoms. Die Zahlen bei den schrägen Strichen sind die Wellenlängen beobachteter Übergänge in nm. Prof. Dr. D. Winklmair Wechselwirkung 1/11 Symmetrische Valenzschwingung
Termschema des neutralen Natriumatoms. Die Zahlen bei den schrägen Strichen sind die Wellenlängen beobachteter Übergänge in nm. Prof. Dr. D. Winklmair Wechselwirkung 1/11 Symmetrische Valenzschwingung
1.8 IR-Spektroskopie. Physikalisches Praktikum für Fortgeschrittene. Abteilung B: Institut für Festkörperphysik
 1.8 IR-Spektroskopie Physikalisches Praktikum für Fortgeschrittene Abteilung B: Institut für Festkörperphysik Inhaltsverzeichnis 1 Einführung 3 2 Theoretische Grundlagen 4 2.1 Rotationsschwingungsspektroskopie......................
1.8 IR-Spektroskopie Physikalisches Praktikum für Fortgeschrittene Abteilung B: Institut für Festkörperphysik Inhaltsverzeichnis 1 Einführung 3 2 Theoretische Grundlagen 4 2.1 Rotationsschwingungsspektroskopie......................
Experimentalphysik E1
 Experimentalphysik E1 Erzwungene & gekoppelte Schwingungen Alle Informationen zur Vorlesung unter : http://www.physik.lmu.de/lehre/vorlesungen/index.html 10. Jan. 016 Gedämpfte Schwingungen m d x dt +
Experimentalphysik E1 Erzwungene & gekoppelte Schwingungen Alle Informationen zur Vorlesung unter : http://www.physik.lmu.de/lehre/vorlesungen/index.html 10. Jan. 016 Gedämpfte Schwingungen m d x dt +
Hilfsmittel sind nicht zugelassen, auch keine Taschenrechner! Heftung nicht lösen! Kein zusätzliches Papier zugelassen!
 Physik / Klausur Anfang WS /3 Heift / Kurtz Name: Vorname: Matrikel-Nr: Unterschrift: Formeln siehe letzte Rückseite! Hilfsmittel sind nicht zugelassen, auch keine Taschenrechner! Heftung nicht lösen!
Physik / Klausur Anfang WS /3 Heift / Kurtz Name: Vorname: Matrikel-Nr: Unterschrift: Formeln siehe letzte Rückseite! Hilfsmittel sind nicht zugelassen, auch keine Taschenrechner! Heftung nicht lösen!
4.2.2.Das Wasserstoff-Molekül H 2 Vergleich der Wellenfunktionen für antiparallele Spinkonfiguration
 g 4.2.2.Das Wasserstoff-Molekül H 2 Vergleich der Wellenfunktionen für antiparallele Spinkonfiguration a () ϕ ( 2) ϕ ( 2) ϕ ( 1) ψ = ϕ + 1 b a b Heitler-London ( ) ϕ ( 2) + ϕ ( 2) ϕ ( 1) + [ ϕ ( 1) ϕ (
g 4.2.2.Das Wasserstoff-Molekül H 2 Vergleich der Wellenfunktionen für antiparallele Spinkonfiguration a () ϕ ( 2) ϕ ( 2) ϕ ( 1) ψ = ϕ + 1 b a b Heitler-London ( ) ϕ ( 2) + ϕ ( 2) ϕ ( 1) + [ ϕ ( 1) ϕ (
Ferienkurs Experimentalphysik Übung 2 - Musterlösung
 Ferienkurs Experimentalphysik 4 00 Übung - Musterlösung Kopplung von Drehimpulsen und spektroskopische Notation (*) Vervollständigen Sie untenstehende Tabelle mit den fehlenden Werten der Quantenzahlen.
Ferienkurs Experimentalphysik 4 00 Übung - Musterlösung Kopplung von Drehimpulsen und spektroskopische Notation (*) Vervollständigen Sie untenstehende Tabelle mit den fehlenden Werten der Quantenzahlen.
PN 2 Einführung in die Experimentalphysik für Chemiker
 PN 2 Einführung in die Experimentalphysik für Chemiker 9. Vorlesung 13.6.08 Evelyn Plötz, Thomas Schmierer, Gunnar Spieß, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
PN 2 Einführung in die Experimentalphysik für Chemiker 9. Vorlesung 13.6.08 Evelyn Plötz, Thomas Schmierer, Gunnar Spieß, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
Kapitel 7: Elektronische Spektroskopie
 Kapitel 7: Elektronische Spektroskopie Übersicht: 7.1 Drehimpuls-Kopplungshierarchien in Molekülen: Hundsche Fälle 7.2 Auswahlregeln für rovibronische Übergänge 7.3 Das Franck-Condon-Prinzip 7.4 Zerfall
Kapitel 7: Elektronische Spektroskopie Übersicht: 7.1 Drehimpuls-Kopplungshierarchien in Molekülen: Hundsche Fälle 7.2 Auswahlregeln für rovibronische Übergänge 7.3 Das Franck-Condon-Prinzip 7.4 Zerfall
PC2: Spektroskopie Störungsrechnung
 PC: Spektroskopie Störungsrechnung (neu überarbeitet im SS 014, nach: Wedler-Freund, Physikalische Chemie) Wir betrachten ein System aus quantenchemischen Zuständen m, n, zwischen denen durch die Absorption
PC: Spektroskopie Störungsrechnung (neu überarbeitet im SS 014, nach: Wedler-Freund, Physikalische Chemie) Wir betrachten ein System aus quantenchemischen Zuständen m, n, zwischen denen durch die Absorption
Protokoll zum Versuch Infrarot-Spektren mehratomiger Gase
 Protokoll zum Versuch Infrarot-Spektren mehratomiger Gase. Versuchsziel / Experimentelles In diesem Versuch wird ein Infrarot-Spektrum von CO im Bereich der Wellenzahlen ν von 6000 bis 400 cm- mit einer
Protokoll zum Versuch Infrarot-Spektren mehratomiger Gase. Versuchsziel / Experimentelles In diesem Versuch wird ein Infrarot-Spektrum von CO im Bereich der Wellenzahlen ν von 6000 bis 400 cm- mit einer
IR-Durchstrahlgeräte. Ältere dispersive Technik. Modernre FT-Technik IR 1. H.Hug/Instrumentelle Analytik/Europa-Nr.:72116, 2010
 -Durchstrahlgeräte Ältere dispersive Technik Modernre FT-Technik H.Hug/Instrumentelle Analytik/Europa-Nr.:72116, 2010 1 -Durchstrahlgeräte Messprinzip : dispersives Einkanal -Gerät http://www.chemgapedia.de/vsengine/vlu/vsc/de/ch/3/anc/ir_spek/ir_geraete.vlu/page/vsc/de/ch/3/anc/ir_spek/ir_spektroskopie/ir_geraetetechnik/ir_8_4/zweistrahl_m35
-Durchstrahlgeräte Ältere dispersive Technik Modernre FT-Technik H.Hug/Instrumentelle Analytik/Europa-Nr.:72116, 2010 1 -Durchstrahlgeräte Messprinzip : dispersives Einkanal -Gerät http://www.chemgapedia.de/vsengine/vlu/vsc/de/ch/3/anc/ir_spek/ir_geraete.vlu/page/vsc/de/ch/3/anc/ir_spek/ir_spektroskopie/ir_geraetetechnik/ir_8_4/zweistrahl_m35
Vorlesung Statistische Mechanik: N-Teilchensystem
 Virialentwicklung Die Berechnung der Zustandssumme bei realen Gasen ist nicht mehr exakt durchführbar. Eine Möglichkeit, die Wechselwirkung in realen Gasen systematisch mitzunehmen ist, eine Entwicklung
Virialentwicklung Die Berechnung der Zustandssumme bei realen Gasen ist nicht mehr exakt durchführbar. Eine Möglichkeit, die Wechselwirkung in realen Gasen systematisch mitzunehmen ist, eine Entwicklung
Infrarot Spektroskopie organischer Verbindungen
 Infrarot Spektroskopie organischer Verbindungen Praktikum (B.C. 3.4) Lehrstuhl für Instrumentelle Analytik Michael Deicke Michael.Deicke@uni-jena.de Ziele des Praktikums IR-Spektren organischer Verbindungen
Infrarot Spektroskopie organischer Verbindungen Praktikum (B.C. 3.4) Lehrstuhl für Instrumentelle Analytik Michael Deicke Michael.Deicke@uni-jena.de Ziele des Praktikums IR-Spektren organischer Verbindungen
Seminar zum Praktikum Anorganische Chemie III III
 Seminar zum Praktikum Anorganische Chemie III III Metallorganische Chemie Dr. J. Wachter IR-Teil3 www.chemie.uni-regensburg.de/anorganische_chemie/scheer/lehre.html www.chemie.uniregensburg.de/anorganische_chemie/wachter/lehre.html
Seminar zum Praktikum Anorganische Chemie III III Metallorganische Chemie Dr. J. Wachter IR-Teil3 www.chemie.uni-regensburg.de/anorganische_chemie/scheer/lehre.html www.chemie.uniregensburg.de/anorganische_chemie/wachter/lehre.html
Einführung in die Physik
 Einführung in die Physik für Pharmazeuten und Biologen (PPh) Mechanik, Elektrizitätslehre, Optik Übung : Vorlesung: Tutorials: Montags 13:15 bis 14 Uhr, Liebig-HS Montags 14:15 bis 15:45, Liebig HS Montags
Einführung in die Physik für Pharmazeuten und Biologen (PPh) Mechanik, Elektrizitätslehre, Optik Übung : Vorlesung: Tutorials: Montags 13:15 bis 14 Uhr, Liebig-HS Montags 14:15 bis 15:45, Liebig HS Montags
Vorlesung Soft Matter" Prof. Dr. F. Kremer
 Vorlesung Soft Matter" Prof. Dr. F. Kremer Outline of the lecture (9.6.0) Vibrational spectroscopy The quantenmechanical rotator The information content of IR-spectra Vibrational modes of molecules being
Vorlesung Soft Matter" Prof. Dr. F. Kremer Outline of the lecture (9.6.0) Vibrational spectroscopy The quantenmechanical rotator The information content of IR-spectra Vibrational modes of molecules being
Chemisches Grundpraktikum II (270002) Kernresonanzspektroskopie. NMR-Spektroskopie
 hemisches Grundpraktikum II (270002) Kernresonanzspektroskopie NMR-Spektroskopie (Nuclear Magnetic Resonance). Kählig, SS 2010 Von der Substanz zur Struktur Substanz NMR - Spektren Struktur N N 1 Spektroskopie
hemisches Grundpraktikum II (270002) Kernresonanzspektroskopie NMR-Spektroskopie (Nuclear Magnetic Resonance). Kählig, SS 2010 Von der Substanz zur Struktur Substanz NMR - Spektren Struktur N N 1 Spektroskopie
Übungsaufgaben zur NMR-Spektrometrie
 Übungsaufgaben NMR 33 Übungsaufgaben zur NMR-Spektrometrie Aufgabe 1 a) Wieviele unterschiedliche Orientierungen des Kernmomentes relativ zu einem externen Magnetfeld sind beim 14 N-Kern (I = 1, γ = 1.932
Übungsaufgaben NMR 33 Übungsaufgaben zur NMR-Spektrometrie Aufgabe 1 a) Wieviele unterschiedliche Orientierungen des Kernmomentes relativ zu einem externen Magnetfeld sind beim 14 N-Kern (I = 1, γ = 1.932
Vorlesung 25: Vibration und Rotation der Moleküle Auswahlregeln. Folien auf dem Web:
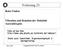 Vorlesung 25: Roter Faden: Vibration und Rotation der Moleküle Auswahlregeln Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: Demtröder, Experimentalphysik 3, Springerverlag
Vorlesung 25: Roter Faden: Vibration und Rotation der Moleküle Auswahlregeln Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: Demtröder, Experimentalphysik 3, Springerverlag
Betrag des Drehimpulses
 Voresung Spektroskopie Sommersemester 001 Prof. Dr. W. Knoche 5. Rotations- und Schwingungsspektren 5.1. Rotationsspektren Freie Rotation eines starren Moeküs um drei Achsen: x y J = J + J + J z J J =
Voresung Spektroskopie Sommersemester 001 Prof. Dr. W. Knoche 5. Rotations- und Schwingungsspektren 5.1. Rotationsspektren Freie Rotation eines starren Moeküs um drei Achsen: x y J = J + J + J z J J =
Experimentelle Physik II
 Experimentelle Physik II Sommersemester 08 Vladimir Dyakonov (Lehrstuhl Experimentelle Physik VI) VL#8 07-05-2008 Tel. 0931/888 3111 dyakonov@physik.uni-wuerzburg.de Experimentelle Physik II 2. Rotationen
Experimentelle Physik II Sommersemester 08 Vladimir Dyakonov (Lehrstuhl Experimentelle Physik VI) VL#8 07-05-2008 Tel. 0931/888 3111 dyakonov@physik.uni-wuerzburg.de Experimentelle Physik II 2. Rotationen
Optische Spektroskopie mit Lasern: Grundlagen und Anwendungen. Wann: Mi Fr Wo: P1 - O1-306
 Laserspektroskopie Was: Optische Spektroskopie mit Lasern: Grundlagen und Anwendungen Wann: Mi 13 15-14 00 Fr 10 15-12 00 Wo: P1 - O1-306 Wer: Dieter Suter Raum P1-O1-216 Tel. 3512 Dieter.Suter@uni-dortmund.de
Laserspektroskopie Was: Optische Spektroskopie mit Lasern: Grundlagen und Anwendungen Wann: Mi 13 15-14 00 Fr 10 15-12 00 Wo: P1 - O1-306 Wer: Dieter Suter Raum P1-O1-216 Tel. 3512 Dieter.Suter@uni-dortmund.de
PC-II-08 Seite 1 von 5 WiSe 09/10. Zusammenhang zwischen Quantenmechanik und MolekÄlspektroskopie
 PC-II-08 Seite 1 von 5 WiSe 09/10 Zusammenhang zwischen Quantenmechanik und MolekÄlspektroskopie PC-II-08 Seite von 5 WiSe 09/10 Rotations- und Schwingungsspektroskopie Rotationsspektroskopie Die Rotationsspektroskopie
PC-II-08 Seite 1 von 5 WiSe 09/10 Zusammenhang zwischen Quantenmechanik und MolekÄlspektroskopie PC-II-08 Seite von 5 WiSe 09/10 Rotations- und Schwingungsspektroskopie Rotationsspektroskopie Die Rotationsspektroskopie
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
Ein Lehrbuch für Studierende der Chemie im 2. Studienabschnitt
 Atom- und Molekülbau Ein Lehrbuch für Studierende der Chemie im 2. Studienabschnitt Von Peter C. Schmidt und Konrad G. Weil 147 Abbildungen, 19 Tabellen Georg Thieme Verlag Stuttgart New York 1982 Vorwort
Atom- und Molekülbau Ein Lehrbuch für Studierende der Chemie im 2. Studienabschnitt Von Peter C. Schmidt und Konrad G. Weil 147 Abbildungen, 19 Tabellen Georg Thieme Verlag Stuttgart New York 1982 Vorwort
Thema heute: Aufbau der Materie: Das Bohr sche Atommodell
 Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Physik im Querschnitt (nicht vertieft) Übungsblatt Atom- und Molekülphysik
 Physik im Querschnitt (nicht vertieft) Übungsblatt Atom- und Molekülphysik WS2018/19 Pupeza/Nubbemeyer 7.12.2018 Aufgabe 25 Spektroskopie von Quantenniveaus a) Benennen Sie zwei Experimente, mit denen
Physik im Querschnitt (nicht vertieft) Übungsblatt Atom- und Molekülphysik WS2018/19 Pupeza/Nubbemeyer 7.12.2018 Aufgabe 25 Spektroskopie von Quantenniveaus a) Benennen Sie zwei Experimente, mit denen
Lösung zur Klausur
 ösung zur Klausur 1..01 Aufgabe 1.) a) Hundsche Regeln: maximaler Spin, dann maximales Bahnmoment. Die beiden Elektronen im 4s kann man vernachlässigen, da sie weder Spin- noch Bahmoment beitragen. Damit
ösung zur Klausur 1..01 Aufgabe 1.) a) Hundsche Regeln: maximaler Spin, dann maximales Bahnmoment. Die beiden Elektronen im 4s kann man vernachlässigen, da sie weder Spin- noch Bahmoment beitragen. Damit
Physik für Maschinenbau. Prof. Dr. Stefan Schael RWTH Aachen
 Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
12.8 Eigenschaften von elektronischen Übergängen. Übergangsfrequenz
 phys4.024 Page 1 12.8 Eigenschaften von elektronischen Übergängen Übergangsfrequenz betrachte die allgemeine Lösung ψ n der zeitabhängigen Schrödinger-Gleichung zum Energieeigenwert E n Erwartungswert
phys4.024 Page 1 12.8 Eigenschaften von elektronischen Übergängen Übergangsfrequenz betrachte die allgemeine Lösung ψ n der zeitabhängigen Schrödinger-Gleichung zum Energieeigenwert E n Erwartungswert
IR- Kurs OC1-Praktikum
 IR- Kurs OC1-Praktikum Dr. Julia Wirmer-Bartoschek Schwalbe Gruppe N160 Raum 315 ferner@nmr.uni-frankfurt.de Seite 1 Spektroskopische Methoden, Messgrössen -rays x-rays UV VIS IR -wave radio 10-10 10-8
IR- Kurs OC1-Praktikum Dr. Julia Wirmer-Bartoschek Schwalbe Gruppe N160 Raum 315 ferner@nmr.uni-frankfurt.de Seite 1 Spektroskopische Methoden, Messgrössen -rays x-rays UV VIS IR -wave radio 10-10 10-8
Experimentalphysik E1
 Experimentalphysik E1 Gedämpfte & erzwungene Schwingungen Alle Informationen zur Vorlesung unter : http://www.physik.lmu.de/lehre/vorlesungen/index.html 16. Dez. 16 Harmonische Schwingungen Auslenkung
Experimentalphysik E1 Gedämpfte & erzwungene Schwingungen Alle Informationen zur Vorlesung unter : http://www.physik.lmu.de/lehre/vorlesungen/index.html 16. Dez. 16 Harmonische Schwingungen Auslenkung
IR-Spektroskopie Seminar Analytische Chemie I (BC3.4, MCB B1; WS2016/17) Dr. Peter Bellstedt NMR Plattform IAAC & IOMC
 IR-Spektroskopie Seminar Analytische Chemie I (BC3.4, MCB B1; WS2016/17) Dr. Peter Bellstedt NMR Plattform IAAC & IOMC Peter.Bellstedt@uni-jena.de Terminübersicht (14 täg.) Gruppe 1 Gruppe 2 1. Seminar
IR-Spektroskopie Seminar Analytische Chemie I (BC3.4, MCB B1; WS2016/17) Dr. Peter Bellstedt NMR Plattform IAAC & IOMC Peter.Bellstedt@uni-jena.de Terminübersicht (14 täg.) Gruppe 1 Gruppe 2 1. Seminar
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Kernmagnetische Resonanzspektroskopie (NMR) Spektroskopische Methoden
 Kernmagnetische Resonanzspektroskopie (NMR) Spektroskopische Methoden Grundlagen Die meisten Atomkerne führen eine Drehbewegung um die eigene Achse aus ("Spin"). Da sie geladene Teilchen (Protonen) enthalten,
Kernmagnetische Resonanzspektroskopie (NMR) Spektroskopische Methoden Grundlagen Die meisten Atomkerne führen eine Drehbewegung um die eigene Achse aus ("Spin"). Da sie geladene Teilchen (Protonen) enthalten,
Übungen zur Spektroskopie 2
 Übungen zur Spektroskopie 2 C. Dubler und Dr. D. S. Stephenson Department Chemie, Universität München Sie finden diese Übungen und alte Klausuren (mit Lösung) auf unserer Homepage: http://cicum200.cup.unimuenchen.de/intranet/depch/analytik/nmr_f/index.php
Übungen zur Spektroskopie 2 C. Dubler und Dr. D. S. Stephenson Department Chemie, Universität München Sie finden diese Übungen und alte Klausuren (mit Lösung) auf unserer Homepage: http://cicum200.cup.unimuenchen.de/intranet/depch/analytik/nmr_f/index.php
Vorlesung 25: Vibration und Rotation der Moleküle Auswahlregeln. Folien auf dem Web:
 Vorlesung 25: Roter Faden: Vibration und Rotation der Moleküle Auswahlregeln Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: Demtröder, Experimentalphysik 3, Springerverlag
Vorlesung 25: Roter Faden: Vibration und Rotation der Moleküle Auswahlregeln Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: Demtröder, Experimentalphysik 3, Springerverlag
Gruppentheorie ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD. Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE
 ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Physikalische Chemie Prof. Dr. Walter Langel Gruppentheorie Molekülschwingungen
ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Physikalische Chemie Prof. Dr. Walter Langel Gruppentheorie Molekülschwingungen
Photonik Technische Nutzung von Licht
 Photonik Technische Nutzung von Licht Produktionsautomatisierung II IR-Spektroskopie Dipolmoment Räumlich getrennte positive und elektrische Ladungen haben zusammen ein Dipolmoment. p = q (r 1 r 2 ) =
Photonik Technische Nutzung von Licht Produktionsautomatisierung II IR-Spektroskopie Dipolmoment Räumlich getrennte positive und elektrische Ladungen haben zusammen ein Dipolmoment. p = q (r 1 r 2 ) =
Übungen zur Vorlesung Physikalische Chemie 2 (B. Sc.) Lösungsvorschlag zu Blatt 12
 Übungen zur Vorlesung Physikalische Chemie B. Sc. ösungsvorschlag zu Blatt 1 Prof. Dr. Norbert Hampp Jens Träger Wintersemester 7/8. 1. 8 Aufgabe 1 Welche Schwingungsübergänge in einem elektronischen Spektrum
Übungen zur Vorlesung Physikalische Chemie B. Sc. ösungsvorschlag zu Blatt 1 Prof. Dr. Norbert Hampp Jens Träger Wintersemester 7/8. 1. 8 Aufgabe 1 Welche Schwingungsübergänge in einem elektronischen Spektrum
Ferienkurs Experimentalphysik 4
 Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Ferienkurs der TU München- - Experimentalphysik 4 Wasserstoffatom, Feinstruktur und Atome im Magnetfeld. Jonas J. Funke
 Ferienkurs der TU München- - Experimentalphysik 4 Wasserstoffatom, Feinstruktur und Atome im Magnetfeld Lösung Jonas J. Funke 0.08.00-0.09.00 Aufgabe (Drehimpulsaddition). : Gegeben seien zwei Drehimpulse
Ferienkurs der TU München- - Experimentalphysik 4 Wasserstoffatom, Feinstruktur und Atome im Magnetfeld Lösung Jonas J. Funke 0.08.00-0.09.00 Aufgabe (Drehimpulsaddition). : Gegeben seien zwei Drehimpulse
Schwingungsspektroskopie (IR, Raman)
 Schwingungsspektroskopie Schwingungsspektroskopie (IR, Raman) Die Schwingungsspektroskopie ist eine energiesensitive Methode. Sie beruht auf den durch Molekülschwingungen hervorgerufenen periodischen Änderungen
Schwingungsspektroskopie Schwingungsspektroskopie (IR, Raman) Die Schwingungsspektroskopie ist eine energiesensitive Methode. Sie beruht auf den durch Molekülschwingungen hervorgerufenen periodischen Änderungen
9. GV: Atom- und Molekülspektren
 Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
Die Rotationsterme werden im Folgenden wegen der geringen Auflösung des Gerätes nicht weiter betrachtet. Für kleine Schwingungsamplituden gilt näherun
 UV/VIS-Spektroskopie: Optische Bestimmung der Dissoziationsenergie von I 2 Es soll ein UV/VIS-Spektrum von Ioddampf aufgenommen werden. Daraus sollen die Bandensysteme der v 00 -Progressionen (v 00 = 0,
UV/VIS-Spektroskopie: Optische Bestimmung der Dissoziationsenergie von I 2 Es soll ein UV/VIS-Spektrum von Ioddampf aufgenommen werden. Daraus sollen die Bandensysteme der v 00 -Progressionen (v 00 = 0,
Linienform- und Breite
 Linienform- und Breite a) Wodurch ist die Breite eienr Absorptions- (Emissions-) Linie gegeben? welche Anteile gibt es, welcher Anteil dominiert im Normalfall? Dopplerbreite, Stossverbreiterung, natuerliche
Linienform- und Breite a) Wodurch ist die Breite eienr Absorptions- (Emissions-) Linie gegeben? welche Anteile gibt es, welcher Anteil dominiert im Normalfall? Dopplerbreite, Stossverbreiterung, natuerliche
UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie
 Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2018/19 www.ruhr-uni-bochum.de/chirality 1 Komplementärfarben Absorbiert eine Probe gelbes
Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2018/19 www.ruhr-uni-bochum.de/chirality 1 Komplementärfarben Absorbiert eine Probe gelbes
UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie
 Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Reminder: MO-Diagramm von O 2 2- MdS-1 UV/Vis-Spektroskopie
Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Reminder: MO-Diagramm von O 2 2- MdS-1 UV/Vis-Spektroskopie
NMR Spektroskopie. 1nm Frequenz X-ray UV/VIS Infrared Microwave Radio
 NMR Spektroskopie 1nm 10 10 2 10 3 10 4 10 5 10 6 10 7 Frequenz X-ray UV/VIS Infrared Microwave Radio Anregungsmodus electronic Vibration Rotation Nuclear Spektroskopie X-ray UV/VIS Infrared/Raman NMR
NMR Spektroskopie 1nm 10 10 2 10 3 10 4 10 5 10 6 10 7 Frequenz X-ray UV/VIS Infrared Microwave Radio Anregungsmodus electronic Vibration Rotation Nuclear Spektroskopie X-ray UV/VIS Infrared/Raman NMR
Einführung in die Spektroskopie für Studenten der Biologie
 Einführung in die Spektroskopie für Studenten der Biologie Jörg H. Kleinschmidt http://www.biologie.uni-konstanz.de/folding/home.html Literatur Banwell, C. N., Elaine M. McCash, Molekülspektroskopie. Ein
Einführung in die Spektroskopie für Studenten der Biologie Jörg H. Kleinschmidt http://www.biologie.uni-konstanz.de/folding/home.html Literatur Banwell, C. N., Elaine M. McCash, Molekülspektroskopie. Ein
Rotationsspektren von Molekülen
 CO 1 Rotationsspektren von Molekülen Bisher haben wir uns ein punkt- oder kugelförmiges Teilchen angeschaut, Moleküle können aber vielfältige Formen (Symmetrien) haben Um die Eigenschaften eines Moleküls
CO 1 Rotationsspektren von Molekülen Bisher haben wir uns ein punkt- oder kugelförmiges Teilchen angeschaut, Moleküle können aber vielfältige Formen (Symmetrien) haben Um die Eigenschaften eines Moleküls
Vorlesung 20: Roter Faden: Auswahlregeln. Folien auf dem Web:
 Vorlesung 20: Roter Faden: Auswahlregeln Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: http://www.uni-stuttgart.de/ipf/lehre/online-skript/ Wim de Boer, Karlsruhe Atome
Vorlesung 20: Roter Faden: Auswahlregeln Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: http://www.uni-stuttgart.de/ipf/lehre/online-skript/ Wim de Boer, Karlsruhe Atome
Schwingungsspektren organischer Moleküle
 1. Theorie Schwingungsspektren organischer Moleküle Die Grundlagen der Rotationsschwingungsspektroskopie werden im Versuch Molekülspektroskopie besprochen, so dass hier lediglich auf die Schwingungsspektroskopie
1. Theorie Schwingungsspektren organischer Moleküle Die Grundlagen der Rotationsschwingungsspektroskopie werden im Versuch Molekülspektroskopie besprochen, so dass hier lediglich auf die Schwingungsspektroskopie
Z 12 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN
 ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
Strukturbestimmung einer unbekannten Verbindung. Daten sammeln über Herstellung und Herkunft der Verbindung.
 Strukturbestimmung einer unbekannten Verbindung Daten sammeln über Herstellung und Herkunft der Verbindung. Sicherstellung hoher Reinheit 1 Zu bestimmende Struktur Elementaranalyse MS UV/VIS Chemische
Strukturbestimmung einer unbekannten Verbindung Daten sammeln über Herstellung und Herkunft der Verbindung. Sicherstellung hoher Reinheit 1 Zu bestimmende Struktur Elementaranalyse MS UV/VIS Chemische
Intensitätsverteilung der Beugung am Spalt ******
 5.10.801 ****** 1 Motivation Beugung am Spalt: Wellen breiten sich nach dem Huygensschen Prinzip aus; ihre Amplituden werden superponiert (überlagert). 2 Experiment Abbildung 1: Experimenteller Aufbau
5.10.801 ****** 1 Motivation Beugung am Spalt: Wellen breiten sich nach dem Huygensschen Prinzip aus; ihre Amplituden werden superponiert (überlagert). 2 Experiment Abbildung 1: Experimenteller Aufbau
Spektroskopie. im IR- und UV/VIS-Bereich. Raman-Spektroskopie. http://www.analytik.ethz.ch
 Spektroskopie im IR- und UV/VIS-Bereich Raman-Spektroskopie Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Raman-Spektroskopie Chandrasekhara Venkata Raman Entdeckung des
Spektroskopie im IR- und UV/VIS-Bereich Raman-Spektroskopie Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Raman-Spektroskopie Chandrasekhara Venkata Raman Entdeckung des
Physikalische Chemie für Fortgeschrittene. Protokoll
 Universität Leipzig Studiengang Chemie (Bachelor) Physikalische Chemie für Fortgeschrittene Sommersemester 014 Protokoll Versuch 3 Infrarotspektroskopie Rotationsschwingungsspektren Betreuer: M.Sc. Marcel
Universität Leipzig Studiengang Chemie (Bachelor) Physikalische Chemie für Fortgeschrittene Sommersemester 014 Protokoll Versuch 3 Infrarotspektroskopie Rotationsschwingungsspektren Betreuer: M.Sc. Marcel
Die Bewegungsgleichungen eines geladenen Teilchens im externen elektromagnetischen Feld sind bekannt d dt m v = e E + e [
 Vorlesung 4 Teilchen im externen Elektromagnetischen Feld Die Bewegungsgleichungen eines geladenen Teilchens im externen elektromagnetischen Feld sind bekannt d dt m v = e E + e v B c ]. 1) Das elektrische
Vorlesung 4 Teilchen im externen Elektromagnetischen Feld Die Bewegungsgleichungen eines geladenen Teilchens im externen elektromagnetischen Feld sind bekannt d dt m v = e E + e v B c ]. 1) Das elektrische
Wechselwirkung zwischen Licht und chemischen Verbindungen
 Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
mit n =1, 2, 3,... (27) Die gesuchten Wellenfunktionen sind Sinuswellen, deren Wellenlänge λ die Bedingung L = n λ 2
 3FREIETEICHEN TEICHEN IM KASTEN 17 Somit kann man z. B. a = 2/ setzen. (Man könnte auch a = e iϕ 2/ wählen, mit beliebigem ϕ.) Damit sind die Energie- Eigenzustände des Teilchens im Kasten gegeben durch
3FREIETEICHEN TEICHEN IM KASTEN 17 Somit kann man z. B. a = 2/ setzen. (Man könnte auch a = e iϕ 2/ wählen, mit beliebigem ϕ.) Damit sind die Energie- Eigenzustände des Teilchens im Kasten gegeben durch
