Alkane und Cycloalkane
|
|
|
- Hannah Heinrich
- vor 9 Jahren
- Abrufe
Transkript
1 Systematik und Nomenklatur Alkane und ycloalkane einfachstes Alkan: Methan 4 Summenformel Strukturformel schrittweise Verlängerung um eine Einheit homologe Reihe rganische hemie I 1
2 Alkane Gesättigte Kohlenwasserstoffe: allgemeine Zusammensetzung n 2n+2 Summenformel Name Strukturformel Vereinfachte Schreibweise 4 Methan 2 6 Ethan 3 8 Propan 4 10 Butan rganische hemie I 2
3 Alkane höhere omologe: griechisches Zahlwort + Silbe an Pentan exan eptan ctan Nonan Decan Undecan Dodecan rganische hemie I 3
4 Verzweigte Alkane -Konstitutionsisomere Butan 4 10 sind zwei Anordnungen möglich Butan 2-Methylpropan = Isobutan Isomere: Verbindungen gleicher Summenformel, aber unterschiedlicher Strukturformel Konstitutionsisomere Pentan 5 12 sind drei Anordnungen möglich Pentan 2-Methylbutan = Isobutan 2,2-Dimethylpropan = Neopentan rganische hemie I 4
5 Verzweigte Alkane -Konstitutionsisomere Isomere Isomere rganische hemie I 5
6 Konstitutionsisomere Konstitutionsisomerie nicht nur bei Alkanen Unterschiedliche funktionelle Gruppen Ethylalkohol Dimethylether 2 6 Unterschiedliche Position der funktionellen Gruppen N N2 3 7 N 2 Isopropylamin Propylamin 3 3 Propanon 2 Allylalkohol Prop-2-enol 3 2 Propanal 3 Methylvinylether 2 2 xetan 2 3 Methyloxiran rganische hemie I 3 6 6
7 Alkylgruppen Alkyl Gruppe: Entfernung eines -Atoms von einem Alkan Allgemeine Abkürzung R (für Radikal, eine unvollständige Verbindung oder der Rest eines Moleküles) Nomenklatur: Ersatz der -an Endung des Alkane durch -yl Endung Methan Ethan Propan Methyl Ethyl Propyl 7 3 Me Et Pr Butan 4 10 Butyl 9 4 n-bu rganische hemie I 7
8 Trivialnamen für verzweigte Alkane Isobutan Isopentan Isohexan verzweigte Alkylgruppen: Neopentan 3 Isopropyl i-pr Isobutyl 3 tert-butyl 3 i-bu 3 t-bu sec-butyl 3 2 Neopentyl s-bu 3 rganische hemie I 8
9 Alkylgruppen primäre, sekundäre und tertiäre Kohlenstoff- und Wasserstoffatome primär 3 quartär tertiär sekundär rganische hemie I 9
10 Nomenklatur für verzweigte Alkane Propyl Butyl Suchen/Benennung der längsten Kette (auptkette) Bestimmung der Namen der gebundenen Alkylgruppen (Substituenten) Nummerierung der auptkette vom Ende des nächsten gebundenen Substituenten exadecan Propyl, Butyl 6, 10 Benennung der Verbindung gemäß alphabetischer Reihenfolge der Substituenten 10-Butyl Butyl-6-propylhexadecan rganische hemie I 10
11 Nomenklatur für verzweigte Alkane Methyl Propyl Suchen/Benennung der längsten Kette (auptkette) Bestimmung der Namen der gebundenen Alkylgruppen (Substituenten) Nummerierung der auptkette vom Ende des nächsten gebundenen Substituenten Decan Propyl, Methyl, Methyl 2, 2, 7 Benennung der Verbindung gemäß alphabetischer Reihenfolge der Substituenten 2,2-Dimethyl Dimethyl-7-propyldecan rganische hemie I 11
12 Übung: Nomenklatur für verzweigte Alkane Übung 5 12 : 3 Konstitutionsisomere Pentan Butane alles Pentan! Propane 2-Methylbutan 2-Methylbutan 2-Methylbutan Isopentan 2,2-Dimethylpropan Neopentan rganische hemie I 12
13 Übung: Nomenklatur für verzweigte Alkane Übung 6 14 : 5 Konstitutionsisomere exan Pentane beides exan! Butane 2-Methylpentan 3-Methylhexan 3-Methylpentan 3-Methylpentan 2,2-Dimethylbutan 2,3-Trimethylbutan rganische hemie I 13
14 Übung: Nomenklatur für verzweigte Alkane Übung 7 16 : 9 Konstitutionsisomere eptan exane beides eptan! 2-Methylhexan 3-Methylhexan 3-Methylhexan 3-Methylhexan rganische hemie I 14
15 Übung: Nomenklatur für verzweigte Alkane Übung Pentane 2,2-Dimethylpentan 2,3-Dimethylpentan 2,4-Dimethylpentan 3,3-Dimethylpentan 3-Ethylpentan 2,3-Dimethylpentan 2,3-Dimethylpentan Butane 2,2,3-Trimethylbutan 2,2,3-Trimethylbutan rganische hemie I 15
16 ycloalkane homologe Reihe: yclopropan, -butan, -pentan, -hexan, -heptan, etc yclopropan allgemeine Summenformel yclobutan n 2n yclopentan yclohexan 2 2 yclopropylgruppe rganische hemie I 16
17 ycloalkane Bicyclische, tricyclische und polycyclische Alkane Bicyclo[2.2.2]octan [1.1.1]Propellan Tricyclo[ ]pentan Nomenklatur: gezählt wird beginnend an einem Brückenkopfatom, über die längste Brücke, dann über die zweitlängste, bis zur kürzesten Brücke. Die Länge der Brücken wird als Klammerausdruck angegeben. Gonan Grundgerüst der Steroide rganische hemie I 17
18 Physikalische Eigenschaften homologer n-alkane Formel Name Schmp./ Sdp./ d 20 4 Methan - 183, Ethan - 183, Propan , ( 2 ) 2-3 Butan ,5 0, ( 2 ) 3-3 Pentan , ( 2 ) 4-3 exan , ( 2 ) 5-3 eptan , ( 2 ) 6-3 ctan , ( 2 ) 7-3 Nonan , ( 2 ) 8-3 Decan , ( 2 ) 9-3 Undecan , ( 2 ) 10-3 Dodecan , ( 2 ) 11-3 Tridecan , ( 2 ) 12-3 Tetradecan , ( 2 ) 13-3 Pentadecan , ( 2 ) 18-3 Eicosan , ( 2 ) 28-3 Triacontan , ( 2 ) n - 3 Polyethylen ,965 rganische hemie I 18
19 Physikalische Eigenschaften homologer n-alkane Siedepunkte, Dichte und Schmelzpunkte von n-alkanen in Abhängigkeit von der Kettenlänge (Anzahl der -Atome) Siedepunkt d Dichte 0.65 Schmelzpunkt rganische hemie I 19
20 Physikalische Eigenschaften Isomerer Pentane Neopentan nahezu kugelförmig Sdp.: 10 Schmp.: -17 Lineare n-pentan hat größere berfläche Sdp.: 36 Schmp.: -130 geringe Wechselwirkung bei zwei kugelförmigen Gestalt bessere Wechselwirkung bei zwei gestreckten Konstitutionsisomeren Zwischenmolekulare Wechselwirkung = van der Waals Kräfte rganische hemie I 20
21 Graham Solomans, rganic hemistry, Seventh Edition Animation rganische hemie I 21
22 Physikalische Eigenschaften Isomerer exane Isomere exane 6 14 n-exan Sdp. Schmp. Dichte Methylpentan Methylpentan ,3-Dimethylbutan ,2-Dimethylbutan rganische hemie I 22
23 rganische Verbindungen Funktionelle Gruppen Einteilung in Stoffklassen I) Bei Kohlenwasserstoffen: Gruppierungen mit doppelt und dreifach gebundenen -Atomen a) Alkene b) Alkine c) Aromatische Verbindungen II) rganische Verbindungen, die eteroelemente wie, N, al, S, P enthalten. Substitution eines oder mehrerer -Atome eines Alkans gegen eteroatome oder eteroatomgruppen rganische hemie I 23
24 rganische Verbindungen Funktionelle Gruppen Substanzklasse allgemeine Struktur funktionelle Gruppe Beispiel Alkane R Alkene R 1 R 3 R 2 R 4 Ethen (Ethylen) Alkine R 1 R 2 Ethin (Acetylen) Aromaten Benzen (Benzol) rganische hemie I 24
25 rganische Verbindungen Funktionelle Gruppen Substanzklasse allgemeine Struktur funktionelle Gruppe Beispiel Alkylhalogenide R X -X (X = F, l, Br, I) alogen 3 Iodmethan, Methyliodid I Alkohole R ydroxygruppe 2 5 Ethanol Ether R 1 R 2 (-R, Alkoxygruppe) Diethylether Epoxide R 1 R 2 R 3 R 4 (3-gliedriger Ether) xiran (Ethylenoxide) Thiole, Thioalkohole, R S S Mercaptogruppe 2 5 S Ethanthiol Sulfide, Thioether R 1 S R 2 S 2 5 S 2 5 Diethylsulfide, Diethylthioether rganische hemie I 25
26 rganische Verbindungen Funktionelle Gruppen Substanzklasse allgemeine Struktur funktionelle Gruppe Beispiel R N 2 Amine, primär -N 2 Aminogruppe 3 N 2 Methylamin Amine, sekundär R 1 N R 2 3 N 3 Dimethylamin Amine, tertiär R 1 N R 2 3 N 3 Dimethylamin Nitrile R N N Nitrilgruppe 3 N Ethannitril, Acetonitril Nitro-Verbindungen R N 2 N 2 Nitrogruppe 3 N 2 Nitromethan rganische hemie I 26
27 rganische Verbindungen Funktionelle Gruppen Substanzklasse allgemeine Struktur funktionelle Gruppe Beispiel Aldehyde R Formylgruppe 3 Ethanal (Acetaldehyd) Ketone R 1 R xogruppe 2-Propanon (Aceton) arbonsäuren R 3 arboxygruppe Ethansäure (Essigsäure) rganische hemie I 27
28 rganische Verbindungen Funktionelle Gruppen Substanzklasse allgemeine Struktur funktionelle Gruppe Beispiel arbonsäuren R 3 arboxygruppe Ethansäure (Essigsäure) Ester R R R 3 3 Estergruppe (Essigsäuremethylester) (Methylethanoat, Methylacetat) arbonsäurehalogenid R l l 3 l arboxygruppe Ethansäurechlorid (Essigsäurechlorid) rganische hemie I 28
29 rganische Verbindungen Funktionelle Gruppen Substanzklasse allgemeine Struktur funktionelle Gruppe Beispiel arbonsäuren R 3 arboxygruppe Ethansäure (Essigsäure) Anhydride R R 3 3 Anhydridgruppe (Essigsäureanhydrid) (Ethanoic anhydrid) Amide R N 2 N 2 3 N 2 Säureamidgruppe Ethanamid (Acetamid) rganische hemie I 29
30 Nomenklatur für substituierte Systeme harakteristische Gruppen, die nur als Präfixe auftreten -X (X = F, l, Br, I) alogen 3 I Fluor-, hlor- Brom-, Iod- Iodmethan, Methyliodid -N 2 3 N 2 Nitromethan R 1 3 (Methyloxy-) rganische hemie I 30
31 Nomenklatur für substituierte Systeme Rangfolge der wichtigsten Verbindungsklassen arbonsäuren arbonsäurederivate Nitrile Aldehyde Ketone Alkohole ydroperoxide Amine Ether Peroxide rganische hemie I 31
32 Valenzungesättigte Kohlenwasserstoffe a) Kationen: + c) arbanionen: - z.b. Methylkation - dreibindig Elektronensextett z.b. Methylanion - dreibindig - Elektronenoktett z. B. b) Radikale: d) arbene. z.b. Methylradikal - 1 ungepaartes Elektron - dreibindig z.b. Methylen - zweibindig - Elektronensextett Im allgemeinen instabile Teilchen reaktive Zwischenstufen rganische hemie I 32
33 Valenzungesättigte Kohlenwasserstoffe Bindungsverhältnisse in valenzungesättigten Teilchen E -Atom im Grundzustand a) Kationen: Bsp. Methylkation 3 + Modell: p 2s E -Atom im angeregten Zustand (Energiezufuhr) E sp 2 ybridisierung 2p mischen 2p sp 2 2s 2s rganische hemie I 33
34 Valenzungesättigte Kohlenwasserstoffe Bindungsverhältnisse in valenzungesättigten Teilchen E 2p sp 2 2s sp 2 ybridisierung a) Kationen: Methylkation 3 + Modell: Form wie sp Anordnung im Raum: VSEPR für AX 3 trigonal planar < vakantes p-rbital 120 eben - vakantes p-rbital rganische hemie I 34
35 Valenzungesättigte Kohlenwasserstoffe Bindungsverhältnisse in valenzungesättigten Teilchen E 2p sp 2 2s sp 2 ybridisierung b) Radikal: Methylradikal 3. sp 2 -ybridisierung analog 3 + p-rbital einfach besetzt rganische hemie I 35
36 Valenzungesättigte Kohlenwasserstoffe Bindungsverhältnisse in valenzungesättigten Teilchen E 2p sp 2 2s sp 2 ybridisierung c) Methylanion: 3 - sp 2 -ybridisierung analog 3 + p-rbital doppelt besetzt isoelektronisch zu N 3 sp 3 -ybridisierung, freies Elektronenpaar beansprucht mehr Raum rganische hemie I 36
Organik KOMPAKT Organik Blatt 1/5
 rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
Kohlenwasserstoffe. Benzol Naphthalin usw. Alkane Alkene Alkine Cycloaliphaten. Ethen (Ethylen) Propen u.s.w. Ethin (Acetylen) Propin u.s.w.
 OI_folie47 Kohlenwasserstoffe Aliphaten Aromaten Benzol Naphthalin usw. Alkane Alkene Alkine ycloaliphaten Methan Ethan u.s.w Ethen (Ethylen) Propen u.s.w. Ethin (Acetylen) Propin u.s.w. ycloalkane ycloalkene
OI_folie47 Kohlenwasserstoffe Aliphaten Aromaten Benzol Naphthalin usw. Alkane Alkene Alkine ycloaliphaten Methan Ethan u.s.w Ethen (Ethylen) Propen u.s.w. Ethin (Acetylen) Propin u.s.w. ycloalkane ycloalkene
Skript zur Vorlesung Organische Chemie (Prof. M. Albrecht) an der RWTH Aachen
 Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: [email protected] Nomenklatur und Isomerie organischer
Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: [email protected] Nomenklatur und Isomerie organischer
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
IUPAC-Nomenklaturregeln als Grundlage für Q11 Chemie
 Nomenklatur 1 IUPA-Nomenklaturregeln als Grundlage für Q11 hemie 1 Kohlenwasserstoffe und Derivate 1.1 Regeln zur Benennung von unverzweigten Alkanen (n-alkane) Der Name der n-alkane enthält die folgenden
Nomenklatur 1 IUPA-Nomenklaturregeln als Grundlage für Q11 hemie 1 Kohlenwasserstoffe und Derivate 1.1 Regeln zur Benennung von unverzweigten Alkanen (n-alkane) Der Name der n-alkane enthält die folgenden
Einführung in die Nomenklatur der organischen Chemie. Einteilung der Kohlenwasserstoffe
 organischen hemie Klasse 8 Einteilung der Kohlenwasserstoffe Alkane Alkene Alkine Kettenverbindungen Organische hemie socyclen ycloalkane ycloalkene ycloalkine Aromate Ringverbindungen eterocyclen Fünfringe
organischen hemie Klasse 8 Einteilung der Kohlenwasserstoffe Alkane Alkene Alkine Kettenverbindungen Organische hemie socyclen ycloalkane ycloalkene ycloalkine Aromate Ringverbindungen eterocyclen Fünfringe
Homologe Reihe der Alkane. Benennung der Alkane. Konstitutionsisomerie. Isomerie. Was versteht man unter der Homologen Reihe der Alkane?
 Grundwissen hemie: NTG 10 1/24 omologe eihe der Alkane Was versteht man unter der omologen eihe der Alkane? Grundwissen hemie: NTG 10 2/24 Benennung der Alkane Benenne die ersten zwölf Vertreter aus der
Grundwissen hemie: NTG 10 1/24 omologe eihe der Alkane Was versteht man unter der omologen eihe der Alkane? Grundwissen hemie: NTG 10 2/24 Benennung der Alkane Benenne die ersten zwölf Vertreter aus der
I. Alkane Homologe Reihe, Nomenklatur
 Organische Chemie Grundkurs (11. Klasse) Theorie und Übungen I. Alkane omologe Reihe, Nomenklatur omologe Reihe der Alkane Aufgabe: Setzen Sie die Tabelle fort Name Summenformel Struktur Rest Methan C
Organische Chemie Grundkurs (11. Klasse) Theorie und Übungen I. Alkane omologe Reihe, Nomenklatur omologe Reihe der Alkane Aufgabe: Setzen Sie die Tabelle fort Name Summenformel Struktur Rest Methan C
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul Rademacher Institut für Organische hemie der Universität Duisburg-Essen (Teil 7: 24.11.2004) MILESS: hemie für Biologen 126 Was
hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul Rademacher Institut für Organische hemie der Universität Duisburg-Essen (Teil 7: 24.11.2004) MILESS: hemie für Biologen 126 Was
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
CHE 172.1: Organische Chemie für die Life Sciences
 1 E 172.1: rganische hemie für die Life Sciences Prof Dr. J. A. Robinson 2. rganische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 2.1 Funktionelle
1 E 172.1: rganische hemie für die Life Sciences Prof Dr. J. A. Robinson 2. rganische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 2.1 Funktionelle
EINFÜHRUNG IN DIE ORGANISCHE CHEMIE
 rganische Chemie Lehrgang CEMIE FÜR BILGIELERKRÄFTE EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs
rganische Chemie Lehrgang CEMIE FÜR BILGIELERKRÄFTE EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs
2. AUFBAU ORGANISCHER VERBINDUNGEN - ISOMERIEN
 2. AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybridisierungskonzepts verstehen und anschaulich darstellen (siehe
2. AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybridisierungskonzepts verstehen und anschaulich darstellen (siehe
Summenformel. Strukturformel. Halbstrukturformel. Fossile Energieträger. ( 10. Klasse NTG 1 / 47 ) ( 10. Klasse NTG 2 / 47 ) ( 10. Klasse NTG 3 / 47 )
 Summenformel ( 10. Klasse NTG 1 / 47 ) Angabe der Atomsorten und deren Anzahl innerhalb eines Moleküls z.b. Ethanol C 2 6 O Strukturformel ( 10. Klasse NTG 2 / 47 ) Darstellung der bindenden und freien
Summenformel ( 10. Klasse NTG 1 / 47 ) Angabe der Atomsorten und deren Anzahl innerhalb eines Moleküls z.b. Ethanol C 2 6 O Strukturformel ( 10. Klasse NTG 2 / 47 ) Darstellung der bindenden und freien
Z 8 EINFÜHRUNG IN DIE ORGANISCHE CHEMIE 1) DEFINITIONEN 2) ELEMENTE UND BINDUNGEN. Organische Chemie. Kunstoffe. Farbstoffe
 EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
Chemie der Kohlenwasserstoffe
 hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
Organische Chemie. Kohlenstoff. Kohlenstoffkreislauf. Erdölverarbeitung. Kohlenwasserstoffe
 rganische hemie Teilgebiet der hemie, welches sich mit Aufbau, erstellung und Eigenschaften der Verbindungen des Kohlenstoffs beschäftigt. NTG 10.1 Kohlenstoff - 4. auptgruppe 4 Valenzelektronen 4 Bindungen
rganische hemie Teilgebiet der hemie, welches sich mit Aufbau, erstellung und Eigenschaften der Verbindungen des Kohlenstoffs beschäftigt. NTG 10.1 Kohlenstoff - 4. auptgruppe 4 Valenzelektronen 4 Bindungen
2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen
 2. rganische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 11 2.1 Funktionellen Gruppen Es gibt heute ungefähr neun Millionen bekannter organischer Substanzen.
2. rganische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 11 2.1 Funktionellen Gruppen Es gibt heute ungefähr neun Millionen bekannter organischer Substanzen.
Alkane. Name: Summenformel: vereinfachte Formel: Zustand: Methan CH 4 CH 4 g (gaseous) Ethan C 2 H 6 CH 3 CH 3 g. Propan C 3 H 8 CH 3 CH 2 CH 3 g
 Alkane Name: Summenformel: vereinfachte Formel: Zustand: Methan C 4 C 4 g (gaseous) Ethan C 2 6 C 3 C 3 g Propan C 3 8 C 3 C 2 C 3 g Butan C 4 10 C 3 C 2 C 2 C 3 g Pentan C 5 12 C 3 C 2 C 2 C 2 C 3 l (liquid)
Alkane Name: Summenformel: vereinfachte Formel: Zustand: Methan C 4 C 4 g (gaseous) Ethan C 2 6 C 3 C 3 g Propan C 3 8 C 3 C 2 C 3 g Butan C 4 10 C 3 C 2 C 2 C 3 g Pentan C 5 12 C 3 C 2 C 2 C 2 C 3 l (liquid)
Organische Chemie. 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8. Lehrstuhl für Organische Chemie
 Organische Chemie 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8 Lehrstuhl für Organische Chemie ([email protected]) Prof. Dr. Ivo C. Ivanov 1 1. Gegenstand der Organischen Chemie,
Organische Chemie 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8 Lehrstuhl für Organische Chemie ([email protected]) Prof. Dr. Ivo C. Ivanov 1 1. Gegenstand der Organischen Chemie,
Homologe Reihe der unverzweigten Alkane C n H (2n+2)
 Organische hemie I 3.01 Homologe Reihe der unverzweigten Alkane n H (2n+2) (Paraffine) (veraltet: normale Alkane = n-alkane) Name Konstitution Siedepunkt ausführliche Schreibweise Stenographie [ ] Methan
Organische hemie I 3.01 Homologe Reihe der unverzweigten Alkane n H (2n+2) (Paraffine) (veraltet: normale Alkane = n-alkane) Name Konstitution Siedepunkt ausführliche Schreibweise Stenographie [ ] Methan
Einführung in die Organische Chemie. Benjamin Grimm
 Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
IUPAC muss das denn sein?
 IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
Chemie Alkohole, Aldehyde & Ketone, Carbonsäuren
 Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Grundwissen 10. Klasse NTG 1
 Grundwissen 10. Klasse NTG 1 1. rganische hemie = Kohlenstoffchemie rganische Verbindungen sind Kohlenstoffverbindungen. Ausnahmen:, 2, Kohlensäure, arbonate; 2. Eigenschaften organischer Verbindungen
Grundwissen 10. Klasse NTG 1 1. rganische hemie = Kohlenstoffchemie rganische Verbindungen sind Kohlenstoffverbindungen. Ausnahmen:, 2, Kohlensäure, arbonate; 2. Eigenschaften organischer Verbindungen
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 E 102.1: Grundlagen der hemie - Organische hemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane: Moleküle ohne funktionelle Gruppen
E 102.1: Grundlagen der hemie - Organische hemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane: Moleküle ohne funktionelle Gruppen
Zur Benennung organischer Moleküle
 Zur Benennung organischer Moleküle Beispiele und Übungen Funktionelle Gruppen Es sind Atomgruppen in organischen Verbindungen. Sie verändern die Stoffeigenschaften und das Reaktionsverhalten des Ausgangskohlenwasserstoffs.
Zur Benennung organischer Moleküle Beispiele und Übungen Funktionelle Gruppen Es sind Atomgruppen in organischen Verbindungen. Sie verändern die Stoffeigenschaften und das Reaktionsverhalten des Ausgangskohlenwasserstoffs.
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1. Grundwissen 10.Klasse NTG 2 Grundwissen 10.Klasse NTG 2
 Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
1 Stoffklasse Alkane : C n H 2n+2 Namensendung an
 rganische hemie LÖSUNGEN Seite 1 von 11 1 Stoffklasse Alkane : n 2n+2 Namensendung an Zahl der -Atome Name Molekülformel Lewisformel Keilstrichformel Skelettformel 1 Methan 4 Sinnlos 2 Ethan 2 6 3 Propan
rganische hemie LÖSUNGEN Seite 1 von 11 1 Stoffklasse Alkane : n 2n+2 Namensendung an Zahl der -Atome Name Molekülformel Lewisformel Keilstrichformel Skelettformel 1 Methan 4 Sinnlos 2 Ethan 2 6 3 Propan
Alkane = aliphatische Kohlenwasserstoffe, Paraffine Organische Verbindungen ohne funktionelle Gruppen
 2. Alkane Alkane = aliphatische Kohlenwasserstoffe, Paraffine Organische Verbindungen ohne funktionelle Gruppen 2.1 unverzweigte Alkane Formel: C n 2n+2 = -(C 2 ) n - homologe Reihe n Name Formel Schmp.
2. Alkane Alkane = aliphatische Kohlenwasserstoffe, Paraffine Organische Verbindungen ohne funktionelle Gruppen 2.1 unverzweigte Alkane Formel: C n 2n+2 = -(C 2 ) n - homologe Reihe n Name Formel Schmp.
Butanol Butanal Butansäure
 Wiederholungsthema: Gesättigte Kohlenwasserstoffe (Alkane) Zusammenfassung: Gesättigte Kohlenwasserstoffe bestehen aus Ketten aus mit einander vernüpften Kohlenstoff-Atomen, an die die maximal mögliche
Wiederholungsthema: Gesättigte Kohlenwasserstoffe (Alkane) Zusammenfassung: Gesättigte Kohlenwasserstoffe bestehen aus Ketten aus mit einander vernüpften Kohlenstoff-Atomen, an die die maximal mögliche
Übung 9: Aufbau und Struktur organischer Verbindungen Übung für Medizinische Biologen - Jun.-Prof. Dr. Michael Giese.
 Zusammenfassung Aufbau und Struktur organischer Verbindungen Kohlenstoff besitzt eine Sonderstellung unter den Elementen ybridisierungsmodell beschreibt die Bindungsverhältnisse in Kohlenstoffverbindungen
Zusammenfassung Aufbau und Struktur organischer Verbindungen Kohlenstoff besitzt eine Sonderstellung unter den Elementen ybridisierungsmodell beschreibt die Bindungsverhältnisse in Kohlenstoffverbindungen
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Prof. Dr. Urs Séquin: Organische Chemie für Studierende der Medizin 1
 rof. Dr. Urs équin: rganische hemie für tudierende der Medizin 1 Übersicht über die wichtigsten Verbindungsklassen und ihre funktionellen Gruppen Verbindungsklasse allgemeine Form; Beispiel ame ( = Kohlenstoffrest,
rof. Dr. Urs équin: rganische hemie für tudierende der Medizin 1 Übersicht über die wichtigsten Verbindungsklassen und ihre funktionellen Gruppen Verbindungsklasse allgemeine Form; Beispiel ame ( = Kohlenstoffrest,
IUPAC muss das denn sein?
 IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
Vorlesung 5. Alkane. Experimentalchemie, Prof. H. Mayr 20 Achtung Lückentext. Nur als Begleittext zur Vorlesung geeignet. Anzahl C-Atome im n-alkan
 Vorlesung 5. Alkane Verbindungen aus Kohlenstoff und Wasserstoff, die nur Einfachbindungen enthalten, nennt man gesättigte Kohlenwasserstoffe. Sie sind ein auptbestandteil von Erdgas und Erdöl. Liegen
Vorlesung 5. Alkane Verbindungen aus Kohlenstoff und Wasserstoff, die nur Einfachbindungen enthalten, nennt man gesättigte Kohlenwasserstoffe. Sie sind ein auptbestandteil von Erdgas und Erdöl. Liegen
Kohlenstoffverbindungen
 Kohlenstoffverbindungen Zusammenfassung Im 19. Jahrhundert begann man die Zusammensetzung von Naturstoffen zu untersuchen. Dieser Zweig der hemie wird Organische hemie genannt. Ursprünglich glaubte man,
Kohlenstoffverbindungen Zusammenfassung Im 19. Jahrhundert begann man die Zusammensetzung von Naturstoffen zu untersuchen. Dieser Zweig der hemie wird Organische hemie genannt. Ursprünglich glaubte man,
Systematische Nomenklatur
 Systematische Nomenklatur Je größer eine chemische Verbindung wird, desto komplizierter wird in der Regel deren Struktur, und desto schwieriger wird es, diese Verbindung eindeutig zu benennen. Dieses Problem
Systematische Nomenklatur Je größer eine chemische Verbindung wird, desto komplizierter wird in der Regel deren Struktur, und desto schwieriger wird es, diese Verbindung eindeutig zu benennen. Dieses Problem
1. Nomenklatur (Fettgedruckt...IUPAC Namen) 1.1. Alkane
 rganisch-chemisches Proseminar für Molekulargenetiker und Mikrobiologen AAG. omenklatur (Fettgedruckt...IUPA amen).. Alkane Die längste Kohlenstoffkette wird bestimmt und daraus ergibt sich der ame Alkan:
rganisch-chemisches Proseminar für Molekulargenetiker und Mikrobiologen AAG. omenklatur (Fettgedruckt...IUPA amen).. Alkane Die längste Kohlenstoffkette wird bestimmt und daraus ergibt sich der ame Alkan:
Organische Chemie. Einstieg. Chemie-Formeldarstellungen. Formeldarstellungen der Chemie: Bei Ionenverbindungen: Verhältnisformeln. , AlF 3. etc.
 Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
Grundwissen Chemie Mittelstufe (10 MNG)
 Grundwissen hemie Mittelstufe (10 MNG) Marie-Therese-Gymnasium Erlangen Einzeldateien: GW8 Grundwissen für die 8. Jahrgangsstufe GW9 Grundwissen für die 9. Jahrgangsstufe (MNG) GW9a Grundwissen für die
Grundwissen hemie Mittelstufe (10 MNG) Marie-Therese-Gymnasium Erlangen Einzeldateien: GW8 Grundwissen für die 8. Jahrgangsstufe GW9 Grundwissen für die 9. Jahrgangsstufe (MNG) GW9a Grundwissen für die
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
GRUNDWISSEN CHEMIE 10. KLASSE
 Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
ORGANISCHE CHEMIE. Struktur organischer Verbindungen: Formeln, Nomenklatur und Reaktionsmechanismen
 ORGANISE EMIE Struktur organischer Verbindungen: Formeln, Nomenklatur und Reaktionsmechanismen hemische Formeln Summenformeln Strukturformeln (Konstitutionsformeln) Ausführliche Strukturformeln Vereinfachte
ORGANISE EMIE Struktur organischer Verbindungen: Formeln, Nomenklatur und Reaktionsmechanismen hemische Formeln Summenformeln Strukturformeln (Konstitutionsformeln) Ausführliche Strukturformeln Vereinfachte
Chemie. für die Berufsmaturität. Günter Baars. Chemie. Baars. Unter Mitarbeit von Franz Heini, Markus Isenschmid und Doris Kohler
 www.hep-verlag.ch/chemie-bm-ergaenzungen Franz eini Studium der Biologie mit ebenfach Biochemie. öheres Lehramt für das Fach Biologie. Unterrichtstätigkeit an der KDMS und an Gymnasien in Fribourg. Lehrer
www.hep-verlag.ch/chemie-bm-ergaenzungen Franz eini Studium der Biologie mit ebenfach Biochemie. öheres Lehramt für das Fach Biologie. Unterrichtstätigkeit an der KDMS und an Gymnasien in Fribourg. Lehrer
Übungen zur Nomenklatur: Zeichne die Formeln auf ein leeres kariertes Blatt und benenne die einzelnen Formeln.
 Übungen zur Nomenklatur: Zeichne die Formeln auf ein leeres kariertes Blatt und benenne die einzelnen Formeln. Einfache Formeln, Verzweigungen, längste Kette, Nummerierung Nr Formel Name A1 Propan 3 2
Übungen zur Nomenklatur: Zeichne die Formeln auf ein leeres kariertes Blatt und benenne die einzelnen Formeln. Einfache Formeln, Verzweigungen, längste Kette, Nummerierung Nr Formel Name A1 Propan 3 2
OSZ Körperpflege Chemie Fachhochschulreife FOS 2009/10
 Name: Klasse: GASCHROMATOGRAFIE Experiment 08 1. Aufgabe: a) Nehmen Sie ein Gaschromatogramm ihres Feuerzeuggases auf. (Füllen Sie dazu 2 ml des Feuerzeuggases in die Spritze!) Siehe Anlage Durchführung!!!
Name: Klasse: GASCHROMATOGRAFIE Experiment 08 1. Aufgabe: a) Nehmen Sie ein Gaschromatogramm ihres Feuerzeuggases auf. (Füllen Sie dazu 2 ml des Feuerzeuggases in die Spritze!) Siehe Anlage Durchführung!!!
Beispielklausur Allgemeine Chemie II (Organische Chemie)
 Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und Herstellung
 6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und erstellung Moleküle, die nur Kohlenstoff und Wasserstoff enthalten, werden Kohlenwasserstoffe genannt Prof. Dr. Ivo C. Ivanov
6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und erstellung Moleküle, die nur Kohlenstoff und Wasserstoff enthalten, werden Kohlenwasserstoffe genannt Prof. Dr. Ivo C. Ivanov
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
Clara Schumann -Gymnasium Grundlagen der organischen Chemie
 1 lara Schumann -Gymnasium Grundlagen der organischen hemie Ein Leitprogramm für den Grundlagen-hemieunterricht der Sekundarstufe II Dr. Daniel Bürgisser Neue Kantonsschule Aarau Revision 2003 Modifiziert:
1 lara Schumann -Gymnasium Grundlagen der organischen hemie Ein Leitprogramm für den Grundlagen-hemieunterricht der Sekundarstufe II Dr. Daniel Bürgisser Neue Kantonsschule Aarau Revision 2003 Modifiziert:
Kohlenwasserstoffe. Alkane Alkene Alkine Cycloaliphaten. Ethin (Acetylen) Propin u.s.w. Cycloalkane Cycloalkene Cycloalkine
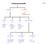 Kohlenwasserstoffe Folie184 Aliphaten Aromaten Benzol Naphthalin usw. Alkane Alkene Alkine ycloaliphaten Methan Ethan u.s.w Ethen (Ethylen) Propen u.s.w. Ethin (Acetylen) Propin u.s.w. ycloalkane ycloalkene
Kohlenwasserstoffe Folie184 Aliphaten Aromaten Benzol Naphthalin usw. Alkane Alkene Alkine ycloaliphaten Methan Ethan u.s.w Ethen (Ethylen) Propen u.s.w. Ethin (Acetylen) Propin u.s.w. ycloalkane ycloalkene
Grundwissen Chemie 10. Klasse NTG
 Grundwissen Chemie 10. Klasse NTG Homologe Reihe der Alkane Methan, Ethan, Propan, Butan, Pentan, Hexan, Heptan, Octan, Nonan, Decan 10.1 C NTG Allg. Summenformel Alkane C n H 2n+2 (gesättigte Kohlenwasserstoffe,
Grundwissen Chemie 10. Klasse NTG Homologe Reihe der Alkane Methan, Ethan, Propan, Butan, Pentan, Hexan, Heptan, Octan, Nonan, Decan 10.1 C NTG Allg. Summenformel Alkane C n H 2n+2 (gesättigte Kohlenwasserstoffe,
Benennung (Nomenklatur) von Alkanen. zusammengestellt von W. Habelitz-Tkotz in Anlehnung an Galvani 3, Oldenbourg-Verlag, S.
 Benennung (Nomenklatur) von Alkanen zusammengestellt von W. abelitz-tkotz in Anlehnung an Galvani 3, Oldenbourg-Verlag, S. 34 + 35 istorische Entwicklung ursprünglich: Trivialnamen für viele Stoffe, z.
Benennung (Nomenklatur) von Alkanen zusammengestellt von W. abelitz-tkotz in Anlehnung an Galvani 3, Oldenbourg-Verlag, S. 34 + 35 istorische Entwicklung ursprünglich: Trivialnamen für viele Stoffe, z.
Chemie. Elektrochemie, Alkane und Alkene
 Zinkhalbzelle Mehr Zusammenfassungen von Malte Jakob findest du hier: hemie Elektrochemie, Alkane und Alkene Elektrochemie Galvanische Zelle: Anode Oxidation - e - e- e U - e - + Kathode Reduktion Zinkelektrode
Zinkhalbzelle Mehr Zusammenfassungen von Malte Jakob findest du hier: hemie Elektrochemie, Alkane und Alkene Elektrochemie Galvanische Zelle: Anode Oxidation - e - e- e U - e - + Kathode Reduktion Zinkelektrode
Lösungen zum Übungsblatt zur Schulaufgabe. 0. Aufgaben aus dem Buch, S. 34
 Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Organische Stofflehre
 Organische hemie hemielaboranten 1-01 Organische Stofflehre 1 Kohlenwasserstoffe Die Kohlenwasserstoffe, abgekärzt KW, sind die einfachsten organischen Verbindungen. Sie bestehen nur aus den Elementen
Organische hemie hemielaboranten 1-01 Organische Stofflehre 1 Kohlenwasserstoffe Die Kohlenwasserstoffe, abgekärzt KW, sind die einfachsten organischen Verbindungen. Sie bestehen nur aus den Elementen
2. Alkane. Allgemeines. Nomenklatur + Konstitutionsisomerie. Konformationsisomerie. Industrielle Bedeutung. Synthetische Darstellung
 2. Alkane Allgemeines Nomenklatur + Konstitutionsisomerie Konformationsisomerie Industrielle Bedeutung Synthetische Darstellung Reaktionen der Alkane Organische Chemie I LA / J. C. Brendel 1 Allgemeines
2. Alkane Allgemeines Nomenklatur + Konstitutionsisomerie Konformationsisomerie Industrielle Bedeutung Synthetische Darstellung Reaktionen der Alkane Organische Chemie I LA / J. C. Brendel 1 Allgemeines
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
IUPAC muss das denn sein?
 IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
2. Alkane. Allgemeines Nomenklatur + Konstitutionsisomerie Konformationsisomerie Industrielle Bedeutung Synthetische Darstellung Reaktionen der Alkane
 2. Alkane Allgemeines Nomenklatur + Konstitutionsisomerie Konformationsisomerie Industrielle Bedeutung Synthetische Darstellung Reaktionen der Alkane OC I Lehramt F. H. Schacher 1 Allgemeines Kohlenwasserstoffe
2. Alkane Allgemeines Nomenklatur + Konstitutionsisomerie Konformationsisomerie Industrielle Bedeutung Synthetische Darstellung Reaktionen der Alkane OC I Lehramt F. H. Schacher 1 Allgemeines Kohlenwasserstoffe
2.1 Homologe Reihe, Nomenklatur, Konstitution, Konformation CH 2
 Prof. hristoffers, Vorlesung rganische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler. Alkane.1 omologe Reihe, Nomenklatur, Konstitution, Konformation.1.1 omologe Reihe
Prof. hristoffers, Vorlesung rganische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler. Alkane.1 omologe Reihe, Nomenklatur, Konstitution, Konformation.1.1 omologe Reihe
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Die Welt der Gifte. Bearbeitet von Karsten Strey
 Die Welt der Gifte Bearbeitet von Karsten Strey 2., erweiterte und überarbeitete Auflage 2015. Buch. 512 S. Softcover ISBN 978 3 86541 728 2 Format (B x L): 14,9 x 21,1 cm Gewicht: 954 g Weitere Fachgebiete
Die Welt der Gifte Bearbeitet von Karsten Strey 2., erweiterte und überarbeitete Auflage 2015. Buch. 512 S. Softcover ISBN 978 3 86541 728 2 Format (B x L): 14,9 x 21,1 cm Gewicht: 954 g Weitere Fachgebiete
Prof. Dr. Stephen Hashmi, Sommersemester Organische Chemie für Technische Biologen, Organische Chemie für Lehramtskandidaten, Teil 2.
 Prof. Dr. ashmi, Sommersemester 2005 13 IV. Alkane Methan -C 2 - Ethan -C 2 -C 2 - Propan -C 2 -C 2 -C 2 - Butan -C 2 -C 2 -C 2 -C 2 - Pentan -C 2 -C 2 -C 2 -C 2 -C 2 - exan -C 2 -C 2 -C 2 -C 2 -C 2 -C
Prof. Dr. ashmi, Sommersemester 2005 13 IV. Alkane Methan -C 2 - Ethan -C 2 -C 2 - Propan -C 2 -C 2 -C 2 - Butan -C 2 -C 2 -C 2 -C 2 - Pentan -C 2 -C 2 -C 2 -C 2 -C 2 - exan -C 2 -C 2 -C 2 -C 2 -C 2 -C
Kapitel 04: Kohlenstoff als Bindungspartner in Alkanen, Alkenen und Alkinen
 Kapitel 04: Kohlenstoff als Bindungspartner in Alkanen, Alkenen und Alkinen Organische hemie - 04 - Kohlenstoff als Bindungspartner in Alkanen, Alkenen und Alkinen 2 nhalt Kapitel 04: Kohlenstoff als Bindungspartner
Kapitel 04: Kohlenstoff als Bindungspartner in Alkanen, Alkenen und Alkinen Organische hemie - 04 - Kohlenstoff als Bindungspartner in Alkanen, Alkenen und Alkinen 2 nhalt Kapitel 04: Kohlenstoff als Bindungspartner
Grundwissen Chemie Jahrgangsstufe 10 (NTG)
 Grundwissen Chemie Jahrgangsstufe 10 (NTG) Die organische Chemie ist die Chemie des Kohlenstoffs und seiner Verbindungen. Kohlenstoffkreislauf ATMSPHÄE (C 2 ) BISPHÄE (Lebewesen) LITHSPHÄE HYDSPHÄE (Gesteine)
Grundwissen Chemie Jahrgangsstufe 10 (NTG) Die organische Chemie ist die Chemie des Kohlenstoffs und seiner Verbindungen. Kohlenstoffkreislauf ATMSPHÄE (C 2 ) BISPHÄE (Lebewesen) LITHSPHÄE HYDSPHÄE (Gesteine)
Organische Chemie 10C1. Funktionelle Gruppen 10C2. Homologe Reihe der Alkane 10C3. Nomenklatur der Alkane (gesättigte Kohlenwasserstoffe) 10C4
 Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Organische Chemie. Kohlenwasserstoffe. Alkane. Alkane
 1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul ademacher Institut für Organische hemie der Universität Duisburg-Essen (Teil 8: 01.12.2004) MILESS: hemie für Biologen 142 Nomenklatur
hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul ademacher Institut für Organische hemie der Universität Duisburg-Essen (Teil 8: 01.12.2004) MILESS: hemie für Biologen 142 Nomenklatur
4-Butyl-2,5-dimethylheptan 5-Ethyl-4,8-dimethylundecan
 Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Polare Atombindung. Elektronegativität (EN) Elektronenpaarabstoßungsmodell. Dipolmoleküle. ( 10. Klasse SG - WSG 01 / 69 )
 Polare Atombindung ( 10. Klasse SG - WSG 01 / 69 ) ierbei ist das bindende Elektronenpaar zum Atom mit der höheren Elektronegativität (EN) verschoben. Dabei entstehen Teilladungen: + δ δ Elektronegativität
Polare Atombindung ( 10. Klasse SG - WSG 01 / 69 ) ierbei ist das bindende Elektronenpaar zum Atom mit der höheren Elektronegativität (EN) verschoben. Dabei entstehen Teilladungen: + δ δ Elektronegativität
Organische Chemie für Mediziner WS 2016/2017. Übungsblatt 3: Ausgewählte Substanzklassen
 1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
Inhaltsverzeichnis zu Kapitel 2. Alkane
 Inhaltsverzeichnis zu Kapitel 2. Alkane 2. Alkane 2.1. Valenzstrichformel, omologe Reihe, Nomenklatur, Konstitution, 22 Konformation 2.1.1. Valenzstrichformel 22 2.1.2. omologe Reihe 23 2.1.3. Konstitutionsisomere
Inhaltsverzeichnis zu Kapitel 2. Alkane 2. Alkane 2.1. Valenzstrichformel, omologe Reihe, Nomenklatur, Konstitution, 22 Konformation 2.1.1. Valenzstrichformel 22 2.1.2. omologe Reihe 23 2.1.3. Konstitutionsisomere
Organische Experimentalchemie
 Dr. Franziska Thomas ([email protected]) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas ([email protected]) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Ein Alkan, dem ein H-Atom fehlt, wird Alkyl-Rest genannt. Der Name ergibt sich aus dem Alkan, jedoch mit der Endung yl:
 Organische Chemie Unter organischer Chemie versteht man die Chemie der Kohlenwasserstoffe und ihre Derivate. Die C- Atome verbinden sich durch Kovalentebindung (Einfach-, Doppel- und Dreifachbindungen)
Organische Chemie Unter organischer Chemie versteht man die Chemie der Kohlenwasserstoffe und ihre Derivate. Die C- Atome verbinden sich durch Kovalentebindung (Einfach-, Doppel- und Dreifachbindungen)
Kennsilbe. -an. -en -in. -yl. -ol. -al (VI) -on. (VII) -säure (VIII)
 Hinweise und Übungen zur Nomenklatur (Benennung) organischer Verbindungen Die Vielfalt organischer Verbindungen ist im Gegensatz zur anorganischen hemie durch wenige Elemente aber zahlreiche Strukturmöglichkeiten
Hinweise und Übungen zur Nomenklatur (Benennung) organischer Verbindungen Die Vielfalt organischer Verbindungen ist im Gegensatz zur anorganischen hemie durch wenige Elemente aber zahlreiche Strukturmöglichkeiten
ORGANISCHE CHEMIE. Prof. Dipl.-Ing. Manfred SUSSITZ. Kernfragen: Mündliche Reifeprüfung: Alpen-Adria-Gymnasium Völkermarkt
 ORGANISCHE CHEMIE Prof. Dipl.-Ing. Manfred SUSSITZ Kernfragen: Mündliche Reifeprüfung: Alpen-Adria-Gymnasium Völkermarkt 1. Kohlenwasserstoffe KW Kohlenstoff "Kohlenstoff ist in organischen Verbindungen
ORGANISCHE CHEMIE Prof. Dipl.-Ing. Manfred SUSSITZ Kernfragen: Mündliche Reifeprüfung: Alpen-Adria-Gymnasium Völkermarkt 1. Kohlenwasserstoffe KW Kohlenstoff "Kohlenstoff ist in organischen Verbindungen
Organische Chemie. Maximilian Ernestus
 rganische hemie Maximilian Ernestus Inhaltsverzeichnis 1 rganische hemie 2 1.1 Wichtige Eigenschaften von Kohlenstoff..................... 2 1.2 Alkane....................................... 3 1.2.1 Isomere..................................
rganische hemie Maximilian Ernestus Inhaltsverzeichnis 1 rganische hemie 2 1.1 Wichtige Eigenschaften von Kohlenstoff..................... 2 1.2 Alkane....................................... 3 1.2.1 Isomere..................................
Grundwissen der 10.Klasse NTG
 Grundwissen der 10.Klasse NTG 1. Kohlenwasserstoffe 1.1 Alkane 1.1.1 Organische Stoffe = Verbindungen, die Kohlenstoffatome enthalten Ausnahme: Kohlenstoffoxide, Kohlensäure, Carbonate 1.1.2 Kohlenwasserstoffe
Grundwissen der 10.Klasse NTG 1. Kohlenwasserstoffe 1.1 Alkane 1.1.1 Organische Stoffe = Verbindungen, die Kohlenstoffatome enthalten Ausnahme: Kohlenstoffoxide, Kohlensäure, Carbonate 1.1.2 Kohlenwasserstoffe
10.1. Was versteht man unter einem Orbital? 10.2
 10.1 Was versteht man unter einem Orbital? Ein Orbital ist ein dreidimensionaler Aufenthaltsraum für maximal 2 Elektronen, in dem diese sich mit 99% Wahrscheinlichkeit aufhalten. Je nach Energiestufe ist
10.1 Was versteht man unter einem Orbital? Ein Orbital ist ein dreidimensionaler Aufenthaltsraum für maximal 2 Elektronen, in dem diese sich mit 99% Wahrscheinlichkeit aufhalten. Je nach Energiestufe ist
1. Methan 2 1.1. Eigenschaften und Zusammensetzung 2 1.2. Molekülstruktur 2 1.3. Vorkommen und Bedeutung 2
 A l k a n e 1. Methan 2 1.1. Eigenschaften und Zusammensetzung 2 1.2. Molekülstruktur 2 1.3. Vorkommen und Bedeutung 2 2. Die homologe Reihe der Alkane 2 2.1. Beispiele: Butan, exan und Eicosan (Paraffin)
A l k a n e 1. Methan 2 1.1. Eigenschaften und Zusammensetzung 2 1.2. Molekülstruktur 2 1.3. Vorkommen und Bedeutung 2 2. Die homologe Reihe der Alkane 2 2.1. Beispiele: Butan, exan und Eicosan (Paraffin)
Aktuelle Beispiele aus der Forschung
 Vorlesung: Allgemeine Chemie Organische Chemie 05.12.; 08.12.; Prof. Dr. C. Meier Eine Einführung in die Organische Chemie Themen: Elektronenstruktur, kovalente Bindung, Säure-Basen-Eigenschaften in Abhängigkeit
Vorlesung: Allgemeine Chemie Organische Chemie 05.12.; 08.12.; Prof. Dr. C. Meier Eine Einführung in die Organische Chemie Themen: Elektronenstruktur, kovalente Bindung, Säure-Basen-Eigenschaften in Abhängigkeit
13.1. Struktur der Carbonyl-Gruppe, Prinzipielle Reaktivität
 13. arbonyl -Verbindungen 13.1. Struktur der arbonyl-gruppe, Prinzipielle Reaktivität 13.2. Aldehyde & Ketone 13.2.1 Nomenklatur 13.2.2 Darstellungen xidationen 13.2.3 Reaktionen Additionen an der = Acetale
13. arbonyl -Verbindungen 13.1. Struktur der arbonyl-gruppe, Prinzipielle Reaktivität 13.2. Aldehyde & Ketone 13.2.1 Nomenklatur 13.2.2 Darstellungen xidationen 13.2.3 Reaktionen Additionen an der = Acetale
Wiederholung Grundlagen OC
 Wiederholung Grundlagen C 28.04.2017 Auswertung Stichprobe Frage 1: Die oben abgebildete Strukturformel zeigt 25 20 15 10 5 0 Ether Ester Acetal Keton Ester+Weiteres Frage 2: Die absolute Konfiguration
Wiederholung Grundlagen C 28.04.2017 Auswertung Stichprobe Frage 1: Die oben abgebildete Strukturformel zeigt 25 20 15 10 5 0 Ether Ester Acetal Keton Ester+Weiteres Frage 2: Die absolute Konfiguration
Nomenklatur organischer Verbindungen nach den IUPAC-Regeln Hier findest Du die Zauberformel!
 Nomenklatur organischer Verbindungen nach den IUPAC-Regeln Hier findest Du die Zauberformel! Prof. Dr. Ivo C. Ivanov Einführung (interaktive Vorlesung) Die genaue Benennung organischer Verbindungen nach
Nomenklatur organischer Verbindungen nach den IUPAC-Regeln Hier findest Du die Zauberformel! Prof. Dr. Ivo C. Ivanov Einführung (interaktive Vorlesung) Die genaue Benennung organischer Verbindungen nach
Berufliche Oberschule Fürstenfeldbruck
 Berufliche Oberschule Fürstenfeldbruck Staatliche Fachoberschule und Berufsoberschule Fach: hemie Aufstellen von Summenformeln und Reaktionsgleichungen, Ausarbeitung: S. Räthel, S. eilmann,. Preller 10,
Berufliche Oberschule Fürstenfeldbruck Staatliche Fachoberschule und Berufsoberschule Fach: hemie Aufstellen von Summenformeln und Reaktionsgleichungen, Ausarbeitung: S. Räthel, S. eilmann,. Preller 10,
Beispielklausur Allgemeine Chemie II (Organische Chemie)
 Beispielklausur Allgemeine Chemie II (rganische Chemie) für Studierende mit Chemie als Nebenfach zum Üben 1. Zeichnen Sie für die folgenden Stoffklassen jeweils die Strukturformel einer dazu passenden
Beispielklausur Allgemeine Chemie II (rganische Chemie) für Studierende mit Chemie als Nebenfach zum Üben 1. Zeichnen Sie für die folgenden Stoffklassen jeweils die Strukturformel einer dazu passenden
L.9 Organische Chemie I
 L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen
 Tuesday, January 30, 2001 Allgemeine Chemie B II Page: 1 2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 2.1 Funktionelle Gruppen Es gibt
Tuesday, January 30, 2001 Allgemeine Chemie B II Page: 1 2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 2.1 Funktionelle Gruppen Es gibt
Kohlenwasserstoffe. sp 3 -Orbitale. Alkane. Alkene. sp 2 - Orbitale p z - Orbital. sp -Orbitale p y, p z - Orbitale. Alkine
 Kohlenwasserstoffe sp 3 -Orbitale Alkane sp 2 - Orbitale p z - Orbital Alkene sp -Orbitale p y, p z - Orbitale Alkine Offenkettige Alkane 4 4 than "Erdgas" 2 6 3 3 Ethan 3 8 3 2 3 Propan Bei Raumtemperatur
Kohlenwasserstoffe sp 3 -Orbitale Alkane sp 2 - Orbitale p z - Orbital Alkene sp -Orbitale p y, p z - Orbitale Alkine Offenkettige Alkane 4 4 than "Erdgas" 2 6 3 3 Ethan 3 8 3 2 3 Propan Bei Raumtemperatur
